Изобретение относится к области фармацевтики и ветеринарной медицины, касается способа получения остеопластического материала для восстановления дефектов костной ткани и ускорения консолидации. Также изобретение относится к области биокомпозиционных материалов для реконструкции дефектов костной ткани животных.
Биокомпозитный материал содержит в качестве действующих веществ гидроксиапатит (ГА), метилурацил, амоксициллин и стабилизатор (альгинат кальция) при следующем соотношении компонентов, мас. %: гидроксиапатит 1-5, метилурацил 1-5, амоксициллин 1-5, альгинат кальция 0,5-3, растворитель вода - остальное. Биокомпозитный материал нетоксичен, не обладает местным раздражающем и аллергизирующим действием.
Изобретение ускоряет сращения переломов благодаря наличию остеокондуктивного потенциала, отличной биосовместимости с полной биоинтеграцией и антибактериальным действием.
В гуманной медицине известен композиционный материал для замещения костной ткани (RU 2622751 С1, МПК A61L 27/08, A61F 2/28, B82Y 5/00, B82Y 99/00, С01В 31/02, опуб. 19.06.2017). Композиционный материал для замещения костной ткани содержит пористую матрицу из волокон кристаллического углерода с межслоевым расстоянием 3,58…3,62 ангстрема при общем количестве волокна 20…80% и материал-наполнитель, состоящий из кристаллического углерода с межслоевым расстоянием 3,42…3,44 ангстрема в количестве 50…70% и аморфного углерода в виде кокса в количестве 10…20% от общего объема пор. Данный композиционный материал имеет следующие недостатки:
1) Используется только при конкретизированном хирургическом случае (эндопротезирование) и не обладает возможностью замещения дефектов трубчатых костей при различных видах переломов.
2) Отсутствие биоинтеграции.
3) Отсутствие антибактериального действия.
Также в гуманной медицине известен композиционный материал для восстановления дефектов костной ткани, способ его получения и применения (RU 2476236 C1, МПК A61K 38/39, A61K 33/42, А61Р 9/00, опуб. 27.02.2013). Композиционный материал на основе нереконструированного коллагена и наногидроксиапатита для восстановления дефектов костной ткани, характеризующийся тем, что нереконструированный коллаген смешивают с водным раствором глюкозы и выдерживают при комнатной температуре до набухания с последующим нагреванием до 35°-45°С гомогенизацией полученной суспензии до образования геля, к которому добавляют суспензию наногидроксиапатита в водном растворе глюкозы при весовом соотношении коллагена к наногидроксиапатиту от 5:1 до 1:5 с последующей гомогенизацией полученного геля и стерилизацией.
Данный композиционный материал имеет следующие недостатки:
1) Отсутствие антибактериального действия.
2) Неудобная форма композиционного материала (суспензия) для замещения костной ткани, возможна утечка препарата.
Также в гуманной медицине известна композиция биорезорбируемого 3D-матрикса для восстановления дефектов костной ткани (RU 2762511 С1, МПК A61K 31/00, A61K 31/726, A61K 31/728, A61K 31/729, А61Р 19/00, опуб. 21.12.2021). Данная композиция предназначена для планирования и лечения костных и костно-хрящевых дефектов. Представленный костный 3D-матрикс заданной формы на основе гиалуроновой кислоты устанавливается на место дефекта и в последующем замещается костной тканью организма. Данный матрикс имеет следующие недостатки:
1) Отсутствие антибактериального действия.
2) Проведение предварительной подготовки. Необходимость проведения моделирования на основе результатов цифровых методов обследования пациента (компьютерной томографии, магнитно-резонансной томографии, УЗИ).
Гидроксиапатит (ГА) - минеральная составляющая кости (50% в костной ткани и 96% в эмали). В хирургии и травматологии используется как наполнитель, заменяющий части утерянной кости и как покрытие имплантов, способствующих нарастанию новой кости.
Метилурацил (МУ) впервые был синтезирован во второй половине прошлого века, соединение было получено из мочевины и ацетоуксусного эфира через b-уреидкротоновый эфир. В Mercklndex приводится следующая характеристика данного вещества: 6-метилурацил; 6-метил2,4(1J, 3J)-пиримидиндион; 4-метилурацил; C5H6N2O2; мол. вес 126,11; С 47,62%, Η 4,80%, N 22,21%, О 25,37%. МУ был предложен в качестве лекарственного средства. На сегодняшний день достоверно продемонстрированы следующие позитивные влияния МУ на организм человека и экспериментальных животных: анаболическое действие; стимуляция регенераторных процессов в органах и тканях, проявляющаяся на разных уровнях организации живой материи - на молекулярном, субклеточном, клеточном, тканевом и органном; способность стимулировать лейко- и эритропоэз; стимуляция механизмов иммунной защиты; противовоспалительная активность; стимуляция процессов фагоцитоза; болеутоляющее действие, которое было выявлено В.И. Русаковым; адаптогенное действие; усиление действия антибиотиков (по-видимому, за счет уменьшения их токсичности) (Белоусова Т.А. Фармакологичесике свойства метилурацила (обзор литературы). / Т.А. Белоусова // Альманах вып. 28. ЗАО Ретиноиды. Москва 2009, стр. 11-43).
Альгинат представляет собой полианионный полисахарид, нетоксичный, биосовместимый, высоко гидрофильный, обычно используемый в качестве стабилизатора в фармацевтической и биотехнологической промышленности. В медицинской практике известно положительное действие солеи альгиновои кислоты как местных тканевых стимуляторов развития грануляционной ткани, процессов регенерации и эпителизации. Также применение альгинатных материалов нашло себя в качестве вспомогательных химико-фармацевтических средств, для производства различных лекарственных форм медицинских препаратов. Альгинатные системы обладают способностью адсорбировать воду в большом количестве, а так же способностью к структурированию жидких растворов (Гусев И.В. Разработка высокоструктурированных гидрогелевых депо-материалов для направленной доставки лекарственных препаратов. ФГБОУ ВО «Московский государственный университет технологий и управления имени К. Г. Разумовского (Первый казачий университет)». - Москва, 2015. - 182 с. - Библиогр.: с. 32-33).
Амоксициллин представляет собой аминобензиловый пенициллин, полусинтетический антибиотик широкого спектра действия, обладающий бактерицидным действием в результате ингибирования синтеза бактериальной клеточной стенки.
Технической задачей является разработка биокомпозиционного остеопластического материала на основе гидроксиапатита, метилурацил а, амоксициллина, альгинат натрия и дистиллированной воды.
Техническая задача решается тем, что для получения биокомпозиционного остеопластического материала растворяют в дистиллированной воде при температуре окружающей среды в 22 градуса при непрерывном размешивании, например, с помощью магнитной мешалки, альгинат натрия до образования однородного раствора молочного цвета. После полного растворения альгината натрия добавляют последовательно при непрерывном перемешивании метилурацил, гидроксиапатит и амоксициллин по 100 мг каждые 15 минут. Затем полученную суспензию заливают в форму, которую помещают в 0,2М раствор хлорида кальция и оставляют при температуре 22-25°С на 48 часов. Полученный композит имеет белый цвет, упругую консистенцию (Фиг. 1).
Техническим результатом заявленного изобретения является получение биокомпозитного материала заданной формы, упругой консистенции, что позволяет вносить его в костномозговой канал трубчатых костей при их переломах для постепенного высвобождения действующих компонентов, тем самым обеспечивая полную биоинтеграцию непосредственно в месте приложения, что способствует ускорению костной репарации.
Заявленное изобретение иллюстрируется следующими фигурами и таблицами.
На фиг. 1 представлен общий вид (фотография) биокомпозитного остеопластического материала.
На фиг. 2 представлено проведение оценки острой токсичности биокомпозитного материала на белых линейных мышах - орально при помощи желудочного зонда (фотография).
На таблице 1 представлены расчетные количества компонентов веществ, входящие в состав биокомпозита.
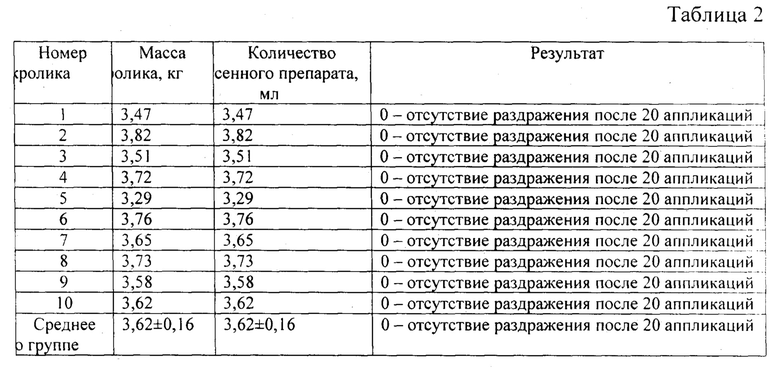
На таблице 2 представлены результаты изучения раздражающего действия биокомпозита на кожу кроликов.
Изобретение характеризуется следующими примерами, которые не ограничивают объем притязаний заявителя.
Пример 1. Получение биокомпозиционного остеопластического материала для ускорения консолидации переломов трубчатых костей животных.
Материал получают путем смешивания расчетных количеств входящих в состав компонентов при постоянной температуре, последующим внесением полученной суспензии в целевую форму, которую помещают в раствор 0,2 Μ хлорида кальция для образования водородных связей между гидроксильными и карбоксильными группами пиранозных циклов L-гулуроновои кислоты соседних полимерных цепей, тем самым получения необходимой плотности конечного препарата, что отражено в таблице 1.
Установлено, что данный материал имеет стабильную форму упругой консистенции, что способствует беспрепятственному введению его в костномозговой канал в месте перелома трубчатой кости.
Пример 2. Оценка острой токсичности полученного лекарственного материала.
Для определения острой токсичности был использован биокомпозит, полученный по примеру 1.
Оценка острой токсичности биокомпозитного материала проводилась на белых линейных мышах согласно ГОСТ 32644-2014.
Исходя из входящих в состав биокомпозита лекарственных веществ, предполагалось, что у препарата низкая токсичность, поэтому эксперимент начали с дозы 2000 мг/кг.
Контрольной группе из трех мышей орально при помощи желудочного зонда, вводили 0,9% раствор натрия хлорида в том же объеме. Физиологических нарушений у данной группы мышей после введения не наблюдалось.
Мышам опытной группы (n=3), живой массой ≈ 23 г, биокомпозит вводили внутрижелудочно, с помощью зонда, в дозе 2000 мг/кг, однократно (Фиг. 2). Спустя час появились первые признаки интоксикации: у подопытных наблюдалось учащенное и глубокое дыхание, 2 мыши сгруппировались и лежали в углу клетки, одна продолжала питаться. Спустя 24 часа клиническая картина интоксикации купировалась. Все опытные животные были активны, подвижны, хорошо принимали корм и практически не отличались от контрольных животных. Повторное тестирование 3-х животных было полностью идентично первому исследованию. Таким образом, биокомпозит, согласно классификации (ГОСТ 32644-2014), относится к 5-му классу в СГС.
Пример 3. Оценка раздражающего действия заявленного биокомпозита
Определение местного раздражающего действия проводили методом кожной пробы на 10 кроликах породы шиншилла массой 2,97±0,3 кг, в соответствии с руководством по проведению доклинических исследований лекарственных средств (Руководство по проведению доклинических исследований лекарственных средств. Часть первая // под ред. А.Н. Миронова. - М.: Гриф и К, 2012. - 944 с).
За 2 дня до эксперимента тщательно выстригли ножницами на спине участки размером 7 x 8 см на симметричных участках спины по обе стороны от позвоночника, оставляя волосяной покров между ними в 2 см. Правый бок служил для аппликации раствора препарата, левый - для контроля. На время экспозиции для исключения слизывания препарата с кожи животных фиксировали воротником из пластика.
Время экспозиции 4 часа. Повторные экспозиции - ежедневно в течение 20 дней. После окончания эксперимента за животными вели наблюдение в течение 14 дней.
Исследуемый биокомпозит наносили в нативном виде из расчета 1 мл на 1 кг массы кролика на выстриженный участок на правом боку кролика. На левый бок наносили такое же количество 0,9% раствор натрия хлорида -контрольное вещество.
Выраженность эритемы определяли визуально и оценивали в баллах по шкале от 0 (отсутствие эритемы) до 4 (резко выраженная - ярко-красный тон).
Результаты испытания раздражающего действия биокомпозитана кожу кроликов представлены в таблице 2.
В результате проведенного эксперимента установлено, что биокомпозитне оказывал раздражающего действия на кожу кроликов после 20 ежедневных аппликаций.
Таким образом, согласно межгосударственному стандарту ГОСТ ISO 10993-10-2011 бйокомпозит не вызывает ответной реакции на раздражение у кроликов.
Нанесение разрешающей дозы биокомпозита сенсибилизированным кроликам не вызывает ответную реакцию со стороны слизистой оболочки глаза и кожного покрова, что говорит об отсутствии аллергизирующих свойств у препарата.
Заявляемое изобретение является новым и промышленно применимым, так как может быть реализовано с использованием известных компонентов, обеспечивает высокое качество получаемого биокомпозиционного материала.

| название | год | авторы | номер документа |
|---|---|---|---|
| Остеокондуктивное и остеоиндуктивное биокомпозиционное покрытие имплантов для ускорения консолидации переломов животных | 2022 |
|
RU2817049C1 |
| Способ оптимизации репаративного остеогенеза трубчатых костей животных | 2023 |
|
RU2816808C1 |
| Способ прагматизации репаративного остеогенеза трубчатых костей животных | 2023 |
|
RU2816809C1 |
| Способ получения остеопластического дисперсного биокомпозита | 2020 |
|
RU2741015C1 |
| Способ получения гидроксиапатит-коллагенового композита | 2016 |
|
RU2631594C1 |
| МЕДИЦИНСКИЙ БИО-КЛЕЙ НОВОГО ПОКОЛЕНИЯ НА ОСНОВЕ БИОПОЛИМЕРНЫХ НАНОКОМПОЗИТОВ В ВИДЕ ПОЛУСИНТЕТИЧЕСКОЙ ПОЛИМЕРНОЙ МАТРИЦЫ C ПРИМЕНЕНИЕМ ЛАЗЕРНЫХ ТЕХНОЛОГИЙ | 2013 |
|
RU2543321C2 |
| КОМПОЗИЦИОННЫЙ МАТЕРИАЛ ДЛЯ ВОССТАНОВЛЕНИЯ ДЕФЕКТОВ КОСТНОЙ ТКАНИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2012 |
|
RU2476236C1 |
| МЕДИЦИНСКИЙ КЛЕЙ-БИОИМПЛАНТАТ НОВОГО ПОКОЛЕНИЯ НА ОСНОВЕ БИОПОЛИМЕРНЫХ НАНОКОМПОЗИТОВ В ВИДЕ ПОЛУСИНТЕТИЧЕСКОЙ ПОЛИМЕРНОЙ МАТРИЦЫ С ПРИМЕНЕНИЕМ ЛАЗЕРНЫХ ТЕХНОЛОГИЙ | 2011 |
|
RU2477996C1 |
| БИОКОМПОЗИТ ДЛЯ ОБЕСПЕЧЕНИЯ ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССОВ ПОСЛЕ ПОВРЕЖДЕНИЯ У МЛЕКОПИТАЮЩЕГО, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ПРИМЕНЕНИЯ | 2011 |
|
RU2519326C2 |
| Способ получения биокомпозита с антибактериальными свойствами | 2023 |
|
RU2824130C1 |

Изобретение относиться к области фармацевтики и ветеринарной медицины, а именно к биокомпозиционному остеопластическому материалу для ускорения консолидации переломов животных. Биокомпозиционный остеопластический материал содержит в качестве действующих веществ 1-5 мас.% гидроксиапатита, 1-5 мас.% метилурацила, 1-5 мас.% амоксициллина, 0,5-3 мас.% стабилизатора альгината кальция и дистиллированную воду остальное. Вышеописанное изобретение позволяет получить биокомпозитный материал заданной формы, упругой консистенции, что позволяет вносить его в костномозговой канал трубчатых костей при их переломах для постепенного высвобождения действующих компонентов, тем самым обеспечивая полную биоинтеграцию непосредственно в месте приложения, что способствует ускорению костной репарации. 2 ил., 2 табл., 3 пр.
Биокомпозиционный остеопластический материал для ускорения консолидации переломов животных содержит в качестве действующих веществ гидроксиапатит, метилурацил, амоксициллин, стабилизатор альгинат кальция и дистиллированную воду при следующем соотношении компонентов, мас.%:
| БИОМАТЕРИАЛ ДЛЯ ВОЗМЕЩЕНИЯ ДЕФЕКТОВ КОСТЕЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2478394C1 |
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Расчеты и испытания на прочность, Методы механических испытаний композиционных материалов с полимерной матрицей (композитов) | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ЩИПУНОВ Ю.А., ПОСТНОВА И.В | |||
| Формирование макрпористых материалов на основе альгината кальция, включающих хитозан и гидроксиапатит// Коллоидный журнал, | |||
Авторы
Даты
2023-10-23—Публикация
2022-10-26—Подача