Изобретение относится к области практической медицины - кардиологии, сердечно-сосудистой и рентгенэндоваскулярной хирургии. Способ может применяться во время выполнения чрескожного коронарного вмешательства (ЧКВ) при массивном тромбозе коронарных артерий или аортокоронарных шунтов у пациентов с острым коронарным синдромом (ОКС) при невозможности или неэффективности традиционной тромбэмболэктомии стандартным аспирационным катетером.
ЧКВ - высокоэффективный и безопасный метод реваскуляризации миокарда, наряду с аортокоронарным шунтированием (АКШ), рекомендуется к рутинному применению у пациентов с хронической и острой формой ишемической болезни сердца (ИБС) [Neumann FJ, Koller A, Yadav R, et al. MO ESC Scientific Document Group. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2018. doi:10.1093/eurheartj/ehy394].
ОКС представляет собой наиболее опасную ситуацию, в связи с гемодинамически нестабильным состоянием пациента, и требует проведения экстренной реваскуляризации миокарда предпочтительно методом ЧКВ. Операция зачастую единственный шанс на спасение. Причина ОКС - разрыв/эрозия нестабильной атеросклеротической бляшки в коронарных артериях, с последующим образованием тромбов/эмболов, которые могут полностью закрыть сосуд (окклюзия) [Yunoki K, Naruko T, Sugioka K, et al. Thrombus aspiration therapy and coronary thrombus components in patients with acute ST-elevation myocardial infarction. J Atheroscler Thromb. 2013;20(6):524-37. doi: 10.5551/jat.17608].
Проводниковая реканализация, баллонная ангиопластика и имплантация коронарного стента - основные этапы ЧКВ при ОКС. При массивном тромбозе для восстановления просвета артерии возможно выполнение аспирационной тромбэмболэктомии аспирационным катетером на фоне применения блокаторов гликопротеиновых рецепторов IIb/IIIa и неэффективности основных этапов ЧКВ. Согласно клиническим рекомендациям рутинное использование устройств аспирации тромба не рекомендуется (Класс IIIA) [Neumann FJ, Koller A, Yadav R, et al. MO ESC Scientific Document Group. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2018. doi:10.1093/eurheartj/ehy394]. Тем не менее, опираясь на клиническую практику, тромбэмболэктомия, как методика последней линии ЧКВ, иногда остается единственным эффективным способом восстановления просвета артерии или аортокоронарного шунта при массивном тромбозе. Однако бывают случаи, когда тромбэмболэктомия аспирационным катетером неэффективна. Такие пациенты зачастую остаются с закрытой (окклюзированной) артерией, что связано с повышенным риском развития неблагоприятных событий и смертности, несмотря на оптимальную медикаментозную терапию.
На сегодняшний день существуют несколько off - label способов тромбэмболэктомии из коронарных артерий или аортокоронарных шунтов у пациентов с ОКС при невозможности или неэффективности традиционной механической аспирационной тромбэмболэктомии стандартным аспирационным катетером:
1. Применение системы тромбэкстракции Penumbra, предназначенной для церебральных сосудов при ишемическом инсульте, основанной на принципе вакуумной аспирации целостных тромбов с использованием реперфузионных катетеров и насоса [Mathews SJ, Brown CL, Kolski BC, et al. Initial experience with a continuous mechanical aspiration system for thrombus removal before percutaneous coronary intervention. Catheter Cardiovasc Interv. 2022 Nov;100(6):950-954. doi:10.1002/ccd.30389].
2. Реолитическая тромбэктомия (AngioJet), которая зачастую применяется для периферических сосудов при первичных тромбозах на фоне атеросклеротического поражения, тромбозах после реконструктивных операций на сосудах (шунтирования, протезирования, пластики, шва артерии), а также при тромботических осложнениях. Система использует струи физраствора под высоким давлением для создания эффекта Venturi-Bernoulli, позволяющие выполнить разрушение тромба и эвакуацию его через зонд [Giglioli C, Cecchi E, Sciagrá R, et al. Comparison between Coronary Thrombus aspiration with Angiojet® or Export® catheter in patients with ST-elevation myocardial infarction submitted to primary angioplasty: The COCOTH Study. Int J Cardiol. 2016 Jan 15;203:757-62. doi:10.1016/j.ijcard.2015.03.158].
Описанные методы являются сложными, высокозатратными и применяются крайне редко только в специализированных центрах, что является главным ограничением в общей когорте пациентов. В связи с этим, за прототип и основу нами взят способ применения традиционного механического ручного аспирационного катетера.
Способ тромбэмболэктомии традиционным механическим ручным аспирационным катетером:
1. Катетеризировать устье левой или правой коронарной артерии проводниковым катетером ≥6F.
2. Под контролем рентгеноскопии завести в дистальные отделы целевой артерии коронарный проводник.
3. Надеть подготовленный аспирационный катетер на коронарный проводник.
4. Убедиться, что комплект трубок и шприц Vaclok® был подсоединен к аспирационному катетеру перед заведением его в проводниковый катетер.
5. Провести аспирационный катетер под рентгеноскопией по коронарному проводнику к выбранному сосудистому участку. Расположить маркер дистального наконечника проксимально к нужному участку. Остановить продвижение аспирационного катетера при возникновении сопротивления.
6. После рентгеноскопического подтверждения положения аспирационного катетера открыть закрывающий кран системы, чтобы начать аспирацию. Медленно продвигать аспирационный катетер по коронарному проводнику дистально от проводникового катетера. Кровь будет попадать в аспирационный шприц Vaclok®, пока не исчезнет весь вакуум или не заполнится шприц.
7. Если шприц Vaclok® не начинает наполняться кровью в течение 5 секунд, необходимо повернуть закрывающий кран и удалить катетер как можно скорее. Промыть аспирационный катетер или использовать новый катетер и повторить вышеописанные шаги.
8. После завершения процесса аспирации необходимо повернуть закрывающий кран в положение «Выкл.» и удалить аспирационный катетер или присоединить второй шприц Vaclok®, и в случае необходимости повторить процесс аспирации.
Недостатком прототипа является его низкая эффективность при массивном тромбозе коронарных артерий или аортокоронарных шунтов большого диаметра (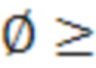 3,5 мм), в связи с большим объемом сформированных тромботических масс и малым диаметром внутреннего просвета стандартного аспирационного катетера.
3,5 мм), в связи с большим объемом сформированных тромботических масс и малым диаметром внутреннего просвета стандартного аспирационного катетера.
Указанные недостатки устраняются в заявленном техническом решении.
Задача настоящего изобретения состоит в разработке способа выполнения аспирационной тромбэмболэктомии проводниковым катетером при массивном тромбозе коронарных артерий или аортокоронарных шунтов у пациентов с ОКС при неэффективности выполнения тромбэмболэктомии стандартным аспирационным катетером во время ЧКВ.
Разрабатываемый способ приемлем как для коронарных артерий, так и для аортокоронарных шунтов и будет иметь одинаковый алгоритм применения независимо от патофизиологического механизма возникновения массивного тромбоза целевого сосуда.
Показания:
• Массивный тромбоз целевого сосуда (коронарной артерии или аортокоронарного шунта), диаметр которого ∅ ≥3,5 мм, у пациентов с острой формой ИБС (инфаркт миокарда (ИМ) с подъемом сегмента ST, ИМ без подъема сегмента ST, нестабильная стенокардия и ранняя постинфарктная стенокардия);
• Неэффективность применения традиционных методов тромбэмболэктомии при ЧКВ на фоне оптимальной медикаментозной терапии блокаторами гликопротеиновых рецепторов IIb/IIIa;
• Техническая возможность и благоприятная анатомия целевого сосуда для применения способа.
Техническим результатом является выполнение успешной аспирационной тромбэмболэктомии при массивном тромбозе коронарных артерий или аортокоронарных шунтов, которая включает в себя удаление несвязанного внутрисосудистого субстрата, восстановление кровотока TIMI II - III по целевому сосуду, отсутствие гемодинамически значимой дистальной эмболизации и интраоперационных осложнений, связанных с применением способа.
Способ осуществляется следующим образом:
1. Катетеризировать устье целевого сосуда (коронарной артерии или аортокоронарного шунта) проводниковым катетером 5F (∅ ≈1,67 мм) или 6F (∅ ≈2 мм).
2. Под контролем рентгеноскопии завести в дистальные отделы целевого сосуда коронарный проводник 0,014”180 см или 0,014”190 см.
3. По коронарному проводнику за место массивного тромбоза под контролем рентгеноскопии завести баллонный катетер размером 1:1 к диаметру целевого сосуда для использования техники «якорного баллона».
4. Используя «якорную» технику, подкручивая катетер по часовой стрелке, под контролем рентгеноскопии выполнить глубокую интубацию проводниковым катетером за место массивного тромбоза.
5. Убрать баллонный катетер и коронарный проводник из целевого сосуда.
6. Напрямую к проводниковому катетеру подсоединить аспирационный шприц отрицательного давления (20-60 мл).
7. На постоянной аспирации, под контролем рентгеноскопии выполнить тракцию проводникового катетера на себя, подкручивая катетер против часовой стрелки, до проксимального сегмента целевого сосуда свободного от тромбоза.
8. Убрать наполненный тромботическими массами шприц отрицательного давления и дополнительно наполнить шприц (10 мл) кровью и остаточными фрагментами тромботических масс из просвета проводникового катетера.
9. Проводниковый катетер под контролем рентгеноскопии подвести к устью целевого сосуда, не выводя в аорту, для выполнения контрольной ангиографии.
10. Провести анализ полученных результатов. При необходимости повторить аспирационную тромбэмболэктомию проводниковым катетером по вышеуказанному алгоритму. В случае необходимости закончить ЧКВ имплантацией коронарного стента.
Предложенный способ выполнения аспирационной тромбэмболэктомии проводниковым катетером используется в клинической практике и показал свою эффективность и безопасность в ретроспективном анализе (n=29), который был проведен на базе ГБУЗ СОККД им. В.П. Полякова (Самара) за 2022 - 2023 гг. Эффективность оценивалась по критериям оптимального ангиографического результата ЧКВ: полное восстановление кровотока TIMI II-III по инфаркт - зависимой артерии без гемодинамически значимой дистальной эмболизации. Безопасность оценивалась по критериям наличия или отсутствия интраоперационных осложнений, связанных с методикой. Медиана диаметра целевого сосуда составила 4 мм (CI95% 3,54 - 3,9). Доля интраоперационных осложнений не превышала среднего показателя в общем объеме ЧКВ при ОКС. Корреляции между техническим успехом, наличием или отсутствием осложнений и локализацией целевого поражения выявлено не было. Летальности и других неблагоприятных событий MACE в период госпитализации не было. В связи с этим, предложенный способ, который требует минимальных экономических затрат, может быть рассмотрен во время выполнения ЧКВ, как вынужденный хирургический выбор при массивном тромбозе коронарных артерий или аортокоронарных шунтов диаметром ∅ ≥3,5 мм у пациентов с острыми формами ИБС и неэффективности стандартных методов тромбоаспирации.
Клинический пример №1.
Пациент, мужчина, 51 год поступил экстренно с жалобами: на интенсивные жгучие боли за грудиной, продолжительностью более 1 часа, сопровождающиеся нехваткой воздуха, холодным потом. Вызвал СМП, снята ЭКГ - фибрилляция предсердий, подъём ST по передней стене. Тропонин слабоположительный с тенденцией к нарастанию. Пациент доставлен в СОККД, госпитализирован в ОРИТ с диагнозом: ИБС. ОКС с ПST.
ЭКГ на этапе СМП: трепетание предсердий, тахисистолия, подъем ST I, AVL, V1-6, депрессия ST II, III, AVF.
ЭКГ при поступлении: ритм синусовый, нормальное положение ЭОС, тахисистолия, подъём ST I, aVL, депрессия ST сохраняется с формированием отриц. Т II, III, aVF, глубокий отрицательный Т V1-V6.
Проведена экстренная коронарография (КГ).
Заключение (% стеноза по диаметру; пограничные стенозы D/A - по диаметру/по площади):
Тип кровоснабжения сердца - правый.
Ствол левой коронарной артерии: без поражений.
Передняя межжелудочковая ветвь (ПМЖВ): окклюзия, вызванная массивным тромбозом, в проксимальном сегменте, дистальные отделы не контрастируются.
Огибающая артерия (ОА): без поражений.
Правая коронарная артерия (ПКА): без поражений.
Пациенту рекомендуется выполнить ЧКВ ПМЖВ в экстренном порядке.
Налажена инфузия блокаторов гликопротеиновых рецепторов IIb/IIIa по стандартной схеме, выполнена механическая проводниковая реканализация коронарным проводником 0,014”190 см и оптимальная баллонная ангиопластика - без эффекта. Выполнена многократная аспирационная тромбэмболэктомия традиционным аспирационным катетером - тромботических масс не получено, кровоток не восстановлен. Принято решение применить предложенный способ выполнения аспирационной тромбэмболэктомии проводниковым катетером.
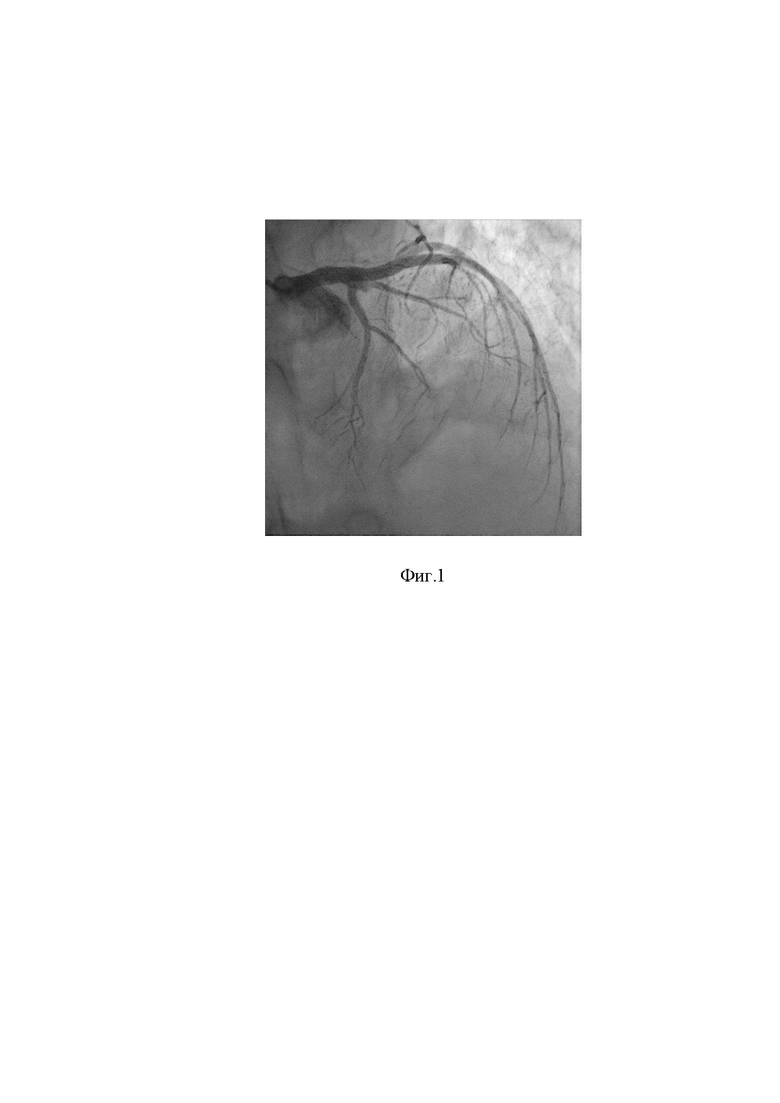
На фигуре 1 показано состояние ПМЖВ до выполнения аспирационной тромбэмболэктомии проводниковым катетером.
Тромбэмболэктомию проводниковым катетером осуществляли следующим образом:
1. Устье левой коронарной артерии катетеризировано проводниковым катетером 5F (∅ ≈1,67 мм).
2. Под контролем рентгеноскопии в дистальные отделы ПМЖВ заведен коронарный проводник 0,014”190 см.
3. По коронарному проводнику за место окклюзии в ПМЖВ под контролем рентгеноскопии заведен баллонный катетер размером 1:1 к диаметру целевой артерии (∅ ≈3,5 мм) для использования техники «якорного баллона».
4. Используя «якорную» технику, подкручивая катетер по часовой стрелке, под контролем рентгеноскопии выполнена глубокая интубация проводниковым катетером за место окклюзии в ПМЖВ.
5. Убран баллонный катетер и коронарный проводник из ПМЖВ.
6. Напрямую к проводниковому катетеру подсоединён аспирационный шприц отрицательного давления (20 мл).
7. На постоянной аспирации, под контролем рентгеноскопии выполнена тракция проводникового катетера на себя, подкручивая катетер против часовой стрелки, до проксимального сегмента ПМЖВ.
8. Убран наполненный тромботическими массами шприц отрицательного давления и дополнительно наполнен шприц (10 мл) кровью и остаточными фрагментами тромботических масс из просвета проводникового катетера.
9. Проводниковый катетер под контролем рентгеноскопии подведен к устью левой коронарной артерии, не выводя в аорту, для выполнения контрольной коронарографии.
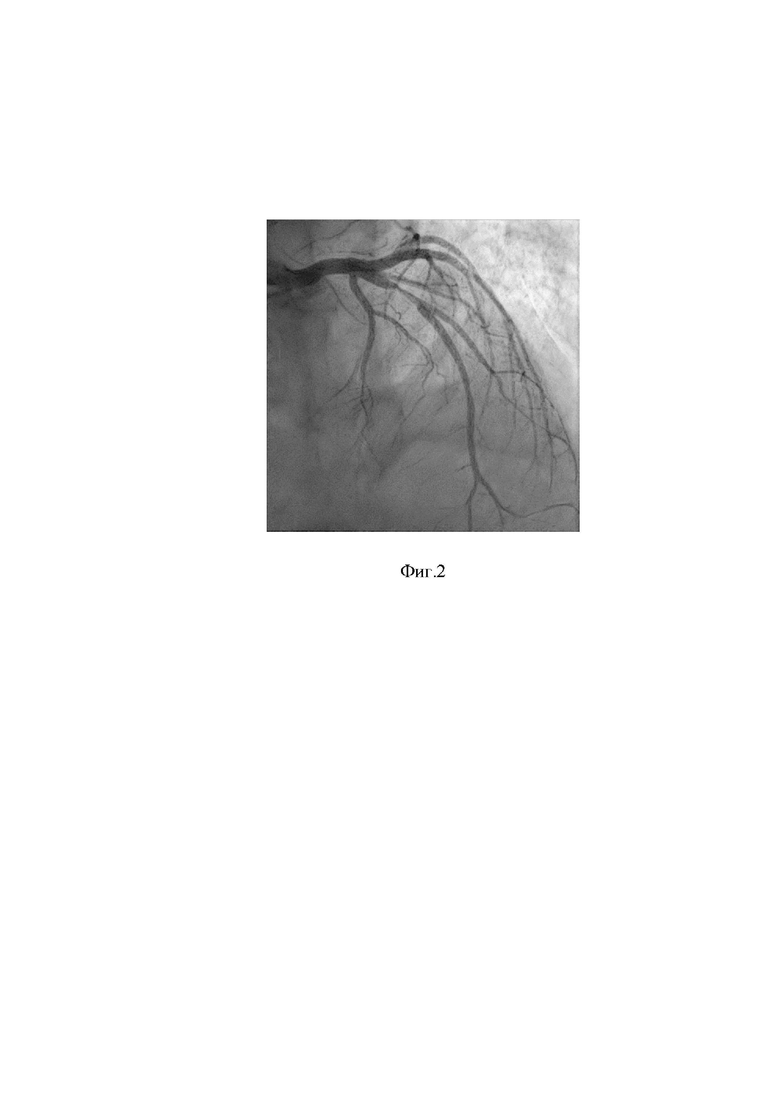
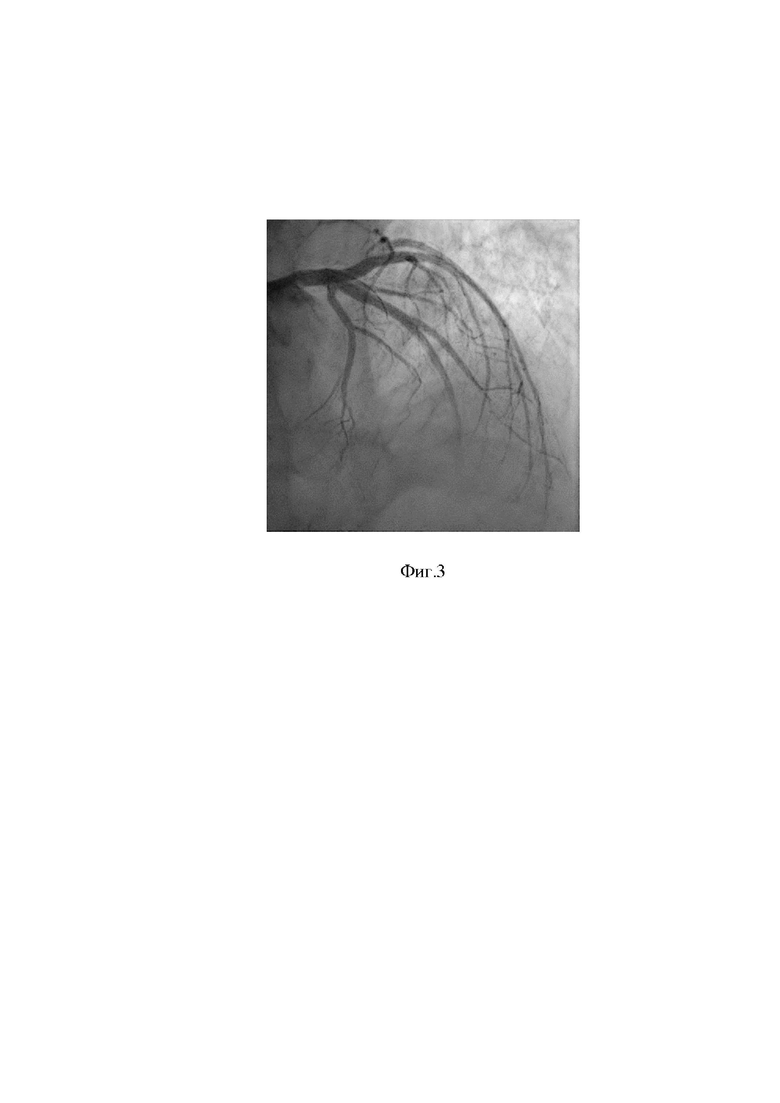
10. Выполнена контрольная коронарография. Проведен анализ полученных результатов - восстановлен антеградный кровоток TIMI III по ПМЖВ без признаков дистальной эмболизации и интраоперационных осложнений, связанных с применением способа. На фигуре 2 показано состояние ПМЖВ после выполнения аспирационной тромбэмболэктомии проводниковым катетером. В зону остаточного стеноза в ПМЖВ имплантирован коронарный стент ∅3,5x18 мм. На фигуре 3 показано состояние ПМЖВ после имплантации коронарного стента.
Контрольная коронарография - антеградный кровоток TIMI III по ПМЖВ без признаков диссекции и дистальной эмболизации. Результат ЧКВ: радикальный.
Ангинозная боль купирована. Пациент переведен в кардиологическое отделение.
ЭКГ при выписке: ритм синусовый, вертикальное положение ЭОС, нормосистолия, патологический зубец Q с отрицательным T I, aVL, V2-V, отрицательный Т II, III, aVF, V2-V6.
ЭХОКГ при выписке: Нарушение локальной и глобальной сократимости ЛЖ. Аневризма в области верхушки ЛЖ с пристеночным тромбом. Дилатация ЛП. Недостаточность АВ клапанов 2 ст. Недостаточность аортального клапана 1 ст. Незначительная гипертрофия ЛЖ.
Выписка: состояние улучшилось - ангинальные боли не рецидивировали, уменьшились признаки сердечной недостаточности, восстановился синусовый ритм, повысилась толерантность к физической нагрузке.
Клинический пример №2.
Пациент, мужчина, 51 год поступил экстренно с жалобами: на жжение в эпигастрии, потливость, слабость. Повышение АД в течение многих лет, мах 160 и 90 мм рт ст. Ухудшение состояния - возникла жгучая боль в эпигастральной области, самостоятельно принимал альмагель с незначительным улучшением. Через два дня вновь возникло чувство жжения в эпигастральной области, распространяющаяся на грудную клетку, принимал корвалол - без эффекта. Боли усилились, продолжались до 40 мин, сопровождались гипотонией, обратился в поликлинику, проведено УЗИ органов брюшной полости, рекомендовано провести ЭКГ. В поликлинике по месту жительства проведена ЭКГ - выявлены очаговые изменения по нижней стенке. Вызвана СМП. Пациент доставлен в СОККД с диагнозом:
Основное: ИБС. Острый коронарный синдром с подъемом ST более 12 часов. Killip 1. Гипертоническая болезнь III ст., риск 4.
Осложнение: Н I. NYHA II ф.кл.
Сопутствующие: Хронический калькулезный холецистит, ремиссия. Аппендектомия в анамнезе.
ЭКГ (при поступлении): ритм синусовый, подъем ST в II, III, AVF, V5-V6, депрессия ST I, AVL, V1-V6.
Проведена экстренная КГ.
Заключение (% стеноза по диаметру; пограничные стенозы D/A - по диаметру/по площади):
Тип кровоснабжения сердца - правый.
Ствол левой коронарной артерии: с неровными контурами.
Передняя межжелудочковая ветвь (ПМЖВ): с неровными контурами, стеноз 90% в дистальной трети 1-го сегмента, стеноз 50% в проксимальной трети 3-го сегмента.
Огибающая артерия (ОА): с неровными контурами, без гемодинамически значимых стенозов.
Правая коронарная артерия (ПКА): с неровными контурами, окклюзия, вызванная массивным тромбозом, в дистальной трети 1-го сегмента, дистальные отделы заполняются через интра- и межкоронарные коллатерали.
Пациенту рекомендуется выполнить ЧКВ ПКА в экстренном порядке.
Налажена инфузия блокаторов гликопротеиновых рецепторов IIb/IIIa по стандартной схеме, выполнена механическая проводниковая реканализация коронарным проводником 0,014”180 см и оптимальная баллонная ангиопластика - без эффекта. Выполнена многократная аспирационная тромбэмболэктомия традиционным аспирационным катетером - тромботических масс не получено, кровоток не восстановлен. Принято решение применить предложенный способ выполнения аспирационной тромбэмболэктомии проводниковым катетером.
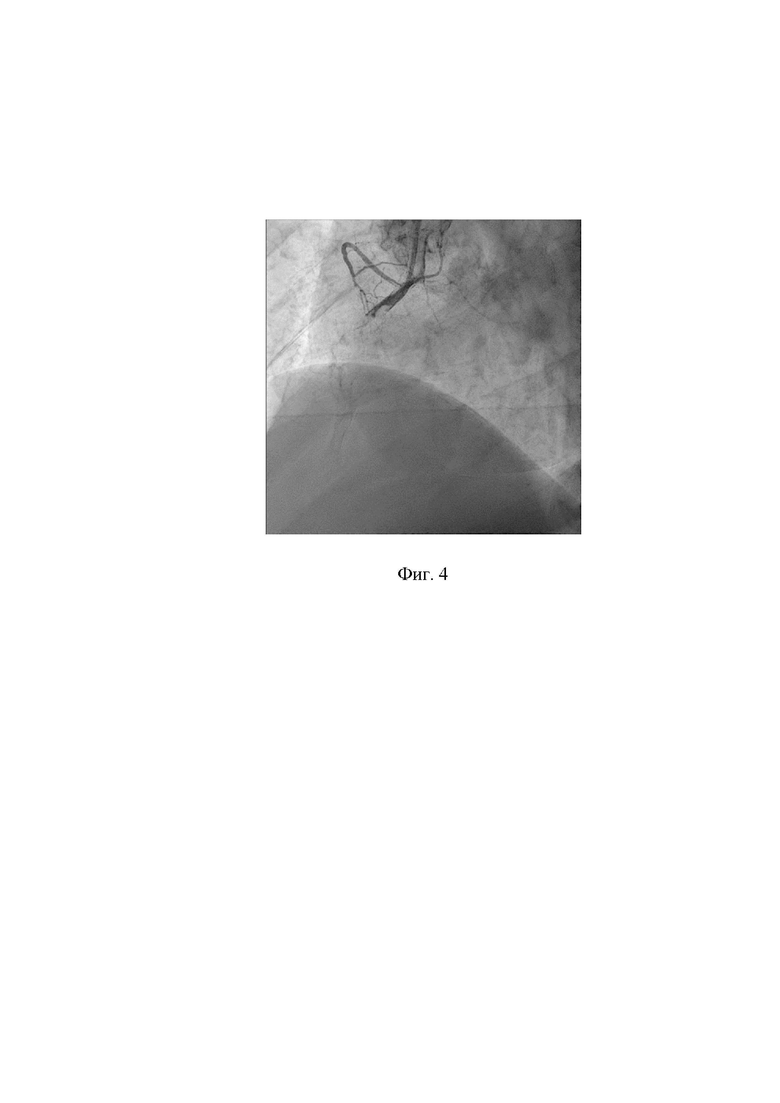
На фигуре 4 показано состояние ПКА до выполнения аспирационной тромбэмболэктомии проводниковым катетером.
Тромбэмболэктомию проводниковым катетером осуществляли следующим образом:
1. Устье ПКА катетеризировано проводниковым катетером 6F (∅ ≈2,0 мм).
2. В дистальные отделы ПКА под контролем рентгеноскопии заведен коронарный проводник 0,014”180 см.
3. По коронарному проводнику за место массивного тромбоза в ПКА под контролем рентгеноскопии заведен баллонный катетер размером 1:1 к диаметру целевой артерии (∅ ≈4,0 мм) для использования техники «якорного баллона».
4. Используя «якорную» технику, подкручивая катетер по часовой стрелке, под контролем рентгеноскопии выполнена глубокая интубация проводниковым катетером за место массивного тромбоза в ПКА.
5. Убран баллонный катетер и коронарный проводник из ПКА.
6. Напрямую к проводниковому катетеру подсоединён аспирационный шприц отрицательного давления (60 мл).
7. На постоянной аспирации, под контролем рентгеноскопии выполнена тракция проводникового катетера на себя, подкручивая катетер против часовой стрелки, до проксимального сегмента ПКА.
8. Убран наполненный тромботическими массами шприц отрицательного давления и дополнительно наполнен шприц (10 мл) кровью и остаточными фрагментами тромботических масс из просвета проводникового катетера.
9. Проводниковый катетер под контролем рентгеноскопии подведен к устью ПКА, не выводя в аорту, для выполнения контрольной коронарографии.
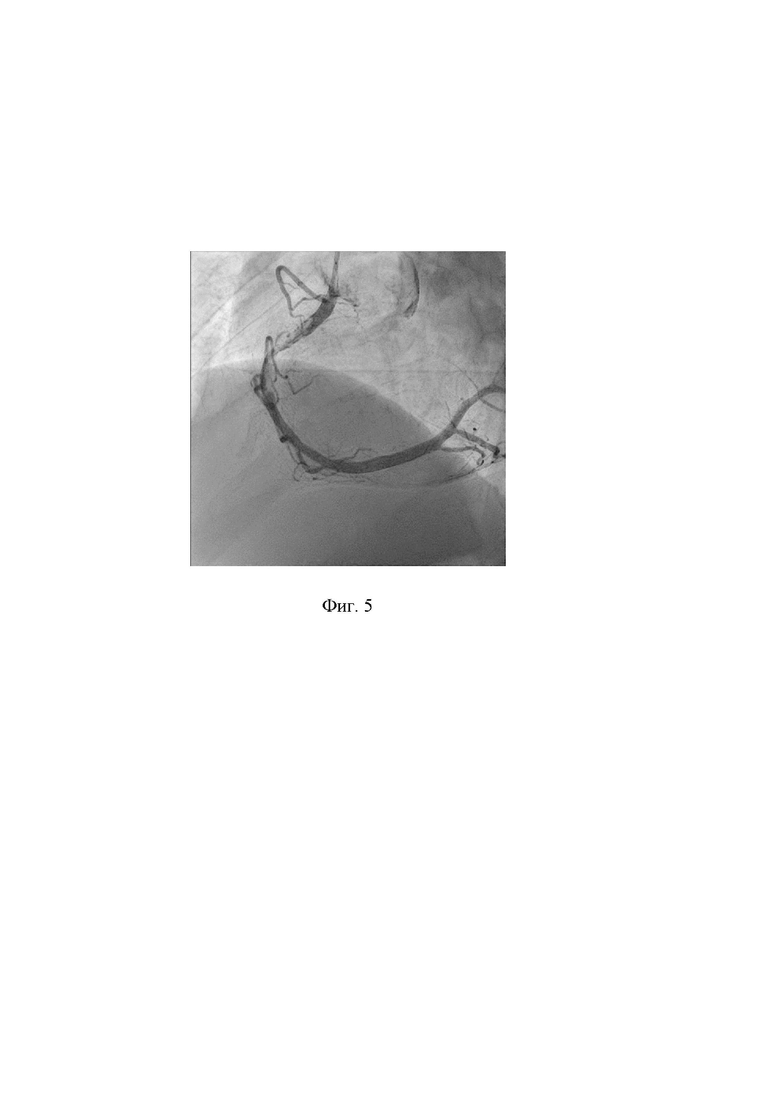
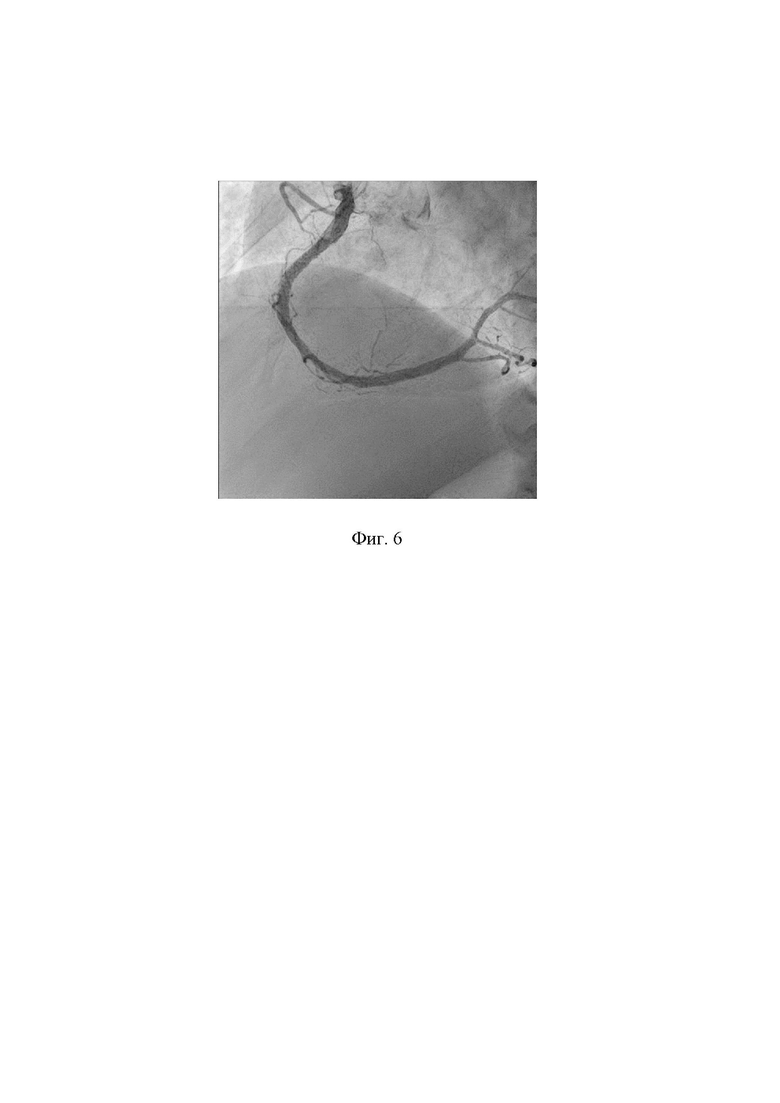
10. Выполнена контрольная коронарография. Проведен анализ полученных результатов - восстановлен антеградный кровоток TIMI III по ПКА без признаков дистальной эмболизации и интраоперационных осложнений, связанных с применением способа. Признаки сохраняющегося пристеночного тромбоза. Стеноз 50% в средней трети задней межжелудочковой ветви (ЗМЖВ). На фигуре 5 показано состояние ПКА после выполнения аспирационной тромбэмболэктомии проводниковым катетером. В зону остаточного стеноза и пристеночного тромбоза в ПКА имплантирован коронарный стент ∅4,0x33 мм. На фигуре 6 показано состояние ПКА после имплантации коронарного стента.
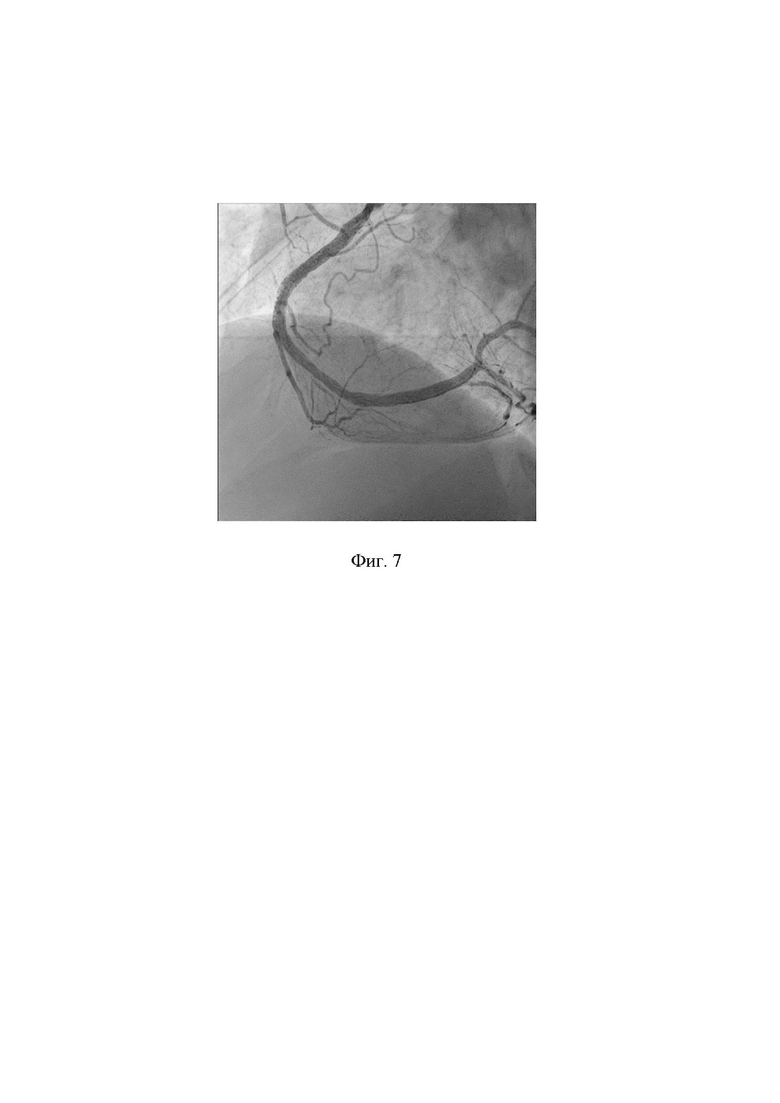
Контрольная коронарография - антеградный кровоток TIMI III по ПКА без признаков дистальной эмболизации, диссекция на проксимальном конце стента. Имплантирован стент в место диссекции ПКА: ∅4,0x12 мм. На фигуре 7 показано состояние ПКА после имплантации дополнительного коронарного стента в зону диссекции.
Контрольная коронарография - антеградный кровоток TIMI III по ПКА без признаков диссекции и дистальной эмболизации. Результат ЧКВ: паллиативный - рекомендовано плановая ЧКВ ПМЖВ.
Ангинозная боль купирована. Пациент переведен в кардиологическое отделение.
ЭКГ (при выписке): ритм синусовый, патологический Q в II, III, aVF; (-)Т в отведениях II, III, aVF.ЭХОКГ при выписке: Нарушение локальной и глобальной сократимости ЛЖ. Диастолическая дисфункция ЛЖ. Атеросклероз аорты.
Выписка: на фоне проведенного лечения состояние улучшилось: уменьшились ангинальные боли, АД стабилизировалось, повысилась толерантность к физической нагрузке. Выписывается с улучшением состояния в удовлетворительном состоянии под наблюдение участкового терапевта, кардиолога. На санаторный этап не направлен: планируется ЧКВ ПМЖВ. Даны рекомендации.
Клинический пример №3.
Пациент, мужчина, 69 лет поступил экстренно с жалобами: на давящие боли за грудиной с иррадиацией в обе руки, чувство нехватки воздуха, выраженную общую слабость; повышение АД до 260 и 120 мм рт. ст.
Анамнез: Повышение АД много лет, максимальное повышение АД до 260 и 120 мм рт. Аортокоронарное шунтирование в 2008г. Коронарография, стентирование ПМЖВ в 2010г. Амбулаторно принимает: АСК, амлодипин, статин, бисопролол.
Ухудшение остро, когда возникли интенсивные сжимающие боли за грудиной, общая слабость, холодный пот, чувство нехватки воздуха. Вызвал СМП. Снята ЭКГ - подъем ST в II III aVF. Пациент доставлен в СОККД с диагнозом: ИБС. ОКС с подъемом ST. Killip I. Госпитализирован в ОРИТ.
ЭКГ (при поступлении): ритм синусовый правильный, нормосистолия, вольтаж удовлетворительный, срединное положение ЭОС, признаки гипертрофии ЛЖ, подъем ST в отведениях II III AVF, депрессия ST в отведениях I aVL.
Проведена экстренная КГ.
Заключение (% стеноза по диаметру; пограничные стенозы D/A - по диаметру/по площади):
Тип кровоснабжения сердца - правый.
Ствол левой коронарной артерии: с неровными контурами.
Передняя межжелудочковая ветвь (ПМЖВ): с неровными контурами, в проксимальном сегменте визуализируется коронарный стент Multi Link 8 (Abbott) ∅4,0х12 мм без признаков рестеноза, кровоток TIMI III. Стеноз 99% в проксимальной трети 2-го сегмента. Окклюзия шунта левой внутренней грудной артерии в проксимальном сегменте.
Огибающая артерия (ОА): с неровными контурами, без гемодинамически значимых стенозов. Протяженный стеноз 30-50% проксимальной трети 1ВТК. Устьевой стеноз 90% ветви второго порядка 1ВТК.
Правая коронарная артерия (ПКА): с неровными контурами, хроническая окклюзия в проксимальном сегменте. Острая окклюзия шунта к ПКА, вызванная массивным тромбозом, в проксимальном сегменте.
Пациенту рекомендуется выполнить ЧКВ шунта к ПКА в экстренном порядке.
Налажена инфузия блокаторов гликопротеиновых рецепторов IIb/IIIa по стандартной схеме, выполнена механическая проводниковая реканализация коронарным проводником 0,014”180 см и оптимальная баллонная ангиопластика - без эффекта. Выполнена многократная аспирационная тромбэмболэктомия традиционным аспирационным катетером - тромботических масс не получено, кровоток не восстановлен. Принято решение применить предложенный способ выполнения аспирационной тромбэмболэктомии проводниковым катетером.
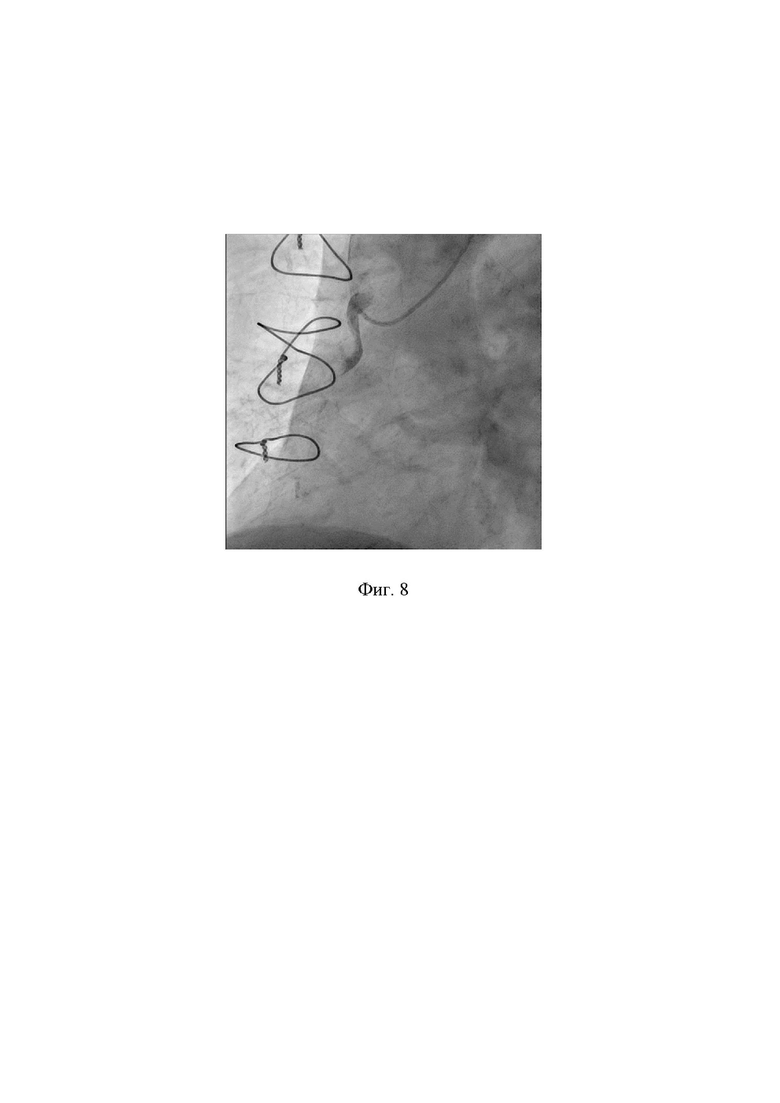
На фигуре 8 показано состояние шунта к ПКА до выполнения аспирационной тромбэмболэктомии проводниковым катетером.
Тромбэмболэктомию проводниковым катетером осуществляли следующим образом:
1. Устье шунта к ПКА катетеризировано проводниковым катетером 5F (∅ ≈1,67 мм).
2. Под контролем рентгеноскопии в дистальные отделы ПКА через шунт к ПКА заведен коронарный проводник 0,014”180 см.
3. По коронарному проводнику за место массивного тромбоза шунта к ПКА под контролем рентгеноскопии заведен баллонный катетер размером 1:1 к диаметру целевой артерии (∅ ≈3,5 мм) для использования техники «якорного баллона».
4. Используя «якорную» технику, подкручивая катетер по часовой стрелке, под контролем рентгеноскопии выполнена глубокая интубация проводниковым катетером за место массивного тромбоза шунта к ПКА.
5. Убран баллонный катетер и коронарный проводник из шунта к ПКА.
6. Напрямую к проводниковому катетеру подсоединён аспирационный шприц отрицательного давления (30 мл).
7. На постоянной аспирации, под контролем рентгеноскопии выполнена тракция проводникового катетера на себя, подкручивая катетер против часовой стрелки, до проксимального сегмента шунта к ПКА, свободного от тромботических масс.
8. Убран наполненный тромботическими массами шприц отрицательного давления и дополнительно наполнен шприц (10 мл) кровью и остаточными фрагментами тромботических масс из просвета проводникового катетера.
9. Проводниковый катетер под контролем рентгеноскопии подведен к устью шунта к ПКА, не выводя в аорту, для выполнения контрольной шунтографии.
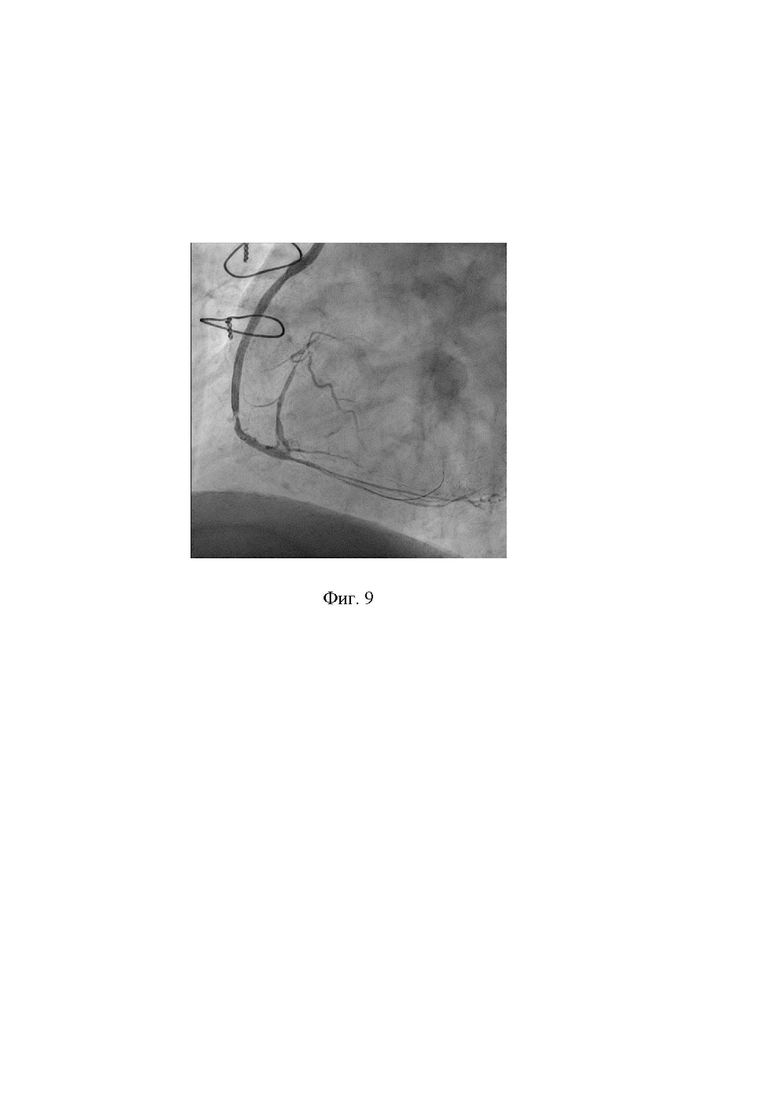
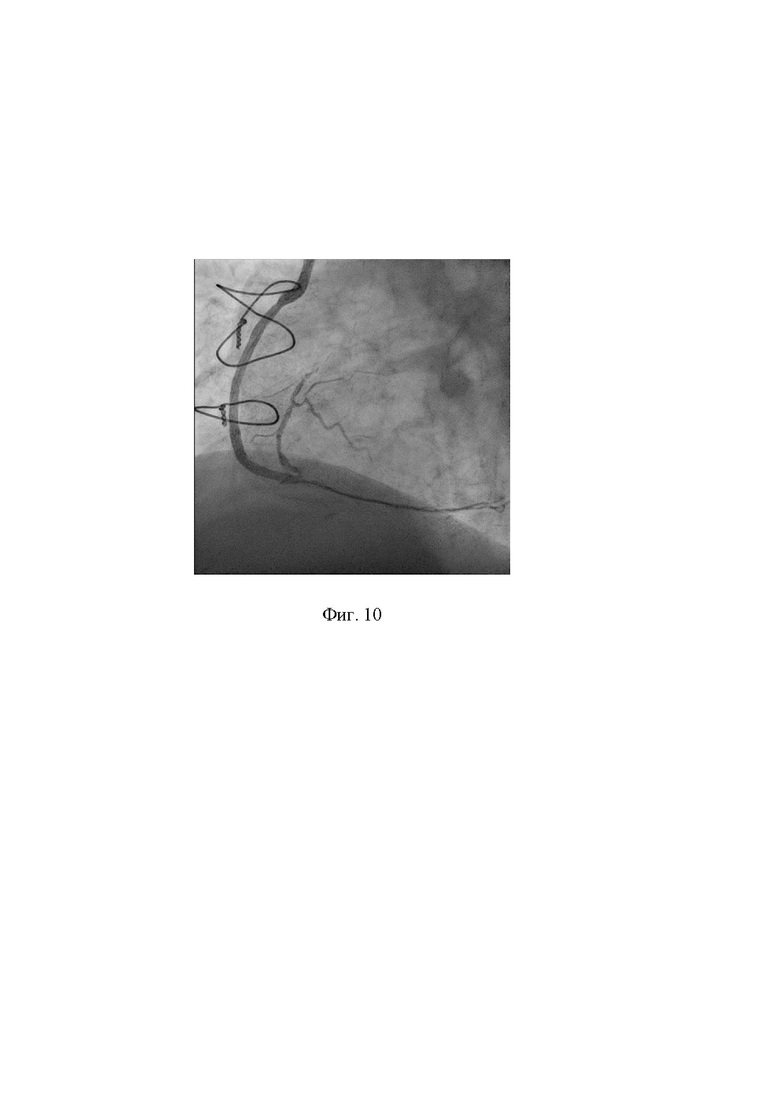
10. Выполнена контрольная шунтография. Проведен анализ полученных результатов - восстановлен антеградный кровоток TIMI III по шунту к ПКА без признаков дистальной эмболизации и интраоперационных осложнений, связанных с применением способа, дистальный анастомоз без особенностей. На фигуре 9 показано состояние шунта к ПКА после выполнения аспирационной тромбэмболэктомии проводниковым катетером. В зону остаточного стеноза шунта к ПКА имплантирован коронарный стент ∅3,5x15 мм. На фигуре 10 показано состояние шунта к ПКА после имплантации коронарного стента.
Контрольная шунтография - антеградный кровоток TIMI III по шунту к ПКА без признаков диссекции и дистальной эмболизации. Результат ЧКВ: паллиативный - рекомендовано плановая ЧКВ ПМЖВ.
Ангинозная боль купирована. Пациент переведен в кардиологическое отделение.
ЭКГ (при выписке): ритм синусовый правильный, ЧСС 77 в мин., вольтаж удовлетворительный, срединное положение ЭОС, признаки гипертрофии ЛЖ, патологический Q и отрицательный T в отведениях II III AVF.
ЭХОКГ при выписке: Нарушение регионарной сократимости ЛЖ. Атеросклероз аорты с дегенеративными изменениями аортального клапана. Недостаточность аортального клапана 1 ст.
Выписка: на фоне проведенного лечения состояние улучшилось: уменьшились ангинальные боли, АД стабилизировалось, повысилась толерантность к физической нагрузке. Выписывается с улучшением состояния в удовлетворительном состоянии под наблюдение участкового терапевта, кардиолога. На санаторный этап не направлен: планируется ЧКВ ПМЖВ. Даны рекомендации.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ эндоваскулярного лечения тромботической окклюзии аутовенозных аортокоронарных шунтов у пациентов с острым инфарктом миокарда с подъемом сегмента ST | 2022 |
|
RU2798161C1 |
| Способ определения послеоперационной тактики ведения пациентов с ишемической болезнью сердца на основе выделенных классов ангиографических результатов чрескожного коронарного вмешательства | 2022 |
|
RU2802854C1 |
| Способ выполнения ручной тромбаспирации у пациентов с острым коронарным синдромом | 2024 |
|
RU2829204C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ИНФАРКТА МИОКАРДА | 2008 |
|
RU2365380C1 |
| СПОСОБ ЭНДОВАСКУЛЯРНОЙ КОРРЕКЦИИ ФЕНОМЕНА "NO-REFLOW" У ПАЦИЕНТОВ С ОСТРЫМ КОРОНАРНЫМ СИНДРОМОМ С ПОДЪЕМОМ СЕГМЕНТА ST ПРИ ПРОВЕДЕНИИ ПЕРВИЧНОГО ЧРЕСКОЖНОГО КОРОНАРНОГО ВМЕШАТЕЛЬСТВА ИНФАРКТ-ЗАВИСИМОЙ АРТЕРИИ | 2014 |
|
RU2574123C1 |
| Способ определения сложного бифуркационного поражения коронарных артерий | 2022 |
|
RU2802855C1 |
| Способ профилактики феномена "no-reflow" при стентировании коронарной артерии у пациентов с острым инфарктом миокарда с подъемом сегмента ST, обусловленным массивным тромбозом | 2021 |
|
RU2786150C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ИНФАРКТА МИОКАРДА | 2018 |
|
RU2702146C1 |
| СПОСОБ КАТЕТЕРИЗАЦИИ СЕРДЦА ДЛЯ УСТАНОВКИ ЭНДОКАРДИАЛЬНОГО ЭЛЕКТРОДА ДЛЯ ВРЕМЕННОЙ ЭЛЕКТРОКАРДИОСТИМУЛЯЦИИ У ПАЦИЕНТОВ С ОСТРЫМ КОРОНАРНЫМ СИНДРОМОМ, С ПОДЪЕМОМ СЕГМЕНТА ST, ОСЛОЖЕННЫМ НАРУШЕНИЯМИ ПРОВОДИМОСТИ (ВАРИАНТЫ) | 2015 |
|
RU2594243C1 |
| Способ лечения больных острым инфарктом миокарда с массивным тромбозом инфаркт-связанной коронарной артерии | 2017 |
|
RU2649572C1 |
Изобретение относится к области практической медицины - кардиологии, сердечно-сосудистой и рентгенэндоваскулярной хирургии, и может применяться во время выполнения чрескожного коронарного вмешательства (ЧКВ) при массивном тромбозе коронарных артерий или аортокоронарных шунтов у пациентов с острым коронарным синдромом (ОКС) при невозможности или неэффективности традиционной тромбэмболэктомии стандартным аспирационным катетером. Способ выполнения аспирационной тромбэмболэктомии проводниковым катетером у пациентов с острым коронарным синдромом включает катетеризацию проводниковым катетером устья целевого сосуда, являющегося коронарной артерией или аортокоронарным шунтом, заведение в дистальные отделы целевого сосуда коронарного проводника под контролем рентгеноскопии, выполнение механической ручной аспирационной тромбэмболэктомии несвязанного внутрисосудистого субстрата из целевого сосуда с помощью аспирационного шприца отрицательного давления под контролем рентгеноскопии. Для катетеризации устья целевого сосуда используют проводниковый катетер 5F диаметром ≈ 1,67 мм или 6F диаметром ≈ 2 мм. В дистальные отделы целевого сосуда под контролем рентгеноскопии заводят коронарный проводник 0,014”180 см или 0,014”190 см. По коронарному проводнику за место массивного тромбоза под контролем рентгеноскопии заводят баллонный катетер размером 1:1 к диаметру целевого сосуда. Используя технику «якорного баллона», под контролем рентгеноскопии выполняют глубокую интубацию проводниковым катетером за место массивного тромбоза, подкручивая катетер по часовой стрелке. Извлекают баллонный катетер и коронарный проводник из целевого сосуда. К проводниковому катетеру напрямую подсоединяют аспирационный шприц отрицательного давления объемом 20-60 мл. При постоянной аспирации, под контролем рентгеноскопии выполняют тракцию проводникового катетера на себя, подкручивая катетер против часовой стрелки, до проксимального сегмента целевого сосуда, свободного от тромбоза. Убирают наполненный тромботическими массами шприц отрицательного давления и дополнительно наполняют шприц объемом 10 мл кровью и остаточными фрагментами тромботических масс из просвета проводникового катетера. Под контролем рентгеноскопии подводят проводниковый катетер к устью целевого сосуда, не выводя в аорту, и выполняют контрольную ангиографию. Техническим результатом является выполнение успешной аспирационной тромбэмболэктомии при массивном тромбозе коронарных артерий или аортокоронарных шунтов, которая включает в себя удаление несвязанного внутрисосудистого субстрата, восстановление кровотока TIMI II - III по целевому сосуду, отсутствие гемодинамически значимой дистальной эмболизации и интраоперационных осложнений, связанных с применением способа. 10 ил.
Способ выполнения аспирационной тромбэмболэктомии проводниковым катетером у пациентов с острым коронарным синдромом,
включающий
катетеризацию проводниковым катетером устья целевого сосуда, являющегося коронарной артерией или аортокоронарным шунтом,
заведение в дистальные отделы целевого сосуда коронарного проводника под контролем рентгеноскопии,
выполнение механической ручной аспирационной тромбэмболэктомии несвязанного внутрисосудистого субстрата из целевого сосуда с помощью аспирационного шприца отрицательного давления под контролем рентгеноскопии,
отличающийся тем, что
для катетеризации устья целевого сосуда используют проводниковый катетер 5F диаметром ≈ 1,67 мм или 6F диаметром ≈ 2 мм;
в дистальные отделы целевого сосуда под контролем рентгеноскопии заводят коронарный проводник 0,014”180 см или 0,014”190 см;
по коронарному проводнику за место массивного тромбоза под контролем рентгеноскопии заводят баллонный катетер размером 1:1 к диаметру целевого сосуда;
используя технику «якорного баллона», под контролем рентгеноскопии выполняют глубокую интубацию проводниковым катетером за место массивного тромбоза, подкручивая катетер по часовой стрелке;
извлекают баллонный катетер и коронарный проводник из целевого сосуда;
к проводниковому катетеру напрямую подсоединяют аспирационный шприц отрицательного давления объемом 20-60 мл;
при постоянной аспирации, под контролем рентгеноскопии выполняют тракцию проводникового катетера на себя, подкручивая катетер против часовой стрелки, до проксимального сегмента целевого сосуда, свободного от тромбоза;
убирают наполненный тромботическими массами шприц отрицательного давления и дополнительно наполняют шприц объемом 10 мл кровью и остаточными фрагментами тромботических масс из просвета проводникового катетера;
под контролем рентгеноскопии подводят проводниковый катетер к устью целевого сосуда, не выводя в аорту, и выполняют контрольную ангиографию.
| Mathews SJ, Brown CL, Kolski BC, et al | |||
| Initial experience with a continuous mechanical aspiration system for thrombus removal before percutaneous coronary intervention | |||
| Catheter Cardiovasc Interv | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Giglioli C, Cecchi E, Sciagra R, et al | |||
| Comparison between Coronary Thrombus aspiration with Angiojet | |||
Авторы
Даты
2023-10-24—Публикация
2023-05-11—Подача