ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композиции для предупреждения, лечения или облегчения состояния при желудочном заболевании, содержащей штамм Corynebacterium sp., продукт его культивирования и треонин.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Язва желудка является причиной самой высокой частоты повреждений желудка и распространена во всем мире у всех народов. Частота язвы желудка увеличивается с развитием отрасли скотоводства, и попытки предупредить возникновение повреждений желудка в аспекте благосостояния животных усиливаются, поскольку, наряду с уменьшением скорости роста вследствие сниженного аппетита, эти симптомы сопровождаются болями.
Треонин (Thr) представляет собой основную аминокислоту (АА), составляющую муцин, защитное вещество для эпителия кишечника. Белок муцин стимулирует всасывание белков и одновременно защищает органы пищеварения от сильнокислотных жидкостей пищеварительного тракта, таких как желудочный сок, и играет важную роль в поддержании здоровья кишечника. Сообщалось, что добавление Thr в корм действительно улучшает здоровье кишечника путем стимулирования синтеза муцина у поросят (непатентный документ 1).
Продуцирование кормового или пищевого Thr осуществляют способом ферментирования микроорганизмами, и типы микроорганизмов, которые используют главным образом, включают Escherichia coli (Е. coli) и Corynebacterium glutamicum (С.glutamicum) и им подобные. Несмотря на продуцирование одной и той же АА, эти два штамма относятся к грамотрицательным и грамположительным бактериям, соответственно. Клеточная стенка как грамотрицательных, так и грамположительных бактерий состоит из пептидогликана (PG). Однако, в случае грамотрицательных бактерий, дополнительно к PG присутствует липополисахаридный (LPS) слой, состоящий из липопротеина и белка, и поскольку Липид А, представляющий собой соматический антиген (О-антиген), присутствует в этом слое LPS, он является токсичным. Следовательно, в фармацевтической промышленности важно удалить из парентеральных лекарственных средств эндогенные токсины с вредными биологическими активностями, такими как пирогенность, летальность, феномен Шварцмана, адъювантная активность и активация макрофагов (непатентный документ 2).
В последнее время продукция аминокислот для корма в форме гранул путем упрощения (или пропуска) процесса глубокой очистки для повышения экономической эффективности пищевых добавок неизбежно связана с попаданием в продукт бактерий, используемых для ферментации, в форме убитых нагреванием бактерий. В нескольких исследованиях показано, что убитые нагреванием бактерии репрезентативных грамположительных бактерий, молочнокислые бактерии, являются стабильными в окружающей среде, обладая сильной устойчивостью к кислоте и нагреванию, и с ними легко работать благодаря возможности получения высоких концентраций, и их используют в качестве пищевого продукта в отношении полезных бактерий, которые населяют кишечник, и следовательно увеличивают активность, усиливающую иммунитет, уникальную для молочнокислых бактерий (непатентный документ 3).
В этом контексте авторы настоящего изобретения поставили задачу разработать фармацевтическую композицию, обладающую эффектом по предупреждению и лечению желудочного заболевания, и в результате подтвердили, что композиция, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин, является эффективной в предупреждении, лечении и облегчении состояния при желудочном заболевании, тем самым создав настоящее изобретение.
ДОКУМЕНТЫ УРОВНЯ ТЕХНИКИ НЕПАТЕНТНЫЕ ДОКУМЕНТЫ
(Непатентный документ 1) Law G. (2000) Threonin requirement and the effect of threonin on gut mucin characteristics in piglets receiving intragastric nutrition. Master thesis of university of Alberta. 1-143.
(Непатентный документ 2) Miyamoto Т., Okono S. and Kasai N (2009) Inactivation of Escherichia coli endotoxin by soft hydrothermal processing. Applied and Environmental Microbiology, 75(15), 5058-5063.
(Непатентный документ 3) Lee I.H. (2018) Latest trend surrounding animal antimicrobial agents and alternatives. Pig & Consulting, 4, 70-73.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ ТЕХНИЧЕСКАЯ ЗАДАЧА
В настоящем изобретении предложена кормовая композиция для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин.
В настоящем изобретении предложена фармацевтическая композиция для предупреждения или лечения желудочного заболевания, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин.
В настоящем изобретении предложена пищевая композиция для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин.
В настоящем изобретении предложена антимикробная композиция против Helicobacter pylori, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин.
ТЕХНИЧЕСКОЕ РЕШЕНИЕ
В одном аспекте предложена композиция для предупреждения, облегчения состояния или лечения желудочного заболевания, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин.
В настоящем изобретении термин "предупреждение" может означать любые действия, которые ингибируют или отсрочивают возникновение заболевания, путем введения композиции согласно одному из примеров, и термин "лечение" может означать любые действия, при которых симптомы субъектов с подозрением на заболевание или с началом заболевания облегчаются или изменяются в лучшую сторону при введении композиции согласно одному из примеров, и термин "облегчение" может означать любые действия, которые по меньшей мере уменьшают параметры, относящиеся к состоянию, при котором лечат заболевание, например, тяжесть симптомов, путем введения композиции согласно одному из примеров. Заболевание может представлять собой желудочное заболевание.
В одном аспекте предложена кормовая композиция для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин.
В настоящем изобретении "штамм Corynebacterium sp.(Coryne sp.)" может представлять собой любой штамм Corynebacterium sp.Штамм Corynebacterium sp.может представлять собой, например, Corynebacterium glutamicum, Corynebacterium ammoniagenes, Corynebacterium crudilactis, Corynebacterium deserti, Corynebacterium efficiens, Corynebacterium callunae, Corynebacterium stationis, Corynebacterium singulare, Corynebacterium halotolerans, Corynebacterium striatum, Corynebacterium pollutisoli, Corynebacterium imitans, Corynebacterium testudinoris и/или Corynebacterium flavescens и, более конкретно, он может представлять собой Corynebacterium glutamicum, Corynebacterium ammoniagenes или их комбинацию (Corynebacterium glutamicum и Corynebacterium ammoniagenes).
В одном примере штамм Corynebacterium sp.может иметь продуктивность по треонину. В настоящем изобретении наличие продуктивности по треонину означает проявление способности продуцировать и накапливать треонин в микроорганизме и/или в среде, когда культивируемый микроорганизм культивируют в среде.
Когда композиция для предупреждения, облегчения состояния или лечения желудочного заболевания согласно одному из примеров содержит Corynebacterium glutamicum, (1) эффект предупреждения, облегчения состояния или лечения желудочного заболевания и/или (2) эффективность против Helicobacter pylori могут быть превосходящими по сравнению с композицией, содержащей любые другие виды штаммов Corynebacterium sp., отличные от Corynebacterium glutamicum (например, Corynebacterium efficiens).
Когда композиция для предупреждения, облегчения состояния или лечения желудочного заболевания согласно одному из примеров содержит Corynebacterium ammoniagenes, (1) эффект предупреждения, облегчения состояния или лечения желудочного заболевания и/или (2) эффективность против Helicobacter pylori могут быть превосходящими по сравнению с композицией, содержащей любые другие виды штаммов Corynebacterium sp., отличные от Corynebacterium ammoniagenes (например, Corynebacterium efficiens).
Когда композиция для предупреждения, облегчения состояния или лечения желудочного заболевания согласно одному из примеров содержит Corynebacterium glutamicum и Corynebacterium ammoniagenes, (1) эффект предупреждения, облегчения состояния или лечения желудочного заболевания и/или (2) эффективность против Helicobacter pylori могут быть превосходящими по сравнению с композицией, содержащей любые другие виды штаммов Corynebacterium sp., отличные от Corynebacterium glutamicum и Corynebacterium ammoniagenes (например, Corynebacterium efficiens).
В одном примере превосходящая эффективность композиции против Helicobacter pylori может означать, что антимикробная активность против штамма Helicobacter pylori является превосходящей, или активность по предупреждению апоптоза клеток (например, клеток слизистой желудка), инфицированных Helicobacter pylori, является превосходящей.
Термин "штамм Corynebacterium sp." может означать концентрат микробных клеток, в котором культуральная среда удалена из культурального раствора, и он возможно был подвергнут процессам центрифугирования и/или фильтрования для отделения только концентрата микробных клеток от продукта культивирования.
В одном примере штамм Corynebacterium sp.может присутствовать в форме бактерий, убитых нагреванием. В настоящем изобретении выражение "бактерии, убитые нагреванием" представляет собой понятие, противоположное жизнеспособным бактериям, означая форму, в которой рост бактерий предупрежден путем термической обработки жизнеспособных бактерий и метаболитов, полученных путем ферментации, и тому подобное. Бактерии, убитые нагреванием, могут содержать антимикробные вещества, такие как цитоплазма, клеточная стенка, бактериоцин и тому подобное, полисахариды и/или органические кислоты и тому подобное.
Композиция, содержащая бактерии, убитые нагреванием, согласно одному из примеров может обладать по меньшей мере одной характеристикой, выбранной из группы, состоящей из следующих подпунктов (1)-(6), в отличие от композиции, содержащей жизнеспособные клетки:
(1) превосходящая кислотоустойчивость;
(2) превосходящая устойчивость к нагреванию;
(2) возможность концентрирования до высокой концентрации;
(4) превосходящая стабильность;
(5) легкость в обращении и хранении; и
(6) возможность использования в качестве источника питания в отношении полезных бактерий желудочно-кишечного тракта.
Бактерии штамма Corynebacterium sp.могут быть убиты обработкой по Тиндалю и/или обработкой нагреванием. В одном примере культуральный раствор для стерилизации бактерий штамма Corynebacterium sp.и продукт его культивирования содержит бактерии этого штамма, убитые нагреванием. Например, термическая обработка может быть выполнена при температуре от 60 до 130°С в течение от 3 до 30 минут. Дополнительно, термическая обработка может быть выполнена путем стерилизации при сверхвысокой температуре, автоклавирования и/или сушки горячим воздухом от одного до 10 раз. Стерилизация при сверхвысокой температуре может быть проведена при температуре от 110°С до 130°С в течение от 3,0 до 10,0 секунд, и например, она может быть проведена при 100°С в течение от 1,0 секунды до 10 секунд двукратно и при 121°С в течение от 1,0 до 10,0 секунд однократно, и автоклавирование может быть выполнено при 120-125°С или при 121°С в течение от 10 минут до 30 минут, от 15 минут до 25 минут или 20 минут, и сушка горячим воздухом может быть выполнена при температуре от 60 до 70°С.
В одном конкретном примере было подтверждено, что композиция, содержащая бактерии штамма Corynebacterium sp., убитые нагреванием, продукт культивирования штамма Corynebacterium sp.и треонин, обладает: (1) превосходящим действием по предупреждению или лечению желудочного заболевания и/или (2) превосходящей эффективностью против Helicobacter pylori in vitro и/или in vivo.
Согласно одному из примеров композиция может содержать штамм Corynebacterium sp.(или бактерии штамма, убитые нагреванием) в концентрации 20-40 OD (оптическая плотность) (длина волны 560-565 нм), 25-35 OD (длина волны 560-565 нм) или 30 OD (длина волны 560-565 нм).
Согласно одному из примеров композиция может содержать 1-100 г/л, 5-100 г/л, 10-100 г/л, 15-100 г/л, 20-100 г/л, 21-100 г/л, 1-80 г/л, 5-80 г/л, 10-80 г/л, 15-80 г/л, 20-80 г/л, 21-80 г/л, 1-60 г/л, 5-60 г/л, 10-60 г/л, 15-60 г/л, 20-60 г/л, 21-60 г/л, 1-50 г/л, 5-50 г/л, 10-50 г/л, 15-50 г/л, 20-50 г/л, 21-50 г/л, 1-30 г/л, 5-30 г/л, 10-30 г/л, 15-30 г/л, 20-30 г/л, 21-30 г/л, 1-25 г/л, 5-25 г/л, 10-25 г/л, 15-25 г/л, 20-25 г/л или 21-25 г/л штамма Corynebacterium sp.(или бактерий штамма, убитых нагреванием) в концентрации 20-40 OD (длина волны 560-565 нм), 25-35 OD (длина волны 560-565 нм) или 30 OD (длина волны 560-565 нм).
Согласно одному из примеров композиция может содержать штамм Corynebacterium sp.(или бактерии штамма, убитые нагреванием) в концентрации 1-100 г/л, 5-100 г/л, 10-100 г/л, 15-100 г/л, 20-100 г/л, 21-100 г/л, 1-80 г/л, 5-80 г/л, 10-80 г/л, 15-80 г/л, 20-80 г/л, 21-80 г/л, 1-60 г/л, 5-60 г/л, 10-60 г/л, 15-60 г/л, 20-60 г/л, 21-60 г/л, 1-50 г/л, 5-50 г/л, 10-50 г/л, 15-50 г/л, 20-50 г/л, 21-50 г/л, 1-30 г/л, 5-30 г/л, 10-30 г/л, 15-30 г/л, 20-30 г/л, 21-30 г/л, 1-25 г/л, 5-25 г/л, 10-25 г/л, 15-25 г/л, 20-25 г/л или 21-25 г/л.
Согласно одному из примеров композиция может содержать штамм Corynebacterium sp.(или бактерии штамма, убитые нагреванием) в количестве 0,1-10% по массе, 0,1-8% по массе, 0,1-5% по массе, 0,1-4% по массе, 0,1-3,5% по массе, 0,1-3% по массе, 0,1-1% по массе, 1-10% по массе, 1-8% по массе, 1-5% по массе, 1-4% по массе, 1-3,5% по массе, 1-3% по массе, 2-10% по массе, 2-8% по массе, 2-5% по массе, 2-4% по массе, 2-3,5% по массе, 2-3% по массе, 3-10% по массе, 3-8% по массе, 3-5% по массе, 3-4% по массе, 3-3,5% по массе, 3,5-10% по массе, 3,5-8% по массе, 3,5-5% по массе или 3,5-4% по массе.
В одном примере штамм Corynebacterium sp.может содержаться в продукте культивирования штамма.
Термин "продукт культивирования" означает продукты, полученные после культивирования штамма Corynebacterium sp., и может содержать ферментированные продукты. В одном примере продукт культивирования может представлять собой ферментированные продукты, полученные при культивировании штамма Corynebacterium sp.в среде. Термин "ферментированные продукты" означает продукты ферментативного или метаболического разрушения органических веществ с использованием микроорганизмов. В настоящем изобретении термин "ферментация" может означать любые действия или процессы, включая ферментативное или метаболическое разрушение органических веществ с использованием микроорганизмов, за исключением реакции гниения.
Продукт культивирования (или ферментированный продукт) может представлять собой суммарный продукт культивирования штамма Corynebacterium sp., его разведенный раствор, концентрат, сухое вещество, лиофилизат и/или лизат и им подобное, и концентрат может быть получен путем центрифугирования или упаривания продукта культивирования, и сухое вещество может быть получено путем высушивания продукта культивирования с использованием сушилки и тому подобного, и лиофилизат может быть получен путем лиофилизации продукта культивирования с использованием лиофилизатора и тому подобного, и лизат может быть получен путем механической или ультразвуковой обработки штамма или продукта культивирования.
Продукт культивирования или ферментированный продукт может находиться в твердой фазе (твердое вещество, например сухое вещество), жидкой фазе (жидкость) или кипящем слое, но не ограничиваясь этим.
В одном примере продукт культивирования может представлять собой любые среды, содержащие культивированный штамм, его метаболит и/или остатки питательного вещества и тому подобное, полученные путем культивирования штамма Corynebacterium sp.в течение определенного периода времени.
В одном примере термин "продукт культивирования" может означать другие компоненты, за исключением штамма (микробных клеток) и/или треонина, в ферментированном продукте, полученном при культивировании штамма Corynebacterium sp.в среде.
В одном примере продукт культивирования может представлять собой такой, из которого штамм Corynebacterium sp.удален или не удален.
В одном примере продукт культивирования может представлять собой культуральный раствор (или продукт культивирования), где штамм удален из культурального раствора, в котором штамм Corynebacterium sp.культивировали в среде. Культуральный раствор (или продукт культивирования), из которого штамм удален, может представлять собой бесклеточный культуральный раствор (или продукт культивирования) или культуральный раствор, содержащий бактерии, убитые нагреванием, и например, может представлять собой фильтрат, из которого штамм удален путем центрифугирования (центрифугированный супернатант) и фильтрации, и/или культуральный раствор (или сухое вещество культурального раствора), содержащий бактерии, убитые нагреванием.
Согласно одному из примеров композиция может содержать продукт культивирования (или ферментированный продукт) в количестве 1-80% по массе, 5-80% по массе, 10-80% по массе, 15-80% по массе, 20-80% по массе, 23-80% по массе, 25-80% по массе, 1-60% по массе, 5-60% по массе, 10-60% по массе, 15-60% по массе, 20-60% по массе, 23-60% по массе, 25-60% по массе, 1-50% по массе, 5-50% по массе, 10-50% по массе, 15-50% по массе, 20-50% по массе, 23-50% по массе, 25-50% по массе, 1-40% по массе, 5-40% по массе, 10-40% по массе, 15-40% по массе, 20-40% по массе, 23-40% по массе, 25-40% по массе, 1-30% по массе, 5-30% по массе, 10-30% по массе, 15-30% по массе, 20-30% по массе, 23-30% по массе, 25-30% по массе, 1-25% по массе, 5-25% по массе, 10-25% по массе, 15-25% по массе, 20-25% по массе или 23-25% по массе. Согласно одному из примеров композиция, содержащая продукт культивирования в вышеуказанном диапазоне, может обладать: (1) превосходящим действием по предупреждению или лечению желудочного заболевания и/или (2) превосходящей эффективностью против Helicobacter pylori по сравнению с композицией, содержащей продукт культивирования в концентрации за пределами вышеуказанного диапазона.
Продукт культивирования может содержать штамм Corynebacterium sp.и может включать штамм Corynebacterium sp.в продукте культивирования в концентрации 0,1-10% по массе, 0,1-8% по массе, 0,1-5% по массе, 0,1-4% по массе, 0,1-3,5% по массе, 0,1-3% по массе, 0,1-1% по массе, 1-10% по массе, 1-8% по массе, 1-5% по массе, 1-4% по массе, 1-3,5% по массе, 1-3% по массе, 2-10% по массе, 2-8% по массе, 2-5% по массе, 2-4% по массе, 2-3,5% по массе, 2-3% по массе, 3-10% по массе, 3-8% по массе, 3-5% по массе, 3-4% по массе, 3-3,5% по массе, 3,5-10% по массе, 3,5-8% по массе, 3,5-5% по массе или 3,5-4% по массе.
В одном примере штамм Corynebacterium sp.и продукт его культивирования может представлять собой продукт культивирования, содержащий бактерии штамма Corynebacterium sp., убитые нагреванием, полученные путем термической обработки (или стерилизации (например, автоклавированием или сушкой горячим воздухом)) продукта культивирования, полученного путем культивирования штамма Corynebacterium sp.в среде в течение определенного периода времени.
В настоящем изобретении термин "культивирование" означает ряд действий по выращиванию и развитию микроорганизма в условиях среды, искусственно отрегулированных подходящим образом. При культивировании можно использовать любые условия культивирования и способ культивирования, известные в данной области техники. Например, культивирование можно выполнять непрерывно в известном способе периодического культивирования, способе непрерывного культивирования, способе периодического культивирования с подпиткой, периодическом процессе или периодическом процессе с подпиткой или повторяющемся периодическом процессе с подпиткой. Затем условия культивирования можно отрегулировать до подходящего рН (например, рН 5-9, рН 6-8 или рН 6,8) с использованием основного соединения (например: гидроксида натрия, гидроксида калия или аммония) или кислотного соединения (например: фосфорной кислоты или серной кислоты), но не ограничиваясь этим. В одном примере образование пузырьков можно ингибировать с использованием пеногасителя, такого как сложный полигликолевый эфир жирной кислоты, и/или аэробные условия можно поддерживать путем подведения кислорода или кислородсодержащей смеси газов к культивируемому продукту.
В одном примере температура в культуре может составлять 20-45°С, 25-40°С, 30-40°С, 30-35°С или 35-40°С, и условие культивирования может представлять собой 100-500 об/мин, 150-300 об/мин, 150-250 об/мин или 200 об/мин, и время культивирования (период) может составлять 1-160 часов, 10-100 часов, 12-72 часа, 24-72 часа, 30-60 часов, 40-50 часов, 45-50 часов или 48 часов. Период культивирования можно продолжать до тех пор, пока желаемое вещество (например L-треонин, треонин) не будет получено в желательном количестве. В одном примере культивирование можно выполнять при температуре культивирования в вышеуказанном диапазоне в течение времени культивирования в вышеуказанном диапазоне.
Среда, используемая для культивирования, должна удовлетворять условиям определенного штамма соответствующим образом, и специалисты в данной области техники могут использовать ее подходящим образом в соответствии с известным содержанием. Согласно одному из примеров ссылку на среду для культивирования штамма Corynebacterium sp.можно найти в известных публикациях (например, Manual of Methods for General Bacteriology. American Society for Bacteriology. Washington D.C., USA, 1981), но не ограничиваясь этим.
Для культивирования штамма Corynebacterium sp.требования для выживания определенного штамма могут быть удовлетворены соответствующим образом путем регулирования температуры, рН и тому подобного, в анаэробных условиях в обычной среде, содержащей подходящие источники углерода, источники азота, аминокислоты, витамины и тому подобное. В качестве источников углерода для использования в среде можно применять сахарид и углевод (например глюкозу, сахарозу, лактозу, фруктозу, мальтозу, мелассу, крахмал и целлюлозу), масло и жир (например, соевое масло, подсолнечное масло, арахисовое масло и кокосовое масло), жирную кислоту (например пальмитиновую кислоту, стеариновую кислоту и линолевую кислоту), спирт (например глицерин и этанол) и органическую кислоту (например уксусную кислоту) и тому подобное, по отдельности или в комбинации, но не ограничиваясь этим. В качестве источника азота можно использовать азотсодержащее органическое соединение (например: пептон, дрожжевой экстракт, мясной бульон, солодовый экстракт, кукурузный экстракт, соевую муку крупного помола и мочевину) или неорганическое соединение (например: сульфат аммония, хлорид аммония, фосфат аммония, карбонат аммония и нитрат аммония) и тому подобное, раздельно или в комбинации, но не ограничиваясь этим. В качестве источника фосфата можно использовать дигидроортофосфат калия, гидроортофосфат калия, соответствующие им азотсодержащие соли и тому подобное, раздельно или в комбинации, но не ограничиваясь этим. Дополнительно культуральная среда может содержать другие соли металлов (например, сульфат магния или сульфат железа), необходимые для роста, и/или содержать необходимые для роста вещества, такие как аминокислоты и витамины, но не ограничиваясь этим.
В одном примере среда может представлять собой среду для продуцирования треонина (например, среда по. 435), и штамм Corynebacterium sp.и продукт его культивирования может представлять собой продукт культивирования, при котором штамм Corynebacterium sp.культивируют в среде для продуцирования треонина, и треонин может высвобождаться в культуральную среду или содержаться в клетках.
В одном примере штамм Corynebacterium sp.и/или продукт его (штамма Corynebacterium sp.) культивирования может содержать треонин.
В одном примере штамм Corynebacterium sp.и/или продукт его культивирования может не содержать треонин.
В настоящем изобретении "треонин (Thr)" представляет собой гидрокси-а-аминокислоту и представляет собой одну из незаменимых аминокислот, которые не продуцируются в организме, подразумевая аминокислоту, имеющую химическую формулу НO2ССН(NН2)СН(ОН)СН3. Треонин может представлять собой оптический изомер типа L (треонин L-типа (L-Треонин, L-Thr)), типа D или их комбинацию. Треонин представляет собой незаменимую аминокислоту и входит в состав муцина, защитного вещества для кишечного эпителия, и когда его недостаточно, это может вызывать остановку роста и потерю веса.
Согласно одному из примеров, когда штамм Corynebacterium sp., продукт его культивирования и/или треонин смешаны, может проявляться: (1) синергетически превосходящий эффект предупреждения или лечения желудочного заболевания и/или (2) синергетически превосходящая эффективность против Helicobacter pylori.
Согласно одному из примеров композиция может содержать треонин в количестве 50-90% по массе, 50-85% по массе, 50-80% по массе, 50-75% по массе, 50-70% по массе, 55-90% по массе, 55-85% по массе, 55-80% по массе, 55-75% по массе, 55-70% по массе, 60-90% по массе, 60-85% по массе, 60-80% по массе, 60-75% по массе, 60-70% по массе, 65-90% по массе, 65-85% по массе, 65-80% по массе, 65-75% по массе, 65-70% по массе, 70-90% по массе, 70-85% по массе, 70-80% по массе, 70-75% по массе или 70% по массе. Композиция, содержащая треонин в вышеуказанном диапазоне, может оказывать (1) превосходящее действие по предупреждению или лечению желудочного заболевания и/или (2) обладать превосходящей эффективностью против Helicobacter pylori в сравнении с композицией, содержащей треонин в концентрации, выходящей за пределы вышеуказанного диапазона.
Треонин может быть доступен в продаже или может быть получен методом экстракции, методом ферментации, ферментативным методом и/или методом синтеза и тому подобными. Например, он может быть получен путем получения ферментированного продукта, содержащего треонин, с использованием штамма Соrуnе-типа и последующей его очистки, или быть синтезирован по пути биосинтеза треонина, и/или синтезирован химически.
Согласно одному из примеров в композиции треонин может (1) содержаться в штамме Corynebacterium sp.и/или продукте его культивирования, или (2) дополнительно содержаться в форме, которая не содержится в штамме Corynebacterium sp.и/или продукте его культивирования, или (3) содержаться в их комбинации (например, штамме Corynebacterium sp.и продукте его культивирования, содержащемся в композиции, содержащей треонин и, кроме того, дополнительно содержать треонин).
Треонин, содержащийся в композиции, согласно одному из примеров, может:
(1) содержаться в штамме Corynebacterium sp., продукте его культивирования или в обоих (штамме и продукте культивирования); или
(2) быть добавленным отдельно; или
(3) содержаться в штамме Corynebacterium sp., продукте его культивирования или в обоих (штамме и продукте культивирования) и быть добавленным туда дополнительно (отдельно).
Случай, когда треонин добавляют отдельно, может означать дополнительное добавление очищенного треонина в добавление к треонину, содержащемуся в штамме и/или продукте культивирования.
Треонин может быть представлен в форме порошка и/или гранул. Треонин в форме гранул может иметь размер частиц 100-1000 мкм или 200-1000 мкм.
Согласно одному из примеров композиция может содержать 0,1-5 частей по массе штамма Corynebacterium sp., 10-90 частей по массе продукта культивирования и 10-80 частей по массе треонина. В частности, может содержать 0,2-5 частей по массе штамма, 12-88 частей по массе продукта культивирования и 10,5-78 частей по массе треонина; 0,3-5 частей по массе штамма, 13-87 частей по массе продукта культивирования и 11-77 частей по массе треонина; 0,4-5 частей по массе штамма, 14-86 частей по массе продукта культивирования и 11,5-76 частей по массе треонина; 0,5-5 частей по массе штамма, 15-85 частей по массе продукта культивирования и 12-75 частей по массе треонина; 0,6-5 частей по массе штамма, 16-84 части по массе продукта культивирования и 12,5-74 части по массе треонина; 0,7-5 частей по массе штамма, 17-83 части по массе продукта культивирования и 13-73 части по массе треонина; 0,8-5 частей по массе штамма, 18-82 части по массе продукта культивирования и 13,5-72 части по массе треонина; 0,9-5 частей по массе штамма, 19-81 часть по массе продукта культивирования и 14-71 часть по массе треонина; 0,9-4 части по массе штамма, 20-80 частей по массе продукта культивирования и 14-70 частей по массе треонина; 1-4 части по массе штамма, 21-79 частей по массе продукта культивирования и 14-69 частей по массе треонина или 1-3 части по массе штамма, 22-78 частей по массе продукта культивирования и 14-68 частей по массе треонина.
Согласно одному из примеров отношение массы штамма и продукта его культивирования к массе треонина (масса штамма и продукта его культивирования: масса треонина) в композиции может составлять 1:0,1-1:10; 1:0,1-1:5; 1:0,1-1:3; 1:0,2-1:10; 1:0,2-1:5; 1:0,2-1:3; 1:0,5-1:10; 1:0,5-1:5; 1:0,5-1:3; 1:1-1:10; 1:1-1:5; 1:1-1:3; 1:3-1:10; 1:3-1:5 или 1:3.
Согласно одному из примеров композиция может дополнительно содержать лигносульфонат.Когда композиция согласно одному из примеров дополнительно содержит лигносульфонат, (1) эффект предупреждения или лечения желудочного заболевания и/или (2) эффективность против Helicobacter pylori могут становиться превосходящими.
Согласно одному из примеров композиция может дополнительно содержать лигносульфонат для регулирования содержания треонина. Согласно одному из примеров композиция может содержать 0,1-50% по массе, 0,1-30% по массе, 0,1-25% по массе, 0,1-20% по массе, 0,1-15% по массе, 0,1-10% по массе, 0,1-7% по массе, 1-50% по массе, 1-30% по массе, 1-25% по массе, 1-20% по массе, 1-15% по массе, 1-10% по массе, 1-7% по массе, 3-50% по массе, 3-30% по массе, 3-25% по массе, 3-20% по массе, 3-15% по массе, 3-10% по массе, 3-7% по массе, 5- 50% по массе, 5-30% по массе, 5-25% по массе, 5-20% по массе, 5-15% по массе, 5-10% по массе, 5-7% по массе, 6,5-50% по массе, 6,5-30% по массе, 6,5-25% по массе, 6,5-20% по массе, 6,5-15% по массе, 6,5-10% по массе или 6,5-7% по массе лигносульфоната кальция. В одном примере композиция может содержать штамм Corynebacterium sp.и продукт его культивирования в высушенной форме (например, сухое вещество "штамма Corynebacterium sp.и продукта его культивирования"). Сухое вещество может быть получено путем высушивания штамма Corynebacterium sp.и продукта его культивирования, и сухое вещество может содержать треонин. В одном примере высушивание может быть выполнено по меньшей мере одним способом, выбранным из группы, состоящей из вакуумной сушки, сушки горячим воздухом, лиофилизации, сушки на открытом воздухе, тонкослойной сушки и/или вакуумной сушки.
В одном примере композиция может содержать штамм Corynebacterium sp., продукт его культивирования и треонин в высушенной форме (например, сухое вещество "штамма Corynebacterium sp.и продукта его культивирования", содержащее треонин).
Согласно одному из примеров композиция может быть представлена в форме эмульсии, суспензии или раствора в масле или водной среде, или в форме экстракта, порошка, гранулы, таблетки, капсулы или геля (например гидрогеля), и может дополнительно содержать диспергирующий агент или стабилизирующий агент.
Композиция согласно одному определенному примеру может быть получена путем высушивания штамма Corynebacterium sp.и продукта его культивирования (ферментированного продукта), и эта композиция может содержать треонин, штамм Corynebacterium sp.(например, штамм в форме бактерий, убитых нагреванием) и компонент продукта культивирования, отличный от треонина и штамма. В одном примере композиция согласно одному из примеров, полученная путем высушивания штамма Corynebacterium sp.и продукта его культивирования, может находиться в форме гранул, и она может: (1) оказывать превосходящий эффект предупреждения или лечения желудочного заболевания и/или (2) иметь превосходящую эффективность против Helicobacter pylori по сравнению с очищенным треонином в форме порошка.
В настоящем изобретении термин "гранула" означает состояние, в котором порошок агрегирует с образованием частиц в 30-150 раз крупнее, и термин "грануляция" может означать индуцирование такого процесса, при котором исходный материал принимает форму гранул при обработке и тому подобное. В одном примере в процессе высушивания композиции, содержащей штамм Corynebacterium sp., продукт его культивирования и/или треонин, композиция может принимать форму гранул.
В одном примере желудочное заболевание может быть вызвано инфекцией Helicobacter pylori.
В одном примере желудочное заболевание может представлять собой по меньшей мере одно, выбранное из группы, состоящей из гастрита, язвы желудка, язвы двенадцатиперстной кишки, пептической язвы и рака желудка.
Термин "гастрит" означает состояние, при котором вызвано воспаление внутренней стенки желудка, и может возникать язва желудка, так как нарушается баланс атакующих факторов, вызывающих повреждение слизистой, и защитных факторов, защищающих слизистую, в желудке и кишечнике. Атакующие факторы, которые можно рассматривать как причины язвы желудка, включают кислоту желудка, различные типы пищеварительных ферментов, желчь, принимаемые лекарственные средства, спирт, инфекцию Helicobacter pylori, прием нестероидных противовоспалительных препаратов, курение и тому подобное.
Когда композицию согласно одному из примеров используют в качестве кормовой композиции, может быть получена кормовая композиция в форме, в которой композицию согласно одному из примеров добавляют в доступную в продаже кормовую композицию. Корм, в котором можно использовать композицию согласно одному из примеров, предпочтительно представляет собой композицию в форме порошка или пеллет или жидкую композицию, но не ограничиваясь этим. Дополнительно, добавляемое количество композиции по настоящему изобретению, которое добавляют в корм, не требует какого-либо специального ограничения.
В настоящем изобретении термин "корм" может означать любой предписанный натуральный или искусственный рацион, еду и тому подобное или компонент пищи для питания животных, переваривания животными или подходящие для них.
Вид корма специально не ограничен, и можно использовать корма, обычно используемые в данной области техники. Неограничивающий пример корма может включать растительные корма, такие как зерна, корни, побочные продукты переработки пищевых продуктов, водоросли, волокно, побочные фармацевтические продукты, жиры и масла, крахмал, кожуру или зерновые субпродукты или тому подобное; и корма для животных, такие как белки, неорганические вещества, жиры и масла, минеральные вещества, жиры и масла, белки одноклеточных, зоопланктон или пищевые продукты или тому подобное. Их можно использовать по отдельности или в комбинации из двух или более.
Субъект (животное), который можно обеспечивать кормом, содержащим композицию согласно одному из примеров, специально не ограничен, но может представлять собой животных, рыб, ракообразных и/или моллюсков, и например, может представлять собой свинью, корову, лошадь, козу, оленя, овцу, курицу, утку, гуся, индейку, собаку, кошку, кролика или рыбу.
Кормовая композиция может дополнительно содержать эксципиент, разбавитель или добавку. Кормовая композиция может содержать компонент, эффективный для стимуляции роста животных, питательный компонент, пищевую добавку, компонент, улучшающий стабильность при хранении, компонент-материал покрытия, аминокислотный препарат для предупреждения заболевания, витаминный препарат, ферментный препарат, небелковое азотистое соединение, силикатный препарат, буфер, экстрагирующее вещество, пробиотик; ферменты, такие как амилаза, липаза и им подобные; витамины, такие как L-аскорбиновая кислота, холина хлорид, инозитол и им подобные; минеральные вещества, такие как хлорид калия, цитрат железа, оксид магния, фосфаты и им подобные; аминокислоты, такие как лизин, аланин, метионин и им подобные; органические кислоты, такие как фумаровая кислота, масляная кислота, молочная кислота и им подобные или их соли; антиоксиданты, такие как витамин С, витамин Е и им подобные; агенты, ингибирующие плесень, такие как пропионат кальция, и тому подобное; эмульгаторы, такие как лецитин, сложные эфиры глицерина и жирных кислот и им подобные; и/или пигменты и им подобные, дополнительно к компонентам. Хотя выше не описано, согласно одному из примеров кормовая композиция может дополнительно содержать другие питательные вещества в пределах диапазона, который может предположить специалист в данной области техники.
В другом аспекте может быть предложена фармацевтическая композиция для предупреждения или лечения желудочного заболевания, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин. Штамм Corynebacterium sp., продукт его культивирования и треонин, содержащиеся в фармацевтической композиции для предупреждения или лечения согласно одному из примеров, и/или желудочное заболевание, являются такими как описано для кормовой композиции для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании.
Согласно одному из примеров фармацевтическая композиция может дополнительно содержать подходящий носитель, эксципиент или разбавитель, обычно используемый для изготовления фармацевтических композиций. В частности, фармацевтическую композицию можно использовать путем изготовления в форме препарата для перорального введения, такого как порошок, гранула, таблетка, капсула, суспензия, эмульсия, сироп, аэрозоль и тому подобное, наружного применения, суппозиториев и стерильных инъецируемых растворов, каждый согласно общепринятому способу. Носитель, эксципиент и разбавитель, которые содержатся в фармацевтической композиции, могут включать лактозу, декстрозу, сахарозу, сорбит, маннит, ксилит, эритрит, мальтит, крахмал, аравийскую камедь, альгинат, желатин, фосфат кальция, силикат кальция, целлюлозу, метилцеллюлозу, микрокристаллическую целлюлозу, поливинилпирролидон, воду, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния и минеральное масло. Для изготовления в форме препарата используют разбавитель или эксципиент, такой как наполнитель, разбавитель, связывающее вещество, увлажняющий агент, разрыхлитель, поверхностно-активное вещество и им подобные. Твердые композиции для перорального введения включают таблетку, пилюлю, порошок, гранулу, капсулу и им подобное, и эти твердые композиции изготавливают путем смешивания по меньшей мере одного эксципиента, например крахмала, карбоната кальция, сахарозы или лактозы, желатина и им подобного, с композицией. Кроме того, дополнительно к простому эксципиенту композиция может содержать смазывающее вещество, такое как стеарат магния и тальк. Жидкие композиции для перорального введения включают суспензию, жидкость для перорального введения, эмульсию, сироп и им подобное, и дополнительно к общепринятым простым разбавителям, воде и жидкому парафину, могут содержать различные эксципиенты, например увлажняющий агент, подсластитель, освежитель воздуха, консервант и тому подобное. Композиции для парентерального введения включают стерилизованный водный раствор, неводный растворитель, суспензию, эмульсию, лиофилизованную композицию и суппозитории. В качестве неводного растворителя и суспензии можно использовать пропиленгликоль, полиэтиленгликоль, растительное масло, такое как оливковое масло, инъецируемые сложные эфиры, такие как этилолеат и им подобные. В качестве соединения-основы суппозиториев можно использовать Витепсол, Макрогол, Твин 61, масло какао, лаурин (laurinum), глицерожелатин и им подобное.
Согласно одному из примеров фармацевтическую композицию можно вводить в фармацевтически эффективном количестве, и в настоящем изобретении термин "фармацевтически эффективное количество" означает количество, достаточное для лечения или предупреждения заболевания при приемлемом соотношении польза/риск, применимом для медицинского лечения или предупреждения, и уровень эффективной дозы можно определить в соответствии с факторами, включающими тяжесть заболевания, активность лекарственного средства, возраст пациента, массу тела, здоровье, пол, чувствительность пациента к лекарственным средствам, время введения, путь введения и скорость выделения используемой композиции по настоящему изобретению, период лечения, лекарственные средства, используемые в комбинации или одновременно с используемой композицией по настоящему изобретению и другие факторы, известные в области медицины. Согласно одному из примеров фармацевтическую композицию можно вводить как отдельный терапевтический агент или вводить в комбинации с другими терапевтическими агентами, и ее можно вводить последовательно или одновременно с традиционным терапевтическим агентом. Кроме того, ее можно вводить однократно или многократно. Важно вводить количество, обеспечивающее возможность получения максимального эффекта при минимальном количестве без побочных эффектов, принимая во внимание все факторы.
Согласно одному из примеров дозировка фармацевтической композиции может составлять примерно 0,0001-100 мг/кг, в частности 0,001-10 мг/кг, для млекопитающего в сутки. Частота введения фармацевтической композиции по настоящему изобретению может составлять введение один раз в сутки или несколько раз путем разделения дозы, но специально не ограничиваясь этим. Дозировка не ограничивает объем настоящего изобретения ни в каком аспекте.
Согласно одному из примеров фармацевтическая композиция не ограничена способом введения, при условии что она может достигать ткани-мишени. Например, включены внутрисуставная инъекция, пероральное введение, внутриартериальное введение, внутривенное введение или чрескожная инъекция или им подобные.
Дополнительно фармацевтическую композицию можно вводить с помощью любого устройства, способного переносить активное вещество к клетке-мишени.
В другом аспекте настоящего изобретения предложена пищевая композиция для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин. Штамм Corynebacterium sp., продукт его культивирования и треонин, содержащиеся в пищевой композиции для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, и/или желудочное заболевание, являются такими как описано для кормовой композиции для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании.
Пищевые продукты включают мясо, колбасу, хлеб, шоколад, конфеты, легкие закуски, кондитерские изделия, пиццу, лапшу быстрого приготовления, другие виды лапши, жевательную резинку, молочные продукты, включая мороженое, различные виды супа, напитки, чай, питьевые напитки, алкогольные напитки, витаминные комплексы, функциональные пищевые продукты и продукты здорового питания и тому подобное, и включают любые пищевые продукты в обычном понимании.
Термин "функциональные пищевые продукты" означает то же самое, что и "специальное питание, полезное для здоровья (FoSHU)", и обозначает пищевые продукты со значительными медицинскими и лечебными эффектами, которые обработаны так, чтобы эффективно проявлять функцию регуляции организма дополнительно к питательной функции. Здесь "функция(функциональный)" означает получение полезного эффекта при использовании для здоровья, такого как регуляция питательных веществ или физиологических эффектов в соответствии со структурой и функцией организма человека. Пищевые продукты по настоящему изобретению могут быть получены путем общепринятого в данной области техники способа, и могут быть получены путем добавления исходного материала и обычно добавляемого компонента. Кроме того, пищевая композиция может быть приготовлена без ограничений, при условии что ее состав признан пищевым. Пищевая композиция по настоящему изобретению может быть приготовлена в различных формах композиций, и в отличие от обычных лекарственных средств она имеет преимущество в отсутствии побочных эффектов, которые могут возникать при приеме лекарственных средств в течение длительного времени, и имеет превосходную переносимость, и следовательно пищевой продукт по настоящему изобретению можно использовать в качестве добавки для усиления предупреждения язвы желудка или облегчения состояния при язве желудка.
Термин "продукты здорового питания" означает пищевые продукты, оказывающие эффект активного поддержания здоровья или улучшения по сравнению с обычной пищей, и термин "пищевая добавка для здорового питания" означает пищевой продукт, предназначенный для дополнения, полезного для здоровья. В некоторых случаях термины "функциональные пищевые продукты", "пищевые продукты здорового питания" и "пищевые добавки для здорового питания" можно использовать взаимозаменяемо.
В частности, функциональные пищевые продукты представляют собой пищевые продукты, в которых композиция согласно одному из примеров добавлена к пищевым продуктам, таким как напитки, чай, специи, жевательная резинка, кондитерские изделия и тому подобное, или пищевые продукты, изготовленные в форме капсулы, порошка, суспензии и тому подобного, и подразумевается, что они оказывают определенный эффект на здоровье при приеме внутрь, но в отличие от обычных лекарственных средств они имеют преимущество в отсутствии побочных эффектов, которые могут присутствовать при приеме лекарственных средств в течение длительного времени, при использовании пищевых продуктов в качестве исходного материала.
Согласно одному из примеров пищевую композицию можно принимать внутрь ежесуточно, и, следовательно, можно ожидать сильный эффект по предупреждению желудочного заболевания или облегчению состояния при желудочном заболевании, и таким образом ее можно использовать с высокой эффективностью.
Пищевая композиция может дополнительно содержать физиологически приемлемый носитель, и тип носителя специально не ограничен, и можно использовать любой носитель, обычно используемый в данной области техники.
Кроме того, пищевая композиция может содержать дополнительный компонент, который может улучшать запах, вкус, вид и тому подобное при обычном использовании в пищевой композиции. Например, она может содержать витамины А, С, D, Е, B1, В2, В6, В12, ниацин, биотин, фолат, пантотеновую кислоту и им подобные. Кроме того, она может содержать такие минералы как цинк (Zn), железо (Fe), кальций (Са), хром (Cr), магний (Mg), марганец (Mn), медь (Cu), хром (Cr) и им подобные. Кроме того, она может содержать такие аминокислоты как лизин, триптофан, цистеин, валин и им подобные.
Дополнительно пищевая композиция может содержать пищевые добавки, такие как консерванты (сорбат калия, бензоат калия, салициловая кислота, натриевая соль дегидроуксусной кислоты и так далее), дезинфицирующее средство (отбеливающий порошок и высокоэффективный отбеливающий порошок, гипохлорит натрия и так далее), антиоксидант (бутилгидроксианизол (ВНА), бутилгидрокситолуол (ВНТ) и так далее), краситель (анилиновый краситель и так далее), краситель (нитрит натрия, натриевая соль азотистой кислоты и так далее), отбеливающий агент (сульфит натрия), приправа (глутамат натрия MSG и так далее), подсластитель (дульцин, цикламат, сахарин, натрий и так далее), ароматизатор (ванилин, лактоны и так далее), вспенивающее вещество (квасцы, D-битартрат калия и так далее), упрочнитель, эмульгатор, уплотнитель (паста), агент-покрытие, резиновая основа, пеногаситель, растворитель, улучшитель и им подобные. Добавки могут быть выбраны в зависимости от типа пищевого продукта и использованы в подходящем количестве.
Согласно одному из примеров композицию можно добавлять отдельно или использовать с другими пищевыми продуктами или компонентами пищи, и ее можно использовать подходящим образом в соответствии с общепринятым способом. Количество активного ингредиента в смеси можно определить подходящим образом в зависимости от цели его использования (предупреждение, улучшение здоровья или терапевтическое лечение). В целом при приготовлении пищи или напитка пищевую композицию по настоящему изобретению можно добавлять в количестве 50 частей по массе или менее, в частности 20 частей по массе или менее, из расчета на массу пищевого продукта или напитка. Однако, принимая во внимание задачу улучшения здоровья и гигиены в течение длительного периода, может быть предусмотрено содержание, выходящее за нижнюю границу указанного выше диапазона, и поскольку с точки зрения безопасности проблем нет, активный ингредиент можно использовать в количестве, выходящем за верхнюю границу указанного выше диапазона.
В одном примере пищевую композицию можно использовать в качестве композиции в форме напитка, полезного для здоровья, и в этом случае, также как обычный напиток она может содержать дополнительные компоненты, такие как различные ароматизаторы или природные углеводы или тому подобное. Вышеупомянутые природные углеводы могут представлять собой моносахариды, такие как глюкоза и фруктоза; дисахариды, такие как мальтоза и сахароза; полисахариды, такие как декстрин и циклодекстрин; сахарные спирты, такие как ксилит, сорбит, эритрит и им подобные. В качестве подсластителя можно использовать такие натуральные подсластители как тауматин и экстракт стевии; можно использовать искусственные подсластители, такие как сахарин и аспартам и им подобные. Соотношение природных углеводов обычно может составлять примерно 0,01-0,04 г, в частности примерно 0,02-0,03 г, на 100 мл композиции-напитка, полезного для здоровья по настоящему изобретению.
Дополнительно, композиция-напиток, полезный для здоровья может содержать различные питательные вещества, витамины, электролиты, ароматизаторы, красители, пектиновую кислоту, соли пектиновой кислоты, альгинат, соли альгината, органические соли, защитные коллоидные загустители, агенты для подведения рН, стабилизаторы, консерванты, глицерин, спирт или агенты для карбонизации или тому подобное. Кроме того, она может содержать мякоть для приготовления натурального фруктового сока, напитка на основе фруктового сока или напитка на основе овощей. Эти компоненты можно использовать независимо или в комбинации. Соотношение этих добавок не является очень важным, но обычно его выбирают в диапазоне 0,01-0,1 частей по массе на 100 частей по массе композиции-напитка, полезного для здоровья по настоящему изобретению.
Согласно одному из примеров содержание пищевой композиции может составлять различный % по массе, при условии что она проявляет эффект предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, но например, согласно одному из примеров содержание композиции может составлять количество 0,00001-100% по массе, 0,01-80% по массе или 10-50% по массе, из расчета на общую массу пищевой композиции.
Согласно одному из примеров композиция, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин, может предупреждать, лечить или облегчать состояние при желудочном заболевании (например, язве желудка) путем ингибирования пролиферации Helicobacter pylori (Н. pylori) и ингибирования воспаления, окислительного стресса, роста кровеносных сосудов и/или апоптоза, индуцированного Helicobacter pylori.
Согласно одному из примеров композиция, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин, может предупреждать, лечить или облегчать состояние при желудочном заболевании путем стимуляции синтеза и высвобождения слизи, стимуляции регенерации ткани, ингибирования повреждения слизистой желудка, стимуляции регенерации ткани, ингибирования окислительного стресса, ингибирования апоптоза клеток слизистой желудка и/или ингибирования воспаления.
В отношении композиции согласно одному из примеров подтверждено, что существует различие в (1) эффекте предупреждения или лечения желудочного заболевания и/или в (2) эффективности против Helicobacter pylori в зависимости от того, содержит ли она штамм Corynebacterium sp.или нет; содержит ли она штамм Corynebacterium sp.в форме бактерий, убитых нагреванием; типа штамма Corynebacterium sp.; наличия или отсутствия продукта культивирования; наличия или отсутствия треонина; и/или комбинации штамма Corynebacterium sp., продукта его культивирования и треонина, и подтверждено, что композиция согласно одному из примеров имеет наиболее превосходящий эффект.
В другом аспекте предложен способ предупреждения, облегчения состояния или лечения желудочного заболевания, включающий введение композиции (кормовой композиции, пищевой композиции или фармацевтической композиции) для предупреждения, облегчения состояния или лечения желудочного заболевания у субъекта (пациента). Кормовая композиция, пищевая композиция, фармацевтическая композиция и желудочное заболевание являются такими как описано выше.
Согласно одному из примеров способ предупреждения, облегчения состояния или лечения желудочного заболевания может дополнительно включать подтверждение (выбор) субъекта (пациента), требующего предупреждения, облегчения состояния или лечения желудочного заболевания, перед введением.
В настоящем изобретении термин "субъект" может означать любое животное, включая человека, имеющее желудочное заболевание или находящееся в группе риска по развитию желудочного заболевания.
Целевой субъект, к которому применяют способ предупреждения или лечения желудочного заболевания, может представлять собой млекопитающее, включая человека, имеющее желудочное заболевание или находящееся в группе риска по развитию желудочного заболевания, и например, может представлять собой свинью, корову, лошадь, козу, северного оленя, овцу, курицу, утку, гуся, индейку, собаку, кошку, и/или.
В настоящем изобретении термин "введение" означает введение композиции для предупреждения, облегчения состояния или лечения желудочного заболевания целевому субъекту любым подходящим способом, и в отношении пути введения, ее можно вводить различными путями перорального или парентерального введения (например, внутривенным, подкожным, внутримышечным, внутрибрюшинным или местным нанесением), так чтобы она могла достигать ткани-мишени.
Способом предупреждения, облегчения состояния или лечения можно вводить кормовую композицию, пищевую композицию или фармацевтическую композицию согласно одному из примеров в (фармацевтически) эффективной дозе. Подходящее общее количество для ежесуточного приема может быть определено при лечении в пределах корректного диапазона медицинского определения, и его можно вводить однократно или за несколько раз. Однако конкретная терапевтически эффективная доза для конкретного субъекта (пациента) может быть определена иным образом в зависимости от различных факторов, включая конкретную композицию, возраст субъекта (пациента), массу тела, общее состояние здоровья, пол и рацион, время введения, путь введения и скорость секреции композиции, период лечения и лекарственные средства, применяемые с конкретной композицией или применяемые одновременно, и подобных факторов, хорошо известных в области фармацевтики, дополнительно к типу и степени реакции, которая должна быть достигнута, и тому, используются ли другие агенты в некоторых случаях.
В другом аспекте предложена антимикробная композиция против Helicobacter pylori, содержащая штамм Corynebacterium sp., продукт его культивирования и треонин. Штамм Corynebacterium sp., продукт его культивирования и треонин, содержащиеся в антимикробной композиции против Helicobacter pylori, и/или желудочное заболевание, являются такими как описано для фармацевтической композиции для предупреждения или лечения желудочного заболевания.
При комбинировании штамма Corynebacterium sp., продукта его культивирования и треонина согласно одному из примеров антимикробное действие против Helicobacter pylori может быть синергетически превосходящим.
В другом аспекте предложена композиция для предупреждения, облегчения состояния или лечения желудочного заболевания, содержащая штамм Corynebacterium sp.и продукт его культивирования, и штамм и продукт его культивирования может содержать треонин.
В другом аспекте предложена композиция для получения активного ингредиента для предупреждения, облегчения состояния или лечения желудочного заболевания, содержащая штамм Corynebacterium sp.и продукт его культивирования (ферментированный продукт), и штамм Corynebacterium sp.или продукт его культивирования (ферментированный продукт) может включать или содержать треонин.
Композиция для получения активного ингредиента для предупреждения, облегчения состояния или лечения желудочного заболевания может содержать 0,1-5 частей по массе штамма Corynebacterium sp., 10-90 частей по массе ферментированного продукта и 10-80 частей по массе треонина, из расчета на общую массу композиции. В частности, она может содержать 0,2-5 частей по массе штамма, 12-88 частей по массе ферментированного продукта и 10,5-78 частей по массе треонина; 0,3-5 частей по массе штамма, 13-87 частей по массе ферментированного продукта и 11-77 частей по массе треонина; 0,4-5 частей по массе штамма, 14-86 частей по массе ферментированного продукта и 11,5-76 частей по массе треонина; 0,5-5 частей по массе штамма, 15-85 частей по массе ферментированного продукта и 12-75 частей по массе треонина; 0,6-5 частей по массе штамма, 16-84 части по массе ферментированного продукта и 12,5-74 части по массе треонина; 0,7-5 частей по массе штамма, 17-83 части по массе ферментированного продукта и 13-73 части по массе треонина; 0,8-5 частей по массе штамма, 18-82 части по массе ферментированного продукта и 13,5-72 части по массе треонина; 0,9-5 частей по массе штамма, 19-81 часть по массе ферментированного продукта и 14-71 часть по массе треонина; 0,9-4 части по массе штамма, 20-80 частей по массе ферментированного продукта и 14-70 частей по массе треонина; 1-4 части по массе штамма, 21-79 частей по массе ферментированного продукта и 14-69 частей по массе треонина; 1-3 части по массе штамма, 22-78 частей по массе ферментированного продукта и 14-68 частей по массе треонина, из расчета на общую массу композиции, но не ограничиваясь этим.
Композиция для приготовления активного ингредиента для предупреждения или лечения желудочного заболевания может дополнительно содержать лигносульфонат кальция для регуляции содержания треонина. Лигносульфонат кальция может содержаться в количестве 0,1-50% по массе, 0,1-30% по массе, 0,1-25% по массе, 0,1-20% по массе, 0,1-15% по массе, 0,1-10% по массе, 0,1-7% по массе, 1-50% по массе, 1-30% по массе, 1-25% по массе, 1-20% по массе, 1-15% по массе, 1-10% по массе, 1-7% по массе, 3-50% по массе, 3-30% по массе, 3-25% по массе, 3-20% по массе, 3-15% по массе, 3-10% по массе, 3-7% по массе, 5-50% по массе, 5-30% по массе, 5-25% по массе, 5-20% по массе, 5-15% по массе, 5-10% по массе, 5-7% по массе, 6,5-50% по массе, 6,5-30% по массе, 6,5-25% по массе, 6,5-20% по массе, 6,5-15% по массе, 6,5-10% по массе, 6,5-7% по массе, 0,1-18% по массе, 0,1-16% по массе, 0,1-14% по массе, 0,1-13% по массе, 0,1-12% по массе, 0,1-11% по массе, 0,1-9% по массе, 0,1-8% по массе или 0,1-7% по массе, из расчета на общую массу композиции, но не ограничиваясь этим, и его можно добавлять без ограничения, так чтобы достичь желаемого содержания треонина в композиции.
В другом аспекте предложена фармацевтическая композиция для предупреждения или лечения желудочного заболевания, содержащая композицию для получения активного ингредиента для предупреждения или лечения желудочного заболевания.
В другом аспекте предложена пищевая композиция для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, содержащая композицию для получения активного ингредиента для предупреждения или лечения желудочного заболевания.
В другом аспекте предложена кормовая композиция для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, содержащая композицию для получения активного ингредиента для предупреждения или лечения желудочного заболевания.
В другом аспекте предложена композиция для лечения желудочного заболевания, содержащая гранулированную композицию для получения активного ингредиента для предупреждения или лечения желудочного заболевания, содержащая штамм Corynebacterium sp.и продукт его культивирования (ферментированный продукт) в качестве активного ингредиента.
Штамм Corynebacterium sp.и его ферментированный продукт, желудочное заболевание, предупреждение, облегчение состояния и лечение являются такими как описано выше.
В настоящем изобретении термин "композиция" имеет отношение к такой обработке, которая обеспечивает удобство для изготовления, хранения или использования и обеспечивает проявление терапевтического эффекта в достаточной степени, главным образом путем механических операций, например, измельчения, смешивания, перемешивания, выщелачивания (варки) или упаривания или тому подобного без изменения природы лекарственных средств, и дополнительно, полученные таким образом продукты также называют медицинскими препаратами (chemical unabridged dictionary, 2001. 5. 20., Sehwa editorial department).
Добавки, используемые при изготовлении композиции в форме препарата, то есть, наполнитель, разбавитель, связывающее вещество, смачивающий агент, разрыхлитель, растворитель или эксципиент, являются такими как описано выше, и твердые композиции для перорального введения и содержащиеся в ней добавки, жидкие композиции для перорального введения и содержащиеся в них добавки или композиции для парентерального введения и включенные в них добавки являются такими как описано выше.
Композиция может представлять собой твердую композицию, жидкую композицию и псевдоожиженную композицию, но не ограничиваясь этим, и любую композицию, проявляющую эффект предупреждения, лечения и облегчения состояния при язве желудка, можно применять без ограничения.
Композиции являются такими как описано выше.
В другом аспекте предложен способ получения активного ингредиента, обладающего: (1) эффектом по предупреждению, облегчению состояния или лечению желудочного заболевания; и/или (2) антимикробным эффектом против Helicobacter pylori, включающий высушивание штамма Corynebacterium sp.и продукта его культивирования.
Штамм Corynebacterium sp.и продукт его культивирования являются такими как описано выше.
В одном примере высушивание может быть выполнено по меньшей мере одним способом, выбранным из группы, состоящей из вакуумной сушки, сушки горячим воздухом, лиофилизации, сушки на открытом воздухе, сушки в тонком слое и/или вакуумной сушки.
В одном примере при высушивании можно сушить композицию, в которой треонин отдельно добавлен к штамму Corynebacterium sp.и продукту его культивирования.
В одном примере способ получения активного ингредиента может дополнительно включать добавление треонина к сухому веществу, полученному после высушивания.
ПОЛЕЗНЫЕ ЭФФЕКТЫ
Подтверждено, что композиция по настоящему изобретению превосходит по эффективности против Helicobacter pylori в экспериментах на клетках и по эффективности облегчения состояния при язве желудка, эффективности синтеза слизи желудка и тому подобному в экспериментах на животных, и следовательно ее можно применять в качестве фармацевтической композиции для предупреждения или лечения желудочного заболевания, или в качестве пищевой или кормовой композиции для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 показана антимикробная активность против Н. pylori для Групп 1-8.
На Фиг. 2а - Фиг. 2в показаны результаты измерения экспрессии медиаторов воспаления при обработке композициями Групп 1-8 клеток RGM1, инфицированных 100 MOI в течение 6 часов с использованием штамма Н. pylori. В частности, на Фиг. 2а показано изменение экспрессии мРНК Сох-2 в соответствии с обработкой Групп 1-8 в клетках RGM1, инфицированных штаммом H. pylori, и на Фиг. 2б показано изменение экспрессии белка iNOS в соответствии с обработкой Групп 1-8 в клетках RGM1, инфицированных штаммом Н. pylori, и на Фиг. 2в показано изменение экспрессии фосфорилированного белка NF-κВ р65 в соответствии с обработкой Групп 1-8 в клетках RGM1, инфицированных штаммом Н. pylori. GAPDH и β-актин использовали в качестве внутренних контролей мРНК и белка, соответственно.
На Фиг. 2а - Фиг. 6б, N (первая позиция слева) представляет группу отрицательного контроля (не обработанные Н. pylori клетки RGM1), и H.p (вторая позиция слева) представляет группу положительного контроля (обработанные Н. pylori клетки RGM1), и Группы 1-8 представляют результаты в клетках RGM1, инфицированных Н. Pylori, обработанных композициями Групп 1-8.
На Фиг. 3а показано изменение экспрессии белка, относящегося к окислительному стрессу (HIF-1a), в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1. β-актин использовали в группе внутреннего контроля. На Фиг. 3б показан результат измерения изменения концентрации внутриклеточного активного кислорода в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1 (результат по увеличению и уменьшению DCF).
На Фиг. 4а показано изменение экспрессии мРНК НО-1 в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1, и на Фиг. 4б показано изменение экспрессии белков GST(pi) и НО-1 в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1. GAPDH и β-актин использовали в группе внутреннего контроля.
На Фиг. 5 показана эффективность по ингибированию апоптоза в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1. В частности, на Фиг. 5а показано изменение экспрессии белков Вах и Всl-2 в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1, и р-актин использовали в группе внутреннего контроля. На Фиг. 5б показано изменение апоптоза (результаты по окраске TUNEL) в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1.
На Фиг. 6 показан результат изменения ангиогенеза и факторов роста пролиферации слизистой в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1. На Фиг. 6а показано изменение экспрессии белков TGF-β и VEGF в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1, и β-актин использовали в группе внутреннего контроля. На Фиг. 6б показано изменение экспрессии белка β-катенина в соответствии с обработкой Групп 1-8 в инфицированных Н. pylori клетках RGM1, и ламин В использовали в группе внутреннего контроля.
На Фиг. 7а - Фиг. 10, Группы 1-4 означают экспериментальные группы животных 1-4 Таблицы 5.
На Фиг. 7 показана эффективность облегчения состояния при SRMD (обусловленное стрессом заболевание слизистой оболочки) при введении композиции согласно одному из примеров в экспериментальной группе животных модели WIRS. В частности, на Фиг. 7а показаны фотографии патологий желудка каждой экспериментальной группы, и фотографии в двух рядах справа представлены при увеличении ×40. На Фиг. 7б показан (А) Индекс макроскопических повреждений (верхний график слева), (Б) Воспаление; показатель патологии (верхний график справа), (В) Язва/эрозия; показатель патологии (нижний график слева), (Г) Регенерация; показатель патологии (нижний график справа) при введении композиции согласно одному из примеров в экспериментальной группе животных модели WIRS.
На Фиг. 8 показано изменение воспаления, ангиогенеза и сигнальных путей при введении композиции согласно одному из примеров в экспериментальной группе модели животных WIRS. (А) На Фиг. 8а показано изменение экспрессии мРНК iNOS, TNF-α и IFN-γ в экспериментальных группах животных 1-4, и на Фиг. 8б показано изменение экспрессии мРНК PDGF в экспериментальных группах животных 1-4, и на Фиг. 8в показано изменение экспрессии белка р-IκВα в экспериментальных группах животных 1-4, и на Фиг. 8 г показано изменение экспрессии белков p-ERK и p-JNK в экспериментальных группах животных 1-4. GAPDH и β-актин использовали в группе внутреннего контроля мРНК и белка, соответственно.
На Фиг. 9 представлен результат, показывающий изменение апоптоза и клеточного цикла при введении композиции согласно одному из примеров в экспериментальной группе животных модели WIRS. В частности, на Фиг. 9а представлен результат анализа TUNEL, показывающий уровень апоптоза в области SRMD слизистой желудка в экспериментальных группах животных 1-4, и на Фиг. 9б показано изменение экспрессии белков PARP-1, Вс1-2, Вах, расщепляющей каспазы-8 и расщепляющей каспазы -3, и на Фиг. 9в показано изменение экспрессии белков CDK4 и циклин D1. β-актин использовали в качестве группы внутреннего контроля.
На Фиг. 10 показано содержание муцина в ткани желудка экспериментальных групп животных 1-4.
На Фиг. 11 показаны фотографии патологий желудка крыс WIRS, которым вводили образцы, содержащие треонин в различном % по массе. Состав и содержание Образцов 1-5 на Фиг. 11 раскрыты в Таблице 4.
ПОДРОБНОЕ ОПИСАНИЕ ВОПЛОЩЕНИЙ
Ниже изобретение будет описано более подробно посредством примеров для лучшего понимания настоящего изобретения. Однако следующие примеры иллюстрируют содержание настоящего изобретения, и объем настоящего изобретения не ограничен следующими примерами. Примеры настоящего изобретения приведены для более подробного описания настоящего изобретения для специалистов в данной области техники.
Пример 1. Композиция, содержащая штамм Corynebacterium sp., и инфицирование клеток
Пример 1-1. Получение композиции, содержащей штамм Corynebacterium sp.
Для проверки различия в эффективности против Helicobacter pylori, ингибировании апоптоза и защиты клеток штамма композиции, содержащей штамм Corynebacterium sp., и эффективности между штаммами Corynebacterium sp., были получены композиции Группы 1-Группы 8.
Штаммы дикого типа Corynebacterium glutamicum (С.glutamicum), Corynebacterium ammoniagenes (С.ammoniagenes) и Corynebacterium efficiens (С. efficiens) получали от CJ CheilJedang BIO R&D Center (Blossom park) и использовали, и штаммы инокулировали в среду для получения треонина, соответственно, и культивировали при 35°С в течение 48 часов при 200 об/мин. Компоненты и содержание среды для получения треонина раскрыты в следующей Таблице 1.
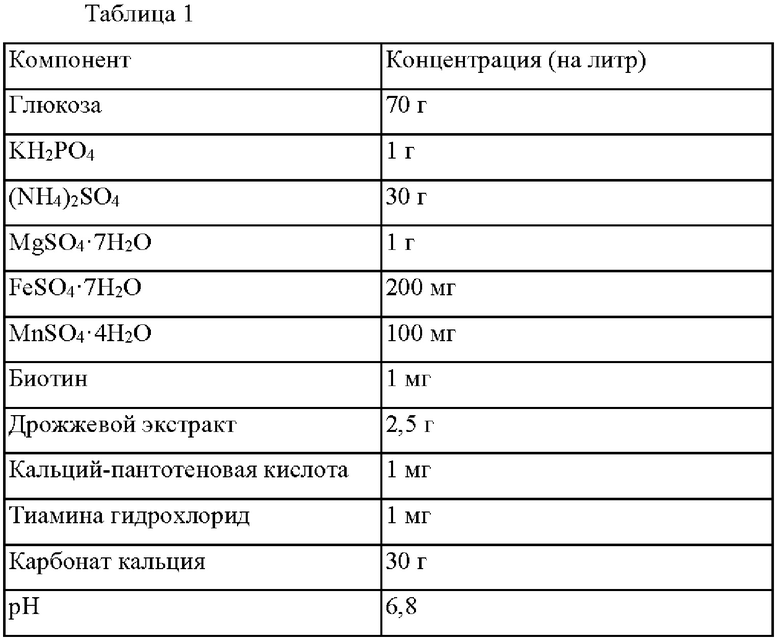
Группа 1 содержит супернатант ферментированной среды, из которой микробные клетки были удалены путем центрифугирования ферментированной среды, полученной путем культивирования Corynebacterium glutamicum в вышеприведенных условиях, а Группа 2 представляет собой буфер (Трис-HCl), содержащий треонин в концентрации 100 г/л. Группы 3-5 были получены путем центрифугирования ферментированной среды, полученной путем культивирования штамма в вышеприведенных условиях для сбора микробных клеток, и ресуспендирования собранных микробных клеток в буфере (Трис-HCl). Группы 6-8 представляют собой ферментированную среду, в которой каждый штамм культивировали в вышеприведенных условиях, и которая содержит каждый штамм и продукт культивирования, при котором каждый штамм был культивирован в среде (раскрыто как "супернатант ферментированной среды" в Таблице 2). Композиции Групп 3-8 содержат каждый штамм в концентрации 30 OD (длина волны 562 нм) и содержат штамм в форме бактерий, убитых нагреванием путем автоклавирования.
Все Группы 1-8 содержат треонин, и есть группа, содержащая треонин в каждом штамме (содержащемся в форме бактерий, убитых нагреванием) или продукт культивирования, и следовательно, треонин (треонин, полученный с помощью штаммов CJ BIO; чистота более 99%) дополнительно добавляли таким образом, чтобы конечная концентрация треонина в Группах 1-8 составила 100 г/л при измерении содержания треонина в штамме и/или продукте культивирования.
Компоненты каждой группы раскрыты в следующей Таблице 2. В Таблице 2 выражение "супернатант ферментированной среды" Группы 1 и Группы 6 означает, что микробные клетки удалены из продукта культивирования, полученного путем культивирования "штамма С.glutamicum" в вышеприведенных условиях, и выражение "супернатант ферментированной среды" Групп 7 и 8 означает, что микробные клетки удалены из продукта культивирования, полученного путем культивирования "штамма С.ammoniagenes" и "штамма С.efficiens" в вышеприведенных условиях.
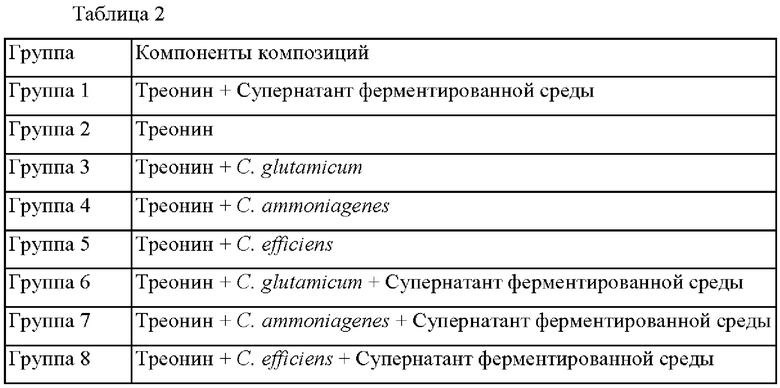
Группы 1-8, раскрытые в следующих Примерах 2-7 и на Фиг. 1 - Фиг. 6б, означают Группы 1-8 Таблицы 2.
Пример 1-2. Культивирование клеточной линии слизистой желудка крысы
Клетки RGM1 клеточной линии слизистой желудка нормальных крыс культивировали в смешанной среде Ham F12 и DMEM (эссенциальная среда, модифицированная по Дульбекко), содержащей 10% эмбриональной сыворотки крупного рогатого скота при 37°С в инкубаторе для клеток (95% воздуха, 5% СО2). Клеточная линия RGM1 была установлена профессором Matsui из Japan Tsukuba University, и использовалась с его согласия.
Пример 1-3. Штамм Н. pylori и инфицирование клеток
Штамм Helicobacter pylori (Н. pylori) (цитотоксин-ассоциированный ген А [CagA]+штамм, NCTC 11637) приобретали в АТСС (Американская коллекция типовых культур, Rockville, MD). Штамм Н. pylori культивировали при встряхивании в условиях 10% CO2 до получения 1X108 КОЕ/мл (OD 600=1) в среде для Бруцеллы с добавлением 5% телячьей сыворотки и антибиотика.
Клетки RGM1 инфицировали штаммом Нpylori в течение 6 часов при множественности заражения (MOI) 100:1 (здесь и далее 100 MOI).
Пример 2. Тестирование эффективности композиции, содержащей штамм Corynebacterium sp., против Helicobacter in vitro
Эффективность по ингибированию роста H. pylori, то есть эффективность против Helicobacter, измеряли на чашках кровяного агара с использованием диско-диффузионного метода. Более подробно, 40 г/л TSA (Соевый агар Trypticase™) растворяли в очищенной воде и затем автоклавировали (121°С, 20 мин). После охлаждения примерно до 50°С добавляли 5% крови овцы и затем добавляли антибиотик {триметоприм (5 мг/л), полимиксин В (2500 ед/л), ванкомицин (10 мг/л)}. Среду разделяли на аликвоты по 20-25 мл в стерильные чашки и затем хранили при 4°С.
200 мкл раствора со штаммом Н. pylori разделяли на аликвоты и распределяли по чашке с кровяным агаром, и 40 мкл каждой композиции Групп 1-8, полученной в Примере 1-1, пропитывали бумажные диски, и культивировали в СО2-инкубаторе при 37°С в течение 48 часов, и затем диаметр чистой зоны вокруг диска измеряли, и он представлен на Фиг. 1 (результат по Группе 1 не представлен на графике). На Фиг. 1 "необработанные" означает клетки RGM1, не инфицированные Н. pylori.
Как показано на Фиг. 1, было подтверждено, что Группы 6 и 7 проявляют значительную активность против Helicobacter, поскольку числовое значение диаметра чистой зоны было значительно выше в Группах 6 и 7 по сравнению с необработанной группой.
Дополнительно была определена подходящая концентрация Групп 1-8 для использования в следующих экспериментах.
Разведенными растворами, в которых композиции Групп 1-8, полученные в Примере 1-1, были разбавлены 1/4, 1/40 или 1/100, обрабатывали Н. pylori по 40 мкл, соответственно, и измеряли жизнеспособность клеток. Так как при разведении концентрации 1/4 жизнеспособность 0,5 или менее была продемонстрирована в многих группах, а при разведении концентрации 1/100 не было очевидного различия результатов между группами, раствор, разведенный 1/40, для которого было показано существенное отличие результата по сравнению с Группой 1, использовали в следующих экспериментах.
Пример 3. Тестирование изменения медиатора воспаления и NF-κB, активирующего транскрипцию этого медиатора, с использованием композиции, содержащей штамм Corynebacterium sp.
Как в способе из Примера 1-3, клетки RGM1, инфицированные Н. pylori (100 MOI), обрабатывали композициями Групп 1-8, разведенными 1/40, по 40 мкл, соответственно, в течение 6 часов. Затем, в клетках RGM1, обработанных этими композициями, уровень экспрессии медиатора воспаления, мРНК Сох-2, подтверждали методом анализа ОТ-ПЦР (ПЦР с обратной транскрипцией), и результат показан на Фиг. 2а.
Более подробно, РНК экстрагировали с использованием TRIzol (Gibco BRL, Rockville, MD), и на матрице экстрагированной РНК синтезировали кДНК с использованием обратной транскриптазы вируса мышиного лейкоза Молони (Perkin Elmer, Morrisville, NC). Последовательность нуклеиновой кислоты каждого праймера, используемого для ПНР-анализа, показана в следующей Таблице 3, и в качестве внутреннего контроля использовали глицеральдегид-3-фосфатдегидрогеназу (GAPDH).
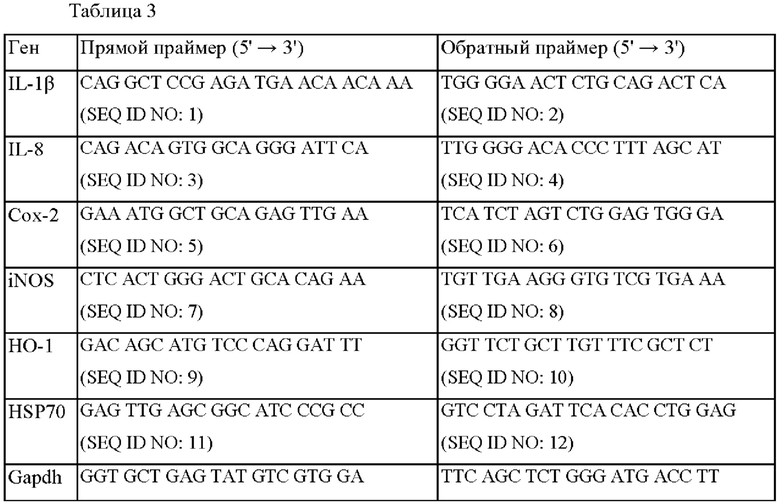

Дополнительно в клетках RGM1, обработанных этими композициями, повышение и понижение уровня экспрессии белка iNOS и фосфорилилирования NF-κB р65, активирующего его транскрипцию, было подтверждено путем анализа методом вестерн-блоттинга, и результат показан на Фиг. 2б и Фиг. 2в.
Более подробно, клетки, культивируемые в условиях обработки композициями, промывали раствором PBS (забуференный фосфатом физиологический раствор) и затем растворяли в буфере для лизиса клеток (150 мМ NaCl, 0,5% Тритон Х-100, 50 мМ трис-НСl, рН 7,4, 25 мМ NaF, 20 мМ этиленгликоль-бис(βN'тетрауксусная кислота, 1 мМ дитиотреитол, 1 мМ Na3VO4, таблетка коктейля ингибитора протеаз [Boehringer, Manneim, Germany]) для получения белкового лизата. После разделения этих белков электрофорезом SDS-PAGE (электрофорез в полиакриламидном геле с додецилсульфатом натрия), несвернутые белки переносили на мембрану PVDF (поливинилиденфторид) (Gelman Sciences, Ann Arbor, MI) для проведения реакции их с первичными антителами и вторичными антителами, соответственно, и затем их анализировали с использованием системы хемилюминесценции.
Как показано на Фиг. 2а, по сравнению с нормальными клетками RGM1 (N), в клетках RGM1, инфицированных Н. pylori (Hp), количество мРНК Сох-2 было значительно увеличено, и повышенная экспрессия мРНК Сох-2, вызванная инфекцией Н. pylori, была наиболее значительно снижена при добавлении композиции Группы 6.
Как показано на Фиг. 2б и Фиг. 2в, экспрессия белка iNOS и фосфорилирование NF-κВ р65, активирующего его транскрипцию, были существенно увеличены при инфекции Н. pylori, но экспрессия белка iNOS и фосфорилирование NF-κВ р65, активирующего его транскрипцию, наиболее существенно уменьшались при добавлении композиции Группы 6. Из этих результатов видно, что композиция согласно одному из примеров регулировала путь передачи воспаления, вызванного штаммом Helicobacter.
Пример 4. Тестирование эффективности композиции, содержащей штамм Corynebacterium sp., по ослаблению окислительного стресса in vitro
Как в способе из Примера 1-3, клетки RGM1, инфицированные Н. pylori (100 MOI), обрабатывали композициями Групп 1-8, разведенными 1/40, по 40 мкл, соответственно, в течение 6 часов. Затем выполняли вестерн-блоттинг таким же способом как в Примере 3 и измеряли уровень экспрессии HIF-1α, ассоциированного с окислительным стрессом, и результат показан на Фиг. 3а.
Как показано на Фиг. 3а, уровень HIF-1a был значительно повышен при инфекции Helicobacter pylori, и экспрессия HIF-1a была значительно снижена в Группах 6 и 7.
Дополнительно для измерения изменения концентрации внутриклеточного активного кислорода, анализировали реакцию усиления DCF с использованием зонда DCF-DA с помощью конфокального устройства для визуализации. Нефлуоресцентное вещество, DCF-DA (2',7'-дихлорфлуоресцеин диацетат) окисляется активными формами кислорода (ROS), когда пероксиды присутствуют в клетке, и проявляет зеленую флуоресценцию, и следовательно количество активных форм кислорода можно непосредственно оценить количественно по интенсивности флуоресценции при определенной длине волны. В частности, клетки RGM-1 (клетки RGM1, необработанные Н. pylori; или клетки RGM1, инфицированные Н. pylori (100 MOI) (Пример 1-3)), 5×105 клеток/лунка распределяли аликвотами в 24-луночный планшет и культивировали в инкубаторе при 37°С (95% воздуха, 5% СО2) в течение ночи, и затем обрабатывали композициями Групп 1-8 в течение определенного времени, соответственно. Клетки промывали DMEM и затем в среду добавляли 10 мкг/мл DCF-DA (2',7'-дихлорфлуоресцеин диацетат, Sigma-Aldrich Co., St Louis, МО) и инкубировали в инкубаторе в течение 30 минут. После инкубации клетки, промытые PBS при 4°С, исследовали визуально и фотографировали под флуоресцентным микроскопом, и результат показан на Фиг. 3б.
Как показано на Фиг. 3б, было подтверждено, что интенсивность флуоресценции DCF-DA, увеличенная после инфицирования Helicobacter pylori, статистически достоверно снижалась в Группах обработки 1, 3, 6 и 8 (Р<0,05), а в Группе обработки 6 степень снижения была самой значительной (Р<0,01). Из этих результатов видно, что композиция согласно одному из примеров может быстро справляться с окислительным стрессом или гипоксической реакцией, вызванными штаммом Helicobacter pylori.
Пример 5. Тестирование эффективности композиции, содержащей штамм Corynebacterium sp., по защите клеток от окислительного стресса, ассоциированного с Helicobacter pylori, in vitro
Как в способе из Примера 1-3, клетки RGM1, инфицированные Н. pylori (100 MOI), обрабатывали композициями Групп 1-8, разведенными 1/40, по 40 мкл, соответственно, в течение 6 часов. Затем изменение экспрессии мРНК НО-1 с антиокислительной функцией, репрезентативного цитопротекторного фактора, анализировали способом в соответствии с Примером 3 (ПЦР) и как показано на Фиг. 4а, и изменение экспрессии белков НО-1 и GST (глутатион-s-трансфераза(рi)) анализировали таким же способом как в Примере 3 (анализ вестерн-блоттингом), и результат представлен на Фиг. 4б.
В результате, как показано на Фиг. 4а и Фиг. 4б, в контрольной группе наблюдали существенное уменьшение количества мРНК и белка НО-1 после инфицирования Helicobacter pylori, и в Группах обработки 6-8 пониженная экспрессия НО-1 существенно повышалась, и среди них в Группе обработки 6 экспрессия НО-1 была наиболее значительно повышена. Дополнительно, как показано на Фиг. 4б, в Группах 6 и 7 экспрессия GST(pi) была существенно понижена, и среди них в Группе обработки 6 экспрессия GST(pi) была наиболее существенно понижена.
Из этих результатов видно, что согласно одному из примеров композиция проявляет анти-окислительное действие и эффективность по защите клеток в основном на основании реакции НО-1 для штамма Helicobacter pylori.
Пример 6. Тестирование эффективности композиции, содержащей штамм Corynebacterium sp., по ингибированию апоптоза, ассоциированного с Helicobacter pylori, in vitro
Как в способе из Примера 1-3, клетки RGM1, инфицированные Н. pylori (100 MOI), обрабатывали композициями из Групп 1-8, разведенными 1/40, по 40 мкл, соответственно, в течение 6 часов. Затем используя способ, подобный способу из Примера 3, экспрессию Всl-2 и Вах подтверждали вестерн-блоттингом, и результат показан на Фиг. 5а, а апоптоз анализировали окрашиванием TUNEL, и результат показан на Фиг. 5б. В частности, окрашивание TUNEL проводили путем аликвотирования клеток в слайд-камере Lab-Tek по 1×105 клеток/камера и затем культивирования в инкубаторе при 37°С (95% воздуха, 5% СО2). Затем после обработки каждым реагентом в течение определенного времени его выполняли согласно экспериментальному методу производителя с использованием набора для детектирования апоптоза (Oncogene Research Products, Cambridge, MA). Культуральный раствор извлекали и промывали раствором PBS 3 раза и затем добавляли 4% PFA (параформальдегид) и фиксировали при комнатной температуре в течение 20 минут. После повторной двукратной промывки PBS проводили обработку 0,1% Тритоном Х-100 при 4°С в течение 5 минут, свет блокировали и затем проводили реакцию с раствором, полученным путем смешивания TdT (концевая дезоксинуклеотидилтрансфераза) и смеси нуклеотидов при 37°С в течение 60 минут. После промывки PBS апоптоз исследовали визуально под флуоресцентным микроскопом.
Как показано на Фиг. 5а, уменьшение экспрессии Всl-2 и увеличение экспрессии Вах можно было наблюдать в клетках, инфицированных Н. pylori (H.p), и было подтверждено, что значительно повышенная экспрессия Вах снижалась, и пониженная экспрессия Всl-2 повышалась в Группах обработки 6-8, и среди них в Группе обработки 6 эффект был наиболее значительным.
Известно, что инфекция Helicobacter pylori вызывает повреждение слизистой и язву путем существенного увеличения апоптоза, и как показано на Фиг. 5б, в результате окрашивания TUNEL наблюдали статистически значимое увеличение апоптоза при инфицировании Helicobacter pylori (Р<0,01), но в Группах обработки 6-8 апоптоз был значительно понижен, и среди них в Группе обработки 6 снижение апоптоза было наиболее значительно.
Пример 7. Тестирование изменения роста клеток, роста кровеносных сосудов и фактора пролиферации, ассоциированных с Helicobacter pylori, при использовании композиции, содержащей штамм Corynebacterium sp.in vitro
Как в способе из Примера 1-3, клетки RGM1, инфицированные Н. pylori (100 MOI), обрабатывали композициями из Групп 1-8, разведенными 1/40 по 40 мкл, соответственно, в течение 6 часов. Затем используя способ, подобный способу из Примера 3, анализировали изменения TGF-β и VEGF путем вестерн-блоттинга, и результат показан на Фиг. 6а.
В результате, как показано на Фиг. 6а, TGF-β и VEGF, повышенные в результате инфицирования Helicobacter pylori, стимулировали беспорядочную пролиферацию слизистой или злокачественное воспаление, но в Группах обработки 6-8 экспрессия TGF-β и VEGF была значительно снижена, и в частности, в Группе обработки 6 экспрессия TGF-β и VEGF снижалась наиболее значительно. Исходя из этого, данный результат продемонстрировал, что согласно одному из примеров композиция может уменьшать воспаление или злокачественное перерождение при инфекции Helicobacter pylori.
Дополнительно, перенос в ядро β-катенина был подтвержден с использованием ядерной фракции клеток, инфицированных Helicobacter pylori, путем вестерн-блоттинга, и результат показан на Фиг. 6б. Как показано на Фиг. 6б, было подтверждено, что перенос в ядро β-катенина, увеличенный при инфекции Helicobacter pylori, может быть существенно ингибирован обработкой Группы 6.
Все экспериментальные значения из Примеров 1-7 были статистически верифицированы методом Стьюдента, и значение р<0,05 или более было определено как статистически значимое.
Пример 8. Получение образца, содержащего треонин
Ферментированную среду, полученную путем инокуляции штамма С.glutamicum дикого типа (CJ CheilJedang BIO R&D Center (Blossom park)) в среду для получения треонина (Таблица 1) и культивирования его в условиях 35°С и 200 об/мин в течение 48 часов, очищали и кристаллизовали с получением Образца 1. Образец 1 содержал 99% или более по массе очищенного треонина в форме порошка.
Ферментированную среду (содержащую С.glutamicum), полученную путем культивирования С.glutamicum в среде для получения треонина, непосредственно высушивали (сушка горячим воздухом при 60-70°С) с получением Образца 2. Дополнительно к ферментированной среде, полученной путем культивирования С.glutamicum в вышеуказанных условиях, добавляли лигносульфонат кальция (Aladdin industrial Co., Shanghai, Chana) в различных концентрациях, и ферментированную среду (содержащую С.glutamicum), в которую был добавлен лигносульфонат кальция, высушивали (сушка горячим воздухом при 60-70°С) с получением Образцов 3-5. Образцы 2-5 содержали С.glutamicum в форме бактерий, убитых нагреванием путем сушки горячим воздухом.
Образцы 2-5 были получены в форме гранул, имеющих размер частиц примерно 200-1000 мкм. Компоненты и содержание Образцов 1-5 раскрыты в Таблице 4. В Таблице 4, Thr (% по массе), лигносульфонат кальция (% по массе) и другие компоненты ферментированного продукта (содержащего микробные клетки С.glutamicum) (% по массе) подразумевают % по массе в сухом веществе, полученном путем высушивания ферментированной среды, и ферментированный продукт в сухом веществе содержит штамм С.glutamicum. Дополнительно содержание штамма С.glutamicum, содержащегося в ферментированном продукте, раскрыто в Таблице 4.
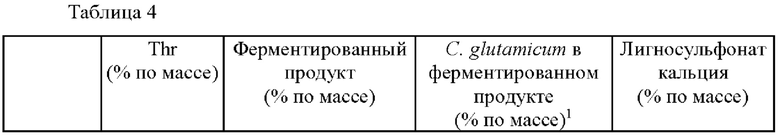
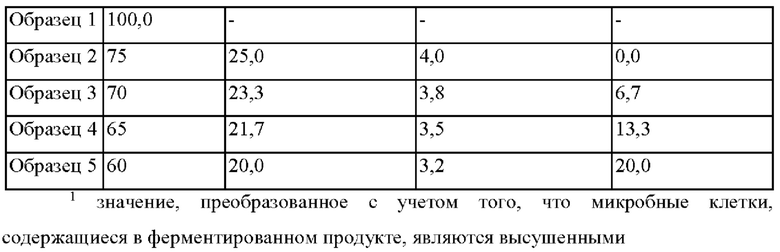
Пример 9. Получение модели WIRS (водно-иммерсионный стресс) для SRMD (обусловленное стрессом заболевание слизистой)
В общей сложности 110 SD крыс приобрели от Charles River (Osaka, Japan) и содержали в виварии. С экспериментальными животными обращались в авторизованном виварии в соответствии с AAALAC International Animal Care Policies. Животные голодали в течение 24 часов до проведения WIRS, и вода была в свободном доступе. 10 крыс из каждой группы помещали в клетку для WIRS и погружали в воду на 6 часов.
Образцы 1-5, полученные в Примере 8, вводили крысам перорально за 8 часов до проведения WIRS, так чтобы было введено одинаковое количество треонина (0,15% по массе/диета), и после проведения WIRS в течение 6 часов животных умерщвляли, извлекали желудок и рассекали, удаляли содержимое и получали изображение внутренней поверхности желудка, и оно представлено на Фиг. 11. Как показано на Фиг. 11, в результате наблюдения ткани желудка крыс невооруженным глазом было подтверждено, что в группе индуцированного WIRS (второй ряд на Фиг. 11), была вызвана гастроррагия, и степень гастроррагии уменьшалась (превосходный терапевтический эффект в отношении язвы желудка) в порядке Образец 1<Образец 5<Образец 4<Образец 3 или Образец 2.
С другой стороны, следующий эксперимент был проведен путем разделения животных на 4 экспериментальные группы, как указано в следующей Таблице 5. Их разделяли на необработанную группу, которая не получала никакой обработки после перорального введения солевого раствора (группа положительного контроля, экспериментальная группа животных 1); группу WIRS, в которой WIRS проводили в течение 6 часов (группа отрицательного контроля, экспериментальная группа животных 2) и экспериментальные группы животных, которым перорально вводили корм, содержащий 0,15% по массе Образца 1 (полученного в Примере 8) (экспериментальная группа животных 3), и корм, содержащий 0,21% по массе Образца 3 (полученного в Примере 8) (экспериментальная группа животных 4), 30 мг/кг массы тела, соответственно, за 8 часов до проведения WIRS. Содержание L-Thr (L-треонина) в корме экспериментальных групп животных 3 и 4 устанавливали на 0,15% по массе/диета равным образом.

Всех экспериментальных животных (крыс) умерщвляли высокой дозой анестетика (тиопентал натрия, 50 мг/кг) через 6 часов WIRS. Экспериментальные группы животных 1-4, раскрытые в следующих Примерах 10-12, означают экспериментальные группы животных 1-4 из Таблицы 5, и на Фиг. 7а - Фиг. 10 Группы 1-4 означают экспериментальные группы животных 1-4 в Таблице 5.
Пример 10. Тестирование эффективности по облегчению состояния при SRMD (обусловленное стрессом заболевание слизистой оболочки)
Желудок крыс, умерщвленных в Примере 9, вырезали и вскрывали вдоль большой кривизны желудка и затем промывали холодным раствором PBS. После определения числа и размера эрозий или язв на увеличенных фотографиях половину вскрывали для анатомических наблюдений. Вырезанный желудок распределяли по пластиковой поверхности и фиксировали 10% буферным формалином в течение 4 часов и использовали для получения парафинового среза ткани, а другую половину хранили в резервуаре с жидким азотом для молекулярно-биологических исследований. Дополнительно хранили гомогенат слизистой животных той же самой экспериментальной группы, полученный путем смешивания.
Образцы желудка исследовали с помощью микроскопа невооруженным глазом (Фиг. 7а), и в контрольной группе и в каждой экспериментальной группе (экспериментальные группы животных 1-4) рассчитывали индекс макроскопического повреждения, воспаление; коэффициент патологии, язва/эрозия; коэффициент патологии, регенерация; коэффициент патологии, и они представлены на Фиг. 7б. Как показано на Фиг. 7а, все крысы экспериментальной группы животных 2 демонстрировали значительную частоту SRMD, таких как эрозии, кровотечения и язвы, но состояние при SRMD значительно облегчалось у животных экспериментальной группы 3 и экспериментальной группы 4. Как показано на Фиг. 7б, индекс макроскопического повреждения, воспаление; коэффициент патологии, язва/эрозия; коэффициент патологии, регенерация; коэффициент патологии были значительно (р<0,05) улучшены в экспериментальных группах животных 3 и 4, и в частности, индекс макроскопического повреждения в экспериментальной группе животных 4 был значительно ниже, чем в экспериментальной группе животных 3, и регенерация; коэффициент патологии был значительно улучшен, чем в экспериментальной группе животных 3.
Пример 11. Тестирование противовоспалительной эффективности
Поскольку SRMD физиологически относится к ишемическому реперфузионному повреждению, в экспериментальных группах животных 1-4 измеряли экспрессию мРНК ангиогенных факторов роста, включая PDGF (тромбоцитарный фактор роста), и экспрессию мРНК медиаторов воспаления, iNOS, TNF-α, IFN-γ и PDGF, и результаты представлены на Фиг. 8а и Фиг. 8б.
В частности, суммарную РНК экстрагировали с помощью RNeasy Mini kit (Qiagen Korea, Seoul, Korea). Праймеры, используемые для измерения экспрессии воспалительных цитокинов и медиаторов, показаны в следующей Таблице 6. Амплификацию анализировали с использованием 10х реакционного буфера (Promega Korea, Seoul, Korea), 1,5 мМ/л MgCl2, 200 мМ/л дезоксинуклеотидтрифосфатов (dNTP), 1 мМ/л каждого праймера и 2,5 единиц ДНК-полимеразы Taq (Promega) с использованием Perkin-Elmer GeneAmp PCR System 2400. Каждый цикл состоял из денатурации при 95°С в течение 1 минуты, отжига при 55°С в течение 45 минут и амплификации при 72°С в течение 45 секунд.
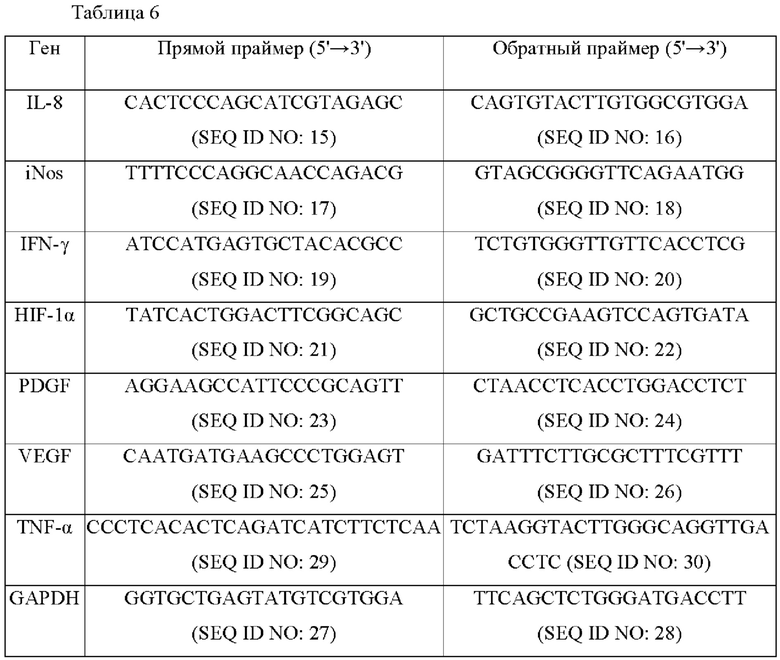
Дополнительно в каждой экспериментальной группе животных 1-4, измеряли уровни белков р-IκВα, p-ERK и р-JNK, и они показаны на Фиг. 8в и Фиг. 8г. В частности, для проведения вестерн-блоттинга для измерения уровня белка собранный материал слизистой желудка гомогенизировали в охлажденном на льду 20 мМ буфере Трис-HCl (рН 7,5), содержащем 2 мМ EDTA (этилендиаминтетрауксусная кислота), 0,5 мМ EGTA (этиленгликольтетрауксусная кислота), 300 мМ сахарозу и 2 мМ PMSF (фенилметилсульфонилфторид) в гомогенизаторе для тканей. После электрофореза 30 мкг белка в 8% геле SDS-PAGE (электрофорез в полиакриламидном геле с додецилсульфатом натрия) его переносили на мембрану PVDF (поливинилиденфторид) с помощью системы полусухого переноса (Hoefer, Holliston, MA, USA). Неспецифическое связывание блокировали путем инкубирования с 5% нежирным сухим молоком. Мембрану термостатически инкубировали в растворе 500-кратного разведения первичных антител при 4°С в течение ночи и затем инкубировали с вторичными антителами, связанными с HRP (пероксидаза хрена), разведенными 1:1000. Иммунный комплекс определяли с использованием набора ECL detection kit (Amersham Biosciences Korea, Seoul, Korea) и рентгеновская пленка засвечивалась автоматически. Для вестерн-блоттинга использовали следующие антитела. Антитела к β-актину, iNOS (синтаза оксида азота), СОХ-2 (циклооксигеназа), P-JNK (фосфорилированная JNK), P-ERK (фосфорилированная ERK), Всl-2 (В-клеточная лимфома 2), Вах (Х-белок, ассоциированный с В-клеточной лимфомой-2) и циклину D1 приобретали от Santa Cruz Biotechnology (Santa Cruz, CA). р-IκВα (фосфорилированный ингибитор каппа В альфа), P-STAT3 (фосфорилированный переносчик сигнала и активатор транскрипции 3), PARP (поли(ADP-рибоза) полимераза), CDK4 (циклин-зависимая киназа 4) и CDK2 (циклин-зависимая киназа 2) приобретали от Cell Signaling Technology (Beverly, MA). Антитела к НО-1 (гемоксигеназа-1) приобретали у Enzo life Sciences (Farmingdale, NY).
Как показано на Фиг. 8а, в экспериментальной группе животных 2 (SRMD, индуцированная WIRD) экспрессия мРНК iNOS, TNF-α и интерферона гамма (IFN-γ) была существенно повышена, но повышенная экспрессия медиаторов воспаления (iNOS, TNF-α, IFN-γ) была значительно снижена в экспериментальной группе животных 3 или экспериментальной группе животных 4 (Р<0,01 или Р<0,05, Фиг. 8а), и экспрессия TNF-α и iFN-γ была существенно снижена, особенно в экспериментальной группе животных 4 по сравнению с экспериментальной группой животных 3 (Р<0,05, Фиг. 8а).
Как показано на Фиг. 8б, экспрессия ангиогенного фактора роста PDGF была существенно повышена в экспериментальной группе животных 2, но она была значительно снижена в экспериментальной группе животных 3 или экспериментальной группе животных 4 (Р<0,01, Фиг. 8б), и в частности, в экспериментальной группе животных 4 степень снижения была более значительной.
Как показано на Фиг. 8в, в результате измерения экспрессии р-IκВα на уровне белка экспрессия р-IκВα была существенно снижена при WIRS в экспериментальной группе животных 2, и снижение экспрессии р-IκВα было связано с активацией транскрипции NF-κВ. Между тем, пониженная экспрессия р-IκВα была существенно повышена (Р<0,01, Фиг. 8в), и экспрессия р-IκВα была существенно повышена в экспериментальной группе животных 4 по сравнению с экспериментальной группой животных 3 (Р<0,01, Фиг. 8в), и повышение экспрессии р-IκВα индуцировало окислительно-восстановительное ингибирование NF-kB.
С другой стороны, в отношении передачи сигнала, относящегося к ишемии и воспалению, как показано на Фиг. 8г, в экспериментальной группе животных 2 была показана активация p-ERK и p-JNK, и в экспериментальной группе животных 4 передача сигнала была полностью инактивирована, а в экспериментальной группе животных 3 она была частично инактивирована (Р<0,01).
Пример 12. Тестирование эффективности по защите слизистой желудка. Поскольку SRMD, вызывающая эрозии или язвы, демонстрировала увеличение апоптоза в соответствующей области, измеряли апоптоз на слизистой желудка в соответствии с экспериментальной группой животных. В частности, апоптоз визуализировали с помощью набора для детекции фрагментации ДНК TdT FragEL (Oncogene Research Products, Cambridge, MA) и метода TUNEL (введение одноцепочечных разрывов и мечение, опосредованное концевой дезоксинуклеотидилтрансферазой). Для измерения AI (апоптотический индекс) путем обнаружения области, в которой происходит апоптоз в большой степени ("горячая точка" апоптоза), в каждой экспериментальной группе, TUNEL-иммуноокрашенный срез (опосредованное концевой дезоксинуклеотидилтрансферазой dUTP введение одноцепочечных разрывов и мечение (TUNEL)-иммуноокрашенный срез) увеличивали в 100 раз и сканировали. Затем число TUNEL-положительных клеток считали в 400 полях для записи AI. Средний коэффициент определяли путем выбора по меньшей мере 5 "горячих точек" случайным образом во фрагментах, включая некротические или язвенные поражения, и результат представлен на Фиг. 9а, и этот результат выражен как средний процент от общего числа клеток. Как показано на Фиг. 9а, уровень апоптоза был существенно повышен в экспериментальной группе животных 2 по сравнению с экспериментальной группой животных 1, и повышенный уровень апоптоза был значительно снижен в экспериментальной группе животных 3 и экспериментальной группе животных 4 по сравнению с экспериментальной группой животных 2 (Р<0,01, Фиг. 9а), и в экспериментальной группе животных 4 наблюдали значительно более низкий уровень апоптоза по сравнению с экспериментальной группой животных 3 (Р<0,01, Фиг. 9а).
Для верификации результатов TUNEL, анализ экспрессии Всl-2, белка, предупреждающего апоптоз, и расщепленного PARP, Вах, расщепляющей каспазы-8 и расщепляющей каспазы-3, индуцирующих апоптоз, методом вестерн-блоттинга проводили способом из Примера 11, и результат показан на Фиг. 9б.
Как показано на Фиг. 9б, расщепление PARP, экспрессия Вах, расщепляющей каспазы-8 и расщепляющей каспазы-3 были существенно повышены в экспериментальной группе животных 2, и повышенные расщепление PARP, экспрессия Вах, расщепляющей каспазы-8 и расщепляющей каспазы-3 были значительно снижены в экспериментальных группах животных 3 и 4, и их наблюдали на значительно более низком уровне, особенно в экспериментальной группе животных 4 по сравнению с экспериментальной группой животных 3. С другой стороны, экспрессия Всl-2, белка, предупреждающего апоптоз, была существенно повышена в экспериментальной группе животных 4 (Фиг. 9б).
Активность CDK4 и циклина D1, генов, регулирующих клеточный цикл, была подтверждена на уровне белка способом согласно Примеру 11, и результат показан на Фиг. 9в. Как показано на Фиг. 9в, экспрессия CDK4 и циклина D1 была существенно повышена в экспериментальной группе животных 2 (Р<0,01), и повышенная экспрессия CDK4 и циклина D1 была существенно снижена в экспериментальных группах животных 3 и 4. В частности, экспрессия CDK4 и циклина D1 была значительно ниже в экспериментальной группе животных 4 по сравнению с экспериментальной группой животных 3 (Фиг. 9в, Р<0,01 ~ 0,05).
В ткани желудка экспериментальных групп животных 1-4 содержание муцина было подтверждено окрашиванием PAS, и результат представлен на Фиг. 10. Как показано на Фиг. 10, в экспериментальной группе животных 2 наблюдали значительно более низкий уровень муцина желудка (Р<0,01), и выработка слизи желудка поддерживалась в значительной степени в экспериментальных группах животных 3 и 4, и выработка слизи была значительно выше в экспериментальной группе животных 4 по сравнению с группой 3 (Р<0,01).
Из вышеизложенных результатов видно, что WIRS ставит под удар целостность слизистой, но эту опасность облегчает предварительная обработка композицией (образцом) согласно одному из примеров.
Результаты из Примеров 8-11 представлены как среднее ±SD. Данные анализировали путем одностороннего дисперсионного анализа (ANOVA), и статистическую значимость между группами определяли с помощью многорангового критерия Дункана. Статистическая значимость сходилась к Р<0,05.
Из вышеприведенного описания специалист в области техники, к которой относится настоящее изобретение, понимает, что настоящее изобретение может быть выполнено в других конкретных формах без изменения его технической идеи или существенных характеристик. В этом отношении следует понимать, что вышеописанные примеры являются иллюстративными во всех аспектах и не ограничивающими. Объем настоящего изобретения следует рассматривать как значение и объем прилагаемой формулы изобретения, в большей степени, чем вышеизложенное подробное описание, и все модификации или модифицированные формы, выводимые из эквивалентной концепции, включены в объем настоящего изобретения.
--->
<110> CJ CheilJedang Corporation
<120> Composition for prevention, treatment or improvement of
gastric
disorders containing Corynebacterium strain and its culture
thereof
<130> OPP20201524KR
<150> KR 10-2019-0071007
<151> 2019-06-14
<160> 30
<170> KoPatentIn 3.0
<210> 1
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> IL-1бета_Прямой
<400> 1
caggctccga gatgaacaac aaa
23
<210> 2
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> IL-1бета_Обратный
<400> 2
tggggaactc tgcagactca
20
<210> 3
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> IL-8_Прямой
<400> 3
cagacagtgg cagggattca
20
<210> 4
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> IL-8_Обратный
<400> 4
ttggggacac cctttagcat
20
<210> 5
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Cox-2_Прямой
<400> 5
gaaatggctg cagagttgaa
20
<210> 6
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Cox-2_Обратный
<400> 6
tcatctagtc tggagtggga
20
<210> 7
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> iNOS_Прямой
<400> 7
ctcactggga ctgcacagaa
20
<210> 8
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> iNOS_Обратный
<400> 8
tgttgaaggg tgtcgtgaaa
20
<210> 9
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HO-1_Прямой
<400> 9
gacagcatgt cccaggattt
20
<210> 10
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HO-1_Обратный
<400> 10
ggttctgctt gtttcgctct
20
<210> 11
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HSP70_Прямой
<400> 11
gagttgagcg gcatcccgcc
20
<210> 12
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> HSP70_Обратный
<400> 12
gtcctagatt cacacctgga g
21
<210> 13
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Gapdh_Прямой
<400> 13
ggtgctgagt atgtcgtgga
20
<210> 14
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Gapdh_Обратный
<400> 14
ttcagctctg ggatgacctt
20
<210> 15
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> IL-8_Прямой
<400> 15
cactcccagc atcgtagagc
20
<210> 16
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> IL-8_Обратный
<400> 16
cagtgtactt gtggcgtgga
20
<210> 17
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> iNos_Прямой
<400> 17
ttttcccagg caaccagacg
20
<210> 18
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> iNos_Обратный
<400> 18
gtagcggggt tcagaatgg
19
<210> 19
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> IFN-гамма_Прямой
<400> 19
atccatgagt gctacacgcc
20
<210> 20
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> IFN-гамма_Обратный
<400> 20
tctgtgggtt gttcacctcg
20
<210> 21
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HIF-1альфа_Прямой
<400> 21
tatcactgga cttcggcagc
20
<210> 22
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HIF-1альфа_Обратный
<400> 22
gctgccgaag tccagtgata
20
<210> 23
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PDGF_Прямой
<400> 23
aggaagccat tcccgcagtt
20
<210> 24
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> PDGF_Обратный
<400> 24
ctaacctcac ctggacctct
20
<210> 25
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> VEGF_Прямой
<400> 25
caatgatgaa gccctggagt
20
<210> 26
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> VEGF_Обратный
<400> 26
gatttcttgc gctttcgttt
20
<210> 27
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> GAPDH_Прямой
<400> 27
ggtgctgagt atgtcgtgga
20
<210> 28
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> GAPDH_Обратный
<400> 28
ttcagctctg ggatgacctt
20
<210> 29
<211> 26
<212> DNA
<213> Artificial Sequence
<220>
<223> TNF-альфа_Прямой
<400> 29
ccctcacact cagatcatct tctcaa
26
<210> 30
<211> 27
<212> DNA
<213> Artificial Sequence
<220>
<223> TNF-альфа_Обратный
<400> 30
tctaaggtac ttgggcaggt tgacctc
27
<---

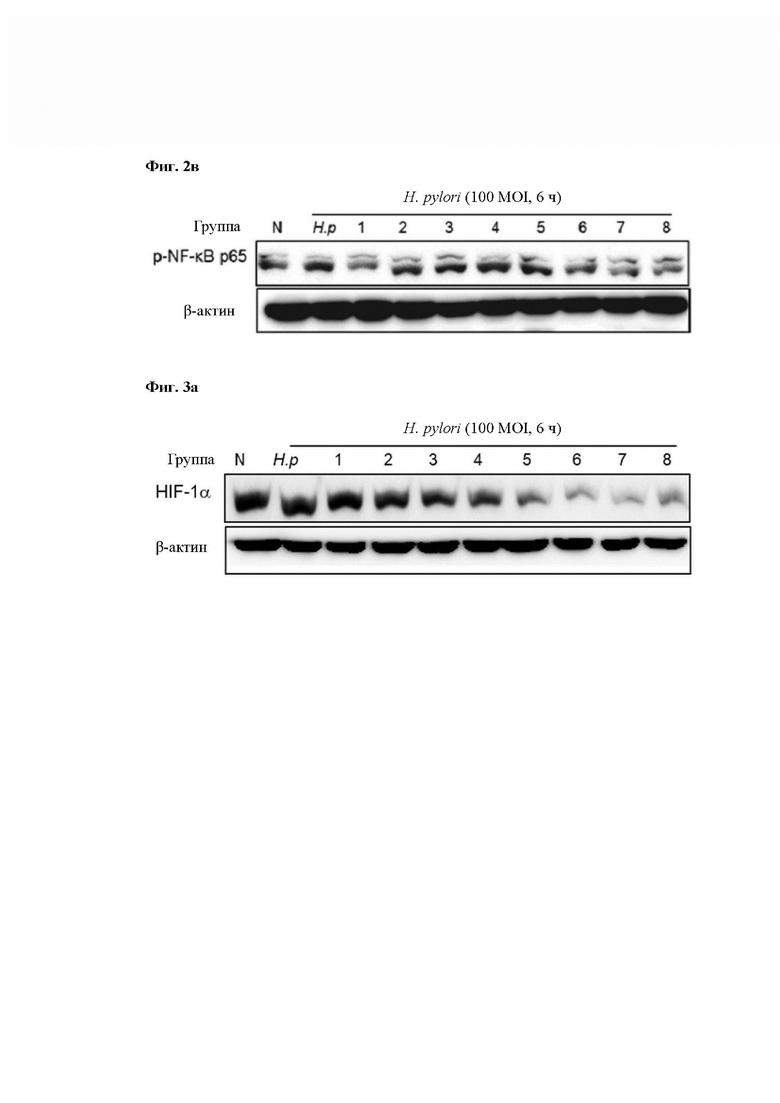

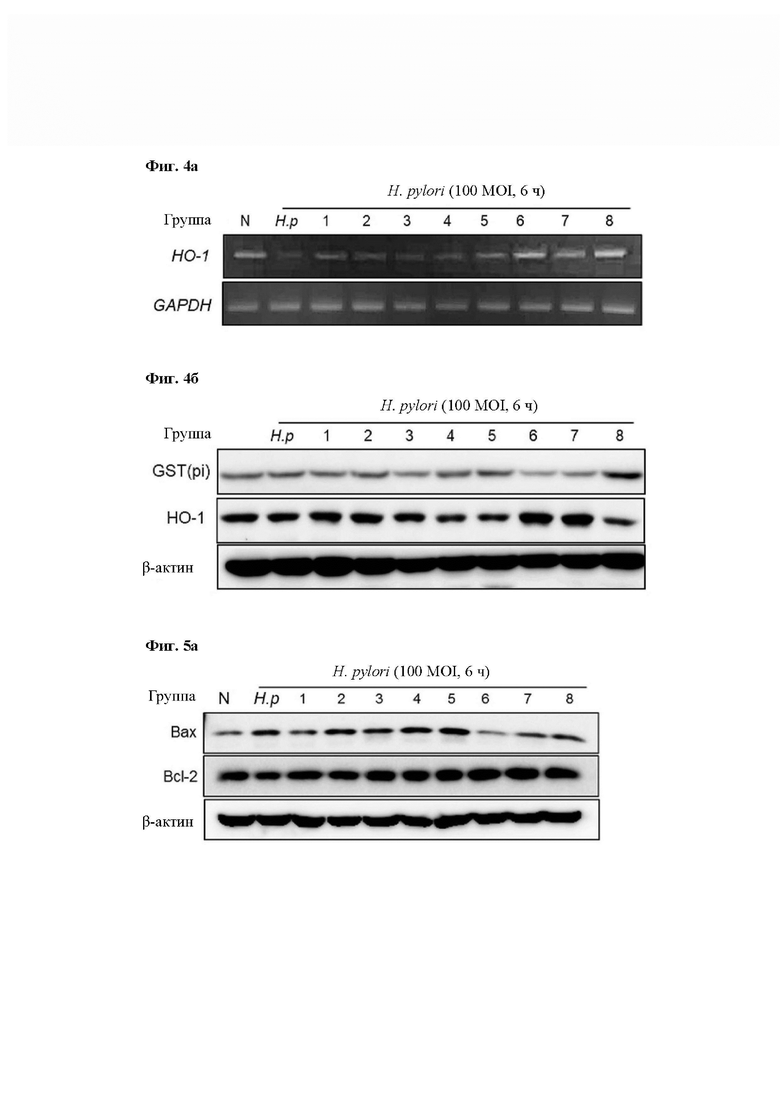
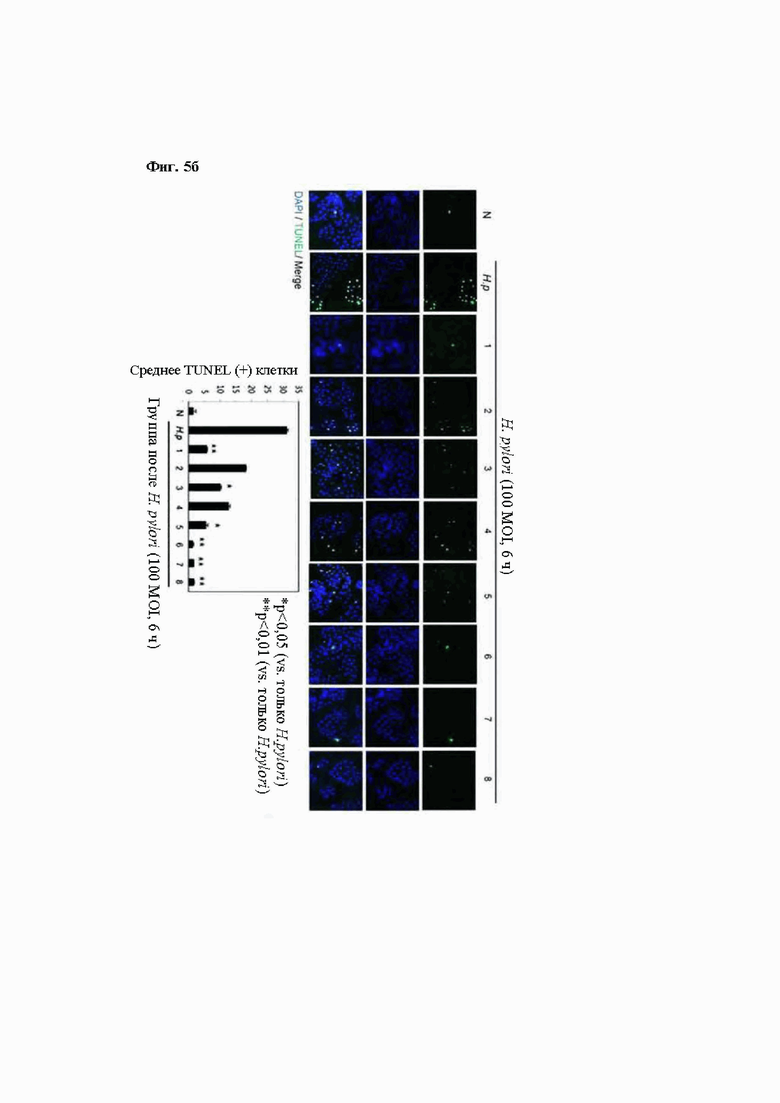
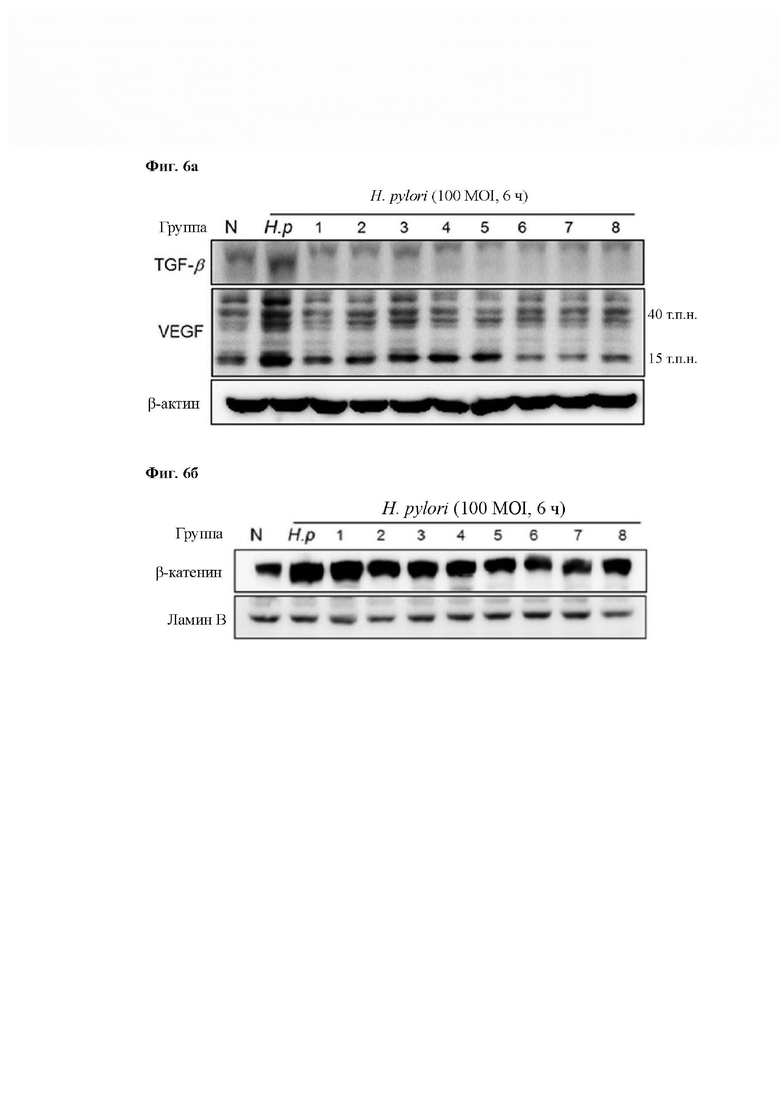
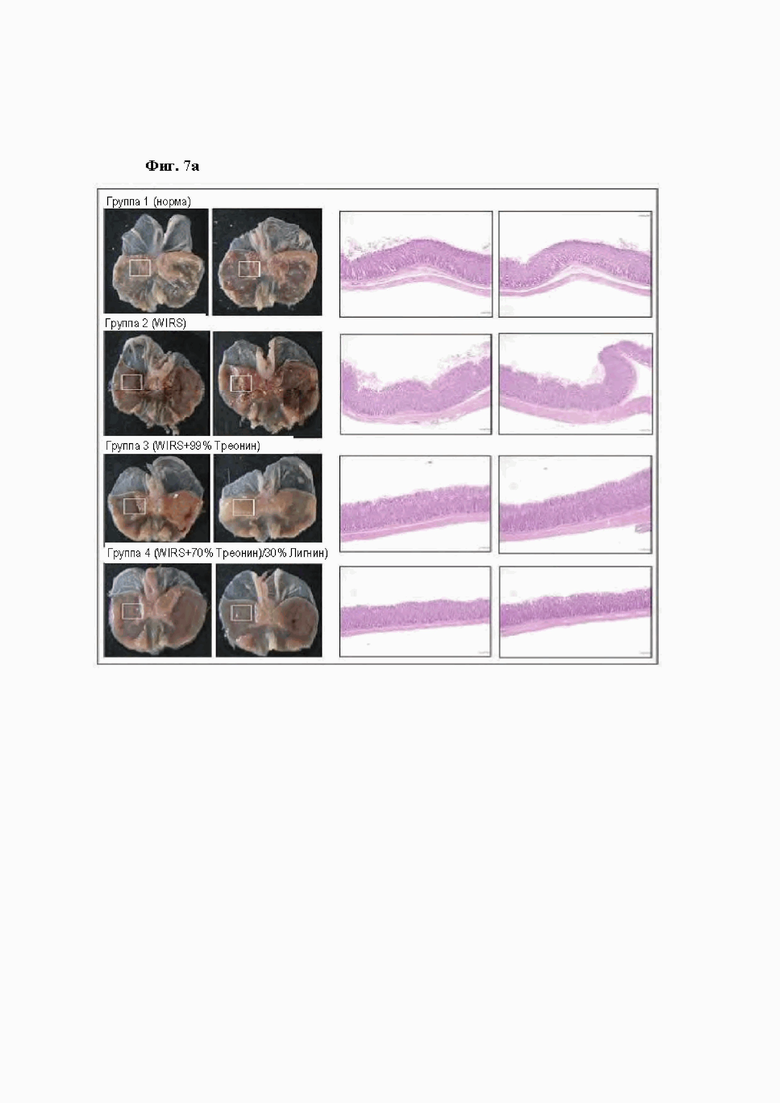
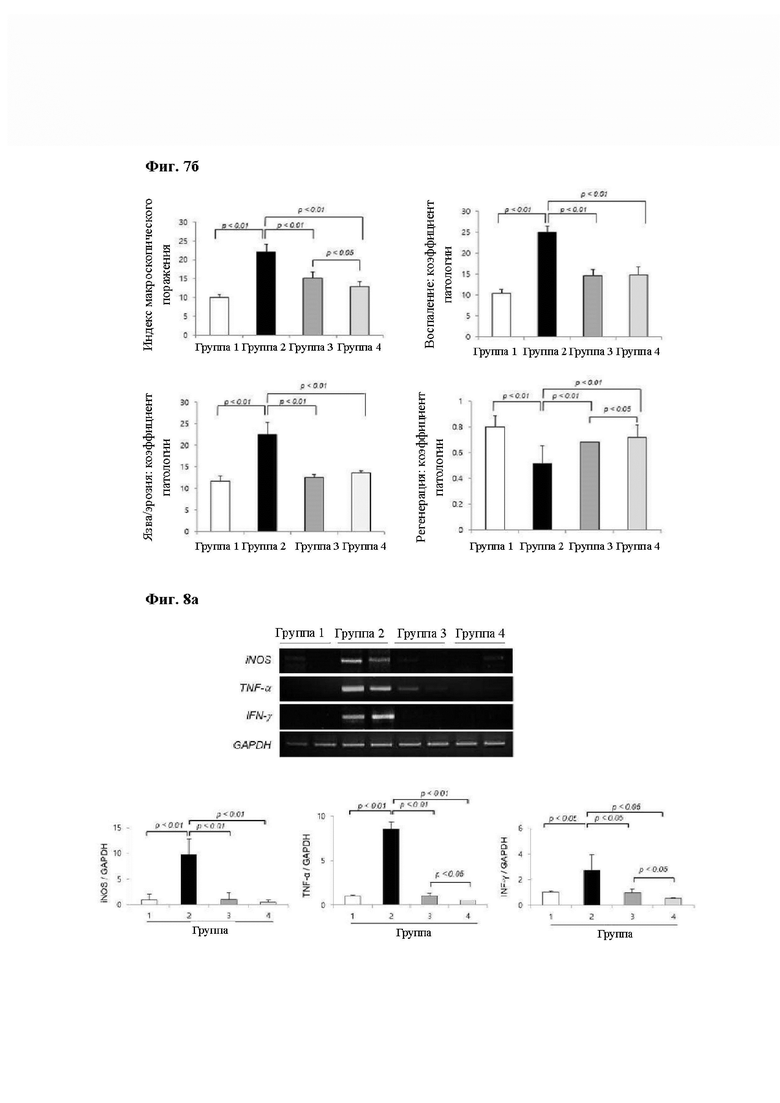
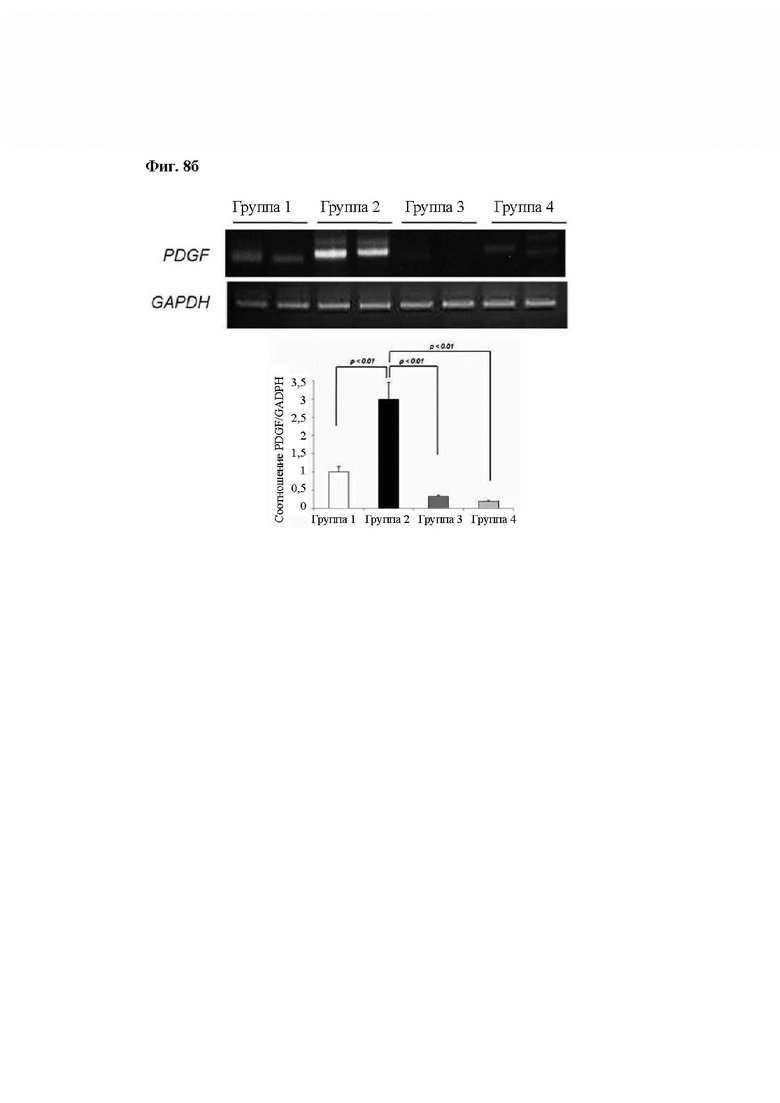
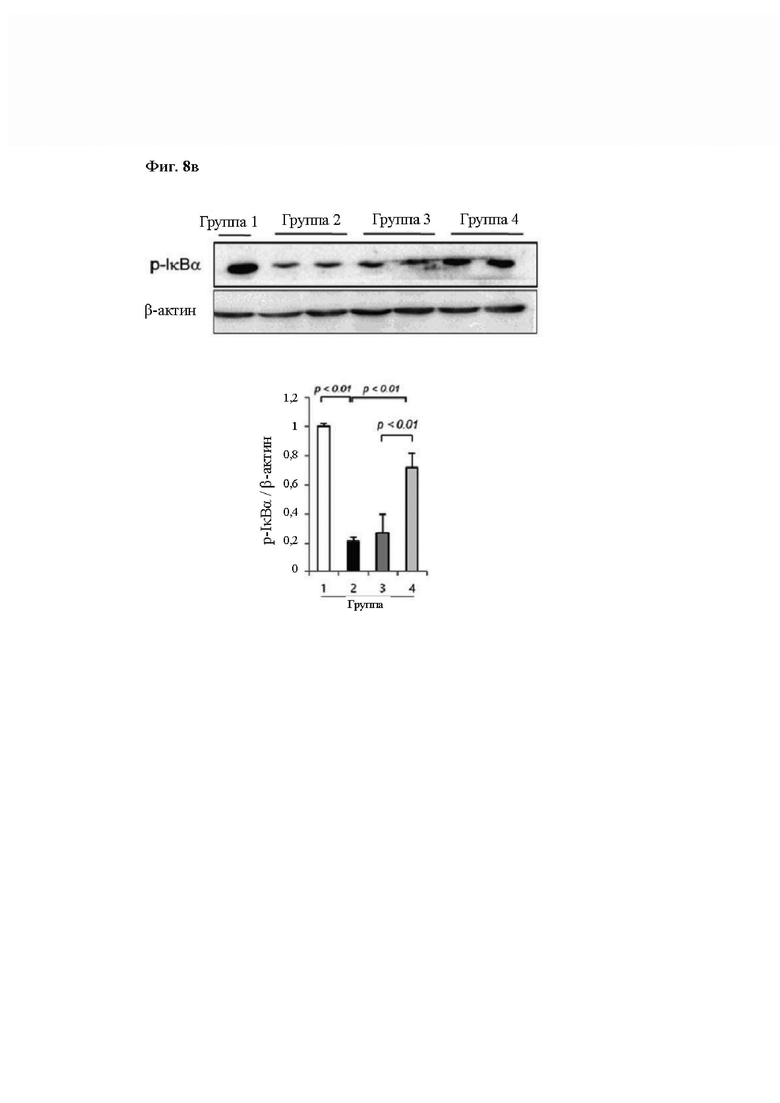
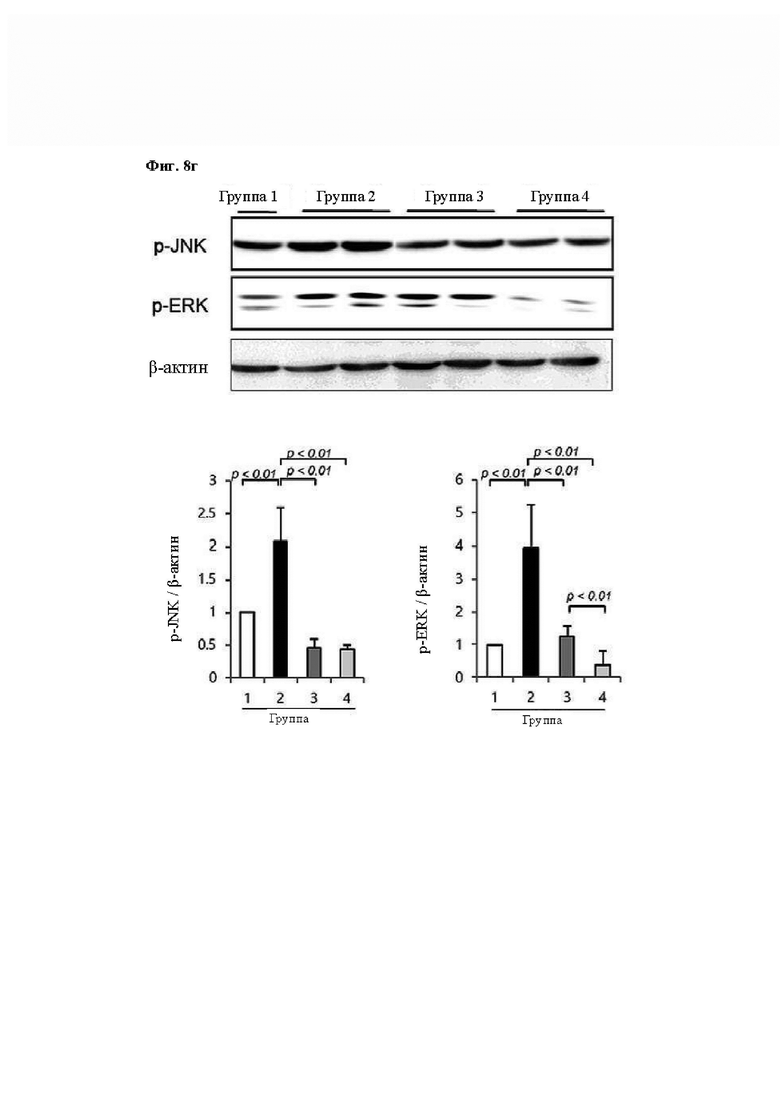
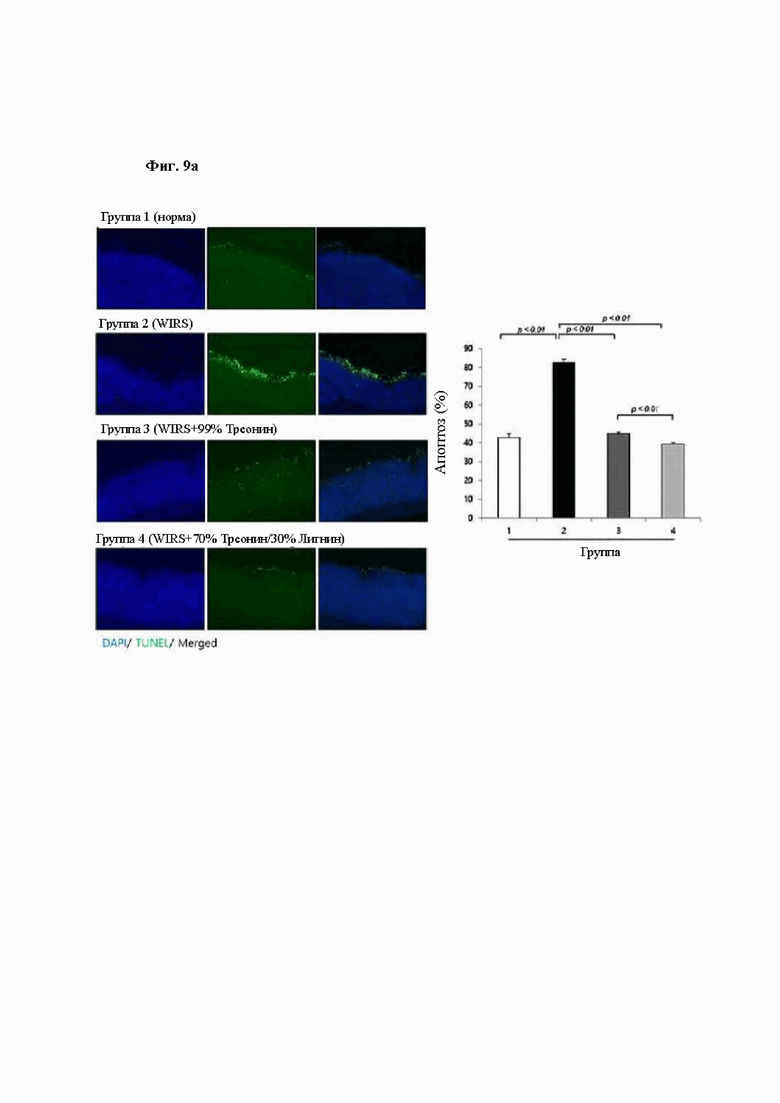
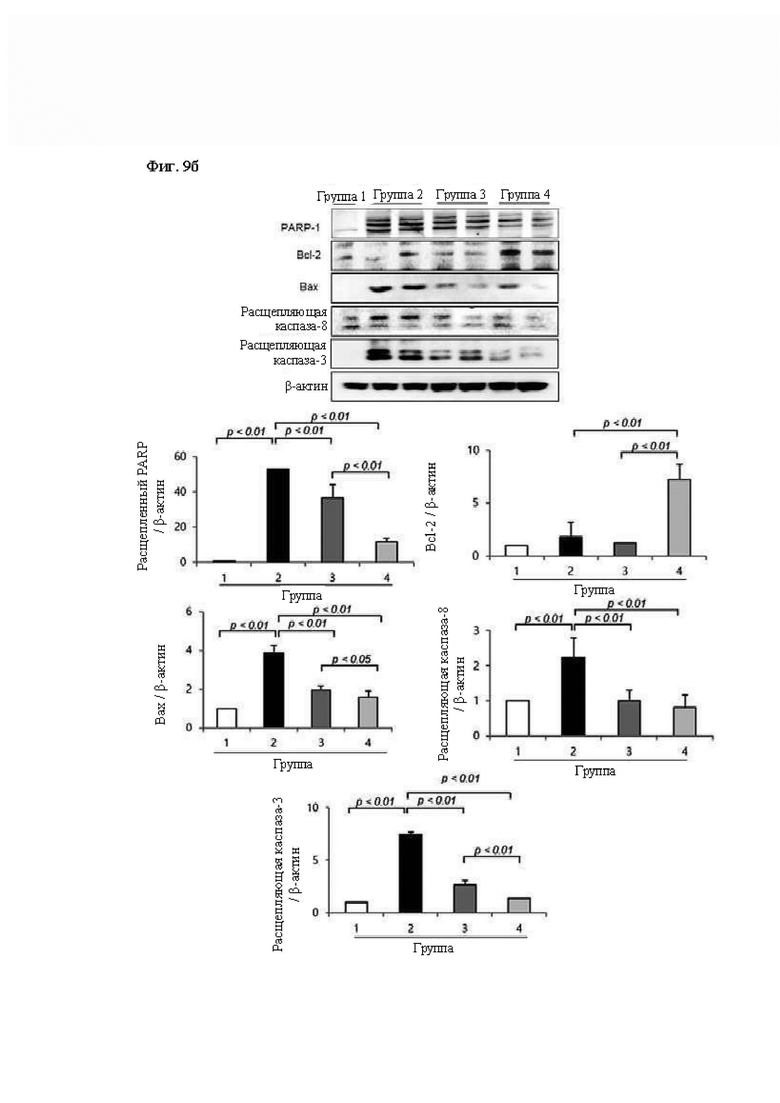
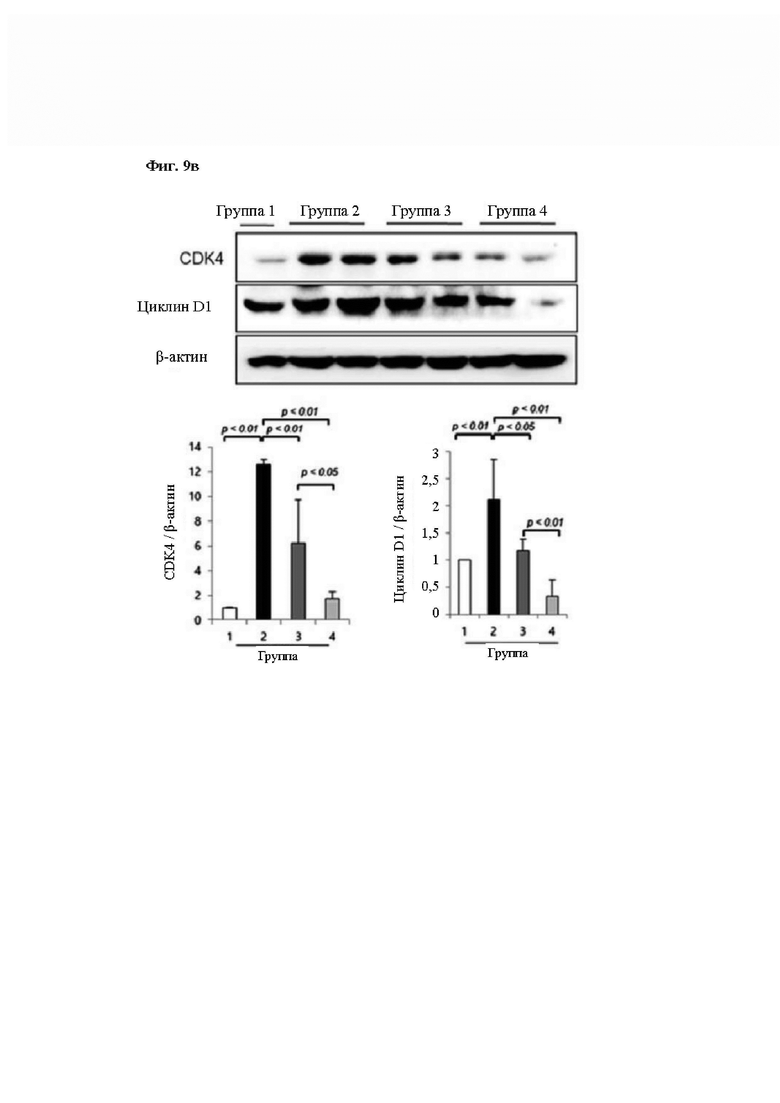
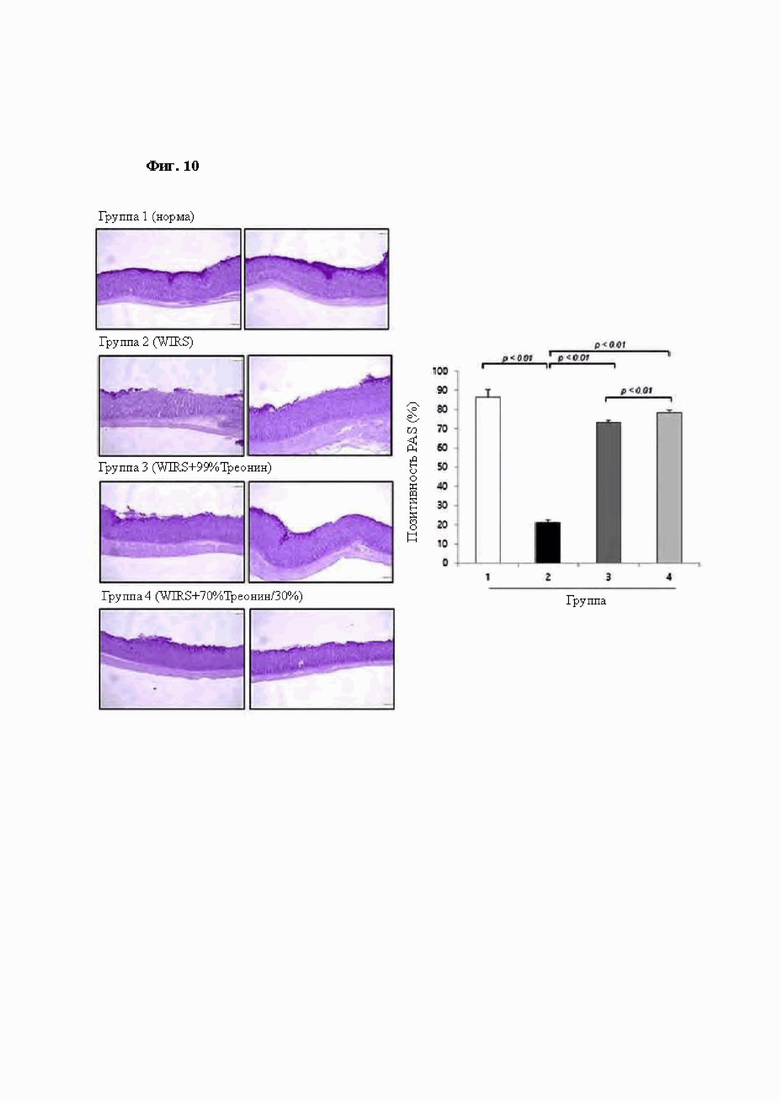

Изобретение относится к применению кормовой композиции для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, содержащей (1) эффективное количество штамма Corynebacterium sp., (2) продукт его культивирования, выбранный из ферментированной среды, полученной путем культивирования указанного штамма Corynebacterium sp. в среде, и указанной ферментированной среды, из которой удалены микробные клетки, и (3) треонин. Также предложены применение фармацевтической композиции, содержащей указанный выше состав, для предупреждения или лечения желудочного заболевания, применение пищевой композиции, содержащей указанный выше состав, для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании, применение антимикробной композиции, содержащей указанный выше состав, для ингибирования Helicobacter pylori. Изобретение эффективно против Helicobacter pylori в экспериментах на клетках, эффективно по облегчению состояния при желудочно-кишечных заболеваниях в экспериментах на животных и эффективно в отношении синтеза слизи желудка. 4 н. и 8 з.п. ф-лы, 11 ил., 6 табл., 12 пр.
1. Применение кормовой композиции, содержащей (1) эффективное количество штамма Corynebacterium sp., (2) продукт его культивирования, выбранный из ферментированной среды, полученной путем культивирования указанного штамма Corynebacterium sp. в среде, и указанной ферментированной среды, из которой удалены микробные клетки, и (3) треонин, для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании,
где желудочное заболевание представляет собой по меньшей мере одно, выбранное из группы, состоящей из гастрита, язвы желудка, язвы двенадцатиперстной кишки, пептической язвы и рака желудка, и
где штамм Corynebacterium sp. представляет собой по меньшей мере один, выбранный из группы, состоящей из Corynebacterium glutamicum, Corynebacterium ammoniagenes и Corynebacterium efficiens.
2. Применение по п. 1, где штамм Corynebacterium sp. представляет собой Corynebacterium glutamicum, Corynebacterium ammoniagenes или их комбинацию.
3. Применение по п. 1, где штамм Corynebacterium sp. представляет собой бактерии, убитые нагреванием.
4. Применение по п. 1, где продукт культивирования представляет собой ферментированный продукт, представляющий собой продукт ферментативного или метаболического разрушения органических веществ, полученный посредством культивирования указанного штамма Corynebacterium sp. в среде.
5. Применение по п. 4, где среда представляет собой среду для продуцирования треонина.
6. Применение по п. 1, где треонин содержится в количестве от 60 до 80% по массе.
7. Применение по п. 1, где штамм Corynebacterium sp. и продукт его культивирования содержатся в высушенной форме.
8. Применение по п. 1, где желудочное заболевание вызвано инфекцией Helicobacter pylori.
9. Применение по любому из пп. 1-8, где треонин:
(1) содержится в штамме Corynebacterium sp., продукте его культивирования или в обоих, или
(2) добавлен отдельно, или
(3) содержится в штамме Corynebacterium sp., продукте его культивирования или в обоих и дополнительно добавлен к ним.
10. Применение фармацевтической композиции, содержащей (1) фармацевтически эффективное количество штамма Corynebacterium sp., (2) продукт его культивирования, выбранный из ферментированной среды, полученной путем культивирования указанного штамма Corynebacterium sp. в среде, и указанной ферментированной среды, из которой удалены микробные клетки, и (3) треонин, для предупреждения или лечения желудочного заболевания,
где желудочное заболевание представляет собой по меньшей мере одно, выбранное из группы, состоящей из гастрита, язвы желудка, язвы двенадцатиперстной кишки, пептической язвы и рака желудка, и
где штамм Corynebacterium sp. представляет собой по меньшей мере один, выбранный из группы, состоящей из Corynebacterium glutamicum, Corynebacterium ammoniagenes и Corynebacterium efficiens.
11. Применение пищевой композиции, содержащей (1) эффективное количество штамма Corynebacterium sp., (2) продукт его культивирования, выбранный из ферментированной среды, полученной путем культивирования указанного штамма Corynebacterium sp. в среде, и указанной ферментированной среды, из которой удалены микробные клетки, и (3) треонин, для предупреждения желудочного заболевания или облегчения состояния при желудочном заболевании,
где желудочное заболевание представляет собой по меньшей мере одно, выбранное из группы, состоящей из гастрита, язвы желудка, язвы двенадцатиперстной кишки, пептической язвы и рака желудка, и
где штамм Corynebacterium sp. представляет собой по меньшей мере один, выбранный из группы, состоящей из Corynebacterium glutamicum, Corynebacterium ammoniagenes и Corynebacterium efficiens.
12. Применение антимикробной композиции, содержащей (1) эффективное количество штамма Corynebacterium sp., (2) продукт его культивирования, выбранный из ферментированной среды, полученной путем культивирования указанного штамма Corynebacterium sp. в среде, и указанной ферментированной среды, из которой удалены микробные клетки, и (3) треонин, для ингибирования Helicobacter pylori, и
где штамм Corynebacterium sp. представляет собой по меньшей мере один, выбранный из группы, состоящей из Corynebacterium glutamicum, Corynebacterium ammoniagenes и Corynebacterium efficiens.
| KR 20060018868 A, 02.03.2006 | |||
| US 20090215133 A1, 27.08.2009 | |||
| МИКРООРГАНИЗМ ДЛЯ ПРОДУЦИРОВАНИЯ ОДНОВРЕМЕННО L-АМИНОКИСЛОТЫ И РИБОФЛАВИНА И СПОСОБ ПРОИЗВОДСТВА L-АМИНОКИСЛОТЫ И РИБОФЛАВИНА С ЕГО ПРИМЕНЕНИЕМ | 2012 |
|
RU2588657C2 |
| WO 2009005379 A1, 08.01.2009 | |||
| MAO X | |||
| ET AL | |||
| Specific roles of threonine in intestinal mucosal integrity and barrier function | |||
| Front | |||
| Biosci | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2023-11-07—Публикация
2020-06-02—Подача