Изобретение относится к координационным соединениям европия(III), а именно к способу получения новых комплексных соединений класса (1,10-фенантролин-κN1,κ(N10)трис((Z)-4-арил-1-метокси-1,4-диоксобут-2-ен-2-олата-κO4)европия, обладающих флуоресцентными свойствами в красной области спектра, которые могут использоваться в промышленности для изготовления светоотражающих красок, маркировки образцов и ценных бумаг, в медицине, ветеринарии и сельском хозяйстве для диагностических целей.
Структурным аналогом заявленных соединений является (2,2'-бипиридин-κН2,κН2')((Z)-4-фенил-1-окси-1,4-диоксобут-2-ен-2-олат-κO4)меди ([Cu(H2O)(bipy)(L)][Cu(bipy)(L)(NO3)](H2O)(NO3), где L=(2)-4-фенил-1-окси-1,4-диоксобут-2-ен-2-олат, bipy=2,2'-бипиридин) (1), который получают реакцией Cu(NO3)2⋅3H2O с 2,2'-бипиридином в этаноле (95%) с последующим добавлением к реакционной смеси спиртового подщелоченного раствора бензоилпировиноградной кислоты (2) при комнатной температуре в условиях медленного испарения растворителя в течение нескольких недель [Landry, B.R., Turnbull, М.М., Twamley, В. J. Chem. Crystallogr. 37, 81-86 (2007), doi: 10.1007/s 10870-006-9098-0]:
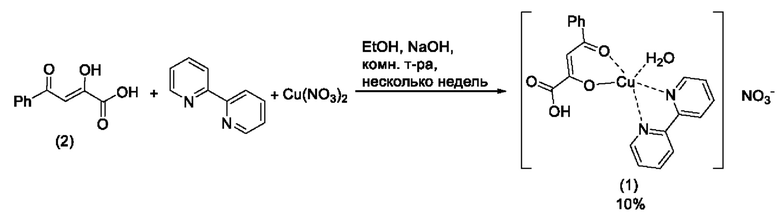
Метод синтеза комплекса (1) характеризуется низкими выходами, и данным методом невозможно получить заявляемый продукт, что является его существенным недостатком. Комплекс (1) является неустойчивым при хранении в обычных условиях, данных о его флуоресцентных свойствах нет.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе (1,10-фенантролин-κN1,κN10)трис((Z)-4-арил-1-метокси-1,4-диоксобут-2-ен-2-олатов-κO4)европия, обладающих флуоресцентными свойствами в красной области спектра.
Поставленная задача осуществляется путем выдерживания метиловых эфиров ароилпировиноградных кислот (Ia-в) в присутствии фенантролина и EuCl3⋅6H2O в метаноле при комнатной температуре в течение 30 мин с последующим добавлением в реакционную смесь триэтиламина и выдерживании реакционной смеси при перемешивании при комнатной температуре в течение 3 дней с последующим выделением целевых продуктов (IIa-в) фильтрованием непосредственно из реакционной смеси. Схема синтеза приведена ниже:
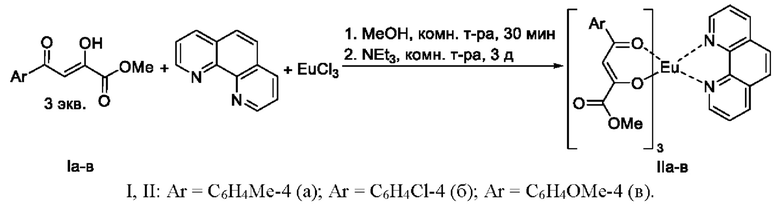
Из патентной и технической литературы не были выявлены способы получения (1,10-фенантролин-κN1,κN10)трис((Z)-4-арил-1-метокси-1,4-диоксобут-2-ен-2-олатов-κO4)европия, имеющие сходные признаки с заявленным способом не использовались исходные продукты, растворитель. На этом основании можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. (1,10-Фенантролин-κN1,κN10)трис((Z)-4-(4-метилфенил)-1-метокси-1,4-диоксобут-2-ен-2-олат-κO4)европия (IIa)
Получение (IIa): смесь, содержащую метиловый эфир 4-метилбензоилпировиноградной кислоты (Ia) (0.3 ммоль, 0.66 г), 1,10-фенантролин (0.1 ммоль, 0.18 г), EuCl3⋅6Н2О (0.1 ммоль, 0.37 г), метанол (50 мл), перемешивают при комнатной температуре в течение 30 мин. Затем туда добавляют триэтиламин (0.1 ммоль, 0.4 мл). Полученную реакционную смесь перемешивают при комнатной температуре в течение 3 д. Образовавшийся светло-желтый осадок соединения (IIa) отфильтровывают, последовательно промывают метанолом (3 мл) и водой (50 мл), сушат на воздухе. Выход 0.71 г, (69%), т.пл. 236-240°С (разл.).
Соединение (IIa) - светло-желтое порошкообразное вещество, легкорастворимое в 1,2-дихлорэтане, дихлорметане, хлороформе, труднорастворимое в ароматических углеводородах, ДМСО и ДМФА, ацетоне, 1,4-диоксане, этилацетате, алканах и нерастворимое в воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIa) снят в виде пасты в вазелиновом масле: 1725 см-1.
Спектр ЯМР 1H соединения (IIa) снят в растворе CDCl3 при частоте 400 МГц: δ=10.35 (м, 2 Н), 9.95 (м, 2 Н), 8.45-8.00 (м, 4 Н), 7.24 (м, 6 Н), 7.05 (м, 6 Н), 7.00 (уш. с, 3 Н), 2.76 (м, 9 Н), 2.70 (м, 9 Н) м.д.
Спектр ЯМР 13С соединения (IIa) снят в растворе CDCl3 при частоте 100 МГц: δ=20.8, 50.0, 93.1, 101.2, 125.9, 127.0, 127.9, 143.7, 149.5, 159.8, 181.3 м.д.
Соединение (IIa) C48H41E11N2O12 ⋅ CH4O. Найдено, %: С, 58.00; Н, 4.32; N, 2.81. Вычислено, %: С, 57.59; Н, 4.44; N, 2.74.
Пример 2. (1,10-Фенантролин-κN1,κN10)трис((2)-4-(4-хлорфенил)-1-метокси-1,4-диоксобут-2-ен-2-олат-κO4)европия (IIб)
Получение (IIб): смесь, содержащую метиловый эфир 4-хлорбензоилпировиноградной кислоты (Iб) (0.3 ммоль, 0.72 г), 1,10-фенантролин (0.1 ммоль, 0.18 г), EuCl3⋅6H2O (0.1 ммоль, 0.37 г), метанол (50 мл), перемешивают при комнатной температуре в течение 30 мин. Затем туда добавляют триэтиламин (0.1 ммоль, 0.4 мл). Полученную реакционную смесь перемешивают при комнатной температуре в течение 3 д. Образовавшийся светло-желтый осадок соединения (IIб) отфильтровывают, последовательно промывают метанолом (3 мл) и водой (50 мл), сушат на воздухе. Выход 0.92 г, (85%), т.пл. 188-192°С (разл.).
Соединение (IIб) - светло-желтое порошкообразное вещество, легкорастворимое в 1,2-дихлорэтане, дихлорметане, хлороформе, труднорастворимое в ароматических углеводородах, ДМСО и ДМФА, ацетоне, 1,4-диоксане, этилацетате, алканах и нерастворимое в воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIб) снят в виде пасты в вазелиновом масле: 1725 см-1.
Спектр ЯМР 1H соединения (IIб) снят в растворе CDCl3 при частоте 400 МГц: 5=10.34 (м, 2 Н), 9.88 (м, 2 Н), 8.45-8.00 (м, 4 Н), 7.80 (уш. с, 3 Н), 7.17 (м, 12 Н), 2.83 (м, 9 Н) м.д.
Спектр ЯМР 13С соединения (IIб) снят в растворе CDCl3 при частоте 100 МГц: 5=50.2, 93.3, 101.1, 125.5, 128.0, 140.0, 161.1, 179.0 м.д.
Соединение (IIб) C45H32Cl3EUN2O12 ⋅ СH4О. Найдено, %: С, 51.37; Н, 3.28; N, 2.33. Вычислено, %: С, 51.01; Н, 3.35; N, 2.59.
Пример 3. (1,10-Фенантролин-κN1,κN10)трис((2)-4-(4-метоксифенил)-1-метокси-1,4-диоксобут-2-ен-2-олат-κO4)европия (IIв)
Получение (IIв): смесь, содержащую метиловый эфир 4-метоксибензоилпировиноградной кислоты (Iв) (0.3 ммоль, 0.71 г), 1,10-фенантролин (0.1 ммоль, 0.18 г), EuCl3⋅6H2O (0.1 ммоль, 0.37 г), метанол (50 мл), перемешивают при комнатной температуре в течение 30 мин. Затем туда добавляют триэтиламин (0.1 ммоль, 0.4 мл). Полученную реакционную смесь перемешивают при комнатной температуре в течение 3 д. Образовавшийся светло-желтый осадок соединения (IIв) отфильтровывают, последовательно промывают метанолом (3 мл) и водой (50 мл), сушат на воздухе. Выход 0.87 г, (81%), т.пл. 194-197°С (разл.).
Соединение (IIв) - светло-желтое порошкообразное вещество, легкорастворимое в 1,2-дихлорэтане, дихлорметане, хлороформе, труднорастворимое в ароматических углеводородах, ДМСО и ДМФА, ацетоне, 1,4-диоксане, этилацетате, алканах и нерастворимое в воде. Устойчиво при хранении в обычных условиях.
ИК спектр соединения (IIв) снят в виде пасты в вазелиновом масле: 1735, 1728, 1718 см-1.
Спектр ЯМР 1H соединения (IIв) снят в растворе CDCl3 при частоте 400 МГц: δ=10.46 (м, 2 Н), 10.09 (м, 2 Н), 8.45-7.77 (м, 4 Н), 7.80 (уш. с, 3 Н), 7.48 (м, 6 Н), 6.79 (м, 6 Н), 3.88 (м, 9 Н), 2.70 (м, 9 Н) м.д.
Спектр ЯМР 13С соединения (IIв) снят в растворе CDCl3 при частоте 100 МГц: 49.9, 55.3, 88.4, 101.3, 107.1, 110.6, 128.2, 128.7, 149.7, 159.2, 164.4, 180.4 м.д.
Соединение (IIв) C48H41E11N2O15 ⋅ CH4O. Найдено, %: С, 54.74; Н, 4.20; N, 2.81. Вычислено, %: С, 55.01; Н, 4.24; N, 2.62.
Пример 4. Исследование флуоресценции (1,10-фенантролин-κN1,κN10)трис((2)-4-арил-1-метокси-1,4-диоксобут-2-ен-2-олатов-κO4)европия (IIa-в).
Исследование флуоресценции проводилось на 1,10-фенантролин-κN1,κN10)трис((Z)-4-арил-1-метокси-1,4-диоксобут-2-ен-2-олатах-κO4)европия (IIa-в) в твердом состоянии на приборе PETROLASER TLC-254/365 при облучении УФ-лампами λ=254 нм и λ=365 нм.
Было выявлено, что 1,10-фенантролин-κN1,κN10)трис((Z)-4-арил-1-метокси-1,4-диоксобут-2-ен-2-олаты-κO4)европия (IIa-в) в твердом состоянии обладают сильной устойчивой флуоресценцией при облучении УФ-лампой λ=365 нм, при этом наблюдается излучение в области красного цвета (λ=630-760 нм), а при облучении УФ-лампой λ=254 нм наблюдается слабая устойчивая флуоресценция с излучением в области желтого цвета (λ=550-590 нм).
Флуоресценция сохраняется при хранении образцов в течение длительного времени без специальных условий.
| название | год | авторы | номер документа |
|---|---|---|---|
| 9-АРИЛ-6,8,20-ТРИОКСА-13-АЗАПЕНТАЦИКЛО [11.8.0.01, 10.02, 7.014,19]ГЕНЭЙКОЗА-9,14,16,18-ТЕТРАЕН-11,12,21-ТРИОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2556998C2 |
| ЛЮМИНЕСЦИРУЮЩИЕ КОМЛЕКСНЫЕ СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ С ПИРАЗОЛСОДЕРЖАЩИМИ ФТОРИРОВАННЫМИ 1,3-ДИКЕТОНАМИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2485163C1 |
| ДИАМИДЫ 4,7-ДИЗАМЕЩЕННЫХ 1,10-ФЕНАНТРОЛИН-2,9-ДИКАРБОНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЭКСТРАКЦИОННАЯ СМЕСЬ НА ИХ ОСНОВЕ | 2014 |
|
RU2601554C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОКСИЗАЩИЩЕННЫХ ГЛИКОПЕПТИДОВ ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ | 1992 |
|
RU2057139C1 |
| 16-АЛКОКСИ-14-АРИЛ-15-ОКСА-3,10-ДИАЗАТЕТРАЦИКЛО [8.7.0.0.0]ГЕПТАДЕКА-4,6,8,13-ТЕТРАЕН-2,11,12-ТРИОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2556999C2 |
| ЛЮМИНЕСЦИРУЮЩИЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ С ПИРАЗОЛСОДЕРЖАЩИМИ 1,3-ДИКЕТОНАМИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2470026C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРАЗОНОВ НИТРО-ТЕТРАЗОЛ-5-КАРБАЛЬДЕГИДА | 2012 |
|
RU2522437C2 |
| ТРИСДИКЕТОНАТНЫЕ КОМПЛЕКСЫ ЛАНТАНИДОВ С ЛИГАНДАМИ ПИРИДИНОВОГО РЯДА В КАЧЕСТВЕ ЛЮМИНОФОРОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2463304C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-АРИЛ-2-(2-ГИДРОКСИФЕНИЛ)-7,15-ДИОКСА-2-АЗАТЕТРАЦИКЛО[6.5.2.0.0]ПЕНТАДЕЦ-5-ЕН-3,4,14-ТРИОНОВ | 2014 |
|
RU2569899C1 |
| РЕАКЦИИ МАКРОЦИКЛИЗАЦИИ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ДРУГИЕ ФРАГМЕНТЫ, ПРИГОДНЫЕ В ПОЛУЧЕНИИ АНАЛОГОВ ХАЛИХОНДРИНА B | 2014 |
|
RU2710545C2 |
Изобретение относится к координационным соединениям европия(III), конкретно к способу получения комплексных соединений (1,10-фенантролин-κN1,κN10)трис((Z)-4-арил-1-метокси-1,4-диоксобут-2-ен-2-олата-κO4)европия, обладающих флуоресцентными свойствами в красной области спектра, которые могут использоваться в промышленности для изготовления светоотражающих красок, маркировки образцов и ценных бумаг, в медицине, ветеринарии и сельском хозяйстве для диагностических целей. Способ получения соединений формулы IIа-в осуществляется взаимодействием метиловых эфиров ароилпировиноградных кислот, фенантролина и EuCl3⋅6H2O в метаноле с последующим добавлением в реакционную смесь триэтиламина:
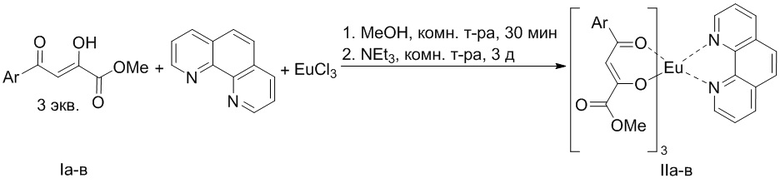 ,
,
где I, II: Ar = C6H4Me-4 (а); Ar = C6H4Cl-4 (б); Ar = C6H4OMe-4 (в). Техническим результатом изобретения является обеспечение простого способа синтеза целевых продуктов. 4 пр.
Способ получения (1,10-фенантролин-κN1,κN10)трис((Z)-4-арил-1-метокси-1,4-диоксобут-2-ен-2-олатов-κO4)европия, при котором осуществляют взаимодействие метиловых эфиров ароилпировиноградных кислот, фенантролина и EuCl3⋅6H2O в метаноле с последующим добавлением в реакционную смесь триэтиламина:
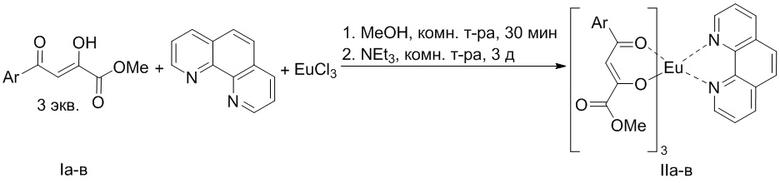
I, II: Ar = C6H4Me-4 (а); Ar = C6H4Cl-4 (б); Ar = C6H4OMe-4 (в).
| Landry, B.R., Turnbull, M.M., Twamley, B | |||
| J | |||
| Chem | |||
| Crystallogr, 37, 2007, p | |||
| Горный компас | 0 |
|
SU81A1 |
| А.В | |||
| Хомяков и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| xxv, 8(124), 2011, с.87-89 | |||
| WO 2013027846 A1, 28.02.2013. | |||
Авторы
Даты
2023-11-28—Публикация
2023-05-05—Подача