Область техники
Настоящее изобретение имеет отношение к области терапии рака и, в частности, к использованию наночастиц в противораковых целях с сохранением T-клеток.
В частности, настоящее изобретение имеет отношение к применению наночастиц для лечения рецидива рака и использованию в качестве противораковой вакцины.
Уровень техники
Эффективное устранение того же самого патогена после повторной инфекции может быть достигнуто в результате способности иммунной системы запоминать свой ответ на те же самые патогены. Иммунная система обладает врожденной памятью, иммунологической памятью, которая существует на основе этой способности.
Наивные T-клетки, вырабатываемые тимусом, являются иммунными клетками, которые активируют вторичный иммунный ответ на патоген. Каждая наивная T-клетка имеет уникальный T-клеточный рецептор, распознающий специфическую часть патогена.
Только те наивные T-клетки, которые распознают патоген посредством своих T-клеточных рецепторов, утрачивают свою «наивность» и дифференцируют в эффекторные клетки, которые могут убивать инфицированные клетки или оказывать помощь другим иммунным клеткам. После устранения патогена большинство эффекторных клеток погибнет, вместе с тем небольшой пул T-клеток развивается в T-клетки памяти, ответственные за более быстрый и сильный иммунный ответ после столкновения с этим же патогеном в дальнейшем. Интересно, что иммунной системой распознаются не только патогены, но также раковые клетки, благодаря тому, что они экспрессируют несколько «не своих» антигенов. Лечение рака, например, химиотерапия, может ослабить иммунную систему, по причине того, что лечение может вызывать резкое сокращение количества лейкоцитов, продуцируемых в костном мозге, и уменьшать количество нейтрофилов в организме, затрудняя борьбу с инфекциями.
Более того, химиотерапия воздействует на T-клетки, уменьшая их количество и активность, ухудшая их способность дифференцироваться в T-клетки, участвующие в борьбе, которые могли бы защитить от опухолевых метастазов.
Рецидивный рак – это опухоль, вернувшаяся после первоначального лечения. Несмотря на то, что первоначальная терапия нацелена на уничтожение всех раковых клеток, незначительное количество клеток может ускользнуть от воздействия и выжить. Эти необнаруженные раковые клетки могут пролиферировать, становясь рецидивным раком, который может появиться через месяцы или годы после первоначального лечения. Рак может возвратиться в том же самом месте, где был первоначальный рак (местный рецидив), или он может распространиться в отдаленные органы и ткани (отдаленный рецидив).
Наличие неизмененной популяции T-клеток может обеспечить активный надзор против рецидивов рака и метастазов. Следовательно, исключительно важно избежать потери T-клеток в ходе первой противоопухолевой терапии, для того, чтобы сохранить эту клеточную популяцию.
Все в большей степени ощущается важность и необходимость в эффективном пути транспортирования химиотерапевтического лекарственного средства в опухолевые клетки, не оказывающем воздействия на функциональность или снижение функциональности T-клеток.
Раскрытие изобретения
Как будет описано далее в подробном описании изобретения, проблемой, лежащей в основе настоящего изобретения, является терапия рака направленного действия, при этом без цитотоксичного воздействия противоопухолевой терапии на популяцию T-клеток пациента.
Для достижения этой цели настоящее изобретение обращено к наночастице ферритина, содержащей химиотерапевтическое средство, предназначенной для применения с целью сохранения T-клеток у ракового пациента.
Кроме того, настоящее изобретение касается наночастицы ферритина, содержащей химиотерапевтическое средство, предназначенной для применения при лечении рецидива рака.
В следующем варианте осуществления изобретение описывает применение наночастицы ферритина, содержащей химиотерапевтическое средство, в качестве противораковой вакцины.
Краткое описание чертежей
Характерные особенности и преимущества настоящего изобретения будут понятны из подробного описания, представленного ниже, из примеров, приведенных с иллюстративными и неограничивающими целями, и из прилагающихся фиг. 1-3, среди которых:
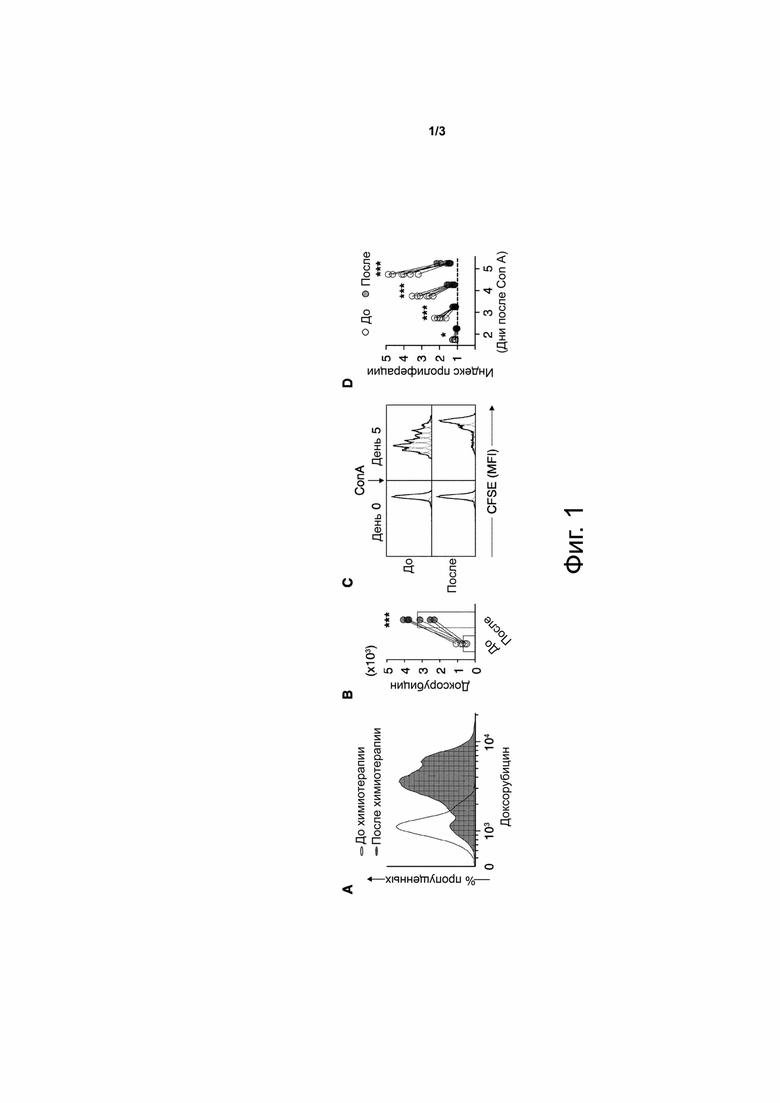
фиг. 1: DOX оказывает влияние на способность к пролиферации МКПК у пациентов при неоадьювантной химиотерапии.
A. Профиль интернализации DOX, полученный с помощью проточной цитометрии, в МКПК, выделенных от типичного пациента до и после парентерального введения DOX.
B. Количественный анализ средней интенсивности флуоресценции (MFI) в МКПК, выделенных от пациентов. Профили представляют значения флуоресценции DOX у каждого пациента до и после химиотерапии. Гистограмма показывает среднее значение флуоресценции DOX между всеми проанализированными образцами. N=3, непарный t-критерий *p<0.05, **p<0.01, ***p<0.001.
C. Типичное изображение анализа пролиферации МКПК, полученных у BC-пациента до и после 1 цикла неоадьювантной химиотерапии DOX, с применением анализа с использованием карбоксифлуоресцеина сукцинимидилового эфира (анализа CFSE).
D. Количественный анализ индекса пролиферации в разные дни культивирования после стимулирования конканавалином A (ConA). Индекс пролиферации – это отношение между пролиферирующими клетками и клетками-предшественниками. Отсутствие пролиферации характеризуется индексом пролиферации, равным 1. N=3, непарный t-критерий *p<0.05, **p<0.01, ***p<0.001.
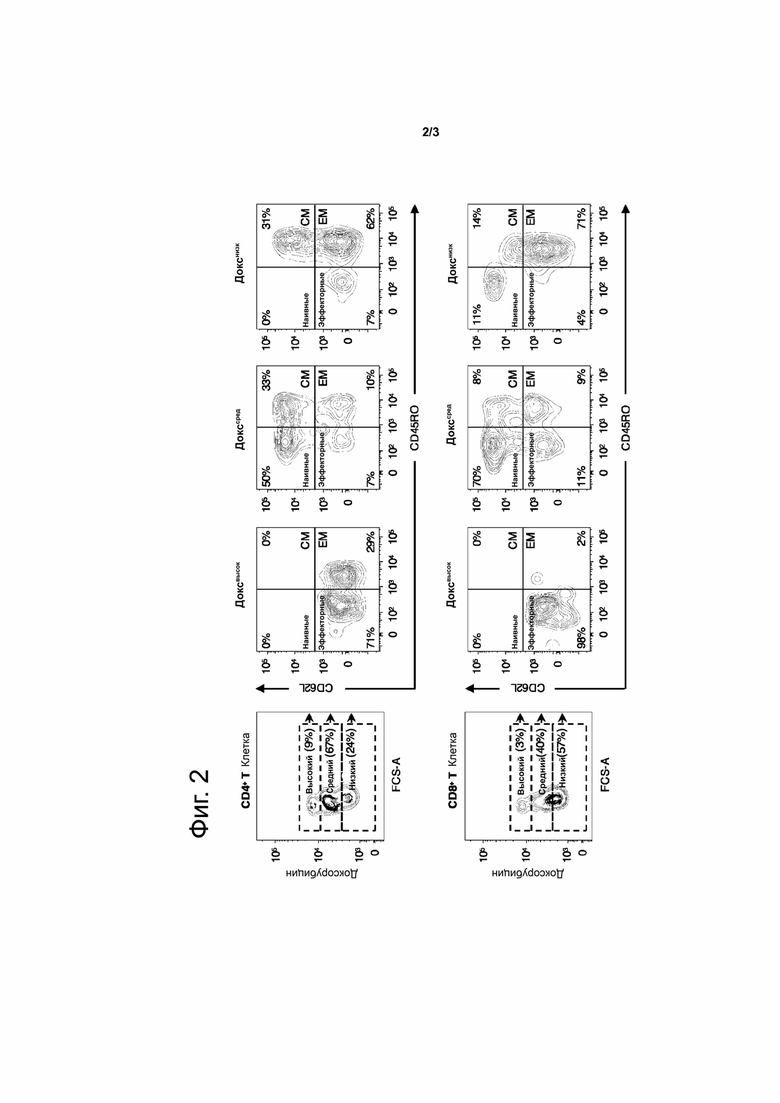
фиг. 2: Характеристика субпопуляций лимфоцитов, которые интернализируют DOX. Иммунофенотипирование T-лимфоцитов CD8+ eCD4+ с применением проточной цитометрии, чтобы идентифицировать популяции, которые поглощают DOX (высокое, умеренное, низкое). CM: Центральная память, EM: Эффекторная память.
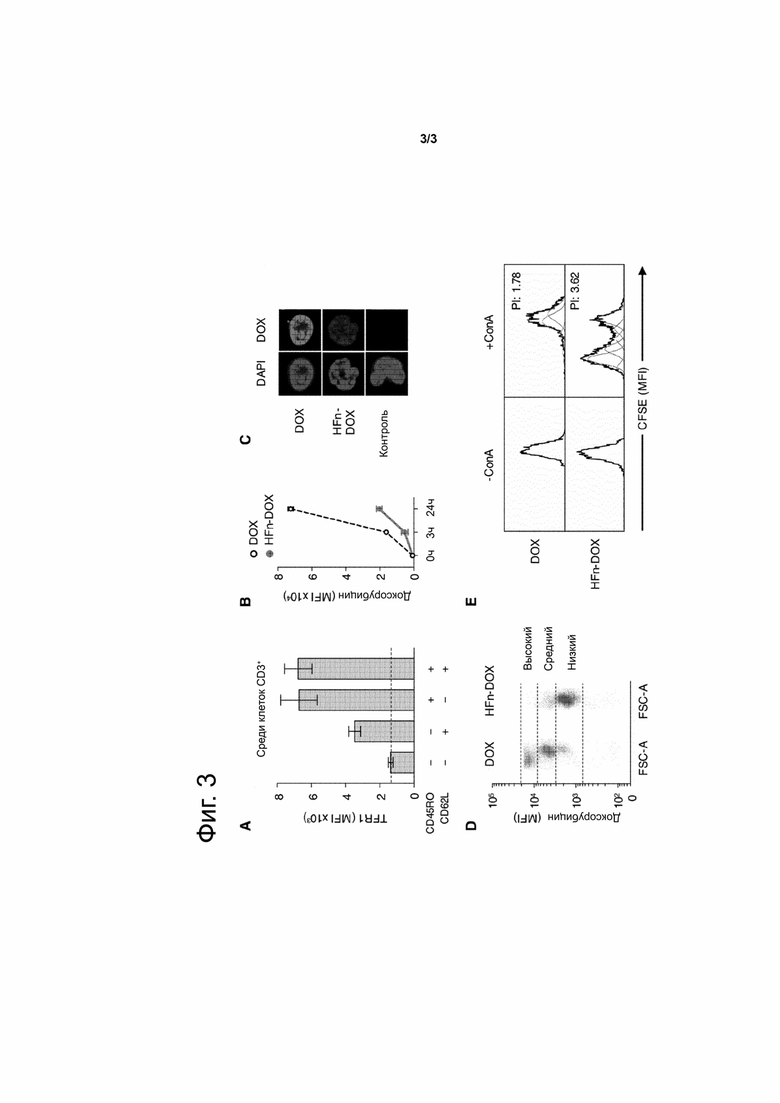
фиг. 3: Интернализация МКПК, заключенных в H-ферритин (HFn) нанокаркасы.
A. Определение количества с помощью проточной цитометрии экспрессии рецептора трансферрина 1 (TfR1) в различных популяциях T-лимфоцитов, изолированных из МКПК здоровых доноров. Пунктирная линия показывает MFI от контроля, использованного, чтобы показать исходный уровень флуоресценции (мышиный IgG1). B. Кинетические параметры взаимодействия свободного DOX или DOX в составе наночастиц в HFn (HFn-DOX) в человеческих МКПК.
C. Внутриклеточная локализация DOX или HFn-DOX с помощью конфокальной микроскопии.
D. Анализ популяции лимфоцитов, которые интернализируют DOX до и после инкубации с DOX или HFn-DOX.
E. Анализ пролиферации с применением карбоксифлуоресцеина сукцинимидилового эфира (CFSE) в МКПК, инкубированных в течение 24 часов с DOX или HFn-DOX (1мкM) и стимулированных ConA в течение 5 дней. PI: Индекс пролиферации.
Подробное описание изобретения
Настоящее изобретение касается области терапии рака и, в частности, касается решения проблемы предотвращения нарушения функций иммунной системы после химиотерапевтического лечения. Согласно наблюдениям, у раковых пациентов наблюдается резкое уменьшение количества и функциональности T-клеток после химиотерапии.
Цель настоящего изобретения, таким образом, заключается в наночастице ферритина, содержащей химиотерапевтическое средство, для применения при сохранении T-клеток у пациентов с раком.
Ферритин представляет собой широко распространенный белок, обнаруженный в эубактериях, археях, растениях и животных, включая человека, но не в дрожжах. Он располагается во внеклеточных и внутриклеточных компартментах, таких как цитозоль, ядро и митохондрия, его основными функциями являются хранение железа и гомеостаз. Следовательно, он представляет собой одну из самых высоко-консервативных молекул.
Ферритин представляет собой крупный белок 450 kDa, состоящий из 24 субъединиц, которые самостоятельно собираются в сферическую камеро-подобную структуру с внутренним и внешним размерами 8 и 12 нм, соответственно. Эукариоты имеют два гена ферритина, кодирующие тяжелую (H; 21 kDa) и легкую (L; 19 kDa) цепи. H-цепь отвечает за окисление Fe(II) в Fe(III) и включает каталитический сайт ферроксидазы, тогда как L-цепь играет роль в нуклеации железа. H и L цепи совместно собираются в 24-мерный гетерополимер, где отношение H-цепи к L-цепи варьирует в соответствии с ткане-специфическим распределением.
Ферритин защищает клетки от повреждения, вызванного реакцией Фентона во время окислительного стресса путем секвестирования Fe2+, источника токсичных активных форм кислорода, и превращения его в безопасный Fe3+, который хранится в виде кристаллов ферригидрита.
«Камера» из белка ферритина может вмещать до 4500 атомов железа. Это защитное действие имеет решающее значение в ядре, где ДНК, в частности, предохраняется от индуцированного железом окислительного повреждения.
Внеклеточный ферритин взаимодействует с клетками через рецептор трансферрина 1 (TfR1), который специфически связывает H-ферритин, тогда как L-ферритин показывает низкое взаимодействие. После связывания на клеточной поверхности комплекс H-ферритин-TfR1 интернализируется (поглощается клеткой) и может обнаруживаться в ранних и рециклирующих эндосомах, демонстрируя, что TfR1 координирует процессинг и использует железо путем связывания как трансферрина, так и H-ферритина. H-ферритин также способен взаимодействовать с T-клеточным иммуноглобулином и доменом-2 муцина (TIM-2), который сверхэкспрессируется в олигодендроцитах и B-клетках, и интернализируется в эндосомах после связывания. H-ферритин, который естественным образом взаимодействует с TfR1, наиболее интенсивно изучается и используется для разработки естественным образом нацеленных наночастиц для применения в наномедицине, используя сверхэкспрессию TfR1 во многих типах опухолевых клеток.
Рекомбинантный ферритин обеспечивает главную полость, которая может быть эффективно загружена переходными металлами, лекарственными средствами, флуоресцентными молекулами или контрастными веществами. Поскольку ферритин имеет однотипную «камеру», обеспечивается возможность точного контроля количества инкапсулированных молекул, что имеет большое значение при определении дозировки лекарственного средства. Более того, протеиновая оболочка ферритинов может быть легко модифицирована, или химически или генетически, с целью введения различных функциональных возможностей. Все эти характерные свойства выделяют ферритин и его производные как эффективные системы с возможным применением в наномедицине.
Использованный в описании термин “наночастица” или “ нанокамера HFn” предназначается для того, чтобы охватывать камеро-подобную структуру, оболочку или композицию, содержащую ферритин и химиотерапевтическое средство. Указанное химиотерапевтическое средство предпочтительно заключено в нанокамеру. Наночастица ферритина, содержащая химиотерапевтическое средство, может также упоминаться как нанокамера ферритина с инкапсулированным химиотерапевтическим средством.
Четвертичная структура ферритина имеет восемь гидрофильных каналов, которые, по-видимому, опосредуют транзит в и из белковой «камеры». Существует также шесть гидрофобных каналов, которые вероятно не участвуют в обмене железа, хотя они могут опосредовать транзит протонов. Несмотря на структурную жесткость ферритинов в физиологической окружающей обстановке, протеиновые «камеры» могут обратимым образом разбираться на части, когда значение pH становится крайне кислым (pH 2-3) или щелочным (pH 10-12). Когда значение pH возвращается к нейтральному, мономеры ферритина способны самособираться, задействуя эффект запоминания формы. Более того, ферритиновая камера является устойчивой к денатурирующим агентам, включая нагревание до высоких температур (>80°C).
Внеклеточный ферритин взаимодействует с клетками посредством рецептора трансферрина 1 (TfR1), который специфически связывается с H-ферритином, тогда как L-ферритин демонстрирует низкое взаимодействие. После связывания на клеточной поверхности комплекс H-ферритин-TfR1 интернализируется и может быть обнаружен в ранних и рециркулирующих эндосомах, демонстрируя, что TfR1 координирует процессинг и использование железа посредством связывания как трансферрина, так и H-ферритина. H-ферритин также способен взаимодействовать с T-клеточным иммуноглобулином и доменом-2 муцина (TIM-2), который сверхэкспрессируется в олигодендроцитах и B-клетках и интернализируется в эндосомах после связывания. H-ферритин, который естественным образом распознается TfR1, наиболее интенсивно изучается и используется для разработки естественным образом нацеленных наночастиц для применения в наномедицине, используя сверхэкспрессию TfR1 во многих типах раковых клеток.
В дополнительном аспекте настоящее изобретение касается применения наночастицы ферритина, содержащей химиотерапевтическое средство, в сохранении T-клеток настоящего изобретения, при этом указанный пациент с раком является пациентом, страдающим от рака молочной железы, рака мочевого пузыря, рака легкого, рака желудка, рака яичника; лимфомы Ходжкина, неходжкинской лимфомы, некоторых типов лейкемии, включая острый лимфобластный лейкоз (ALL) и острый миелоидный лейкоз (AML, ANLL). Она применяется вместе с другими лекарственными средствами при лечении некоторых типов рака щитовидной железы и некоторых типов сарком мягких тканей или костей, нейробластомы и опухоли Вильмса.
В предпочтительном аспекте наночастица ферритина, содержащая химиотерапевтическое средство, используется в сохранении T-клеток пациента, страдающего от рака молочной железы.
В дополнительном предпочтительном аспекте химиотерапевтическое средство, входящее в состав наночастицы ферритина, выбирают из группы, состоящей из доксорубицина (DOX), производных платины, таксана, ингибиторов PARP-1, ингибиторов mTOR, ингибиторов PI3K, бензотиазолов, куркуминоидов, десфероксамина B. Мы изучали фенотипические и функциональные эффекты DOX на совместимо-спаренные лимфоциты, полученные у пациентов с раком молочной железы (BC) до и после неоадьювантной химиотерапии. Мы обнаружили, что полученные от пациентов МКПК, изолированные после химиотерапии, быстро интернализировали DOX и продемонстрировали значительное ослабление пролиферации в ответ на митогенное симулирование по сравнению с совместимо-спаренными МКПК, изолированными до лечения (фиг. 1). Интересно отметить, что исследование FC показало, что разные субпопуляции лимфоцитов интернализировали DOX в разных масштабах, при этом наивные T-клетки (CD3+CD8+/CD4+CD45RO-) продемонстрировали самое высокое поглощение DOX (фиг. 2). Поскольку важнейшим фактором для каждого адаптивного иммунного ответа является активация и массовая пролиферация T-клеток из их состояния покоя, мы разработали композицию DOX в нанокамерах ферритина (HFn-DOX), поглощение которого специфически опосредуется рецептором 1 трансферрина 1 (TfR-1), для того, чтобы избежать интернализации лекарственного средства иммунными клетками. Тот факт, что T-клетки и, в частности, наивные T-клетки, экспрессируют низкие уровни TfR-1, дал нам возможность показать способность HFn-DOX защищать лимфоциты от воздействия DOX, при этом сохраняя их способность генерировать иммунный ответ (фиг. 3). Эти открытия были подтверждены in vivo на мышиной модели рака молочной железы, в которой рост опухоли контролировался еженедельными внутривенными инъекциями HFn-DOX и, в то же самое время, предотвращая нецелевое воздействие во вторичных лимфоидных органах. В целом, наши результаты показывают, что предотвращение связанной с химиотерапией токсичного воздействия на T-клетки посредством HFn-DOX может позволить адаптивной иммунной системе хозяина полностью извлечь пользу из DOX-индуцированной смерти иммуногенной клетки для вакцинирования против рака.
Дополнительная цель настоящего изобретения касается применения наночастиц ферритина, содержащих химиотерапевтическое средство, в качестве вакцины.
Без привязки к какой-либо теории, предварительный вывод показывает, что:
a) у пациентов, которых лечили HFn-DOX, эти неоантигены могут подвергаться фагоцитозу и затем экспонироваться антиген-презентирующими клетками (APC). Опухолевый неоантиген, экспонированный на поверхности APC, используется для того, чтобы отобрать подходящий клон T-клеток, способный распознавать такой антиген и способный «запускать» противораковый иммунный ответ, за которым следует этот подход “новой вакцинации”,
b) у пациентов, которых лечили DOX, T-клетки еще не являются функциональными и предрасположены к индуцированию клональной экспансии, необходимой для опосредования противоракового иммунного ответа, несмотря на то, что эти неоантигены продуцируются, фагоцитируются APC и затем экспонируются на их поверхности. В предпочтительном аспекте указанная противораковая вакцина является вакциной против рака молочной железы, и указанное химиотерапевтическое средство является доксорубицином.
Несмотря на естественное нацеливание ферритина на раковые клетки, поверхность нанокамер ферритина может быть модифицирована вставкой некоторого количества нацеленных мотивов, таких как антитела, пептиды и фрагменты антител, для того, чтобы запустить селективное распознавание специфических подтипов клеток. Более того, их высокая стабильность, биосовместимость, способность к разборке и повторной сборке по принципу эффекта запоминания формы и доступность для модификации поверхности делает наночастицы ферритина идеальной платформой для доставки лекарственного средства.
Действительно, при физиологических условиях ферритин имеет стабильную архитектуру 24-мерной «камеры», тогда как в сильно кислых и основных условиях его четвертичная структура разбирается, а затем повторно собирается, когда значение pH раствора доводится до нейтрального, обеспечивая возможность инкапсулирования молекул в растворе внутри полостей ферритина, просто путем разборки и повторной сборки 24-мерной структуры.
Лекарственные средства с естественной тенденцией к связыванию с металлами, такие как цисплатин и десфероксамин B, легко можно заключить в ферритиновую оболочку. Однако, большинство используемых в настоящее время химиотерапевтических средств не основывается на металлах, как цисплатин, и включение не содержащих металл лекарственных средств внутрь ферритина осложняется их ограниченными взаимодействиями с протеиновой «камерой».
Инкапсулирование доксорубицина (DOX) в нанокамеры ферритина представляет собой наиболее интенсивно изучаемую систему для доставки противораковых лекарственных средств. DOX, предварительно включенный в комплекс с Cu(II), загружали внутрь нанокамер ферритина и оценивали на опухолевых моделях U87MG глиобластомы in vitro и in vivo.
Теперь было неожиданно показано, что наночастица ферритина, содержащая химиотерапевтическое средство (нанокамера ферритина с инкапсулированным химиотерапевтическим средством), таким как доксорубицин, дает возможность предохранения клеток иммунной системы, и, в частности, наивных T-клеток у ракового пациента.
Восемьдесят процентов DOX постепенно высвобождалось из RGD-функционализированного апоферритина в течение 10 часов инкубации при 37°C в фосфатно-буферном солевом растворе (PBS), в то время как медь оставалась связанной с внутренней поверхностью нанокамер. Такая нацеленная наноформа демонстрирует повышенное поглощение и накопление лекарственного средства опухолью, ингибирование роста опухоли, время полужизни в кровотоке и обладает пониженной кардиотоксичностью, индуцированной свободным DOX. Другие группы создают стратегии «загрузки» DOX, не затрагивающие комплексообразование с переходными металлами. В этих случаях, также наблюдалась хорошая эффективность включения, и сообщалось об отличных результатах, имея в виду ингибирование роста опухоли и уменьшенную токсичность как in vitro, так и in vivo. Результаты in vivo явно демонстрируют, что нанокамеры ферритина улучшают биодоступность DOX, накопление в опухоли и выведение, и указывают на то, что активное нацеливание, опосредованное ферритином, обеспечивает основной вклад. Механизмы и кинетика высвобождения лекарственного средства из ферритиновой оболочки изучены не полностью, хотя сообщенные данные в случае DOX говорят о том, что инкапсулирование является стабильным в сыворотке и что pH-инициируемое высвобождение происходит in vitro.
В еще одном предпочтительном аспекте при использовании наночастицы ферритина, содержащей химиотерапевтическое средство, для сохранения наивных T-клеток указанный раковый пациент страдает от первичного рака или от рецидивного рака.
В частности, неожиданно было установлено, что инкубация МКПК от здоровых доноров с наночастицами, содержащими химиотерапевтическое средство, дает возможность предохранения МКПК. Действительно, MFI вследствие поглощения DOX ниже в МКПК, обработанных наночастицей, содержащей химиотерапевтическое средство, чем в МКПК, обработанных свободным лекарственным средством (фиг. 3B). Это разное поглощение сочетается с разным накоплением в ядерном компартменте, который является местом воздействия DOX (фиг. 3C). Более того, лечение наночастицами ферритина, содержащими химиотерапевтическое средство, позволяет идентифицировать только одну популяцию с низким поглощением DOX (фиг. 3D), вероятно вследствие умеренной экспрессии TfR1 в этих клетках (фиг. 3A). Следовательно, в образцах, обработанных наночастицами ферритина, содержащими химиотерапевтическое средство, индекс пролиферации остается высоким (фиг. 3E).
Более того, было неожиданно обнаружено, что лечение пациента наночастицами, содержащими химиотерапевтическое средство настоящего изобретения, не оказывает вредных воздействий, таких как гемолиз эритроцитов, и не является токсичным для печени, почек, селезенки, мозга, кишечника и легких.
В действительности, тяжелым недостатком химиотерапии доксорубицином является кардиотоксичность. Неожиданно было установлено, что наночастицы согласно настоящему изобретению позволяют избежать этой проблемы, тогда как лечение DOX вызывает тяжелую и необратимую кардиотоксичность I типа. Кардиобезопасность, наблюдаемая в случае образцов, обработанных наночастицами ферритина, содержащими химиотерапевтическое средство, позволяет предлагать комбинацию с другими очень эффективными, но кардиотоксичными лекарственными средствами, такими как моноклональное антитело трастузумаб.
В дополнительном варианте осуществления настоящее изобретение касается наночастицы ферритина, содержащей химиотерапевтическое средство, предназначенной для применения при лечении рецидива рака.
В предпочтительном аспекте наночастица ферритина, содержащая химиотерапевтическое средство, предназначается для применения при лечении рецидива рака.
В еще одном предпочтительном аспекте наночастица ферритина, содержащая химиотерапевтическое средство, используется при лечении рецидива рака молочной железы, рака мочевого пузыря, рака легкого, рака желудка, рака яичника; лимфомы Ходжкина, неходжкинской лимфомы, некоторых типов лейкемии, включая острый лимфобластный лейкоз (ALL) и острый миелоцитарный лейкоз (AML, ANLL). Наночастица используется с другими лекарственными средствами при лечении некоторых типов рака щитовидной железы и некоторых типов сарком мягких тканей или костей, нейробластомы и опухоли Вильмса.
В еще более предпочтительном аспекте наночастица ферритина для применения при лечении рецидива рака содержит химиотерапевтическое средство, которое представляет собой доксорубицин, производные платины, таксан, ингибиторы PARP-1, ингибиторы mTOR, ингибиторы PI3K, бензотиазолы, куркуминоиды и десфероксамин B.
Также в описании раскрывается способ лечения субъекта, страдающего от рака, включающий стадии:
- введения наночастиц ферритина, содержащих химиотерапевтическое средство, указанному субъекту,
при этом указанное лечение направляется на сохранение T-клеток указанного субъекта.
В предпочтительном аспекте указанный способ относится к сохранению T-клеток указанного субъекта, страдающего от рака молочной железы и подвергающегося лечению химиотерапевтическим средством, включая стадии:
- введения наночастиц ферритина, содержащих химиотерапевтическое средство, указанному субъекту.
В еще одном предпочтительном аспекте, указанный способ относится к сохранению T- клеток указанного субъекта, страдающего от рака молочной железы и подвергающегося лечению доксорубицином, включающему стадии:
- введения наночастицы ферритина, содержащей доксорубицин, указанному субъекту.
Различные варианты осуществления и аспекты настоящего изобретения, описанные выше и заявленные в разделе формула изобретения ниже, находят экспериментальную поддержку в следующих примерах.
Примеры
Далее будут приведены примеры, которые вместе с приведенным выше описанием иллюстрируют некоторые варианты осуществления изобретения.
Пример 1. Получение HFn-DOX: дизайн, синтез, загрузка и характеристика HFn
Наночастица ферритина, также называемая в данном описании “нанокамера HFn”, согласно настоящему изобретению была получена с помощью технологии рекомбинантных ДНК в E. coli после создания соответствующего вектора экспрессии. Обратный комплемент кДНК, кодирующей тяжелую цепь человеческого ферритина, был модифицирован путем вставки сайтов рестрикции для NotI и NdeI (в 5′ и 3′ соответственно) и синтезирован с помощью Eurofins MWG Operon. Полученный фрагмент ДНК был субклонирован в pET30b(+) вектор между NotI и NdeI сайтами рестрикции для экспрессии HFn под контролем T7 промотора. Полученную в результате плазмиду pET30b(+)/HFn использовали для трансформации с использованием теплового шока экспрессирующего штамма E. coli BL21(DE3), и трансформированные клоны были отобраны по резистентности к канамицину.
Процедура получения HFn была разработана для 1 л флакона, а затем масштабирована на 1 л биореактор с сохранением по существу той же самой процедуры производства и очистки белка. Трансформированные клетки выращивали при 37°C в среде LB/канамицин при встряхивании при 220 об/мин до лаг-фазы (OD 600 нм = 0,6). Затем, выработку белка индуцировали с помощью 0,5 мM изопропилтиогалактозида (IPTG) в течение 2 часов 30 минут, и клетки собирали центрифугированием при 4000×g в течение 15 минут и промывали PBS буфером. Мы получили 4-4,5 г/л культуры с помощью стандартной процедуры, в то время как при использовании биореактора мы могли получить 20-22 г осадка на 1 л культуры. Клетки ресуспендировали в лизирующем буфере с добавлением лизоцима и ДНКазы I, обрабатывали ультразвуком, чтобы разрушить клеточную мембрану, и центрифугировали, чтобы собрать первичный экстракт. Первичный экстракт подвергали тепловой обработке в течение 15 мин при 70°C, что вызывало денатурацию почти всех белков за исключением HFn. Затем супернатант был загружен на ионообменную смолу DEAE Sepharose, предварительно уравновешенную 20мM KMES, pH 6,0 и элюировали HFn с помощью пошагового градиента хлорида натрия от 70 мM до 420 мM, в 20мM KMES, pH 6,0. Выход процесса составляет около 56 мг/л культуры.
Процедура очистки в основном одинаковая как при использовании осадка, полученного в 1 л биореакторе. В этом случае осадок делили на три аликвоты около 7 г каждая. Более того, процесс разрушения ультразвуком был заменен прессом Френча, и объем слоя для хроматографии был увеличен до 10 мл.
Этот процесс приводил к трехкратному увеличению выработки HFn после увеличения масштаба с применением системы 1 л биореактора. Чтобы увеличить чистоту HFn мы ввели дополнительную стадию, состоящую из жидкостной гель-фильтрационной хроматографии быстрого разрешения с применением колонки Superose 6 Increase 6 Increase 10/300 GL. Белковый гель-электрофорез проводили в неденатурирующих условиях, и визуализация с помощью трансмиссионной электронной микроскопии показала, что структурная целостность нанокамеры HFn сохраняется после очистки. Профили, полученные по методу динамического рассеяния света (DLS), подтвердили однородную монодисперсную популяцию со средним гидродинамическим размером 11,98. HFn является отрицательно заряженным с ζ-потенциалом –24,8 ± 0,8 мВ. Анализ микоплазмы и бактериальная культура показали, что продукт HFn не содержит загрязнений. Более того, анализ активации TNF-альфа выявил, что стадия очистки на основе жидкостной хроматографии быстрого разрешения необходима для того, чтобы избежать активации TNF-альфа.
Загрузку HFn доксорубицином осуществляли с помощью pH-зависимой процедуры разборки. Раствор 200 мкM доксорубицина гидрохлорида (8 мкмоль) добавили к раствору HFn (20 мг, 0,5 мг мл−1 в 0,15 M NaCl) и довели значение до pH 2,0 с помощью 0,1 M хлористой кислоты (HCl). Затем, значение pH поддерживали в течение примерно 15 минут, и когда диссоциация HFn была завершена, значение pH повышали до 7,5, используя 0,1 M гидроксид натрия (NaOH).
Полученный в результате раствор перемешивали при комнатной температуре в течение 2 часов. Для того, чтобы удалить избыток доксорубицина (DOX) и абсорбировать молекулы, раствор загружали в колонку для обессоливания ZEBA (Thermofisher). Эта процедура является воспроизводимой и дает возможность восстановить около 25% инкубированного HFn. Восстановление DOX составляет около 27%. Смесь HFn-DOX (наночастица ферритина, содержащая доксорубицин) можно было концентрировать до концентрации 400 мкг/мл DOX. Нанолекарственное средство может храниться при 4°C в случае непродолжительного хранения или при -20°C в случае длительного хранения. Гель-электрофорез нативного белка и изображения, полученные с помощью просвечивающего электронного ПЭМ, подтвердили, что структурная целостность нанокамеры HFn-DOX сохраняется после загрузки. Профили, полученные с помощью DLS, подтвердили однородную монодисперсную популяцию со средним гидродинамическим размером 12,44± 1,1 нм. HFn является отрицательно заряженным с ζ-потенциалом -25± 0,9 мВ.
Этот продукт является стабильным при 4°C до 1 месяца, как показано с помощью DLS. При хранении при -20°C стабильность сохраняется дольше. Мы обнаруживали стабильность вплоть до 8 месяцев.
Пример 2. Противоопухолевая активность HFn-DOX in vitro и in vivo
Что касается активности in vitro, взаимодействие HFn с раковыми клетками было оценено при помощи проточной цитометрии после инкубации FITC-меченого HFn с применением панели линий мышиных и человеческих раковых клеток, главным образом, рака молочной железы, в течение 2 часов при 4°C. Клетки HUVEC были выбраны в качестве здоровых клеток с высокой TfR1-экспрессией. Конкурентный анализ, проведенный с применением немеченых HFn в качестве конкурента, показал, что взаимодействие между HFn и клеточными линиями является специфическим. Конфокальная микроскопия подтвердила, что HFns быстро интернализируются и солокализуются с рецептором трансферрина 1.
Нанолекарственное средство HFn-DOX является более эффективным в уменьшении жизнеспособности раковой клетки по сравнению со свободным DOX, как сообщалось в анализе жизнеспособности, проводимом с помощью 4T1 и HeLa клеток.
Затем, мы оценили in vivo активность HFn-DOX нанолекарственного средства. Для доказательства идеи мы использовали ортотопическую модель аллогенного трансплантата рака молочной железы, полученную с помощью инъекции 4T1 клеток в жировое тело молочной железы самок мышей BALB/c 6-8 недельного возраста. Эта модель характеризуется высоким уровнем пролиферации, миграции и инвазивности, DOX-индуцибельной экспрессией MDR-1 (или P-гликопротеина) и устойчивой экспрессией люциферазы. Во-первых, мы оценили нацеливание на опухоль и биораспределение пустой HFn. HFn, меченые Alexa fluor 660, вводили в хвостовую вену мышей, несущих опухоль. В разные временные точки флуоресцентный сигнал от HFn регистрировали in vivo и ex vivo в опухолевых образцах, обнаруживая, что HFn достигает опухоли через 1 час после инъекции. Затем наблюдалось быстрое исчезновение флуоресцентного сигнала. Конфокальные изображения криосрезов опухоли показали, что HFn глубоко проникает в опухолевую ткань, как продемонстрировано внутриклеточной локализацией зеленого сигнала.
Исследование биораспределения показало массивное накопление в печени, хотя этот сигнал полностью пропадает через 48 часов после инъекции. По-видимому, HFn не достигают легких, мозга и сердца, в то время как имеется небольшая локализация в почках и селезенке в пределах первых двух часов после инъекции.
Присутствие флуоресцентного сигнала в почках, в сочетании с сигналом в мочевом пузыре и моче, дает веские основания предполагать выведение HFns с мочой. Что касается HFn-DOX, то мы оценивали биодоступность лекарственного средства, измеряя с помощью масс-спектрометрии количество доксорубицина и доксорубицинола в плазме в разные временные точки после введения лекарственного средства в сравнении со свободным DOX и CAELYX, который представляет собой липосомальную форму DOX.
Липосомальный DOX улучшает биодоступность DOX, в то время как нанокомпозиция на основе HFn является сходной со свободным DOX. Однако, липосомальный DOX показывает также большое увеличение количества доксорубицинола, который является самым токсичным производным DOX. Накопление в опухоли HFn-DOX является сходным с накоплением, наблюдаемым для свободного DOX, что подтверждает отсутствие улучшения доставки лекарственного средства в опухоль.
Нанокомпозиция на основе нанокамер HFn улучшает биораспределение DOX в сравнении со свободным DOX, уменьшая количество DOX и DOXol, накопленного в нецелевых органах, и выводится с мочой. В нашей схеме лечения HFn-DOX, свободный DOX, липосомальный DOX или плацебо вводили мышам-опухоленосителям в дни 5, 9, 13 и 17 после имплантирования клеток в дозировке 1,24 мг/кг (примерно в 20 раз меньше терапевтической дозировки DOX на мышиных моделях).
Обе нанокомпозиции значительно уменьшали прогрессирование опухоли, воздействуя на количество апоптотических клеток в опухолевой ткани, и также на ангиогенез опухоли, как показано с помощью основанного на CD31 иммуногистохимического исследования опухолевых срезов, иссеченных на 21 день. HFn-DOX не стимулирует сверхэкспрессию MDR-1 и, следовательно, химиорезистентость. Для оценки токсичности мы проводили анализ гемолиза, измеряя коэффициент поглощения гемовой группы. Мы подтвердили, что нанокомпозиция на основе нанокамер HFn не способна индуцировать гемолиз в эритроцитах. Гистопатологическая оценка, проведенная на печени, почках, селезенке, мозге, кишечнике и легких, иссеченных на 21 день у мышей, леченых HFn-DOX, DOX, липосомальным DOX и плацебо, подтвердила общую безопасность HFn-DOX в этих органах.
Оценка функционального состояния печени, проведенная по анализу AST и ALT, показала, что HFn-DOX является безопасным в тестируемых условиях. Для проверки функционального состояния почек использовали отношение креатинин/мочевина, которое свидетельствовало о том, что состояние почек не затрагивается лечением HFn-DOX. Наконец, мы сосредоточили наши исследования на кардиотоксичности, которая является основным и наиболее тяжелым недостатком химиотерапии доксорубицином. Наши исследования показали, что HFn-DOX не вызывает увеличения площади поперечного сечения кардиомиоцитов, что является первым сигналом повреждения сердца, наблюдаемого при использовании DOX и липосомального DOX. Анализируя подробно морфологию ткани сердца, мы наблюдали увеличение числа митохондрий в образцах, леченых DOX и липосомальным DOX, в сравнении с плацебо. Этого не отмечалось в образцах, леченых HFn-DOX. Более того, увеличение числа митохондрий сочеталось с изменением поверхности митохондрий и морфологии крист, которые не регистрировались в образцах, пролеченных HFn-DOX. Лечение DOX и липосомальным DOX индуцировало изменения в потенциале митохондриальной мембраны и в количестве восстановленного глутатиона, что является сигналами ненормального функционального состояния митохондрий. Наоборот, HFn-DOX демонстрировал функциональное поведение, сходное с плацебо.
Следует принять во внимание, что HFn-DOX может обеспечить возможность лечения пациентов, усиливая противораковую активность DOX и в то же время сводя к минимуму кардиотоксичность. Наша идея заключается в том, что вид лекарственного наносредства может быть инновационным в клиническом подходе к лечению HER2-положительного рака молочной железы, поскольку для лечения этого подтипа рака существует два высокоэффективных лекарственных средства, трастузумаб и доксорубицин, которые не могут быть введены в комбинации из-за их тяжелой кардиотоксичности, как показано испытаниями NOAH. Действительно, блокировка HER2 сигнального пути трастузумабом предотвращает активацию сигнальных путей, которые опосредуют рост кардиомиоцитов и механизмы сердечной репарации, приводя в результате к чувствительности к сердечному стрессу. Антрациклины оказывают прямое цитотоксическое действие на кардиомиоциты, приводя к тяжелым кардиотоксическим эффектам. Следовательно, ингибирование HER2 димеризации совместно с терапией антрациклином может усугубить антрациклин-индуцированное повреждение сердца. Наномедицина отвечает на эту клиническую проблему, причем ответом наномедицины на эту клиническую проблему является HFn-DOX.
Мышей с опухолью HER2+ BC лечили 5 раз, два раза в неделю, используя плацебо, HFn-DOX (1 мг/кг, внутривенно), TZ (5 мг/кг, внутрибрюшинно) и их комбинацию. Главной конечной точкой были кардиотоксичность и противораковая эффективность. Хотя однократное лечение HFn-DOX или TZ продемонстрировало хорошую способность к уменьшению прогрессирования опухоли, их комбинация улучшает противоопухолевый потенциал, воздействуя на размер опухоли и ангиогенез. Поскольку основной активностью TZ является индуцирование антителозависимой клеточноопосредованной цитотоксичности, мы оценили эффект HFn-DOX на инфильтрирующие опухоль лимфоциты (TIL), показав, что и численность TILs и активность TIL не поддается влиянию HFn-DOX. С другой стороны, HFn-DOX повышает индукцию апоптоза, указывая на то, что уменьшение размера опухоли, наблюдаемое у мышей, которых лечили комбинацией TZ и HFn-DOX, объясняется сопряжением этих активностей. Морфология митохондрий была исследована на предмет кардиотоксичности. Патологическое увеличение поверхности митохондрий наряду с истощением крист наблюдалась только у мышей, которых лечили одним TZ, подтвердив общую безопасность композиции HFn-DOX. Интересно отметить, что мыши, леченые TZ и HFn-DOX, не демонстрировали признаков сердечной болезни. Определение количества TZ в опухоли и сердце выявило, что комбинация с HFn-DOX ассоциируется с повышенным накоплением TZ и проникновением TZ в опухоль вместе с уменьшением TZ в сердце, что приводит к отсутствию кардиотоксичности. Наши результаты показывают, что комбинированная терапия с HFn-DOX и TZ обеспечивает повышенную противораковую активность и пониженную кардиотоксичность, с возможными трансляционными воздействиями в отношении лечения HER2+ BC.
Пример 3. Новшество: композиция DOX способна сохранять иммуннокомпетентность T-клеток
Рак молочной железы (BC) является наиболее часто диагностируемым злокачественным новообразованием и второй лидирующей причиной смерти среди женщин, связанной с раком. Антрациклины, такие как доксорубицин (DOX), считаются фундаментальной основой химиотерапии для лечения BC благодаря их превосходной цитотоксической активности. Действительно, DOX проявляет прямую цитотоксичность в клетках BC, напрямую вмешиваясь в репликацию ДНК, и, таким образом, он является очень эффективным против высоко-пролиферативных видов рака. Кроме непосредственной убивающей активности, DOX действует, увеличивая опухолевую иммуногенность: DOX индуцирует иммунологическую смерть раковой клетки (ICCD), что облегчает антиген-презентацию дендритными клетками (DC). Действительно, раковые клетки распознаются как «не свои» иммунной системой, так как они экспрессируют определенные опухоль-ассоциированные антигены и/или неоантигены. Первые распознаются как «не свои», так как они экспрессируются ненормальным образом в опухолях, тогда как неоантигены являются белками, которые несут опухоль-специфические мутации, как результат высокой геномной нестабильности рака, которая приводит к прогрессирующему накоплению мутированных генов. После смерти раковой клетки, происходящей во время лечения химиотерапией на основе DOX, некоторые раковые неоантигены становятся непосредственно доступными и активируют DC. DC в свою очередь стимулируют созревание немногочисленных наивных рак-специфических T-клеток и клональную экспансию, для того, чтобы индуцировать адаптивный противоопухолевый иммунный ответ. Противоопухолевый иммунитет может иметь решающее значение для получения полной ремиссии, чтобы генерировать эффективную иммунологическую память (IM), которая может «вести наблюдение» за рецидивом и/или метастазами. Этот способ развития противоопухолевого иммунитета, на котором основывается представление о “in situ вакцине”, усиленно развивается как исследователями, так и клиницистами, потому что: 1) неоантигены, высвобождаемые во время иммуногенной смерти раковых клеток, имеют сходство со всем антигенным набором BC, таким образом, предотвращая возможный «уход» опухоли от иммунного ответа; 2) этот тип “вакцинации от рака” является персонализированным и не нуждается в идентификации единых раковых антигенов; 3) он является относительно простым вариантом использования противораковой иммунной стратегии; 4) наиболее агрессивные BC, такие как TNBC и HER2-положительный, являются высоко-иммуногенными раками, следовательно, эта стратегия может быть особенно эффективной в виде неоадьювантной терапии.
Однако, некоторые серьезные проблемы в настоящее время ограничивают применение этой иммунной стратегии для BC, леченых DOX. Во-первых, существует парадокс в связи с возможными последствиями для иммунитета DOX-лечения: DOX допускает и стимулирует гибель иммуногенных раковых клеток (ICCD), которая является необходимой для инициирования этого противоопухолевого иммунного ответа, однако в то же самое время она ограничивается самим DOX. Действительно, клональная экспансия T-клеток является одним из самых больших пролиферативных событий, наблюдаемых в биологических системах, таким образом, ожидается, что она будет сильно уменьшена или даже подавлена лечением DOX. Поэтому эффект антрациклинов на делящиеся T-клетки настоятельно требует изучения с целью улучшения DOX-опосредованного противоопухолевого иммунитета.
Эта стратегия является многообещающей, когда речь идет о полной ликвидации опухоли, и может обеспечить длительный иммунологический надзор за рецидивами и метастазированием.
На основании приведенных выше описания и примеров очевидны преимущества, достигнутые при использовании способов, описанных и полученных согласно настоящему изобретению.
Ссылки
Bellini M, Mazzucchelli S, Galbiati E, Sommaruga S, Fiandra L, Truffi M, Rizzuto MA, Colombo M, Tortora P, Corsi F, Prosperi D. J Control Release. 2014 Dec 28;196:184-96. doi: 10.1016/j.jconrel.2014.10.002. Epub 2014 Oct 13.
Mazzucchelli S, Bellini M, Fiandra L, Truffi M, Rizzuto MA, Sorrentino L, Longhi E, Nebuloni M, Prosperi D, Corsi F. Oncotarget. 2017 Jan 31;8(5):8383-8396. doi: 10.18632/oncotarget.14204
Ma, Y., et al., Anticancer chemotherapy-induced intratumoral recruitment and differentiation of antigen-presenting cells. Immunity, 2013. 38(4): p. 729-41.
Reuschenbach, M., M. von Knebel Doeberitz, and N. Wentzensen, A systematic review of humoral immune responses against tumor antigens. Cancer Immunol Immunother, 2009. 58(10): p. 1535-44.
Mattarollo, S.R., et al., Pivotal role of innate and adaptive immunity in anthracycline chemotherapy of established tumors. Cancer Res, 2011. 71(14): p. 4809-20.
Bracci, L., et al., Immune-based mechanisms of cytotoxic chemotherapy: implications for the design of novel and rationale-based combined treatments against cancer. Cell Death Differ, 2014. 21(1): p. 15-25.
Tsung, K. and J.A. Norton, In situ vaccine, immunological memory and cancer cure. Hum Vaccin Immunother, 2016. 12(1): p. 117-9.
Verma, R., et al., Lymphocyte depletion and repopulation after chemotherapy for primary breast cancer. Breast Cancer Res, 2016. 18(1): p. 10.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОСНОВАННАЯ НА НАНОЧАСТИЦАХ, НАЦЕЛЕННАЯ НА ОПУХОЛИ ДОСТАВКА ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2011 |
|
RU2593367C2 |
| АДРЕСНОЕ ВОЗДЕЙСТВИЕ НА УСТОЙЧИВЫЙ К ТРАСТУЗУМАБУ HER2+ РАК МОЛОЧНОЙ ЖЕЛЕЗЫ ПОСРЕДСТВОМ HER3-НАЦЕЛЕННЫХ НАНОЧАСТИЦ | 2015 |
|
RU2692104C2 |
| СПОСОБЫ ПРИМЕНЕНИЯ АНТАГОНИСТОВ ВАЗОПРЕССИНА С АНТРАЦИКЛИНОВЫМИ ХИМИОТЕРАПЕВТИЧЕСКИМИ СРЕДСТВАМИ ДЛЯ СНИЖЕНИЯ КАРДИОТОКСИЧНОСТИ И/ИЛИ УЛУЧШЕНИЯ ВЫЖИВАНИЯ | 2008 |
|
RU2470643C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ БОРЬБЫ С КАРДИОТОКСИЧНОСТЬЮ, ВЫЗВАННОЙ ХИМИОТЕРАПИЕЙ | 2017 |
|
RU2743433C2 |
| СПОСОБ СОЧЕТАННОЙ ТЕРАПИИ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС С ИСПОЛЬЗОВАНИЕМ КОНЬЮГАТА ДИПРОПОКСИБАКТЕРИОПУРПУРИНА С ДОКСОРУБИЦИНОМ | 2023 |
|
RU2808909C1 |
| СПОСОБ УЛУЧШЕНИЯ ФУНКЦИИ ИММУННЫХ КЛЕТОК И ОЦЕНКИ МУЛЬТИФУНКЦИОНАЛЬНОСТИ ИММУННЫХ КЛЕТОК | 2015 |
|
RU2731098C2 |
| РЕЦЕПТОР-НАПРАВЛЕННЫЕ КОНСТРУКЦИИ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2682335C2 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ С ИСПОЛЬЗОВАНИЕМ СОЕДИНЕНИЯ, ОКАЗЫВАЮЩЕГО ВОЗДЕЙСТВИЕ НА ГЛИКОЛИЗ | 2016 |
|
RU2723215C2 |
| ЛЕЧЕНИЕ РАКА КОМБИНАЦИЕЙ ЛУЧЕВОЙ ТЕРАПИИ, НАНОЧАСТИЦ ОКСИДА ЦЕРИЯ И ХИМИОТЕРАПЕВТИЧЕСКОГО СРЕДСТВА | 2015 |
|
RU2704811C2 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2675233C1 |
Изобретение касается области терапии рака. Предложено применение наночастицы ферритина, содержащей химиотерапевтическое средство, представляющее собой доксорубицин, при лечении рецидива рака для снижения кардиотоксичности, вызываемой химиотерапией доксорубицином. Изобретение обеспечивает эффективное лечение рака при снижении кардиотоксичности химиотерапии. 2 з.п. ф-лы, 3 ил., 3 пр.
1. Применение наночастицы ферритина, содержащей химиотерапевтическое средство, представляющее собой доксорубицин, при лечении рецидива рака для снижения кардиотоксичности, вызываемой химиотерапией доксорубицином.
2. Применение по п. 1, согласно которому указанный рак является раком молочной железы, раком мочевого пузыря, раком легкого, раком желудка, раком яичника; лимфомой Ходжкина, неходжкинской лимфомой, некоторыми типами лейкемии, включая острый лимфобластный лейкоз (ALL) и острый миелоцитарный лейкоз (AML, ANLL).
3. Применение по любому из пп. 1 или 2, в котором указанное химиотерапевтическое средство применяют в лечении рака щитовидной железы, сарком мягких тканей или костей, нейробластомы и опухоли Вильмса.
| WO 2015135597 A1, 17.09.2015 | |||
| ДВУХДИАПАЗОННАЯ ПОЛОСКОВАЯ АНТЕННА | 1991 |
|
RU2012956C1 |
| BELLINI M et al | |||
| Protein nanocages for self-triggered nuclear delivery of DNA-targeted chemotherapeutics in Cancer Cells | |||
| J Control Release, 2014, 196:184-96 | |||
| LIANG M et al | |||
| H-ferritin-nanocaged doxorubicin nanoparticles specifically target and kill tumors with a single-dose injection | |||
| Proc | |||
Авторы
Даты
2023-12-27—Публикация
2019-10-31—Подача