Область техники
Настоящее изобретение относится к фармацевтической композиции для лечения опухоли и, в частности, к фармацевтической композиции, содержащей терапевтически эффективное количество экзосомы, несущей нацеленную на антиген-4 цитотоксических Т лимфоцитов (CTLA-4) микроРНК (миРНК), и терапевтически эффективное количество онколитического вируса простого герпеса (oHSV). Настоящее изобретение также относится к набору, содержащему экзосому, несущую нацеленную на CTLA-4 миРНК и oHSV, и к способам применения фармацевтической композиции и набора для лечения опухоли.
Уровень техники
Рак как заболевание является многогранным врагом, который может поддаваться назначенному лечению, а может развить устойчивость к различным видам терапии. Субпопуляция клеток внутри опухолей устойчива к традиционным способам лечения и может нести ответственность за рецидив заболевания.
Хирургическое лечение рака является распространенным способом местного лечения. В дополнение к некоторым злокачественным опухолям системы крови, таким как лейкоз, лимфома и т.д., другие различные злокачественные опухоли включают одну или более отчетливых солидных опухолей, которые можно удалить хирургически. Однако хирургическое лечение всегда несет определенные риски и зачастую связано с возникновением других сопутствующих заболеваний или потенциальным нарушением функции органов.
К настоящему моменту консервативные методы лечения рака (в основном традиционная химиотерапия, таргетная биологическая терапия и лучевая терапия) не дали полностью удовлетворительных результатов. Сохраняющиеся проблемы включают низкую селективность в отношении мишени, устойчивость к препарату, отсутствие возможности эффективно влиять на течение метастатического заболевания, а также тяжелые побочные эффекты. В противовес этому иммунологические методы лечения, которые в целом стимулируют иммунитет хозяина на выработку системного ответа против опухолей, в настоящее время имеют большие клинические перспективы.
Для лечения солидных опухолей широко исследуются онколитические вирусы простого герпеса (oHSV). Как группа они обладают многими преимуществами по сравнению с традиционными методами лечения рака. В частности oHSV обычно содержат мутацию, которая делает их чувствительными к ингибирующему действию некоторых аспектов врожденного иммунитета. Как следствие, они реплицируются в раковых клетках, в которых нарушен один или более врожденных иммунных ответов на инфекцию, однако в нормальных клетках с неизмененными врожденными иммунными ответами репликация не происходит. oHSV обычно вводят непосредственно в массу опухолевой ткани, характеризующаяся тем, что вирус может реплицироваться. Вследствие того, что вирус вводят в целевую ткань, а не системно, отсутствуют характерные для противораковых препаратов побочные эффекты. Вирусы характерным образом индуцируют адаптивные иммунные ответы, которые сокращают возможность их многократного введения. oHSV вводили в опухоли множество раз без признаков потери эффективности или способности индуцировать нежелательную реакцию, например, в виде воспалительных ответов. HSV являются крупными ДНК-содержащими вирусами, в геномы которых можно встраивать чужеродные ДНК и регулировать экспрессию этих генов при введении в опухоли. Чужеродные гены, подходящие для использования с oHSV, представляют собой гены, которые помогают индуцировать адаптивный иммунный ответ на опухоль.
Дефект преодоления врожденного клеточного иммунного ответа определяет ряд опухолей, в которых вирус oHSV, демонстрируя свою онколитическую способность, проявляет себя как противораковый препарат. Чем обширнее делеции, тем более ограничен диапазон раковых клеток, в которых oHSV эффективен, что зависит от функции удаленного вирусного гена. Самый новый oHSV несет по меньшей мере один клеточный ген для усиления противораковой активности вируса.
Успех терапии на основе oHSV зависит от степени разрушения раковых клеток. На ранних этапах разработки oHSV было установлено, что применение только HSV не может уничтожить все раковые клетки в солидной опухоли, и маловероятно, что лечение с применением oHSV может эффективно удалить все раковые клетки, при этом в клинических исследованиях было установлено, что разрушение опухолей под действием oHSV должно проходить с развитием адаптивного иммунного ответа на опухоль. Дальнейшие исследования показали, что противоопухолевый иммунный ответ, генерируемый остатками клеток инфицированной опухоли, может быть усилен встраиванием цитокинов. Сравнение oHSV без гена цитокина с oHSV, содержащим ген иммуностимулирующего цитокина, подтвердило эту гипотезу и в конечном итоге привело к включению гена ГМ-КСФ в oHSV, разработанный для лечения меланомы.
Встраивание генов, кодирующих иммуностимулирующие цитокины, усиливает иммунный ответ на опухоль, однако не усиливает эффективным образом цитототоксичность Т-клеток, которая имеет решающее значение для противоопухолевых эффектов. Опухоли обладают ингибирующими сигнальными путями PD-1 и CTLA-4, которые заставляют «молчать» иммунную систему. PD-1 экспрессируется как на активированных Т-клетках, так и на других гемопоэтических клетках, a CTLA-4 экспрессируется на активированных Т-клетках, включая регуляторные Т-клетки. Опухоли активируют ингибиторные сигнальные пути PD-1 и CTLA-4 для ускользания от иммунного ответа хозяина.
Несмотря на широкое изучение и анализ в доклинических и клинических условиях, сохраняется неудовлетворенная потребность в разработке способов лечения опухолей.
Краткое описание
В одном аспекте изобретение относится к фармацевтической композиции, содержащей терапевтически эффективное количество экзосомы, несущей нацеленную на CTLA-4 миРНК, и терапевтически эффективное количество онколитического вируса простого герпеса (oHSV), экспрессирующего иммуностимулирующий агент или иммуностимулирующий агент и анти-PD-1 антитело.
Экзосома содержит ассоциированный с упаковокой в экзосому мотив (далее также называемый «экзомотив»), функционально связанный, необязательно через линкер, с миРНК, нацеленной на CTLA-4. В одном варианте реализации экзосома содержит ингибирующее количество нацеленной на CTLA-4 миРНК, при этом нацеленная на CTLA-4 миРНК обладает затравочной последовательностью, связывающейся с мРНК CTLA-4; и экзомотив, функционально связанный с затравочной последовательностью нацеленной на CTLA-4 миРНК, для улучшения упаковки нацеленной на CTLA-4 миРНК в эзкосому. В некоторых вариантах реализации экзомотив расположен ниже и ковалентно связан с затравочной последовательностью нацеленной на CTLA-4 миРНК. В некоторых вариантах реализации экзомотив расположен ниже и ковалентно связан с затравочной последовательностью CTLA-4 линкером. В некоторых вариантах реализации экзомотив получают путем мутации одной или более нуклеиновых кислот нацеленной на CTLA-4 миРНК, за исключением затравочной последовательности. В некоторых вариантах реализации экзомотив представлен двойным мотивом, образованным в результате комбинации двух отдельных экзомотивов. В некоторых вариантах реализации нацеленная на CTLA-4 миРНК и экзомотив, если они функционально связаны, имеют по меньшей мере один или два общих нуклеотида.
oHSV представляет собой рекомбинантный онколитический вирус простого герпеса первого типа (ВПГ-1, HSV-1), экспрессирующий иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело.
Другой аспект изобретения относится к фармацевтической композиции, содержащей терапевтически эффективное количество экзосомы, несущей нацеленную на CTLA-4 миРНК, терапевтически эффективное количество oHSV и фармацевтически приемлемый носитель. Экзосома содержит ассоциированный с упаковокой в экзосому мотив, функционально связанный, необязательно через линкер, с миРНК, нацеленной на CTLA-4. oHSV экспрессирует иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело.
Другой аспект изобретения относится к набору для лечения опухоли, содержащему экзосому, несущую миРНК, нацеленную на CTLA-4, и oHSV, экспрессирующий иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело. Набор может дополнительно содержать инструкции по использованию экзосомы и oHSV для лечения опухолей.
Дополнительный аспект изобретения относится к способу лечения опухоли у субъекта, включающему одновременное введение субъекту терапевтически эффективного количества экзосомы, несущей миРНК, нацеленную на CTLA-4, и терапевтически эффективное количество oHSV, экспрессирующего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело.
Дополнительный аспект изобретения относится к способу повышения эффективности терапии oHSV у субъекта, включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества экзосомы, несущей миРНК, нацеленную на CTLA-4, изобретения в дополнение к терапии oHSV.
Другие аспекты изобретения будут доступны в приведенном ниже описании.
Краткое описание фигур
Фигура 1. Панель А представляет собой схематическую диаграмму плазмиды, кодирующей миРНК, нацеленной на CTLA4. Плазмида состоит из последовательности, кодирующей усиленный зеленый флуоресцентный белок (EGFP), содержащей на своей 3'-нетранслируемой области (3'-НТО) последовательность, кодирующую разработанную миРНК, нацеленную на ген CTLA-4 (miR-CTLA-4). Панель В показывает нуклеотидную последовательность миРНК, нацеленную на ген CTLA-4 мышей. Нуклеотиды, выделенные жирным курсивом и подчеркнутые, обозначают ассоциированные с упаковкой в экзосомы мотивы (ЭКЗО-мотивы). На Панели С показано подавление CTLA4 разработанными миРНК. Клетки НЕр-2, высеянные в 24-луночные планшеты, котрансфицировали с использованием 0,25 мкг плазмид, экспрессирующих 10 последовательностей ДНК, кодирующих миРНК против CTLA-4 (№1 - №10) или нецелевые миРНК (NT), и 0,25 мкг плазмиды, кодирующей меченный гистидиновой меткой CTLA-4 мышей (меченный гистидиновой меткой CTLA-4). Клетки собирали через 72 часа после трансфекции. Накопление CTLA4 и глицеральдегид-3-фосфатдегидрогеназы (GAPDH) измеряли методом, известным специалисту в данной области техники.
Фигура 2. Характеристика экзосомы, несущей miR-CTLA-4. Клетки НЕр-2, высеянные в колбу Т150, трансфицировали с 10 мкг плазмиды miR-CTLA-4-3# или плазмиды, экспрессирующей нецелевую миРНК (NT), затем инкубировали в бессывороточной среде. Через 48 часов среду собирали, а экзосомы очищали, как описано в разделе «Материалы и методы». Очищенные экзосомы подвергли 2 сериям анализов. Сначала (панель А) равные количества клеток, в которых образовались экзосомы, и равные количества экзосом растворили, подвергли электрофорезу в денатурирующем геле, анализировали с помощью антител к CD9, флотилину-1 и калнексину. В основном очищенные экзосомы содержали CD9, флотилии-1, но не содержали калнексина. Распределение по размеру экзосом (панель В), образованных трансфицированными клетками, проводили, как описано в разделе «Материалы и методы».
Фигура 3. Влияние экзосом, несущих miR-CTLA-4, введенных изолированно (панель А) или одновременно с T1012G (панель В), Т2850 (панель С) или Т3855 (панель D), на рост опухоли MFC. Опухолевые клетки MFC вводили мышам C57BL/6J подкожно путем инъекции в правый бок. В группах по 8 животных, у которых опухоль MFC в среднем составляла 80 мм3, внутрь опухоли вводили путем инъекции 10 мкг экзосомы изолированно или одновременно с 50 мкл 1×107 БОЕ T1012G, Т2850 или Т3855. Все исследования проводили одновременно, однако результаты представлены на 4 панелях. Объемы опухолей представлены как среднее значение ±SEM у 8 животных в каждой группе.
Подробное описание изобретения
Определения
Следует отметить, что «объект/сущность» с грамматическими показателями единственного числа относится к одному или более этим объектам/сущностям; например, следует понимать что "экзосома" представляет одну или более экзосом. По существу, грамматические показатели единственного числа, термины "один или более" и "по меньшей мере один" могут быть использованы в настоящем документе взаимозаменяемо.
«Гомология» или «идентичность» или «схожесть» относится к схожести последовательностей двух белков или двух молекул нуклеиновых кислот. Гомология может быть определена путем сравнения положения в каждой последовательности, которая может быть выровнена в целях сравнения. Если положение в сравниваемой последовательности занято одним и тем же основанием или аминокислотой, тогда молекулы гомологичны по этому положению. Степень гомологии между последовательностями является функцией числа совпадающих или гомологичных положений, общих для последовательностей. «Неродственная» или «негомологичная» последовательность обладает менее 40% идентичности, однако предпочтительнее менее 25% идентичности, с одной из последовательностей по настоящему изобретению.
Полинуклеотид или область полипептида (или полипептид или область полипептида) обладает определенным процентом (например, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98% или 99%) «идентичности последовательности» с другой последовательностью, означая, что при выравнивании этот процент оснований (или аминокислот) одинаков при сравнении двух последовательностей. Такое выравнивание и процент гомологии или идентичности последовательности можно определить с помощью программных продуктов, известных в технике.
В настоящем документе термин «линкер» относится к короткому фрагменту нуклеотидной последовательности, содержащему два или более нуклеотида, которые могут быть одинаковыми или различаться, причем нуклеотиды выбраны из группы, состоящей из аденина (А), гуанина (G), тимина (Т) и урацила (U).
В настоящем документе термины «лечить» или «лечение» относятся как к терапевтическому лечению, так и к профилактическим или превентивным мерам, целью которых является предотвращение или замедление (уменьшение) нежелательного физиологического изменения или нарушения, такого как прогрессирование опухоли. Благоприятные или желаемые клинические результаты включают, но не ограничиваются перечисленным, облегчение симптомов, минимизация выраженности заболевания, стабилизация (т.е. отсутствие ухудшения) состояния опухоли, ингибирование роста опухоли, снижение объема опухоли, задержка или замедление прогрессирование опухоли, улучшение состояния опухоли или временное облегчение, а также ремиссия (частичная или полная), поддающиеся определению или неопределяемые. Те, кто нуждается в лечении, включают тех, у кого уже есть опухоль, а также тех, у кого есть предрасположенность к опухоли.
Под «субъектом» или «индивируумом» или «животным» или «пациентом» или «млекопитающим» понимается любой субъект, в частности субъект, относящийся к млекопитающим, для которого желательна диагностика, прогноз или терапия. Субъекты, относящиеся к млекопитающим, включают людей, одомашненных животных, сельскохозяйственных животных и животных в зоопарках, спортивных или домашних животных, таких как собаки, кошки, морские свинки, кролики, крысы, мыши, лошади, крупный рогатый скот, коровы и так далее. Субъектом в настоящем документе предпочтительно является человек.
В настоящем документе выражения, такие как «пациенту, нуждающемуся в лечении» или «субъекту, нуждающемуся в лечении», включают субъектов, таких как субъекты -млекопитающие, которые могут получить пользу от введения композиции настоящего изобретения, используемого, например, для определения, для диагностической процедуры и/или для лечения.
В настоящем изобретении, помимо прочего, применяются антисмысловые олигомеры и схожие молекулы, использующиеся в модулировании функции или эффекта молекул нуклеиновых кислот, кодирующих CTLA4. Гибридизация олигомера данного изобретения с его нуклеиновой кислотой-мишенью в целом относится к «антисмысловой». Следовательно, предпочтительный механизм, считающийся включенным в реализацию некоторых предпочтительных вариантов изобретения, называется в настоящем документе «антисмысловым ингибированием». Такое антисмысловое ингибирование обычно основано на гибридизации олигонуклеотидных цепей или сегментов с образованием водородных связей, в результате чего по меньшей мере одна цепь или сегмент расщепляется, деградирует или иным образом становится нефункциональным. В связи с этим антисмысловое ингибирование в данном случае предпочтительно нацелено на определенные молекулы нуклеиновых кислот и их функции.
Функции РНК, подлежащие нарушению, могут включать такие функции как транслокация РНК к месту трансляции белка, транслокация РНК к местам внутри клетки, которые удалены от места синтеза РНК, трансляция белка с РНК, сплайсинг РНК с образованием одного или более видов РНК и каталитическая активность или комплексообразование с участием РНК, в которых РНК может быть задействована или которым может способствовать. Одним предпочтительным результатом такого нарушения функции нуклеиновой кислоты-мишени является модуляция экспрессии CTLA4. В контексте настоящего изобретения «модуляция» и «модуляция экспрессии» означает снижение (ингибирование) количества или уровней молекулы нуклеиновой кислоты, кодирующей ген, например, ДНК или РНК. Зачастую предпочтительной нуклеиновой кислотой-мишенью является мРНК.
В контексте данного изобретения «гибридизация» означает спаривание комплементарных цепей олигомеров. В настоящем изобретении предпочтительный механизм спаривания между комплементарными нуклеозидными или нуклеотидными основаниями (нуклеиновые основания) цепей олигомерных соединений включает образование водородных связей, которое может протекать по Уотсону-Крику, по Хугстину или по принципу обратной связи Хугстина. Например, аденин и тимин являются комплементарными нуклеиновыми основаниями, которые спариваются посредством образования водородных связей. Гибридизация может происходить при различных обстоятельствах.
В настоящем изобретении выражение «жесткие условия гибридизации» или «жесткие условия» относится к условиям, при которых соединение согласно изобретению будет гибридизироваться со своей последовательность-мишенью, но с минимальным числом других последовательностей. Жесткие условия зависят от последовательности и будут различны при различных обстоятельствах, и в контексте этого изобретения «жесткие условия», при которых олигомерные соединения гибридизируются с последовательностью-мишенью, определяются природой и составом олигомеров и исследованиями, с помощью которых они изучаются.
Термин «комплементарный» в настоящем документ, относится к способности точного спаривания между двумя нуклеиновыми основаниями олигомерного соединения. Например, если нуклеиновое основание в конкретной позиции олигонуклеотида (олигомерного соединения) способно к образованию водородной связи с нуклеиновым основанием в конкретной позиции нуклеиновой кислоты-мишени, целевая нуклеиновая кислота представлена ДНК, РНК или молекулой олигонуклеотида, то позиция образования водородной связи между олигонуклеотидом и нуклеиновой кислотой-мишенью считается комплементарной позицией. Олигонуклеотид и дополнительная молекула ДНК, РНК или олигонуклеотида комплементарны друг другу, если достаточное количество комплементарных позиций в каждой молекуле занято нуклеиновыми основаниями, которые могут связываться друг с другом водородными связями. Таким образом, «специфически гибридизующийся» и «комплементарный» являются терминами, которые используют для обозначения достаточной степени точного спаривания или комплементарности по достаточному количеству нуклеиновых оснований, в результате чего между олигонуклеотидом и нуклеиновой кислотой-мишенью происходит стабильное и специфическое связывание.
В данной области известно, что последовательность антисмыслового нуклеотида не должна быть на 100% комплементарна его нуклеиновой кислоте-мишени, чтобы специфически гибридизироваться. Кроме того, олигонуклеотид может гибридизоваться с одним или более сегментами, так что промежуточные или соседние сегменты не участвуют в событии гибридизации (например, структура петли или структура шпильки). Предпочтительно, чтобы антисмысловые соединения согласно настоящему изобретению имели по меньшей мере 70% или по меньшей мере 75% или по меньшей мере 80% или по меньшей мере 85% комплементарности последовательности с областью-мишенью в пределах нуклеиновой кислоты-мишени, более предпочтительно, чтобы они имели по меньшей мере 90% комплемертарности последовательности, и еще более предпочтительно, чтобы они имели по меньшей мере 95% или по меньшей мере 99% комплементарности последовательности с последовательностью-мишенью в пределах последовательности нуклеиновой кислоты-мишени, на которую они нацелены. Например, антисмысловое соединение, в котором 18 из 20 нуклеиновых оснований антисмыслового олигомера комплементарны области-мишени, и, следовательно, будут специфически гибридизоваться, будет иметь 90-процентную комплементарность. В настоящем примере оставшиеся некомплементарные нуклеиновые основания могут быть сгруппированы или находиться вперемежку с комплементарными нуклеиновыми основаниями и не обязательно должны быть смежными друг с другом или с комплементарными нуклеиновыми основаниями. Таким образом, антисмысловой олигомер длиной 18 нуклеиновых оснований, содержащий 4 (четыре) некомплементарных нуклеиновых основания, по обе стороны от которых находятся две области полной комплементарности к нуклеиновой кислоте-мишени, будет иметь общую комплементарность к нуклеиновой кислоте-мишени, составляющую 77,8% и, таким образом, попадет в рамки объема настоящего изобретения. Процент комплементарности антисмыслового соединения к области нуклеиновой кислоты-мишени может быть определен рутинно с использованием программ BLAST (средство поиска основного локального выравнивания) и программ PowerBLAST, известных в области техники.
В контексте этого изобретения термин «олигонуклеотид» относится к олигомеру или полимеру рибонуклеиновой кислоты (РНК) или дезоксирибонуклеиновой кислоты (ДНК) или к их миметикам, химерам, аналогам и гомологам. Этот термин включает олигонуклеотиды, содержащие природные нуклеиновые основания, сахара и ковалентные межнуклеозидные (остов) связи, а также олигонуклеотиды, содержащие неприродные фрагменты, которые функционально схожи. Такие модифицированные или замещенные олигонуклеотиды часто предпочтительнее нативных форм вследствие желательных свойств, таких как, например, улучшенный захват клетками, улучшенная аффинность к нуклеиновой кислоте-мишени и повышенная стабильность в присутствии нуклеаз.
В настоящем документе термин «микроРНК», «миРНК» или «миР» (miR) относится к РНК, которая функционирует, посттранскрипционно регулируя экспрессию генов, обычно путем связывания с комплементарными последовательностями в три-штрих (3') нетранслируемых областях (3'-НТО) транскриптов матричной РНК (мРНК), результатом чего обычно является сайленсинг генов. миРНК обычно представляют собой малые молекулы регуляторной РНК, например, состоящие из 21 или 22 нуклеотидов. Термины «микроРНК», «миРНК» и «миР» используются взаимозаменяемо.
В настоящем документе термин «опухоль» относится к злокачественной ткани, содержащей трансформированные клетки, которые неконтролируемо растут (т.е. это гиперпролиферативное заболевание). Опухоли включают лейкозы, лимфомы, миеломы, плазмацитомы и т.п.; и солидные опухоли. Примеры солидных опухолей, которые можно лечить согласно изобретению включают, но не ограничиваются перечисленными: саркомы и карциномы, такие как меланома, фибросаркома, миксосаркома, липосаркома, хондросаркома, остеогенная саркома, хордома, ангиосаркома, эндотелиосаркома, лимфангиосаркома, лимфангиоэндотелиосаркома, синовиома, мезотелиома, опухоль Юинга, лейомиосаркома, рабдомиосаркома, карцинома толстой кишки, рак поджелудочной железы, рак молочной железы, рак яичников, рак предстательной железы, плоскоклеточная карцинома, базальноклеточная карцинома, аденокарцинома, карцинома потовых желез, карцинома сальных желез, папиллярная карцинома, папиллярная аденокарцинома, цистаденокарцинома, медуллярная карцинома, бронхогенная карцинома, почечно-клеточная карцинома, гепатома, карцинома желчного протока, хориокарцинома, семинома, эмбриональная карцинома, опухоль Вильмса, рак шейки матки, опухоль яичка, карцинома легких, мелкоклеточная карцинома легких, карцинома мочевого пузыря, эпителиальная карцинома, глиома, астроцитома, медуллобластома, краниофарингиома, эпендимома, пинеалома, гемангиобластома, акустическая невринома, олигодендроглиома, менингиома, нейробластома, ретинобластома, карцинома желудка и карцинома кардиального отдела желудка.
В настоящем документе термин «CTLA4» относится к «цитотоксическому Т-лимфоцит-ассоциированному белку 4», который является одним из многих коингибиторных молекул, которые способны подавлять активацию Т-клеток путем ингибирующей костимуляции и передачи ингибирующих сигналов в Т-клетки. Аминокислотная последовательность CTLA4 доступна в NCBI под номерами доступа NP_033973.2 или NP_001268905.1. CTLA4 также известен под обозначениями Ctla-4, Cd152 или Ly-56. Номер доступа NCBI для последовательности CTLA4 - NC_000067.6, а идентификатор гена - 12477. Человеческий ген CTLA4 кодирует белок, состоящий из 233 аминокислот, принадлежащий к суперсемейству иммуноглобулинов. CTLA4 состоит из одного домена V-типа, окруженного с двух сторон двумя гидрофобными областями. CTLA4 также может изменять структуру иммунных синапсов, которые играют ключевую роль в пролиферации Т-клеток и дифференцировке CTLA4. Полиморфизм CTLA4 связан с предрасположенностью ко многим заболеваниям, включая диабет I типа, первичный билиарный цирроз и болезнь Грейвса.
Термин «Ил-12» в настоящем документе относится к «интерлейкину 12», который является цитокином с мощным противоопухолевым действием. Так, Ил-12 индуцирует ТН-1 тип иммунного ответа, который может обеспечить устойчивый противоопухолевый эффект. Было отмечено, что Ил-12 в условиях in vivo обладает анти-ангиогенной активностью, что может также вносить вклад в его противоопухолевое действие. Наконец, было отмечено, что Ил-12 стимулирует выработку высоких уровней интерферона гамма (IFN-γ), который обладает множественным иммунорегуляторным действием, включая способность стимулировать активацию цитотоксических Т-лимфоцитов (CTL), натуральных киллеров и макрофагов, а также индуцировать/усиливать экспрессию антигенов главного комплекса гистосовместимости (МНС) II класса. IFN-γ играет значимую роль в процессе индуцирования миграции Т-клеток в очаги опухолей. Повышение внутриопухолевых уровней IFN-γ коррелирует со снижением объема опухолевой массы.
Рецептор программируемой гибели клеток 1 (PD-1) представляет собой трансмембранный рецептор I типа массой 50-55 кДа, изначально выявленный методом вычитающей гибридизации линии Т-клеток мышей, подвергающейся апоптозу (Ishida et al., 1992, Embo J. 11:3887-95). Будучи членом семейства генов CD28, PD-1 экспрессируется на активированных Т-, В-клетках и клетках миелоидного ростка (Greenwald et al., 2005. Annu. Rev. Immunol. 23:515-48; Sharpe et al., 2007, Nat. Immunol. 8:239-45). Аминокислотная последовательность человеческого и мышиного PD-1 совпадают приблизительно на 60% с сохранением четырех потенциальных сайтов N-гликозилирования и остатков, которые определяют домен lg-V. PD-1 отрицательным образом модулирует Т-клеточную активацию, и эта ингибиторная функция связана с иммунорецепторным тирозиновым ингибирующим мотивом (ITIM) его цитоплазматического домена (Parry et al., 2005, Mol. Cell. Biol. 25:9543-53). Нарушение этой ингибирующей функции PD-1 может привести к аутоиммунным реакциям.
В настоящем документе термин «антитело» или «антиген-связывающий полипептид» относится к полипептиду или полипептидному комплексу, который специфически распознает и связывается с одним или более антигенами. Антитело может быть целым антителом и любым антигенсвязывающим фрагментом или его отдельной цепью. Таким образом, термин «антитело» включает любой белок или пептид, содержащий молекулу, которая включает по меньшей мере часть молекулы иммуноглобулина, обладающую биологической активностью связывания с антигеном. Примеры этого включают, но не ограничиваются этим, определяющую комплементарность область (CDR) тяжелой или легкой цепи или ее лиганд-связывающую часть, вариабельную область тяжелой или легкой цепи, константную область тяжелой или легкой цепи, каркасную (FR) область или любую ее часть, или по меньшей мере одну часть связывающего белка. Термин антитело также включает в себя полипептиды или полипептидные комплексы, которые при активации обладают способностью связываться с антигеном.
Под «терапевтически эффективным количеством» понимается то, что онколитический вирус и/или экзосому согласно настоящему изобретению вводят в количестве, которое достаточно для «лечения», как описано выше. Количество, которое будет терапевтически эффективным в лечении конкретного отдельного нарушения или состояния, будет зависеть от симптомов и тяжести заболевания, и оно может быть определено стандартными клиническими методами. Кроме того, для помощи в определении оптимальных диапазонов дозы могут необязательно применяться анализы in vivo или in vitro. Точная доза для применения в составе будет также зависеть от пути введения и тяжести заболевания или нарушения, и должна определяться в соответствии с суждением практикующего врача и обстоятельствами каждого пациента. Эффективные дозы могут быть экстраполированы по кривым «доза-ответ», полученным в тест-системах in vitro или на животных моделях.
миРНК, нацеленные на CTLA4
Термины «миРНК, нацеленные на CTLA4», «миРНК, нацеленная на CTLA4» и «нацеленная на CTLA4 миРНК», которые используются в настоящем документе взаимозаменяемо, относятся к малой некодирующей РНК (микроРНК или миРНК), выполненной с возможностью нацеливания на или специфического связывания с мРНК, кодирующей белок CTLA4, таким образом, чтобы нарушалась, снижалась или устранялась транскрипция, трансляция и, как следствие, экспрессия CTLA4. Как описано выше, миРНК не обязательно связывается с целевой мРНК со 100% специфичностью. Известно, что миРНК обладает затравочной последовательностью (2-8 нуклеотидов со стороны 5'-конца), которая определяет специфичность связывания с целевой мРНК, при этом оставшиеся нуклеотиды не обязательно точно комплементарны целевой мРНК. Таким образом, в одном варианте изобретения миРНК обладает затравочной последовательностью из любых нуклеотидных последовательностей SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 4. В некоторых вариантах реализации миРНК, нацеленная на CTLA4, блокирует экспрессию белка CTLA4 в клетке после ее доставки в опухолевую клетку.
Экзосомы, несущие миРНК, нацеленную на CTLA4
Экзосомы представляют собой малые везикулы относительно универсального размера, образующиеся из клеточных мембран. Например, экзосомы могут иметь диаметр от примерно 30 до примерно 100 нм. Они содержат несколько ключевых белков (например, CD9, CD63, CD81, CD82, аннексии, флотиллин и т.д.) и, кроме того, в них упаковывают белки, мРНК, длинные некодирующие РНК и миРНК. Экзосомы осуществляют транспорт веществ от клетки к клетке. При входе в клетки-реципиенты содержимое экзосомы высвобождается в цитоплазму.
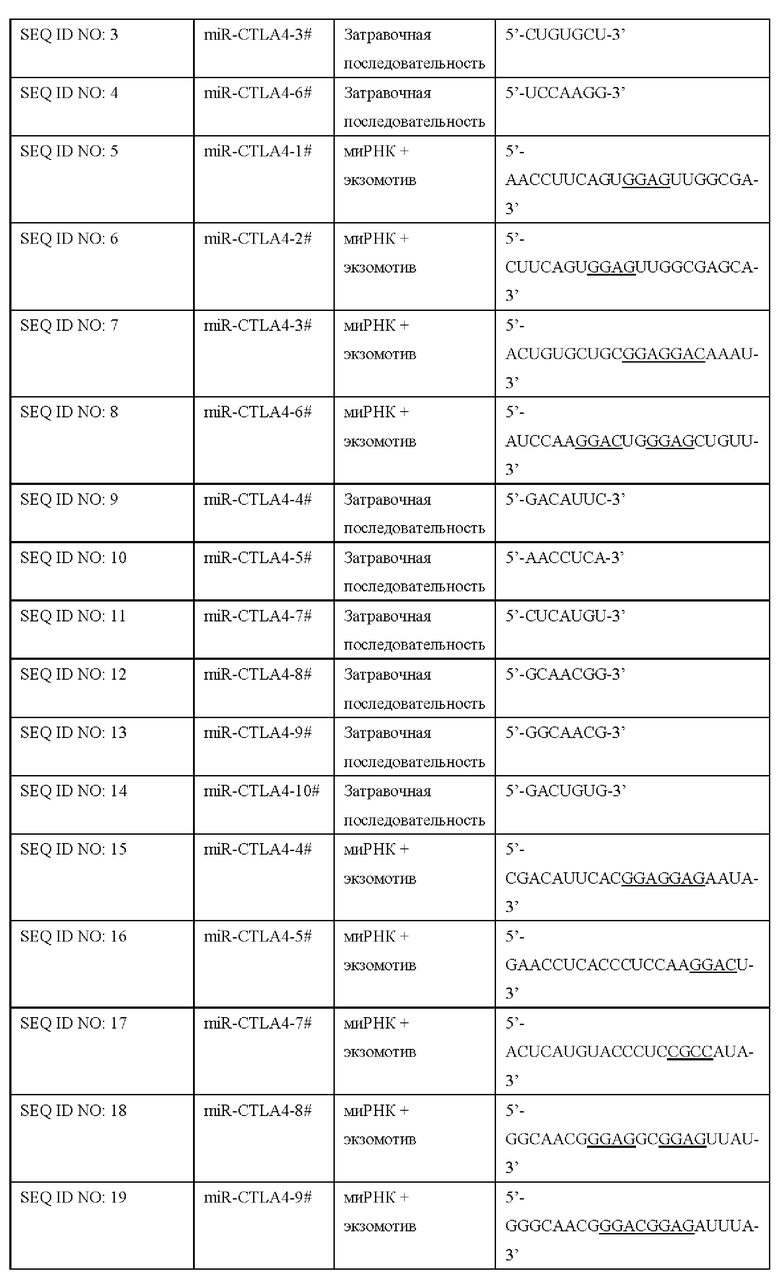
В некоторых вариантах реализации миРНК, нацеленная на CTLA4, доставляется в клетку с помощью экзосомы. Таким образом, в одном варианте изобретения предложена экзосома, несущая любые нацеленные на CTLA4 миРНК, как описано выше. В настоящем изобретении используется фрагмент нуклеотидной последовательности, называющийся здесь «экзомотивом», для способствования или стимуляции упаковки миРНК в экзосому. В одном варианте изобретения экзомотив выбран из любых последовательностей, определенных в таблице 1.

В некоторых вариантах реализации экзомотивы используются в комбинации. Например, два или более экзомотивов, определенных в таблице, объединяют с образованием двойного экзомотива. Мотивы могут быть объединяют линейно, путем связывания 5'-конца одного экзомова с 3'-концом другого экзомотива. В этом контексте, если первый нуклеотид 5'-конца одного экзомотива идентичен последнему нуклеотиду 3'-конца другого экзомотива, один из идентичных нуклеотидов может быть исключен. Например, «GGAG» (SEQ ID NO: 21) комбинирована с «GGAC» (SEQ ID NO: 22) с образованием двойного экзомотива «GGAGGAC» (SEQ ID NO: 48). Если первый нуклеотид 5'-конца одного экзомотива отличается от последнего нуклеотида 3'-конца другого экзомотива, два экзомотива могут быть соединены линкером или напрямую ковалентной связью. Например, «GGAC» (SEQ ID NO: 22) можно объединять с «GGAG» (SEQ ID NO: 21) линкером «TG» с образованием двойного экзомотива «GGACUGGGAG» (SEQ ID NO: 49), «GGAC» (SEQ ID NO: 22) можно также объединять с «GGAG» (SEQ ID NO: 21) ковалентной связью с образованием двойного экзомотива «GGACUGGGAG» (SEQ ID NO: 51). Настоящее изобретение также предполагает тройной или более экзомотив, например, экзомотив, содержащий три или более мотивов от SEQ ID NO: 21 по SEQ ID NO: 47. Таким образом, термин «экзомотив», использованный в настоящем документе, включает нуклеотидные последовательности, которые способны стимулировать или способствовать упаковке миРНК в экзосому, включая любой из отдельных экзомотивов от SEQ ID NO: 21 по SEQ ID NO: 47, а также любой двойной (например, любая из SEQ ID NO: 48-52), тройной или более кратные экзомотивы, полученные с помощью комбинации отдельных мотивов.
В настоящем изобретении экзомотив функционально связан с затравочной последовательностью миРНК. Термин «функционально связан» относится к функциональной связи между регуляторной последовательностью (например, экзомотив) и последовательностью нуклеиновой кислоты (например, затравочная последовательность миРНК), приводящей к стимулированию или способствованию упаковки миРНК в экзосому. Например, первая последовательность нуклеиновой кислоты функционально связана со второй последовательностью нуклеиновой кислоты, когда первая последовательность нуклеиновой кислоты находится в функциональной взаимосвязи со второй последовательностью нуклеиновой кислоты. Функционально связанные последовательности РНК могут граничить друг с другом или могут быть связанными с линкером.
В некоторых вариантах реализации экзомотив расположен ниже затравочной последовательности миРНК. В некоторых вариантах реализации экзомотив расположен выше затравочной последовательности миРНК. В некоторых вариантах реализации затравочная последовательность миРНК окружена с двух сторон экзомотивами. В одном варианте изобретения экзомотив функционально связан с затравочной последовательностью миРНК. В одном варианте изобретения экзомотив получают посредством мутации одного более нуклеотидных последовательностей миРНК, за исключением затравочной последовательности. В одном варианте изобретения миРНК, нацеленная на CTLA4, с экзомотивом содержит нуклеотидную последовательность SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8. В одном варианте изобретения миРНК, нацеленная на CTLA4, с экзомотивом представляет собой нуклеотидную последовательность SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8.
В некоторых вариантах реализации, в которых экзомотив расположен ниже затравочной последовательности миРНК, последний нуклеотид на 3'-конце затравочной поверхности и первый нуклеотид на 5'-конце экзомотива являются одним и тем же нуклеотидом, например, гуаниновым нуклеотидом «G». Например, SEQ ID NO: 6 показывает, что экзомотив и затравочная последовательность делят между собой гуаниновый нуклеотид «G». В некоторых вариантах реализации, в которых экзомотив расположен ниже затравочной последовательности миРНК, последние два нуклеотида на 3'-конце затравочной последовательности и первые два нуклеотида на 5'-конце экзомотива являются одними и теми же нуклеотидами, например, гуаниновыми нуклеотидами «GG». Например, SEQ ID NO: 8 показывает, что экзомотив и затравочная последовательность делят между собой два гуаниновых нуклеотида «GG».
В некоторых вариантах реализации экзомотив расположен ниже затравочной последовательности миРНК и связан с затравочной последовательностью миРНК линкером, например, «GC». Например, SEQ ID NO: 7 показывает, что экзомотив и затравочная последовательность связаны линкером «GC».
В дополнение к затравочной последовательности и экзомотиву миРНК также включает дополнительную последовательность нуклеиновой кислоты для улучшения (усиления) с целевой областью-мишенью мРНК. Эти дополнительные нуклеиновые кислоты обычно находятся ниже экзомотива с длиной в несколько нуклеотидов, например, от 1 до 10 нуклеотидов. Дополнительные последовательности нуклеиновой кислоты предпочтительно комплементарны соответствующему сегменту целевой мРНК, однако, как описано выше, комплементарность не обязательно должна быть 100%.
Способы переноса миРНК в экзосому доступны в уровне техники, такие как котрансфекция клетки с миРНК экспресссирующим вектором и плазмидой, кодирующей CTLA4, как описано в Примере. Выделение, идентификация и определение характеристик экзосомы технически выполнимо в уровне техники. Некоторые белки, например, CD9, CD63, CD81, CD82, аннексии, флотиллин и т.д., могут быть использованы в качестве маркера экзосом. Другие способы упаковки миРНК в экзосомы также могут быть применимы к настоящему изобретению.
Экзосома по настоящему изобретению содержит ингибирующее количество миРНК, нацеленной на CTLA4. Ингибирующее количество означает количество, достаточное для ингибирования экспрессии белка CTLA4 после того, как рассматриваемая миРНК была доставлена в опухолевую клетку.
В таблице ниже перечислены последовательности нуклеиновой кислоты миРНК, затравочных последовательностей и миРНК-мотивов, использованных в Примере изобретения.


Онколитический вирус простого герпеса (oHSV)
Онколитический вирус простого герпеса (oHSV), используемый в настоящем документе, относится к любому онколитическому вирусу простого герпеса 1 типа (ВПГ-1, HSV-1), известному в уровне техники, разработанному, пригодному для использования или эффективному для уничтожения опухолевой клетки. Кроме того, oHSV, используемый в настоящем изобретении, может также быть генетически сконструирован (модифицирован) таким образом, что один или более признаков встречающегося в природе oHSV удалены. В дополнение или альтернативным способом встречающийся в природе oHSV может быть генетически сконструирован для внедрения в геном вируса одного или более экзогенных фрагментов кодирующих последовательностей так, чтобы придать одну или более дополнительных функций вирусу, таких как иммунотерапевтические или иммуностимулирующие свойства.
Специалисту в данной области техники должно быть понятно, что точные начальные и конечные положения нуклеотидов, подлежащих делеции в соответствии с настоящим изобретением, зависят от штаммов и изомеров генома вируса ВПГ-1 и могут быть легко определены методами, известными в уровне техники. В некоторых вариантах реализации делеция становится причиной эксцизии нуклеотидов с 117005 по 132096 в геноме. В некоторых вариантах реализации oHSV выбран из штамма 17 (номер доступа в GenBank NC 001806.2), штамма KOS 1.1 (номер доступа в GenBank No. КТ899744) или штамма F (номер доступа в GenBank No.GU734771.1) ВПГ-1. В некоторых вариантах реализации oHSV представлен штаммом F ВПГ-1.
В некоторых вариантах реализации oHSV представлен генетически сконструированным штаммом F ВПГ-1, экспрессирующим иммуностимулирующий агент, который выбран из ГМ-КСФ, Ил-2, Ил-5, Ил-12, Ил-15, Ил-24 и Ил-27. В некоторых вариантах реализации oHSV представляет собой генетически сконструированный штамм F ВПГ-1, экспрессирующий только Ил-12. В некоторых вариантах реализации oHSV представляет собой генетически сконструированный штамм F ВПГ-1, экспрессирующий как Ил-12, так и анти-PD-1 антитело.
Способы и средства терапии
В одном из аспектов изобретения предложен способ лечения опухоли у субъекта, включающий введение субъекту, нуждающемуся в этом, терапевтически эффективного количества экзосомы, несущей миРНК, нацеленную на CTLA-4, и терапевтически эффективное количество oHSV, экспрессирующего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело.
В одном из аспектов изобретения предложен способ повышения эффективности терапии oHSV у субъекта, включающему введение субъекту, нуждающемуся в этом, терапевтически эффективного количества экзосомы, несущей миРНК, нацеленную на CTLA-4, изобретения в дополнение к терапии oHSV. В некоторых вариантах реализации oHSV экспрессирует иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело. В некоторых вариантах реализации oHSV экспрессирует только Ил-12. В некоторых вариантах реализации oHSV экспрессирует Ил-12 и анти-PD-1 антитело.
В некоторых вариантах в способах изобретения введение экзосом, несущих миРНК, нацеленную на ингибитор CTLA-4, и oHSV, экспрессирующего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело, выполняют путем введения субъекту фармацевтической композиции, содержащей терапевтически эффективное количество экзосомы, несущей миРНК, нацеленную на CTLA-4, и терапевтически эффективное количество oHSV, экспрессирущего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело, и фармацевтически приемлемый носитель.
В некоторых вариантах в способах согласно изобретению введение экзосом, несущих миРНК, нацеленную на CTLA-4, и oHSV, экспрессирующего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело, выполняют путем введения субъекту экзосом, несущих миРНК, нацеленную на CTLA-4, и oHSV, экспрессирущего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело, по отдельности. В некоторых вариантах изобретения экзосомы, несущие миРНК, нацеленную на CTLA-4, вводят перед, одновременно или после введения oHSV, экспрессирующего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело. В таких случаях предполагается, что субъекту можно вводить оба средства с интервалом примерно 12-72 часа между введениями. Однако в некоторых ситуациях может быть желательным значительно увеличить срок лечения, когда между соответствующими введениями проходит от нескольких дней (2, 3, 4, 5, 6 или 7) до нескольких недель (1, 2, 3, 4, 5, 6, 7 или 8).
В некоторых вариантах изобретения экзосомы, несущие миРНК, нацеленную на CTLA-4, вводят одновременно с введением oHSV, экспрессирущего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело. В некоторых вариантах изобретения экзосомы, несущие миРНК, нацеленную на CTLA-4, вводят в форме фармацевтической композиции, содержащей терапевтически эффективное количество экзосом, несущих миРНК, нацеленную на CTLA-4, и фармацевтически приемлемый носитель, a oHSV, экспрессирущий иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело, вводят в форме фармацевтической композиции, содержащей терапевтически эффективное количество oHSV, экспрессирующего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело, и фармацевтически приемлемый носитель. В таких вариантах изобретения фармацевтическая композиция, содержащая терапевтически эффективное количество экзосом, несущих миРНК, нацеленную на CTLA-4, и фармацевтически приемлемый носитель, а также фармацевтическая композиция, содержащая терапевтически эффективное количество oHSV, экспрессирующего иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело, и фармацевтически приемлемый носитель, могут быть упакованы в один набор.
В отдельных вариантах осуществления изобретения любую фармацевтическую композицию вводят парентерально или непарентерально, т.е. интратуморально, внутривенно, внутримышечно, чрескожно или внутрикожно. В некоторых вариантах реализации любая фармацевтическая композиция предпочтительно вводится интратуморально.
В некоторых вариантах осуществления изобретения способ лечения опухоли направлен на повышение противоопухолевой эффективности терапии oHSV, например, в плане ингибирования опухолевого роста и/или уменьшения объема опухолей. Соответственно, в некоторых вариантах реализации предложен способ лечения опухоли, включающий введение субъекту, нуждающемуся в этом, терапевтически эффективного количества экзосомы в комбинации с терапевтически эффективным количеством oHSV, как описано выше. В отдельных вариантах осуществления изобретения способ лечения опухоли предотвращает начало, прогрессирование и/или рецидив симптомов, связанных с опухолью. Таким образом, в некоторых вариантах реализации способ профилактики симптомов, связанных с опухолью, у субъекта, включает введение терапевтически эффективного количества экзосомы и терапевтически эффективного количества oHSV, как описано выше субъекту, нуждающемуся в этом.
В некоторых вариантах реализации oHSV представлен генетически сконструированным штаммом F ВПГ-1, экспрессирующим иммуностимулирующий агент, который выбран из ГМ-КСФ, Ил-2, Ил-5, Ил-12, Ил-15, Ил-24 и Ил-27. В некоторых вариантах изобретения oHSV представляет собой генетически сконструированный штамм F ВПГ-1, экспрессирующий только Ил-12. В некоторых вариантах изобретения oHSV представляет собой генетически сконструированный штамм F ВПГ-1, экспрессирующий как Ил-12, так и анти-PD-1 антитело.
Способы согласно изобретению предполагают лечение различных опухолей, в частности, солидных опухолей. Примеры солидных опухолей, которые можно лечить согласно изобретению включают, но не ограничиваются перечисленными, саркомы и карциномы, такие как меланома, фибросаркома, миосаркома, липосаркома, хондросаркома, остеогенная саркома, хордома, ангиосаркома, эндотелиосаркома, лимфангиосаркома, лимфангиоэндотелиосаркома, синовиома, мезотелиома, опухоль Юинга, лейомиосаркома, рабдомиосаркома, карцинома толстой кишки, рак поджелудочной железы, рак молочной железы, рак яичников, рак предстательной железы, плоскоклеточная карцинома, базальноклеточная карцинома, аденокарцинома, карцинома потовых желез, карцинома сальных желез, папиллярная карцинома, папиллярная аденокарцинома, цистаденокарцинома, медуллярная карцинома, бронхогенная карцинома, почечно-клеточная карцинома, гепатома, карцинома желчного протока, хориокарцинома, семинома, эмбриональная карцинома, опухоль Вильмса, рак шейки матки, опухоль яичка, карцинома легких, мелкоклеточная карцинома легких, карцинома мочевого пузыря, эпителиальная карцинома, глиома, астроцитома, медуллобластома, краниофарингиома, эпендимома, пинеалома, гемангиобластома, акустическая невринома, олигодендроглиома, менингиома, нейробластома, ретинобластома, карцинома желудка и карцинома кардиального отдела желудка.
Фармацевтические композиции и наборы
В одном из аспектов изобретения предложена фармацевтическая композиция, содержащая терапевтически эффективное количество экзосомы, терапевтически эффективное количество oHSV, как описано выше, и фармацевтически приемлемый носитель. Фармацевтическую композицию применяют для профилактики и лечения опухоли у субъекта. Фармацевтическая композиция может быть приготовлена в подходящем фармацевтически приемлемом носителе или вспомогательном веществе.
В другом аспекте изобретения предложена первая фармацевтическая композиция, содержащая терапевтически эффективное количество экзосомы, как описано выше, и фармацевтически приемлемый носитель. В дополнение предложена вторая фармацевтическая композиция, содержащая терапевтически эффективное количество oHSV, как описано выше, и фармацевтически приемлемый носитель. В таком аспекте предложен набор, содержащий первую фармацевтическую композицию и вторую фармацевтическую композицию в одной упаковке. Набор может дополнительно включать спецификацию по применению, к которой может обращаться врач во время клинического использования.
В некоторых вариантах реализации oHSV представлен генетически сконструированным штаммом F ВПГ-1, экспрессирующий иммуностимулирующий агент, который выбран из ГМ-КСФ, Ил-2, Ил-5, Ил-12, Ил-15, Ил-24 и Ил-27. В некоторых вариантах изобретения oHSV представляет собой генетически сконструированный штамм F ВПГ-1, экспрессирующий только Ил-12. В некоторых вариантах изобретения oHSV представляет собой генетически сконструированный штамм F ВПГ-1, экспрессирующий как Ил-12, так и анти-PD-1 антитело.
В обычных условиях хранения и использования такие препараты/композиции содержат консервант для предотвращения роста микроорганизмов. Фармацевтические формы, подходящие для инъекций, включают стерильные водные растворы или дисперсии, и стерильные порошки для экстемпорального приготовления стерильных растворов или дисперсий для инъекций. Во всех случаях форма должна быть стерильной и достаточно жидкой для легкого введения посредством шприца. Она должна быть стабильной при изготовлении и хранении, и должна быть защищена от загрязнения микроорганизмами, такими как бактерии и грибки.
Носитель может представлять собой растворитель или дисперсионную среду, включающие, например, воду, этанол, многоатомный спирт (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль, и т.п.), их подходящие смеси и/или растительные масла. Подходящую текучесть можно поддерживать, например, используя покрытие, такое как лецитин, поддерживая требуемый размер частиц в случае дисперсии и используя поверхностно-активные вещества. Действие микроорганизмов можно предотвратить с помощью различных антибактериальных и противогрибковых агентов, например, парабенов, хлорбутанола, фенола, сорбиновой кислоты, тимеросала и т.п. Во многих случаях будет предпочтительно включать изотонические вещества, например, сахара, хлорид натрия или фосфатно-солевой буфер. Пролонгированную абсорбцию вводимых с помощью инъекции композиций можно обеспечить, используя в композициях агенты, задерживающие абсорбцию, например, моностеарат алюминия и желатин.
Для парентерального введения в водном растворе, например, раствор при необходимости должен содержать буфер, и жидкому растворителю сначала необходимо придать изотоничность с помощью достаточного количества соли или глюкозы. Эти конкретные водные растворы особенно подходят для внутривенного, внутримышечного, подкожного, интратуморального и внутрибрюшинного введения. В этом отношении, специалистам в данной области известна стерильная водная среда, которую можно будет использовать для настоящего изобретения. Например, одну дозу можно растворить в 1 мл изотонического раствора NaCl и либо добавить к 1000 мл гиподермоклизисной жидкости, либо ввести с помощью инъекции в предполагаемое место инфузии (см., например, «Remington's Pharmaceutical Sciences», 15-е издание, страницы 1035-1038 и 1570-1580). Некоторые изменения дозировки будут неизбежны в зависимости от состояния субъекта, которого лечат. Лицо, отвечающее за введение препарата, будет в любом случае определять соответствующую дозу для конкретного субъекта. Более того, для введения людям, препараты должны соответствовать стандартам стерильности, пирогенности, общей безопасности и чистоты согласно требованиям FDA (Управления США по надзору за качеством пищевых продуктов и лекарственных средств).
Стерильные растворы для инъекций приготавливают, включая активные соединения в требуемом количестве в соответствующий растворитель совместно с рядом других ингредиентов, перечисленных выше, в случае необходимости, с последующей стерилизацией фильтрованием. Обычно дисперсии готовят, включая различные стерильные активные ингредиенты в стерильный носитель, который содержит базовую дисперсионную среду и необходимые другие ингредиенты из перечисленных выше. В случае стерильных порошков для приготовления стерильных растворов для инъекций предпочтительными способами приготовления являются вакуумная сушка и лиофилизация, дающие порошок действующего ингредиента плюс любой дополнительный желаемый ингредиент, из их раствора, ранее стерилизованного фильтрованием.
Композиции согласно настоящему изобретению можно составить в нейтральной форме или в виде соли. Фармацевтически приемлемые соли включают кислотно-аддитивные соли (образуемые свободными аминогруппами белков), которые образуются с неорганическими кислотами, такими как, например, хлористоводородная или фосфорная кислоты, или органическими кислотами, такими как уксусная, щавелевая, винная, миндальная и т.п. Соли, образуемые со свободными карбоксильными группами, также можно получить с неорганическими основаниями, такими как, например, гидроксиды натрия, калия, аммония, кальция или железа, и такими органическими основаниями, как изопропиламин, триметиламин, гистидин, прокаин и т.п. После составления растворы будут вводить способом, совместимым с дозированной формой, и в количестве, которое является терапевтически эффективным. Составы легко вводить в ряде дозированных форм, таких как растворы для инъекций, капсулы для высвобождения лекарственных препаратов и т.п.
В настоящем документе термин «носитель» включает любой и все растворители, дисперсионные среды, несущие среды, разбавители, покрытия, антибактериальные и противогрибковые агенты, изотонические агенты и агенты, замедляющие абсорбцию, буферы, растворы-носители, суспензии, коллоиды и т.п. Применения таких сред и агентов для фармацевтически активных веществ хорошо известно в уровне техники. За исключением случаев, когда любая обычная среда или агент являются несовместимыми с активным ингредиентом, предусмотрено их использование в терапевтических композициях. Также в композиции можно включать вспомогательные активные ингредиенты.
Выражение «фармацевтически приемлемый» относится к молекулам и композициям, которые не вызывают аллергической или схожей неблагоприятной реакции при введении людям. Приготовление водной композиции, которая содержит белок в качестве активного ингредиента, хорошо известно в уровне техники. Обычно такие композиции готовят в виде инъекционных препаратов либо в виде жидких растворов, либо в виде суспензий; также могут готовиться твердые формы, подходящие для растворения в жидкости или суспензии перед инъекцией.
Примеры
Мы описали разработку вспомогательной терапии, включающей экзосомы, сконструированные для переноса и высвобождения в опухолевые клетки миРНК, выполненной с возможностью специфического нацеливания на мРНК, кодирующие контрольную точку CTLA-4.
Экзосомы представляют собой внеклеточные везикулы, определенные в целях терапевтического применения по размеру и содержанию белка. Они упаковывают РНК и белки в клетках, в которых они продуцируются, и доставляют груз в клетки, на которые воздействуют. В исследованиях, описанных в этом отчете, желаемым содержимым экзосомы являлась миРНК.
миРНК представляют собой эффективные инструменты, которые в принципе могут использоваться для контроля репликации отдельных кодирующих белок РНК. Задачи заключались в разработке миРНК, которые могут блокировать репликацию цитотоксического Т-лимфоцит-ассоциированного белка 4, и которые могут быть доставлены в инфицированные клетки с помощью экзосом. Были разработаны 10 миРНК, нацеленных на мРНК, кодирующую CTLA4. Из этих 10 миРНК, miR-CTLA4-1#, miR-CTLA4-2#, miR-CTLA4-3# и miR-CTLA4-6# при трансфекции в восприимчивые клетки эффективно блокировали накопление CTLA4. Для того чтобы способствовать упаковке миРНК в экзосомы мы вводили в последовательность miR-CTLA4-3# мотив, отвечающий за упаковку в экзосому. Как и в нашем предшествующем исследовании, miR-CTLA4-3# может быть упакована в экзосомы и успешно доставлена экзосомами в восприимчивые клетки, в которых она остается стабильной по меньшей мере в течение 72 часов. Более того, miR-CTLA4-3#, доставленная в опухоли экзосомами, эффективно снижала экспрессию CTLA4.
Встраивание РНК в экзосомы зависит от последовательности и способствует этому действие hnRNPA2B1, компонента экзосом. hnRNPA2B1 сортирует в экзосомы РНК, содержащие один из двух известных отвечающих за упаковку в экзосомы мотивов (ЭКЗО-мотивы). Ключевая функция hnRNPA2B1 заключается в регуляции транспорта мРНК к аксонам в нервных клетках, который опосредуется связыванием 21-нуклеотидной последовательности РНК, называемой транспортная последовательность РНК (RTS). Эти последовательности содержат оба ЭКЗО-мотива.
Было установлено, что опухоль у мышей относительно устойчива к онколитическому действию мышиных T1, Т2 и Т3 серий oHSV. Т1-серия oHSV представляет собой штамм F ВПГ-1, который не экспрессирует иммунорегуляторный агент (в дальнейшем также обозначаемый как «T1012G»). Т2-серия oHSV представляет собой штамм F ВПГ-1, который экспрессирует только Ил-12 (в дальнейшем также упоминается как «Т2850»). Т3-серия oHSV представляет собой штамм F ВПГ-1, который одновременно экспрессирует Ил-12 и анти-PD-1 антитела (в дальнейшем также упоминается как «Т3855»).
Примеры показывают, что противоопухолевая эффективность Т2850 и особенно Т3855 может быть усилена, и объем опухолей может быть снижен посредством доставки в опухоли композиции, содержащей Т3855 (или Т2850) и экзосомы, несущие миРНК, предназначенную для нацеливания на мРНК, кодирующую CTLA-4.
Материалы и методы
Модель с использованием сингенных мышей. Для модели опухоли MFC использовали сингенных мышей линии Balb/c.
Плазмиды, экспрессирующие miR-CTLA-4. Целевые последовательности миРНК против CTLA4 мышей были разработаны с использованием программного обеспечения Life Technologies' BLOCK-iT™ RNAi Designer и синтезированы компанией Ige Biotechnology (Гуанчжоу, Китай). Синтезированные фрагменты миРНК расщепляли с помощью рестриктаз BamHI и XhoI и клонировали в соответствующих сайтах контрольной плазмиды pcDNA6.2-GW/EmGFP-miR-neg (mvitrogen).
Последовательности миРНК представлены ниже:
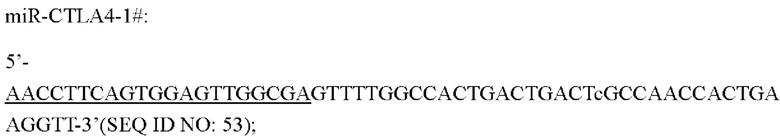



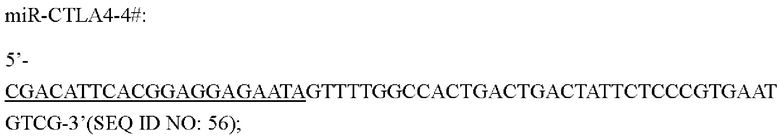


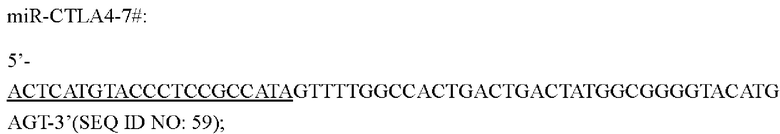




Подчеркивание указывает на зрелую последовательность миРНК.
Плазмиду, экспрессирующую несущий меченный гистидином CTLA4 мыши (mCTLA4-his), закупали в компании YouBio Biotechnology (Чанша, Китай).
Клеточные линии Клетки НЕр-2 получали от организации «Американская коллекция типовых культур» и согласно обычной практике культивировали в минимальной эссенциальной среде Игла, модифицированной по способу Дульбекко (Life Technologies) с добавлением 5% (об/об) фетальной бычьей сыворотки (FBS). Клетки MFC (карцинома преджелудка мышей) были любезно предоставлены компанией JOINN Laboratories, Inc. (Пекин, Китай). В16 (мышиная меланома) были любезно предоставлены Шеньчжэньским международным институтом биомедицинских исследований (Шеньчжэнь, Китай).
Антитела. Антитела, использованные в этом исследовании, представляли собой антитела к гистидиновой метке (anti-His-tag) (каталожный номер: 66005-1-Ig, Proteintech Group) и к глицеральдегид-3-фосфатдегидрогеназе (anti-GAPDH) (каталожный номер: #2118, Cell Signaling Technology).
Выделение экзосомы. Клетки НЕр-2 (5×10б) трансфицировали с использованием 10 мкг плазмид, экспрессирующих miR-CTLA-4. После 4 часов инкубации клетки три раза промывали раствором PBS для исключения потенциального загрязнения экзосомы в сыворотке, и клетки культивировали в бессывороточной среде в течение следующих 48 часов. Надосадочную жидкость собирали, смешивали с рекомендованной дозой реагента набора Total Exosome Isolation kit (каталожный номер компании Thermo Fisher: 4478359), хранили на протяжении ночного периода при температуре 4°С и затем центрифугировали в течение 1 часа. Осажденные центрифугированием экзосомы затем ре суспендировали в 200 мл PBS или лизировали в буфере для радиоиммунопреципитации (RIPA), и затем проводили количественную оценку с помощью метода с бицинхониновой кислотой (ВСА), используя набор Enhanced ВСА Protein Assay Kit (Beyotime Biotechnology, Китай) согласно инструкциям производителя. Содержание белка в экзосоме определяли методом калибровки по стандартной кривой, которую получили построением графика поглощения на волне 562 нм по сравнению со стандартной концентрацией бычьего сывороточного альбумина.
Анализы размера экзосомы и количественное определение Распределение по размеру экзосом анализировали с помощью системы qNano (Izon, Крайстчерч, Новая Зеландия). Технологию Izon's qNano (www.izon.com) использовали для определения внеклеточных везикул, проходящих через нанопору путем одномолекулярного электрофореза. На практике это позволяет получать точные размеры частиц везикул при размерах экзосом от 75 до 150 мн без усреднения размеров частиц. Очищенные экзосомы разбавили в соотношении 1:10 в PBS с 0,05% полисорбат-20, энергично встряхнули и измерили, используя апертуру нанопоры NP150 (А45540) согласно инструкциям производителя. Обработку данных и анализ выполняли с помощью программного обеспечения Izon Control Suite версии 3.3 (Izon Science).
Анализ иммуноблот.Определение CTLA-4, несущих меченный гистидин, GAPDH и участвующих в образовании экзосомы белков с помощью анализа иммуноблот.Клетки собирали и лизировали с помощью лизирующего буфера RIPA (Beyotime) с добавлением 1 ммоль ингибитора протеазы фенилметилсульфонилфторида (PMSF) (Beyotime) и ингибитора фосфатазы (Beyotime). Лизаты клеток денатурировали нагреванием и отделяли методом электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE), переносили на поливинилидендифторидные мембраны (Millipore). Белки определяли методом инкубации с соответствующим первичным антителом, затем вторичным антителом, конъюгированным с пероксидазой хрена (Pierce), и ЭХЛ-реагентом (Pierce) и снимали на пленку или делали изображения с помощью системы ChemiDoc Touch Imaging System (Bio-Rad), и обрабатывали с помощью программного обеспечения ImageLab. Плотности соответствующих слоев определяли количественно с помощью программного обеспечения ImageJ.
Конструкция oHSV. Конструкция иллюстративного oHSV (такого как Т2850 и Т3855) включает рекомбинантный онколитический вирус простого герпеса 1 типа (ВПГ-1), содержащий (а) модифицированный геном ВПГ-1, в котором модификация содержит делецию между промотором гена U,56 и промотором гена Us1 генома ВПГ-1 дикого типа таким образом, что (i) одна копия всех сдвоенных генов отсутствует и (ii) последовательности, требующиеся для экспрессии всех имеющихся открытых рамок считывания (ORF) в вирусной ДНК после делеции, интактны: и (b) гетерологичные последовательности нуклеиновой кислоты, кодирующие иммуностимулирующий и/или иммунотерапевтический агент, причем геторологичная последовательность нуклеиновой кислоты стабильно встроена в по меньшей мере удаленную область модифицированного генома ВПГ-1. При встраивании только одной гетерологичной последовательности нуклеиновой кислоты, кодирующей иммуностимулирующий или иммунотерапевтический агент, гетерологичная последовательность нуклеиновой кислоты предпочтительно инкорпорирована в удаленную область генома. При инкорпорации более одной гетерологичных последовательностей нуклеиновой кислоты, кодирующих иммуностимулирующие и/или иммунотерапевтические агенты, первые гетерологичные последовательности нуклеиновой кислоты предпочтительно встроены в удаленную область генома. Вторая или последующие гетерологичные последовательности нуклеиновой кислоты могут быть встроены в L-компонент генома.
Более подробное описание конструкции и свойств онколитического вируса простого герпеса (oHSV) доступно в документе WO 2017/181420.
Результаты
Конструирование и получение экзосом, содержащих miR-CTLA-4 (miR-CTLA-4 exo)
Задача первой серии экспериментов заключалась в конструировании и получении экзосом, содержащих миРНК, нацеленную на CTLA4. Для этого мы сначала сконструировали 10 миРНК, обозначенных как miR-CTLA4-l#, miR-CTLA4-2#, miR-CTLA4-3#, miR-CTLA4-4#, miR-CTLA4-5#, miR-CTLA4-6#, miR-CTLA4-7#, miR-CTLA4-8#, miR-CTLA4-9# и miR-CTLA4-10#. Последовательность каждой миРНК показана на фигуре 1, включающим лежащие ниже затравочной последовательности миРНК дополнительные последовательности, являющиеся связанные с упаковкой экзосомы мотивы (экзомотивы). Как показано на фигуре 1А, миРНК клонировали ниже открытой рамки считывания, кодирующей EGFP, в миРНК экспрессирующий вектор, называемый «контрольная плазмида pcDNA6.2-GW/EmGFP-miR-neg», как описано в разделе «Материалы и методы».
Затем, для анализа миРНК клетки НЕр-2 котрансфицировали с миРНК экспрессирующими векторами (miRmCTLA4-l#, miRmCTLA4-2#, miRmCTLA4-3#, miRmCTLA4-4#, miRmCTLA4-5#, miRmCTLA4-6#, miRmCTLA4-7#, miRmCTLA4-8#, miRmCTLA4-9#, miRmCTLA4-10#.), описанными выше, и плазмидой, кодирующей меченный гистидином на С-конце CTLA4 (mCTLA4-His). Как показано на фигуре 1 В, из 10 конструкций miR-CTLA4-3# была наиболее эффективна в подавлении накопления CTLA4. Результаты показывают, что накопление CTLA4 подавляется miR-CTLA4-3# с более высокой эффективностью. miR-CTLA4-l#, miR-CTLA4-2#, miR-CTLA4-4#, miR-CTLA4-5#, miR-CTLA4-6# и miR-CTLA4-7# продемонстрировали умеренный эффект, при этом нецелевые (NT) плазмиды miR-CTLA4-8#, miR-CTLA4-9# и miR-CTLA4-10# не оказывали влияния на накопление CTLA4 (фигура 1В). Таким образом, для дальнейших исследований была выбрана miR-CTLA4-3#.
На следующем этапе мы сконструировали экзосомы, кодирующие выбранную miR-CTLA-4. Клетки НЕр-2, высеянные в колбу Т150, трансфицировали с 10 мкг плазмиды, кодирующей miR-CTLA-4-3#, или плазмиды, экспрессирующей нецелевую миРНК (NT). Через 48 часов внеклеточную среду собирали, а экзосомы очищали, как описано в разделе «Материалы и методы».
Характеристика экзосомы, несущей miR-CTLA-4.
Было проведено несколько экспериментов для характеризации экзосомы, несущей miR-CTLA-4. Сначала равные количества клеток, в которых образовались экзосомы, и равные количества экзосом растворили, подвергли электрофорезу в денатурирующем геле, проанализировали с помощью антител к CD9, флотилину-1 и калнексину. Как и ожидалось, результат (фигура 2А) показывает, что экзосомы содержат CD9 и флотилин-1, но не калнексин.
Затем экзосомы, очищенные от клеток НЕр-2, трансфицированных с 10 мкг плазмиды, кодирующей miR-CTLA, или плазмиды, экспрессирующей нецелевую миРНК (miR-NT), измеряли в отношении размера с помощью анализа траекторий движения наночастиц с использованием технологии Izon's qNano. Результат (фигура 2В) показывает, что диаметр экзосом, полученных в трансфицированных клетках, в среднем составляет 100-200 нм.
Одновременное введение экзосом, несущих miR-CTLA-4, и oHSV в имплантированные опухоли MFC усиливают онколитическую активность Т3, но не Т1 или Т2 oHSVs.
На первом этапе этой серии экспериментов реплицируемые культуры НЕр-2 трансфицировали с плазмидой miR-CTLA4-3#, и клетки культивировали в течение 48 часов. Затем полученную в НЕр-2 экзосому (miR-CTLA-4 ехо) очищали, как описано в разделе «Материалы и методы».
На втором этапе конструировали oHSV T1012G, Т2850 и Т3855, как описано в разделе «Материалы и методы». Затем клетки карциномы преджелудка мышей (MFC) вводили мышам C57BL/6J (8 групп по 8 мышей) подкожно с помощью инъекции в правый бок для образования опухоли. Когда опухоли достигли в среднем 80 мм3, в них интратуморально однократно с помощью инъекции ввели 1×107 БОЕ T1012G (панель В), Т2850 (панель С) или Т3855 (панель D) изолированно или в комбинации с 10 Пг экзосом miR-CTLA-4.
На заключительном этапе каждые 3 или 4 дня до 26 дня после инъекции измеряли объемы опухоли. Результат показывает, что объем опухоли в каждой группе постепенно увеличивался после инъекции. Фигура 3А показывает, что объем опухоли у мыши, получившей инъекцию miRNA-CTLA4 ехо, увеличивался почти с такой же скоростью, что и в контрольной группе, и на 26 день после инъекции объем опухоли у мыши, получившей инъекцию miRNA-CTLA4 ехо, был больше, чем в группе контроля. Фигура 3В показывает, что объем опухоли в контрольной группе, группах T1012G и T1012G+miRNA-CTLA4 ехо постепенно увеличивался после инъекции. Через 26 дней после инъекции объем опухоли у мыши, получившей инъекцию T1012G + miRNA-CTLA4 ехо, был меньше, чем в контрольной группе и группе T1012G. На фигуре 3С объем опухоли в группах Т2850 и T2850 + miRNA-CTLA4 ехо увеличивался медленнее, чем в контрольной группе. Через 26 дней после инъекции объем опухоли в группах Т2850 и T2850 + miPvNA-CTLA4 ехо был меньше, чем в контрольной группе. И объем опухоли в группе T2850 + miRNA-CTLA4 ехо значимо не отличался от объема опухоли в группе применения только Т2850. На фигуре 3D объем опухоли в группе T3855 + miRNA-CTLA4 ехо увеличивался медленнее всего, за ней следовала группа Т3855 и, наконец, контрольная группа. Через 26 дней после инъекции объем опухоли в контрольной группе был наибольшим, за ней по объему следовала группа Т3855 и наименьший объем опухоли был в группе T3855 + miRNA-CTLA4 ехо.
Результаты этой серии экспериментов показывают, что Т2850 и Т3855 могут эффективно ингибировать рост опухолей, и одновременное интратуморальное введение Т3855 и miRNA-CTLA4 ехо усиливает противоопухолевую эффективность Т3855 и ингибирует рост опухолей.
Результаты показывают, что miR-CTLA4-3# нацеливается на CTLA-4 и подавляет экспрессию CTLA-4. Мы также показали, что miR-CTLA4-3# упакована в экзосомы и очищенные экзосомы содержали CD9, флотилии-1, но не содержали калнексина. Экзосомы, полученные с помощью клеток Нер-2, трансфицированных с плазмидой miR-CTLA4-3# или нецелевой миРНК (NT), в среднем составляют 100-200 нм в диаметре. Представленные в настоящем документе результаты также показывают, что oHSV, экспрессирующий только Ил-12 или как Ил-12, так и анти-PD-1 антитело, может эффективно ингибировать рост опухолей. В заключение, мы показали, что одновременное интратуморальное введение экзосомы, несущей миРНК, нацеленную на CTLA-4, и oHSV, экспрессирующий как Ил-12, так и анти-PD-1 антитело, усиливает противоопухолевую эффективность oHSV и ингибирует рост опухолей.
Следует понимать, что, хотя настоящее изобретение было конкретно раскрыто посредством предпочтительных вариантов осуществления и необязательных признаков, специалисты в данной области техники могут прибегнуть к модификации, улучшению и изменению описаний, воплощенных в нем, и что такие модификации, усовершенствования и изменения считаются входящими в объем настоящего изобретения. Материалы, способы и примеры, представленные здесь, представляют предпочтительные варианты изобретения, являются иллюстративными и не предназначены для ограничения объема изобретения.
Все публикации, заявки на патенты, патенты и другие источники, упомянутые здесь, прямо включены в качестве ссылки во всей их полноте, в той же степени, как если бы каждая из них была включена в качестве ссылки по отдельности. В случае конфликта настоящая спецификация, включая определения, будет иметь преимущественную силу. Раскрытия, иллюстративно описанные в настоящем документе, могут надлежащим образом применяться на практике при отсутствии какого-либо элемента или элементов, ограничений или ограничений, конкретно не раскрытых в настоящем документе. Таким образом, например, термины «содержащий», «включающий», «вмещающий» и т.д. следует понимать расширительно и без ограничений. Кроме того, термины и выражения, используемые в данном документе, использованы в качестве терминов описания, а не ограничения, и при использовании таких терминов и выражений нет намерения исключить любые эквиваленты показанных и описанных признаков или их частей, но признано, что возможны различные модификации в пределах объема заявленного изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> IMMVIRA CO., LIMITED
<120> PHARMACEUTICAL COMPOSITIONS, KITS AND METHODS FOR TREATING TUMORS
<130> 191549-21D-RUP
<160> 62
<170> PatentIn version 3.5
<210> 1
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-1# seed Sequence
<400> 1
accuuca 7
<210> 2
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-2# seed Sequence
<400> 2
uucagug 7
<210> 3
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-3# seed Sequence
<400> 3
cugugcu 7
<210> 4
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-6# seed Sequence
<400> 4
uccaagg 7
<210> 5
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-1# + exo-motif
<400> 5
aaccuucagu ggaguuggcg a 21
<210> 6
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-2# + exo-motif
<400> 6
cuucagugga guuggcgagc a 21
<210> 7
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-3# + exo-motif
<400> 7
acugugcugc ggaggacaaa u 21
<210> 8
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-6# + exo-motif
<400> 8
auccaaggac ugggagcugu u 21
<210> 9
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-4# seed Sequence
<400> 9
gacauuc 7
<210> 10
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-5# seed Sequence
<400> 10
aaccuca 7
<210> 11
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-7# seed Sequence
<400> 11
cucaugu 7
<210> 12
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-8# seed Sequence
<400> 12
gcaacgg 7
<210> 13
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-9# seed Sequence
<400> 13
ggcaacg 7
<210> 14
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-10# seed Sequence
<400> 14
gacugug 7
<210> 15
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-4# + exo-motif
<400> 15
cgacauucac ggaggagaau a 21
<210> 16
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-5# + exo-motif
<400> 16
gaaccucacc cuccaaggac u 21
<210> 17
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-7# + exo-motif
<400> 17
acucauguac ccuccgccau a 21
<210> 18
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-8# + exo-motif
<400> 18
ggcaacggga ggcggaguua u 21
<210> 19
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-9# + exo-motif
<400> 19
gggcaacggg acggagauuu a 21
<210> 20
<211> 21
<212> RNA
<213> Artificial Sequence
<220>
<223> miR-CTLA4-10# + exo-motif
<400> 20
ugacugugcu gcggcggaca a 21
<210> 21
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 21
ggag 4
<210> 22
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 22
ggac 4
<210> 23
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 23
ggcg 4
<210> 24
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 24
ggcc 4
<210> 25
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 25
gggg 4
<210> 26
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 26
gggc 4
<210> 27
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 27
ugag 4
<210> 28
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 28
ugac 4
<210> 29
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 29
ugcg 4
<210> 30
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 30
ugcc 4
<210> 31
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 31
uggg 4
<210> 32
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 32
uggc 4
<210> 33
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 33
cgag 4
<210> 34
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 34
cgac 4
<210> 35
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 35
cgcg 4
<210> 36
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 36
cgcc 4
<210> 37
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 37
cggg 4
<210> 38
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 38
cggc 4
<210> 39
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 39
cccu 4
<210> 40
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 40
cccg 4
<210> 41
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 41
ccca 4
<210> 42
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 42
uccu 4
<210> 43
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 43
uccg 4
<210> 44
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 44
ucca 4
<210> 45
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 45
gccu 4
<210> 46
<211> 4
<212> DNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 46
gccg 4
<210> 47
<211> 4
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 47
gcca 4
<210> 48
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 48
ggaggac 7
<210> 49
<211> 10
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 49
ggacugggag 10
<210> 50
<211> 7
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 50
ggaggag 7
<210> 51
<211> 8
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 51
ggacggag 8
<210> 52
<211> 10
<212> RNA
<213> Artificial Sequence
<220>
<223> exo-motif
<400> 52
ggaggcggag 10
<210> 53
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-1#
<400> 53
aaccttcagt ggagttggcg agttttggcc actgactgac tcgccaacca ctgaaggtt 59
<210> 54
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-2#
<400> 54
cttcagtgga gttggcgagc agttttggcc actgactgac tgctcgccct ccactgaag 59
<210> 55
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-3#
<400> 55
actgtgctgc ggaggacaaa tgttttggcc actgactgac atttgtcccg cagcacagt 59
<210> 56
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-4#
<400> 56
cgacattcac ggaggagaat agttttggcc actgactgac tattctcccg tgaatgtcg 59
<210> 57
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-5#
<400> 57
gaacctcacc ctccaaggac tgttttggcc actgactgac agtccttggg gtgaggttc 59
<210> 58
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-6#
<400> 58
atccaaggac tgggagctgt tgttttggcc actgactgac aacagctcag tccttggat 59
<210> 59
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-7#
<400> 59
actcatgtac cctccgccat agttttggcc actgactgac tatggcgggg tacatgagt 59
<210> 60
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-8#
<400> 60
ggcaacggga ggcggagtta tgttttggcc actgactgac ataactccct cccgttgcc 59
<210> 61
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-9#
<400> 61
gggcaacggg acggagattt agttttggcc actgactgac taaatctctc ccgttgccc 59
<210> 62
<211> 59
<212> DNA
<213> Artificial Sequence
<220>
<223> sequences of miR-CTLA4-10#
<400> 62
tgactgtgct gcggcggaca agttttggcc actgactgac ttgtccgcca gcacagtca 59
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И НАБОРЫ, ИМЕЮЩИЕ ОТНОШЕНИЕ К ЗАХВАТУ CA-IX-ПОЗИТИВНЫХ ЭКЗОСОМ | 2018 |
|
RU2770592C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ФИБРОЗА ТКАНЕЙ НА ОСНОВЕ КОМПОНЕНТОВ СЕКРЕТОМА МЕЗЕНХИМНЫХ СТРОМАЛЬНЫХ КЛЕТОК, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ СРЕДСТВА | 2020 |
|
RU2766707C1 |
| ОНКОЛИТИЧЕСКИЕ ВИРУСЫ ПРОСТОГО ГЕРПЕСА 1 ТИПА ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА | 2021 |
|
RU2824514C1 |
| ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫЙ ОНКОЛИТИЧЕСКИЙ ВИРУС ПРОСТОГО ГЕРПЕСА, ДОСТАВЛЯЮЩИЙ ХЕМОКИН И ОПУХОЛЬ-АССОЦИИРОВАННЫЙ/СПЕЦИФИЧЕСКИЙ АНТИГЕН | 2022 |
|
RU2827338C1 |
| ОНКОЛИТИЧЕСКИЙ HSV-ВЕКТОР | 2014 |
|
RU2719190C2 |
| ПОСЛЕДОВАТЕЛЬНОСТИ 3'-UTR ДЛЯ СТАБИЛИЗАЦИИ РНК | 2016 |
|
RU2783165C1 |
| ДНК-СОДЕРЖАЩИЕ ПОЛИНУКЛЕОТИДЫ И РУКОВОДЯЩИЕ ПОСЛЕДОВАТЕЛЬНОСТИ ДЛЯ СИСТЕМ CRISPR ТИПА V И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2021 |
|
RU2832314C1 |
| ПОСЛЕДОВАТЕЛЬНОСТИ 3'-UTR ДЛЯ СТАБИЛИЗАЦИИ РНК | 2016 |
|
RU2720934C2 |
| НОВЫЕ ФЕРМЕНТЫ CRISPR И СИСТЕМЫ | 2016 |
|
RU2771826C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ ИНТЕРЛЕЙКИНУ-2 И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2745451C1 |
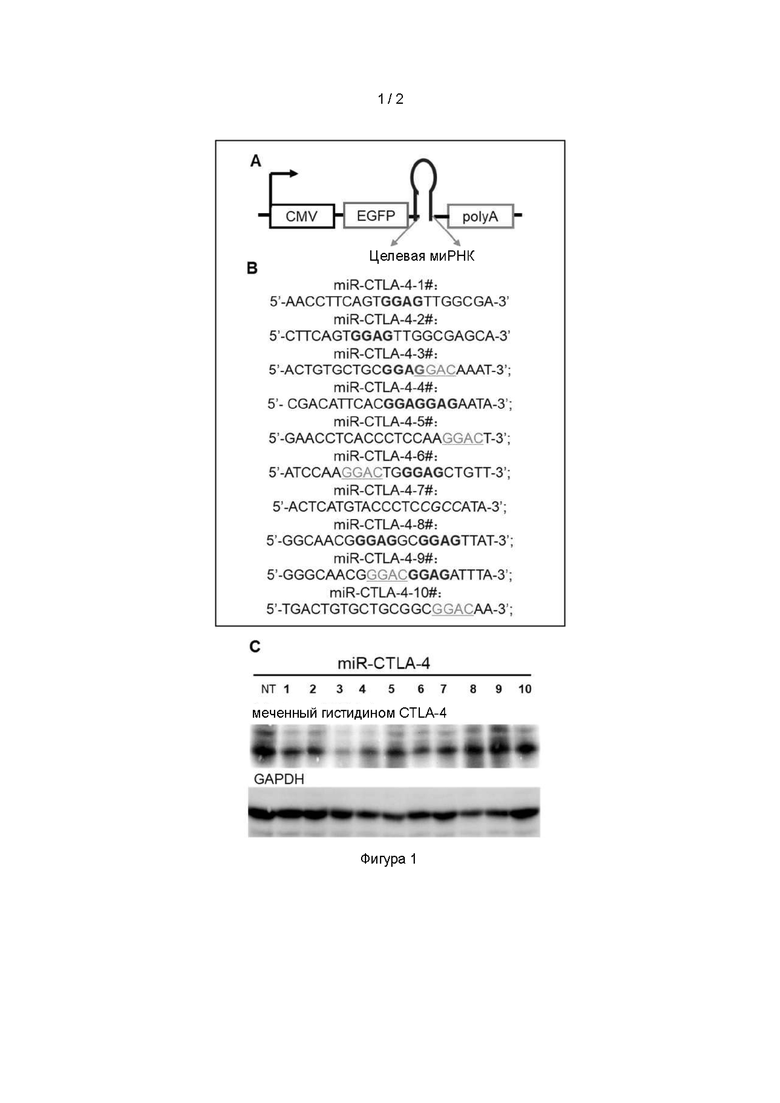

Изобретение относится к области биотехнологии. Описана группа изобретений, включающая фармацевтическую композицию для лечения опухоли у субъекта и набор для лечения опухоли у субъекта. Фармацевтическая композиция содержит терапевтически эффективное количество экзосомы, терапевтически эффективное количество онколитического вируса простого герпеса и фармацевтически приемлемый носитель, причем экзосома содержит ингибирующее количество нацеленной на CTLA4 миРНК и экзомотив, функционально связанный с затравочной последовательностью нацеленной на CTLA4 миРНК, для улучшения упаковки нацеленной на CTLA4 миРНК в эзкосому, и причем онколитический вирус простого герпеса экспрессирует иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело. Изобретение расширяет арсенал средств для лечения опухолей у субъекта. 2 н. и 38 з.п. ф-лы, 3 ил., 2 табл., 1 пр.
1. Фармацевтическая композиция для лечения опухоли у субъекта, содержащая
(a) терапевтически эффективное количество экзосомы,
(b) терапевтически эффективное количество онколитического вируса простого герпеса и
(c) фармацевтически приемлемый носитель,
причем экзосома содержит ингибирующее количество нацеленной на CTLA4 миРНК и экзомотив, функционально связанный с затравочной последовательностью нацеленной на CTLA4 миРНК, для улучшения упаковки нацеленной на CTLA4 миРНК в эзкосому, и
причем онколитический вирус простого герпеса экспрессирует иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело.
2. Композиция по п. 1, характеризующаяся тем, что затравочная последовательность нацеленной на CTLA4 миРНК содержит любую из последовательностей нуклеиновой кислоты с SEQ ID NO: 1 по SEQ ID NO: 4.
3. Композиция по п. 1 или 2, характеризующаяся тем, что экзомотив выбран из группы, состоящей из последовательности нуклеиновой кислоты с SEQ ID NO: 21 по SEQ ID NO: 49.
4. Композиция по п. 1, характеризующаяся тем, что экзомотив расположен ниже и связан с затравочной последовательностью нацеленной на CTLA4 миРНК ковалентно.
5. Композиция по п. 1, характеризующаяся тем, что экзомотив получен путем мутации одной или более нуклеиновых кислот нацеленной на CTLA4 миРНК, за исключением затравочной последовательности.
6. Композиция по п. 1, характеризующаяся тем, что экзомотив является сдвоенным мотивом, образованным посредством объединения двух отдельных экзомотивов, причем любой из двух отдельных экзомотивов выбран из группы, состоящей из последовательности нуклеиновой кислоты с SEQ ID NO: 21 по SEQ ID NO: 47.
7. Композиция по п. 1, характеризующаяся тем, что сдвоенный мотив имеет последовательность нуклеиновой кислоты SEQ ID NO: 48.
8. Композиция по п. 1, характеризующаяся тем, что нацеленная на CTLA4 миРНК и экзомотив, если они функционально связаны, содержат по меньшей мере один общий нуклеотид или два общих нуклеотида или соединены через линкер.
9. Композиция по п. 8, характеризующаяся тем, что линкер состоит из двух или более нуклеотидов, выбранных из группы, состоящей из аденина (А), гуанина (G), цитозина (С), тимина (Т) и урацила (U).
10. Композиция по п. 9, характеризующаяся тем, что линкер представляет собой -GC-.
11. Композиция по п. 1, характеризующаяся тем, что нацеленная на CTLA4 миРНК и экзомотив, если они функционально связаны, имеют последовательность нуклеиновой кислоты SEQ ID NO: 7.
12. Композиция по п. 1, характеризующаяся тем, что иммуностимулирующий агент выбран из ГМ-КСФ, Ил-2, Ил-5, Ил-12, Ил-15, Ил-24 и Ил-27.
13. Композиция по п. 12, характеризующаяся тем, что иммуностимулирующий агент представляет собой Ил-12.
14. Композиция по п. 1, характеризующаяся тем, что онколитический вирус простого герпеса экспрессирует как Ил-12, так и анти-PD-1 антитело.
15. Композиция по п. 1, характеризующаяся тем, что онколитический вирус простого герпеса представляет собой ВПГ-1, экспрессирующий Ил-12 и анти-PD-1 антитело.
16. Композиция по п. 15, характеризующаяся тем, что ВПГ-1 представляет собой штамм F ВПГ-1.
17. Композиция по п. 16, характеризующаяся тем, что фрагмент нуклеотидной последовательности с 117005 по 132096 нативного остова делетирован.
18. Композиция по п. 1, характеризующаяся тем, что опухоль является злокачественной опухолью.
19. Композиция по п. 18, характеризующаяся тем, что злокачественная опухоль выбрана из группы, состоящей из меланомы, фибросаркомы, миксосаркомы, липосаркомы, хондросаркомы, остеогенной саркомы, хордомы, ангиосаркомы, эндотелиосаркомы, лимфангиосаркомы, лимфангиоэндотелиосаркомы, синовиомы, мезотелиомы, опухоли Юинга, лейомиосаркомы, рабдомиосаркомы, карциномы толстой кишки, рака поджелудочной железы, рака молочной железы, рака яичников, рака предстательной железы, плоскоклеточной карциномы, базальноклеточной карциномы, аденокарциномы, карциномы потовых желез, карциномы сальных желез, папиллярной карциномы, папиллярных аденокарцином, цистаденокарциномы, медуллярной карциномы, бронхогенной карциномы, почечно-клеточной карциномы, гепатомы, карциномы желчного протока, хориокарциномы, семиномы, эмбриональной карциномы, опухоли Вильмса, рака шейки матки, опухоли яичка, карциномы легких, мелкоклеточной карциномы легких, карциномы мочевого пузыря, эпителиальной карциномы, глиомы, астроцитомы, медуллобластомы, краниофарингиомы, эпендимомы, пинеаломы, гемангиобластомы, акустической невриномы, олигодендроглиомы, менингиомы, нейробластомы, ретинобластомы, карциномы желудка и карциномы кардиального отдела желудка.
20. Композиция по п. 1, характеризующаяся тем, что субъектом является человек.
21. Набор для лечения опухоли у субъекта, содержащий
(a) терапевтически эффективное количество экзосомы, причем экзосома содержит ингибирующее количество нацеленной на CTLA4 миРНК и экзомотив, функционально связанный с затравочной последовательностью нацеленной на CTLA4 миРНК, для улучшения упаковки нацеленной на CTLA4 миРНК в эзкосому,
(b) терапевтически эффективное количество онколитического вируса простого герпеса, причем онколитический вирус простого герпеса экспрессирует иммуностимулирующий агент или как иммуностимулирующий агент, так и анти-PD-1 антитело, и необязательно
(c) инструкции по применению.
22. Набор по п. 21, характеризующийся тем, что затравочная последовательность нацеленной на CTLA4 миРНК содержит любую из последовательностей нуклеиновой кислоты с SEQ ID NO: 1 по SEQ ID NO: 4.
23. Набор по п. 21 или 22, характеризующийся тем, что экзомотив выбран из группы, состоящей из последовательности нуклеиновой кислоты с SEQ ID NO: 21 по SEQ ID NO: 49.
24. Набор по п. 21, характеризующийся тем, что экзомотив расположен ниже и связан с затравочной последовательностью нацеленной на CTLA4 миРНК ковалентно.
25. Набор по п. 21, характеризующийся тем, что экзомотив получен путем мутации одной или более нуклеиновых кислот нацеленной на CTLA4 миРНК, за исключением затравочной последовательности.
26. Набор по п. 21, характеризующийся тем, что экзомотив является сдвоенным мотивом, образованным посредством объединения двух отдельных экзомотивов, причем любой из двух отдельных экзомотивов выбран из группы, состоящей из последовательности нуклеиновой кислоты с SEQ ID NO: 21 по SEQ ID NO: 47.
27. Набор по п. 21, характеризующийся тем, что сдвоенный мотив имеет последовательность нуклеиновой кислоты SEQ ID NO: 48.
28. Набор по п. 21, характеризующийся тем, что нацеленная на CTLA4 миРНК и экзомотив, если они функционально связаны, содержат по меньшей мере один общий нуклеотид или два общих нуклеотида или соединены через линкер.
29. Набор по п. 28, характеризующийся тем, что линкер состоит из двух или более нуклеотидов, выбранных из группы, состоящей из аденина (А), гуанина (G), цитозина (С), тимина (Т) и урацила (U).
30. Набор по п. 29, характеризующийся тем, что линкер представляет собой -GC-.
31. Набор по п. 21, характеризующийся тем, что нацеленная на CTLA4 миРНК и экзомотив, если они функционально связаны, имеют последовательность нуклеиновой кислоты SEQ ID NO: 7.
32. Набор по п. 21, характеризующийся тем, что иммуностимулирующий агент выбран из ГМ-КСФ, Ил-2, Ил-5, Ил-12, Ил-15, Ил-24 и Ил-27.
33. Набор по п. 32, характеризующийся тем, что иммуностимулирующий агент представляет собой Ил-12.
34. Набор по п. 21, характеризующийся тем, что онколитический вирус простого герпеса экспрессирует как Ил-12, так и анти-PD-1 антитело.
35. Набор по п. 21, характеризующийся тем, что онколитический вирус простого герпеса представляет собой ВПГ-1, экспрессирующий Ил-12 и анти-PD-1 антитело.
36. Набор по п. 35, характеризующийся тем, что ВПГ-1 представляет собой штамм F ВПГ-1.
37. Набор по п. 36, характеризующийся тем, что фрагмент нуклеотидной последовательности с 117005 по 132096 нативного остова делетирован.
38. Набор по п. 21, характеризующийся тем, что опухоль является злокачественной опухолью.
39. Набор по п. 38, характеризующийся тем, что злокачественная опухоль выбрана из группы, состоящей из меланомы, фибросаркомы, миксосаркомы, липосаркомы, хондросаркомы, остеогенной саркомы, хордомы, ангиосаркомы, эндотелиосаркомы, лимфангиосаркомы, лимфангиоэндотелиосаркомы, синовиомы, мезотелиомы, опухоли Юинга, лейомиосаркомы, рабдомиосаркомы, карциномы толстой кишки, рака поджелудочной железы, рака молочной железы, рака яичников, рака предстательной железы, плоскоклеточной карциномы, базальноклеточной карциномы, аденокарциномы, карциномы потовых желез, карциномы сальных желез, папиллярной карциномы, папиллярных аденокарцином, цистаденокарциномы, медуллярной карциномы, бронхогенной карциномы, почечно-клеточной карциномы, гепатомы, карциномы желчного протока, хориокарциномы, семиномы, эмбриональной карциномы, опухоли Вильмса, рака шейки матки, опухоли яичка, карциномы легких, мелкоклеточной карциномы легких, карциномы мочевого пузыря, эпителиальной карциномы, глиомы, астроцитомы, медуллобластомы, краниофарингиомы, эпендимомы, пинеаломы, гемангиобластомы, акустической невриномы, олигодендроглиомы, менингиомы, нейробластомы, ретинобластомы, карциномы желудка и карциномы кардиального отдела желудка.
40. Набор по п. 21, характеризующийся тем, что субъектом является человек.
| WO 2020132946 A1 02.07.2020 | |||
| WO 2017181420 A1 26.10.2017 | |||
| Agarwal A | |||
| et al | |||
| Regulatory T cell-derived exosomes: possible therapeutic and diagnostic tools in transplantation //Frontiers in immunology, 2014, 5, article 555, p | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Johnsen K | |||
| B | |||
| et al | |||
| A comprehensive overview of exosomes as drug delivery vehicles-endogenous nanocarriers for | |||
Авторы
Даты
2023-12-29—Публикация
2019-07-04—Подача