Область техники, к которой относится изобретение
Изобретение относится к области медицины и фармакологии и может быть использовано для получения лекарственных средств и биоматериалов для лечения фиброза тканей, включая предупреждение прогрессирования и стимуляцию реверсии фибротических изменений, после повреждений различного генеза (механических, термических, химических), в том числе фиброза легких при интерстициальных заболеваниях легких и вирусных пневмониях.
Уровень техники
Из уровня техники (Mansouri N. et al. Mesenchymal stromal cell exosomes prevent and revert experimental pulmonary fibrosis through modulation of monocyte phenotypes // JCI insight. - 2019. - Т. 4. - №. 21.) известен способ получения экзосом с помощью коммерческого набора из МСК костного мозга человека, где выделенные экзосомы имеют поверхностные маркеры CD9, CD63, средний размер экзосом составил - 35-150 нм, а также способ лечения индуцированного блеомицином фиброза легких с помощью вышеуказанных экзосом. Однако, в данной работе не раскрыта информация, касающаяся профиля микроРНК для полученных экзосом и не показан вклад некодирующих РНК в реализацию антифибротических эффектов. Кроме того, получение МСК костного мозга является менее перспективным по своей доступности и безопасности для донора.
Также, из уровня техники известен способ получения экзосом с использованием метода ультрафильтрации из секретома МСК жировой ткани мышей C57BL/6, где выделенные экзосомы имеют поверхностные маркеры CD9, CD63, CD81, средний размер экзосом составил - 145 нм и 285 нм, а также способ лечения фиброза легких, индуцированного двуокисью кремния, с помощью вышеуказанных экзосом (Bandeira E. et al. Therapeutic effects of adipose-tissue-derived mesenchymal stromal cells and their extracellular vesicles in experimental silicosis //Respiratory research. - 2018. - Т. 19. - №. 1. - С. 1-10.). Однако, в данной работе не раскрыта информация, касающаяся профиля микроРНК для полученных экзосом и не показан вклад некодирующих РНК в реализацию антифибротических эффектов, а наличие бимодальности в средних размерах экзосом указывает на присутствие смесь из двух типов частиц, которые могут быть как смесью двух типов внеклеточных везикул, так и загрязнением при анализе размера экзосом.
Из уровня техники известен способ лечения заболевания, ассоциированного с фиброзом, который включает применение в эффективном количестве, по меньшей мере, одной микроРНК, выбранной из группы: hsa-miR-452-3p, hsa-miR-224-3p, hsa-miR-378i, hsa-miR-10b-5p, hsa-miR-99a-3p, hsa-miR-105-3p, hsa-miR-224-5p, hsa-miR-10b-3p, hsa-miR-338-5p, hsa-miR-767-5p, hsa-miR-196b-5p, hsa-miR-148a-3p, hsa-miR-452-5p, hsa-miR-873-5p, hsa-miR-873-3p, hsa-let-7a-3p, hsa-miR-208b-3p, hsa-miR-582-3p, hsa-miR-196a-5p, hsa-miR-99b-3p, hsa-miR-320d, hsa-let-7e-3p, hsa-miR-183-5p, hsa-miR-532-5p, hsa-miR-30c-2-3p, novel_mirl8, hsa-miR-3529-3p, hsa-miR-3074-5p, hsa-miR-423-5p, hsa-let-7f-l-3p, hsa-let-7c-3p, hsa-miR-378c, hsa-miR-486-5p, hsa-miR-185-3p, hsa-miR-320e, hsa-miR-182-5p, novel_mir78, hsa-miR-340-3p, hsa-miR-24-2-5p, hsa-miR-330-3p, hsa-miR-192-3p, hsa-miR-26a-2-3p, hsa-miR-26b-3p, hsa-miR-99a-5p, hsa-miR-148b-3p, hsa-miR-374a-3p, hsa-miR-30a-3p, novel-mir32, hsa-miR-17-3p, hsa-miR-193b-5p, hsa-let-7i-5p and hsa-miR-19b-3p; также известен способ лечения заболевания, ассоциированного с фиброзом, который включает применение в эффективном количестве, по меньшей мере, двух микроРНК, выбранных из группы: hsa-miR-452-3p, hsa-miR-224-3p, hsa-miR-378i, hsa-miR-10b-5p, hsa-miR-99a-3p, hsa-miR-105-3p, hsa-miR-224-5p, hsa-miR-10b-3p, hsa-miR-338-5p, hsa-miR-767-5p, hsa-miR-196b-5p, hsa-miR-148a-3p, hsa-miR-452-5p, hsa-miR-873-5p, hsa-miR-873-3p, hsa-let-7a-3p, hsa-miR-208b-3p, hsa-miR-582-3p, hsa-miR-196a-5p, hsa-miR-99b-3p, hsa-miR-320d, hsa-let-7e-3p, hsa-miR-378a-3p, hsa-miR-183-5p, hsa-miR-532-5p, hsa-miR-30c-2-3p, novel_mirl8, hsa-miR-3529-3p, hsa-miR-3074-5p, hsa-miR-423-5p, hsa-let-7f-l-3p, hsa-let-7c-3p, hsa-miR-378c, hsa-miR-486-5p, hsa-miR-185-3p, hsa-miR-320e, hsa-miR-182-5p, novel_mir78, hsa-miR-340-3p, hsa-miR-24-2-5p, hsa-miR-330-3p, hsa-miR-192-3p, hsa-miR-26a-2-3p, hsa-miR-26b-3p, hsa-miR-99a-5p, hsa-miR-148b-3p, hsa-miR-374a-3p, hsa-miR-30a-3p, novel-mir32, hsa-miR-17-3p, hsa-miR-193b-5p, hsa-let-7i-5p and hsa-miR-19b-3p; а также известен способ лечения заболевания, ассоциированного с фиброзом, который включает применение терапевтически эффективного количества экзосом, полученных из кондиционированной среды гепатоцитов (WO 2019043709 A1, 2017 г.). Однако вышеперечисленные известные способы не предоставляют информации о характеристиках клеток, из которых получены кондиционированная среда, экзосомы или микроРНК, кроме того, что используемые клетки - это первично выделенные гепатоциты. При этом, из уровня техники известно, что первично выделенные клетки являются гетерогенными, а также могут быть контаминированы другими типами клеток (например, резидентными клетками иммунной системы). Также в известном техническом решении отсутствует информация, где описано, что используемые в способах микроРНК применяются в составе экзосом или внеклеточных везикул, или в составе фармацевтической композиции.
Из уровня техники известна композиция, включающая две, три или четыре микроРНК из группы: hsa-miR-1246, hsa-miR-4492, hsa-miR-4488 и hsa-miR-4532, для лечения среди прочего идиопатического фиброза легких (EP 2956146 B1 (2013 г.)). Однако в данном техническом решении не указан источник и способ получения вышеуказанных микроРНК, что является критичным для реализации назначения, а именно лечения фиброза.
Из уровня техники известен способ получения экзосом из МСК костного мозга человека, с использованием метода ультрацентрифугирования, где выделенные экзосомы имеют поверхностные маркеры CD63, CD81, и которые содержат среди прочих микроРНК - miR-21-5p, miR-34a-5p, miR-196a-5p, miR-199b-5p (Shentu T. P. et al. Thy-1 dependent uptake of mesenchymal stem cell-derived extracellular vesicles blocks myofibroblastic differentiation // Scientific reports. - 2017. - Т. 7. - №. 1. - С. 1-11.). Однако в данной работе авторы продемонстрировали влияние экзосом на процесс перехода фибробластов в миофибробласты, но не показали какого-либо эффекта на фибротические процессы in vivo, что не позволяет рассматривать описанный подход в качестве антифибротического средства.
Из уровня техники известна фармацевтическая композиция, которая включает полинуклеотиды, в том числе охарактеризованные последовательностями miR-143-3p UGAGAUGAAGCACUGUAGCUC (SEQ ID NO: 58) и miR-145-5p GUCCAGUUUUCCCAGGAAUCCCU (SEQ ID NO: 59), где полинуклеотиды могут быть заключены в экзосомы, секретируемые иммортализованными клетками или, среди прочих, стволовыми клетками жировой ткани (WO 2019169380 A1, 2018 г.). Однако в данном техническом решении не указана характеристика экзосом, которые включают вышеупомянутые микроРНК, а также характеристик (например, поверхностные маркеры или другие характеристики) клеток, из которых получены данные экзосомы. Из уровня техники известно, что эти параметры могут значительно варьировать в зависимости от клеток - продуцентов экзосом.
Наиболее близким к заявляемому является способ получения секретома, в том числе обогащенного экзосомами, МСК костного мозга человека и зрелых клеток легких, с поверхностными маркерами, характерными для эпителиальных и мезенхимных клеток, с использованием метода ультрафильтрации, где выделенные экзосомы имеют поверхностные маркеры CD9, CD63, CD81, а средний размер экзосом составил - 114.67 +/-2.5 нм, и которые содержат среди прочих микроРНК - hsa-miR-10a-5p, а также способ лечения идиопатического фиброза легких с помощью вышеуказанных компонентов секретома, включая экзосомы, МСК или зрелых клеток легких на модели блеомицин-индуцированного фиброза легких (Dinh P. U. C. et al. Inhalation of lung spheroid cell secretome and exosomes promotes lung repair in pulmonary fibrosis //Nature communications. - 2020. - Т. 11. - №. 1. - С. 1-14.). Таким образом, среди общих признаков данного средства с заявляемым можно выделить схожие методы получения средства (кондиционирование МСК человека при 75% конфлуенте в бессывороточной среде в течение 3 дней, обогащение фракцией внеклеточных везикул с помощью ультрафильтрации, характеристика внеклеточных везикул по размеру, поверхностным маркерам и морфологии по результатам просвечивающей микроскопии, оценку состава микроРНК в везикулах методом РНК секвенирования), а также общую экспериментальную модель блеомицин-индуцированного фиброза легких, на которой был изучен антифибротический эффект секретома клеток. Однако есть ряд существенных отличий. Во-первых, в данной работе были использованы МСК костного мозга и зрелые клетки легких, получение которых требует применения инвазивных и болезненных методов и является менее перспективным по своей доступности и безопасности для донора. Во-вторых, неизвестно, какая среда использована для культивирования МСК в данной работе и насколько она специфична для поддержания свойств МСК. Известно, что состав культуральной среды роста для МСК влияет на качественный и количественный состав секретома этих клеток. Во-третьих, способ получения кондиционированной среды (секретома) МСК включал фильтрацию через 0,22 мкм фильтры с целью очистки, что приводит к отсечению и повреждению фракции внеклеточных везикул размером более 200 нм. Затем в данной работе концентрирование методом ультрафильтрации проводили с использованием фильтров на 100 кДа, что приводило к потере части внеклеточных везикул большего размера, вклад которых в антифибротический эффект секретома авторами не был определен. В работе Dinh и соавторы продемонстрировали преимущество экзосом, полученных из секретома клеток легких по сравнению с МСК костного мозга, что указывает на зависимость эффективности воздействия экзосом на мишень от тканеспецифичности клеток-доноров экзосом и клеток-акцепторов. Вероятно, с отличиями в способе получения секретома связано отсутствие значимых различий в антифибротическом эффекте компонентов секретома МСК, обогащенных внеклеточными везикулами, по сравнению с отрицательным контролем (по шкале Эшкрофта при оценке гистологических изменения в легких). Важным отличием является тот факт, что в работе Dinh и соавторов содержание микроРНК во внеклеточных везикулах показано только методом РНК секвенирования, точность и специфичность которого относительно не высоки, и не валидировано с помощью ПЦР анализа. Вклад определенных микроРНК в антифибротические эффекты секретома клеток никак не установлен. Кроме того, в работе Dinh и соавторов описан только подход к лечению фиброза легких со специфичным путем введения (ингаляционным) компонентов секретома клеток, включая экзосомы.
Технической проблемой, на решение которой направлено заявляемое изобретение является создание нового лекарственного средства для лечения фиброза тканей, направленного на предотвращение развития фибротических процессов в тканях и стимуляцию реверсии этих процессов, обладающего комплексным действием, по крайней мере, на фибробласты и миофибробласты как ключевые клеточные медиаторы фиброза.
Раскрытие изобретения
Техническим результатом заявляемого изобретения является получение средства, эффективно подавляющего фиброз тканей или предотвращающего развитие фиброза тканей, в частности, легких, за счет сбалансированного действия компонентов кондиционированной среды (КС) мезенхимных стромальных клеток (МСК) человека или ее отдельных фракций, по крайней мере, внеклеточных везикул, на тканевые фибробласты или миофибробласты, в частности, фибробласты или миофибробласты легких, что приводит к полноценному структурному и функциональному восстановлению поврежденных тканей без развития фибротических осложнений, сокращению сроков заживления повреждений и повышению качества жизни пациентов. Эффективность средства обеспечивается, по крайней мере, за счет содержания в составе лекарственного средства внеклеточных везикул, содержащих регулирующие фибротические процессы микроРНК (SEQ ID NO 1 - SEQ ID NO 61), подавляющих дифференцировку фибробластов, индуцируемую профиброгенным стимулом трансформирующим фактором роста бета (TGF-beta), и стимулирующих редифференцировку TGF-beta-активированных миофибробластов в нормальные фибробласты. В отличие от прототипа, для получения средства в заявленном изобретении используются МСК жировой ткани, а не МСК костного мозга и зрелые клетки легких, получение которых требует применения инвазивных и болезненных методов и является менее перспективным по своей доступности и безопасности для донора. Следует также учитывать, что именно жировая ткань считается одним из основных источников внеклеточных везикул, циркулирующих в организме человека. В отличие от прототипа, для заявленного средства показаны выраженные антифибротические эффекты как на in vitro моделях дифференцировки фибробластов (как минимум, двух типов - дермальных и легочных) в миофибробласты, так и на животных моделях фиброза легких и фиброза в исходе ранозаживления кожи.
Техническая проблема решается способом получения средства, эффективно подавляющего фиброз или предотвращающего развитие фиброза, включающим культивирование первичных МСК жировой ткани человека 2-5 пассажей или линейных иммортализованных МСК человека 15-25 пассажей в бессывороточной и лишенной продуктов животного происхождения среде роста, содержащей 1% антибиотика/антимикотика, 1% глутамина, 1% пирувата, а также в других средах для культивирования, в том числе, с добавками, поддерживающих жизнеспособность клеток не менее 90% и пригодных для терапевтического применения, в течение 2-7 дней, отбор среды культивирования и ее очистка от дебриса путем центрифугирования на скорости 5000 g при температуре +2-+6°С в течение 10 минут с последующим отбором супернатанта, его фракционированием методом ультрафильтрации на центрифуге или тангенциальной ультрафильтрации с применением фильтров, позволяющих получить фракцию, содержащую внеклеточные везикулы МСК человека, в концентрации не менее 1-3*10^10 частиц на мл фракции за вычетом содержания частиц к фоновом контрольном образце, определяемой посредством трекинга наночастиц (Nanoparticle Tracking Analysis, NTA), или его фракционированием и концентрированием методом ультрафильтрации на центрифуге или тангенциальной ультрафильтрации с применением фильтров, позволяющих получить фракцию, обедненную по содержанию внеклеточных везикул МСК человека и обогащенную растворимыми белковыми факторами в концентрации, не менее пятикратной по отношению к количеству белка в кондиционированной среде МСК (КС-МСК) до фракционирования, что устанавливается методами анализа содержания общего белка или отдельных белков в смеси, или в виде полной КС-МСК при достижении концентрации, не менее пятикратной по отношению к количеству белка в КС-МСК до фракционирования, что устанавливается методами анализа содержания общего белка или отдельных белков в смеси. Лекарственное средство может быть подвергнуто лиофилизации в 8-14 стадий при давлении 0,013 кПа, температуре от -40°С до -5°С, время лиофилизации не более 36 часов при максимальной загрузке лиофильной сушки, или аналогичным способом лиофильной сушки.
В отличие от прототипа, в заявленном изобретении МСК наращивают в специфической среде, поддерживающей рост недифференцированных мезенхимных клеток человека (AdvanceSTEM Cell Culture Media, содержащей 9-11% добавки к среде роста AdvanceSTEM Stem Cell Growth Supplement, HyClone, USA) или аналогичной, способной поддерживать рост недифференцированных МСК на протяжении не менее 5 пассажей для МСК жировой ткани человека и не менее 25 пассажей для линейных иммортализованных МСК (далее - среда роста МСК). Культивирование может быть осуществлено в культуральных флаконах или чашках (фирмы Corning или аналогичные), при этом клетки выращивают на плоской подложке со стартовой плотностью 5-15*103/см2 в среде роста в объеме 0,1-0,2 мл/см2 в условиях СО2 инкубатора при 37±1°С, 5%-м содержании СО2 и относительной влажности ≥ 95% до достижения 90% конфлюента, с полной сменой среды 1 раз в 3 дня. Для получения КС-МСК клетки трижды отмывают раствором Хэнкса объемом 0.2 мл/см2 заселенной поверхности, в течение не менее 10 минут в условиях комнатной температуры, контролируя качество отмывки через 1 час после нанесения бессывороточной среды для кондиционирования, которая представляет собой бессывороточную и лишенную продуктов животного происхождения среду роста, содержащую 1% антибиотика/антимикотика, 1% глутамина, 1% пирувата, или аналогичные среды для культивирования, в том числе, с добавками, поддерживающими жизнеспособность клеток не менее 70% и пригодными для терапевтического применения. В отличие от прототипа в настоящем изобретении использован метод очистки и концентрирования с помощью центрифугирования и дальнейшей ультрафильтрации с использованием фильтров на 1000 кДа (с допустимой величиной погрешности не более 5%), что позволило сохранить максимальное количество внеклеточных везикул в секретоме и обогатить ими заявленное средство.
Техническая проблема решается лекарственным средством для предотвращения или профилактики фибротических явлений в тканях, обладающего комплексным действием, по крайней мере, на фибробласты и миофибробласты, содержит концентрации внеклеточных везикул или белков в количествах, не менее 95% от указанных для каждого типа фракции выше и демонстрирует специфическую активность на 95% и более от исходного лекарственного средства до лиофилизации, что устанавливается путем анализа способности лекарственного средства подавлять дифференцировку фибробластов, индуцированную стимуляцией TGF-beta, в миофибробласты, а также стимулировать редифференцировку миофибробластов, полученных при индукции дифференцировки TGF-beta, в фибробласты, измеренную методами иммуноцитохимии, Western-Blot, ПЦР или аналогичными.
Таким образом, технический результат достигается за счет того, что средство для предотвращения или профилактики фибротических явлений в тканях, обладающего комплексным действием, по крайней мере, на фибробласты и миофибробласты, получают при культивировании МСК человека в бессывороточной среде, лишенной животных компонентов, с потенциально безопасным для клинического применения составом, поддерживающей жизнеспособность клеток в течение подобранного срока кондиционирования, путем сбора кондиционированной среды, содержащей биологически активные факторы и внеклеточные везикулы, секретируемые клетками в культуральную среду, очистки полученной среды и ее фракционирования с помощью центрифугирования и ультрафильтрации и ее стабилизации путем лиофилизации. Полученный лиофилизат, разведенный в стерильном физиологическом растворе, можно использовать как лекарственное средство, в том числе в виде ингаляционной или инъекционной форм.
Эффективность заявляемого средства предполагает наличие целого комплекса воздействий, направленных на предотвращение или профилактику фибротических явлений в тканях, таких как дифференцировка фибробластов в миофибробласты. При этом необходимость сдерживания избыточного фиброзирования для физиологического восстановления поврежденной ткани является актуальной задачей. Использование КС-МСК человека, позволит обеспечить комплексное решение проблем, возникающих при избыточном фиброзировании ткани после повреждений различного генеза, в том числе индуцированного проникновением в организм живых и неживых чужеродных агентов. Полноценное восстановление ткани после различных повреждений без фибротических осложнений, в том числе за счет снижения количества миофибробластов в ткани, может быть осуществлено с помощью введения КС-МСК или ее фракций, содержащих комбинацию факторов роста, внеклеточных везикул, переносящих определенные микроРНК, или других биологически активных компонентов, секретированных МСК человека. Данное решение позволяет получить оптимальное сочетание активных компонентов различной природы, секретированных клетками человека, способствующее предотвращению или профилактике избыточного фиброза тканей, в среде, не содержащей белков животного происхождения и бактериальных фрагментов, а также обеспечить сбалансированный эффект секретируемых клетками продуктов за счет наличия различных по природе и механизму действия факторов, представленных в различных фракциях КС-МСК.
Для получения кондиционированной среды в заявляемом изобретении использованы мультипотентные мезенхимные стволовые/стромальные клетки (МСК) человека, отвечающие за репарацию и регенерацию тканей и органов как в норме, так и при повреждениях. Одним из наиболее доступных источников МСК у человека является жировая ткань. МСК могут быть легко выделены в результате ферментативной обработки образцов жировой ткани, полученной в результате косметической липосакции или в ходе хирургического удаления жирового отложения. Культивирование изолированных МСК ЖТ приводит к получению относительно гомогенной популяции мультипотентных стромальных фибробластоподобных клеток. Следует также учитывать, что именно жировая ткань считается одним из основных источников внеклеточных везикул, циркулирующих в организме человека.
В заявленном изобретении могут быть использованы МСК, полученные самостоятельно по любому известному из уровня техники способу (например, из хирургических биопсий, липоаспирата и др.), так и в виде коммерческих препаратов МСК, имеющих сертификат качества и предназначенных, в том числе, для клинического применения, например, такие как продукт ATCC (ATCC® PCS-500-011), представляющий собой МСК человека, выделенные из липоаспирата, культивированные до 2 пассажа и подвергнутые криоконсервации, или аналогичные, в частности иммортализованные линии МСК жировой ткани человека (ATCC® SCRC-4000™).
Ранее на моделях блеомицин-индуцированного фиброза легких было показано, что локальное введение КС-МСК, обогащенной внеклеточными везикулами, способствовало разрешению фиброза. Так, мыши, которым вводили КС-МСК, обогащенную внеклеточными везикулами, демонстрировали лучшее состояние по сравнению с контрольными животными. В модели профилактики фиброза легких мыши, которым вводили КС-МСК, обогащенную внеклеточными везикулами, также показывали лучшее состояние по сравнению с животными из контрольной группы. Согласно данным наших исследований и работ других научных коллективов, основным механизмом, лежащим в основе антифибротического эффекта МСК, является продукция этими клетками широкого спектра биологически активных компонентов различной природы, действующих как индивидуально, так и в составе внеклеточных везикул, и способствующих сбалансированному восстановлению поврежденной ткани. В отличие от прототипа, в настоящем изобретении представлены антифибротические эффекты компонентов секретома МСК на разных моделях фиброза и при разных путях введения, а для фиброза легких представлены данные по эффективности не только лечения фиброза легочной ткани, но и предотвращения развития фиброза, что может быть необходимо для профилактики развития фибротических осложнений интерстициальных пневмоний, в том числе вирусных, включая коронавирусные инфекции.
В большинстве протоколов выделения и культивирования МСК жировой ткани используется среда с добавлением эмбриональной телячьей сыворотки (ЭТС) или фетальной бычьей сыворотки (ФБС). Эти сыворотки содержат необходимый коктейль факторов роста, гормонов и витаминов, стимулирующих клеточную адгезию и пролиферацию в условиях культивирования in vitro. В то же время накапливается все больше сведений о том, что клетки, выращенные с использованием сывороток животных, потенциально небезопасны, в частности, существует риск заражения прионами или вирусами культуры клеток при культивировании с использованием сывороток животных, а также возможность иммунной реакции со стороны организма реципиента. Кроме того, было показано, что длительное культивирование в присутствии ФБС значительно изменяет свойства клеток различного происхождения. Так, мезенхимные клетки костного мозга, культивированные в присутствии ФБС, характеризуются нестабильностью транскриптома, включая изменение экспрессии генов, ответственных за регуляцию клеточного цикла, апоптоз и клеточную адгезию.
Отличительной особенностью заявляемого изобретения является использование специализированной среды, поддерживающей рост и функциональные свойства недифференцированных МСК человека, на этапах, предшествующих кондиционированию МСК: AdvanceSTEM Cell Culture Media (HyClone, USA) с добавлением раствора антибиотиков Penicillin-Streptomycin (HyClone, USA) и добавки к среде роста AdvanceSTEM Stem Cell Growth Supplement (HyClone, USA), которые берут при следующем соотношении компонентов, об.%:
AdvanceSTEM Cell Culture Media - 89-91;
Раствор антибиотиков Penicillin-Streptomycin - 0,95-1,05;
Добавки к среде роста AdvanceSTEM Stem Cell Growth Supplement - 9,5-10,5.
МСК выделяют из подкожной жировой ткани человека и культивируют в приготовленной по указанной выше схеме среде роста до 4-5 пассажа либо используют линию иммортализованных МСК 15-25 пассажей. Затем клетки тщательно отмывают от компонентов среды роста раствором Хэнкса (фирмы ПанЭко или аналогичным) и помещают в бессывороточную и лишенную продуктов животного происхождения среду роста, в качестве последней используют DMEM с низким содержанием глюкозы (HyClone, USA) или другую среду роста, поддерживающую жизнеспособность МСК человека (не ниже 70%) в течение всего срока кондиционирования и пригодную для терапевтического применения. Указанную среду для кондиционирования клеткам добавляют в объеме 0,1-0,2 мл/см2 и культивируют в условиях СО2 инкубатора при 37+1°С, 5%-м содержании СО2 и относительной влажности ≥ 95% в течение 2-7 дней. КС-МСК, содержащую все продукты секреции МСК человека, собирают в стерильные емкости для центрифугирования, удаляют путем центрифугирования остатки клеток и полученный супернатант подвергают концентрированию или фракционированию с последующим концентрированием с помощью тангенциальной фильтрации или ультрафильтрации на фильтрах для центрифуги. При использовании соответствующего оборудования и соблюдении асептических условий можно получить стерильный продукт КС-МСК, так и ее отдельных фракций. Полученный продукт для хранения можно подвергнуть лиофилизации для получения итогового продукта (лиофилизат кондиционированной среды, содержащей продукты секреции МСК человека, или ее отдельных фракций), содержащего в том числе ключевые биологически активные компоненты, по которым проводится стандартизация конечного продукта. Так, выявляемые концентрации внеклеточных везикул или белков не должны быть менее 95% от указанных для каждого типа фракции до лиофилизации, а также специфическую активность должна представлена на 95% и более от исходной фракции продукта до лиофилизации, что устанавливается путем анализа способности лекарственного средства подавлять дифференцировку фибробластов, индуцированную стимуляцией TGF-beta, в миофибробласты, а также стимулировать редифференцировку миофибробластов, полученных при индукции дифференцировки TGF-beta, в фибробласты, измеренную методами иммуноцитохимии, Western-Blot, ПЦР или аналогичными.
Другой технической особенностью заявляемого изобретения является возможность не только концентрировать, а при необходимости и одновременно очищать кондиционированную среду с использованием системы фильтрации в тангенциальном потоке Minim II (Life Sciences, США) или аналогичной, используя ультрафильтрационные кассеты (Minimate TFF capsule, PALL) или аналогичные, а также с использованием фильтров для центрифуги (Vivaspin, Sartorius) или аналогичные, что позволяет значительно увеличить чистоту получаемых фракций и избавиться от нежелательных компонентов среды, в частности, антибиотиков. В отличие от прототипа, для которого способ получения кондиционированной среды (секретома) МСК включал фильтрацию через 0,22 мкм фильтры с целью очистки, что приводит к отсечению и повреждению фракции внеклеточных везикул размером более 200 нм, а концентрирование методом ультрафильтрации проводили с использованием фильтров на 100 кДа, что приводило к потере части внеклеточных везикул большего размера, вклад которых в антифибротический эффект секретома авторами не был определен, в настоящем изобретении использован метод очистки и концентрирования с помощью центрифугирования и дальнейшей ультрафильтрации с использованием фильтром на 1000 кДа (с допустимой величиной погрешности не более 5%), что позволило сохранить максимальное количество внеклеточных везикул в секретоме и обогатить ими заявленное средство. Кроме того, в описании прототипа его антифибротические эффекты после всех этапов процессинга не проверены на каких-либо in vitro моделях, а статистически значимая эффективность на животной модели фиброза легких не показана (для МСК костного мозга).
В конкретных примерах микроРНК, входящие в состав внеклеточных везикул и/или кондиционированной среды для лечения фиброза ткани, могут быть представлены одной или несколькими микроРНК, охарактеризованными последовательностями SEQ ID NO: 1-61. В отличие от прототипа, в котором содержание некоторых микроРНК во внеклеточных везикулах показано только методом РНК секвенирования, точность и специфичность которого относительно не высоки, и не валидировано с помощью ПЦР анализа, а вклад определенных микроРНК в антифибротические эффекты секретома клеток никак не установлен, в настоящем изобретении представлены данные по валидации представленности фиброз-ассоциированных микроРНК во внеклеточных везикулах в составе секретома МСК и приведены данные по прямой оценке вклада отдельных микроРНК в реализацию антифибротических эффектов секретома МСК.
В результате осуществления данного изобретения получают средство на основе продуктов секреции МСК человека, которое может быть использовано как лекарственное средство для лечения фиброза тканей, включая предупреждение прогрессирования и стимуляцию реверсии фибротических изменений, после повреждений различного генеза, обладающего комплексным действием, по крайней мере, на фибробласты и миофибробласты. При этом, фиброз может быть вызван механическими, химическими или термическими повреждениями тканей; или развивается в результате вирусной пневмонии, в частности вызванной коронавирусами; или развивается в результате профессиональных заболеваний легких.
Краткое описание чертежей
Изобретение поясняется следующими чертежами.
На фиг. 1 представлена характеристика внеклеточных везикул (ВВ-МСК), высвобождаемых из мезенхимных стромальных клеток (МСК) после 48 ч кондиционирования. Позициями на фигуре 1 обозначены: 1 - Распределение частиц по размеру ВВ: в образце (красный) и в контрольной аликвоте КС-МСК после 30 мин кондиционирования (серый) для неконцентрированных (A) и 5-кратно концентрированных (Б) образцов, измеренных с помощью метода анализа траекторий наночастиц (NTA), 2 - Изображение ВВ-МСК (ВВ указаны стрелками), просвечивающая электронная микроскопия, 3 - Экспрессия везикулярных маркеров в образце ВВ-МСК и лизате МСК, вестерн-блот.
На фиг. 2 представлены изображения, иллюстрирующие способность фибробластов к захвату ВВ-МСК. Иммунофлуоресцентный анализ (ВВ + миРНК - FAM (зеленый), PKH26 (красный), DAPI (синий)). Позициями на фигуре 2 обозначены: 1 - Изображения, полученные с помощью широкопольной микроскопии, 2 - Изображение, полученное с помощью конфокальной микроскопии, 3 - Изображение, полученное с помощью конфокальной микроскопии, сагиттальный разрез.
На фиг. 3 представлены графики, иллюстрирующие способность ВВ-МСК, добавленных одновременно с TGFβ, предотвращать индуцированное TGFβ увеличение экспрессии альфа-актина в фибробластах. Анализ экспрессии в культивируемых контрольных фибробластах без сыворотки (- TGFβ), в фибробластах после воздействия TGFβ (+ TGFβ), TGFβ с ВВ-МСК (+ TGFβ + ВВ-МСК) и TGFβ с РФ-МСК (+ TGFβ + РФ-МСК). Позициями на фигуре 3 обозначены: - ОТ-ПЦР, альфа-актин (n = 9), 2 - Вестерн-блоттинг, альфа-актин (n = 3). Столбиками отмечены значения медиан по каждому фактору. Планками ограничиваются 25-ые и 75-е процентили. Над планками показан уровень значимости различий. Для сравнения групп применяли U-критерий Манна-Уитни.
На фиг. 4 представлены фотографии, иллюстрирующие способность ВВ-МСК, добавленных одновременно с TGFβ, предотвращать индуцированное TGFβ формирование стресс-фибрилл в фибробластах. Иммунофлуоресцентный анализ (альфа-актин (зеленый), фаллоидин (красный), DAPI (синий)) содержания альфа-актин в культивируемых контрольных фибробластах без сыворотки (- TGFβ), в фибробластах после воздействия TGFβ (+ TGFβ), TGFβ с ВВ-МСК (+ TGFβ + ВВ-МСК) и TGFβ с РФ-МСК (+ TGFβ + РФ-МСК).
На фиг. 5 представлены фотографии, иллюстрирующие способность ВВ-МСК, добавленных одновременно с TGFβ, предотвращать индуцированное TGFβ формирование фокальных контактов в фибробластах. Иммунофлуоресцентный анализ (винкулин (зеленый), фаллоидин (красный), DAPI (синий)) содержания винкулина в культивируемых контрольных фибробластах без сыворотки (- TGFβ), в фибробластах после воздействия TGFβ (+ TGFβ), TGFβ с ВВ-МСК (+ TGFβ + ВВ-МСК) и TGFβ с РФ-МСК (+ TGFβ + РФ-МСК).
На фиг. 6 представлены данные, иллюстрирующие способность ВВ-МСК, добавленных одновременно с TGFβ, предотвращать индуцированное TGFβ увеличение экспрессии коллагена I типа в дермальных фибробластах и уменьшать их контрактильную активность. Анализ экспрессии коллагена в культивируемых контрольных фибробластах без сыворотки (- TGFβ), в фибробластах после воздействия TGFβ (+ TGFβ), TGFβ с ВВ-МСК (+ TGFβ + ВВ-МСК) и TGFβ с РФ-МСК (+ TGFβ + РФ-МСК). Позициями на фигуре 6 обозначены: 1 - ОТ-ПЦР, коллаген I типа (n=9). Столбиками отмечены значения медиан по каждому фактору. Планками ограничиваются 25-е и 75-е процентили. 2 - Контракция коллагенового геля, график (n=3), данные отображены в виде среднего значения ± стандартное отклонение (SD). 3 - Контракция коллагенового геля, репрезентативные макрофотографии. Черный контур - граница лунки, красный - размер коллагенового диска. Над планками показан уровень значимости различий. Для сравнения групп применяли U-критерий Манна-Уитни.
На фиг. 7 представлены фотографии, иллюстрирующие способность ВВ-МСК, добавленных одновременно с TGFβ, предотвращать индуцированное TGFβ формирование стресс-фибрилл и увеличение экспрессии альфа-актина и коллагена I типа в фибробластах легких. А - Иммунофлуоресцентный анализ (альфа-актин (зеленый), фаллоидин (красный), DAPI (синий)) содержания альфа-актин в культивируемых контрольных фибробластах без сыворотки (- TGFβ), в фибробластах после воздействия TGFβ (+ TGFβ), TGFβ с ВВ-МСК (+ TGFβ + ВВ-МСК), TGFβ с РФ-МСК (+ TGFβ + РФ-МСК) и TGFβ с КС-МСК (+ TGFβ + КС-МСК). Б - ОТ-ПЦР, альфа-актин (n=3), данные отображены в виде среднего значения ± стандартное отклонение (SD). В - Б - ОТ-ПЦР, коллаген I типа (n=3), данные отображены в виде среднего значения ± стандартное отклонение (SD). Над планками показан уровень значимости различий. Для сравнения групп применяли U-критерий Манна-Уитни.
На фиг. 8 представлены данные, иллюстрирующие способность ВВ-МСК, добавленных к миофибробластам, стимулировать их дедифференцировку в фибробласты. Анализ экспрессии в культивируемых контрольных миофибробластах после добавления контрольной среды DMEM (TGFβ -> DMEM), в фибробластах после воздействия ВВ-МСК (TGFβ -> ВВ-МСК) и РФ-МСК (TGFβ -> РФ-МСК). Позициями на фигуре 8 обозначены: 1 - Вестерн-блоттинг, альфа-актин (n = 3), Столбиками отмечены значения медиан по каждому фактору. Планками ограничиваются 25-е и 75-е процентили. 2 - Имуноцитохимический анализ. Масштабный отрезок - 100 мкм. 3 - Контракция коллагенового геля, график (n=3), данные отображены в виде среднего значения ± стандартное отклонение (SD). 4 - Контракция коллагенового геля, репрезентативные макрофотографии. Черный контур - граница лунки, красный - размер коллагенового диска. Над планками показан уровень значимости различий. Для сравнения групп применяли U-критерий Манна-Уитни.
На фиг. 9 представлены данные, иллюстрирующие анализ профиля РНК в ВВ-МСК методом РНК секвенирования. Позициями на фигуре 9 обозначены 1 - Различные типы РНК, представленные в ВВ-МСК. Кластер миРНК отмечен красным овалом. 2 - Изменчивость представленности миРНК в донорских ВВ-МСК, полученных из жировой ткани, по диаграмме Венна. 3 - Наиболее распространенные миРНК в ВВ-МСК (топ-10). 4 - Представленность миРНК, ассоциированных с фиброзом, в ВВ-МСК на основе анализа их прогнозируемого гена-мишени.
На фиг. 10 представлены данные, иллюстрирующие, что внеклеточные везикулы стимулируют разрешение фиброза легких на модели индуцированного блеомицином фиброза легких у мышей. Анализ проводился в группах после добавления контрольной среды DMEM (DMEM) или введения ВВ-МСК через 1 день или две недели после введения блеомицина. Позициями на фигуре 10 обозначены 1 - Результаты клинического осмотра. 2 - Результаты исследования бронхоальвеолярного лаважа. 3. Результаты МРТ.
На фиг. 11 представлены фотографии, иллюстрирующие, что внеклеточные везикулы стимулируют разрешение фиброза легких на модели индуцированного блеомицином фиброза легких у мышей. Анализ проводился в группах после добавления контрольной среды DMEM (DMEM) или введения ВВ-МСК через 1 день или две недели после введения блеомицина. Позициями на фигуре 11 обозначены: 1 - введение через 1 день. 2 - введение через 14 дней. А - окрашивание по Ван-Гизону. Б - окрашивание по Верхгофу.
На фиг. 12 представлены фотографии, иллюстрирующие, что кондиционированная среда МСК стимулирует ранозаживление на модели глубокой кожной раны у мышей. Окрашивание гематоксилин-эозином. Анализ проводился в группах на 3 сутки после нанесения на рану препарата сравнения Левомиколь (А), контрольной среды DMEM (DMEM) (Б) или введения КС-МСК (В). На вставках отмечены: Г - Скопления фибробластов. Д - Начало ангиогенеза.
На фиг. 13 представлены фотографии, иллюстрирующие, что кондиционированная среда МСК стимулирует ранозаживление на модели глубокой кожной раны у мышей. Окрашивание гематоксилин-эозином. Анализ проводился в группах на 7 сутки после нанесения на рану препарата сравнения Левомиколь (А), контрольной среды DMEM (DMEM) (Б) или введения КС-МСК (В). На вставке отмечена: Г - Миграция фибробластов в область раны.
На фиг. 14 представлены фотографии, иллюстрирующие, что кондиционированная среда МСК стимулирует ранозаживление на модели глубокой кожной раны у мышей. Окрашивание гематоксилин-эозином. Анализ проводился в группах на 14 сутки после нанесения на рану препарата сравнения Левомиколь (А), контрольной среды DMEM (DMEM) (Б) или введения КС-МСК (В). На вставке отмечен: Г - Ангиогенез.
На фиг. 15 представлены фотографии, иллюстрирующие, что кондиционированная среда МСК стимулирует безрубцовое ранозаживление на модели глубокой кожной раны у мышей. Макрофотографии. Анализ проводился в группах на 21 сутки после нанесения на рану препарата сравнения Левомиколь (А), контрольной среды DMEM (DMEM) (Б) или введения КС-МСК (В).
На фиг. 16 представлены фотографии, иллюстрирующие, что кондиционированная среда МСК стимулирует безрубцовое ранозаживление и формирование дериватов кожи на модели глубокой кожной раны у мышей. Окрашивание гематоксилин-эозином. Анализ проводился в группах на 21 сутки после нанесения на рану препарата сравнения Левомиколь (А), контрольной среды DMEM (DMEM) (Б) или введения КС-МСК (В). На вставке отмечены: Г - Дериваты кожи.
Осуществление изобретения
Ниже представлено более подробное описание заявляемого изобретения. Настоящее изобретение может подвергаться различным изменениям и модификациям, понятным специалисту на основе прочтения данного описания. Такие изменения не ограничивают объем притязаний.
Пример 1. Получение МСК жировой ткани (МСК ЖТ) человека
МСК выделяют из подкожного жирового отложения здоровых доноров обоих полов. Клетки выделяют из материала, полученного при проведении малогоинвазивного хирургического вмешательства под местной анестезией или в ходе плановых хирургических операций. Хирургический материал (15 г жировой ткани, взятой из околопупочной области или другой области локализации подкожного жира) помещают в одноразовую пробирку с буфером HBSS (HyClone) содержащим 5-ти кратную концентрацию антибиотика пенициллина-стрептомицина 500 ед/мл (HyClone). В стерильных условиях культурального бокса биоптат фрагментируют до однородной массы, используя стерильные инструменты, после чего подвергают его ферментативной обработке в растворе, содержащем среду AdvanceSTEM (HyClone) /500 ед/мл антибиотика пенициллина-стрептомицина (HyClone), 200 ед/мл коллагеназы I типа и диспазы (40 ед/ml) (Worthington Biochemical) (соотношение объема ферментов и жира должно быть 1:1:1), при 37°С в течение 30-45 минут при постоянном помешивании. По окончании инкубации к образцу добавляют равный объем среды роста МСК и фильтруют через нейлоновые мембраны с размером пор 100 мкм (BD). Профильтрованную суспензию центрифугируют в течение 5 мин при 200g, после чего супернатант полностью удаляют. Осадок клеток подвергают обработке буфером для лизиса эритроцитов (BD) до покраснения раствора, после чего центрифугируют в течение 5 мин при 200g. Супернатант полностью удаляют, а осажденные клетки ресуспендируют в среде роста МСК. Для культивирования мезенхимных клеток используют среду AdvanceSTEM support expansion and maintenance of undifferentiated human MSCs (HyClone) в сочетании с добавлением 10% раствора добавок AdvanceSTEM Stem Cell Growth Supplement (HyClone) и 100 ед/мл антибиотика (HyClone). Эта среда была разработана фирмой-производителем (HyClone) для культивирования недифференцированных МСК, в частности клеток, происходящих из жировой ткани, без добавления сыворотки (http://www.thermo.com).
Выделенные ресуспендированные МСК высевают в концентрации 200 тыс. в мл в чашках Петри и культивируют в среде роста в инкубаторе при 37°C и при 5%-ой концентрации CO2. При достижении 80% монослоя МСК ЖТ клетки пассируют 1:4.
Пример 2. Получение кондиционированной среды МСК жировой ткани человека
Для получения кондиционированной среды МСК ЖТ наращивают до 2-5 пассажа. МСК ЖТ человека добавляют в количестве 5-15*103/см2 в культуральные емкости для выращивания эукариотических клеток, после прикрепления промывают культуральные сосуды с клетками солевым раствором Хэнкса (Панэко, Россия) (в количестве 0,1-0,2 мл/см2 трижды по 10 минут) и заполняют их свежей средой роста для кондиционирования в количестве 0,1-0,2 мл/см2. В качестве последней используют универсальную среду роста для разных типов клеток DMEM with Low Glucose (HyClone, USA), с добавлением раствора антибиотиков Penicillin-Streptomycin (HyClone, USA) (1,00±0,05 мл на 100±5 мл среды). Затем клетки культивируют в условиях СО2 инкубатора при 37+1°С, 5%-м содержании СО2 и относительной влажности ≥ 95% в течение 2 суток.
В качестве культуральных емкостей для выращивания эукариотических клеток используют культуральные флаконы или чашки Петри (фирмы Corning или аналогичные), при этом клетки выращивают на плоской подложке плотностью 5-15*103/см2.
Кондиционированную среду, содержащую все продукты секреции МСК ЖТ человека, собирают в стерильные емкости для центрифугирования, центрифугируют при 300 g (5000±10) об/мин, температуре (6±2)°С, в течение 10 минут для удаления клеточного дебриса. Полученный супернатант отбирают в новые стерильные емкости объемом 100 мкл - 50 мл.
Пример 3. Получение кондиционированной среды МСК жировой ткани человека, обогащенной фракцией внеклеточных везикул
Получение фракции кондиционированной среды, обогащенной внеклеточными везикулами, проводят с помощью системы фильтрации в тангенциальном потоке Minim II (Life Sciences), используя ультрафильтрационные кассеты (Minimate TFF capsule, PALL, США, 10 кДа) или аналогичные. Для этого питающий резервуар заполняют 100 мл кондиционированной среды. Производительность насоса устанавливают на уровне 90-120 мл/мин, давление не более 2 атмосфер, скорость потока фильтрата не более 20-30 мл/мин. Проводят 1 раунд очистки, восполняя объем добавлением раствора Хэнкса в питающий резервуар. После этого выключают насос, переносят возвращающий шланг в сосуд для сбора очищенного раствора, включают насос и дожидаются осушения питающего резервуара. Для вытеснения остатков очищенной среды в питающий резервуар добавляют раствор Хэнкса, включают насос и под визуальным контролем собирают очищенную среду до момента выхода из системы всего раствора.
Аналогом системы фильтрации в тангенциальном потоке Minim II (Life Sciences) также могут служить центриконы Amicon (10 кДа, 50 мл, Sigma, Италия) или их аналоги. Для очистки от низкомолекулярных компонентов кондиционированную среду переносят в верхний резервуар центрикона. После этого центрикон помещают в предварительно охлажденную центрифугу (6±2)°С и центрифугируют на скорости 3000 g ± 500 g 10-60 минут до тех пор, пока в верхнем резервуаре не останется минимальный объем среды (200±50 мкл). После этого концентрированную очищенную кондиционированную среду доводят до прежнего объема добавлением DMEM with Low Glucose (HyClone, USA), с добавлением раствора антибиотиков Penicillin-Streptomycin (HyClone, USA) (1,00±0,05 мл на 100±5 мл среды).
Для получения кондиционированной среды, обогащенной фракцией внеклеточных везикул, используют центриконы Amicon (1000 кДа, 50 мл, Sigma, Италия) или их аналоги. Для концентрирования очищенную кондиционированную среду переносят в верхний резервуар центрикона. После этого центрикон помещают в предварительно охлажденную центрифугу (6±2)°С и центрифугируют на скорости 3000 g ± 500 g 10-60 минут до тех пор, пока в верхнем резервуаре не останется минимальный объем среды (100±50 мкл). После этого концентрированную очищенную кондиционированную среду, обогащенную фракцией внеклеточных везикул, доводят до необходимого объема добавлением DMEM with Low Glucose (HyClone, USA), с добавлением раствора антибиотиков Penicillin-Streptomycin (HyClone, USA) (1,00±0,05 мл на 100±5 мл среды).
Пример 4. Методы оценки качества кондиционированной среды МСК, обогащенной внеклеточными везикулами
Оценку содержания внеклеточных везикул (ВВ) в концентрированной кондиционированной МСК жировой ткани, проводят следующими методами. Характеристика ВВ-МСК была выполнена с помощью метода, позволяющего анализировать траектории наночастиц (Nanoparticle tracking analysis, NTA, см. ниже п.1), просвечивающей электронной микроскопии (ПЭM, см. ниже п.2) и вестерн-блот-анализа (см. ниже п.3). Так, по результатам анализа ВВ, выделенные с помощью ультрафильтрации, демонстрировали круглую или чашеобразную форму со средним диаметром около 114 нм (диапазон размеров от 10 до 490 нм). Количество частиц составляет не менее 3,12±0.5×109 частиц/мл неконцентрированной КС-МСК и не менее 1,53±0,2×1010 частиц/мл 5-кратно сконцентрированной КС-МСК. Вестерн-блот анализ экзосомальных маркеров показал, что образцы были положительными для типичных экзосомальных маркеров, включая HSP70, CD9, CD81 и CD63 (Фиг. 1).
1. Анализ траектории наночастиц (NTA)
Для определения размера и формы частиц, содержащихся в кондиционированной среды МСК, обогащенной внеклеточными везикулами, использовали метод анализа траектории наночастиц, применяя прибор Nanosight LM10 (Nanosight Ltd., Великобритания) или аналогичный.
Определение характеристик ВВ с помощью NTA было выполнено с помощью Nanosight LM10 (Nanosight Ltd., Великобритания), оснащенного лазером с длиной волны 405 нм, 65 мВт с пассивным считыванием температуры и высокочувствительной камерой Andor Luca типа EMCCD. Все измерения были выполнены в соответствии с рекомендациями стандарта ASTM E2834-12 [ASTM E2834-12(2018), Standard Guide for Measurement of Particle Size Distribution of Nanomaterials in Suspension by Nanoparticle Tracking Analysis (NTA); ASTM International: West Conshohocken, PA, USA, 2018, doi:10.1520/E2834-12R18] с использованием протокола [Silachev, D.N.; Goryunov, K.V.; Shpilyuk, M.A.; Beznoschenko, O.S.; Morozova, N.Y.; Kraevaya, E.E.; Popkov, V.A.; Pevzner, I.B.; Zorova, L.D.; Evtushenko, E.A.; et al. Effect of MSCs and MSC-Derived Extracellular Vesicles on Human Blood Coagulation. Cells 2019, 8, 258, doi:10.3390/cells8030258], оптимизированного для ВВ для конкретной конфигурации прибора Nanosight. Из-за слабого флуоресцентного фона КС-МСК были сделаны незначительные корректировки нижнего и более высокого порогов (910 и 10920 вместо 715 и 10725 соответственно).
Поскольку ВВ не являются единственными частицами, которые могут быть детектированы с помощью NTA даже в бессывороточной кондиционированной среде, с помощью NTA были проанализированы два типа образцов: аликвоты КС-МСК после 30 мин инкубации со свежей бессывороточной средой (DMEM LG) и в последующие 48 ч инкубации. Образец после 30 мин инкубации с клетками служил контролем случайных частиц в среде перед высвобождением ВВ. Были проанализированы как неконцентрированные, так и концентрированные образцы КС-МСК.
Измерения каждого образца проводили в 16-20 повторах для достижения суммарного количества измеренных траекторий не менее 5000 шт. Размеры и концентрации частиц из индивидуальных измерений суммировали в единую таблицу, для которой строили гистограмму распределения частиц по размерам с шагом 20 нм и рассчитывали средний размер и общую концентрацию всех частиц. Доверительные интервалы измерения среднего размера и концентрации рассчитывали из значений для индивидуальных измерений, используя статистику Стьюдента с 95% двухсторонней вероятностью (Гланц С. Медико-биологическая статистика. - М.: Практика, 1998. - 459 с.)
2. Просвечивающая электронная микроскопия (ПЭМ)
Для определения размера и формы частиц, содержащихся в кондиционированной среде МСК, обогащенной внеклеточными везикулами, использовали метод просвечивающей электронной микроскопии, применяя ПЭМ JEOL JEM-1011 с цифровой камерой ORIUS SC1000W или аналоги. Получение изображений ПЭМ проводили для ВВ-МСК, нанесенных на сетки с углеродным покрытием, обработанные тлеющим разрядом в Emitech K100X в воздушной атмосфере и окрашенные 1% раствором уранилацетата дважды в течение 30 с. Изображения получали при 80 кВ с помощью ПЭМ JEOL JEM-1011 с цифровой камерой ORIUS SC1000W.
3. Вестерн-блоттинг
Анализ белковых маркеров, характерных для внеклеточных везикул, проводили с помощью метода вестерн-блоттинга, используя набор антител для детекциии соответствующих белков-маркеров (HSP70, CD81, CD63, CD9; EXOAB-KIT-1, System Biosciences, США) или аналогичный. Для этого осадок ВВ лизировали в буфере Лэмли. Количество белка в лизате определяли с помощью метода анализа белка амидовым черным. Пробы подвергали электрофорезу в геле SDS-PAGE и переносили на мембрану PVDF. Мембрану инкубировали с первичными антителами к маркерам внеклеточных везикул (HSP70, CD81, CD63, CD9; EXOAB-KIT-1, System Biosciences, США) в течение ночи при 4°C. После промывания в TBST блоты инкубировали с вторичными антителами, меченными пероксидазой (HRP) (P-RAM Iss, P-RAQ Iss, Имтэк, Россия), в течение 1 часа. Меченые белки визуализировали с помощью системы визуализации ChemiDocTM Touch (Bio-Rad Laboratories, США) с использованием набора для усиленной хемилюминесценции (ECL) (Pierce, США).
Пример 5. Метод оценки поглощения частиц кондиционированной среды МСК, обогащенной внеклеточными везикулами, фибробластами in vitro
Для того, чтобы выяснить, могут ли ВВ-МСК поглощаться исследуемыми клетками, использовали внеклеточные везикулы, в которые был загружен по методике, описанной ниже, флуоресцентный олигонуклеотид, представляющий собой короткую нуклеотидную последовательность (14-22 пар оснований), соединенных с флуоресцентным красителем. Такие внеклеточные везикулы добавляли к фибробластам кожи человека, мембраны которых были мечены с помощью липофильного красителя pkh26 (Sigma) (Basalova et al., 2020). Через 48 часов смотрели накопление частиц в клетках с помощью широкопольной и конфокальной микроскопии.
Так, через 12 часов в клетках начинают появляться отдельные зеленые флуоресцентные скопления, а через 24-48 часов инкубирования клеток с ВВ-МСК методом широкопольной микроскопии было показано, что большинство клеток (78±7%) накапливают внеклеточные везикулы в периядерной зоне.
Для того, чтобы убедиться, что ВВ действительно поглощаются клетками, а не налипают на поверхность мембраны, клеточная культура была проанализирована через 48 часов с помощью конфокальной микроскопии. Было показано, что сигнал от внеклеточных везикул действительно локализуется в периядерной зоне под клеточной мембраной, что говорит о способности клеточной культуры фибробластов захватывать ВВ (Фиг. 2).
Трансфекция ВВ-МСК мечеными олигонуклеотидами
Трансфекцию ВВ-МСК проводили с использованием Exo-Fect™ Exosome Transfection Kit (EXFT20A-1, System Biosciences) или аналогичного. Использовали протокол, описанный в инструкции производителя. Для детекции поглощения ВВ-МСК клетками-мишенями трансфицировали ВВ-МСК с FAM-меченым мимиком (флуоресцеином) (miRCURY LNA miRNA mimic negative control (YM00479902-ADB), Qiagen). Для этого в стерильных условиях ламинарного бокса смешивали 10 мкл Exo-Fect solution, 20 мкл FAM-меченого мимика (20 пикомоль), 70 мкл стерильного ФБС, 50 мкл концентрированной суспензии ВВ-МСК. Полученную смесь перемешивали переворачиванием пробирки три раза, инкубировали при 37°С в течение 10 мин, а затем реакцию останавливали, перемещая пробирку в лед и добавляя полимер ExoQuickTC в объеме 30 мкл. Перемешивали полученную смесь переворачиванием пробирки 6 раз. После дальнейшей инкубации при 4°С в течение 30 мин с полимером трансфицированные ВВ-МСК центрифугировали при 13000 об/мин в течение 10 минут и растворяли в DMEM LG (Gibco) с добавлением 1% пенициллин-стрептомицина (Gibco) до концентрации 5× и добавляли к исследуемым клеткам.
Поглощение ВВ-МСК, трансфицированных FAM-меченным олигонуклеотидам (Qiagen), фибробластами, меченным PKH26 (PKH26GL, Sigma), через 4, 8, 24 и 48 часов оценивали с помощью широкопольной и конфокальной микроскопии (Leica TCS SP5). Дермальные фибробласты после инкубации с немеченым ВВ-МСК использовали в качестве отрицательного контроля.
Мечение культуры клеток PKH26GL
Культуру клеток дермальных фибробластов человека промывали два раза раствором Хэнкса в течение 5 минут и фиксировали в 4% параформальдегиде на ФСБ в течение 7 минут в условиях тяги.
Отбирали в чистую полипропиленовую пробирку 2 мл Дилюэнта С (CGLDIL, Sigma, США) и немедленно добавляли 4 мкл раствора PKH26 (P9691, Sigma, США), перемешивали смесь на вортексе в течение 10 сек. Полученный раствор добавляли к зафиксированным клеткам в объеме, достаточном для закрывания поверхности. Инкубировали 1-5 минут. После инкубации удаляли раствор PKH26 и добавляли 1% раствор БСА на ФСБ на 1 минуту для ингибирования реакции. Удаляли раствор БСА и затем добавляли ФСБ для дальнейшего микроскопирования.
Пример 6. Методы оценки способности кондиционированной среды МСК, обогащенной внеклеточными везикулами, подавлять дифференцировку фибробластов в миофибробласты и вызывать дедифференцировку миофибробластов в фибробласты in vitro
Чтобы изучить способность внеклеточных везикул МСК (ВВ-МСК) влиять на дифференцировку фибробластов в миофибробласты, выделяли фракцию, обогащенную ВВ, из кондиционированной среды МСК (КС-МСК) и оценивали ее влияние на ранее разработанную in vitro модель TGFbeta - индуцированной дифференцировки дермальных фибробластов (ДФ) в бессывороточных условиях (Basalova et al., 2020).
Известно, что одним из ключевых признаков дифференцировки фибробластов в миофибробласты является увеличение экспрессии гладкомышечного альфа-актина и встраивание его в стресс-фибриллы. Как было показано ранее, добавление только TGFbeta вызывало повышение синтеза альфа-актина и его включение в микрофиламенты, что способствовало приобретению фенотипа миофибробластов этими клетками. Однако добавление к клеткам ВВ-МСК предотвращало увеличение мРНК альфа-актина в ДФ, вызванное TGFbeta. Более того, применение фракции ВВ-МСК привело к снижению мРНК альфа-актин ниже уровня, наблюдаемого в группе отрицательного контроля (0,6±0,05, р<0,05). Добавление фракции растворимых факторов секретома МСК (РФ-МСК) также приводило к значимому снижению экспрессии мРНК альфа-актина (0,8±0,03, р<0,05)
Внесение TGFbeta повышает уровень белка альфа-актина более чем в 2 раза в ДФ по сравнению с группой отрицательного контроля (2,9±0,1 против 1,13±0,03, р<0,05). Тогда как добавление РФ-МСК или ВВ-МСК вызывало уменьшение уровня экспрессии данного белка (0,4±0,13 и 0.25±0.15 против 1,13±0,03, р<0,05) даже ниже уровня, наблюдаемого в контрольных клетках (Фиг. 3).
Следует отметить, что добавление в культуру РФ-МСК, ВВ-МСК предотвращало также морфологические изменения ДФ, вызванные TGFbeta. Так, TGFbeta способствовал формированию стресс-фибрилл и включению в их состав альфа-актина. Одновременное добавление вместе с TGFbeta фракции, обогащенной ВВ-МСК, ингибировало образование стресс-фибрилл и встраивание в них альфа-актина (Фиг. 4).
Другим важным признаком сократительного фенотипа миофибробластов является наличие большого количества фокальных контактов. Инкубация клеток с TGFβ вызывает частичное внутриклеточное перераспределение винкулина и его локализацию в зоне фокальных контактов. В клетках, которым одновременно с TGFβ добавляли фракции КС-МСК, как содержащую растворимые факторы, так и фракцию, обогащенную внеклеточными везикулами, перераспределения винкулина не происходило и этот белок был преимущественно локализован в околоядерной зоне. Такое внутриклеточное распределение винкулина наблюдалось и в клетках, не обработанных TGF-β (Фиг. 5).
Для проверки гипотезы о том, что факторы, содержащиеся в кондиционированной среде МСК, могут влиять на дифференцировку фибробластов, были использованы in vitro тесты, отражающие функциональную активность миофибробластов - способность к гиперпродукции внеклеточного матрикса и его контракции.
Было проанализировано влияние секретома МСК на экспрессию коллагена I типа миофибробластами. Было показано, что добавление фракции КС-МСК, содержащей растворимые факторы, так и фракции, обогащенной внеклеточными везикулами, вызывало тенденцию к уменьшению содержания мРНК коллагена I типа (Фиг. 6).
Также оценили влияние фракций КС-МСК на способность миофибробластов к контракции коллагенового геля. Было показано, что миофибробласты, дифференцировка которых была индуцирована с помощью добавления TGFβ, сокращали коллагеновый гель более чем в 4 раза по сравнению с контрольными клетками (сократительная активность 87.7±1.4% против 48.3±14.6%, p<0.05). Напротив, клетки, которым одновременно с TGFβ добавляли фракции КС-МСК, обладали сниженной способностью сокращать коллагеновый гель (37.1±7.7% для ВВ-МСК и 23.1±4.1% для РФ-МСК, p<0.05) (Фиг. 6).
Таким образом, полученные данные указывают на то, что компоненты секретома МСК, как внеклеточные везикулы, так и растворимые факторы, способны подавлять функциональную активность миофибробластов.
На модели дифференцировки легочных фибробластов при сравнении фракций КС-МСК, обогащенных ВВ, РФ, или обеими фракциями вместе было показано, что добавление к клеткам ВВ-МСК предотвращало увеличение мРНК альфа-актина в фибробластах легких, вызванное TGFbeta, снижая его количество в 4,3 раза по сравнению с группой положительного контроля. Добавление фракции РФ-МСК также приводило к значимому снижению экспрессии мРНК альфа-актина в 1,5 раз. Самым эффективным для ингибирования дифференцировки оказалось добавление одновременно с TGFbeta фракции, содержащей два типа компонентов - ВВ-МСК и РФ-МСК; при добавлении данных компонентов экспрессия мРНК снижалась в 20,9 раз по сравнению с группой положительного контроля. Аналогичные результаты получены при оценке экспрессии мРНК коллагена первого типа (Фиг. 7).
Одним из негативных последствий фибропролиферативных заболеваний является накопление клеток с морфологией и функцией фибробластов. Для эффективной терапии необходимо найти способ, вызывающий дедифференцировку миофибробластов.
С помощью иммуноблоттинга установили, что добавление миофибробластам фракций КС-МСК, как содержащей растворимые факторы, так и фракции, обогащенной внеклеточными везикулами, вызывало уменьшение содержания альфа-актина в клетках более чем в 2 раза по сравнению с дифференцированными миофибробластами.
С помощью иммунофлуоресцентного окрашивания установлено, что добавление миофибробластам фракции КС-МСК, содержащей растворимые факторы, так и фракции, обогащенной внеклеточными везикулами, вызывало уменьшение встраивания α-актина в стресс-фибриллы.
Добавление фракций КС-МСК также вызывало снижение способности миофибробластов сжимать коллагеновый гель. При этом наиболее выраженным эффектом обладала фракция внеклеточных везикул (сократительная активность 18±9% для ВВ-МСК и 78±6% для РФ-МСК против 98±3% для контрольных клеток). Таким образом, секретом МСК может быть использован для реверсии фибротических процессов (Фиг. 8).
Индукция дифференцировки фибробластов in vitro
Для создания модели фиброза in vitro, использовали модель индукции дифференцировки фибробластов кожи человека, фибробластов легких человека, фибробластов легких мыши в миофибробласты с помощью добавления в среду культивирования 5 нг/мл TGFβ (R&D). Для этого в лунку 24-луночного планшета высаживали фибробласты кожи человека 3-10 пассажей из расчета 2×105 клеток/лунка. Через стуки культивирования клетки депривировали в среде DMEM LG (Gibco) с содержанием 1% HyClone Penicillin-Streptomycin 100X Solution (HyClone) в течение ночи. После депривации меняли в клетках среду на фракцию, обогащенную ВВ-МСК или РФ-МСК (500 мкл на лунку). В качестве индуктора дифференцировки одновременно добавляли 5 нг/мл TGFbeta (R&D, США). DMEM LG без ФБС и без TGFbeta использовали в качестве отрицательного контроля (группа «-TGFbeta»); DMEM LG без ФБС с 5 нг/мл TGFbeta использовали в качестве положительного контроля (группа «+TGFbeta»). Клетки помещали в СО2-инкубатор при 37°С и анализировали через 4 дня.
Для создания модели дедифференцировки миофибробластов в лунку 24-луночного планшета высаживали фибробласты кожи человека 3-10 пассажей из расчета 2×105 клеток/лунка. Через стуки культивирования клетки депривировали в среде DMEM LG (Gibco) с содержанием 1% HyClone Penicillin-Streptomycin 100X Solution (HyClone) в течение ночи. После депривации меняли в клетках среду на DMEM LG с добавлением 5 нг/мл TGFbeta (R&D, США). После 4 суток инкубации в культуре меняли среду на фракцию, обогащенную ВВ-МСК или РФ-МСК (500 мкл на лунку). DMEM LG без ФБС и без TGFbeta использовали в качестве контроля (группа «-TGFbeta») Клетки помещали в СО2-инкубатор при 37°С и анализировали через 3-4 дня.
Иммуноцитохимическое исследование клеточных культур
Клетки фиксировали 4% параформальдегидом на фосфатно-солевом буфере (ФСБ) в течение 15 минут при комнатной температуре и пермеабилизовали 0,1% Triton X-100 в течение 10 минут при комнатной температуре. После блокирования неспецифического связывания с 10% нормальной козьей сывороткой на 1% БСА (Abcam, Великобритания) клетки инкубировали с антителами к α-альфа-гладкомышечному актину (ab32575; Abcam), винкулин (Sigma, V4139), кроличьими IgG (NSC-2025; Santa Cruz Biotechnology, США) или Alexa 594-фаллоидину (А12381; Molecular probe, США) в течение ночи при 4°С. Детекцию антител проводили с использованием вторичных антител, конъюгированных с Alexa 488 (A11037; Invitrogen, CША), в течение 1 часа при комнатной температуре в темноте. Ядра были окрашены DAPI (D9542, Sigma). Изображения получали с использованием инвертированного микроскопа с флуоресцентным модулем и камерой (Leica DMi8, камера Leica DFC 7000 T, Leica Microsystems GmbH, Германия) и обрабатывали с помощью программного обеспечения FIJI (GitHub Inc., США).
In vitro модель сокращения коллагенового геля
Для выполнения этой модели использовали протокол, описанный в работе Ngo (Ngo et al. 2006).
Фибробласты кожи человека 3-10 пассажей, достигшие ≈80% конфлюэнтности промывали раствором Версена (ПанЭко) и обрабатывали раствором 0,25% трипсина и 0,02% ЭДТА (Gibco) для того, чтобы клетки открепились от пластика. После открепления определяли необходимую концентрацию клеточной суспензии методом подсчета в камере Горяева и осаждали необходимое количество из суспензии методом центрифугирования в культуральной среде, не содержащей ростовых добавок. К осажденным клеткам (80 тыс кл/лунка) добавляли 400 мкл исследуемого вещества и 5 нг/мл TGFβ (R&D). В качестве отрицательного контроля использовали DMEM (Gibco), положительного DMEM (Gibco) с добавлением 5 нг/мл TGFβ (R&D). Далее к полученной суспензии добавляли 0,2 мл коллагена (3мг/мл на 0,1% уксусной кислоте, Имтек) и быстро вносили 4-5 мкл 1М NaOH для выравнивания уровня рН. Быстро переносили cуспензию в лунку 24-луночного планшета и аккуратно наносили. Затем оставляли гель на комнатной температуре на 20-30 мин для полимеризации, после чего добавляли культуральную среду DMEM (Gibcо) в количестве 500 мкл и аккуратно открепляли гель от краев лунки для инициации контракции. Далее планшет помещали в инкубатор на 37°С и 5%-ной концентрации СО2. Изменение диаметра диска оценивали через 24 часа визуально, репрезентативные фотографии дисков были получены при помощи использования камеры мобильного устройства. Площадь лунки и диска измерялась в программе ImageJ. Размер площади диска нормировался на размер площади дна лунки.
Иммуноблоттинг
ДФ или осадок ВВ лизировали в буфере Лэмли. Количество белка в лизате определяли с помощью метода анализа бычьего сывороточного альбумина (BSA), подвергали электрофорезу в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE) и переносили на поливинилиденфторидную мембрану (PVDF). Мембрану инкубировали с первичными антителами к альфа-актину (a-SMA) (ab32575, Abcam), коллагену I типа (ab34710, Abcam), Bcl2 (sc-509, Santa Cruz Biotechnology), MMP2 (ab97779, Abcam), винкулину (V4139, Sigma) в течение ночи при 4°C. После промывания в Твин буфере для переноса с добавлением 0,05% Tween-20 (TBST) блоты инкубировали с вторичными антителами, меченными пероксидазой (HRP) (P-RAM Iss, P-RAQ Iss, Имтэк, Россия), в течение 1 часа. Меченые белки визуализировали с помощью системы визуализации ChemiDocTM Touch (Bio-Rad Laboratories, США) с использованием набора для усиленной хемилюминесценции (ECL) (Pierce, США).
Выделение РНК
Тотальную РНК выделяли из культивируемых фибробластов с помощью набора miRNeasy Mini Kit (Qiagen) согласно инструкции, прилагаемой к набору. Для этого лунку с культивируемыми клетками промывали 2 раза ФСБ по 2 мл по 1-2 минуты, и затем растворяли клетки в 350 мкл лизирующего раствора (RLT, Qiagen) и инкубации при комнатной температуре в течение 5 мин. Затем к раствору клеток добавляли 1,5 объема 96% этанола по отношению к исследуемому образцу, перемешивали и наносили на колонку с сорбирующей мембраной. Нуклеиновые кислоты осаждали на колонке с помощью центрифугирования при 8000g в течение 15 с. Далее удаляли геномную ДНК с помощью не содержащей РНКаз ДНКазы I (РНКse-Free DNase Set, Qiagen). Для этого наносили 80 мкл раствора ДНКазы I в буфере RDD из набора и инкубировали в течение 15 мин при КТ. После этого колонку промывали 700 мкл буфера RWT из набора с помощью центрифугирования при 8000g в течение 15 с при комнатной температуре. Далее колонку дважды промывали 500 мкл буфера RPE из набора с помощью центрифугирования при 8000g в первый раз в течение 15 с, а во второй - 2 мин. Затем колонку переносили в новую центрифужную пробирку и осушали остатки буферного раствора с помощью центрифугирования при 12000g в течение 1 мин. Высушенную колонку переносили в новую центрифужную пробирку и элюировали РНК в 30-50 мкл деионизованной стерильной, не содержащей РНКаз воды с помощью центрифугирования при 8000g в течение 1мин. Концентрацию выделенной тотальной РНК определяли на спектрофотометре NanoDrop 1000 (Thermo Scientific, США) с использованием программного обеспечения ND-1000 V 3.7.1 (Thermo Scientific, США). Также с использованием спектрофотометра NanoDrop 1000 осуществляли контроль качества выделенной РНК. Для этого анализировали показатели отношений значений поглощения при длинах волн 260 нм и 280 нм, а также при длинах волн 260 нм и 230 нм. Для последующей процедуры обратной транскрипции отбирали образцы РНК со следующими показателями: 260 нм / 280 нм = 2, 260 нм / 230 нм = 1,8-2,2.
ПЦР в реальном времени
Для определения содержания мРНК гладкомышечного актина и коллагена проводили синтез кДНК с использованием набора MMLV RT (Евроген, Россия) согласно руководству пользователя, приложенному к набору. Для этого собирали смесь, содержащую 1-6 мкл РНК-матрицы (концентрация РНК 0.5-2 мкг), 1-3 мкл праймера и 0-7 мкл стерильной, свободной от РНКаз воды. Аккуратно перемешивали смесь, центрифугировали. Прогревали смесь в течение 2 мин при 70°C и помещали пробирки на лед. После этого добавляли 11 мкл предварительно подготовленной смеси 0-2 мкл стерильной воды, свободной от РНКаз, 4 мкл 5х буфера для синтеза первой цепи, 2 мкл смеси dNTP (10 мМ каждого), 2 мкл DTT (20 мМ), 1-3 мкл MMLV ревертазы. Аккуратно перемешивали смесь, центрифугировали. Инкубировали реакционную смесь 30-60 мин при 37-42°C, затем при 70°C в течение 10 мин. Реакцию проводили в ПЦР - амплификаторе с горячей крышкой Nexus Mastercycler® gradient (Eppendorf, Германия). Все манипуляции осуществляли в перчатках и под ламинаром во избежание контаминации. Полученную кДНК затем хранили при -20°С.
ПЦР в реальном времени проводили с использованием готовой реакционной смеси, содержащей ДНК-полимеразу, интеркалирующий краситель SYBR Green I и референсный краситель ROX (Евроген) в соответствии с протоколами производителя на приборе QuantStudio™ 5 Real-Time PCR System (Applied Biosystems, США). В одну ПЦР реакцию добавляли 5 мкл qPCRmix-HS SYBR+LowROX (Евроген), 9 мкл стерильной воды, 1 мкл смеси праймеров (концентрация прямого и обратного праймера в смеси по 5 мкМ) и 10 мкл кДНК до конечной концентрации 50 нг кДНК на реакцию. Для контроля неспецифического отжига праймеров (non template control, NTC) вместо кДНК в реакцию добавляли 10 мкл стерильной воды.
Режим ПЦР: 95°С в течение 5 мин, затем 40 циклов 95°С - 20 сек, n°С - 20 сек (где n - температура, эмпирически подобранная для каждой пары праймеров), 70°С - 20 сек. Праймеры подбирали с помощью базы олигонуклеотидных последовательностей PrimerBank (http://pga.mgh.harvard.edu/primerbank/) либо с помощью инструмента Primer-BLAST (http://www.ncbi.nlm.nih.gov/tools/primer-blast/).
В качестве праймеров использовали уникальные комплементарные пары олигодезоксинуклеотидов к анализируемым генам с последовательностями (SEQ ID NO 62 - SEQ ID NO 67), синтез которых осуществляли с помощью стандартной технологии и оборудования, применяемых для решения подобных задач в генной инженерии [Sambrook J et al., Molecular Cloning - A laboratory Manual, Cold Spring Harbor Laboratory Press, New York, (1989)], [Watson, J.D., Oilman, M., Witkowski, J., Zoller, M. Recombinant DNA, Scientific American Books, New York, 1992].
Последовательности праймеров:
Коллаген I типа типа (Col1A1) (SEQ ID NO 62): CCCAGCCACAAAGAGTCTACA,
обр. (SEQ ID NO 63) GTTTCCACACGTCTCGGTCA
Гладкомышечный актин (ACTA2) (SEQ ID NO 64): CAATGAGCTTCGTGTTGCCC,
обр. (SEQ ID NO 65) TCTCCAGAGTCCAGCACGAT
60S кислый рибосомный белок P0 (RPLP0) (SEQ ID NO 66): GCTGCTGCCCGTGCTGGTG
обр. (SEQ ID NO 67) TGGTGCCCCTGGAGATTTTAGTGG
Содержание исследуемых мРНК нормировали по уровню сигнала, получаемого для кДНК RPLP0 (ген кислого рибосомального белка «домашнего хозяйства»). После проведения ПЦР с детекцией в режиме реального времени полученные данные по значениям порогового цикла для каждого гена обрабатывали согласно формуле:
N = 2^(-ΔCt), ΔСt = Сt1-Сthk, где Сt1 - значение порогового цикла для исследуемого гена, Сthk- значение порогового цикла гена «домашнего хозяйства» (housekeeping genes, RPLP0), N - результат в относительных единицах.
Пример 7. Способ оценки содержания некодирующих РНК в кондиционированной среде МСК, обогащенной внеклеточными везикулами
Используя высокопроизводительное секвенирование РНК (RNA-seq), было обнаружено, что несколько классов РНК представлены в ВВ-hTERT-МСК. Используя кластеризацию генов KEGG, было обнаружено, что наиболее репрезентативные 3000 генов, обнаруженных в ВВ-МСК, включают кластеры, связанные с фокальной адгезией (79 генов), формированием ВКМ (только 27 коллагенов, представленных 27 генами) и взаимодействием рецепторов с ВКМ (39 генов), сигнальным путем PI3K-Akt (90 генов), сигнальным путем TGFbeta (17) и другими процессами, участвующими в регуляции фиброза.
Среди некодирующих РНК одним из наиболее представленных и аннотированных классов были микроРНК (миРНК). Из 2652 миРНК 270 были обнаружены в ВВ-МСК. Большинство из них были также обнаружены в ВВ, секретируемых МСК из жировой ткани здоровых доноров. Однако наблюдалась некоторая изменчивость между донорами; таким образом, только 170 миРНК были представлены во всех трех биологических повторностях. Наиболее распространенные миРНК в ВВ-МСК представлены на Фиг. 9, включая миРНК-21, миРНК-155, миРНК-92a и другие с установленными специфическими генами-мишенями, вовлеченными в развитие фиброза. По результатам кластерного анализа было показано, что среди мишеней обнаруженных миРНК было несколько факторов, связанных с фиброзом. Большинство генов вносят значительный вклад в специфические процессы, связанные с развитием фиброза, такие как ремоделирование ВКМ, сигнальные пути Wnt, PDGF и TGFbeta. Аналогичные результаты были получены при анализе общих мишеней 170 миРНК, совпадающих между тремя донорами МСК: 117 генов были связаны с фиброзом, 63 гена с передачей сигналов TGFbeta и 76 генов с образованием и ремоделированием ВКМ (Фиг.9).
Метод высокопроизводительного секвенирования РНК
РНК из ВВ, секретируемых hTERT МСК и первичными МСК (число доноров n = 3), выделяли с использованием miRNeasy Mini Kit (Qiagen) в соответствии с инструкциями производителя. Количество и чистоту выделенной РНК определяли на спектрофотометре Nanodrop (Thermo Scientific) по соотношению 260/230 нм. Были построены и проанализированы библиотеки для массового параллельного секвенирования для анализа миРНК (Illumina, США). Перед анализом данных RNA-seq последовательности адаптеров для SNA / Illumina 1.9 / TruSeq Small RNA сначала удаляли с использованием программы cutadapt-1.16, затем проводили дополнительную очистку с использованием программы Trimmomatic-0.38. Контроль качества проводили с помощью программы FastQC.
Анализ RNA-seq массива миРНК был выполнен с использованием программы sRNAtoolbox (параметры: miRNAs: miRBase v22; ncRNA: (Ensembl release 91 (ncRNA)); length of the seed: 20; количество допустимых несовпадений: 2; оценка phred: 20). миРНК, связанные с развитием фиброза и их представленность в ВВ-МСК были оценены при использовании баз данных TargetScan 7.2, HMDD, miR2Disease, miRwayDB. Предсказанию функций мРНК способствовало использование баз Gene Ontology (GO) и Kyoto Encyclopedia of Genes and Genomes (KEGG). Кластеризация генов GO и KEGG была выполнена с использованием ресурса David 6.8. Контроль качества, картирование и нормализация данных RNA-seq массива мРНК были выполнены с помощью сервиса BrowserGenome 1.0 (геном hg38 GENCODE 22). Анализ ключевых слов проводился с использованием сценариев с использованием следующих команд: while read line; grep; awk sed; sort (uniq). Общие прогнозируемые мишени микроРНК анализировались с использованием сервиса miRNet.
Необработанные данные доступны как PRJNA592301 (ncbi / sra).
Пример 8. Способ оценки микроРНК, ассоциированных с фиброзом, в кондиционированной среде МСК, обогащенной внеклеточными везикулами
С помощью метода ПЦР в реальном времени на основные миРНК, ассоциированные с фиброзом, было показано, что в составе ВВ-МСК на детектируемом ПЦР в реальном времени уровне экспрессируются 60 из 84 исследованных миРНК, ассоциированных с фиброзом. Только в ВВ, секретированных первичными МСК, экспрессируются 12 миРНК, только в ВВ, секретированных иммортализованными линейными МСК (hTERT-МСК) -2. Не экспрессируются ни в одном из изученных типов клеток 10 миРНК. Более подробный список миРНК представлен в таблице ниже (Табл. 1).
Таблица 1. Список участвующих в регуляции фиброза микроРНК, выявленных методом РНК секвенирования и валидированных методом ПЦР в реальном времени, которые представлены в ВВ, секретируемых МСК человека
Выделение РНК, обогащенной миРНК
Тотальную РНК, обогащенную миРНК, выделяли из кондиционированной среды МСК, обогащенной внеклеточными везикулами, с помощью набора miRNeasy Mini Kit (Qiagen) согласно инструкции, прилагаемой к набору. Для этого кондиционированную среду МСК, обогащенную внеклеточными везикулами, концентрировали согласно примеру 3 и растворяли в 700 мкл лизирующего раствора (QIAzol Lysis Reagent, Qiagen) с помощью интенсивного встряхивания на вортексе в течение 1 мин и инкубации при комнатной температуре в течение 5 мин. После этого лизаты ресуспендировали через инсулиновый шприц 5 раз, согласно протоколу производителя. Затем к лизату везикул добавляли 140 мкл хлороформа, перемешивали с помощью интенсивного встряхивания на вортексе в течение 15 с и инкубировали при комнатной температуре в течение 3 мин. По окончании инкубации отделяли водорастворимую фракцию объемом 350±50 мкл с помощью центрифугирования при 12000g в течение 15 мин при 4°С и переносили ее в новую центрифужную пробирку. Водорастворимую фракцию перемешивали с 1,5 объемами 96% этанола относительно объема исследуемого образца и наносили на колонку с сорбирующей мембраной из набора. Нуклеиновые кислоты осаждали на колонке с помощью центрифугирования при 8000g в течение 15 с. Далее удаляли геномную ДНК с помощью не содержащей РНКаз ДНКазы I (РНКse-Free DNase Set, Qiagen). Для этого наносили 80 мкл раствора ДНКазы I в буфере RDD из набора и инкубировали в течение 15 мин при КТ. После этого колонку промывали 700 мкл буфера RWT из набора с помощью центрифугирования при 8000g в течение 15 с при комнатной температуре. Далее колонку дважды промывали 500 мкл буфера RPE из набора с помощью центрифугирования при 8000g в первый раз в течение 15 с, а во второй - 2 мин. Затем колонку переносили в новую центрифужную пробирку и осушали остатки буферного раствора с помощью центрифугирования при 12000g в течение 1 мин. Высушенную колонку переносили в новую центрифужную пробирку и элюировали РНК в 30-50 мкл деионизованной стерильной, не содержащей РНКаз воды с помощью центрифугирования при 8000g в течение 1 мин. Концентрацию выделенной тотальной РНК определяли на спектрофотометре NanoDrop 1000 (Thermo Scientific, США) с использованием программного обеспечения ND-1000 V 3.7.1 (Thermo Scientific, США). Также с использованием спектрофотометра NanoDrop 1000 осуществляли контроль качества выделенной РНК. Для этого анализировали показатели отношений значений поглощения при длинах волн 260 нм и 280 нм, а также при длинах волн 260 нм и 230 нм. Для последующей процедуры обратной транскрипции отбирали образцы РНК со следующими показателями: 260 нм / 280 нм = 2, 260 нм / 230 нм = 1,8-2,2.
Обратная транскрипция
Обратную транскрипцию выполняли с использованием miScript II RT Kit (Qiagen), как описано в протоколе производителя. Для этого готовили мастер микс содержащий 4 мкл 5x miScript HiSpec Buffer (mature miRNA profiling using miScript miRNA PCR Arrays or quantification of mature miRNAs only using miScript Primer Assays) или 5x miScript HiFlex Buffer (f mature miRNAs in parallel with precursor miRNAs, mRNAs and/or other noncoding RNAs using miScript Primer Assays, miScript Precursor Assays and/or QuantiTect® Primer Assays), 2 мкл 10x miScript Nucleics Mix, 2 мкл miScript Reverse Transcriptase Mix, 1-12 мкл образца РНК (содержащего не менее 100 нг и не более 2 мкг РНК) и 1-11 мкл RNase-free water.
Приготовленный мастер-микс помещали в пробирки объемом 100 мкл для обратной транскрипции. Амплификацию осуществляли с помощью прибора Nexus Mastercycler® gradient (Eppendorf, Германия) в режиме 37°C - 60 мин, 95°C - 5 мин. Полученную кДНК использовали сразу или хранили на -20°C.
ПЦР в реальном времени
ПЦР в реальном времени проводили с использованием miScript miRNA PCR Array Human Fibrosis (Qiagen). Для этого в условиях ПЦР-бокса готовили мастер-микс, содержащий 1375 мкл 2x QuantiTect SYBR Green PCR Master Mix, 275 мкл 10x miScript Universal Primer, 1000 мкл RNase-free water и 100 мкл образца кДНК, содержащего 48-96 нг кДНК.
После пипетирования раскапывали полученную смесь по 25 мкл в лунки планшета 96-well miScript miRNA PCR Array. Центрифугировали планшет в течение 1 минуты при 1000g. Помещали планшет в ПЦР-систему QuantStudio 5 (Thermo Fisher Scientific). Проводили ПЦР в реальном времени, используя следующий режим:
95°С - 15 мин, затем 40 циклов 94°С - 15 сек, 55°С - 30 сек, 70°С - 30 сек.
Содержание исследуемых миРНК нормировали по уровню сигнала, получаемого для кДНК SNORD61, SNORD95, SNORD96A, SNORD68, SNORD72, RNU6B/RNU6-2. После проведения ПЦР с детекцией в режиме реального времени полученные данные по значениям порогового цикла для каждого гена обрабатывали согласно формуле:
N = 2^(-ΔCt), ΔСt = Сt1-Сthk, где Сt1 - значение порогового цикла для исследуемого гена, Сthk - усредненные значения пороговых циклов SNORD61, SNORD95, SNORD96A, SNORD68, SNORD72, RNU6B/RNU6-2, N - результат в относительных единицах.
Пример 9. Методы оценки способности кондиционированной среды МСК, обогащенной внеклеточными везикулами, разрешать фиброз легких на модели фиброза легких
В экспериментах были использованы мыши линии C57Bl/6N, самцы и самки возрастом от 9 до 20 недель собственного разведения. Мышей содержали в виварии лаборатории трансляционной медицины ФФМ МГУ в соответствии с ГОСТ 33215-2014 Руководство по содержанию и уходу за лабораторными животными (Правила оборудования помещений и организации процедур).
Препарат блеомицина (Блеоцин «Ниппон Кайяку Ко., ЛТД», Япония, Рег. номер П N0113322/01)) готовили к введению в условиях стерильного ламинарного бокса на основе физиологического раствора в и вводили мышам эндотрахеально в концентрации 3 мг/кг (в объеме 30 мкл). Для проверки гипотезы о влиянии ВВ-МСК на ранние стадии развития фиброза, ВВ-МСК 10х вводили через сутки после введения препарата блеомицин (группа профилактика, (Блеомицин 3 мг/кг, ВВ-МСК 10х, n=5). Для проверки гипотезы о влиянии ВВ-МСК на лечение уже сформировавшегося фиброза, ВВ-МСК 10х вводили через 14 дней после введения блеомицина (группа профилактика, (Блеомицин 3 мг/кг, ВВ-МСК 10х, n=5). В качестве контроля для этих групп было введено две группы с использованием DMEM LG + 1% пенициллин-стрептомицин при введении через 1 и 14 суток от введения блеомицина (в каждой группе n=5). Фракция ВВ-МСК и DMEM LG вводились в объеме 30 мкл интратрахеально.
Для оценки состояния животных использовали динамику веса животных после введения блеомицина, и, кроме этого, отмечали проявление признаков неблагополучия: низкая подвижность, сгорбленная поза животного и наличие характерных хрипов при дыхании. Изменения клинического состояния животных оценивали по специальной балльной шкале. Всем мышам проводилось МРТ-сканирование на 0, 7, 14, 21 день от начала эксперимента. На 22 сутки после введения препарата, мышей эвтаназировали, легкие извлекали, фиксировали в 10% нейтральном формалине и отправляли на гистологическое исследование.
Гистохимический анализ ткани легких
Зафиксированную 10% нейтральным формалином ткань заливали в парафин. Полученные блоки нарезали на микротоме (толщина срезов 1 мкм, интервал между срезами 50 мкм) срезы монтировали на покрытые полилизином стекла (Menzel-Glaserpolysineslides, Thermo FS). Срезы депарафинизировали в толуоле и понижающейся концентрации спиртов до воды. Для анализа выраженности фибротических изменений срезы были окрашены гематоксилином и эозином (Dako), согласно протоколу производителя. Степень коллагенообразования оценивали методом гистохимического окрашивания по Ван-Гизону, окрашивание на эластические волокна проводили с помощью железного гематоксилина Верхгофа, согласно протоколу производителя. Полученные окрашенные срезы заключали в канадский бальзам и анализировали с помощью микроскопа Leica DM600Β (LeicaMicrosystemsGmbH, Germany). Изображения фрагментов полученных срезов получали с помощью цифровой камеры Leica DFC 420C (LeicaMicrosystemsGmbH, Germany). Изображения оценивались по балльной шкале Эшкрофта от 0 (норма) до 8 (полная фиброзная облитерация в поле зрения) (Hübner et al., 2008).
Бронхоальвеолярный лаваж
Для оценки воспалительной реакции, индуцируемой при повреждении легочной ткани у мышей брали бронхоальвеолярный лаваж. Для его выделения мышей эвтаназировали, производили небольшой разрез трахеи, куда вводили силиконовую трубку, фиксированную на игле шприца диаметром 23G. Делали смыв содержимого бронхов и легких с помощью 0,5 мл фосфатно-солевого буфера с добавлением 10% ФБС (Gibco, США). Смыв проводили 4-6 раз для каждого животного, для увеличения количества полученных клеток. Для каждой мыши по 15 мкл от полученной суспензии помещали на предметное стекло, высушивали сутки. Полученные препараты окрашивали раствором Гимзы в течение 12 часов, заключали в канадский бальзам и анализировали с помощью микроскопа Leica DM600Β (LeicaMicrosystemsGmbH, Germany). Изображения фрагментов полученных мазков получали с помощью цифровой камеры Leica DFC 420C (LeicaMicrosystemsGmbH, Germany). На каждом препарате исследовали 10 случайных полей зрения на увеличении 20Х. В каждом поле зрения считали среднее количество лимфоцитов и макрофагов. Для дальнейшего анализа структуру клеточного состава выразили в процентах от общего числа клеток в образце.
Оценка клинического состояния животных
Благополучие мышей оценивали ежедневно по следующим параметрам: вес тела и его изменение в процентах к начальному, внешний вид, поведение в домашней клетке, внешние признаки нарушения дыхания, вызванное поведение, общий балл за указанный день (Табл. 2). Чем больше оказывался балл у животного по шкале, тем хуже было его состояние на момент осмотра. Для количественной оценки неблагополучия мы брали максимальный балл, накопленный к 21-му дню эксперимента. Для доживших до этого срока животных выбирался общий балл, подсчитанный в этот день. Исходя из соображения, что смерть является максимальной степенью неблагополучия животного, для погибших раньше 21 дня мышей, мы принимали общий балл равным 11 - максимальному по нашей шкале.
Оценку состояния проводили одновременно с процедурой взвешивания животных. Сначала необходимо понаблюдать за интактным животным и оценить параметры 2-4. После проведения взвешивания и возвращения мыши в домашнюю клетку оценить параметр 5. Параметр 1 оценивается по результатам взвешивания (за 100% принимается вес животного до введения веществ - см. карточку на клетку).
Решение об эвтаназии принимается при суммарном балле 10-11 на основании возможности провести перфузию легких для сохранения гистологических данных.
МР-сканирование
МРТ проводили с использованием прибора ClinScan 7T, Bruker Biospin, USA. Для получения МРТ снимков животных наркотизировали воздушной смесью кислород/изофлуран (98%/2%). Жизнедеятельность отслеживали с помощью монитора дыхательного цикла. Визуализацию легких проводили в Т2 взвешенном режиме с подавлением сигнала от жировой ткани с помощью последовательсности Turbo Spin Echo со следующими параметрами: TR = 1175 мс, TE = 55 мс, Echo train length = 8, FOV 42x60 mm, base resolution 216x384.
Анализ полученных изображений проводили с использованием программы ImageJ (National Institutes of Health, Bethesda, MA, USA). Использовали лишь изображения срезов, прошедших через грудную клетку во фронтальной плоскости. Для каждой мыши отбирали несколько фронтальных срезов, которые, предположительно, проходили через легкие (n=3-10). На изображениях вручную выделяли зону проекции легких, за исключением органов средостения и магистральных сосудов. Для коррекции вариаций интенсивности сигнала между снимками и получения нормированных показателей, на каждом изображении выделяли дополнительный участок мышечной ткани. Для каждого участка оценивали площадь, средняя интенсивность сигнала, ее максимальное и минимальное значения и стандартное отклонение.
Результаты клинического осмотра
После обработки данных по клиническому состоянию животных были получены следующие результаты: В группе лечения фиброза ВВ-МСК медиана максимального накопленного балла у контрольных животных составляет 7, а у экспериментальных - 1. Это говорит о том, что состояние мышей, получавших кондиционированную среду МСК, обогащенную ВВ, благополучнее, чем у тех, которые получали контрольную среду DMEM.
В группе профилактики фиброза медиана максимального накопленного балла у контрольных животных составляет 9, а у экспериментальных - 5. Это также говорит о том, что состояние мышей, получавших кондиционированную среду МСК, обогащенную ВВ, благополучнее, чем у тех, которые получали DMEM, однако эти животные чувствовали себя хуже, чем в группе лечения фиброза (Фиг. 10).
Результаты БАЛ
После подсчета клеток в образцах промывной жидкости легких, получили следующую структуру клеточного состава. Лимфоциты являются наиболее преобладающим видом иммунных клеток в образцах, поскольку их процентное содержание в среднем по группе - больше 70%. Их снижение косвенно говорит о снижении интенсивности воспаления. В группе «лечение» при введении ВВ-МСК наблюдается тенденция к снижению лимфоцитарной инфильтрации (70% клеток из подсчитанных в лаваже являются лимфоцитами), в то время как в остальных группах количество лимфоцитов колеблется от 85 до 92%.
Вторым исследованным типом клеток были макрофаги, и их доля в клеточном составе промывной жидкости значительно различается между некоторыми из групп. Была отмечена тенденция к изменению количества макрофагов в группе лечения фиброза между экспериментальной группой, получавшей КС и контрольной. В контрольной группе было 15% макрофагов, а в экспериментальной - 27%. За нормальную долю макрофагов приняты значения у мышей группы отрицательного контроля, получавших PBS вместо блеомицина. Макрофаги в очаге воспаления играют роль как в развитии фиброза и воспаления, так и в резорбции очага фиброза. Изменение их доли говорит как об увеличении интенсивности воспаления, так и о процессе резорбции очага фиброза (Фиг. 10).
Результаты МРТ
Данные по интенсивности сигнала на снимках МРТ были получены для каждой из групп в виде разброса значений Delta -изменение относительной интенсивности сигнала по сравнению с первым МРТ, по отдельности - для каждого из последующих МРТ. В группе лечения фиброза общая динамика похожа - нарастание относительной интенсивности к третьему МРТ и спад к четвертому, однако медианы различаются: по порядку - 0,18 0,32 и 0,14 для контрольной группы и 0,28 0,34 и 0,16 в экспериментальной группе. В целом значения выше в экспериментальной подгруппе, чем в контрольной. В группе профилактики фиброза динамика отличается - в экспериментальной подгруппе значения Delta стабильны (медианы по порядку - 0,26 0,29 0,28), а в контрольной подгруппе значения стабильны на 2 и 3 МРТ, но отмечался спад к четвертому группе (медианы по порядку - 0,17 0,14 0,09) (Фиг. 10).
Результаты гистологического анализа
Результаты гистологического анализа срезов легких мышей из различных экспериментальных групп представлены в Табл. 3 и на Фиг. 11. Можно отметить, что при использовании ВВ-МСК в группе «лечение» гистологическая оценка тяжести фиброза на 1 балл меньше, чем в контрольной группе, а в группе «профилактика» - на 0,5.
Пример 10. Методы оценки способности кондиционированной среды МСК, обогащенной внеклеточными везикулами и растворимыми компонентами, разрешать фиброз на модели глубокой кожной раны
Характеристика экспериментальных групп
Экспериментальные исследования были проведены на линии беспородных белых мышей, содержащей 51 половозрелую особь. Все животные были одного возраста (3-5 месяцев), вес одной особи в среднем составлял 25-30 г. Эксперимент проводился после предварительной адаптации мышей в виварии в течение 10 суток. Мышей содержали на обычном рационе вивария. После нанесения повреждения каждая мышь находилась в отдельной клетке.
Подопытные животные линии были разделены на несколько групп в зависимости от способа лечения ран (Табл. 4).
Схема эксперимента
При проведении эксперимента руководствовались Европейской конвенцией о защите позвоночных животных, используемых для экспериментов или в иных научных целях №123 от 18.03.1986 г. и Приказом МЗ СССР №755 от 12.08.1975 г. «О мерах по дальнейшему совершенствованию организационных форм работы с использованием экспериментальных животных».
Наркотизирование животных проводилось препаратом авертин. Препарат вводился внутрибрюшинно в дозе 20 мкл/1 г веса животного. Расход препарата на одну белую мышь составлял 0,5-0,6 мл. Формирование раны проводили, иссекая кожу на выбранном участке скальпелем. Края раны для предотвращения констрикции подшивали к пластиковому кольцу диаметром 12 мм.
В зависимости от группы проводили местное лечение раны следующим образом (Табл. 4):
В группе №1 (положительный контроль) рану покрывали тонким слоем препарата «Левомеколь» и укрывали сухой стерильной марлевой повязкой, которую фиксировали к пластиковому кольцу одиночными швами. Перевязку раны делали дважды в день в течение первых трех суток путем смены повязки.
В группе №2 (опыт-инъекция) - в дно и окружающие мягкие ткани раны путем микроинъекций вводили концентрированную (5х) кондиционированную среду в объеме 400 мкл (что соответствовало 0,4-1,2*10^10 внеклеточных везикул). Затем рану укрывали марлевой повязкой, которую фиксировали к пластиковому кольцу одиночными швами. В данной группе перевязку раны не проводили.
В группе №3 (отрицательный контроль) - в дно и окружающие мягкие ткани раны путем микроинъекций вводили культуральную среду DMEM (Gibco) в объеме 400 мкл. Затем рану укрывали марлевой повязкой, которую фиксировали к пластиковому кольцу одиночными швами. В данной группе перевязку раны не выполняли.
Вывод мышей из эксперимента проводили на 3, 7, 14 и 28 сутки. На 3, 7 и 14 сутки выводили по 5 особей, на 28 сутки выводили по 2 особи. Вывод производили методом дислокации спинного мозга в шейном отделе. В качестве критериев оценки эффективности воздействия кондиционированной среды на заживление кожной раны были выбраны следующие: выраженность воспалительной реакции в ране и окружающих мягких тканях, скорость и полноценность восстановления кожного покрова. Макроскопически оценивали также характер раневого отделяемого, отек и гиперемию окружающих тканей, формирование струпа, скорость и полноценность восстановления кожного покрова. В ходе микроскопического исследования оценивали наличие и характер клеточной инфильтрации, рост сосудов, степень эпителизации, восстановление дериватов кожи.
Для микроскопического исследования послойные фрагменты тканей на выбранных сроках были удалены из области раны с захватом краев и фиксировали в 10% растворе формалина. После стандартной гистологической проводки и заливки в парафин были приготовлены гистологические срезы. Для получения обзорной картины срезы были окрашены гематоксилином и эозином. Степень коллагенообразования оценивали с помощью гистохимического окрашивания по Ван-Гизону. Полученные окрашенные срезы заключали в канадский бальзам и анализировали с помощью микроскопа Leica DM600Β (Leica Microsystems GmbH, Germany). Изображения фрагментов полученных срезов получали с помощью цифровой камеры Leica DFC 420C (Leica Microsystems GmbH, Germany). Обработку изображений проводили в программе ImageJ.
Результаты (Фиг. 12-16).
Для проверки гипотезы о том, что секретом МСК человека может влиять на регенеративные процессы, была использована модель кожной раны у мышей. Сразу после нанесения раны в нее вводили кондиционированную среду МСК. Оценку заживления проводили через 3, 7, 14 и 28 дней после нанесения раны и аппликации кондиционированной среды или препарата сравнения.
Через 3 суток после нанесения раны, что соответствует стадии воспаления, во всех группах наблюдали изменения характерные для этой фазы. В ранах, на которые наносили кондиционированную среду МСК, экссудация и гиперемия окружающих тканей были выражены слабее, чем в контрольных группах, отмечалось наличие островков грануляционной ткани и набухание краев раны. Такая картина свидетельствовала о завершении воспаления. При микроскопическом исследовании у животных в группе с введением кондиционированная среда МСК, наблюдали менее выраженную инфильтрацию лейкоцитами. При этом преобладающими типами лейкоцитов оказались лимфоциты и макрофаги. Диапедез эритроцитов в таких ранах также был менее выражен и отмечался только у 2 животных из 5. Более того, в таких ранах уже через 3 дня после повреждения были обнаружены единичные новообразованные сосуды, а также наблюдали начало роста краевого эпителиального пласта. Инфильтрат таких ран, помимо лейкоцитов включал фибробласты, ядра которых содержали слабо-конденсированный хроматин, что может свидетельствовать о высокой синтетической активности этих клеток. Таким образом, введение в рану среды, содержащей продукты секреции МСК, вызывало ускоренное завершение воспаления и появление таких признаков начала репаративного процесса, как накопление в ране фибробластов, рост краевого эпителиального пласта и неоваскулогенез.
Через 7 суток после нанесения раны наблюдали признаки, характерные для фазы ранней пролиферации раневого процесса. В ранах, куда была введена кондиционированная среда МСК, отмечали интенсивный рост грануляционной ткани (у 3 из 5 животных), образование большого числа петель тонкостенных сосудов, мягкие ткани были инфильтрированы фибробластами и клетками воспаления. Также наблюдали активный рост краевого эпителиального пласта под струп. В контрольных группах наблюдали незначительное формирование грануляционной ткани, пронизанной мелкими сосудами, отмечали слабый рост эпителиального пласта под струп, появление фибробластов у наружных слоев раны.
Фаза пролиферации раневого процесса обычно завершается формированием полноценной грануляционной ткани в дне раны. Восстановление кровоснабжения в участке повреждения, в свою очередь, создает благоприятное микроокружение для миграции и пролиферации эпидермальных и дермальных клеток, что и обусловливает восстановление целостности эпидермиса в области раны.
Через 14 дней после нанесения, в ранах, обработанных мазью «Левомеколь» эпителизация не была полной. В грануляционной ткани преобладали полиморфноядерные лейкоциты, макрофаги и тонкостенные сосуды, была отмечена выраженная пикринофилия коллагеновых волокон, которая распространялась на всю глубину дермы. Необходимо подчеркнуть, что рисунок расположения коллагеновых волокон, в целом, соответствовал тому, что наблюдается в дерме.
В ранах, на которые наносили среду ДМЕМ, не содержащую продуктов секреции МСК, также отмечали рост эпителиального пласта под струп и частичное отслоение струпа. Инфильтрация лейкоцитами и пикринофилия коллагеновых волокон отсутствовали, а расположение коллагеновых волокон соответствовало норме. Несмотря на то, что у 2 из 5 животных эпителизация раны через 14 дней после нанесения была почти завершена, а на месте раны отмечали утолщение эпидермиса, содержащего все слои клеток, микрорельеф ткани в таких участках не визуализировался. Отсутствие микрорельефа эпителия в ране свидетельствует о продолжении их эпителизации.
В ранах, куда была введена кондиционированная среда МСК, отмечался выраженный рост краевого эпителиального пласта под струп, большая часть раны была покрыта неоэпителием (у 3 из 5 мышей рана оказалась полностью покрыта эпителием). При гистологическом исследовании была отмечена полная эпителизация раны, в зоне раны определялась грануляционная ткань, содержащая большое количество тонкостенных сосудов. Эпидермис утолщен, микрорельеф не визуализировался, были сформированы все слои клеток. Инфильтрация клетками воспаления и пикринофилия коллагеновых волокон отсутствовали, расположение коллагеновых волокон соответствовало норме
Через 28 суток у животных контрольных групп (раны которых были обработаны мазью «Левомеколь» или средой ДМЕМ, не содержащей продукты секреции МСК), было отмечено полное заживление раны с формированием рубца. При этом дериваты кожи были сформированы слабо либо полностью отсутствовали.
В ранах, куда была введена кондиционированная среда МСК, было отмечено восстановление кожного покрова без образования рубцовой ткани. Кроме того, наблюдали частичное восстановление волосяного покрова. При гистологическом исследовании так же, как и у животных контрольных групп была выявлена полная эпителизация раны. В отличие от ран животных контрольных групп, в ранах, обработанных кондиционированной средой МСК, было отмечено формирование сальных желез и волосяных фолликулов, а также формирование микрорельефа.
Таким образом, введение кондиционированной среды, содержащей продукты секреции МСК человека, уменьшает сроки заживления раны, ускоряет эпителизацию раны, формирование дериватов кожи и препятствует формированию рубцовой ткани. Эти результаты указывают на то, что МСК продуцируют факторы, не только стимулирующие регенерацию кожи, но и препятствующие формированию рубцовой (фиброзной) ткани.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Московский государственный университет имени М.В.Ломоносова" (МГУ)
<120> СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ФИБРОЗА ТКАНЕЙ НА ОСНОВЕ КОМПОНЕНТОВ СЕКРЕТОМА МЕЗЕНХИМНЫХ СТРОМАЛЬНЫХ КЛЕТОК, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ СРЕДСТВА
<160> SEQ ID NО:1
<210> 1
<211> 24
<212> human microRNA
<213> natural sequence
<223> miR-7-5p
<400> 1
1 uggaagacua gugauuuugu uguu
<160> SEQ ID NО:2
<210> 2
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-10b-5p
<400> 2
1 UACCCUGUAG AACCGAAUUU GUG
<160> SEQ ID NО:3
<210> 3
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-10a-5p
<400> 3
1 UACCCUGUAG AUCCGAAUUU GUG
<160> SEQ ID NО:4
<210> 4
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-15b-5p
<400> 4
1 UAGCAGCACA UCAUGGUUUA CA
<160> SEQ ID NО:5
<210> 5
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-16-5p
<400> 5
1 uagcagcacg uaaauauugg cg
<160> SEQ ID NО:6
<210> 6
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-17-5p
<400> 6
1 CAAAGUGCUU ACAGUGCAGG UAG
<160> SEQ ID NО:7
<210> 7
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-18a-5p
<400> 7
1 UAAGGUGCAU CUAGUGCAGA UAG
<160> SEQ ID NО:8
<210> 8
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-19a-3p
<400> 8
1 UGUGCAAAUC UAUGCAAAAC UGA
<160> SEQ ID NО:9
<210> 9
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-19b-3p
<400> 9
1 UGUGCAAAUC CAUGCAAAAC UGA
<160> SEQ ID NО:10
<210> 10
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-20a-5p
<400> 10
1 UAAAGUGCUU AUAGUGCAGG UAG
<160> SEQ ID NО:11
<210> 11
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-21-5p
<400> 11
1 UAGCUUAUCA GACUGAUGUU GA
<160> SEQ ID NО:12
<210> 12
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-23a-3p
<400> 12
1 GGGGUUCCUG GGGAUGGGAU UU
<160> SEQ ID NО:13
<210> 13
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-25-3p
<400> 13
1 CAUUGCACUU GUCUCGGUCU GA
<160> SEQ ID NО:14
<210> 14
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-26a-5p
<400> 14
1 UUCAAGUAAU CCAGGAUAGG CU
<160> SEQ ID NО:15
<210> 15
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-27a-3p
<400> 15
1 UUCACAGUGG CUAAGUUCCG C
<160> SEQ ID NО:16
<210> 16
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-27b-3p
<400> 16
1 UUCACAGUGG CUAAGUUCUG C
<160> SEQ ID NО:17
<210> 17
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-29a-3p
<400> 17
1 UAGCACCAUC UGAAAUCGGU UA
<160> SEQ ID NО:18
<210> 18
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-29b-3p
<400> 18
1 uagcaccauu ugaaaucagu guu
<160> SEQ ID NО:19
<210> 19
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-29c-3p
<400> 19
1 UAGCACCAUU UGAAAUCGGU UA
<160> SEQ ID NО:20
<210> 20
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-30a-5p
<400> 20
1 UGUAAACAUC CUCGACUGGA AG
<160> SEQ ID NО:21
<210> 21
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-31-5p
<400> 21
1 AGGCAAGAUG CUGGCAUAGC U
<160> SEQ ID NО:22
<210> 22
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-34a-5p
<400> 22
1 UGGCAGUGUC UUAGCUGGUU GU
<160> SEQ ID NО:23
<210> 23
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-92a-3p
<400> 23
1 uauugcacuu gucccggccu gu
<160> SEQ ID NО:24
<210> 24
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-101-3p
<400> 24
1 UACAGUACUG UGAUAACUGA A
<160> SEQ ID NО:25
<210> 25
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-106a-5p
<400> 25
1 AAAAGUGCUU ACAGUGCAGG UAG
<160> SEQ ID NО:26
<210> 26
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-125b-5p
<400> 26
1 UCCCUGAGAC CCUAACUUGU GA
<160> SEQ ID NО:27
<210> 27
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-126-3p
<400> 27
1 ucguaccgug aguaauaaug cg
<160> SEQ ID NО:28
<210> 28
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-129-5p
<400> 28
1 CUUUUUGCGG UCUGGGCUUG C
<160> SEQ ID NО:29
<210> 29
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-143-3p
<400> 29
1 UGAGAUGAAG CACUGUAGCU C
<160> SEQ ID NО:30
<210> 30
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-145-5p
<400> 30
1 GUCCAGUUUU CCCAGGAAUC CCU
<160> SEQ ID NО:31
<210> 31
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-146a-5p
<400> 31
1 UGAGAACUGA AUUCCAUGGG UU
<160> SEQ ID NО:32
<210> 32
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-146b-5p
<400> 32
1 UGAGAACUGA AUUCCAUAGG CUG
<160> SEQ ID NО:33
<210> 33
<211> 24
<212> human microRNA
<213> Natural sequence
<223> miR-155-5p
<400> 33
1 UUAAUGCUAA UCGUGAUAGG GGUU
<160> SEQ ID NО:34
<210> 34
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-192-5p
<400> 34
1 CUGACCUAUG AAUUGACAGC C
<160> SEQ ID NО:35
<210> 35
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-194-5p
<400> 35
1 UGUAACAGCA ACUCCAUGUG GA
<160> SEQ ID NО:36
<210> 36
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-195-5p
<400> 36
1 uagcagcaca gaaauauugg c
<160> SEQ ID NО:37
<210> 37
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-196a-5p
<400> 37
1 uagguaguuu cauguuguug gg
<160> SEQ ID NО:38
<210> 38
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-199a-5p
<400> 38
1 CCCAGUGUUC AGACUACCUG UUC
<160> SEQ ID NО:39
<210> 39
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-199b-5p
<400> 39
1 CCCAGUGUUU AGACUAUCUG UUC
<160> SEQ ID NО:40
<210> 40
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-203a-3p
<400> 40
1 GUGAAAUGUU UAGGACCACU AG
<160> SEQ ID NО:41
<210> 41
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-204-5p
<400> 41
1 UUCCCUUUGU CAUCCUAUGC CU
<160> SEQ ID NО:42
<210> 42
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-215-5p
<400> 42
1 AUGACCUAUG AAUUGACAGA C
<160> SEQ ID NО:43
<210> 43
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-324-3p
<400> 43
1 CCCACUGCCC CAGGUGCUGC UGG
<160> SEQ ID NО:44
<210> 44
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-324-5p
<400> 44
1 CGCAUCCCCU AGGGCAUUGG UG
<160> SEQ ID NО:45
<210> 45
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-328-3p
<400> 45
1 CUGGCCCUCU CUGCCCUUCC GU
<160> SEQ ID NО:46
<210> 23
<211> 46
<212> human microRNA
<213> Natural sequence
<223> miR-335-5p
<400> 46
1 UCAAGAGCAA UAACGAAAAA UGU
<160> SEQ ID NО:47
<210> 47
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-338-5p
<400> 47
1 AACAAUAUCC UGGUGCUGAG UG
<160> SEQ ID NО:48
<210> 48
<211> 64
<212> human microRNA
<213> Natural sequence
<223> miR-375
<400> 48
1 CCCCGCGACG AGCCCCUCGC ACAAACCGGA CCUGAGCGUU UUGUUCGUUC
51 GGCUCGCGUG AGGC
<160> SEQ ID NО:49
<210> 49
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-378a-3p
<400> 49
1 ACUGGACUUG GAGUCAGAAG GC
<160> SEQ ID NО:50
<210> 50
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-382-5p
<400> 50
1 GAAGUUGUUC GUGGUGGAUU CG
<160> SEQ ID NО:51
<210> 51
<211> 91
<212> human microRNA
<213> Natural sequence
<223> miR-449a
<400> 51
1 CUGUGUGUGA UGAGCUGGCA GUGUAUUGUU AGCUGGUUGA AUAUGUGAAU
51 GGCAUCGGCU AACAUGCAAC UGCUGUCUUA UUGCAUAUAC A
<160> SEQ ID NО:52
<210> 52
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-449b-5p
<400> 52
1 aggcagugua uuguuagcug gc
<160> SEQ ID NО:53
<210> 53
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-491-5p
<400> 53
1 AGUGGGGAAC CCUUCCAUGA GG
<160> SEQ ID NО:54
<210> 54
<211> 23
<212> human microRNA
<213> Natural sequence
<223> miR-503-5p
<400> 54
1 UAGCAGCGGG AACAGUUCUG CAG
<160> SEQ ID NО:55
<210> 55
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-590-5p
<400> 55
1 GAGCUUAUUC AUAAAAGUGC AG
<160> SEQ ID NО:56
<210> 56
<211> 89
<212> human microRNA
<213> Natural sequence
<223> miR-661
<400> 56
1 GGAGAGGCUG UGCUGUGGGG CAGGCGCAGG CCUGAGCCCU GGUUUCGGGC
51 UGCCUGGGUC UCUGGCCUGC GCGUGACUUU GGGGUGGCU
<160> SEQ ID NО:57
<210> 57
<211> 93
<212> human microRNA
<213> Natural sequence
<223> miR-663a
<400> 57
1 CCUUCCGGCG UCCCAGGCGG GGCGCCGCGG GACCGCCCUC GUGUCUGUGG
51 CGGUGGGAUC CCGCGGCCGU GUUUUCCUGG UGGCCCGGCC AUG
<160> SEQ ID NО:58
<210> 58
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-744-5p
<400> 58
1 UGCGGGGCUA GGGCUAACAG CA
<160> SEQ ID NО:59
<210> 59
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-874-3p
<400> 59
1 CUGCCCUGGC CCGAGGGACC GA
<160> SEQ ID NО:60
<210> 60
<211> 21
<212> human microRNA
<213> Natural sequence
<223> miR-5011-5p
<400> 60
1 UAUAUAUACA GCCAUGCACU C
<160> SEQ ID NО:61
<210> 61
<211> 22
<212> human microRNA
<213> Natural sequence
<223> miR-5692a
<400> 61
1 caaauaauac cacagugggu gu
<160> SEQ ID NО:62
<210> 62
<211> 21
<213> Artificial sequence, primer
<223> Коллаген I типа (Col1A1)
<400> 62
1 CCCAGCCACA AAGAGTCTAC A
<160> SEQ ID NО:63
<210> 63
<211> 20
<213> Artificial sequence, primer
<223> Коллаген I типа (Col1A1)
<400> 63
1 GTTTCCACAC GTCTCGGTCA
<160> SEQ ID NО:64
<210> 64
<211> 20
<213> Artificial sequence, primer
<223> Гладкомышечный актин (ACTA2)
<400> 64
1 CAATGAGCTT CGTGTTGCCC
<160> SEQ ID NО:65
<210> 65
<211> 20
<213> Artificial sequence, primer
<223> Гладкомышечный актин (ACTA2)
<400> 65
1 TCTCCAGAGT CCAGCACGAT
<160> SEQ ID NО:66
<210> 66
<211> 19
<213> Artificial sequence, primer
<223> 60S кислый рибосомный белок P0 (RPLP0)
<400> 66
1 GCTGCTGCCC GTGCTGGTG
<160> SEQ ID NО:67
<210> 67
<211> 24
<213> Artificial sequence, primer
<223> 60S кислый рибосомный белок P0 (RPLP0)
<400> 67
1 TGGTGCCCCT GGAGATTTTA GTGG
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ НЕЙРОПРОТЕКЦИИ И СТИМУЛЯЦИИ НЕЙРОРЕГЕНЕРАЦИИ ГОЛОВНОГО МОЗГА ПОСЛЕ ПОВРЕЖДЕНИЯ, СРЕДСТВО НА ЕЕ ОСНОВЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2022 |
|
RU2803286C1 |
| БИОМАРКЕРЫ ТРАВМАТИЧЕСКОГО ПОВРЕЖДЕНИЯ ГОЛОВНОГО МОЗГА | 2017 |
|
RU2771757C2 |
| Аналитическая система для диагностики рака лёгкого при помощи свободных и ассоциированных с клетками крови циркулирующих микроРНК | 2020 |
|
RU2755651C1 |
| МИМЕТИКИ MIR-29 И ПУТИ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2712511C2 |
| СООТВЕТСТВУЮЩАЯ МИШЕНЬ ДЛЯ ЛЕЧЕНИЯ ФИБРОЗИРУЮЩИХ ЗАБОЛЕВАНИЙ И ЕЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2830698C1 |
| БИОМАРКЕР | 2019 |
|
RU2808079C2 |
| ЛИНЕЙНАЯ ДУПЛЕКСНАЯ ДНК С ЗАКРЫТЫМ КОНЦОМ ДЛЯ НЕВИРУСНОГО ПЕРЕНОСА ГЕНОВ | 2017 |
|
RU2752882C2 |
| ВНЕКЛЕТОЧНЫЕ ВЕЗИКУЛЫ ДЛЯ ИНГАЛЯЦИИ | 2019 |
|
RU2799315C2 |
| Набор реагентов для определения малых рибонуклеиновых кислот (микроРНК) при диагностике множественной миеломы | 2024 |
|
RU2836054C1 |
| ОНКОЛИТИЧЕСКИЕ ВИРУСНЫЕ ВЕКТОРЫ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2771110C2 |
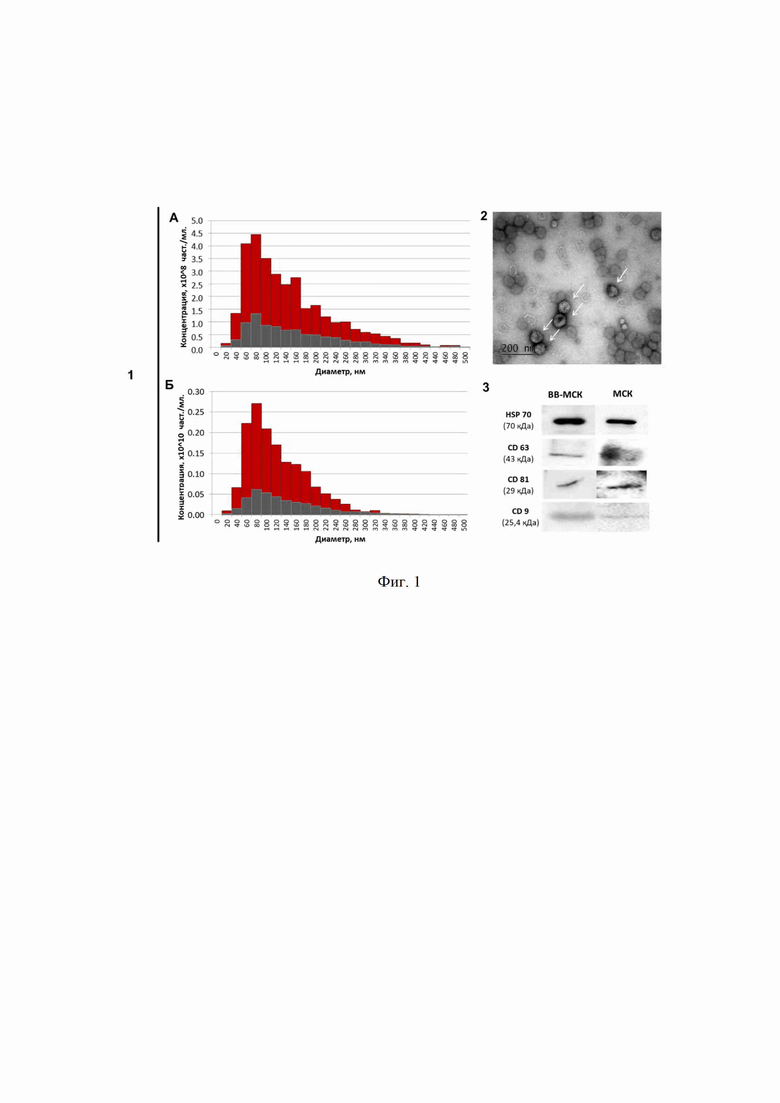
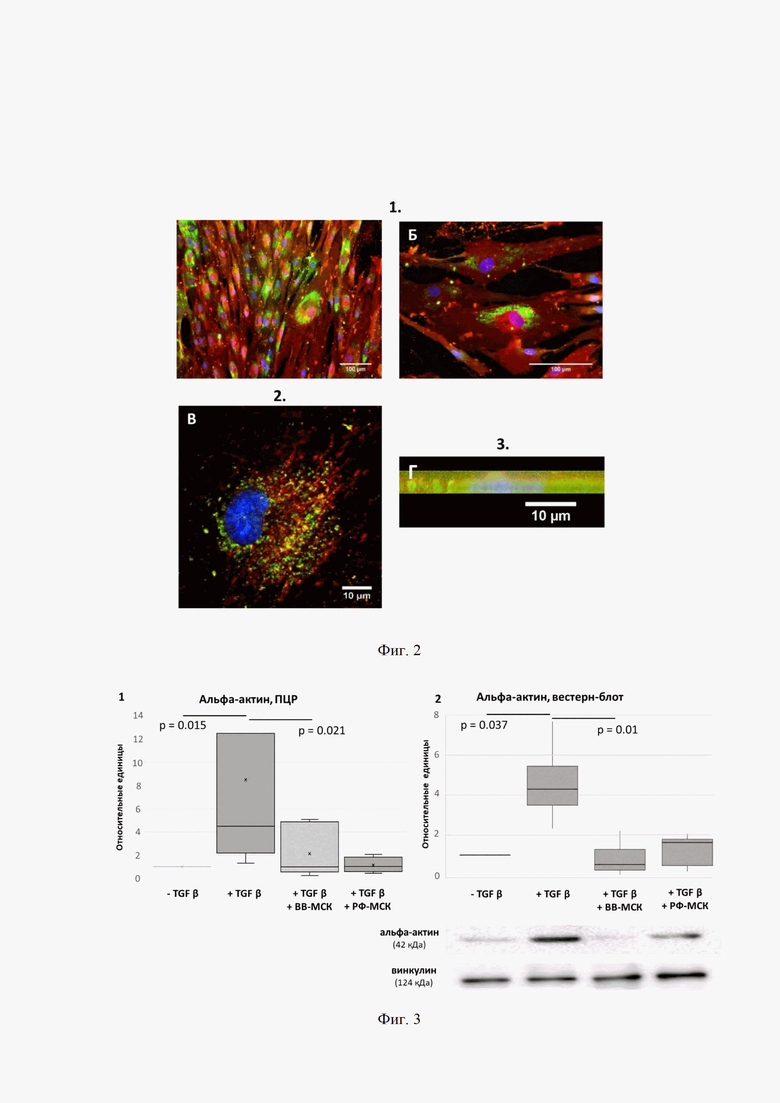
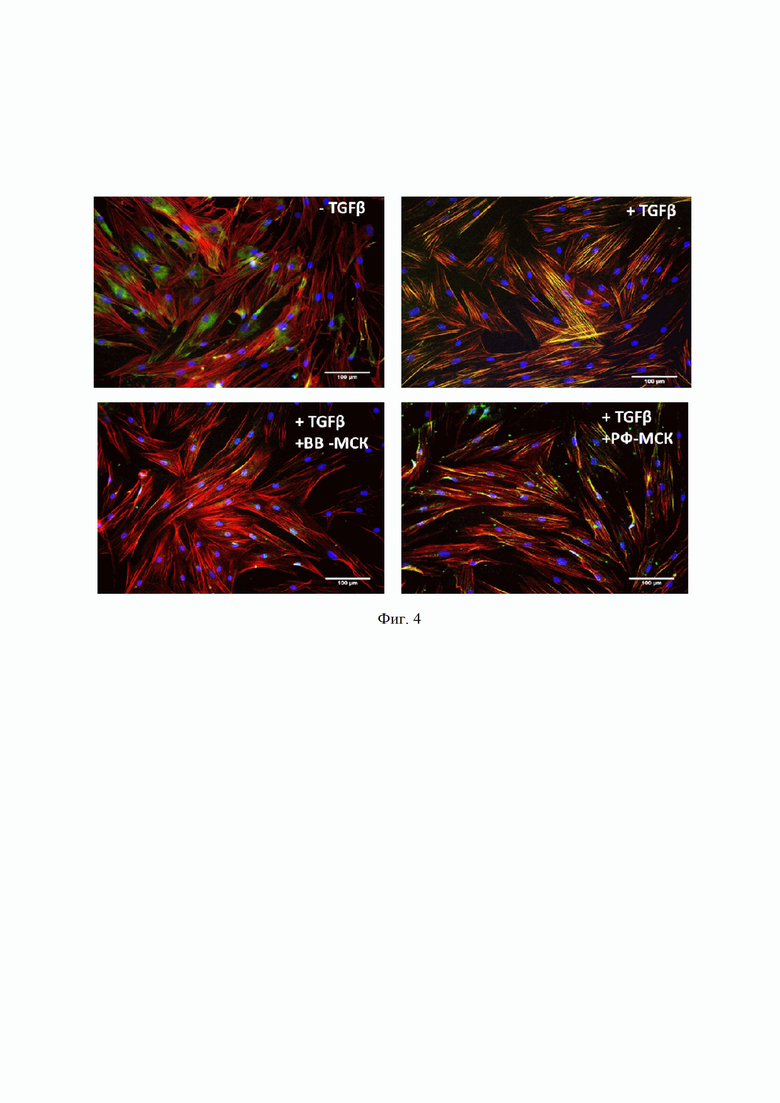
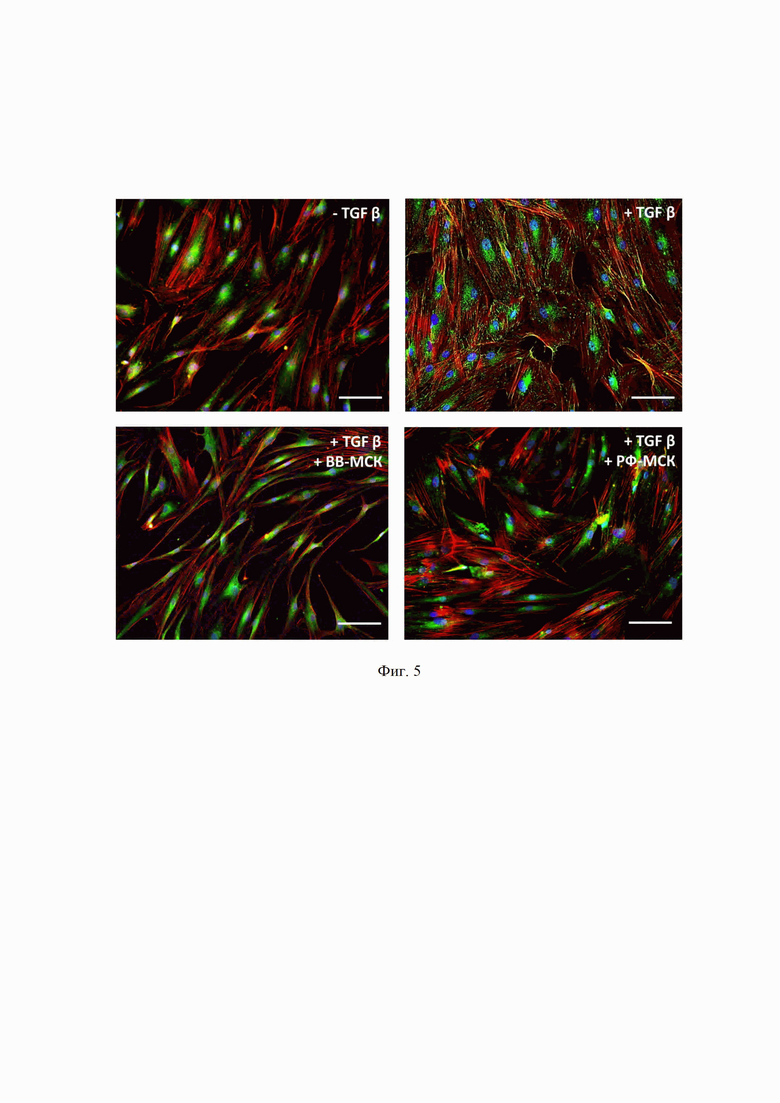
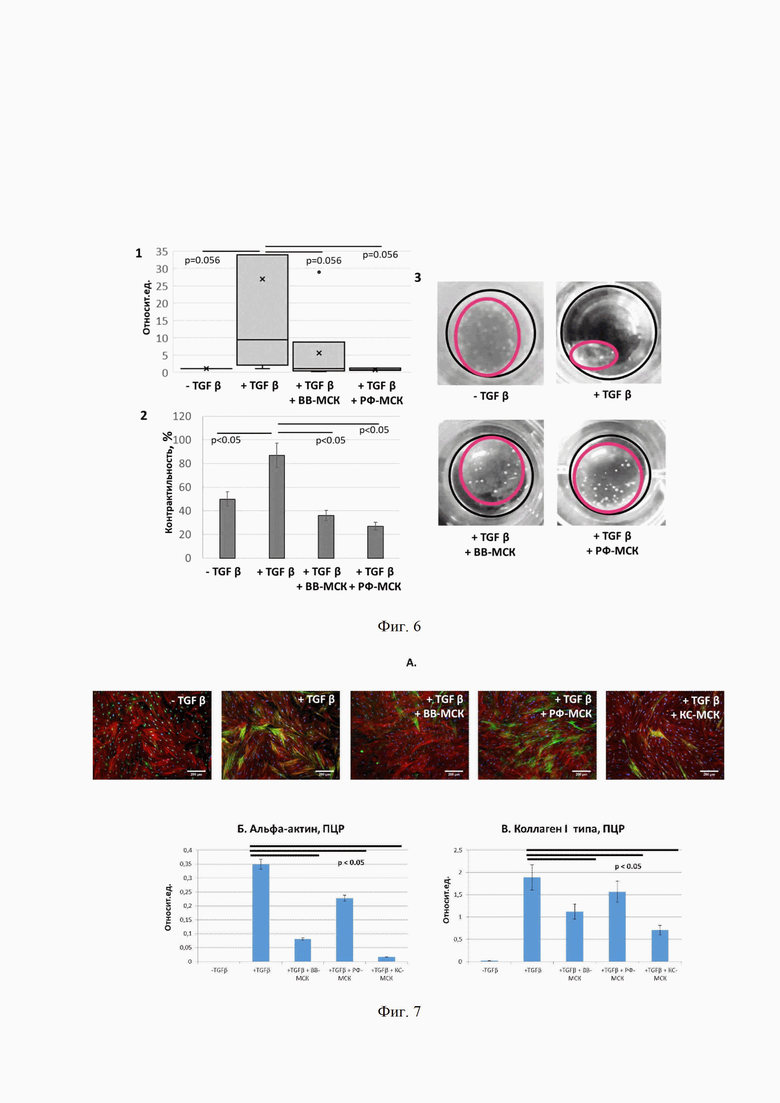
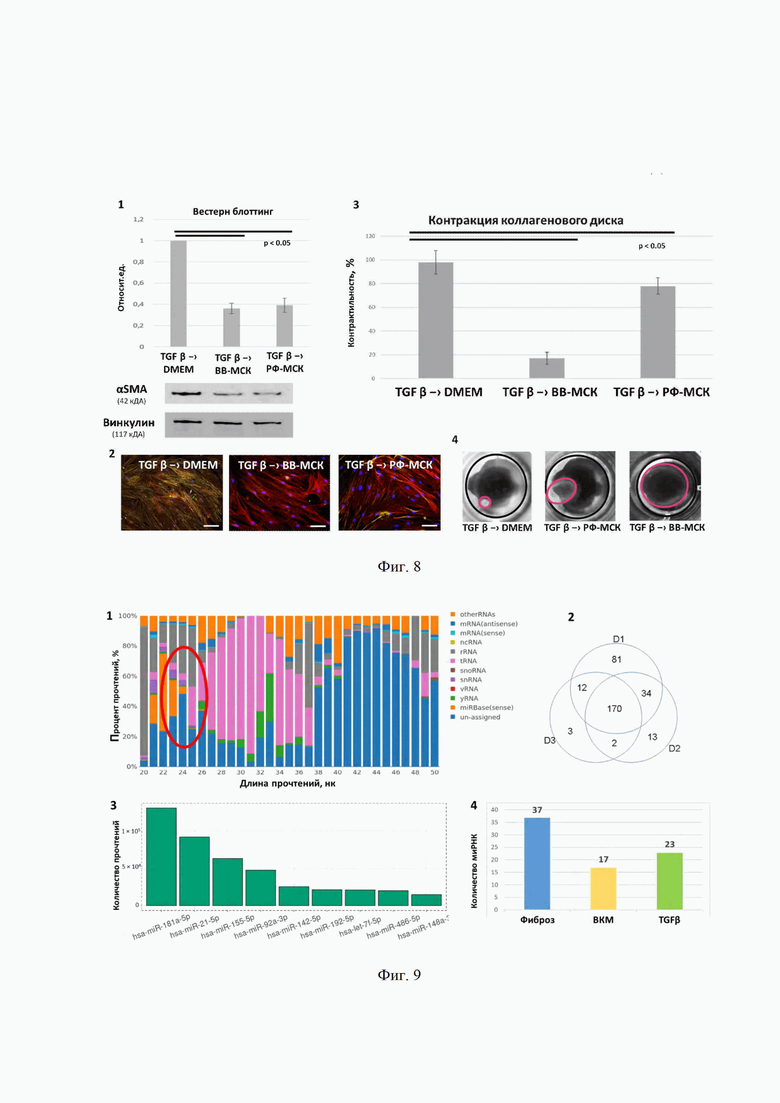
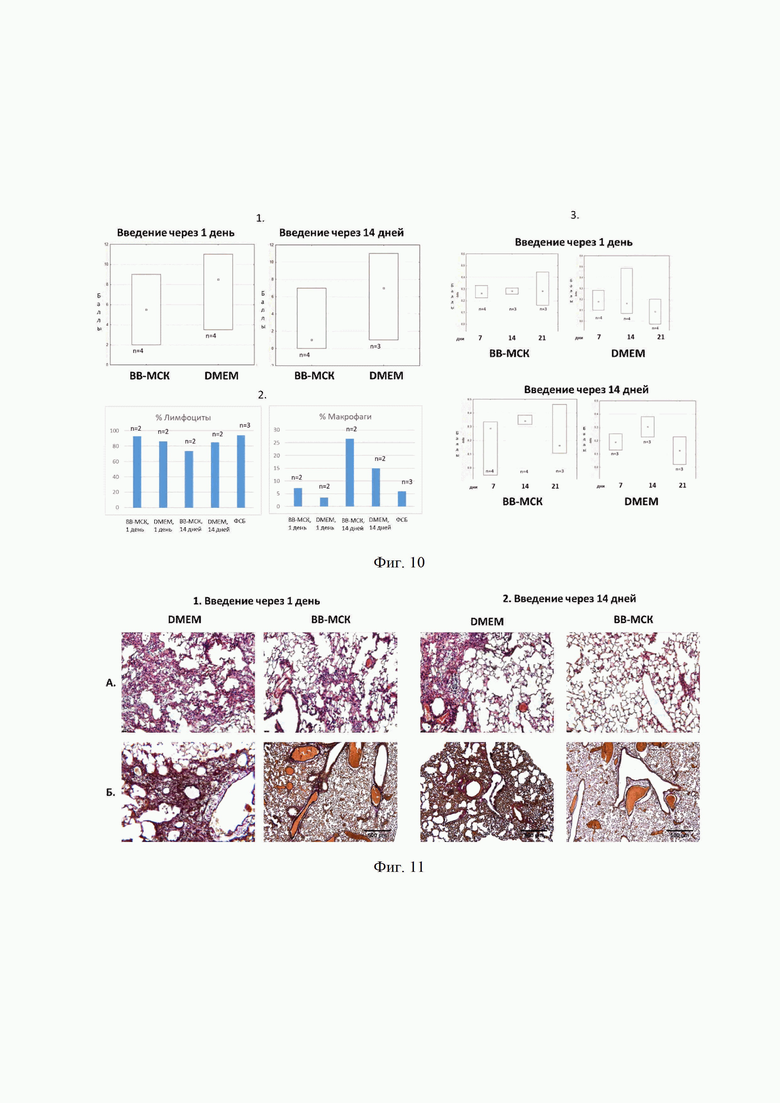
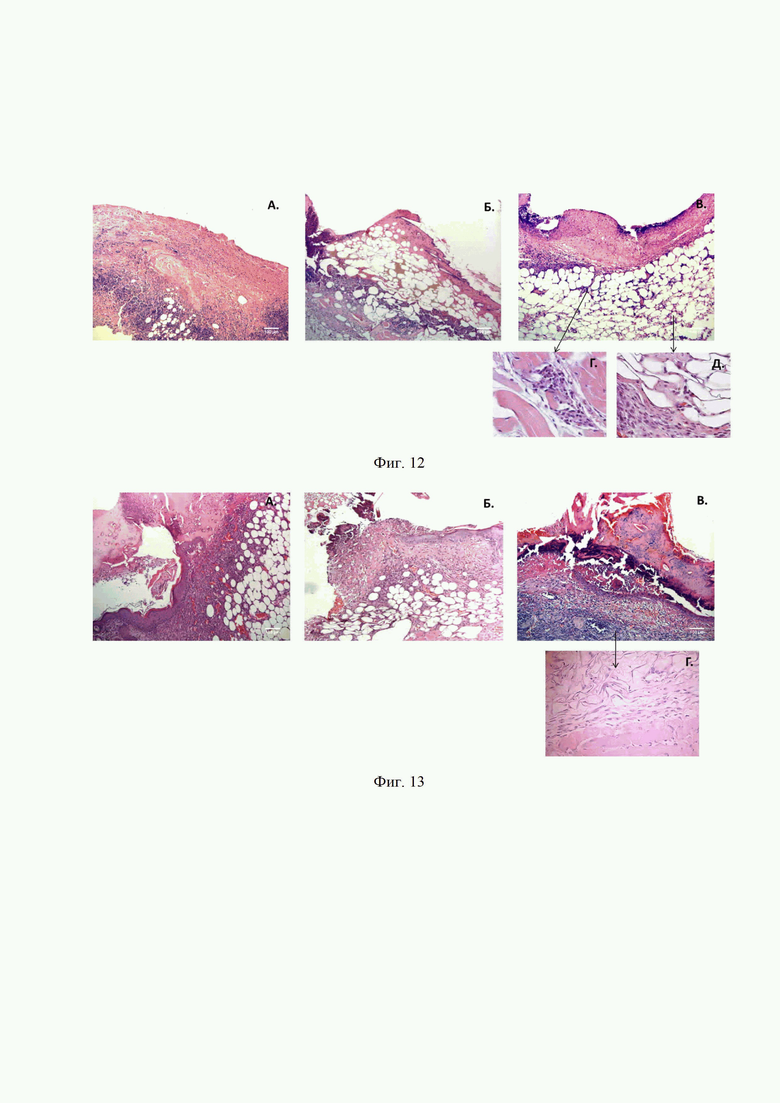
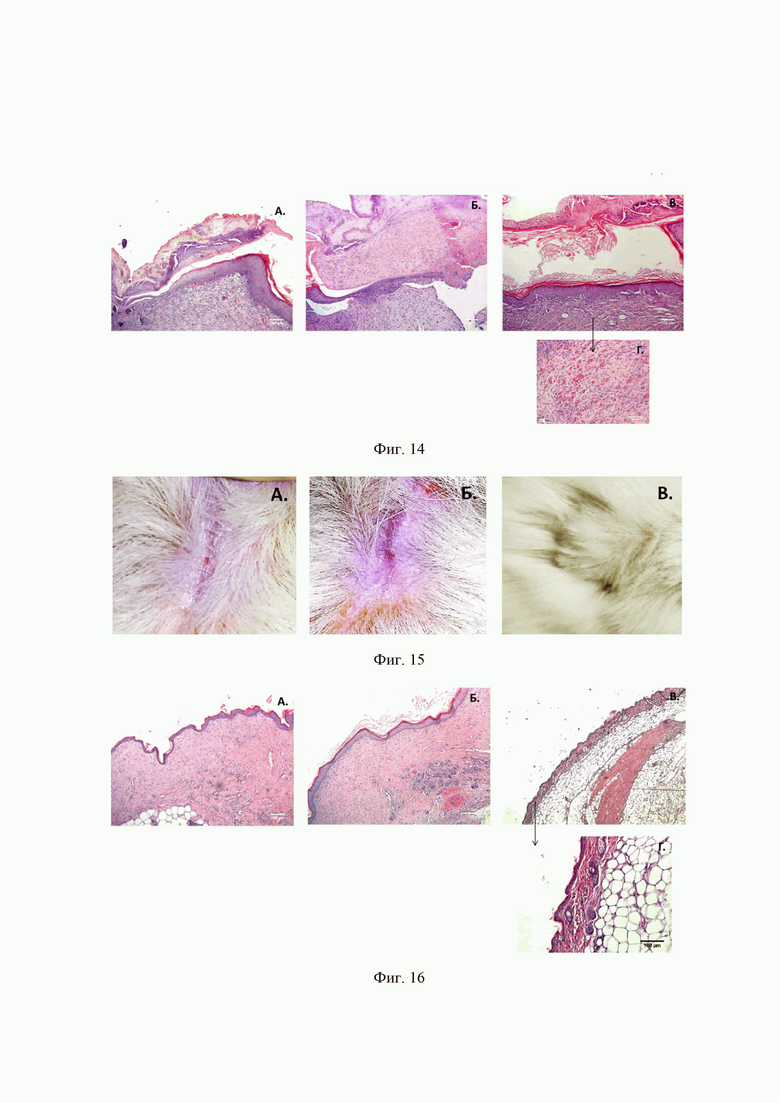
Изобретение относится к области молекулярной и клеточной биологии, медицины и фармакологии, в частности к лекарственному средству для лечения фиброза тканей, способу его получения и способу лечения фиброза, вызванного повреждением тканей, с использованием указанного средства. Лекарственное средство содержит фракцию внеклеточных везикул в составе секретома мезенхимных стромальных клеток (МСК) или изолированную фракцию внеклеточных везикул, выделенных из секретома МСК, имеющих поверхностные маркеры HSP70, CD9, CD81 и CD63, а также размер диаметра от 20 до 420 нм, в количестве 1-3*10^10 частиц на мл. Внеклеточные везикулы переносят в своём составе особые микроРНК. Для осуществления способа получения указанного лекарственного средства сначала культивируют МСК человека до 90% конфлюэнта или монослоя в среде, поддерживающей рост недифференцированных мезенхимных клеток человека. Затем отмывают клетки буферным раствором и кондиционируют МСК в бессывороточной и лишенной продуктов животного происхождения среде роста, поддерживающей жизнеспособность клеток не менее 70% и пригодной для терапевтического применения, в течение 2-7 дней. После этого проводят отбор среды культивирования, содержащей продукты секреции МСК ЖТ человека, удаление из нее остатков клеток и очистку от низкомолекулярных компонентов с последующим концентрированием с использованием ультрафильтрации. Далее проводят оценку указанной среды на содержание фракции внеклеточных везикул, имеющих поверхностные маркеры, определение размера и количества частиц на мл, а также оценку наличия в их составе указанных микроРНК. При этом для получения фракции внеклеточных везикул в составе секретома МСК человека используют фильтры 10 кДа, а для получения изолированной фракции внеклеточных везикул, выделенных из секретома МСК, используют фильтры 1000 кДа, с допустимой величиной погрешности не более 5%. Настоящее изобретение позволяет расширить арсенал средств, эффективно подавляющих фиброз тканей или предотвращающих развитие фиброза тканей. 3 н. и 25 з.п. ф-лы, 16 ил., 4 табл., 10 пр.
1. Лекарственное средство для лечения фиброза тканей, содержащее фракцию внеклеточных везикул в составе секретома мезенхимных стромальных клеток (МСК) или изолированную фракцию внеклеточных везикул, выделенных из секретома МСК, имеющих поверхностные маркеры HSP70, CD9, CD81 и CD63, а также размер диаметра от 20 до 420 нм, в количестве 1-3*10^10 частиц на мл, переносящих в своем составе микроРНК с последовательностью, выбранной из SEQ ID NO 1-61.
2. Средство по п.1, характеризующееся тем, что в составе внеклеточных везикул присутствуют, по меньшей мере, miR-21-5p с последовательностью SEQ ID NO 11 и miR-29c-3p с последовательностью SEQ ID NO 19.
3. Средство по п.2, характеризующееся тем, что в составе внеклеточных везикул присутствует miR-129-5p с последовательностью SEQ ID NO 28.
4. Средство по п.3, характеризующееся тем, что в составе внеклеточных везикул присутствует miR-92а-3p с последовательностью SEQ ID NO 23.
5. Средство по п.4, характеризующееся тем, что в составе внеклеточных везикул присутствуют микроРНК с нуклеотидными последовательностями SEQ ID NO: 1, 4-8, 10, 12-18, 20-22, 24-27, 29-36, 38-46, 48, 50-61.
6. Способ получения средства по п.1 для лечения фиброза тканей, включающий следующие стадии: культивирование МСК человека до 90% конфлюэнта или монослоя в среде, поддерживающей рост недифференцированных мезенхимных клеток человека, отмывку клеток буферным раствором, кондиционирование МСК в бессывороточной и лишенной продуктов животного происхождения среде роста, поддерживающей жизнеспособность клеток не менее 70% и пригодной для терапевтического применения, в течение 2-7 дней, отбор среды культивирования, содержащей продукты секреции МСК ЖТ человека, удаление из нее остатков клеток и очистку от низкомолекулярных компонентов с последующим концентрированием с использованием ультрафильтрации, оценку указанной среды на содержание фракции внеклеточных везикул, имеющих поверхностные маркеры HSP70, CD9, CD81 и CD63, определение размера и количества частиц на мл, а также оценку наличия в их составе микроРНК с последовательностью, выбранной из SEQ ID NO 1-61, для получения лекарственного средства по п.1, при этом для получения фракции внеклеточных везикул в составе секретома МСК человека используют фильтры 10кДа, а для получения изолированной фракции внеклеточных везикул, выделенных из секретома МСК, используют фильтры 1000 кДа, с допустимой величиной погрешности не более 5%.
7. Способ по п.6, характеризующийся тем, что для получения фракции внеклеточных везикул в составе секретома МСК человека культивирование клеток осуществляют в течение 5-7 дней.
8. Способ по п.6, характеризующийся тем, что для получения изолированной фракции внеклеточных везикул, выделенных из секретома МСК, имеющих поверхностные маркеры HSP70, CD9, CD81 и CD63, а также размер диаметра от 20 до 420 нм, в количестве 1-3*10^10 частиц на мл, переносящих в своем составе микроРНК с последовательностью, выбранной из SEQ ID NO 1-61, культивирование клеток осуществляют в течение 2-3 дней.
9. Способ по п.6, характеризующийся тем, что МСК представляют собой первично выделенные МСК человека, культивированные до 2-5 пассажей.
10. Способ по п.6, характеризующийся тем, что МСК выделены из жировой ткани.
11. Способ по п.6, характеризующийся тем, что МСК представляют собой иммортализованные МСК жировой ткани человека.
12. Способ по п.6, характеризующийся тем, что среда, поддерживающая рост недифференцированных мезенхимных клеток человека, представляет собой раствор, содержащий базовую среду - AdvanceSTEM Cell Culture Media, и добавку - AdvanceSTEM Stem Cell Growth Supplement, при этом добавку берут в объеме 9-11% на 100% объема базовой среды.
13. Способ по п.6, характеризующийся тем, что в качестве буферного раствора для отмывки клеток от компонентов среды роста используют раствор Хэнкса, при этом отмывку клеток осуществляют трех-пятикратным размещением клеток в упомянутый раствор из расчета 0,1-0,2 мл раствора на см2 клеток на 5-10 минут.
14. Способ по п.6, характеризующийся тем, что в качестве базальной среды для кондиционирования используется ДМЕМ с низким содержанием глюкозы без фенолового красного или другая среда роста, поддерживающая жизнеспособность МСК человека в течение всего срока кондиционирования.
15. Способ по п.6, характеризующийся тем, что удаление из среды культивирования остатков клеток осуществляют центрифугированием.
16. Способ по п.6, характеризующийся тем, что очистку среды культивирования осуществляют посредством ее ультрафильтрации с удалением низкомолекулярных соединений массой менее 10 кДа с допустимой величиной погрешности не более 5%.
17. Способ по п.15, характеризующийся тем, что центрифугирование осуществляют при 5000±10 об/мин, температуре 6±2°C в течение 10±1 минут.
18. Способ по п.6, характеризующийся тем, что очистку от низкомолекулярных компонентов с последующим фракционированием и концентрированием осуществляют с использованием системы фильтрации в тангенциальном потоке, обеспечивающей удаление низкомолекулярных компонентов заданного фильтром размера.
19. Способ по п.18, характеризующийся тем, что в качестве системы фильтрации в тангенциальном потоке используют Minim II с использованием ультрафильтрационных кассет Minimate TFF capsule, PALL.
20. Способ по п.6, характеризующийся тем, что очистку от низкомолекулярных компонентов с последующим фракционированием и концентрированием осуществляют методом ультрафильтрации с использованием центриконов Amicon (Sigma, Италия).
21. Способ лечения фиброза, вызванного повреждением тканей, с помощью средства по п.1, полученного способом по п.6, путем введения в область фиброза с целью предупреждения прогрессирования и стимуляции реверсии фибротических изменений.
22. Способ лечения по п.21, характеризующийся тем, что фиброз вызван механическими, химическими или термическими повреждениями тканей.
23. Способ лечения по п.21, характеризующийся тем, что фиброз развивается в тканях легких.
24. Способ лечения по п.23, характеризующийся тем, что фиброз представляет собой идиопатический фиброз легких.
25. Способ лечения по п.23, характеризующийся тем, что фиброз развивается в результате интерстициальных заболеваний легких.
26. Способ лечения по п.23, характеризующийся тем, что фиброз развивается в результате вирусной пневмонии.
27. Способ лечения по п.26, характеризующийся тем, что фиброз развивается в результате вирусной пневмонии, вызванной коронавирусами.
28. Способ лечения по п.23, характеризующийся тем, что фиброз развивается в результате профессиональных заболеваний легких.
| WO 2019043709 A1, 07.03.2019 | |||
| Dinh P.U.C | |||
| et al | |||
| Inhalation of lung spheroid cell secretome and exosomes promotes lung repair in pulmonary fibrosis // Nature communications | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| - Т | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| - No | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - С | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Shentu T.P | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2022-03-15—Публикация
2020-11-13—Подача