Группа изобретений относится к области биологии и медицины и может быть использовано для стимуляции полнослойных раневых дефектов кожи в практическом здравоохранении и ветеринарии для ускорения репаративных процессов и заживления ран.
Распространенность острых и хронических ран как в России, так и за рубежом остается на высоком уровне. Нарушение заживления ран могут сопровождаться различными осложнениями, включая раневую инфекцию, формирование гипертрофированных рубцов и келоидов. В этой связи в настоящее время особое внимание уделяется разработке новых материалов для создания биодеградируемых покрытий, свойства которых позволят стимулировать заживление кожных ран.
Известны раневые покрытия, основой которых является пленка, содержащая в своем составе полилактид [патенты RU №№2666599, CN №115487341]. Способы изготовления данных пленок [патенты RU №2540468, CN №110180013] заключаются в смешивании полилактида с другими сополимерами до формирования пленки регулируемой толщины без дальнейшего структурирования. В процессе изготовления активные компоненты могут быть сорбированы на поверхность таких пленок или добавлены в её состав для обеспечения адресной доставки и пролонгированного высвобождения за счет растворения с поверхности и/или деградации структуры самой пленки.
Однако подобные типы раневых покрытий имеют выраженную зависимость от характера химических веществ, сорбированных на пленку или включенных в ее состав.
Известны фибриллярные полилактидные раневые покрытия [патенты RU №2120306, CN № 101439200; Bi H., Feng T., Li B., Han Y. In vitro and in vivo comparison study of electrospun PLA and PLA/PVA/SA fiber membranes for wound healing // Polymers (Basel). - 2020. - V.12, №4. - P. 839; Богданова А.С., Соколова А.И., Павлова Е.Р., Клинов Д.В., Багров Д.В. Investigation of cellular morphology and proliferation on patterned electrospun PLA-gelatin mats Journal of Biological Physics, 47, 205-214 (2021)], структура которых обеспечивает больший потенциал для загрузки активных компонентов путем сорбции на поверхности фибрилл по сравнению с покрытиями пленочного типа. Данные раневые покрытия изготавливаются путем электроспининга. Загрузка активных компонентов в такой тип раневых покрытий осуществляется либо добавлением веществ в состав раствора для электроформования, либо сорбцией веществ на поверхности уже изготовленных фибрилл.
Однако для фибриллярных раневых покрытий, также как и в случае с пленочными покрытиями, сохраняются ограничения по классам отдельных компонентов, сорбируемых на поверхность. Изготовление данного вида покрытий требует применение метода электроспининга, который характеризуется использованием дорогостоящего оборудования.
Кроме того, все способы изготовления описанных ранее покрытий (смешение, электроспининг) позволяют добавлять в смесь полимеров только стабильные молекулы с определенными химическими свойствами и могут быть реализованы не для всех активных компонентов, используемых для заживления ран.
Известны раневые покрытия с микрокамерной структурой, позволяющие загружать в качестве активного вещества любые компоненты, например, покрытие для высвобождения адреналина [Polymer microchamber arrays for geometry-controlled drug release: a functional study in human cells of neuronal phenotype / O. Kopach, K.Zheng,a O.A. Sindeeva et al. // The Royal Society of Chemistry. - 2019. - № 7. - Р. 2358-2371], микрокамеры которого изготовлены из сополимеров полилактида с гликолидом с использованием штампа. При этом загрузка активного вещества и дальнейшее запечатывание микрокамер происходит на стекле. При этом высвобождение активного вещества происходит путем открытия микрокамер под влиянием ультразвука.
Однако, открытие микрокамер ультразвуком происходит порционно, а не постепенно, что затрудняет пролонгированное высвобождение активных компонентов. Практическое применение таких покрытий ограничено в связи с необходимостью использования ультразвуковой установки.
Известно также полилактидное раневое покрытие с микрокамерной структурой [Site-specific release of reactive oxygen species from ordered arrays of microchambers based on polylactic acid and carbon nanodots / A.V. Ermakov et al. //J. Mater. Chem. B. 2020. №8. Р. 7977-7986], высвобождающее в качестве активного компонента кислородсодерщее вещество. Способ изготовления включает покрытие шаблона с массивом лунок раствором 1,5% полилактида в хлороформе с равномерным распределением его по стенкам лунок и последующим высушиванием при комнатной температуре. Затем заполняют сформированные микрокамеры активным веществом - перкарбонатом натрия. Предварительно формируют штамповкой на стекле пленку из полилактида, которую приводят в контакт с открытой стороной заполненных лунок. После высушивания шаблон удаляют, в результате чего на стекле образуется массив микрокамер с полимерной оболочкой в полости которых содержится активное вещество с последующим механическим отславиванием их от стекла, образуя при этом массив отдельно стоящих микрокамер. Дальнейшее открытие контейнеров микрокамер с последующим выходом активного вещества осуществляется ультразвуком или инфракрасным лазером.
Однако, способ формирования массива микрокамер, основанный на использовании штампа, запечатывание которого происходит на стекле без формирования эластичной подложки, создает риски технологической травматизации микрокамер и частичной потери активного вещества при хранении и нанесении на рану.
Наиболее близким аналогом к заявляемому полилактидному раневому покрытию является раневое покрытия [патент RU №2788283] в виде массивов полимерных микрорезервуаров (микрокамер), изготовленных с применением шаблона с рельефом в виде лунок микронного размера. Площадь покрытия соответствует размеру раневого дефекта и составляет порядка 1 см2. Толщина стенок микрокамер покрытия составляет 0,3-0,5 мкм, горизонтальное сечение микрокамер покрытия имеет форму квадрата со стороной 10 мкм, высота микроконтейнеров составляет 12 мкм. Массив микроконтейнеров иммобилизован на подложке, образованной желатином толщиной 2 мм. Микрокамеры покрытий загружены раствором таниновой кислоты (Sigma-Aldrich, Германия) с концентрацией 1мг/мл.
Недостатком данного покрытия является толщина внешнего слоя в размере 2 мм желатиновой подложки, снижающая эластичность покрытия. Кроме того гидрофобные свойства полилактида затрудняют адгезию в ране, что в сочетании с низкой эластичностью приводит к отклеиванию отдельных участков покрытия от раны, создавая риски инфицирования этих участков.
Задачей заявляемой группы изобретений является разработка микрокамерного покрытия со сбалансированными адгезивными и эластичными свойствами, обеспечивающими механическую прочность изделия, позволяющую применять его на различных участках кожного покрова, в том числе в зоне сгибательных поверхностей суставов, и снижающими риск отслоения покрытия от раневой поверхности, а также создание технологии изготовления покрытия, позволяющей дозированно регулировать толщину внутреннего и внешнего слоя в зависимости от локализации повреждения и снизить до минимума возможность появления скрытых дефектов.
Сущность заявляемой группы изобретений заключается в разработке
раневого микрокамерного покрытия из полилактида, представляющего собой многослойную структуру, состоящую из глянцевой защитной основы, на которой последовательно друг за другом расположены внешний поддерживающий слой в виде гибкой пленки, сформированной из 50 мас. % водного раствора желатина, и иммобилизованный на нем основной активный слой в виде массива полимерных микрокамер с загруженным в них модулятором оксидативного гомеостаза, внешний поддерживающий слой сформирован толщиной 250-500 мкм, микрокамеры выполнены из 3 мас. % полилактида в хлороформе и имеют овальную форму, на основной активный слой покрытия дополнительно нанесен внутренний гидрофильный адгезивный слой толщиной 30-150 мкм в зоне вершины полимерных микрокамер, сформированный из 1 мас. % водного раствора желатина.
В способе получения раневого микрокамерного покрытия из полилактида, заключающемся в последовательном создании многослойной структуры, для чего формируют: сначала внешний поддерживающий слой покрытия путем распределения геля, содержащего 50 мас. % раствор желатина, по глянцевой поверхности с последующим высушиванием до образования гибкой пленки, затем основной активный слой посредством покрытия шаблона с массивом лунок раствором полилактида в хлороформе с равномерным распределением его по стенкам лунок, последующим высушиванием при комнатной температуре и их заполнением модулятором оксидативного гомеостаза, после проводят иммобилизацию основного активного слоя на внешнем поддерживающем слое за счет смачивания последнего полилактидом в хлороформе, приведением его в контакт с открытой поверхностью заполненных лунок, запечатывая их с образованием массива замкнутых полимерных микрокамер, содержащих в своей полости модулятор оксидативного гомеостаза, и удаления шаблона, при формировании внешнего поддерживающего слоя регулировку толщины обеспечивают путем его открепления после высушивания от глянцевой поверхности с последующим равномерным механическим растягиванием на 10-50% от начальной площади и креплением на глянцевую защитную основу, при создании основного активного слоя используют 3 мас. % полилактид в хлороформе и шаблон с массивом лунок овальной формы, на заключительном этапе дополнительно формируют последний внутренний гидрофильный адгезивный слой, регулирование толщины которого обеспечивают путем последовательного повторения цикла, состоящего из поэтапного смачивания основного активного слоя 1 мас. % водным раствором желатина, равномерным его распределением за счет собственной текучести и высушиванием до образования пленочной поверхности.
Технический результат заявляемой группы изобретения.
Такой технический прием как дополнительное формирование внутреннего гидрофильного адгезивного слоя из водного раствора желатина позволяет обеспечить сцепление изделия с раневой поверхностью за счет их плотного равномерного прилегания друг к другу. Использование при этом именно 1 мас. % раствора желатина позволяет снизить вязко-упругие свойства получаемого геля, способствуя повышению его текучести, с целью формирования равномерного слоя на неровной поверхности, образованной массивом полимерных микрокамер и выемками между ними. При этом данная концентрация водного раствора желатина обеспечивает формирование пространственной сетки геля, образуя после высушивания равномерный пленочный слой на поверхности.
Выполнение покрытия в виде многослойной структуры, в которой основной активный слой с обеих сторон защищен внешним и внутренним желатиновыми слоями позволяет обеспечить механическую прочность изделия. Варьирование толщины желатиновых слоев осуществляют в зависимости от локализации поврежденной поверхности с учетом регулирования способности изделия изгибаться без разрушения путем дозированного изменения толщины внешнего и внутреннего слоев, максимально сохраняя для каждого случая применения адгезивные и эластичные свойства.
При увеличении концентрации полимолочной кислоты в хлороформе до 3% возрастают прочностные показатели пленки, образующей микрокамеры, за счет увеличения формоустойчивости используемого раствора. При этом данная концентрация не влечет увеличение вязкости раствора, которое препятствовало бы равномерному растеканию по поверхности шаблона с лунками. Применение последнего с лунками овальной формы позволяет снизить до минимума возможность появления скрытых дефектов на поверхности образованных микрокамер в виде микротрещин, возникающих в момент удаления шаблона.
Заявляемое изобретение поясняется с помощью Фиг.1-2.
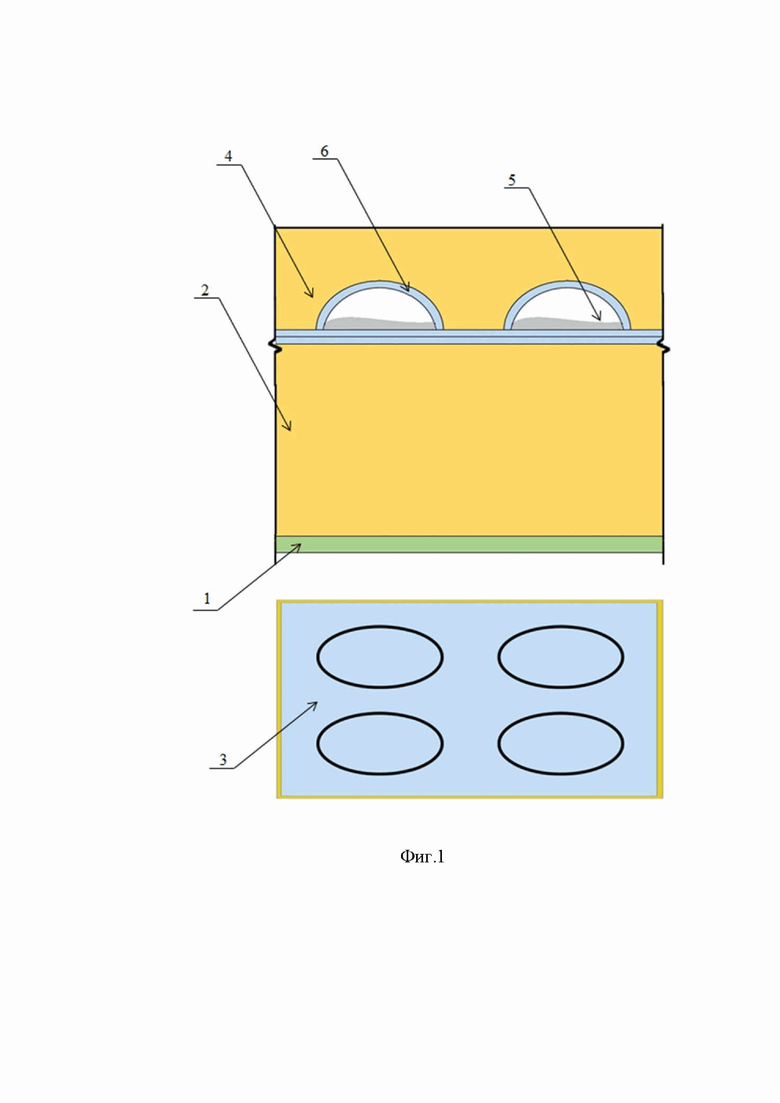
На Фиг. 1 схематично изображена многослойная структура покрытия, где позициями 1-6 обозначены:
1 - глянцевая защитная основа;
2 - внешний поддерживающий слой;
3 - основной активный слой;
4 - внутренний гидрофильный адгезивный слой;
5 - модулятор оксидативного гомеостаза;
6 - стенки микрокамер основного активного слоя.
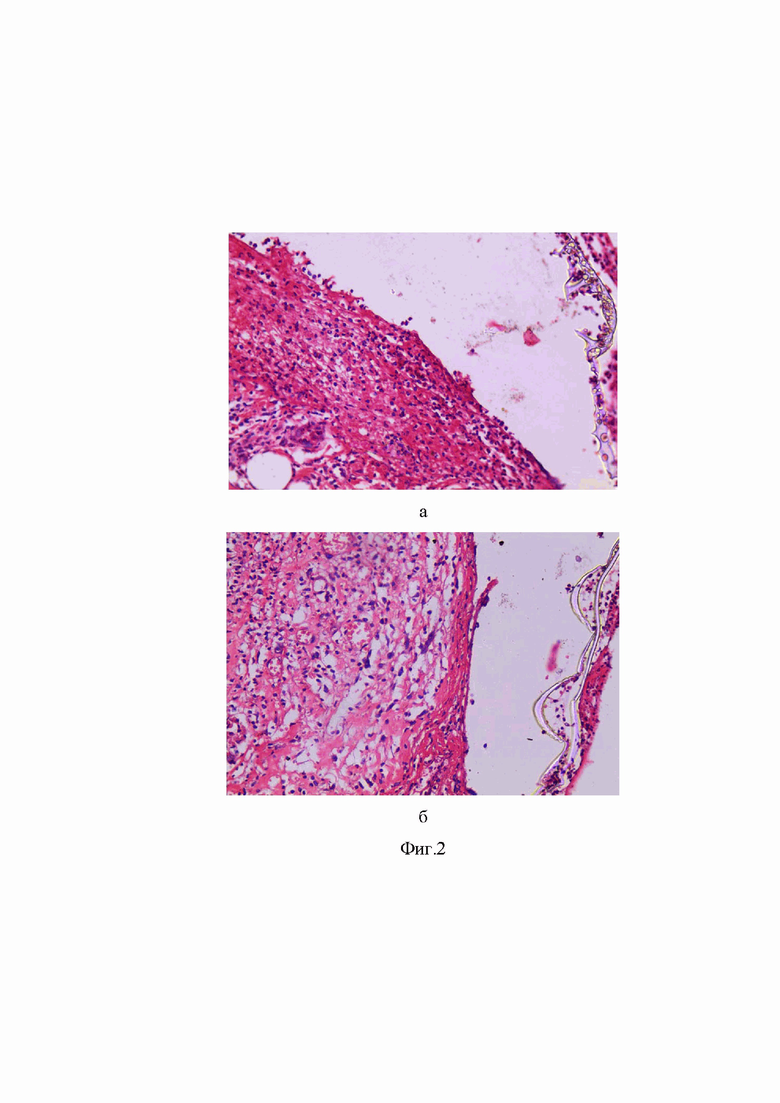
На Фиг.2 изображены микрофотографии гистологического препарата раневого дефекта кожи закрытого разработанным раневым микрокамерным покрытием из полилактида. окр. Г-Э. об. 20х., где визуалированы:
а - открытые микрокамеры;
б - закрытые микрокамеры.
Раневое микрокамерное покрытие из полилактида представляет собой многослойную структуру, состоящую из последовательно расположенных друг за другом на глянцевой защитной основе 1 внешнего поддерживающего 2, основного активного 3 и внутреннего гидрофильного адгезивного 4 слоев. Внешний поддерживающий слой 2 выполнен в виде гибкой пленки толщиной 250-500 мкм, сформированной из 50 мас. % водного раствора желатина. На нем иммобилизован основной активный слой 3 в виде массива полимерных микрокамер овальной формой, полость которых загружена модулятором 5 оксидативного гомеостаза. В качестве последнего могут быть использованы про- или антиоксиданты в зависимости от характера раневого процесса, а именно риска инфицирования, наличия в ране некротических масс, стадии репаративного процесса, кратности наложения покрытия. При этом стенки микрокамер 6 выполнены из 3 мас. % полилактида в хлороформе. Внутренний гидрофильный адгезивный слой 4 сформирован из 1 мас. % водного раствора желатина и имеет толщину в зоне вершины микрокамер 30-150 мкм.
Способ получения раневого микрокамерного покрытия из полилактида осуществляют следующим образом.
Процесс изготовления покрытий включает в себя последовательное создание многослойной структуры, расположенной на глянцевой защитной основе, препятствующей деформации покрытия и склеивания её отдельных участков адгезивным слоем, а также выступающей в виде подложки трафарета при разрезке и аппликатора при нанесении на рану. При наложении покрытия на рану глянцевую защитную поверхность удаляют.
Сначала формируют внешний поддерживающий слой покрытия. Для чего готовят гель, содержащий 50 мас. % водный раствор желатина, путем размешивания последнего в течение 3 часов при температуре 75°С до полного растворения желатина и получения равномерного цвета. Выкапывают гель на глянцевую поверхность, по площади которой он равномерно распределяется за счет собственной текучести до минимально возможной толщины, которая ограничена силой поверхностного натяжения геля и составляющая порядка 500 мкм для состава, содержащего 50 мас. % желатина. Гель высушивают до образования гибкой пленки. Затем регулируют толщину внешнего поддерживающего слоя путем его открепления от глянцевой поверхности с последующим равномерным механическим растягиванием на 10-50% от начальной площади и креплением на глянцевую защитную основу. Равномерное механическое растягивание внешнего может быть обеспечено путем одномоментного придавливания образованной гибкой пленки ровной поверхностью, например, стеклянной, позволяющей визуально контролировать площадь растяжения.
Затем создают основной активный слой. С целью формирования полимерных микрокамер для загрузки активного действующего вещества покрывают шаблон с массивом лунок овальной формы 3 мас. % раствором полилактида в хлороформе, равномерно распределяя его по их стенкам путем плавного переворачивания шаблона в разные стороны, создавая, тем самым, ровный слой. После чего созданную полимерную поверхность высушивают при комнатной температуре до образования пленки. Лунки шаблона, покрытые пленкой из полилактида, заполняют активным действующим веществом - модулятором оксидативного гомеостаза. В качестве последнего используют прооксидант - кристаллы перкарбогната натрия или антиоксидант - порошок или раствор с различной концентрацией таниновой кислоты. В созданные лунки могут быть загружены как жидкие, так и сухие вещества. Например, перекись водорода обладает низкой стабильностью в растворе, поэтому в лунки загружают кристаллы перкарбоната натрия в виде твердого вещества. При контакте с водой жидкости раневого отделяемого из кристаллов перкарбоната натрия образуется перекись водорода.
После заполнения лунок модулятором оксидативного гомеостаза проводят иммобилизацию основного активного слоя на внешнем поддерживающем слое за счет смачивания последнего полилактидом в хлороформе, приведением его в контакт с открытой поверхностью заполненных лунок, запечатывая их с образованием массива замкнутых полимерных микрокамер, содержащих в своей полости них модулятор оксидативного гомеостаза. После испарения хлороформа шаблон с массивом лунок удаляют, получив соединенные между собой массив отдельно стоящих замкнутых микрокамер основного активного слоя на гибкой пленке внешнего поддерживающего слоя. На заключительном этапе дополнительно формируют последний внутренний гидрофильный адгезивный слой толщиной в зоне вершины микрокамер 30-150 мкм путем последовательного повторения цикла, состоящего из поэтапного смачивания основного активного слоя 1 мас. % водным раствором желатина, равномерным его распределением за счет собственной текучести и высушиванием до образования пленочной поверхности.
Примеры
По заявляемой технологии получения раневого микрокамерного покрытия из полилактида были изготовлены экспериментальные образцы изделия в виде многослойной структуры из последовательно расположенных друг за другом на глянцевой защитной основе внешнего поддерживающего, основного активного и внутреннего гидрофильного адгезивного слоев. Типо-размеры изготовленных образцов были различны, а именно 2 образца с толщиной внешнего поддерживающего 250 мкм, основного активного - 30 мкм и внутреннего гидрофильного адгезивного слоя в зоне вершины полимерных микрокамер - 30 мкм; 2 образца с толщиной внешнего поддерживающего 350 мкм, основного активного - 30 мкм и внутреннего гидрофильного адгезивного слоя в зоне вершины полимерных микрокамер - 90 мкм; 2 образца с толщиной внешнего поддерживающего 500 мкм, основного активного - 30 мкм и внутреннего гидрофильного адгезивного слоя в зоне вершины полимерных микрокамер - 150 мкм. Внешний поддерживающий слой покрытия был создан путем выкапывания геля, содержащего 50 мас. % водный раствор желатина. Полимерные микрокамеры были выполнены из 3 мас. % раствора полилактида в хлороформе. При формировании полимерных микрокамер использовали шаблон с лунками овальной формы, что позволило исключить травматизацию стенок микрокамер при удалении шаблона. В сравнении с результатами изготовления предыдущей модификации раневого покрытия [патент RU №2788283] с использованием шаблона с лунками прямоугольной формы, во время производства которых материал затекал в углы формы и было затруднено его открепление после высушивания в этих зонах, приводя к разрыву пленки или возникновению трещин, при удалении полимерного покрытия из шаблона с лунками овальной формы данных проблем не наблюдалось, структура микрокамер была полностью сохранена.
Внутренний гидрофильный адгезивный слой формировался из 1 мас. % водного раствора желатина. В одном образце каждого типа-размера в микрокамеры был загружен модулятором оксидативного гомеостаза - порошок таниновой кислоты, соответственно в оставшихся образцах - кристаллы перкарбогната натрия.
Все образцы покрытия были эластичными, легко сгибались и повторяли рельеф горизонтальной поверхности, на которую их размещали. Для проведения испытания на эластичность был использован метод изгиба на подготовленных металлических стержнях цилиндрической формы. Диаметр стержней составлял 5, 10 и 15 мм. После открепления микрокамерного раневого покрытия с толщиной внешнего поддерживающего слоя 250 мкм и толщиной внутреннего гидрофильного адгезивного слоя 30 мкм и сгибании его на стержнях было установлено, что покрытие даже на стержне с минимальным диаметром растягивалось и принимало форму без растрескивания и разрыва поверхности, что свидетельствовало о хорошей эластичности полученного изделия. Покрытие с толщиной внешнего поддерживающего слоя 350 мкм и толщиной внутреннего гидрофильного адгезивного слоя 90 мкм и сгибании его на стержнях на стержне с диаметром 10 и 15 мм растягивалось и принимало форму без растрескивания и разрыва поверхности, что свидетельствовало о хорошей эластичности полученного изделия, а на стержне с диаметром 5 мм - были затруднения при его укладке с деформацией внутреннего гидрофильного адгезивного слоя, что в дальнейшем бы привело к его разрушению. При исследовании последней партии изделий с толщиной внешнего поддерживающего слоя 500 мкм и толщиной внутреннего гидрофильного адгезивного слоя 150 мкм, уже на стержне с диаметром 10 мм наблюдались описанные выше затруднения. Однако перерастяжение слоев при исследовании всех образцов изделий с возникновением микротрещин не наблюдалось, что свидетельствует о высокой эластичности полученных раневых микрокамерных покрытий и необходимость в разных типо-размерах обосновывается только локализацией поврежденной поверхности в зависимости от её функциональной нагрузки, а именно необходимости сгибания-разгибания.
Адгезию полученного полилактидного микрокамерного покрытия проверяли методом параллельных надрезов. Из каждого образца было выполнено покрытие площадью 1 см2, которое было надразрезано на толщину внутреннего гидрофильного адгезивного слоя на равномерные квадраты 2х2 мм. После нанесения надрезов для удаления отслоившихся кусочков покрытия проводили мягкой кистью по поверхности решетки в диагональном направлении по пять раз в прямом и обратном направлении. При анализе полученных результатов было выявлено незначительное отслаивание покрытия у всех образцов в виде мелких чешуек в местах пересечения линий решетки. Нарушение наблюдалось не более, чем на 5 % поверхности решетки. Испытания были сопоставлены между двумя образцами покрытий каждого типа-размера с получением одинакового результат, что свидетельствовало о высоких адгезионных свойствах внутреннего гидрофильного адгезивного слоя полилактидного микрокамерного покрытия, полученного по заявляемому способу изготовления.
Для подтверждения биологических свойств покрытия было проведено испытание на лабораторных крысах-самцах. Наркотизированным животным на экспериментально сформированные раневые дефекты в межлопаточной области были приклеены непосредственно после формирования раны полилактидные микрокамерные покрытия площадью 1 см2. Через 3 суток животные были выведены из эксперимента. Были изготовлены гистологические препараты (по стандартной методике) зоны раневого дефекта, окрашенные гематоксилином и эозином. При микроскопии препаратов в зоне раневого дефекта визуализировались элементы раневого покрытия, что свидетельствовало о его удержании в ране без дополнительной фиксации на протяжении 3 суток (удовлетворительные адгезивные свойства). При этом было установлено, что большая часть микрокамер открыта (Фиг. 2а). Отдельные микрокамеры покрытия имели изначальную структуру (Фиг. 2б). Данный пример иллюстрирует, что микрокамеры покрытия открываются постепнно в срок до 3 дней после нанесения под влиянием раневой среды, выделяя активные компоненты.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки биосовместимости раневых покрытий | 2022 |
|
RU2788283C1 |
| Фармацевтическая композиция противоопухолевого действия и способ ее производства | 2023 |
|
RU2831545C1 |
| ПЕРЕВЯЗОЧНОЕ СРЕДСТВО | 2004 |
|
RU2270646C2 |
| ПРОФИЛАКТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ВЕЩЕСТВ ФЕНОЛЬНОЙ ПРИРОДЫ В ЛИПОСОМНОЙ ФОРМЕ | 2008 |
|
RU2372929C1 |
| Антибактериальное покрытие на ортопедический имплантат из титана и его сплавов и способ его получения (варианты) | 2023 |
|
RU2816023C1 |
| СРЕДСТВО В ВИДЕ ПЛЕНКИ ЛЕКАРСТВЕННОЙ, СОДЕРЖАЩЕЙ МЕЛАТОНИН, ДЛЯ ЛЕЧЕНИЯ ТЕРМИЧЕСКОЙ ТРАВМЫ | 2020 |
|
RU2751048C1 |
| ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ ПЛЕНОК, ЭЛЮИРУЮЩИХ ЛЕКАРСТВЕННЫЕ СРЕДСТВА | 2022 |
|
RU2807080C1 |
| АКТИВНЫЙ ПОЛИМЕРНЫЙ СЛОЙ ИЗ ПРОИЗВОДНЫХ ХИТИНА, В ЧАСТНОСТИ, ДЛЯ ПОВЯЗОК И ЕГО ПРИМЕНЕНИЕ | 2013 |
|
RU2683273C2 |
| Композиционное полимерное раневое покрытие на основе нановолокон | 2017 |
|
RU2647609C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ПРОТЕЗОВ СОСУДОВ МАЛОГО ДИАМЕТРА С НИЗКОЙ ПОРИСТОСТЬЮ(ВАРИАНТЫ) | 2014 |
|
RU2572333C1 |
Группа изобретений относится к области биологии и медицины и может быть использована для ускорения репаративных процессов и заживления ран. Раневое микрокамерное покрытие представляет собой многослойную структуру, состоящую из глянцевой защитной основы, на которой последовательно друг за другом расположены внешний поддерживающий, основной активный и внутренний гидрофильный адгезивный слои. Внешний поддерживающий слой выполнен в виде гибкой пленки, сформированной из 50 мас. % водного раствора желатина, с толщиной 250-500 мкм. Основной активный слой, иммобилизованный на внешний поддерживающий слой, сформирован из 3 мас. % полилактида в хлороформе в виде массива полимерных микрокамер овальной формы с загруженным в них модулятором оксидативного гомеостаза. На основной активный слой покрытия дополнительно нанесен внутренний гидрофильный адгезивный слой толщиной 30-150 мкм в зоне вершины микрокамер, сформированный из 1 мас. % водного раствора желатина. Предложен также способ получения указанного раневого микрокамерного покрытия. Изобретение обеспечивает механическую прочность изделия, что позволяет использовать его на различных участках кожного покрова, в том числе в зоне сгибательных поверхностей суставов, при этом снизив риск отслоения покрытия от раневой поверхности. Полученное раневое покрытие характеризуется оптимальными адгезионными и эластичными свойствами за счет дозированного регулирования толщины внутреннего и внешнего слоев, а также сниженной до минимума возможностью появления скрытых дефектов. 2 н.п. ф-лы, 2 ил., 1 пр.
1. Раневое микрокамерное покрытие из полилактида, представляющее собой многослойную структуру, состоящую из глянцевой защитной основы, на которой последовательно друг за другом расположены внешний поддерживающий слой в виде гибкой пленки, сформированной из 50 мас. % водного раствора желатина, и иммобилизованный на нем основной активный слой в виде массива полимерных микрокамер с загруженным в них модулятором оксидативного гомеостаза, отличающееся тем, что внешний поддерживающий слой сформирован толщиной 250-500 мкм, микрокамеры выполнены из 3 мас. % полилактида в хлороформе и имеют овальную форму, на основной активный слой покрытия дополнительно нанесен внутренний гидрофильный адгезивный слой толщиной 30-150 мкм в зоне вершины полимерных микрокамер, сформированный из 1 мас. % водного раствора желатина.
2. Способ получения раневого микрокамерного покрытия из полилактида, заключающийся в последовательном создании многослойной структуры, для чего формируют: сначала внешний поддерживающий слой покрытия путем распределения геля, содержащего 50 мас. % раствор желатина, по глянцевой поверхности с последующим высушиванием до образования гибкой пленки, затем основной активный слой посредством покрытия шаблона с массивом лунок раствором полилактида в хлороформе с равномерным распределением его по стенкам лунок, последующим высушиванием при комнатной температуре и их заполнением модулятором оксидативного гомеостаза, после проводят иммобилизацию основного активного слоя на внешнем поддерживающем слое за счет смачивания последнего полилактидом в хлороформе, приведением его в контакт с открытой поверхностью заполненных лунок, запечатывая их с образованием массива замкнутых полимерных микрокамер, содержащих в своей полости модулятор оксидативного гомеостаза, и удаления шаблона, отличающийся тем, что при формировании внешнего поддерживающего слоя регулировку толщины обеспечивают путем его открепления после высушивания от глянцевой поверхности с последующим равномерным механическим растягиванием на 10-50% от начальной площади и креплением на глянцевую защитную основу, при создании основного активного слоя используют 3 мас. % полилактид в хлороформе и шаблон с массивом лунок овальной формы, на заключительном этапе дополнительно формируют последний внутренний гидрофильный адгезивный слой, регулирование толщины которого обеспечивают путем последовательного повторения цикла, состоящего из поэтапного смачивания основного активного слоя 1 мас. % водным раствором желатина, равномерным его распределением за счет собственной текучести и высушиванием до образования пленочной поверхности.
| M.GAI et al | |||
| Polylactic acid nano- and microchamber arrays for encapsulation of small hydrophilic molecules featuring drug release via high intensity focused ultrasound | |||
| Nanoscale, 2017, 9, 7063-7070 | |||
| A.V | |||
| ERMAKOV et al | |||
| Site-specific release of reactive oxygen species from ordered arrays of microchambers based on polylactic acid and carbon |
Авторы
Даты
2024-01-11—Публикация
2023-06-30—Подача