Группа изобретений относится к медицине, в частности к химико-фармацевтической промышленности. Данные технические решения могут быть использованы при производстве средств растительного происхождения, а именно препаратов, где действующим веществом является биологически активный растительный компонент – экстракт аврана лекарственного.
Растительное сырье широко используется в медицинской практике для производства различных лекарственных препаратов: экстрактов, водных извлечений (настоев и отваров), настоек, сборов и др. Одним из перспективных компонентов для создания фармацевтических композиций является Авран лекарственный (Gratiola officinalis L.) – растение семейства подорожниковых, достаточно широко распространенное в Европейской части Российской Федерации. Известно, что трава аврана лекарственного обладает противоглистным, противотуберкулезным, противомутагенным, антиоксидантным и противоопухолевым действиями [Куркин В.А. Фармакогнозия: учебник для студентов фармацевтических вузов (факультетов). – Самара, 2016. – 1279 с.; Большой энциклопедический словарь лекарственных растений: учебное пособие под ред. Г. П. Яковлева. – Санкт-Петербург: СпецЛит, 2015. – 759 с.].
Известен противоопухолевый сбор Здренко в виде травяной основы из 17 измельченных растительных ингредиентов для приготовления микстуры, расфасованный по пакетам [см. Информационный сайт: https://fb.ru/article/456775/protivoopuholevyiy-sbor-zdrenko-primenenie-sostav-otzyivyi?ysclid=lqkwm8nmeb310237225]. При этом в одном пакете ингредиенты содержатся в следующем соотношении: 16 растительных ингредиентов по 7 г и авран лекарственный 3 г.
Известен способ приготовления микстуры противоопухолевого сбора Здренко [Библиотечка лекарственных растений, том 2, составитель Зимин В.Н., Санкт-Петербург, АО «Дорваль», 1992, с.181-182] путем длительного кипячения в течение 2 часов до получения водного настоя трав.
Однако при изготовлении микстуры, в состав которой входит авран лекарственный, происходит его водное извлечение, которое обладает высокой токсичностью за счет присутствия ядовитых соединений, и недостаточное количество выхода целевых продуктов, в частности флавоноидов, а также трудность расчета точной дозировки для дальнейшего использования.
В литературных источниках также описана возможность выпуска экстракта аврана лекарственного в дозированных лекарственных формах - твердых желатиновых капсулах [Дырина К.С., Абрамович Н.А., Потанина О.Г. Авран лекарственный (Gratiola officinalis L.) – перспективное лекарственное сырье для создания энтеральных лекарственных препаратов (обзор литературы)// Вопросы обеспечения качества лекарственных средств. №3 (41). – 2023. – С. 64-72]. Известен способ производства данных капсул, включающий введение в гидрофильный густой экстракт аврана лекарственного застывающих тиксотропных жидкостей, а именно полиэтиленгликоля различной вязкости.
Несмотря на то, что полиэтиленгликоли совместимы с большинством лекарственных веществ, однако они несовместимы с фенолами, а при сочетании с лекарственными веществами, содержащими окси- и карбоксильные группы, возможна потеря их терапевтической активности. Поскольку основными компонентами фармацевтической композиции являются флавоноиды, которые являются полифенольными соединениями, то применение полиэтиленгликолей в качестве вспомогательных веществ может снизить эффективность фармакологического действия. Полиэтиленгликоли гигроскопичны, скорость высвобождения из их основ ниже по сравнению с другими гидрофильными соединениями. Их основы обезвоживают слизистую [Фармацевтическая технология. Высокомолекулярные соединения в фармации и медицине/ А.И. Сливкин [и др.]; под ред. И.И. Краснюка (ст.). – М: ГЭОТАР-Медиа, 2017. – 560с.]
Наиболее близким аналогом заявляемой фармацевтической композиции противоопухолевого действия является препарат, описанный в статье авторов К.С. Дыриной и соавторов [Дырина К.С., Абрамович Н.А., Потанина О.Г. Авран лекарственный (Gratiola officinalis L.) – перспективное лекарственное сырье для создания энтеральных лекарственных препаратов (обзор литературы)// Вопросы обеспечения качества лекарственных средств. №3 (41). – 2023. – С. 64-72], изготовленный из густого экстракта аврана лекарственного, абсорбированного порошками кремния диоксида коллоидного (Aerosil), фосфата кальция (Fujikalin, Di-Cafos), карбонатов кальция и магния, алюминометасиликата магния (Neusilin).
Однако добавление в качестве вспомогательных веществ карбонатов кальция и магния для пероральных лекарственных форм может быть ограничено тем, что эти соединения в кислой среде желудка зачастую распадаются с выделением газообразных продуктов (углекислый газ), что приводит к вздутию. Добавление в качестве вспомогательных веществ соединений, содержащих алюминий (алюмометасиликат магния), может привести к образованию комплексных фенольных соединений (флавоноидов), что, в свою очередь, снизит их терапевтический эффект.
Наиболее близким аналогом к заявляемому способу производства фармацевтической композиции является способ получения средства на основе сухого экстракта пустырника [патент RU на изобретение №2589507], который имеет основные технологические этапы производства, совпадающие с заявляемым. Способ приготовления вышеописанного средства заключается в том, что в смеситель загружают экстракт пустырника сухого, микрокристаллическую целлюлозу, лактозы моногидрат и перемешивают 5 минут, гранулируют 10%-ым водным раствором поливинилпирролидона, проводят влажную грануляцию, сушку, опудривание массы примогелем, стеаратом кальция или магния и тальком, проводят сухую грануляцию, стадию таблетирования и полученные ядра таблеток покрывают оболочкой.
Однако особенность фитохимического состава аврана лекарственного не позволяет полностью использовать для производства лекарственной формы технологическую схему описанного выше способа.
Задачей заявляемой фармацевтической композиции является разработка безопасного лекарственного препарата с низкой токсичностью при сохранении выраженного противоопухолевого эффекта.
Задачей заявляемого способа производства является разработка технологии изготовления фармацевтической композиции противоопухолевого действия с четко нормированным содержанием биологически активных соединений – флавоноидов.
Сущность заявляемой фармацевтической композиции противоопухолевого действия, выполненной в виде таблеток, содержащей в качестве активного вещества экстракт аврана лекарственного и вспомогательные вещества – кремния диоксид коллоидный, магния стеарат, заключатся в том, что в качестве активного вещества используют сухой экстракт, в композицию дополнительно добавляют картофельный крахмал, лактозы моногидрат, при этом таблетка содержит компоненты в следующем соотношении, мас. %:
Сущность заявляемого способа производства фармацевтической композиции, включающего перемешивание компонентов композиции, проведение влажной грануляции, сушки, опудривания массы магния стеаратом, стадии таблетирования, заключается в том, что смесь аврана лекарственного экстракта сухого с лактозы моногидратом, содержащей 3% флавоноидов в пересчете на лютеолин-7-глюкозид и сухое вещество, приготавливают путем определения количества флавоноидов в сухом экстракте методом дифференциальной спектрофотометрии и стандартизируют их сумму до 3% за счет выполнения перерасчета и изменения количества лактозы моногидрата в смеси по формуле:
N= (э×M×3×100)/(m×Х×(100-W)),
где Э – номинальная масса экстракта в таблетке, мг;
М – масса загрузки, кг;
m – масса таблетки, мг;
Х – содержание флавоноидов в сухом экстракте в пересчете на лютеолин-7-глюкозид и абсолютно сухое вещество, %;
W – потеря в массе при высушивании сухого экстракта, %,
затем перемешивают приготовленную смесь с крахмалом картофельным, кремния диоксидом коллоидным, лактозы моногидратом, влажную грануляцию осуществляют спиртом этиловым 95%.
Технический результат заявляемой группы изобретений.
Оптимальный набор вспомогательных веществ и их соотношение позволяет произвести лекарственную форму таблетки, удовлетворяющую основным фармацевтико-технологическим параметрам – истираемость, прочность, распадаемость, растворимость.
Использование в качестве активного вещества именного сухого экстракта обеспечивает стабильность физико-химических характеристик фармацевтической композиции при увеличении срока годности лекарственных препаратов.
Такой технологический прием как нормирование 3% содержания флавоноидов путем приготовления сухой смеси аврана лекарственного с лактозы моногидратом перед формированием фармацевтической композиции с пересчётом лактозы моногидрата в основном составе позволяет обеспечить максимальный терапевтический эффект при обеспечении безопасности лекарственного препарата, снизив токсичность аврана лекарственного при сохранении выраженного противоопухолевого эффекта.
Фармацевтическая композиция противоопухолевого действия выполнена в виде таблеток. В её состав входят компоненты в следующих соотношениях, мас. %: смесь аврана лекарственного экстракта сухого с лактозы моногидратом, содержащей 3% флавоноидов в пересчете на лютеолин-7-глюкозид и сухое вещество – 50,0; крахмал картофельный – 24,4; кремния диоксид коллоидный – 0,6; магния стеарат – 1,0; лактозы моногидрат – оставшееся.
Способ производства фармацевтической композиции осуществляется следующим образом.
Авран лекарственный экстракт сухой производят в соответствии с разработанной технологией учеными заявителя данной группы изобретений – СГМУ имени В.И. Разумовского, описанной в патенте №2482863. Растительное сырье (трава Аврана лекарственного), заготовленное во время цветения и плодоношения, измельчают на мельнице до размера частиц 5 мм, загружают в экстрактор и заливают 95% спиртом этиловым. Экстракцию измельченной травы проводят в реакторе двукратно при соотношении сырья и экстрагента 1:10. Время 1-й экстракции 15 минут при непрерывном перемешивании и температуре кипения, 2-й – до начала конденсации паров растворителя. Объединенные 1-й и 2-й экстракты фильтруют и затем упаривают на циркуляционном вакуум-выпарном аппарате при температуре 50-55 °С до полного удаления спирта. Получают кубовый остаток, к которому прибавляют воду и доупаривают. Упаренный водный кубовый остаток обрабатывают хлороформом в соотношении 5:1 для очистки от балластных и токсичных веществ. Хлороформный экстракт удаляют, водную фазу, содержащую целевой продукт, доупаривают при температуре 55-60°С. К очищенному водному кубовому остатку добавляют 95% спирта этилового (50% от объема), сливают на противень и помещают в электрошкаф сушильный вакуумный. Сушку ведут при температуре (60±2)°C в течение 12 ч, высушенный продукт измельчают на мельнице. Получают готовый продукт с содержанием суммы флавоноидов не менее 3 % в пересчете на лютеолин-7-глюкозид и сухое вещество с потерей в массе при высушивании не более 5,0%.
Для определения суммы флавоноидов используют метод дифференциальной спектрофотометрии в УФ- и видимой областях, который широко применяется в фармакопейном анализе при оценке содержания целевых аналитов в лекарственных растительных средствах [Государственная фармакопея Российской Федерации – XV изд. – Текст : электронный // Федеральная электронная медицинская библиотека : [сайт]. – URL:https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/?PAGEN_1=5].
Определение суммы флавоноидов в растительном сырье основано на реакции комплексообразования флавоноидов с хлоридом трехвалентного алюминия, в результате чего происходит батохромный сдвиг полосы поглощения с 330–350 нм до 390–410 нм, что позволяет проводить количественное определение искомых соединений в растворе по разнице аналитического сигнала тех же растворов без добавления солей алюминия. В качестве стандартов используются растворы стандартных образцов (СО) различных флавоноидов (рутина, лютеолин-7-глюкозид, гиперозида, кверцетина и др.) в этиловом спирте. Методики определения суммарного содержания флавоноидов применяются для стандартизации и контроля качества лекарственных растительных средств и фармацевтической продукции на его основе (настойки, экстракты, таблетки и т.д.) [Корулькин, Д. Ю., Абилов, Ж. А., Музычкина, Р. А., Толстиков, Г. А. Природные флавоноиды [Текст] / Д. Ю. Корулькин, Ж. А. Абилов, Р. А. Музычкина, Г. А. Толстиков – Рос. акад. наук, Сиб. отд., Новосиб. ин-т органической химии. – Новосибирск: Академическое изд-во "Тео", 2007. – 232 c.].
Определение суммарного содержания флавоноидов в сухом экстракте проводят по следующей методике:
Приготовление растворов.
Раствор стандартного образца (СО) лютеолин-7-глюкозида. Около 0,010 г (точная навеска) СО лютеолин-7-глюкозида помещают в мерную колбу вместимостью 100 мл, прибавляют 80 мл спирта 70 %, перемешивают при нагревании до полного растворения, охлаждают, доводят объем раствора тем же растворителем до метки и перемешивают (раствор СО 1).
Испытуемый раствор. 0,15 г сухого экстракта (точная навеска) помещают в мерную колбу вместимостью 50 мл и растворяют в 15 мл 70 % спирта этилового. Доводят объём раствора тем же растворителем до метки и перемешивают (раствор А).
10,0 мл раствора А помещают в мерную колбу вместимостью 50 мл, добавляют 10,0 мл 5 % спиртового раствора алюминия хлорида в 70% этиловом спирте, доводят объем раствора спиртом 70 % до метки и перемешивают (раствор Б).
9,0 мл раствора СО 1 помещают в мерную колбу вместимостью 50 мл, добавляют 10,0 мл 5 % спиртового раствора алюминия хлорида в 70% этиловом спирте, доводят объем раствора спиртом 70 % до метки и перемешивают (раствор СО 2).
Оптическую плотность раствора Б измеряют через 40 мин на спектрофотометре при длине волны 398±1 нм в кювете с толщиной слоя 10 мм относительно раствора сравнения. В качестве раствора сравнения используют раствор, состоящий из 10,0 мл раствора А, доведенного этиловым спиртом 70 % до метки в мерной колбе вместимостью 50 мл.
Параллельно измеряют оптическую плотность раствора СО 2 через 40 мин на спектрофотометре в тех же условиях относительно раствора сравнения. В качестве раствора сравнения используют раствор, состоящий из 9,0 мл раствора СО 1, доведенного этиловым спиртом 70 % до метки в мерной колбе вместимостью 50 мл.
Содержание суммы флавоноидов в пересчете на лютеолин-7-глюкозид и абсолютно сухое вещество в процентах (Х) вычисляют по формуле:
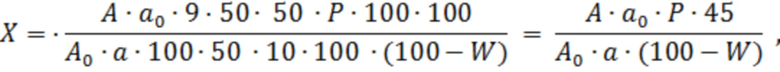
где A – оптическая плотность испытуемого раствора Б;
Aо – оптическая плотность раствора СО 2 лютеолин-7-глюкозида;
А – навеска субстанции, г;
Ао – навеска СО лютеолин-7-глюкозида, г;
P – содержание основного вещества в СО лютеолин-7-глюкозида, %;
W – потеря в массе при высушивании, %.
Содержание суммы флавоноидов в пересчете на лютеолин-7-глюкозид и абсолютно сухое вещество должно быть не менее 3 %.
Производство таблеток [ОСТ 64-02-003-2002 Стандарт отрасли Продукция медицинской промышленности. Технологические регламенты производства: URL:http://consultpharma.ru/index.php/ru/documents/proizvodstvo/688-ost64-02-003-2002].
Количество Аврана лекарственного экстракта сухого указано для препарата с содержанием суммы флавоноидов – 3,0 % (в пересчете на лютеолин-7-глюкозид и сухое вещество, с относительной влажностью не более 5 %). При большем или меньшем содержании суммы флавоноидов в субстанции делают перерасчет и соответственно увеличивают или уменьшают количество лактозы моногидрата на загрузку по формуле:
N= 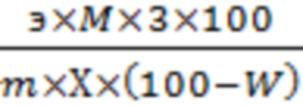 ,
,
где Э – номинальная масса экстракта в таблетке, мг;
М – масса загрузки, кг;
M – масса таблетки, мг;
Х – содержание флавоноидов в сухом экстракте в пересчете на лютеолин-7-глюкозид и абсолютно сухое вещество, %;
W – потеря в массе при высушивании сухого экстракта, %.
Всё сырьё, необходимое для приготовления таблеточной массы, предварительно просеивают, обеспечивая равномерное смешивание с относительно одинаковой величиной частиц без механических загрязнений.
Взвешивают на весах рассчитанные количества субстанции Аврана лекарственного экстракта сухого и вспомогательных веществ – крахмала картофельного, лактозы моногидрата, кремния диоксида коллоидного и магния стеарата.
Массу для таблетирования, состоящую из лактозы моногидрата, аврана лекарственного экстракта сухого, крахмала картофельного и кремния диоксида коллоидного, готовят на установке псевдоожиженного слоя. При нагревании компонентов до температуры 30 ºС и непрерывном увлажнении компонентов спиртом этиловым 95 % до окончания увлажнителя. Полученный влажный гранулят сушат до температуры 30-36 °С, и затем при перемешивании добавляют магния стеарат. Массу для таблетирования просеивают через сито с размером отверстий 1-1,5 мм. Определяют остаточную влагу таблеточной массы, которая должна быть 2,0-4,0 %.
Определение суммарного содержания флавоноидов в таблетках проводят по следующей методике:
Приготовление растворов.
Раствор стандартного образца (СО) лютеолин-7-глюкозида. Около 0,010 г (точная навеска) СО лютеолин-7-глюкозида помещают в мерную колбу вместимостью 100 мл, прибавляют 80 мл спирта 70 %, перемешивают при нагревании до полного растворения, охлаждают, доводят объем раствора тем же растворителем до метки и перемешивают (раствор СО 1).
Испытуемый раствор. 0,15 г (точная навеска) порошка растертых таблеток помещают в мерную колбу вместимостью 25 мл прибавляют 15 мл спирта этилового 70 % и взбалтывают в течение 30 мин. Объем раствора доводят спиртом этиловым 70 % до метки, перемешивают и фильтруют через бумажный или беззольный фильтр с красной полосой, отбрасывая первые 10 мл фильтрата (раствор А).
5,0 мл раствора А помещают в мерную колбу вместимостью 25 мл, добавляют 5,0 мл 5% спиртового раствора алюминия хлорида в 70% этиловом спирте, доводят объем раствора спиртом 70 % до метки и перемешивают ( раствор Б).
7,5 мл раствора СО1 помещают в мерную колбу вместимостью 50 мл, добавляют 10,0 мл 5% спиртового раствора алюминия хлорида в 70% этиловом спирте, доводят объем раствора спиртом 70% до метки и перемешивают (раствор СО2).
Оптическую плотность раствора Б измеряют через 40 мин на спектрофотометре при длине волны 398 нм в кювете с толщиной слоя 10 мм относительно раствора сравнения. В качестве раствора сравнения используют раствор, состоящий из 5,0 мл раствора А, доведенного этиловым спиртом 70 % до метки в мерной колбе вместимостью 25 мл.
Параллельно измеряют оптическую плотность раствора СО2 через 40 мин на спектрофотометре в тех же условиях относительно раствора сравнения. В качестве раствора сравнения используют раствор, состоящий из 7,5 мл раствора СО1, доведенного этиловым спиртом 70 % до метки в мерной колбе вместимостью 50 мл.
Содержание суммы флавоноидов в пересчете на лютеолин-7-глюкозид и абсолютно сухое вещество в процентах (Х) вычисляют по формуле:
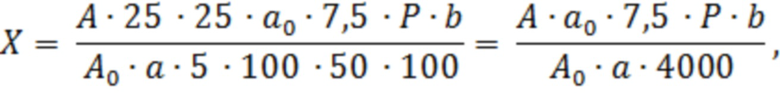
где A – оптическая плотность испытуемого раствора Б;
Aо – оптическая плотность раствора СО2 лютеолин-7-глюкозида;
А – навеска субстанции, г;
ао– навеска СО лютеолин-7-глюкозида, г;
P – содержание основного вещества в СО лютеолин-7-глюкозида, %;
W – влажность сырья, %.
Пример. Была произведена опытно-промышленная партия таблеток с фармацевтической композией противоопухолевого действия «Аврана лекарственного экстракт таблетки, 125 мг» и «Аврана лекарственного экстракт таблетки, 250 мг» со следующим составом:
(с содержанием суммы флавоноидов в пересчете на цинарозид и сухое вещество 3,0 %)
(АО «Фармцентр ВИЛАР», Россия);
(Европейская Фармакопея)
(Европейская Фармакопея)
(Европейская Фармакопея)
(Европейская Фармакопея)
Таблетки были произведены в соответствии с заявляемым способом с обеспечением 3% содержания флавоноидов в сухой смеси аврана лекрственного с лактозы моногидратом. Стадия таблетирования проводилась на таблеточном прессе, на котором устанавливали соответствующий пресс-инструмент (диаметр пуансонов 9 мм – для таблеток с дозировкой 125 мг и 11 мм – для таблеток с дозировкой 250 мг, круглые плоскоцилиндрической формы с риской с одной стороны и фаской с двух сторон). Содержание суммы флавоноидов в пересчете на лютеолин-7-глюкозид и среднюю массу таблетки составляло от 0,00338 до 0,00413 г (для таблеток дозировкой 125 мг) и от 0,00675 до 0,00825 г (для таблеток дозировкой 250 мг). Это является подтверждением того, что разработанная технология производства таблеток «Аврана лекарственного экстракт» позволяет четко нормировать содержание биологически активных соединений – флавоноидов.
Безопасность лекарственного препарата, его низкая токсичность с сохранением выраженного противоопухолевого эффекта была подтверждена в результате оценки острой токсичности на лабораторных животных (белых нелинейных крысах, кроликах). Изучение острой токсичности при пероральном введении лекарственного средства провели на белых нелинейных крысах. Препарат «Аврана лекарственного экстракт таблетки 125 мг» вводили в желудок крысам однократно в виде 40% раствора в течение 14 дней в дозах: 3500, 4000, 4500 мг/кг по действующему веществу. Устанавливали параметры токсичности LD0, LD 50, LD100 и класс опасности препарата. Результаты проведенных исследований позволили сделать следующие выводы:
- значение LD50 препаратов «Аврана лекарственного экстракт таблетки 125 мг» и «Аврана лекарственного экстракт таблетки 250 мг» при однократном внутрижелудочном введении крысам составило 3892,071±140,13 мг/кг;
- по параметрам острой токсичности, установленным на крысах, водный раствор препаратов «Аврана лекарственного экстракт таблетки 125 мг», «Аврана лекарственного экстракт таблетки 250 мг» согласно общепринятой гигиенической классификации ГОСТ 12.1.007-76 относится к 3 классу опасности - «вещества умеренно опасные».
Сохранение противоопухолевого действия таблеток «Аврана лекарственного экстракт таблетки 125 мг» и «Аврана лекарственного экстракт таблетки 250 мг», произведенных в соответствии с заявляемым способом, было доказано путем оценки динамики роста перевитого рака почки РА на белых нелинейных крысах. Было выявлено, что уменьшение объема опухоли на конец эксперимента по сравнению c размерами опухоли у животных без воздействия фармацевтической композиции составило 40%, индекс торможения роста опухоли (ИТРО) по массе – 73%. На конец эксперимента объем опухоли был меньше на 23% по сравнению с группой крыс без воздействия.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения суммы флавоноидов в траве аврана лекарственного | 2023 |
|
RU2829551C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ СЕДАТИВНОГО И АНКСИОЛИТИЧЕСКОГО ДЕЙСТВИЯ | 2020 |
|
RU2737701C1 |
| ЭКСТРАКТ Cetraria islandica (L.) Ach. СУХОЙ, ТАБЛЕТИРОВАННАЯ ФОРМА | 2006 |
|
RU2321419C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОТУБЕРКУЛЕЗНЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2549477C1 |
| СРЕДСТВО НА ОСНОВЕ СУХОГО ЭКСТРАКТА ПУСТЫРНИКА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2589507C1 |
| СЕДАТИВНОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2291705C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ТВЕРДОЙ ФОРМЕ С АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2545861C1 |
| Способ комбинированной терапии рака печени РС-1 в эксперименте | 2020 |
|
RU2734143C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ, ЖАРОПОНИЖАЮЩИМ И АНТИМИКРОБНЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2535155C1 |
| Фармацевтическая композиция с противогрибковой активностью и способ ее получения | 2016 |
|
RU2624857C1 |
Изобретение относится к области фармацевтической промышленности, а именно к фармацевтической композиции противоопухолевого действия. Фармацевтическая композиция противоопухолевого действия, выполненная в виде таблеток, содержит в качестве активного вещества экстракт аврана лекарственного и вспомогательные вещества - кремния диоксид коллоидный, при этом в качестве активного вещества используют сухой экстракт аврана лекарственного травы, в композицию дополнительно добавляют картофельный крахмал, лактозы моногидрат, магния стеарат, при этом таблетка содержит компоненты в следующем соотношении, мас. %: смесь аврана лекарственного травы экстракта сухого с лактозы моногидратом, содержащей 3% флавоноидов в пересчете на лютеолин-7-глюкозид и сухое вещество 50,0, крахмал картофельный 24,4, кремния диоксид коллоидный 0,6, магния стеарат 1,0, лактозы моногидрат - оставшееся. Использование изобретения обеспечивает получение фармацевтической композиции в виде таблетки, которая соответствует таким технологическим параметрам как истираемость, прочность, распадаемость, растворимость, а также является стабильной, безопасной и имеет увеличенный срок годности, обладает выраженным противоопухолевым эффектом. 1 пр.
Фармацевтическая композиция противоопухолевого действия, выполненная в виде таблеток, содержащая в качестве активного вещества экстракт аврана лекарственного и вспомогательные вещества - кремния диоксид коллоидный, отличающаяся тем, что в качестве активного вещества используют сухой экстракт аврана лекарственного травы, в композицию дополнительно добавляют картофельный крахмал, лактозы моногидрат, магния стеарат, при этом таблетка содержит компоненты в следующем соотношении, мас. %:
| Дырина и др., Авран лекарственный, Перспективное лекарственное сырье для создания энтеральных лекарственных препаратов, Вопросы обеспечения качества лекарственных средств, 2023, с.64-72 | |||
| СРЕДСТВО НА ОСНОВЕ СУХОГО ЭКСТРАКТА ПУСТЫРНИКА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2589507C1 |
| Дырина К.С | |||
| и др., Перспективы создания лекарственных средств на основе аврана лекарственного в регенеративной медицине | |||
| Гены и | |||
Авторы
Даты
2024-12-09—Публикация
2023-12-28—Подача