Настоящее изобретение относится к фармацевтической композиции в виде жевательной таблетки с высокой дозой микронизированного диосмина.
Настоящее изобретение также относится к фармацевтической композиции в виде жевательной таблетки с высокой дозой очищенной и микронизированной флавоноидной фракции (MPFF).
Флавоноидную фракцию получают из экстракта рутовых. Используемая в изобретении очищенная и микронизированная флавоноидная фракция содержит одновременно от 87% до 93% диосмина и других флавоноидов. Эти другие флавоноиды в количестве примерно 10% содержат от 2,5% до 5,0% гесперидина, от 0,9% до 2,8% изорхоифолина, от 0,9% до 2,8% линарина и менее 1% диосметина.
В соответствии с изобретением диосмин и флавоноидная фракция микронизированы. Микронизация действующего вещества значительно увеличивает его биодоступность. Микронизация флавоноидов, включая диосмин, является особенно ценной для улучшения пищеварительной абсорбции этих веществ, которые плохо растворимы в воде и поэтому плохо всасываются слизистой оболочкой пищеварительного тракта. Следовательно, предпочтительно разрабатывать галеновые формы, содержащие микронизированный диосмин или микронизированную флавоноидную фракцию, чтобы улучшить биодоступность.
Кроме того, флавоноидную фракцию в соответствии с изобретением вводят в суточных дозах от 1000 до 3000 мг для лечения проявлений хронической венозной недостаточности нижних конечностей. При лечении основных терапевтических показаний из-за увеличения суточных дозировок флавоноидной фракции и диосмина эти действующие вещества должны иметь высокую дозировку при каждом их введении. Помимо этого, лечение, основанное на флавоноидной фракции, представляет собой долгосрочное лечение, требующее легкого приема, чтобы способствовать соблюдению пациентом режима лечения. Соответственно, предпочтительно разрабатывать лекарственные формы, которые позволяют легко принимать их пожилым людям и без добавления воды пациентам, потребляющим их вне дома.
Терапевтическое применение флавоноидной фракции, экстрагированной из рутовых согласно изобретению, описано в патенте ЕР 0711560. В этом патенте описана композиция шипучих гранул с высокой дозой флавоноидной фракции в 1000 мг. Перед употреблением эти шипучие гранулы следует развести в воде.
Фармацевтические формы жевательных, рассасываемых таблеток или таблеток для жевания, содержащих диосмин, описаны в международной заявке на патент WO 2004/032942. Фармацевтические формы согласно заявке WO 2004/032942 не содержат высоких доз диосмина и не используют действующее вещество в микронизированной форме.
Таким образом, настоящее изобретение относится к фармацевтическим композициям в виде жевательной таблетки с высокой дозой микронизированного диосмина или очищенной и микронизованной флавоноидной фракции (MPFF).
Фармацевтическая композиция жевательной таблетки в соответствии с изобретением должна обладать определенными функциональными свойствами, чтобы соответствовать технологическим трудностям, связанным с жевательными таблетками с высокой дозой микронизированного действующего вещества.
Действительно, необходимо, чтобы фармацевтическая композиция была достаточно спрессовываемой, избегая явлений расщепления и хрупкости. Очень высокое содержание действующего вещества и низкая доля содержания наполнителей, чтобы не увеличивать конечную массу жевательной таблетки, отрицательно влияют на желаемые механические свойства жевательной таблетки.
Кроме того, микронизация порошков действующих веществ приводит к снижению свойств сыпучести указанных порошков, учитывая увеличение сил между частицами. Размер частиц является важным фактором сыпучести порошков, на которую равным образом могут влиять форма частиц и/или влажность.
Объектом настоящего изобретения является фармацевтическая композиция в виде жевательной таблетки с высокой дозой очищенной и микронизированной флавоноидной фракцией, содержащей диосмин, гесперидин, изорхоифолин, линарин и диосметин.
Под «жевательной таблеткой» в соответствии с изобретением подразумевают фармацевтическую форму, известную в англо-саксонской терминологии под термином «chewable tablet». «Жевательная таблетка» или таблетка «для жевания» в данном контексте означают эквивалентные фармацевтические формы.
Жевательные лекарственные формы очень хорошо воспринимаются пациентами и улучшают соблюдение режима лечения, несмотря на то что эти жевательные формы представляют собой большие таблетки с единичной массой не менее 3000 мг.
В фармацевтических композициях согласно изобретению диосмин и флавоноидная фракция являются микронизированными. Микронизация представляет собой способ, позволяющий уменьшить размер частиц порошка. Микронизацию действующего вещества, такого как диосмин или флавоноидная фракция, можно осуществлять с помощью различных систем микронизации. Эти системы микронизации могут представлять собой мельницу, воздушно-струйный микронайзер или шаровой микронайзер, где давление воздушной струи или скорость подачи порошка варьируются в зависимости от ожидаемого размера частиц микронизированного действующего вещества.
Размер зерен является особенно важной характеристикой порошкообразных материалов, таких как порошки. Размер частицы определяется по ее диаметру или диаметру эквивалентных сфер, если частица имеет неправильную форму. Диаметр зерен, определенный с помощью лазерного дифракционного анализатора размера частиц, позволяет охарактеризовать гранулометрический состав или размер частиц d50, d90 (распределение по размерам частиц).
В настоящем изобретении «d50 менее X мкм» означает, что по меньшей мере 50% частиц микронизата имеют размер менее X мкм. В настоящем изобретении «d90 менее X мкм» означает, что по меньшей мере 90% частиц микронизата имеют размер менее X мкм.
В одном варианте осуществления d90 микронизированного действующего вещества составляет менее 5 мкм. Значение d90 менее 5 мкм включает в себя d50 менее 4 мкм, 3 мкм, 2 мкм, 1,8 мкм, 1,6 мкм, 1,5 мкм.
В одном варианте осуществления d50 микронизированного действующего вещества составляет менее 5 мкм. Значение d50 менее 5 мкм включает в себя d50 менее 4 мкм, 3 мкм, 2 мкм, 1,8 мкм, 1,6 мкм, 1,5 мкм.
В некоторых вариантах осуществления микронизированный диосмин или очищенная и микронизированная флавоноидная фракция характеризуются следующей гранулометрией:
- d50 менее 2 мкм, предпочтительно менее 1,6 мкм и/или
- d90 менее 5 мкм, предпочтительно менее 2 мкм, более предпочтительно менее 1,6 мкм.
Средний диаметр частиц микронизированного действующего вещества в фармацевтической композиции в соответствии с изобретением составляет строго менее 5 мкм, предпочтительно строго менее 1,6 мкм.
Процент содержания микронизированного диосмина или очищенной и микронизированной флавоноидной фракции в фармацевтической композиции составляет от 20% до 80% от общей массы композиции. Предпочтительно процент содержания микронизированного действующего вещества составляет от 30% до 60% от общей массы композиции. Предлагаемые в изобретении фармацевтические композиции обеспечивают пероральное введение большого количества флавоноидов для каждой стандартной дозы. Под «высокодозированными» фармацевтическими композициями понимают композиции, содержащие по меньшей мере 20% действующего вещества. Количество диосмина или флавоноидной фракции в фармацевтической композиции составляет от 1000 мг до 3000 мг, включая 2000 мг, 1500 мг, 2500 мг.
Фармацевтические композиции в форме жевательных таблеток с высокой дозой содержат от 30% до 60% по весу микронизированного диосмина или очищенной и микронизированной флавоноидной фракции от общей массы композиции и от 40% до 70% по весу полиолов от общей массы композиции.
Чтобы удовлетворить промышленные ограничения, присущие производству жевательной таблетки, содержащей микронизированное и высокодозированное действующее вещество, необходимо выбрать вспомогательные вещества, которые помогают преодолеть указанные промышленные ограничения. Под вспомогательным веществом следует понимать любое соединение, входящее в состав препарата, которое должно действовать как простой носитель, то есть не должно иметь биологической активности.
Фармацевтические композиции в соответствии с изобретением содержат по меньшей мере один полиол, выполняющий функцию разбавителя.
Разбавитель служит для получения для получения объема порошка, достаточного для изготовления таблетки желаемого размера, физические характеристики которой совместимы с производственными процессами, например, путем прямого прессования. В качестве разбавителя используют один или несколько полиолов. Предпочтительно используемый полиол представляет собой сорбит. Преимущественно можно использовать два разных полиола и предпочтительно смесь маннита и сорбита. Преимущество полиолов в качестве разбавителей состоит в том, что они обеспечивают сладкий аромат и обладают превосходными свойствами связывания и сжимаемости. Маннит или сорбит можно заменить другим полиолом, в частности ксилитом или мальтитом.
В фармацевтической композиции в соответствии с изобретением соотношение массы полиола или полиолов к массе действующего вещества составляет строго менее 2, предпочтительно соотношение меньше 1,6.
Помимо микронизированного действующего вещества и полиола или полиолов фармацевтическая композиция в соответствии с изобретением содержит одно или несколько фармацевтически приемлемых вспомогательных веществ. Например, объектом изобретения может быть фармацевтическая композиция, содержащая микронизированное действующее вещество, полиол(ы) и связующее вещество или же фармацевтическая композиция, содержащая микронизированное действующее вещество, полиол(ы), связующее вещество и смазывающее вещество.
Связующие вещества или вяжущие вещества представляют собой средства, роль которых заключается в связывании различных частиц фармацевтической композиции. Среди связующих веществ можно упомянуть мальтодекстрин и повидон. Смазывающие вещества предназначены для предотвращения явлений схватывания, адгезии и когезии во время различных производственных процессов. Смазывающее вещество, среди прочего, выбирают из стеариновой кислоты, стеарата магния или талька.
К фармацевтической композиции в соответствии с изобретением могут быть добавлены другие фармацевтически приемлемые вспомогательные вещества, такие как ароматизаторы или подсластители.
В качестве примера вспомогательных веществ можно упомянуть:
Ароматизирующие вещества или ароматизаторы, цель которых состоит в том, чтобы замаскировать неприятный вкус и смягчить землистую консистенцию: апельсиновый ароматизатор, лимонный ароматизатор, ароматизатор мягкой карамели, ароматизатор ванили/лимона;
Подсластители, усиливающие сладкий вкус композиции: аспартам, ацесульфам калия, сахарин натрия, цикламат калия; и
Средства, повышающие сыпучесть, такие как коллоидный безводный диоксид кремния.
Композиция в соответствии с изобретением может представлять собой фармацевтическую композицию с немедленным, пролонгированным или отсроченным высвобождением. Предпочтительно композиция в соответствии с изобретением представляет собой композицию с немедленным высвобождением.
Изобретение относится к способу получения путем влажной грануляции описанной выше жевательной таблетки, включающему в себя по меньшей мере, следующие стадии:
а) смешивание микронизированного диосмина или очищенной и микронизированной флавоноидной фракции, полиолов, связующих веществ, ароматизаторов и подсластителей;
б) после смешивания осуществляют смачивание. Полученную таким образом влажную массу затем гранулируют, сушат и затем калибруют;
в) смазывание гранул, полученных на стадии б) с помощью коллоидного диоксида кремния и стеарата магния;
г) прессование смазанной смеси.
В предпочтительном варианте осуществления жевательную таблетку в соответствии с изобретением получают в соответствии со способом прямого прессования, включающего в себя по меньшей мере следующие стадии:
а) смешивание микронизированного диосмина или очищенной и микронизированной флавоноидной фракции, полиолов, связующих веществ, ароматизаторов и подсластителей;
б) смазывание полученной на стадии а) смеси с помощью коллоидного диоксида кремния и стеарата магния;
в) прямое прессование смазанной смеси.
В столь же предпочтительном варианте осуществления жевательную таблетку в соответствии с изобретением получают в соответствии со способом грануляции уплотнением или сухой грануляции, включающим в себя по меньшей мере следующие стадии:
а) смешивание микронизированного диосмина или очищенной и микронизированной флавоноидной фракции, полиолов, связующих веществ, ароматизаторов и подсластителей;
б) после смешивания осуществляют уплотнение в гранулы;
в) смазывание полученных на стадии б) гранул с помощью коллоидного диоксида кремния и стеарата магния;
г) прессование смазанной смеси.
Предпочтительно в конце способа получают жевательные таблетки, твердость которых, измеренная путем диаметрального раздавливания, составляет от 180 до 220 Н (Н = ньютоны). Предпочтительно жевательные таблетки имеют твердость от 180 до 200 Н.
Равным образом настоящее изобретение относится к применению предлагаемых в изобретении фармацевтических композиций в лечении заболеваний вен, в частности венозной недостаточности, такой как тяжесть в ногах, боли, синдром беспокойных ног, ломкость капилляров и лечение геморроидального криза. Эти фармацевтические композиции используют в качестве венотонизирующего средства и протектора сосудов.
Приведенные ниже примеры иллюстрируют изобретение, но не ограничивают его.
Пример 1: Фармацевтические композиции жевательных таблеток
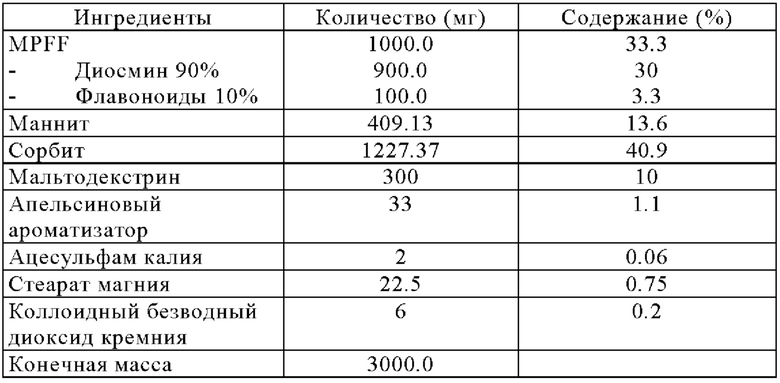
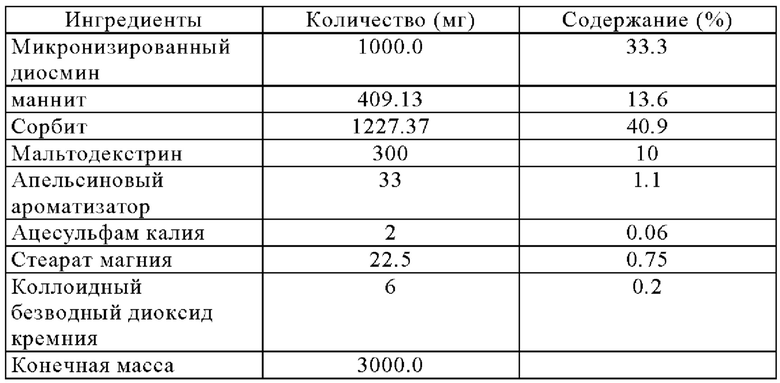
Производство жевательных таблеток из Примера 1:
Микронизированный диосмин или очищенную и микронизированную флавоноидную фракцию осторожно смешивают со вспомогательными веществами внутренней фазы, т.е. с маннитом, сорбитом, мальтодекстрином, апельсиновым ароматизатором, ацесульфамом калия. Смесь смачивают очищенной водой в сосуде под давлением, а затем гранулируют.
Гранулы сушат, чтобы получить остаточную влажность в соответствии со спецификациями, то есть около 2% остаточной влажности. Затем гранулы калибруют, гомогенизируют и смазывают стеаратом магния. Наконец, гранулы просеивают через сито с размером ячеек 0,8 мм и затем прессуют с помощью штампов.
Жевательные таблетки микронизированного диосмина и очищенной и микронизированной флавоноидной фракции согласно Примеру 1 соответственно имеют твердость от 196 до 192 Н (Н = ньютон).
Пример 2: Свойства сыпучести фармацевтических композиций в соответствии с изобретением
Сыпучесть порошка является его способностью свободно сыпаться, равномерно и постоянно в виде отдельных частиц. Таким образом, сыпучесть порошков обуславливает производительность и правильное функционирование производственных процессов и имеет значение для качества конечного продукта. Таким образом, порошок с хорошей сыпучестью сыпется без посторонней помощи. Напротив, когезионный порошок имеет слабую сыпучесть и для облегчения его перемещения необходимо обеспечить механическое (перемешивание, вибрация) или химическое (покрытие) устройство.
Сыпучесть порошков и гранул высокодозированной микронизированного диосмина и очищенной микронизированной флавоноидной высокодозированной фракции в соответствии с изобретением, измеренная различными методами (индекс Карра, коэффициент Хауснера и функция сыпучести Шульце), показывает, что фармацевтические композиции в соответствии с изобретением очень эффективны в способах производства жевательных таблеток. Несмотря на факторы, которые очень неблагоприятны для продуктивности производственных процессов, таких как микронизация действующего вещества и/или высокая доза действующего вещества, сыпучесть фармацевтических композиций в соответствии с изобретением соответствует промышленным и нормативным требованиям.
Индекс Карра (Ic) характеризует сыпучесть порошкового слоя как функцию плотности. Это определяется уравнением ниже:
Ic=(ρнасыпная-ρvобъемная)/ρнасыпная
где ρ представляет собой плотность, а Ic безразмерную физическую величину. Значения индекса Карра интерпретируют следующим образом:
Ic<0,15 хорошая сыпучесть
0,15<Ic<0,25 умеренная сыпучесть
Ic>0,25 плохая сыпучесть
Коэффициент Хауснера (Hr) определяет сжимаемость и сыпучесть порошка на основе измерений плотности (ρ). Ее рассчитывают как отношение насыпной плотности (ρнасыпная) к объемной плотности (ρобъемная) в соответствии с уравнением:
Hr=ρнасыпная/ρобъемная
Hr представляет собой безразмерную физическую величину. Если Hr составляет от 1,0 до 1,2, то порошок имеет малую способность к сжиманию, является мало когезионным и хорошую сыпучесть; если Hr составляет от 1,2 до 1,4, то порошок является сжимаемым, когезионным и проявляет плохую сыпучесть.
Наконец, аппарат Шульце представляет собой ячейку сдвига для измерения функции сыпучести (FFC). Легкая сыпучесть характеризуется FFC в пределах от 4 до 10, а свободная сыпучесть характеризуется FFC более 10.

| название | год | авторы | номер документа |
|---|---|---|---|
| МИКРОНИЗАЦИЯ ПОЛИОЛОВ | 2008 |
|
RU2479587C2 |
| КОМПОЗИЦИЯ ДЛЯ ФЛЕБОПРОТЕКТОРА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2021 |
|
RU2806345C2 |
| СТАБИЛЬНЫЕ СОСТАВЫ ШИПУЧЕГО БИСФОСФОНАТА СО СВОЙСТВАМИ БЫСТРОЙ СОЛЮБИЛИЗАЦИИ | 2011 |
|
RU2608724C2 |
| ТВЕРДАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДИОСМИНА | 2005 |
|
RU2314812C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ ПЕРОРАЛЬНОЙ СУСПЕНЗИИ, КОТОРАЯ СОДЕРЖИТ ФРАКЦИЮ ФЛАВОНОИДА И КСАНТАНОВУЮ КАМЕДЬ | 2013 |
|
RU2582954C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ЭНТАКАПОНА, ЛЕВОДОПЫ И КАРБИДОПЫ С УЛУЧШЕННОЙ БИОДОСТУПНОСТЬЮ | 2009 |
|
RU2485947C2 |
| ДЕКСТРОЗА ДЛЯ ПРЯМОГО ПРЕССОВАНИЯ | 2008 |
|
RU2471356C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ОМЕГАКАРБОКСИАРИЛЗАМЕЩЕННУЮ ДИФЕНИЛМОЧЕВИНУ, ДЛЯ ЛЕЧЕНИЯ РАКА | 2006 |
|
RU2420283C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНГАЛЯЦИИ | 2010 |
|
RU2493833C2 |
| НОВЫЙ ПРЕПАРАТ ДЛЯ ИНГАЛЯЦИИ, ИМЕЮЩИЙ НАСЫПНУЮ ОБЪЕМНУЮ ПЛОТНОСТЬ ОТ 0,28 ДО 0,38 Г/МЛ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 1998 |
|
RU2194497C2 |
Группа изобретений относится к области фармацевтики, а именно, к фармацевтической композиции и в виде жевательной таблетки для лечения венозной недостаточности или геморроидального криза и способу её получения. Фармацевтическая композиция в виде жевательной таблетки для лечения венозной недостаточности или геморроидального криза содержит 1000 мг микронизированного диосмина в качестве действующего вещества, причем: d50 микронизированного диосмина составляет менее 5 мкм; композиция содержит по меньшей мере один полиол, композиция содержит от 30 мас.% до 60 мас.% микронизированного диосмина от общей массы композиции. Способ изготовления фармацевтической композиции представляет собой способ влажной грануляции, сухой грануляции или прямого прессования. Вышеописанная группа изобретений позволяет получить фармацевтическую композицию, содержащую высокую дозу микронизированного действующего вещества, с механическими свойствами, позволяющими избежать явлений расщепления и хрупкости, и при этом обладающей достаточной для возможности ее производства сыпучестью. 2 н. и 5 з.п. ф-лы, 2 пр.
1. Фармацевтическая композиция в виде жевательной таблетки для лечения венозной недостаточности или геморроидального криза, содержащая 1000 мг микронизированного диосмина в качестве действующего вещества, причем:
- d50 микронизированного диосмина составляет менее 5 мкм,
- композиция содержит по меньшей мере один полиол,
- композиция содержит от 30 мас.% до 60 мас.% микронизированного диосмина от общей массы композиции.
2. Фармацевтическая композиция по п. 1, отличающаяся тем, что она содержит от 40 мас.% до 70 мас% полиолов от общей массы композиции.
3. Фармацевтическая композиция по любому из пп. 1 или 2, отличающаяся тем, что соотношение массы полиола или полиолов к массе действующего вещества составляет менее 2.
4. Фармацевтическая композиция по любому из пп. 1-3, в которой полиол представляет собой сорбит.
5. Фармацевтическая композиция по любому из пп. 1-4, содержащая полиол и связующее вещество.
6. Фармацевтическая композиция по любому из пп. 1-5, содержащая полиол и связующее вещество и смазывающее вещество.
7. Способ изготовления фармацевтической композиции по любому из пп. 1-6, отличающийся тем, что он представляет собой способ влажной грануляции, сухой грануляции или прямого прессования.
| FR 2845597 A1, 16.04.2004 | |||
| Устройство для логарифмирования | 1978 |
|
SU711560A1 |
| Шлакообразующая смесь | 1975 |
|
SU541874A1 |
| ТВЕРДАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДИОСМИНА | 2005 |
|
RU2314812C2 |
| ТАЛИБОВ О.Б., Фармакология препаратов, применяющихся при хронических заболеваниях вен // Хирургия | |||
| Журнал им | |||
| Н.И | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Светоэлектрический измеритель длин и площадей | 1919 |
|
SU106A1 |
Авторы
Даты
2024-01-18—Публикация
2019-07-19—Подача