Перекрестная ссылка на родственные заявки
[0001] В настоящей заявке испрашивается приоритет китайской патентной заявки с регистрационным номером 201810502359.7, поданной 23 мая 2018 г., и китайской патентной заявки с регистрационным номером 201810502387.9, поданной 23 мая 2018 г., каждая из которых включена в настоящее описание в полном объеме и во всех целях посредством ссылки.
Область изобретения
[0002] Настоящее изобретение относится к композициям и способам скрининга на рак прямой и ободочной кишки и прогрессирующую аденому, и к другим их применениям.
Описание текстового файла, представленного в электронном формате
[0003] Содержимое текстового файла, представленного здесь в электронном формате, полностью включено в настоящую заявку посредством ссылки: Копия Списка последовательностей в электронном формате (имя файла: NEWH-017_01WO_SeqList_ST25.txt, дата регистрации: 22 мая 2019 г., размер файла: 22 килобайта).
Предпосылки создания изобретения
[0004] Рак прямой и ободочной кишки (РПОК) по своей распространенности в мире занимает четвертое место, и смертность от него уступает лишь смертности от рака легких, рака печени и рака желудка. Ежегодная смертность от РПОК составляет почти 700000 человек. РПОК представляет собой «модернизированное» заболевание, заболеваемость которым в развитых странах выше, чем в развивающихся странах. В Соединенных Штатах Америки, рак прямой и ободочной кишки остается второй основной причиной смерти (Clinical Interventions in Aging 2016; 11:967-976). С повышением уровня жизни людей в Китае, с 2000 года заболеваемость и смертность от РПОК увеличиваются (CA CANCER J CLIN 2016; 66: 115-132). Выживаемость пациентов с локализованным заболеванием на ранней стадии (на стадии I и II) в течение 5 лет приближается к 90%, в то время как выживаемость пациентов с РПОК на поздней стадии составляет всего 13,1%. Лечение пациентов с РПОК на поздней стадии часто бывает очень дорогостоящим и может лишь облегчить симптомы заболевания (Clinical Interventions in Aging 2016; 11: 967-976).
[0005] Развитие РПОК представляет собой медленный процесс, который обычно протекает бессимптомно, и его трудно диагностировать на ранней стадии, пока опухоль не достигнет размеров в несколько сантиметров, что может блокировать отхождение кала и приводить к спазмам, боли или видимым кровотечениям. Развитие РПОК проходит через многостадийный процесс, включающий ряд гистологических, морфологических и генетических изменений, которые накапливаются с течением времени, а именно, от здорового состояния, гиперплазии, небольших полипов, крупных полипов и аденокарциномы до рака. Полипы представляют собой аномальные клетки, которые растут или накапливаются локально в слизистой кишечника. Делящиеся клетки полипов могут аккумулировать генетические изменения, достаточные для проникновения через стенку кишечника и, в конечном итоге, превращения в РПОК. Однако лишь небольшое количество полипов превращается в РПОК после более чем десятилетнего развития. К двум основным типам потенциально злокачественных полипов относятся аденомы и зубчатые полипы без ножки (SSP), которые развиваются в РПОК с различными степенями риска. Риск превращения аденомы в РПОК зависит от ее размера. Обычно, чем больше размер аденомы, тем больше вероятность ее превращения в РПОК. Прогрессирующие аденомы (ПА) имеют размер ≥1 см или имеют ≥25% ворсинчатого компонента или высокую степень дисплазии любого размера. Хотя, в большинстве случаев, лишь приблизительно 10% ПA становятся злокачественными, однако, 60-70% РПОК развиваются из аденом, а остальные 25-35% РПОК развиваются из SSP (Clinical Interventions in Aging 2016; 11: 967-976). Следовательно, раннее обнаружение РПОК и ПA и удаление поражений может эффективно блокировать прогрессирование РПОК, и тем самым спасти жизнь пациентов, значительно повысить выживаемость пациентов в течение более, чем 5 лет и снизить дорогостоящие затраты на лечение РПОК на поздней стадии, что позволит значительно снизить экономическое бремя на семью и общество.
[0006] В настоящее время существует несколько тестов для обнаружения РПОК, в основном, включающих колоноскопию, сигмоидоскопию, КТ-колонографию, анализ кала на скрытую кровь (FOBT) и иммунохимический анализ кала (FIT).
[0007] Чувствительность колоноскопии для обнаружения РПОК составляет >95%. Интервал между скринингами составляет 10 лет. Преимуществом колоноскопии является высокая чувствительность, позволяющая обследовать всю толстую кишку и одновременно удалить поражение. Однако ее недостатком является инвазивное обследование и подготовка кишечника, которая вызывает у пациента дискомфорт, а поэтому после такой процедуры пациент нуждается в покое. Во время колоноскопии существует риск перфорации кишечника и кровотечения. Из-за этих ограничений пациенты часто не дают согласия на колоноскопический скрининг.
[0008] Чувствительность сигмоидоскопии для обнаружения поражения дистального отдела толстой кишки превышает 95%. Интервал скрининга РПОК с помощью сигмоидоскопии составляет 5 лет в комбинации с FOBT. Преимуществом скрининга РПОК посредством сигмоидоскопии является высокая чувствительность, отсутствие необходимости в приеме системных седативных средств, а также возможность удаления очага поражения во время обследования. Недостатком такой процедуры является полуинвазивное обследование, легко вызывающее дискомфорт при обследовании, и высокая стоимость такого обследования.
[0009] При КТ-колонографии проводят облучение для визуализации толстой кишки, при этом, чувствительность такой процедуры составляет >90%, и эта процедура проводится каждые 5 лет. Преимуществом такого метода является настолько высокая чувствительность, что она позволяет наблюдать всю толстую кишку и не требует введения седативных средств. Недостатком этого анализа является то, что он представляет собой полуинвазивное обследование, а поэтому пациенты могут легко почувствовать дискомфорт во время процесса скрининга. Кроме того, поражения нельзя удалить во время обследования, и необходимо учитывать радиационную безопасность.
[0010] В общих чертах, вышеупомянутые тесты для диагностики РПОК на основе визуализации имеют высокую чувствительность, но они являются дорогостоящми, а подготовка кишечника часто вызывает дискомфорт и другие побочные эффекты. Как следствие, пациент плохо соблюдает режим такого скрининга. Кроме того, для этих анализов требуется профессиональное оборудование, и нужны врачи с профессиональными навыками и богатым опытом, что не всегда бывает возможно. В результате, общий уровень скрининга/диагностики является низким. Кроме того, некоторым пациентам не показаны такие анализы. Так, например, у пациентов с диабетом, подготовка кишечника является менее успешной, и это повышает риск побочных эффектов (J. Gastrointestin Liver Dis 2010; 19: 369-372, World J Gastrointest Endosc 2013; 5: 39-46).
[0011] FOBT и FIT позволяют детектировать гемоглобин в кале пациентов с помощью ферментативной реакции и иммунохимического метода, соответственно, с чувствительностью 33-75% и 60-85% соответственно, для диагностики РПОК, и эти анализы проводят каждый год. Хотя FOBT и FIT являются легкодоступными, неинвазивными и недорогостоящими анализами, однако, частота выявления предраковых поражений является низкой (Clinical Interventions in Aging 2016; 11 967-976).
[0012] Во время превращения полипов в РПОК, мутации и изменения метилирования аккумулируются в некоторых генах, таких как APC, KRAS, p53, BRAF, NDRG4, BMP3 и т.п. (Clinical Interventions in Aging 2016; 11:967-976). Следовательно, обнаружение этих мутаций или изменений метилирования помогает обнаруживать РПОК и предраковые поражения.
[0013] Zou и др. (Clinical Chemistry 2012; 58: 2375-383) проводили метилирующую кол.ПЦР для определения уровней метилирования генов BMP3, NDRG4, VIM и TFPI2 в образцах тканей. Всего было протестировано 37 образцов ткани РПОК, 25 образцов ткани аденомы и 29 образцов здоровой ткани человека. Когда специфичность составляла 95%, то чувствительность обнаружения генов BMP3, NDRG4, VIM и TFPI2 при диагностике РПОК составляла 84%, 92%, 86% и 92% соответственно, а их чувствительность при диагностике аденомы составляла 68%, 76%, 76% и 88%, соответственно. Было показано, что детектирование метилирования генов в тканях рака толстой кишки имеет высокую чувствительность и специфичность. Однако метод отбора проб ткани пока еще не нашел широкого применения, поскольку процесс отбора проб приводит к определенным повреждениям в организме пациента. Следовательно, он не подходит для скрининга на РПОК и предраковые поражения у населения в целом.
[0014] Многоцелевое тестирование ДНК кала (mt-sДНК) включает обнаружение метилирования и мутаций в слущенных клетках опухолей и обнаружение гемоглобина в пробах кала, и это тестирование, которое проводят каждые 3 года, имеет такие преимущества, как высокая чувствительность, неинвазивность и доступность для населения (Clinical Interventions in Aging 2016; 11:967-976). В качестве метода скрининга, mt-sДНК позволяет обнаруживать РПОК и ПA на ранней стадии, что значительно повышает выживаемость пациентов. Imperiale et al. (N. Eng.l J. Med. 2014; 370: 1287-97) разработали систему на основе mt-sДНК для детектирования метилирования генов BMP3 и NDRG4, для обнаружения точковых мутаций гена KRAS и для обнаружения гемоглобина в кале, с последующей оценкой риска развития РПОК и ПA по формуле логистической регрессии. Чувствительность определения РПОК и ПА составляет 92,3% и 42,4%, соответственно, а специфичность составляет 86,6%.
[0015] mt-sДНК применяется для скрининга спорадических РПОК и ПА с преимуществом неинвазивности по сравнению с колоноскопией и большей чувствительностью по сравнению с FOBT и FIT, но чувствительность обнаружения ПA все еще намного ниже, чем чувствительность обнаружения РПОК (Clinical Interventions in Aging 2016; 11:967-976).
[0016] В настоящее время, продукты на основе mt-sДНК для диагностики РПОК или ПA, такие как Cologuard®, в основном, разрабатываются для населения Европы и Америки. Доступных продуктов для определения РПОК и ПА у населения Азии пока не существует. В частности, согласно «Сводке данных по безопасности и эффективности (SSED)» Cologuard®, выпущенной Управлением по контролю качества пищевых продуктов и лекарственных средств США (www.accessdata.fda.gov/cdrh_docs/pdf13/P130017b.pdf), чувствительность обнаружения ПА с использованием Cologuard® среди белого населения и афроамериканцев составляет 42,3% и 42,4%, соответственно, но чувствительность обнаружения ПА с использованием того же продукта у населения Азии составляет всего 30,8%. Следовательно, необходимость в разработке эффективной системы выявления РПОК и/или ПA у населения Азии в целях борьбы с текущим ростом заболеваемости и смертности от рака прямой и ободочной кишки в странах Азии остается актуальной.
[0017] Несмотря на то, что было проведено много исследований с применением методов обнаружения метилирования генов BMP3 и NDRG4 в пробах кала пациентов с РПОК и ПА, однако, тщательных и исчерпывающих исследований гиперметилированных сайтов CpG в генах BMP3 и NDRG4 у населения Азии не проводилось (ONCOLOGY LETTERS 2014;8:1751-1756; ONCOLOGY LETTERS 2015;9:1383-1387). Кроме того, из-за ограниченного размера выборки, предыдущие исследования по метилированию генов BMP3 и NDRG4 у пациентов в Азии не помогли определить сайты метилирования, которые являются наиболее релевантными для РПОК и ПА. Следовательно, необходимо определить точную локализацию гиперметилированных сайтов CpG генов BMP3 и NDRG4 у населения в Азии, а также разработать и оптимизировать наборы на основе этих метилированных сайтов CpG, что позволило бы повысить чувствительность обнаружения ПA.
Сущность изобретения
[0018] Настоящее изобретение относится к последовательностям ДНК, содержащим гиперметилированные сайты CpG в промоторной области генов BMP3 и NDRG4.
[0019] Настоящее изобретение также относится к предпочтительным праймерам и зондам для детектирования метилирования генов BMP3 или NDRG4 и к их комбинациям для детектирования метилирования генов BMP3 и NDRG4.
[0020] Настоящее изобретение также относится к набору для диагностики РПОК и ПА у населения Азии. Последовательности ДНК, содержащие гиперметилированные сайты CpG в промоторной области генов BMP3 и NDRG4, могут быть использованы в качестве маркеров для диагностики РПОК и/или ПA у населения Азии.
[0021] По сравнению с другими праймерами и зондами, пары предпочтительных праймеров и зондов для определения уровней метилирования генов BMP3 и/или NDRG4 обладают неожиданно более высокой чувствительностью и специфичностью к опухолевой ткани, такой как ткани РПОК и ПА, а особенно ПA. Кроме того, комбинации этих предпочтительных праймеров и зондов согласно изобретению также обеспечивают неожиданно более высокую чувствительность и специфичность при обнаружении опухолевой ткани, такой как ткань РПОК и ПА, а особенно ПA.
[0022] Настоящее изобретение также относится к набору для для диагностики РПОК и ПA у населения Азии на основе вышеуказанных предпочтительных комбинаций праймеров и зондов.
[0023] В некоторых вариантах осуществления изобретения, набор включает: (1) предпочтительную комбинацию пар праймеров и зондов и соответствующих реагентов для кол.ПЦР; (2) праймеры и зонды для детектирования семи мутаций в кодирующей области гена KRAS и соответствующие реагенты для кол.ПЦР; (3) реагенты для определения гемоглобина в кале.
[0024] В некоторых вариантах осуществления изобретения, данные, полученные в результате анализа с использованием набора, корректируют и анализируют по формуле логистической регрессии. В некоторых вариантах осуществления изобретения, эту формулу используют для вычисления значения при определении наличия или отсутствия РПОК и/или ПA. В некоторых вариантах осуществления изобретения, формула представляет собой P=eK/(1+eK), где P - общий индекс, а K=a*ΔCt1+b*ΔCt2+c*ΔCt3+d*FIT+X, где e означает натуральную константу, и a, b, c, d, X означают клинические константы. В некоторых вариантах осуществления, если значение P равно заданному порогу или превышает этот порог, то результат указывает на наличие РПОК и/или ПА у пациента. В некоторых вариантах осуществления, если значение P меньше порогового значения, то результат указывает на отсутствие РПОК и/или ПА у пациента, и пациент определяется как здоровый.
[0025] Настоящее изобретение относится к набору для определения наличия или отсутствия рака прямой и ободочной кишки (РПОК) или прогрессирующей аденомы (ПA) у пациента, нуждающегося в этом. Пациентом, нуждающимся в этом, является пациент с подозрением на РПОК и/или ПА, например, пациент, имеющий по меньшей мере один признак развития РПОК и/или ПА, или пациент, имеющий риск развития РПОК и/или ПА, или индивидуум, проходящий плановое медицинское обследование, но не имеющий никаких признаков заболевания или риска его развития.
[0026] В некоторых вариантах осуществления изобретения, набор включает: (а) первую пару праймеров и первый зонд для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента. В некоторых вариантах осуществления изобретения, каждая первая пара праймеров и первый зонд включают непрерывную последовательность по меньшей мере из 16 нуклеотидов, которая идентична и комплементарна последовательности SEQ ID NO. 1 или гибридизуется с этой последовательностью в жестких условиях гибридизации.
[0027] В некоторых вариантах осуществления изобретения, набор включает: (b) вторую пару праймеров и второй зонд для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента. В некоторых вариантах осуществления изобретения, каждая вторая пара праймеров и второй зонд включают непрерывную последовательность по меньшей мере из 16 нуклеотидов, которая идентична и комплементарна последовательности SEQ ID NO: 2 или гибридизуется с этой последовательностью в жестких условиях гибридизации.
[0028] В некоторых вариантах осуществления изобретения, первая пара праймеров и первый зонд выбраны из группы, состоящей из:
[0029] i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5;
[0030] ii) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11; и
[0031] iii) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17.
[0032] В некоторых вариантах осуществления изобретения, вторая пара праймеров и второй зонд выбраны из группы, состоящей из:
[0033] iv) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8;
[0034] v) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14; b
[0035] vi) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20.
[0036] В некоторых вариантах осуществления изобретения, набор включает:
i) прямой праймер, содержащий SEQ ID NO: 3, обратный праймер, содержащий SEQ ID NO: 4, и зонд, содержащий SEQ ID NO: 5, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямой праймер, содержащий SEQ ID NO: 6, обратный праймер, содержащий SEQ ID NO: 7, и зонд, содержащий SEQ ID NO: 8, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
[0037] В некоторых вариантах осуществления изобретения, набор включает:
i) прямой праймер, содержащий SEQ ID NO: 9, обратный праймер, содержащий SEQ ID NO: 10, и зонд, содержащий SEQ ID NO: 11, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямой праймер, содержащий SEQ ID NO: 12, обратный праймер, содержащий SEQ ID NO: 13, и зонд, содержащий SEQ ID NO: 14, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
[0038] В некоторых вариантах осуществления изобретения, набор включает:
i) прямой праймер, содержащий SEQ ID NO: 15, обратный праймер, содержащий SEQ ID NO: 16, и зонд, содержащий SEQ ID NO: 17, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямой праймер, содержащий SEQ ID NO: 18, обратный праймер, содержащий SEQ ID NO: 19, и зонд, содержащий SEQ ID NO: 20, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
[0039] В некоторых вариантах осуществления изобретения, первый зонд и второй зонд содержат флуоресцентный донор и акцепторный флуорофор.
[0040] В некоторых вариантах осуществления изобретения, первый зонд и второй зонд представляют собой зонды TAQMAN®.
[0041] В некоторых вариантах осуществления изобретения, набор дополнительно включает:
(1) средство для обнаружения наличия или отсутствия по меньшей мере одной мутации в гене KRAS у пациента; и
(2) средство для обнаружения наличия или отсутствия гемоглобина в биологическом образце, взятом у пациента.
[0042] В некоторых вариантах осуществления изобретения, средство для обнаружения присутствия или отсутствия по меньшей мере одной мутации в гене KRAS у пациента включает по меньшей мере одну пару праймеров, способных амплифицировать область экзона 12 и/или экзона 13 гена KRAS в полимеразной цепной реакции (ПЦР).
[0043] В некоторых вариантах осуществления изобретения, средство для обнаружения присутствия или отсутствия гемоглобина в биологическом образце включает антитело против гемоглобина.
[0044] В некоторых вариантах осуществления изобретения, праймеры способны амплифицировать область гена KRAS, содержащую по меньшей мере одну мутацию KRAS, выбранную из группы, состоящей из G12D, G12V, G12C, G13D, G12A, G12R, G12S и G13C.
[0045] В некоторых вариантах осуществления изобретения, антитело представляет собой антитело, конъюгированное с коллоидным золотом.
В некоторых вариантах осуществления изобретения, набор дополнительно включает средство для амплификации гена внутреннего контроля качества. Внутренний контроль может обнаруживать (1) ингибирующее загрязнение, вносимое образцом или методом экстракции, (2) неисправность прибора, (3) химические факторы (например, просроченный или испорченный набор или испорченные компоненты или несоответствующую комбинацию реагентов) и (4) человеческий фактор. В некоторых вариантах осуществления изобретения, ген внутреннего контроля представляет собой позитивный контроль, такой как ген в образце позитивного контроля, который, как было установлено, имеет метилирование. В некоторых вариантах осуществления изобретения, ген внутреннего контроля представляет собой негативный контроль, такой как ген в образце негативного контроля, который, как было установлено, не имеет метилирования.
[0046] В некоторых вариантах осуществления изобретения, набор дополнительно содержит инструкции по применению и/или интерпретации результата теста, полученного с помощью набора.
[0047] В некоторых вариантах осуществления изобретения, набор дополнительно включает средства для детектирования комплекса, образованного антителом и гемоглобином в биологическом образце.
[0048] В некоторых вариантах осуществления изобретения, биологический образец, взятый у пациента, представляет собой пробу кала.
[0049] В некоторых вариантах осуществления изобретения, набор дополнительно включает бисульфитный реагент и контейнер, подходящий для смешивания бисульфитного реагента и биологического образца пациента или полинуклеотидов, полученных из биологического образца.
[0050] В некоторых вариантах осуществления изобретения, набор, вместо бисульфита, дополнительно включает рестриктирующий фермент-реагент, чувствительный к метилированию.
[0051] В некоторых вариантах осуществления изобретения, набор дополнительно включает: (1) позитивный стандарт и негативный стандарт для детектирования метилирования BMP3 в биологическом образце и (2) позитивный стандарт и негативный стандарт для детектирования метилирования NDRG4 в биологическом образце.
[0052] В некоторых вариантах осуществления изобретения, позитивный стандарт для детектирования метилирования BMP3 содержит полинуклеотидную последовательность:
GTTAGTTTGGTCGGGTGTTTTTAAAAATAAAGCGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTCGGGTTATATACGTCGCGATTTATAGTTTTTTTTTAGCGTTGGAGTGGAGACGGCGTTCGTAGCGTTTTGCGCGGGTGAGGTTCGCGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGCGTTGGGTTAGCGTAGTAAGTGGGGTTGGTCGTTATTTCGTTGTATTCGGTCGCGTTTCGGGTTTCGTGCGTTTTCGTTTTAG (SEQ ID NO: 67).
[0053] В некоторых вариантах осуществления изобретения, негативный стандарт для детектирования метилирования BMP3 содержит полинуклеотидную последовательность:
GTTAGTTTGGTTGGGTGTTTTTAAAAATAAAGTGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTTGGGTTATATATGTTGTGATTTATAGTTTTTTTTTAGTGTTGGAGTGGAGATGGTGTTTGTAGTGTTTTGTGTGGGTGAGGTTTGTGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGTGTTGGGTTAGTGTAGTAAGTGGGGTTGGTTGTTATTTTGTTGTATTTGGTTGTGTTTTGGGTTTTGTGTGTTTTTGTTTTAG (SEQ ID NO: 68);
[0054] В некоторых вариантах осуществления изобретения, позитивный стандарт для детектирования метилирования NDRG4 содержит полинуклеотидную последовательность:
TGAGAAGTCGGCGGGGGCGCGGATCGATCGGGGTGTTTTTTAGGTTTCGCGTCGCGGTTTTCGTTCGTTTTTTCGTTCGTTTATCGGGTATTTTAGTCGCGTAGAAGGCGGAAGTTACGCGCGAGGGATCGCGGTTCGTTCGGGATTAGTTTTAGGTTCGGTATCGTTTCGCGGGTCGAGCGTTTATATTCGTTAAATTTACGCGGGTACGTTTTCGCGGCGTATCGTTTTTAGTT (SEQ ID NO: 69).
[0055] В некоторых вариантах осуществления изобретения, негативный стандарт для детектирования метилирования NDRG4 содержит полинуклеотидную последовательность:
TGAGAAGTTGGTGGGGGTGTGGATTGATTGGGGTGTTTTTTAGGTTTTGTGTTGTGGTTTTTGTTTGTTTTTTTGTTTGTTTATTGGGTATTTTAGTTGTGTAGAAGGTGGAAGTTATGTGTGAGGGATTGTGGTTTGTTTGGGATTAGTTTTAGGTTTGGTATTGTTTTGTGGGTTGAGTGTTTATATTTGTTAAATTTATGTGGGTATGTTTTTGTGGTGTATTGTTTTTAGTT (SEQ ID NO: 70).
[0056] Настоящее изобретение также относится к способу обнаружения наличия или отсутствия рака прямой и ободочной кишки (РПОК) или прогрессирующей аденомы (ПA) у пациента, нуждающегося в этом.
[0057] В некоторых вариантах осуществления изобретения, способ включает а) получение геномной ДНК из биологического образца пациента.
[0058] В некоторых вариантах осуществления изобретения, способ дополнительно включает b) обработку геномной ДНК (а) или ее фрагмента одним или несколькими реагентами для превращения цитозиновых оснований, которые не являются метилированными, в урацил или в другое основание, которое заметно отличается от цитозина с точки зрения свойств гибридизации.
[0059] В некоторых вариантах осуществления изобретения, способ дополнительно включает с) контактирование обработанной геномной ДНК или ее обработанного фрагмента с первой парой праймеров для обнаружения наличия или отсутствия сайтов метилирования гена, кодирующего белок морфогенеза кости 3 (BMP3) у пациента. В некоторых вариантах осуществления изобретения, способ дополнительно включает контактирование обработанной геномной ДНК или ее фрагмента со второй парой праймеров для обнаружения у пациента наличия или отсутствия сайтов метилирования гена, кодирующего белок члена семейства NDRG4 (NDRG4) у пациента.
[0060] В некоторых вариантах осуществления изобретения, первая пара праймеров содержит непрерывную последовательность по меньшей мере из 9 нуклеотидов, которая идентична или комплементарна SEQ ID NО: 1 или гибридизуется с этой последовательностью в жестких условиях гибридизации. В некоторых вариантах осуществления изобретения, вторая пара праймеров содержит непрерывную последовательность по меньшей мере из 9 нуклеотидов, которая идентична или комплементарна SEQ ID NО: 2 или гибридизуется с этой последовательностью в жестких условиях гибридизации.
[0061] В некоторых вариантах осуществления изобретения, обработанная геномная ДНК или ее фрагмент либо амплифицируют для получения по меньшей мере одного амплификата с помощью первой пары праймеров или второй пары праймеров, либо не амплифицируют.
[0062] В некоторых вариантах осуществления изобретения, способ дополнительно включает d) определение присутствия или отсутствия РПОК или ПA у пациента исходя из наличия или отсутствия указанного амплификата, состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 и гена NDRG4 у пациента.
[0063] В некоторых вариантах осуществления изобретения, количественную ПЦР проводят для амплификации метилированного гена BMP3 в образце. В некоторых вариантах осуществления изобретения, количественную ПЦР проводят для амплификации метилированного гена NDRG4 в образце.
[0064] В некоторых вариантах осуществления изобретения, способ также включает использование праймеров для амплификации контрольного гена (также известного как нормализатор, ген «домашнего хозяйства» или эндогенный контроль). В некоторых вариантах осуществления изобретения, количественную ПЦР проводит для амплификации контрольного гена в образце.
[0065] В некоторых вариантах осуществления изобретения, первая пара праймеров и первый зонд выбраны из группы, состоящей из:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5;
ii) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11; и
iii) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17.
[0066] В некоторых вариантах осуществления изобретения, вторая первая пара праймеров и второй зонд выбраны из группы, состоящей из:
iv) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8;
v) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14; и
vi) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20.
[0067] В некоторых вариантах осуществления изобретения, способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
[0068] В некоторых вариантах осуществления изобретения, способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
[0069] В некоторых вариантах осуществления изобретения, способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
[0070] В некоторых вариантах осуществления изобретения, первый зонд и второй зонд содержат флуоресцентный донор и акцепторный флуорофор. В некоторых вариантах осуществления изобретения, первый зонд и второй зонд представляют собой зонды TAQMAN®.
[0071] В некоторых вариантах осуществления изобретения, способ дополнительно включает стадию обнаружения присутствия или отсутствия по меньшей мере одной мутации в гене KRAS в биологическом образце, взятом у пациента.
[0072] В некоторых вариантах осуществления изобретения, способ дополнительно включает стадию обнаружения присутствия или отсутствия гемоглобина в биологическом образце, взятом у пациента. В некоторых вариантах осуществления изобретения, стадия обнаружения наличия или отсутствия гемоглобина в биологическом образце включает использование антитела против гемоглобина. В некоторых вариантах осуществления изобретения, антитело представляет собой антитело, конъюгированное с коллоидным золотом.
[0073] В некоторых вариантах осуществления изобретения, стадия обнаружения наличия или отсутствия по меньшей мере одной мутации в гене KRAS у пациента включает использование по меньшей мере одной пары праймеров, способных амплифицировать область экзона 12 и/или экзона 13 гена KRAS в полимеразной цепной реакции (ПЦР). В некоторых вариантах осуществления изобретения, праймеры способны амплифицировать область гена KRAS, содержащую по меньшей мере одну мутацию KRAS, выбранную из группы, состоящей из G12D, G12V, G12C, G13D, G12A, G12R, G12S и G13C.
[0074] В некоторых вариантах осуществления изобретения, мутантный ген KRAS амплифицируют с использованием одной или более пар праймеров, выбранных из группы, состоящей из:
(1) прямого праймера G12D-F, содержащего SEQ ID NO: 35, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(2) прямого праймера G13D-F, содержащего SEQ ID NO: 36, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(3) прямого праймера G12V-F, содержащего SEQ ID NO: 37, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(4) прямого праймера G12C-F, содержащего SEQ ID NO: 38, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(5) прямого праймера G12S-F, содержащего SEQ ID NO: 39, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(6) прямого праймера G12A-F, содержащего SEQ ID NO: 40, и обратного праймера Kras-R, содержащего SEQ ID NO: 42; и
(7) прямого праймера G12R-F, содержащего SEQ ID NO: 41, и обратного праймера Kras-R, содержащего SEQ ID NO: 42.
[0075] В некоторых вариантах осуществления изобретения, зонд KRAS для кол.ПЦР содержит SEQ ID NO: 46.
[0076] В некоторых вариантах осуществления изобретения, амплификацию гена BMP3 проводят с помощью количественной ПЦР (кол.ПЦР), и способ дополнительно включает амплификацию первого контрольного гена (то есть, первого эталонного гена) для определения значения Ct амплификации BMP3 как ΔCt1.
[0077] В некоторых вариантах осуществления изобретения, амплификацию гена NDRG4 проводят с помощью количественной ПЦР (кол.ПЦР), и способ дополнительно включает амплификацию второго контрольного гена (то есть, второго эталонного гена) для определения значения Ct амплификации NDRG4 как ΔCt2.
[0078] В некоторых вариантах осуществления изобретения, амплификацию мутантного гена KRAS проводят с помощью количественной ПЦР (кол.ПЦР), и способ дополнительно включает амплификацию третьего контрольного гена (то есть, третьего эталонного гена) для определения значения Ct амплификации мутантного KRAS как ΔCt3.
[0079] В некоторых вариантах осуществления изобретения, первый и второй контрольные гены являются одинаковыми. В некоторых вариантах осуществления изобретения, указанный контрольный ген представляет собой ген B2M.
[0080] В некоторых вариантах осуществления изобретения, третий контрольный ген представляет собой ген ACTB. В некоторых вариантах осуществления изобретения, праймеры кол.ПЦР для амплификации гена ACTB содержат SEQ ID NO: 43 и 44, а зонд содержит SEQ ID NO: 46.
[0081] В некоторых вариантах осуществления изобретения, способ включает применение (1) позитивного стандарта и негативного стандарта для детектирования метилирования BMP3 в образце и (2) позитивного стандарта и негативного стандарта для детектирования метилирования NDRG4 в образце.
[0082] В некоторых вариантах осуществления изобретения, позитивный стандарт для детектирования метилирования BMP3 содержит полинуклеотидную последовательность:
GTTAGTTTGGTCGGGTGTTTTTAAAAATAAAGCGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTCGGGTTATATACGTCGCGATTTATAGTTTTTTTTTAGCGTTGGAGTGGAGACGGCGTTCGTAGCGTTTTGCGCGGGTGAGGTTCGCGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGCGTTGGGTTAGCGTAGTAAGTGGGGTTGGTCGTTATTTCGTTGTATTCGGTCGCGTTTCGGGTTTCGTGCGTTTTCGTTTTAG (SEQ ID NO: 67);
[0083] В некоторых вариантах осуществления изобретения, негативный стандарт для детектирования метилирования BMP3 содержит полинуклеотидную последовательность
GTTAGTTTGGTTGGGTGTTTTTAAAAATAAAGTGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTTGGGTTATATATGTTGTGATTTATAGTTTTTTTTTAGTGTTGGAGTGGAGATGGTGTTTGTAGTGTTTTGTGTGGGTGAGGTTTGTGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGTGTTGGGTTAGTGTAGTAAGTGGGGTTGGTTGTTATTTTGTTGTATTTGGTTGTGTTTTGGGTTTTGTGTGTTTTTGTTTTAG (SEQ ID NO: 68);
[0084] В некоторых вариантах осуществления изобретения, позитивный стандарт для детектирования метилирования NDRG4 содержит полинуклеотидную последовательность
TGAGAAGTCGGCGGGGGCGCGGATCGATCGGGGTGTTTTTTAGGTTTCGCGTCGCGGTTTTCGTTCGTTTTTTCGTTCGTTTATCGGGTATTTTAGTCGCGTAGAAGGCGGAAGTTACGCGCGAGGGATCGCGGTTCGTTCGGGATTAGTTTTAGGTTCGGTATCGTTTCGCGGGTCGAGCGTTTATATTCGTTAAATTTACGCGGGTACGTTTTCGCGGCGTATCGTTTTTAGTT (SEQ ID NO: 69).
[0085] В некоторых вариантах осуществления изобретения, негативный стандарт для детектирования метилирования NDRG4 содержит полинуклеотидную последовательность
TGAGAAGTTGGTGGGGGTGTGGATTGATTGGGGTGTTTTTTAGGTTTTGTGTTGTGGTTTTTGTTTGTTTTTTTGTTTGTTTATTGGGTATTTTAGTTGTGTAGAAGGTGGAAGTTATGTGTGAGGGATTGTGGTTTGTTTGGGATTAGTTTTAGGTTTGGTATTGTTTTGTGGGTTGAGTGTTTATATTTGTTAAATTTATGTGGGTATGTTTTTGTGGTGTATTGTTTTTAGTT (SEQ ID NO: 70).
[0086] В некоторых вариантах осуществления изобретения, способ включает амплификацию стандарта контроля качества.
[0087] В некоторых вариантах осуществления изобретения, способ обнаружения наличия или отсутствия рака прямой и ободочной кишки (РПОК) или прогрессирующей аденомы (ПA) у пациента, нуждающегося в этом, включает использование набора согласно изобретению.
[0088] Настоящее изобретение также относится к способу обнаружения наличия или отсутствия рака прямой и ободочной кишки (РПОК) или прогрессирующей аденомы (AA) у пациента, нуждающегося в этом, где указанный способ включает:
а) получение необработанной геномной ДНК из пробы кала пациента;
b) обработку геномной ДНК (а) или ее фрагмента одним или более реагентами для превращения цитозиновых оснований, которые являются неметилированнными, в урацил или другое основание, которое заметно отличается от цитозина с точки зрения свойств гибридизации;
c) проведение количественной ПЦР (кол.ПЦР) с использованием обработанной геномной ДНК (b) в качестве матрицы и определение значения Ct гена BMP3 у пациента как ΔCt1;
d) проведение кол.ПЦР с использованием обработанной геномной ДНК (b) в качестве матрицы и определение значения Ct гена NDRG4 у пациента как ΔCt2;
e) проведение кол.ПЦР с использованием необработанной геномной ДНК в качестве матрицы и определение значения мутантного гена KRAS у пациента как ΔCt3;
f) проведение иммунохимического анализа кала на белок гемоглобин в образце кала и оценку результата как FIT;
g) определение значения K, где K=a*ΔCt1+b*ΔCt2+c*ΔCt3+d*FIT+X, где a, b, c, d, X=клинические константы; и
h) определение значения общего индекса P, где Р=eK/(1+eK), где e представляет собой натуральную константу.
[0089] Клинические константы a, b, c, d и X могут быть определены путем анализа распределения клинических данных у групп пациентов.
[0090] В некоторых вариантах осуществления изобретения, если P равно заданному пороговому значению или превышает это значение, то пациент определяется как пациент с РПОК и/или ПА, а если P меньше заданного порогового значения, то пациент определяется как здоровый.
[0091] В некоторых вариантах осуществления изобретения, заданное пороговое значение вычисляют из распределения клинических данных, таких как клинические данные, полученные от пациентов, у которых было установлено наличие РПОК и/или ПА, и пациентов, у которых не были диагностированы РПОК и/или ПА.
[0092] В некоторых вариантах осуществления изобретения, кол.ПЦР для амплификации гена BMP3 включает первую пару праймеров и первый зонд, где первая пара праймеров и первый зонд выбраны из группы, состоящей из:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5;
ii) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11; и
iii) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17.
[0093] В некоторых вариантах осуществления изобретения, кол.ПЦР для амплификации гена NDRG4 включает вторую пару праймеров и второй зонд, где вторая пара праймеров и второй зонд выбраны из группы, состоящей из:
iv) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8;
v) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14; и
vi) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20.
[0094] В некоторых вариантах осуществления изобретения, способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в образце, и
ii) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в образце.
[0095] В некоторых вариантах осуществления изобретения, способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в образце; и
ii) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в образце.
[0096] В некоторых вариантах осуществления изобретения, способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в образце; и
ii) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в образце.
[0097] В некоторых вариантах осуществления изобретения, первый зонд и второй зонд содержат флуоресцентный донор и акцепторный флуорофор. В некоторых вариантах осуществления изобретения, первый зонд и второй зонд представляют собой зонды TAQMAN®.
[0098] В некоторых вариантах осуществления изобретения, мутантный ген KRAS содержит по меньшей мере одну мутацию KRAS, выбранную из группы, состоящей из G12D, G12V, G12C, G13D, G12A, G12R, G12S и G13C.
[0099] В некоторых вариантах осуществления изобретения, иммунохимический анализ кала включает антитело, конъюгированное с коллоидным золотом.
[00100] В некоторых вариантах осуществления изобретения, стадия c) и стадия d) способа включают использование гена B2M в качестве контрольного гена.
[00101] В некоторых вариантах осуществления изобретения, способ включает применение:
(1) позитивного стандарта и негативного стандарта для детектирования метилирования BMP3 в образце, и
(2) позитивного стандарта и негативного стандарта для детектирования метилирования NDRG4 в образце.
[00102] В некоторых вариантах осуществления изобретения, позитивный стандарт для детектирования метилирования BMP3 содержит полинуклеотидную последовательность
GTTAGTTTGGTCGGGTGTTTTTAAAAATAAAGCGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTCGGGTTATATACGTCGCGATTTATAGTTTTTTTTTAGCGTTGGAGTGGAGACGGCGTTCGTAGCGTTTTGCGCGGGTGAGGTTCGCGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGCGTTGGGTTAGCGTAGTAAGTGGGGTTGGTCGTTATTTCGTTGTATTCGGTCGCGTTTCGGGTTTCGTGCGTTTTCGTTTTAG (SEQ ID NO: 67).
[00103] В некоторых вариантах осуществления изобретения, негативный стандарт для детектирования метилирования BMP3 содержит полинуклеотидную последовательность
GTTAGTTTGGTTGGGTGTTTTTAAAAATAAAGTGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTTGGGTTATATATGTTGTGATTTATAGTTTTTTTTTAGTGTTGGAGTGGAGATGGTGTTTGTAGTGTTTTGTGTGGGTGAGGTTTGTGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGTGTTGGGTTAGTGTAGTAAGTGGGGTTGGTTGTTATTTTGTTGTATTTGGTTGTGTTTTGGGTTTTGTGTGTTTTTGTTTTAG (SEQ ID NO: 68).
[00104] В некоторых вариантах осуществления изобретения, позитивный стандарт для детектирования метилирования NDRG4 содержит полинуклеотидную последовательность
TGAGAAGTCGGCGGGGGCGCGGATCGATCGGGGTGTTTTTTAGGTTTCGCGTCGCGGTTTTCGTTCGTTTTTTCGTTCGTTTATCGGGTATTTTAGTCGCGTAGAAGGCGGAAGTTACGCGCGAGGGATCGCGGTTCGTTCGGGATTAGTTTTAGGTTCGGTATCGTTTCGCGGGTCGAGCGTTTATATTCGTTAAATTTACGCGGGTACGTTTTCGCGGCGTATCGTTTTTAGTT (SEQ ID NO: 69).
[00105] В некоторых вариантах осуществления изобретения, негативный стандарт для детектирования метилирования NDRG4 включает полинуклеотидную последовательность
TGAGAAGTTGGTGGGGGTGTGGATTGATTGGGGTGTTTTTTAGGTTTTGTGTTGTGGTTTTTGTTTGTTTTTTTGTTTGTTTATTGGGTATTTTAGTTGTGTAGAAGGTGGAAGTTATGTGTGAGGGATTGTGGTTTGTTTGGGATTAGTTTTAGGTTTGGTATTGTTTTGTGGGTTGAGTGTTTATATTTGTTAAATTTATGTGGGTATGTTTTTGTGGTGTATTGTTTTTAGTT (SEQ ID NO: 70).
В некоторых вариантах осуществления способ включает амплификацию стандарта контроля качества на стадии c) и стадии d).
[00106] Настоящее изобретение также относится к способу диагностики и лечения рака прямой и ободочной кишки (РПОК) и/или прогрессирующей аденомы (AA) у пациента, нуждающегося в этом, где указанный способ включает определение наличия или отсутствия РПОК и/или ПА у пациента с использованием набора согласно изобретению, и лечение пациента в зависимости от наличия или отсутствия у него РПОК и/или ПА.
[00107] Настоящее изобретение также относится к способу диагностики и лечения рака прямой и ободочной кишки (РПОК) и/или прогрессирующей аденомы (AA) у пациента, нуждающегося в этом, где указанный способ включает определение наличия или отсутствия РПОК и/или ПА у пациента с применением описанного здесь способа, и лечение пациента в зависимости от наличия или отсутствия у него РПОК и/или ПА.
Краткое описание чертежей
[00108] На фигурах 1А-1D показаны результаты предсказания наличия области CpG и относительного положения ампликонов двух генов BMP3 и NDRG4. «Y», «R» представляют собой вырожденные основания. На Фигуре 1A представлен результат предсказания области CpG промотора генов BMP3; На Фигуре 1B показано относительное положение ампликонов гена BMP3; на Фигуре 1C представлен результат предсказания области CpG промотора генов NDRG4; на Фигуре 1D показано относительное положение ампликонов гена NDRG4.
[00109] На Фигуре 2А показано различие в CpG-сайтах метилирования BMP у белого населения и у населения Азии. На Фигуре 2В показано различие в CpG-сайтах метилирования гена NDRG4 у белого населения и у населения Азии.
[00110] На Фигуре 3A представлена аналитическая кривая амплификации чувствительности для BMP3 вместе с праймерами и зондами в предпочтительной группе 1. На Фигуре 3B представлена аналитическая кривая амплификации чувствительности для NDRG4 вместе с праймерами и зондами в предпочтительной группе 1. На Фигуре 3С представлена аналитическая кривая амплификации чувствительности для BMP3 вместе с праймерами и зондами в предпочтительной группе 2. На Фигуре 3D представлена аналитическая кривая амплификации чувствительности для NDRG4 вместе с праймерами и зондами в предпочтительной группе 2. На Фигуре 3E представлена аналитическая кривая амплификации чувствительности для BMP3 вместе с праймерами и зондами в предпочтительной группе 3. На Фигуре 3F представлена аналитическая кривая амплификации чувствительности для NDRG4 вместе с праймерами и зондами в предпочтительной группе 3. На Фигуре 3G представлена аналитическая кривая амплификации чувствительности для BMP3, вместе с праймерами и зондами в сравнительной группе 1. На фигуре 3H представлена кривая амплификации аналитической чувствительности для NDRG4 вместе с праймерами и зондами в сравнительной группе 1. На Фигуре 3I представлена аналитическая кривая амплификации чувствительности для BMP3, вместе с праймерами и зондами в сравнительной группе 2. На фигуре 3J представлена кривая амплификации аналитической чувствительности для NDRG4 вместе с праймерами и зондами в сравнительной группе 2. На Фигуре 3K представлена аналитическая кривая амплификации чувствительности для BMP3, вместе с праймерами и зондами в сравнительной группе 3. На фигуре 3L представлена кривая амплификации аналитической чувствительности для NDRG4 вместе с праймерами и зондами в сравнительной группе 3.
[00111] На Фигуре 4A представлена аналитическая кривая амплификации специфичности для BMP3 вместе с праймерами и зондами в предпочтительной группе 1. На Фигуре 4B представлена аналитическая кривая амплификации специфичности для NDRG4 вместе с праймерами и зондами в предпочтительной группе 1. На Фигуре 4С представлена аналитическая кривая амплификации специфичности для BMP3 вместе с праймерами и зондами в предпочтительной группе 2. На Фигуре 4D представлена аналитическая кривая амплификации специфичности для NDRG4 вместе с праймерами и зондами в предпочтительной группе 2. На Фигуре 4E представлена аналитическая кривая амплификации специфичности для BMP3 вместе с праймерами и зондами в предпочтительной группе 3. На Фигуре 4F представлена аналитическая кривая амплификации специфичности для NDRG4 вместе с праймерами и зондами в предпочтительной группе 3. На Фигуре 4G представлена аналитическая кривая амплификации специфичности для BMP3, вместе с праймерами и зондами в сравнительной группе 1. На фигуре 4H представлена кривая амплификации аналитической специфичности для NDRG4 вместе с праймерами и зондами в сравнительной группе 1. На Фигуре 4I представлена аналитическая кривая амплификации специфичности для BMP3, вместе с праймерами и зондами в сравнительной группе 2. На фигуре 4J представлена кривая амплификации аналитической специфичности для NDRG4 вместе с праймерами и зондами в сравнительной группе 2. На Фигуре 4K представлена аналитическая кривая амплификации специфичности для BMP3, вместе с праймерами и зондами в сравнительной группе 3. На фигуре 4L представлена кривая амплификации аналитической специфичности для NDRG4 вместе с праймерами и зондами в сравнительной группе 3.
[00112] На фигурах 5A-5C показаны кривые амплификации с использованием праймеров и зондов в предпочтительной группе 1, в предпочтительной группе 2 и в предпочтительной группе 3, соответственно, для детектирования метилирования BMP3 в клиническом образце. На фигурах 5D-5F показаны кривые амплификации с использованием праймеров и зондов в сравнительной группе 1, в сравнительной группе 2 и в сравнительной группе 3, соответственно, для детектирования метилирования BMP3 в том же анализе.
[00113] На фигурах 6A-6C показаны кривые амплификации с использованием праймеров и зондов в предпочтительной группе 1, в предпочтительной группе 2 и в предпочтительной группе 3, соответственно, для детектирования метилирования NDRG4 в клиническом образце. На фигурах 6D-6F показаны кривые амплификации с использованием праймеров и зондов в сравнительной группе 1, в сравнительной группе 2 и в сравнительной группе 3, соответственно, для детектирования метилирования NDRG4 в том же анализе.
Подробное описание изобретения
Определения
[00114] Ссылки на «один вариант осуществления изобретения», «вариант осуществления изобретения», «один пример» и «пример» указывают на то, что описанный(е) таким образом вариант(ы) или пример(ы) может (могут) включать конкретный признак, структуру, характеристику, свойство, элемент или ограничение, однако, не каждый вариант или пример обязательно включает такую конкретную функцию, структуру, характеристику, свойство, элемент или ограничение. Кроме того, повторное использование фразы «в одном варианте осуществления» необязательно относится к одному и тому же варианту осуществления, хотя возможен и такой вариант.
[00115] Используемые здесь термины «нуклеиновая кислота», или «олигонуклеотид», или «полинуклеотид» означают по меньшей мере два нуклеотида, ковалентно связанные друг с другом. Описание одной цепи также определяет последовательность комплементарной цепи. Таким образом, нуклеиновая кислота также включает комплементарную цепь описанной одной цепи. Многие варианты нуклеиновой кислоты могут быть использованы для той же цели, что и данная нуклеиновая кислота. Таким образом, нуклеиновая кислота также включает практически идентичные нуклеиновые кислоты и их комплементы. Одна цепь представляет собой зонд, который может гибридизоваться с последовательностью-мишенью в жестких условиях гибридизации. Таким образом, нуклеиновая кислота также включает зонд, который гибридизуется в жестких условиях гибридизации. Нуклеиновые кислоты могут быть одноцепочечными или двухцепочечными, либо они могут содержать части как двухцепочечных, так и одноцепочечных последовательностей. Нуклеиновая кислота может представлять собой ДНК, как геномную, так и кДНК, РНК или гибрид, где нуклеиновая кислота может содержать комбинации дезоксирибо- и рибонуклеотидов и комбинации оснований, включая урацил, аденин, тимин, цитозин, гуанин, инозин, ксантин, гипоксантин, изоцитозин и изогуанин. Нуклеиновые кислоты могут быть получены методами химического синтеза или рекомбинантными методами.
[00116] Используемое здесь выражение «индивидуум, нуждающийся в этом» относится к животному или человеку, у которого был диагностирован рак, у которого имеется риск развития рака (например, у индивидуума с генетической предрасположенностью к раку, у индивидуума с медицинским и/или семейным анамнезом, у индивидуума, который подвергался воздействию канцерогенов, опасности, связанной с профессиональной деятельностью, и опасности, связанной с неблагоприятной окружающей средой), и/или у которого наблюдаются подозрительные клинические признаки рака (например, кровь в стуле или в мелене, необъяснимая боль, потливость, необъяснимая лихорадка, необъяснимая потеря веса вплоть до анорексии, изменения в поведении кишечника (запор и/или диарея), тенезмы (ощущение неполной дефекации, особенно для рака прямой кишки), анемия и/или общая слабость). Дополнительно или альтернативно, индивидуумом, нуждающимся в этом, может быть здоровый человек, проходящий обычное обследование состояния здоровья.
[00117] Используемый здесь термин «приблизительно» означает ±10%.
[00118] Фраза «состоящий, по существу, из» означает, что композиция или способ могут включать дополнительные ингредиенты и/или стадии, но только в том случае, если эти дополнительные ингредиенты и/или стадии существенно не изменяют основные и новые свойства заявленной композиции или способа.
[00119] Используемые в настоящей заявке артикли «a», «an» и «the», употребляемые с существительными в единственном числе, могут относиться и к существительным во множественном числе, если из контекста описания не следует обратное. Так, например, термин «соединение» или «по меньшей мере одно соединение» может включать множество соединений, включая их смеси.
[00120] Используемый здесь термин «жесткие условия гибридизации» означает условия, при которых первая последовательность нуклеиновой кислоты (например, зонд) будет гибридизоваться со второй последовательностью нуклеиновой кислоты (например, мишенью), например, в сложной смеси нуклеиновых кислот. Жесткие условия гибридизации зависят от последовательности и будут отличаться в различных случаях. Могут быть выбраны жесткие условия, при которых температура приблизительно на 5-10°C ниже, чем температура плавления (Tm) для конкретной последовательности при определенной ионной силе и pH. Tm может представлять собой температуру (при определенной ионной силе, pH и концентрации нуклеиновых кислот), при которой 50% зондов, комплементарных мишени, гибридизуются с последовательностью-мишенью в равновесном состоянии (поскольку последовательности-мишени присутствуют в избытке при такой Tm, а 50% зондов находятся в состоянии равновесия). Жесткие условия могут представлять собой такие условия, при которых концентрация соли составляет менее, чем приблизительно 1,0 М иона натрия, например, приблизительно 0,01-1,0 М иона натрия (или других солей) при pH от 7,0 до 8,3, а температура составляет по меньшей мере приблизительно 30°C для коротких зондов (например, приблизительно 10-50 нуклеотидов) и по меньшей мере приблизительно 60°С для длинных зондов (например, приблизительно более, чем 50 нуклеотидов). Жесткие условия также могут быть достигнуты путем добавления дестабилизирующих агентов, таких как формамид. Для селективной или специфической гибридизации, позитивный сигнал может по меньшей мере в 2-10 раз превышать сигнал фоновой гибридизации. Примеры жестких условий гибридизации включают следующие условия: 50% формамида, 5 × SSC и 1% ДСН, инкубирование при 42°С, или 5 × SSC, 1% ДСН, инкубирование при 65°С, с промывкой в 0,2 × SSC и 0,1% ДСН при 65°С.
[00121] Используемый здесь термин «по существу комплементарный» означает, что первая последовательность по меньшей мере на 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98% или 99% идентична комплементу второй последовательности в области из 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или более нуклеотидов, или что две последовательности гибридизуются в жестких условиях гибридизации.
[00122] Используемый здесь термин «по существу идентичный» означает, что первая и вторая последовательности по меньшей мере на 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98% или 99% идентичны в области из 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 или более нуклеотидов или аминокислот, или, если это касается нуклеиновых кислот, то это означает, что первая последовательность, по существу, комплементарна комплементу второй последовательности.
[00123] Используемый здесь термин «диагностика» относится к классификации патологии или симптомов, определению тяжести патологии (например, степени или стадии), мониторингу прогрессирования патологии, прогнозированию исхода патологии и/или к перспективам на выздоровление.
[00124] Выражение «состоящий, в основном, из» означает, что композиция или способ могут включать дополнительные ингредиенты и/или стадии, но только в том случае, если эти дополнительные ингредиенты и/или стадии существенно не изменяют основные и новые свойства заявленной композиции или заявленного способа.
1. Последовательности ДНК, содержащие гиперметилированные сайты CpG в промоторной области генов BMP3 и NDRG4 у населения Китая с РПОК и ПА.
[00125] Настоящее изобретение относится к последовательностям ДНК, содержащим подробно описанные гиперметилированные сайты CpG в промоторной области генов BMP3 и NDRG4 у населения Азии (например, у населения Китая), которые могут быть использованы в качестве маркеров для диагностики РПОК и ПА.
[00126] В некоторых своих вариантах, настоящее изобретение относится к природной последовательности гена BMP3, представленной ниже (от 5' до 3'), где потенциально метилированные сайты обозначены надстрочным индексом «m»:
GCCAGTTTGGCmCGGGTGTTCCCAAAAATAAAGmCGAGGAGGGAAGGTACAGACAGATCTTGAAAACACCmCGGGCCACACAmCGCmCGmCGACCTACAGCTCTTTCTCAGmCGTTGGAGTGGAGAmCGGmCGCCCGCAGmCGCCCTGmCGmCGGGTGAGGTCmCGmCGCAGCTGCTGGGGAAGAGCCCACCTGTCAGGCTGmCGCTGGGTCAGmCGCAGCAAGTGGGGCTGGCmCGCTATCTmCGCTGCACCCGGCmCGmCGTCCmCGGGCTCmCGTGmCGCCCTmCGCCCCAG(SEQ ID NO: 65).
[00127] В некоторых своих вариантах, настоящее изобретение относится к природной последовательности гена NDRG4, представленной ниже (от 5' до 3'), где потенциально метилированные сайты обозначены надстрочным индексом «m»::
tgagaagtmcggmcgggggmcgmcggatmcgacmcggggtgtcccccaggctcmcgmcgtmcgmcggtcccmcgctmcgccctccmcgccmcgcccacmcgggcaccccagcmcgmcgcagaaggmcggaagccamcgmcgmcgagggacmcgmcggtcmcgtcmcgggactagccccaggccmcggcacmcgcccmcgmcgggcmcgagmcgcccacaccmcgccaaacccamcgmcgggcamcgccccmcgmcggmcgcacmcgcccccagcc(SEQ ID NO.: 66).
{00128] После обработки природной геномной ДНК или ее фрагмента одним или несколькими реагентами для превращения цитозиновых оснований, которые не являются метилированными, в урацил (например, бисульфитом) или в другое основание, которое заметно отличается от цитозина с точки зрения свойств гибридизации, была получена преобразованная последовательность гена BMP3 (от 5' до 3'), представленная ниже, где потенциально метилированные сайты отмечены надстрочным индексом «m»:
GTTAGTTTGGTmCGGGTGTTTTTAAAAATAAAGmCGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTmCGGGTTATATAmCGTmCGmCGATTTATAGTTTTTTTTTAGmCGTTGGAGTGGAGAmCGGmCGTTmCGTAGmCGTTTTGmCGmCGGGTGAGGTTmCGmCGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGmCGTTGGGTTAGmCGTAGTAAGTGGGGTTGGTmCGTTATTTmCGTTGTATTmCGGTmCGmCGTTTmCGGGTTTmCGTGmCGTTTTmCGTTTTAG (SEQ ID NO:1).
[00129] После обработки природной геномной ДНК или ее фрагмента одним или несколькими реагентами для превращения цитозиновых оснований, которые не являются метилированными, в урацил (например, бисульфитом) или в другое основание, которое заметно отличается от цитозина с точки зрения свойств гибридизации, была получена преобразованная последовательность гена NDRG4 (от 5' до 3'), представленная ниже, где потенциально метилированные сайты отмечены надстрочным индексом «m»:
tgagaagtmcggmcgggggmcgmcggatmcgaTmcggggtgtTTTTTaggTtTmcgmcgtmcgmcggtTTTmcgTtmcgTTTtTTmcgTTmcgTTTaTmcgggTaTTTTagTmcgmcgTagaaggmcggaagTTamcgmcgmcgagggaTmcgmcggtTmcgtTmcgggaTtagTTTTaggTTmcggTaTmcgTTTmcgmcgggTmcgagmcgTTTaTaTTmcgTTaaaTTTamcgmcgggTamcgTTTTmcgmcggmcgTaTmcgTTTTTagTT(SEQ ID NO:2).
[00130] Последовательности ДНК, содержащие конкретно отмеченные гиперметилированные сайты CpG в промоторной области генов BMP3 и NDRG4 у населения Азии согласно изобретению, являются особенно подходящими для диагностики РПОК и/или ПА у населения Азии. Так, например, праймеры и зонды могут быть сконструированы для нацеливания на один или более конкретных сайтов метилирования в генах BMP3 и/или NDRG4 в качестве средств для определения состояния и уровня метилирования BMP3 и/или NDRG4, и следовательно, для определения состояния опухоли у пациента, нуждающегося в этом.
2. Три пары предпочтительных праймеров и зондов для детектирования метилирования гена BMP3 и NDRG4, соответственно, и соответствующие реагенты.
[00131] Настоящее изобретение относится к трем парам предпочтительных праймеров и зондов для определения уровней метилирования генов BMP3 и NDRG4, соответственно. Эти праймеры и зонды были сконструированы для нацеливания на метилированные сайты CpG, часто встречающиеся у населения Азии (например, у населения Китая).
[00132] Эти специфические пары предпочтительных праймеров и зондов обладают удивительно более высокой чувствительностью и специфичностью при диагностике РПОК и ПА, особенно при диагностике ПA у населения Азии, по сравнению с праймерами и зондами, присутствующими в коммерчески доступных продуктах, таких как Cologuard®.
Ниже представлены последовательности праймеров и зондов.
[00133] Олигонуклеотиды согласно изобретению преимущественно позволяют осуществлять чрезвычайно специфическую амплификацию гиперметилированных сайтов CpG в промоторной области BMP3 или NDRG4 в биологическом образце, взятом у пациента из Азии.
[00134] В некоторых вариантах осуществления изобретения представлены олигонуклеотиды, которые частично или полностью комплементарны последовательности SEQ ID NO: 3-20.
[00135] В некоторых вариантах осуществления изобретения представлены олигонуклеотиды, имеющие одну или более модификаций по сравнению с последовательностью зонда, такие как SEQ ID NO: 5, 11, 17, 8, 14 и 20. В некоторых вариантах осуществления изобретения, модификация может происходить у 5'-конца и/или 3'-конца одной из нуклеотидных последовательностей, представленных в SEQ ID NO: 5, 11, 17, 8, 14 и 20.
[00136] Примерами модифицированных фрагментов оснований, которые могут быть использованы для модификации нуклеотидов в любом положении в его структуре, являются, но не ограничиваются ими: 5-фторурацил, 5-бромурацил, 5-хлороурацил, 5-йодурацил, гипоксантин, ксантин, ацетилцитозин, 5-(карбоксигидроксилметил) урацил, 5-карбоксиметиламинометил-2-тиоуридин, 5-карбоксиметиламинометилурацил, дигидроурацил, бета-D-галактозилквеозин, инозин, N-6-изопентениладенин, 1-метилгуанин, 1-метилинозин, 2,2-диметилгуанин, 2-метиладенин, 2-метилгуанин, 3-метилцитозин, 5-метилцитозин, N6-аденин, 7-метилгуанин, 5-метиламинометилурацил, метоксиаминометил-2-тиоурацил, бета-D-маннозилквеозин, 5'-метоксикарбоксиметилурацил, 5-метоксиурацил, 2-метилтио-N6-изопентениладенин, урацил-5-оксиуксусная кислота, псевдурацил, квеозин, 2-тиоцитозин, 5-метил-2-тиоурацил, 2-тиоурацил, 4-тиоурацил, 5-метилурацил, метиловый эфир урацил-5-оксиуксусной кислоты, урацил-5-оксиуксусная кислота, 5-метил-2-тиоурацил, 3-(3-амино-3-N-2-карбоксипропил)урацил и 2,6-диаминопурин и т.п.
[00137] Примерами модифицированных сахарных фрагментов, которые могут быть использованы для модификации нуклеотидов в любом положении в его структуре, являются, но не ограничиваются ими: арабиноза, 2-фторарабиноза, ксилоза и гексоза или модифицированный компонент фосфатного остова, такой как фосфортиоат, фосфордитиоат, фосфорамидотиоат, фосфорамидат, фосфордиамидат, метилфосфонат, алкилфосфотриэфир или формацеталь или их аналоги.
[00138] В некоторых вариантах осуществления изобретения, олигонуклеотид в последовательностях SEQ ID NO: 5, 11, 17, 8, 14 и 20 заменен не-природным нуклеотидом, таким как искусственная нуклеиновая кислота. Искусственными нуклеиновыми кислотами являются, но не ограничиваются ими, пептид-нуклеиновая кислота (PNA), морфолино-нуклеиновая кислота, блокированная нуклеиновая кислота (LNA), гликоль-нуклеиновая кислота (GNA) и треозо-нуклеиновая кислота (TNA). Каждый из них отличается от природной ДНК или РНК изменениями в остове молекулы.
[00139] В некоторых вариантах осуществления изобретения, зонд согласно изобретению содержит метку у своего 5'-конца.
[00140] В некоторых вариантах осуществления изобретения, метка у 5'-конца зонда содержит флуоресцентный краситель, такой как флуорофор. Используемый здесь флуорофор представляет собой флуоресцентное химическое соединение, которое может повторно излучать свет после воздействия на него световым излучением. Флуорофоры обычно содержат несколько комбинированных ароматических групп или плоские или циклические молекулы с несколькими π-связями. Небелковыми органическими флуорофорами являются, но не ограничиваются ими, производное ксантина (например, флуоресцеин, родамин, Орегон зеленый, эозин и техасский красный); производные цианина (например, цианин, индокарбоцианин, оксакарбоцианин, тиакарбоцианин и мероцианин), производные сквараина и сквараины с замещениями на кольце (например, красители Seta, SeTau и Square), производные нафталина (например, производные дансила и продана), производные кумарина, производные оксадиазола (например, пиридилоксазол, нитробензоксадиазол и бензоксадиазол); производные антрацена (например, антрахиноны, включая DRAQ5, DRAQ7 и оранжевый CyTRAK); производные пирена (каскадный синий и т.п.), производные оксазина (например, нильский красный, нильский синий, крезиловый фиолетовый, оксазин 170 и т.п.); производные акридина (например, профлавин, акридиновый оранжевый, акридиновый желтый и т.п.); производные арилметина (например, аурамин, кристаллический фиолетовый, малахитовый зеленый); производные тетрапиррола (например, порфин, фталоцианин, билирубин). Конкретными примерами являются, но не ограничиваются ими, VIC, PET, техасский красный, Cy3, Cy5, FAM (6-карбоксифлуоресцеин), HEX (6-карбокси-2',4,4',5',7,7'-гексахлорфлуоресцеин), ROX (5(6)-карбокси-X-родамин), JOE (6-карбокси-4',5'-дихлор-21,71-диметоксифлуоресцеин), TET(5'-тетрахлорфлуоресцеин-фосфорамидит), NED (флуоресцеин-бензоксантин), TAMRA (6-карбокси-N, N,N, N-тетраметилродамин), ФИТЦ (флуоресцеин-изотиоцианат). Примеры конкретных флуорофоров, которые могут быть использованы в описанных здесь зондах, известны специалистам в данной области и включают флуорофоры, описанные в патенте США № 5866366, Nazarenko и др., такие как 4-ацетамидо-4'-изотиоцианатостильбен-2,2'-дисульфоновая кислота; акридин и производные, такие как акридин и изотиоцианат акридина, 5-(2'-аминоэтил)аминонафталин-1-сульфоновая кислота (EDANS), 4-амино-N-[3-винилсульфонил)фенил]нафталимид-3,5- дисульфонат (желтый Люцифер VS), N-(4-анилино-1-нафтил)малеимид, антраниламид; бриллиантовый желтый; кумарин и производные, такие как кумарин, 7-амино-4-метилкумарин (AMC, кумарин 120), 7-амино-4-трифторметилкулуарин (кумаран 151); цианозин; 4',6-диаминидино-2-фенилиндол (DAPI); 5',5'-дибромпирогаллол-сульфонфталеин (бромпирогаллоловый красный); 7-диэтиламино-3- (4'-изотиоцианатофенил)-4-метилкумарин; пентаацетат диэтилентриамина; 4,4'-диизотиоцианатодигидро-стильбен-2,2'-дисульфоновая кислота; 4,4'-диизотиоцианатостильбен-2,2'-дисульфоновая кислота; 5-[диметиламино]нафталин-1-сульфонилхлорид (DNS, данзилхлорид); 4-диметиламинофенилазофенил-4'-изотиоцианат (DABITC); эозин и его производные, такие как эозин и изотиоцианат эозина; эритрозин и производные, такие как эритрозин B и изотиоцианат эритрозина; этидий; флуоресцеин и производные, такие как 5-карбоксифлуоресцеин (FAM), 5-(4,6-дихлортриазин-2-ил) аминофлуоресцеин (DTAF), 2'7'-диметокси-4'5'-дихлор-6-карбоксифлуоресцеин (JOE), флуоресцеин, изотиоцианат флуоресцеина (FITC), QFITC (XRITC), 6-карбоксифлуоресцеин (HEX) и TET (тетраметилфлуоресцеин); флуорескамин; IR144; IR1446; изотиоцианат малахитового зеленого; 4-метилумбеллиферон; орто-крезольфталеин; нитротирозин; парарозанилин; феноловый красный; B-фикоэритрин; о-фталдиальдегид; пирен и производные, такие как пирен, пиренбутират и сукцинимидил-1-пиренбутират; реактивный красный 4 (CIBACRON™, бриллиантовый красный 3B-A); родамин и производные, такие как 6-карбокси-X-родамин (ROX), 6-карбоксирадамин (R6G), сульфонилхлорид лиссамина-родамина B, родамин (Rhod), родамин B, родамин 123, изотиоцианат родамина X, N, N,N',N'-тетраметил-6-карбоксиродамин (TAMRA), тетраметилродамин и изотиоцианат тетраметилродамина (TRITC); сульфородамин B; сульфородамин 101 и сульфонилхлоридное производное сульфородамина 101 (техасский красный); рибофлавин; розолиевая кислота и производные хелата тербия; LightCycler красный 640; Cy5.5; и Cy56-карбоксифлуоресцеин; дипиррометендифторид бора (BODIPY); акридин; стильбен; 6-карбокси-X-родамин (ROX); Cy3; Cy3.5, Cy5, Cy5.5, VIC® (Applied Biosystems); LC красный 640; LC красный 705; Орегон зеленый™; CALRedTM; красный 640; и Якима желтый; LighterCycler®Cyan500; LighterCycler®; красный 610; Alexa 647; Alexa 555; 5-(2-аминоэтил)амино-1-нафталинсульфоновая кислота (EDANS); тетраметилродамин (TMR); изоцианат тетраметилродамина (TMRITC), флуоресцеинизоцианат (FITC), γ-родамин, их производные или любые их комбинации и т.п. Другие флуоресцентные красители описаны в патентах США №№: 5866366, 6818431, 6056859, 9140688, 9581587, 6165765, 6485909, 8158358, 7625723, 7560236, 7867701, 9150912, 7960543, 65551383, 6881570, 8198026, 5625081, 8445291, 9194801, 8835110, 7893227, 9243289, 7427674, 9512493, в публикациях заявок на патенты США: 20170152552, 20030170672, 20160281151, 20130084558, 20060281100, 20140234833, 20150072340, 20050089910, 20090081677, 20140024022201801711393, 200601418886, 20010018185, 20110151446 и WO/2000/017330A1, WO/2008/030071A1, WO/2013/049631A1, WO/2016/179090A1, WO/2016/123895A1, WO/2003/079022A1, каждая из которых включена в настоящее описание в полном объеме посредством ссылки.
[00141] В некоторых вариантах осуществления изобретения, зонд согласно изобретению содержит флуоресцентный донор и акцепторный флуорофор. Используемый здесь акцепторный флуорофор (например, «гаситель флуоресценции») представляет собой флуорофор, который поглощает энергию от донорного флуорофора, например, в диапазоне приблизительно от 400 до 900 нм. Акцепторные флуорофоры обычно поглощают свет на длине волны, которая обычно по меньшей мере на 10 нм выше (например, по меньшей мере на 20 нм выше), чем максимальная длина волны поглощения донорного флуорофора. Акцепторные флуорофоры имеют спектр возбуждения, который перекрывается с излучением донорного флуорофора, так что энергия, излучаемая донором, может возбуждать гаситель. Могут быть использованы любые акцепторные флуорофоры, известные специалистам в данной области. В конкретном примере, акцепторный флуорофор представляет собой гаситель темнового излучения, такой как Dabcyl, QSY7 (Molecular Probes), QSY9 (Molecular Probes), QSY21 (Molecular Probes), QSY33 (Molecular Probes), BLACK HOLE QUENCHERS™ (Glen Research, e.g., BHQ-1, BHQ-2, BHQ-3), гаситель темнового излучения ECLIPSE™ (Epoch Biosciences), DDQ-I, DDQ-II, Dabcyl, Eclipse, или IOWA BLACK™ (Integrated DNA Technologies, например, Iowa Black FQ, Iowa Black RQ). Другие гасители флуоресценции описаны в патентах США NO: 9957546, US9274008, в публикациях патентов США NO: 20140295422, 20090042205, 20160281182, 20180142284, 20140147929, и WO/2009/009615A1, WO/2016/160572A1, WO/2016/178953A1, WO/2018/229663A1, WO/2010/051544A2, WO/2013/152220A2, которые включены в настоящее описание в полном объеме посредством ссылки. Гаситель может уменьшать или подавлять излучение донорного флуорофора. В таком примере, вместо детектирования увеличения сигнала излучения от акцепторного флуорофора, когда он находится в достаточной близости от донорного флуорофора (или детектирования уменьшения сигнала излучения от акцепторного флуорофора, когда он находится на значительном расстоянии от донорного флуорофора), может быть детектировано усиление сигнала излучения от донорного флуорофора, когда гаситель находится на значительном расстоянии от флуорофора-донора (или уменьшение сигнала излучения от флуорофора-донора, когда он находится в достаточной близости от акцепторного флуорофора-гасителя).
[00142] В некоторых вариантах осуществления изобретения, праймеры и зонды согласно изобретению основаны на переносе резонансной энергии флуоресценции (FRET). Примерами олигонуклеотидов, участвующих во FRET, которые могут быть использованы для детектирования ампликонов, являются линейные олигозонды, такие как HybProbes, 5'-нуклеазные олигозонды, такие как зонды TAQMAN®, шпилечные олигозонды, такие как молекулярные маяки, праймеры Scorpion и UniPrimers, зонды, связывающиеся с малыми бороздками и самофлуоресцирующие ампликоны, такие как праймеры Sunrise.
[00143] В некоторых вариантах осуществления изобретения, праймеры и/или зонды согласно изобретению помечены другими функциональными молекулами, такими как биотин, гаптены, антигены, химические группы, радиоактивные вещества, ферментные маркеры и т.п. Детектирование маркированного продукта амплификации может быть осуществлено, например, с применением методов флуоресценции, методов хемолюминесценции, методов денситометрии, методов фотометрии, реакций осаждения, ферментативных реакций, включая реакции ферментативной активации, методов ППР («поверхностного плазмонного резонанса»), методов эллипсометрии, измерений показателя преломления, измерений отражательной способности и аналогичных методов.
[00144] В некоторых вариантах осуществления изобретения, описанные здесь праймеры и зонды могут быть использованы в количественной ПЦР для определения состояния и уровня метилирования в гене BMP3 и/или NDRG4 у пациента. В некоторых вариантах осуществления изобретения может быть включена дополнительная реакция для амплификации одного или более контрольных генов. В некоторых вариантах осуществления изобретения, контрольный ген представляет собой ген пациента, на активность которого не влияет наличие или отсутствие РПОК и ПА, а также не влияют состояние и уровень метилирования BMP3 и NDRG4. В некоторых вариантах осуществления изобретения, контрольные гены включают, но не ограничиваются ими, β-глобин (HBB), теломеразу (TERT), глицеральдегид-3-фосфатдегидрогеназу (GAPDH), альбумин (ALB), β-актин (ACTB), микроглобулин бета 2 (B2M) и Т-клеточный рецептор γ (TRG).
[00145] В некоторых вариантах осуществления изобретения, ген B2M используется в качестве контрольного гена в количественной ПЦР для детектирования состояния и уровня метилирования BMP3/NDRG4.
[00146] В некоторых вариантах осуществления изобретения, могут быть введены один или несколько других контролей, включая, но не ограничиваясь этим, контроль без матрицы (для обнаружения загрязнения реагента или оборудования и подтверждения позитивных результатов); контроль без амплификации (для обнаружения фоновой флуоресценции, генерируемой деградируемыми мечеными зондами) и позитивный контроль (для обнаружения ингибиторов или нарушения функции, и для подтверждения того, что реагенты и оборудование находятся в рабочем состоянии).
[00147] В некоторых вариантах осуществления изобретения, кол.ПЦР используется для определения наличия амплификации метилированного гена BMP3 или метилированного гена NDRG4 в образце. Детектированный сигнал от зонда BMP3 или NDRG4 количественно оценивают либо по стандартной кривой, либо путем сравнения значений Ct со значением контрольного гена. Для нормализации результатов часто проводят анализ с использованием генов «домашнего хозяйства». Порог цикла (Ct) определяют как количество циклов, необходимых для того, чтобы флуоресцентный сигнал превышал заданный порог (например, превышал фоновый уровень, например, уровень амплификации в образце негативного контроля). В некоторых вариантах осуществления изобретения, порог автоматически определяют с помощью программы в устройстве для кол.ПЦР или другими подходящими методами. В некоторых вариантах осуществления изобретения, порог устанавливают чуть выше (например, приблизительно на 0,01%, 0,1%, 1%, 5% или 10% выше) конечного значения флуоресценции в образце негативного контроля.
[00148] В некоторых вариантах осуществления изобретения, если значение Ct, связанное с амплификацией BMP3 или NDRG4 в тестируемом образце, составляет не более, чем (≤) приблизительно 35, 34, 33, 32, 31, 30 или менее, то образец определяется как содержащий метилированный BMP3 или NDRG4, и у пациента диагностируется РПОК и/или ПА (положительный результат), а в противном случае, образец определяется как не содержащий метилированного BMP3 или NDRG4, и считается, что у пациента отсутствуют РПОК или ПA (отрицательный результат). Для амплификации контрольного гена, если значение Ct, связанное с амплификацией контрольного гена в образце, не превышает (≤) приблизительно 34, 33, 32, 31, 30, 29 или менее, то амплификация контрольного гена определяется как позитивная, а в противном случае, амплификация контрольного гена будет рассматриваться как негативная. Если амплификация контрольного гена определена как негативная, то результат теста недействителен.
[00149] В некоторых вариантах осуществления изобретения, разница между значением Ct, связанным с BMP3, и значением Ct, связанным с амплификацией контрольного гена (ΔCt=Ctпредставляющего интерес гена - Ctконтрольного гена), обозначается как ΔCt1. В некоторых вариантах осуществления изобретения, если ΔCt1 не превышает заранее определенного критического значения (≤ критического значения), то образец определяется как имеющий метилирование BMP3 (положительный результат), то есть, это означает, что у пациента имеется РПОК или ПA. В некоторых вариантах осуществления изобретения, если ΔCt1 больше заранее определенного критического значения (> критического значения), то это означает, что образец не имеет метилирования BMP3 (отрицательный результат), и пациент считается здоровым. В некоторых вариантах осуществления изобретения, критическим значением является соответствующее значение ΔCt для образца, содержащего 5 нг/мкл нуклеотидной последовательности, имеющей степень метилирования 1%, например, приблизительно 8, 9 или 10.
[00150] В некоторых вариантах осуществления изобретения, разница между значением Ct, связанным с NDRG4, и значением Ct, связанным с амплификацией контрольного гена (ΔCt=Ctпредставляющего интерес гена - Ctконтрольного гена), обозначается как ΔCt2. В некоторых вариантах осуществления изобретения, если ΔCt2 не превышает заранее определенного критического значения (≤ критического значения), то образец определяется как имеющий метилирование NDRG4 (положительный результат), то есть, это означает, что пациент имеет РПОК или ПA. В некоторых вариантах осуществления изобретения, если ΔCt2 больше заранее определенного критического значения (> критического значения), то это означает, что образец не имеет метилирования NDRG4 (отрицательный результат), и пациент считается здоровым. В некоторых вариантах осуществления изобретения, критическое значение представляет собой соответствующее значение ΔCt для образца, содержащего 5 нг/мкл нуклеотидной последовательности, имеющей степень метилирования 1%, например, приблизительно 8, 9 или 10.
[00151] Предпочтительные праймеры и зонды согласно изобретению обладают удивительно высокой чувствительностью и специфичностью при обнаружении РПОК и ПА у населения Азии, а особенно при обнаружении ПA, по сравнению с такими же параметрами для коммерчески доступных продуктов, таких как Cologuard®.
[00152] Используемый здесь термин «чувствительность» определяется как уровень чувствительности, при котором пациенты, действительно имеющие РПОК и/или ПА в данной группе, выявляются правильно. В некоторых вариантах осуществления изобретения, чувствительность составляет по меньшей мере приблизительно 65%, по меньшей мере приблизительно 70%, по меньшей мере приблизительно 75%, по меньшей мере приблизительно 80%, по меньшей мере приблизительно 85%, по меньшей мере приблизительно 86%, по меньшей мере приблизительно 87%, по меньшей мере приблизительно 88%, по меньшей мере приблизительно 89%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 91%, по меньшей мере приблизительно 92%, по меньшей мере приблизительно 93%, по меньшей мере приблизительно 94%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или более, или 100%. В некоторых вариантах осуществления изобретения, число индивидуумов в группе составляет по меньшей мере приблизительно 50, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 2000, 3000, 4000, 5000, 6000, 7000, 8000, 9000, 10000 или более.
[00153] Используемый здесь термин «специфичность» определяется как степень специфичности, при которой пациенты, фактически не имеющие РПОК или ПA в данной группе, правильно диагностируются как не страдающие этим заболеванием. В некоторых вариантах осуществления изобретения, специфичность составляет по меньшей мере приблизительно 85%, по меньшей мере приблизительно 86%, по меньшей мере приблизительно 87%, по меньшей мере приблизительно 88%, по меньшей мере приблизительно 89%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 91%, при по меньшей мере приблизительно 92%, по меньшей мере приблизительно 93%, по меньшей мере приблизительно 94%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 99% или более или 100%. В некоторых вариантах осуществления изобретения, число индивидуумов в группе составляет по меньшей мере приблизительно 50, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 2000, 3000, 4000, 5000, 6000, 7000, 8000, 9000, 10000 или более.
[00154] Как показано в примерах, предпочтительные праймеры и зонды обеспечивают удивительно высокую чувствительность и специфичность при детектировании метилирования BMP3 и NDRG4, что обеспечивает удивительно высокую чувствительность и специфичность при диагностике РПОК и/или ПА. Так, например, чувствительность диагностики РПОК с использованием трех пар предпочтительных праймеров и зондов гена BMP3 составляет по меньшей мере 85%; чувствительность диагностики РПОК с использованием трех пар предпочтительных праймеров и зондов гена NDRG4 составляет не менее 90%; чувствительность диагностики ПА с использованием трех пар предпочтительных праймеров и зондов гена BMP3 составляет по меньшей мере 66%; а чувствительность диагностики ПА с использованием трех пар предпочтительных праймеров и зондов гена NDRG4 составляет по меньшей мере 73%. Кроме того, специфичность диагностики РПОК и ПА с использованием трех пар предпочтительных праймеров и зондов гена BMP3 составляет приблизительно 97% - 100% (например, по меньшей мере приблизительно 97,8%); а специфичность диагностики РПОК и ПА с использованием трех пар предпочтительных праймеров и зондов гена NDRG4 составляет приблизительно 97% - 100% (например, по меньшей мере приблизительно 97,8%).
3. Три набора предпочтительных комбинаций праймеров и зондов для диагностики РПОК и/или ПА у пациентов.
[00155] Настоящее изобретение также относится к трем наборам предпочтительных комбинаций праймеров и зондов для детектирования уровней метилирования генов BMP3 и NDRG4 в целях определения наличия или отсутствия РПОК или ПA у пациента. Эти специфические комбинации обладают удивительно высокой чувствительностью и специфичностью при обнаружении РПОК и ПА у населения Азии, особенно при диагностике ПA, по сравнению с этими параметрами для существующих коммерческих продуктов, таких как Cologuard®.
Последовательности трех наборов предпочтительных праймеров и зондов представлены ниже:
(5' - 3')
[00156] Как показано в примерах, предпочтительные комбинации наборов праймеров-зондов BMP3 и NDRG4 обеспечивают удивительно высокую чувствительность и специфичность при детектировании метилирования BMP3 и NDRG4, и тем самым обеспечивают удивительно высокую чувствительность и специфичность при диагностике РПОК и/или ПА. В некоторых вариантах осуществления изобретения, эта чувствительность и специфичность достигаются в том случае, когда один и тот же анализ также включает анализ на ген KRAS и анализ на гемоглобин, как это объясняется в Примере 5. Так, например, общая чувствительность диагностики РПОК с использованием трех предпочтительных комбинаций праймеров и зондов генов BMP3 и NDRG4 при проведении комбинированного анализа на ген KRAS и гемоглобин составляет по меньшей мере 95%; чувствительность диагностики ПА с использованием трех предпочтительных комбинаций праймеров и зондов генов BMP3 и NDRG4 при проведении комбинированного анализа на ген KRAS и гемоглобин составляет по меньшей мере 93%; чувствительность диагностики РПОК+ПА с использованием трех предпочтительных комбинаций праймеров и зондов генов BMP3 и NDRG4 при проведении комбинированного анализа на ген KRAS и гемоглобин составляет по меньшей мере 97%; а специфичность диагностики РПОК+ПА с использованием трех предпочтительных комбинаций праймеров и зондов генов BMP3 и NDRG4 при проведении комбинированного анализа на ген KRAS и гемоглобин составляет по меньшей мере 97%.
4. Набор для диагностики РПОК и ПА
[00157] Настоящее изобретение относится к наборам для детектирования метилирования BMP3/NDRG4 и/или для диагностики РПОК/ПA у пациента, нуждающегося в этом. В некоторых вариантах осуществления изобретения, эти наборы особенно подходят для пациентов из Азии, например пациентов из Китая.
[00158] В некоторых вариантах осуществления изобретения, этот набор включает: (1) по меньшей мере один из трех наборов предпочтительных комбинаций праймеров и зондов для диагностики РПОК и ПА (комбинации № 4, 5 и 7 в Таблице 20) и соответствующие реагенты для кол.ПЦР; (2) средства для детектирования семи мутаций в кодирующей области гена KRAS (то есть, G12D, G13D, G12V, G12C, G12S, G12A и G13R), такие как подходящие праймеры и зонды и соответствующие реагенты для кол.ПЦР; (3) средства для детектирования гемоглобина в пробе кала, такие как реагенты, полученные на основе технологии FIT (например, антитело против гемоглобина и реагенты для обнаружения комплекса, образованного антителом и гемоглобином в пробе кала).
[00159] В некоторых вариантах осуществления изобретения, набор включает по меньшей мере один набор из предпочтительной комбинации праймеров-зондов, указанной ниже:
(1) Три набора предпочтительных комбинаций праймера и зонда представлены ниже:
(2) Реагенты для триплексной количественной ПЦР, проводимой для определения уровня метилирования генов BMP3 и NDRG4.
[00160] В некоторых вариантах осуществления изобретения, наборы содержат реагенты для осуществления мультиплексной ПЦР в целях одновременного детектирования метилирования BMP3 и NDRG4. В некоторых вариантах осуществления изобретения, мультиплексная ПЦР представляет собой количественную ПЦР.
[00161] В некоторых вариантах осуществления изобретения, реагенты включают ДНК-полимеразу Taq. В некоторых вариантах осуществления изобретения, конечная концентрация ДНК-полимеразы Taq составляет приблизительно 2 ед./реакцию. В некоторых вариантах осуществления изобретения, реагенты включают MgCl2. В некоторых вариантах осуществления изобретения, конечная концентрация MgCl2 в реакции составляет 2 мМ. В некоторых вариантах осуществления изобретения, реагенты включают dNTP. В некоторых вариантах осуществления изобретения, dNTP имеет конечную концентрацию 0,2 мМ. В некоторых вариантах осуществления изобретения, реагенты включают от приблизительно от 0,5 мМ до 0,75 мМ праймеров для амплификации BMP3, NDRG4 и контрольных генов. В некоторых вариантах осуществления изобретения, реагенты включают приблизительно от 0,1 мМ до 0,25 мМ зондов, гибридизованных с последовательностями ДНК BMP3, NDRG4 и контрольных генов. В некоторых вариантах осуществления изобретения, реагенты дополнительно включают буфер для ПЦР, такой как концентрированный буфер для ПЦР (например, 5× или 10×), который может быть разведен до конечной концентрации 1×. В некоторых вариантах осуществления изобретения, B2M представляет собой контрольный ген, который был амплифицирован для контроля качества в количественной ПЦР.
(3) Праймеры и зонды для детектирования семи мутаций в кодирующей области гена KRAS.
[00162] В некоторых вариантах осуществления изобретения, наборы содержат средства для детектирования мутаций в гене KRAS. В некоторых вариантах осуществления изобретения, наборы содержат праймеры и зонды, которые были сконструированы для амплификации и детектирования семи мутантных горячих точек в экзоне 12 и в экзоне 13 в открытой рамке считывания гена KRAS, где указанными мутациями являются G12D, G13D, G12V, G12C, G12S, G12A и G13R. В некоторых вариантах осуществления изобретения, последовательности праймеров и зондов представлены ниже:
(4) Реагенты для мультиплексной количественной ПЦР, проводимой для определения мутаций кодонов гена KRAS
[00163] Настоящее изобретение также относится к системе мультиплексной количественной ПЦР для детектирования всех семи мутаций гена KRAS. В некоторых вариантах осуществления изобретения, мультиплексная количественная ПЦР включает ДНК-полимеразу Taq в конечной концентрации 2,5 ед./реакцию, MgCl2 в конечной концентрации 1 мМ, dNTP в конечной концентрации 0,1 мМ, 0,3-0,9 мкМ праймеров для амплификации генов KRAS и ACTB, 0,05-0,1 мкМ зондов, гибридизованных с последовательностями ДНК генов KRAS и ACTB, и 1 × буфер для ПЦР. ACTB является контрольным геном и амплифицирован для контроля качества количественной ПЦР.
(5) Набор для определения гемоглобина в кале
[00164] В некоторых вариантах осуществления изобретения, наборы содержат реагенты для определения гемоглобина. В некоторых вариантах осуществления изобретения, гемоглобин был качественно оценен с помощью твердофазного иммуноферментного анализа (ELISA).
5. Модель логистической регрессии
[00165] В некоторых вариантах осуществления изобретения, после получения результатов анализа на метилирование BMP3/NDRG4, анализа на мутацию KRAS и анализа на гемоглобин, все результаты были компилированы и подвергнуты логистической регрессии, в целях определения наличия или отсутствия РПОК и/или ПА у пациентов.
[00166] В некоторых вариантах осуществления изобретения, способ включает вычисление значения P общего индекса рака, где P=eK/(1+eK), где e означает натуральную константу.
[00167] В некоторых вариантах осуществления изобретения, K определяется как K=a*ΔCt1+b*ΔCt2+c*ΔCt3+d*FIT+X, где a, b, c, d, X являются клиническими константами. ΔCt1, ΔCt2 и ΔCt3 представляют собой величину Ct BMP3, NDRG4 и KRAS, вычитаемую из значений контрольных генов.
[00168] В некоторых вариантах осуществления, если значение P равно или превышает заданный порог, то результат теста будет положительным, а в противном случае - отрицательным. Положительный результат указывает на то, что человек может иметь РПОК или ПA, а отрицательный результат указывает на то, что он является здоровым.
6. Способы лечения
[00169] В некоторых вариантах осуществления изобретения, способы согласно изобретению включают лечение пациентов, нуждающихся в этом, после того, как пациенты были классифицированы как имеющие рак прямой и ободочной кишки и/или аденому. В некоторых вариантах осуществления изобретения, такое лечение включает, но не ограничивается ими, хирургическое вмешательство, химиотерапию, лучевую терапию, иммунотерапию, паллиативную терапию, физические упражнения.
[00170] Используемый здесь термин «схема лечения» означает протокол лечения, который определяет тип лечения, дозы, график и/или продолжительность лечения индивидуума, нуждающегося в этом (например, индивидуума, у которого была диагностирована патология). Выбранная схема лечения может быть радикальной, которая, как ожидается, приведет к наилучшему клиническому результату (например, к полному излечению патологии), или более умеренной, которая может облегчать симптомы патологии, но при этом, на дает полного излечения пациента с патологией. Следует отметить, что в некоторых случаях, схема лечения может быть связана с некоторым дискомфортом для пациента или с неблагоприятными побочными эффектами (например, повреждением здоровых клеток или тканей). Тип лечения может включать хирургическое вмешательство (например, удаление поражения, пораженных клеток, ткани или органа), заместительную клеточную терапию, введение терапевтического препарата (например, агонистов рецепторов, антагонистов, гормонов, химиотерапевтических агентов) местно или системно, лучевую терапию с использованием внешнего источника (например, внешнего излучения) и/или внутреннего источника (например, брахитерапию) и/или любую их комбинацию. Дозировка, график и продолжительность лечения могут варьироваться в зависимости от тяжести патологии и выбранного типа лечения, и специалисты в данной области могут самостоятельно скорректировать тип лечения в зависимости от дозы, графика и продолжительности лечения.
[00171] В некоторых вариантах осуществления изобретения, способы лечения включают, но не ограничиваются ими, введение фторурацила, капецитабина, оксалиплатина, иринотекана, UFT, FOLFOX, FOLFOXIRI и FOLFIRI, антиангиогенных лекарственных средств, таких как бевацизумаб, и ингибиторов рецепторов эпидермального фактора роста (например, цетуксимаба и панитумумаба).
7. Преимущества настоящего изобретения
Не ограничиваясь какой-либо конкретной теорией, авторы настоящего изобретения отмечают по меньшей мере следующие преимущества:
(1) Подробно описанные метилированные сайты CpG промоторных областей генов BMP3 и NDRG4 у населения Китая представлены и могут использоваться в качестве биомаркера для диагностики РПОК и/или ПА.
(2) Набор больше подходит для диагностики РПОК и ПА у населения Китая, чем другие аналогичные продукты на основе mt-sДНК, такие как Cologuard®, поскольку настоящее изобретение нацелено на сайты метилирования CpG, специфичные для китайцев, в то время как ранее используемые продукты были предназначены для населения белой расы.
(3) Чувствительность и специфичность диагностики РПОК выше по сравнению с этими параметрами для других аналогичных продуктов на основе mt-sДНК.
(4) Чувствительность и специфичность обнаружения ПА значительно выше по сравнению с этими параметрами для других аналогичных продуктов на основе mt-sДНК.
(5) Этот метод является неинвазивным и простым для взятия проб на дому, а поэтому он обеспечивает хорошее соблюдение пациентом режима лечения, и он может быть широко применен в качестве метода скрининга на РПОК и ПА. Этот метод снижает заболеваемость и смертность от РПОК среди населения Азии.
ПРИМЕРЫ
Пример 1
Обнаружение метилированных сайтов CpG в промоторных областях генов BMP3 и NDRG4, соответственно, у населения Китая с РПОК и ПА.
(1) Сбор образцов
[00172] Всего был взят 191 образец ткани FFPE толстой кишки у пациентов с РПОК и ПА, которые были подтверждены с помощью колоноскопии, включая 50 тканей рака прямой и ободочной кишки и 49 пар соседних нормальных тканей, 46 тканей злокачественной аденомы и 46 пар дополнительных нормальных тканей.
(2) Экстракция ДНК
[00173] Геномные ДНК экстрагировали из образцов FFPE с помощью набора для экстракции ДНК TaKaRa MiniBEST FFPE (номер по каталогу: 9782). Стадии этой процедуры подробно описаны ниже:
i. Снятие 30 мг парафинового среза ткани стерильным скальпелем и удаление избытка парафина.
ii. Помещение парафинового среза ткани в центрифужную 1,5 мл-пробирку и добавление 500 мкл буфера DP, перемешивание и инкубирование в воде при 80°C в течение 1 минуты, а затем встряхивание в течение 10 секунд. Добавление 180 мкл буфера GL и встряхивание.
iii. Смесь центрифугировали при 12000 об/мин в течение 1 минуты при комнатной температуре, а затем раствор разделяли на два слоя (на верхнюю масляную фазу и нижнюю водную фазу). К нижней водной фазе добавляли 20 мкл протеиназы K (20 мг/мл) и 10 мкл РНКазы (10 мг/мл) и тщательно перемешивали пипеткой вверх и вниз. При этом, соблюдали осторожность, чтобы не повредить слои. А затем смесь помещали на водяную баню при 56°С на 1 час.
iv. Раствор, полученный в предыдущей стадии, инкубировали при 90°С в течение 30 минут и охлаждали до комнатной температуры. Затем к раствору добавляли 200 мкл буфера GB и 200 мкл 100% этанола, и перемешивали путем встряхивания в течение 10 секунд. Затем центрифугировали при 12000 об/мин в течение 1 минуты при комнатной температуре, и раствор разделяли на два слоя (на верхнюю масляную фазу и нижнюю водную фазу).
v. В пробирку для сбора помещали центрифужную колонку и в эту колонку добавляли нижнюю водную фазу, полученную в предыдущей стадии. При этом, следовало соблюдать осторожность, чтобы не повредить слои. Затем проводили центрифугирование при 12000 об/мин в течение 2 минут при комнатной температуре, и отходы выбрасывали.
vi. В центрифужную колонку добавляли 500 мкл буфера WA и центрифугировали при 12000 об/мин в течение 1 минуты при комнатной температуре, а затем отходы выбрасывали.
vii. В центрифужную колонку добавляли 500 мкл буфера WB и центрифугировали при 12000 об/мин в течение 1 минуты при комнатной температуре, а затем отходы выбрасывали. Эту процедуру повторяли еще один раз.
viii. В пробирку для сбора помещали центрифужную колонку и центрифугировали при 12000 об/мин в течение 2 минут при комнатной температуре.
ix. В новую центрифужную 1,5 мл-пробирку добавляли центрифужную колонку, затем в центр перегородки центрифужной колонки добавляли 50-100 мкл стерилизованной воды или элюирующего буфера, а затем оставляли на 5 минут при комнатной температуре.
x. Центрифугировали при 12000 об/мин в течение 2 минут при комнатной температуре, и элюировали ДНК.
xi. Элюированную ДНК количественно оценивали с помощью флуориметра Nanodrop 2000 и хранили при -20°C для последующего применения.
(3) Предсказание областей CpG в промоторных областях генов BMP3 и NDRG4 и конструирование праймеров для секвенирования ампликонов.
i. Предсказание областей CpG в промоторных областях генов BMP3 и NDRG4.
[00174] Были загружены промоторные последовательности генов BMP3 и NDRG4, включая последовательности ДНК приблизительно на 1000-1500 п.о. выше сайта инициации транскрипции (TSS) и области 5'UTR. Области CpG последовательностей были предсказаны с помощью программы MethPrimer (www.urogene.org/methprimer/). Как показано на фигурах 1A-1D, две более крупных из трех областей CpG гена BMP3 были расположены приблизительно на 400 п.н. выше TSS и всей области 5'UTR (chr4: 81951752-81952760), и только одна область CpG гена NDRG4 была расположена приблизительно на 500 п.о. выше TSS и неполной области 5'UTR (chr16: 58497061-58497938). Конструкция контрольного генома человека представляет собой GRCh37/hg19.
ii. Конструирование праймера для амплификации последовательности областей CpG, предсказанных в генах BMP3 и NDRG4.
[00175] Исходя из длины амплифицируемых последовательностей и длины секвенирующих ридов были сконструированы четыре и пять пар праймеров для генов BMP3 и NDRG4, соответственно. Между соседними ампликонами существует максимально возможное перекрывание, для того, чтобы можно было полностью секвенировать области CpG двух генов. Праймеры двух генов перечислены в Таблице 1, а относительное положение ампликонов двух генов показано на фигурах 1A-1D.
Таблица 1. Праймеры для секвенирования ампликонов генов BMP3 и NDRG4
[00176] Образцы ДНК подвергали обработке бисульфитом, как описано ниже.
(4) Обработка бисульфитом
i. Экстрагированную ДНК оставляли при комнатной температуре для оттаивания и концентрацию ДНК доводили до 20 нг/мкл. Затем в центрифужную 1,5 мл-пробирку добавляли 40 мкл разведенной ДНК, а затем добавляли 4 мкл 3М раствора NaOH и инкубировали при 42°С в течение 20 минут.
ii. Добавляли 400 мкл раствора для превращения, перемешивали и инкубировали при 50°С в течение 16 часов в темноте.
iii. Добавляли 550 мкл связывающего раствора, перемешивали и раствор переносили в колонку для очистки ДНК. Центрифугировали при 13000 об/мин в течение 90 секунд и отходы выбрасывали. Затем снова центрифугировали в течение 3 минут и отходы выбрасывали.
iv. В колонку для очистки ДНК добавляли 600 мкл 90% этанола, центрифугировали при 13000 об/мин в течение 90 секунд и отходы выбрасывали. Затем снова центрифугировали при 13000 об/мин в течение 15 секунд.
v. Добавляли 300 мкл раствора для десульфуризации (0,3 М NaOH в 90% растворе этанола) для очистки ДНК, затем оставляли на 30 минут при комнатной температуре. После чего центрифугировали при 13000 об/мин в течение 90 секунд, и отходы выбрасывали.
vi. Добавляли 600 мкл 90% этанола, центрифугировали при 13000 об/мин в течение 90 секунд и отходы выбрасывали. Эту стадию повторяли еще один раз и снова центрифугировали при 13000 об/мин в течение 3 минут.
vii. В новую центрифужную 1,5 мл-пробирку добавляли колонку для очистки ДНК и добавляли 40 мкл элюата. Пробирку инкубировали при 50°С в течение 30 минут и центрифугировали при 13000 об/мин в течение 90 секунд. Превращенный раствор ДНК хранили при -20°C для дальнейшего применения.
[00177]
(5) Создание библиотеки и секвенирование ампликона
(a) Мультиплексная ПЦР-амплификация
i. ПЦР-смесь Master приготовливали следующим образом:
Таблица 2
ii. Смесь осторожно встряхивали и в каждую ПЦР-пробирку пипетировали 40 мкл смеси, а затем добавляли 10 мкл ДНК, обработанной бисульфатом.
iii. Смесь осторожно встряхивали и проводили ПЦР-амплификацию следующим образом: один цикл денатурации при 95°С в течение 15 минут, 35 циклов денатурации при 94°С в течение 30 секунд, отжиг при 55°С в течение 90 секунд и удлинение при 72°C в течение 90 секунд, и один цикл удлинения при 72°C в течение 10 минут и, наконец, смесь постоянно выдерживали при 4°C.
iv. 5 мкл ПЦР-продуктов смешивали с 6 × загрузочным буфером (TakaRa, номер по каталогу 9156) и загружали в 1% (масс./об.) агарозный гель с контрольным ДНК-маркером DL2000 (TakaRa, номер по каталогу: 3427Q) и подвергали электрофорезу при 120В в течение 40 минут.
v. Если наблюдалась неспецифическая амплификация, то необходимо было восстановить оставшиеся 45 мкл ПЦР-продуктов после электрофореза в соответствии с инструкциями к набору (QIAGEN, номер по каталогу: 28704).
[00178]
(b) Очистка и количественная оценка ПЦР-продуктов
ПЦР-продукт очищали с помощью набора для ПЦР-очистки MinElute в соответствии с инструкциями к набору (QIAGEN, номер по каталогу: 28004). Очищенный ПЦР-продукт количественно определяли с помощью набора для анализа на дцДНК BR Qubit™ (номер по каталогу: Q32850).
[00179]
(c) Лигирование адаптера
Адаптеры лигировали с очищенными ПЦР-продуктами с помощью модуля для быстрого лигирования NEBNext (NEB, номер по каталогу: E6056L), и реакционную смесь приготовливали следующим образом:
Таблица 3. Реакционная смесь для лигирования адаптера
В каждую ПЦР-пробирку добавляли 30 мкл смеси, а затем добавляли 20 мкл очищенных ПЦР-продуктов, соответственно. Раствор осторожно перемешивали, инкубировали при 20°C в течение 15 минут и выдерживали при 4°C в течение 10 минут.
[00180]
(d) Очистка продуктов лигирования
i. Сферы Agencourt AMpure XP (Beckman, номер по каталогу: A63882) выдерживали при комнатной температуре для последующего использования.
ii. ПЦР-пробирки центрифугировали при 280× g в течение 1 минуты при 20°C, и 50 мкл продуктов лигирования переносили в новый 96-луночный планшет для ПЦР.
iii. Сферы AMpure XP встряхивали в течение 30 секунд для равномерного распределения и в каждую лунку планшета для ПЦР добавляли 56 мкл сфер. Смесь осторожно иипетировали 10 раз для перемешивания и выдерживали при комнатной температуре в течение 5 минут.
iv. 96-луночный планшет для ПЦР помещали на 96-луночный магнитный планшет, и выдедерживали его в течение 2 минут до тех пор, пока супернатант не становился прозрачным. Затем 96-луночный планшет для ПЦР выдерживали на 96-луночном магнитном планшете и удаляли супернатант, после чего в каждую лунку добавляли 200 мкл свежеприготовленного 80% этанола и инкубировали при комнатной температуре в течение 30 секунд, и супернатант удаляли.
v. 96-луночный планшет для ПЦР выдерживали на 96-луночном магнитном планшете, после чего в каждую лунку добавляли 200 мкл свежеприготовленного 80% этанола. Затем инкубировали при комнатной температуре в течение 30 секунд. Супернатант отбрасывали и остатки этанола удаляли с помощью 10 мкл-пипетки.
vi. 96-луночный планшет для ПЦР выдерживали на магнитном планшете и сферам давали высохнуть естественным путем в течение 10 минут.
vii. 96-луночный планшет для ПЦР снимали с магнитного планшета, и в каждую лунку 96-луночного планшета добавляли 27,5 мкл 10 мМ Триса (pH 8,5). Сферы осторожно перемешивали пипеткой вверх и вниз и 10 раз добавляли Трис, пока сферы не были полностью распределены. Планшет выдерживали при комнатной температуре в течение 2 минут.
viii. 96-луночный планшет для ПЦР помещали на магнитный планшет и оставляли на 2 минуты до тех пор, пока супернатант не становился прозрачным. В новую ПЦР-пробирку пипетировали 25 мкл супернатанта и хранили при -20°C для последующего использования.
[00181]
(е) ПЦР-амплификация и очистка продукта
ПЦР-смесь Master приготавливали как описано ниже и осторожно перемешивали. В каждую ПЦР-пробирку добавляли 40 мкл ПЦР-смеси, а затем добавляли 5 мкл очищенных продуктов лигирования.
Таблица 4. Реакционная смесь для ПЦР
(NEB, номер по каталогу: M0544)
ПЦР-пробирки осторожно встряхивали и быстро центрифугировали, а затем проводили ПЦР в следующих условиях: один цикл денатурации при 98°С в течение 30 секунд, от 8 до 15 циклов денатурации при 98°С в течение 10 секунд и удлинение при 65°С в течение 75 секунд, один цикл денатурации при 65°С в течение 5 минут и, наконец, выдерживание при 4°C. Продукты ПЦР очищали как описано в стадии (d) «Очистка продуктов лигирования».
[00182]
(f) Детектирование и секвенирование библиотеки
Концентрацию и распределение очищенных продуктов ПЦР по размеру анализировали с помощью набора QubitTM для анализа на дцДНК BR (номер по каталогу: Q32850) и биоанализатора Agilent 2100, соответственно. Библиотеки с равной молярной концентрацией объединяли и секвенировали на Illumina HiSeq2500 с длиной рида PE125.
[00183]
(g) Анализ данных секвенирования
Исходные данные были подвергали демультиплексированию в соответствии с индексами образцов, и данные ридов секвенирования были картированы с последовательностями контрольных генов BMP3 и NDRG4 с помощью программы SHRiMP V2.04. Метилированные сайты CpG были идентифицированы исходя из результатов картирования. И наконец, было установлено, что 26 и 39 сайтов CpG генов BMP3 и NDRG4 были гиперметилированы в тканях с РПОК и ПА по сравнению с соседними нормальными тканями (p<0,05), что указывает на то, что эти метилированные сайты CpG могут быть использованы в качестве биомаркеров ДНК для ранней диагностики РПОК и ПА.
Таблица 5. Частота метилирования сайтов CpG гена BMP3 в тканях РПОК и в соседних нормальных тканях
(hg19)
(NM_001201.3)
Таблица 6. Частота метилирования сайтов CpG гена BMP3 в тканях ПА и в соседних нормальных тканях
(hg19)
(NM_001201.3)
Таблица 7. Частота метилирования сайтов CpG гена NDRG4 в тканях ПА и в соседних нормальных тканях
(hg19)
(NM_0020465.3)
Таблица 8. Частота метилирования сайтов CpG гена NDRG4 в тканях ПА и в соседних нормальных тканях
(hg19)
(NM_020465.3)
ПРИМЕР 2
Сравнение сайтов CpG дифференциального метилирования генов BMP3 и NDRG4, ассоциированных с РПОК, у различных рас.
[00184] Авторами были проанализированы данные метилирования микромассивов генов BMP3 и NDRG4 в базе данных TCGA (данные по метилированию у человека Illumina 450), и было обнаружено, что существует пять существенно отличающихся сайтов метилирования CpG в промоторной области генов NDRG4 у белого населения и у населения Азии (фигура 2 и Таблица 9). Для дальнейшего подтверждения сайтов дифференциального метилирования CpG были взяты образцы ткани и пробы крови у 106 пациентов с РПОК и ПА в Китае. ДНК экстрагировали и обрабатывали бисульфатом. Промоторные области генов BMP3 и NDRG4 были амплифицированы и секвенированы. Авторами были проанализированы данные секвенирования, в результате чего было обнаружено, что сайты гиперметилирования CpG у населения Азии отличаются от сайтов гиперметилирования CpG у белого населения, взятых из базы данных TCGA, и сайты гиперметилирования CpG отличаются в образцах ткани с РПОК и с ПА. Что касается этих различных сайтов метилирования CpG, то авторами был получен набор для детектирования, а в частности, для обнаружения РПОК и ПА у населения Азии (например, у населения Китая).
Таблица 9. Различия в сайтах метилирования CpG генов BMP3 и NDRG4 у белого населения и у населения Азии
ПРИМЕР 3
Скрининг праймеров и зондов для генов BMP3 и NDRG4
(1) Конструирование и отбор праймеров и зондов для генов BMP3 и NDRG4.
[00185] Праймеры и зонды для кол.ПЦР были сконструированы на основе метилированных сайтов CpG генов BMP3 и NDRG4. Были идентифицированы три пары предпочтительных праймеров и зондов. Предпочтительные праймеры и зонды сравнивали с несколькими другими кандидатами на праймеры и зонды генов BMP3 и NDRG4 с позитивными контролями и негативными контролями. Информация о праймерах и зондах представлена в таблице 10.
Таблица 10. Информация о предпочтительных и остальных праймерах и зондах
Контроль 2,
Контроль 3
Контроль 2,
Контроль 3
(2) Сравнение предпочтительных праймеров и зондов с позитивным и негативным контролями генов BMP3 и NDRG4
[00186] Стандартные образцы с различными уровнями метилирования были получены путем добавления ДНК в качестве позитивного контроля к ДНК негативного контроля генов BMP3 и NDRG4, соответственно, в различных соотношениях (Таблица 11). Аналитическую чувствительность сравнивали путем амплификации стандартного образца ДНК с предпочтительными и контрольными праймерами и зондами генов BMP3 и NDRG4, соответственно. Аналитическую специфичность сравнивали путем амплификации ДНК негативного контроля генов BMP3 и NDRG4 с предпочтительными и контрольными праймерами и зондами генов BMP3 и NDRG4 соответственно, при этом, количество ДНК негативного контроля составляло 104 копий, 105 копий, 106 копий, 107 копий и 108 копий на реакцию.
Таблица 11. Стандартный образец генов BMP3 и NDRG4
[00187] Основная смесь была приготовлена как описано в Таблице 5, и условия количественной ПЦР включают сначала денатурацию при 95°С в течение 1 минуты, а затем 50 циклов денатурации при 95°С в течение 20 секунд и удлинение при 60°С в течение 1 минуты.
Таблица 12. Конечные концентрации реагентов для кол.ПЦР с метилированием
[00188] Как показано в Таблице 13 и на фигурах 3А-3L, 1/104 метилированной ДНК может быть детектировано с использованием трех пар предпочтительных праймеров и зондов, но три пары контролей не могут быть детектированы.
[00189] Как показано в Таблице 13 и на фигурах 3А-3L, предпочтительные три пары праймеров и зондов BMP3 и NDRG4 согласно изобретению способны стабильно детектировать уровни метилирования вплоть до одного из десяти тысяч, тогда как три пары сравнительных праймеров и зондов не способны детектировать даже один из десяти тысяч уровней метилирования.
Таблица 13: Сравнение аналитической чувствительности предпочтительных и контрольных праймеров и зондов генов BMP3 и NDRG4
Y: обнаружено, N: не определено.
[00190] Аналитические кривые амплификации чувствительности BMP3 и NDRG4 показаны на фигурах 3A-3L для каждой из предпочтительных комбинаций по сравнению с контрольными группами.
[00191] Как показано в Таблице 14 и на фигурах 4А-4L, три пары предпочтительных праймеров и зондов для генов BMP3 и NDRG4 не имеют сигналов амплификации при различных концентрацях неметилированной ДНК, в то время как сравнительные праймеры и зонды демонстрировали различные уровни неспецифической амплификации.
Таблица 14. Сравнение аналитической специфичности предпочтительных и контрольных праймеров и зондов
(Копии на реакцию)
(Копии на реакцию)
1
Y: без амплификации, N: неспецифическая амплификация.
Ааналитические кривые амплификации специфичности BMP3 и NDRG4
Пример 4
Подтверждение предпочтительных и сравнительных метилированных праймеров и зондов осуществляют на пробах кала с генами BMP3 и NDRG4.
[00192] Уровень метилирования генов BMP3 и NDRG4 в 81 пробе кала определяли с использованием трех пар предпочтительных и сравнительных праймеров и зондов. Три сравнительных праймера и зонда представляют собой:
Сравнительные праймеры и зонды 1: прямой праймер BMP3 SEQ ID NO: 21, обратный праймер BMP3 SEQ ID NO: 22 и зонд BMP3 SEQ ID NO: 23; прямой праймер NDRG4 SEQ ID NO: 24, обратный праймер NDRG4 SEQ ID NO: 25 и зонд NDRG4 SEQ ID NO: 26;
Сравнительные праймеры и зонды 2: прямой праймер BMP3 SEQ ID NO: 27, обратный праймер BMP3 SEQ ID NO: 28 и зонд BMP3 SEQ ID NO: 29; прямой праймер NDRG4 SEQ ID NO: 24, обратный праймер NDRG4 SEQ ID NO: 30 и зонд NDRG4 SEQ ID NO: 26;
Сравнительные праймеры и зонды 3: прямой праймер BMP3 SEQ ID NO: 31, обратный праймер BMP3 SEQ ID NO: 32 и зонд BMP3 SEQ ID NO: 33; прямой праймер NDRG4 SEQ ID NO: 24, обратный праймер NDRG4 SEQ ID NO: 34 и зонд NDRG4 SEQ ID NO: 26.
[00193] Информация об образцах кала представлена в Таблице 15.
Таблица 15. Статистика для 81 пробы кала
[00194] ДНК кала экстрагировали из образцов в соответствии с описанным ниже методом.
(1) Экстракция ДНК кала:
i. К 4-6 г проб кала добавляют 40 мл лизата, тщательно встряхивают, а затем инкубируют при 50°С в течение 16 часов.
ii. Затем центрифугруют при 5000 об/мин в течение 10 минут. При этом, следует обратить внимание на весы для взвешивания перед центрифугированием. После окончания центрифугирования, центрифужные пробирки осторожно извлекают и встряхивают, но не интенсивно.
iii. 9 мл супернатанта иипетируют в новую центрифужную 50 мл-пробирку, а затем добавляют 1 мл экстрагирующего адъюванта, 60 мкл магнитных сфер и 10 мл изопропанола. Затем перемешивают в течение 10 секунд и инкубируют при 65°С в течение 20 минут. Во время инкубирования, осуществляют перемешивание вверх и вниз один раз в 5 минут.
iv. После инкубирования, центрифужную 50 мл-пробирку помещают на магнитную подставку и оставляют на 3 минуты, пока супернатант не станет прозрачным, после чего супернатант отбрасывают.
v. Затем центрифужную 50 мл-пробирку снимают с магнитной подставки и добавляют 12 мл промывочного раствора. Раствор перемешивают до тех пор, пока магнитные сферы не упадут с пробирки, содержащейся в лунках, и выдерживают в течение 3 минут, а затем центрифужную 50 мл-пробирку снова ставят на магнитную подставку на 3 минуты, пока супернатант не станет прозрачным, после чего супернатант отбрасывают.
vi. Добавляют 15 мл 80% раствора этанола, встряхивают, пока сферы не выпадут из пробирки, содержащейся в лунках, и выдерживают в течение 3 минут. Затем пробирку снова ставят на магнитную подставку на 3 минуты, пока супернатант не станет прозрачным, после чего супернатант отбрасывают.
vii. Предыдущую стадию повторяют еще один раз.
viii. Оставшуюся на дне жидкость пипетируют, при этом пробирку держат открытой и инкубируют при 65°С в течение 5 минут. Затем пробирку снимают с магнитной подставки и оставляют для высыхания сферы, и добавляют 1,5 мл предварительно нагретого элюента I. Сферы переносят из лунки в элюент I с помощью 1000 мкл-пипетки, после чего смесь переносят в центрифужную 2 мл-пробирку и закрывают крышку, а затем инкубируют при 65°С в течение 5 минут.
ix. Затем центрифугируют при 13000 об/мин в течение 3 минут, 600 мкл супернатанта пипетируют в новую 1,5 мл-пробирку, а затем добавляют 600 мкл связывающего раствора и тщательно перемешивают.
x. 600 мкл вышеуказанной смеси переносят в колонку для очистки ДНК, центрифугируют при 13000 об/мин в течение 1 минуты и отходы выбрасывают.
xi. Оставшуюся смесь обрабатывают, как и в предыдущей стадии, и центрифугируют при 13000 об/мин в течение 2 минут.
xii. 600 мкл 90% раствора этанола добавляют в колонку для очистки ДНК, центрифугируют при 13000 об/мин в течение 1 минуты и отходы выбрасывают.
xiii. Предыдущую стадию повторяют 2 раза.
xiv. Затем центрифугируют при 13000 об/мин в течение 3 минут и колонку для очистки ДНК помещают в новую центрифужную 1,5 мл-пробирку. Колонку для очистки ДНК открывают и инкубируют при 65°С в течение 5 минут до высыхания.
xv. 100 мкл предварительно нагретого элюата II по каплям добавлячют в середину колонки для очистки ДНК, крышку закрывают и инкубируют при 65°С в течение 5 минут. Затем центрифугируют при 13000 об/мин в течение 2 минут. Полученный раствор элюированной ДНК хранят при 2-8°C до последующего использования. Температура при длительном хранении должна составлять от -25°С до -15°С.
[00195]
(2) Обработка бисульфитом
Подробное описание стадий процедур приводится в Примере 3.
[00196]
(3) кол.ПЦР
Смесь Master для кол.ПЦР была приготовлена следующим образом:
Таблица 16
Условия реакции кол.ПЦР: Один цикл денатурации при 95°С в течение 2 минут, 50 циклов денатурации при 95°С в течение 20 секунд и удлинение при 95°С в течение 1 минуты. Ген B2M представляет собой контрольный ген для контроля качества реакции кол.ПЦР.
(4) Результаты
[00197] Как показано в Таблице 17, чувствительность диагностики РПОК и ПА в 81 пробе кала с использованием трех пар предпочтительных праймеров и зондов генов BMP3 и NDRG4 составляет до 85,0-95,0% (РПОК по метилированию BMP3), 66,7% -73,3% (ПA по метилированию BMP3) и 90,0% - 95,0% (РПОК по метилированию NDRG4) и 73,3% -86,7% (ПA по метилированию NDRG4), соответственно. Кроме того, специфичность диагностики РПОК и ПА с использованием данных метилирования BMP3 или данных метилирования NDRG4 составляет приблизительно 97,8% - 100,0%.
[00198] Однако чувствительность диагностики РПОК и ПА в 81 пробе кала с использованием трех пар сравнительных праймеров и зондов генов BMP3 и NDRG4 составляет 85,0-90,0% (РПОК по метилированию BMP3), 46,7-60,0% (ПA по метилированию BMP3) и 90,0% -95,0% (РПОК по метилированию NDRG4) и 66,7% -73,3% соответственно (ПA по метилированию NDRG4). Кроме того, общая специфичность диагностики РПОК и ПА с использованием данных по метилированию BMP3 или данных по метилированию NDRG4 увеличилась приблизительно до 91,3-93,5% и 93,5-95,7%, соответственно.
[00199] При этом, очевидно, что предпочтительные праймеры и зонды превосходят сравнительные праймеры и зонды при анализе клинических образцов, особенно при диагностике ПА.
Таблица 17.
Результаты статистического анализа исследуемых клинических образцов
Таблица 18.
Результаты детектирования для 81 пробы кала
Примечания: U: не определяли.
Пример 5
Скрининг комбинаций праймеров и зондов для метилирования генов BMP3 и DNRG4
(1) Экстракция ДНК из кала
[00200] ДНК экстрагировали из кала согласно протоколу Примера 3.
(2) Определение метилирования генов BMP3 и NDRG4
[00201] Комбинации праймера и зонда генов BMP3 и NDRG4 показаны ниже. кол.ПЦР осуществляли с девятью комбинациями соответственно, как описано в стадиях Примера 3.
Таблица 19. Комбинации праймера и зонда
Последовательности праймеров и зондов девяти комбинаций генов BMP3 и NDRG4 представлены ниже:
Таблица 20. Последовательности праймеров и зондов в комбинациях
[00202] Смесь Master для кол.ПЦР, используемая в реакции, представлена ниже:
Таблица 21. Смесь Master для кол.ПЦР для BMP3/NDRG4
[00203] Условия реакции кол.ПЦР представляют собой один цикл денатурации при 95°С в течение 2 минут и 50 циклов денатурации при 95°С в течение 20 секунд и удлинение при 60°С в течение 1 минуты.
(3) Детектирование вариантов гена KRAS
[00204] Было детектировано семь горячих точек мутации в кодонах 12 и 13 гена KRAS. Семь мутантов представляют собой G12D, G13D, G12V, G12C, G12S, G12A и G13R, а последовательности праймеров и зондов представлены в таблице 22.
Таблица 22. Праймеры и зонды для детектирования семи мутаций гена KRAS
Смесь Master для кол.ПЦР, используемая в реакции, представлена ниже:
Таблица 23. Смесь Master для кол.ПЦР KRAS
[00205] Условия реакции кол.ПЦР представляют собой один цикл денатурации при 95°С в течение 5 минут и 45 циклов денатурации при 95°С в течение 15 секунд, отжиг при 71°C в течение 60 секунд, а затем удлинение при 55°С в течение 50 секунд.
[00206] кол.ПЦР для контроля качества проводили с использованием ACTB в качестве контрольного гена.
(4) Анализ на гемоглобин в кале
[00207] Гемоглобин в кале определяли с помощью иммунохимического анализа кала (FIT), и результат является положительным или отрицательным.
(5) Вычисление величин по формуле
[00208] Значение Ct для детектирования генов BMP3, NDRG4 и KRAS с помощью кол.ПЦР, а также положительный или отрицательный результат анализа на гемоглобин в кале вводили в формулу логистической регрессии, как показано ниже:
P=eK/(1+eK)
[00209] где: P означает общий индекс,
K=a*ΔCt1+b*ΔCt2+c*ΔCt3+d*FIT+X, где e означает натуральную константу, a, b, c, d, X означают клинические константы. ΔCt1, ΔCt2 и ΔCt3 представляют собой значение Ct генов-мишеней, вычитаемое из значений контрольных генов.
[00210] Результат анализа является положительным, если значение P равно или выше заданного порога, а в противном случае этот результат является отрицательным. Положительный результат указывает на то, что у индивидуума могут быть диагностированы РПОК или ПА.
(6) Результат анализа
[00211] Была проанализирована восемьдесят одна проба кала Примера 3, и результаты различных комбинаций праймеров и зондов генов BMP3 и NDRG4 представлены в Таблице 24.
Таблица 24. Результат анализа 81 пробы кала
(РПОК+ПA)
(РПОК+ПA)
(РПОК)
(ПA)
[00212] Очевидно, что: (1) Комбинации №№ 4, 5 и 7 превосходят другие шесть комбинаций. Если учесть, что все протестированные праймеры и зонды являются предпочтительными и превосходят другие праймеры и зонды (см. Пример 3), то эти три конкретные комбинации превосходят любые известные комбинации праймеров/зондов BMP3 и NDRG4. (2) Чувствительность и специфичность набора для диагностики РПОК и ПА, включающего гены BMP3, NDRG4, KRAS, и набора для детектирования гемоглобина в кале, значительно лучше, чем чувствительность и специфичность детектирования метилирования одного гена BMP3 или NDRG4. (3) Чувствительность и специфичность набора для диагностики РПОК у населения Азии (например, у населения Китая) явно превосходит чувствительность и специфичность существующих аналогичных продуктов, таких как Cologuard®. (4) Чувствительность и специфичность набора для диагностики ПА у населения Азии (например, у населения Китая) значительно лучше, чем чувствительность и специфичность существующих аналогичных продуктов, таких как Cologuard®.
[00213] Описание изобретения, включая формулу изобретения, фигуры и/или чертежи, каждого из цитируемых здесь патентов, патентных заявок и публикаций включены в настоящее описание в полном объеме посредством ссылки.
[00214] Если это не оговорено особо, то все технические и научные термины в настоящей заявке имеют общепринятое значение, известное специалистам в области, к которой относится изобретение. Хотя для практического осуществления настоящего изобретения или для проведения тестов согласно изобретению могут быть применены любые методы и материалы, аналогичные или эквивалентные описанным здесь методам и материалам, однако, следует отдать предпочтение методам и материалам, описанным в настоящей заявке. Все цитируемые здесь публикации, патенты и патентные заявки включены в настоящее описание во всех целях и в полном объеме посредством ссылки.
[00215] Обсуждаемые здесь публикации представлены исключительно для их раскрытия до даты подачи настоящей заявки. Ничто в данном документе не должно истолковываться как признание того, что авторы настоящего изобретения не имеют права датировать такую публикацию более ранней датой на основании предшествующего изобретения.
[00216] Хотя настоящее изобретение было описано в комбинации с его конкретными вариантами осуществления, однако, следует отметить, что в него могут быть внесены дополнительные модификации, и эта заявка охватывает любые варианты, применения или адаптации изобретения в основном, в соответствии с принципами изобретения, и включает такие отклонения от раскрытия изобретения, которые входят в известную или обычную практику в области техники, к которой относится изобретение, и которые могут быть применены к основным признакам, изложенным выше и ниже в объеме прилагаемой формулы изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Hangzhou New Horizon Health Technology Co. Ltd.
Li, Hui
Li, Cunyao
Zheng, Weixian
Yang, Jiao
Liu, Gang
Lv, Ning
Chen, Yiyou
<120> НАБОР ДЛЯ СКРИНИНГА НА РАК ПРЯМОЙ И ОБОДОЧНОЙ КИШКИ И
ПРОГРЕССИРУЮЩЕЙ АДЕНОМЫ И ЕГО ПРИМЕНЕНИЕ
<130> NEWH-017/01WO 333709-2028
<150> CN 201810502387.9
<151> 2018-05-23
<150> CN 201810502359.7
<151> 2018-05-23
<160> 70
<170> PatentIn version 3.5
<210> 1
<211> 271
<212> ДНК
<213> Homo sapiens
<220>
<221> модифицированное_основание
<222> (12)..(12)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (33)..(33)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (69)..(69)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (80)..(80)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (83)..(83)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (85)..(85)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (106)..(106)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (120)..(120)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (123)..(123)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (127)..(127)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (132)..(132)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (139)..(139)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (141)..(141)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (152)..(152)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (154)..(154)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (189)..(189)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (200)..(200)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (219)..(219)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (227)..(227)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (236)..(236)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (240)..(240)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (242)..(242)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (247)..(247)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (254)..(254)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (258)..(258)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (264)..(264)
<223> метилированный
<400> 1
gttagtttgg tcgggtgttt ttaaaaataa agcgaggagg gaaggtatag atagattttg 60
aaaatattcg ggttatatac gtcgcgattt atagtttttt tttagcgttg gagtggagac 120
ggcgttcgta gcgttttgcg cgggtgaggt tcgcgtagtt gttggggaag agtttatttg 180
ttaggttgcg ttgggttagc gtagtaagtg gggttggtcg ttatttcgtt gtattcggtc 240
gcgtttcggg tttcgtgcgt tttcgtttta g 271
<210> 2
<211> 236
<212> ДНК
<213> Homo sapiens
<220>
<221> модифицированное_основание
<222> (9)..(9)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (12)..(12)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (18)..(18)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (20)..(20)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (25)..(25)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (29)..(29)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (48)..(48)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (50)..(50)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (53)..(53)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (55)..(55)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (62)..(62)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (66)..(66)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (74)..(74)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (78)..(78)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (85)..(85)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (98)..(98)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (100)..(100)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (109)..(109)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (118)..(118)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (120)..(120)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (122)..(122)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (130)..(130)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (132)..(132)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (137)..(137)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (141)..(141)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (159)..(159)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (165)..(165)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (170)..(170)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (172)..(172)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (177)..(177)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (181)..(181)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (191)..(191)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (202)..(202)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (204)..(204)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (210)..(210)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (216)..(216)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (218)..(218)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (221)..(221)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (226)..(226)
<223> метилированный
<400> 2
tgagaagtcg gcgggggcgc ggatcgatcg gggtgttttt taggtttcgc gtcgcggttt 60
tcgttcgttt tttcgttcgt ttatcgggta ttttagtcgc gtagaaggcg gaagttacgc 120
gcgagggatc gcggttcgtt cgggattagt tttaggttcg gtatcgtttc gcgggtcgag 180
cgtttatatt cgttaaattt acgcgggtac gttttcgcgg cgtatcgttt ttagtt 236
<210> 3
<211> 29
<212> ДНК
<213> Homo sapiens
<400> 3
tttgaaaata ttcgggttat atacgtcgc 29
<210> 4
<211> 28
<212> ДНК
<213> Homo sapiens
<400> 4
ataaactctt ccccaacaac tacgcgaa 28
<210> 5
<211> 25
<212> ДНК
<213> Homo sapiens
<400> 5
agcgttggag tggagacggc gttcg 25
<210> 6
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 6
atcgatcggg gtgtttttta ggtttc 26
<210> 7
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 7
ccttctacgc gactaaaata cccgat 26
<210> 8
<211> 31
<212> ДНК
<213> Homo sapiens
<400> 8
cgtcgcggtt ttcgttcgtt ttttcgttcg t 31
<210> 9
<211> 25
<212> ДНК
<213> Homo sapiens
<400> 9
aatattcggg ttatatacgt cgcga 25
<210> 10
<211> 28
<212> ДНК
<213> Homo sapiens
<400> 10
gcaacctaac aaataaactc ttccccaa 28
<210> 11
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 11
tggagtggag acggcgttcg tagcgt 26
<210> 12
<211> 17
<212> ДНК
<213> Homo sapiens
<400> 12
gcgggtgaga agtcggc 17
<210> 13
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 13
gtaacttccg ccttctacgc 20
<210> 14
<211> 25
<212> ДНК
<213> Homo sapiens
<400> 14
taggtttcgc gtcgcggttt tcgtt 25
<210> 15
<211> 27
<212> ДНК
<213> Homo sapiens
<400> 15
aatattcggg ttatatacgt cgcgatt 27
<210> 16
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 16
acttactacg ctaacccaac g 21
<210> 17
<211> 28
<212> ДНК
<213> Homo sapiens
<400> 17
tagcgttgga gtggagacgg cgttcgta 28
<210> 18
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 18
cggttttcgt tcgttttttc g 21
<210> 19
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 19
aacctaaaac taatcccgaa cgaacc 26
<210> 20
<211> 28
<212> ДНК
<213> Homo sapiens
<400> 20
tcgtttatcg ggtattttag tcgcgtag 28
<210> 21
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 21
gagtggagac ggcgttcgta 20
<210> 22
<211> 23
<212> ДНК
<213> Homo sapiens
<400> 22
ccacttacta cgctaaccca acg 23
<210> 23
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 23
cgggtgaggt tcgcgtagtt gttggg 26
<210> 24
<211> 23
<212> ДНК
<213> Homo sapiens
<400> 24
gggtgttttt taggtttcgc gtc 23
<210> 25
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 25
cgtaacttcc gccttctacg c 21
<210> 26
<211> 40
<212> ДНК
<213> Homo sapiens
<400> 26
acgcgactaa aatacccgat aaacgaacga aaaaacgaac 40
<210> 27
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 27
ttaggttgcg ttgggttagc g 21
<210> 28
<211> 22
<212> ДНК
<213> Homo sapiens
<400> 28
actccgaaaa cgcaaaaaac cg 22
<210> 29
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 29
attcggtcgc gtttcgggtt tcgtgc 26
<210> 30
<211> 19
<212> ДНК
<213> Homo sapiens
<400> 30
gacccgcgaa acgataccg 19
<210> 31
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 31
tattcgggtt atatacgtcg c 21
<210> 32
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 32
cttactacgc taacccaacg 20
<210> 33
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 33
cccaacaact acgcgaacct cacccg 26
<210> 34
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 34
tcgcgcgtaa cttccgcctt 20
<210> 35
<211> 22
<212> ДНК
<213> Homo sapiens
<400> 35
aacttgtggt agttggaggt ga 22
<210> 36
<211> 25
<212> ДНК
<213> Homo sapiens
<400> 36
aacttgtggt agttggagct gggga 25
<210> 37
<211> 22
<212> ДНК
<213> Homo sapiens
<400> 37
aacttgtggt agttggagtt gt 22
<210> 38
<211> 22
<212> ДНК
<213> Homo sapiens
<400> 38
aaacttgtgg tagttggggc tt 22
<210> 39
<211> 22
<212> ДНК
<213> Homo sapiens
<400> 39
aaacttgtgg tagttggtgc ta 22
<210> 40
<211> 22
<212> ДНК
<213> Homo sapiens
<400> 40
aacttgtggt agttggagca gc 22
<210> 41
<211> 22
<212> ДНК
<213> Homo sapiens
<400> 41
aaacttgtgg tagttggagc tc 22
<210> 42
<211> 24
<212> ДНК
<213> Homo sapiens
<400> 42
gaatggtcct gcaccagtaa tatg 24
<210> 43
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 43
agggcttctt gtcctttcct t 21
<210> 44
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 44
cgtgctcgat ggggtacttc 20
<210> 45
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 45
aggcaagagt gccttgacga tacagc 26
<210> 46
<211> 27
<212> ДНК
<213> Homo sapiens
<400> 46
cgtgatggtg ggcatgggtc agaagga 27
<210> 47
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 47
agtttggtgt aagttaagag 20
<210> 48
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 48
ctaactctat tttaaacrcc a 21
<210> 49
<211> 23
<212> ДНК
<213> Homo sapiens
<400> 49
gttttaattt ttggaaaagg taa 23
<210> 50
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 50
acctaacaaa taaactcttc c 21
<210> 51
<211> 22
<212> ДНК
<213> Homo sapiens
<400> 51
gaaggtatag atagattttg aa 22
<210> 52
<211> 24
<212> ДНК
<213> Homo sapiens
<400> 52
cacctaacac aactttacra aact 24
<210> 53
<211> 26
<212> ДНК
<213> Homo sapiens
<400> 53
gtatttagtt atggttgggg ygagta 26
<210> 54
<211> 21
<212> ДНК
<213> Homo sapiens
<400> 54
ctcacctact actaccgccc r 21
<210> 55
<211> 25
<212> ДНК
<213> Homo sapiens
<400> 55
aggtttttga gtttttggtt ttttt 25
<210> 56
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 56
ccctccaaac cccctataac 20
<210> 57
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 57
ggatggggat gtttttgtag 20
<210> 58
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 58
rgrgaaacct aaaaaacacc 20
<210> 59
<211> 18
<212> ДНК
<213> Homo sapiens
<400> 59
gyggagyggg tgagaagt 18
<210> 60
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 60
craacaacca aaaacccctc 20
<210> 61
<211> 23
<212> ДНК
<213> Homo sapiens
<400> 61
gttygttygg gattagtttt agg 23
<210> 62
<211> 19
<212> ДНК
<213> Homo sapiens
<400> 62
crcaaacraa aaacraaac 19
<210> 63
<211> 18
<212> ДНК
<213> Homo sapiens
<400> 63
gyggygtttt ygtttttg 18
<210> 64
<211> 20
<212> ДНК
<213> Homo sapiens
<400> 64
cracractaa aaatccccaa 20
<210> 65
<211> 271
<212> ДНК
<213> Homo sapiens
<220>
<221> модифицированное_основание
<222> (12)..(12)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (33)..(33)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (69)..(69)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (80)..(80)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (83)..(83)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (85)..(85)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (106)..(106)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (120)..(120)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (123)..(123)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (132)..(132)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (139)..(139)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (141)..(141)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (152)..(152)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (154)..(154)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (189)..(189)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (200)..(200)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (219)..(219)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (227)..(227)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (240)..(240)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (242)..(242)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (247)..(247)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (254)..(254)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (258)..(258)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (264)..(264)
<223> метилированный
<400> 65
gccagtttgg ccgggtgttc ccaaaaataa agcgaggagg gaaggtacag acagatcttg 60
aaaacacccg ggccacacac gccgcgacct acagctcttt ctcagcgttg gagtggagac 120
ggcgcccgca gcgccctgcg cgggtgaggt ccgcgcagct gctggggaag agcccacctg 180
tcaggctgcg ctgggtcagc gcagcaagtg gggctggccg ctatctcgct gcacccggcc 240
gcgtcccggg ctccgtgcgc cctcgcccca g 271
<210> 66
<211> 236
<212> ДНК
<213> Homo sapiens
<220>
<221> модифицированное_основание
<222> (9)..(9)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (12)..(12)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (18)..(18)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (20)..(20)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (25)..(25)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (29)..(29)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (48)..(48)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (50)..(50)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (53)..(53)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (55)..(55)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (62)..(62)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (66)..(66)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (74)..(74)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (78)..(78)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (85)..(85)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (98)..(98)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (100)..(100)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (109)..(109)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (118)..(118)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (120)..(120)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (122)..(122)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (130)..(130)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (132)..(132)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (137)..(137)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (141)..(141)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (159)..(159)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (165)..(165)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (170)..(170)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (172)..(172)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (177)..(177)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (181)..(181)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (191)..(191)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (202)..(202)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (204)..(204)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (210)..(210)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (216)..(216)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (218)..(218)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (221)..(221)
<223> метилированный
<220>
<221> модифицированное_основание
<222> (226)..(226)
<223> метилированный
<400> 66
tgagaagtcg gcgggggcgc ggatcgaccg gggtgtcccc caggctccgc gtcgcggtcc 60
ccgctcgccc tcccgcccgc ccaccgggca ccccagccgc gcagaaggcg gaagccacgc 120
gcgagggacc gcggtccgtc cgggactagc cccaggcccg gcaccgcccc gcgggccgag 180
cgcccacacc cgccaaaccc acgcgggcac gcccccgcgg cgcaccgccc ccagcc 236
<210> 67
<211> 271
<212> ДНК
<213> Homo sapiens
<400> 67
gttagtttgg tcgggtgttt ttaaaaataa agcgaggagg gaaggtatag atagattttg 60
aaaatattcg ggttatatac gtcgcgattt atagtttttt tttagcgttg gagtggagac 120
ggcgttcgta gcgttttgcg cgggtgaggt tcgcgtagtt gttggggaag agtttatttg 180
ttaggttgcg ttgggttagc gtagtaagtg gggttggtcg ttatttcgtt gtattcggtc 240
gcgtttcggg tttcgtgcgt tttcgtttta g 271
<210> 68
<211> 271
<212> ДНК
<213> Homo sapiens
<400> 68
gttagtttgg ttgggtgttt ttaaaaataa agtgaggagg gaaggtatag atagattttg 60
aaaatatttg ggttatatat gttgtgattt atagtttttt tttagtgttg gagtggagat 120
ggtgtttgta gtgttttgtg tgggtgaggt ttgtgtagtt gttggggaag agtttatttg 180
ttaggttgtg ttgggttagt gtagtaagtg gggttggttg ttattttgtt gtatttggtt 240
gtgttttggg ttttgtgtgt ttttgtttta g 271
<210> 69
<211> 236
<212> ДНК
<213> Homo sapiens
<400> 69
tgagaagtcg gcgggggcgc ggatcgatcg gggtgttttt taggtttcgc gtcgcggttt 60
tcgttcgttt tttcgttcgt ttatcgggta ttttagtcgc gtagaaggcg gaagttacgc 120
gcgagggatc gcggttcgtt cgggattagt tttaggttcg gtatcgtttc gcgggtcgag 180
cgtttatatt cgttaaattt acgcgggtac gttttcgcgg cgtatcgttt ttagtt 236
<210> 70
<211> 236
<212> ДНК
<213> Homo sapiens
<400> 70
tgagaagttg gtgggggtgt ggattgattg gggtgttttt taggttttgt gttgtggttt 60
ttgtttgttt ttttgtttgt ttattgggta ttttagttgt gtagaaggtg gaagttatgt 120
gtgagggatt gtggtttgtt tgggattagt tttaggtttg gtattgtttt gtgggttgag 180
tgtttatatt tgttaaattt atgtgggtat gtttttgtgg tgtattgttt ttagtt 236
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ, НАБОР И ПРИМЕНЕНИЕ ДЛЯ ВЫЯВЛЕНИЯ КОЛОРЕКТАЛЬНОГО РАКА | 2021 |
|
RU2836003C2 |
| ОБЪЕДИНЕННАЯ ОЧИСТКА И ИЗМЕРЕНИЕ МЕТИЛИРОВАНИЯ ДНК С СОВМЕСТНЫМ ИЗМЕРЕНИЕМ МУТАЦИЙ И/ИЛИ УРОВНЕЙ ЭКСПРЕССИИ мРНК В АВТОМАТИЧЕСКОМ РЕАКЦИОННОМ КАРТРИДЖЕ | 2017 |
|
RU2780660C2 |
| КОМБИНАЦИЯ ГЕННЫХ МАРКЕРОВ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2824399C1 |
| СПОСОБ АНАЛИЗА НАРУШЕНИЙ, СВЯЗАННЫХ С РАКОМ ЯИЧНИКОВ | 2008 |
|
RU2511408C2 |
| СПОСОБ АНАЛИЗА ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2008 |
|
RU2492243C2 |
| ОПУХОЛЕВЫЙ МАРКЕР, РЕАГЕНТ ДЛЯ ВЫЯВЛЕНИЯ МЕТИЛИРОВАНИЯ, НАБОР И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2770928C1 |
| БИОМАРКЕРЫ МЕТИЛИРОВАНИЯ ДНК ДЛЯ РАННЕГО ВЫЯВЛЕНИЯ РАКА ШЕЙКИ МАТКИ | 2020 |
|
RU2817569C2 |
| СПОСОБ IN VITRO ДИАГНОСТИКИ ИЛИ ПРОГНОЗИРОВАНИЯ КОЛОРЕКТАЛЬНОГО РАКА ИЛИ ЕГО ПРЕДРАКОВОЙ СТАДИИ | 2020 |
|
RU2831090C2 |
| РЕАГЕНТ ДЛЯ ВЫЯВЛЕНИЯ, НАБОР ДЛЯ ВЫЯВЛЕНИЯ И СПОСОБ ВЫЯВЛЕНИЯ МЕТИЛИРОВАНИЯ ГЕНА ITGA4 | 2017 |
|
RU2739071C1 |
| ОПУХОЛЕВЫЙ МАРКЕР, РЕАГЕНТ ДЛЯ ВЫЯВЛЕНИЯ МЕТИЛИРОВАНИЯ, НАБОР И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2775177C1 |
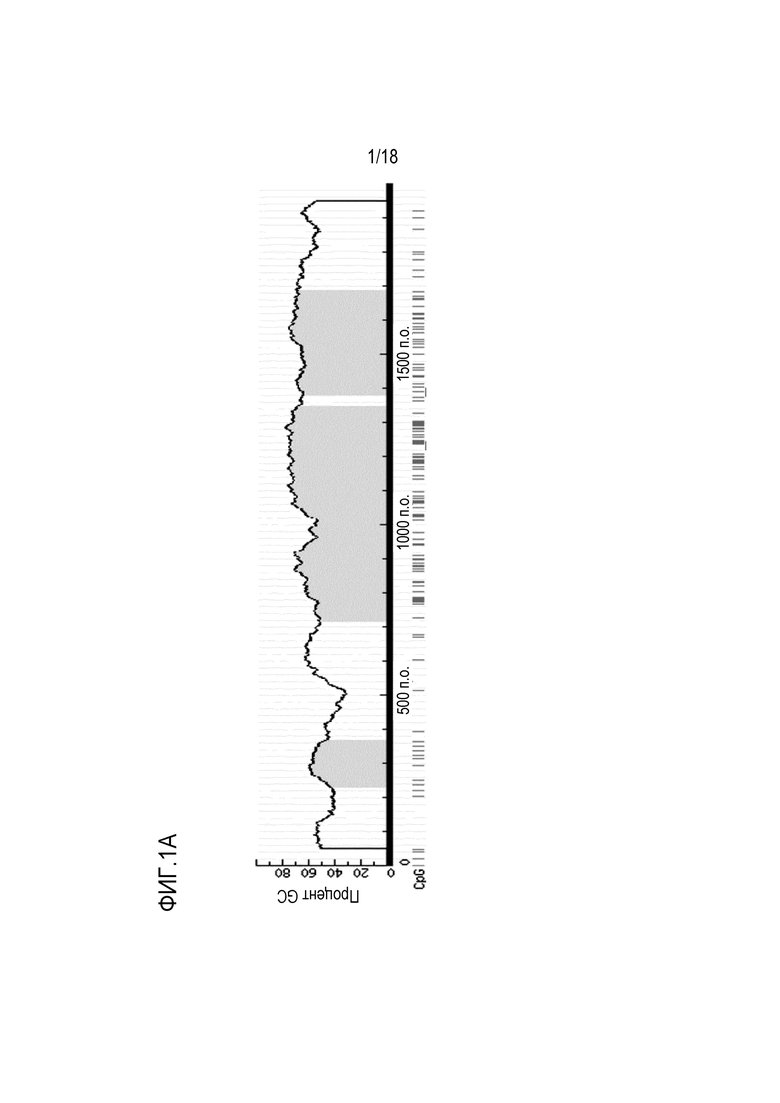
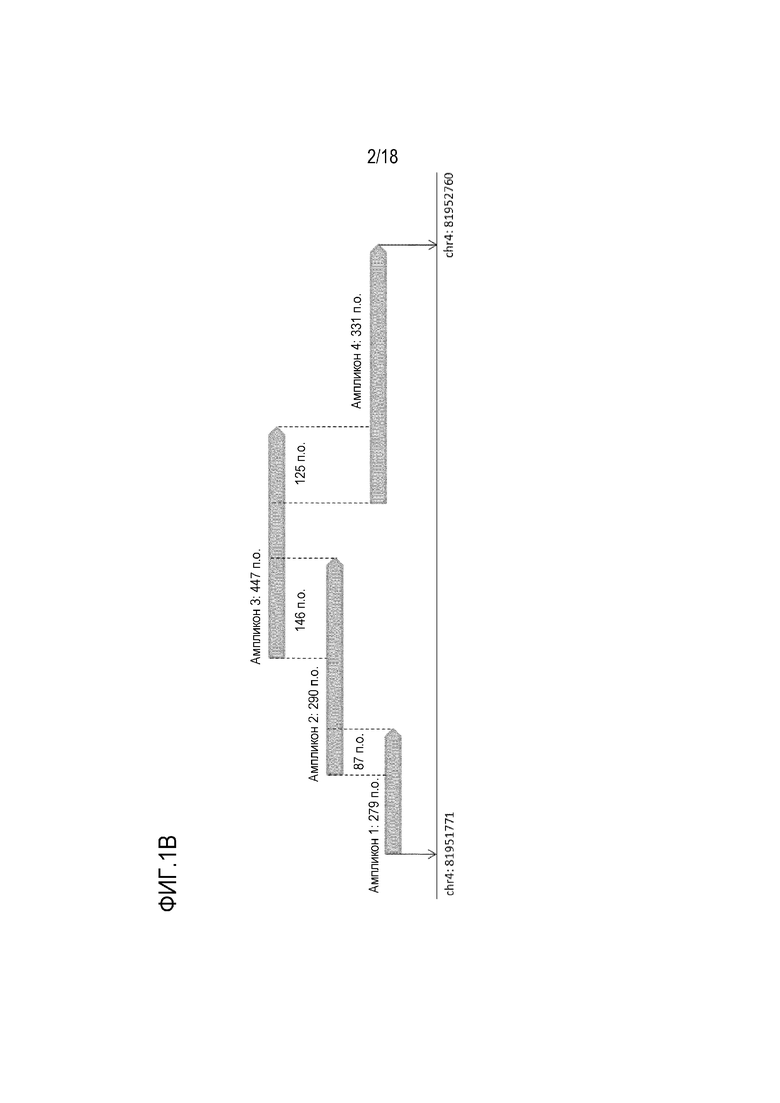
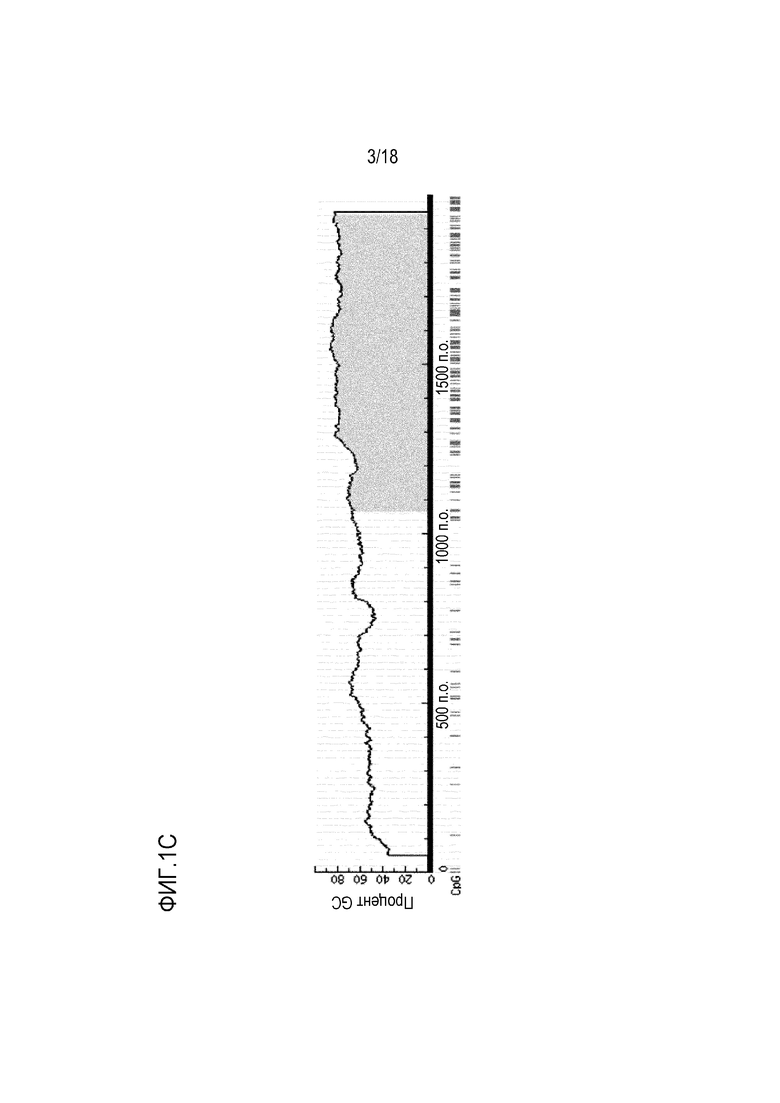
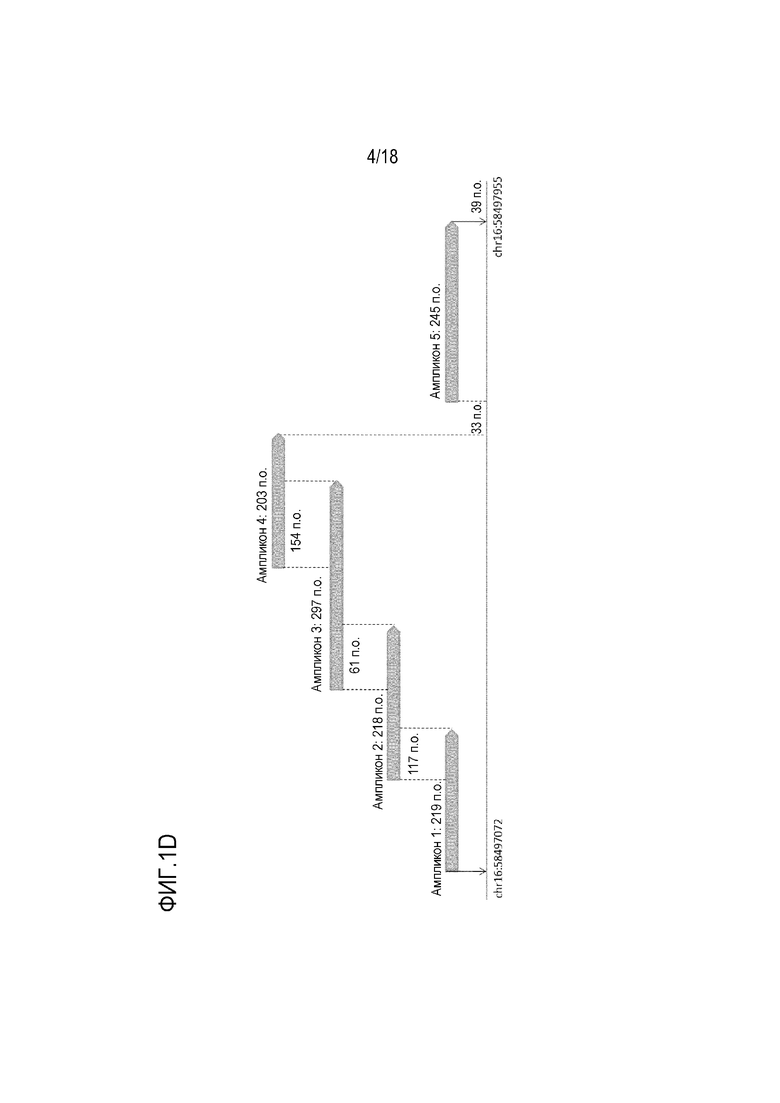
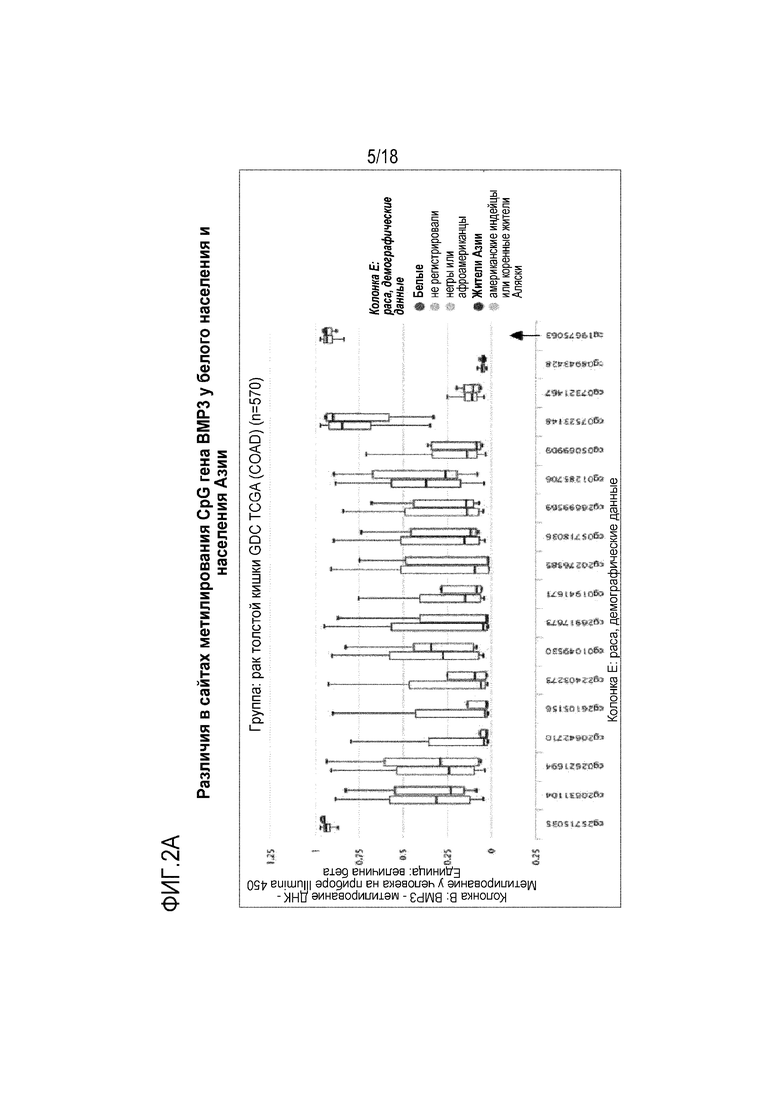
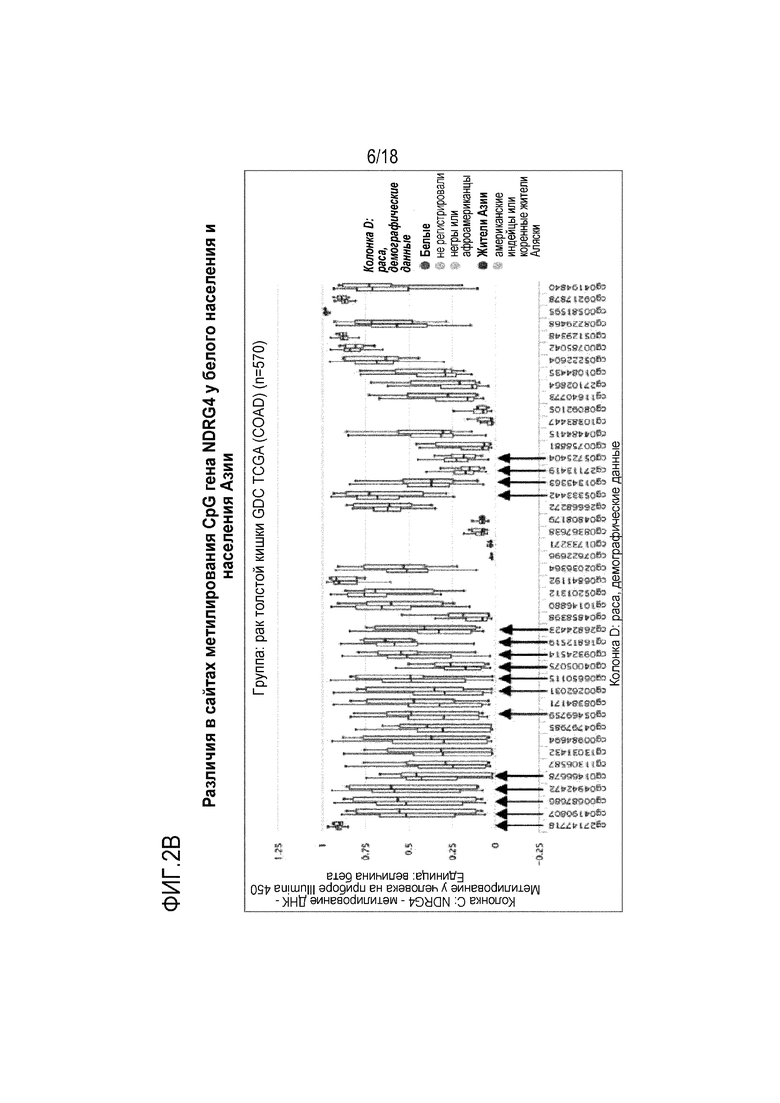
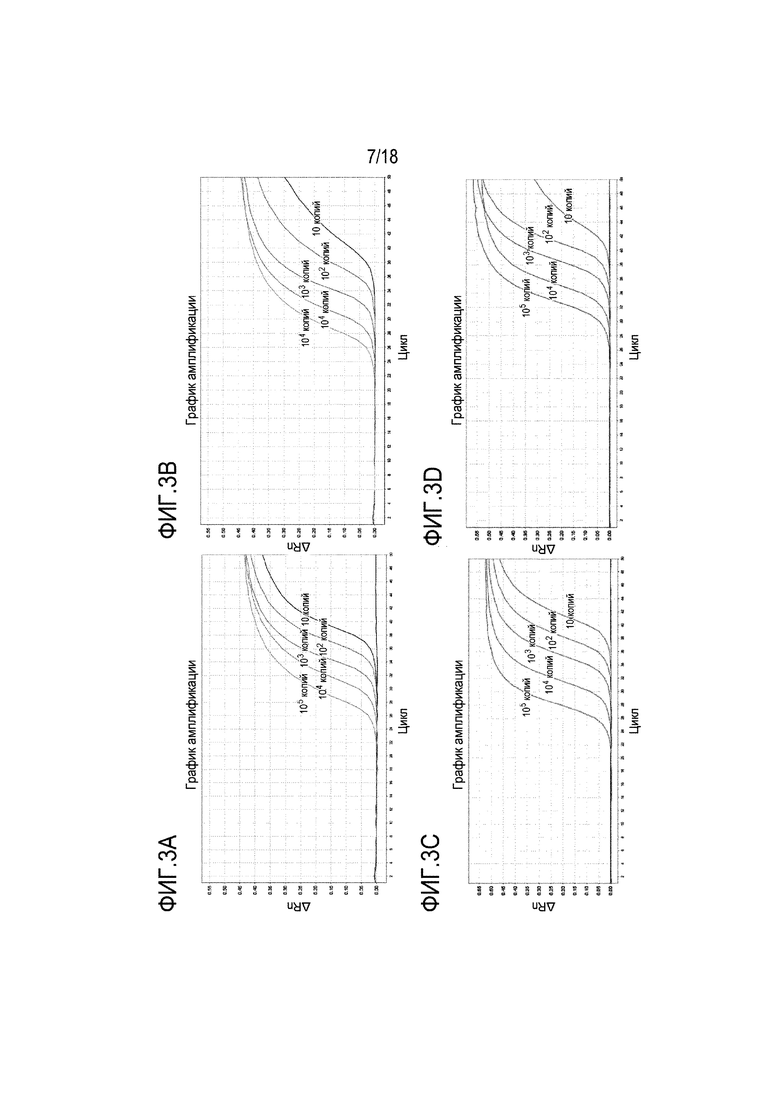
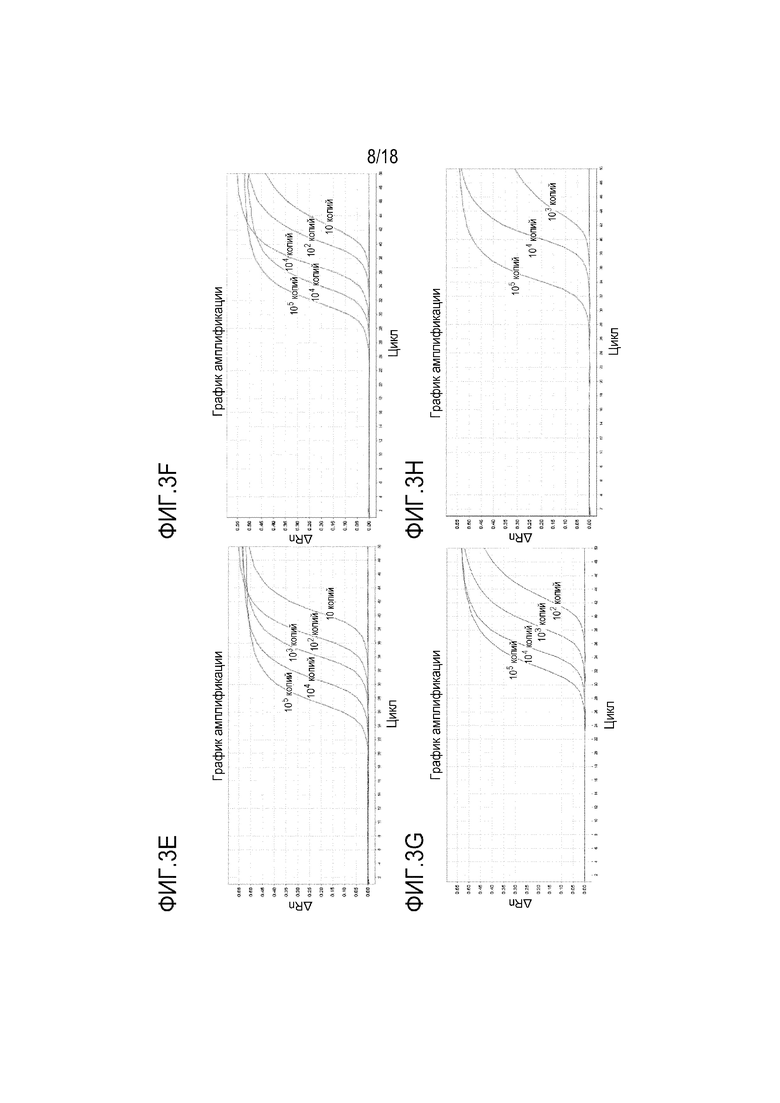
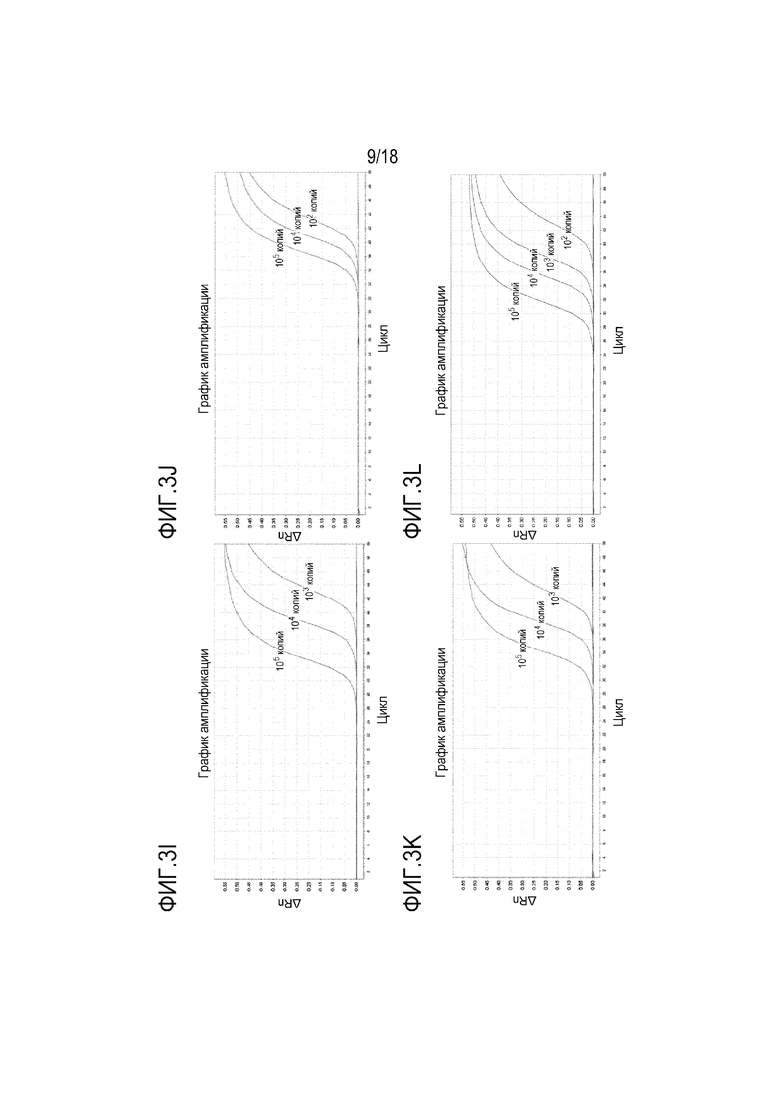
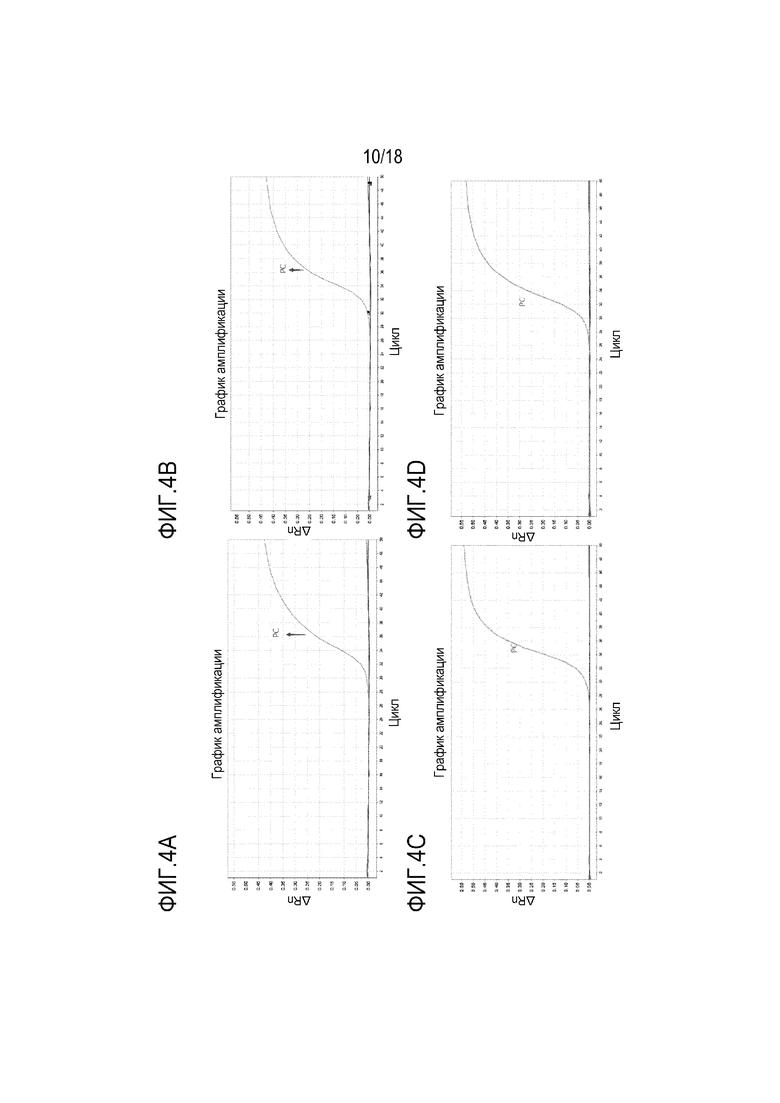
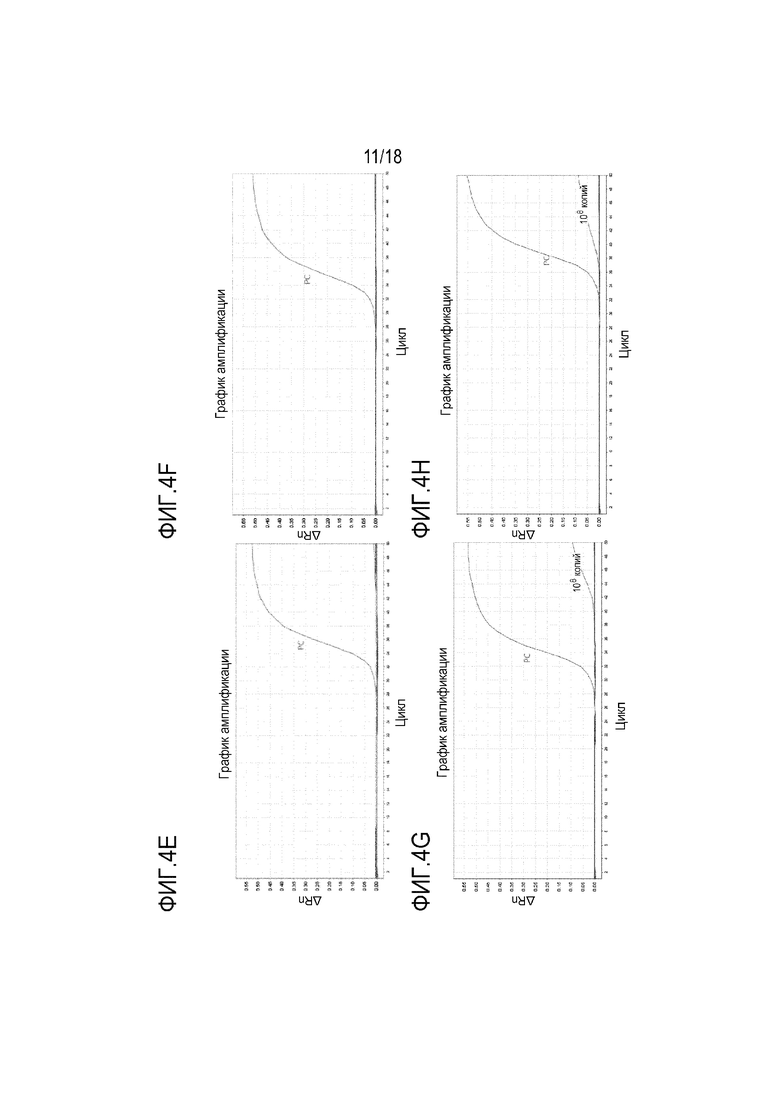
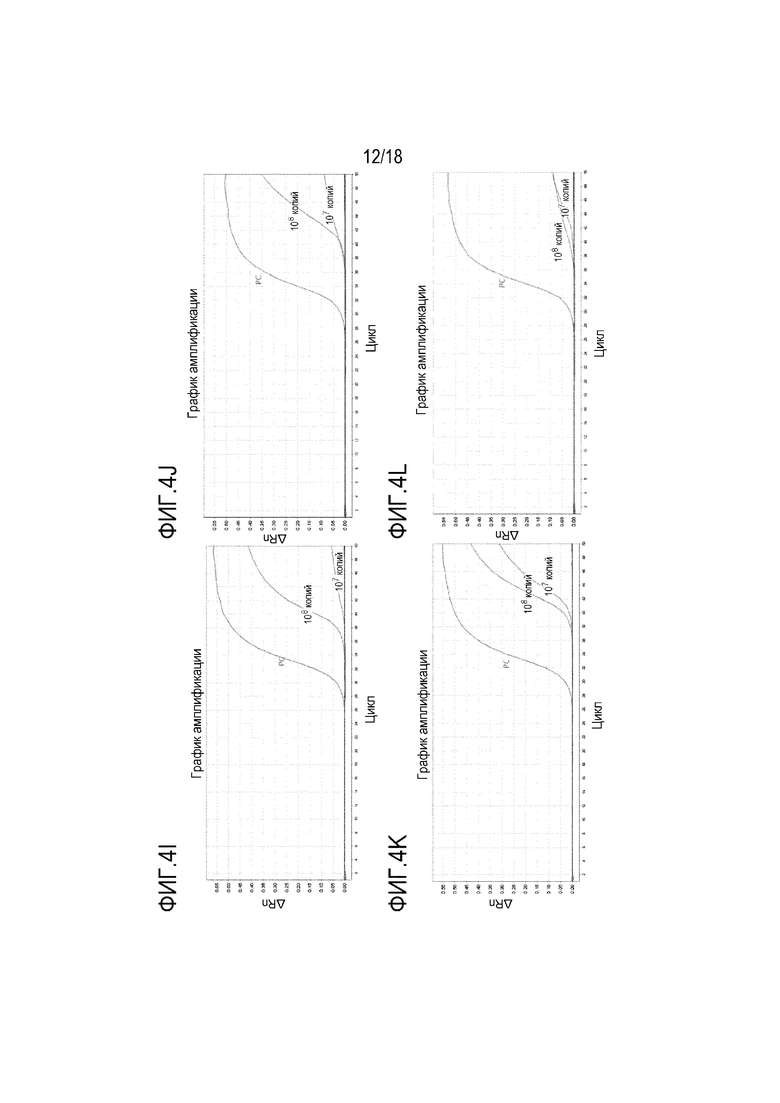
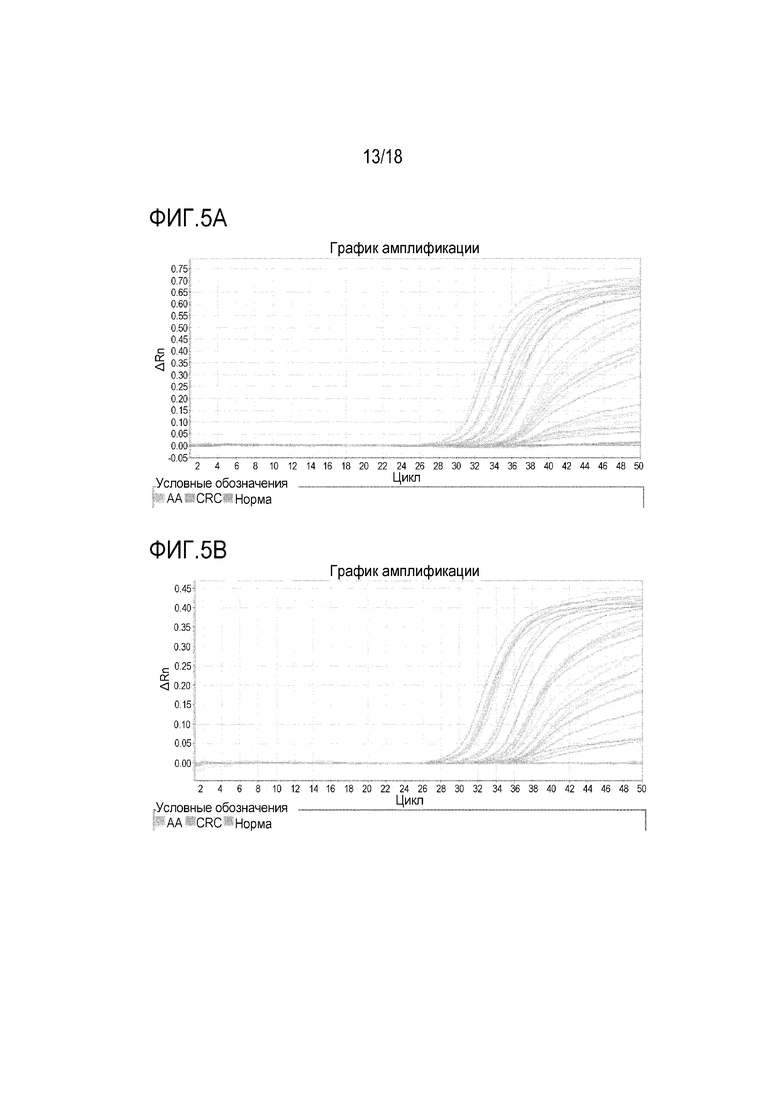
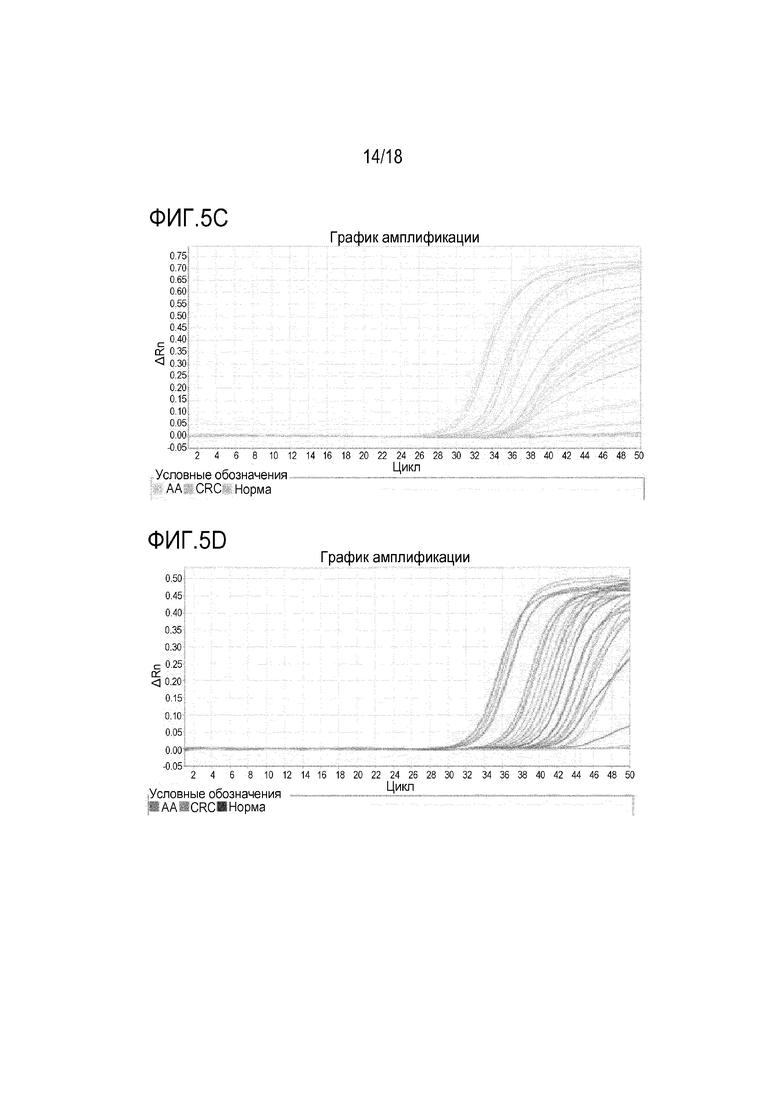
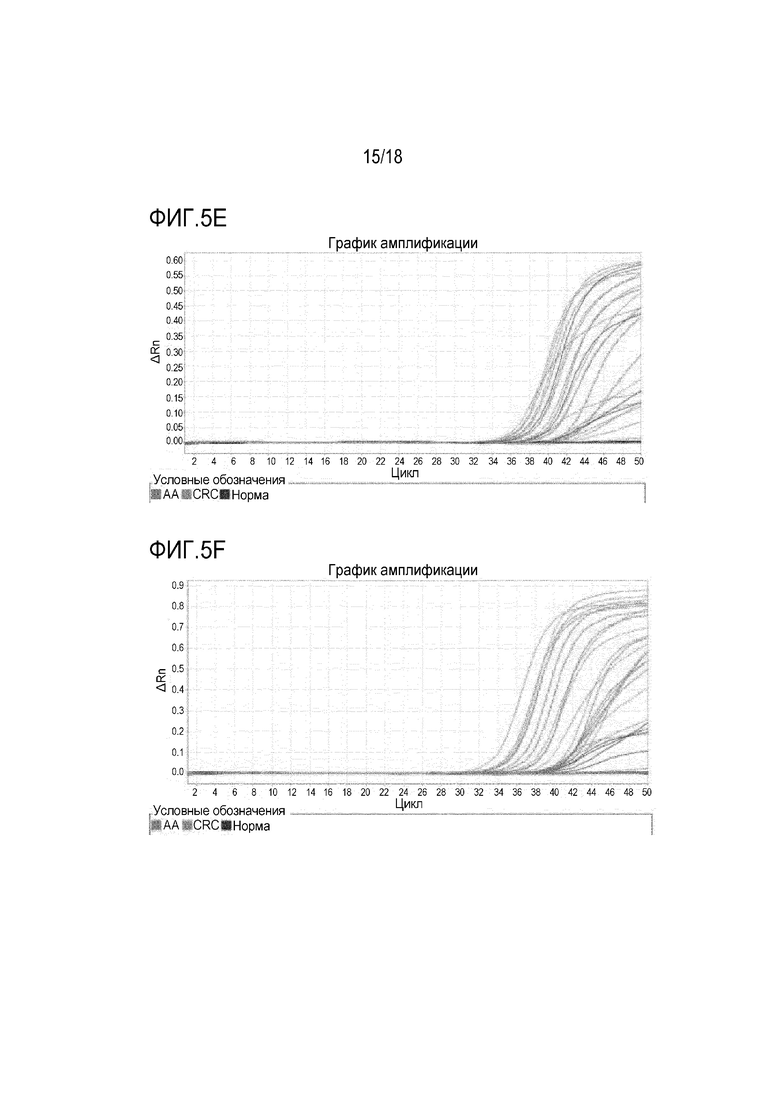
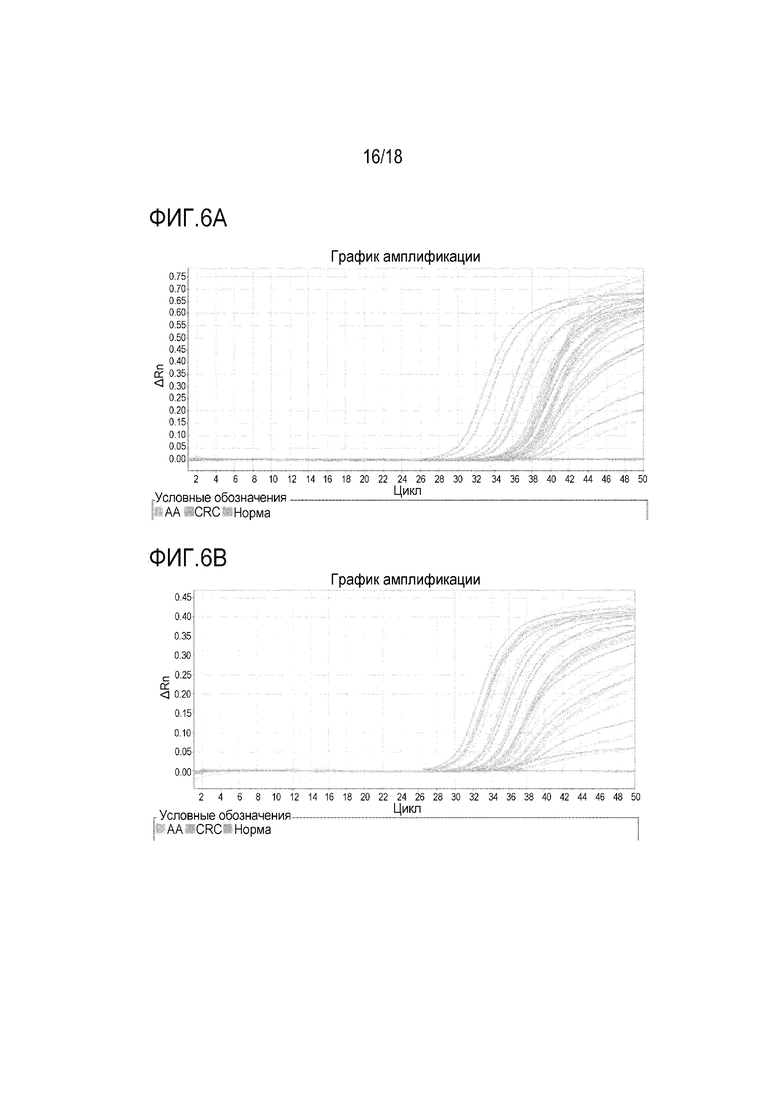
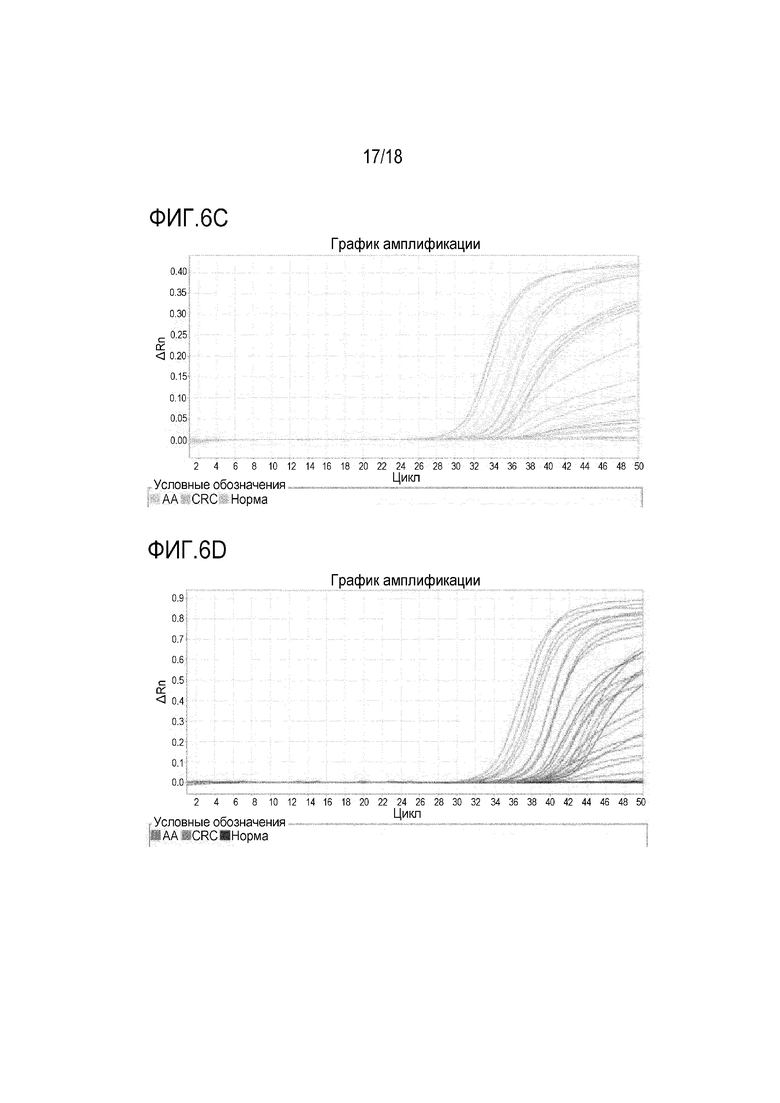
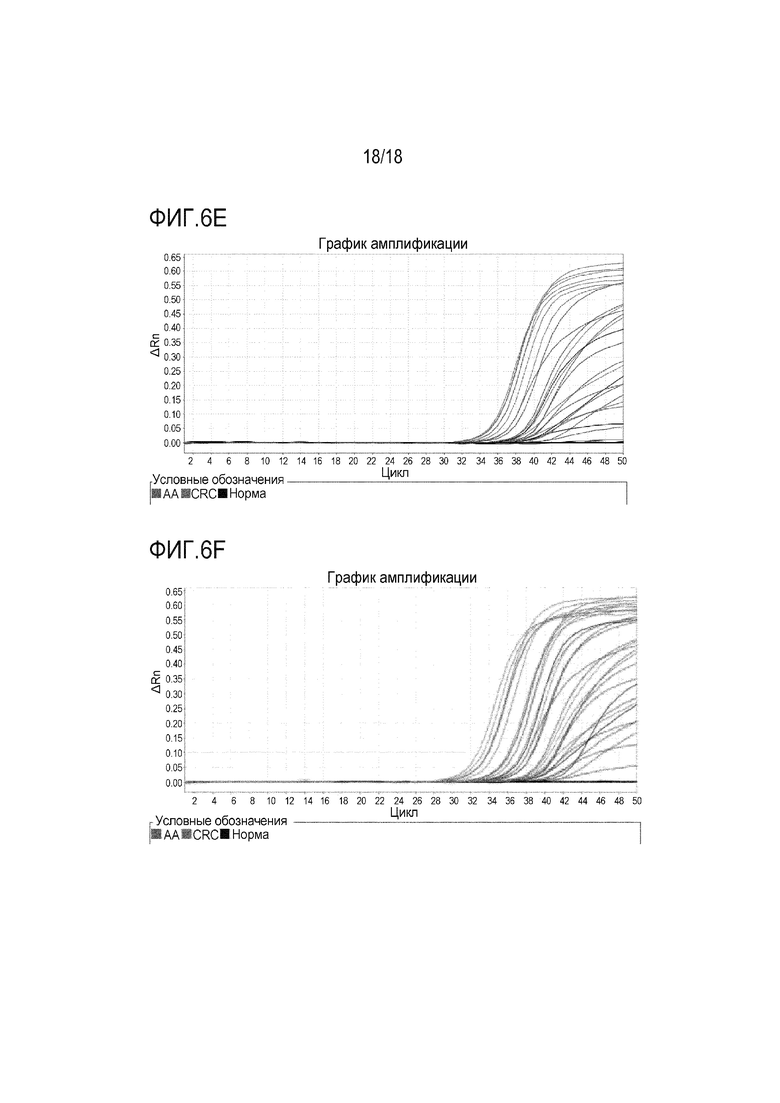
Настоящее изобретение относится к области молекулярной диагностики. Описаны комбинации праймеров и зондов для проведения количественных ПЦР, которые могут быть использованы для определения состояния и уровня метилирования генов BMP3 и NDRG4 у пациента, нуждающегося в этом, что обеспечивает удивительно высокую специфичность и чувствительность диагностики при определении наличия или отсутствия рака прямой и ободочной кишки (РПОК) и/или прогрессирующей аденомы (ПA) у пациента, нуждающегося в этом. Представлены также композиции и способы проведения диагностики. Технический результат заключается в том, что комбинации предпочтительных праймеров и зондов согласно изобретению обеспечивают неожиданно более высокую чувствительность и специфичность при обнаружении опухолевой ткани. 6 н. и 58 з.п. ф-лы, 42 ил., 24 табл., 5 пр.
1. Набор для обнаружения наличия или отсутствия рака прямой и ободочной кишки (РПОК) у пациента, нуждающегося в этом, где указанный набор содержит:
(а) первую пару праймеров и первый зонд для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, где каждый из первой пары праймеров и первого зонда включает непрерывную последовательность по меньшей мере из 16 нуклеотидов, которая идентична, комплементарна фрагменту последовательности SEQ ID NO. 1 или гибридизуется с этим фрагментом в жестких условиях гибридизации;
(b) вторую пару праймеров и второй зонд для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента, где каждый из второй пары праймеров и второго зонда включает непрерывную последовательность по меньшей мере из 16 нуклеотидов, которая идентична, комплементарна фрагменту последовательности SEQ ID NO. 2 или гибридизуется с этим фрагментом в жестких условиях гибридизации,
где первая пара праймеров и первый зонд выбраны из группы, состоящей из:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5;
ii) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11; и
iii) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17; или
где вторая пара праймеров и второй зонд выбраны из группы, состоящей из:
iv) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8;
v) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14; и
vi) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20.
2. Набор по п. 1, содержащий (а) первую пару праймеров и первый зонд; и (b) вторую пару праймеров и второй зонд.
3. Набор по п. 1, где указанный набор включает:
i) прямой праймер, содержащий SEQ ID NO: 3, обратный праймер, содержащий SEQ ID NO: 4, и зонд, содержащий SEQ ID NO: 5, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямой праймер, содержащий SEQ ID NO: 6, обратный праймер, содержащий SEQ ID NO: 7, и зонд, содержащий SEQ ID NO: 8, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
4. Набор по п. 1, где указанный набор включает:
i) прямой праймер, содержащий SEQ ID NO: 9, обратный праймер, содержащий SEQ ID NO: 10, и зонд, содержащий SEQ ID NO: 11, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямой праймер, содержащий SEQ ID NO: 12, обратный праймер, содержащий SEQ ID NO: 13, и зонд, содержащий SEQ ID NO: 14, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
5. Набор по п. 1, где указанный набор включает:
i) прямой праймер, содержащий SEQ ID NO: 15, обратный праймер, содержащий SEQ ID NO: 16, и зонд, содержащий SEQ ID NO: 17, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямой праймер, содержащий SEQ ID NO: 18, обратный праймер, содержащий SEQ ID NO: 19, и зонд, содержащий SEQ ID NO: 20, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
6. Набор по любому из пп. 1-5, где первый зонд и второй зонд содержат флуоресцентный донор и акцепторный флуорофор.
7. Набор по п. 6, где первый зонд и второй зонд представляют собой зонды TAQMAN®.
8. Набор по любому из пп. 1-7, где набор дополнительно включает:
(1) средство для детектирования присутствия или отсутствия по меньшей мере одной мутации в гене KRAS у пациента; и
(2) средство для детектирования наличия или отсутствия гемоглобина в биологическом образце, взятом у пациента.
9. Набор по п. 8, где средство для детектирования присутствия или отсутствия по меньшей мере одной мутации в гене KRAS у пациента включает по меньшей мере одну пару праймеров, способных амплифицировать область экзона 12 и/или экзона 13 гена KRAS в полимеразной цепной реакции (ПЦР).
10. Набор по п. 8, где средство для детектирования присутствия или отсутствия гемоглобина в биологическом образце включает антитело против гемоглобина.
11. Набор по п.9, где праймеры способны амплифицировать область гена KRAS, содержащую по меньшей мере одну мутацию KRAS, выбранную из группы, состоящей из G12D, G12V, G12C, G13D, G12A, G12R, G12S и G13C.
12. Набор по п. 10, в котором антитело представляет собой антитело, конъюгированное с коллоидным золотом.
13. Набор по любому из пп. 1-12, где набор дополнительно включает средство для амплификации контрольного гена для количественной оценки.
14. Набор по любому из пп. 1-12, где набор дополнительно содержит инструкции по применению и/или интерпретации результата теста, полученного с использованием набора.
15. Набор по п. 10, где набор дополнительно включает средство для детектирования комплекса, образованного антителом и гемоглобином в биологическом образце.
16. Набор по любому из пп. 1-15, в котором биологический образец, взятый у пациента, представляет собой пробу кала.
17. Набор по любому из пп. 1-16, где набор дополнительно включает бисульфитный реагент и контейнер, подходящий для смешивания бисульфитного реагента и биологического образца пациента или полинуклеотидов, полученных из биологического образца.
18. Набор по любому из пп. 1-17, где набор дополнительно включает рестриктирующий фермент-реагент, чувствительный к метилированию.
19. Набор по любому из пп. 1-18, где набор дополнительно включает:
(1) позитивный стандарт и негативный стандарт для детектирования метилирования BMP3 в биологическом образце, и
(2) позитивный стандарт и негативный стандарт для детектирования метилирования NDRG4 в биологическом образце.
20. Набор по п.19, в котором:
позитивный стандарт для обнаружения метилирования BMP3 включает полинуклеотидную последовательность
GTTAGTTTGGTCGGGTGTTTTTAAAAATAAAGCGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTCGGGTTATATACGTCGCGATTTATAGTTTTTTTTTAGCGTTGGAGTGGAGACGGCGTTCGTAGCGTTTTGCGCGGGTGAGGTTCGCGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGCGTTGGGTTAGCGTAGTAAGTGGGGTTGGTCGTTATTTCGTTGTATTCGGTCGCGTTTCGGGTTTCGTGCGTTTTCGTTTTAG (SEQ ID NO: 67);
негативный стандарт для детектирования метилирования BMP3 включает полинуклеотидную последовательность
GTTAGTTTGGTTGGGTGTTTTTAAAAATAAAGTGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTTGGGTTATATATGTTGTGATTTATAGTTTTTTTTTAGTGTTGGAGTGGAGATGGTGTTTGTAGTGTTTTGTGTGGGTGAGGTTTGTGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGTGTTGGGTTAGTGTAGTAAGTGGGGTTGGTTGTTATTTTGTTGTATTTGGTTGTGTTTTGGGTTTTGTGTGTTTTTGTTTTAG (SEQ ID NO: 68);
позитивный стандарт для детектирования метилирования NDRG4 включает полинуклеотидную последовательность
TGAGAAGTCGGCGGGGGCGCGGATCGATCGGGGTGTTTTTTAGGTTTCGCGTCGCGGTTTTCGTTCGTTTTTTCGTTCGTTTATCGGGTATTTTAGTCGCGTAGAAGGCGGAAGTTACGCGCGAGGGATCGCGGTTCGTTCGGGATTAGTTTTAGGTTCGGTATCGTTTCGCGGGTCGAGCGTTTATATTCGTTAAATTTACGCGGGTACGTTTTCGCGGCGTATCGTTTTTAGTT (SEQ ID NO.: 69); и
негативный стандарт для детектирования метилирования NDRG4 включает полинуклеотидную последовательность
TGAGAAGTTGGTGGGGGTGTGGATTGATTGGGGTGTTTTTTAGGTTTTGTGTTGTGGTTTTTGTTTGTTTTTTTGTTTGTTTATTGGGTATTTTAGTTGTGTAGAAGGTGGAAGTTATGTGTGAGGGATTGTGGTTTGTTTGGGATTAGTTTTAGGTTTGGTATTGTTTTGTGGGTTGAGTGTTTATATTTGTTAAATTTATGTGGGTATGTTTTTGTGGTGTATTGTTTTTAGTT (SEQ ID NO.: 70).
21. Набор по п. 13, где средство для амплификации гена внутреннего контроля содержит праймеры для амплификации гена позитивного контроля и/или гена негативного контроля.
22. Способ определения наличия или отсутствия рака прямой и ободочной кишки (РПОК) у пациента, нуждающегося в этом, где указанный способ включает:
а) получение геномной ДНК из биологического образца пациента;
b) обработку геномной ДНК (а) или ее фрагмента одним или несколькими реагентами для превращения цитозиновых оснований, которые не являются метилированными, в урацил или другое основание, которое заметно отличается от цитозина с точки зрения свойств гибридизации;
c) контактирование обработанной геномной ДНК или ее обработанного фрагмента с первой парой праймеров для детектирования присутствия или отсутствия сайтов метилирования гена, кодирующего белок морфогенеза кости 3 (BMP3) у пациента, и со второй парой праймеров для детектирования у пациента присутствия или отсутствия сайтов метилирования гена, кодирующего белок члена 4 семейства NDRG (NDRG4), где первая пара праймеров включает непрерывную последовательность по меньшей мере из 9 нуклеотидов, которая идентична, комплементарна фрагменту SEQ ID NO: 1 или гибридизуется с ним в жестких условиях гибридизации, и где вторая пара праймеров содержит непрерывную последовательность по меньшей мере из 9 нуклеотидов, которая комплементарна фрагменту SEQ ID NO: 2 или гибридизуется с ним в жестких условиях гибридизации, где обработанная геномная ДНК или ее фрагмент были либо амплифицированы для получения по меньшей мере одного амплификата с использованием первой пары праймеров или второй пары праймеров, либо не были амплифицированы; и
d) определение наличия или отсутствия РПОК у пациента исходя из присутствия или отсутствия указанного амплификата, состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 и гена NDRG4 у пациента, с использованием первого зонда для выявления присутствия или отсутствия сайтов метилирования гена BMP3 и второго зонда для выявления присутствия или отсутствия сайтов метилирования гена NDRG4,
где первая пара праймеров и первый зонд выбраны из группы, состоящей из:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5;
ii) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11; и
iii) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17; или
где вторая пара праймеров и второй зонд выбраны из группы, состоящей из:
iv) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8;
v) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14; и
vi) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20.
23. Способ по п. 22, содержащий применение (а) первой пары праймеров и первого зонда и (b) второй пары праймеров и второго зонда.
24. Способ по п.22, который включает применение:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
25. Способ по п.22, который включает применение:
i) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
26. Способ по п. 22, который включает применение:
i) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в биологическом образце, взятом у пациента, и
ii) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в биологическом образце, взятом у пациента.
27. Способ по любому из пп. 22-26, в котором первый зонд и второй зонд содержат флуоресцентный донор и акцепторный флуорофор.
28. Способ по любому из пп. 22-26, в котором первый зонд и второй зонд представляют собой зонды TAQMAN®.
29. Способ по любому из пп. 22-28, где указанный способ дополнительно включает стадию детектирования присутствия или отсутствия по меньшей мере одной мутации в гене KRAS в биологическом образце, взятом у пациента, и стадию детектирования присутствия или отсутствия гемоглобина в биологическом образце, взятом у пациента.
30. Способ по п. 29, где стадия детектирования присутствия или отсутствия по меньшей мере одной мутации в гене KRAS у пациента включает применение по меньшей мере одной пары праймеров, способных амплифицировать область экзона 12 и/или экзона 13 гена KRAS в полимеразной цепной реакции (ПЦР).
31. Способ по п. 29, где стадия детектирования присутствия или отсутствия гемоглобина в биологическом образце включает использование антитела против гемоглобина.
32. Способ по п. 30, где праймеры способны амплифицировать область гена KRAS, содержащую по меньшей мере одну мутацию KRAS, выбранную из группы, состоящей из G12D, G12V, G12C, G13D, G12A, G12R, G12S и G13C.
33. Способ по п. 31, где антитело представляет собой антитело, конъюгированное с коллоидным золотом.
34. Способ по любому из пп. 22-33, где амплификацию гена BMP3 осуществляют с помощью количественной ПЦР (кол.ПЦР), и этот способ дополнительно включает амплификацию первого контрольного гена для определения значения Ct амплификации BMP3 как ∆Ct1.
35. Способ по любому из пп. 22-33, где амплификацию гена NDRG4 осуществляют с помощью количественной ПЦР (кол.ПЦР), и этот способ дополнительно включает амплификацию второго контрольного гена для определения значения Ct амплификации NDRG4 как ΔCt2.
36. Способ по любому из пп. 30-33, где амплификацию мутантного гена KRAS осуществляют с помощью количественной ПЦР (кол.ПЦР), и этот способ дополнительно включает амплификацию третьего контрольного гена для определения значения Ct амплификации мутантного KRAS как ∆Ct3.
37. Способ по п. 34 или 35, где первый и второй контрольные гены являются одинаковыми.
38. Способ по п. 37, где тот же самый контрольный ген является геном B2M.
39. Способ по п. 36, где мутантный ген KRAS содержит мутацию, выбранную из группы, состоящей из G12D, G13D, G12V, G12C, G12S, G12A и G13R.
40. Способ по п. 39, где мутантный ген KRAS амплифицируют с использованием одной или более пар праймеров, выбранных из группы, состоящей из:
(1) прямого праймера G12D-F, содержащего SEQ ID NO: 35, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(2) прямого праймера G13D-F, содержащего SEQ ID NO: 36, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(3) прямого праймера G12V-F, содержащего SEQ ID NO: 37, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(4) прямого праймера G12C-F, содержащего SEQ ID NO: 38, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(5) прямого праймера G12S-F, содержащего SEQ ID NO: 39, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(6) прямого праймера G12A-F, содержащего SEQ ID NO: 40, и обратного праймера Kras-R, содержащего SEQ ID NO: 42; и
(7) прямого праймера G12R-F, содержащего SEQ ID NO: 41, и обратного праймера Kras-R, содержащего SEQ ID NO: 42,
и где зонд KRAS для кол.ПЦР содержит SEQ ID NO: 45.
41. Способ по п. 36, где третий контрольный ген представляет собой ген ACTB.
42. Способ по п. 41, где праймеры для кол.ПЦР для амплификации гена ACTB содержат SEQ ID NO: 43 и 44, а зонд содержит SEQ ID NO: 46.
43. Способ по любому из пп. 22-42, где указанный способ включает применение:
(1) позитивного стандарта и негативного стандарта для детектирования метилирования BMP3 в образце, и
(2) позитивного стандарта и негативного стандарта для детектирования метилирования NDRG4 в образце.
44. Способ по п. 43, где
позитивный стандарт для детектирования метилирования BMP3 включает полинуклеотидную последовательность
GTTAGTTTGGTCGGGTGTTTTTAAAAATAAAGCGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTCGGGTTATATACGTCGCGATTTATAGTTTTTTTTTAGCGTTGGAGTGGAGACGGCGTTCGTAGCGTTTTGCGCGGGTGAGGTTCGCGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGCGTTGGGTTAGCGTAGTAAGTGGGGTTGGTCGTTATTTCGTTGTATTCGGTCGCGTTTCGGGTTTCGTGCGTTTTCGTTTTAG (SEQ ID NO: 67);
негативный стандарт для детектирования метилирования BMP3 включает полинуклеотидную последовательность
GTTAGTTTGGTTGGGTGTTTTTAAAAATAAAGTGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTTGGGTTATATATGTTGTGATTTATAGTTTTTTTTTAGTGTTGGAGTGGAGATGGTGTTTGTAGTGTTTTGTGTGGGTGAGGTTTGTGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGTGTTGGGTTAGTGTAGTAAGTGGGGTTGGTTGTTATTTTGTTGTATTTGGTTGTGTTTTGGGTTTTGTGTGTTTTTGTTTTAG (SEQ ID NO: 68);
позитивный стандарт для детектирования метилирования NDRG4 включает полинуклеотидную последовательность
TGAGAAGTCGGCGGGGGCGCGGATCGATCGGGGTGTTTTTTAGGTTTCGCGTCGCGGTTTTCGTTCGTTTTTTCGTTCGTTTATCGGGTATTTTAGTCGCGTAGAAGGCGGAAGTTACGCGCGAGGGATCGCGGTTCGTTCGGGATTAGTTTTAGGTTCGGTATCGTTTCGCGGGTCGAGCGTTTATATTCGTTAAATTTACGCGGGTACGTTTTCGCGGCGTATCGTTTTTAGTT (SEQ ID NO.: 69); и
негативный стандарт для детектирования метилирования NDRG4 включает полинуклеотидную последовательность
TGAGAAGTTGGTGGGGGTGTGGATTGATTGGGGTGTTTTTTAGGTTTTGTGTTGTGGTTTTTGTTTGTTTTTTTGTTTGTTTATTGGGTATTTTAGTTGTGTAGAAGGTGGAAGTTATGTGTGAGGGATTGTGGTTTGTTTGGGATTAGTTTTAGGTTTGGTATTGTTTTGTGGGTTGAGTGTTTATATTTGTTAAATTTATGTGGGTATGTTTTTGTGGTGTATTGTTTTTAGTT (SEQ ID NO.: 70).
45. Способ по любому из пп. 22-44, где способ включает амплификацию стандарта контроля качества.
46. Способ обнаружения наличия или отсутствия рака прямой и ободочной кишки (РПОК) у пациента, нуждающегося в этом, где указанный способ включает использование набора по любому из пп. 1-21.
47. Способ обнаружения наличия или отсутствия рака прямой и ободочной кишки (РПОК) у пациента, нуждающегося в этом, где указанный способ включает:
а) получение необработанной геномной ДНК из пробы кала пациента;
b) обработку геномной ДНК (а) или ее фрагмента одним или более реагентами для превращения цитозиновых оснований, которые являются неметилированнными, в урацил или другое основание, которое заметно отличается от цитозина с точки зрения свойств гибридизации;
c) проведение количественной ПЦР (кол.ПЦР) с использованием обработанной геномной ДНК (b) в качестве матрицы и определение значения Ct гена BMP3, вычитаемое из значения первого контрольного гена у пациента как ΔCt1;
d) проведение кол.ПЦР с использованием обработанной геномной ДНК (b) в качестве матрицы и определение значения Ct гена NDRG4, вычитаемое из значения первого контрольного гена у пациента как ΔCt2;
e) проведение кол.ПЦР с использованием необработанной геномной ДНК в качестве матрицы и определение значения Ct мутантного гена KRAS, вычитаемое из значения второго контрольного гена у пациента как ∆Ct3;
f) проведение иммунохимического анализа кала на белок гемоглобин в пробе кала и оценку результата как FIT;
g) определение значения K, где K=a*ΔCt1+b*ΔCt2+c*ΔCt3+d*FIT+X, где a, b, c, d, X представляют собой клинические константы; и
h) определение значения общего индекса P, где Р=eK/(1+eK), где e представляет собой натуральную константу, при этом, если P равно или больше заданного порога, то у пациента диагностируют РПОК, а если P меньше этого порога, то считается, что у пациента отсутствует РПОК,
где кол.ПЦР для амплификации гена BMP3 включает первую пару праймеров и первый зонд, выбранные из группы, состоящей из:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5;
ii) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11; и
iii) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17; или
где кол.ПЦР для амплификации гена NDRG4 включает вторую пару праймеров и второй зонд, выбранные из группы, состоящей из:
iv) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8;
v) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14; и
vi) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20.
48. Способ по п. 47, где кол.ПЦР для амплификации гена BMP3 включает первую пару праймеров и первый зонд, и где кол.ПЦР для амплификации гена NDRG4 включает вторую пару праймеров и второй зонд.
49. Способ по п. 47, где способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 3, обратного праймера, содержащего SEQ ID NO: 4, и зонда, содержащего SEQ ID NO: 5, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в образце, и
ii) прямого праймера, содержащего SEQ ID NO: 6, обратного праймера, содержащего SEQ ID NO: 7, и зонда, содержащего SEQ ID NO: 8, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в образце.
50. Способ по п. 47, где способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 9, обратного праймера, содержащего SEQ ID NO: 10, и зонда, содержащего SEQ ID NO: 11, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в образце, и
ii) прямого праймера, содержащего SEQ ID NO: 12, обратного праймера, содержащего SEQ ID NO: 13, и зонда, содержащего SEQ ID NO: 14, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в образце.
51. Способ по п. 47, где указанный способ включает применение:
i) прямого праймера, содержащего SEQ ID NO: 15, обратного праймера, содержащего SEQ ID NO: 16, и зонда, содержащего SEQ ID NO: 17, для детектирования состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена BMP3 в образце, и
ii) прямого праймера, содержащего SEQ ID NO: 18, обратного праймера, содержащего SEQ ID NO: 19, и зонда, содержащего SEQ ID NO: 20, для определения состояния или уровня метилирования по меньшей мере одного динуклеотида CpG гена NDRG4 в образце.
52. Способ по любому из пп. 47-51, где первый зонд и второй зонд содержат флуоресцентный донор и акцепторный флуорофор.
53. Способ по любому из пп. 47-52, где первый зонд и второй зонд представляют собой зонды TAQMAN®.
54. Способ по любому из пп. 47-53, где мутантный ген KRAS содержит по меньшей мере одну мутацию KRAS, выбранную из группы, состоящей из G12D, G12V, G12C, G13D, G12A, G12R, G12S и G13C.
55. Способ по любому из пп. 47-54, в котором иммунохимический анализ кала включает антитело, конъюгированное с коллоидным золотом.
56. Способ по любому из пп. 47-55, в котором стадия с) и стадия d) включают использование гена B2M в качестве первого контрольного гена.
57. Способ по п. 54, где мутантный ген KRAS амплифицируют с использованием одной или более пар праймеров, выбранных из группы, состоящей из:
(1) прямого праймера G12D-F, содержащего SEQ ID NO: 35, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(2) прямого праймера G13D-F, содержащего SEQ ID NO: 36, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(3) прямого праймера G12V-F, содержащего SEQ ID NO: 37, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(4) прямого праймера G12C-F, содержащего SEQ ID NO: 38, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(5) прямого праймера G12S-F, содержащего SEQ ID NO: 39, и обратного праймера Kras-R, содержащего SEQ ID NO: 42;
(6) прямого праймера G12A-F, содержащего SEQ ID NO: 40, и обратного праймера Kras-R, содержащего SEQ ID NO: 42; и
(7) прямого праймера G12R-F, содержащего SEQ ID NO: 41, и обратного праймера Kras-R, содержащего SEQ ID NO: 42,
и где амплифицированный продукт кол.ПЦР мутантного гена KRAS обнаруживают зондом KRAS, содержащим SEQ ID NO: 45.
58. Способ по п. 57, где ген ACTB используют в качестве второго контрольного гена в кол.ПЦР для амплификации мутантного гена KRAS.
59. Способ по п.58, где праймеры для кол.ПЦР для амплификации гена ACTB содержат SEQ ID NO: 43 и 44, а зонд для кол.ПЦР гена ACTB содержит SEQ ID NO: 46.
60. Способ по пп. 47-59, где способ включает применение:
(1) позитивного стандарта и негативного стандарта для детектирования метилирования BMP3 в образце, и
(2) позитивного стандарта и негативного стандарта для детектирования метилирования NDRG4 в образце.
61. Способ по п. 60, где
позитивный стандарт для детектирования метилирования BMP3 включает полинуклеотидную последовательность
GTTAGTTTGGTCGGGTGTTTTTAAAAATAAAGCGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTCGGGTTATATACGTCGCGATTTATAGTTTTTTTTTAGCGTTGGAGTGGAGACGGCGTTCGTAGCGTTTTGCGCGGGTGAGGTTCGCGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGCGTTGGGTTAGCGTAGTAAGTGGGGTTGGTCGTTATTTCGTTGTATTCGGTCGCGTTTCGGGTTTCGTGCGTTTTCGTTTTAG (SEQ ID NO: 67);
негативный стандарт для детектирования метилирования BMP3 включает полинуклеотидную последовательность
GTTAGTTTGGTTGGGTGTTTTTAAAAATAAAGTGAGGAGGGAAGGTATAGATAGATTTTGAAAATATTTGGGTTATATATGTTGTGATTTATAGTTTTTTTTTAGTGTTGGAGTGGAGATGGTGTTTGTAGTGTTTTGTGTGGGTGAGGTTTGTGTAGTTGTTGGGGAAGAGTTTATTTGTTAGGTTGTGTTGGGTTAGTGTAGTAAGTGGGGTTGGTTGTTATTTTGTTGTATTTGGTTGTGTTTTGGGTTTTGTGTGTTTTTGTTTTAG (SEQ ID NO: 68);
позитивный стандарт для детектирования метилирования NDRG4 включает полинуклеотидную последовательность
TGAGAAGTCGGCGGGGGCGCGGATCGATCGGGGTGTTTTTTAGGTTTCGCGTCGCGGTTTTCGTTCGTTTTTTCGTTCGTTTATCGGGTATTTTAGTCGCGTAGAAGGCGGAAGTTACGCGCGAGGGATCGCGGTTCGTTCGGGATTAGTTTTAGGTTCGGTATCGTTTCGCGGGTCGAGCGTTTATATTCGTTAAATTTACGCGGGTACGTTTTCGCGGCGTATCGTTTTTAGTT (SEQ ID NO.: 69); и
негативный стандарт для детектирования метилирования NDRG4 включает полинуклеотидную последовательность
TGAGAAGTTGGTGGGGGTGTGGATTGATTGGGGTGTTTTTTAGGTTTTGTGTTGTGGTTTTTGTTTGTTTTTTTGTTTGTTTATTGGGTATTTTAGTTGTGTAGAAGGTGGAAGTTATGTGTGAGGGATTGTGGTTTGTTTGGGATTAGTTTTAGGTTTGGTATTGTTTTGTGGGTTGAGTGTTTATATTTGTTAAATTTATGTGGGTATGTTTTTGTGGTGTATTGTTTTTAGTT (SEQ ID NO: 70).
62. Способ по любому из пп. 47-61, где способ включает амплификацию стандарта контроля качества в стадии c) и в стадии d).
63. Способ лечения рака прямой и ободочной кишки (РПОК) у пациента, нуждающегося в этом, где указанный способ включает определение наличия или отсутствия РПОК у пациента с использованием набора по любому из пп. 1-21, и лечение пациента в зависимости от наличия или отсутствия у него РПОК.
64. Способ лечения рака прямой и ободочной кишки (РПОК) у пациента, нуждающегося в этом, где указанный способ включает определение наличия или отсутствия РПОК у пациента с применением способа по любому из пп. 22-62, и лечение пациента в зависимости от наличия или отсутствия у него РПОК.
| US2011136687 A1 09.06.2011 | |||
| US2012107807 A1 03.05.2012 | |||
| US2015072866 A1 12.03.2015 | |||
| RU 2015111627 A 20.10.2016. |
Авторы
Даты
2024-01-22—Публикация
2019-05-23—Подача