Изобретение относится к области органической химии, к синтезу гетероциклических соединений, а именно производных (E)-2-(3-(1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-диона общей формулы I:
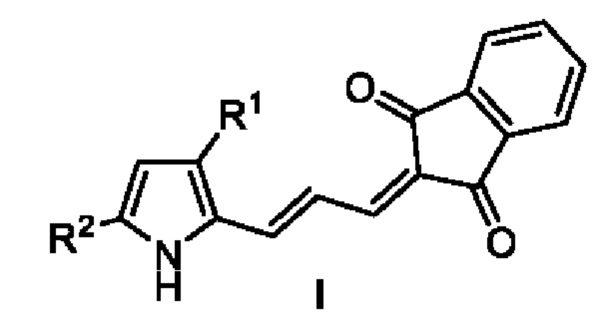

обладающих высокими показателями молярного коэффициента поглощения электромагнитного излучения в зеленой части видимого диапазона, а также небольшим значением ширины запрещенной зоны, которые могут быть использованы в фотовольтаике в качестве фотосенсибилизаторов для солнечных батарей [Dyes Pigm. 2018, 149, 707-718; doi: 10.1016/i.dyepig.2017.11.0451, [Macromol. Rapid Commun. 2015, 36, 943-58; doi: 10.1002/marc.2014007491.
Соединения пиррольного ряда нашли широкое применение в качестве хромофоров и флуорофоров, используемых в оптоэлектронике и фотовольтаике. Была получена серия сенсибилизированных красителей, содержащих 1-(2-этилгексил)-пиррол как пи-спейсер. Для полученных структур наблюдалось поглощение в диапазоне 350-500 нм с высокими коэффициентами молярного коэффициента поглощения, что свидетельствует о его способности эффективно поглощать свет. Исходя из потенциалов возбужденного состояния (1.63, 1.27, 1.18 эВ), можно ожидать эффективной инжекции электронов из возбужденных молекул красителя в полупроводник. Эффективность преобразования энергии в устройстве с использованием составила 5.80% [Dyes Pigm. 2020, 182, 108655; doi: 10.1016/i.dvepig.2020.1086551.
Из 2,5-диметокситетрагидрофурана и соответствующих анилинов были получены пирролы, содержащие пентафторфенильный и 4-цианофенильный заместители при атоме азота, которые далее применялись в качестве пи-спейсеров в структуре хромофоров. Для полученных соединений наблюдаются высокие коэффициенты экстинкции (44733 и 26300 М-1 см-1, соответственно). При этом, краситель, содержащий пентафторфенильную группу в качестве вспомогательного акцептора, показал хорошую эффективность преобразования энергии до 6.23% [DyesPigm. 2013, 99, 863-870; doi: 10.1016/i.dvepig.2013.05.0301.
В основе заявляемого метода получения соединении I лежит реакция конденсации замещенных (E)-3-(1H-пиррол-2-ил)акрилальдегидов с индандионом в присутствии основания.
Задачей изобретения является разработка метода получения новых замещенных (Е)-2-(3-(1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2R)-дионов Ia-д.
Задачей изобретения является изучение оптических и электрохимических свойств соединений Ia-д с целью их дальнейшего использования в качестве фотосенсибилизаторов для солнечных батарей.
Техническим результатом является способ синтеза новых производных (Е)-2-(3-(1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-диона I.
Техническим результатом являются соединения Ia-д, отличающиеся высокими значениями молярного коэффициента поглощения, а также небольшим значением ширины запрещенной зоны.
Технический результат достигается соединениями Ia-д, а также способом их получения, заключающимся в кипячении замещенных (E)-3-(1H-пиррол-2-ил)акрилальдегидов IIa-д с индандионом (III) в этиловом спирте в присутствии органического основания с последующей очисткой известными методами.

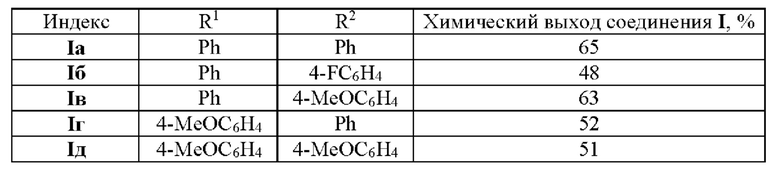
Пример 1. Получение (E)-3-(3,5-дифенил-1H-пиррол-2-ил)акрилальдегида IIa
В круглодонную колбу объемом 25 мл помещают иодид меди(I) (32 мг, 0.17 ммоль) и тетрагидрофуран (3 мл). Полученную суспензию охлаждают до 0°С. Раствор (E)-3-(фуран-2-ил)-1-фенилпроп-2-ен-1-она в тетрагидрофуране (1 мл, содержание 0.5 ммоль/мл) и раствор фенилмагнийбромида (2.2 мл, 1.5 М в тетрагидрофуране) добавляют к суспензии иодида меди(I) в тетрагидрофуране одновременно при 0°С и перемешивании. Полученную смесь перемешивают при той же температуре в течение 1 часа (контроль ТСХ). После этого к реакционной массе добавляют насыщенный раствор хлорида аммония (1 мл), полученную смесь выливают в воду (25 мл) и экстрагируют этилацетатом (2 × 20 мл). Объединенную органическую фазу сушат над безводным сульфатом натрия и концентрируют.Полученное масло растворяют в метаноле (10 мл), к метанольному раствору добавляют ацетат натрия тригидрат (82 мг, 0.6 ммоль) и гидроксиламина гидрохлорид (42 мг, 0.6 ммоль). Полученную массу кипятят с обратным холодильником в течение 12 часов (контроль ТСХ). Через 12 часов реакционную массу выливают в воду (100 мл) и экстрагируют этилацетатом (2×25 мл). Объединенную органическую фазу промывают водой (2 × 15 мл), сушат над безводным сульфатом натрия и концентрируют. Полученное масло растворяют в безводном диоксане, добавляют к раствору уксусный ангидрид (71 мкл, 0,75 ммоль) и перемешивают при комнатной температуре в течение 30 минут. По прошествии 30 минут к реакционной массе добавляют раствор хлорида железа гексагидрата в диоксане (100 мкл, содержание 13.5 мг/мл), и реакционную массу продолжают перемешивать при температуре 80 0°С в течение 1.5 часов (контроль ТСХ). По окончании реакции массу охлаждают до комнатной температуры, фильтруют через тонкий слой силикагеля, промывая смесью петролейного эфира и этилацетата в соотношении 1:1 (15 мл) и концентрируют. Полученный порошок растворяют в этилацетате (30 мл) и облучают светом голубых светодиодов (465-475 им) при комнатной температуре и перемешивании в течение 30 минут (контроль ТСХ). После этого реакционную массу концентрируют. Соединение На очищают методом колоночной хроматографии на силикагеле (элюент - этилацетат/петролейный эфир от 1:10 до 1:5).
(E)-3-(3,5-дифенил-1H-пиррол-2-ил)акролеин IIa: желтоватые кристаллы (188 мг, 69%) Rf=0.54 (петролейный эфир/этилацетат, 2:1); Тпл=218 - 219°С (CH3CN). ЯМР 1H (400 МГц, ДМСО-d6) δ 11.68 (с, 1H), 9.52 (д, 3J=7.8 Гц, 1H), 7.89 (д, 3J=8.5 Гц, 2Н), 7.53-7.43 (м, 7Н), 7.41-7.29 (м, 2Н), 6.96-6.82 (м, 2Н) м. д. ЯМР 13С (101 МГц, ДМСО-d6) 5 193.31, 139.88, 137.46, 134.58, 133.51, 130.83, 128.70 (2С), 128.66 (2С), 128.57 (2С), 127.59, 126.95, 125.79, 125.04 (2С), 122.97, 109.23 м. д. HRMS (ESI/TOF) m/z: [М+Н]+ вычислено для C19H16NO+ 274.1226, найдено 274.1218.
Соединения IIб-д получают аналогичным образом с использованием в качестве исходных соединений замещенных (E)-3-(фуран-2-ил)-1-фенилпроп-2-ен-1-онов.
Пример 2. Получение (E)-2-(3-(3,5-дифенил-1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-диона IIa
В круглодонную колбу емкостью 50 мл помещают (E)-3-(3,5-дифенил-1H-пиррол-2-ил)акрилальдегид IIa (137 мг, 0.5 ммоль), индандион (III) (183 мг, 1.25 ммоль), пиперидин (50 мкл, 0.5 ммоль) и этиловый спирт (25 мл). Полученную массу кипятят с обратным холодильником в течение 12 часов, после чего выливают в 2% водный раствор гидроксида натрия (300 мл) и энергично встряхивают. Полученную суспензию экстрагируют дихлорметаном (2×50 мл). Объединенную органическую фазу сушат над безводным сульфатом натрия и концентрируют.Соединение Ia очищают методом колоночной хроматографии на силикагеле (элюент дихлорметан/петролейный эфир от 1:4 до 1:1).
Соединения Iб-д получают аналогичным образом с использованием соединений IIб-д в качестве стартовых субстратов.
(Е)-2-(3-(3,5-дифенил-1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-дион (Ia). Темно-зеленые кристаллы (130 мг, 65%). Rf=0.50 (петролейный эфир/этилацетат, 2:1); Тпл=218-220°С (CH3CN). ЯМР 1Н (400 МГц, хлороформ-d): δ=9.46 (уш с, 1Н), 7.97 (дд, 3J=15.2, 12.1Hz, 1H), 7.66-7.64 (м, 1Н), 7.60-7.58 (м, 1Н), 7.49-7.44 (м, 4Н), 7.39 (д 3J=12.1 Hz, 1H), 7.29 -7.24 (м, 4Н), 7.22 -7.17 (м, 3Н), 7.13-7.06 (м, 2Н), 6.55 (д, 4J=2.5 Hz, 1H) м. д. ЯМР 13С (101 МГц, хлороформ-d): δ=191.89, 190.62, 145.90, 142.19, 140.92, 139.76, 139.54, 136.94, 134.62, 134.49 (2С), 130.76, 129.30 (2С), 129.15 (2С), 128.97 (2С), 128.75, 128.67, 127.86, 125.33 (2С), 124.41, 122.75, 122.47, 118.31, 110.42 м. д. HRMS (ESI/TOF) m/z: [М]⋅+вычислено для C28H19NO2⋅+401.1410, найдено 401.1398.
(E)-2-(3-(5-(4-фторфенил)-3-фенил-1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-дион (Iб). Темно-зеленые кристаллы (100 мг, 48%). Rf=0.48 (петролейный эфир/этилацетат, 2:1); Тпл=256-258°С (CH3CN). ЯМР 1Н (400 МГц, ДМСО-d6): δ=12.26 (с, 1H), 8.25 (дд, 3J=14.8, 12.3 Hz, 1Н), 8.05-8.00 (м, 2Н), 7.87-7.80 (м, 4Н), 7.61 (д, 3J=12.2 Hz, 1Н), 7.54 -7.47 (м, 5Н), 7.42-7.37 (м, 1H), 7.35-7.31 (м, 2Н), 6.98 (с, 1Н) м.д. ЯМР 13С (400 МГц, ДМСО-d6): δ=189.84, 189.54, 161.95 (д, 1JCF=2A6 Гц), 146.42, 141.26, 141.11, 139.93, 139.06, 136.02, 134.78, 134.64, 134.25, 128.80 (2С), 128.69 (2С), 128.38, 127.85 (д, 3JCF=8 Гц, 2С), 127.25, 127.20, 122.86, 121.95 (д, 2JCF=27 Гц, 2С), 118.67, 115.77, 115.56, 110.52 м. д. HRMS (ESI/TOF) m/z: [М+Н]⋅+вычислено для C28H19FNO2+420.1394, найдено 420.1386.
(E)-2-(3-(5-(4-метоксифенил)-3-фенил-1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-дион (Iв). Темно-зеленые кристаллы (136 мг, 63%). Rf=0.32 (петролейный эфир/этилацетат, 2:1); Тпл=213-215°С (CH3CN). ЯМР 1H (400 МГц, ДМСО-d6): δ=12.21 (с, 1H), 8.24 (дд, 3J=14.7, 12.4 Hz, 1H), 7.97-7.93 (м, 2Н), 7.84-7.82 (м, 4Н), 7.60 (д, 3J=12.3 Hz, 1H), 7.54-7.51 (м, 3Н), 7.50-7.47 (м, 2Н), 7.42-7.38 (м, 1H), 7.08-7.05 (м, 2Н), 6.94 (д, 4J=2.3 Hz, 1Н), 3.84 (с, 3Н) м. д. ЯМР 13С (400 МГц, ДМСО-d6): δ=190.01, 189.75, 159.62, 146.74, 141.46, 141.29, 140.94, 139.95, 136.96, 134.76, 134.60, 134.35, 128.93 (2С), 128.80 (2С), 128.17, 127.44 (2С), 127.40, 123.12, 122.06 (2С), 121.79, 118.10, 114.33 (2С), 110.10, 55.31 м. д. HRMS (ESI/TOF) m/z: [М]⋅+ вычислено для C29H21NO3⋅+431.1516, найдено 431.1517.
(E)-2-(3-(3-(4-метоксифенил)-5-фенил-1H-пиррол-2-ил)аллилиден)-1Н-индан-1,3(2H)-дион (Iг). Темно-зеленые кристаллы (112 мг, 52%). Rf=0.40 (петролейный эфир/этилацетат, 2:1); Тпл=261-263°С (CH3CN). ЯМР 1H (400 МГц, ДМСО-d6): δ=12.23 (с, 1Н), 8.25 (дд, 3J=14.8, 12.3 Hz, 1Н), 7.99-7.97 (м, 2Н), 7.84-7.82 (м, 4Н), 7.60 (д, 3J=12.3 Hz, 1H), 7.54-7.44 (м, 5Н), 7.39-7.35 (м, 1H), 7.08-7.04 (м, 2Н), 6.97 (д, 4J=2.3 Hz, 1H), 3.83 (с, 3Н) м. д. ЯМР 13С (400 МГц, ДМСО-d6): δ=189.82, 189.57, 158.79, 146.53, 141.43, 141.24, 140.28, 139.90, 136.34, 134.68, 134.53, 130.52, 129.99 (2С), 128.67 (2С), 128.37, 128.14, 126.63, 125.68 (2С), 122.40, 121.99, 121.72, 118.31, 114.26 (2С), 110.31, 55.11 м. д. HRMS (ESFTOF) m/z: [М+Н]⋅+ вычислено для C29H22NO3⋅+ 432.1594, найдено 432.1583.
(Е)-2-(3-(3,5-бис(4-метоксифенил)-1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-дион (Iд). Темно-зеленые кристаллы (117 мг, 51%). Rf=0.32 (петролейный эфир/этилацетат, 2:1); Тпл=192-194°С (CH3CN). ЯМР 1Н (400 МГц, ДМСО-d6): δ=12.13 (с, 1H), 8.19 (т, 3J=13.5 Hz, 1H), 7.93 (д, 3J=8.3 Hz, 2Н), 7.84-7.74 (м, 4Н), 7.55 (д, 3J=12.4 Hz, 1H), 7.45-7.42 (м, 3Н), 7.06-7.04 (м, 4Н), 6.87 (с, 1H), 3.83 (с, 6Н) м.д. ЯМР 13С (400 МГц, ДМСО-d6): δ=189.85, 189.63, 159.58, 158.83, 146.58, 141.50, 141.22, 141.09, 139.88, 137.13, 134.50, 134.34, 130.00 (2С), 128.09, 127.36 (2С), 126.63, 123.07, 121.85, 121.60, 121.57, 117.62, 114.25 (4С), 109.73, 55.22, 55.11 м. д. HRMS (ESI/TOF) m/z: [М]⋅+ вычислено для C30H23NO4⋅+ 461.1622, найдено 461.1611.
Электронные спектры поглощения соединений I были зафиксированы на спектрофотометре в растворе (ацетонитрил, 3×10-3 М). Электрохимические свойства соединений I были изучены методом циклической вольтамперометрии в стандартной трехэлектродной электрохимической ячейке в растворе (ацетонитрил, 3×10-3 М, фоновый электролит - Et4NClO4 1 мМ; рабочий электрод - стеклоуглерод; вспомогательный электрод платиновая пластина; электрод сравнения хлорсеребряный, развертка 100 мВ; диапазон сканирования: от -2 В до +2 В). Значения молярного показателя поглощения вычисляли по закону Бугера-Ламберта-Бера. Значение энергий граничных орбиталей определяли по следующим формулам:


где λonset соответствует длине волны, при которой наблюдается начало поглощения в длинноволновой области спектра.
Результаты исследования оптических и электрохимических свойств соединений I представлены в таблице 1.
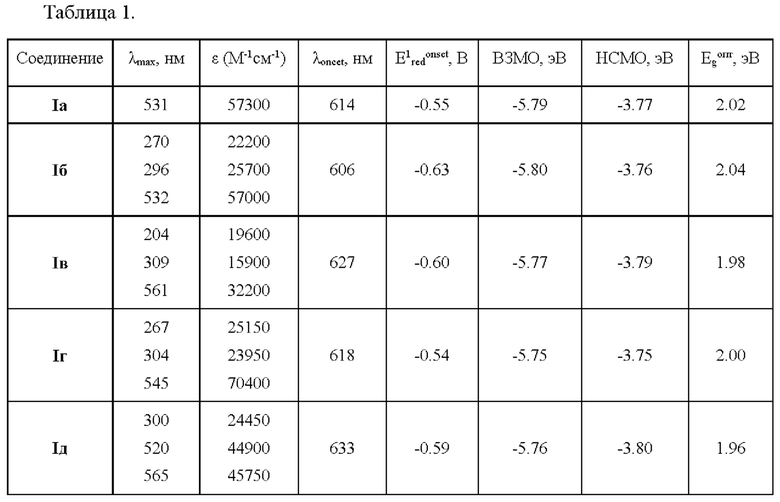
Как видно из таблицы 1, соединения I обладают высокими значениями молярного показателя поглощения, поглощают в зеленой части видимого диапазона электромагнитного излучения, имея значения ширины запрещенной зоны около 2 эВ, что говорит о их полупроводниковой природе и указывает на то, что соединения I могут найти применение в фотовольтаике, а именно, могут быть использованы в качестве фотосенсибилизаторов для солнечных батарей [Chem. Mater. 2014, 26, 587-593; doi: 10.1021/cm4021063].
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ 2',5'-ДИАРИЛСПИРО[ИНДОЛ-3,3'-ПИРРОЛИДИН]-2(1Н)-ОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2019 |
|
RU2730287C1 |
| Способ получения 4-галоген-1Н-пирроло[3,4-с]пиридин-1,3(2Н)-дионов | 2022 |
|
RU2790399C1 |
| ЛИГАНДЫ, ТРОПНЫЕ К ПРОСТАТИЧЕСКОМУ СПЕЦИФИЧЕСКОМУ МЕМБРАННОМУ АНТИГЕНУ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ДВОЙНЫХ КОНЪЮГАТОВ С ТЕРАПЕВТИЧЕСКИМИ АГЕНТАМИ НА ИХ ОСНОВЕ ДЛЯ КОМБИНИРОВАННОЙ ТЕРАПИИ ПСМА ЭКСПРЕССИРУЮЩИХ ОПУХОЛЕЙ | 2023 |
|
RU2841078C1 |
| ПРОИЗВОДНОЕ 1",2",3"-ТРИМЕТОКСИБЕНЗО[5",6":5',4']1H-(aR,1S)-1-АЦЕТАМИДО-6',7'-ДИГИДРОЦИКЛОГЕПТА[2',3'-f]-2,3-ДИГИДРОФУРАНА И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2678440C1 |
| Способ получения 3-ароил-N-бензил-2-гидрокси-1-оксобензо[d]пирроло[2,1-b]тиазол-3а(1Н)-карбоксамидов | 2021 |
|
RU2764906C1 |
| Соединения фторхинолонового ряда на основе производных пиридоксина, обладающие антибактериальными свойствами | 2019 |
|
RU2713932C1 |
| 1-имино-2,3,4,5-тетрагидро-1Н-пирроло[3,4-с]пиридин-3,4-дионов | 2016 |
|
RU2613967C1 |
| Способ получения 5-нитро-6-(2-оксо-2R-этил)-1Н-изоиндол-1,3(2Н)-дионов | 2015 |
|
RU2613560C1 |
| ПРОИЗВОДНЫЕ 2-ИМИНОПИРРОЛИДИНА | 2002 |
|
RU2270192C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИСПИРОИНДОЛИНОНОВ НА ОСНОВЕ 5-ИНДОЛИДЕН-2-ТИОГИДАНТОИНОВ | 2020 |
|
RU2756463C1 |
Изобретение относится к области органической химии, а именно к способу получения производных (E)-2-(3-(1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-диона общей формулы Iа-д. Способ осуществляется кипячением замещенных (E)-3-(1H-пиррол-2-ил)акрилальдегидов формулы IIa-д с индандионом формулы III в этиловом спирте в присутствии органического основания с последующей очисткой в соответствии с приведенной схемой. Технический результат изобретения заключается в получении ряда производных (E)-2-(3-(1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-диона общей формулы Iа-д, которые могут быть использованы в фотовольтаике в качестве фотосенсибилизаторов для солнечных батарей. 1 табл., 2 пр.
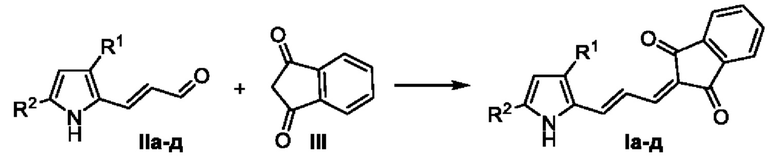

Способ получения замещенных (E)-2-(3-(1H-пиррол-2-ил)аллилиден)-1H-индан-1,3(2H)-дионов общей формулы I,

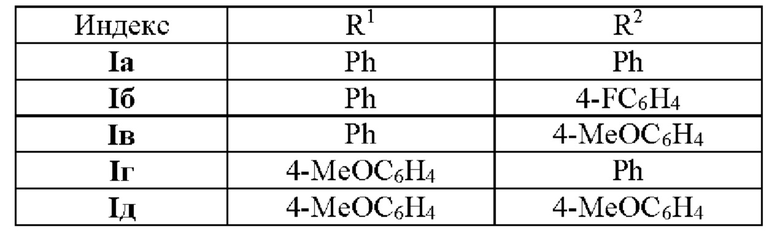
заключающийся в кипячении замещенных (E)-3-(1H-пиррол-2-ил)акрилальдегидов формулы IIa-д с индандионом формулы III в этиловом спирте в присутствии органического основания с последующей очисткой в соответствии с приведенной схемой:

| KIM T-D | |||
| et al | |||
| D-π-A Conjugated Molecules for Optoelectronic Applications, Macromol | |||
| Rapid Commun., 2015, vol.36, no.11, p.943-958 | |||
| ESHMEMETEVA D.A | |||
| et al | |||
| Synthetic strategy toward furyl- and benzofuryl-containing building blocks for organic materials, Chimica Techno Acta, 2022, vol.9, no.4, p.1-6 | |||
| ZHANG H | |||
| et al | |||
| Synthesis of novel sensitizers |
Авторы
Даты
2024-01-22—Публикация
2023-04-29—Подача