Изобретение относится к области медицинской химии и фармакологии, а именно к применению 3-амино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанона формулы (I) в качестве противовоспалительного средства, которое может быть использовано в медицине и в ветеринарии.
Проблема эффективности и безопасности использования нестероидных противовоспалительных препаратов (НПВП) в клинической практике на сегодняшний день весьма актуальна. Статистические исследования последнего десятилетия свидетельствуют о том, что на всех континентах более 30 миллионов человек принимают НПВП постоянно для устранения проявлений болевого, лихорадочного и воспалительного синдромов. Периодически этой группой лекарственных средств пользуется около 300 миллионов пациентов. Причем из этого количества до 200 миллионов человек приобретают препараты без рецепта [Максимов М.Л. Актуальные вопросы эффективности и безопасности нестероидных противовоспалительных препаратов // Русский медицинский журнал. 2014. 28. 2015; Матвеев А.В., Крашенинников А.Е., Егорова Е.А., Коняева Е.И., Корянова К.Н. Нежелательные лекарственные реакции на нестероидные противовоспалительные препараты в педиатрической практике: исследование серии случаев по данным врачебных извещений в Республике Крым за 2010-2018 гг. // Вопросы современной педиатрии. 2019. 18(3). 160-166.].
По результатам анализа почти 4000 спонтанных сообщений, поступивших в российскую базу Росздравнадзора за период 2008-2017 гг. для фиксации информации о нежелательных реакциях, возникавших при применении НПВП, сообщается, что наиболее часто реакции регистрировались на ацетилсалициловую кислоту, диклофенак, ибупрофен и кеторолак. Преобладающими в перечне из 6500 сообщений были нарушения со стороны иммунной системы, со стороны кожи, подкожных тканей и со стороны пищеварительного тракта. Также высокой частотой характеризуются такие реакции на ангионевротический отек, крапивница, эрозивный гастрит, кожная сыпь и повышение артериального давления [Вельц Н.Ю., Журавлева Е.О., Букатина Т.М., Кутехова Г.В. Нестероидные противовоспалительные препараты: проблема безопасности применения // Безопасность и риск фармакотерапии. 2018. 6(1). 11-18.]. Важно отметить, что не у всех пациентов использование НПВП сопровождается желаемым облегчением болевых ощущений и устранения признаков отечности воспалительного генеза при заболеваниях различной этиологии [Костина И.Н., Огнев М.Ю. Применение нестероидных противовоспалительных препаратов (НПВП) разной химической структуры для лечения послеоперационной боли: рандомизированное проспективное клиническое исследование // Проблемы стоматологии. 2017. 13(2). 45-48].
Низкий профиль безопасности НПВП и анальгетиков-антипиретиков, распространенных в клинической практике, а также обширный список противопоказаний к их применению подчеркивают важность целенаправленного поиска новых высокоэффективных и безопасных лекарственных средств. В связи с этим поиск вновь синтезированных эффективных и безопасных болеутоляющих и противовоспалительных средств в настоящее время сохраняет свою актуальность [Дядык А.И., Куглер Т.Е. Побочные эффекты нестероидных противовоспалительных препаратов // Consilium Medicum. 2017. 19(12). 94-99; Han M.N., Nam J.H., Noh E., Lee E.-K. Gastrointestinal risk of non-steroidal anti-inflammatory drugs and gastroprotective agents used in the treatment of osteoarthritis in elderly patients: a nationwide retrospective cohort study // International Journal of Clinical Pharmacology and Therapeutics. 2019. 57(11). 531-511; Bakhriansyah M., Souverein P.C., Boer A., Klungel О.H. Risk of myocardial infarction associated with non-steroidal anti-inflammatory drugs: Impact of additional confounding control for variables collected from self-reported data // Journal of Clinical Pharmacy and Therapeutics. 2019. 44(4). 623-631; Toshmatov B.N., Teshaev S.Z. Effect of non-steroidal anti-inflammatory drugs on the mucous membrane of the stomach in experimental chronic atrophic gastritis // International Conference on Scientific Research and Advancements in Sciences. 2021. 6. 143-145].
В последнее десятилетие новые органические соединения из ряда производных цианотиоацетамида представляют особый интерес для ученых химического, биологического, фармацевтического и медицинского профиля, поскольку цианотиоацетамид служит легкодоступным и полифункциональным реагентом, имеющим несколько нуклео- и электрофильных центров, он легко вступает в реакции конденсации и циклизации с широким кругом реагентов. Это обстоятельство обуславливает существенное разнообразие возможных продуктов таких реакций - серо- и азотсодержащих гетероциклических соединений, которые во многих случаях являются структурными фрагментами природных молекул, среди них обнаружено большое количество биологически активных соединений [Магеррамов А.М., Шихалиев Н.Г., Дяченко В.Д., Дяченко И.В., Ненайденко В.Г. α-Цианотиоацетамид // М.: Техносфера. 2018. 224 с. ISBN 978-5-94836-510-7].
Немаловажной особенностью производных цианотиоацетамида являются результаты исследования их острой пероральной токсичности in vivo, указывающие на их низкую токсичность (4-5 класс токсичности) [Бибик И.В., Корокин М.В., Бибик Е.Ю., Доценко В.В., Кривоколыско С.Г. Определение острой пероральной токсичности тетрагидропиридонов и гексагидрохинолинов, производных α-цианотиоацетамида // Курский научно-практический вестник «Человек и здоровье». 2019. 4. 96-103].
Задача, на решение которой направлено изобретение, заключается в установлении противовоспалительной активности среди новых гетероциклических соединений.
Поставленная задача решается применением 3-амино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанона (I) в качестве противовоспалительного средства, способствующего уменьшению проявления декстранового отека конечности в сравнении с лекарственными средствами из группы нестероидных противовоспалительных средств кислотой ацетисалициловой и нимесулидом.
Наиболее близкими по своей структуре к предлагаемому соединению являются многочисленные производные тиено[2,3-b]пиридина. Спектр биологического действия этого класса соединений довольно обширен [Литвинов В.П., Доценко В.В., Кривоколыско С.Г. Химия тиенопиридинов и родственных систем // М.: Наука. 2006. 407 с. ISBN 5-02-033674-2].
Неожиданно было обнаружено, что соединение 3-амино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанон (I), проявляет противовоспалительное действие в эксперименте на половозрелых крысах при сравнении с препаратами из группы нестероидных противовоспалительных средств, производных салицилатов (кислота ацетисалициловая) и производных сульфонанилида (нимесулид).
3-Aмино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанон (I) (название по IUPAC - 3-amino-4-(5-methyl-2-furyl)-5,6,7,8-tetrahydrothieno[2,3-b]quinolin-2-yl](phenyl)methanone; CAS RN 305853-71-8) для исследований был получен в НИЛ «Химэкс» ФГБОУ ВО «Луганский государственный университет им. Владимира Даля». Элементный анализ был проводен на C,H,N-анализаторе Carlo Erba 1106. Найдено, %: С 71.06; H 5.22; N 7.16. C23H20N2О2S (M 388.5). Вычислено, %: C 71.11; H 5.19; N 7.21.
Фармакологические свойства заявленного соединения
Пример 1.
Предварительно осуществленный виртуальный биоскрининг и предикторный анализ согласно [Yang J., Kwon S., Bae Park S.H. [et al.] GalaxySagittarius: Structure- and Similarity-Based Prediction of Protein Targets for Druglike Compounds // J. Chem. Inf. Model. 2020. 60. 3246-3254; Gfeller D., Grosdidier A., Wirth М. [et al.] SwissTargetPrediction: a web server for target prediction of bioactive small molecules // Nucleic Acids Research. 2014. 42 (1). 32-39; Gfeller D., Michielin O., Zoete V. Shaping the interaction landscape of bioactive molecules // Bioinformatics. 2013. 29. 3073-3079] показали, что механизм действия 3-амино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанона связан с тем, что его молекулы с высокой степенью вероятности способны связываться простаноидными рецепторами типов ЕР1, ЕР2 и ЕР4, каннабиоидными рецепторами СВ1 типа и арахидонат-5-липоксигеназой, и, как следствие, потенциально способны уменьшать проявления болевого и воспалительного синдромов.
Пример 2.
Эксперимент проводили в лаборатории кафедры фундаментальной и клинической фармакологии Луганского государственного медицинского университета имени Святителя Луки на половозрелых беспородных крысах. Все манипуляции с лабораторными животными осуществляли в соответствии с принципами биоэтики, правилами лабораторной практики (GLP), требованиями ФЗ РФ от 14.05.1993 №4979-1 «О ветеринарии» (с изменениями от 02.07.2021), директивы 2010/63/EU Европейского парламента и Совета Европейского Союза «О защите животных, используемых в научных целях», ГОСТа №33216-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами», ГОСТа 33215-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур», ГОСТа 33044-2014 «Принципы надлежащей лабораторной практики».
Рандомизация производилась методом «конвертов». В эксперименте использовались группы, состоящие из 10 белых крыс-самцов. Животные разделялись на интактную группу, контрольную группу, в которой крысам вводили 2 мл 0,9% раствора натрия хлорида внутрижелудочно до моделирования теста, первая референтная группа, в которой крысам вводили кислоту ацетилсалициловую, вторая референтная группа, в которой крысам вводили нимесулид, и опытную группу, крысам которой вводили соединение (I) в виде водной взвеси. В эксперимент были включены крысы со стандартными признаками воспаления, сформировавшимися в процессе моделирования.
Оценку противовоспалительных свойств синтезированного соединения (I) производили на модели острого «декстранового отека», формируемого после подапоневротической инъекции в правую заднюю лапу 6% раствора декстрана объемом 0,1 мл. Соединение (I) в дозе 5 мг/кг и препараты сравнения: кислоту ацетилсалициловую (ОАО «Уралбиофарм») в дозе 50 мг/кг, нимесулид (ЗАО «Березовский фармацевтический завод») в дозе 5 мг/кг от массы тела вводили крысам соответствующих групп внутрижелудочно за 1,5 часа до индукции отека.
Крысы контрольной группы в эквивалентном объеме получали 0,9% раствор хлорида натрия.
Регистрацию и количественное измерение отечности инъецированной конечности у животных всех экспериментальных групп проводили онкометрически по изменению обхвата правой задней конечности через 1 и 3 часа после индукции воспаления. Осуществляли сопоставление данных по сравнению с аналогичными значениями симметричной конечности и с показателями у крыс интактной группы. Наблюдение за животными всех групп проводилось в течение двух недель.
Исследование одобрено комиссией по биоэтике Государственного учреждения Луганской Народной Республики «Луганский государственный медицинский университет имени Святителя Луки», Министерства здравоохранения Луганской Народной Республики (Луганск, кв.50-летия Обороны Луганска, 1Г), протокол №6 от 1.11.2021г.
Животные содержались в одинаковых условиях, получали корм и воду в свободном доступе.
Противовоспалительную активность под действием соединения (I) сравнивали с таковыми у кислоты ацетисалициловой и нимесулида.
Статистическая обработка полученных данных производилась по известным формулам и методам математической статистики, характеризующим количественную изменчивость. При обработке экспериментальных данных определялись: среднее арифметическое обхвата конечности а; дисперсия значений σ2 вокруг среднего арифметического; среднеквадратическое отклонение σ. Однородность полученных экспериментальных данных оценивалась коэффициентом вариации V.
Определение достоверности различий между образцами и препаратами сравнения производилось по t-критерию Стьюдента при критическом значении t-критерия Стьюдента, равном 2,101, уровне значимости α = 0,05 и числе степеней свободы f = 18.
Данные экспериментальных исследований по противовоспалительной активности исследуемого соединения (I) и препаратов сравнения в тесте декстранового отека представлены в таблицах 1 и 2.
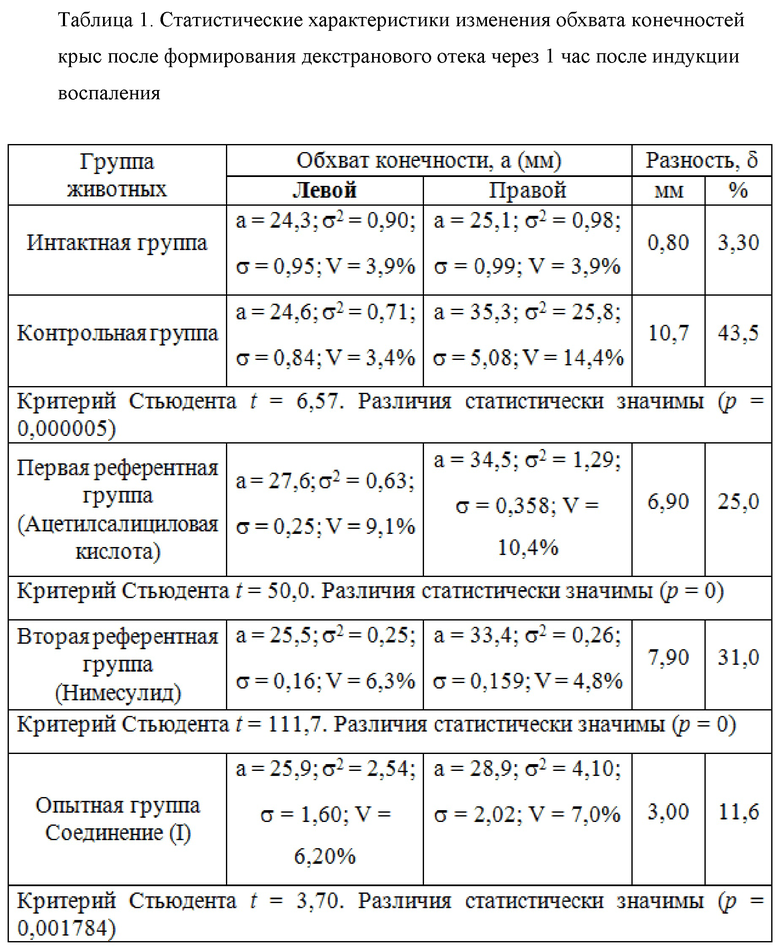

Результаты экспериментального фармакологического исследования в тесте декстранового отека лапы крыс засвидетельствовали следующее: подапоневротическая инъекция 6% раствора декстрана лабораторным крысам контрольной группы способствовала возникновению выраженного отека. При этом через 1 час после инъекции раствора декстрана обхват правой задней лапки превышал соответствующее значение симметричной левой лапки на 43,5% (табл.1). Через 3 часа после воспроизведения в модельном опыте воспалительной реакции «декстрановый отек» обхват правой лапы крыс контрольной группы был больше аналогичного значения левой на 43,9% (табл.2) . Иными словами, к этому моменту наблюдения был зарегистрирован ярко выраженный отек, покраснение, болезненность и дисфункция дистального отдела свободной задней конечности.
Предварительное за 90 минут до моделирования острой воспалительной реакции внутрижелудочное введение ацетилсалициловой кислоты крысам первой референтной группы способствовало формированию не столь выраженного отека инъецированной правой лапки: разница в показателе обхвата правой и левой конечности составила 25% на раннем сроке наблюдения (табл.1). Важно отметить следующее обстоятельство: через три часа после введения раствора декстрана у крыс референтной группы, получавших ацетилсалициловую кислоту, разность в обхвате задних лапок уменьшается вдвое, составляя почти 12% (табл.2).
Нимесулид, вводимый внутрижелудочно крысам второй референтной группы, обладает умеренными противоотечными свойствами. Так, через час после моделирования воспалительной реакции, разница в обхвате инъецированной и неинъецированной лапок составила 31% (табл.1). Еще через 2 часа признаки отечности существенно снижаются, а разница в обхвате лапок животных этой группы составляет 21,2% (табл. 2).
Как видно из данных табл. 1, значительно более выраженными противовоспалительными свойствами, по результатам экспериментов, обладает соединение (I), вводимое за 90 минут до фармакологического теста крысам опытной группы. Разность в обхвате дистальных отделов конечностей животных этих опытных групп на часовом сроке опыта составляет 11,6% (табл.1). Это более чем в 2,5 раза меньше показателя, зарегистрированного в группе сравнения после введения нимесулида, и в 2,2 раза меньше после использования кислоты ацетилсалициловой. При этом не зарегистрировано признаков резкой болезненности при передвижении по клетке крыс в этих трех опытных группах, что присутствовало у крыс контрольной группы без фармакокоррекции.
Как видно из таблицы 2, наблюдение в динамике эксперимента показало, что через трехчасовый интервал с момента введения раствора декстрана, разность в обхвате между инъецированной и неинъецированной конечностями крыс опытной группы, получавших 3-амино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанон, составляет 7,3%.
Таким образом, приведенные примеры подтверждают, что соединение (I), применяемое однократно в дозе 5 мг/кг обнаруживает отчетливо выраженную противовоспалительную активность на модели декстранового отека лапы белых крыс в спектре своей фармакодинамической активности. Причем оно эффективнее препаратов-референтов: нимесулида в 2,5 раза, и в 2,2 раза эффективнее кислоты ацетилсалициловой.
В ходе экспериментальных исследований нежелательных явлений зафиксировано не было.
Резюмируя вышеописанное, приведенные результаты наглядно демонстрируют способность соединения (I) проявлять в эксперименте in vivо в тесте декстранового отека лапы крыс отчетливо выраженную противовоспалительную активность. Причем, по степени выраженности противовоспалительных свойств исследуемое соединение превосходит препараты сравнения кислоту ацетилсалициловую и нимесулид в 2,2 и 2,5 раза соответственно.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭТИЛОВЫЙ ЭФИР 4-(2-МЕТИЛ-6-{ [2-(ДИФЕНИЛАМИНО)-2-ОКСОЭТИЛ]ТИО} -4-ФУР-2-ИЛ-5-ЦИАНО-1,4-ДИГИДРОПИРИДИН-3-КАРБОКСАМИДО)БЕНЗОЙНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНЫЕ СВОЙСТВА | 2022 |
|
RU2792595C1 |
| АЛЛИЛ-2-МЕТИЛ-6-((2-((4-НИТРОФЕНИЛ)АМИНО)-2-ОКСИЭТИЛ)ТИО)-5-ЦИАНО-4-(ФУРАН-2-ИЛ)-1,4-ДИГИДРОПИРИДИН-3-КАРБОКСИЛАТ, ПРОЯВЛЯЮЩИЙ АНАЛЬГЕТИЧЕСКИЕ СВОЙСТВА | 2024 |
|
RU2840384C1 |
| ГЕЛЕВАЯ ФОРМА НИМЕСУЛИДА, ОБЛАДАЮЩАЯ ПРОТИВОВОСПАЛИТЕЛЬНЫМ И АНАЛЬГЕТИЧЕСКИМ ДЕЙСТВИЕМ | 2015 |
|
RU2593777C1 |
| СОЕДИНЕНИЯ, ПОЛУЧЕННЫЕ ИЗ ТАУРИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2009 |
|
RU2502729C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ НПВП-ПАНКРЕАТОПАТИИ В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2541739C1 |
| 2-МЕТИЛ-N-(2-МЕТИЛФЕНИЛ)-4-(2-ФУРИЛ)-5-ЦИАНО-6-({ 2-[(4-ЭТОКСИФЕНИЛ)АМИНО]-2-ОКСОЭТИЛ} ТИО)-1,4-ДИГИДРОПИРИДИН-3-КАРБОКСАМИД, ПРОЯВЛЯЮЩИЙ АНАЛЬГЕТИЧЕСКИЕ СВОЙСТВА | 2023 |
|
RU2813896C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ГАСТРОПАТИИ | 2009 |
|
RU2424578C1 |
| Средство, обладающее противовоспалительным и анальгезирующим действием | 2017 |
|
RU2657803C1 |
| Применение 2-метил-N-(2-метилфенил)-4-(2-фурил)-5-циано-6-({ 2-[(4-этоксифенил)амино]-2-оксоэтил} тио)-1,4-дигидропиридин-3-карбоксамида в качестве гипогликемического, гиполипидемического средства, способствующего снижению массы тела | 2023 |
|
RU2812569C1 |
| Применение метил 5-бензоил-6-(4-фторфенил)-4-метокси-2-тиоксогексагидропиримидин-4-карбоксилата в качестве средства, обладающего противовоспалительной активностью | 2022 |
|
RU2786805C1 |
Изобретение относится к применению 3-амино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанона формулы (I) в качестве противовоспалительного средства. Технический результат - выраженное противовоспалительное действие 3-амино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанона, который может быть использован в медицине и в ветеринарии в качестве противовоспалительного средства. 2 табл., 2 пр.
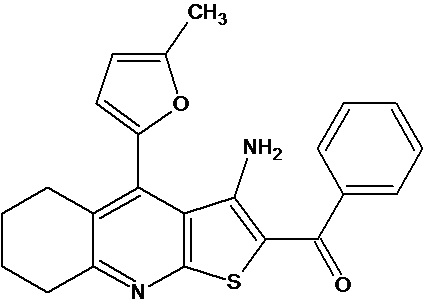
(I)
Применение 3-амино-4-(5-метил-2-фурил)-5,6,7,8-тетрагидротиено[2,3-b]хинолин-2-ил](фенил)метанона формулы (I)
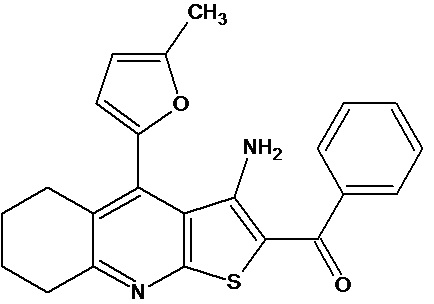
(I)
в качестве противовоспалительного средства.
| WO 2007146602 A8, 29.10.2009 | |||
| US 20160318948 A1, 03.11.2016 | |||
| АЗАБЕНЗОТИОФЕНИЛЬНЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ПРИМЕНЕНИЯ | 2007 |
|
RU2444524C2 |
| ПРИМЕНЕНИЕ БЕНЗИЛАМИДА N-(2-ФУРАНОИЛ)-5-ЙОДАНТРАНИЛОВОЙ КИСЛОТЫ И ДИМЕТИЛАМИДА N-(2-ФУРАНОИЛ)-5-ЙОДАНТРАНИЛОВОЙ КИСЛОТЫ В КАЧЕСТВЕ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СРЕДСТВ | 2006 |
|
RU2337101C1 |
| ЭТИЛОВЫЙ ЭФИР 4-(2-МЕТИЛ-6-{ [2-(ДИФЕНИЛАМИНО)-2-ОКСОЭТИЛ]ТИО} -4-ФУР-2-ИЛ-5-ЦИАНО-1,4-ДИГИДРОПИРИДИН-3-КАРБОКСАМИДО)БЕНЗОЙНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНЫЕ СВОЙСТВА | 2022 |
|
RU2792595C1 |
| EA 201690089 A1, 28.04.2017. | |||
Авторы
Даты
2024-01-30—Публикация
2023-07-19—Подача