Изобретение относится к химико-фармацевтической промышленности, к группе нестероидных противовоспалительных средств (далее - НПВС) и может быть использовано для лечения как острых, так и хронических воспалительных процессов (ОРЗ, ОРВИ, ревматизм, хронический и псориатический артрит и других).
Поиск новых НПВС является одним из важнейших направлений современной фармацевтической промышленности по причине неуклонного увеличения числа пациентов с хроническими воспалительными заболеваниями. Для данной группы пациентов необходимы эффективные и безопасные лекарственные средства. НПВС занимают лидирующие позиции по объемам потребления в мире, что объясняется, в первую очередь, высокой эффективностью при болевом синдроме воспалительного происхождения. Уникальность НПВС как класса лекарственных средств обусловлена сочетанием противовоспалительного, обезболивающего, жаропонижающего и антиагрегантного действия [Pirmohamed М. et al. Adverse drug reactions as cause of admission to hospital: prospective analysis of 18 820 patients // Bmj. - 2004. - T. 329. - №.7456. - C. 15-19]. Более тридцати миллионов людей в мире ежедневно принимают нестероидные противовоспалительные средства, при этом 40% из них в возрасте старше 60 лет [Champion G.D. et al. NSAID-induced gastrointestinal damage // Drugs. - 1997. - T. 53. - №.1. - C. 6-19]. Около 20% стационарных больных получают нестероидные противовоспалительные средства. Анальгезирующая активность НПВС применяется не только при острых воспалительных заболеваниях, они так же являются препаратом выбора при лечении злокачественных новообразований со слабо и умеренно выраженным болевым синдромом [Вершинина С.Ф., Стуков А.Н. Противоболевая терапия в онкологии // Психофармакология и биологическая наркология. - 2007. - Т. 7. - №.1]. Снижение агрегационной способности тромбоцитов у пациентов с высоким риском развития инфаркта миокарда и инсульта достоверно увеличивает продолжительность жизни [Antithrombotic  : Collaborative metaanalysis of randomized trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high-risk patients // B.M. J. - 2002. - Vol. 324. - P. 71-86], но необходимо также помнить о том, что существует ряд лиц с тромбоцитопенией и новые противовоспалительные средства, не влияющие на данное звено гемостаза, являются востребованным в настоящее время. Длительная терапия нестероидными противовоспалительными средствами несет в себе множество осложнений. В структуре побочных реакций у препаратов группы НПВС доминирует гастроэнтеральная патология [Михайлов И.Б. Настольная книга врача по клинической фармакологии: руководство для врачей // СПб.: Фолиант. - 2001. - С 736-740], в большей степени связанная с язвенным дефектом, с клинически бессимптомным вплоть до прободения [Насонова В.А. и др. Рациональная фармакотерапия ревматических заболеваний. - М.: Литтерра, 2003. - 507-512]. Со стороны сердечно-сосудистой системы лидирует повышение АД, вызванное угнетением циклооксигеназы в почках, следствие задержки воды и натрия в организме [Bjorkman D.J. Current status of nonsteroidal anti-inflammatory drug (NSAID) use in the United States: risk factors and frequency of complications // The American journal of medicine. - 1999. - T. 107. - №.6. - C. 3-8]. В системе кроветворения наблюдаются осложнения, такие как лейкопения и агранулоцитоз, тромбоцитопения [Strom В.L. et al. Nonsteroidal anti-inflammatory drugs and neutropenia // Archives of internal medicine. - 1993. - T. 153. - №.18. - C. 2119-2124]. Грозным побочным эффектом является токсическое воздействие на гепатоциты, вызванное повреждением митохондрий, которые перестают в должной мере обеспечивать энергоемкие процессы [Bort R. et al. Diclofenac toxicity to hepatocytes: a role for drug metabolism in cell toxicity // Journal of Pharmacology and Experimental Therapeutics. - 1999. - T. 288. - №.1. - C. 65-72].
: Collaborative metaanalysis of randomized trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high-risk patients // B.M. J. - 2002. - Vol. 324. - P. 71-86], но необходимо также помнить о том, что существует ряд лиц с тромбоцитопенией и новые противовоспалительные средства, не влияющие на данное звено гемостаза, являются востребованным в настоящее время. Длительная терапия нестероидными противовоспалительными средствами несет в себе множество осложнений. В структуре побочных реакций у препаратов группы НПВС доминирует гастроэнтеральная патология [Михайлов И.Б. Настольная книга врача по клинической фармакологии: руководство для врачей // СПб.: Фолиант. - 2001. - С 736-740], в большей степени связанная с язвенным дефектом, с клинически бессимптомным вплоть до прободения [Насонова В.А. и др. Рациональная фармакотерапия ревматических заболеваний. - М.: Литтерра, 2003. - 507-512]. Со стороны сердечно-сосудистой системы лидирует повышение АД, вызванное угнетением циклооксигеназы в почках, следствие задержки воды и натрия в организме [Bjorkman D.J. Current status of nonsteroidal anti-inflammatory drug (NSAID) use in the United States: risk factors and frequency of complications // The American journal of medicine. - 1999. - T. 107. - №.6. - C. 3-8]. В системе кроветворения наблюдаются осложнения, такие как лейкопения и агранулоцитоз, тромбоцитопения [Strom В.L. et al. Nonsteroidal anti-inflammatory drugs and neutropenia // Archives of internal medicine. - 1993. - T. 153. - №.18. - C. 2119-2124]. Грозным побочным эффектом является токсическое воздействие на гепатоциты, вызванное повреждением митохондрий, которые перестают в должной мере обеспечивать энергоемкие процессы [Bort R. et al. Diclofenac toxicity to hepatocytes: a role for drug metabolism in cell toxicity // Journal of Pharmacology and Experimental Therapeutics. - 1999. - T. 288. - №.1. - C. 65-72].
Известно средство, обладающее противовоспалительным действием, а именно ацетилсалициловая кислота, которая используется также в качестве жаропонижающего, болеутоляющего и антиагрегантного средства.
Недостатком ацетилсалициловой кислоты является ульцерогенное влияние на желудочно-кишечный тракт путем как прямого, так и непрямого воздействия на слизистую оболочку, вызывающее снижение синтеза простагландинов в ней. Что в свою очередь снижает опосредованную простагландинами выработку защитной слизи и бикарбонатов, вызывая тем самым появление эрозий и язв. Также возможно развитие «аспириновой астмы», тяжелого осложнения от приема ацетилсалициловой кислоты [Михайлов И.Б. Настольная книга врача по клинической фармакологии: руководство для врачей // СПб.: Фолиант. - 2001. - С. 736-740].
Одним из наиболее близких по достигаемому результату являются нимесулид, обладающий противовоспалительной активностью, связанной с селективным ингибированием циклооксигеназы 2 типа, в отличие от неселективной в отношении циклооксигеназ ацетилсалициловой кислоты.
Основными недостатком нимесулида является его гепатотоксичность [Каратеев А.Е., Насонова В.А. // «Научно-практическая ревматология»; №4; 2003. - С. 87-91].
Техническим результатом заявляемого средства является расширение арсенала отечественных средств синтетического происхождения, обладающих выраженным противовоспалительным и жаропонижающим эффектом.
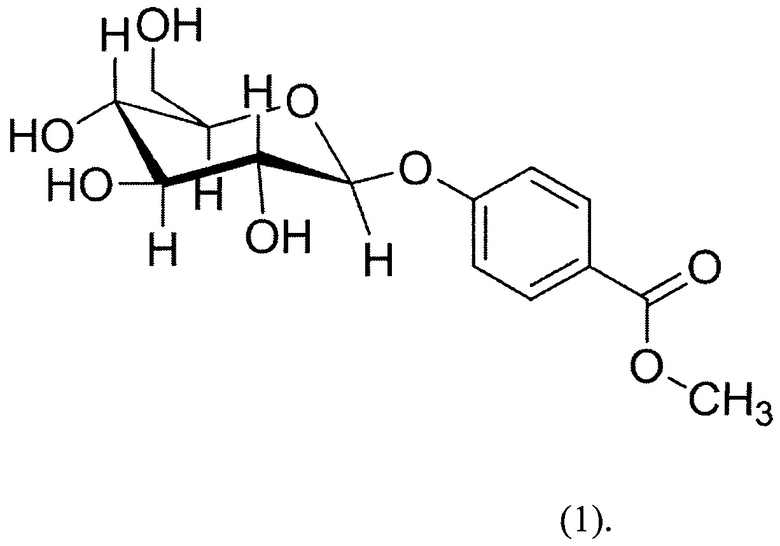
Технический результат достигается тем, что применяют метиловый эфир 4-(бета-д-глюкопиранозилокси) бензойной кислоты
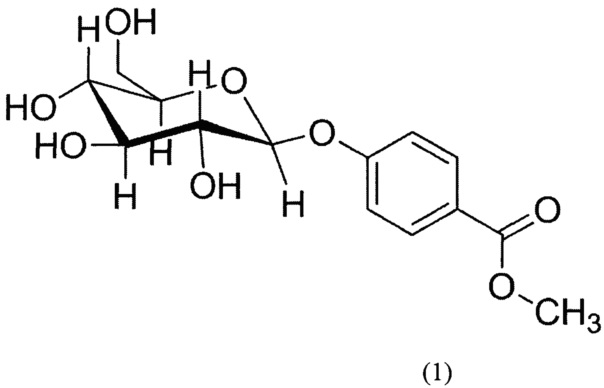
в качестве средства, обладающего противовоспалительным и жаропонижающим действием.
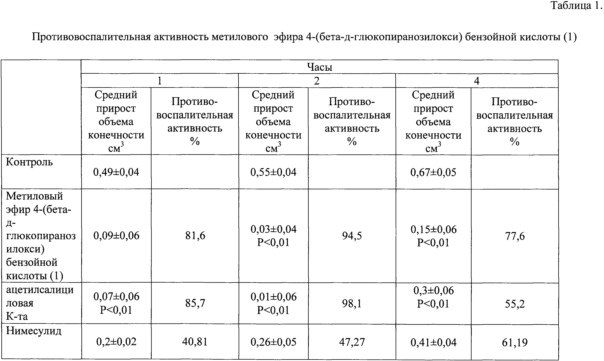
В таблице 1 представлена сравнительная характеристика противовоспалительной активности метилового эфира 4-(бета-д-глюкопиранозилокси) бензойной кислоты (1), ацетилсалициловой кислоты и нимесулида.
Как видно из таблицы 1, соединение (1) по изобретению обладает выраженной противовоспалительной активностью, которая немногим выше у ацетилсалициловой кислоты и более выражена по сравнению с нимесулидом.
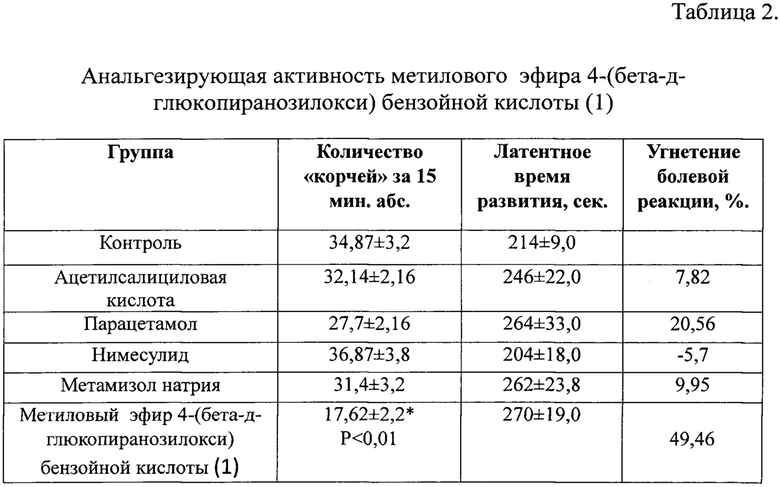
Как видно из таблицы 2, применение метилового эфира 4-(бета-д-глюкопиранозилокси) бензойной кислоты (1) привело к выраженному анальгетическому эффекту, который заключался в значительном снижении количества «корчей» (P<0,01) и увеличении латентного времени развития болевой реакции, при этом ее угнетение составило 20% и 50% соответственно. Препараты сравнения в данной дозе не оказали выраженного терапевтического эффекта.
Сущность технического решения подтверждается следующими примерами.
Пример 1. Синтез метиловый эфир 4-(бета-д-глюкопиранозилокси) бензойной кислоты (1).
1) Получение метилового эфира 4-карбоксифенил-2,3,4,6-тетра ацетил-O-β-D-глюкопиранозида. К раствору 3,9 г (10 ммоль) β-пентаацетата глюкозы и 1,52 г (15 ммоль) метил-4-гидроксибензоата в 40 мл сухого хлороформа вливают раствор 0,7 мл триэтиламина в 5 мл сухого хлороформа. Реакционную массу выдерживают 30 мин при перемешивании. Затем под атмосферой азота вносят 3,3 мл эфирата трифторида бора. Реакционную массу перемешивают при комнатной температуре 12 часов. Хлороформ промывают насыщенным раствором бикарбоната натрия до прекращения газовыделения, водой (1×50 мл), 5% раствором гидроксида натрия (2×50 мл), водой (1×50 мл). После этого хлороформный слой сушат сульфатом магния. Растворитель отгоняют, маслообразный остаток кристаллизуют из этанола. Получают 3,2 г (выход: 66%) белых кристаллов с температурой плавления 1560C.
Спектр ЯМР 1H (CDCl3), δ, м.д: 2.04, 2.05, 2.07, 2.08 (4×3H, с, COCH3'); 3.91 (м, H-5', COCH3); 4.14-4.31 (2H, м, H-6'a, H-6'b); 5.13-5.31 (4Н, м, H-1', H-2', H-3', H-4'); 7.00 (2Н, д, J=9.0 Гц, Н-2, Н-6); 7.99 (2Н, д, Н-3, Н-5, J=8.7 Гц).
Спектр ЯМР 13C, (CDCl3), δ, м.д.: 20.5 (4×CH3, COCH3'); 52.0 (CH3, COCH3), 61.8 (CH2, C6'); 68.0 (CH, С-4'); 70.9 (CH, С-2'); 72.1 (CH, С-5'); 72.4 (CH, С-3'); 98.1 (CH, C-1'); 116.1 (2×CH, С-2, С-6); 125.0 (С, С-4); 131.5 (2×CH, С-3, С-5); 160.1 (С, С-1); 166.3, 169.3, 170.1, 170.4 (4×C, COCH3').
2) Получение метилового эфира 4-(бета-д-глюкопиранозилокси) бензойной кислоты (1). К суспензии 1.2 г метилового эфира 4-карбоксифенил-2,3,4,6-тетра ацетил-O-β-D-глюкопиранозида в 12 мл метанола вливают 2 мл 5% раствора метилата натрия в метаноле. Реакционную массу интенсивно перемешивают до полного растворения и оставляют при комнатной температуре на 10 часов. Получают 1.11 г (выход: 93%) белых кристаллов с температурой плавления 1700C.
Спектр ЯМР 1H (D2O), δ, м.д,:; 3.49-3.80 (6Н, м, Н-2', Н-3', Н-4', Н-5', Н-6'b, H-6'a); 3.77 (3H, с, COCH3); 5.1 (1Н, м, H-1'); 7.05 (2Н, д, J=8.7 Гц, Н-3, Н-5); 8.36 (2Н, д, Н-2, Н-6, J=8.7 Гц).
Спектр ЯМР 13C, (D2O), δ, м.д.: 52.3 (CH3, COCH3); 60.2 (CH2, С6'); 69.1 (CH, С-4'); 72.6 (CH, С-2'); 75.4 (CH, С-5'), 76,0 (CH, С-3'); 99.2 (CH, С-1'); 115.8 (2×CH, С-2, С-6); 123.7 (С, С-4); 131.4 (2×CH, С-3, С-5); 160.3 (С, С-1); 169.3 (CO, COCH3).
Спектры ЯМР 1H, 13C записывали на Фурье-спектрометре Brucker Avante-300 (300 МГц) фирмы Bruker (Германия) внутренний стандарт - ГМДС. Температуры плавления определяли на микронагревательном столике Boetius фирмы Boetius (Германия).
Полученное средство характеризуется следующими свойствами: белые кристаллы. Растворим в воде, слабо в спирте.
Пример 2. Оценка противовоспалительной активности.
Фармакологическое действие заявляемого средства проверяли путем биологических исследований. Противовоспалительную активность средства оценивали на 12 лабораторных крысах-самках массой 200-220 грамм в каждой экспериментальной группе. Острое экссудативное воспаление индуцировали субплантарным введением 0,1 мл 1%-ного раствора каррагенина. Измерение объема правой задней конечности проводили с помощью плетизмометра до введения, а также через 60, 120 и 240 минут после инъекции флогистика. На основании данных среднего прироста конечности животных, полученных в результате трех параллельных измерений, рассчитывали степень противовоспалительной активности. Считалось, что вещество обладает выраженной противовоспалительной активностью, если полученный результат превышал 30%. В качестве препаратов сравнения использовалась ацетилсалициловая кислота и нимесулид. Исследуемые вещества вводили внутрижелудочно зондом в 2 миллилитрах дистиллированной воды. Вещества применяли в количестве: метиловый эфир 4-(бета-д-глюкопиранозилокси) бензойной кислоты 54 мкМ/кг (17 мг/кг), ацетилсалициловой кислоты 54 мкМ/кг (9,75 мг/кг), нимесулида 130 мкМ/кг (40 мг/кг). Результаты экспериментальных исследований обрабатывали статистическим методом с использованием критерия Манна-Уитни. Разница сравниваемых средних считалась достоверной, если показатель достоверности (Р) был меньше 0,05.
Пример 3. Оценка анальгезирующий активности.
Анальгезирующую активность исследовали путем биологических исследований. Анальгезирующая активность средства оценивалась на 10 лабораторных мышах в каждой экспериментальной группе. Исследование анальгезирующей активности препарата проведено в соответствии с методическими указаниями, опубликованными в «Руководстве по проведению доклинических исследований лекарственных средств» (Москва, 2012). В качестве модели химического болевого раздражения использовали тест «уксусные корчи», который представляет собой модель острого перитонита. Специфическую болевую реакцию - «корчи» (характерные движения животных, включающие сокращения брюшных мышц, чередующиеся с их расслаблением, вытягиванием задних конечностей и прогибанием спины) - вызывали внутрибрюшинным введением 0,75% раствора уксусной кислоты мышам в дозе 0,1 мл/10 г массы тела. О реакции мышей на болевые раздражения, в генезе которых основную роль играют образующиеся в условиях кислой среды эндогенные кинины, судили по количеству «корчей», регистрируемых в течение 15 мин после введения кислоты. Тестируемые вещества мышам вводили в виде растворов за 2 часа до инъекции 0,75% раствора уксусной кислоты. Мышам вводили ацетилсалициловую кислоту, метиловый эфир 4-(бета-д-глюкопиранозилокси) бензойной кислоты (1), парацетамол, нимесулид, метамизол натрия в эквималярных дозах 54 мкМ/кг в 0,3 мл дистиллированной воды. Результаты экспериментальных исследований обрабатывали с использованием критерия Манна-Уитни. Разница сравниваемых средних считалась достоверной, если показатель достоверности (Р) был меньше 0,05.
| название | год | авторы | номер документа |
|---|---|---|---|
| (Z)-3-(2-ОКСО-2-(4-ТОЛИЛ)ЭТИЛИДЕН)ПИПЕРАЗИН-2-ОН, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ И/ИЛИ АНТИНОЦИЦЕПТИВНОЙ АКТИВНОСТЬЮ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2014 |
|
RU2602500C2 |
| СПОСОБ УСИЛЕНИЯ ПРОЛОНГИРОВАННОГО ЖАРОПОНИЖАЮЩЕГО ДЕЙСТВИЯ И СНИЖЕНИЯ ТОКСИЧНОСТИ САЛИЦИЛАТОВ | 2008 |
|
RU2382763C2 |
| НЕСТЕРОИДНОЕ ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО НА ОСНОВЕ НАПРОКСЕНА, ОБЛАДАЮЩЕЕ НИЗКОЙ ГАСТРОТОКСИЧНОСТЬЮ | 2016 |
|
RU2629367C1 |
| ПРИМЕНЕНИЕ МЕТИЛ 5-БЕНЗОИЛ-4-ГИДРОКСИ-6-(4-ХЛОРФЕНИЛ)-2-ТИОКСОГЕКСАГИДРОПИРИМИДИН-4-КАРБОКСИЛАТА В КАЧЕСТВЕ СРЕДСТВА, ОБЛАДАЮЩЕГО АНАЛЬГЕТИЧЕСКИМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2024 |
|
RU2835600C1 |
| ПРИМЕНЕНИЕ 3-АМИНО-4-(5-МЕТИЛ-2-ФУРИЛ)-5,6,7,8-ТЕТРАГИДРОТИЕНО[2,3-B]ХИНОЛИН-2-ИЛ](ФЕНИЛ)МЕТАНОН В КАЧЕСТВЕ ПРОТИВОВОСПАЛИТЕЛЬНОГО СРЕДСТВА | 2023 |
|
RU2812570C1 |
| ДИАЛКИЛ-БЕТА-(О-САЛИЦИЛОИЛ)ЭТИЛФОСФОНАТЫ, ОБЛАДАЮЩИЕ ЖАРОПОНИЖАЮЩЕЙ АКТИВНОСТЬЮ | 2009 |
|
RU2420532C1 |
| ПРОИЗВОДНЫЕ ПРОСТАГЛАНДИНА, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ И АНАЛЬГЕЗИРУЮЩЕЙ АКТИВНОСТЬЮ | 2015 |
|
RU2568603C1 |
| НЕСТЕРОИДНЫЕ ПРОТИВОВОСПАЛИТЕЛЬНЫЕ СРЕДСТВА НА ОСНОВЕ ПРОИЗВОДНЫХ ПИРИДОКСИНА | 2012 |
|
RU2513089C1 |
| 3-АРИЛ-4а-ИЗОПРОПИЛ-4аН-ХРОМЕНО[6',7':4,5]ФУРО[3,2-с][1,2]ОКСАЗИН-8-ОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ И АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2622768C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ МОЧЕГОННЫМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2522925C1 |
Изобретение относится к фармацевтической промышленности и представляет собой средство, обладающее противовоспалительным и анальгезирующим действием, представляющее собой метиловый эфир 4-(бета-д-глюкопиранозилокси) бензойной кислоты. Изобретение обеспечивает расширение арсенала средств, обладающих противовоспалительным и анальгезирующим эффектом синтетического происхождения. 3 пр., 2 табл.
Средство, обладающее противовоспалительным и анальгезирующим действием, характеризующееся тем, что оно включает метиловый эфир 4-(бета-д-глюкопиранозилокси) бензойной кислоты формулы
| ПРОТИВОВОСПАЛИТЕЛЬНЫЙ ПРЕПАРАТ ДЛЯ НАРУЖНОГО ПРИМЕНЕНИЯ | 1996 |
|
RU2157683C2 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ НИТРООКСИПРОИЗВОДНЫХ НЕСТЕРОИДНЫХ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СРЕДСТВ | 2006 |
|
RU2406482C2 |
| НОВАЯ ЛЕКАРСТВЕННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ БОЛЕВОГО СИНДРОМА ПРИ СПАЗМЕ ГЛАДКОЙ МУСКУЛАТУРЫ | 2012 |
|
RU2497505C1 |
| WO 2016089951 A1, 09.06.2016. | |||
Авторы
Даты
2018-06-15—Публикация
2017-03-21—Подача