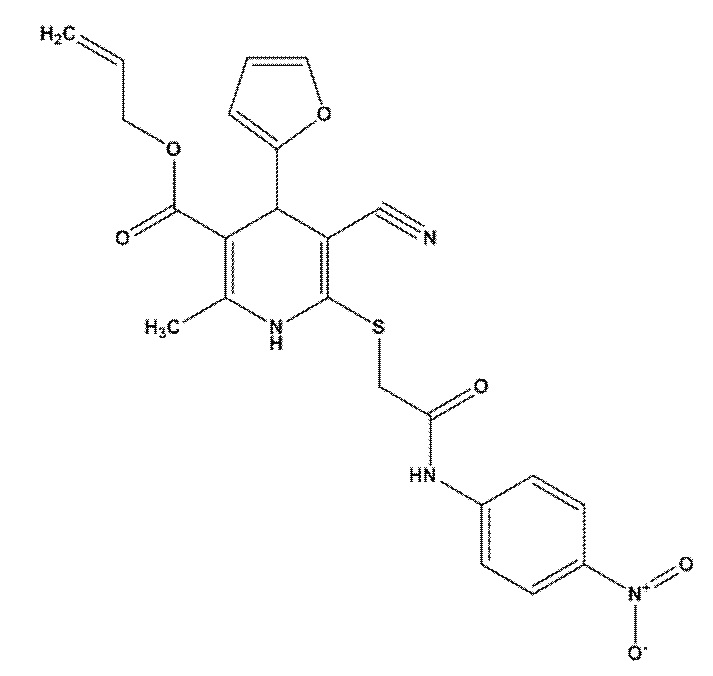
Изобретение относится к области медицинской и фармацевтической химии, фармакологии, а именно к применению органического соединения, аллил 2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилата формулы (I), в качестве анальгетического средства, обладающего антиноцицептивной активностью, которое может быть использовано в медицине и ветеринарии.
Современная медицина ежедневно сталкивается с проблемами, связанными с фармакокоррекцией болевого синдрома. Боль представляет собой самый частый феномен, с которым имеют дело врачи самых разных специальностей, составляя от 11 до 40% всех обращений к врачу в системе первичной медицинской помощи (данные ВОЗ). Около 70-90% всех заболеваний связано с болью. Являясь симптомом большинства заболеваний человека, боль затрагивает различные аспекты деятельности человека и общества в целом (медицинские, социальные и экономические).
Болевой синдром, как реакция на повреждающие (ноцицептивные) воздействия, представляет собой важнейший биологический феномен, непосредственно обеспечивающий выживание организма в экстремальных условиях [Болевые синдромы в неврологии: учебное пособие / Р.В. Магжанов, Р.А. Ибатуллин. - Уфа: ФГБОУ ВО БГМУ Минздрава России, 2021. - С. 6-8].
Практически половина населения нашей планеты ежедневно сталкиваются с острой, а также хронической, в том числе рецидивирующей болью [Андреева Г.О., Емельянов А.Ю., Евдокимов В.И. Хронический болевой синдром при заболеваниях периферической нервной системы (клиника, психопатологические нарушения, лечение и прогноз): монография. - СПб.: Политехника сервис, 2014. С. 29-33]. Данный симптом сопровождает практически 70% всех известных заболеваний и патологических состояний [Ахмадеева Л.Р., Ахмадеева Э.Н., Вейцман Б.А., Раянова Г.Ш., Липатова Е.Е., Мунасыпова Р.Р., Валеева Д.С. Боль как междисциплинарная проблема от периода новорожденности до пожилого возраста // ПМ. 2013. №1 (66). С. 70-71].
По данным отечественных эпидемиологических исследований, распространение хронического болевого синдрома (без учета онкологических заболеваний), составляет не менее 40% среди взрослого, работоспособного населения, и эти цифры имеют тенденцию к неуклонному росту [Шабалов В.А., Исагулян Э.Д. Нейромодуляция - современные методы хирургии боли // ТМЖ. 2008. №1 (31). С. 16-17].
В настоящее время алгоритм терапии болевого синдрома включает в себя применение следующих групп лекарственных средств: местные анестетики (для кратковременного локального купирования болевого синдрома), наркотические и ненаркотические анальгетики, а также препараты, косвенно влияющие на восприятие боли (седативные средства растительного и синтетического происхождения, транквилизаторы и др.) совместно со вспомогательными (адъювантными) препаратами [Принципы применения анальгетических средств при острой и хронической боли. М.: ФГБУ «МНИОИ им. П.А.Герцена Минздравсоцразвития России», 2010. - С. 64-78].
Наряду с высокой терапевтической активностью, ненаркотические анальгетики проявляют и множество нежелательных (побочных) фармакологических эффектов, таких как геморрагии, тромбоцитопения, угнетение лейкопоэза, задержка ионов натрия и воды, метгемоглобинемия, развитие синдрома Рея (особенно у детей), синдрома Видаля и др.
Высок риск возникновения аллергических реакций, бронхоспазма, а также доказанная нефротоксичность, гепатотоксичность, гематотоксичность, выраженное ульцерогенное действие на фоне применения нестероидных противовоспалительных средств, с точки зрения «риск-польза» в некоторых случаях ставит под сомнение применение того или иного препарата из данной фармакотерапевтической группы [Дядык А.И., Куглер Т.Е. Побочные эффекты нестероидных противовоспалительных препаратов // Consilium Medicum. 2017. №12. С. 94-98].
Поэтому особой актуальностью характеризуется проблематика адекватного, эффективного и безопасного обезболивания в реальной клинической практике. Один из векторов современных фармакологических исследований направлен на поиск новых активных и эффективных, безопасных фармацевтических субстанций, обладающих высокой специфичностью относительно предполагаемых биомишеней. Одними из таких потенциальных субстанций являются частично гидрированные производные α-цианотиоацетамида, которые обладают высокой анальгетической и противовоспалительной активностью. Данные свойства определяют перспективность новых соединений с точки зрения их биологической активности [Кетова Е.С., Бибик Е.Ю., Батищева Г.А., Кривоколыско С.Г. Комплексная оценка гепатопротекторной активности новых производных альфа-цианотиоацетамида // Дальневосточный медицинский журнал. 2024. №1. С. 22-27; Бибик Е.Ю., Олейник И.С., Панков А.А., Фролов К.А., Доценко В.В., Кривоколыско С.Г. Исследование новых производных 1,4-дигидропиридина как потенциальных средств с болеутоляющей активностью в тесте орофациальной тригеминальной боли: экспериментальное доклиническое рандомизированное исследование // Кубанский научный медицинский вестник. 2023. №30 (2). С. 64-75; Бибик И.В., Панков А.А., Фролов К.А., Доценко В.В., Кривоколыско С.Г., Бибик Е.Ю. Исследование гематотоксичности новых производных конденсированных 3-аминотиено[2,3-b]пиридинов и 1,4-дигидропиридинов с высокой анальгетической активностью // Вестник Авиценны. 2023. №4. С. 499-507].
Задача, на решение которой направлено изобретение, заключается в установлении болеутоляющей активности среди новых 1,4-дигидропиридинов.
Поставленная задача решается применением аллил 2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилата (I) (название по IUPAC - allyl 5-cyano-4-(furan-2-yl)-2-methyl-6-((2-((4-nitrophenyl)amino)-2-oxoethyl)thio)-1,4-dihydropyridine-3-carboxylate; Commercial Substance ID 10064964, CAS Registry Number 799770-28-8 [reaxys.com] в качестве анальгетического средства, которое обладает более выраженными антиноцицептивными свойствами в сравнении с эталонными препаратами - метамизолом натрия и мефенаминовой кислотой.
Соединение (I) было получено в НИЛ «Химэкс» ФГБОУ ВО «Луганский государственный университет им. Владимира Даля» по методике, описанной для аналогичных соединений [Krivokolysko D.S., Dotsenko V.V., Bibik E.Yu., Samokish A.A., Venidiktova Yu.S., Frolov K.A., Krivokolysko S.G., Vasilin V.K., Pankov A.A., Aksenov N.A., Aksenova I.V. New 4-(2-Furyl)-1,4-dihydronicotinonitriles and 1,4,5,6-Tetrahydronicotinonitriles: Synthesis, Structure, and Analgesic Activity // Russian Journal of General Chemistry. 2021. Vol. 91. No 9. P. 1646-1660; Krivokolysko D.S., Dotsenko V.V., Bibik E.Yu., Samokish A.A., Venidiktova Yu.S., Frolov K.A., Krivokolysko S.G., Pankov A.A., Aksenov N.A., Aksenova I.V. New Hybrid Molecules Based on Sulfur-Containing Nicotinonitriles: Synthesis, Analgesic Activity in Acetic Acid-Induced Writhing Test, and Molecular Docking Studies // Russian Journal of Bioorganic Chemistry. 2022. Vol. 48. No 3. P. 628-635; Tilchenko D.A., Bibik E.Yu., Dotsenko V.V., Krivokolysko S.G., Frolov K.A., Aksenov N.A., Aksenova I.V.. Synthesis and Hypoglycemic Activity of New Nicotinonitrile-Furan Molecular Hybrids // Russian Journal of Bioorganic Chemistry. 2024. Vol. 50. No. 2. P. 554-570].
Наиболее схожими по структуре описанному соединению являются различные биологически активные вещества, послужившие объектами для создания анальгетических, гипотензивных, противоаллергических, диуретических лекарственных средств [Gouda M.A., Hussein B.H., Helal M.H. [et al.] A Review: Synthesis and Medicinal Importance of Nicotinonitriles and Their Analogous // Journal of Heterocyclic Chemistry. 2018. Vol. 55 (7). P. 1524-1553; Rucins М., Plotniece А., Bernotiene Е. [et al.] Recent Approaches to Chiral 1,4-Dihydropyridines and their Fused Analogues // Catalysts. 2020. Vol. 10 (9). P. 1019; Ling Y., Hao Z.Y., Liang D. [et al.] The Expanding Role of Pyridine and Dihydropyridine Scaffolds in Drug Design // Drug Design, Development and Therapy. 2021. Vol. 15. P. 4289-4338; Salem M.A., Helel M.H., Gouda M.A. [et al.] Overview on the synthetic routes to nicotine nitriles // Synthetic Communications Reviews. 2018. Vol. 48 (4). P. 345-374].
Впервые было установлено, что биологически активное вещество аллил 2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилат (I) проявляет анальгетическую активность в эксперименте на лабораторных животных (белых беспородных половозрелых крысах-самцах) при сравнении с препаратами из группы нестероидных противовоспалительных средств - мефенаминовой кислотой и метамизолом натрия, превосходя референтные образцы.
Фармакологические свойства заявленного соединения
Пример 1
Предварительно осуществленный нами виртуальный биоскрининг и предикторный анализ согласно [Yang J., Kwon S., Bae Park S.H. [et al.] GalaxySagittarius: Structure- and Similarity-Based Prediction of Protein Targets for Druglike Compounds // Journal of Chemical Information and Modeling. 2020. Vol. 60. P. 3246-3254; Gfeller D., Grosdidier A., Wirth М. [et al.] SwissTargetPrediction: a web server for target prediction of bioactive small molecules // Nucleic Acids Research. 2014. Vol. 42 (1). P. 32-39; Gfeller D., Michielin O., Zoete V. Shaping the interaction landscape of bioactive molecules // Bioinformatics. 2013. Vol. 29. P. 3073-3079] показали, что механизм действия аллил 2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилат (I) связан с тем, что его молекулы с высокой степенью вероятности воздействуют на такие рецепторы как арахидонат-5-липоксигеназа, циклооксигеназа-2 и аденозиновые рецепторы A1, A2a, A2b, и, как следствие, потенциально способны уменьшать болевую чувствительность при этом оказывая противовоспалительный, жаропонижающий и антиэкссудативный эффект [Бочева А.А., Кривоколыско С.Г. Исследование антипиретической активности новых частично гидрированных пиридинов, производных α-цианотиоацетамида // Актуальные проблемы экспериментальной и клинической медицины. Сборник статей 81-й международной научно-практической конференции молодых ученых и студентов. Волгоград, 2023. С. 425-426; Бибик Е.Ю., Бущик А.А., Самокиш А.А., Венедиктова Ю.С., Кривоколыско Д.С. и др. Эффективность новых производных 1,4-дигидротиопиридинов в тесте орофасциальной тригеминальной боли // Безопасность фармакотерапии: Noli Nocere! Сборник тезисов IV Всероссийской научно-практической конференции с международным участием. Казань, 2021. С. 19-21].
Пример 2
Экспериментальное исследование реализовано на половозрелых беспородных крысах-самцах, массой 280±10 г, полученных из вивария федерального государственного бюджетного образовательного учреждения высшего образования «Луганский государственный медицинский университет имени Святителя Луки» Министерства Здравоохранения Российской Федерации (ФГБОУ ВО «ЛГМУ им. Свт. Луки Минздава России) в условиях специализированной лаборатории кафедры фундаментальной и клинической фармакологии ФГБОУ ВО «ЛГМУ им. Свт. Луки Минздава России в соответствии с руководством ARRIVE (Animal Research: Reporting of In Vivo Experiments) и правилами работы с животными на основе положений Хельсинкской декларации и рекомендаций, содержащихся в Директиве ЕС 86/609/ECC и Конвенции Совета Европы по защите позвоночных животных, используемых для экспериментальных и других научных целей, а также в соответствии с правилами качественной лабораторной практики при проведении доклинических исследований в Российской Федерации (Статья 11 Федерального закона №61-ФЗ от 12.04.2010 «Об обращении лекарственных средств», с приказом Министерства здравоохранения Российской Федерации от 1 апреля 2016 года № 199н (Об утверждении Правил надлежащей лабораторной практики) и ГОСТ 33044-2014 «Принципы надлежащей лабораторной практики», утвержденному Приказом Федерального агентства по техническому регулированию и метрологии № 1700-ст от 20 ноября 2014 г.).
Исследования одобрены комиссией по биоэтике федерального государственного бюджетного образовательного учреждения высшего образования «Луганский государственный медицинский университет имени Святителя Луки» Министерства Здравоохранения Российской Федерации (Российская Федерация, г. Луганск, кв. 50-летия Обороны Луганска, д. 1г), протокол № 5 от 10.12.2022 г.
Распределение на группы производилось случайным образом с использованием «метода конвертов». Животные были распределены на контрольную (с моделируемой орофациальной тригеминальной болью), две референтные группы (получавших препараты-сравнения метамизол натрия и мефенаминовую кислоту), а также опытную группу (получавших оригинальное производное α-цианотиоацетамида). Каждая группа состояла из 8 животных одного пола, а также минимальное для достижения цели и решения задач исследования количество экспериментальных групп (общее количество лабораторных животных).
Животные содержались в одинаковых условиях, получали корм и воду в свободном доступе.
Определение анальгетической активности нового производного цианотиоацетамида производилось с помощью двух тестов, согласно рекомендациям по доклиническому исследованию [Руководство по экспериментальному доклиническому изучению новых фармакологических веществ / Под ред. Г.У. Хабриева. - М.: Медицина. - 2005. - 832 с.]:
а) орофациальной тригеминальной боли, моделируемой подкожным введением 0,1 мл 5% раствора формалина в область вибрисс у подопытных животных. Болеутоляющий эффект оценивался по фиксации количества чесательных движений передними лапами орофациальной области за минуту, которое подсчитывалось через 10-, 15- и 20-минутный интервал времени после введения 0,1 мл 5% раствора формалина в область вибрисс;
б) тепловой иммерсии хвоста. Эксперимент основан на спинальном флексорном рефлексе в ответ на погружение хвоста крысы в горячую воду, нагретую в среднем до 50…53°С, с измерением временного промежутка латентного периода реакции.
Исследуемое конденсированное производное дигидропиридина вводили внутрижелудочно в дозе 5 мг/кг за 1,5 часа до моделирования острого болевого синдрома в экспериментах in vivo. В качестве препарата сравнения использован метамизол натрия, вводимый в дозе 7 мг/кг внутри астрально, а также мефенаминовую кислоту, вводимую в дозе 5 мг/кг внутригастрально.
Показателями анальгетического эффекта считались: количество чесательных движений в тесте орофациальной тригеминальной боли и достоверное увеличение латентного периода реакции после введения исследуемых веществ в тестах тепловой иммерсии хвоста и горячей пластины.
Анальгетическую активность под действием аллил 2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилата сравнивали с таковой у препаратов сравнения - метамизола натрия (анальгина) и мефенаминовой кислоты.
Для статистической оценки полученных данных в ходе исследования использовали программу Microsoft Exel 2019, онлайн калькулятора для расчета статистических критериев https://medstatistic.ru/calculators.html , а также лицензионной компьютерной программы Statistica 10.0 для Windows.
В процессе оценки биологических показателей, в опытах на беспородных лабораторных животных, рекомендовано использование непараметрических методов статистической обработки данных, ввиду ненормального характера распределения выборки [Луговик И.А., Макарова М.Н. Токсикологические исследования. Референтные интервалы массовых коэффициентов внутренних органов на выборке, состоящей из 1000 аутбредных крыс. Лабораторные животные для научных исследований. 2021. С. 1. https://doi.org/10.29296/2618723X-2021-01-01].
Однородность и достоверность экспериментальных данных оценивались коэффициентом вариации V и T (W)-критерием Уилкоксона. Если коэффициент вариации менее 10%, то изменчивость ряда данных принято считать незначительной.
При обработке экспериментальных данных определялись: среднее арифметическое показтелей n, а, t; дисперсия значений σ2 вокруг среднего арифметического и среднеквадратическое отклонение σ.
Данные экспериментальных исследований анальгетической активности в трех фармакологических тестах представлены в таблицах 1, 2.
Таблица 1. Результаты фармакологического теста орофациальной тригеминальной боли по выявлению анальгетической активности нового оригинального производного 1,4-дигидропиридинов
количественные показатели (n, a, t), дисперсия σ2, среднеквадратическое отклонение σ, коэффициент вариации V, %
σ2 = 70,36;
σ = 8,39;
V = 9,23%
σ2 = 53,19;
σ = 7,29;
V = 11,53%
σ2 = 90,48;
σ = 9,51;
V = 25,97%
(метамизол натрия)
σ2 = 33,3;
σ = 5,8;
V = 9,6%
σ2 = 6,5;
σ = 2,5;
V = 6,8%
σ2 = 84,0;
σ = 9,2;
V = 46,5%
(мефенаминовая кислоты)
σ2 = 73,19;
σ = 8,55;
V = 21,25%
σ2 = 65,11;
σ = 8,07;
V = 32,12%
σ2 = 44,75;
σ = 6,69;
V = 49,55%
σ2 = 21,73;
σ = 4,66;
V = 21,81%
σ2 = 3,69;
σ = 1,92;
V = 17,86%
σ2 = 3,98;
σ = 1,99;
V = 84,05%
*** p=0,0140
*** p=0,0142
*** p=0,0140
** - достоверно в сравнении с референтной группой №1
*** - достоверно в сравнении с референтной группой №2
Оценивая данные, приведенные в таблице 1, можно сделать вывод о том, что в тесте моделирования орофациальной тригеминальной боли опытное соединение снижает частоту чесательных движений в 5,5 раз по отношению к контрольной группе, в 3,4 раза превосходя результаты, полученные в группе, получавшей препарат метамизол натрия и в 2,3 раза активнее препарата-референта мефенаминовой кислоты.
В тесте тепловой иммерсии хвоста - опытный образец (новое производное 1,4-дигидропиридина) увеличивает латентный период одергивания хвоста при контакте с внешним раздражителем в 1,95 раз по отношению к группе контроля. Превосходит по активности метамизол натрия в 1,2 раза, а мефенаминовую кислоту в 1,4 раза (таблица 2).
Таблица 2. Результаты фармакологического теста тепловой иммерсии хвоста при погружении в горячую воду по выявлению анальгетической активности нового оригинального производного 1,4-дигидропиридинов
количественные показатели (n, a, t), дисперсия σ2, среднеквадратическое отклонение σ, коэффициент вариации V, %
σ2 = 1,98
σ = 1,4;
V = 13,6%
(метамизол натрия)
σ2 = 2,79
σ = 1,67;
V = 9,96%
(мефенаминовая кислоты)
σ2 = 3,2
σ = 10,25;
V = 22,08%
σ2 = 2,82
σ = 7,94;
V = 13,91%
Таким образом, фармакологическая коррекция новым производным 1,4-дигидропиридина - аллил 2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилатом (I), острого болевого синдрома, смоделированного в двух классических фармакологических тестах на белых крысах, характеризуется высокой степенью выраженности антиноцицептивной активности, превышая таковую у препаратов групп-сравнения - мефенаминовой кислоты и метамизола натрия.
В ходе экспериментальных исследований нежелательных явлений зафиксировано не было.
Резюмируя вышеизложенные данные статистической обработки и выводы, описанные факты и наблюдения отчетливо демонстрируют способность аллил 2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилата (I) проявлять в эксперименте in vivo в тестах орофациальной боли и тепловой иммерсии хвоста отчетливо выраженную болеутоляющую активность. Причем, по степени выраженности анальгетических свойств исследуемое соединение превосходило препараты сравнения в 1,12-5,5 раз.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-МЕТИЛ-N-(2-МЕТИЛФЕНИЛ)-4-(2-ФУРИЛ)-5-ЦИАНО-6-({ 2-[(4-ЭТОКСИФЕНИЛ)АМИНО]-2-ОКСОЭТИЛ} ТИО)-1,4-ДИГИДРОПИРИДИН-3-КАРБОКСАМИД, ПРОЯВЛЯЮЩИЙ АНАЛЬГЕТИЧЕСКИЕ СВОЙСТВА | 2023 |
|
RU2813896C1 |
| ЭТИЛОВЫЙ ЭФИР 4-(2-МЕТИЛ-6-{ [2-(ДИФЕНИЛАМИНО)-2-ОКСОЭТИЛ]ТИО} -4-ФУР-2-ИЛ-5-ЦИАНО-1,4-ДИГИДРОПИРИДИН-3-КАРБОКСАМИДО)БЕНЗОЙНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНЫЕ СВОЙСТВА | 2022 |
|
RU2792595C1 |
| Применение 2-метил-N-(2-метилфенил)-4-(2-фурил)-5-циано-6-({ 2-[(4-этоксифенил)амино]-2-оксоэтил} тио)-1,4-дигидропиридин-3-карбоксамида в качестве гипогликемического, гиполипидемического средства, способствующего снижению массы тела | 2023 |
|
RU2812569C1 |
| ПРИМЕНЕНИЕ 3-АМИНО-4-(5-МЕТИЛ-2-ФУРИЛ)-5,6,7,8-ТЕТРАГИДРОТИЕНО[2,3-B]ХИНОЛИН-2-ИЛ](ФЕНИЛ)МЕТАНОН В КАЧЕСТВЕ ПРОТИВОВОСПАЛИТЕЛЬНОГО СРЕДСТВА | 2023 |
|
RU2812570C1 |
| Способ получения 6-амино-4-арил-2-тиоксо-1,2-дигидропиридин-3,5-дикарбонитрилов | 2022 |
|
RU2792625C1 |
| Применение бензил 6-({ 2-[(3,4-диметилфенил)амино]-2-оксоэтил} тио)-2-метил-4-(4-хлорфенил)-5-циано-1,4-дигидропиридин-3-карбоксилата в качестве гепатопротекторного средства | 2021 |
|
RU2755349C1 |
| Фуран-2-илметил-2-(2-(дифенилметилен)гидразинил)-5,5-диметил-4-оксогекс-2-еноат, обладающий анальгетической и противовоспалительной активностью | 2021 |
|
RU2784447C2 |
| 4-ОКСО-N-(ФУРАН-2-ИЛМЕТИЛ)-4-(4-ХЛОРФЕНИЛ)-2-((3-ЦИАНО-4,5,6,7-ТЕТРАГИДРОБЕНЗО[b]ТИОФЕН-2-ИЛ)АМИНО)БУТ-2-ЕНАМИД, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2022 |
|
RU2798425C1 |
| N-(5-БРОМПИРИДИЛ)АМИДЫ 4-АРИЛ-4-ОКСО-2-(ОКСО-1,2-ДИФЕНИЛЭТИЛИДЕНГИДРАЗИНО)БУТ-2-ЕНОВЫЕ КИСЛОТЫ, ОБЛАДАЮЩИЕ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2537381C1 |
| 2-(5-ЭТИЛ-1,3,4-ТИАДИАЗОЛИЛ)АМИД 2-(4-БРОМФЕНИЛ)-4-ОКСО-4-ФЕНИЛ-2-БУТЕНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2549572C2 |
Изобретение относится к области медицинской или фармацевтической химии и фармакологии. Предложено применение аллил-2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилата формулы (I), указанной ниже, в качестве анальгетического средства. Технический результат изобретения заключается в выраженном анальгетическом действии соединения формулы (I). 2 табл., 2 пр. 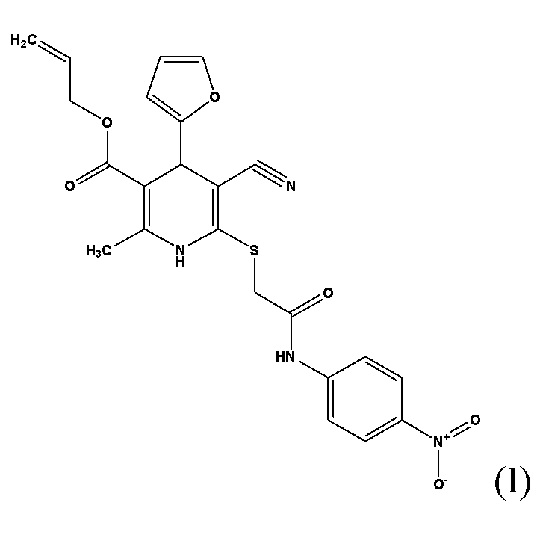
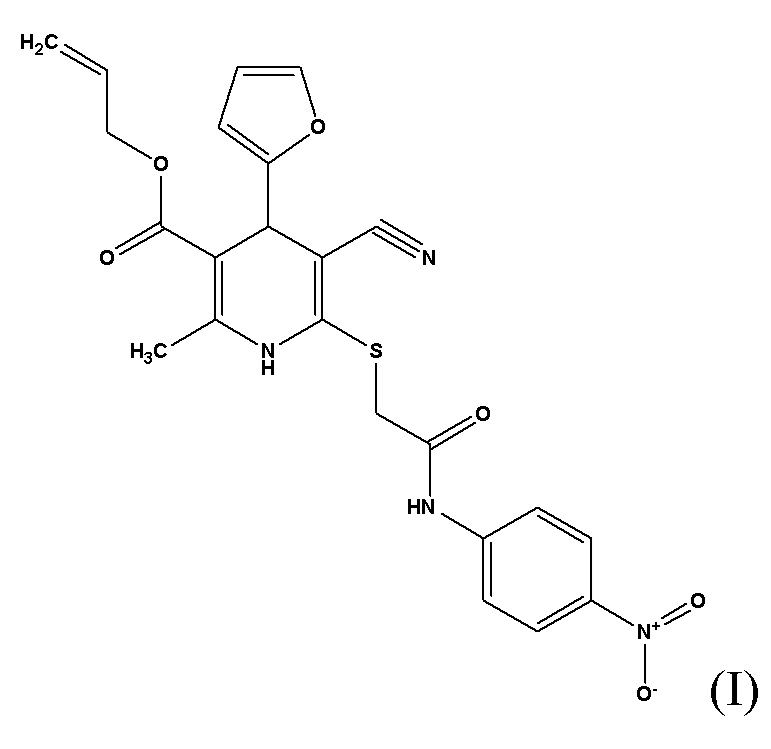
Применение аллил-2-метил-6-((2-((4-нитрофенил)амино)-2-оксиэтил)тио)-5-циано-4-(фуран-2-ил)-1,4-дигидропиридин-3-карбоксилата формулы (I) в качестве анальгетического средства.
| КРИВОКОЛЫСКО Д.С | |||
| и др | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Карбюратор | 1923 |
|
SU1359A1 |
| КРИВОКОЛЫСКО Д.С | |||
| и др | |||
| Новые гибридные молекулы на основе серосодержащих никотинонитрилов: синтез, анальгетическая активность in vivo в тесте | |||
Авторы
Даты
2025-05-22—Публикация
2024-08-07—Подача