Изобретение относится к бесферментному электрохимическому анализу, а именно, к определению содержания хлорамфеникола в водной среде. Изобретение создано с целью сокращения этапов проведения анализа с использованием малых количеств органических растворителей. Изобретение может быть использовано в экологическом мониторинге и пищевой промышленности.
Известна методика определения содержания остаточных количеств хлорамфеникола в сырье животного происхождения и пищевых продуктах [Полянских Е. И. [и др.]. Методика Контроля Остаточного Содержания Хлорамфеникола (Левомицетина) В Пищевой Продукции Животного Происхождения // Журнал Аналитической Химии. 2019. № 6 (74). C. 455-463]. Методика включает экстракцию аналита этилацетатом из раствора пробы в 4 М растворе сульфата аммония, упаривание органического растворителя, растворение полученного сухого остатка в воде, обезжиривание н-гексаном, концентрирование методом твердофазной экстракции и количественное определение методом ВЭЖХ-МС/МС. Недостатком описанной методики является длительность пробоподготовки и многостадийность анализа, с использованием большого количества органических растворителей и дорогостоящего оборудования.
Известен способ кулонометрического определения хлорамфеникола (торговое наименование “Левомицетин”) в лекарственных формах [Зиятдинова Г. К. [и др.]. КУЛОНОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ЛЕВОМИЦЕТИНА В ЛЕКАРСТВЕННЫХ ФОРМАХ // Ученые записки Казанского университета. Серия Естественные науки. 2007. № 4 (149). C. 98-195]. В данном способе электрогенерированные галогены - хлор, бром и йод - были использованы для установления возможности количественного реагирования и стехиометрии реакций с левомицетином. Установлено, что только восстановленный левомицетин взаимодействует с электрогенерированными галогенами в условиях гальваностатической кулонометрии. Результаты кулонометрического титрования позволили установить, что восстановленный левомицетин взаимодействует с электрогенерированным бромом в соотношении 1 : 2. Недостатком представленного способа является многостадийность анализа и косвенное определение левомицетина с помощью электрогенерированных галогенов.
Предложен способ определения хлорамфеникола в молоке и меде с использованием прямого конкурентного иммуноферментного анализа (ИФА) [Wu S. W. [и др.]. Sensitive enzyme-linked immunosorbent assay and gold nanoparticle immunochromatocgraphic strip for rapid detecting chloramphenicol in food // Journal of Food Safety. 2020. № 2 (40)]. Для его осуществления антитела к хлорамфениколу, разбавленные фосфатным буферным раствором (ФБР), помещали в лунки планшета для иммуноферментного анализа, затем инкубировали 1 час при 37°, затем четыре раза промывали лунки смесью буферного раствора и реактива Твин-20 (Твин-ФБР). Далее в лунки добавляли раствор бычьего сывороточного альбумина в ФБР и инкубировали 30 мин при 37° для блокирования неспецифических центров связывания антител. Непрореагировавшие компоненты удалялись четырехкратным промыванием лунок раствором Твин-ФБР. Затем в лунки добавляли исследуемый образец с добавлением конъюгата «хлорамфеникол-пероксидаза хрена» с последующей инкубацией в течение 1 часа и последующим промыванием. После добавления субстрата 3,3’,5,5’-тетраметилбензидина (для протекания иммуноферментной реакции) и выдерживания луночного планшета в темноте в течение 20 минут в лунки добавляли соляную кислоту для прекращения ферментативной реакции и регистрировали спектры поглощения с помощью прибора Vmax® (автоматического ИФА ридера). Кроме описанного способа авторами предложены иммунохроматографические тест-полоски для чувствительного определения наличия хлорамфеникола в пробах с использованием меченых золотыми наночастицами антител к хлорамфениколу и конъюгатов “хлорамфеникол-овальбумин”. Однако недостатками указанных способов и подходов является наличие биологических компонентов (антитела, ферменты, белки), при использовании которых обязательно соблюдение жестких условий хранения. Еще одним недостатком является многостадийность иммуноферментного анализа.
Недостатками вышеописанных методов и подходов являются использование дорогостоящего лабораторного оборудования, длительность и многостадийность анализа, особые требования к хранению и использованию биологических реагентов с необходимостью предварительного получения и очистки конъюгатов.
Достоинством электрохимических способов определения является возможность детектирования прямого сигнала от хлорамфеникола в мутных и окрашенных пробах малого объема, что позволяет существенно упростить пробоподготовку из-за необязательной дополнительной очистки пробы.
В качестве сенсорной молекулы был использован 3,6-бис[(триметилсилил)этинил]-9Н-карбазол, полученный с выходом 82% по ранее описанной в литературе методике [S. Shanmugaraju, A. K. Bar, K.-W. Chi, P. S. Mukherjee. Coordination-Driven Self-Assembly of Metallamacrocycles via a New PtII2 Organometallic Building Block with 90° Geometry and Optical Sensing of Anions. // Organometallics 2010, 29, 2971-2980]. В литературе известно о применении данного соединения для получения кремнийсодержащих арилацетиленовых смол с высокой термической устойчивостью [L. Wan, K. Guo, J. Zhu, F. Wang, Y. Zhu, S, Deng, H. Qi. Improvement of the oxidation resistance of siliconcontaining arylacetylene resins upon the introduction of carbazoles. // Journal of Applied Polymer Science 2021, 138 (1), 49642]; кроме того, описано получение к координационных соединений на основе платины (II), которые могут быть использованы как флуоресцентные сенсоры на пирофосфат анион (Р2О74-) [R. A. Al-Balushi, A. Haque, M. Jayapal, M. K. Al-Suti, J. Husband, M. S. Khan, O. F. Koentjoro, K. C. Molloy, J. M. Skelton, P. R. Raithby. Experimental and Theoretical Investigation for the Level of Conjugation in Carbazole-Based Precursors and Their Mono, Di, and Polynuclear Pt(II) Complexes. // Inorganic Chemistry 2016, 55 (13), 6465-6480; S. Shanmugaraju, A. K. Bar, K.-W. Chi, P. S. Mukherjee. Coordination-Driven Self-Assembly of Metallamacrocycles via a New PtII2 Organometallic Building Block with 90° Geometry and Optical Sensing of Anions. // Organometallics 2010, 29, 2971-2980]; также данные соединения были применены для создания молекулярных систем хранения солнечной энергии на основе обратимой фотоизомеризации метастабильных изомеров [M. Mansø, B. E. Tebikachew, K. Moth-Poulsen, M. Brøndsted Nielsen. Heteroaryl-linked norbornadiene dimers with redshifted absorptions. // Organic & Biomolecular Chemistry 2018, 16 (31), 5585-5590]. Наиболее близким вариантом использования 3,6-бис[(триметилсилил)этинил]-9Н-карбазола является его использование в качестве высокоэффективного флуоресцентного сенсора на нитроароматические взрывчатые вещества [S. Shanmugaraju, S. A. Joshi, P. S. Mukherjee. Fluorescence and visual sensing of nitroaromatic explosives using electron rich discrete fluorophores. // J. Mater. Chem., 2011, 21, 9130-9138].
Предлагаемый способ определения содержания хлорамфеникола в анализируемой водной среде с использованием углеродсодержащего рабочего электрода, модифицированного 3,6-бис[(триметилсилил)этинил]-9Н-карбазолом, включает молекулярное распознавание данной органической молекулой молекулы хлорамфеникола в водной среде путем погружения электрода в электрохимическую ячейку, содержащую 0,05% раствор 3,6-бис[(триметилсилил)этинил]-9Н-карбазола в ацетонитриле, наложения трех циклических разверток потенциала в диапазоне 0,3 В до 1,8 В для формирования на электроде электроосажденного слоя бис((триметилсилил)этинил)-9Н-карбазола, перемещения электрода в водный анализируемый раствор, выдерживания в нем в течение 30 минут, затем детектирование прямого электрохимического сигнала от хлорамфеникола путем переноса электрода в водный раствор фонового электролита 0.1 M KCl, регистрации линейной вольтамперограммы в диапазоне от 0 В до -0.8 В и определение содержания хлорамфеникола по величине тока электровосстановления нитрогруппы в структуре хлорамфеникола с использованием метода градуировочного графика, распространенного в аналитической химии.
Сущность метода градуировочного графика можно изложить следующим образом: «В координатах аналитический сигнал-содержание компонента строят график с использованием образцов сравнения с различным, точно известным содержанием определяемого компонента. Затем, измерив аналитический сигнал анализируемой пробы, находят содержание определяемого компонента по градуировочному графику» [стр. 27, Основы аналитической химии. В 2 т. Т. 1 : учеб. для студ. учреждений высш. проф. образования / [Т.А.Большова и др.] ; под ред. Ю.А.Золотова. - 5 е изд., стер. - М. : Издательский центр «Академия», 2012 - 384 с. ISBN 978 5 7695 9124 2].
Общая схема процедуры анализа приведена в приложении 1.
Таким образом, предлагаемое техническое решение направлено на создание на поверхности рабочего электрода тонкого рецепторного слоя на основе молекул 3,6-бис[(триметилсилил)этинил]-9Н-карбазола. Благодаря ковалентному взаимодействию данной молекулы с хлорамфениколом обеспечивается селективность и чувствительность анализа с осуществлением малого количества стадий.
Способ иллюстрируется следующими примерами.
Пример 1.
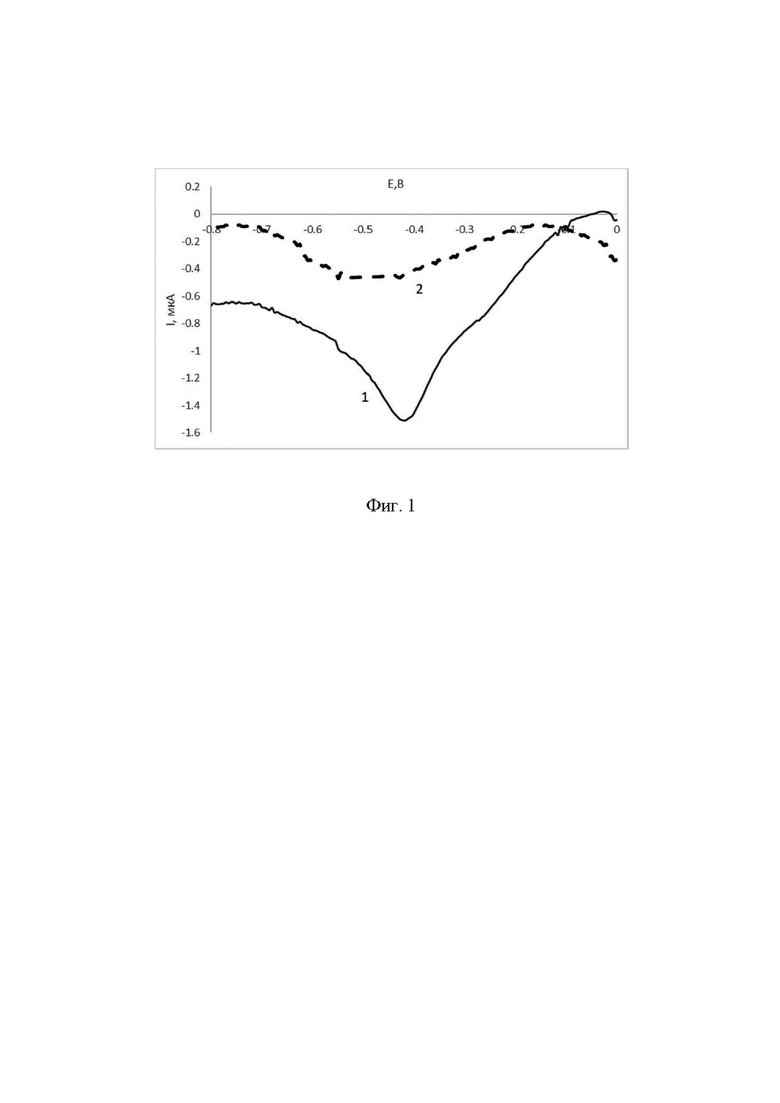
В электрохимическую ячейку, содержащую 2,5 мл 0,05% раствор 3,6-бис[(триметилсилил)этинил]-9Н-карбазола в ацетонитриле погружают углеродсодержащий электрод. Затем накладывают три последовательных циклических развертки потенциала в диапазоне 0,3 В до 1,8 В для формирования на электроде электроосажденного рецепторного слоя 3,6-бис((триметилсилил)этинил)-9Н-карбазола. Об успешном электроосаждении слоя свидетельствует снижение токов пиков молекулы при каждом последующем цикле. Затем электрод переносят в водный анализируемый раствор (смывы с мяса), выдерживают в нем в течение 30 минут, после этого переносят электрод в водный раствор фонового электролита 0.1 M KCl, не содержащий хлорамфеникола и регистрируют линейную развертку потенциала в диапазоне от 0В до -0,8 В (поскольку известно, что нитрогруппа в структуре хлорамфеникола электровосстанавливается в данном диапазоне потенциалов [Svalova T. S. и др. Electrochemical behavior of chloramphenicol on carbon electrodes in a microelectrochemical cell // Chim. Techno Acta. 2022. Т. 9. № 4. С. 5-9.]). Измеряемой величиной является значение тока электровосстановления нитрогруппы, последующее определение содержания хлорамфеникола осуществляется с использованием метода градуировочного графика. Градуировочная зависимость между величиной регистрируемого тока и концентрацией хлорамфеникола в модельных суспензиях (смывах с мяса с известной добавленной концентрацией хлорамфеникола): I, мкА = (-0.2026±0,0351)⋅CXA,мкМ - (1,1816±0,3402). Зарегистрированная величина тока составила -1.2525 мкА, следовательно, в анализируемой пробе обнаружено 0,35 мкМ хлорамфеникола
На фигуре 1 приведены линейные вольтамперограммы, зарегистрированные на планарном углеродсодержащем электроде с электроосажденным рецепторным слоем до (1) и после (2) выдерживания в анализируемом растворе.
Пример 2.
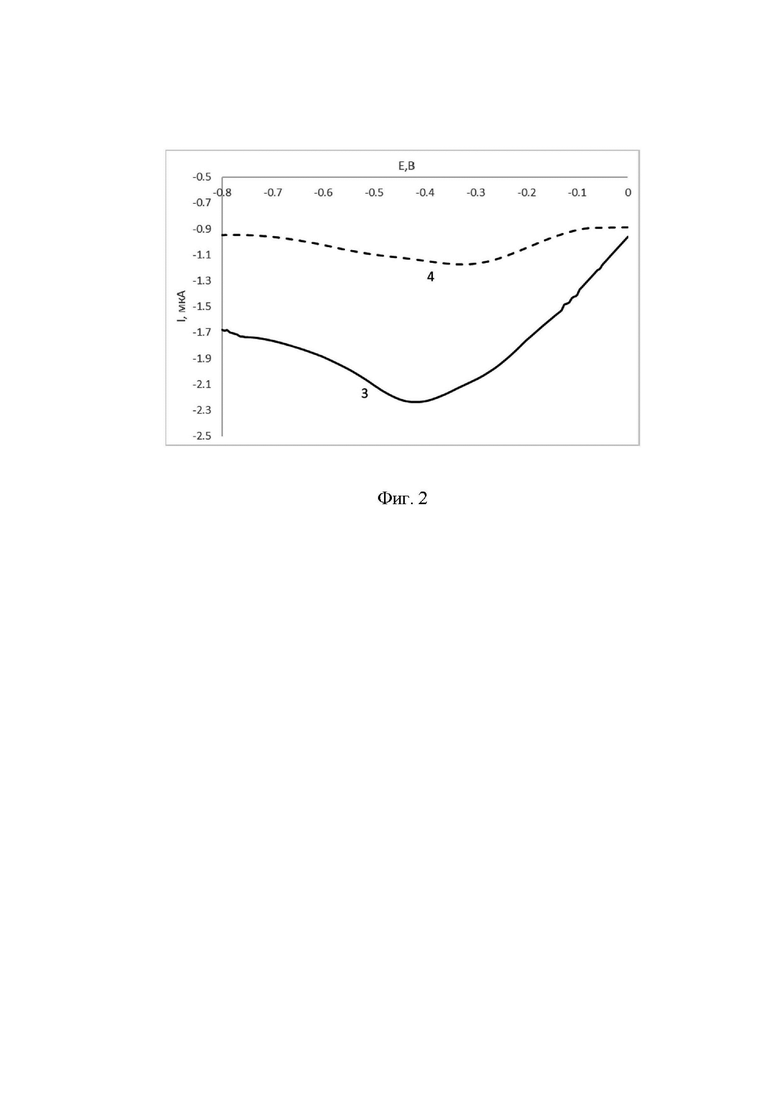
В электрохимическую ячейку, содержащую 2,5 мл 0,05% раствор 3,6-бис[(триметилсилил)этинил]-9Н-карбазола в ацетонитриле погружают углеродсодержащий электрод. Затем накладывают три последовательных циклических развертки потенциала в диапазоне 0,3 В до 1,8 В для формирования на электроде электроосажденного рецепторного слоя 3,6-бис((триметилсилил)этинил)-9Н-карбазола. Об успешном электроосаждении слоя свидетельствует снижение токов пиков молекулы при каждом последующем цикле. Затем электрод переносят в водный анализируемый раствор (молочная сыворотка), выдерживают в нем в течение 30 минут, после этого переносят электрод в водный раствор фонового электролита 0.1 M KCl, не содержащий хлорамфеникола и регистрируют линейную развертку потенциала в диапазоне от 0В до -0,8 В (поскольку известно, что нитрогруппа в структуре хлорамфеникола электровосстанавливается в данном диапазоне потенциалов). Измеряемой величиной является значение тока электровосстановления нитрогруппы, последующее определение содержания хлорамфеникола осуществляется с использованием метода градуировочного графика. Градуировочная зависимость между величиной регистрируемого тока и концентрацией хлорамфеникола в модельных суспензиях (молочных сыворотках с известной добавленной концентрацией хлорамфеникола): I, мкА = (-0.1442±0,0276)⋅CXA,мкМ - (1,1053±0,2154). Зарегистрированная величина тока составила -1.1083 мкА, следовательно, в анализируемой пробе обнаружено 0,021 мкМ хлорамфеникола.
На фигуре 2 приведены линейные вольтамперограммы, зарегистрированные на планарном углеродсодержащем электроде с электроосажденным рецепторным слоем до (3) и после (4) выдерживания в анализируемом растворе.
Таким образом, предложенный способ является одним из способов электрохимического определения хлорамфеникола в водной среде с использованием углеродсодержащего электрода.
На фиг. 1 приведены линейные вольтамперограммы, зарегистрированные на планарном углеродсодержащем электроде с электроосажденным рецепторным слоем до (1) и после (2) выдерживания в анализируемом растворе.
На фиг. 2 приведены линейные вольтамперограммы, зарегистрированные на планарном углеродсодержащем электроде с электроосажденным рецепторным слоем до (3) и после (4) выдерживания в анализируемом растворе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ТРИАЗИДА МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ | 2019 |
|
RU2733397C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ПОТЕНЦИАЛЬНОГО ПРОТИВООПУХОЛЕВОГО СРЕДСТВА -ЭТИЛ 6-НИТРО-7-(4"-НИТРОФЕНИЛ)-5-ЭТИЛ-4,7-ДИГИДРОПИРАЗОЛО[1,5-А]ПИРИМИДИН-3-КАРБОКСИЛАТА- МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ | 2022 |
|
RU2802831C1 |
| СПОСОБ АДРЕСНОЙ КОВАЛЕНТНОЙ ИММОБИЛИЗАЦИИ БЕЛКОВ НА ПОВЕРХНОСТИ РАБОЧЕГО ЭЛЕКТРОДА | 2019 |
|
RU2733935C2 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ КОЭНЗИМА Q10 В КРЕМАХ КОСМЕТИЧЕСКИХ | 2015 |
|
RU2613897C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИРАДИКАЛЬНОЙ АКТИВНОСТИ ВЕЩЕСТВ | 2020 |
|
RU2752017C1 |
| ВОЛЬТАМПЕРМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ ИОНОВ ТУЛИЯ В ВОДНЫХ РАСТВОРАХ | 1996 |
|
RU2097757C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАНОЧАСТИЦ Au, Ni И Cu В ЖИДКИХ ОБЪЕКТАХ | 2015 |
|
RU2612845C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ СУММАРНОЙ АКТИВНОСТИ АНТИОКСИДАНТОВ | 2002 |
|
RU2224997C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АСКОРБИНОВОЙ КИСЛОТЫ И ДОФАМИНА В ВОДЕ ПРИ СОВМЕСТНОМ ПРИСУТСТВИИ С ИСПОЛЬЗОВАНИЕМ МОДИФИЦИРОВАННЫХ ЭЛЕКТРОДОВ | 2015 |
|
RU2610220C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЛЕВОМИЦЕТИНА В ПИЩЕВЫХ ПРОДУКТАХ И ФАРМПРЕПАРАТАХ | 2000 |
|
RU2180748C1 |
Изобретение относится к электрохимическому анализу. Раскрыт способ определения содержания хлорамфеникола в анализируемой водной среде с использованием углеродсодержащего рабочего электрода, модифицированного 3,6-бис[(триметилсилил)этинил]-9Н-карбазолом, включающий молекулярное распознавание данной органической молекулой молекулы хлорамфеникола в водной среде путем погружения электрода в электрохимическую ячейку, содержащую 0,05% раствор 3,6-бис[(триметилсилил)этинил]-9Н-карбазола в ацетонитриле, наложения трех циклических разверток потенциала в диапазоне 0,3 до 1,8 В для формирования на электроде электроосажденного слоя 3,6-бис[(триметилсилил)этинил]-9Н-карбазола, перемещения электрода в водный анализируемый раствор, выдерживания в нем в течение 30 минут, затем детектирование прямого электрохимического сигнала от хлорамфеникола путем переноса электрода в водный раствор фонового электролита 0.1 M KCl, регистрации линейной вольтамперограммы в диапазоне от 0 до -0.8 В и определение содержания хлорамфеникола по величине тока электровосстановления нитрогруппы в структуре хлорамфеникола с использованием метода градуировочного графика. Изобретение обеспечивает селективность и чувствительность анализа с осуществлением малого количества стадий. 2 ил., 2 пр.
Способ определения содержания хлорамфеникола в анализируемой водной среде с использованием углеродсодержащего рабочего электрода, модифицированного 3,6-бис[(триметилсилил)этинил]-9Н-карбазолом, включающий молекулярное распознавание данной органической молекулой молекулы хлорамфеникола в водной среде путем погружения электрода в электрохимическую ячейку, содержащую 0,05% раствор 3,6-бис[(триметилсилил)этинил]-9Н-карбазола в ацетонитриле, наложения трех циклических разверток потенциала в диапазоне 0,3 до 1,8 В для формирования на электроде электроосажденного слоя 3,6-бис[(триметилсилил)этинил]-9Н-карбазола, перемещения электрода в водный анализируемый раствор, выдерживания в нем в течение 30 минут, затем детектирование прямого электрохимического сигнала от хлорамфеникола путем переноса электрода в водный раствор фонового электролита 0.1 M KCl, регистрации линейной вольтамперограммы в диапазоне от 0 до -0.8 В и определение содержания хлорамфеникола по величине тока электровосстановления нитрогруппы в структуре хлорамфеникола с использованием метода градуировочного графика.
| SVALOVA T | |||
| S | |||
| et al | |||
| Electrochemical behavior of chloramphenicol on carbon electrodes in a microelectrochemical cell // Chim | |||
| Techno Acta., 2022 | |||
| V | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ качественного и количественного детектирования антибиотиков тетрациклинового и пенициллинового ряда, стрептомицина и левомицетина в молоке и молочных изделиях | 2021 |
|
RU2777265C1 |
| CN 107255664 B, 29.03.2019 | |||
| CN 104677962 A, 03.06.2015 | |||
| SHANMUGARAJU S | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2024-01-31—Публикация
2023-05-05—Подача