ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка заявляет право на результат и приоритет по предварительным заявкам США № 62/555156, поданной 7 сентября 2017 года, № 62/624843, поданной 1 февраля 2018 года и № 62/657323, поданной 13 апреля 2018 года, все из которых включены посредством ссылки в полном объеме.
ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Перечень последовательностей, поданный 6 сентября 2018 года в виде текстового файла под названием «064466.071 sequence listing_ST25.txt», созданного 20 августа 2018 года, и имеющего размер 55,2 килобайт, включен в данный документ посредством ссылки в соответствии с § 1.52(e)(5) раздела 37 Свода федеральных нормативных актов США.
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение в целом относится к иммуномодулированию и антителам, которые специфично связываются с PD-1, и способам их применения.
УРОВЕНЬ ТЕХНИКИ
Путь с участием рецепторного белка программируемой клеточной смерти 1 (PD-1)/лиганда рецепторного белка программируемой клеточной смерти 1 (PD-L1) продемонстрировал перспективную клиническую эффективность в качестве мишени при иммунотерапии рака. Существующие в настоящее время антитела, которые целенаправленно воздействуют либо на PD-1, либо на PD-L1 могут блокировать указанное взаимодействие и стимулировать иммунный ответ против раковых клеток. Успешные клинические исследования с применением моноклональных антител к PD-1 и других ингибиторов иммунных контрольных точек открыли новые перспективы в иммунологии рака. В то же время неспособность большой подгруппы пациентов, страдающих раком, отвечать на новые иммунотерапевтические препараты привела к усиленному исследованию комбинированных видов терапии и предиктивных биомаркеров (Iwai, Y., et al., Journal of Biomedical Science, 24:26 (2017)).
Таким образом, целью данного изобретения является предоставление композиций и способов модулирования передачи сигнала с участием PD-1.
Другой целью данного изобретения является предоставление антител и их антигенсвязывающих фрагментов, которые специфично связываются с PD-1 и модулируют передачу сигнала с участием PD-1.
Другой целью данного изобретения является предоставление композиций и способов лечения рака.
Другой целью данного изобретения является предоставление композиций и способов лечения инфекций.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Предоставлены антитела и их антигенсвязывающие фрагменты, которые специфично связываются с PD-1, предпочтительно PD-1 человека или мыши, и индуцируют или стимулируют иммунный ответ, который активирует пролиферацию или активность иммунных клеток. В одном варианте осуществления раскрываемые антитела и их антигенсвязывающие фрагменты специфично связываются с PD-1, экспрессируемым на иммунных клетках. Связывание раскрываемых антител и их антигенсвязывающих фрагментов с PD-1 на иммунных клетках вызывает активацию сигнала, подлежащего передаче в иммунную клетку, например, сигнала, который усиливает или стимулирует продуцирование цитокинов и/или активацию пролиферации иммунных клеток. Иммунные клетки, которые экспрессируют PD-1, включают, но не ограничиваясь ими, B- и T-клетки, а также клетки миелоидного происхождения (Riley, J., Immunol Rev. 229(1):114-125 (2009)). В одном варианте осуществления иммунная клетка представляет собой T-клетку, предпочтительно CD8+ T-клетку.
В другом варианте осуществления предоставлен способ стимуляции, активации или усиления адаптивного иммунного ответа у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества раскрываемых анти-PD-1 антител или их антигенсвязывающих фрагментов с целью индукции, усиления или стимуляции адаптивного иммунного ответа у субъекта.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие определяющие комплементарность области (CDR) тяжелой цепи, имеющие аминокислотные последовательности в соответствии с SEQ ID NO:6, 7 и 8, и CDR легкой цепи, имеющие аминокислотные последовательности в соответствии с SEQ ID NO:12, 13 и 14, при этом антитело или его антигенсвязывающий фрагмент связывает PD-1.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:4 или 5.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:10 или 11.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:4 или 5, и легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:10 или 11.
В одном варианте осуществления предоставлено трансгенное животное, разработанное с целью экспрессии любого из раскрываемых антител или их антигенсвязывающих фрагментов. В одном варианте осуществления животное представляет собой мышь.
В одном варианте осуществления предоставлена нуклеиновая кислота, кодирующая тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:4 или 5.
В одном варианте осуществления предоставлена нуклеиновая кислота, кодирующая легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:10 или 11.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие CDR тяжелой цепи, имеющие аминокислотные последовательности в соответствии с SEQ ID NO:18, 19 и 20, и CDR легкой цепи, имеющие аминокислотные последовательности в соответствии с SEQ ID NO:24, 13 и 25.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:16 или 17.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:22 или 23.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:16 или 17, и легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:22 или 23.
В одном варианте осуществления предоставлена нуклеиновая кислота, кодирующая тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:16 или 17.
В одном варианте осуществления предоставлена нуклеиновая кислота, кодирующая легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:22 или 23.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие CDR тяжелой цепи, имеющие аминокислотные последовательности в соответствии с SEQ ID NO:29, 30 и 31, и CDR легкой цепи, имеющие аминокислотные последовательности в соответствии с SEQ ID NO:35, 36 и 37.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:27 или 28.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:33 или 34.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:27 или 28, и легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:33 или 34.
В одном варианте осуществления предоставлена нуклеиновая кислота, кодирующая тяжелую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:27 или 28.
В одном варианте осуществления предоставлена нуклеиновая кислота, кодирующая легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:33 или 34.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, содержащие три CDR легкой цепи с аминокислотными последовательностями, которые выбирают из группы, состоящей из SEQ ID NO: 12, 13, 14, 24, 25, 35, 36 или 37.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, содержащие три CDR тяжелой цепи с аминокислотными последовательностями, которые выбирают из группы, состоящей из SEQ ID NO: 6, 7, 8, 18, 19, 20, 29, 30 или 31.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, содержащие три CDR легкой цепи с аминокислотными последовательностями, которые выбирают из группы, состоящей из SEQ ID NO: 12, 13, 14, 24, 25, 35, 36 или 37, и три CDR тяжелой цепи с аминокислотными последовательностями, которые выбирают из группы, состоящей из SEQ ID NO: 6, 7, 8, 18, 19, 20, 29, 30 или 31.
В одном варианте осуществления предоставлены антитело или его эпитопсвязывающий фрагмент или слитый белок, которые иммуноспецифично связываются с SEQ ID NO:38. В одном варианте осуществления антитело связывается с SEQ ID NO:38 на PD-1. В одном варианте осуществления антитело связывается с PD-1, экспрессируемым на поверхности иммунной клетки и индуцирует или стимулирует сигнал с участием PD-1, который активирует или стимулирует иммунную клетку. В одном варианте осуществления иммунная клетка, которая активируется или стимулируется, представляет собой T-клетку, например, CD8+ T-клетку.
В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент являются человеческими, мышиными, химерными, гуманизированными, моноклональными, биспецифическими, триспецифическими или мультиспецифическими.
В одном варианте осуществления предоставлена фармацевтическая композиция, содержащая одно или более из раскрываемых антител или их антигенсвязывающих фрагментов. В некоторых вариантах осуществления фармацевтическая композиция содержат второе терапевтическое средство и/или фармацевтически приемлемый наполнитель. Иллюстративный второй терапевтический агент включает в себя циклофосфамид.
В одном варианте осуществления предоставлен способ индукции, активации или усиления иммунного ответа у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества одного или более раскрываемых антител или их антигенсвязывающих фрагментов с целью индукции, стимуляции или усиления иммунного ответа у субъекта.
В одном варианте осуществления предоставлен способ лечения рака у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества одного или более раскрываемых антител или их антигенсвязывающих фрагментов с целью лечения рака у субъекта.
В одном варианте осуществления предоставлен способ снижения опухолевой нагрузки у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества одного или более раскрываемых антител или их антигенсвязывающих фрагментов с целью снижения опухолевой нагрузки у субъекта.
В одном варианте осуществления предоставлен способ лечения инфекции у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества одного или более раскрываемых антител или их антигенсвязывающих фрагментов с целью лечения инфекции у субъекта.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 изображен график, демонстрирующий кинетику взаимодействия в виде функции от времени между моноклональным антителом 4G9 и PD-1 человека. На графике изображены кривые концентраций PD-1 человека при 0, 125, 250, 500, 500 и 1000 нM.
На Фиг. 2 изображен график, демонстрирующий кинетику взаимодействия в виде функции от времени между моноклональным антителом 4G9 и PD-1 мыши. На графике изображены кривые концентраций PD-1 мыши при 0, 62,5, 125, 500, 500 и 1000 нM.
На Фиг. 3 изображен график, демонстрирующий кинетику взаимодействия в виде функции от времени между моноклональным антителом 4C12 и PD-1 человека. На графике изображены кривые концентраций PD-1 человека при 0, 125, 250, 500, 500 и 1000 нM.
На Фиг. 4 изображен график, демонстрирующий кинетику взаимодействия в виде функции от времени между моноклональным антителом 5C2 и PD-1 человека. На графике изображены кривые концентраций PD-1 мыши при 0 и 1000 нM.
На Фиг. 5 изображен график, демонстрирующий кинетику взаимодействия в виде функции от времени между моноклональным антителом 5C2 и PD-1 мыши. На графике изображены кривые концентраций PD-1 человека при 0, 62,5, 125, 250, 500, 500 и 1000 нM.
На Фиг. 6A изображена гистограмма проточной цитометрии клеток EL4, окрашенных антителом изотипического контроля или коммерческим анти-PD-1 антителом J43. На Фиг. 6B изображена гистограмма проточной цитометрии клеток EL4, окрашенных только вторичным антителом или антителами 4G9, 5C2 и 4C12. На Фиг. 6С изображена гистограмма проточной цитометрии клеток El4, окрашенных только вторичным антителом или антителом 4G9. На Фиг. 6D изображена гистограмма проточной цитометрии клеток El4, окрашенных только вторичным антителом или антителом 5C2. На Фиг. 6E изображена гистограмма проточной цитометрии клеток El4, окрашенных только вторичным антителом или антителом 4C12. На Фиг. 6F изображена столбиковая диаграмма, на которое продемонстрировано связывание различных очищенных антител к PD-1 мыши с клетками EL4.
На Фиг. 7A и 7B изображены столбиковые диаграммы, на которых продемонстрирована концентрация IFNγ (Фиг. 7A) или IL-2 в супернатанте из клеток CD4 T-клеток, обработанных различными антителами. Ось X представляет группу обработки, а ось Y представляет концентрацию (нг/мл). На Фиг. 7C изображена столбиковая диаграмма, на которой продемонстрирована концентрация IFNγ в супернатанте из CD4 T-клеток человека, обработанных антителами 4G9 или 5C2. Ось X представляет группу обработки, а ось Y представляет концентрацию (нг/мл).
На Фиг. 8 изображена столбиковая диаграмма, на которой продемонстрированы уровни внутриклеточного окрашивания pAKT в CD4 T-клетках мыши, обработанных различными антителами. Ось X представляет группу обработки, а ось Y представляет MFI AKT (S473).
На Фиг. 9 изображен вестерн-блот, на котором продемонстрированы тяжелая цепь и легкая цепь IgG в различных антителах.
На Фиг. 10 изображена столбиковая диаграмма, на которой продемонстрировано связывание антител 4G9 и 5C2 с PD-1-Fc человека. Ось X представляет концентрацию антител, а ось Y представляет OD450.
На Фиг. 11A и 11B изображены гистограммы проточной цитометрии, на которых продемонстрировано связывание антител 4G9 и 5C2 к PD-1 в CD4 T-клетках от мышей PD-1 KO (Фиг. 11A) или мышей PD-1 ДТ (Фиг. 11B).
На Фиг. 12 изображен линейный график, на котором продемонстрирована экспрессия pS6 в CD4 T-клетках, обработанных 4G9, 5C2, коммерческим АТ-1, коммерческим АТ-2, или оставшихся без обработки. Ось X представляет концентрацию общего белка (мкг/мл), а ось Y представляет ОП450.
На Фиг. 13A изображена схематическая иллюстрация, на которой продемонстрирована экспериментальная схема экспериментов в случае опухоли TC-1. На Фиг. 13B изображен линейный график, на котором продемонстрирован средний объем опухоли (см3) в динамике (сутки) для мышей, несущих опухоль TC-1, обработанных E7 Vax, 4G9, RMP 1-14, E7 Vax+RMP 1-14, E7 Vax+4G9 или оставшихся без обработки. Ось X представляет время (сутки), а ось Y представляет средний объем опухоли (см3). На Фиг. 13С изображен линейный график, на котором продемонстрирован процент выживаемости в динамике для мышей, несущих опухоль TC-1, обработанных E7 Vax, 4G9, RMP 1-14, E7 Vax+RMP 1-14, E7 Vax+4G9 или оставшихся без обработки. На Фиг. 13D изображен линейный график, на котором продемонстрирован средний объем опухоли (см3) в динамике (сутки) для мышей, несущих опухоль TC-1, обработанных E7 Vax, 4C12, 5C2, RMP 1-14, E7 Vax+RMP 1-14, E7 Vax+4C12, E7 Vax+5C2 или оставшихся без обработки.
На Фиг. 14A изображена схематическая иллюстрация экспериментальной схемы экспериментов в случае опухоли TC-1. На Фиг. 14B изображен линейный график, на котором продемонстрирован средний объем опухоли (см3) в динамике (сутки) для мышей, несущих опухоль TC-1, обработанных E7 Vax, 4G9, RMP 1-14, J43, E7 Vax+4G9, E7 Vax+RMP 1-14, E7 Vax+J43 или оставшихся без обработки. Ось X представляет время (сутки), а ось Y представляет средний объем опухоли (см3). На Фиг. 14С изображен линейный график, на котором продемонстрирован процент выживаемости в динамике для мышей, несущих опухоль TC-1, обработанных E7 Vax, 4G9, 4C12, 5C2, RMP 1-14, J43, E7 Vax+4G9, E7 Vax+4C12, E7 Vax+5C2, E7 Vax+RMP 1-14, E7 Vax+J43 или оставшихся без обработки. Ось X представляет время (сутки), а ось Y представляет процент выживаемости.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
I. Определения
Используемая в данном документе молекула считается способной «иммуноспецифично связываться» со второй молекулой, если такое связывание демонстрирует специфичность и аффинность антитела в отношении своего когнатного антигена. Считается, что антитела способны к «иммуноспецифичному связыванию» с целевой областью или конформацией («эпитопом») антигена, если такое связывание включает сайт распознавания антигена молекулы иммуноглобулина. Антитело, которое иммуноспецифично связывается с определенным антигеном, может связываться с другими антигенами с более низкой аффинностью, если другой антиген имеет некоторое сходство последовательности или конформационное сходство, которое распознается сайтом распознавания антигена, что определяется, например, с помощью иммунологических методов анализа, анализов BIACORE® или других анализов, известных в данной области техники, однако, не будет связываться с абсолютно неродственным антигеном. Предпочтительно, однако, чтобы антитела (и их антигенсвязывающие фрагменты) не давали перекрестную реакцию с другими антигенами. Антитела также могут связываться с другими молекулами с помощью способа, который не является иммуноспецифичным, например, с Fc-рецепторами, в результате связывания доменов в других областях/доменах молекулы, которые не включают в себя сайт распознавания антигена, такой как Fc-область.
Считается, что используемая в данном документе молекула «специфично связывается» со второй молекулой, если такое связывание демонстрирует специфичность и аффинность рецептора в отношении своего когнатного антигена. Молекула может быть способной физиологически связываться с более чем одной другой молекулой.
Предполагается, что используемый в данном документе термин «антитело» обозначает молекулу иммуноглобулина, которая имеет сайт распознавания антигена «вариабельной области». Предполагается, что термин «вариабельная область» разграничивает такой домен иммуноглобулина от доменов, которые повсеместно являются общими для антител (таких как Fc-домен антител). Вариабельная область содержит «гипервариабельную область», остатки которой отвечают за связывание с антигеном. Гипервариабельная область содержит аминокислотные остатки из «определяющей комплементарность области» или «CDR» (т.е. в типичном случае остатки в положениях примерно 24-34 (L1), 50-56 (L2) и 89-97 (L3) в вариабельном домене легкой цепи и остатки в положениях примерно 27-35 (H1), 50-65 (H2) и 95-102 (H3) в вариабельном домене тяжелой цепи; Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991)), и/или такие остатки из «гипервариабельной петли» (т.е., остатки в положениях 26-32 (L1), 50-52 (L2) и 91-96 (L3) в вариабельном домене легкой цепи и 26-32 (H1), 53-55 (H2) и 96-101 (H3) в вариабельном домене тяжелой цепи; Chothia and Lesk, 1987, J. Mol. Biol. 196:901-917). Остатки «каркасной области» или «FR» остатки представляют собой такие остатки вариабельного домена, которые отличаются от остатков гипервариабельной области, определенной в данном документе. Термин антитело включает моноклональные антитела, мультиспецифичные антитела, человеческие антитела, гуманизированные антитела, синтетические антитела, химерные антитела, камелизованные антитела (см., например, Muyldermans et al., 2001, Trends Biochem. Sci. 26:230; Nuttall et al., 2000, Cur. Pharm. Biotech. 1:253; Reichmann and Muyldermans, 1999, J. Immunol. Meth. 231:25; международную публикацию №№ WO 94/04678 и WO 94/25591; патент США № 6005079), одноцепочечные Fv (scFv) (см., например, Pluckthun в The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds. Springer-Verlag, New York, pp. 269-315 (1994)), одноцепочечные антитела, связанные дисульфидными связями Fv (sdFv), интратела и антиидиотипические (aнти-Id) антитела (в том числе, например, анти-Id и анти-анти-Id антитела, раскрываемые в данном документе). В частности, такие антитела включают молекулы иммуноглобулинов любого типа (например, IgG, IgE, IgM, IgD, IgA и IgY), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подкласса.
Используемый в данном документе термин «антигенсвязывающий фрагмент» антитела относится к одной или более частям антитела, которые содержат области, определяющие комплементарность («CDR»), и необязательно каркасные остатки, которые включают сайт распознавания антигена «вариабельной области», и проявляют способность иммуноспецифично связываться с антигеном. Такие фрагменты включают Fab', F(ab')2, Fv, одноцепочечный фрагмент (ScFv) и их мутантные формы, встречающиеся в природе варианты и слитые белки, включающие сайт распознавания антигена «вариабельной области» антитела и гетерологический белок (например, токсин, сайт распознавания антигена для другого антигена, фермент, рецептор или лиганд рецептора и т.д.).
Используемый в данном документе термин «фрагмент» относится к пептиду или полипептиду, содержащему аминокислотную последовательность из, по меньшей мере, 5 смежных аминокислотных остатков, по меньшей мере, 10 смежных аминокислотных остатков, по меньшей мере, 15 смежных аминокислотных остатков, по меньшей мере, 20 смежных аминокислотных остатков, по меньшей мере, 25 смежных аминокислотных остатков, по меньшей мере, 40 смежных аминокислотных остатков, по меньшей мере, 50 смежных аминокислотных остатков, по меньшей мере, 60 смежных аминокислотных остатков, по меньшей мере, 70 смежных аминокислотных остатков, по меньшей мере, 80 смежных аминокислотных остатков, по меньшей мере, 90 смежных аминокислотных остатков, по меньшей мере, 100 смежных аминокислотных остатков, по меньшей мере, 125 смежных аминокислотных остатков, по меньшей мере, 150 смежных аминокислотных остатков, по меньшей мере, 175 смежных аминокислотных остатков, по меньшей мере, 200 смежных аминокислотных остатков или, по меньшей мере, 250 смежных аминокислотных остатков.
Предполагается, что термин «связывающая молекула», используемый в данном документе, относится к молекулам, которые специфично взаимодействуют и связываются с определенной мишенью. Мишень может представлять собой биологическую или малую (химическую) молекулу. Целевая мишень может определять антиген или антигенный фрагмент. Примеры связывающих молекул включают в себя, но не ограничиваясь ими, антитела (в том числе моноклональные антитела, биспецифические антитела, а также фрагменты антител), слитые белки и другие антигенсвязывающие молекулы, известные специалистам в данной области техники.
Используемый в данном документе термин «модулировать» относится к способности изменять эффект, результат или активность (например, передачу сигнала). Такое модулирование может быть агонистическим или антагонистическим. Антагонистическое модулирование может быть частичным (т.е. облегчающим, но не устраняющим) или оно может полностью устранять такую активность (например, нейтрализация). Модулирование может включать интернализацию рецептора после связывания антитела или снижение экспрессии рецептора на целевой клетке. Агонистическое модулирование может усиливать или иным образом повышать или усиливать активность (например, передачу сигнала). В еще одном дополнительно варианте осуществления такое модулирование может изменять природу взаимодействия между лигандом и его когнатным рецептором таким образом, чтобы измерять природу вызванной передачи сигнала. Например, молекулы могут в результате связывания с лигандом или рецептором изменять способность таких молекул связываться с другими лигандами или рецепторами и тем самым изменять их общую активность. Предпочтительно такое модулирование будет обеспечивать, по меньшей мере, 10% изменение измеряемой активности иммунной системы, более предпочтительно, по меньшей мере, 50% изменение такой активности или, по меньшей мере, 2-кратное, 5-кратное, 10-кратное ил еще более предпочтительно, по меньшей мере, 100-кратное изменение такой активности.
Предполагается, что термин «по сути», используемый в контексте связывания или проявляемого эффекта, обозначает, что наблюдаемый эффект является физиологически или терапевтически значимым. Так, например, молекула способна значительно блокировать активность лиганда или рецептора, если степень блокады является физиологически или терапевтически значимой (например, если такая степень составляет более 60% полной величины, более 70% полной величины, более 75% полной величины, более 80% полной величины, более 85% полной величины, более 90% полной величины, более 95% полной величины или более 97% полной величины). Аналогично, считается, что молекула имеет по сути такую же иммуноспецифичность и/или характеристику, как другая молекула, если такие иммуноспецифичности и характеристики более чем на 60% идентичны, более чем на 70% идентичны, более чем 75% идентичны, более чем на 80% идентичны, более чем на 85% идентичны, более чем на 90% идентичны, более чем на 95% идентичны или более чем на 97% идентичны.
Используемые в данном документе «костимулирующие» сигналы включают в себя положительные костимулирующие сигналы (например, сигналы, которые приводят к повышению активности) и отрицательные костимулирующие сигналы (например, сигналы, которые приводят к ингибированию активности).
Используемый в данном документе термин «производное» относится к антителу или его антигенсвязывающему фрагменту, который иммуноспецифично связывается с той же самой мишенью исходного или эталонного антитела, но который отличается аминокислотной последовательностью от исходного или эталонного антитела или его антигенсвязывающего фрагмента в результате включения одной, двух, трех, четырех, пяти или более аминокислотных замен, добавлений, делеций или модификаций по отношению к исходному или эталонному антителу или его антигенсвязывающему фрагменту. Предпочтительно такие производные будут иметь по сути ту же самую иммуноспецифичность и/или характеристики или ту же самую иммуноспецифичность и характеристики, что и исходное или эталонное антитело или его антигенсвязывающий фрагмент. Аминокислотные замены или добавления таких производных могут включать встречающиеся в природе (т.е. кодируемые ДНК) или не встречающиеся в природе аминокислотные остатки. Термин «производное» включает в себя, например, химерные или гуманизированные варианты, а также варианты, имеющие измененные CH1-области, шарнирные области, CH2-, CH3- или CH4-области, для получения, например, антител и т.д., имеющих различные Fc-области, которые проявляют усиленные или ослабленные эффекторные или связывающие характеристики.
Используемый в данном документе термин «химерное антитело» представляет собой молекулу, в которой различные части антитела происходят из различных молекул иммуноглобулинов, например, антитела, имеющие вариабельную область, происходящую из отличного от человеческого антитела, и константную область человеческого иммуноглобулина.
Используемый в данном документе термин «гуманизированное антитело» относится к иммуноглобулину, включающему каркасную область человеческого иммуноглобулина и один или более CDR отличных от человеческого (как правило, мышиного или крысиного) иммуноглобулина. Отличный от человеческого иммуноглобулин, представляющий CDR, называется «донорским», а человеческий иммуноглобулин, представляющий каркас, называется «акцепторным». Константные области могут не присутствовать, однако, если они имеются, они должны быть по сути идентичны константным областям человеческих иммуноглобулинов, т.е., по меньшей мере, на около 85-99%, предпочтительно на около 95% или более идентичны. Таким образом, все части гуманизированного иммуноглобулина, за исключением, возможно, CDR, по сути идентичны соответствующим частям встречающихся в природе последовательностей человеческих иммуноглобулинов. Гуманизированное антитело представляет собой антитело, содержащее легкую цепь гуманизированного иммуноглобулина и тяжелую цепь гуманизированного иммуноглобулина. Например, гуманизированное антитело не будет включать в себя типичное химерное антитело, поскольку, например, вся вариабельная область химерного антитела является отличной от человеческой.
Используемый в данном документе термин «эндогенная концентрация» относится к уровню, при котором молекула экспрессируется в нативном состоянии (например, в отсутствие векторов экспрессии или рекомбинантных промоторов) клеткой (при этом клетка может представлять собой нормальную клетку, раковую клетку или инфицированную клетку).
Используемый в данном документе термин «лечить», «лечебный», «лечение» и «терапевтическое применение» относятся к устранению, ослаблению или нормализации одного или более обостренных симптомов заболевания или нарушения с помощью анти-PD-1 антител или их антигенного фрагмента.
Используемое в данном документе «терапетвически эффективное количество» относится к количеству терапевтического агента, которое является эффективным для опосредования клинически значимого устранения, ослабления или нормализации таких симптомов. Эффект является клинически значимым, если его величина является достаточной для оказания влияния на здоровье или прогноз заболевания субъекта-реципиента. Терапевтически эффективное количество может относиться к количеству терапевтического агента, достаточного для замедления или сведения к минимуму начала заболевания, например, задержки или сведения к минимуму распространения рака. Терапевтически эффективное количество может также относиться к количеству терапевтического агента, которое обеспечивает терапевтический эффект при лечении или контроле заболевания.
Используемый в данном документе термин «профилактичесий агент» относится к агенту, который может быть использован для предупреждения нарушения или заболевания до выявления каких-либо симптомов такого нарушения или заболевания. «Профилактически эффективное» количество представляет собой количество профилактического агента, достаточного для опосредования такой защиты. Профилактически эффективное количество может также относиться к количеству профилактического агента, которое обеспечивает профилактический эффект в предупреждении заболевания.
Используемый в данном документе термин «рак» относится к новообразованию или опухоли, образованной в результате патологического неконтролируемого роста клеток. Используемый в данном документе рак явным образом включает лейкозы и лимфомы. Термин «рак» относится к заболеванию, вовлекающему клетки, которые имеют потенциал к метастазированию в отдаленные участки и проявляют фенотипические признаки, которые отличаются от таковых клеток, не являющихся раковыми, например, образование колоний в трехмерном субстрате, таком как мягкий агар, или образование тубулярных сетей или паутинообразных матриц в трехмерной базальной мембране или препарате внеклеточного матрикса. Клетки, не являющиеся раковыми, не образуют колоний в мягком агаре и образуют отличающиеся структуры сферического типа в трехмерной базальной мембране или препаратах внеклеточного матрикса.
Используемая в данном документе «иммунная клетка» относится к любой клетке гемопоэтического происхождения, в том числе, но не ограничиваясь ими, Т-клеткам, B-клеткам, моноцитам, дендритным клеткам и макрофагам.
Используемая в данном документе «валентность» относится к числу сайтов связывания, доступных на молекулу.
Используемый в данном документе термин «иммунологический» или «иммунный» ответ представляет собой развитие полезного гуморального (антителоопосредованного) и/или клеточного (опосредованного антигенспецифичными Т-клетками или продуктами их секреции) ответа, направленного против пептида у пациента-реципиента. Такой ответ может представлять собой активный ответ, индуцированный введением иммуногена, или пассивный ответ, индуцированный введением антитела или примированных T-клеток. Клеточный иммунный ответ вызывается презентацией полипептидных эпитопов в ассоциации с молекулами MHC I или II класса в целях активации антигенспецифичных CD4+ T-хелперных клеток и/или CD8+ цитотоксических T-клеток. Ответ также может включать в себя активацию моноцитов, макрофагов, NK-клеток, базофилов, дендритных клеток, астроцитов, клеток микроглии, эозинофилов, активацию или рекрутинг нейтрофилов или других компонентов врожденного иммунитета. Наличие клеточно-опосредованного иммунологического ответа может быть определено с помощью анализов пролиферации (CD4+ T-клетки) или анализов с использованием CTL (цитотоксических Т-лимфоцитов). Относительный вклад гуморальных и клеточных ответов в защитный или терапевтический эффект иммуногена может быть охарактеризован с помощью раздельного выделения антител и Т-клеток из иммунизированного сингенного животного и измерения защитного или терапевтического эффекта у второго субъекта.
Используемый в данном документе «иммуногенный агент» или «иммуноген» способен индуцировать иммунологический ответ против самого себя при введении млекопитающему, необязательно в сочетании с вспомогательным веществом.
Используемые в данном документе термины «индивидуум», «хозяин», «субъект» и «пациент» используются в данном документе взаимозаменяемо и относятся к млекопитающему, в том числе, не ограничиваясь ими, человеку, грызунам, таким как мыши и крысы, и другим лабораторным животным.
Используемый в данном документе термин «полипептид» относится к цепи аминокислот любой длины, вне зависимости от модификации (например, фосфорилирования или гликозилирования). Термин полипептид включает в себя белки и их фрагменты. Полипептиды могут быть «экзогенными», означая, что они являются «гетерологичными», т.е., чужеродными по отношению к клетке-хозяину, подлежащей использованию, такими как человеческий полипептид, продуцируемый бактериальной клеткой. Полипептиды раскрыты в данном документе в виде последовательностей аминокислотных остатков. Эти последовательности пишутся слева направо в направлении от амино- к карбоксиконцу. В соответствии со стандартной номенклатурой последовательности аминокислотных остатков обозначаются как с помощью трехбуквенного, так и однобуквенного кода, указанного следующим образом: аланин (Ala, A), аргинин (Arg, R), аспарагин (Asn, N), аспарагиновая кислота (Asp, D), цистеин (Cys, C), глутамин (Gln, Q), глутаминовая кислота (Glu, E), глицин (Gly, G), гистидин (His, H), изолейцин (Ile, I), лейцин (Leu, L), лизин (Lys, K), метионин (Met, M), фенилаланин (Phe, F), пролин (Pro, P), серин (Ser, S), треонин (Thr, T), триптофан (Trp, W), тирозин (Tyr, Y) и валин (Val, V).
Используемый в данном документе термин «вариант» относится к полипептиду или полинуклеотиду, который отличается от эталонного полипептида или полинуклеотида, однако сохраняет основные свойства. Типичный вариант полипептида отличается аминокислотной последовательностью от другого, эталонного, полипептида. Как правило, отличия ограничены таким образом, что последовательности эталонного полипептида и варианта в целом очень похожи и во многих областях идентичны. Вариант и эталонный полипептид могут отличаться аминокислотной последовательностью вследствие одной или более модификаций (например, замен, добавлений и/или делеций). Замещенный или вставленный аминокислотный остаток может представлять собой или может не представлять собой таковой, кодируемый с помощью генетического кода. Вариант полипептида может встречаться в природе, например, аллельный вариант или может представлять собой вариант, который, как известно, не встречается в природе.
Модификации и изменения могут быть выполнены в структуре полипептидов по данному раскрытию и по-прежнему можно получить молекулу, имеющую аналогичные характеристики, как и полипептид (например, консервативную аминокислотную замену). Например, определенные аминокислоты могут быть замещены на другие аминокислоты в последовательности без заметной потери активности. Поскольку это является интерактивной способностью и природой полипептида, которая определяет биологическую функциональную активность этого полипептида, то определенные аминокислотные замены могут быть выполнены в полипептидной последовательности и при этом по-прежнему можно получать полипептид с аналогичными свойствами.
При выполнении таких замен можно учитывать индекс гидропатичности аминокислот. Важность индекса гидропатичности аминокислот в обеспечении биологической функции полипептида в целом понятна в данной области техники. Известно, что определенные аминокислоты могут быть замещены другими аминокислотами, имеющими аналогичный индекс или балл гидропатичности, и по-прежнему приводить к образованию полипептида с аналогичной биологической активностью. Каждой аминокислоте был присвоен индекс гидропатичности на основании ее гидрофобности и зарядных характеристик. Эти индексы являются следующими: изолейцин (+4,5); валин (+4,2); лейцин (+3,8); фенилаланин (+2,8); цистеин/цистин (+2,5); метионин (+1,9); аланин (+1,8); глицин (-0,4); треонин (-0,7); серин (-0,8); триптофан (-0,9); тирозин (-1,3); пролин (-1,6); гистидин (-3,2); глутамат (-3,5); глутамин (-3,5); аспартат (-3,5); аспарагин (-3,5); лизин (-3,9); и аргинин (-4,5).
Считается, что относительный гидропатичный характер аминокислоты определяет вторичную структуру образующегося пептида, которая, в свою очередь, определяет взаимодействие с другими молекулами, такими как ферменты, субстраты, рецепторы, антитела, антигены и кофакторы. В данной области техники известно, что аминокислота может быть замещена другой аминокислотой, имеющей аналогичный индекс гидропатичности, и по-прежнему можно получать функционально эквивалентный полипептид. При таких изменениях замена аминокислот, индексы гидропатичности которых находятся в пределах ± 2, является предпочтительной, таковые в пределах ± 1 являются особенно предпочтительными и таковые в пределах ± 0,5 являются еще более предпочтительными.
Замена подобных аминокислот также может быть выполнена на основании гидрофильности, в частности, если полипептид или пептид с эквивалентной биологической функцией, полученный подобным образом, предполагается использовать в иммунологических вариантах осуществления. Следующие значения гидрофильности были присвоены аминокислотным остаткам: аргинин (+3,0); лизин (+3,0); аспартат (+3,0 ± 1); глутамат (+3,0 ± 1); серин (+0,3); аспаригин (+0,2); глутамин (+0,2); глицин (0); пролин (-0,5 ± 1); треонин (-0,4); аланин (-0,5); гистидин (-0,5); цистеин (-1,0); метионин (-1,3); валин (-1,5); лейцин (-1,8); изолейцин (-1,8); тирозин (-2,3); фенилаланин (-2,5); триптофан (-3,4). Считается, что аминокислота может быть замещена другой, имеющей аналогичное значение гидрофильности, и по-прежнему можно получать биологически эквивалентный, и, в частности, иммунологически эквивалентный полипептид. При таких изменениях замена аминокислот, значения гидрофильности которых находятся в пределах ± 2, является предпочтительной, таковые в пределах ± 1 являются особенно предпочтительными и таковые в пределах ± 0,5 являются еще более предпочтительными.
Как указано выше, аминокислотные замены, как правило, основаны на относительном сходстве заместителей боковых цепей аминокислот, например, их гидрофобности, гидрофильности, заряде, размере и т.п. Иллюстративные замены, которые учитывают вышеизложенные характеристики, хорошо известны специалистам в данной области техники и включают (исходный остаток: иллюстративная замена): (Ala: Gly, Ser), (Arg: Lys), (Asn: Gln, His), (Asp: Glu, Cys, Ser), (Gln: Asn), (Glu: Asp), (Gly: Ala), (His: Asn, Gln), (Ile: Leu, Val), (Leu: Ile, Val), (Lys: Arg), (Met: Leu, Tyr), (Ser: Thr), (Thr: Ser), (Tip: Tyr), (Tyr: Trp, Phe) и (Val: Ile, Leu). Таким образом, варианты осуществления по данному раскрытию предусматривают биологические эквиваленты полипептида, изложенные выше. В частности, варианты осуществления полипептидов могут включать варианты, которые на около 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% или более идентичны последовательности полипептида, представляющего интерес.
Термин «процент (%) идентичности последовательности» определяют в виде процента нуклеотидов или аминокислот в кандидатной последовательности, которые идентичны нуклеотидам или аминокислотам в эталонной последовательности нуклеиновой кислоты, после выравнивания последовательностей и введения промежутков, при необходимости, для достижения максимального процента идентичности последовательностей. Выравнивание в целях определения процента идентичности последовательностей может быть достигнуто различными способами, которые находятся в пределах компетенции специалиста в данной области техники, например, с помощью общедоступного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN, ALIGN-2 или Megalign (DNASTAR). Подходящие параметры для измерения выравнивания, в том числе любых выравниваний, необходимых для достижения максимального выравнивания по отношению к полному размеру последовательностей, подлежащих сравнению, могут быть определены с помощью известных способов.
В целях данного документа % идентичности последовательностей определенной нуклеотидной или аминокислотной последовательности C по отношению, с или против определенной нуклеотидной последовательности D (который альтернативно может быть перефразирован в виде определенной последовательности C, которая имеет или содержит определенный % идентичности последовательности по отношению, с или против определенной последовательности D) рассчитывается следующим образом:
100 умножить на дробь W/Z,
где W представляет собой число нуклеотидов или аминокислот, оцениваемых в качестве идентичных совпадений с помощью программы выравнивания последовательностей при выравнивании C и D в этой программе, и где Z представляет собой общее число нуклеотидов или аминокислот в D. Будет понятно, что в случае, если длина последовательности C не равна длине последовательности D, % идентичности последовательностей C по отношению к D не будет равной % идентичности последовательностей D по отношению к C.
Используемый в данном документе термин «фармацевтически приемлемый носитель» включает в себя любой из стандартных фармацевтических носителей, такой как фосфатно-солевой буферный раствор, вода и эмульсии, такие как эмульсия масло/вода или вода/масло, и различные типы увлажняющих агентов.
Используемые в данном документе термины «антигенная детерминанта» и «эпитоп» используются взаимозаменяемо и относятся к структуре, распознаваемой антителом.
Используемый в данном документе «конформационный эпитоп» представляет собой эпитоп, который содержит непрерывные участки аминокислотной последовательности антигена. Антитела связывают конформационный эпитоп на основании трехмерных свойств поверхности, формы или третичной структуры антигена.
Используемый в данном документе «линейный эпитоп» представляет собой эпитоп, который образован непрерывной последовательностью аминокислот из антигена. Линейные эпитопы в типичном случае содержат от около 5 до около 10 непрерывных аминокислотных остатков. Антитела связывают линейный эпитоп на основании первичной последовательности антигена.
Используемый в данном документе термин «паратоп», также называемый «антигенсвязывающим сайтом», представляет собой часть антитела, которое распознает и связывается с антигеном.
II. Композиции
Предложены антитела и их антигенсвязывающие фрагменты, которые иммуноспецифично связываются с PD-1. В отличие от существующей парадигмы о том, что PD-1 исключительно стимулирует супрессорный иммунный ответ (Riley, J., Immunol Rev. 229(1):114-125 (2009)), раскрываемые антитела и их антигенсвязывающие фрагменты иммуноспецифически связываются с PD-1 и вызывают доставку активирующего сигнала в иммунную клетку, который активирует иммунную клетку вместо супрессии иммунной клетки.
A. Рецепторный белок программируемой клеточной смерти 1 (PD-1)
Раскрываемые антитела и их антигенсвязывающие фрагменты иммуноспецифично связываются с PD-1. Антитела и их антигенсвязывающие фрагменты могут связываться с PD-1, имеющим, например, аминокислотные последовательности, предложенные ниже.
Аминокислотные последовательности PD-1 человека и PD-1 мыши известны в данной области техники, и включают в себя, например,
PD-1 человека
MQIPQAPWPVVWAVLQLGWRPGWFLDSPDRPWNPPTFSPALLVVTEGDNATFTCSFSNTSESFVLNWYRMSPSNQTDKLAAFPEDRSQPGQDCRFRVTQLPNGRDFHMSVVRARRNDSGTYLCGAISLAPKAQIKESLRAELRVTERRAEVPTAHPSPSPRPAGQFQTLVVGVVGGLLGSLVLLVWVLAVICSRAARGTIGARRTGQPLKEDPSAVPVFSVDYGELDFQWREKTPEPPVPCVPEQTEYATIVFPSGMGTSSPARRGSADGPRSAQPLRPEDGHCSWPL (SEQ ID NO:1), № доступа: AJS10360, которая особым образом включена посредством ссылки в полном объеме;
PD-1 мыши
MWVRQVPWSFTWAVLQLSWQSGWLLEVPNGPWRSLTFYPAWLTVSEGANATFTCSLSNWSEDLMLNWNRLSPSNQTEKQAAFCNGLSQPVQDARFQIIQLPNRHDFHMNILDTRRNDSGIYLCGAISLHPKAKIEESPGAELVVTERILETSTRYPSPSPKPEGRFQGMVIGIMSALVGIPVLLLLAWALAVFCSTSMSEARGAGSKDDTLKEEPSAAPVPSVAYEELDFQGREKTPELPTACVHTEYATIVFTEGLGASAMGRRGSADGLQGPRPPRHEDGHCSWPL
(SEQ ID NO:2) UniProtKB - Q02242 (PDCD1_MOUSE), которая особым образом включена посредством ссылки в полном объеме.
B. Композиции антител
Раскрываемые анти-PD-1 антитела и их антигенсвязывающие фрагменты включают в себя целый иммуноглобулин (т.е., интактное антитело) любого класса, его фрагменты и синтетические белки, содержащие, по меньшей мере, антигенсвязывающий вариабельный домен антитела. В некоторых вариантах осуществления раскрываемое антитело содержит как легкую цепь, так и, по меньшей мере, вариабельный домен тяжелой цепи антитела. В других вариантах осуществления такие молекулы могут дополнительно содержать одно или более из CH1-областей, шарнирных областей, CH2-, CH3- и CH4-областей тяжелой цепи (в особенности CH1-области и шарнирные области, или CH1-области, шарнирные области и CH2-области, или CH1-области, шарнирные области, CH2- и CH3-области). Антитело может быть выбрано из любого класса иммуноглобулинов, в том числе IgM, IgG, IgD, IgA и IgE и любого изотипа, в том числе IgG1, IgG2, IgG3 и IgG4. В некоторых вариантах осуществления константный домен представляет собой фиксирующий комплемент константный домен, при этом предпочтительно, чтобы антитело проявляло цитотоксическую активность, а класс в типичном случае представлял бы собой IgG1. В других вариантах осуществления, в которых такая цитотоксическая активность не является необходимой, константный домен может представлять собой класс IgG2 или IgG4. Антитело может содержать последовательности из более одного класса или изотипа, и выбор определенных константных доменов для оптимизации необходимых эффекторных функций находится в пределах компетенции специалиста в данной области техники.
Вариабельные домены отличаются последовательностью среди антител и используются в связывании и специфичности каждого конкретного антитела в отношении своего определенного антигена. Однако вариабельность обычно не распределена равномерно в вариабельных доменах антител. В типичном случае она сосредоточена в трех сегментах, называемых определяющих комплементарность областями (CDR) или гипервариабельными областями в вариабельных доменах как легкой цепи, так и тяжелой цепи. Наиболее высококонсервативные участки вариабельных доменов называются каркасом (FR). Каждый из вариабельных доменов нативных тяжелых и легких цепей содержит четыре FR-области, по большей части принимающих конфигурацию бета-листа, соединенных тремя CDR, которые образуют петли, объединяющие структуру бета-листа и в некоторых случаях образующие ее часть. CDR в каждой цепи удерживаются в непосредственной близости друг с другом с помощью FR-областей и совместно с CDR из другой цепи участвуют в образовании антигенсвязывающего сайта антител.
В некоторых вариантах осуществления предоставлены анти-PD-1 антитела, которые имеют биологическую активность. Фрагменты, присоединенные или не присоединенные к другим последовательностям, могут содержать вставки, делеции, замены или другие выбранные модификации определенных областей или определенных аминокислотных остатков, при условии, что активность фрагмента по сути не является измененной или нарушенной по сравнению с немодифицированным антителом или фрагментом антитела.
В другом варианте осуществления предоставлены одноцепочечные антитела, специфичные по отношению к PD-1. Способы получения одноцепочечных антител хорошо известны специалистам в данной области техники. Одноцепочечное антитело может быть получено с помощью слияния друг с другом вариабельных доменов тяжелой и легкой цепей с использованием короткого пептидного линкера, при этом восстанавливается антигенсвязывающий сайт на одной молекуле. Вариабельные фрагменты одноцепочечных антител (scFv), в которых C-конец одного вариабельного домена связан с N-концом другого вариабельного домена с помощью пептида или линкера из 15-25 аминокислот были разработаны без существенного нарушения связывания с антигеном или специфичности связывания. Линкер выбирают таким образом, чтобы он обеспечивал связывание тяжелой цепи и легкой цепи друг с другом в их соответствующей конформационной ориентации.
В другом варианте осуществления предоставлены двухвалентные одноцепочечные вариабельные фрагменты (di-scFv), которые могут быть разработаны с помощью связывания двух scFv. Это может быть выполнено в результате получения одной пептидной цепи с двумя VH- и двумя VL-областями, образующими тандемные scFv. ScFv также могут быть сконструированы с помощью линкерных пептидов, которые являются слишком короткими, чтобы две вариабельные области складывались вместе (около пяти аминокислот), обеспечивая димеризацию scFv. Указанный тип известен как диатела. Было продемонстрировано, что диатела имеют константы диссоциации до 40 раз ниже, чем соответствующие scFv, означая, что они имеют намного более высокую аффиность по отношению к своей мишени. Еще более короткие линкеры (одна или две аминокислоты) приводят к образованию тримеров (триател или триотел). Также были получены тетратела. Они проявляют даже более высокую аффинность в отношении своих мишеней по сравнению с диателами.
В другом варианте осуществления предоставлено моноклональное антитело, специфичное по отношению к PD-1, которое индуцирует активирующий сигнал в отношении иммунных клеток. Указанное моноклональное антитело может быть получено по сути из гомогенной популяции антител, т.е., отдельные антитела в популяции являются идентичными, за исключением возможных встречающихся в природе мутаций, которые могут присутствовать в небольшой подгруппе молекул антител. Моноклональные антитела включают в себя «химерные» антитела, в которых часть тяжелой и/или легкой цепи идентична или гомологична соответствующим последовательностям в антителах, происходящих из определенного вида или принадлежащих к определенному классу или подклассу антител, тогда как остальная часть цепи (цепей) идентична или гомологична соответствующим последовательностям в антителах, происходящих из другого вида или принадлежащих к другому классу или подклассу антител, а также фрагментам таких антител, до тех пор, пока они проявляют необходимую антагонистическую активность.
1. Химерные и гуманизированные антитела
В другом варианте осуществления предоставлены химерные анти-PD-1 антитела и их антигенсвязывающие фрагменты, в том числе также предоставлены одно или более из раскрываемых последовательностей и их функциональных вариантов, которые связываются с PD-1 и вызывают передачу активирующего сигнала в иммунную клетку, экспрессирующую PD-1.
Способы получения химерных антител известны в данной области техники. См., например, Morrison, 1985, Science 229:1202; Oi et al., 1986, BioTechniques 4:214; Gillies et al., 1989, J. Immunol. Methods 125:191-202, и патенты США №№ 6311415, 5807715, 4816567 и 4816397. Химерные антитела, содержащие одну или более CDR от отличных от человека видов и каркасные области из молекулы человеческого иммуноглобулина, могут быть получены с помощью ряда методик, известных в данной области техники, в том числе, например, встраивания CDR (EP 239400, международная публикация № WO 91/09967; и патенты США №№ 5225539, 5530101 и 5585089), венирования и перекладки (EP 592106; EP 519596; Padlan, 1991, Molecular Immunology 28(4/5):489-498; Studnicka et al., 1994, Protein Engineering 7:805; и Roguska et al., 1994, Proc. Natl. Acad. Sci. USA 91:969) и перестановки цепей (патент США № 5565332).
Раскрываемые анти-PD-1 антитела или их антигенсвязывающие фрагменты могут представлять собой человеческие или гуманизированные антитела или их антигенсвязывающие фрагменты. Многие отличные от человеческих антитела (например, антитела, происходящие от мышей, крыс или кроликов) являются естественным образом антигенными у человека и, тем самым, вызывают нежелательные иммунные ответы при введении человеку. Таким образом, использование человеческих или гуманизированных антител в способах способствует снижению вероятности того, что антитело, вводимое человеку, вызовет нежелательный иммунный ответ.
Могут быть использованы трансгенные животные (например, мыши), которые способны при иммунизации продуцировать полный репертуар человеческих антител в отсутствие продуцирования эндогенных иммуноглобулинов. Например, было описано, что гомозиготная делеция гена связывающего участка тяжелой цепи антитела (J(H)) у химерных и мутантных в отношении зародышевой линии мышей приводит к полному ингибированию продуцирования эндогенных антител. Перенос набора генов иммуноглобулинов зародышевой линии человека в таких мутантных в отношении зародышевой линии мышей приведет к продуцированию человеческих антител при антигенной стимуляции.
Необязательно антитела получают у других видов и «гуманизируют» для введения у человека. Гуманизированные формы отличных от человеческих (например, мышиных) антител представляют собой химерные иммуноглобулины, иммуноглобулиновые цепи или их фрагменты (такие как Fv, Fab, Fab’, F(ab’)2 или другие антигенсвязывающие последовательности антител), которые содержат минимальную последовательность, происходящую из отличного от человеческого иммуноглобулина. Гуманизированные антитела включают в себя человеческие иммуноглобулины (реципиентное антитело), в которых остатки из области, определяющей комплементарность (CDR) реципиентного антитела замещены остатками из CDR отличного от человека вида (донорское антитело), такого как мышь, крыса или кролик, имеющего необходимую специфичность, аффинность и способность. В некоторых случаях остатки каркасной Fv-области человеческого иммуноглобулина замещены соответствующими отличными от человеческих остатками. Гуманизированные антитела также могут содержать остатки, которые не встречаются ни в реципиентном антителе, ни в импортированных последовательностях CDR или каркасных последовательностях. Как правило, гуманизированное антитело будет включать по сути все из, по меньшей мере, одного или в типичном случае двух вариабельных доменов, в которых все или фактически все из CDR-областей соответствуют таковым отличным от человеческого иммуноглобулина и все или фактически все из FR-областей происходят из консенсусной последовательности человеческого иммуноглобулина. Гуманизированное антитело в оптимальном случае также будет содержать, по меньшей мере, часть константной области иммуноглобулина (Fc), в типичном случае такового человеческого иммуноглобулина.
Способы гуманизации отличных от человеческих антител хорошо известны в данной области техники, см., например, европейские патенты №№ EP 239400, EP 592106 и EP 519596; международные публикации WO 91/09967 и WO 93/17105; патенты США №№ 5225539, 5530101, 5565332, 5585089, 5766886 и 6407213; и Padlan, 1991, Molecular Immunology 28(4/5):489498; Studnicka et al., 1994, Protein Engineering 7(6):805-814; Roguska et al., 1994, PNAS 91:969973; Tan et al., 2002, J. Immunol. 169:1119-1125; Caldas et al., 2000, Protein Eng. 13:353-360; Morea et al., 2000, Methods 20:26779; Baca et al., 1997, J. Biol. Chem. 272:1067810684; Roguska et al., 1996, Protein Eng. 9:895904; Couto et al., 1995, Cancer Res. 55 (23 Supp):5973s5977s; Couto et al., 1995, Cancer Res. 55:171722; Sandhu, 1994, Gene 150:40910; Pedersen et al., 1994, J. Mol. Biol. 235:959-973; Jones et al., 1986, Nature 321:522-525; Reichmann et al., 1988, Nature 332:323-329; и Presta, 1992, Curr. Op. Struct. Biol. 2:593-596).
Как правило, гуманизированное антитело имеет один или более аминокислотных остатков, введенных в него из источника, который отличается от человеческого. Эти отличные от человеческих аминокислотные остатки часто называется «импортируемыми» остатками, которые в типичном случае получают из «импортируемого» вариабельного домена. Методики гуманизации антител, как правило, включают использование технологии рекомбинантных ДНК в целях манипуляции с последовательностью ДНК, кодирующей одну или более полипептидных цепей молекулы антитела. Гуманизация может быть по сути осуществлена с помощью замены CDR грызунов или последовательностей CDR на соответствующие последовательности человеческого антитела. Соответственно, гуманизированная форма отличного от человеческого антитела (или его фрагмента) представляет собой химерное антитело или фрагмент, в котором по сути менее чем интактный человеческий вариабельный домен был замещен соответствующей последовательностью от отличного от человека вида. При практическом применении гуманизированные антитела в типичном случае представляют собой человеческие антитела, в которых некоторых остатки CDR и возможно некоторые остатки FR замещены остатками из аналогичных сайтов в антителах грызунов.
Выбор человеческих вариабельных доменов, как легких, так и тяжелых цепей, подлежащих использованию при получении гуманизированных антител, может быть очень важным для снижения антигенности. В соответствии с методом «наилучшего приближения» последовательность вариабельного домена антитела грызуна подвергают скринингу против всей библиотеки известных последовательностей человеческих вариабельных доменов. Человеческую последовательность, которая является наиболее близкой к таковой грызуна, затем принимают в качестве человеческой каркасной области (FR) иммунизированного антитела. В другом способе используется определенная каркасная область, происходящая из консенсусной последовательности всех человеческих антител определенной подгруппы легких или тяжелых цепей. Одинаковая каркасная область может быть использована для нескольких отличающихся гуманизированных антител.
Кроме того, важно, чтобы антитела были гуманизированными с сохранением высокой аффинности в отношении антигена и других благоприятных биологических свойств. Для достижения этой цели гуманизированные антитела могут быть получены в результате анализа исходных последовательностей и различных концептуальных гуманизированных продуктов с помощью пространственных моделей исходных и гуманизированных последовательностей. Пространственные модели иммуноглобулинов являются общедоступными и известными специалистам в данной области техники. Доступны компьютерные программы, которые иллюстрируют и демонстрируют возможные пространственные конформационные структуры некоторых кандидатных иммуноглобулиновых последовательностей. Исследование этих изображений способствует анализу вероятной роли остатков в функционировании кандидатной иммуноглобулиновой последовательности, т.е., анализу остатков, которые влияют на способность кандидатного иммуноглобулина связываться со своим антигеном. В этом отношении остатки FR можно выбирать и комбинировать из консенсусной и импортируемой последовательности таким образом, чтобы была достигнута необходимая характеристика антитела, такая как повышенная аффинность в отношении целевого(целевых) антигена(антигенов). Как правило, остатки CDR непосредственно и в наибольшей степени по сути оказывают влияние на связывание с антигеном.
Производное человеческого, гуманизированного или химерного антитела может содержать по сути все, по меньшей мере, из одного или в типичном случае из двух вариабельных доменов, в которых все или по сути все из CDR-областей соответствуют таковым отличным от человеческого иммуноглобулина (т.е., донорского антитела) и все или по сути все из каркасных областей соответствуют таковым консенсусной последовательности человеческого иммуноглобулина. Такие антитела также могут включать, по меньшей мере, часть константного участка иммуноглобулина (Fc), в типичном случае такового человеческого иммуноглобулина. Константные домены таких антител могут быть выбраны исходя из предполагаемой функции антитела, в частности, эффекторной функции, которая может быть необходимой. В некоторых вариантах осуществления константные домены таких антител представляют собой или могут включать в себя домены IgA, IgD, IgE, IgG или IgM человека. В конкретном варианте осуществления используют константные домены IgG человека, особенно изотипов IgG1 и IgG3, если производное гуманизированного антитела предполагается использовать для терапевтического применения, и необходимы эффекторные функции антител, такие активность в направлении антителозависимой клеточноопосредованной цитотоксичности (ADCC) и комплементзависимой цитотоксичности (CDC). В альтернативных вариантах осуществления используют изотипы IgG2 и IgG4, если антитело предполагается использовать для терапевтических целей и не требуется эффекторная функция антител. Константные Fc-домены, содержащие одну или более аминокислотных модификаций, которые изменяют эффекторные функции антител, такие как таковые, раскрыты в опубликованных патентных заявках США №№ 2005/0037000 и 2005/0064514.
Каркасные облсти и CDR-области гуманизированного антитела не должны точно соответствовать исходным последовательностям, например, донорская CDR или консенсусный каркасный участок можно мутировать с помощью замены, вставки или делеции, по меньшей мере, одного остатка таким образом, CDR или каркасный остаток в этом сайте не соответствовал ни консенсусной области, ни донорскому антителу. В некоторых вариантах осуществления такие мутация не являются значительными. Как правило, по меньшей мере, 75% остатков гуманизированного антитела будут соответствовать таковым исходного каркасной области (FR) и последовательностям CDR, более часто 90% и наиболее часто 95%. Гуманизированные антитела могут быть получены с помощью ряда методик, известных в данной области техники, в том числе, но не ограничиваясь ими, встраивания CDR (Европейский патент № 239400; международная публикация № WO 91/09967; и патенты США №№ 5225539, 5530101 и 5585089), венирования и перекладки (Европейские патенты №№ 592106 и 519596; Padlan, 1991, Molecular Immunology 28(4/5):489-498; Studnicka et al., 1994, Protein Engineering 7(6):805-814, и Roguska et al., 1994, Proc. Natl. Acad. Sci. 91:969973-973), перестановки цепей (патент США №5565332), а также методик, раскрываемых, например, в патентах США №№ 6407213, 5766886, 5585089, международной публикации № WO 9317105, Tan et al., 2002, J. Immunol. 169:1119-25, Caldas et al., 2000, Protein Eng. 13:353-60, Morea et al., 2000, Methods 20:267-79, Baca et al., 1997, J. Biol. Chem. 272:10678-84, Roguska et al., 1996, Protein Eng. 9:895-904, Couto et al., 1995, Cancer Res. 55 (23 Supp):5973s5977s, Couto et al., 1995, Cancer Res. 55:171722, Sandhu, 1994, Gene 150:40910, Pedersen et al., 1994, J. Mol. Biol. 235:95973, Jones et al., 1986, Nature 321:522-525, Riechmann et al., 1988, Nature 332:323, и Presta, 1992, Curr. Op. Struct. Biol. 2:593-596.
Часто каркасные остатки в каркасных областях будут замещаться соответствующим остатком из CDR донорского антитела для изменения, предпочтительно, повышения связывания с антигеном. Эти каркасные замены идентифицируют с помощью способов, хорошо известных в данной области техники, например, с помощью моделирования взаимодействий CDR и каркасных остатков в целях идентификации каркасных остатков, важных для связывания с антигеном, и сравнения последовательностей в целях идентификации необычных каркасных областях в определенных положениях. (См., например, Queen et al., патент США № 5585089; публикации США №№2004/0049014 и 2003/0229208; патенты США №№ 6350861; 6180370; 5693762; 5693761; 5585089 и 5530101, и Riechmann et al., 1988, Nature 332:323).
Человеческие, химерные или гуманизированные производные раскрываемых мышиных анти-человеческий Siglec-15 антител могут быть использованы для способов in vivo у человека. Мышиные антитела или антитела других видов могут быть предпочтительно использованы для многих применений (например, анализов детекции in vitro или in situ, экстренного применения in vivo и т.д.). Такое человеческое или гуманизированное антитело может содержать аминокислотные замены, делеции или добавления в одном или более отличных от человеческих CDR. Производное гуманизированного антитела может иметь по сути такое же связывание, более сильное связывание или более слабое связывание по сравнению с не являющимся производным гуманизированным антителом. В конкретных вариантах осуществления один, два, три, четыре или пять аминокислотных остатков CDR были замещены, удалены или добавлены (т.е., мутированы). Полностью человеческие антитела особенно предпочтительны для терапевтического лечения субъектов-людей.
Такие антитела человека могут быть получены с помощью ряда способов, известных в данной области техники, в том числе способов фагового дисплея с использованием библиотек антител, происходящих из человеческих иммуноглобулиновых последовательностей (см. патенты США №№ 4444887 и 4716111; и международные публикации №№ WO 98/46645, WO 98/50433, WO 98/24893, WO 98/16654, WO 96/34096, WO 96/33735 и WO 91/10741). Такие антитела человека могут быть получены с помощью трансгенных мышей, которые неспособны экспрессировать функциональные эндогенные иммуноглобулины, однако которые могут экспрессировать гены человеческих иммуноглобулинов.
Например, генные комплексы тяжелой и легкой цепи человеческих иммуноглобулинов могут быть введены случайным образом или с помощью гомологичной рекомбинации в эмбриональные стволовые клетки мыши. Альтернативно человеческая вариабельная область, константная область и область разнообразия могут быть введены в мышиные эмбриональные стволовые клетки, помимо генов человеческой тяжелой и легкой цепи. Генам мышиных иммуноглобулинов тяжелой и легкой цепи можно придать нефункциональность в отдельности или одновременно с введением локусов человеческих иммуноглобулинов с помощью гомологичной рекомбинации. В частности, гомозиготная делеция участка JH предупреждает продуцирование эндогенных антител. Модифицированные эмбриональные стволовые клетки экспандируют и их вводят при помощи микроинъекции в бластоцисты с получением химерных мышей. Затем химерных мышей скрещивают с получением гомозиготного потомства, которое экспрессирует человеческие антитела. Трансгенных мышей иммунизируют с помощью стандартных методик выбранным антигеном, например, всем или частью полипептида. Моноклональные антитела, направленные против антигена, могут быть получены от иммунизированных трансгенных мышей с помощью стандартной методики получения гибридом (см., например, патент США № 5916771). Трансгены человеческих иммуноглобулинов, находящиеся в трансгенных мышах, перестраиваются во время дифференцировки B-клеток и впоследствии подвергаются переключению класса и соматической мутации. Таким образом, с помощью такой методики можно получить терапевтически пригодные антитела IgG, IgA, IgM и IgE. Описание этой методики получения антител человека см. в Lonberg and Huszar (1995, Int. Rev. Immunol. 13:65-93, которая включена в данный документ посредством ссылки в полном объеме). Подробное описание этой методики получения человеческих антител и человеческих моноклональных антител и протоколы получения таких антител см., например, в международных публикациях №№ WO 98/24893, WO 96/34096 и WO 96/33735; и патентах США №№ 5413923, 5625126, 5633425, 5569825, 5661016, 5545806, 5814318 и 5939598, которые включены в данный документ посредством ссылки в полном объеме. Помимо этого, производством человеческих антител, направленных против выбранного антигена, могут заниматься компании, используя методики, аналогичные методике, которая описана выше.
Последовательности ДНК, кодирующие человеческие акцепторные каркасные последовательности включают в себя, но не ограничиваясь ими, сегменты FR из сегмента VH1-18 и JH6 зародышевой линии человека VH и сегмента VK-A26 и JK4 из зародышевой линии человека VL. В конкретном варианте осуществления одна или более из CDR вводят в каркасные области с помощью стандартных методик рекомбинантной ДНК. Каркасные области могут встречаться в природе или представлять собой консенсусные каркасные области, и, предпочтительно человеческие каркасные области (см., например, Chothia et al., 1998, “Structural Determinants In The Sequences Of Immunoglobulin Variable Domain,” J. Mol. Biol. 278: 457-479 в отношении перечня человеческих каркасных областей).
C. Последовательности антител
1. Последовательности тяжелой цепи 4C12
В одном варианте осуществления предоставлено мышиное моноклональное антитело или его антигенсвязывающий фрагмент, выделенные из гибридомы 4С12.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
ATGAGATGGAGCTGTATCATCCTCTTCTTGGTAGCAACAGCTACAGGTGTCCACTCCCAGGTCCAAC
TGCAGCAGCCTGGGGCTGAACTGGTGAAGCCTGGGGCTTCAGTGAAGGTGTCCTGCAAGGCTTCTGG
CTACACCTTCACCAGCTACTGGATGCACTGGGTGAAGCAGAGGCCTGGCCAAGGCCTTGAGTGGATT
GGAAGGATTCATCCTTCTGATAGTGATACTAACTACAATCAAAAGTTCAAGGGCAAGGCCACATTGA
CTGTAGACAAATCCTCCAGCACAGCCTACATGCAGCTCAGCAGCCTGACATCTGAGGACTCTGCGGT
CTATTACTGTGCACCCTATGGTAACTACGCCTCCGGGTTTGCTTACTGGGGCCAAGGGACTCTGGTC
ACTGTCTCTGCAGCCAAAACGACACCCCCATCTGTCTATCCACTGGCCCCTGGATCTGCTGCCCAAA
CTAACTCCATGGTGACCCTGGGATGCCTGGTCAAGGGCTATTTCCCTGAGCCAGTGACAGTGACCTG
GAACTCTGGATCCCTGTCCAGCGGTGTGCACACCTTCCCAGCTGTCCTGCAGTCTGACCTCTACACT
CTGAGCAGCTCAGTGACTGTCCCCTCCAGCACCTGGCCCAGCCAGACCGTCACCTGCAACGTTGCCC
ACCCGGCCAGCAGCACCAAGGTGGACAAGAAAATTGTGCCCAGGGATTGTGGTTGTAAGCCTTGCAT
ATGTACAGTCCCAGAAGTATCATCTGTCTTCATCTTCCCCCCAAAGCCCAAGGATGTGCTCACCATT
ACTCTGACTCCTAAGGTCACGTGTGTTGTGGTAGACATCAGCAAGGATGATCCCGAGGTCCAGTTCA
GCTGGTTTGTAGATGATGTGGAGGTGCACACAGCTCAGACGAAACCCCGGGAGGAGCAGATCAACAG
CACTTTCCGTTCAGTCAGTGAACTTCCCATCATGCACCAGGACTGGCTCAATGGCAAGGAGTTCAAA
TGCAGGGTCAACAGTGCAGCTTTCCCTGCCCCCATCGAGAAAACCATCTCCAAAACCAAAGGCAGAC
CGAAGGCTCCACAGGTGTACACCATTCCACCTCCCAAGGAGCAGATGGCCAAGGATAAAGTCAGTCT
GACCTGCATGATAACAAACTTCTTCCCTGAAGACATTACTGTGGAGTGGCAGTGGAATGGGCAGCCA
GCGGAGAACTACAAGAACACTCAGCCCATCATGGACACAGATGGCTCTTACTTCGTCTACAGCAAGC
TCAATGTGCAGAAGAGCAACTGGGAGGCAGGAAATACTTTCACCTGCTCTGTGTTACATGAGGGCCT
GCACAACCACCATACTGAGAAGAGCCTCTCCCACTCTCCTGGTAAATGA (SEQ ID NO:3).
Подчеркнутые последовательности соответствуют определяющим комплементарность областям (CDR). Последовательность с двойным подчеркиванием соответствует константной области. Последовательности с пунктирным подчеркиванием соответствуют лидерной последовательности.
Нуклеиновая кислота может находиться в векторе, например, экспрессионном векторе. Нуклеиновая кислота может быть внехромосомной или вставленной в хромосому клетки-хозяина, например, клетки яичника китайского хомячка.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к:
MRWSCIILFLVATATGVHSQVQLQQPGAELVKPGASVKVSCKASGYTFTSYWMHWVKQRPGQGLEWI
GRIHPSDSDTNYNQKFKGKATLTVDKSSSTAYMQLSSLTSEDSAVYYCAPYGNYASGFAYWGQGTLV
TVSAAKTTPPSVYPLAPGSAAQTNSMVTLGCLVKGYFPEPVTVTWNSGSLSSGVHTFPAVLQSDLYT
LSSSVTVPSSTWPSQTVTCNVAHPASSTKVDKKIVPRDCGCKPCICTVPEVSSVFIFPPKPKDVLTI
TLTPKVTCVVVDISKDDPEVQFSWFVDDVEVHTAQTKPREEQINSTFRSVSELPIMHQDWLNGKEFK
CRVNSAAFPAPIEKTISKTKGRPKAPQVYTIPPPKEQMAKDKVSLTCMITNFFPEDITVEWQWNGQP
AENYKNTQPIMDTDGSYFVYSKLNVQKSNWEAGNTFTCSVLHEGLHNHHTEKSLSHSPGK (SEQ ID NO:4).
Одинарное подчеркивание соответствует лидерной последовательности. Двойное подчеркивание соответствует CDR, а пунктирное подчеркивание соответствует константной области.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь без лидерной последовательности с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к:
QVQLQQPGAELVKPGASVKVSCKASGYTFTSYWMHWVKQRPGQGLEWIGRIHPSDSDTNYNQKFKGKATLTVDKSSSTAYMQLSSLTSEDSAVYYCAPYGNYASGFAYWGQGTLVTVSAAKTTPPSVYPLAPGSAAQTNSMVTLGCLVKGYFPEPVTVTWNSGSLSSGVHTFPAVLQSDLYTLSSSVTVPSSTWPSQTVTCNVAHPASSTKVDKKIVPRDCGCKPCICTVPEVSSVFIFPPKPKDVLTITLTPKVTCVVVDISKDDPEVQFSWFVDDVEVHTAQTKPREEQINSTFRSVSELPIMHQDWLNGKEFKCRVNSAAFPAPIEKTISKTKGRPKAPQVYTIPPPKEQMAKDKVSLTCMITNFFPEDITVEWQWNGQPAENYKNTQPIMDTDGSYFVYSKLNVQKSNWEAGNTFTCSVLHEGLHNHHTEKSLSHSPGK (SEQ ID NO:5).
Двойное подчеркивание соответствует CDR, а прерывистое подчеркивание соответствует константной области.
Аминокислотная последовательность CDR1 тяжелой цепи 4C12 представляет собой
SYWMH (SEQ ID NO:6).
Аминокислотная последовательность CDR2 тяжелой цепи 4C12 представляет собой
RIHPSDSDTNYNQKFKG (SEQ ID NO:7).
Аминокислотная последовательность CDR3 тяжелой цепи 4C12 представляет собой
YGNYASGFAY (SEQ ID NO:8).
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь в соответствии с SEQ ID NO:5 или 5.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:3.
В одном варианте осуществления предоставлено антитело, имеющее три различные CDR, выбранные из группы, состоящей из SEQ ID NO: 6, 7 и 8.
2. Последовательности легкой цепи 4C12
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
ATGGGCATCAAGATGGAGTCACAGATTCAGGCATTTGTATTCGTGTTTCTCTGGTTGTCTGGTGTTG
ACGGAGACATTGTGATGACCCAGTCTCACAAATTCATGTCCACATCAGTAGGAGACAGGGTCAGCAT
CACCTGCAAGGCCAGTCAGGATGTGAGTACTGCTGTAGCCTGGTATCAACAAAAACCAGGGCAATCT
CCTAAACTACTGATTTACTGGGCATCCACCCGGCACACTGGAGTCCCTGATCGCTTCACAGGCAGTG
GATCTGGGACAGATTATACTCTCACCATCAGCAGTGTGCAGGCTGAAGACCTGGCACTTTATTACTG
TCAGCAACATTATAGCACTCCGTGGACGTTCGGTGGAGGCACCAAGCTGGAAATCAAACGGGCTGAT
GCTGCACCAACTGTATCCATCTTCCCACCATCCAGTGAGCAGTTAACATCTGGAGGTGCCTCAGTCG
TGTGCTTCTTGAACAACTTCTACCCCAAAGACATCAATGTCAAGTGGAAGATTGATGGCAGTGAACG
ACAAAATGGCGTCCTGAACAGTTGGACTGATCAGGACAGCAAAGACAGCACCTACAGCATGAGCAGC
ACCCTCACGTTGACCAAGGACGAGTATGAACGACATAACAGCTATACCTGTGAGGCCACTCACAAGA
CATCAACTTCACCCATTGTCAAGAGCTTCAACAGGAATGAGTGTTAG (SEQ ID NO:9).
Пунктирное подчеркивание представляет собой лидерную последовательность. Одинарное подчеркивание представляет собой CDR. Двойное подчеркивание представляет собой константную область.
Нуклеиновая кислота может находиться в векторе, например, экспрессионном векторе. Нуклеиновая кислота может быть внехромосомной или вставленной в хромосому клетки-хозяина, например, клетки яичника китайского хомячка.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, имеющую аминокислотную последовательность, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
MGIKMESQIQAFVFVFLWLSGVDGDIVMTQSHKFMSTSVGDRVSITCKASQDVSTAVAWYQQKPGQS
PKLLIYWASTRHTGVPDRFTGSGSGTDYTLTISSVQAEDLALYYCQQHYSTPWTFGGGTKLEIKRAD
AAPTVSIFPPSSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSS
TLTLTKDEYERHNSYTCEATHKTSTSPIVKSFNRNEC (SEQ ID NO:10).
Подчеркивание представляет собой лидерную последовательность. Двойное подчеркивание представляет собой CDR. Пунктирное подчеркивание представляет собой константную область.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь без лидерной последовательности, имеющую аминокислотную последовательность, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
DIVMTQSHKFMSTSVGDRVSITCKASQDVSTAVAWYQQKPGQSPKLLIYWASTRHTGVPDRFTGSGSGTDYTLTISSVQAEDLALYYCQQHYSTPWTFGGGTKLEIKRADAAPTVSIFPPSSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSSTLTLTKDEYERHNSYTCEATHKTSTSPIVKSFNRNEC (SEQ ID NO:11).
Двойное подчеркивание представляет собой CDR. Пунктирное подчеркивание представляет собой константную область.
Аминокислотная последовательность CDR1 легкой цепи 4C12 представляет собой
KASQDVSTAVA (SEQ ID NO:12).
Аминокислотная последовательность CDR2 легкой цепи 4C12 представляет собой
WASTRHT (SEQ ID NO:13).
Аминокислотная последовательность CDR3 легкой цепи 4C12 представляет собой
QQHYSTPWT (SEQ ID NO:14).
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:10 или 11.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:9.
В одном варианте осуществления предоставлено антитело, имеющее три различные CDR, выбранные из группы, состоящей из SEQ ID NO: 12, 13 и 14.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к SEQ ID NO:4 или 5, и легкую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к SEQ ID NO:10 или 11, или комбинации их легкой и тяжелой цепей.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие три различные CDR тяжелой цепи с аминокислотой, выбранной из группы, состоящей из SEQ ID NO:6, 7 и 8, и три различные CDR легкой цепи с аминокислотами, выбранными из группы, состоящей из SEQ ID NO: 12, 13 и 14.
3. Последовательности тяжелой цепи 2B5
В одном варианте осуществления предоставлено мышиное моноклональное антитело или его антигенсвязывающий фрагмент, выделенные из гибридомы 2B5.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
ATGGAATGGAGCAGAGTCTTTATCTTTCTCCTATCAGTAACTGCAGGTGTTCACTCCCAGGTCCAGC
TGCAGCAGTCTGGAGCTGAGCTGGTAAGGCCTGGGACTTCAGTGAAGGTGTCCTGCAAGGCTTCTGG
ATACGCCTTCACTAATTACTTGATAGAGTGGGTAAAGCAGAGGCCTGGACAGGGCCTTGAGTGGATT
GGAGTGATTAATCCTGGAAGTGGTGGTACTAACTACAATGAGAAGTTCAAGGGCAAGGCAACACTGA
CTGCAGACAAATCCTCCAGCACTGCCTACATGCAGCTCAGCAGCCTGACATCTGAGGACTCTGCGGT
CTATTTCTGTGCAAGATCAGCTCAGGCCCCTGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCC
TCAGAGAGTCAGTCCTTCCCAAATGTCTTCCCCCTCGTCTCCTGCGAGAGCCCCCTGTCTGATAAGA
ATCTGGTGGCCATGGGCTGCCTGGCCCGGGACTTCCTGCCCAGCACCATTTCCTTCACCTGGAACTA
CCAGAACAACACTGAAGTCATCCAGGGTATCAGAACCTTCCCAACACTGAGGACAGGGGGCAAGTAC
CTAGCCACCTCGCAGGTGTTGCTGTCTCCCAAGAGCATCCTTGAAGGTTCAGATGAATACCTGGTAT
GCAAAATCCACTACGGAGGCAAAAACAAAGATCTGCATGTGCCCATTCCAGCTGTCGCAGAGATGAA
CCCCAATGTAAATGTGTTCGTCCCACCACGGGATGGCTTCTCTGGCCCTGCACCACGCAAGTCTAAA
CTCATCTGCGAGGCCACGAACTTCACTCCAAAACCGATCACAGTATCCTGGCTAAAGGATGGGAAGC
TCGTGGAATCTGGCTTCACCACAGATCCGGTGACCATCGAGAACAAAGGATCCACACCCCAAACCTA
CAAGGTCATAAGCACACTTACCATCTCTGAAATCGACTGGCTGAACCTGAATGTGTACACCTGCCGT
GTGGATCACAGGGGTCTCACCTTCTTGAAGAACGTGTCCTCCACATGTGCTGCCAGTCCCTCCACAG
ACATCCTAACCTTCACCATCCCCCCCTCCTTTGCCGACATCTTCCTCAGCAAGTCCGCTAACCTGAC
CTGTCTGGTCTCAAACCTGGCAACCTATGAAACCCTGAATATCTCCTGGGCTTCTCAAAGTGGTGAA
CCACTGGAAACCAAAATTAAAATCATGGAAAGCCATCCCAATGGCACCTTCAGTGCTAAGGGTGTGG
CTAGTGTTTGTGTGGAAGACTGGAATAACAGGAAGGAATTTGTGTGTACTGTGACTCACAGGGATCT
GCCTTCACCACAGAAGAAATTCATCTCAAAACCCAATGAGGTGCACAAACATCCACCTGCTGTGTAC
CTGCTGCCACCAGCTCGTGAGCAACTGAACCTGAGGGAGTCAGCCACAGTCACCTGCCTGGTGAAGG
GCTTCTCTCCTGCAGACATCAGTGTGCAGTGGCTTCAGAGAGGGCAACTCTTGCCCCAAGAGAAGTA
TGTGACCAGTGCCCCGATGCCAGAGCCTGGGGCCCCAGGCTTCTACTTTACCCACAGCATCCTGACT
GTGACAGAGGAGGAATGGAACTCCGGAGAGACCTATACCTGTGTTGTAGGCCACGAGGCCCTGCCAC
ACCTGGTGACCGAGAGGACCGTGGACAAGTCCACTGGTAAACCCACACTGTACAATGTCTCCCTGAT
CATGTCTGACACAGGCGGCACCTGCTATTGA (SEQ ID NO:15).
Подчеркнутые последовательности соответствуют определяющим комплементарность областям (CDR). Последовательность с двойным подчеркиванием соответствует константной области. Последовательности с пунктирным подчеркиванием соответствуют лидерной последовательности.
Нуклеиновая кислота может находиться в векторе, например, экспрессионном векторе. Нуклеиновая кислота может быть внехромосомной или вставленной в хромосому клетки-хозяина, например, клетки яичника китайского хомячка.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к:
MEWSRVFIFLLSVTAGVHSQVQLQQSGAELVRPGTSVKVSCKASGYAFTNYLIEWVKQRPGQGLEWI
GVINPGSGGTNYNEKFKGKATLTADKSSSTAYMQLSSLTSEDSAVYFCARSAQAPDYWGQGTTLTVS
SESQSFPNVFPLVSCESPLSDKNLVAMGCLARDFLPSTISFTWNYQNNTEVIQGIRTFPTLRTGGKY
LATSQVLLSPKSILEGSDEYLVCKIHYGGKNKDLHVPIPAVAEMNPNVNVFVPPRDGFSGPAPRKSK
LICEATNFTPKPITVSWLKDGKLVESGFTTDPVTIENKGSTPQTYKVISTLTISEIDWLNLNVYTCR
VDHRGLTFLKNVSSTCAASPSTDILTFTIPPSFADIFLSKSANLTCLVSNLATYETLNISWASQSGE
PLETKIKIMESHPNGTFSAKGVASVCVEDWNNRKEFVCTVTHRDLPSPQKKFISKPNEVHKHPPAVY
LLPPAREQLNLRESATVTCLVKGFSPADISVQWLQRGQLLPQEKYVTSAPMPEPGAPGFYFTHSILT
VTEEEWNSGETYTCVVGHEALPHLVTERTVDKSTGKPTLYNVSLIMSDTGGTCY (SEQ ID NO:16).
Одинарное подчеркивание соответствует лидерной последовательности. Двойное подчеркивание соответствует CDR, а пунктирное подчеркивание соответствует константной области.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь без лидерной последовательности с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к:
QVQLQQSGAELVRPGTSVKVSCKASGYAFTNYLIEWVKQRPGQGLEWIGVINPGSGGTNYNEKFKGKATLTADKSSSTAYMQLSSLTSEDSAVYFCARSAQAPDYWGQGTTLTVSSESQSFPNVFPLVSCESPLSDKNLVAMGCLARDFLPSTISFTWNYQNNTEVIQGIRTFPTLRTGGKYLATSQVLLSPKSILEGSDEYLVCKIHYGGKNKDLHVPIPAVAEMNPNVNVFVPPRDGFSGPAPRKSKLICEATNFTPKPITVSWLKDGKLVESGFTTDPVTIENKGSTPQTYKVISTLTISEIDWLNLNVYTCRVDHRGLTFLKNVSSTCAASPSTDILTFTIPPSFADIFLSKSANLTCLVSNLATYETLNISWASQSGEPLETKIKIMESHPNGTFSAKGVASVCVEDWNNRKEFVCTVTHRDLPSPQKKFISKPNEVHKHPPAVYLLPPAREQLNLRESATVTCLVKGFSPADISVQWLQRGQLLPQEKYVTSAPMPEPGAPGFYFTHSILTVTEEEWNSGETYTCVVGHEALPHLVTERTVDKSTGKPTLYNVSLIMSDTGGTCY (SEQ ID NO:17).
Двойное подчеркивание соответствует CDR, а пунктирное подчеркивание соответствует константной области.
Аминокислотная последовательность CDR1 тяжелой цепи 2B5 представляет собой
NYLIE (SEQ ID NO:18).
Аминокислотная последовательность CDR2 тяжелой цепи 2B5 представляет собой
VINPGSGGTNYNEKFKG (SEQ ID NO:19).
Аминокислотная последовательность CDR3 тяжелой цепи 2B5 представляет собой
SAQAPDY (SEQ ID NO:20).
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь в соответствии с SEQ ID NO:16 или 17.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:15.
В одном варианте осуществления предоставлено антитело, имеющее три различные CDR, выбранные из группы, состоящей из SEQ ID NO: 18, 19 и 20.
4. Последовательности легкой цепи 2B5
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
ATGGGCATCAAGATGGAGACACATTCTCAGGTCTTTGTATACATGTTGCTGTGGTTGTCTGGTGTTG
AAGGAGACATTGTGATGACCCAGTCTCACAAATTCATGTCCACATCAGTAGGAGACAGGGTCAGCAT
CACCTGCAAGGCCAGTCAGGATGTGGGTACTGCTGTAGCCTGGTATCAACAGAAACCAGGGCAATCT
CCTAAACTACTGATTTACTGGGCATCCACCCGGCACACTGGAGTCCCTGATCGCTTCACAGGCAGTG
GATCTGGGACAGATTTCACTCTCACCATTAGCAATGTGCAGTCTGAAGACTTGGCAGATTATTTCTG
TCAGCAATATAGCAGCTATCCATTCACGTTCGGCTCGGGGACAAAGTTGGAAATAAAACGGGCTGAT
GCTGCACCAACTGTATCCATCTTCCCACCATCCAGTGAGCAGTTAACATCTGGAGGTGCCTCAGTCG
TGTGCTTCTTGAACAACTTCTACCCCAAAGACATCAATGTCAAGTGGAAGATTGATGGCAGTGAACG
ACAAAATGGCGTCCTGAACAGTTGGACTGATCAGGACAGCAAAGACAGCACCTACAGCATGAGCAGC
ACCCTCACGTTGACCAAGGACGAGTATGAACGACATAACAGCTATACCTGTGAGGCCACTCACAAGA
CATCAACTTCACCCATTGTCAAGAGCTTCAACAGGAATGAGTGTTAG (SEQ ID NO:21).
Пунктирное подчеркивание представляет собой лидерную последовательность. Одинарное подчеркивание представляет собой CDR. Двойное подчеркивание представляет собой константную область.
Нуклеиновая кислота может находиться в векторе, например, экспрессионном векторе. Нуклеиновая кислота может быть внехромосомной или вставленной в хромосому клетки-хозяина, например, клетки яичника китайского хомячка.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, имеющую аминокислотную последовательность, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
MGIKMETHSQVFVYMLLWLSGVEGDIVMTQSHKFMSTSVGDRVSITCKASQDVGTAVAWYQQKPGQS
PKLLIYWASTRHTGVPDRFTGSGSGTDFTLTISNVQSEDLADYFCQQYSSYPFTFGSGTKLEIKRAD
AAPTVSIFPPSSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSS
TLTLTKDEYERHNSYTCEATHKTSTSPIVKSFNRNEC (SEQ ID NO:22).
Подчеркивание представляет собой лидерную последовательность. Двойное подчеркивание представляет собой CDR. Пунктирное подчеркивание представляет собой константную область.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь без лидерной последовательности, имеющую аминокислотную последовательность, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
DIVMTQSHKFMSTSVGDRVSITCKASQDVSTAVAWYQQKPGQSPKLLIYWASTRHTGVPDRFTGSGSGTDYTLTISSVQAEDLALYYCQQHYSTPWTFGGGTKLEIKRADAAPTVSIFPPSSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSSTLTLTKDEYERHNSYTCEATHKTSTSPIVKSFNRNEC (SEQ ID NO:23).
Двойное подчеркивание представляет собой CDR. Пунктирное подчеркивание представляет собой константную область.
Аминокислотная последовательность CDR1 легкой цепи 2B5 представляет собой
KASQDVSTAVA (SEQ ID NO:24).
Аминокислотная последовательность CDR2 легкой цепи 2B5 представляет собой
WASTRHT (SEQ ID NO:13).
Аминокислотная последовательность CDR3 легкой цепи 2B5 представляет собой
QQHYSTPWT (SEQ ID NO:25).
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:22 или 23.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:21.
В одном варианте осуществления предоставлено антитело, имеющее три различные CDR, выбранные из группы, состоящей из SEQ ID NO: 24, 13 и 25.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к SEQ ID NO:16 или 17, и легкую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к SEQ ID NO:22 или 23, или комбинации их легкой и тяжелой цепей.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие три различные CDR тяжелой цепи с аминокислотой, выбранной из группы, состоящей из SEQ ID NO:18, 19 и 20, и три различные CDR легкой цепи с аминокислотами, выбранными из группы, состоящей из SEQ ID NO: 24, 13 и 25.
6. Последовательности тяжелой цепи 4G9
В одном варианте осуществления предоставлено мышиное моноклональное антитело или его антигенсвязывающий фрагмент, выделенные из гибридомы 4G9.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
ATGGGTTGGCTGTGGAACTTGCTATTCCTGATGGCAGCTGCCCAAAGTGCCCAAGCACAGATCCAGT
TGGTACAGTCTGGACCTGAGCTGAAGAAGCCTGGAGAGACAGTCAAGATCTCCTGCAAGGCTTCTGG
GTATACCTTCACAACCTATGGAATGACCTGGGTGAAACAGGCTCCAGGAAAGGGTTTAAAGTGGATG
GGCTGGATAAACACCTACTCTGGAGTGCCAACATATGCTGATGACTTCAAGGGACGGTTTGCCTTCT
CTTTGGAAACCTCTGCCAGCACTGCCTATTTGCAGATCAACAACCTCAAAAATGAGGACACGGCTAC
ATATTTCTGTGCAAGAGGGGGACGGGGGTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCT
GCAGCCAAAACAACACCCCCATCAGTCTATCCACTGGCCCCTGGGTGTGGAGATACAACTGGTTCCT
CTGTGACTCTGGGATGCCTGGTCAAGGGCTACTTCCCTGAGTCAGTGACTGTGACTTGGAACTCTGG
ATCCCTGTCCAGCAGTGTGCACACCTTCCCAGCTCTCCTGCAGTCTGGACTCTACACTATGAGCAGC
TCAGTGACTGTCCCCTCCAGCACCTGGCCAAGTCAGACCGTCACCTGCAGCGTTGCTCACCCAGCCA
GCAGCACCACGGTGGACAAAAAACTTGAGCCCAGCGGGCCCATTTCAACAATCAACCCCTGTCCTCC
ATGCAAGGAGTGTCACAAATGCCCAGCTCCTAACCTCGAGGGTGGACCATCCGTCTTCATCTTCCCT
CCAAATATCAAGGATGTACTCATGATCTCCCTGACACCCAAGGTCACGTGTGTGGTGGTGGATGTGA
GCGAGGATGACCCAGACGTCCGGATCAGCTGGTTTGTGAACAACGTGGAAGTACACACAGCTCAGAC
ACAAACCCATAGAGAGGATTACAACAGTACTATCCGGGTGGTCAGTGCCCTCCCCATCCAGCACCAG
GACTGGATGAGTGGCAAGGAGTTCAAATGCAAGGTCAACAACAAAGACCTCCCATCACCCATCGAGA
GAACCATCTCAAAAATTAAAGGGCTAGTCAGAGCTCCACAAGTATACATCTTGCCGCCACCAGCAGA
GCAGTTGTCCAGGAAAGATGTCAGTCTCACTTGCCTGGTCGTGGGCTTCAACCCTGGAGACATCAGT
GTGGAGTGGACCAGCAATGGGCATACAGAGGAGAACTACAAGGACACCGCACCAGTCCTGGACTCTG
ACGGTTCTTACTTCATATACAGCAAGCTCGATATAAAAACAAGCAAGTGGGAGAAAACAGATTCCTT
CTCATGCAACGTGAGACACGAGGGTCTGAAAAATTACTACCTGAAGAAGACCATCTCCCGGTCTCCG
GGTAAATGA (SEQ ID NO:26).
Подчеркнутые последовательности соответствуют определяющим комплементарность областям (CDR). Последовательность с двойным подчеркиванием соответствует константной области. Последовательности с пунктирным подчеркиванием соответствуют лидерной последовательности.
Нуклеиновая кислота может находиться в векторе, например, экспрессионном векторе. Нуклеиновая кислота может быть внехромосомной или вставленной в хромосому клетки-хозяина, например, клетки яичника китайского хомячка.
В одном варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к:
MGWLWNLLFLMAAAQSAQAQIQLVQSGPELKKPGETVKISCKASGYTFTTYGMTWVKQAPGKGLKWM GWINTYSGVPTYADDFKGRFAFSLETSASTAYLQINNLKNEDTATYFCARGGRGFAYWGQGTLVTVS
AAKTTPPSVYPLAPGCGDTTGSSVTLGCLVKGYFPESVTVTWNSGSLSSSVHTFPALLQSGLYTMSS
SVTVPSSTWPSQTVTCSVAHPASSTTVDKKLEPSGPISTINPCPPCKECHKCPAPNLEGGPSVFIFP
PNIKDVLMISLTPKVTCVVVDVSEDDPDVRISWFVNNVEVHTAQTQTHREDYNSTIRVVSALPIQHQ
DWMSGKEFKCKVNNKDLPSPIERTISKIKGLVRAPQVYILPPPAEQLSRKDVSLTCLVVGFNPGDIS
VEWTSNGHTEENYKDTAPVLDSDGSYFIYSKLDIKTSKWEKTDSFSCNVRHEGLKNYYLKKTISRSP
GK (SEQ ID NO:27).
Одинарное подчеркивание соответствует лидерной последовательности. Двойное подчеркивание соответствует CDR, а пунктирное подчеркивание соответствует константной области.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь без лидерной последовательности с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к:
QIQLVQSGPELKKPGETVKISCKASGYTFTTYGMTWVKQAPGKGLKWMGWINTYSGVPTYADDFKGRFAFSLETSASTAYLQINNLKNEDTATYFCARGGRGFAYWGQGTLVTVSAAKTTPPSVYPLAPGCGDTTGSSVTLGCLVKGYFPESVTVTWNSGSLSSSVHTFPALLQSGLYTMSSSVTVPSSTWPSQTVTCSVAHPASSTTVDKKLEPSGPISTINPCPPCKECHKCPAPNLEGGPSVFIFPPNIKDVLMISLTPKVTCVVVDVSEDDPDVRISWFVNNVEVHTAQTQTHREDYNSTIRVVSALPIQHQDWMSGKEFKCKVNNKDLPSPIERTISKIKGLVRAPQVYILPPPAEQLSRKDVSLTCLVVGFNPGDISVEWTSNGHTEENYKDTAPVLDSDGSYFIYSKLDIKTSKWEKTDSFSCNVRHEGLKNYYLKKTISRSP
GK (SEQ ID NO:28).
Двойное подчеркивание соответствует CDR, а пунктирное подчеркивание соответствует константной области.
Аминокислотная последовательность CDR1 тяжелой цепи 4G9 представляет собой
TYGMT (SEQ ID NO:29).
Аминокислотная последовательность CDR2 тяжелой цепи 4G9 представляет собой
WINTYSGVPTYADDFKG (SEQ ID NO:30).
GGRGFAY (SEQ ID NO:31).
В одном варианте осуществления предоставлены антитело 4G9 или его антигенсвязывающий фрагмент, имеющие тяжелую цепь в соответствии с SEQ ID NO:27 или 28.
В другом варианте осуществления предоставлены антитело 4G9 или его антигенсвязывающий фрагмент, имеющие тяжелую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:26.
В одном варианте осуществления предоставлено антитело 4G9, имеющее три различные CDR, выбранные из группы, состоящей из SEQ ID NO: 29, 30 и 31.
7. Последовательности легкой цепи 4G9
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
ATGGTATCCACACCTCAGTTCCTTGTATTTTTGCTTTTCTGGATTCCAGCCTCCAGAGGTGACATCT
TGCTGACTCAGTCTCCAGCCATCCTGTCTGTGAGTCCAGGAGAAAGAGTCAGTTTCTCCTGCAGGGC
CAGTCAGAGCATTGGCACAAGCATACACTGGTATCAGCAAAGAACAAATGGTTCTCCAAGGCTTCTC
ATAAAGTATGCTTCTGAGTCTATCTCTGGGATCCCTTCCAGGTTTAGTGGCAGTGGATCAGGGACAG
ATTTTACTCTTAGCATCAACAGTGTGGAGTCTGAAGATATTGCAGATTATTACTGTCAACAAAGTAA
TAGCTGGCCGTACACGTTCGGAGGGGGGACCAAGCTGGAAATAAAACGGGCTGATGCTGCACCAACT
GTATCCATCTTCCCACCATCCAGTGAGCAGTTAACATCTGGAGGTGCCTCAGTCGTGTGCTTCTTGA
ACAACTTCTACCCCAAAGACATCAATGTCAAGTGGAAGATTGATGGCAGTGAACGACAAAATGGCGT
CCTGAACAGTTGGACTGATCAGGACAGCAAAGACAGCACCTACAGCATGAGCAGCACCCTCACGTTG
ACCAAGGACGAGTATGAACGACATAACAGCTATACCTGTGAGGCCACTCACAAGACATCAACTTCAC
CCATTGTCAAGAGCTTCAACAGGAATGAGTGTTAG (SEQ ID NO:32).
Пунктирное подчеркивание представляет собой лидерную последовательность. Одинарное подчеркивание представляет собой CDR. Двойное подчеркивание представляет собой константную область.
Нуклеиновая кислота может находиться в векторе, например, экспрессионном векторе. Нуклеиновая кислота может быть внехромосомной или вставленной в хромосому клетки-хозяина, например, клетки яичника китайского хомячка.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь, имеющую аминокислотную последовательность, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
MVSTPQFLVFLLFWIPASRGDILLTQSPAILSVSPGERVSFSCRASQSIGTSIHWYQQRTNGSPRLLIKYASESISGIPSRFSGSGSGTDFTLSINSVESEDIADYYCQQSNSWPYTFGGGTKLEIKRADAAPTVSIFPPSSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSSTLTLTKDEYERHNSYTCEATHKTSTSPIVKSFNRNEC (SEQ ID NO:33).
Подчеркивание представляет собой лидерную последовательность. Двойное подчеркивание представляет собой CDR. Пунктирное подчеркивание представляет собой константную область.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие легкую цепь без лидерной последовательности, имеющую аминокислотную последовательность, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к:
DILLTQSPAILSVSPGERVSFSCRASQSIGTSIHWYQQRTNGSPRLLIKYASESISGIPSRFSGSGSGTDFTLSINSVESEDIADYYCQQSNSWPYTFGGGTKLEIKRADAAPTVSIFPPSSEQLTSGGASVVCFLNNFYPKDINVKWKIDGSERQNGVLNSWTDQDSKDSTYSMSSTLTLTKDEYERHNSYTCEATHKTSTSPIVKSFNRNEC (SEQ ID NO:34).
Двойное подчеркивание представляет собой CDR. Пунктирное подчеркивание представляет собой константную область.
Аминокислотная последовательность CDR1 легкой цепи 4G9 представляет собой
RASQSIGTSIH (SEQ ID NO:35).
Аминокислотная последовательность CDR2 легкой цепи 4G9 представляет собой
YASESIS (SEQ ID NO:36).
Аминокислотная последовательность CDR3 легкой цепи 4G9 представляет собой
QQSNSWPYT (SEQ ID NO:37).
В одном варианте осуществления предоставлены антитело 4G9 или его антигенсвязывающий фрагмент, имеющие легкую цепь, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:33 или 34.
В другом варианте осуществления предоставлены антитело 4G9 или его антигенсвязывающий фрагмент, имеющие легкую цепь, кодируемую нуклеиновой кислотой, по меньшей мере, с 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичностью последовательности по отношению к SEQ ID NO:32.
В одном варианте осуществления предоставлено антитело 4G9, имеющее три различные CDR, выбранные из группы, состоящей из SEQ ID NO:35, 36 и 37.
В другом варианте осуществления предоставлены антитело или его антигенсвязывающий фрагмент, имеющие тяжелую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к SEQ ID NO:27 или 28, и легкую цепь с аминокислотной последовательностью, имеющей, по меньшей мере, 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или 100% идентичность последовательности по отношению к SEQ ID NO:33 или 34, или комбинации их легкой и тяжелой цепей.
В другом варианте осуществления предоставлены антитело 4G9 или его антигенсвязывающий фрагмент, имеющие три различные CDR тяжелой цепи с аминокислотой, выбранной из группы, состоящей из SEQ ID NO:29, 30 и 31, и три различные CDR легкой цепи с аминокислотами, выбранными из группы, состоящей из SEQ ID NO:35, 36 и 37.
D. Активирующий эпитоп PD-1
В данном документе раскрыты эпитоп-специфичные фрагменты, связывающие PD-1. В одном варианте осуществления раскрываемые связывающие фрагменты иммуноспецифично связываются с PD-1 и активируют опосредованную PD-1 передачу сигнала.
Раскрываемый эпитоп PD-1 образован аминокислотами 96-110 SEQ ID NO:1 и имеет следующую аминокислотную последовательность:
TYLCGAISLAPKAQI (SEQ ID NO:38).
1. Антитела
В одном варианте осуществления предоставлено антитело или его эпитопсвязывающий фрагмент, которые иммуноспецифично связываются с SEQ ID NO:38 на поверхности иммунной клетки и активирует иммунную клетку. В одном варианте осуществления предпочтительная иммунная клетка представляет собой T-клетку, более конкретно CD8+ T-клетку. В другом варианте осуществления антитело или его эпитопсвязывающий фрагмент иммуноспецифично связывают SEQ ID NO:38 PD-1 на поверхности иммунной клетки и стимулирует или индуцирует активирующей сигнал посредством PD-1 с целью активации иммунной клетки.
Эпитопспецифичное антитело может представлять собой моноклональное антитело, гуманизированное антитело, человеческое антитело, мышиное антитело, химерное антитело или их фрагмент. Иллюстративные антитела и способы их получения обсуждаются ниже.
2. Слитый белок
В одном варианте осуществления эпитопспецифичный связывающий фрагмент PD-1 представляет собой слитый белок. Все или часть одного или более из раскрываемых антител к эпитопу PD-1 или эпитопсвязывающих фрагментов могут связываться с другими полипептидами с образованием слитых белков. Слитые полипептиды имеют первого партнера слияния, включающего в себя все или часть из одного или более из раскрываемых антител к эпитопу PD-1 или эпитопсвязывающих фрагментов, слитого со вторым полипептидом непосредственно или с помощью последовательности линкерного пептида, который слит со вторым полипептидом. Слитые белки необязательно содержат домен, который функционирует с целью димеризации двух или более слитых белков. Пептидный/полипептидный линкерный домен может представлять собой либо отдельный домен, либо в качестве альтернативы содержаться в одном из других доменов (первом полипептиде или втором полипепиде) слитого белка. Аналогичным образом, домен, который функционирует с целью димеризации или мультимеризации слитых белков, может представлять собой либо отдельный домен, либо в качестве альтернативые содержаться в одном из других доменов (первом полипептиде, втором полипептиде или пептидном/полипептидном линкерном домене) слитого белка. В одном варианте осуществления домен димеризации/мультимеризации и пептидный/полипептидный линкерный домен представляют собой одно и то же.
Слитые белки, раскрываемые в данном документе, представлены формулой I:
N-R1-R2-R3-C,
где «N» представляет собой N-конец слитого белка, «C» представляет собой C-конец слитого белка, «R1» представляет собой все или часть одного из раскрываемых антител к эпитопу PD-1 или эпитопсвязывающим фрагментам или их функциональному варианту или фрагменту, «R2» представляет собой необязательный пептидный/полипептидный линкерный домен и «R3» представляет собой второй полипептид. В качестве альтернативы R3 представляет собой все или часть из одного из раскрываемых антител к эпитопу PD-1 или эпитопсвязывающих фрагментов или их функционального варианта или фрагмента, а R1 представляет собой второй полипептид.
Димеризация или мультимеризация может происходить между или в пределах одного или более слитых белков с участием доменов димеризации или мультимеризации. В альтернативном случае димеризация или мультимеризация слитых белков может происходить с помощью химического сшивания. Димеры или мультимеры, которые образуются, могут быть гомодимерными/гомомультимерными или гетеродимерными/гетеромультимерными.
3. Аптамеры
В некоторых вариантах осуществления эпитопспецифичный связывающий фрагмент представляет собой аптамер. Аптамеры представляют собой молекулы, которые взаимодействуют с целевой молекулой, предпочтительно специфичным образом. В одном варианте осуществления аптамер связывается с SEQ ID NO:38 на поверхности иммунной клетки и стимулирует или индуцирует активирующей сигнал посредством PD-1 с целью активации иммунной клетки. В типичном случае аптамеры представляют собой малые нуклеиновые кислоты, длина которых находится в диапазоне 15-50 оснований, которые свернуты в определенные вторичные и третичные структуры, такие как петли на стебле или G-квартеты. Аптамеры могут связываться с белком, клетками, малыми органическими молекулами или пептидами. Аптамеры могут связывать малые молекулы, такие как АТФ и теофиллин, а также крупные молекулы, такие как обратную транскриптазу и тромбин. Аптамеры могут связываться очень прочно со значением Kd в отношении целевой молекулы, составляющим менее 10-12 M. Предпочтительно, что аптамеры связывают целевую молекулу со значением Kd, составляющим менее 10-6, 10-8, 10-10 или 10-12. Аптамеры могут связывать целевую молекулу с очень высокой степенью специфичности. Например, были выделены аптамеры, которые имеют более чем 10000-кратную разницу аффинностей связывания по отношению к целевой молекуле и другой молекуле, которые отличаются только в одном положении молекулы. Предпочтительно, чтобы аптамер имел значение Kd в отношении целевой молекулы, составляющее, по меньшей мере в 10, 100, 1000, 10000 или 100000 раз меньше, чем значение Kd в отношении фоновой связывающей молекулы. При сравнении полипептида предпочтительно, чтобы фоновая молекула представляла собой другой полипептид. Иллюстративные примеры того, как получать и применять аптамеры для связывания ряда различных целевых молекул известны в данной области техники.
4. Малые молекулы
В некоторых вариантах осуществления эпитопсвязывающий фрагмент может представлять собой малую молекулу. Термин «малая молекула» в целом относится к малым неорганическим соединениям, имеющим молекулярную массу, составляющую более около 100 и менее около 2500 дальтон, предпочтительно от 100 до 2000, более предпочтительно от около 100 до около 1250, более предпочтительно от около 100 до около 1000, более предпочтительно от около 100 до около 750, более предпочтительно от около 200 до около 500 дальтон. Агонисты малых молекул активирующего эпитопа PD-1 могут быть определены с помощью стандартных способов скрининга. В некоторых вариантах осуществления скрининговый анализ может включать в себя случайный скрининг крупных библиотек исследуемых соединений. Анализы могут включать в себя определения индуцированных PD-1 иммунного ответа или активации T-клеток.
E. Фармацевтические композиции
Предложены фармацевтические композиции, содержащие раскрываемые антитела и их антигенсвязывающие фрагменты. Фармацевтические композиции, содержащие антитела и их антигенсвязывающие фрагменты, могут быть предназначены для введения путем парентеральной (внутримышечной, интраперитонеальной, внутривенной (в/в) или подкожной инъекции.
В некоторых подходах in vivo композиции, раскрываемые в данном документе, вводят субъекту в терапевтически эффективном количестве. Используемый в данном документе термин «эффективное количество» или «терапевтически эффективное количество» означает дозу, достаточную для лечения, ингибирования или нормализации одного или более симптомов нарушения, подлежащего лечению, или для обеспечения иным образом необходимого фармакологического и/или физиологического эффекта. Точная доза будет варьировать в зависимости от ряда факторов, таких как зависящие от субъекта переменные (например, возраст, состояние иммунной системы и т.д.), заболевание и лечение, подлежащее проведению.
В отношении раскрываемых антител и их антигенсвязывающих фрагментов, по мере проведения дополнительных исследований, будет появляться информация в отношении уровней доз для лечения различных состояний, и специалист в данной области техники, учитывая терапевтический контекст, возраст и общее состояние здоровья реципиента, будет способен определить соответствующую дозу. Выбранная доза зависит от необходимого терапевтического эффекта, от пути введения и от длительности необходимого лечения. В отношении раскрываемых антител и их антигенсвязывающих фрагментов, как правило, млекопитающим вводят уровни доз, составляющие от 0,001 до 20 мг/кг массы тела. Как правило, в случае внутривенной инъекции или инфузии, доза может быть более низкой.
В определенных вариантах осуществления антитела или их антигенсвязывающие фрагменты вводят локально, например, путем инъекции непосредственно в участок, подлежащий лечению. В типичном случае инъекция вызывает повышенную локальную концентрацию композиции иммуномодулирующего агента, которая является более высокой, чем концентрация, которая может быть достигнута в результате системного введения. Композиции иммуномодулирующего агента могут быть комбинированы с матрицей, как описано выше, для содействия в создании повышенной локальной концентрации полипептидных композиций в результате снижения пассивной диффузии полипептидов вне участка, подлежащего лечению.
1. Составы для парентерального введения
В некоторых вариантах осуществления композиции, содержащие раскрываемые антитела и антигенсвязывающие фрагменты, вводят в водном растворе, путем парентеральной инъекции. Состав также может находиться в форме суспензии или эмульсии. В целом предоставлены фармацевтические композиции, содержащие эффективные количества антитела или его антигенсвязыавющего фрагмента, и необязательно содержащие фармацевтически приемлемые разбавители, консерванты, солюбилизаторы, эмульгаторы, вспомогательные вещества и/или носители. Такие композиции необязательно содержат одно или более из следующего: разбавители, стерильную воду, забуференный физиологический раствор с различным содержанием буфера (например, Трис-HCl, ацетатный, фосфатный), pH и ионной силой; и вспомогательные вещества, такие как детергенты и солюбилизирующие агенты (например, TWEEN 20 (полисорбат-20), TWEEN 80 (полисорбат-80)), антиоксиданты (например, аскорбиновую кислоту, метабисульфит натрия) и консерванты (например, тимерасол, бензиловый спирт) и объемообразующие вещества (например, лактозу, маннит). Примеры неводных растворителей и носителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин и инъекционные органические сложные эфиры, такие как этилолеат. Составы могут быть лиофилизированными или повторно растворенными/ресуспендированными непосредственно перед использованием. Состав может быть стерилизован, например, с помощью фильтрации через фильтр, удерживающий бактерий, с помощью включения стерилизующих агентов в композиции, с помощью облучения композиций или с помощью нагревания композиций.
2. Составы для перорального введения
В некоторых вариантах осуществления композиции антитела составляют для пероральной доставки. Лекарственные формы антител для перорального введения являются устойчивыми к протеолизу и могут доставлять более высокую часть иммунореактивного антитела локально в желудочно-кишечный тракт для лечения инфекций или обеспечения всасывания антител для лечения или предупреждения системных патологических состояний (Reilly, RM, et al. Clin Pharmacokinet., 32(4):313-23 (1997); Victoria S Jasion and Bruce P Burnett, Nutr J.; 14: 22 (2015); и Philippart, M., et al., Drug Res (Stuttg) 66(03):113-120 (2016)).
Твердые лекарственные формы для перорального введения в целом описаны в Remington's Pharmaceutical Sciences, 18th Ed. 1990 (Mack Publishing Co. Easton Pa. 18042) во главе 89. Твердые лекарственные формы включают в себя таблетки, капсулы, пилюли, троше или пастилки для рассасывания, облатки, пеллеты, порошки или гранулы или включение вещества в препараты на основе микрочастиц полимерных соединений, таких как полилактидная кислота, полигликолевая кислота и т.д. в липосомы. Такие композиции могут влиять на физическое состояние, стабильность, скорость высвобождения in vivo и скорость выведения in vivo раскрываемого соединения. См., например, Remington's Pharmaceutical Sciences, 18th Ed. (1990, Mack Publishing Co., Easton, Pa. 18042), стр. 1435-1712, которая включена в данный документ посредством ссылки. Композиции могут быть приготовлены в жидкой форме или могут находиться в сухо порошковой (например, лиофилизированной) форме. Инкапсулирование в липосомы или протеноиды может быть использовано для составления композиций. Может быть использовано инкапсулирование в липосомы, и липосомы могут быть дериватизированы различными полимерами (например, патент США № 5013556). См. также Marshall, K. в: Modern Pharmaceutics Edited by G. S. Banker and C. T. Rhodes Chapter 10, 1979. Как правило, состав будет содержать пептид (или их химически модифицированные формы) и инертные ингредиенты, которые защищают пептид в среде желудка и высвобождают биологически активное вещество в кишечник.
Антитела и их антигенсвязывающие фрагменты могут быть химически модифицированы для того, чтобы пероральная доставка производного была эффективной. Как правило, предполагаемая химическая модификация представляет собой присоединение, по меньшей мере, одного фрагмента к молекуле самого компонента, при этом фрагмент обеспечивает поступление в кровоток из желудка или кишечника или поступление непосредственно в слизистую оболочку кишечника. Кроме того, необходимо повышение общей стабильности компонента или компонентов и повышение времени циркуляции в организме. Пэгилирование представляет собой иллюстративную химическую модификацию для фармацевтического применения. Другие фрагменты, которые могут быть использованы, включают в себя: пропиленгликоль, сополимеры этиленгликоля и пропиленгликоля, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, полипролин, поли-1,3-диоксолан и поли-1,3,6-тиоксокан [см., например, Abuchowski and Davis (1981) "Soluble Polymer-Enzyme Adducts," в Enzymes as Drugs. Hocenberg and Roberts, eds. (Wiley-Interscience: New York, N.Y.) pp. 367-383; и Newmark, et al. (1982) J. Appl. Biochem. 4:185-189].
В другом варианте осуществления предоставлены жидкие лекарственные формы для перорального введения, в том числе фармацевтически приемлемые эмульсии, растворы, суспензии и сиропы, которые могут содержать другие компоненты, в том числе инертные растворители; вспомогательные вещества, такие как смачивающие средства, эмульгирующие и суспендирующие средства; и подсластители, ароматизаторы и отдушки.
В случае составов для перорального введения участком высвобождения может быть желудок, тонкий кишечник (двенадцатиперстная кишка, тощая кишка или подвздошная кишка) или толстый кишечник. В некоторых вариантах осуществления высвобождение будет устранять вредные эффекты среды желудка, либо в результате защиты агента (или производного), либо в результате высвобождения агента (или производного) за пределами среды желудка, например, в кишечнике. Для обеспечения полной устойчивости к действию желудочного сока необходимо покрытие, не пропускающее его при, по меньшей мере, значении pH, составляющем 5,0. Примеры более распространенных инертных ингредиентов, которые используются в качестве кишечнорастворимых покрытий, представляют собой ацетаттримеллитат целлюлозы (CAT), гидроксипропилметилцеллюлозу (HPMCP), HPMCP 50, HPMCP 55, поливинилацетата фталат (PVAP), Eudragit L30D™, Aquateric™, ацетатфталат целлюлозы (CAP), Eudragit L™, Eudragit S™ и Shellac™. Указанные покрытия могут быть использованы в качестве смешанных пленок.
3. Полимерные матрицы с контролируемой доставкой
Антитела и их антигенсвязывающие фрагменты, раскрываемые в данном документе, также могут быть введены в составах с контролируемым высвобождением. Антитела и их антигенсвязывающие фрагменты могут быть включены в инертную матрицу, которая обеспечивает высвобождение либо в результате механизмов диффузии, либо в результате механизмов вымывания, например, камеди. Медленно разлагающиеся матрицы также могут быть включены в состав. Другая форма контролируемого высвобождения основана на терапевтической системе Oros (Alza Corp.), т.е., антитело или его антигенсвязывающий фрагмент заключают в полупроницаемую мембрану, которая обеспечивает поступление воды и выталкивание лекарственного средства через одно небольшое отверстие в результате осмотических эффектов.
Полимерные изделия с контролируемым высвобождением могут быть изготовлены для длительного системного высвобождения после имплантации полимерного изделия (стержня, цилиндра, пленки, диска) или инъекции (микрочастицы). Матрица может быть представлена в форме микрочастиц, таких как микросферы, в которых агент диспергирован в твердой полимерной матрице, или микрокапсулы, в которых ядро состоит из материла, отличного от полимерной оболочки, и пептид диспергирован или суспендирован в ядре, которое может быть жидким или твердым по своей природе. Если в данном документе специально не определено, то микрочастицы, микросферы и микрокапсулы используются взаимозаменяемо. В качестве альтернативы полимер может быть отлит в виде тонкой пластины или пленки, варьирующих от нанометров до четырех сантиметров, порошка, полученного с помощью измельчения или с помощью других стандартных методика, или даже геля, такого как гидрогель.
Либо бионеразлагаемые, либо биоразлагаемые матрицы могут быть использованы для доставки слитых полипептидов или нуклеиновых кислот, кодирующих слитые полипептиды, хотя в некоторых вариантах осуществления биоразлагаемые матрицы являются предпочтительными. Они могут представлять собой природные или синтетические полимеры, однако синтетические полимеры являются предпочтительными в некоторых вариантах осуществления в связи с лучшей характеристикой профилей разложения и высвобождения. Полимер выбирают на основе периода времени, в течение которого требуется высвобождение. В некоторых случаях линейное высвобождение может быть наиболее пригодным, хотя в других случаях импульсное высвобождение или «масштабное высвобождение» могут обеспечить более эффективные результаты. Полимер может находиться в форме гидрогеля (в типичном случае при всасывании до около 90% от массы воды) и может необязательно быть перекрестно сшитым с помощью многовалентных ионов или полимеров.
Матрицы могут быть получены с помощью испарения растворителя, высушивания распылением, экстракции растворителя и других способов, известных специалистам в данной области техники. Биоразлагаемые микросферы могут быть приготовлены с помощью любых способов, разработанных для получения микросфер в целях лекарственной доставки, например, как описано Mathiowitz and Langer, J. Controlled Release, 5:13-22 (1987); Mathiowitz, et al., Reactive Polymers, 6:275-283 (1987); и Mathiowitz, et al., J. Appl. Polymer Sci., 35:755-774 (1988).
Могут быть разработаны устройства для локального высвобождения в целях воздействия на область имплантации или инъекции, которые в типичном случае будут доставлять дозу, которая представляет собой намного меньшую дозу, чем доза для лечения всего организма или системной доставки. Их можно имплантировать или вводить подкожно, в мышцу, жировую ткань или проглатывать.
III. Способы получения
A. Способы получения антител
Раскрываемые антитела могут быть получены в клеточной культуре, в фаге или в организмах различных животных, в том числе, но не ограничиваясь ими, коров, кроликов, коз, мышей, крыс, хомяков, морских свинок, овец, собак, кошек, обезьян, шимпанзе, человекообразных обезьян. В одном варианте осуществления различные животные могут представлять собой трансгенных животных, генетических разработанных с целью продуцирования человеческих или гуманизированных антител. Таким образом, в одном варианте осуществления антитело представляет собой антитело млекопитающих. Методики с применением фагов могут быть использованы для выделения исходного антитела или для образования вариантов с измененными характеристиками специфичности или авидности. Такие методики являются стандартными и хорошо известными в данной области техники. В одном варианте осуществления антитело образуется с помощью рекомбинантных средств, известных в данной области техники. Например, рекомбинантное антитело может быть получено с помощью трансфекции клетки-хозяина вектором, содержащим последовательность ДНК, кодирующую антитело. Один или более векторов могут быть использованы для трансфекции последовательности ДНК, экспрессирующей, по меньшей мере, одну VL- и одну VH-область в клетке-хозяине. Иллюстративные описания рекомбинантных средств для получения и продуцирования антител включают в себя Delves, Antibody Production: Essential Techniques (Wiley, 1997); Shephard, et al., Monoclonal Antibodies (Oxford University Press, 2000); Goding, Monoclonal Antibodies: Principles And Practice (Academic Press, 1993); Current Protocols In Immunology (John Wiley & Sons, most recent edition).
Раскрываемые антитела могут быть модифицированы с помощью рекомбинантных средств в целях повышения эффективности антитела при опосредовании необходимой функции. Таким образом, в объеме данного изобретения антитела могут быть модифицированы с помощью замен с использованием рекомбинантных средств. В типичном случае замены будут представлять собой консервативные замены. Например, по меньшей мере, одну аминокислоту в константной области антитела можно заменить другим остатком. См., например, патент США № 5624821, патент США № 6194551, заявку № 9958572; и Angal, et al., Mol. Immunol. 30:105-08 (1993). Модификация аминокислот включает в себя делеции, добавления и замены аминокислот. В некоторых случаях такие изменения выполняют с целью ослабления нежелательных активностей, например, комплементзависимой цитотоксичности. Часто антитела метят путем связывания, либо ковалентно, либо нековалентно, вещества, которое обеспечивает детектируемый сигнал. Большое разнообразие меток и методик конъюгирования известны и широко описаны как в научной, так и в патентной литературе. Указанные антитела могут быть подвергнуты скринингу в отношении связывания с белками, полипептидами. См., например, Antibody Engineering: A Practical Approach (Oxford University Press, 1996).
Например, соответствующие антитела с необходимыми видами биологической активности могут быть определены с помощью анализов in vitro, в том числе, но не ограничиваясь ими: пролиферации, миграции, адгезии, роста на мягком агаре, ангиогенеза, межклеточной связи, апоптоза, транспорта, передачи сигналов и анализов in vivo, таких как ингибирование опухолевого роста. Антитела, предложенные в данном документе, также могут быть пригодными в диагностических областях применения. В качестве захватывающих или ненейтрализующих антител они могут быть подвергнуты скринингу в отношении своей способности связываться с конкретных антигеном без ингибирования связывания с рецептором или биологической активности антигена. В качестве нейтрализующих антител антитела могут быть пригодны в анализах конкурентного связывания.
Антитела, которые могут быть использованы в раскрываемых композициях и способах, включают в себя целый иммуноглобулин (т.е., интактное антитело) любого класса, его фрагмент и синтетические белки, содержащие, по меньшей мере, антигенсвязывающий вариабельный домен антитела. Вариабельные домены в антителах отличаются последовательностью и используются при связывании и специфичности каждого конкретного антитела в отношении своего определенного антигена. Однако вариабельность обычно не распределена равномерно в вариабельных доменах антител. В типичном случае она сосредоточена в трех сегментах, называемых определяющих комплементарность областями (CDR) или гипервариабельными областями, как в вариабельных доменах легкой цепи, так и тяжелой цепи. Наиболее высококонсервативные области вариабельных доменов называются каркасом (FR). Каждый из вариабельных доменов нативных тяжелых и легких цепей содержит четыре FR-области, по большей части принимающих конфигурацию бета-листа, соединенных тремя CDR, которые образуют петли, объединяющие структуру бета-листа и в некоторых случаях образующие ее часть. CDR в каждой цепи удерживаются в непосредственной близости друг с другом с помощью FR-областей и совместно с CDR из другой цепи участвуют в образовании антигенсвязывающего сайта антител.
Также раскрыты фрагменты антител, которые имеют биологическую активность. Фрагменты, присоединенные или не присоединенные к другим последовательностям, содержат вставки, делеции, замены или другие определенные модификации определенных областей или определенных аминокислотных остатков, при условии, что активность фрагмента по сути не является измененной или нарушенной по сравнению с немодифицированным антителом или фрагментом антитела.
Методики также могут быть приспособлены для получения одноцепочечных антител на основе раскрываемых антител и их антигенсвязывающих фрагментов. Способы получения одноцепочечных антител хорошо известны специалистам в данной области техники. Одноцепочечное антитело может быть получено с помощью слияния друг с другом вариабельных доменов тяжелой и легкой цепей с использованием короткого пептидного линкера, при этом восстанавливается антигенсвязывающий сайт на одной молекуле. Вариабельные фрагменты одноцепочечных антител (scFv), в которых C-конец одного вариабельного домена связан с N-концом другого вариабельного домена с помощью пептида или линкера из 15-25 аминокислот были разработаны без существенного нарушения связывания с антигеном или специфичности связывания. Линкер выбирают таким образом, чтобы он обеспечивал связывание тяжелой цепи и легкой цепи друг с другом в их соответствующей конформационной ориентации.
В одном варианте осуществления предоставлены двухвалентные одноцепочечные вариабельные фрагменты (di-scFv), которые могут быть разработаны с помощью связывания двух scFv. Это может быть выполнено в результате получения одной пептидной цепи с двумя VH- и двумя VL-областями, образующими тандемные scFv. ScFv также могут быть сконструированы с помощью линкерных пептидов, которые являются слишком короткими, чтобы две вариабельные области складывались вместе (около пяти аминокислот), обеспечивая димеризацию scFv. Указанный тип известен как диатела. Было продемонстрировано, что диатела имеют константы диссоциации до 40 раз ниже, чем соответствующие scFv, означая, что они имеют намного более высокую аффиность по отношению к своей мишени. Еще более короткие линкеры (одна или две аминокислоты) приводят к образованию тримеров (триател или триотел). Также были получены тетратела. Они проявляют даже более высокую аффинность в отношении мишеней по сравнению с диателами.
В другом варианте осуществления предоставлено моноклональное антитело, полученное из по сути гомогенной популяции антител, т.е., отдельные антитела в популяции являются идентичными, за исключением возможных встречающихся в природе мутаций, которые могут присутствовать в небольшой подгруппе молекул антител. Моноклональные антитела включают в себя «химерные» антитела, в которых часть тяжелой и/или легкой цепи идентична или гомологична соответствующим последовательностям в антителах, происходящих от определенного вида или принадлежащих к определенному классу или подклассу антител, тогда как остальная часть цепи (цепей) идентична или гомологична соответствующим последовательностям в антителах, происходящих из другого вида или принадлежащих к другому классу или подклассу антител, а также фрагментам таких антител, до тех пор, пока они проявляют необходимую антагонистическую активность.
Моноклональные антитела могут быть получены с помощью любой процедуры, которая приводит к образованию моноклональных антител. При гибридомном способе мышь или другое подходящее животное-хозяина в типичном случае иммунизируют иммунизирующим агентом для активации лимфоцитов, которые продуцируют или способны продуцировать антитела, которые будут специфично связываться с иммунизирующим агентом. В качестве альтернативы лимфоциты могут быть иммунизированы in vitro.
Раскрываемые антитела также могут быть получены с помощью способов рекомбинантной ДНК. ДНК, кодирующую раскрываемые антитела, может быть легко выделена и/или сиквенирована с использованием стандартных процедур (например, путем использования олигонуклеотидных зондов, которые способны к специфичному связыванию с генами, кодирующими тяжелую и легкую цепи мышиных антител). Библиотеки антител или активных фрагментов антител также могут быть получены и подвергнуты скринингу с помощью методик фагового дисплея.
Способы получения антител с помощью химии белков также известны в данной области техники. Одним способов получения белков, представляющих собой антитела, является связывание двух или более пептидов или полипептидов друг с другом с помощью методик химии белков. Например, пептиды или полипептиды могут быть химически синтезированы с помощью доступного в настоящее время лабораторного оборудования с применением либо химии Fmoc (9-флуоренилметилоксикарбонила), либо химии Boc (трет-бутилкарбоноила). (Applied Biosystems, Inc., Фостер-Сити, Калифорния). Специалист в данной области техники может легко понять, что пептид или полипептид, соответствующий антителу, например, могут быть синтезированы с помощью стандартных химических реакций. Например, пептид или полипептид могут быть синтезированы и не отделены от своей синтетической смолы, в то время как другой фрагмент антитела может быть синтезирован и затем отделен от смолы, при этом воздействию подвергается терминальная группа, которая функционально заблокирована на другом фрагменте. В результате реакций конденсации пептидов указанные два фрагмента могут быть ковалентно связаны с помощью пептидной связи на своих карбоксильных и аминоконцах соответственно, с образованием антитела или его фрагмента. В качестве альтернативы пептид или полипептид независимо синтезируют in vivo, как описано выше. После выделения указанные независимые пептиды или полипептиды могут быть связаны с образованием антитела или его антигенсвязывающего фрагмента с использованием аналогичных реакций конденсации пептидов.
Например, ферментативное лигирование клонируемых или синтетических пептидных сегментов способствует связыванию сравнительно коротких пептидных фрагментов с образованием более крупных пептидных фрагментов, полипептидов или целых белковых доменов. В качестве альтернативы нативное химическое лигирование синтетических пептидов может быть использовано с целью синтетического конструирования крупных пептидов или полипептидов из более коротких пептидных фрагментов. Указанный способ состоит из двухстадийной химической реакции. Первая стадия представляет собой хемоселективную реакцию незащищенного синтетического пептида и альфа-тиоэфира с другим незащищенным пептидным сегментом, содержащим аминотерминальный остаток Cys с образованием промежуточного продукта, связанного тиоэфирной связью, в качестве исходного ковалентного продукта. Без изменения условий реакции указанный промежуточный продукт подвергается спонтанной быстрой внутримолекулярной реакции с образованием нативной пептидной связи в сайте лигирования.
B. Способы получения выделенных молекул нуклеиновой кислоты
В одном варианте осуществления предоставлены нуклеиновые кислоты, кодирующие раскрываемые антитела или их антигенсвязывающие фрагменты. Нуклеиновые кислоты могут кодировать все антитело или его антигенсвязывающие фрагменты или легкую цепь, тяжелую цепь, их комбинации или их CDR.
Выделенные молекулы нуклеиновой кислоты могут быть получены с помощью стандартных методик, в том числе, но не ограничиваясь ими, методик обычного молекулярного клонирования и химического синтеза нуклеиновых кислот. Например, методики полимеразной цепной реакции (ПЦР) могут быть использованы для получения выделенной нуклеиновой кислоты, кодирующей полипептид варианта. ПЦР представляет собой методику, в которой целевые нуклеиновые кислоты ферментативно амплифицируют. В типичном случае информация о последовательности, начиная с концов участка, представляющего интерес, или за его пределами, может быть использована для разработки олигонуклеотидных праймеров, которые являются идентичными по последовательности противоположным нитям матрицы, подлежащей амплификации. ПЦР может быть использована для амплификации определенных последовательностей из ДНК, а также РНК, в том числе последовательностей из суммарной геномной ДНК или суммарной клеточной РНК. Праймеры в типичном случае представляют собой от 14 до 40 нуклеотидов в длину, однако могут варьировать от 10 нуклеотидов до сотен нуклеотидов в длину. Общие методики ПЦР описаны, например, в PCR Primer: A Laboratory Manual, ed. by Dieffenbach and Dveksler, Cold Spring Harbor Laboratory Press, 1995. При использовании РНК в качестве источника матрицы обратная транскриптаза может быть использована для синтеза комплементарной нити ДНК (кДНК). Для получения выделенных нуклеиновых кислот также могут быть использованы лигазная цепная реакция, амплификация с замещением цепей, самоподдерживающя репликация последовательностей или амплификация, основанная на последовательности нуклеиновых кислот. См., например, Lewis (1992) Genetic Engineering News 12:1; Guatelli et al. (1990) Proc. Natl. Acad. Sci. USA 87:1874-1878; и Weiss (1991) Science 254:1292-1293.
Выделенные нуклеиновые кислоты могут быть синтезированы химически, либо в виде одной молекулы нуклеиновой кислоты, либо в виде серии олигонуклеотидов (например, с помощью технологии с использованием амидофосфидов для автоматического синтеза ДНК в направлении от 3’ до 5’). Например, одна или более пар длинных олигонуклеотидов (например, >100 нуклеотидов) могут быть синтезированы с тем, чтобы содержать необходимую последовательность, при этом каждая пара содержит короткий сегмент комплементарности (например, около 15 нуклеотидов) таким образом, что образуется дуплекс, когда олигонуклеотидная пара отжигается. ДНК-полимераза может быть использована для удлинения олигонуклеотидов, приводя к образованию одной двухнитевой молекулы нуклеиновой кислоты на олигонуклеотидную пару, которая затем может быть лигирована в вектор. Выделенные нуклеиновые кислоты также могут быть получены с помощью мутагенеза. Нуклеиновые кислоты, кодирующие белки, могут быть подвергнуты мутированию с помощью стандартных методик, в том числе олигонуклеотид-направленного мутагенеза и/или сайт-направленного мутагенеза с использованием ПЦР. См. Short Protocols in Molecular Biology. Chapter 8, Green Publishing Associates and John Wiley & Sons, edited by Ausubel et al, 1992.
IV. Способы применения
Раскрываемые антитела и их антигенсвязывающие фрагменты могут быть использованы для модулирования иммунного ответа у субъекта, нуждающегося в этом. В одном варианте осуществления предоставлен способ активации иммунных клеток, экспрессирующих PD-1, например, T-клеток, для пролиферации или усиления биологической активности иммунных клеток, экспрессирующих PD-1, в результате введения раскрываемых антител и их антигенсвязывающих фрагментов, необязательно содержащих второй терапевтический агент.
A. Стимуляция иммунных ответов
1. Терапевтические стратегии
Предложены способы индукции или усиления иммунного ответа у субъекта. В типичном случае способы включают введение субъекту эффективного количества одного или нескольких из раскрываемых антител и их антигенсвязывающих фрагментов с целью иммуноспецифичного связывания с PD-1 и индукции, стимуляции или усиления стимулирующего или активирующего сигнала с участием PD-1 с целью активации иммунной клетки. Иммунный ответ может представлять собой, например, индукцию, стимуляцию или усиление Т-клеточной активации, секреции цитокинов иммунными клетками, T-клеточной пролиферации. Раскрываемые антитела или их антигенсвязывающие фрагменты могут быть введены субъекту, нуждающемуся в этом, в эффективном количестве с целью преодоления T-клеточного истощения и/или T-клеточной анергии. Преодоление T-клеточного истощения или T-клеточной анергии могут быть определены путем измерения Т-клеточной функции с помощью известных методик.
Способы могут быть использованы in vivo или ex vivo для индукции, стимуляции или усиления иммунного ответа.
В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент, или нуклеиновую кислоту, кодирующую антитело или его антигенсвязывающий фрагмент, вводят непосредственно субъекту. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент приводят в контакт с клетками (например, иммунными клетками) ex vivo, и обработанные клетки вводят субъекту (например, адаптивный перенос). Антитело или его антигенсвязывающий фрагмент могут способствовать тому, чтобы был возможен более устойчивый иммунный ответ. Раскрываемые композиции являются пригодными для стимуляции или усиления иммунных ответов, включающих T-клетки, вызывающих активирующий сигнал с участием PD-1 на иммунных клетках.
2. Субъекты, подлежащие лечению
a. Лечение рака
Раскрываемые антитела и их композиции и способы могут быть использованы для лечения рака. Как правило, агенты используются для стимуляции или усиления иммунного ответа в отношении рака у субъекта с помощью введения субъекту количества раскрываемого антитела или его антигенсвязывающего фрагмента, которые индуцируют, стимулируют или усиливают активирующий сигнал с участием PD-1. Способ может ослаблять один или более симптомов рака.
Иммунные клетки, активируемые раскрываемыми антителами или их фрагментами, могут уничтожать раковые клетки и снижать опухолевую нагрузку у субъекта. Термин «раковая клетка» предусматривает включение в себя предзлокачественных и злокачественных раковых клеток. В некоторых вариантах осуществления рак относится к доброкачественной опухоли, которая сохранилась локализованной. В других вариантах осуществления рак относится к злокачественной опухоли, которая инвазировала и разрушила соседние структуры организма и распространилась в отдаленные участки. В еще одних вариантах осуществления рак ассоциирован со специфическим раковым антигеном (например, антигеном, свойственным для всех видов карциномы (KS 1/4), антигеном карциномы яичника (CA125), простатспецифическим антигеном (PSA), раково-эмбриональным антигеном (CEA), CD19, CD20, HER2/neu и др.).
Способы и композиции антител, раскрываемые в данном документе, пригодны при лечении или предупреждении ряда различных видов рака и других патологических пролиферативных заболеваний, в том числе (но не ограничиваясь ими) следующих: карциномы, в том числе карциномы мочевого пузыря, молочной железы, кишечника, почки, печени, легкого, яичника, поджелудочной железы, желудка, шейки матки, щитовидной железы и кожи; в том числе плоскоклеточной карциномы; гематопоэтических опухолей лимфоидной клеточной линии, в том числе лейкоза, острого лимфоцитарного лейкоза, острого лимфобластного лейкоза, B-клеточной лимфомы, T-клеточной лимфомы, лимфомы Беркитта; гематопоэтических опухолей миелоидной клеточной линии, в том числе острых и хронических миелогенных лейкозов и промиелоцитарного лейкоза; опухолей мезенхимального происхождения, в том числе фибросаркомы и рабдомиосаркомы; другие опухоли, в том числе меланомы, семиномы, тератокарциномы, нейробластомы и глиомы; опухолей центральной и периферической нервной системы, в том числе астроцитомы, нейробластомы, глиомы и шванномы; опухолей мезенхимального происхождения, в том числе фибросаркомы, рабдомиосаркомы и остеосаркомы; и других опухолей, в том числе меланомы, пигментной ксеродермы, кератоакантому, семиномы, фолликулярного рака щитовидной железы и тератокарциномы.
Виды рака, вызванные нарушениями апоптоза, также могут подлежать лечению с помощью раскрываемых способов и композиций. Такие виды рака могут включать в себя, но не ограничиваясь ими, фолликулярные лимфомы, карциномы с мутациями p53, гормонзависимые опухоли молочной железы, предстательной железы и яичника, и предраковые поражения, такие как семейный аденоматозный полипоз и миелодиспластические синдромы. В конкретных вариантах осуществления злокачественную опухоль или диспролиферативные изменения (такие как метаплазии и дисплазии) или гиперпролиферативные нарушения лечат или предупреждают с помощью этих способов и композиций в яичнике, мочевом пузыре, молочной железе, кишечнике, легком, коже, поджелудочной железе или матке. В других конкретных вариантах осуществления саркому, меланому или лейкоз лечат или предупреждают с помощью раскрываемых способов и композиций.
Конкретные виды рака и соответствующие нарушения, которые можно лечить или предупреждать с помощью способов и композиций, раскрываемых в данном документе, включают в себя, но не ограничиваясь ими, лейкозы, в том числе, но не ограничиваясь ими, острый лейкоз, острый лимфоцитарный лейкоз, острые миелоцитарные лейкозы, такие как миелобластические, промиелоцитарные, миеломоноцитарные, моноцитарные лейкозы, эритролейкозы и миелодиспластический синдром, хронические лейкозы, такие как, но не ограничиваясь ими, хронический миелоцитарный (гранулоцитарный) лейкоз, хронический лимфоцитарный лейкоз, лейкоз волосковых клеток; истинная полицитемия; лимфомы, такие как, но не ограничиваясь ими, ходжкинская лимфома или неходжкинская лимфома; лимфомы (например, диффузную B-крупноклеточную лимфому (DLBCL), негативную в отношении киназы анапластической лимфомы (ALK); диффузную B-крупноклеточную лимфому (DLBCL), позитивную в отношении киназы анапластической лимфомы (ALK); ALK+ анапластическую крупноклеточную лимфому(ALCL), позитивную в отношении киназы анапластической лимфомы (ALK), острую миелоидную лимфому (AML)); множественные миеломы, такие как, но не ограничиваясь ими, тлеющая множественная миелома, несекреторная миелома, остеосклеротическая миелома, лейкоз плазматических клеток, солитарная плазмоцитома и экстрамедуллярная плазмоцитома; макроглобулинемия Вальденстрема; моноклональная гаммапатия неустановленной этиологии; доброкачественная моноклональная гаммапатия; болезнь тяжелых цепей; саркомы костей и соединительной ткани, такие как, но не ограничиваясь ими, саркома кости, остеосаркома, хондросаркома, саркома Юинга, гигантоклеточная саркома, фибросаркома кости, хордома, периостальная саркома, саркомы мягких тканей, ангиосаркома (гемангиосаркома), фибросаркома, саркома Капоши, лейомиосаркома, липосаркома, лимфангиосаркома, неврилеммома, рабдомиосаркома, синовиальная саркома; опухоли мозга, в том числе, но не ограничиваясь ими, глиому, астроцитому, глиому ствола мозга, эпендимому, олигодендроглиому, неглиальную опухоль, неврилеммому слухового нерва, краниофарингиому, медуллобластому, менингиому, пинеоцитому, пинеобластому, первичную лимфому мозга; рак молочной железы, в том числе, но не ограничиваясь ими, аденокарциному, лобулярную (мелкоклеточная) карциному, внутрипротоковую карциному, медуллярный рак молочной железы, слизеобразующий рак молочной железы, тубулярный рак молочной железы, папиллярный рак молочной железы, болезнь Пэджета и отечно-инфильтративный рак молочной железы; рак надпочечников, в том числе, но не ограничиваясь ими, феохромоцитомную и адренокортикальную карциному; рак щитовидной железы, такой как, но не ограничиваясь ими, папиллярный или фолликулярный рак щитовидной железы, медуллярный рак щитовидной железы и анапластический рак щитовидной железы; рак поджелудочной железы, в том числе, но не ограничиваясь ими, инсулиному, гастриному, глюкагоному, випому, соматостатиному и карциноидную опухоль и опухоль островковых клеток; злокачественные опухоли гипофиза, в том числе, но не ограничиваясь ими, болезнь Кушинга, пролактиному, акромегалию и несахарный диабет; злокачественные опухоли глаз, в том числе, но не ограничиваясь ими, меланому глаза, такую как меланома радужной оболочки, хороидальная меланома и меланома цилиарного тела и ретинобластома; злокачественные опухоли влагалища, в том числе, но не ограничиваясь ими, плоскоклеточную карциному, аденокарциному и меланому; рак вульвы, в том числе, но не ограничиваясь ими, плоскоклеточную карциному, меланому, аденокарциному, карциному базальных клеток, саркому и болезнь Пэджета; злокачественные опухоли шейки матки, в том числе, но не ограничиваясь ими, плоскоклеточную карциному и аденокарциному; злокачественные опухоли матки, в том числе, но не ограничиваясь ими, карциному эндометрия и саркому матки; злокачественные опухоли яичника, в том числе, но не ограничиваясь ими, эпителиальную карциному яичника, пограничную опухоль, эмбрионально-клеточную опухоль и стромальную опухоль; злокачественные опухоли пищевода, в том числе, но не ограничиваясь ими, плоскоклеточный рак, аденокарциному, аденоидно-кистозную карциному, мукоэпидермоидную карциному, аденосквамозную карциному, саркому, меланому, плазмоцитому, бородавчатую карциному и овсяно-клеточную (мелкоклеточную) карциному; злокачественные опухоли желудка, в том числе, но не ограничиваясь ими, аденокарциному, грибовидно разрастающуюся (полипоид), изъязвленную, поверхностно распространяющуюся, диффузно распространяющуюся, злокачественную лимфому, липосаркому, фибросаркому и карциносаркому; злокачественные опухоли кишечника; злокачественные опухоли прямой кишки; злокачественные опухоли печени, в том числе, но не ограничиваясь ими, гепатоцеллюлярную карциному и гепатобластому, злокачественные опухоли желчного пузыря, в том числе, но не ограничиваясь ей, аденокарциному; холангиокарциномы, в том числе, но не ограничиваясь ими, папиллярные, узловые и диффузные; злокачественные опухоли легких, в том числе, но не ограничиваясь ими, немелкоклеточный рак легких, плоскоклеточную карциному (эпидермоидную карциному), аденокарциному, крупноклеточную карциному и мелкоклеточный рак легких; злокачественные опухоли яичек, в том числе, но не ограничиваясь ими, герминому, семиному, анапластическую, классическую (типичную), сперматоцитарную, несеминому, эмбриональную карциному, тератому, карциному, хориокарциному (опухоль желточного мешка), злокачественные опухоли предстательной железы, в том числе, но не ограничиваясь ими, аденокарциному, лейомиосаркому и рабдомиосаркому; злокачественные опухоли пениса; злокачественные опухли ротовой полости, в том числе, но не ограничиваясь ими, плоскоклеточную карциному; базальноклеточные злокачественные опухоли; злокачественные опухоли слюнных желез, в том числе, но не ограничиваясь ими, аденокарциному, мукоэпидермоидную карциному и аденоидо-кистозную карциному; злокачественные опухоли глотки, в том числе, но не ограничиваясь ими, плоскоклеточный рак и бородавчатый рак; злокачественные опухоли кожи, в том числе, но не ограничиваясь ими, базальноклеточную карциному, плоскоклеточную карциному и меланому, поверхностно распространяющуюся меланому, узелковую меланому, злокачественную меланому лентиго, акральную лентигинозную меланому; злокачественные опухоли почек, в том числе, но не ограничиваясь ими, почечно-клеточный рак, аденокарциному, гипернефрому, фибросаркому, рак переходных клеток (почечной лоханки и/или мочеточника); опухоль Вильмса; злокачественные опухоли мочевого пузыря, в том числе, но не ограничиваясь ими, карциному переходных клеток, плоскоклеточный рак, аденокарциному, карциносаркому. Кроме того, виды рака включают в себя миксосаркому, остеогенную саркому, эндотелиосаркому, лимфангиотелиосаркому, мезотелиому, синовиому, гемангиобластому, эпителиальную карциному, цистаденосаркому, бронхогенную карциному, карциному потовых желез, карциному сальных желез, папиллярную карциному и папиллярные аденокарциномы (обзор таких нарушений см. в Fishman et al., 1985, Medicine, 2d Ed., J.B. Lippincott Co., Philadelphia and Murphy et al., 1997, Informed Decisions: The Complete Book of Cancer Diagnosis, Treatment, and Recovery, Viking Penguin, Penguin Books U.S.A., Inc., United States of America).
b. Лечение инфекций
Раскрываемые композиции антител и способы могут быть использованы для лечения инфекций и инфекционных заболеваний. Как правило, агенты используются для стимуляции или усиления иммунного ответа в отношении инфекции у субъекта с помощью введения субъекту количества одного или более из раскрываемых антител или их антигенсвязывающих фрагментов, которые передают активирующий или стимулирующий сигнал с участием PD-1. Способ может ослаблять один или более симптомов инфекции.
Инфекция или заболевание может быть вызвано бактерией, вирусом, простейшим, гельминтом или другим микробным патогеном, который проникает внутриклеточно и подвергается атаке, например, со стороны цитотоксических T-лимфоцитов.
Инфекция или заболевание может быть острым или хроническим. Острая инфекция в типичном случае представляет собой инфекцию малой длительности. Во время острой микробной инфекции иммунные клетки начинают экспрессировать иммуномодулирующие рецепторы. Соответственно, в некоторых вариантах осуществления способ включает повышение иммунного стимулирующего ответа против острой инфекции.
Инфекция может быть вызвана, например, но не ограничиваясь ими, Candida albicans, Listeria monocytogenes, Streptococcus pyogenes, Streptococcus pneumoniae, Neisseria meningitidis, Staphylococcus aureus, Escherichia coli, Acinetobacter baumannii, Pseudomonas aeruginosa или Mycobacterium.
В некоторых вариантах осуществления раскрываемые композиции антител используют для лечения хронических инфекций, например, инфекций, в которых происходило T-клеточное истощение или T-клеточная анергия, приводя к тому, что инфекция сохраняется у хозяина в течение длительного периода времени.
Иллюстративные инфекции, подлежащие лечению, представляют собой хронические инфекции, вызванные вирусом гепатита, вирусом иммунодефицита человека (ВИЧ), T-лимфотропным вирусом человека (HTLV), вирусом герпеса, вирусом Эпштейна-Барр или вирусом папилломы человека.
Поскольку вирусные инфекции удаляются преимущественно T-клетками, то повышение T-клеточной активности было бы терапевтически полезным в ситуациях, когда более быстрое или тщательное удаление инфекционного вирусного агента было бы предпочтительным для субъекта-животного или субъекта-человека. Таким образом, раскрываемые композиции можно вводить для лечения местных или системных вирусных инфекций, в том числе, но не ограничиваясь ими, иммунодефицита (например, ВИЧ), папилломы (например, ВПЧ), герпеса (например, ВПГ), энцефалита, гриппа (например, вируса гриппа A человека) и простуды (например, риновируса человека) и других вирусных инфекций, вызванных, например, HTLV, вирусом гепатита, респираторным синцитальным вирусом, вирусом осповакцины и вирусом бешенства. Молекулы могут быть введены местно для лечения вирусных кожных заболеваний, таких как герпетические поражения или опоясывающий герпес или генитальные бородавки. Молекулы также могут быть введены системно для лечения системных вирусных заболеваний, в том числе, но не ограничиваясь ими, СПИДа, гриппа, простуды или энцефалита.
Иллюстративные инфекции, которые могут подлежать лечению, включают, но не ограничиваясь ими, инфекции, вызванные микроорганизмами, в том числе, но не ограничиваясь ими, Actinomyces, Anabaena, Bacillus, Bacteroides, Bdellovibrio, Bordetella, Borrelia, Campylobacter, Caulobacter, Chlamydia, Chlorobium, Chromatium, Clostridium, Corynebacterium, Cytophaga, Deinococcus, Escherichia, Francisella, Halobacterium, Heliobacter, Haemophilus, Hemophilus influenza тип B (HIB), Hyphomicrobium, Legionella, Leptspirosis, Listeria, Meningococcus A, B и C, Methanobacterium, Micrococcus, Myobacterium, Mycoplasma, Myxococcus, Neisseria, Nitrobacter, Oscillatoria, Prochloron, Proteus, Pseudomonas, Phodospirillum, Rickettsia, Salmonella, Shigella, Spirillum, Spirochaeta, Staphylococcus, Streptococcus, Streptomyces, Sulfolobus, Thermoplasma, Thiobacillus, and Treponema, Vibrio, Yersinia, Cryptococcus neoformans, Histoplasma capsulatum, Candida albicans, Candida tropicalis, Nocardia asteroides, Rickettsia ricketsii, Rickettsia typhi, Mycoplasma pneumoniae, Chlamydial psittaci, Chlamydial trachomatis, Plasmodium falciparum, Trypanosoma brucei, Entamoeba histolytica, Toxoplasma gondii, Trichomonas vaginalis и Schistosoma mansoni.
Другие микроорганизмы, которые могут подлежать лечению с помощью раскрываемых композиций и способов, включают в себя бактерии, такие как таковые Klebsiella, Serratia, Pasteurella; патогены, ассоциированные с холерой, столбняком, ботулизмом, сибирской язвой, чумой и болезнью Лайма; или грибковые или паразитические патогены, такие как Candida (albicans, krusei, glabrata, tropicalis и др.), Cryptococcus, Aspergillus (fumigatus, niger и др.), Genus Mucorales (mucor, absidia, rhizophus), Sporothrix (schenkii), Blastomyces (dermatitidis), Paracoccidioides (brasiliensis), Coccidioides (immitis) и Histoplasma (capsulatuma), Entamoeba, histolytica, Balantidium coli, Naegleria fowleri, Acanthamoeba sp., Giardia lambia, Cryptosporidium sp., Pneumocystis carinii, Plasmodium vivax, Babesia microti, Trypanosoma brucei, Trypanosoma cruzi, Toxoplasma gondi и др.), Sporothrix, Blastomyces, Paracoccidioides, Coccidioides, Histoplasma, Entamoeba, Histolytica, Balantidium, Naegleria, Acanthamoeba, Giardia, Cryptosporidium, Pneumocystis, Plasmodium, Babesia или Trypanosoma и др.
V. Комбинированные виды терапии для повышения иммунных ответов
Раскрываемые антитела и их антигенсвязывающие фрагменты и их композиции могут быть введены субъекту, нуждающемуся в этом, в отдельности или в комбинации с одним или несколькими дополнительными терапевтическими агентами. В некоторых вариантах осуществления антитела и их антигенсвязывающие фрагменты и дополнительный терапевтический агент вводят отдельно, но одновременно. Антитела и их антигенсвязывающие фрагменты и дополнительный терапевтический агент также могут быть введены в виде части одной и той же композиции. В некоторых вариантах осуществления антитела и их антигенсвязывающие фрагменты и второй терапевтический агент вводят раздельно и в различное время, однако в виде части одной и той же схемы лечения. Дополнительные терапевтические агенты могут быть введены до, после или поочередно с введением раскрываемых антител и их антигенсвязывающих фрамгентов.
Субъекту может быть введен первый терапевтический агент за 1, 2, 3, 4, 5, 6 или более часов или за 1, 2, 3, 4, 5, 6, 7 или более суток до введения второго терапевтического агента. В некоторых вариантах осуществления субъекту могут быть введены одна или более доз первого агента каждые 1, 2, 3, 4, 5, 6 7, 14, 21, 28, 35 или 48 суток до первого введения второго агента. Антитела и их антигенсвязывающие фрагменты могут представлять собой первый или второй терапевтический агент.
Антитела и их антигенсвязывающие фрагменты и дополнительный терапевтический агент также могут быть введены в виде части лечебного режима. Например, если первый терапевтический агент моет быть введен субъекту на каждый четвертый день, то второй терапевтический агент может быть введен на первый, второй, третий или четвертый день или их комбинации. Первый терапевтический агент или второй терапевтический агент могут быть введены повторно в течение всей схемы лечения.
Иллюстративные дополнительные терапевтические агенты включают в себя, но не ограничиваясь ими, цитокины, химиотерапевтические агенты, радионуклиды, другие иммунотерапевтические препараты, ферменты, антибиотики, противовирусные препараты (особенно ингибиторы протеаз в отдельности или в комбинации с нуклеозидами для лечения ВИЧ или гепатита B или C), противопаразитарные препараты (для лечения гельминтов, простейших), факторы роста, ингибиторы роста, гормоны, антагонисты гормонов, антитела и их биоактивные фрагменты (в том числе гуманизированные, одноцепочечные и химерные антитела), препараты на основе антигенов и вакцин (в том числе адъюванты), пептидные лекарственные препараты, противовоспалительные препараты, лиганды, которые связываются с Toll-подобными рецепторами (в том числе, но не ограничиваясь ими, олигонуклеотиды CpG) в целях активации врожденной иммунной системы, молекулы, которые мобилизуют и адаптируют иммунную систему, другие молекулы, которые активируют или усиливают действие цитотоксических T-лимфоцитов, естественных клеток-киллеров и T-хелперов, а также других молекул, которые дезактивируют или оказывают отрицательную регуляцию на супрессорные или регуляторные T-клетки.
Дополнительные терапевтические агенты выбирают на основе патологического состояния, нарушения или заболевания, подлежащих лечению. Например, иммуномодулирующий агент может быть введен совместно с одним или несколькими дополнительными агентами, которые функционируют таким образом, чтобы усиливать или активировать иммунный ответ или ослаблять или ингибировать иммунный ответ.
A. Противомикробные препараты
В одном варианте осуществления антитела и их антигенсвязывающие фрамгенты могут быть ввеедны субъекту в комбинации с противомикробным препаратом, таким как антибиотик, противогрибковый препарат, противовирусный препарат, противопаразитарный препарат или эфирное масло. В другом варианте осуществления раскрываемые антитела и их антигенсвязыающие фрагменты могут быть использованы с превентивной или профилактической ролью при лечении и предупреждении заболевания, а также в контексте тяжелых травматических повреждений, таких как большой ожог, открытый перелом, ампутация в результате несчастного случая или другие ранения.
В некоторых вариантах осуществления субъекту вводят антитела и их антигенсвязывающие фрагменты и/или противомикробный препарат во время приема в больницу в целях предупреждения последующих бактериальных, грибковых или вирусных осложнений. Антибиотик может целенаправленно воздействовать на патогены, а антитела и их антигенсвязывающие фрагменты могут стимулировать иммунную систему обеспечивать усиленный ответ с целью лечения или предупреждения последующей инфекции или заболевания.
1. Химиотерапевтические агенты
Антитела и их антигенсвязывающие фрагменты можно комбинировать с одним или несколькими химиотерапевтическими агентами и проапоптическими агентами. Иллюстративные химиотерапевтические агенты включают в себя, но не ограничиваясь ими, амсакрин, блеомицин, бусульфан, капецитабин, карбоплатин, кармустин, хлорамбуцил, цисплатин, кладрибин, клофарабин, кризантаспазу, циклофосфамид, цитарабин, дакарбазин, дактиномицин, даунорубицин, доцетаксел, доксорубицин, эпирубицин, этопозид, флударабин, фторурацил, гемцитабин, гидроксикарбамид, идарубицин, ифосфамид, иринотекан, лейковорин, липосомальный доксорубицин, липосомальный даунорубицин, ломустин, мелфалан, меркаптопурин, месну, метотрексат, митомицин, митоксантрон, оксалиплатин, паклитаксел, пеметрексед, пентостатин, прокарбазин, ралтитрексид, сатраплатин, стрептозоцин, тегафур-урацил, темозоломид, тенипозид, тиотепу, тиогуанин, топотекан, треосульфан, винбластин, винкристин, виндезин, винорелбин или их комбинацию. Иллюстративные проапотические агенты включают в себя, но не ограничиваясь ими, флударабин, стауроспорин, циклогексимид, актиномицин D, лактозилкерамид, 15d-PGJ(2) и их комбинации.
2. Другие иммуномодуляторы
a. Антагонисты PD-1
В некоторых вариантах осуществления антитела и их антигенсвязывающие фрагменты вводят совместно с антагонистом PD-1. Белок программируемой клеточной смерти-1 (PD-1) представляет собой члена семейства рецепторов CD28, который доставляет отрицательный иммунный ответ при индуцировании на T-клетках. Контакт между PD-1 и одним из его лигандом (B7-H1 или B7-DC) индуцирует ингибирующий ответ, который снижает T-клеточную мультипликацию и/или силу и/или длительность T-клеточного ответа. Соответствующие антагонисты PD-1 описаны в патентах США №№ 8114845, 8609089 и 8709416, которые особым образом включены в данный документ посредством ссылки в полном объеме, и включают в себя соединения или агенты, которые как связываются с лигандом PD-1, так и блокируют его в целях нарушения или ингибирования связывания лиганда с рецептором PD-1, или связываются непосредственно с рецептором PD-1 и блокируют его, не индуцируя передачу ингибирующего сигнала через рецептор PD-1.
В некоторых вариантах осуществления антагонист рецептора PD-1 связывается непосредственно с рецептором PD-1, не вызывая передачу ингибирующего сигнала, и также связывается с лигандом рецептора PD-1 в целях ослабления или ингибирования передачи сигнала с помощью лиганда через рецептор PD-1. Благодаря снижению числа и/или содержания лигандов, которые связываются с рецептором PD-1 и вызывают передачу ингибирующего сигнала, меньше клеток ослабляется в результате отрицательного сигнала, доставляемого с помощью передачи сигнала с участием PD-1, и может быть достигнут более устойчивый иммунный ответ.
Считается, что передача сигнала с участием PD-1 регулируется с помощью связывания с лигандом PD-1 (таким как B7-H1 или B7-DC) в непосредственной близости к пептидному антигену, презентируемому главным комплексом гистосовместимости (MHC) (см., например, Freeman, Proc. Natl. Acad. Sci. U. S. A, 105:10275-10276 (2008)). Таким образом, белки, антитела или малые молекулы, которые предупреждают колигирование PD-1 и TCR на T-клеточной мембране также являются пригодными антагонистами PD-1.
В некоторых вариантах осуществления антагонисты рецептора PD-1 представляют собой низкомолекулярные антагонисты или антитела, которые ослабляют или нарушают передачу сигнала с участием рецептора PD-1 в результате связывания с лигандами PD-1 или с самим PD-1, особенно в случаях, если колигирование PD-1 с TCR не следует за таким связыванием, тем самым, не вызывая передачу ингибирующего сигнала через рецептор PD-1. Другие антагонисты PD-1, предусмотренные способами данного изобретения, включают в себя антитела, которые связываются с PD-1 или лигандами PD-1 и другими антителами.
Подходящие анти-PD-1 антитела включают в себя, но не ограничиваясь ими, таковые, описанные в следующих патентах США: 7332582, 7488802, 7521051, 7524498, 7563869, 7981416, 8088905, 8287856, 8580247, 8728474, 8779105, 9067999, 9073994, 9084776, 9205148, 9358289, 9387247, 9492539, 9492540, все из которых включены посредством ссылки в полном объеме.
См. также Berger et al., Clin. Cancer Res., 14:30443051 (2008).
Иллюстративные анти-PD-L1 антитела включают в себя, но не ограничиваясь ими, таковые, описанные в следующих патентах США №№: 8383796, 9102725, 9273135, 9393301 и 9580507, все из которых особым образом включены в данный документ посредством ссылки в полном объеме.
В отношении анти-B7-DC (также называемых анти-PD-L2) антитела см. патенты США №№: 7411051, 7052694, 7390888, 8188238 и 9255147.
Другие иллюстративные антагонисты рецептора PD-1 включают в себя, но не ограничиваясь ими, полипептиды PD-L2, в том числе гомологи и варианты таковых, а также активные фрагменты любого из вышеуказанных и слитые белки, которые включают любой из них. В некоторых вариантах осуществления слитые белки включают в себя растворенный участок B7-DC, связанный с Fc-областью антитела, такого как IgG человека, и не включает все или часть из трансмембранного участка B7-DC человека.
Антагонист PD-1 также может представлять собой фрагмент PD-L1 млекопитающего, например, от мыши или примата, такого как человека, при этом фрагмент связывается с PD-1 и блокирует его, но не приводит к передаче ингибирующего сигнала через PD-1. Фрагменты также могут представлять собой часть слитого белка, например, слитого белка Ig.
Другие пригодные полипептиды-антагонисты PD-1 включают в себя таковые, которые связываются с лигандами рецептора PD-1. Они включают в себя рецепторный белок PD-1 или их растворенные фрагменты, которые связываются с лигандами PD-1, такими как PD-L1 или B7-DC, и предупреждают связывание с эндогенным рецептором PD-1, тем самым предупреждая передачу ингибирующего сигнала. Также было продемонстрировано, что PD-L1 связывается с белком B7.1 (Butte et al., Immunity, Vol. 27, pp. 111-122, (2007)). Такие фрагменты также включают в себя растворенную часть ECD белка PD-1, который содержит мутации, такие как мутация A99L, которая повышает связывание с природными лигандами (Molnar et al., PNAS, 105:10483-10488 (2008)). B7-1 или его растворенные фрагменты, которые связываются с лигандом PD-L1 и предупреждают связывание с эндогенным рецептором PD-1, тем самым предупреждая передачу ингибирующего сигнала, также являются пригодными.
Антисмысловые нуклеиновые кислоты PD-1 и PD-L1, как ДНК, так и РНК, а также молекулы siRNA, также могут представлять собой антагонисты PD-1. Такие антисмысловые молекулы предупреждают экспрессию PD-1 на T-клетках, а также продуцирование T-клеточных лигандов, таких как PD-L1 и/или PD-L2. Например, siRNA (например, из около 21 нуклеотида в длину, которая является специфичной в отношении гена, кодирующего PD-1 или кодирующего лиганд PD-1, и олигонуклеотиды которой можно легко приобрести коммерчески), образующая комплексы с носителями, такими как полиэтиленимин (см. Cubillos-Ruiz et al., J. Clin. Invest. 119(8): 2231-2244 (2009), легко захватывается клетками, которые экспрессируют PD-1, а также лиганды PD-1, и ослабляют экспрессию этих рецепторов и лигандов в целях достижения снижения передачи ингибирующего сигнала в T-клетках, тем самым, активируя T-клетки.
b. Антагонисты CTLA4
Другие молекулы, пригодные в опосредовании эффектов T-клеток в иммунном ответе, также предусмотрены в качестве дополнительных терапевтических агентов. В некоторых вариантах осуществления молекула представляет собой антагонист CTLA4, например, антагонистическое анти-CTLA4 антитело. Пример анти-CTLA4 антитела для применения в способах данного изобретения включает в себя антитело, описанное в PCT/US2006/043690 (Fischkoff et al., WO/2007/056539).
Дозы анти-PD-1, анти-B7-H1 и анти-CTLA4 антитела известны в данной области техники и могут находиться в диапазоне, например, от 0,1 до 100 мг/кг или в более коротких диапазонах от 1 до 50 мг/кг или от 10 до 20 мг/кг. Подходящая доза для субъекта-человека может составлять от 5 до 15 мг/кг, при этом 10 мг/кг антитела (например, человеческого анти-PD-1 антитела) представляет собой конкретный вариант осуществления.
Конкретные примеры анти-CTLA4 антитела, пригодного в способах данного изобретения, представляют собой ипилимумаб, человеческое анти-CTLA4 антитело, вводимое в дозе, например, около 10 мг/кг, и тремелимумуб, человеческое анти-CTLA4 антитело, вводимое в дозе, например, около 15 мг/кг. См. также Sammartino, et al., Clinical Kidney Journal, 3(2):135-137 (2010), опубликованную он-лайн в декабре 2009 г.
В других вариантах осуществления антагонист представляет собой малую молекулу. Было продемонстрировано, что ряд малых органических молекул связывается с лигандом B7-1 с предупреждением связывания с CTLA4 (см. Erbe et al., J. Biol. Chem., 277:7363-7368 (2002). Такие малые органические молекулы можно вводить в отдельности или совместно с анти-CTLA4 антителом в целях ослабления передачи ингибирующего сигнала T-клеток.
3. Потенциирующие агенты
В некоторых вариантах осуществления дополнительные терапевтические агенты включают в себя потенциирующий агент. Потенциирующий агент действует в целях повышения эффективности положительного регулятора иммунного ответа, возможно, в результате более одного механизма, несмотря на то, что точный механизм действия не является обязательным для широкого практического применения данного изобретения.
В некоторых вариантах осуществления потенциирующий агент представляет собой циклофосфамид. Циклофосфамид (CTX, Cytoxan® или Neosar®) представляет собой оксазофосфориновый лекарственный препарат, а аналоги включают в себя ифосфамид (IFO, ифекс), перфосфамид, трофосфамид (трофосфамид; иксотен) и фармацевтически приемлемые соли, сольваты, пролекарственные препараты и их метаболиты (заявка на патент США 20070202077, которая включена в полном объеме). Ифосфамид (MITOXANA®) представляет собой структурный аналог циклофосфамида и считается, что его механизм действия является идентичным или по сути аналогичным таковому циклофосфамида. Перфосфамид (4-гидропероксициклофосфамид) и трофосфамид также представляют собой алкилирующие агенты, которые являются структурно связанными с циклофосфамидом. Например, перфосфамид алкилирует ДНК, тем самым ингибируя репликацию ДНК и синтез РНК и белков. Новые оксазофосфориновые производные были разработаны и оценены в целях повышения избирательности и ответа при пониженной токсичности для хозяина (Liang J, Huang M, Duan W, Yu XQ, Zhou S. Design of new oxazaphosphorine anticancer drugs. Curr Pharm Des. 2007;13(9):963-78. Review). Они включают в себя мафосфамид (NSC 345842), глуфосфамад (D19575, бета-D-глюкозилфосфорамидиприт), S-(-)-бромфосфамид (CBM-11), NSC 612567 (алдофосфамид пергидротиазин) и NSC 613060 (алдофосфамид тиазолидин). Мафосфамид представляет собой оксазофосфориновый аналог, который представляет собой химически стабильную соль 4-тиоэтансульфоновой кислоты 4-гидрокси-CPA. Глюфосфамид представляет собой производное IFO, в котором изофосфорамидиприт, алкилирующий метаболит IFO, гликозидически связан с молекулой бета-D-глюкозы. Дополнительные циклофосфамидные аналоги описаны в патенте США 5190929 под названием «Циклофосфамидные аналоги, пригодные в качестве противоопухолевых агентов», который включен в данный документ посредством ссылки в полном объеме.
Несмотря на то, что сам по себе CTX является нетоксичным, некоторые из его метаболитов представляют собой цитотоксические алкилирующие агенты, которые вызывают сшивание ДНК, а в более высоких дозах разрывы нитей. Многие клетки являются устойчивыми к CTX, поскольку они экспрессируют высокие уровни детоксифицирующего фермента альдегиддегидрогеназы (ALDH). CTX нацеливается на пролиферирующие лимфоциты, поскольку лимфоциты (но не гепатопоэтические стволовые клетки) экспрессируют лишь незначительные уровни ALDH, а делящиеся клетки являются наиболее чувствительными к агентам алкилирования ДНК.
В одном варианте осуществления низкие дозы CTX используются в комбинации с раскрываемыми антителами и их антигенсвязывающими фрагментами. Низкие дозы CTX (< 200 мг/кг) могут оказывать иммуностимулирующие эффекты, в том числе стимуляцию противоопухолевых иммунных ответов у человека и в мышиных моделях рака (Brode & Cooke Crit Rev. Immunol. 28:109-126 (2008)). Такие низкие дозы являются субтерапевтическими и не имеют прямой противоопухолевой активности. В отличие от этого, высокие дозы CTX ингибируют противоопухолевый ответ. Несколько механизмов могут объяснять роль CTX в потенциации противоопухолевого иммунного ответа: (a) истощение CD4+CD25+FoxP3+ Treg (и, в частности, пролиферирующих Treg, которые могут быть особенно супрессивными), (b) истощение B-лимфоцитов; (c) индукция оксида нитрита (NO), приводящая к супрессии роста опухолевых клеток; (d) мобилизация и экспансия CD11b+Gr-1+ MDSC. Эти первичные эффекты оказывают многочисленные вторичные эффекты; например, после истощения Treg макрофаги продуцируют больше IFN-γ и меньше IL-10. Также было продемонстрировано, что CTX индуцирует экспрессию IFN I типа и активирует гомеостатическую пролиферацию лимфоцитов.
Истощение Treg наиболее часто указывается в качестве механизма, с помощью которого CTX потенциирует противоопухолевый ответ. Это заключение основано отчасти на результатах экспериментов по адаптивному переносу. В опухолевой модели AB1-HA обработка CTX на сутки 9 приводит к 75% уровню излечения. Перенос очищенных Treg на сутки 12 почти полностью ингибировал ответ со стороны CTX (van der Most et al. Cancer Immunol. Immunother. 58:1219-1228 (2009). Аналогичный результат наблюдали в опухолевой модели HHD2: адаптивный перенос CD4+CD25+ Treg после предварительной обработки CTX устранял терапевтический ответ на вакцину (Taieb, J. J. Immunol. 176:2722-2729 (2006)).
Многочисленные клинические исследования у человека продемонстрировали, что низкодозный CTX является безопасный, хорошо переносимым и эффективным агентом для активации противоопухолевых ответов (Bas, & Mastrangelo Cancer Immunol. Immunother. 47:1-12 (1998)).
В одном варианте осуществления оптимальная доза CTX для потенциирования противоопухолевого иммунного ответа представляет собой таковую, которая снижает общее количество T-клеток в результате снижения уровней Treg ниже нормального диапазона, но который остается субтерапевтическим (см. Machiels et al. Cancer Res. 61:3689-3697 (2001)).
В некоторых вариантах осуществления CTX используется в качестве иммунопотенциируюего агента в дозе 300 мг/м2. В другом варианте осуществления для среднего мужчины (6 футов, 170 фунтов (78 кг) с площадью поверхности тела 1,98 м2), составляющей 300 мг/м2, доза СТХ составляет 8 мг/кг или 624 мг от общего белка. В мышиных моделях рака эффективность была продемонстрирована при дозах, находящихся в диапазоне 15-150 мг/кг, что соответствует 0,45-4,5 мг от общего белка у мыши весом 30 г (Machiels et al. Cancer Res. 61:3689-3697 (2001), Hengst et al Cancer Res. 41:2163-2167 (1981), Hengst Cancer Res. 40:2135-2141 (1980)).
В случае более крупных млекопитающих, таких как примат, таких как пациент-человек, могут быть использованы такие дозы в мг/м2, однако также могут быть использованы однократные дозы в течение конечного периода времени. Такие однократные дозы можно вводить на ежедневной основе в течение конечного периода времени, такого как до 3 суток, или до 5 суток, или до 7 суток, или до 10 суток, или до 15 суток или до 20 суток или до 25 суток, все они особым образом предусмотрены данным изобретением. Та же самая схема может быть использована в отношении других потенциирующих агентов, упомянутых в данном документе.
В других вариантах осуществления потенциирующий агент представляет собой агент, который снижает активность и/или число регуляторных T-лимфоцитов (T-reg), таких как синитиниб (SUTENT®), анти-TGFβ антитело или иматиниб (GLEEVAC®). Упомянутая схема лечения может также включать в себя введение вспомогательного вещества.
Пригодные потенциирующие агенты также включают в себя ингибиторы митоза, такие как паклитаксел, ингибиторы ароматазы (например, летрозол) и ингибиторы ангиогенеза (ингибиторы VEGF, например, авастин, VEGF-Trap) (см., например, Li et al., Vascular endothelial growth factor blockade reduces intratumoral regulatory T cells and enhances the efficacy of a GM-CSF-secreting cancer immunotherapy. Clin Cancer Res. 2006 Nov 15; 12(22):6808-16.), антрациклины, оксалиплатин, доксорубицин, антагонисты TLR4 и антагонисты IL-18.
VI. Трансгенные животные
В одном варианте осуществления предоставлено трансгенное животное, которое продуцирует антитела или их антигенсвязывающие фрагменты, имеющие CDR тяжелой цепи с аминокислотными последовательностями в соответствии с SEQ ID NO:6, 7 и 8, и CDR легкой цепи с аминокислотными последовательностями в соответствии с SEQ ID NO: 12, 13 и 14. В одном варианте осуществления трансгенное животное представляет собой грызуна, например, мышь.
В другом варианте осуществления предоставлено трансгенное животное, которое продуцирует антитела или их антигенсвязывающие фрагменты, имеющие CDR тяжелой цепи с аминокислотными последовательностями в соответствии с SEQ ID NO:18, 19 и 20, и три различные CDR легкой цепи с аминокислотными последовательностями, выбранными из группы, состоящей из SEQ ID NO: 24, 13 и 25. В одном варианте осуществления трансгенное животное представляет собой грызуна, например, мышь.
В другом варианте осуществления предоставлено трансгенное животное, которое продуцирует антитела или их антигенсвязывающие фрагменты, имеющие CDR тяжелой цепи с аминокислотными последовательностями в соответствии с SEQ ID NO: 29, 30 и 31, и CDR легкой цепи с аминокислотами в соответствии с SEQ ID NO: 35, 36 и 37. В одном варианте осуществления трансгенное животное представляет собой грызуна, например, мышь.
Способы получения трансгенных животных, которые продуцируют антитела, известны в данной области техники. См., например, A. Jakobovits, Curr Opin Biotechnol.,6(5):561-6 (1995), и Brüggemann, M., et al., . Arch Immunol Ther Exp (Warsz)., 63(2):101-108 (2015); Jakobovits, A., et al., “From XenoMouse technology to panitumumab, the first fully human antibody product from transgenic mice.” Nat Biotechnol. 25(10):1134-43 (2007); Lonberg N. (2005) “Human antibodies from transgenic animals.” Nat Biotechnol. 23(9):1117-25, а также патенты США №№ 9708635; 9686970; 9499838; 9445581; 9388446; 8835712; 8703485; 8232449; 7795494; и 5939598.
Примеры
Пример 1: Получение анти-PD-1 антител
Результаты
Получение анти-PD-1 антител приводило к образованию клонов 4G9, 4C12 и 5C2, которые выбирали для характеристики.
Пример 2: Кинетика взаимодействия между анти-PD-1 антителами и PD-1
Материалы и способы
Антитела из клонов 4G9, 4C12 и 5C2 характеризовали с помощью системы Biocore™, доступной от GE. Аналит представлял собой PD-1 мыши или человека, а лиганд представлял собой анти-PD-1 антитело. Концентрации аналита представляли собой 0, 62,5, 125, 250, 500 и 1000 нM в оговоренных случаях.
Результаты
На Фиг. 1 и в Табл. 1 изображен анализ взаимодействия 4G9 с PD-1 человека. Равновесная константа ассоциации (KA) составляла 9,52×105 (1/M). Равновесная константа диссоциации (KD) составляла 1,05×10-6 (M).
Таблица 1. Анализ взаимодействия 4G9 с PD-1 человека.
580 ОЕ
125
250
500
500
1000
На Фиг. 2 и в Табл. 2 изображен анализ взаимодействия 4G9 с PD-1 мыши. Равновесная константа ассоциации (KA) составляла 1,94×105 (1/M). Равновесная константа диссоциации (KD) составляла 5,15×10-6 (M).
Таблица 2. Анализ взаимодействия 4G9 с PD-1 мыши.
580 ОЕ
125
250
500
500
1000
На Фиг. 3 и в Табл. 3 изображен анализ взаимодействия 4C12 с PD-1 человека. Равновесная константа ассоциации (KA) составляла 3,14×106 (1/M). Равновесная константа диссоциации (KD) составляла 3,19×10-7 (M).
Таблица 3. Анализ взаимодействия 4C12 с PD-1 человека.
425 ОЕ
125
250
500
500
1000
На Фиг. 4 и в Табл. 4 изображен анализ взаимодействия 5C2 с PD-1 человека. Равновесная константа ассоциации (KA) составляла 2,02×105 (1/M). Равновесная константа диссоциации (KD) составляла 4,95×10-6 (M).
Таблица 4. Анализ взаимодействия 5C2 с PD-1 человека.
320 ОЕ
125
250
500
500
1000
На Фиг. 5 и в Табл. 5 изображен анализ взаимодействия 5C2 с PD-1 мыши. Равновесная константа ассоциации (KA) составляла 1,18×106 (1/M). Равновесная константа диссоциации (KD) составляла 8,50×10-7 (M).
Таблица 5. Анализ взаимодействия 5C2 с PD-1 мыши.
320 ОЕ
125
250
500
500
1000
Пример 3: Связывание анти-PD-1 антител с клетками EL4
Материалы и способы
Клетки EL4 мыши, которые конститутивно экспрессируют PD-1, использовали в клеточном сортере с активацией флуоресценции для оценки связывания 4G9, 5C2 и 4C12 с клетками.
Результаты
На Фиг. 6A изображена гистограмма проточной цитометрии, на которой продемонстрировано, что коммерческое анти-PD-1 антитело связывается с клетками EL4, а антитело изотипического контроля не связывается с клетками EL4. На Фиг. 6B изображена гистограмма проточной цитометрии, на которой продемонстрировано, что 4G9, 5C2 и 4C12 связываются с клетками EL4, а вторичное антитело в отдельности не связывается. На Фиг. 6С изображена гистограмма проточной цитометрии, на которой продемонстрировано, что анти-PD-1 антитело 4G9 связывается с клетками EL4, а вторичное антитело в отдельности не связывается. На Фиг. 6D изображена гистограмма проточной цитометрии, на которой продемонстрировано, что анти-PD-1 антитело 5C2 связывается с клетками EL4, а вторичное антитело в отдельности не связывается. На Фиг. 6E изображена гистограмма проточной цитометрии, на которой продемонстрировано, что анти-PD-1 антитело 4C12 связывается с клетками EL4, а вторичное антитело в отдельности не связывается.
Пример 4: Агонистическая активность анти-PD-1 антител
Материалы и способы
CD4 T-клетки мыши
Очищенные CD4 T-клетки мыши стимулировали анти-CD3/анти-CD28 АТ в течение 48 часов, затем анти-PD-1 АТ (10 мкг/мл) добавляли в культуру совместно с гранулами белка A еще в течение 48 часов. В некоторых образцах анти-PD-L1 АТ добавляли для блокирования взаимодействия PD-1/PD-L1 с целью анализа агонистического эффекта исследуемых АТ. Анализ CBA использовали для определения концентраций IFNγ и IL-2 в супернатантах.
CD4 T-клетки человека
Очищенные CD4 T-клетки человека стимулировали анти-CD3/анти-CD28 АТ в течение 48 часов, затем анти-PD-1 АТ (1 или 10 мкг/мл) добавляли в культуру совместно с гранулами белка A еще в течение 48 часов. Анализ CBA использовали для определения концентраций IFNγ в супернатантах.
Результаты
На Фиг. 7A и 7B изображено, что стимулированные CD4 T-клетки, обработанные анти-PD-1 антителами 5C2, 4C12 и 4G9, имели более высокие концентрации IFNγ и IL-2 в супернатантах по сравнению с необработанными клетками или клетками, обработанными анти-PD-L1 антителами. На Фиг. 7C изображено, что стимулированные CD4 T-клетки человека, обработанные анти-PD-1 антителами 4G9 и 5C2, имели более высокую концентрацию супернатанта IFNγ по сравнению с необработанными клетками или клетками, обработанными антителом изотипического контроля.
Пример 5: Гибридомы усиливают фосфорилирование Akt
Материалы и способы
Внутриклеточное окрашивание pAKT (S473) использовали в качестве маркера T-клеточной активации.
Результаты
Гибридомы от мышей, иммунизированных пептидом E, усиливали фосфорилирование Akt (S473) в CD4 T-клетках мышей (Фиг. 8).
Пример 6: Характеристика трех анти-PD-1 антител
Материалы и способы
Очищенные антитела из гибридом 5C2, 4C12 и 4G9 характеризовали.
Результаты
Определяли изотипы для каждого их трех анти-PD-1 антител. Как 5C2, так и 4C12 принадлежали к изотипу IgG1, и, как было обнаружено, 4G9 принадлежало к изотипу IgG2b (Фиг. 9). Секвенирование гибридом показало 100% идентичности последовательностей в случае антител 5C2 и 4C12.
Пример 7: 4G9 и 5C2 специфично связываются с PD-1 человека
Материалы и способы
ИФА использовали для определения связывания 4G9 и 5C2 с PD-1-Fc человека.
Результаты
На Фиг. 10 изображены результаты ИФА для оценки связывания антител 4G9 и 5C2 с PD-1-Fc человека. Как 4G9, так и 5C2 специфично связываются с PD-1 человека. На Фиг. 11 A изображена гистограмма проточной цитометрии, на которой продемонстрировано, что 4G9 и 5C2 не связывают PD-1 KO CD4 T-клетки, в то время как они связывают CD4 T-клетки от мышей дикого типа (Фиг. 11B).
Пример 8: Передача сигнала
Материалы и способы
CD4 T-клетки мыши предстимулировали в течение 48 часов для обеспечения экспрессии PD-1, после чего обрабатывали очищенными антителами 4G9 и 5C2. Концентрацию pS6 определяли с помощью набора для ИФА (Cell Signaling Tech).
Результаты
В отличие от блокирующих антител (RMP1-14 и J43), 4G9 и 5C2 активируют T-клетки посредством пути с участием S6. Обработка предстимулированных в течение 48 часов (для обеспечения экспрессии PD-1) CD4 T-клеток мыши очищенными антителами 4G9 и 5C2 приводила к значительному повышению pS6 в пределах линейного диапазона (набор для ИФА, Cell Signaling Tech, * P<0,05, ** P<0,01, *** P<0,001 по сравнению с необработанными). Указанный феномен обусловлен скорее прямой активацией, а не блокадой PD-1/PD-L1, поскольку обработка коммерческими АТ-1 (RMP1-14) и АТ-2 (J43), которые блокируют взаимодействие PD-1/PD-L1, не приводит к повышению pS6.
Пример 8: Оценка эффективности in vivo
Материалы и способы
На Фиг. 13A изображена схематическая иллюстрация модели опухоли TC-1, используемой в данном эксперименте. Вкратце, мышам подкожно инъецировали опухолевыми клетками TC-1 на день 0. На день 10 (Д10), день 17 (Д17) и день 24 (Д24) после инъекции опухоли мышей обрабатывали вакциной (E7+PADRE+Quil A). Мышей обрабатывали анти-PD-1 антителами на день 10, день 14, день 17, день 21, день 24 и день 28.
Результаты
Анти-PD-1 антитела 4G9, 4C12 и 5C2 снижали объем опухоли и повышали выживаемость при комбинировании с вакциной E7 (Фиг. 13B-13D).
Пример 9: Оценка эффективности in vivo - анти-EpE антитела
Материалы и способы
Антитела против этипопа E получали и исследовали в модели опухоли TC-1, как описано в Примере 8 выше и на Фиг. 14A.
Результаты
Мыши, обработанные 4G9, антителом, полученным против эпитопа E, демонстрировали значимо более низкий объем опухоли и более высокий уровень выживаемости по сравнению с традиционными ингибиторами контрольных точек, анти-PD1 блокирующими антителами RMP1-14 и J43 (Фиг. 14B-14C).
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА АНТИ-TNFRSF25 | 2017 |
|
RU2746314C2 |
| АНТИТЕЛО ПРОТИВ ЛИГАНДА 1 ЗАПРОГРАММИРОВАННОЙ ГИБЕЛИ КЛЕТОК (PD-L1), ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2727914C2 |
| АНТИТЕЛА К PD-1 СОБАК | 2014 |
|
RU2761663C2 |
| АНТИ-PD-L1 АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2783685C2 |
| АНТИТЕЛА ПРОТИВ PD-1 И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2788616C2 |
| НОВЫЕ АНТИ-PD-1 АНТИТЕЛА | 2016 |
|
RU2729830C2 |
| СПОСОБЫ И АНТИТЕЛА ДЛЯ МОДУЛЯЦИИ ИММУННОГО ОТВЕТА | 2016 |
|
RU2757489C2 |
| АНТИТЕЛА, КОТОРЫЕ СВЯЗЫВАЮТСЯ С ЛИГАНДОМ ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ 1 (PD-L1) | 2013 |
|
RU2689953C2 |
| АНТИТЕЛА, НАПРАВЛЕННЫЕ ПРОТИВ ILT2, И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2832673C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2016 |
|
RU2731202C2 |
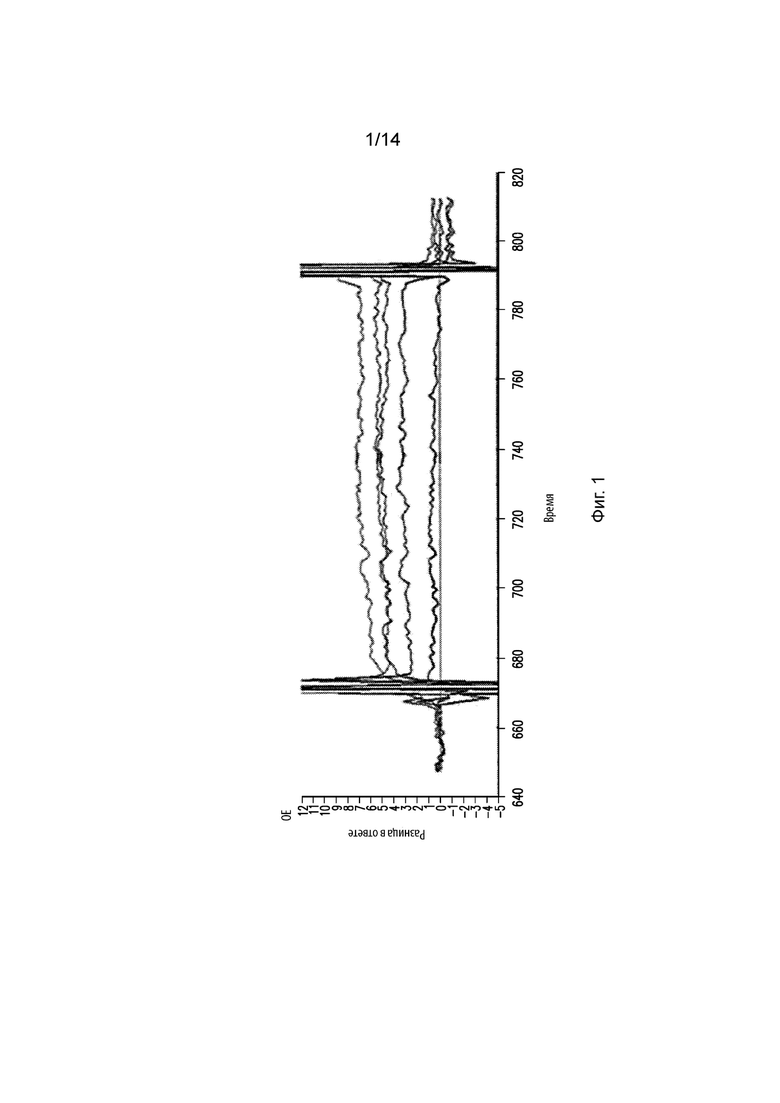
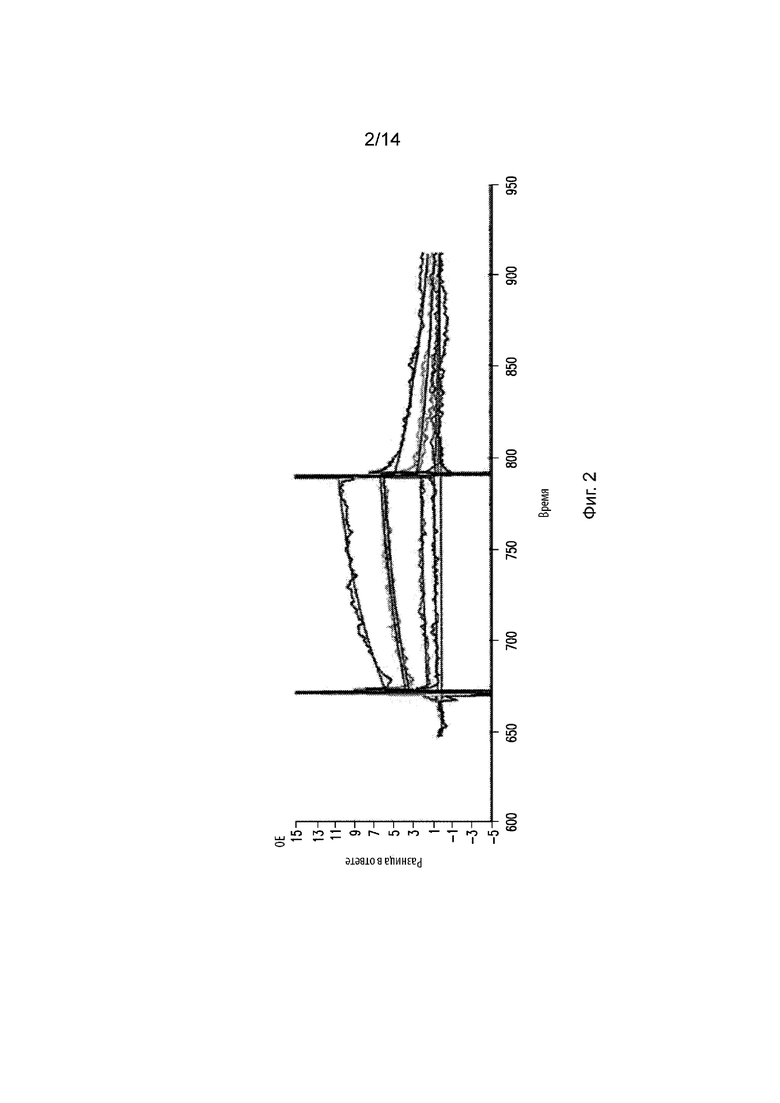
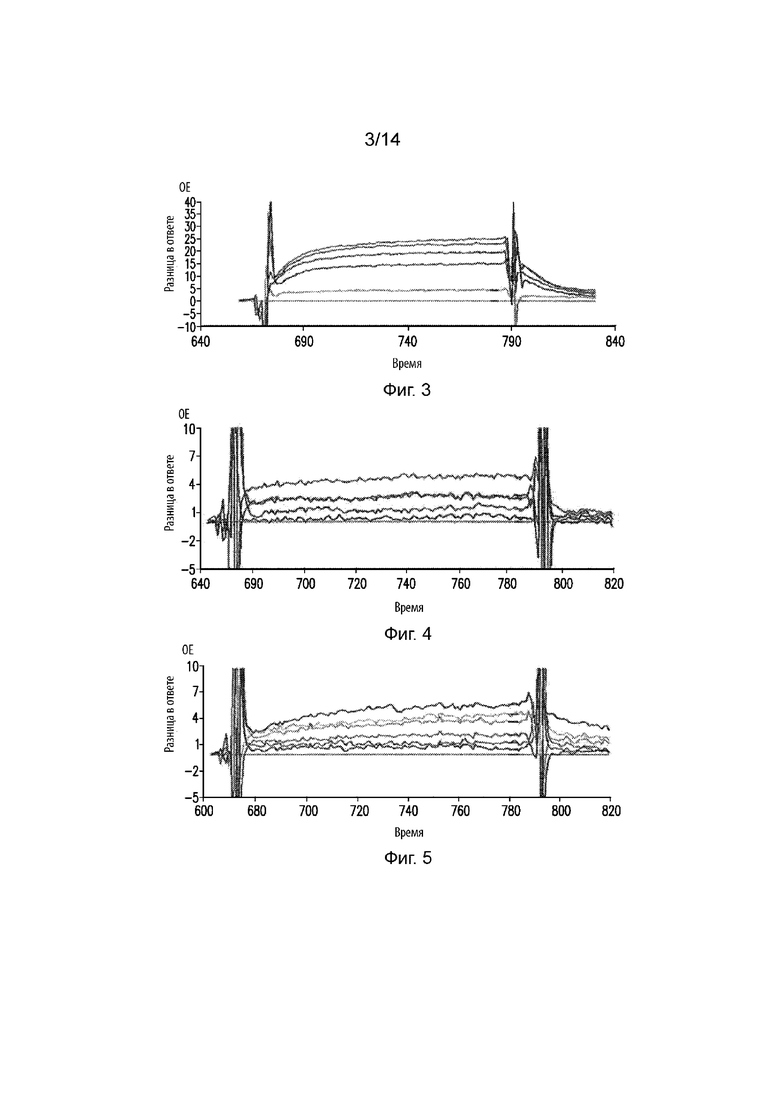
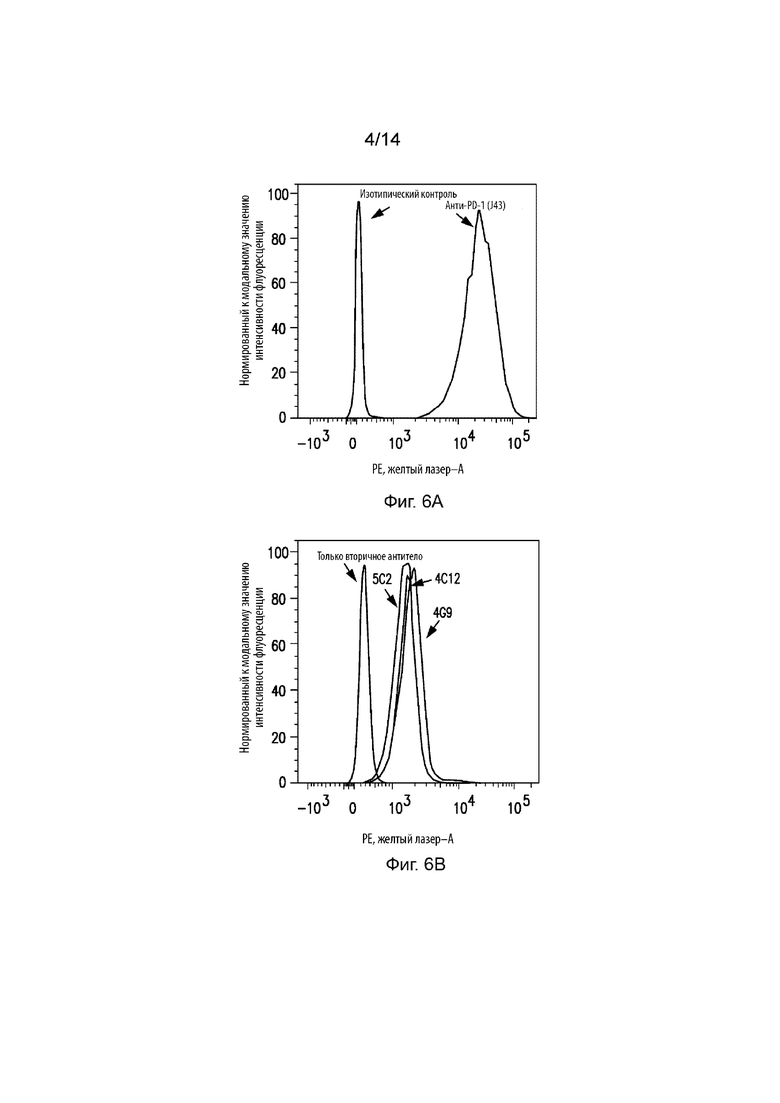
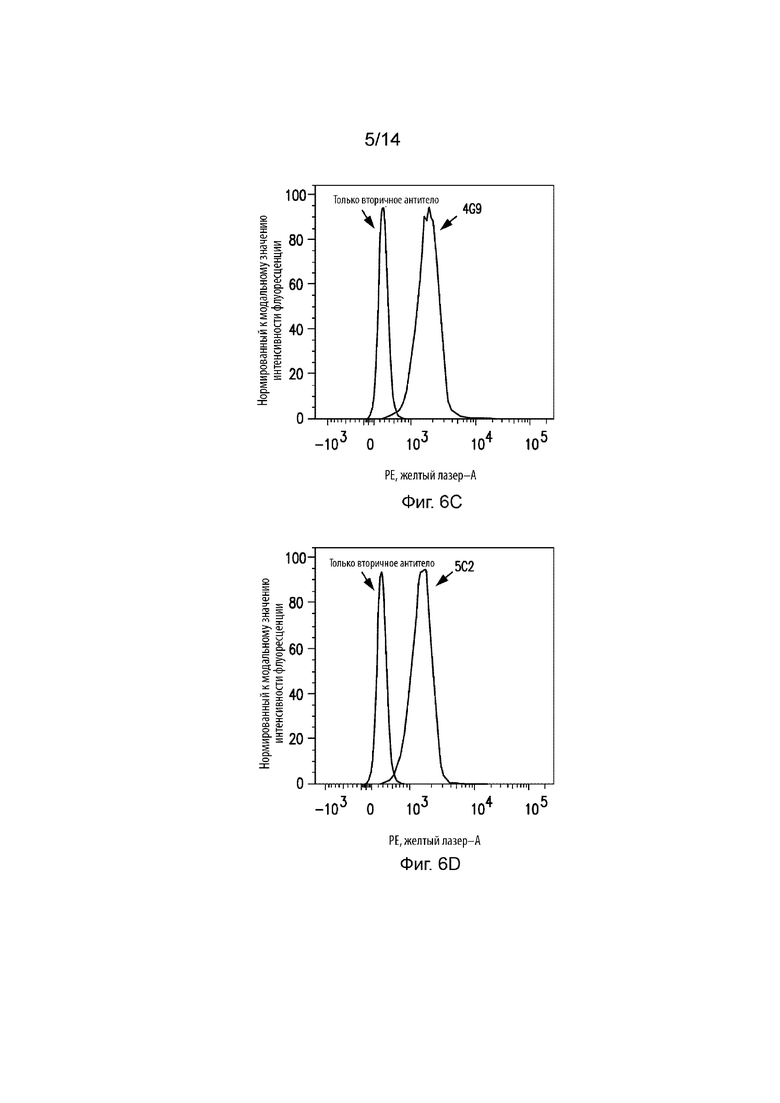
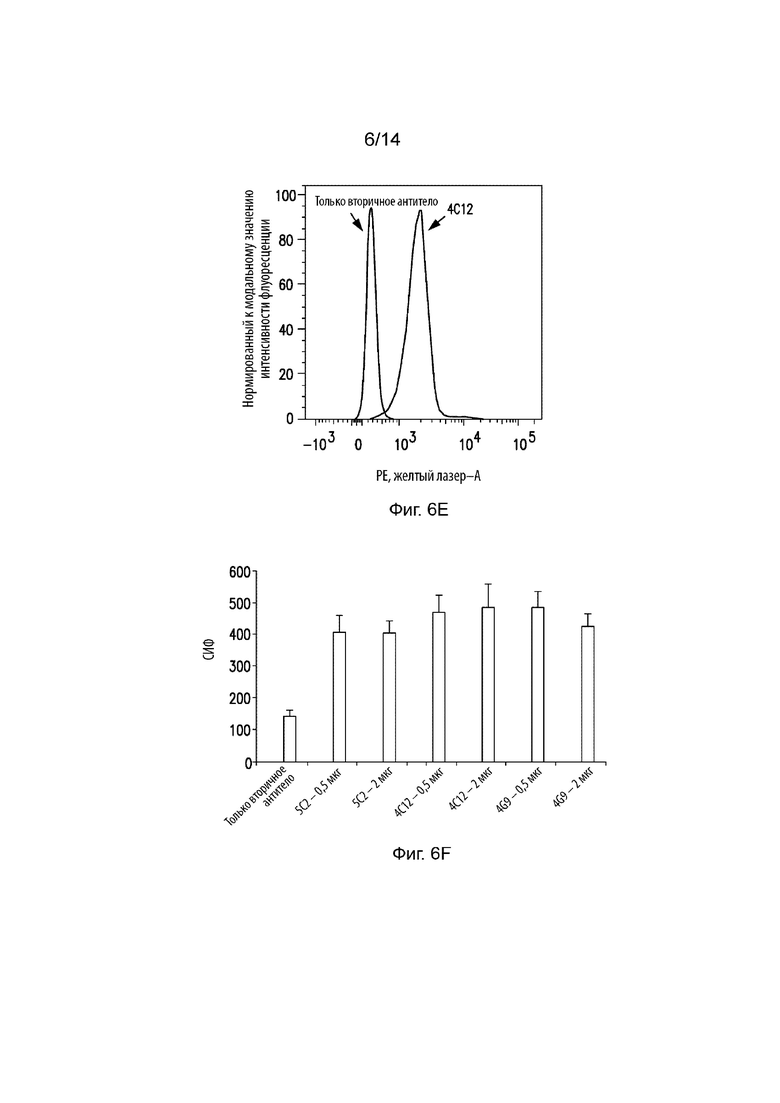
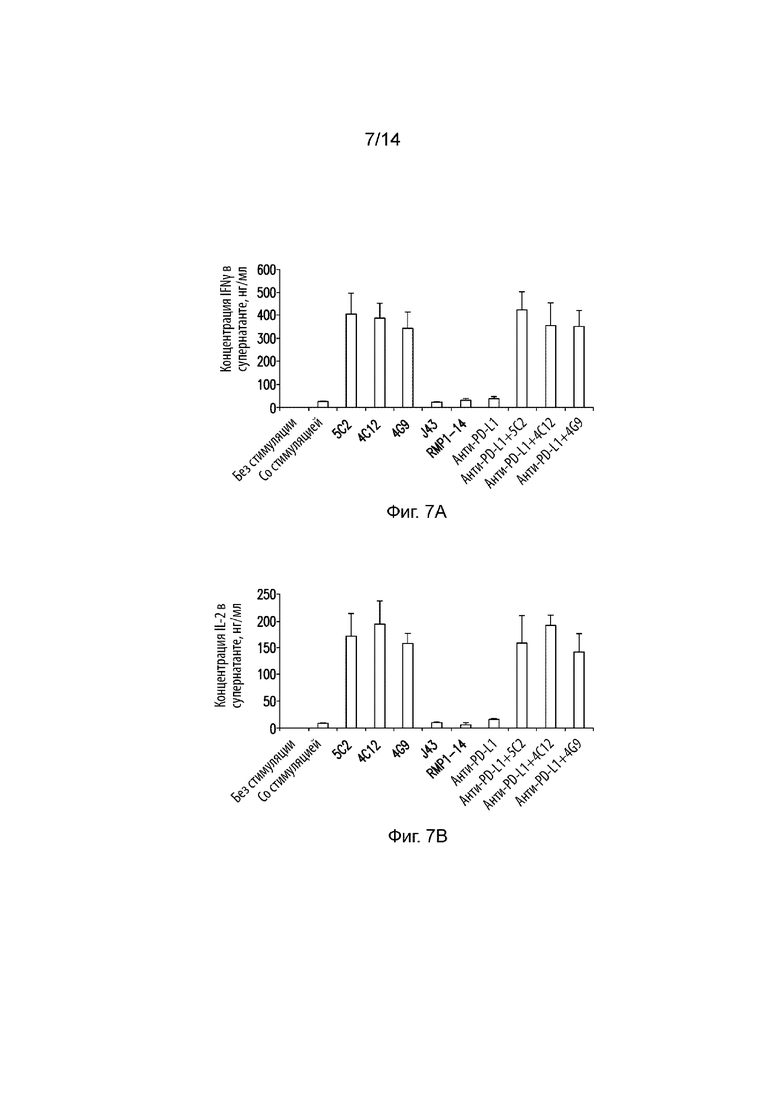
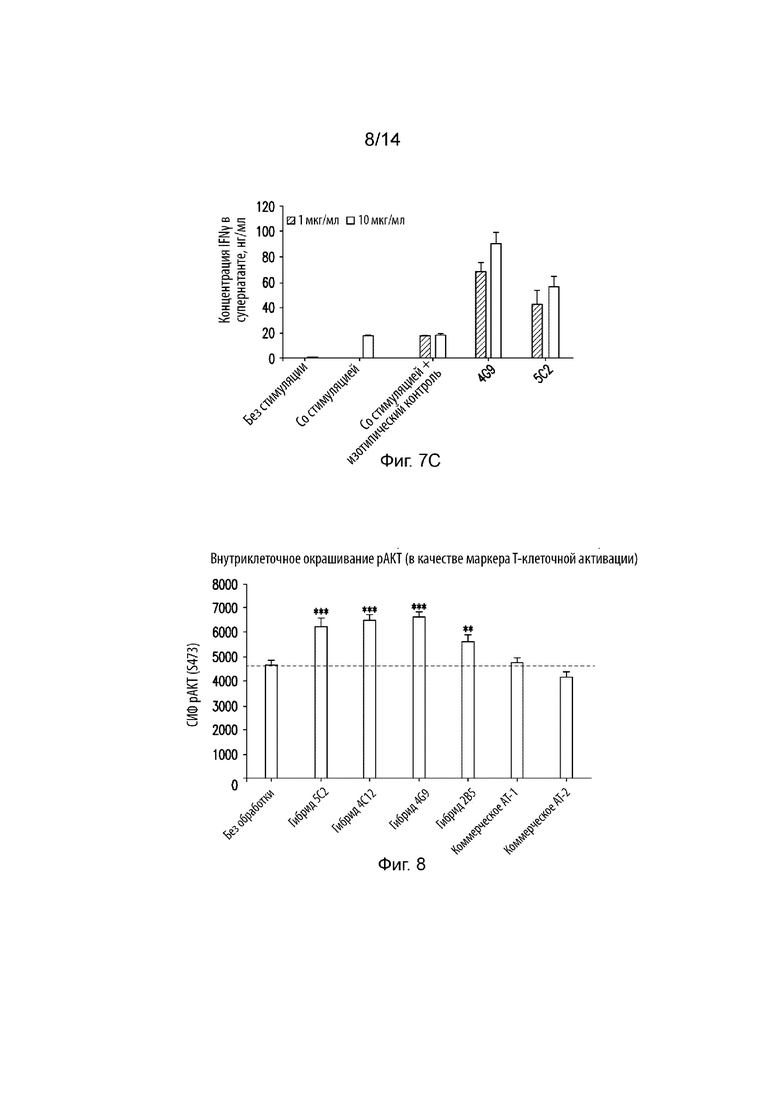
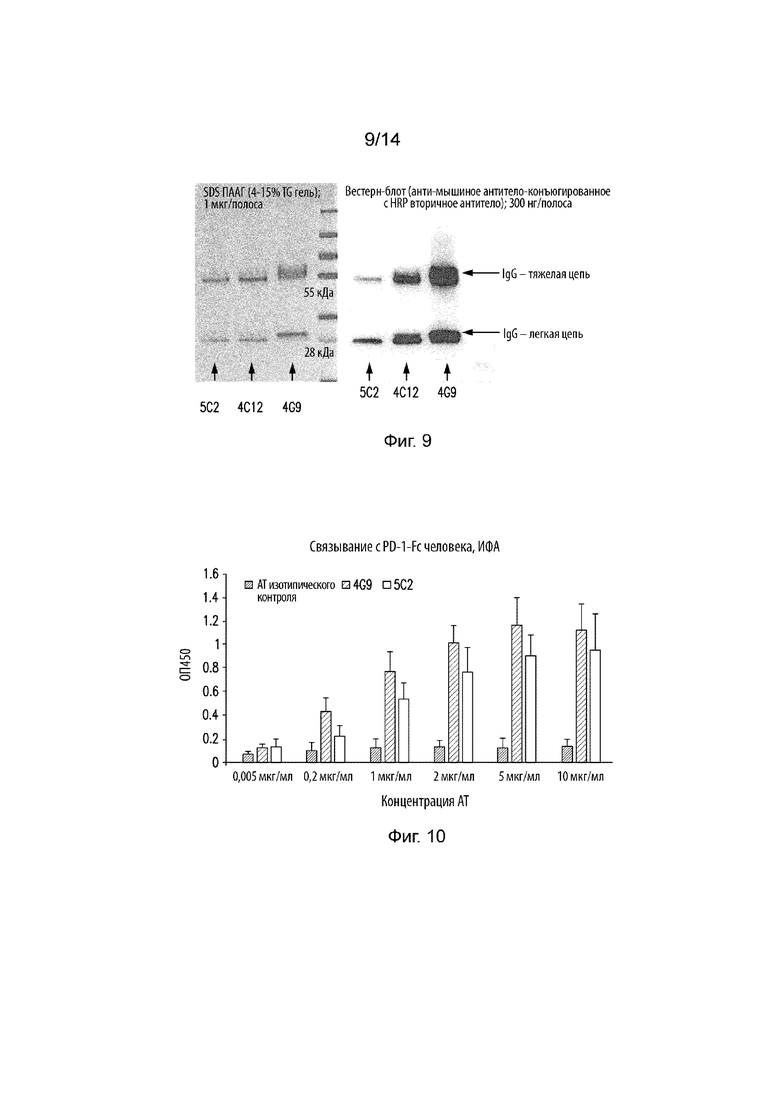
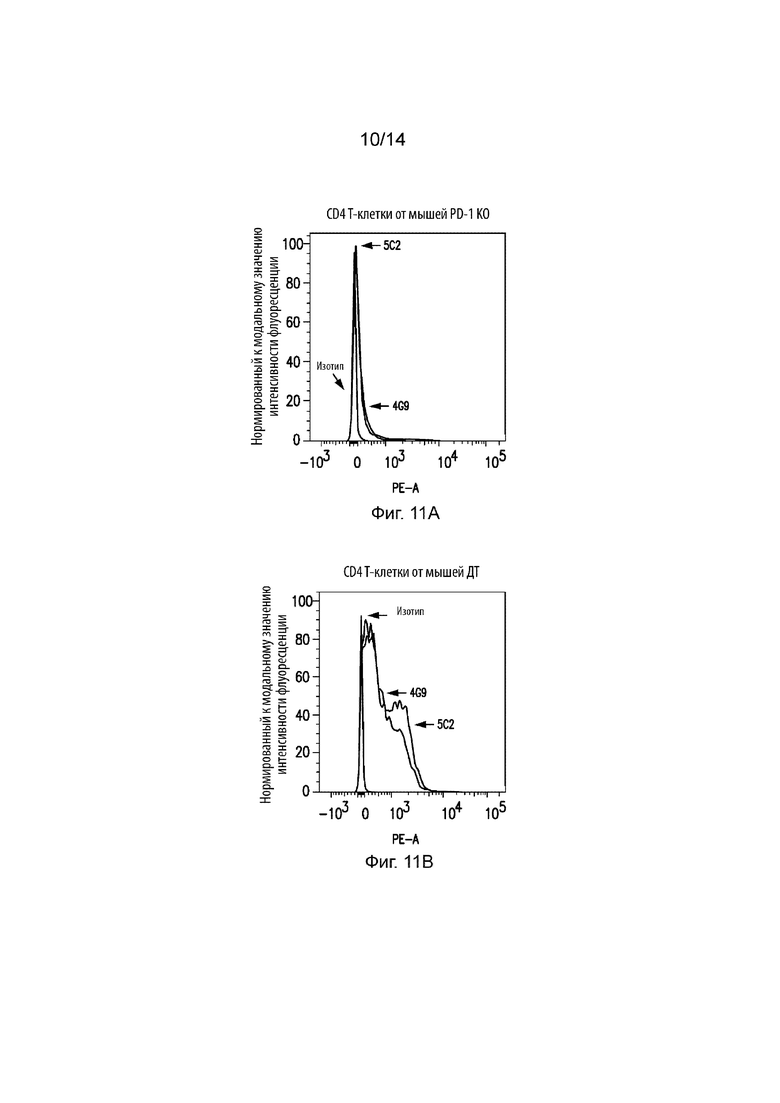
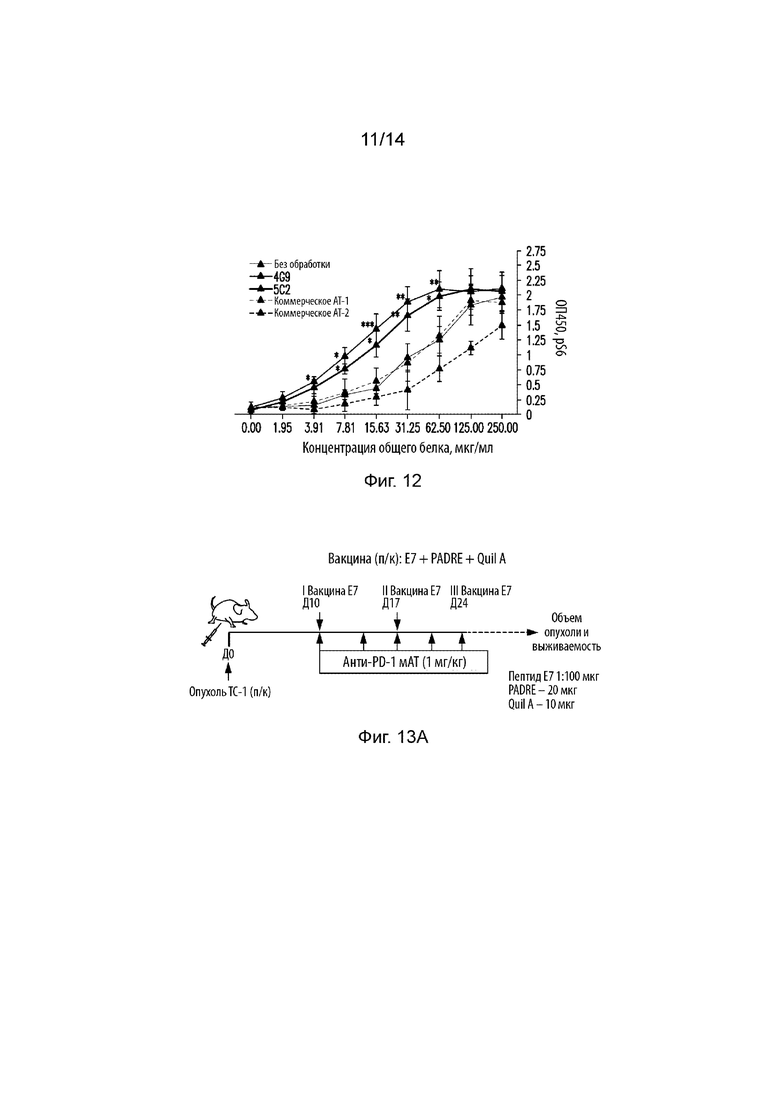
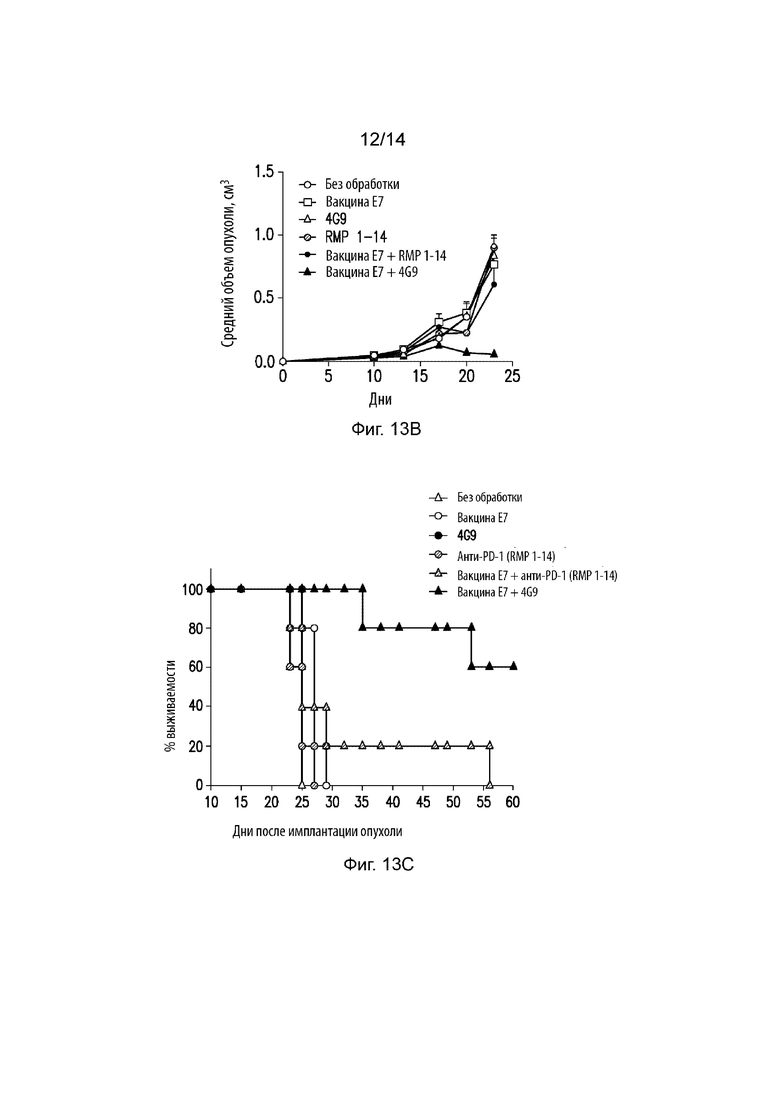
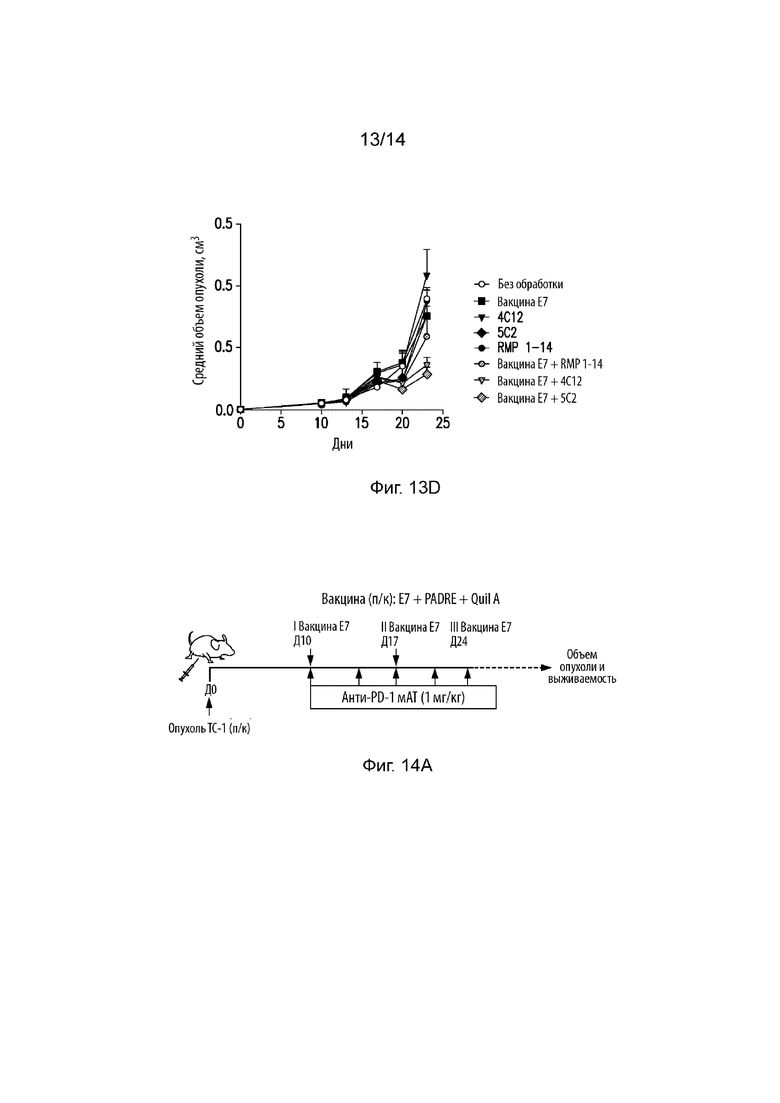
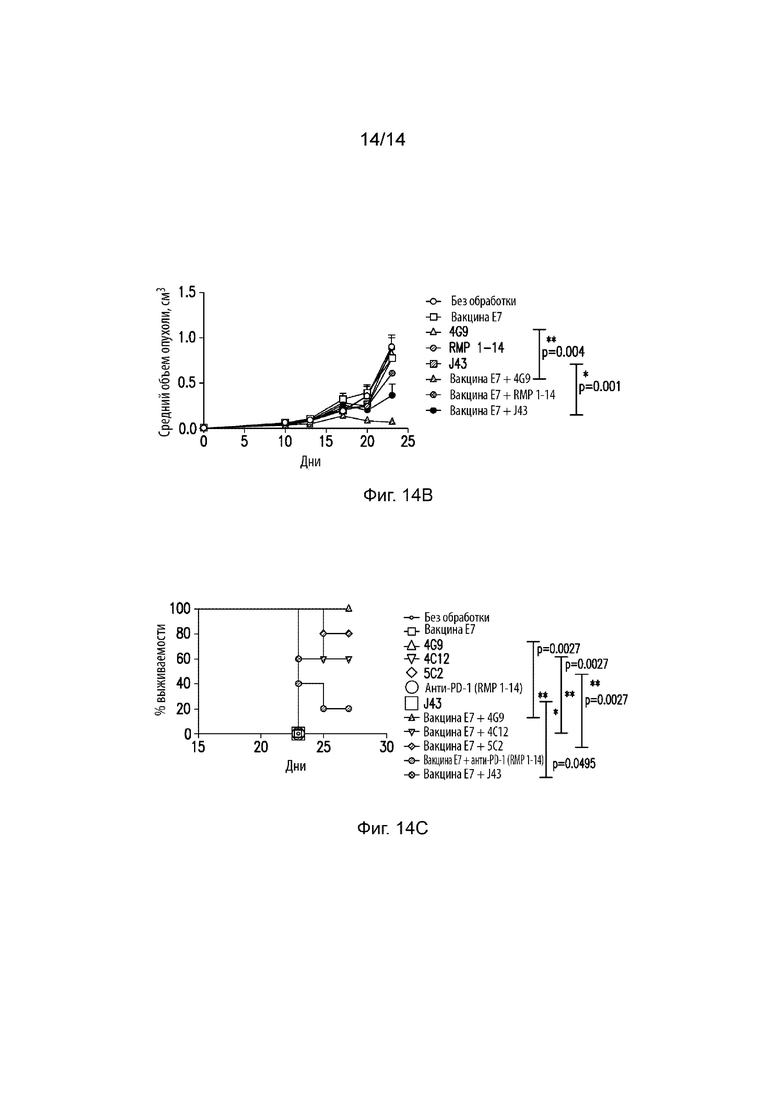
Группа изобретений относится к биотехнологии. Представлены антитела и их антигенсвязывающие фрагменты, которые связываются с PD-1, трансгенный грызун, продуцирующий антитело или его антигенсвязывающего фрагмента, нуклеиновая кислота, кодирующая антитело или антигенсвязывающий фрагмент, клетка для продукции антитела или антигенсвязывающего фрагмента. Также раскрыты Фармацевтическая композиция для индукции, стимуляции или усиления иммунного ответа, способ индукции, стимуляции или усиления иммунного ответа у пациента, способ лечения рака у пациента, способ снижения опухолевой нагрузки у пациента и способ лечения инфекции у пациента. Изобретение направлено на получение новых антител, которые иммуноспецифично связываются с PD-1 и индуцируют иммунный ответ, который активирует пролиферацию или активность иммунных клеток. 10 н. и 17 з.п. ф-лы, 5 табл.,14 ил., 8 пр.
1. Антитело или его антигенсвязывающий фрагмент, которые специфически связываются с PD-1,
где антитело или его антигенсвязывающий фрагмент содержат
три CDR тяжелой цепи (HCDR1, HCDR2 и HCD3), содержащиеся в вариабельной области тяжелой цепи (HCVR) с последовательностью SEQ ID NO:27 или SEQ ID NO:28; и
три CDR легкой цепи (LCDR1, LCDR2 и LCD3), содержащиеся в вариабельной области легкой цепи (LCVR) с последовательностью SEQ ID NO:33 или SEQ ID NO:34.
2. Антитело или его антигенсвязывающий фрагмент, которые специфически связываются с PD-1,
где антитело или его антигенсвязывающий фрагмент содержат
CDR1 тяжелой цепи с последовательностью SEQ ID NO:29,
CDR2 тяжелой цепи с последовательностью SEQ ID NO:30, и
CDR3 тяжелой цепи с последовательностью SEQ ID NO:31, и
CDR1 легкой цепи с последовательностью SEQ ID NO:35,
CDR2 легкой цепи с последовательностью SEQ ID NO:36, и
CDR3 легкой цепи с последовательностью SEQ ID NO:37.
3. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, содержащее тяжелую цепь, которая по меньшей мере на 90%, 95%, 99% или 100% идентична последовательности SEQ ID NO:27 или 28.
4. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, содержащее легкую цепь, которая по меньшей мере на 90%, 95%, 99% или 100% идентична последовательности SEQ ID NO:33 или 34.
5. Антитело или его антигенсвязывающий фрагмент по п.1 или 2, содержащие
тяжелую цепь, которая по меньшей мере на 90%, 95%, 99% или 100% идентична последовательности SEQ ID NO:27 или 28, и
легкую цепь, которая по меньшей мере на 90%, 95%, 99% или 100% идентична последовательности SEQ ID NO:33 или 34.
6. Трансгенный грызун, продуцирующий антитело или его антигенсвязывающего фрагмента по любому из пп.1-5, содержащий нуклеиновую кислоту, кодирующую антитело или его антигенсвязывающий фрагмент по любому из пп.1-5.
7. Трансгенный грызун по п.6, где грызун представляет собой мышь.
8. Нуклеиновая кислота, кодирующая антитело или антигенсвязывающий фрагмент по любому из пп.1-5.
9. Клетка для продукции антитела или антигенсвязывающего фрагмента по любому из пп.1-5, содержащая нуклеиновую кислоту по п.8.
10. Клетка по п.9, где нуклеиновая кислота экспрессируется из вектора.
11. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-5, где антитело или его антигенсвязывающий фрагмент являются человеческими, мышиными, химерными, гуманизированными или моноклональными.
12. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-5, где антитело или его антигенсвязывающий фрагмент являются человеческими или химерными.
13. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-5, где антитело или его антигенсвязывающий фрагмент представляет собой полноразмерный иммуноглобулин.
14. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-5, где антитело или его антигенсвязывающий фрагмент представляет собой IgG, IgE, IgM, IgD, IgA или IgY.
15. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-5, где антитело или его антигенсвязывающий фрагмент представляет собой IgG1, IgG2, IgG3, IgG4, IgA1 или IgA2.
16. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-5, где антигенсвязывающий фрагмент выбран из группы, состоящей из Fab', F(ab')2, Fv, одноцепочечного (ScFv), ди-ScFv, диатела и тритела.
17. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-5 или 11-16, которые иммуноспецифично связываются с TYLCGAISLAPKAQI (SEQ ID NO:38) PD-1 на поверхности иммунной клетки.
18. Антитело или его антигенсвязывающий фрагмент по п.17, где иммунная клетка представляет собой T-клетку.
19. Антитело или его антигенсвязывающий фрагмент по п.18, где Т-клетка представляет собой CD8+ T-клетку.
20. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-5 или по п.19, которые иммуноспецифично связываются с SEQ ID NO:38 на PD-1, экспрессируемом на поверхности иммунной клетки, и индуцируют или стимулируют сигнал с участием PD-1, который активирует или стимулирует иммунную клетку.
21. Фармацевтическая композиция для индукции, стимуляции или усиления иммунного ответа, содержащая эффективное количество антитела или его антигенсвязывающего фрагмента по любому из пп.1-5 или 11-19 и фармацевтически приемлемый эксципиент.
22. Фармацевтическая композиция по п.21, дополнительно содержащая второй терапевтический агент.
23. Фармацевтическая композиция по п.22, где второй терапевтический агент представляет собой циклофосфамид.
24. Способ индукции, стимуляции или усиления иммунного ответа у пациента, включающий:
введение пациенту эффективного количества антитела или антигенсвязывающего фрагмента по любому из пп.1-5 или 11-19 или фармацевтической композиции по любому из пп.21-23 для индукции, стимуляции или усиления иммунного ответа у пациента.
25. Способ лечения рака у пациента, включающий:
введение пациенту эффективного количества антитела или антигенсвязывающего фрагмента по любому из пп.1-5 или 11-19, или фармацевтической композиции по любому из пп.21-23 для лечения рака у пациента.
26. Способ снижения опухолевой нагрузки у пациента, включающий:
введение пациенту эффективного количества антитела или антигенсвязывающего фрагмента по любому из пп.1-5 или 11-19, или фармацевтической композиции по любому из пп.21-23 для снижения опухолевой нагрузки у пациента.
27. Способ лечения инфекции у пациента, включающий:
введение пациенту эффективного количества антитела или антигенсвязывающего фрагмента по любому из пп.1-5 или 11-19 или фармацевтической композиции по любому из пп.21-23 для лечения хронической инфекции у пациента.
| US 2009130114 A1, 21.05.2009 | |||
| WO 2008112017 A2, 18.09.2008 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
Авторы
Даты
2024-02-05—Публикация
2018-09-07—Подача