Изобретение относится к медицине, а именно, к средствам диагностирования с использованием ультразвуковых волн в полостях и трактах организма, томографии и лечения печени и расстройств желчного пузыря с помощью средств, способствующих растворению конкрементов, и может широко использоваться в практической медицине, в частности, в гастроэнтерологии для сочетанного лечения неалкогольной жировой болезни печени и желчнокаменной болезни.
Известен способ лечения больных желчнокаменной болезнью первой стадии, представленный в одноименном патенте РФ №2519198 по кл. А61К 36/68, А61Р 1/10, 1/16, з. 21.08.2012 г., оп. 10.06.2014 г.
Известный способ лечения больных желчнокаменной болезнью первой стадии, заключается в медикаментозном воздействии и отличается тем, что больному вводят Мукофальк, в дозе по 1 пакетику 3 раза в день в течение 22-24 недель.
Недостатком известного способа являются его ограниченные возможности - лечение желчнокаменной болезни только первой стадии и при отсутствии побочных эффектов.
Известен способ диагностики и лечения желчнокаменной болезни, представленный в ст. Селиверстова П.В. и др. «Возможности терапевтического лечения больных желчнокаменной болезнью» в журн. «Медицинский совет». 2019 г, №14, стр.: 44-51. (см. Приложение 1 к заявке).
Известный способ включает в себя диагностику, где после сбора анамнеза и общеклинического обследования основным диагностическим методом при подозрении на ЖКБ является ультразвуковое исследование (УЗИ). Однако дифференциация типов камней с помощью УЗИ в целом не представляется возможной. Так, например, кальцификация может быть выявлена только с помощью обзорной рентгенографии или компьютерной томографии (КТ). Наиболее современным диагностическим методом является КТ с оценкой плотности камней по шкале Хаунсфилда. КТ дает возможность заменить обзорную рентгеноскопию (рентгенографию) брюшной полости на более точную методику, позволяющую оценить плотность камней в течение 5-10 минут, причем без применения контрастных препаратов. По данным обзорной рентгенографии конкременты в желчном пузыре начинают быть видны примерно с+350^00 единиц плотности (в сравнении с единицами КТ). С учетом того, что плотность камней, доступных для перорального литолиза, как правило, не превышает +100 единиц, результаты классического рентгенологического исследования могут дать ложные надежды на успех лечения.
Для решения вопроса о тактике ведения пациента с ЖКБ также проводят необходимые лабораторные исследования, включающие клинический анализ крови, общий анализ мочи, копрограмму, оценку состояния микробиоты толстой кишки, биохимический анализ крови (АЛТ, ACT, ЩФ, ГГТП, липидограмма, сахар, амилаза, липаза, общий и прямой билирубин, ПТИ). Также при подозрении и для подтверждения различных стадий и форм ЖКБ в поликлинических и стационарных условиях в настоящее время могут применяться такие методы, как эндоскопическая ультрасонография, эндоскопическая ретроградная панкреатохолангиография, динамическая ультразвуковая холецистография, динамическая гепатоби-лиосцинтиграфия, мультиспиральная компьютерная томография, магнитно-резонансная холангиография и этапное хроматическое дуоденальное зондирование с биохимическим исследованием желчи.
Необходимыми условиями для проведения пероральной литолитической терапии УДХК являются рентгенопрозрачность желчных камней и хорошая сократительная способность желчного пузыря. Диаметр камней, как правило, не должен превышать 10 мм. Критериями отбора пациентов для литолитической терапии служат следующие обстоятельства:
 желчные камни должны быть чисто холестериновыми (рентгенопрозрачными при обзорной рентгенографии или КТ: плотность < 100 HU);
желчные камни должны быть чисто холестериновыми (рентгенопрозрачными при обзорной рентгенографии или КТ: плотность < 100 HU);
 максимальный диаметр камня не должен превышать, как правило, 15-20 мм (возможно растворение камней; большего диаметра - до 25-30 мм, но при условии, что их плотность не превышает 75 HU);
максимальный диаметр камня не должен превышать, как правило, 15-20 мм (возможно растворение камней; большего диаметра - до 25-30 мм, но при условии, что их плотность не превышает 75 HU);
 желчный пузырь должен нормально функционировать;
желчный пузырь должен нормально функционировать;
 просвет желчного пузыря должен быть наполнен камнями, как правило, не более чем наполовину (максимум - до 2/3 объема);
просвет желчного пузыря должен быть наполнен камнями, как правило, не более чем наполовину (максимум - до 2/3 объема);
 пузырный проток должен быть проходим;
пузырный проток должен быть проходим;
 отсутствие осложнений ЖКБ.
отсутствие осложнений ЖКБ.
Критерии исключения: частые колики, серьезные осложнения ЖКБ, «фарфоровый» желчный пузырь, цирроз печени, диарея, резекция тонкой кишки, беременность. Отечественные исследования показали, что отсутствие рентгеноконтрастных конкрементов у пациента является гораздо более важным критерием эффективного литолиза, чем диаметр камней. Литолитический эффект отмечается у пациентов с плотностью камней до 100 HU. Уменьшение размеров конкрементов в течение 3 мес. наблюдается у 85% пациентов, а эффективность растворения составляет в среднем 2,86 мм за 3 мес.
Алгоритм лечебных мероприятий ЖКБ на фоне литолиза должен включать лечение сопутствующих заболеваний, вызывающих камнеобразование, по возможности исключение медикаментов (контрацептивы, средства для снижения уровня холестерина, цефалоспорины 3-го поколения и др.) и воздействие на факторы риска, инициирующие холелитиаз.
Медикаментозная терапия должна быть направлена на:
 коррекцию кишечного дисбиоза (пре-, про-, син-, сими метабиотики);
коррекцию кишечного дисбиоза (пре-, про-, син-, сими метабиотики);
 нормализацию реологии желчи и профилактику дальнейшего камнеобразования (УДХК, из расчета 1 кап. На 25 кг массы тела);
нормализацию реологии желчи и профилактику дальнейшего камнеобразования (УДХК, из расчета 1 кап. На 25 кг массы тела);
 нормализацию тонуса желчного пузыря и сфинктера Одди (спазмолитик гимекромон, по 1 т 3 р/д, 14 дней).
нормализацию тонуса желчного пузыря и сфинктера Одди (спазмолитик гимекромон, по 1 т 3 р/д, 14 дней).
После полного растворения камней рецидивы ЖКБ могут развиваться у 10% пациентов в год в течение первых пяти лет. Рецидивирование является признаком продолжающихся расстройств обмена веществ, вновь приводящих к развитию перенасыщения желчи холестерином после прекращения приема литолитических препаратов. После растворения желчных камней основное внимание должно уделяться профилактике рецидивов ЖКБ. Основные меры профилактики рецидивов ЖКБ: нормализация массы тела, занятия физкультурой и спортом, ограничение употребления животных жиров и углеводов, регулярный прием пищи каждые 3-4 часа, исключение длительных периодов голодания, прием достаточного количества жидкости (не менее 1,5 л/сут), устранение запоров, УЗИ желчного пузыря каждые 6-12 мес., профилактические курсы УДХК 1-2 раза в год, контроль уровня холестерина в крови.
Недостатком известного способа лечения ЖКБ является значительная сложность обследования.
Главной же проблемой является тот факт, что учеными доказана тесная связь желчнокаменной болезни (ЖКБ) с другим не менее распространенным заболеванием - неалкогольной жировой болезни печени (НАЖБП), которая характеризуется некротически-воспалительными изменениями в клетках печени, которые развиваются в результате стеатоза и обладают потенциалом к прогрессированию в цирроз печени (ЦП) и гепатоцеллюлярную карциному.
Сами по себе диагностика и лечение неалкогольной жировой болезни печени (НАЖБП), также известны и представлены, в частности, в ст. Никонова Е.Л. и Аксенова В.А. «Современные подходы к диагностике и лечению неалкогольной жировой болезни печени» в журн. «Профилактическая медицина». 2018; 21(3):62-69. (см. Приложение 2 к заявке).
Клиническая картина и диагностика.
Обычно НАЖБП характеризуется бессимптомным течением и часто диагностируется случайно при обследовании пациентов по другому поводу. Часто НАЖБП обнаруживается при обращении пациентов к врачу по поводу артериальной гипертензии, ишемической болезни сердца, заболеваний периферических сосудов, ожирения, сахарного диабета 2-го типа (СД2) и др. У этих больных НАЖБП можно заподозрить по наличию синдрома цитолиза и/или гепатомегалии.
В клинической картине на первый план могут выходить симптомы, характерные для метаболического синдрома (МС): висцеральное ожирение, признаки нарушения обмена глюкозы, дислипидемия и артериальная гипертензия. Часть пациентов предъявляют неспецифические жалобы на повышенную утомляемость, ноющую боль или дискомфорт в области правого подреберья без четкой связи с приемом пищи.
Комплексная оценка пациентов с подозрением на НАЖБП включает в себя:
1. Начальное обследование:
- употребление алкоголя (о неалкогольном генезе свидетельствует употребление менее 20 г этанола в сутки женщинами и менее 30 г/сут мужчинами);
- личный и семейный анамнез по СД, артериальной гипертензии и сердечно-сосудистым заболеваниям;
- ИМТ, окружность талии, изменение массы тела;
- инфекция, вызванная вирусами гепатитов В и С;
- применение препаратов, связанных со стеатозом, в анамнезе;
- печеночные ферменты - аспартат- (ACT) и аланинаминотрансфераза (АЛТ), γ-глутамилтранспептидаза (ГГТ);
- уровень гликемии натощак, HbA1c, пероральный глюкозотолерантный тест, уровень инсулина натощак (HOMA-IR);
- общий анализ крови;
- уровень общего холестерина (ХС), ЛПВП, триацилглицерола, мочевой кислоты в сыворотке;
- УЗИ (при повышенном уровне ферментов печени).
2. Расширенное обследование:
- ферритин и насыщение трансферрина;
- обследование на целиакию, заболевания щитовидной железы, синдром поликистозных яичников (СПКЯ);
- обследование на редкие заболевания печени (болезнь Вильсона-Коновалова, аутоиммунный гепатит, дефицит α1-антитрипсина).
Для установления степени выраженности стеатоза, некровоспалительных изменений и стадии фиброза печени у больных НАЖБП применяют различные расчетные тесты (FibroTest, Fatty Liver Index, SteatoTest, NAFLD Liver Fat score и др.). С их помощью на основе ряда показателей путем математического анализа проводят расчет соответствующего индекса.
Например, в шкале оценки содержания жира в печени при НАЖБП (NAFLD Liver Fat score) для расчета используют данные о наличии или отсутствии метаболического синдрома, сахарный диабет 2-ой стадии (СД2), уровне инсулина сыворотки крови натощак, ACT и АЛТ. Этот показатель может быть рассчитан с помощью представленного в интернете калькулятора, основанного на определениях номера метаболического синдрома, наличие диабета 2-го типа, инсулин в mu/L, AST в U/L, ALL в U/L. https://www.mdapp.co/non-alcoholic-fatty-liver-disease-liver-fat-score-nafld-lfs-calculator-358/. К неинвазивным методам диагностики НАЖБП также относится транзиентная эластография (фибросканирование, фиброэластометрия), определяющая эластичность ткани печени с помощью аппарата FibroScan. Наиболее высокая диагностическая точность метода наблюдается при выраженных стадиях фиброза. Недостатком является невозможность оценки выраженности некровоспалительного процесса, низкая информативность у пациентов с избыточной массой тела, невозможность оценки состояния печени на стадиях стеатоза, стеатогепатита и ранних стадиях фиброза.
В случае выявления выраженного фиброза окончательный диагноз устанавливают с помощью биопсии печени.
Биопсия печени - это «золотой стандарт» диагностики НАЖБП, позволяющий с высокой степенью достоверности подтвердить наличие стеатоза и воспаления, определить стадию фиброза, а также провести дифференциальный диагноз между стеатозом и неалкогольный стеатогепатит (НАСГ), исключить другие причины поражения печени и прогнозировать дальнейшее течение заболевания.
В диагностический алгоритм оценки и мониторинга тяжести заболевания у пациентов с подозрением на НАЖБП и метаболическими факторами риска (ФР) вошли: биомаркеры стеатоза (индекс ожирения печени [FLI], SteatoTest, шкала содержания жира в печени при НАЖБП); 2 печеночные пробы (АЛТ, ACT, ГГТ); любое повышение активности АЛТ, ACT или ГГТ; сывороточные маркеры фиброза (шкала фиброза при НАЖБП [NFS], FIB-4, коммерческие тесты (FibroTest, FibroMeter, ELF);
Лечение.
Основной целью терапии является профилактика прогрессирования болезни, главным образом, за счет модификации образа жизни, отмены потенциально гепатотоксичных препаратов, коррекции метаболических и липидных нарушений.
Модификация образа жизни (МОЖ) пациентов с НАЖБП - рекомендуют использовать структурированные программы МОЖ в отношении питания и физической активности.
Лекарственная терапия НАЖБП рекомендуется при прогрессирующем НАСГ и на ранней стадии НАСГ с повышенным риском прогрессирования фиброза. К этой группе пациентов относятся лица старше 50 лет с СД, МС и устойчивым повышением уровня АЛТ. Фармакотерапия также показана при НАСГ с выраженной некровоспалительной активностью. Рекомендовано применение следующих групп препратов: тиазолидиндионы (глитазоны), витамин Е, урсодезоксихолевая кислота, обетихолевая кислота, статины. При отсутствии эффекта от МОЖ и медикаментозного лечения может применяться бариатрическая хирургия, которая позволяет снизить массу тела и частоту метаболических осложнений со стабильными результатами в долгосрочной перспективе. Пациентов с НАСГ в сочетании с печеночной недостаточностью и/или ГЦК следует рассматривать как кандидатов на трансплантацию печени.
Недостатком известных способа диагностики и лечения является то, что при этом не учитывается сопутствующее наличие желчнокаменной болезни с оценкой эффективности возможного литолиза и прогноза течения заболевания в этом случае.
Известен также способ диагностики ЖКБ с НАЖБП, представленный в ст.авторов Черкащенко Н.А., Ливзан М.А., Кролевец Т.С. «Клинические проявления коморбидного течения желчнокаменной болезни и неалкогольной жировой болезни печени», в журн. «Терапевтический архив». 2020 г., т 92 (8): стр. 29-36. (см. Приложение 3 к заявке).
Информация представлена в следующем виде.
Материалы и методы. В открытое сравнительное исследование включены 183 пациента с НАЖБП. Основная группа представлена пациентами с НАЖБП и ЖКБ (n=88), из которых 53 перенесли холецистэктомию (ХЭ), группа сравнения - пациенты с НАЖБП без ЖКБ (n=95). Проведено стандартное лабораторно-инструментальное обследование, в том числе оценка стадии фиброза печени с помощью эластометрии. Проведено открытое сравнительное исследование пациентов с установленным диагнозом НАЖБП в возрасте старше 18 лет.Критериями исключения считались подозрение на чрезмерное и/или опасное употребление спиртных напитков по результатам опросников AUDIT и CAGE, также подозрение по результатам обследования на лекарственный гепатит, аутоиммунный, гемохроматоз или болезнь Вильсона-Коновалова. Из исследования исключались пациенты с циррозом печени, онкологическими заболеваниями, сопутствующими заболеваниями в случае недостижения целевых уровней основных показателей, характеризующих их течение и риски (такие как артериальная гипертензия - АГ, ишемическая болезнь сердца - ИБС, СД 2-го типа и др.). Сформирована исследовательская группа из 183 человек, среди которых 127 (69,39%) мужчин и 56 (30,6%) женщин. Средний возраст пациентов составил 48,9 года, в частности 46,9 года у мужчин и 53,1 года у женщин. Для достижения цели исследования проводилось клиническое и лабораторное обследование пациентов, стандартное для лиц с заболеваниями гастроэнтерологического профиля. Из инструментальных методов диагностики применены ультразвуковое абдоминальное исследование и эластометрия печени для установления стадии фиброза печени. Для определения диагностически ценных клинических признаков коморбидного течения НАЖБП и ЖКБ полученные результаты обследования изучались в группах: в основную вошли пациенты, страдающие НАЖБП и ЖКБ (n=88), из которых 53 пациента перенесли холецистэктомию (ХЭ), в группу сравнения - пациенты, страдающие НАЖБП без ЖКБ (n=95).
Обработка результатов исследования и графический анализ данных проводились при помощи программ Microsoft Excel, Statistica 10.0. При ненормальном распределении данные представлены в виде медианы. Нулевая гипотеза отвергалась при значениях p<0,01. Сравнение 2 и более не связанных друг с другом групп проводили при помощи критерия Краскела-Уоллиса и Манна-Уитни для количественных показателей и с использованием точного двустороннего критерия Фишера, критерия сопряженности х2 Пирсона для номинальных данных. Взаимосвязи между показателями оценивались при помощи корреляционного анализа Спирмена.
При объективном осмотре оценивались состояние кожных покровов, наличие «печеночных» знаков. Пациенты с НАЖБП страдали ожирением или имели избыточную массу тела. Пациентов с нормальной массой тела не зафиксировано, 50 (27,32%) человек имели избыток массы тела, среднее значение индекса массы тела - 33,2±4,49 кг/м2. Следует отметить, что у лиц как основной группы, так и группы сравнения показатели индекса массы тела не имели статистически достоверных различий. Известно, что висцеральный тип ожирения вносит наиболее существенный вклад в формирование метаболических расстройств, поэтому ключевым показателем, который рассчитывался нами для диагностики абдоминального типа ожирения, стало соотношение объема талии к объему бедер (ОТ/ОБ). Данный показатель соответствовал абдоминальному характеру распределения жировой ткани независимо от пола пациентов (среднее значение ОТ/ОБ=1,02±0,07). При анализе этого показателя установлено, что пациенты группы сравнения имеют более высокие значения в сравнении с пациентами с сопутствующей ЖКБ (U-1,96; р<0,01, г=(-0,164); р<0,01), что наглядно представлено на рис. 2.
При осмотре органов брюшной полости увеличение размеров живота за счет увеличения объема жировой ткани отмечено у 103 (56,28%) пациентов. Перкуторно и методом флюктуации признаков наличия жидкости в брюшной полости ни у одного пациента не выявлено. При глубокой пальпации болезненность в эпигастрии зафиксирована у 101 (55,19%) пациента, в правом подреберье - у 125 (83,06%), болезненность при пальпации поджелудочной железы по Гроту - у 21 (12,4%), симптомы желчного пузыря (Кера, Ортнера, Мюсси) положительны у 80 (43,72%). Увеличение размеров печени по Курлову отмечено у 78 (42,62%) лиц.
Боль в правом подреберье у пациентов без ЖКБ выявлена достоверно чаще: 73 (76,84%) пациента в сравнении с сопутствующей ЖКБ - 52 (59,09%) человека (х2=6,65; р<0,01), что может быть обусловлено, по-видимому, увеличением печени в размерах, нежели билиарными симптомами. Симптом болезненности при пальпации поджелудочной железы по Гроту, наоборот, в 2 раза чаще у пациентов с ЖКБ - 18 (20,45%) пациентов против 9 (9,47%) без ЖКБ (Х2=4,38; р<0,01), что отражает частоту билиарнозависимого панкреатита у данной категории лиц.
При анализе данных, полученных в результате проведения общего анализа крови, отклонений от нормы не выявлено. Наличие лейкоцитоза, повышенного СОЭ, являющееся проявлением обострения заболевания, отмечено критерием исключения. При анализе показателей биохимического исследования крови активность заболевания (неалкогольный стеатогепатит) выявлена у 89 (53%) пациентов, при этом повышение аланинаминотрансферазы (АЛТ) - у 55 (30,05%), увеличение аспартатаминотрансферазы (ACT) - у 35 (19,13%), повышение у-глутамилтранспептидазы (ГГТ) -у 42 (22,95%) и щелочной фосфатазы - у 36 (19,67%). Повышение уровня маркеров цитолиза в пределах минимальной степени активности (до 5 норм) выявлено у 89 (48,63%) человек, умеренной степени (от 5 до 10 норм) не выявлено. В исследование не включались пациенты с высокой биохимической активностью, поскольку высокая активность процесса могла исказить данные по фиброзу печени, оцениваемые по эластометрии, и затруднять проведение статистического анализа.
Дополнительно авторами рассчитывался коэффициент соотношения АЛТ и ACT. Известно, что доминирование ACT над АЛТ является косвенным признаком токсического поражения печени и требует дополнительного внимания для исключения как алкогольного, так и лекарственного поражения печени. Вместе с тем, согласно международным рекомендациям по диагностике и лечению НАЖБП, преобладание ACT над АЛТ - неблагоприятный фактор прогрессирования НАЖБП от стеатогепатита в цирроз печени. Соотношение трансаминаз (АЛТ и ACT) продемонстрировало доминирование АЛТ над ACT и составило более 1,0 у всех обследуемых пациентов (1,69±0,85).
Помимо оценки функциональных печеночных проб проведен анализ данных лабораторных исследований, полученных в ходе биохимического анализа крови, по выявлению тех изменений, которые свидетельствуют о наличии выраженности факторов риска прогрессирования НАЖБП.
При сравнительном анализе данных биохимического исследования крови установлено, что показатели цитолиза (повышение уровня АЛТ, ACT) не имели статистически достоверных различий. Вместе с тем такой показатель, как ГГТ, повышен прежде всего среди пациентов основной группы, имеющих сопутствующую ЖКБ, имел статистически значимую прямую корреляционную связь с ЖКБ и ХЭ (г=0,242; р<0,01 и г=0,298; р<0,01 соответственно). Из показателей, отражающих метаболические стигмы жирового и углеводного обмена, установлено, что у лиц с сопутствующей ЖКБ и перенесенной ХЭ отмечаются более высокие показатели липопротеидов низкой плотности - ЛПНП (г=0,228; р<0,01).
Ультразвуковое исследование (УЗИ) органов брюшной полости является обязательным методом по оценке структуры печени для пациентов, страдающих НАЖБП. Наиболее информативными признаками, указывающими на наличие НАЖБП у лиц с факторами риска этого заболевания, считаются: увеличение размеров печени и повышение ее эхогенности, которое по данным УЗИ зафиксировано у 130 (71,43%) пациентов. У 88 (48,09%) человек по данным УЗИ диагностирована ЖКБ разной стадии, из них у 31 (18,3%) выявлено наличие конкрементов и билиарной взвеси в полости желчного пузыря, а именно: конкременты - у 20 (11,98%) пациентов, сладж - у 12 (7,19%), а у 53 (28,96%) проведена ХЭ, поэтому по УЗИ описано отсутствие желчного пузыря и проводилась оценка состояния его ложа, которое у всех пациентов без особенностей. У 159 (86,89%) лиц по данным УЗИ при описании структуры поджелудочной железы выявлены диффузные изменения поджелудочной железы, а также повышенная эхогенность у 92 (50,27%) и зернистость - у 5 (2,73%) пациентов.
Достоверные различия при анализе данных авторы выявили по показателю эхогенности печени: у пациентов без ЖКБ она у всех повышена, а у лиц с ЖКБ - без такого признака [13 (15,12%) человек (х2=14,38; р<0,01)]. Также выявлена отрицательная корреляционная связь с ЖКБ и ХЭ и диаметром портальной вены [г=(-0,345), р<0,01]. Пациентам проведена эластометрия печени, которая позволяет оценить неинвазивно стадию фиброза. Выявлено превалирующее большинство пациентов с I и II стадией фиброза печени - 71 (38,79%) и 40 (21,86%) человек соответственно. У 61 (33,3%) пациента фиброз не выявлен. Результаты распределения стадии фиброза в группах сравнения представлены на рис. 5. Обращает на себя внимание соотношение лиц с прогрессирующими стадиями фиброза (II и III) и непрогрессирующими (I и II) или его отсутствием у лиц в зависимости от сопутствующей ЖКБ или перенесенной ХЭ. У основной группы статистически достоверно выше число лиц с прогрессирующими стадиями фиброза (26,31% против 20,45% у пациентов группы сравнения), особенно у лиц после ХЭ (30,18%). Стадия фиброза печени имела положительную достоверно значимую взаимосвязь с ХЭ (г,=0,366; р<0,01).
Обсуждение.
Очевидным становится тот факт, что коморбидность НАЖБП и ЖКБ обусловлена общими факторами риска развития и прогрессирования болезней. Метаболический синдром (МС), ведущими механизмами развития которого являются висцеральное ожирение и инсулинорезистентность, лежит в основе патогенетического взаимодействия рассматриваемых патологий. Результаты крупных исследований на популяциях лиц различных национальностей (азиатской, европейской, американской) демонстрируют существенно более высокую распространенность ЖКБ среди лиц с НАЖБП, при этом последняя рассматривается в качестве независимого предиктора холелитиаза. В некоторых работах указывается, что фактором риска ЖКБ выступает первоначально МС, а не самостоятельно НАЖБП, которая рассматривается только как его компонент.Привлекают внимание исследования, презентирующие ХЭ как неблагоприятный фактор по прогрессированию проявлений МС (гипер-и дислипидемии, стеатоза печени, АГ) и ставящие под сомнение безобидность данной процедуры у пациентов с ЖКБ.
Недостатком известного способа является то, что в нем не описано совместное лечение ЖКБ и НАЖБП и прогнозирование исхода заболеваний.
Известны диагностика и лечение болезней желчного пузыря и НАЖБП, представленные в ст. Мехтиева С.Н., Мехтиевой О.А., Ибрагимовой З.М. «Функциональные расстройства желчного пузыря (ФРЖП) и неалкогольная жировая болезнь печени: клинические особенности и новые подходы к терапии» в журн. «Медицинский совет», 2020 г., №15, стр.: 54-64. (см. Приложение 4 к заявке)
Известный способ включает в себя:
1. Лабораторное обследование пациентов с ФРЖП и НАЖБП, содержащее следующие действия:
1. Исключение активного воспалительного процесса в ЖП (клинический анализ крови, С-реактивный белок).
2. Дифференциальный диагноз с функциональными расстройствами сфинктера Одди (СО) (при билиарном расстройстве СО возможно повышение АЛТ, ACT, билирубина, а при панкреатическом расстройстве - повышение амилазы/липазы в течение 6 ч после болевого эпизода).
3. Оценка функционального состояния печени (биохимический анализ крови: АЛТ, ACT, гамма-глутамилтранс-пептидаза, щелочная фосфатаза, общий билирубин и его фракции, общий белок, альбумин. При возможности - проведение Фибро-теста).
4. Оценка метаболического статуса пациента (липидограмма, гликемия натощак, гликированный гемоглобин).
5. Оценка выраженности синдромов мальдигестии и СИБР: копрограмма, фекальная эластаза, посев кала на дисбактериоз (ориентировочный метод). Одним из более точных и относительно доступных методов диагностики СИБР в настоящее время следует признать водородный дыхательный тест с лактулозой.
2. Инструментальное обследование ФРЖП и НАЖБП, включающее:
1. Обязательные методы. Согласно рекомендациям ведущих специалистов, к обязательным исследованиям при подозрении на ФРЖП относятся ультразвуковое исследование (УЗИ) органов брюшной полости и стандартная эзофагога-стродуоденоскопия (ЭГДС) с осмотром области большого сосочка ДПК, позволяющие исключить органические изменения в желчном пузыре (ЖП), поджелудочной железе, ДПК и функциональные нарушения сфинктера Одди.
2. Уточняющие методы. Уточняющим методом диагностики ФРЖП является динамическое УЗИ с желчегонным завтраком (или УЗИ-холецистография). Этот наиболее доступный и неинвазивный метод дает возможность определить сократительную функцию ЖП, которая считается нормальной, если объем ЖП к 30-40 мин после приема желчегонного завтрака уменьшается на 1/2 от первоначального, а коэффициент опорожнения составляет 50-80%. Снижение данного показателя менее 40% свидетельствует о наличии гипомоторной дискинезии ЖП.
По результатам исследований состояния функции ЖП у пациентов с НЖБП методом динамической УЗИ-холецистографии нормальный тонус ЖП обнаруживается только у 11% больных, тогда как гипотонус - в 85% случаев, а гипертоническое состояние ЖП выявляется лишь у 3% больных 3.
3. Дополнительные (специальные) методы используются только в спорных случаях, когда необходимо проведение дифференциальной диагностики с органической патологией билиарного тракта, холедохолитиазом, обструкцией или функциональным расстройством сфинктера Одди. Наиболее эффективным неинвазивным методом диагностики в данном случае является магнитно-резонансная холангиопанкреатография (МРХПГ). Если существует необходимость в дальнейшем уточнении диагноза, выполняется эндоскопическое УЗИ (эндо-УЗИ), которое является самым высокочувствительным методом обнаружения микрохолецистохоледохолитиаза с размерами конкрементов менее 3 мм, стриктур холедоха и других органических изменений панкреатобилиарной системы. С целью оценки состояния гепатоэнтеральной циркуляции, параметров накопления и выделения желчи используется динамическая гепатобилиарная сцинтиграфия, но данный метод выполняется только в специализированных учреждениях, и трактовка его результатов до настоящего времени является спорной. Тем не менее, по данным отечественных исследователей, применение ДГБС у больных НЖБП дало возможность обнаружить снижение поглотительной способности гепатоцитов на 43,2%, пассажа желчи из паренхимы печени в протоки - на 43,7%, увеличение концентрационно-депонирующей функции ЖП - на 21,1% и замедление моторно-эвакуаторной функции ЖП4.
3. Терапия пациентов с ФРЖП и НАЖБП включает:
А) немедикаментозный подход:
1. Рациональное питание, соответствующее диете №5 по М.И. Певзнеру, с исключением избыточного потребления простых углеводов, холестерина, жареного, прием пищи каждые 3 ч небольшими порциями. При дисфункции ЖП по гипотоническому типу пища должна быть с достаточным содержанием растительного жира (до 80 г/сут), рекомендуется употреблять яйца, морковь, тыкву, кабачки, зелень, отруби.
2. Немедикаментозный подход включает также достижение и поддержание нормального индекса массы тела, нормализацию психоэмоциональной сферы, физической активности, соблюдение режима труда и отдыха, борьбу с вредными привычками (курением и злоупотреблением алкоголем), исключение применения лекарственных препаратов, ухудшающих физико-химические свойства желчи и моторику ЖП (эстрогены, фибраты, цефтриаксон, амиодарон), а также гепатотоксичных средств (НПВС, антибиотиков тетрациклинового ряда и др.).
Б) Медикаментозную терапию, включающую:
1. Нормализацию моторики ЖП (селективные спазмолитики, холекинетики, прокинетики, растительные препараты комбинированного действия). Среди селективных спазмолитиков, применяемых для лечения ФРЖП, используются мебеверин, тримебутин, гиосцина бутилбромид и гимекромон.
2. Гепатопротективную терапию, направленную на улучшение поглотительной и секреторной функции гепатоцитов путем уменьшения воспалительных и фибротических процессов в ткани печени (глицирризиновая кислота (ГК), эссенциальные фосфолипиды (ЭФЛ), урсодезоксихолевая кислота (УДХК), янтарная и альфа-липоевая кислоты, обладающие антиоксидантным потенциалом, адеметионин.
3. Улучшение физико-химических свойств желчи и профилактика камнеобразования (УДХК, экстракт из листьев артишока). Эффективным лекарственным средством, обладающим доказанным воздействием на реологию желчи, является УДХК, терапия которой общепризнанно рассматривается основой базисного лечения всех пациентов с ФРЖП.
На сегодняшний день известно, что УДХК обладает литолитическим и холеретическим действием, а также оказывает противовоспалительный эффект на эпителиальные и мышечные клетки ЖП и, вероятно, восстанавливает чувствительность гладкомышечных клеток ЖП к ХЦК. Являясь гидрофильной кислотой, препарат имеет терапевтический потенциал в виде уменьшения избытка холестерина в гладкомышечных клетках ЖП у пациентов с литогенной желчью.
4. Коррекцию гепатоэнтеральной циркуляции желчных кислот (УДХК; лечение СИБР - кишечные антисептики (рифаксимин), симбиотики).
5. Коррекция процессов пищеварения и всасывания в ДПК, купирование стеатореи и дуоденальной гипертензии (ферменты, антациды, прокинетики, лечение СИБР).
6. Коррекция психовегетативного статуса.
7. Противорецидивное лечение и вторичная профилактика. Существенным дополнением медикаментозной терапии в фазу ремиссии является применение растительных препаратов комбинированного действия, оказывающих холеретическое, спазмолитическое, противовоспалительное и прокинетическое действие (бессмертник, кукурузные рыльца, мята, холосас, петрушка, гепабене, артишок, куркума, шиповник), а также минеральных вод без газа (ессентуки-4, арзни, боржоми, белинска киселка).
Если в ходе динамического наблюдения за пациентом с ФРЖП и НЖБП с коэффициентом опорожнения ЖП менее 35-30% на протяжении каждых 3 мес.в течение года у больного сохраняется упорный болевой синдром, резко ухудшающий трудоспособность и качество жизни, несмотря на все немедикаментозные и медикаментозные подходы, рассматривается вопрос о выполнении плановой холецистэктомии. При этом облегчение симптомов после холецистэктомии регистрируется у 94% больных с низкой сократимостью ЖП и у 85% пациентов с нормальным коэффициентом опорожнения ЖП. Однако важно заметить, что в последующем у многих пациентов могут развиваться функциональные расстройства сфинктера Одди (более чем в 20% случаев). Но еще более неблагоприятным последствием холецистэктомии у больных НЖБП является усугубление нарушений липидного, углеводного и основного обменов, а также прогрессирования фиброзного процесса в ткани печени. Поэтому необходимо стремиться к максимальному сохранению ЖП у больных с НЖБП.
Перспективным в терапевтическом плане может быть одновременное воздействие на состояние желчи, воспалительный и фиброзный процессы в печени. В данном аспекте весьма интересным представляется новый оригинальный двухкомпонентный гепатопротекторный препарат Фосфоглив® УРСО, имеющий в своем составе гли-цирризиновую кислоту и УДХК и обеспечивающий более эффективное воздействие на печень и ФРЖП, чем монопрепараты УДХК.
Недостатками известного способа диагностики и лечения ЖКБ и НАЖБП являются весьма ощутимая сложность инструментального обследования при их диагностике и лечении, а также отсутствие возможности прогнозирования эффективности одновременного медикаментозного лечения таких сочетанных болезней как желчнокаменная болезнь печени и неалкогольная жировая болезнь печени.
Наиболее близким по технической сущности к заявляемому представляется способ диагностики и лечения ЖКБ в сочетании с НАЖБП, описанный в статье Кролевец Г.С. и др. «Патогенетические аспекты коморбидного течения неалкогольной жировой болезни печени и желчнокаменной болезни: обзор и собственные данные» в «Русском медицинском журнале», 2022 г., №6(5), стр. 278-285 и выбранный в качестве прототипа (см. Приложение 5 к заявке)..
Указанная информация представлена следующим образом.
На кафедре факультетской терапии и гастроэнтерологии ФГБОУ ВО ОмГМУ Минздрава России было проведено исследование, включившее 183 пациента, страдающих НАЖБП. Для определения диагностически ценных клинических признаков коморбидного течения НАЖБП и ЖКБ полученные результаты обследования изучались в группах и подгруппах: в основную группу вошли пациенты, страдающие НАЖБП и ЖКБ (n=88), из которых 53 пациента перенесли холецистэктомию (ХЭ), группу сравнения составили пациенты, страдающие НАЖБП без ЖКБ (n=95).
Всем пациентам проводилось стандартное лабораторно-инструментальное обследование, а также измерение уровня лептина, его растворимого рецептора, инсулина, адипонектина в сыворотке крови. Фиброз печени оценивали с помощью транзиентной эластометрии.
При анализе пола и возраста лиц, страдающих НАЖБП и ЖКБ, было установлено, что женщин среди пациентов основной группы статистически значимо больше: 36 (40,9%) пациенток основной группы против 20 (21,1%) пациенток группы сравнения (χ2=8,48, р<0,01) - при отсутствии статистически значимых различий по возрасту. Достоверно чаще пациенты основной группы предъявляли жалобы на ощущение горечи во рту (χ2=11,66, р<0,01), при этом сила положительной взаимосвязи возрастала после холецистэктомии (χ2=0,231, р<0,01). Выявлено, что у пациентов с НАЖБП и ЖКБ чаще была диагностирована ишемическая болезнь сердца (у 25% лиц основной группы и у 9,47% - группы сравнения, χ2=7,83, р<0,01, rs=0,207, р<0,01). Большая распространенность сердечно-сосудистых заболеваний (ССЗ) была отмечена у лиц с ЖКБ, перенесших холецистэктомию (rs=0,258, р<0,01). Также установлено, что при коморбидном течении НАЖБП и ЖКБ характерным было наличие сопутствующего сахарного диабета 2 типа, более высоких значений у-глутамилтрансферазы и липопротеидов низкой плотности (р<0,01). Достоверно чаще были зафиксированы прогрессирующие стадии фиброза печени (F2-3) у пациентов с НАЖБП и ЖКБ, при этом стадия фиброза имела положительную достоверно значимую взаимосвязь с холецистэктомией (rs=0,366, р≤0,01), что говорит об увеличении риска прогрессирующего течения НАЖБП после удаления желчного пузыря. В целом для пациентов с НАЖБП и ЖКБ были характерны высокие значения инсулина, лептина и более низкие значения адипонектина. Установлено, что у лиц с сохраненным желчным пузырем уровень лептина сопоставим с таковым у пациентов, страдающих НАЖБП без ЖКБ, а после перенесенной холецистэктомии отмечен скачкообразный, более чем двукратный рост уровня лептина по сравнению с лицами с ЖКБ до операции.
Для того, чтобы оценить влияние рассматриваемых патологий на уровень риска развития фатальных ССЗ, проведена оценка риска по шкале SCORE 2019 г. в группах сравнения. В подгруппе пациентов с коморбидным течением и проведенной холецистэктомией выявлена достоверно большая доля лиц с высоким уровнем риска ССЗ в течение следующих 10 лет.
Таким образом, коморбидное течение НАЖБП и ЖКБ имеет клинико-лабораторные особенности. Постхолецистэктомическое течение ЖКБ у пациентов с НАЖБП характеризуется повышением кардиоваскулярного риска и прогрессированием фиброза печени.
Фармакотерапия при НАЖБП и ЖКБ.
Для профилактики развития кардиоваскулярных заболеваний у пациентов с НАЖБП и ЖКБ необходимо использовать патогенетически обоснованную и высокоэффективную терапию. Урсодезоксихолевая кислота (УДХК) обладает мощным литолитическим эффектом и является препаратом первого выбора у пациентов с ЖКБ. Имеются неоспоримые данные о том, что монотерапия УДХК при лечении НАЖБП от 5 до 24 мес.достоверно снижает клинико-биохимическую активность заболевания и выраженность фиброза. В исследовании с участием 207 пациентов с НАЖБП, которые имели признаки раннего атеросклероза, было обнаружено, что прием УДХК в дозе 15 мг на 1 кг массы тела привел к статистически значимому уменьшению стеатоза печени (оценивался по индексу FLI) и толщины комплекса интима-медиа, это позволяет говорить о самостоятельном гиполипидемическом эффекте УДХК, который реализуется через уменьшение инсулинорезистентности и повышение уровня аполипопротеина А1 (липопротеида высокой плотности).
В 2019 г. впервые в России и в мире была зарегистрирована фиксированная комбинация ГК и УДХК (Фосфоглив® УРСО) в форме капсул, содержащих действующие вещества в количестве 35 мг и 250 мг соответственно. Учитывая его более выраженный плейотропный эффект в сравнении с монотерапией УДХК, препарат используют в лечении пациентов с сочетанной патологией - функциональными расстройствами, билиарным сладжем и НАЖБП. Препарат показал хорошую переносимость и минимальное количество побочных эффектов.
Недостатком известных способа диагностики и лечения является тот факт, что в нем оценка риска производится с точки зрения возможности развития фатальных сердечно сосудистых заболеваний, а не с точки зрения оценки возможности эффективного совместного неинвазивного лечения сочетанных болезней - ЖКБ и НАЖБП и прогнозирования исходов обоих заболеваний с учетом коморбидности пациента.
Задачей является обеспечение возможности прогнозирования эффективности совместного неинвазивного лечения сочетанных болезней - НАЖБП и ЖКБ.
Поставленная задача решается тем, что в способе прогнозирования эффективности литолиза на основе диагностики желчнокаменной болезни в сочетании с неалкогольной жировой болезни печени, включающей проведение лабораторных исследований с определением индекса инсулинорезистентности НОМА, индекса CIRS-G, и инструментальных исследований с выполнением мультиспиральной компьютерной томографии без контрастирования, в процессе которой определяют размер и плотности желчных камней, затем рассчитывают плотность камней по шкале Хаунсфилда (HU), после чего на основании данных показателей прогнозируют эффективность литолиза (Р), по математической формуле:
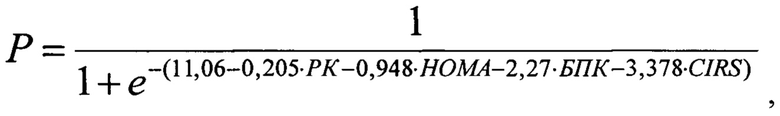
где: Р - вероятность наступления события, РК - размер желчного камня в мм, НОМА - индекс инсулинорезистентности, БПК - большая плотность камня (1 - более или равно 100 HU, 0 - менее 100 HU), CIRS-G- индекс коморбидности в баллах, рассчитывают значение Р и при значении P>0,5 прогнозируют эффективность литолиза для выбора консервативного метода лечения.
Определение для пациента прогноза для выбора метода лечения при диагностике желчнокаменной болезни в сочетании с неалкогольной жировой болезни печени, включающей проведение лабораторных исследований с определением индекса инсулинорезистентности НОМА, индекса CIRS-G, в совокупности с дальнейшим проведением инструментальных исследований в виде проведения без контрастирования мультиспиральной компьютерной томографии (МСКТ) для визуализации всех отделов желчного пузыря и желчных путей, определения размеров, структуры и формы камней с выполнением при этом также определения размера и плотности желчных камней и с последующим расчетом плотности камней по шкале Хаунсфилда (HU), дает возможность по данным расчетных индексов при статистической обработке полученных данных прогнозировать эффективность литолиза с помощью приведенной выше формулы обеспечивает возможность достаточно просто и доступно рассчитать соотношение шансов с учетом данных конкретного пациента эффективность возможного проведения его литолитической терапии и выбрать метод лечения.
Технический результат - обеспечение возможности прогнозирования эффективного совместного неинвазивного лечения сочетанных болезней - ЖКБ и НАЖБП. иагностики.
Заявляемый способ обладает новизной в сравнении с прототипом, отличаясь от него такими существенными признаками как расчет для пациента при проведении неинвазивной диагностики фиброза и стеатоза печени в виде лабораторных исследований: индекса инсулинорезистентности НОМА, индекса коморбидности Чарльсона и индекса CIRS-G, определение при проведении инструментальных исследований выполнение МСКТ без контрастирования и при ее выполнении определение плотности и размера желчных камней, размера и толщины стенки желчного пузыря, плотности и размера печени и поджелудочной железы и подсчет плотности по шкале Хаунсфилда (HU), составление на основании полученных показателей математической формулы для расчета прогностической модели литолиза:
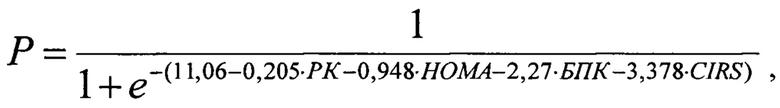
где: Р - вероятность наступления события, РК - размер желчного камня в мм, НОМА - индекс инсулинорезистентности, БПК - большая плотность камня (1 - более или равно 100 HU, 0 - менее 100 HU), CIRS-G - индекс коморбидности в баллах, расчет значения Р и прогнозирование при значении р>0,5 эффективности литолиза для выбора консервативного метода лечения, обеспечивающими в совокупности достижение заданного результата.
Хотя сами по себе известны отдельные отличительные существенные признаки, такие как расчет сывороточных тестов, в т.ч. индекса инсулинорезистентности НОМА, индекса коморбидности CIRS-G, выполнение МСКТ, однако их совокупное указанное выше использование, обеспечивающее возможность прогноза эффективности сочетанного лечения НАЖБП и ЖКБ с помощью прогностической модели, оформленной в виде калькулятора формулы, заявителю неизвестно, поэтому он считает, что заявляемый способ прогнозирования эффективности литолиза соответствует критерию «изобретательский уровень».
Заявляемый способ может найти широкое применение в медицине, в частности, в гастроэнтерологии и потому соответствует критерию «промышленная применимость».
Изобретение иллюстрируется чертежами, где представлены на:
- фиг. 1 - дизайн исследования;
- фиг. 2 - снимок УЗИ пациента с ЖКБ 1 стадии;
- фиг. 3 - снимки УЗИ пациента с ЖКБ 4 стадии;
- фиг. 4 - снимки МСКТ пациентов со слабоконтрастными конкрементами желчного пузыря;
- фиг. 5 - снимки МСКТ пациентов с рентгеноконтрастными конкрементами желчного пузыря;
- фиг. 6 - протокол эластометрии на аппарате FibroScan 502 TOUCH XL пациента с ЖКБ.
- фиг. 7 - таблица 1 «Показатели размера желчного камня (РК), и плотности камня (ПК) в группах»;
- фиг. 8 - таблица 2 «Результаты множественной логистической регрессии»;
- фиг. 9 - Кривая ROC;
- фиг. 10 - Образец таблицы с расчетом вероятности литолиза у пациентов с ЖКБ;
- фиг. 11 - Снимки УЗИ пациентки П. до и после лечения;
- фиг. 12 а, б - Снимки МСКТ пациентки П. до и после лечения;
- фиг. 13 а, б - Протоколы эластометрии пациентки П. до и после лечения;
- фиг. 14а, б - Снимки МСКТ пациента Б. до и после лечения;
- фиг. 15а, б - Снимки пациентки Н. до и после лечения;
Заявляемый способ заключается в следующем.
На основе диагностики желчнокаменной болезни в сочетании с неалкогольной жировой болезни печени, включающей проведение лабораторных исследований инструментальных исследований, определяют индекс инсулинорезистентности НОМА, индекс CIRS-G, и выполняют мультиспиральную компьютерную томографию (MKT) без контрастирования. В процессе MKT определяют размер и плотности желчных камней, затем рассчитывают плотность камней по шкале Хаунсфилда (HU). После этого на основании данных показателей прогнозируют эффективность литолиза (Р), по математической формуле:
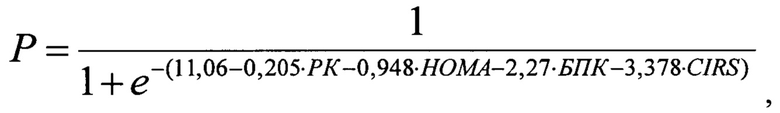
где: Р - вероятность наступления события, РК - размер желчного камня в мм, НОМА - индекс инсулинорезистентности, БПК - большая плотность камня (1 - более или равно 100 HU, 0 - менее 100 HU), CIRS-G - индекс коморбидности в баллах,
рассчитывают значение Р и при значении р>0,5 прогнозируют эффективность литолиза для выбора консервативного метода лечения».
На практике способ осуществляют следующим образом.
Вначале проводят диагностику лечения желчнокаменной болезни в сочетании с неалкогольной жировой болезнью печени. Диагностика включает в себя сбор анамнеза, выполнение объективного физикального обследования, проведение лабораторных исследований, проведение инструментальных исследований, включающих в себя ультразвуковое исследование брюшной полости, проведение мультиспиральной компьютерной томографии (МСКТ), эластометрию печени, статистическую обработку материалов обследования, установление диагноза сочетания НАЖБП и ЖКБ на основании клинической картины, данных лабораторных и инструментальных исследований и расчетных индексов в зависимости от диагноза при показаниях к литолитической терапии и назначение ее пациенту в виде диетотерапии и курса пероральной литолитической терапии.
При этом лабораторные исследования включают в себя обязательные анализы, такие как. клинический анализ крови, биохимическое исследование крови (общий билирубин и фракции, общий белок, глюкоза, амилаза, АЛТ, ACT, ЩФ, ГГТП), ВИЧ, СОЭ, вирусные маркеры гепатитов (HBsAg; анти-HCV), исследование липидного спектра крови с определением коэффициента атерогенности (ХС липопротеинов высокой плотности, ХС липопротеинов низкой плотности, триглицериды). Также для пациента рассчитывают сывороточные тесты неинвазивной диагностики фиброза и стеатоза печени: индексы фиброза печени APRI и FIB4, индекс стеатоза печени FLI, индекс инсулинорезистентности НОМА, индекс коморбидности Чарльсона и индекс CIRS-G.
При проведении инструментальных исследований выполняют УЗИ брюшной полости, обеспечивающее визуализацию отделов желчного пузыря, желчных путей, определяют наличие желчных камней, размеры желчного пузыря, толщину стенки желчного пузыря, эхогенность желчи, размеры печени и ее структуру, размеры и структуру поджелудочной железы, а также наличие сопутствующих заболеваний. Также с помощью технологии Vibration-controlled Transientelastography (VCTE) с ультразвуковым датчиком с частотой 3,5 МГц на глубине от 25 до 65 мм в децибелах на метр проводят эластометрию печени на аппарате FibroScan 502 TOUCH с ультразвуковым датчиком XL и с программным обеспечением САР с определением степени фиброза и стеатоза. МСКТ проводят без контрастирования и при ее выполнении определяют плотность и размер желчных камней, размер и толщину стенки желчного пузыря, плотность и размер печени и поджелудочной железы. Также производят подсчет плотности по шкале Хаунсфилда (HU), которая является количественной шкалой денситометрических показателей рентгеновской плотности и шкалой линейного ослабления излучения по отношению к дистиллированной воде, рентгеновская плотность которой принята за 0 HU (при стандартных давлении и температуре).
Выполняют статистическую обработку полученных материалов обследования, после чего производят окончательное определение фиброза печени по данным эластометрии и по данным расчетных индексов и устанавливают диагноз ЖКБ и НАЖБП на основании клинической картины, данных лабораторных и инструментальных исследований и расчетных индексов..
При статистической обработке также производят прогнозирование эффективности литолиза с помощью метода простой логистической регрессии, показывающей связь между наступлением литолиза и потенциальными предикторами и пошаговой множественной логистической регрессии, как метода подгонки регрессионных моделей с помощью автоматического выбора предикторов путем построения ROC кривой, в которую в качестве предикторов включены переменные: РК, НОМА, БПК, возраст, ССЗ, ЭЗ, ЗП, пол пациента, НАЖБП, оказывающие наибольшее влияние на исход и отобранные в ходе простой логистической регрессии. Подставляют данные пациента в оформленную в виде калькулятора формулу расчета прогностической модели литолиза:
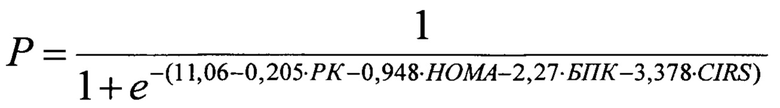
где: Р - вероятность наступления события (литолиза), РК - размер желчного камня в мм, НОМА - индекс инсулинорезистентности, БПК - большая плотность камня (1 - более или равно 100 HU, 0 - менее 100 HU), CIRS-G - индекс коморбидности в баллах.
Рассчитывают значение Р и при значении р>0,5 считают литолиз эффективным. После этого назначают литолитическую терапию с помощью УДХК. Отбирают пациентов налитолитическую терапию с учетом рассчитанного для них значения Р>0,5, когда литолиз становится возможен (чувствительность метода 83,9%, специфичность 82,8%, AUC 0,918 [0,867; 0,969]). Назначают пациенту лечение в виде диетотерапии и курса пероральной терапии урсодезоксихолевой кислоты (УДХК) в дозе 10-15 мг/кг/сут. Также в процессе литолитической терапии применяют курсы препаратов, рекомендованных для лечения желчнокаменной болезни при сочетании с неалкогольной жировой болезнью печени: спазмолитики (мебеверин, гимекромон, тримебудин), ингибиторы протонной помпы, ферменты, антибиотики, пробиотики и пребиотики. Курс лечения составляет 12 месяцев.
На практике заявляемый способ диагностики и лечения осуществлялся следующим образом.
Клиническая характеристика исследуемых групп.
В скрининге участвовало всего 125 человек, в связи с наличием критериев исключения, в исследовательскую когорту было отобрано 114 человек, среди которых женщин было 75 человек (65,7%), а количество мужчин составило 39 человек (34,3%). Средний возраст пациентов был 48,4±13,3 лет.
На этапе скрининга все пациенты заполняли стандартизованные опросники по выявлению алкоголизма AUDIT. Для исключения заболеваний печени другой этиологии всем пациентам были проведены исследования крови на маркеры вирусных гепатитов В и С, скрининг на аутоиммунные заболевания печени, были исключены паразитарные заболевания с помощью исследования кала на яйца гельминтов.
При сборе анамнеза отмечалась давность заболевания ЖКБ, наличие наследственности по данному заболеванию у ближайших родственников, давность обнаружения НАЖБП у пациентов с ЖКБ, наличие коморбидных заболеваний у пациента, проводилась оценка пищевого поведения и лекарственного анамнеза. В индивидуальной регистрационной карте отмечались данные в отношении рисков формирования ЖКБ и НАЖБП (СД 2 тип, нарушение толерантности к глюкозе, ожирение, избыток массы тела, окружность талии, артериальная гипертензия и др.). При осмотре пациентов проводились антропометрические замеры с измерением роста (ростомер), массы тела в килограммах (медицинские электронные весы) с расчетом избыточной массы тела (ИМТ) по Кетле по формуле I=m/h2, где I - значение ИМТ, m - масса тела (кг), h - рост (м)., окружности талии и бедер (сантиметровая лента). Использовались стандартные рекомендованные методы перкуссии, пальпации и аускультации при физикальном обследовании пациентов. После проведенного обследования пациенты были разделены на группы сравнения. Критерием распределения на группы было наличие у пациентов НАЖБП. Основную группу составили пациенты с ЖКБ в сочетании с НАЖБП (65 человек), группой сравнения была группа пациентов с ЖКБ без НАЖБП (49 человек).Обе группы были разделены на подгруппы:
1 подгруппа - пациенты с наличием желчных камней плотностью менее 100 единиц Хаунсфилда, определяемой по данным MCKT(HU). В первой группе-31 человек, во второй группе- 30 человек.
2 подгруппа - пациенты с наличием желчных камней плотностью более 100 HU. В первой группе - 34 человека, во второй группе 19 человек.
Методы исследования.
Клинико-лабораторные методы исследования.
Материалом для общего анализа крови и биохимических анализов крови была венозная кровь, взятая из локтевой вены натощак. Пробирки с кровью транспортировали в клинико-диагностическую лабораторию ООО «Многофункциональный Центр (МЦ) «Лотос». Транспортировка крови производилась в специальных контейнерах для биоматериалов в течение 2 часов с соблюдением холодовой цепи. Для проведения исследования общего анализа крови использовался гематологический автоматический анализатор CELL-DYN Ruby США, СОЭ метр VACUETTE SRS 20/11 Австрия. Для подсчета мазков крови использовался микроскоп цифровой Olympus СХ 31, Япония. В общем анализе крови определяли уровни гемоглобина, лейкоцитов, тромбоцитов, лейкоцитарную формулу крови, СОЭ. Для проведения биохимического исследования крови использовался иммуно-хемилюминесцентный анализатор «Architect i4000 SR. Биохимические анализы крови включали: исследование уровня аспартатаминотрансферазы (ACT), аланина-минотранферазы (АЛТ), гаммаглютамилтранспептидазы (ГГТП), амилазы, общего билирубина, глюкозы, инсулина, общего холестерина, триглицеридов, липопротеинов низкой плотности (ЛПНП), липопротеинов высокой плотности (ЛПВП) сыворотки крови. Индекс инсулинорезистентности HOMA-IR (Homeostasis Model Assessment of Insulin Resistance) рассчитывался по формуле: HOMA-IR = концентрация глюкозы (ммоль/л) * уровень инсулина (мкЕД на 1 мл)/22,5. За норму принимались значения HOMA-IR для взрослых без диабета от 0 до 2,7. Индекс атерогенности рассчитывался по формуле: (ОХС-ЛПВП)/ЛПВП.
Всем пациентам были рассчитаны сывороточные тесты неинвазивной диагностики фиброза и стеатоза печени. Индекс фиброза печени APRI рассчитывался по формуле: APRI=ACT*100/[(верхний предел ACT) × тромбоциты (109/л)]. Известно, что, индекс APRI, превышающий 1,0, имеет чувствительность 76% и специфичность 72% для прогнозирования цирроза печени, APRI, превышающий 0,7, имеет чувствительность 77% и специфичность 72% для прогнозирования значительного (F2-F3 по Metavir)) фиброза печени [23]. Индекс фиброза FIB 4 рассчитывался по формуле: FIB4=(Возраст × ACT)/(Количество тромбоцитов × (квадратный корень из АЛТ)). Для НАЖБП оценка по шкале FIB-4<1,30 соответствует F0 - F1 по Metavir, оценка по шкале FIB-4>2,67 соответствует F3 - F4 по Metavir.
Для оценки стеатоза печени авторы использовали индекс FLI, являющийся маркером НАЖБП и включающий показатели ИМТ, окружность талии, уровень триглицеридов и ГГТП сыворотки крови. Индекс FLI рассчитывался по логарифмической формуле. Индекс FLI (Fatty Liver Index)=(e0,953×loge (ТГ) + 0,139×(ИМТ) + 0,718×loge (ГГТП) + 0,053×(ОТ) - 15,745)/(1 + e0,953×loge (ТГ) + 0,139×(ИМТ) + 0,718×loge (ГГТП) + 0,053×(ОТ) - 15,745)×100, где ТГ - триглицериды, ИМТ - индекс массы тела, ГГТП - гаммаглутамилтранспептидаза, ОТ - окружность талии. Значение FLI менее 30 указывает на отсутствие стеатоза, при значениях 30-60 стеатоз возможен и требуется дальнейшее обследование, более 60 с вероятностью 78% указывает о наличии НАЖБП.
Коморбидность среди пациентов с ЖКБ авторами была рассчитана с помощью индексов коморбидности Чарльсона и индекса CIRS-G, которые являются наиболее используемыми методами оценки сопутствующей патологии. Расчеты сопутствующей патологии проводились в графическом интерфейсе Microsoft Excel. Индекс коморбидности Чарльсон представляет собой балльную систему оценки возраста и наличия сопутствующих заболеваний. При его расчете суммируются баллы, соответствующие сопутствующим заболеваниям, а также добавляется один балл на каждую декаду жизни при превышении пациентом сорокалетнего возраста. Риск смерти при отсутствии коморбидности составляет 12%, при 1-2 баллах - 26%, при 3-4 баллах - 52%, а при сумме более 5 баллов - 85%.. Индекс коморбидности более 3 ассоциируется с высоким риском смерти. Система CIRS дает возможность оценивать количество и тяжесть хронических заболеваний в структуре коморбидного статуса пациента и подразумевает суммарную оценку состояния каждой из систем органов, где «0» баллов соответствует отсутствию заболеваний в этой системе органов или наличии патологии, не влияющей на жизнедеятельность, не влияет на прогноз и не требует лечения, «1» - это легкие отклонения от нормы или перенесенные в прошлом заболевания, «2» балла соответствуют заболеванию, при котором необходимо назначение медикаментозной терапии, «3» балла - заболеванию, ставшему причиной инвалидности, а «4» - заболеванию, угрожающему жизни. Пациенты, у которых при расчете сумма составила более 2 баллов по индексу Чарльсон и более 7 баллов по индексу CIRS-G отнесены в группу с высокой коморбидностью, а пациенты, набравшие менее 2 баллов по Чарльсон и менее 7 баллов по CIRS-G отнесены в группу с низкой коморбидностью.
Инструментальные методы исследования.
Инструментальные методы диагностики включали проведение ультразвукового метода исследования брюшной полости на аппарате УЗИ Voluson Е 8 ВТ 15 США, являющимся профессиональной диагностической ультразвуковой системой, которая направляет ультразвуковой пучок в ткани организма и формирует изображения на основе информации, содержащейся в отраженном сигнале. С помощью УЗИ исследования авторы определяли наличие желчных камней, размеры желчного пузыря, толщину стенки желчного пузыря, эхогенность желчи, размеры печени и ее структуру, размеры и структуру поджелудочной железы, а также наличие сопутствующих заболеваний. На фиг. 2 представлены снимки УЗИ у пациента с ЖКБ 1 стадии. На фиг. 3 представлены снимки УЗИ пациента с ЖКБ 4 стадии.
Мультиспиральная компьютерная томография (МСКТ) проводилась на аппарате Philips МХ-8000 IDT-16CT с изотропной системой отображения (0,5 мм толщина сканирования) и генератором 60 Кв 6.5 MHU без применения контрастирования. С помощью МСКТ авторы определяли плотность и размер желчных камней, размер и толщину стенки желчного пузыря, плотность и размер печени и поджелудочной железы. Подсчет плотности проводился по шкале Хаунсфилда (HU), которая является количественной шкалой денситометрических показателей рентгеновской плотности и шкалой линейного ослабления излучения по отношению к дистиллированной воде, рентгеновская плотность которой принята за 0 HU (при стандартных давлении и температуре). Методика МСКТ брюшной полости без контрастирования удобна при обследовании пациентов с сочетанием ЖКБ и НАЖБП, доступна в настоящее время, неинвазивна, имеет чувствительность 88-95% и специфичность 90-95%. Плотность печени пропорциональна степени стеатоза, в норме превышает плотность селезенки на 8-10 HU. Показатели плотности печени, соответствующие степени стеатоза, представлены в таблице (фиг. 8). В случаях выраженного стеатоза (более 30%) плотность сосудов печени равна плотности паренхимы или превышает ее. В норме плотность печени составляет 50-65HU. На фиг. 4-5 представлены снимки МСКТ пациентов с ЖКБ.
Плотность желчного камня определялась в единицах Хаунсфилда (HU). Показатели плотности желчных камней представлены ранее в таблице (фиг. 8).
Эластометрию печени с определением степени фиброза и стеатоза авторы проводили на аппарате FibroScan 502 TOUCH с ультразвуковым датчиком XL, программное обеспечение САР. Показатель САР™ является величиной затухания ультразвука, которая соответствует уменьшению амплитуды ультразвуковых волн при их распространении через ткань печени. Снижение амплитуды ультразвукового сигнала зависит от количества липидных везикул в ткани печени. САР™ руководствуется и приводится в действие сложным процессом, основанным на технологии Vibration-controlled Transient elastography (VCTE™), который гарантирует что: САР™ и эластичность печени измеряются одновременно в том же самом объеме печени, САР™ будет измерен, только если исследование эластичности печени проведено достоверно, САР™ измеряется с помощью датчика M-probe, частота 3,5 МГц на глубине от 25 до 65 мм и выражается в децибелах на метр (дБ/м). Возможности данной методики позволяют верифицировать стеатоз печени на ранних стадиях (S0-S1), когда диагностика при помощи УЗИ затруднена. На фиг. 6 6 представлены протоколы эластометрии пациента с ЖКБ с оценкой степени фиброза и стеатоза печени. Авторами были использованы следующие критерии диагностики НАЖБП: наличие жирового гепатоза по УЗИ брюшной полости, значение расчетного индекса стеатоза FLI более 60, значение плотности печени МСКТ менее 50 HU, значение Сар эластометрии печени более 200. Фиброз печени по данным расчетных индексов (APRI>0,7,FLI>2,5) и данным эластометрии на аппарате FibroSkan с датчиком XL (при средних значениях эластичности печени >7,3 КПа) был выявлен у 14 человек (13%), что соответствует F1-F2 по Metavir. Пациентов с тяжелым фиброзом F3-F4 в когорте не было.
Статистические методы обработки материала.
Статистическая обработка исследования и графический анализ проводились на персональном комьютере с помощью прикладных программы IBMSPSS Statistics 19. При статистической обработке также производили прогнозирование эффективности литолиза с помощью метода простой логистической регрессии, показывающей связь между наступлением литолиза и потенциальными предикторами и пошаговой множественной логистической регрессии, как метода подгонки регрессионных моделей с помощью автоматического выбора предикторов путем построения ROC кривой, в которую в качестве предикторов включены переменные: РК, НОМА, БПК, возраст, ССЗ, ЭЗ, ЗП, пол пациента, НАЖБП, оказывающие наибольшее влияние на исход и отобранные в ходе простой логистической регрессии. Подставляли данные пациента в оформленную в виде калькулятора формулу расчета прогностической модели литолиза:
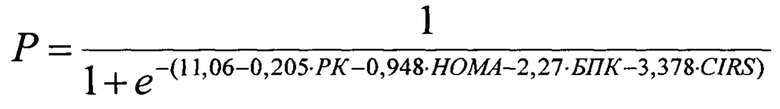
где: Р - вероятность наступления события (литолиза), РК - размер желчного камня в мм, НОМА - индекс инсулинорезистентности, БПК - большая плотность камня (1 - более или равно 100 HU, 0 - менее 100 HU), CIRS-G - индекс коморбидности в баллах. Рассчитывали значение Р.
На всех этапах статистического анализа нулевая гипотеза отвергалась при значениях Р<0,05. Гипотезы о виде распределения проверяли, используя критерии Шапиро-Уилка и Колмогорова-Смирнова с поправкой Лиллиефорса. В большинстве случаев распределение показателей в исследуемых группах было отличным от нормального, поэтому количественные данные представлены в виде медианы (Me) с указанием интерквартильного размаха [P25; P75]. При сравнении двух несвязанных групп использовался критерий Манна-Уитни, который проверяет гипотезу о статистической однородности двух независимых выборок. Для сравнения двух связанных выборок по уровню количественного признака использовался непараметрический статистический критерий Уилкоксона, позволяющий оценить различия между рядами измерений, выполненной для одной и той же совокупности исследуемых, но в разных условиях (до и после лечения). Для сравнения групп по признакам, выраженным в номинальной шкале использовался Xu2 критерий Пирсона. Корреляционный анализ Спирмена использовался для оценки взаимосвязи между исследуемыми показателями и установления связи с помощью количественного коэффициента. Для прогнозирования вероятности возникновения литолиза у пациентов с ЖКБ авторы использовали метод логистической регрессии. Простая логистическая регрессия позволила рассчитать отношение шансов по каждому из множества признаков. Для составления прогностической модели эффективности литолиза авторами был использован метод пошаговой множественной логистической регрессии как метод подгонки регрессионных моделей, в котором выбор прогностических переменных осуществляется с помощью автоматической процедуры. На каждом шаге программа добавляет новую переменную из набора объясняющих переменных. Для оценки модели логистической регрессии использовали анализ ROC-кривой. ROC-кривая, построенная на основе спрогнозированной для каждого объекта вероятности исхода, показывает зависимость количества верно классифицированных положительных исходов от количества неверно классифицированных отрицательных исходов. Площадь под кривой (AUC) показывает численное значение клинической значимости теста. Значение AUC от 0,9 до 1 соответствует отличной дискриминирующей способности модели, от 0,9 до 0,8 - очень хорошей, от 0,8 до 0,7 - хорошей, от 0,7 до 0,6 - средней, от 0,5 до 0,6 - неудовлетворительной способности.
Рассчитывали значение Р и при значении р>0,5 назначали литолитическую терапию с помощью УДХК. Отбирали пациентов на литолитическую терапию с учетом рассчитанного для них значения Р>0,5, когда литолиз становится возможен (чувствительность метода 83,9%, специфичность 82,8%, AUC 0,918 [0,867; 0,969]).
Диагностическая чувствительность показывает процент истинно положительных результатов литолиза у лиц, имеющих ЖКБ. Диагностическая специфичность показывает процент лиц, не имеющих положительного результата у лиц с ЖКБ, и модель это предсказала. Предсказательная значимость положительного исхода устанавливается по отношению полученного количества положительных результатов к общему числу положительных результатов.
Результаты исследования:
Клиническая характеристика пациентов с ЖКБ в группах, коморбидность, факторы кардиометаболического риска.
Исследовательская когорта в соответствии с критериями включения составила 114 человек, среди которых 75 женщин (65,7%) и 39 мужчин (34,3%). Средний возраст пациентов составил 48,4±13,3 лет. Авторами был проанализирован возрастно-половой состав групп, длительность заболевания ЖКБ в группах, факторы риска ЖКБ (неправильное питание, наследственность по ЖКБ, инсулинорезистентность, наличие неалкогольного стеатогепатита (НАСГ), ожирение), сопутствующая патология: заболевания сердечно-сосудистой системы (гипертоническая болезнь, ИБС, атеросклероз), эндокринной системы (аутоиммунный тиреоидит, гипотиреоз, гипертиреоз, ожирение, нарушение гликемии натощак), заболевания почек и мочевыделительной системы (мочекаменная болезнь, хронический пиелонефрит, хронический цистит), заболевания органов пищеварения (хронический гастрит, гастроэзофагеальная рефлюксная болезнь, язвенная болезнь желудка и двенадцатиперстной кишки, хронический неинфекционный колит, хронический панкреатит). Характеристика пациентов представлена в таблице 9. При анализе пола пациентов двух групп выявлено статистически не значимое преобладание женщин в обеих группах (65,7 и 74,3%) над мужчинами (35,3 и 26,5%). Наследственность по ЖКБ достоверно чаще встречалась в 1 группе (58,5%), в отличие от второй (30,6%), р=0,03. Ожирение (56,9%) и инсулинорезистентность (66,2%) существенно преобладали в группе с НАЖБП в отличие от 2 группы (4,1 и 36,7% соответственно) р<0,001.
Дислипидемия и нарушение гликемии натощак достоверно чаще (р<0,05) встречались в 1 группе 89,2% и 43% соответственно, в отличие от пациентов 2 группы - 63,3 и 14,2% соответственно. Артериальная гипертензия преобладала в 1 группе (78,4%), в отличие от 2 группы (22,4%) р=0,001. Ожирение зафиксировано у 56,9% в группе сочетания ЖКБ и НАЖБП, что значительно больше, чем в группе с ЖКБ (4,1%) р<0,001. Пациенты первой группы также достоверно чаще имели большую ОТ (73,8%), чем в группе без НАЖБП (8,1%) р<0,001.
Всем пациентам были рассчитаны индексы фиброза (FIB 4, APRI). Значения у всех пациентов индекса APRI было менее 1, индекса FIB 4 менее 1,3, что соответствует значениям F0 - Fl по Metavir или находились в «серой зоне». Индекс стеатоза печени-FLI, выше 60 зафиксирован у 65 пациентов. НАЖБП была диагностирована у 65 пациентов с ЖКБ (48%) по наличию хотя бы 2 критериев. Фиброз печени по данным расчетных индексов (APRI>0,7,FLI>2,5) и данным эластометрии на аппарате FibroSkan с датчиком XL (при средних значениях эластичности печени >7,3 КПа) был выявлен у 14 человек (13%), что соответствует F1-F2 по Metavir. Пациентов с тяжелым фиброзом F3-F4 в когорте не было.
Был выполнен проспективный анализ влияния терапии УДХК на биохимические маркеры, рентгенологические показатели желчного камня, показатели стеатоза и фиброза печени. Результаты мониторинга биохимических и инструментальных показателей в группах у пациентов до и после лечения.
Все пациенты с ЖКБ в течение года принимали препарат УДХК 15 мг/кг, а также получали лечение по поводу сопутствующей патологии ЖКТ курсами в течение года (спазмолитики, ферменты, пробиотики, ингибиторы протонной помпы) по потребности. Динамика общеклинических и биохимических показателей крови, индексов фиброза и стеатоза, рентгенологические параметры желчного камня и плотности печени оценивалась после лечения.
В результате анализа полученных лабораторных данных авторы получили показатели Me статистически значимые различия в группах (значимость Манна-Уитни, р<0,05) были достигнуты при сравнении уровней ACT, АЛТ, ГГТП, общего холестерина, ТГ, ЛПНП, глюкозы, НОМА индекса. Оценка биохимических показателей в группах проводилась до лечения и после завершения литолитической терапии. Статистически значимые различия до и после лечения (критерий Уилкоксона р<0,05) были получены для показателей: ACT, АЛТ, общий билирубин, амилаза, ГГТП, ОХС, ЛПНП, ЛПВП, НОМА индекс.
В группе 1 показатели ГГТП, глюкозы, НОМА индекса, ЛПНП, ТГ, АЛТ были статистически значимо выше до и после лечения по сравнению со 2 группой. После лечения в обеих группах снижались показатели НОМА индекса, ЛПНП, ТГ, ОХС, ГГТП и ACT (р<0,001).
Размер камня достоверно уменьшался во второй группе (Me снизилась от 7 до 0,1 мм), р=0,001, в отличие от первой, где динамика была минимальной (Ме=8,1-8,0 мм). Плотность камня также достоверно уменьшалась на фоне проводимого лечения во 2 группе (Me снизилась от 85 до 35 HU) при р=0,002, различия в 1 группе были статистически не значимы. Показатели плотности печени были изначально различны в группах (Ме=44 в 1 группе и 56 во второй) р<0,001, что объясняется тем, что при наличии стеатоза в печени происходит снижение ее плотности по шкале Хаунсфилда в связи с повышением количества липидных везикул. После проведенного лечения плотность печени повышались и обеих группах. В 1 группе Me увеличиласьот 44 до 48 HU р<0,001, во 2 группе Me от 56 до 58 HU при р=0,024. Это свидетельствует о регрессе стеатоза и уменьшении количества липидных везикул в печени. Индекс фиброза FIB 4 был различен в группах до лечения (Ме=1,03 и 0,89 соответственно) р=0,022, после лечения он снизился в обеих группах: в 1 группе до 0,98 р=<0,001, во 2 группе до 0,8, р=0,007. Индекс стеатоза FLI был существенно выше в 1 группе в отличие от второй (Ме=69 и 28 соответственно), при р=0,001, также наблюдалось его снижение после лечения во 2 группе до Ме=20, р<0,001, а в 1 группе снижения авторы не увидели (Ме=70, р<0,001). Показатели эластометрии печени S(c1B/m) достоверно различались в группах: в 1 группе Ме=305 dB/м, во 2 группе Ме=167 dB/м, р=0,050, после лечения показатели эластометрии достоверно снизились: в 1 группе Ме=243 dB/м, р<0,001, различия во 2 группе были статистически не значимы.
Оценка рентгенологических параметров желчных камней в группах.
Характеристики размера и плотности желчного камня оказывают влияние на эффективный литолиз, поэтому авторы оценили эти показатели в группах. В группе ЖКБ преобладали камни до 10 мм в 73,5% случаев, в отличие от группы ЖКБ+НАЖБП, где камни малого размера встречались в 56,9% случаев, камни малой плотности чаще встречались также в 1 группе (41,5%), но различия не были статистически з значимыми. Сочетание мелких камней с малой плотностью является благоприятным для проведения литолиза. Это сочетание в группах было примерно одинаково (43,1 и 46,9% соответственно). Таким образом, пациенты обеих групп имеют равный шанс на литолиз по данным характеристики камня. Характеристики желчного камня в группах представлены в таблице (фиг. 7).
При размере камня менее 10 мм процент литолиза составил 82,1%, в отличие от пациентов с камнями более 10 мм, где литолиз был эффективен только в 17,9% случаев (р<0,001). При плотности желчного камня более 100 HU литолиз состоялся в 19% случаев, а при низкой плотности (менее 100 HU) в 80,4%, при р<0,001. Обнаружено, что у пациентов с высоким индексом коморбидности преобладает большая плотность камня (50,9%) в отличие от лиц без коморбидности (28,8%) р<0,001, инсулинорезистентность также превалирует (66,7%) в отличие от группы без коморбидности (29,8%) р=0,023, чаще встречается НАЖБП в 75,4% случаев, в группе без коморбидности в 38,6%, р=0,001. Литолиз оказался более эффективен в группе без коморбидности в 71,4% случаев в отличие от группы с коморбидностью в 29,3% случаев, р<0,001.
Авторы определили, что наиболее значимые корреляционные взаимодействия были между НОМА индексом и плотностью печени (r=0,440), ИМТ (r=0,430), окружностью талии (r=0,400), коморбидностью (r=0,453), глюкозой крови (r=0,570), размером камня (r=0,358). Также статистически значимо коррелировали между собой коморбидность и возраст пациента (r=0,511), окружность талии (r=0,425), размер камня (r=0,308), индекс фиброза FIB 4 (r=0,360).
Прогностическая модель эффективности литолиза при ЖКБ, логистическая регрессия, рекомендации для использования математической модели в практической медицине.
Для выявления связи между зависимой дихотомической переменной (наступление литолиза) и потенциальными предикторами авторы использовали простую логистическую регрессию, позволяющую оценить статистически значимые предикторы. Степень влияния предиктора на исход оценивалась по отношению шансов (ОШ). Все предикторы являлись статистически значимыми и между ними и зависимой переменной наблюдалась обратная связь, авторы рассчитали величину, обратную ОШ (1/ОШ). регрессия позволяет оценить влияние каждого предиктора на исход при фиксированном значении других предикторов. Кроме перечисленных признаков, в первую модель был включен CIRSG, а во вторую Чарльсона.
На основании отобранных моделью предикторов: HOMA-IR, значениях размера и плотности камня и индекса коморбидности авторы сформировали систему расчета для помощи практикующим врачам в принятии решения в отношении консервативного лечения ЖКБ.
Результаты проведения пошаговой множественной логистической регрессии и представлены в таблице (фиг. 8).
Примечание: РК - размер желчного камня в мм, НОМА - индекс инсулинорезистентности, БПК - большая плотность желчного камня, составляющая 100 и более единиц Хаунсфилда (1 - при ПК≥100 HU, 0 - при ПК менее 100), CIRS-G - индекс коморбидности. Из таблицы (фиг. 8) видно, что если РК увеличится на 1 мм при фиксированных значения других предикторов, то шанс литолиза уменьшается в 1,23 раза. Если НОМА индекс увеличится на единицу, то шанс литолиза уменьшится на 2,58 раза. Если желчный камень будет большой плотности, то шанс литолиза уменьшится в 9,67 раза. При увеличении индекса CIRS-G на один балл шанс литолиза снизится в 29,6 раза. Исходя из полученных данных, авторы составили формулу расчета прогностической модели литолиза:

Примечание: Р - вероятность наступления события, РК - размер желчного камня в мм, НОМА - индекс инсулинорезистентности, БПК - большая плотность камня (1 - более или равно 100 HU, 0 - менее 100 HU), CIRS-G - индекс коморбидности в баллах.
Чувствительность модели составила 83,9%, а специфичность 82,8%, а процент правильно классифицированных 83,3%.
Для оценки качества модели был проведен ROC-анализ. Площадь под кривой была равна 0,918 [0,867; 0,969] при р<0,001, что говорит об отличной дискриминирующей способности модели.
Рассчитывали значение Р и если Р>0,5, то делали вывод, что литолиз произойдет.
Кривая ROC, демонстрирующая чувствительность и специфичность прогностической модели, представлена на фиг. 9.
Таким образом, неблагоприятный прогноз и низкий процент литолиза ожидается у пациентов с большим размером и большой плотностью желчного камня, с инсулинорезистентностью и высоким индексом коморбидности. Таким пациентам будет рекомендована выжидательная тактика, при наличии клинических проявлений или осложеннного течения ЖКБ плановая холецистэктомия, а также коррекция липидного и углеводного обмена, массы тела для улучшения метаболического статуса и снижения рисков развития сердечно-сосудистых заболеваний после холецистэктомии.
Для проверки работы формулы в исследование было включено 42 человека с известным исходом литолиза. У тех, у кого литолиз произошел, модель предсказывала литолиз у 70%, у кого литолиз не произошел, модель у всех предсказывала, что не произойдет (100%). На примере расчетов в группе, набранной для проверки формулы мы можем увидеть, что вероятность наступления события будет различной, в зависимости от исходных данных пациента. Образец расчетной таблицы с формулой представлен в таблице на фиг. 10.
Из таблицы (фиг. 10) видно, например, что у пациента №4 с камнем размером 3 мм, НОМА=1,5, индексом CIRS-G=3 и плотностью камня менее 100 HU литолиз произойдет с вероятностью 90%, а у пациента №8 с размером камня 17 мм, НОМА=3, CIRS-G=5 и плотностью камня более 100 HU литолиза не произойдет с вероятностью 100%.
Клинические случаи.
Пациентка П. 1961 г. обратилась в МЦ «Лотос» с жалобами на тупые боли в правом подреберье после еды, тошноту, горечь во рту, метеоризм, неоформленный стул 1 раз в день. В анамнезе ЖКБ. Хронический кальку л езный холецистит в течение 2 лет, гипертоническая болезнь 2 стадия, дислипилемия, ожирение 1 степени (ИМТ 32). Индекс коморбидности Чарльсон составил 1 балл, CIRS-G 4 балла.
Общее состояние удовлетворительное, кожа чистая. Дыхание везикулярное, хрипов нет. Тоны сердца ритмичные ЧСС 75, АД 140/90. Живот мягкий, болезненный в правом и левом подреберье, печень не увеличена по Курлову 10\ 10\9 см, не выступает из под реберной дуги. Живот вздут, урчит.Стул неоформленный 1 раз в день без примесей.
Из обследования: OAK без изменений, ACT 36 ЕД/л, АЛТ 37 ЕД/л, ГГТП 41 ЕД/л, билирубин общий 20 ммоль/л, глюкоза 5,9 ммоль/л, амилаза 96 ЕД/л, ХС 6,5 ммоль/л, ТГ 1,8 ммоль/л, ЛПНП 3,8 ммоль/л, ЛПВП 1,2 ммоль/л, НОМА индекс 2,0. УЗИ брюшной полости: признаки калькулезного холецистита, мелкие камни желчного пузыря до 8 мм, стеатоз печени, диффузные изменения поджелудочной железы. МСКТ желчного пузыря: стеатоз печени (плотность печени 43 HU), рентгенпозитивных камней не обнаружено (плотность желчи 38 HU), липоматоз поджелудочной железы. Также пациентке была проведена транзиентная эластометрия на аппарате FibroScan 502 TOUCH с ультразвуковым датчиком XL, программное обеспечение САР, по данным которой стеатоз печени составил 306 dB/m, что соответствует 3 степени стеатоза по NAS, а фиброз печени составил 6 КПа, что соответствует фиброзу 1 степени по Metavir. Назначено лечение: гиполипидемическая диета, регулярные физические нагрузки. Проводилось комплексное лечение холецистита включая спазмолитики, ферменты, антибиотики, пробиотики. А также был назначен курс УДХК в дозе 15 м/кг длительностью 12 месяцев. После проведенного лечения самочувствие улучшилось, болей не было, прошли явления диспепсии, нормализовался стул. Из обследования: ACT 27 ЕД/л, АЛТ 16 ЕД/л, ГГТП 31 ЕД/л, билирубин общий 18 ммоль/л, глюкоза 5,2 ммоль/л, амилаза 38, ХС 5,5 ммоль/л, ТГ 1,4 ммоль/л, ЛПНП 2,0 ммоль/л, ЛПВП 1,3 ммоль/л, НОМА индекс 1,5. УЗИ брюшной полости: признаки хронического некалькулезного холецистита, данных за холецистолитиаз нет. По данным МСКТ желчного пузыря: нормализация плотности печени (51 HU), снижение плотности желчи до 25 HU. По данным эластометрии печени: стеатоз печени составил 254 dB/m (2 степень стеатоза), фиброз печени 5,8 Кпа (1 степень фиброза). На фиг. 11 представлены снимки УЗИ пациентки до и после лечения. На фиг. 12 приведены снимки данной пациентки МСКТ до и после лечения. На фиг. 13 представлены протоколы эластометрии.
Таким образом, в данном клиническом случае, авторы показали положительное влияние препарата УДХК на липидный и жировой обмен (нормализация показателей липидограммы, глюкозы крови и НОМА индекса), а также положительный эффект на литолиз мелких желчных камней и степень стеатоза печени на фоне лечения. При расчете прогностической модели литолиза вероятность наступления события составила 0,123.
Пациент Б. 1974. Обратился в МЦ Лотос с жалобами на острые боли в правом и левом подреберье после еды, тошноту, рвоту с желчью по утрам. Болеет ЖКБ в течение 5 лет, обострения 1 раз в год при нарушении диеты. В анамнезе у пациента язвенная болезнь желудка, гипертоническая болезнь 2 стадия, гипотиреоз (компенсированный препаратами тироксина), дислипидемия, ожирение 2 степени (ИМТ 35). Индекс коморбидности Чарльсон составил 3 балла, CIRS-G 8 баллов. Общее состояние удовлетворительное, кожа чистая. Дыхание везикулярное, хрипов нет. Тоны сердца ритмичные ЧСС 75, АД 142/90. Живот мягкий, болезненный в правом и левом подреберье, печень не увеличена по Курлову 10\10\9 см, не выступает из под реберной дуги. Стул оформленный 1 раз в день без примесей. Из обследования: ОХС 7,0 ммоль/л, ЛПНП 3,4 ммоль/л, ТГ 2,5 ммоль/л, ЛПВП 0,9 ммоль/л, ACT 28 ЕД/л, АЛТ 24 ЕД/л, ГГТП 28 ЕД/л, билирубин общий 9 ммоль/л, амилаза 30 ЕД/л, глюкоза 6,3 ммоль/л, НОМА индекс 3,5. МСКТ : микролиты желчного пузыря 3-5 мм плотностью до 150 HU, стеатоз печени (плотность печени 38-43HU), киста печени 11 мм, липоматоз поджелудочной железы. Назначено комплексное лечение холецистита на 4 недели (спазмолитики, холеретики, ферменты, пробиотики), а также препараты УДХК 15 мг/кг сроком на 12 месяцев. После лечения пациент отметил улучшение самочувствия, отсутствие болей и диспепсических явлений. Из обследования: ОХС 5,7 ммоль/л, ЛПНП 3,1 ммоль/л, ТГ 1,9 ммоль/л, ЛПВП 0,98 ммоль/л, ACT 17 ЕД/л, АЛТ 12 ЕД/л, ГГТП 21 ЕД/л, билирубин общий 13 ммоль/л, амилаза 23 ЕД/л, глюкоза 5,1 ммоль/л. НОМА индекс 2,4. По данным МСКТ: сохраняются микролиты желчного пузыря 3-5 мм плотностью до 143 HU, данных за стеатоз нет, липоматоз поджелудочной железы. Из данного клинического случая мы можем сделать вывод о позитивном влиянии лечения на показатели углеводного и жирового обмена и снижение степени стеатоза печени. Полного литолиза желчных камней в данном случае достигнуть не удалось в связи с большой плотностью желчного камня. Снимки МСКТ пациента Б.представлены на фиг. 14. Пациентка Н. 1987 г.р. Обратилась в МЦ Лотос с жалобами на приступообразные острые боли в правом подреберье через 30 минут после еды, тошноту, запоры в течение 3-4 дней. В анамнезе хронических заболеваний не было. Общее состояние удовлетворительное, кожа чистая. Дыхание везикулярное, хрипов нет.Тоны сердца ритмичные ЧСС 68, АД 110/70. Живот мягкий, болезненный в правом и левом подреберье, печень не увеличена по Курлову 10\10\9 см, не выступает из под реберной дуги. Живот вздут, урчит. Стул 1 раз в 3-4 дня. ИМТ 21. Индекс коморбидности Чарльсон 0 баллов, CIRS-G-1 балл. Из обследования: OAK без изменений, ACT 25 ЕД/л, АЛТ 19 ЕД/л, общий билирубин 15 ммоль/л, глюкоза 4,5 ммоль/л, ХС 4,5 ммоль/л, ЛПНП 2,4 ммоль/л, ЛПВП 1,6 ммоль/л, ТГ 0,98 ммоль/л, НОМА индекс 0,96. МСКТ признаки хронического калькулезного холецистита, мелких камней желчного пузыря 3 мм до 53 ед. Назначено лечение, включавшее спазмолитики, пробиотики, лактулозу на 4 недели, и препарат УДХК в дозировке 15 мг/ кг сроком на 12 месяцев. После проведенного лечения болей нет, прошли явления диспепсии, стул нормализовался. Из обследования: ACT 17 ЕД\л, АЛТ 15 ЕД\л, билирубин общий 9 ммоль/л, глюкоза 4,3 ммоль/л, ХС 3,5 ммоль/л, ЛПНП 1,9 ммоль/л, ЛПВП 1,7 ммоль/л, ТГ 0,86 ммоль/л. По данным МСКТ рентгенпозитивных камней не определено. Снимки пациентки Н. представлены на фиг. 15.
В сравнении с прототипом заявляемый способ обеспечивает возможность прогнозирования эффективного совместного неинвазивного лечения сочетанных болезней - ЖКБ и НАЖБП.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ ранней диагностики неалкогольной жировой болезни печени | 2022 |
|
RU2798723C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ СТЕАТОЗА И НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА У ЖЕНЩИН | 2020 |
|
RU2744021C1 |
| Способ диагностики фиброза печени у больных неалкогольной жировой болезнью печени с сахарным диабетом 2 типа | 2019 |
|
RU2732526C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ ПРИ МЕТАБОЛИЧЕСКОМ СИНДРОМЕ | 2018 |
|
RU2686042C1 |
| СПОСОБ НЕИНВАЗИВНОЙ ДИАГНОСТИКИ ФИБРОЗА ПРИ ДИФФУЗНЫХ ЗАБОЛЕВАНИЯХ ПЕЧЕНИ | 2010 |
|
RU2422091C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ У ПАЦИЕНТОВ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ ПРИ НЕДОСТАТОЧНОСТИ ВИТАМИНА D | 2018 |
|
RU2694842C1 |
| Способ лечения неалкогольной жировой болезни печени и сахарного диабета второго типа | 2018 |
|
RU2706026C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ЖЕЛЧЕКАМЕННОЙ БОЛЕЗНЬЮ ПЕРВОЙ СТАДИИ | 2012 |
|
RU2519198C2 |
| Способ коррекции функций печени с неалкогольной жировой болезнью печени | 2023 |
|
RU2838116C1 |
| СПОСОБ ДИАГНОСТИКИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ ПРИ МЕТАБОЛИЧЕСКОМ СИНДРОМЕ | 2022 |
|
RU2803945C1 |





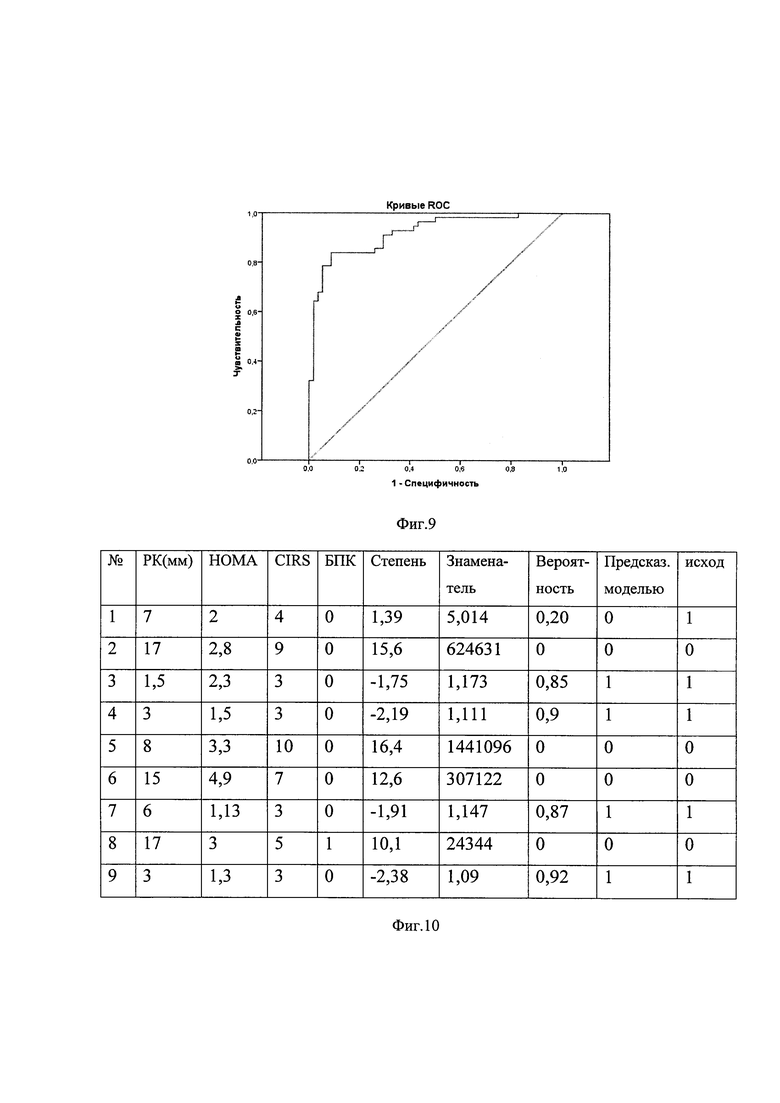
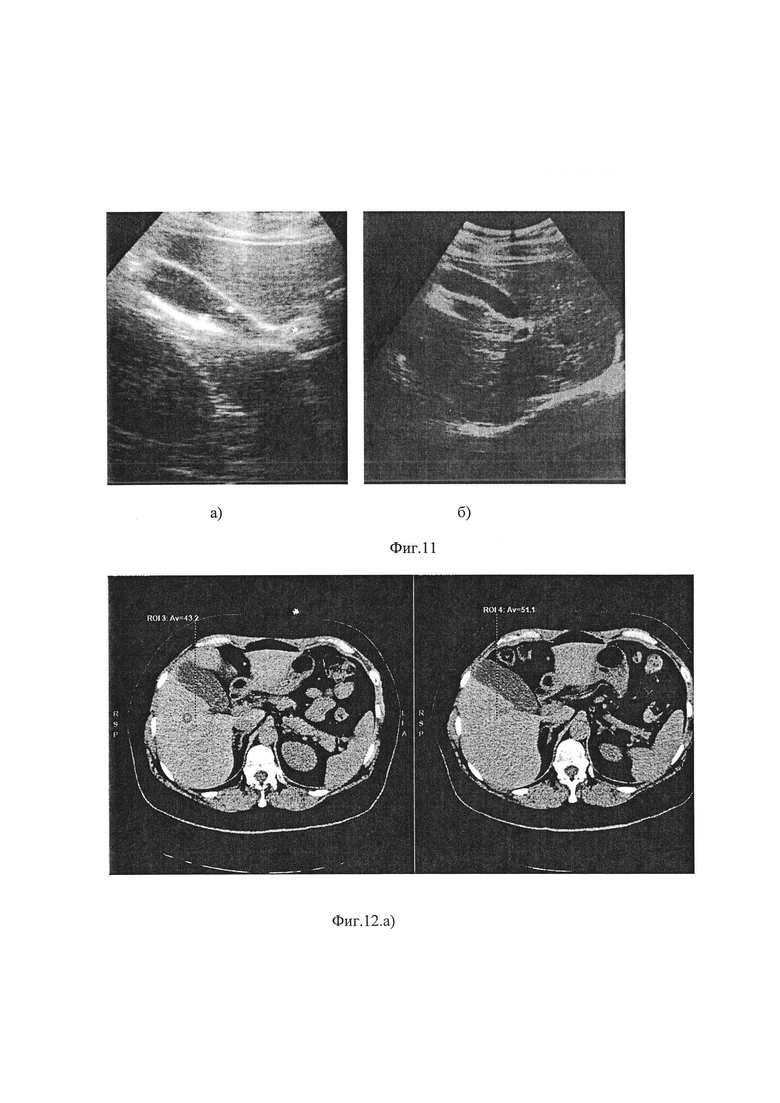

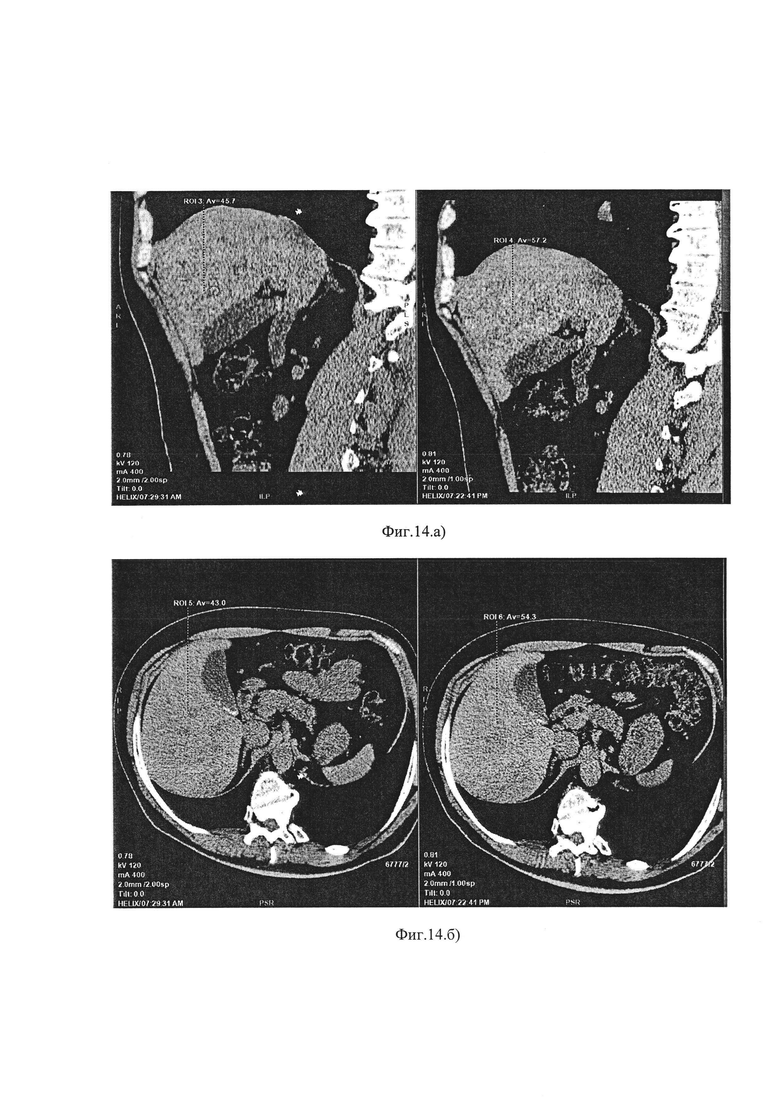

Изобретение относится к медицине, а именно гастроэнтерологии. У пациентов с желчнокаменной болезнью (ЖКБ) в сочетании с неалкогольной жировой болезнью печени (НАЖБП) определяют индекс инсулино-резистентности НОМА, индекс CIRS-G и на основании инструментальных исследований с выполнением мультиспиральной компьютерной томографии без контрастирования определяют размер и плотности желчных камней. Затем рассчитывают плотность камней по шкале Хаунсфилда (HU). После чего на основании данных показателей прогнозируют эффективность литолиза (Р) по математической формуле. И при значении P>0,5 прогнозируют эффективность литолиза для выбора консервативного метода лечения. Способ позволяет, не используя инвазивные средства, до проведения лечения осуществить прогнозирование эффективности литолиза консервативными методами при совместном неинвазивном лечения сочетанных болезней - ЖКБ и НАЖБП. 2 пр., 15 ил.
Способ прогнозирования эффективности литолиза при желчнокаменной болезни в сочетании с неалкогольной жировой болезни печени, включающий диагностику с проведением лабораторных исследований с определением индекса инсулино-резистентности НОМА, индекса CIRS-G и инструментальных исследований с выполнением мультиспиральной компьютерной томографии без контрастирования, в процессе которой определяют размер и плотности желчных камней, затем рассчитывают плотность камней по шкале Хаунсфилда (HU), после чего на основании данных показателей прогнозируют эффективность литолиза (Р) по математической формуле:
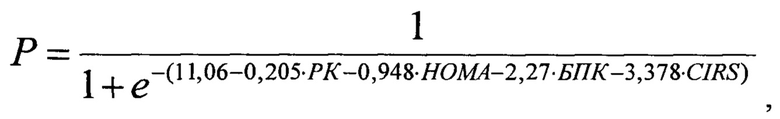
где Р - вероятность наступления события, РК - размер желчного камня в мм, НОМА - индекс инсулино-резистентности, БПК - большая плотность камня (1 - более или равно 100 HU, 0 - менее 100 HU), CIRS-G - индекс коморбидности в баллах, рассчитывают значение Р и при значении P>0,5 прогнозируют эффективность литолиза для выбора консервативного метода лечения.
| Гаус О.В., Ахмедов В.А | |||
| ПРОГНОЗИРОВАНИЕ ЭФФЕКТИВНОСТИ ПЕРОРАЛЬНОЙ ЛИТОЛИТИЧЕСКОЙ ТЕРАПИИ У БОЛЬНЫХ ЖЕЛЧНОКАМЕННОЙ БОЛЕЗНЬЮ, АССОЦИИРОВАННОЙ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ, Современные проблемы науки и образования, 2016, 5, с | |||
| Механический грохот | 1922 |
|
SU41A1 |
| СПОСОБ ПРОФИЛАКТИКИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ У ПАЦИЕНТОВ С ЖЕЛЧНОКАМЕННОЙ БОЛЕЗНЬЮ ПОСЛЕ ЛАПАРОСКОПИЧЕСКОЙ ХОЛЕЦИСТЭКТОМИИ | 2017 |
|
RU2657838C1 |
| СПОСОБ ЛЕЧЕНИЯ ЖЕЛЧНОКАМЕННОЙ БОЛЕЗНИ В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2535150C2 |
| Caroli A, et al, Computed tomography in predicting gall stone | |||
Авторы
Даты
2024-02-06—Публикация
2023-02-15—Подача