Изобретение относится к области медицины, а именно к хирургии и вспомогательным материалам, применяемым при оперативных вмешательствах на различных отделах желудочно-кишечного тракта и других полых органах, требующих наложения швов или анастомозов для увеличения степени герметичности, укрепления травмированных или измененных патологическим процессом стенок, укрытия перфораций и т.п.
Одной из актуальных проблем современной абдоминальной хирургии является несостоятельность межкишечных анастомозов в условиях скомпрометированной кишечной стенки (сдавление спайками, наличие воспалительных изменений как в самой стенки анастомозируемого участка, так и в брюшной полости), перфорации полых органов и т.п. В связи с этим существует множество способов повышения герметичности швов, накладываемых на стенку полого органа: различные варианты ушивания перфораций и техники наложения анастомоза, в том числе и с применением пленочных покрытий для «изоляции» зоны наложения швов. Причем важным является многокомпонентная структура такого изделия, которая позволяет достичь желаемого эффекта засчет слоистого строения. Каждый слой имеет свои особенности и задачи: так, первый слой, прилежащий к стенке органа, обеспечивает высокую адгезию, второй слой – прочность покрытия, а внешний слой – противоспаечное действие.
Наиболее близким является трехслойное раневое покрытие для внутренних органов, в котором первый, прилегающий к ране, слой выполнен из водорастворимого полимера, второй слой – основа – из биодеструктируемого материала, представляющего собой сополимер гликолида с лактидом, а третий, защитный, слой выполнен в виде микрофильтрационной мембраны из алифатического полиамида или полисилоксана, при этом второй слой содержит фармакологический раствор лекарственных веществ, включающий препарат, выбранный из группы антибиотиков – Пефлоксацин (Абактал), также известны модификации данного покрытия с добавлением Контрикала, Фраксипарина, Тромбина [Патент N 2 325 926 Российская Федерация, МПК A61L 15/22 (2006.01), A61F 13/00(2006.01), A61L 15/44 (2006.01), N 2006143093/15, 06.12.2006: опубликовано 10.06.2008.Бюл. № 16 / Шабунин А.В., Лебединский И.Н., Ходателев К.А, Багателия З.А., Тавобилов М.М. — 7 с. : ил. — Текст : непосредственный]. Однако,материалыдля изготовления данного покрытия обладают высокой себестоимостью. Кроме того, полисилоксановый слой обладает низкими биодеградируемыми свойствами, что замедляет процессы регенерации тканей и увеличивает продолжительность расщепления элементов раневого покрытия для внутренних органов.
Техническим результатом изобретения является разработка хирургической полимерной мембраны, обеспечивающей достижение надежного укрепления линии швов анастомоза, отдельных швов в условиях скомпрометированной кишечной стенки и позволяющей снизить вероятность развития их несостоятельности, а также – спаечного процесса в области вмешательства.
Технический результат достигается тем, что хирургическая полимерная мембрана представляет собой трехслойную композицию: первый слой, обращенный к брюшной полости, выполнен из натриевой соли карбоксиметилцеллюлозы, препятствует развитию спаечных сращений в области интереса, второй или основной слой выполнен из медленно биодеградируемого материала – альгинатов натрия и кальция и составляет формообразующую часть пленки, которая может служить матрицей для внесения лекарственных средств (обладающих различным спектром действия), а третий слой, прилегающий к ране, выполнен из водорастворимого полимера – поливинилпирролидона, который обладает высокими адгезивными свойствами.
Изобретение поясняется фигурами:
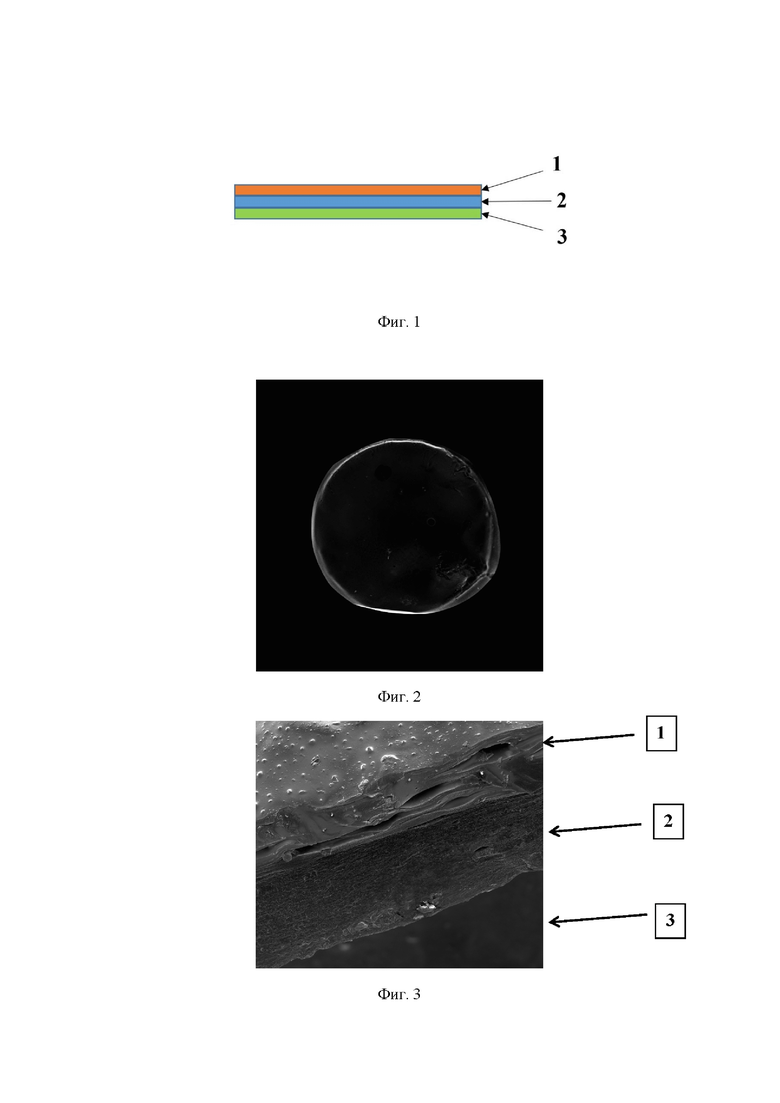
На фиг. 1 изображена схема трехслойного строения хирургической полимерной мембраны;
На фиг. 2 изображена рентгенограмма рентгенконтрастной хирургической полимерной мембраны (с добавлением йогексола);
На фиг. 3 изображена фотография бокового среза хирургической полимерной мембраны, выполненная с помощью сканирующего электронного микроскопа, увеличение 400 крат, отмечается трехслойное строение;
На фиг. 4 изображена хирургическая полимерная мембрана в области межкишечного анастомоза (указана стрелкой);
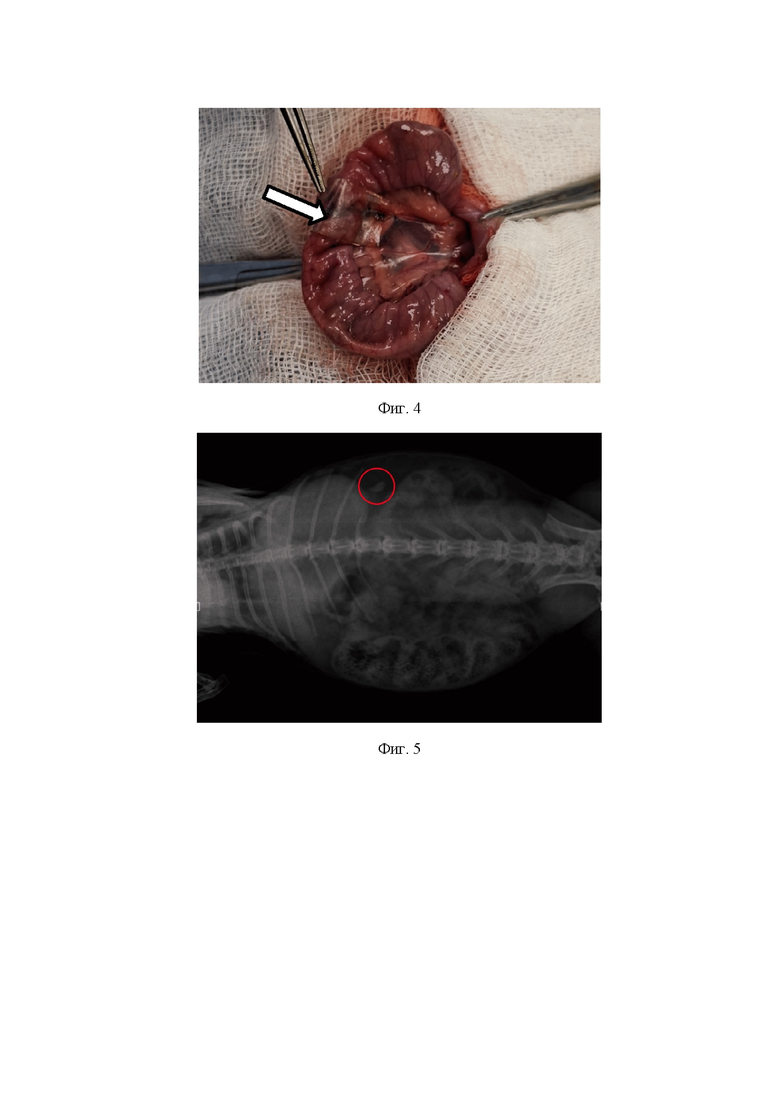
На фиг. 5 изображена рентгенограмма органов брюшной полости кролика с рентгенконтрастной хирургической полимерной мембраны (с добавлением йогексола), которая обведена кругом;
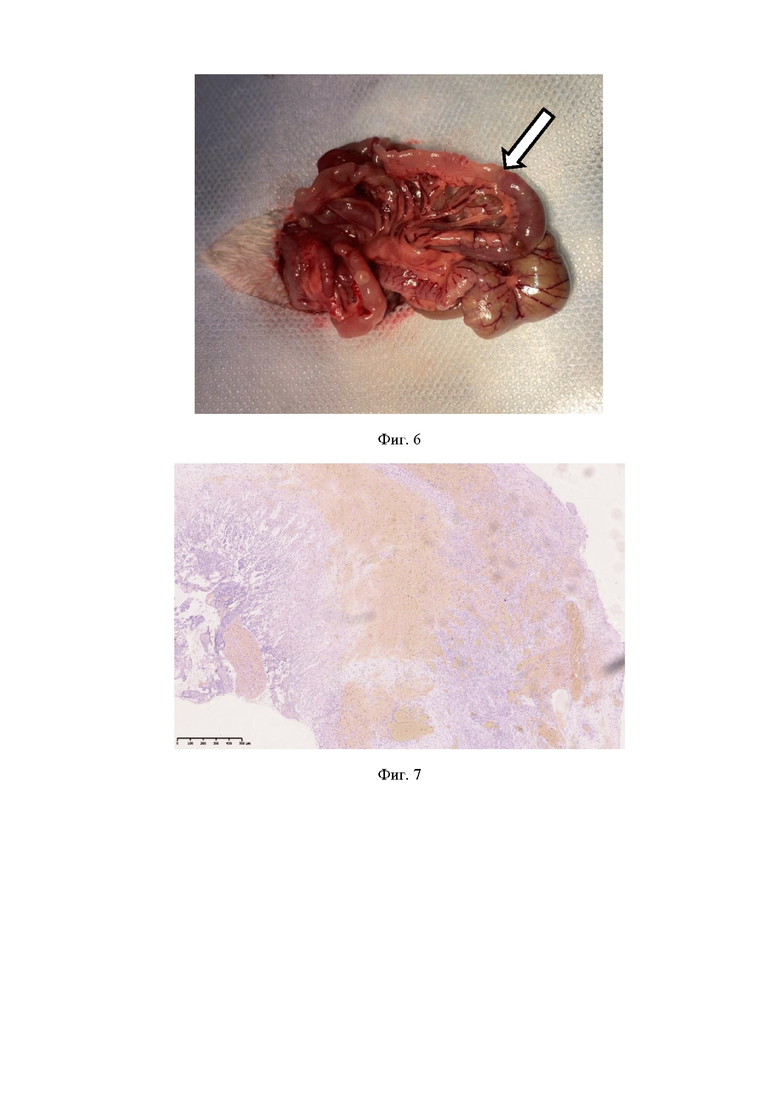
На фиг. 6 изображена интраоперационная картина при лапаротомии через 7 дней с момента имплантации хирургической полимерной мембраны(указана стрелкой), спаечных сращений не определяется;
На фиг. 7 изображен микропрепарат тонкой кишки в зоне анастомоза, укрытого полимерной хирургической мембраной, увеличение 100 крат, окрашен гематоксилином и эозином;
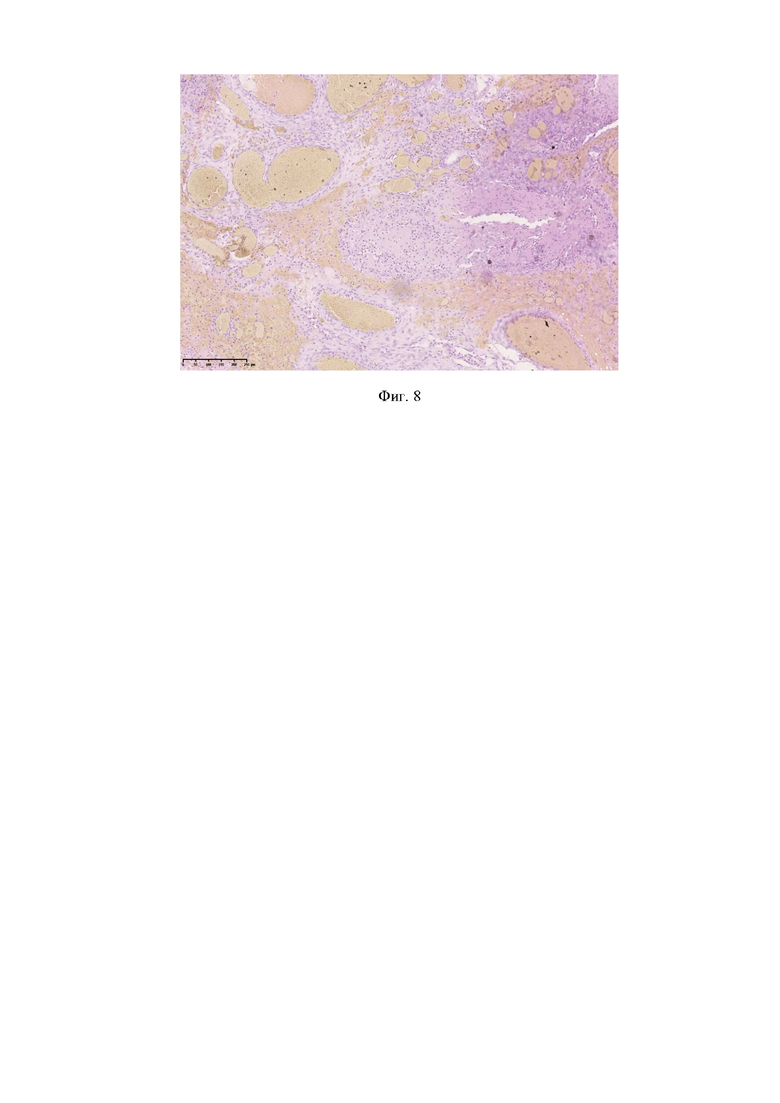
На фиг. 8 изображен микропрепарат тонкой кишки, на котором отмечаются фрагменты полимерной хирургической мембраны, увеличение 200 крат, окрашен гематоксилином и эозином.
СПОСОБ ОСУЩЕСТВЛЯЕТСЯ СЛЕДУЮЩИМ ОБРАЗОМ
Технология изготовления хирургических полимерных мембран осуществляется в асептических условиях и заключается в последовательном приготовлении водных растворов полимеров (натриевой соли карбоксиметилцеллюлозы с концентрацией 1% по массе, альгината натрия с концентрацией 1% по массе, а также поливинилпирролидона с концентрацией 5% по массе) и последующем их послойном высушивании в сушильном шкафу до постоянной массы. Учитывая трехслойную структуру изделия, формируют его композицию, начиная с третьего слоя, обращенного к брюшной полости. Подготавливают растворы полимеров. К раствору Na-КМЦ и альгината натрия прибавляют глицерин в количестве 50% от массы сухого полимера, взятого для растворения. К раствору поливинилпирролидона прибавляют глицерин в количестве 10% от массы сухого полимера. Далее к раствору альгината натрия медленно при интенсивном перемешивании прибавляют CaCl2 в количестве 5% от массы используемого сухого альгината натрия, в виде 1 %-ного раствора; смесь интенсивно перемешивают в течение 6 часов для гомогенизации.
На дно чашки Петри наносят раствор Na-КМЦ в количестве 80-90 г, чашки выдерживают в сушильном шкафу при температуре 45-50°С в течение 12 часов до полного высыхания. Затем поверх высушенного слоя Na-КМЦ наносят раствор альгината натрия-кальция в количестве 80-90 г. Композицию выдерживают в сушильном шкафу в течение 12 часов до полного высыхания. После чего на поверхность высушенной двухслойной композиции наносят слой 5%-ного раствора поливинилпирролидона в количестве 16-20 г, и вновь выдерживают в сушильном шкафу в течение 6-7 часов при температуре 45-50°С.
В результате в течение 30-32 часов получают трехслойную пленку из биодеградируемых и биосовместимых полимеров, в которой слой из поливинилпирролидона обеспечивает адгезию композиции к раневой поверхности, слой альгината-натрия-кальция придает композиции прочность за счет медленной (в течение 5-7 дней) деградации, а внешний слой из Na-КМЦ препятствует развитию выраженного спаечного процесса в зоне вмешательства.
Способ иллюстрируется следующими примерами.
ПРИМЕР ПО СПОСОБУ ПОЛУЧЕНИЯ
Пример 1. Для получения первого слоя материала к нагретым до 45-50°С 178,2 мл воды порциями при интенсивном перемешивании прибавляли 1,8 г Na-КМЦ (4000-8000 сП). Далее вносили 0,9 г глицерина (50 % от массы Na-КМЦ) и перемешивали полученную смесь в течение 4 часов при указанной температуре до достижения гомогенного раствора. Полученный раствор разливали по двум чашкам Петри диаметром 10,5 см, при этом масса раствора в одной чашке Петри составляла 88-89 г. Чашки помещали в сушильный шкаф при температуре 45-50°С с одновременной воздушной конвекцией и выдерживали при указанной температуре 12 часовдо постоянной массы.
Аналогичным способом получали второй слой:к нагретым до 45-50 °С 178,2 мл воды порциями при интенсивном перемешивании прибавляли 1,8 г альгината натрия (средней вязкости) и перемешивали в течение 4 часов до достижения гомогенного раствора. Далее к полученному раствору при интенсивном перемешивании медленно прибавляли 9 мл 1 %-ного (от массы альгината натрия) раствора CaCl2 (5% от массы альгината натрия) и 0,9 г глицерина (50% от массы альгината натрия)и интенсивно перемешивали смесь в течение 6 часов до полной гомогенизации. Полученный раствор разливали по двум чашкам Петри в количестве 88-89 г поверх предварительно высушенного слоя Na-КМЦ. Чашки помещали в сушильный шкаф при температуре 45-50°С с одновременной воздушной конвекцией и выдерживали при указанной температуре 12 часов до постоянной массы.
Для приготовления третьего слоя к 34,2 мл воды порциями при интенсивном перемешивании прибавляли 1,8 г поливинилпирролидона, 0,18 г глицерина (10 % от массы поливинилпирролидона, молекулярная масса – 25000), смесь перемешивали до полной гомогенизации. Полученный раствор распределяли поровну (по 16,5-17,5 г) по двум чашкам Петри поверх предварительно высушенного слоя альгината натрия-кальция и высушивали в сушильном шкафу при температуре 45-50°С с одновременной воздушной конвекцией в течение 8 часов до постоянной массы. Получали две пленки массой 2,6-2,7 г и диаметром 10,5 см (фиг. 1).
Пример 2.Отличается о описанного в примере 1 тем, что при получении второго слоя вносили 2,6 мл раствора йогексола (рентген-контрастное вещество) с содержанием йода 350мг/мл (содержание йогексола в композиции в пересчете на йод составляет 50 % от массы альгината натрия) (фиг. 2).
Пример 3. Отличается от описанного в примере 1 тем, что при получении третьего слоя вносили 0,3 г субстанции левофлоксацина, смесь перемешивали до полной гомогенизации.
Пример 4. Отличается от описанного в примере 1 тем, что при получении второго слоя вносили 2,6 мл раствора йогексола с содержанием йода 350мг/мл, а при получении третьего слоя вносили 0,3 г субстанции левофлоксацина.
ПРИМЕР ЭКСПЕРИМЕНТАЛЬНОГО ПРИМЕНЕНИЯ
Все полученные хирургические полимерные мембраны исследовали с помощью сканирующего электронного микроскопа, при исследовании боковой поверхности во всех случаях выявлено их трехслойное строение (фиг. 3).
Оценку эффективности применения (состоятельность фиксации и укрытия)противоспаечной активности и макроскопической реакции организма на имплантацию полимерных мембран для операций на полых органах проводили в хроническом эксперименте invivo на5 кроликах породы Шиншилла массой 3-3,5кг.Тестируемые образцы полимерных мембран изготавливали согласно описанному способу получения, после чего из полученной пленки вырезали фрагмент размерами 2*1 см. Под ингаляционным масочным наркозом кроликам проводили минилапаротомию (длина разреза 4 см). Петли тонкой кишки эвентрировали в рану, пересекали петлю тонкой кишки с помощью электрокоагулятора в поперечном направлении. Выполняли гемостаз. После чего формировали межкишечный анастомоз по типу «конец-в-конец» нитью Викрил 5/0.Зону анастомоза укрывали полимерной мембраной (фиг. 4). Погружали петли в брюшную полость. Рану ушивали послойно наглухо. Кролику выполняли рентгенографию органов брюшной полости в прямой проекции для идентификации мембраны (фиг. 5). На 7-е сутки после имплантации хирургической полимерной мембраны выполняли лапаротомию – при ревизии брюшной полости спаечного процесса, выпота воспалительного характера не обнаружено, сама пленчатая мембрана также не обнаружена, что говорит о ее высоких биодеградируемых свойствах. Петля кишки в зоне размещения хирургической полимерной мембраны не изменена, цвет её и перистальтика не нарушены (фиг. 6). После чегоживотных выводили из эксперимента при помощи CO2-индуцированной эвтаназии. Резецировали участков анастомоза, изготавливали гистологические срезы для морфологической оценки, микропрепараты окрашивали гемотоксилином и эозином по стандартным прописям.
При микроскопическом исследовании фрагмента стенки кишки в зоне межкишечного анастомоза, укрытого полимерной хирургической мембраной, определяется замещение дефекта незрелой грануляционной тканью с полиморфноклеточной инфильтрацией и ангиогенезом (фиг. 7). Здесь же имеются малых размеров фрагментыполимерной хирургической мембраной, вокруг которыхотсутствуетвыраженная клеточная реакция (фиг. 8).Микроскопически также отсутствуют признаки фиброза в серозной оболочке резецированного участка тонкой кишки, что подтверждает отсутствие выраженного спаечного процесса в данной области.
Таким образом, хирургическая полимерная мембрана характеризуется простотой получения и легко воспроизводимой технологией, не требующей использования дорогостоящего и высокотехнологичного оборудования. Экспериментальное применение мембраны доказывает перспективность разработки, так как повышает герметичность кишечного анастомоза, не приводит к спайкообразованию. Указанные положительные свойства хирургической полимерной мембраны достигаются её трехслойной структурой: первой слой (обращенный к кишечной стенке) обеспечивает плотную фиксацию к месту анастомоза, второй слой служит в качестве депо лекарственных средств или активных компонентов, является каркасом, третий слой уменьшает спайкообразование.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ИЗОЛИРОВАНИЯ КИШЕЧНОГО АНАСТАМОЗА И ПРЕДОТВРАЩЕНИЯ ПОСЛЕОПЕРАЦИОННОГО СПАЕЧНОГО ПРОЦЕССА | 2022 |
|
RU2796007C1 |
| СПОСОБ ЗАЩИТЫ АНАСТОМОЗОВ ПРИ РЕЗЕКЦИЯХ КИШЕЧНИКА | 2000 |
|
RU2192256C2 |
| Способ укрепления межкишечных анастомозов | 2020 |
|
RU2747662C1 |
| РАНЕВОЕ ПОКРЫТИЕ ДЛЯ ВНУТРЕННИХ ОРГАНОВ | 2006 |
|
RU2325926C1 |
| СПОСОБ ПРОФИЛАКТИКИ НЕСОСТОЯТЕЛЬНОСТИ ШВОВ ЭНТЕРОЭНТЕРОАНАСТОМОЗА | 2010 |
|
RU2445022C2 |
| Способ комплексного хирургического лечения больных с несформированными дуоденальными и высокими тонкокишечными свищами с использованием биологического импланта и селективного продолжительного введения ангиопротекторов | 2018 |
|
RU2681741C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОСПАЕЧНОГО МАТЕРИАЛА | 2020 |
|
RU2744752C1 |
| СПОСОБ ПОСЛЕОПЕРАЦИОННОЙ ПРОФИЛАКТИКИ НЕСОСТОЯТЕЛЬНОСТИ ТОЛСТО-ТОЛСТОКИШЕЧНОГО АНАСТОМОЗА | 2013 |
|
RU2523822C1 |
| СПОСОБ РЕЗЕКЦИИ И РЕРЕЗЕКЦИИ ЖЕЛУДКА | 2005 |
|
RU2283045C1 |
| Способ получения противоспаечного пленочного материала на основе карбоксиметилцеллюлозы | 2016 |
|
RU2629841C1 |
Изобретение относится к области медицины, а именно к хирургии. Предложена хирургическая полимерная мембрана, которая является трехслойной, и её слои получены путем приготовления и последовательного нанесения на стеклянную подложку растворов полимеров с последующим их послойным высушиванием при температуре 45-50°С с одновременной воздушной конвекцией до постоянной массы, причем: раствор полимера, из которого получен первый слой, представляет собой водный 1%-ный по массе раствор натриевой соли карбоксиметилцеллюлозы; раствор полимера, из которого получен второй слой, представляет собой водный 1%-ный по массе раствор альгината-натрия-кальция; раствор полимера, из которого получен третий слой, представляет собой водный 5%-ный по массе раствор поливинилпирролидона. Во второй и третий слои возможно внесение соответственно раствора йогексола и субстанции левофлоксацина. Изобретение обеспечивает достижение надежного укрепления линии швов анастомоза и отдельных швов в условиях скомпрометированной кишечной стенки, а также снижение вероятности развития их несостоятельности и спаечного процесса в области хирургического вмешательства. 8 ил., 4 пр.
Хирургическая полимерная мембрана, характеризующаяся тем, что является трехслойной, отличающаяся тем, что слои указанной мембраны получены путем приготовления и последовательного нанесения на стеклянную подложку растворов полимеров с последующим их послойным высушиванием при температуре 45-50°С с одновременной воздушной конвекцией до постоянной массы, причем раствор полимера, из которого получен первый слой, представляет собой водный 1%-ный по массе раствор натриевой соли карбоксиметилцеллюлозы, раствор полимера, из которого получен второй слой, представляет собой водный 1%-ный по массе раствор альгината-натрия-кальция, а раствор полимера, из которого получен третий слой, представляет собой водный 5%-ный по массе раствор поливинилпирролидона, при этом во второй и третий слои возможно внесение соответственно раствора йогексола и субстанции левофлоксацина.
| МЕДИЦИНСКАЯ ПОВЯЗКА | 1995 |
|
RU2125859C1 |
| Forysenkova A.A | |||
| et al | |||
| Polyvinylpyrrolidone-Alginate Film Barriers for Abdominal Surgery: Anti-Adhesion Effect in Murine Model / Materials, 2023, V | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Телефонная трансляция | 1926 |
|
SU5532A1 |
| РАНЕВОЕ ПОКРЫТИЕ ДЛЯ ВНУТРЕННИХ ОРГАНОВ | 2006 |
|
RU2325926C1 |
| СПОСОБ МОДИФИКАЦИИ БУТАДИЕН-НИТРИЛЬНЫХ КАУЧУКОВ ДЛЯ ПОВЫШЕНИЯ ИХ МОРОЗОСТОЙКОСТИ | 2020 |
|
RU2745289C1 |
| МЕДИЦИНСКАЯ МНОГОСЛОЙНАЯ ПОВЯЗКА С МНОГОФУНКЦИОНАЛЬНЫМИ НАНОМЕМБРАНАМИ И ИЗДЕЛИЯ НА ЕЕ ОСНОВЕ | 2014 |
|
RU2578458C2 |
Авторы
Даты
2024-02-06—Публикация
2023-10-27—Подача