Изобретение относится к области медицины и химико-фармацевтической промышленности, в частности - к средствам хондропротекторного действия и может быть использовано для стимуляции регенерации и замедления дегенерации хрящевой ткани, для образования новых коллагеновых волокон и коррекции локального иммунного статуса в суставах и позвоночнике у пациентов с остеоартритом различной локализации и для улучшения функционального состояния опорно-двигательного аппарата у разных групп населения, в том числе, после травм и физических нагрузок.
Разработка новых средств хондропротекторного действия является актуальной задачей современной медицины в силу широкого распространения заболеваний, связанных с нарушением функционального состояния опорно-двигательного аппарата и дегенерации хрящевой ткани, с одной стороны, и недостаточной эффективностью известных хондропротекторов, с другой стороны.
Среди известных хондропротекторов особую роль играют препараты на основе солей хондроитина и глюкозмина, а также комбинации солей хондроитина и глюкозамина. Известно большое количество лекарственных средств, БАД, пищевых добавок, продуктов для питания спортсменов, включающих комбинацию хондроитина сульфата и глюкозамина сульфата или глюкозамина гидрохлорида (см., например, патенты RU 2381029, RU 2432166, RU 2468805, RU 2547572, RU 2739184, RU 2739746 и др.; лекарственные препараты «Терафлекс», «Артра», «Хондролекс», «Сусталонг» и др.; БАД и пищевые добавки «ГКХ Глюкозамин и Хондроитин комплекс», «Солгарт», «Move Free», «Хонда» и др.). Препараты и БАД на основе комбинации солей хондроитина и глюкозамина показали высокую эффективность и получили очень широкое распространение во многих странах, однако, несмотря на это, дальнейшее повышение эффективности этих хондропротекторов остается важной задачей, и поэтому ведутся разработки по дополнению комбинаций солей хондроитина и глюкозамина новыми компонентами.
Отдельным направлением таких разработок является использование в комбинированных хондропротекторных средствах коллагена дополнительно к солям хондроитина и глюкозамина. Такие хондропротекторы (как правило, с добавлением еще белков и/или витаминов, и/или микроэлементов) описаны, например, в патентах RU 2463811, RU 2564841, RU 2635995, RU 2648641, а также известны в качестве готовых БАД и пищевых добавок: БАД «ГКХ комплекс с коллагеном» (компании «Фармакор продакш», Россия), БАД «В-VIT» (компании «Pharma Market Solutions)), Латвия), БАД «НБЛ Plus» (компании Nobel Ilac Sanayii ve Ticaret A.S., Турция), БАД «Флексиново» (компании ADAMED PHARMA, S.A., Польша), БАД «SOLAB» (компании ООО «Со Лаб», Россия), БАД «1 WIN» (компании ООО «ВанВин», Россия), БАД «Глюкозамин максимум Адванс» (компании Valeant Pharmaceuticals International, Inc., Россия).
Анализ составов указанных известных хондропротекторов с коллагеном показал, что эти составы нуждаются в дальнейшей оптимизации, причем как при подборе конкретных форм активных компонентов, так и при подборе их количественного содержания.
Во всех перечисленных выше разработках (как в патентах, так и в готовых БАД; за исключением БАД «НБД Plus») используется коллаген в виде гидролизованного коллагена, который, однако, имеет существенные недостатки. При его получении используется метод полной денатурации, в результате чего гидролизованный коллаген характеризуется нарушенной пространственной структурой (отсутствием активных эпитопов в структуре) и поэтому не оказывает иммуномодулирующего действия в отношении тканей сустава при появлении в них антигенов, стимулирующих прогрессирование различных фенотипов остеоартрита.
Также существенным недостатком многих перечисленных известных хондропротекторов с коллагеном является выбор соли глюкозамина, а именно включение в состав гидрохлорида глюкозамина. Эта соль включена, например, в составы БАД «НБЛ Pus», «Глюкозамин максимум Адванс». В инструкциях некоторых БАД (например БАД «SOLAB», БАД «1 WIN») вообще не конкретизируется соль глюкозамина. Между тем используемые в настоящее время в хондропротекторах две соли глюкозамина -гидрохлорид и сульфат - имеют важные отличия в формировании механизма физиологического действия. Для биосинтеза хондроитина сульфата необходим именно глюкозамина сульфат, который сразу включается в полимеризацию. Глюкозамина гидрохлорид должен предварительно сульфатироваться, что требует достаточного количества атомов серы. Хондроитина сульфат при непосредственном контакте с хрящевой тканью включается в каскад синтеза хондроитин-серной кислоты за счет наличия в своем составе атома серы. В результате прикрепления SH-группы происходит фиксация полимерной цепочки хондроитина сульфата на хряще. После фиксации цепочки хондроитина сульфата на хряще образуются полости для удержания воды и повышается коэффициент задержки кальция, используемого для реконструктивных процессов.
Как уже говорилось, в оптимизации нуждается и количественный состав известных хондропротекторов, включающих хондроитин, глюкозамин и коллаген.
В некоторых из перечисленных выше известных разработок (RU 2463811, RU 2648641, БАД «SOLAB», БАД «1 WIN») вообще не приводится сведений о разовой и суточной дозе входящих в состав хондропротекторов (приводятся либо сведения только о качественном составе, либо сведения о количественном составе в масс % для каждого ингредиента).
В большинстве известных разработок (RU 2463811, БАД «ГКХ комплекс с коллагеном», БАД «В-VIT» БАД «Флексиново») содержание хондроитина сульфата и глюкозамина сульфата (или глюкозамина гидрохлорида) составляет от 100 до 240 мг на 1 таблетку или капсулу (при приеме 1-2 таблеток/капсул 2 раза в день) или порядка 500 мг - 700 мг при приеме 1 раз в день. Однако это гораздо ниже необходимой суточной потребности, составляющей для глюкозамина сульфата 1500 мг, а для хондроитина сульфата 1200 мг в сутки (https://www.theraf1ex.ru/dlva-specialistov/pravilnaya-doza/; https://www.pharmocean.ru/articles/hondroitin-i-qlyukozamin#:~:text=Суточная%20норма%20потребления%20глюкозамина%20составляет,являются%20 рыба%20и%20другие%20 морепродукты).
При отсутствии суточных норм для гидролизованного коллагена в известных БАД показатели содержания этого компонента значительно отличаются: например, RU 2648641 - 80 мг гидролизованного коллагена в сутки; БАД «Флексиново» - 300 мг гидролизованного коллагена в сутки. Как уже указывалось, сведения о ряде известных комбинированных хондропротекторов с коллагеном вообще не содержат информации о количественном содержании ингредиентов, в частности гидролизованного коллагена.
Подавляющее большинство известных в настоящее время комбинированных хондропротекторов подразумевает необходимость приема несколько раз в течение суток, что достаточно неудобно для пациента и также требует дальнейшей оптимизации.
За прототип предлагаемого изобретения выбрано хондропротекторное средство, представляющее собою БАД и включающее глюкозамина гидрохлорид, хондроитина сульфат, неденатурированный коллаген II типа, несколько дополнительных активных компонентов (гиалуроновая кислота, метилсульфонилметан, витамин Д) и вспомогательные вещества, при этом БАД выполнена в виде таблеток и включает на 1 таблетку глюкозамина гидрохлорида 750 мг, хондроитина сульфата 600 мг, неденатурированного коллагена II типа 20 мг (БАД «НБЛ Plus», производитель Nobel Ilac Sanayii ve Ticaret A.S., Турция, https://www.nobel.com.tr/ru-ru/наши-продукты/пищевые-добавки/nbl-glukozamin-kondroitin-msm-60-tablets). Согласно инструкции, данную БАД рекомендовано принимать по 1 таблетке 2 раза в день общим курсом не более месяца, с перерывами между курсами не более 2 месяцев; указано, что БАД «способствует поддержанию функций опорно-двигательного аппарата и является дополнительным источником глюкозамина, хондроитина, метилсульфонилметана, коллагена, гиалуроновой кислоты и витамина D.
В выбранной в качестве прототипа БАД нет гидролизованного коллагена, который, как уже отмечалось, в силу полной денатурации характеризуется нарушенной пространственной структурой (отсутствием активных эпитопов в структуре) и поэтому не оказывает иммуномодулирующего действия в отношении тканей сустава; используется неденатурированный коллаген II типа.
С учетом рекомендуемого курса применения (по 1 таблетке 2 раза в день) суточная доза активных веществ при приеме этой БАД составляет для глюкозамина гидрохлорида 1500 мг, для хондроитина сульфата 1200 мг, неденатурированного коллагена II типа 40 мг, что соответствует суточным потребностям организма человека в этих веществах (https://www.theraflex.ru/dlva-specialistov/pravilnaya-doza/; https://www.pharmocean.ru/articles/hondroitin-i-glyukozamin#:~:text=Суточная%20норма%20потребления%20глюкозамина%20составляет,являются%20 рыба%20и%20другие%20 морепродукты; https://umedp.ru/articles/nedenaturirovannyy_kollagen_ii_tipa_stroenie_tiziologicheskaya_rol_vozmozhnost_medikamentoznoy_korre.html; http://dx.doi.org/10.18203/issn.2455-4510IntJResOrthop20183386).
Однако выбранная в качестве прототипа БАД имеет ряд недостатков. К ним в первую очередь относится использование глюкозамина в виде гидрохлоридной соли. Как уже отмечалось, для биосинтеза хондроитина сульфата необходим глюкозамина сульфат (а не глюкозамин гидрохлорид), который сразу включается в полимеризацию. Глюкозамина гидрохлорид должен предварительно сульфатироваться, что требует достаточного количества атомов серы. Хондроитина сульфат при непосредственном контакте с хрящевой тканью включается в каскад синтеза хондроитин-серной кислоты за счет наличия в своем составе атома серы. В результате прикрепления SH - группы происходит фиксация полимерной цепочки хондроитина сульфата на хряще. После фиксации цепочки хондроитина сульфата на хряще образуются полости для удержания воды и повышается коэффициент задержки кальция, используемого для реконструктивных процессов.
Определенным недостатком БАД «НБЛ Plus» являются дополнительные активные соединения (гиалуроновая кислота, метилсульфонилметан, витамин Д), в определенном отличающем ее эквивалентном составе, что определяет другой механизм действия и профиль эффектов, эффективность и безопасность БАД.
БАД «НБЛ Plus» выполнена в форме таблеток, покрытых пленочной оболочкой. Производство такой лекарственной формы (далее - лек. формы) в сравнении, например, с лек. формой порошков, является сложной, требует довольно значительных временных и финансовых затрат.В состав таблетки и пленочной оболочки входит большое число вспомогательных веществ, что увеличивает химическую нагрузку на организм пациента. Так, согласно инструкции БАД «НБЛ Plus», перечень вспомогательных веществ включает следующие: ядро таблетки: стабилизаторы: поливинилпирролидон (Е1201), кроскармеллоза натрия (Е468); носитель: целлюлоза микрокристаллическая (E460(i)); агенты антислеживающие: жирные кислоты (Е570), магниевые соли жирных кислот (E570b); глазирователь: полиэтиленгликоль (Е1521); состав пленочной оболочки 1(114F280000 Белый): стабилизатор: поливиниловый спирт (Е1203); краситель: титана диоксид (Е171); глазирователи: полиэтиленгликоль 8000 Р (Е1521), тальк (E553b);Состав пленочной оболочки 2(опадрай fx серебристый 62W28547):
загустители: карбоксиметилцеллюлозы натриевая соль (Е466), мальтодекстрин (Е1400), дестрозы моногидрат (Е1200); носитель: алюмосиликат калия (Е555); краситель: титана диоксид (Е171); эмульгатор: лецитин (соя) (Е322).
К определенным недостаткам БАД «НБЛ Plus» можно также отнести необходимость 2-кратного приема БАД в течение суток, что довольно неудобно для пациентов в сравнении с БАД, требующими приема 1 раз в сутки.
В задачу предлагаемого изобретения входит расширение арсенала средств хондропротекторного действия; оптимизация состава активных компонентов и за счет этого повышение эффективности хондропротекторного действия; разработка препарата в более простой в производстве лек. форме (порошок) и за счет этого снижение временных и финансовых затрат на производство; уменьшение количества необходимых вспомогательных веществ и за счет этого снижение химической нагрузки на организм пациента; уменьшение необходимого количества приемов препарата в течение суток.
Поставленная задача решается тем, что предлагается средство хондропротекторного действия, включающее глюкозамина сульфат, хондроитина сульфат, неденатурированный коллаген II типа, выполненное в виде порошка, при следующем соотношении компонентов:
При этом в заявляемом средстве неденатурированный коллаген II типа присутствует в составе натурального неденатурированного коллагена, содержащегося в количестве 333 -400 мг.
Заявляемое средство хондропротекторного действия дополнительно может включать вспомогательные вещества в виде носителя и по меньшей мере одного из следующих компонентов: регулятора кислотности, ароматизатора пищевого, антислеживающегося агента, подсластителя.
При этом оно характеризуется следующим соотношением компонентов:
В одном из аспектов предлагаемое хондропротекторное средство включает носитель в виде палатинозы, регулятор кислотности в виде лимонной кислоты, антислеживающийся агент в виде кремния диоксида, подсластитель в виде сукралозы, при следующем соотношении компонентов на 1 порошок-саше:
Другим аспектом является хондропротекторное средство, характеризующееся следующим соотношении компонентов на 1 порошок-саше:
Поставленная задача достигается также предлагаемым способом хондропротекторного воздействия на опорно-двигательную систему человека, включающим введение предлагаемого хондропротекторного средства в количестве 1 порошка-саше однократно в сутки общим курсом 6-8 недель. Перед приемом содержимое пакета-саше растворяют в 100-200 мл теплой вода (t=40°) и затем принимают внутрь.
Если не определено иначе, все используемые в настоящем документе технические и научные термины имеют значения, общепринятые среди специалистов в областях, к которым принадлежит изобретение. В случае, если имеется множество определений для терминов, действительным считается описанный в настоящей заявке. Следует обратить внимание, что в случае, если ссылка дана в виде URL или в виде аналогичного адреса или идентификатора, очевидно, что идентификатор может меняться, а конкретная информация в Интернете может появляться и исчезать, но при этом эквивалентная информация может быть найдена путем Интернет-поиска. Ссылка на данную информацию свидетельствует о том, что она доступна и ее можно распространять. Очевидно, что приведенное выше краткое описание и приведенное ниже подробное описание изобретения даны исключительно с иллюстративной целью и ни в коей мере не ограничивают ни один из заявленных объектов. Использование терминов "к которым относятся", "включая", и их синонимов не является ограничивающим. Следует заметить, что описанные в настоящем изобретении способы и композиции не ограничены конкретными методологиями, протоколами, конструктами и реагентами, которые описаны в настоящем документе и могут варьировать. Также следует заметить, что используемая в настоящем документе терминология используется исключительно с целью описания конкретных вариантов осуществления и не ограничивает объем описанных способов и композиций, которые ограничивает только прилагаемая формула изобретения.
Предлагаемое хондропротекторное средство расширило арсенал комбинированных хондопротекторов на основе глюкозамина, хондроитина и коллагена. В нем оптимизирован состав активных компонентов и за счет этого повышена эффективность хондропротекторного действия: в составе нет гидролизованного коллагена (используется неденатурированный коллаген типа II, содержащийся в натуральном неденатурированном коллагене) и нет глюкозамина гидрохлорида (используется глюкозамина сульфат); количественные показатели активных компонентов соответствуют суточным потребностям организма в этих веществах: глюкозамина сульфат 1500 мг (в пересчете на чистый глюкозамин 900 мг); хондроитина сульфат 1200 мг; неденатурированный коллаген II типа 40 мг. Указанные показатели могут несколько варьировать (в пределах 10-20%), с учетом веса пациентов (стандартные суточные нормы обычно разрабатываются для веса 70 кг, поэтому при большем или меньшем весе возможны определенные отклонения от стандартных норм), допустимых отклонений в ходе технологического производства препарата, медицинских потребностей, зависящих от выраженности патологии опорно-двигательной системы.
Проведенные в процессе разработки заявляемого изобретения исследования показали возможность объединения указанных трех хондропротекторов в одной лекарственной форме и включение их в препарат в количествах, рекомендованных в качестве необходимых суточных доз. Несовместимости компонентов не отмечено, препарат соответствует всем необходимым требованиям, установленным для БАД, он стабилен, имеет срок хранения 2 года.
Проведенные клинические исследования показали высокую эффективность препарата в профилактике и лечении патологий опорно-двигательной системы, а также его безопасность (что подробно отражено далее при описании клинических результатов). Препарат разработан в лекарственной форме порошка, что является гораздо более простой в производстве, чем таблетки и капсулы, лекарственной формой, требующей значительно меньших временных и финансовых затрат.
Кроме того, лекарственная форма порошка позволила очень значительно уменьшить необходимое количество вспомогательных веществ (в сравнении с БАД в форме таблеток или капсул) и тем самым снизить химическую нагрузку на организм пациента. Разработанный препарат характеризуется удобством в применении, он требует только 1 прием в сутки.
Существенным в созданной композиции является сбалансированный состав, который предусматривает все указанные компоненты в оптимальном соотношении, что позволяет получить потенцирование их положительных фармакологических эффектов, а также дополнить новым иммуномодулирующим эффектом на уровне тканей сустава.
В созданной композиции представлены биологически активные соединения, которые при растворении в воде образуют молекулярные кластеры. При употреблении раствора композиции комбинированного фармацевтического хондропротектора внутрь происходит практически моментальное усвоение активных структур, запускающих многоцелевое действие на организм человека:
глюкозамина сульфат - активирует синтез протеогликанов, гиалуроновой, хондроитинсерной кислот и около 40 регуляторных белков на внутриклеточном уровне, которые являются строительным материалом для синовиальной ткани сустава, внутрисуставной жидкости и хрящевой ткани; оказывает противовоспалительное действие за счет ингибирования транслокации внутрь клеточного ядра транскрипционного фактора NF-kB (ядерный фактор kB), посредством связывания с центральным таргетным белком-рецептором CD44 со снижением активности провоспалительных цитокинов (ФНОα, ИЛ1β), а также за счет блокады экспрессии гена циклооксигеназы (ЦОГ) 2, кодирующего фермент ЦОГ2; синтез IgA в кишечнике (первая линия защиты против микроорганизмов в слизистой оболочке кишечника), регуляция трансэндотелиальной миграции лейкоцитов; связывание рецепторов гематопоэтина/интерферонов; повышение секреции компонентов внеклеточного матрикса соединительной ткани (коллаген, аннексии, тенасцин, аггрекан); возрастание уровня факторов роста соединительной ткани; снижение содержания протеаз, деградирующих соединительную ткань; оказывает быстрый анальгетический и противовоспалительный эффект, замедляет прогрессирование дегенеративных процессов в суставах, позвоночнике и околопозвоночных мягких тканях, ограничивает активность нейродегенеративных процессов;
хондроитина сульфат - высокомолекулярный мукополисахарид, являющийся дополнительным субстратом для образования хрящевого матрикса, нормализует обмен веществ в хрящевой ткани, стимулирует синтез протеогликанов, гиалурона, коллагена II типа, способствует регенеративным процессам в суставном хряще, суставной сумке, поддержанию вязкости синовиальной жидкости; фармакологические эффекты появляются вследствие связывания хондроитина сульфата с 5 мембранными рецепторами (TLR4, CD44, CD97, ICAM1, интегринами), что приводит к существенному снижению ядерной транслокации транскрипционного фактора NF-кВ, уменьшению активности свободно-радикального окисления, снижению активности провоспалительных цитокинов (ФНОα, ИЛ1β), увеличению синтеза коллагена, с появлением умеренного и пролонгированного противовоспалительного и болеутоляющего действия, при систематическом применении замедляет прогрессирование остеоартрита, уменьшает потребность в применении нестероидных противовоспалительных препаратов;
неденатурированный коллаген II типа содержит в своем составе активные эпитопы, что подтверждается иммуноферментным анализом и позволяет отличить эту форму коллагена от гидролизованного или денатурированного коллагена; пероральный прием небольших количеств неденатурированного коллагена II типа представляет активные эпитопы с правильной трехмерной структурой для пейеровых бляшек кишечника, что влияет на передачу сигналов, необходимую для развития иммунной оральной толерантности к антигену и препятствует системной атаке Т-клеток-киллеров на суставной хрящ; неденатурированный коллаген II типа подавляет экспрессию связанного с ИЛ-17 активатора NF-кВ (RANKL) CD4+Т-клеток; в результате уменьшает выработку ферментов, разрушающих в организме коллаген II типа и снижает образование артритогенных антигенов, формирующих в хряще аутоиммунную реакцию; сохранение в организме человека коллагена II типа поддерживает основу соединительной ткани человека (хрящей, костей, связок, сухожилий, кожи и др.) и обеспечивает ее прочность, усиливают регенерацию соединительнотканных элементов, препятствует развитию заболеваний костно-мышечной системы; обладает стимулирующим влиянием на фибробласты соединительных тканей, что приводит к восстановлению целостности хряща, укреплению связок и облегчению боли при остеоартрите и функциональных поражениях суставов; укрепляет костную ткань за счет активирующего влияния на остеобласты.
В качестве вспомогательных веществ используются носитель (палатиноза, мальтодекстрин, инулин, мальтоза, эритритол, фруктоза, сахар), регулятор кислотности (лимонная кислота, аскорбиновая кислота, яблочная кислота), ароматизатор пищевой (клубника, яблоко, апельсин, другие), антислеживающий агент (кремния диоксид, ТНН неосил, аэросил), подсластитель (сукралоза, фруктоза, сахар, стевиозид, эритритол, натрия сахарин).
Количественные значения вспомогательных веществ были разработаны экспериментально и подбирались с учетом необходимости соблюдения в готовом препарате действующих в фармацевтике требований.
В результате проведенных исследований были предложены следующие показатели в расчете на 1 порошок-саше 6±0,6 г:
Предлагаемое средство получают следующим образом. Готовят исходные компоненты из расчета на 1 порошок-саше (6±0,6 г):
Например, готовят состав с использованием следующих вспомогательных веществ:
должно приходится 2 или 3 порошка, дающих в сумме необходимые суточные дозы активных компонентов БАД.
Пример 1.
Получение предлагаемого хондропротектрного средства.
Произведено взвешивание необходимых компонентов из расчета на 1 пакетик-саше (6 г):
Произведено просеивание компонентов (с использованием вибросита диаметром 1 мм), измельчение на молотковой мельнице и повторное просеивание. Полученная смесь не содержит комков и посторонних включений. Проведено смешивание компонентов с использованием V-образного смесителя С-300. Полученная смесь однородна (при надавливании пестиком на поверхности смеси не должно быть комков и посторонних включений).
Полученный продукт представляет собою порошок (цвет от белого до светло-коричневого), который по показателям качества соответствует всем требованиям к БАД в соответствии с TP ТС 021/2011 «О безопасности пищевой продукции».
Перед употреблением содержимое 1 порошка-саше необходимо растворить в 100-200 мл теплой воды (t=40°).
БАД необходимо принимать по 1 порошку 1 раз в сутки в течение 6-8 недель.
Приведенные выше в примере 1 показатели количественного содержания компонентов являются оптимальными. Ниже в таблице приведены примеры с другими соотношениями количественных показателей содержания ингредиентов, которые были получены в отдельных экспериментах:
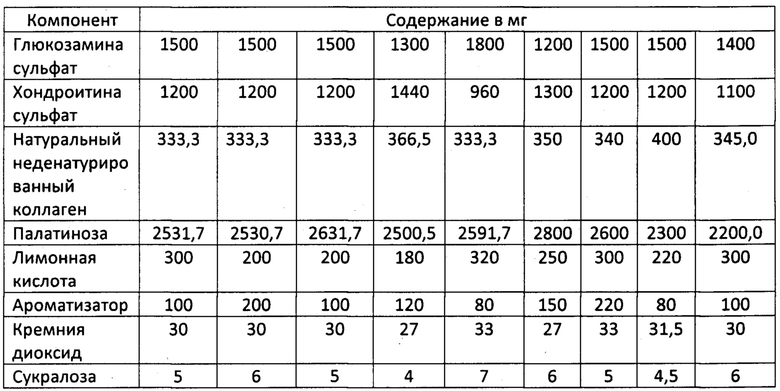
Пример 2.
Применение в клинической практике.
Пациент М., 65 лет, поступил в медицинский центр «Новомедицина» (г. Ростов-на-Дону) с жалобами на выраженные боли в коленных суставах при ходьбе и физических нагрузках после утренней скованности, менее выраженная боль в коленных суставах в течение ночи, в положении стоя в течение 30 мин и после 2 ч в положении сидя, ограничение дистанции ходьбы, ограничение возможности подъема на 1 лестничный пролет вверх и ходьбы по пересеченной местности при менее выраженном ограничении возможности спуска на 1 лестничный пролет вниз и сидения на корточках или на коленях. Отмечает хруст в коленных суставах при движении, а также деформацию и припухлость коленных суставов. За медицинской помощью не обращался. Боли в суставах уменьшаются при самостоятельном приеме топических и пероральных нестероидных противовоспалительных препаратов 1-2 раза в неделю.
Считает себя больным в течение 7 лет, когда впервые стал отмечать появление болей в коленных суставах, неинтенсивных, возникавших к концу дня, которые проходили после прекращения физической нагрузки. Из перенесенных заболеваний отмечает: частые простудные заболевания, травм и операций не было. Профессиональных заболеваний и вредных привычек не имеет. Наследственность не отягощена. Наличие кожных и венерических заболеваний, ревматизма, туберкулеза, нарушений обменных процессов, вирусного гепатита В больной у себя и родственников отрицает. Аллергических реакций на лекарственные препараты и продукты питания не отмечает.Гемотрансфузий не было.
При осмотре: общее состояние средней степени тяжести. Сознание ясное, выражение лица спокойное. Телосложение правильное, конституция гиперстеническая. Вес 89 кг, рост 178 см, температура тела в подмышечной впадине 36,6°С. ИМТ=28,1 кг/м2. Кожные покровы розового цвета, гиперпигментации не наблюдается, повышенной потливости, сыпи, шелушения, расчесов нет. Гнойников, язв, пролежней и рубцов на коже нет. Влажность кожи умеренная, тургор тканей и эластичность кожи сохранены. Видимые слизистые бледно-розовые, влажные, высыпаний нет, склеры не изменены, иктеричности не наблюдается. Пальпируются одиночные подчелюстные лимфатические узлы, размером 1 см, овальной формы, эластичные, безболезненные, не сращенные с кожей, окружающими тканями и между собой; кожа над ними не изменена. Затылочные, околоушные, подбородочные, шейные, подключичные, надключичные, подмышечные, локтевые, паховые и подколенные лимфоузлы не пальпируются.
Данные визуального исследования: в легких дыхание везикулярное, хрипов нет, тоны сердца приглушены, ритмичные, акцент II тона над аортой. АД=135/85 мм рт.ст., ЧСС - 84 ударов в минуту, ЧД - 18 в минуту, живот при пальпации безболезненный и мягкий, печень увеличена на 0,25 см. Поясничная область визуально не изменена, симптом поколачивания отрицателен с обеих сторон.
При осмотре и пальпации коленных суставов: выявляется варусная деформация, локальная гипертермия, припухлость и болезненность при пальпации обоих коленных суставов. Симптом "плавающего надколенника" не определяется. При пальпации в период всего движения определяется хруст в обоих коленных суставах. Сгибание/разгибание в коленных суставах справа до 90/170 градусов, слева до 60/175 градусов, боль при максимальном сгибании справа, крепитация с обеих сторон. Наличия мышечных атрофий не выявлено.
Данные тестирования по ВАШ: боль в покое - 37 мм (умеренная боль), боль при движении - 54 мм (сильная боль).
Данные тестирования по индексу Лекена: 7 баллов (средняя степень тяжести)
Данные тестирования по общему индексу WOMAC: 50 мм
Диагноз: Первичный деформирующий полиостеоартрит с преимущественным двусторонним поражением коленных суставов. Рентгенологическая стадия 2. ФНС II степени. Вторичный синовит коленных суставов. Осложнения основного: нет Сопутствующий: Избыточная масса тела.
Инструментальные и лабораторные исследования (до терапии).
Рентгенограмма коленных суставов: незначительное сужение суставной щели, субхондральный склероз, мелкие краевые остеофиты.
Ультразвуковое исследование коленных суставов (правый/левый): размер надколенниковой сумки - 1,1 см; толщина синовиальной оболочки - 0,3 см, изменений не выявлено; слабовыраженный синовит коленных суставов.
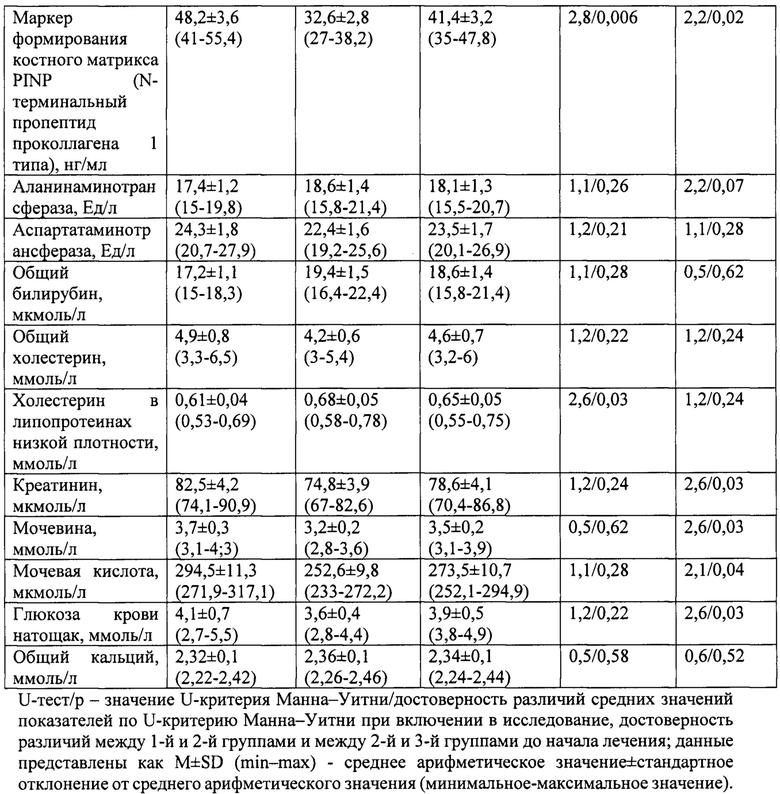
Общий анализ крови: СОЭ - 22 мм/ч, показатели клеточного состава крови в пределах референсных значений. Биохимия крови: сывороточный альбумин - 44 г/л, С-реактивный белок высокочувствительный - 6,65 мг/л; ревматоидный фактор (РФ) - 5,12 МЕ/мл, антитела к циклическому цитруллиновому пептиду - 6 Ед/мл, С-концевые телопетиды коллагена I типа (Beta-Cross laps) - 0,273 нг/мл, маркер формирования костного матрикса PINP (N-терминальный пропептид проколлагена 1 типа) - 48,2 нг/мл, аланинаминотрансфераза - 17,4 Ед/л, аспартатаминотрансфераза - 24,3 Ед/л, общий билирубин - 17 мкмоль/л, общий холестерин - 4,94 ммоль/л, холестерин в липопротеинах низкой плотности - 0,61 ммоль/л, креатинин - 82 мкмоль/л, мочевина - 37 ммоль/л, мочевая кислота - 294 мкмоль/л, глюкоза крови натощак - 4,08 ммоль/л, общий кальций - 2,32 ммоль/л. Увеличение концентрации С-реактивного белка высокочувствительного, маркера формирования костного матрикса PINP (N-терминальный пропептид проколлагена 1 типа) в крови, остальные показатели в пределах референсных значений.
Проводимая терапия. Диета с уменьшением потребления соли, приемом пищи каждые 4 часа с основным объемом в обед, нежирные сорта рыбы, мяса, хлеб с отрубями, овощи и фрукты, молочные продукты, холодец и желе, крупы (гречневая, чечевица), приготовление блюд на нерафинированном масле, исключение из меню соленой рыбы, полуфабрикатов, майонеза, чипсов, отказ от спиртных напитков. Физические упражнения при остеоартрите коленных суставов. Ортезы на коленные суставы. Пациент принимал топическую форму мелоксикама в форме геля, наружно, на область пораженных коленных суставов, 4 раза в день в течение 10 дней до момента обращения к врачу. Пациенту было назначено заявляемое хондропротекторное средство внутрь, содержимое одного пакета-саше (6,0 г) растворяют в 200 мл воды, по 1 пакету-саше (6,0 г) 1 раз в сутки в течение 8 недель.
Обследование проводилось по вышеуказанной схеме.
Эффективность проводимого лечения отмечалась через 2 месяца после приема заявляемого хондропротекторного средства и выражалась в следующем. Отмечалось уменьшение субъективной симптоматики остеоартрита коленных суставов: уменьшение выраженности боли в коленных суставах при ходьбе и физических нагрузках, утренней скованности, отсутствовала боль в коленных суставах в течение ночи, в положении стоя в течение 30 мин и после 2 ч в положении сидя, отмечено увеличение дистанции ходьбы, отсутствовало ограничение возможности подъема на 1 лестничный пролет вверх, ходьбы по пересеченной местности, устранено ограничение возможности спуска на 1 лестничный пролет вниз и сидения на корточках или на коленях. Отмечает исчезновение хруста в коленных суставах при движении, припухлости коленных суставов.
При осмотре: общее состояние удовлетворительное. При осмотре и пальпации коленных суставов: отсутствует локальная гипертермия, припухлость и болезненность при пальпации обоих коленных суставов; при пальпации в период всего движения существенно уменьшается хруст в обоих коленных суставах.
Сгибание/разгибание в коленных суставах справа до 60/175 градусов, слева до 40/180 градусов, боль при максимальном сгибании справа и крепитация с обеих сторон отсутствует.
Данные тестирования по ВАШ: боль в покое - 15 мм (легкая боль), боль при движении - 40 мм (умеренная боль).
Данные тестирования по индексу Лекена: 4 балла (легкая степень тяжести). Данные тестирования по общему индексу WOMAC: 35 мм.
Отмечены положительные изменения в показателях ультразвукового исследования коленных суставов: размер надколенниковой сумки - отсутствует; толщина синовиальной оболочки - 0,2 см, изменений не выявлено; синовит коленных суставов отсутствует. Отмечена положительная динамика следующих показателей крови: СОЭ - 12 мм/ч, С-реактивный белок высокочувствительный - 0,82 мг/л, маркер формирования костного матрикса PINP (N-терминальный пропептид проколлагена 1 типа) - 35,6 нг/мл, остальные показатели регистрировались в пределах референсных значений.
Улучшение данных тестирования боли в коленных суставах способствовало снижению суточной потребности в приеме топического нестероидного противовоспалительного препарата мелоксикам до 2 раз в сутки 3 раза в неделю, начиная со 2 месяца применения пациентом заявляемого хондропротекторного средства. Больной выписан из отделения с диагнозом: Первичный деформирующий полиостеоартрит с преимущественным двусторонним поражением коленных суставов. Рентгенологическая стадия 2. ФНС I степени. Осложнения основного: нет.Сопутствующий: Избыточная масса тела.
Больному рекомендовано: 1) диета с уменьшением потребления соли, приемом пищи каждые 4 часа с основным объемом в обед, нежирные сорта рыбы, мяса, хлеб с отрубями, овощи и фрукты, молочные продукты, холодец и желе, крупы (гречневая, чечевица), приготовление блюд на нерафинированном масле, исключение из меню соленой рыбы, полуфабрикатов, майонеза, чипсов, отказ от спиртных напитков; 2) физические упражнения при остеоартрите коленных суставов; 3) ортезы на коленные суставы; 4) топические формы нестероидных противовоспалительных препаратов по требованию; 5) повторный курс заявляемого хондропротекторного средства через 2 месяца после окончания первого курса терапии; 6) наблюдение травматологом и врачом общей практики поликлиники и оценка эффективности применения заявляемого хондропротекторного средства на поликлиническом этапе лечения в течение 2 месяцев отсутствия терапии заявляемого патент хондропротекторного средства и при проведении повторного курса в течение 2 месяцев.
В процессе мониторирования жалоб пациента, показателей физикального обследования, рентгенологических параметров, показателей ультразвуковой диагностики, параметров биохимического профиля крови, после выполнения режима терапии заявляемым хондропротекторным средством в течение 2 месяцев отмечены значимое снижение выраженности боли, воспаления, функциональных нарушений в суставах и стабилизация всех показателей инструментальных и лабораторных методов исследования. Курс лечения не вызвал нежелательных явлений и побочных эффектов.
Пример 3.
Применение в клинической практике.
Пациент Ч., 52 лет, поступил в медицинский центр «Новомедицина» (г. Ростов-на-Дону) с жалобами на выраженные боли в правом коленном суставе при занятиях фитнесом. Отдых приносил кратковременное облегчение. Отмечал припухлость правого коленного сустава при подъеме и спуске по лестнице. За медицинской помощью не обращался. Самостоятельного лечения не проводил.
Считает себя больным в течение года, когда впервые стал отмечать появление боли в правом коленном суставе при физической нагрузке. Из перенесенных заболеваний: нет частых простудных заболеваний, травм и операций. Профессиональных заболеваний и вредных привычек не имеет. Наследственность не отягощена. Наличие кожных и венерических заболеваний, ревматизма, туберкулеза, нарушений обменных процессов, вирусного гепатита В больной у себя и родственников отрицает. Аллергических реакций на лекарственные препараты и продукты питания не отмечает.Гемотрансфузий не было.
При осмотре: общее состояние удовлетворительное. Сознание ясное, выражение лица спокойное. Телосложение правильное, конституция нормостеническая. Вес 82 кг, рост 178 см, температура тела в подмышечной впадине 36,5°С. ИМТ=25,6 кг/м2. Кожные покровы розового цвета, гиперпигментации не наблюдается, повышенной потливости, сыпи, шелушения, расчесов нет. Гнойников, язв, пролежней и рубцов на коже нет. Влажность кожи умеренная, тургор тканей и эластичность кожи сохранены. Видимые слизистые бледно-розовые, влажные, высыпаний нет, склеры не изменены, иктеричности не наблюдается.
Подчелюстные, затылочные, околоушные, подбородочные, шейные, подключичные, надключичные, подмышечные, локтевые, паховые и подколенные лимфоузлы не пальпируются.
Данные визуального исследования: в легких дыхание везикулярное, хрипов нет, тоны сердца приглушены, ритмичные, акцент II тона над аортой. АД=125/75 мм рт.ст., ЧСС - 82 ударов в минуту, ЧД - 16 в минуту, живот при пальпации безболезненный и мягкий, печень не увеличена. Поясничная область визуально не изменена, симптом поколачивания отрицателен с обеих сторон.
При осмотре и пальпации правого коленного сустава: выявляются локальная гипертермия, припухлость и болезненность при пальпации. Симптом "плавающего надколенника" не определяется. При пальпации в период всего движения хруст в правом коленном суставе не определяется. Сгибание/разгибание в правом коленном суставе до 60/176 градусов, боль при максимальном сгибании справа. Наличия мышечных атрофий не выявлено.
Данные тестирования по ВАШ: боль в покое - 26 мм (умеренная боль), боль при движении - 38 мм (умеренная боль).
Данные тестирования по индексу Лекена: 4 балла (легкая степень тяжести). Данные тестирования по общему индексу WOMAC: 42 мм.
Диагноз: Посттравматический остеоартрит с поражением правого коленного сустава. Рентгенологическая стадия 1. ФНС I степени. Вторичный синовит правого коленного сустава. Осложнения основного: нет. Сопутствующий: нет.
Инструментальные и лабораторные исследования (до терапии).
Рентгенограмма правого коленного сустава: незначительное сужение суставной щели.
Ультразвуковое исследование правого коленного сустава: размер надколенниковой сумки - отсутствует; толщина синовиальной оболочки - 0,3 см, изменений не выявлено; слабовыраженный синовит правого коленного сустава.
Общий анализ крови: СОЭ - 15 мм/ч, показатели клеточного состава крови в пределах референсных значений. Биохимия крови: сывороточный альбумин - 42 г/л, С-реактивный белок высокочувствительный - 3,42 мг/л; ревматоидный фактор (РФ) - 2,18 МЕ/мл, антитела к циклическому цитруллиновому пептиду - 3 Ед/мл, С-концевые телопетиды коллагена I типа (Beta-Cross laps) - 0,284 нг/мл, маркер формирования костного матрикса PINP (N-терминальный пропептид проколлагена 1 типа) - 32,6 нг/мл, аланинаминотрансфераза - 18,6 Ед/л, аспартатаминотрансфераза - 22,4 Ед/л, общий билирубин - 19 мкмоль/л, общий холестерин - 4,22 ммоль/л, холестерин в липопротеинах низкой плотности - 0,68 ммоль/л, креатинин - 74 мкмоль/л, мочевина - 32 ммоль/л, мочевая кислота - 252 мкмоль/л, глюкоза крови натощак - 3,59 ммоль/л, общий кальций - 2,36 ммоль/л. Все лабораторные показатели в пределах референсных значений.
Проводимая терапия. Диета с уменьшением потребления соли, приемом пищи каждые 4 часа с основным объемом в обед, нежирные сорта рыбы, мяса, хлеб с отрубями, овощи и фрукты, молочные продукты, холодец и желе, крупы (гречневая, чечевица), приготовление блюд на нерафинированном масле, исключение из меню соленой рыбы, полуфабрикатов, майонеза, чипсов, отказ от спиртных напитков. Физические упражнения при остеоартрите коленных суставов. Ортез на правый коленный сустав. Пациенту было назначено заявляемое хондропротекторное средство внутрь, содержимое одного пакета-саше (6,0 г) растворяют 150 мл воды, по 1 пакету-саше (6,0 г) 1 раз в сутки в течение 8 недель.
Обследование проводилось по вышеуказанной схеме.
Эффективность проводимого лечения отмечалась через 2 месяца после приема заявляемого хондропротекторного средства и выражалась в следующем. Отмечалось уменьшение субъективной симптоматики остеоартрита правого коленного сустава: отсутствие боли в правом коленном суставе при физической нагрузке, припухлости правого коленного сустава при подъеме и спуске по лестнице.
При осмотре: общее состояние удовлетворительное. При осмотре и пальпации коленных суставов: отсутствует локальная гипертермия, припухлость и болезненность при пальпации обоих коленных суставов. Сгибание/разгибание в коленном суставе справа до 40/180 градусов, боль при максимальном сгибании справа отсутствует.
Данные тестирования по ВАШ: боль в покое - 0 мм (отсутствие боли), боль при движении - 0 мм (отсутствие боли).
Данные тестирования по индексу Лекена: 0 баллов (отсутствует функциональная недостаточность).
Данные тестирования по общему индексу WOMAC: 0 мм.
Отмечены положительные изменения в показателях ультразвукового исследования коленных суставов: размер надколенниковой сумки - отсутствует; толщина синовиальной оболочки - 0,1 см, изменений не выявлено; синовит коленных суставов отсутствует.Все лабораторные показатели оставались в пределах референсных значений.
Больной выписан из отделения с диагнозом: Посттравматический остеоартрит с поражением правого коленного сустава. Рентгенологическая стадия 1. Осложнения основного: нет. Сопутствующий: нет.
Больному рекомендовано: 1) диета с уменьшением потребления соли, приемом пищи каждые 4 часа с основным объемом в обед, нежирные сорта рыбы, мяса, хлеб с отрубями, овощи и фрукты, молочные продукты, холодец и желе, крупы (гречневая, чечевица), приготовление блюд на нерафинированном масле, исключение из меню соленой рыбы, полуфабрикатов, майонеза, чипсов, отказ от спиртных напитков; 2) физические упражнения при остеоартрите коленных суставов; 3) ортез на правый коленный сустав; 4) повторный курс заявляемого хондропротекторного средства через 2 месяца после окончания первого курса терапии; 6) наблюдение травматологом и врачом общей практики поликлиники и оценка эффективности применения заявляемого хондропротекторного средства на поликлиническом этапе лечения в течение 2 месяцев отсутствия терапии заявляемого в данной заявке на патент хондропротекторного средства и при проведении повторного курса в течение 2 месяцев.
В процессе мониторирования жалоб пациента, показателей физикального обследования, рентгенологических параметров, показателей ультразвуковой диагностики, параметров биохимического профиля крови, после выполнения режима терапии заявляемым хондропротекторным средством в течение 2 месяцев отмечены устранение боли, клинических признаков воспаления, функциональных нарушений в суставе и стабилизация всех показателей клинических и инструментальных методов исследования при сохранении показателей лабораторных параметров в пределах референсных значений. Курс лечения не вызвал нежелательных явлений и побочных эффектов.
Далее приводятся обобщенные сведения о проведенных исследованиях клинического использования заявляемого хондропротекторного средства.
Заявляемая композиция комбинированного фармацевтического хондропротектора показала хорошие результаты в клиническом исследовании, данные которого подтверждают терапевтическую эффективность предлагаемого медицинского продукта.
Лечение с использованием заявляемого хондропротекторного средства было проведено в медицинском центре «Новомедицина» г. Ростова-на-Дону в рамках проспективного рандомизированного плацебо-контролируемого исследования у 30 пациентов (группа 1) с диагнозом: Первичный деформирующий полиостеоартрит с преимущественным двусторонним поражением коленных суставов. Рентгенологическая стадия 2. ФНС II степени. Вторичный синовит коленных суставов. Осложнений основного заболевания отмечено не было.
У пациентов группы 1 выявлена следующая сопутствующая патология: избыточная масса тела (n=30), артериальная гипертензия (n=16), хронический тубулоинтерстициальный нефрит, стадия ремиссии (n=5), хронический гастродуоденит, стадия ремисии (n=4). Возраст пациентов группы 1 составил от 54 до 70 лет. Пациенты группы 1 получали композицию заявляемого хондропротекторного средства по 1 пакету - саше (6 г) 1 раз в сутки, предварительно растворив в 100-200 мл воды, в течение 2 месяцев. Пациенты группы 1 не принимали обезболивающих лекарственных средств на протяжении всего клинического исследования.
Также лечение предложенной композицией заявляемого хондропротекторного средства в исследовании проводили 25 пациентов (группа 2) с диагнозом: Посттравматический остеоартрит с поражением правого или левого коленного сустава. Рентгенологическая стадия 1. ФНС I степени. Вторичный синовит правого или левого коленного сустава. Осложнений основного заболевания и сопутствующей патологии у пациентов группы 2 отмечено не было.
Возраст пациентов группы 2 составил от 35 до 50 лет. Пациенты группы 2 получали композицию заявляемого хондропротекторного средства по 1 пакету - саше (6 г) 1 раз в сутки, предварительно растворив в 100-200 мл воды, в течение 2 месяцев.
Пациенты группы 2 не принимали обезболивающих лекарственных средств на протяжении всего клинического исследования.
Контрольную группу в клиническом исследовании составили 22 пациента (группа 3) с первичным деформирующим полиостеоартритом с преимущественным двусторонним поражением коленных суставов (рентгенологическая стадия 2, ФНС II степени, вторичный синовит коленных суставов, n=12), у которых также выявлена сопутствующая патология (избыточная масса тела [n=10], артериальная гипертензия [n=8], хронический тубулоинтерстициальный нефрит, стадия ремиссии [n=2], хронический гастродуоденит, стадия ремисии [n=2]) и посттравматическим остеоартритом с поражением правого или левого коленного сустава (рентгенологическая стадия 1, ФНС I степени, вторичный синовит правого или левого коленного сустава, n=10) без сопутствующей патологии. Все пациенты группы 3 получали плацебо (чистую воду) по 100-200 мл 3 раза в день в течение 2 месяцев. Пациенты контрольной группы принимали топические или пероральные формы нестероидных противовоспалительных препаратов по требованию при возникновении боли. Возраст пациентов группы 3 составил от 34 до 70 лет.
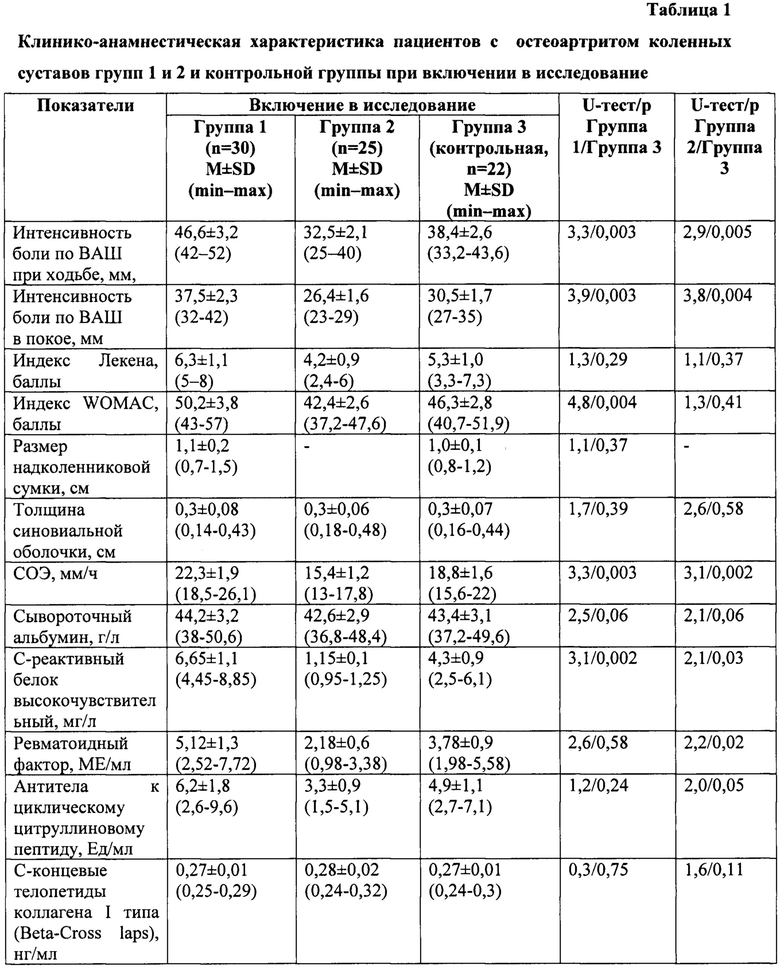
У пациентов группы 1 при включении в исследование отмечались выраженные боли в коленных суставах при ходьбе и физических нагрузках после утренней скованности, менее выраженная боль в коленных суставах в течение ночи, в положении стоя в течение 30 мин и после 2 ч в положении сидя, ограничение дистанции ходьбы, ограничение возможности подъема на 1 лестничный пролет вверх и ходьбы по пересеченной местности при менее выраженном ограничении возможности спуска на 1 лестничный пролет вниз и сидения на корточках или на коленях. Пациенты отмечали хруст в коленных суставах при движении, а также деформацию и припухлость коленных суставов. По данным визуальной аналоговой шкалы (ВАШ), индекса Лекена, индекса WOMAC выявили боли в покое и при движении до умеренной и сильной степени, а также функциональную недостаточность суставов средней степени выраженности и слабовыраженный синовит по данным ультразвукового исследования суставов, увеличение концентрации С-реактивного белка высокочувствительного, маркера формирования костного матрикса PINP (N-терминальный пропептид проколлагена 1 типа) в крови при регистрации остальных лабораторных показателей в пределах референсных значений (Таблица 1). За медицинской помощью пациенты не обращались. Боли в суставах уменьшались при самостоятельном приеме топических и пероральных нестероидных противовоспалительных препаратов 1-2 раза в неделю.
Длительность первичного деформирующего полиостеоартрита с преимущественным двусторонним поражением коленных суставов составила от 5 до 10 лет. Из перенесенных заболеваний пациенты группы 1 отмечали: частые простудные заболевания; травм и операций не было. Профессиональных заболеваний и вредных привычек не имели. Наследственность не отягощена. Наличие кожных и венерических заболеваний, ревматизма, туберкулеза, нарушений обменных процессов, вирусного гепатита у себя и родственников отрицали. Аллергических реакций на лекарственные препараты и продукты питания не отмечали. Гемотрансфузий не было. ИМТ у пациентов группы 1 составил 27,5±1,7 кг/м2.
При осмотре и пальпации коленных суставов у пациентов группы 1 выявлялась варусная деформация, локальная гипертермия, припухлость и болезненность при пальпации обоих коленных суставов. Симптом "плавающего надколенника" не определялся. При пальпации в период всего движения определялся хруст в обоих коленных суставах.
Сгибание/разгибание в коленных суставах справа до 90/170 градусов, слева до 60/175 градусов, крепитация с обеих сторон. Наличия мышечных атрофии не выявили.
У пациентов группы 2 отмечались жалобы на выраженные боли в правом или левом коленном суставе при занятиях фитнесом. Отдых приносил кратковременное облегчение. Отмечали припухлость правого/левого коленного сустава при подъеме и спуске по лестнице. По данным визуальной аналоговой шкалы (ВАШ), индекса Лекена, индекса WOMAC выявили выраженность боли в покое и при движении до умеренной степени, а также функциональную недостаточность суставов легкой степени выраженности и отсутствие синовита по данным ультразвукового исследования суставов, все лабораторные показатели оставались в пределах референсных значений (Таблица 1). За медицинской помощью пациенты группы 2 не обращались и самостоятельного лечения не проводили.
Длительность посттравматического остеоартрита с поражением правого или левого коленного сустава у пациентов группы 2 составила от 1 месяца до 1 года. Из перенесенных заболеваний не отмечали частых простудных заболеваний, а также травм и операций. Профессиональных заболеваний и вредных привычек не имели. Наследственность не отягощена. Наличие кожных и венерических заболеваний, ревматизма, туберкулеза, нарушений обменных процессов, вирусного гепатита у себя и родственников отрицали. Аллергических реакций на лекарственные препараты и продукты питания не отмечали. Гемотрансфузий не было. ИМТ у пациентов группы 2 составил 25,6±1,4 кг/м2.
При осмотре и пальпации правого/левого коленного сустава у пациентов группы 2 выявляли локальную гипертермию, припухлость и болезненность при пальпации. Симптом "плавающего надколенника" не определялся. При пальпации в период всего движения хруст в правом/левом коленном суставе не определялся. Сгибание/разгибание в правом/левом коленном суставе до 60/176 градусов, боль при максимальном сгибании справа или слева. Наличия мышечных атрофий не выявлено.
У пациентов группы 3 отмечались жалобы на выраженные боли в правом и/или левом коленном суставе в покое и при движениях, при занятиях фитнесом. Отдых приносил кратковременное облегчение у части пациентов (n=10). Отмечали у всех пациентов припухлость правого/левого коленного сустава при подъеме и спуске по лестнице. По данным визуальной аналоговой шкалы (ВАШ), индекса Лекена, индекса WOMAC выявили выраженность боли в покое и при движении до умеренной и сильной степени, функциональную недостаточность суставов легкой средней степени выраженности, слабовыраженный синовит по данным ультразвукового исследования суставов, а также увеличение концентрации С-реактивного белка высокочувствительного, маркера формирования костного матрикса PINP (N-терминальный пропептид проколлагена 1 типа) в крови при регистрации остальных лабораторных показателей в пределах референсных значений (Таблица 1). За медицинской помощью пациенты группы 3 не обращались и самостоятельного лечения не проводили.
Длительность остеоартрита с поражением правого/ левого коленного сустава у пациентов группы 3 составила от 1 месяца до 10 лет. Из перенесенных заболеваний не отметили частых простудных заболеваний, травм и операций. Профессиональных заболеваний и вредных привычек не имели. Наследственность не отягощена. Наличие кожных и венерических заболеваний, ревматизма, туберкулеза, нарушений обменных процессов, вирусного гепатита В пациенты у себя и родственников отрицали. Аллергических реакций на лекарственные препараты и продукты питания не отмечали. Гемотрансфузий не было. ИМТ у пациентов 2 группы составил 26,8±1,6 кг/м2.
При осмотре и пальпации правого/левого коленного сустава у пациентов группы 3 выявлялись локальная гипертермия, припухлость и болезненность при пальпации. Симптом "плавающего надколенника" не определялся. При пальпации в период всего движения у части пациентов определялся хруст в правом/левом коленном суставе (n=12), у части пациентов (n=10) не определялся хруст в суставах. У части пациентов (n=12) сгибание/разгибание в коленных суставах справа до 90/170 градусов, слева до 60/175 градусов, крепитация с обеих сторон, у другой части пациентов (n=10) сгибание/разгибание в правом/левом коленном суставе до 60/176 градусов, боль при максимальном сгибании справа или слева. Наличия мышечных атрофий не выявили.
По данным рентгенографии коленных суставов при включении в исследование у пациентов в группах 1 и 3 с первичным деформирующим полиостеоартритом с преимущественным двусторонним поражением коленных суставов выявили незначительное сужение суставной щели, субхондральный склероз, мелкие краевые остеофиты, у пациентов в группах 2 и 3 с посттравматическим остеоартритом с поражением правого или левого коленного сустава зарегистрировали незначительное сужение суставной щели.
Пациентам всех групп рекомендовали диету с уменьшением потребления соли, приемом пищи каждые 4 часа с основным объемом в обед, нежирные сорта рыбы, мяса, хлеб с отрубями, овощи и фрукты, молочные продукты, холодец и желе, крупы (гречневая, чечевица), приготовление блюд на нерафинированном масле, исключение из меню соленой рыбы, полуфабрикатов, майонеза, чипсов, отказ от спиртных напитков, а также ношение ортезов на коленные суставы согласно Федеральным клиническим рекомендациям МЗ РФ по диагностике и лечению остеоартроза от 2016 г.
Эффективность проведенного лечения отмечалась через 2 месяца после приема заявляемого хондропротекторного средства и выражалась в следующем. У пациентов группы 1 отмечалось уменьшение субъективной симптоматики остеоартрита коленных суставов: уменьшение выраженности боли в коленных суставах при ходьбе и физических нагрузках, утренней скованности, отсутствовала боль в коленных суставах в течение ночи, в положении стоя в течение 30 мин и после 2 ч в положении сидя, отмечено увеличение дистанции ходьбы, отсутствовало ограничение возможности подъема на 1 лестничный пролет вверх, ходьбы по пересеченной местности, устранено ограничение возможности спуска на 1 лестничный пролет вниз и сидения на корточках или на коленях. Пациенты отмечали исчезновение хруста в коленных суставах при движении, припухлости коленных суставов. При осмотре и пальпации коленных суставов пациентов группы 1 отсутствовала локальная гипертермия, припухлость и болезненность при пальпации обоих коленных суставов; при пальпации в период всего движения существенно уменьшался хруст в обоих коленных суставах. Сгибание/разгибание в коленных суставах справа до 60/175 градусов, слева до 40/180 градусов, боль при максимальном сгибании справа и крепитация с обеих сторон отсутствовала.
Эффективность проведенного лечения показали у пациентов группы 2 через 2 месяца после приема заявляемого хондропротекторного средства: отмечали уменьшение субъективной симптоматики остеоартрита правого/левого коленного сустава: отсутствие боли в правом коленном суставе при физической нагрузке, припухлости правого коленного сустава при подъеме и спуске по лестнице. У пациентов группы 2 отсутствовала локальная гипертермия, припухлость и болезненность при пальпации обоих коленных суставов. Сгибание/разгибание в коленном суставе справа до 40/180 градусов, боль при максимальном сгибании справа отсутствовала. Зарегистрировали уменьшение выраженности болевого синдрома и функциональной недостаточности суставов у пациентов групп 1 и 2 на фоне терапии композицией заявляемого хондропротекторного средства в течение 2 месяцев в сравнении с пациентами контрольной группы (Таблица 2). Отметили эффективность терапии композицией заявляемого хондропротекторного средства в течение 2 месяцев у пациентов групп 1 и 2 в сравнении с пациентами контрольной группы в отношении показателей ультразвукового исследования суставов (Таблица 2). В результате проведенного лечения у пациентов групп 1 и 2 выявили положительную динамику лабораторных показателей крови, значения которых по истечении 2 месяцев терапии новым медицинским продуктом находились в пределах физиологического референсного диапазона по сравнению со значениями аналогичных показателей в контрольной группе (Таблица 2).

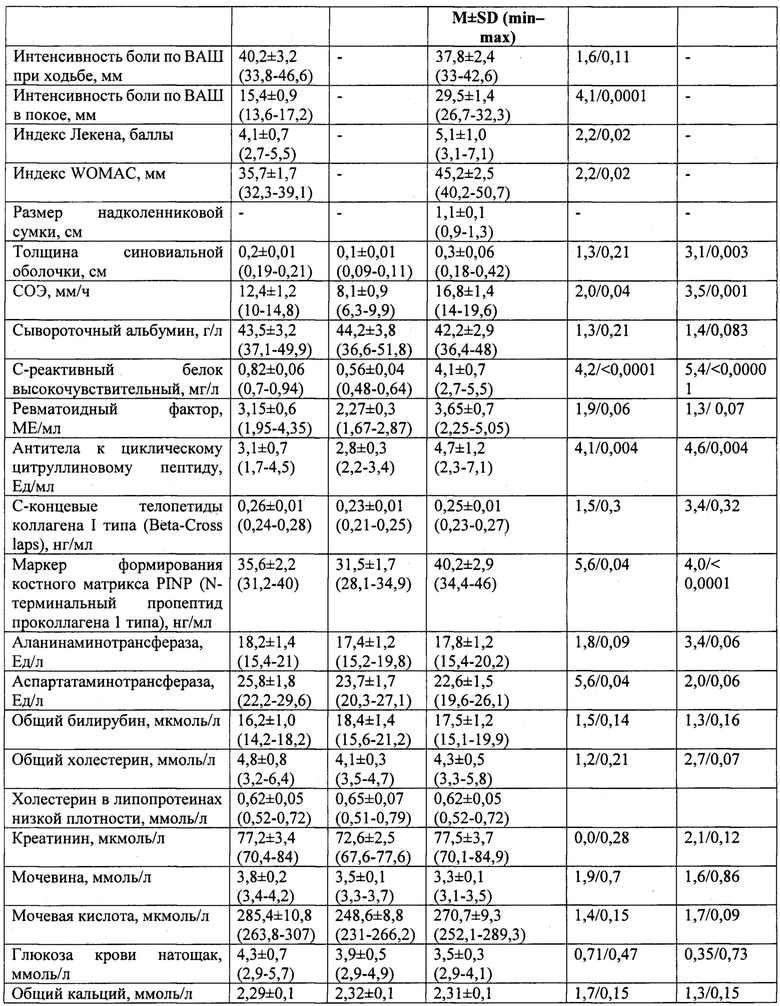

Всем пациентам исследуемых групп 1 и 2 рекомендовали: 1) диету с уменьшением потребления соли, приемом пищи каждые 4 часа с основным объемом в обед, нежирные сорта рыбы, мяса, хлеб с отрубями, овощи и фрукты, молочные продукты, холодец и желе, крупы (гречневая, чечевица), приготовление блюд на нерафинированном масле, исключение из меню соленой рыбы, полуфабрикатов, майонеза, чипсов, отказ от спиртных напитков; 2) физические упражнения при остеоартрите коленных суставов; 3) ортезы на коленные суставы; 4) повторный курс композицией заявляемого хондропротекторного средства через 2 месяца после окончания первого курса терапии; 5) наблюдение травматологом и врачом общей практики поликлиники и оценка эффективности применения заявляемого хондропротекторного средства на поликлиническом этапе лечения в течение 2 месяцев отсутствия терапии заявляемым хондропротекторным средством и при проведении повторного курса в течение 2 месяцев.
Таким образом, в процессе мониторирования жалоб пациента, показателей физикального обследования, рентгенологических параметров, показателей ультразвуковой диагностики, лабораторных параметров крови, после выполнения режима терапии заявляемым хондропротекторным средством в течение 2 месяцев у пациентов с первичным деформирующим полиостеоартритом с преимущественным двусторонним поражением коленных суставов и с посттравматическим остеоартритом с поражением правого или левого коленного сустава отметили значимое снижение выраженности боли, воспаления, функциональных нарушений в суставах и стабилизацию всех показателей инструментальных и лабораторных методов исследования при сохранении показателей лабораторных параметров в пределах физиологических референсных значений. Курс лечения не вызвал нежелательных явлений и побочных эффектов.
Подводя общий итог, следует отметить, что заявляемое новое хондропротекторное средство обладает высокой эффективностью в профилактике и лечении патологий опорно-двигательной системы, выполнено в удобной для применения лекарственной форме порошка, производство которой не требует значительных временных и финансовых затрат, характеризуется простым для пациента курсом с однократным приемом в течение суток, что в целом свидетельствует о широких перспективах для его использования.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ ХОНДРОПРОТЕКТОРНОГО ДЕЙСТВИЯ | 2016 |
|
RU2648641C2 |
| СПОСОБ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА И ПОСТТРАВМАТИЧЕСКИХ БОЛЕВЫХ СИНДРОМОВ | 2004 |
|
RU2274472C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНО-ДИСТРОФИЧЕСКИХ ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА И ПОСТТРАВМАТИЧЕСКИХ БОЛЕВЫХ СИНДРОМОВ | 2010 |
|
RU2433844C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЕГЕРАТИВНО-ДИСТРОФИЧЕСКИХ ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА И ПОСТТРАВМАТИЧЕСКИХ СПАЕЧНЫХ ПРОЦЕССОВ | 2010 |
|
RU2436584C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНО-ДИСТРОФИЧЕСКИХ ЗАБОЛЕВАНИЙ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА И ПОСТТРАВМАТИЧЕСКИХ СПАЕЧНЫХ ПРОЦЕССОВ | 2006 |
|
RU2299733C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ОСТЕОАРТРИТА, ОСТЕОПОРОЗА И ОСТЕОАРТРОЗА СУСТАВОВ | 2013 |
|
RU2521227C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ОСТЕОАРТРИТА И ОСТЕОАРТРОЗА СУСТАВОВ | 2011 |
|
RU2509569C2 |
| КОМБИНИРОВАННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АРТРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2024 |
|
RU2827069C1 |
| НАРУЖНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ СУСТАВОВ И МЯГКИХ ТКАНЕЙ | 2007 |
|
RU2377974C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АРТРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ В ЛИОФИЛИЗИРОВАННОЙ ФОРМЕ ДЛЯ ИНЪЕКЦИЙ | 2024 |
|
RU2827073C1 |
Группа изобретений относится к фармацевтической промышленности, а именно к средству хондропротекторного действия и способу хондропротекторного воздействия на опорно-двигательную систему человека. Средство хондропротекторного действия, которое содержит в качестве активных компонентов глюкозамина сульфат, хондроитина сульфат, неденатурированный коллаген II типа и вспомогательные вещества при следующем соотношении активных компонентов на 1 порошок-саше: глюкозамина сульфат 1200-1800 мг, хондроитина сульфат 960-1440 мг, неденатурированный коллаген II типа 40-48 мг. Способ хондропротекторного воздействия на опорно-двигательную систему человека, включающий введение вышеописанного средства в количестве 1 порошка-саше однократно в сутки общим курсом 6-8 недель. Вышеописанная группа изобретений расширяет арсенал средств хондропротекторного действия, средство обладает оптимизированным составом активных компонентов, характеризуется повышенной эффективностью хондропротекторного действия, при этом снижена химическая нагрузка на организм пациента; уменьшено необходимое количество приемов средства в течение суток. 2 н. и 6 з.п. ф-лы, 2 табл., 3 пр.
1. Средство хондропротекторного действия, которое содержит в качестве активных компонентов глюкозамина сульфат, хондроитина сульфат, неденатурированный коллаген II типа и вспомогательные вещества при следующем соотношении активных компонентов на 1 порошок-саше:
2. Средство хондропротекторного действия по п. 1, в котором неденатурированный коллаген II типа присутствует в составе натурального неденатурированного коллагена, содержащегося в количестве 333-400 мг.
3. Средство хондропротекторного действия по любому из пп. 1, 2, включающее вспомогательные вещества в виде носителя и по меньшей мере одного из следующих компонентов: регулятора кислотности, ароматизатора пищевого, антислеживающегося агента, подсластителя.
4. Средство хондропротекторного действия по п. 3, характеризующееся следующим соотношением компонентов на 1 порошок-саше:
5. Средство хондропротекторного действия по любому из пп. 3, 4, включающее носитель в виде палатинозы, регулятор кислотности в виде лимонной кислоты, антислеживающийся агент в виде кремния диоксида, подсластитель в виде сукралозы при следующем соотношении компонентов на 1 порошок-саше:
6. Средство хондропротекторного действия по п. 5, характеризующееся следующим соотношении компонентов на 1 порошок-саше:
7. Способ хондропротекторного воздействия на опорно-двигательную систему человека, включающий введение средства по любому из пп. 1-6 в количестве 1 порошка-саше однократно в сутки общим курсом 6-8 недель.
8. Способ по п. 7, отличающийся тем, что порошок-саше перед употреблением разводят в 100-200 мл воды и затем принимают внутрь.
| Всасывающе-нагнетательное устройство для передвижения судов | 1925 |
|
SU1800A1 |
| NBL GLUKOZAMİN KONDROİTİN MSM, Найдено в | |||
Авторы
Даты
2024-02-13—Публикация
2022-09-09—Подача