Изобретение относится к области фармацевтической химии и касается способов качественного определения биологически активных веществ, в частности содержания флавоноидов - кверцетина и его основных производных (флавандиона и бензофуранона) в экстракте калины красной (Viburnum Opulus L.). Способ представляется собой двух стадийный процесс, включающий в себя стадию кислородонасыщения и стадию регистрации спектрального отклика (люминесценции). Наночастицы золота с флавоноидами формируют люминесцентные комплексы, которые в результате фотохимических радикальных реакций с участием молекул кислорода испускают люминесценцию, характерную основным производным кверцетина. Вместе с тем плазмонные свойства наночастиц золота увеличивают интенсивность люминесценции флавоноидов при фотовозбуждении длиной волны 400 нм. Изобретение может быть использовано в области пищевых биотехнологий, медицине и фармацевтике в качестве метода определения отдельных компонентов флавоноидной природы в составе сочного растительного сырья.
Кверцетин является наиболее распространенным соединением класса флавоноидов, он является сильным антиоксидантом, что обеспечивает его широкое практическое применение. Поэтому идентификация продуктов окисления кверцетина в растительных экстрактах крайне важна.
Известны работы, являющиеся предпосылками заявляемого изобретения. Нижеприведенные примеры, которые составляют часть предпосылок заявляемого изобретения и/или раскрывают методики, которые можно применять к некоторым аспектам заявляемого изобретения.
Кверцетин, согласно литературным данным, чаще всего определяют несколькими аналитическими методами, включая высокоэффективную жидкостную хроматографию с детектированием в УФ-видимой области (ВЭЖХ-УФ), высокоэффективную тонкослойную хроматографию (ВЭТСХ), инфракрасное преобразование Фурье (ФП-ИК). Так, в работе (Tugba Dursun Capar, Tugba Dedebas, Hasan Yalcin, Lutfiye Ekici. Extraction method affects seed oil yield, composition, and antioxidant properties of European cranberrybush (Viburnum opulus). Industrial Crops & Products. 2021, 168, 113632) было исследовано содержание активных веществ в составе семечек калины физико-химическими и спектральными (ИК-Фурье) методами. Экстракцию масла семечек проводили с использованием экстрактора Сокслета в диэтиловом эфире. Авторы показали, что увеличение времени экстракции приводит к увеличению количества масла примерно в 6 раз. Авторы установили наличие различных жирных кислот в составе масла используя различные методы экстракции (ультразвуковая, микроволновая экстракция и экстракция с использованием Сокслета). Так было выявлено наличие лауриновой, миристиновой, пальмитиновой, стеариновой, олеиновой, линолевой кислот и других.
В работе (Koray Ozrenk, Gulce Ilhan, Halil Ibrahim Sagbas, Neva Karatas, Sezai Ercisii, Aysen Melda Colak. Characterization of European cranberrybush (Viburnum opulus L.) genetic resources in Turkey. Scientia Horticulturae. 2020, 273, 109611) были исследованы морфологические особенности ягод (урожайность с куста, средний диаметр ягод и пр.), был проведен биохимический анализ рефлектометрия ягод калины. Было установлено количественное определение флавоноидов (кверцетин глюкозид и кверцетин-3-глюкозид) в плодах калины. Так содержание данных веществ в экстракте калины, произрастающей в Турции составляло в среднем 4 мг/100 г. Так же было определено общее содержание фенолов, которое составляло 700-800 мг/100 г.
В работе (Зенкевич И.Г., Пушкарева Т.И. О моделировании механизма образования димерных продуктов окисления флавоноидов. Химия растительного сырья. 2018, №3, 185-197. http://jounal.asu.ru/cw/article/view/3589) окисление флавоноидов проводили бар-ботированием воздуха через раствор, содержащий флавоноиды со скоростью ~2 л/мин в течение четырех часов при рассеянном люминесцентном освещении и последующего контакта с воздухом в течение суток без перемешивания, после того, как продуктов окисления обнаружено не было, для активации окисления в систему добавили водный раствор аммиака (10%) до рН ~10 и дополнительно барботировали воздух в течение часа. Для детектирования продуктов окисления применяли в ВЭЖХ электрохимические детекторы. При этом, в отличие от химических процессов, степень конверсии аналитов можно регулировать, изменяя потенциалы на электродах электрохимической ячейки. Авторы использовали ячейку ROXI, специально предназначенную для включения в системы ВЭЖХ-МС, что позволило детектировать и идентифицировать продукты окисления фактически одновременно с их генерированием.
Известна работа (So-Hyeon Hwang, Laura Rojas Lorz, Dong-Keun Yi, Jin Kyoung Noh, Young-Su Yi, Jae Youl Cho. Viburnum pichinchense methanol extract exerts antiinflammatory effects via targeting the NF-κB and caspase-11 non-canonical inflammasome pathways in macrophages. Journal of Ethnopharmacology. 2019, 245, 112161, https://doi.org/10.1016/i.jep.2019.l12161), в которой методом ВЭЖХ идентифицировали кверцетин, наряду с другими составляющими (ресвератрол, лютеолин, кемпферол), как противовоспалительный компонент в спиртовом экстракте плодов калины.
В работе (Ayca Aktas Karacelik, Murat Kucuk, Zeynep Iskefiyeli, Sezgin Aydemir, Seppe De Smet, Bram Miserez, Patrick Sandra. Antioxidant components of Viburnum opulus L. determined by on-line HPLC-UV-ABTS radical scavenging and LC-UV-ESI-MS methods, Food Chemistry, 2015, 175, 106-114, doi.org/10.1016/j.foodchem.2014.11.085) впервые проведен анализ сока, семян и экстрактов кожуры плодов V. opulus в отношении антиоксидантной композиции на основе ранее использовавшегося онлайн-анализа ВЭЖХ-ДФПГ и недавно использованного анализа ВЭЖХ-ABTS. Общая антиоксидантная способность определялась тремя антиоксидантными тестами: ABTS удаление радикалов, антиоксидантная способность, снижающая содержание железа (FRAP), и определение общего содержания фенолов с помощью реагента Фолина для сока и экстрактов его семян и кожицы, приготовленных с использованием метанола, ацетонитрила и воды. Образцы также были оценены на наличие в них отдельных антиоксидантов на основе онлайн-анализов ВЭЖХ-ABTS/DPPH, в которых используются постколоночные реакции, которые можно отслеживать с помощью обнаружения в УФ-видимой области. Сравнивали результаты онлайн и офлайн анализов антиоксидантной активности ABTS. Наконец, предварительная идентификация наиболее важных антиоксидантов в соке была проведена с помощью ЖХ-УФ-ЭСИ-МС.
Авторы работы (Javid Hussain, Najeeb Ur Rehman, Fazal Mabood, Ahmed Al-Harrasi, Liaqat Ali, Tania Shamim Rizvi, Ajmal Khan, Kashif Rafiq, Hamida Al-Rabaani, Farah Jabeen. Application of fluorescence spectroscopy coupled with PLSR for the estimation of quercetin in four medicinal plants, Chemical Data Collections. 2019, 21, 100228, https://doi.org/10.1016/j.cdc.2019.100228) предлагают использовать метод флуоресцентной спектроскопии в сочетании с PLSR. В своем исследовании оценка кверцетина в метанольных экстрактах четырех лекарственных растений, включая Amaranthus cruentus, Berberis calliobotrys, Solanum muricatum и Ribes himalense, была проведена с помощью разработанного метода флуоресцентной спектроскопии в сочетании с PLSR. Полученные результаты показали, что метанольный экстракт R.. himalense показал более высокое содержание кверцетина (3,83±0,01%), за которым следуют B. calliobotrys (1,91±0,01%), A eruentus (1,83±0,02%) и S. muricatum (0,87±0,05%). Эти результаты также были проверены с помощью УФ-видимой спектроскопии, и было обнаружено, что они очень близки к методу флуоресценции.
Много внимания уделяется не только качественному и количественному определению флавоноидов, но и их антиоксидантной активности. Изучению именно фенольных веществ калины и их активности посвящены работы Mi-Yeon Kim, Kunihisa Iwai, в частности в исследовании (Mi-Yeon Kim, Kunihisa Iwai, Hajime Matsue. Phenolic compositions of Viburnum dilatatum Thunb. fruits and their antiradical properties. Journal of Food Composition and Analysis, 2005, 18, 789-802, https://doi.org/10.1016/j.jfca.2004.09.009) было установлено с помощью ЯМР и жидкостной хроматографии/масс-спектрометрии/МС, пять основных фенольных соединений плодов Viburnum: цианидин-3-глюкозид (Су-3-sam), цианидин-3-глюкозид (Cy-3-glc), 5-O-кофеоил-4-метоксилхинная кислота (4-МеО-5-CQA), кверцетин и хлорогеновая кислота (5-КАК). Эти концентрации в плодах составляли по порядку 5-CQA, 4-MeO-5-CQA, Cy-3-sam, кверцетин и Cy-3-glc, а их общее содержание равнялось 42,4% от общего количества полифенолов. По методу ЭПР активность по удалению супероксидных анион-радикалов располагалась в следующем порядке: Су-3-sam, 4-MeO-5-CQA, Cy-3-glc, 5-CQA, кверцетин; активность в отношении гидроксильных радикалов была в порядке Cy-3-sam, 5-CQA, кверцетин, 4-MeO-5-CQA, Су-3-glc. Исследования доказали, что эти фенольные соединения, обуславливают антирадикальную активности и физиологические эффекты плодов калины.
Не только кверцетин, но и продукты его окисления могут обладать антиокислительными свойствами. Данный вопрос рассматривается Атала Э. с соавторами в работе (Атала Э., Фуэнтес Дж., Верхан М. Дж., Спейски X. Кверцетин и родственные ему флавоноиды сохраняют свои антиоксидантные свойства, несмотря на химическое или ферментативное окисление. Пищевая химия. 2017. 234, 479-485. doi: 10.1016/j.foodchem.2017.05.23).
Широко известен эффект усиления флуоресценции комплексов кверцетина (Qu) с наночастицами серебра. Именно этому посвящено исследование (Ping Liu, Liangliang Zhao, Xia Wu, Fei Huang, Minqin Wang, Xiaodan Liu, Fluorescence enhancement of quercetin complexes by silver nanoparticles and its analytical application, Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2014, 122, 238-245, doi.org/10.1016/j.saa.2013.11.055). В работе авторы описывают эффективное усиливающее действие наночастиц Ag на флуоресценцию системы Qu-нуклеиновой кислоты. Комплексную систему, содержащую наночастицы в сочетании с Qu, использовали для определения нуклеиновых кислот в растворе и в агарозном геле. В отличие от системы без наночастиц Ag флуоресценция системы AgNPs-fsDNA-Qu показала явный синергетический эффект усиления. Кроме того, механизм взаимодействия системы AgNPs-fsDNA-Qu был изучен с использованием нескольких методов, включая флуоресцентную спектрометрию, флуоресцентную поляризацию (FP), УФ-видимую спектрометрию, круговой дихроизм (CD) и просвечивающую электронную микроскопию (ТЕМ).
Авторы работы (Liliya О. Usoltseva, Tatiana О. Samarina, Sergei S. Abramchuk, Aleksandra F. Prokhorova, Mikhail K. Beklemishev, Selective Rayleigh light scattering determination of trace quercetin with silver nanoparticles, Journal of Luminescence, 2016, 179, 438-444, doi.org/10.1016/j.jlumin.2016.07.020) предлагают способ обнаружения кверцетина также с использованием раствора наночастиц серебра. Рэлеевское светорассеяние (RLS) представляет собой метод с высоким потенциалом чувствительного определения малых органических молекул. Авторы обнаружили, что количество кверцетина (Qu) в миллиардных долях значительно увеличивает RLS раствора наночастиц серебра (AgNP), стабилизированного бромидом цетилтриметиламмония или н-додецилсульфатом натрия. Усиление светорассеяния наблюдается только в присутствии избытка AgNO3, что позволяет предположить, что оно является результатом роста наночастиц; другой причиной усиленного рассеяния является агрегация наночастиц Ag аналитом, что было подтверждено методом динамического светорассеяния.
Представленные выше результаты исследований указывают на большой интерес к вопросу изучения и определения флавоноидов в сложных органических системах. Но как можно заметить, у рассмотренных способов имеется ряд недостатков: все они требуют использование дополнительных химических реактивов, экстрагентов, дорогостоящего оборудования. Являются более затратными, по сравнению с предлагаемым решением по ресурсам и времени.
На основании анализа вышеизложенных результатов можно сделать вывод, что флуоресцентная спектроскопия является альтернативой ВЭЖХ-УФ, высокоэффективной тонкослойной хроматографии (ВЭТСХ), инфракрасному преобразование Фурье (ФП-ИК) для оценки флавоноидов, в частности кверцитина в растительных экстрактах. Метод фоточувствительной флуоресцентной спектроскопии является точным и надежным.
Известны изобретения, которые, на наш взгляд, так или иначе соприкасаются с тематикой заявленного изобретения.
Авторы изобретения «Способ количественного определения флавоноидов в желчегонном сборе №3» (Патент RU 2554780 С1), предлагают определение флавоноидов выполнять методом дифференциальной спектрофотометрии, в пересчете на цинарозид, при длине волны 400 нм. При проведении анализа измеряют оптическую плотность комплекса флавоноидов с алюминием хлоридом анализируемого раствора на фоне исходного раствора. В результате наблюдается батохромный сдвиг полосы поглощения флавоноидов, который обнаруживается в спектре в виде максимума поглощения на длине волны 406 нм. Изучение спектров чистого цинарозида показало, что раствор в присутствии алюминия хлорида имеет близкий максимум поглощения (на длине волны 400 нм). Следовательно, цинарозид может быть использован в методике анализа в качестве стандартного образца. Содержание суммы флавоноидов в пересчете на цинарозид и абсолютно сухое сырье в процентах вычисляют с использованием формулы.
Известно изобретение (патент RU 2358475 С1), в котором в качестве экстрагента используют молочную сыворотку для получения экстракта калины. Экстракцию проводят при температуре 40°С в течение 1 ч - 1 ч 30 мин. Изобретение позволяет получить экстракт с повышенной биологической активностью и высокими органолептическими показателями. Способ получения экстракта на основе молочной сыворотки с использованием растительного сырья, включает измельчение растительного сырья, экстрагирование молочной сывороткой и фильтрацию, отличается тем, что в качестве растительного сырья используют дикорастущие ягоды калины, а экстрагирование измельченной мезги молочной сывороткой осуществляют при следующих технологических режимах: ξ=1:20-1:30; τ=1 ч - 1 ч 30 мин; Т=40°С, где ξ - гидромодуль растворителя; τ - время экстрагирования; Т - температура экстрагирования.
К недостаткам данного изобретения можно отнести использование специфичного, не стабильного по составу экстрагента, использование которого может привести к потере в ходе пробоподготовки флуоресцирующих соединений ягод калины.
Прототипом данного изобретения является изобретение является изобретение «Вольтамперометрический способ количественного определения суммарного содержания флавоноидов в растительном сырье» (Патент RU 2441224 С1). Изобретение относится к области фармацевтической химии и касается способов количественного определения биологически активных веществ, в частности суммарного содержания флавоноидов -веществ с выраженными антиоксидантными свойствами. Представленный метод состоит в измерении вольт-амперных характеристик растительного сырья в буферном растворе (рН=6.86) с регистрацией анодного пика окисления веществ. Суммарная концентрация флавоноидов определялась относительно насыщенного хлорид-серебряного электрода. В качестве примера использования данного метода авторы приводят два эксперимента по определению суммарного содержания флавоноидов: 1 - в субстанции методом циклической вольтамперометрии и 2) - в листьях брусники. Анодный пик регистрируют при потенциале +0.3 В. В результате первого эксперимента концентрацию суммарного содержания флавоноидов в аликвоте 1% раствора (рутина, кверцетина, дигидрокверцетина, катехина в равных пропорциях) в воде объемом 0.5 мл определяли по высоте анодного пика методом градуировочного графика, построенного по стандартным растворам одного из флавоноидов (например, дигидрокверцетина) с точно известными концентрациями, измеряя высоту полученного анодного пика. В результате второго эксперимента в тех же условиях снимают вольтамперограмму. Анодный пик регистрируют при потенциале +0.3 В. Концентрацию суммарного содержания флавоноидов определяют методом градуировочного графика, построенного по стандартным растворам одного из флавоноидов (например, дигидрокверцетина) с точно известными концентрациями, измеряя высоту полученного анодного пика на вольтамперограмме.
Несовершенство данного изобретения заключается в недостаточности сведений о влиянии на антиоксидантные свойства флавоноидов таких факторов как рН среды, природы самих антиоксидантов, растворителя и др.
Недостаточно изученными факторами являются эффективная концентрация антиоксидантов, время их активного действия и совместимость компонентов в смесях антиоксидантов. Поверхностно-активные вещества, сопутствующие антиоксидантам в объектах искусственного и природного происхождения, оказывают основное мешающее влияние в вольтамперометрическом анализе.
Задачей заявляемого изобретения является разработка способа регистрации флавоноидов калины красной спектрально-люминесцентным методом с предварительным кислородонасыщением раствора экстракта в присутствии плазмонного резонанса наночастиц золота.
Поставленная задача решается тем, что подготовленный раствор экстракта со стабилизирующей оболочной биополимера(хитозан) в присутствии наночастиц золота размером 45 нм сначала насыщается молекулами кислорода концентрацией С=6⋅10-3 моль. Далее выполняется запись спектра люминесценции в видимо диапазоне длин волн при возбуждении λ=400 нм. Появление максимума на длине волны λ=590 нм помимо основного спектрального максимума на λ=480 нм свидетельствует о люминесценции кверцетина и его основных производных в составе экстракта.
Заявленный способ позволяет получать сведения о содержании кверцетина в растворах растительных экстрактов.
Заявленный способ основан на процессе окисления флавоноидов калины красной и регистрации люминесценции продуктов окисления с усилением сигнала люминесценции за счет плазмонной энергии наночастиц золота, допированных в раствор экстракта с биополимерной стабилизирующей оболочкой (хотозан).
Приготовление водно-спиртового экстракта ягод калины Viburnum opulus L на кремовой основе проводили следующим образом.
Свежие ягоды калины массой 213 г измельчали в ступке, затем полученную массу отжимали. К полученному соку добавляли равное количество водно-этанольного раствора в соотношении этанола и дистиллированной воды 3:7, экстракцию вели в течение 48 часов при комнатной температуре. Полученный экстракт неоднократно пропускали через бумажные фильтры до получения прозрачной жидкости ярко-красного цвета, из которой после отстаивания в течение 24 часов не выпадал осадок. К полученному раствору экстракта добавляли раствор гидрозоля наночастиц золота, полученных методом наносекундной лазерной абляции на установке Solar Laser System (Беларусь), работающей в режиме модуляции добротности при следующих параметрах лазерного излучения: длина волны 532 нм, длительность импульса 10 не, частота 15 Гц, энергия импульса 20 мкДж. Время одного сеанса абляции составляло 5 минут. Объем раствора за один сеанс абляции составлял V=1,2 мл. После процесса абляции раствор приобрел розовый цвет. Средний гидродинамический радиус полученных наночастиц был исследован методом фотонно-корреляционной спектроскопии (Photocor-Compact Z) и составлял 40 нм.
Далее к полученному раствору экстракта с наночастицами золота был добавлен раствор хитозана с молекулярной массой М=87 кДа и степенью деацетилирования 83%. Раствор хитозана (ω=2%) был приготовлен в 2% растворе щавелевой кислоты с использованием магнитной мешалки при 1000 об/мин. Уровень кислотности раствора хитозана составял рН≈3.5. Эталонный раствор экстракта калины в хитозане готовили следующим образом: экстракт смешивали с раствором хитозана в соотношении 1:1 с добавлением 0,5 мл дистиллированной воды.
При приготовлении образца с наночастицами золота данный объем воды был заменен на раствор гидрозоля абляционных наночастиц золота (объемом 0,5 мл) концентрацией С=10-9 М.
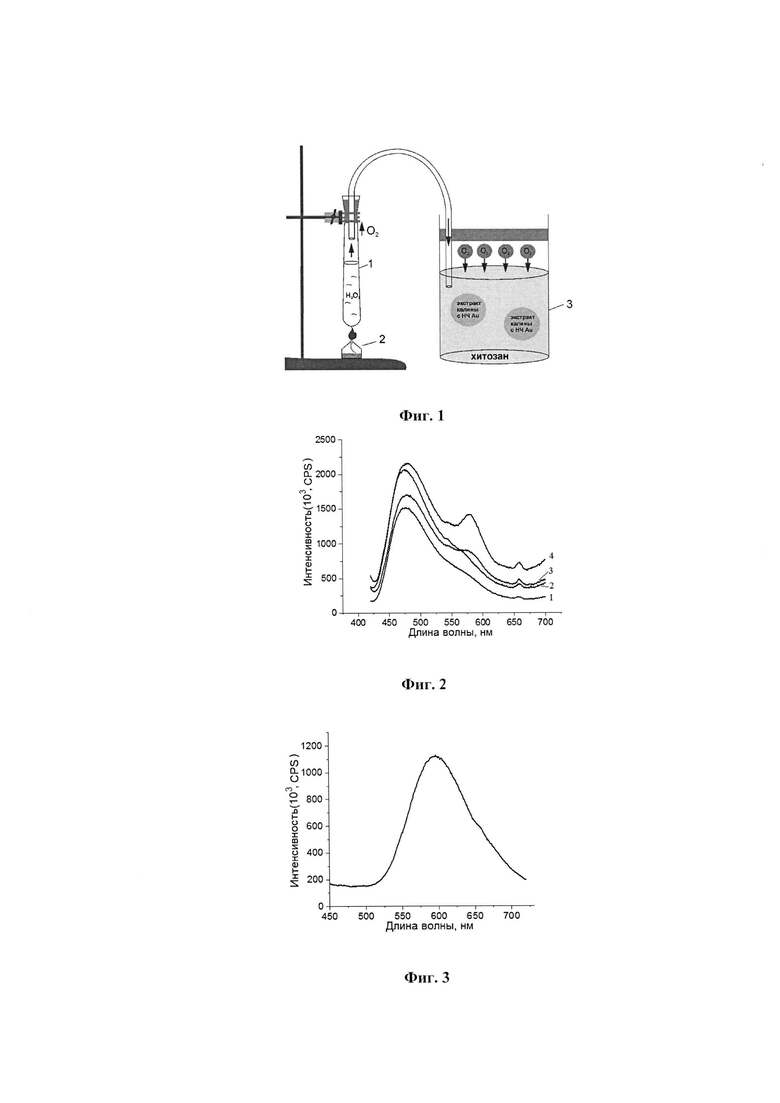
Полученные растворы экстракта калины в хитозане с наночастицами и без наночастиц далее были подвержены процессу кислородонасыщения. Процесс кислородного насыщения растворов проводили при разложении перекиси водорода согласно схеме, представленной на Фиг. 1, где: 1 - пробирка с раствором перекиси водорода; 2 -спиртовка; 3 - раствор экстракта калины с наночастицами золота С=10-9 М в хитозане.
Приготовленные растворы были исследованы в видимой области флуоресцентным методом на модульном спектрофлуориметре Fluorolog 3 фирмы Horiba and Jobin Yvon (Франция). Спектры флуоресценции калины красной в хитозане представлены на Фиг. 2., где: 1 - без наночастиц золота; 2 - с наночастицами золота концентрацией С=10-9 М; 3 - с молекулами кислорода концентрацией С=25⋅10-3 моль; 3 - с наночастицами золота концентрацией С=10-9 М и молекулами кислорода концентрацией С=25⋅10-3 моль.
Процесс кислородонасыщения растворов был проведен при разложении перекиси водорода. Концентрация молекул кислорода в растворе варьировалась с учетом изменения времени кислородонасыщения: С1[О2]=3⋅10-3 моль (2 мин), С2[О2]=6⋅10-3 моль (4 мин), С3[О2]=12⋅10-3 моль(10 мин), С4[O2]=25⋅10-3 моль(15 мин), С5[O2]=52⋅10-3 моль(25 мин). После 10 минут барботирования (С3[O2]=12⋅10-3 моль) наблюдаются спектральные изменения люминесценции молекул экстракта в области 590 нм. Происходит формирование разрешенного максимума на длине волны λ=590 нм со спектральной шириной линии Δλ≈40 нм, которого ранее в спектре люминесцении экстракта не было. В присутствии наночастиц золота спектральные изменения люминесцентных свойств экстракта наступают уже спустя 5 минут кислородонасыщения при концентрации молекул O2 в растворе С[O2]=6⋅10-3 моль. Вместе с тем увеличивается интенсивность люминесценции при добавлении наночастиц золота в результате плазмонного диполь-дипольного переноса энергии в комплексе молекула экстракта-наночастица золота. Максимум в области 590 нм обусловлен эмиссией кверцетина и его производных в растворе экстракта калины. на Спектр люминесценции водно-спиртового раствора кверцетина показан на Фиг. 3. Максимум люминесценции чистого раствора кверцетина располагается на длине волны 590 нм (Фиг. 3).
| название | год | авторы | номер документа |
|---|---|---|---|
| Крем, поглощающий ультрафиолетовое излучение, на основе калины красной и наночастиц серебра и способ его получения | 2022 |
|
RU2809099C1 |
| Бальзам для губ, поглощающий ультрафиолетовое излучение, на основе калины красной и способ его получения | 2024 |
|
RU2840428C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ (ВАРИАНТЫ) | 2001 |
|
RU2199249C1 |
| ЭКСТРАКТ КАЛИНЫ, ОБЛАДАЮЩИЙ АНТИРАДИКАЛЬНОЙ АКТИВНОСТЬЮ | 2001 |
|
RU2220614C2 |
| СПОСОБ ПОЛУЧЕНИЯ НОВОГАЛЕНОВЫХ ЭКСТРАКТОВ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2016 |
|
RU2635397C1 |
| Способ получения высокоэффективной апконверсионной люминесценции комплексов оксида иттербия с наночастицами золота | 2021 |
|
RU2779620C1 |
| КОМПОЗИЦИЯ ДЛЯ ПРИГОТОВЛЕНИЯ КВАСА | 2012 |
|
RU2489064C1 |
| КОМПОЗИЦИЯ ИНГРЕДИЕНТОВ ДЛЯ НАПИТКОВ | 2008 |
|
RU2372798C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММАРНОГО СОДЕРЖАНИЯ ФЛАВОНОИДОВ В РАСТИТЕЛЬНОМ СЫРЬЕ | 2010 |
|
RU2441224C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИОКСИДАНТА ДЛЯ КОСМЕТИЧЕСКИХ ИЗДЕЛИЙ | 2013 |
|
RU2533255C1 |
Изобретение относится к области фармацевтической химии. Раскрыт способ определения флавоноидов в водно-спиртовом растворе экстракта калины красной в присутствии наночастиц золота, добавленных с целью усиления сигнала люминесценции, при этом способ является двухстадийным и спектральным, обеспечивая регистрацию оптического сигнала кверцетина и его окисленных форм после кислородонасыщения раствора экстракта методом барботирования с определенным временным интервалом и контролем концентрации молекул кислорода в растворе. Изобретение позволяет осуществлять качественный контроль присутствия флавоноидов и их окисленных форм в составе экстрактов растительного происхождения. 3 ил.
Способ определения флавоноидов в водно-спиртовом растворе экстракта калины красной в присутствии наночастиц золота, добавленных с целью усиления сигнала люминесценции, отличающийся тем, что он является двухстадийным и спектральным, обеспечивая регистрацию оптического сигнала кверцетина и его окисленных форм после кислородонасыщения раствора экстракта методом барботирования с определенным временным интервалом и контролем концентрации молекул кислорода в растворе.
| DUZ M | |||
| et al | |||
| Determination of Total Phenolic, Flavonoid Content and Antimicrobial Properties in Different Solvent Extracts of Viburnum opulus L | |||
| (Gilaburu) in Afyonkarahisar // Pak | |||
| J | |||
| Anal | |||
| Environ | |||
| Chem., 2021, V.22, N.2, pp.388-395 | |||
| YURKIV K | |||
| et al | |||
| HPLC-analysis of phenolic compounds of European cranberry bush fruits (Viburnum opulus L.) // |
Авторы
Даты
2024-03-12—Публикация
2023-07-12—Подача