Изобретение относится к области химии, а именно к способам разложения сероводорода и может применяться для производства водорода и элементарной серы из сероводорода, а также для очистки от сероводорода газовых выбросов.
Разложение сероводорода на элементы по реакции
H2S ⇔ H2 + S - Q1
в настоящее время рассматривается как перспективный вариант получения водорода для нужд экологически чистой энергетики и производств экологически чистых топлив с одновременным решением проблемы утилизации высокотоксичного H2S.
Известен способ термического разложения сероводорода на водород и серу включающий пропускание сероводородсодержащего газа через реакционную зону при температуре 850-16000С, где происходит разложение H2S на водород и серу, и последующее охлаждение указанного газа до температуры 110-150°С для конденсации образовавшейся серы. (Патент США №4302434, С01В 17/04, 24.11.81). Недостатками известного способа являются: высокая температура, требуемая для достижения высокой степени разложения сероводорода; высокое потребление энергии на осуществление реакции и компенсацию возможных теплопотерь; возможность снижения степени разложения сероводорода за счет обратного взаимодействия водорода и серы при охлаждении газа; невозможность применения способа для переработки газов, содержащих углеводороды и другие примеси, которые могут подвергаться пиролизу при высокой температуре; низкая эффективность способа при снижении концентрации сероводорода в исходном сероводородсодержащем газе; необходимость применения специальных дорогостоящих конструкционных материалов с повышенной термостойкостью для оформления высокотемпературной реакционной зоны.
Понижение температуры, требуемой для разложения сероводорода, возможно за счет применения катализаторов. Известен способ каталитического разложения сероводорода на водород и серу, включающий пропускание сероводородсодержащего газа через слой катализатора при температуре 450 - 8000С (Патент США №3962409, С01В 17/04, 8.06.76). Достоинством способа является относительно низкая температура осуществления реакции разложения сероводорода. Недостатком известного способа является низкая равновесная степень разложения сероводорода в указанном диапазоне температур (не более 15%), которая не зависит от применяемого катализатора.
Известен способ разложения сероводорода на водород и серу, включающий периодическое пропускание сероводородсодержащего газа через слой сорбента, содержащего сульфиды железа, кобальта или никеля, при температуре 258-536°С, которое чередуют с периодическим нагревом сорбента до температур около 700°С для его регенерации (Патент США №2979384, кл.423/573, 01.04.61). Во время пропускания сероводородсодержащего газа указанные компоненты сорбента взаимодействуют с сероводородом с образованием газообразного водорода и твердых полисульфидов указанных металлов. Во время регенерации сорбента происходит термическое разложение указанных полисульфидов с образованием исходных сульфидов и паров элементарной серы. Достоинством известного способа является возможность достижения высокой степени разложения сероводорода. Недостатком известного способа является его периодичность, относительно высокая температура разложения сероводорода, дальнейшее снижение которой лимитируется малой скоростью протекания указанных химических реакций при пониженной температуре, вероятность неполного превращения сероводорода, а также высокая температура регенерации сорбента.
Известен способ получения водорода и элементарной серы из сероводорода (Патент РФ №2709374, МПК C01B 17/04, C01B 3/02, B01D 53/52, приоритет от 03.06.2019), включающий пропускание исходного сероводородсодержащего газа через неподвижный слой гранулированного твердого хемосорбента, способного адсорбировать сероводород с образованием водорода и образованием твердых серосодержащих соединений на поверхности хемосорбента, выделение водорода из полученного газового потока и периодическую регенерацию слоя путем разложения указанных серосодержащих соединений и выделения паров элементарной серы при повышенной температуре с последующей конденсации паров серы при пониженной температуре, отличающийся тем, что способ осуществляют не менее, чем в двух параллельных реакторах, содержащих слои указанного хемосорбента, при этом в каждом из реакторов попеременно чередуют режим хемосорбции с подачей исходного сероводородсодержащего газа с температурой от -30 до 100°С и режим регенерации с подачей в противоположном направлении регенерирующего газа, не содержащего водорода, с температурой 500-700°С, осуществляя переход с режима хемосорбции на режим регенерации при снижении температуры хемосорбента ниже заданного значения в диапазоне 150-250°С в точке слоя хемосорбента, отстоящей от точки входа сероводородсодержащего газа на расстоянии от 30 до 60% от высоты слоя. В качестве указанного хемосорбента могут использовать материал, содержащий сульфиды никеля, железа или кобальта в индивидуальном виде или в виде их смесей, в общем количестве не менее 85%. В качестве регенерирующего газа может использоваться технический азот. Из газового потока, выходящего из реактора, работающего в режиме хемосорбции, могут раздельно выделять водород и непрореагировавший сероводород, при этом выделенный сероводород могут рециркулировать обратно на вход реактора, работающего в режиме хемосорбции. Достоинством способа является возможность достижения высокой степени разложения сероводорода при умеренных температурах, а также непрерывность технологического процесса. К недостаткам способа можно отнести высокие энергозатраты на осуществление регенерации хемосорбента, требующие нагрева регенерирующего газа до высоких температур за счет использования внешней энергии.
Изобретение решает задачу разработки эффективного способа непрерывного разложения сероводорода на водород и серу с минимальными энергетическими затратами на регенерацию хемосорбента.
Задача решается с помощью заявленного изобретения, характеризующего способ получения водорода, элементарной серы и товарных продуктов из сероводорода, включающий пропускание исходного сероводородсодержащего газа через неподвижный слой гранулированного твердого хемосорбента, способного адсорбировать сероводород с образованием водорода и образованием твердых серосодержащих соединений на поверхности хемосорбента, выделение водорода из полученного газового потока и периодическую регенерацию слоя путем разложения указанных серосодержащих соединений и выделения паров элементарной серы при повышенной температуре с последующей конденсацией паров серы при пониженной температуре, указанный способ осуществляют не менее, чем в двух параллельных реакторах, содержащих слои указанного хемосорбента, при этом в каждом из реакторов попеременно чередуют режим хемосорбции с подачей исходного сероводородсодержащего газа и режим регенерации с подачей в противоположном направлении регенерирующего газа, не содержащего водорода, причем регенерацию осуществляют с подачей в слой хемосорбента регенерирующего газа, содержащего от 0,1 до 50% об. кислорода, с температурой от 0 до 250°С. В качестве регенерирующего газа могут использоваться смеси кислорода с одним или несколькими газообразными веществами, в том числе из списка: азот, водяной пар, углекислый газ, аргон, метан, также возможно использование воздуха в качестве регенерирующего газа. Переход с режима хемосорбции на режим регенерации может осуществляться при снижении температуры хемосорбента ниже заданного значения в диапазоне 120-250°С в точке слоя хемосорбента, отстоящей от точки входа сероводородсодержащего газа на расстоянии от 30 до 60% высоты слоя. В качестве указанного хемосорбента могут использовать материал, содержащий соединения никеля, железа или кобальта в индивидуальном виде или в виде их смесей, в общем количестве не менее 85%, остальное составляет минеральное связующее. Из газового потока, выходящего из реактора, работающего в режиме хемосорбции, могут раздельно выделять водород и непрореагировавший сероводород, при этом выделенный сероводород могут рециркулировать обратно на вход реактора, работающего в режиме хемосорбции. Диоксид серы, содержащийся в газовом потоке, выходящем из реактора, работающего в режиме регенерации, могут подвергать дальнейшему окислению с получением товарных продуктов, в частности, серной кислоты и ее солей, например сульфата аммония (путем взаимодействия с аммиаком).
Технический результат предлагаемого способа заключается в достижении полного разложения H2S в непрерывном циклическом режиме, с использованием тепла частичного окисления поверхностных продуктов хемосорбции кислородом, что позволяет отказаться от использования внешней энергии на разогрев регенерационного потока, тем самым обеспечивая существенное снижение энергозатрат на регенерацию хемосорбента, а также повысить эффективность регенерации хемосорбента и исключить теплопотери за счет того, что выделение указанного тепла происходит непосредственно в слое хемосорбента. Для реализации суперадиабатической тепловой волны с высокими максимальными температурами в слое хеморбента во время регенерации необходимо, чтобы температура газа на входе в слой была ниже температуры зажигания реакций окисления сульфидов и полисульфидов кислородом, для сульфидов и полисульфидов железа, никеля или кобальта эта температура составляет не менее 200-250°С. Столь существенное снижение температуры регенерирующего газа (не выше 250°С вместо 500-700°С) позволяет упростить и удешевить оборудование для осуществления способа, включая его теплообменную инфраструктуру, используя при этом доступные и недорогие конструкционные материалы, существенно снизить энергетические затраты на его осуществление, а также дает возможность переработки сероводородсодержащих газов без предварительного концентрирования H2S, удаления из них углеводородов и других примесей.
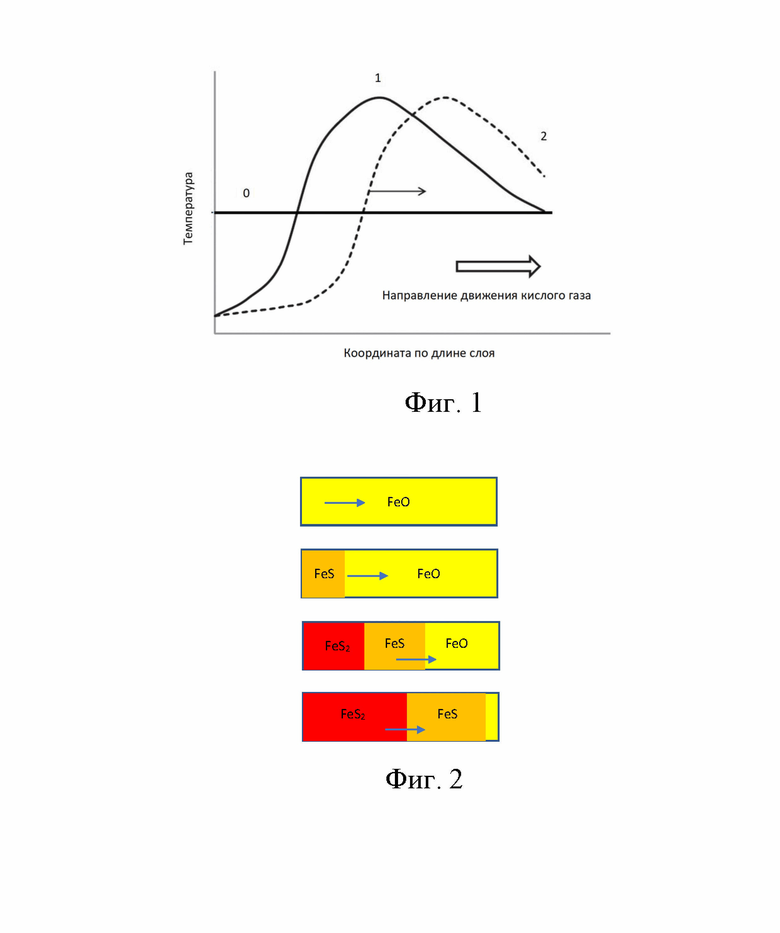
На фиг. 1 проиллюстрирован профиль температур вдоль оси слоя сорбента-катализатора в пусковом режиме. 0 - начальный профиль перед пуском кислого газа, 1 и 2 - профили в различные моменты времени после пуска кислого газа.
На фиг. 2 проиллюстрировано распределение соединений Fe по длине слоя сорбента в различные моменты цикла сульфидирования. Направление фильтрации кислого газа через слой показано стрелками.
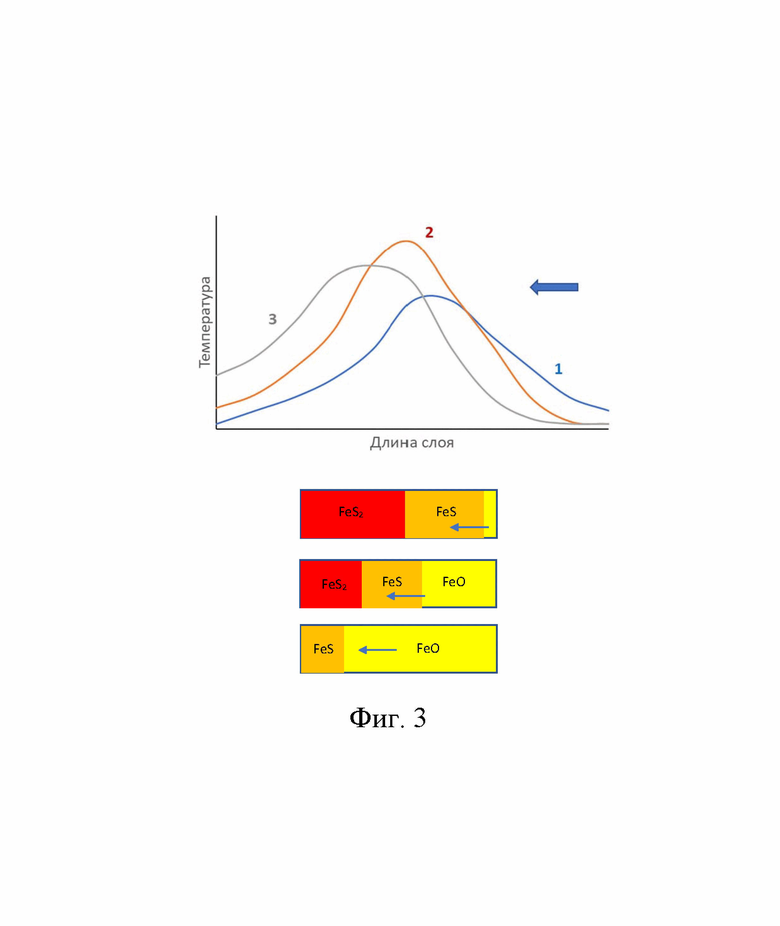
На фиг. 3 проиллюстрировано распределение температуры и содержания соединений Fe по длине слоя сорбента в различные моменты цикла окислительной регенерации. Направление фильтрации регенерирующего газа через слой показано стрелками.
Способ может осуществляться в неподвижном слое хемосорбента на основе соединения никеля, железа или кобальта в индивидуальном виде или в виде их смесей. Ниже приведен пример реализации способа с использованием соединений железа.
Исходно хемосорбент загружается в реактор в виде гранул оксида железа. Перед пуском слой сорбента прогревается в токе воздуха до ~300-400°С, после чего в слой подают кислый газ, содержащий сероводород. Кислый сероводород-содержащий газ подается с естественной температурой (например, 20-60°С), без подогрева, либо с небольшим нагревом (до 120-140°С).
В слое происходит реакция сульфидирования оксида железа:
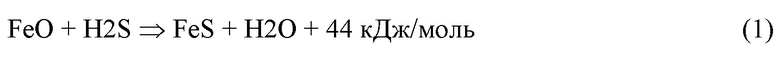
Реакция (1) практически необратима (ΔG = - 43 кДж/моль) и экзотермична. В лобовом слое сорбента протекает два противонаправленных тепловых процесса: охлаждение нагретого сорбента при теплообмене с холодным потоком кислого газа и нагрев сорбента за счет тепловыделения протекающей на нем реакции (1). В результате температура сорбента на входе в слой снижается, но в более далекой от входа области слоя она начинает расти, что приводит к образованию в слое тепловой волны, медленно движущейся в направлении фильтрации кислого газа (см. фиг. 1).
По мере накопления сульфида железа во входной части слоя, в этой части слоя начинает протекать реакция
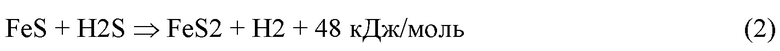
с выделением водорода, которая также участвует в формировании тепловой волны. Важно, что такая тепловая волна обладает свойством суперадиабатичности, то есть разность между максимальной температурой в ней и входной температурой газа может заметно превышать адиабатический разогрев протекающих реакций.
На фиг.2 схематично показано распределение различных соединений железа по длине слоя в различные моменты времени.
В начале цикла весь слой состоит из оксида железа, потом в нем возникает волна распространения FeS, затем следующая за ней волна распространения FeS2. Все эти волны двигаются сонаправленно направлению фильтрации кислого газа.
Зона расположения FeO на выходе позволяет полностью поглощать сероводород, не прореагировавший с FeS в предшествующих частях слоя, что обеспечивает его высокую конверсию. В итоге выходящий из слоя газ не содержит сероводорода, зато содержит водород и инертные компоненты кислого газа (пары воды, углекислый газ, углеводороды).
Перед тем, как концентрационная волна распространения FeS достигнет конца слоя (последний рисунок на фиг.2), когда H2S уже может появиться на выходе из слоя в значительной концентрации, слой переводят в режим окислительной регенерации. Для этого прекращают подачу кислого газа и начинают подачу в слой кислород-содержащего регенерирующего газа, направление подачи которого противоположно направлению подачи кислого газа.
При этом во входной части слоя со стороны подачи воздуха протекает реакция окисления сульфида железа кислородом:
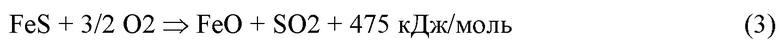
Реакция (3) сильно экзотермична и необратима (ΔG = - 426 кДж/моль). Как и в предыдущем случае, в слое происходит движение тепловой волны, однако, на этот раз она движется в обратном направлении, спутно направлению подачи регенерирующего газа в слой.
За счет высокого теплового эффекта реакции (3) максимальная температура в такой волне при низкой температуре подаваемого воздуха и исходной температуре сорбента во входной части слоя порядка 200-400°С может достигать 600-700°С. При этом расход регенерирующего газа и содержание кислорода в нем подбирается таким образом, чтобы обеспечить полную конверсию кислорода во входной части слоя. В совокупности это дает возможность получить в центральной и выходной части слоя инертный поток, состоящий из азота и аргона, с высокой температурой, необходимой для разложения FeS2:
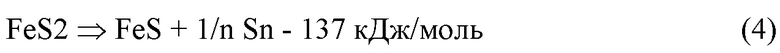
Динамика движения тепловых и концентрационных волн схематично представлена на фиг.3.
При этом в центральной части слоя, помимо термического разложения дисульфида железа, может также протекать взаимодействие FeS с SO2:
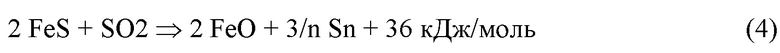
Эта реакция хорошо термодинамически обусловлена при низких и умеренных температурах, она позволяет минимизировать концентрации SO2 на выходе слоя при регенерации. Совокупность реакций (2-4) можно условно представить в виде общей брутто-реакции окислительной регенерации
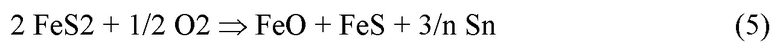
В области температур ниже 250°С эта реакция экзотермична (ΔН от -40 кДж/моль при 20°С до 0 при ~ 250°С), при температуре 600°С эндотермический эффект составляет 161 кДж/моль. При этом она очень хорошо обусловлена термодинамически (ΔG от -41 кДж/моль при 20°С до -75 кДж/моль при 600°С). Такая обусловленность связана с ростом энтропии в реакции на 270 Дж/моль/К.
Такой режим регенерации обеспечивает разложение дисульфидов и возврат сорбента в исходное состояние (FeO + FeS), после чего можно начинать следующий цикл хемосорбции.
Циклы хемосорбции и регенерации образуют устойчивый нестационарный реакционный цикл и могут далее повторяться неограниченное число раз. Исходя из условия повторяемости циклов брутто-превращения на стадиях хемосорбции и регенерации можно представить следующими уравнениями:
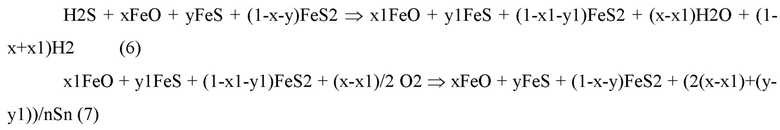
где x и y - относительные доли FeO и FeS в составе сорбента в начале цикла хемосорбции (и в конце цикла регенерации), x1 и y1 - относительные доли FeO и FeS в составе сорбента в начале цикла регенерации (и в конце цикла хемосорбции). Соотношение x и y в установившихся нестационарных циклах будет зависеть от параметров реализации способа (длительности циклов, расходы кислого газа и регенерирующего газа и пр.) и может варьироваться как при разработке, так и в процессе эксплуатации процесса. Суммарное превращение в описываемом способе описывается линейной суммой уравнений (6) и (7):
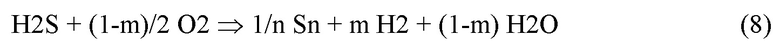
Общий тепловой эффект по стадии хемосорбции (6) - экзотермический, по стадии регенерации (7) - эндотермический. Общий тепловой эффект по уравнению (8) зависит от величины m. Суммарный нулевой тепловой эффект достигается при m≈0.85, то есть энергонейтральность способа обеспечивается при выходе водорода на превращённый сероводород 85%. При m<0.85 выход водорода становится ниже, но при этом обеспечивается энергоизбыточность способа. Наоборот, при m>0.85 теоретически можно достигать выхода водорода выше 85% за счет дополнительных энергозатрат.
Перенос энергии с энергоизбыточной стадии хемосорбции на энергодефицитную стадию регенерации производится за счет регенеративного теплообмена, то есть за счет накопления/расходования тепла при нагреве/охлаждении сорбента. Подвод внешней тепловой энергии требуется только при предварительном нагреве слоев сорбента во время пусковых процедур.
Выходной газовый поток на стадии хемосорбции будет содержать минимальное количество сероводорода, в его состав также войдут водород и инертные компоненты кислого газа (пары воды, углекислый газ, углеводороды). Вода может быть затем удалена конденсацией, а СО2 при необходимости может быть отделен с помощью аминовой очистки, в том числе и для последующей утилизации. После этого продуктовый поток будет содержать водород и углеводороды (соотношение концентраций будет зависеть от состава кислого газа) и может направляться на дальнейшую очистку для выделения водорода или иное использование.
Выходной газовый поток на стадии регенерации будет содержать инертные компоненты (азот, аргон) и пары серы, которые могут быть выделены из потока путем конденсации. При необходимости выходящий газ после конденсации серы может быть использован в качестве технического инерта. Также в составе регенерационного газа н выходе реактора может содержаться диоксид серы SO2, который может затем подвергаться окислению до триоксида серы SO3, который далее может быть утилизирован с производством ценных товарных продуктов, таких как серная кислота или ее соли, например сульфата аммония, который является ценным минеральным удобрением. При этом для производства сульфата аммония может использоваться аммиак, который иногда содержится в сероводород-содержащих кислых газах на нефтеперерабатывающих предприятиях.
Оценочно, типичная длительность циклов хемосорбции и регенерации может составлять 15-40 минут, что приемлемо с технической точки зрения: с такими длительностями циклов работают многочисленные промышленные каталитические реверс-процессы различного назначения (окисление SO2, дожиг органических соединений, восстановление NOx и др.).
Способ может быть реализован в схеме с двумя и более параллельными реакторами с попеременным неодновременным чередованием режимов хемосорбции и регенерации в каждом из них. Важно, что оба исходных потока подаются в переключающие клапаны с низкой температурой (от 0 до 250°С), а температура выходящих из реакторов потоков не превышает, оценочно, 400-500°С. Такая рабочая температура приемлема для переключающих клапанов. Более высокие температуры (более 500°С) реализуются только в слоях хемосорбента сорбента, где их влияние на оборудование некритично.
В качестве хемосорбента могут использоваться гранулированные материалы, состоящие из соединений железа, никеля или кобальта в их индивидуальном виде, либо в виде любых их смесей. Эти соединения смогу включать в себя сульфиды, полисульфиды, оксиды и соли указанных металлов. Кроме этих соединений в состав хемосорбентов могут входить связующие, обеспечивающие механическую прочность гранул и их проницаемость для газовых компонентов реакционной смеси. Предпочтительно использование хемосорбентов с высоким содержанием описанных соединений - не менее 85% вес., меньшее содержание нежелательно, так как это будет приводить к снижению удельной хемосорбционной емкости хемосорбентов.
Основным преимуществом заявляемого способа является возможность разложения сероводорода с выделением водорода при низкой (например, комнатной) входной температуре исходного сероводородсодержащего газа, что в свою очередь, позволяет перерабатывать сероводородсодержащий газ без предварительного нагрева, обеспечивая снижение энергетических затрат на осуществление способа и минимизацию использования дорогостоящей и громоздкой теплообменной аппаратуры. Кроме того, в этом случае в переработку вовлекается только сероводород, и исключаются нежелательные побочные реакции других компонентов и примесей сероводородсодержащего газа (углеводородов, органических соединений и пр.), что позволяет перерабатывать исходные газы с низкой концентрацией сероводорода и сложным составом без предварительного концентрирования и очистки сероводорода. При этом разделение во времени стадий хемосорбции сероводорода с выделением водорода и регенерации твердого материала с выделением серы позволяет сдвигать равновесие реакции разложения сероводорода в сторону образования водорода и серы и достигать степени превращения сероводорода, существенно превышающей теоретический равновесный уровень для осуществления реакции в одну стадию. Кроме того, существенный вклад в достижение высокой конверсии сероводорода вносит поглощение сероводорода оксидами металлов на выходе из слоя в цикле хемосорбции. Проведение регенерации твердого материала в потоке кислород-содержащего регенерирующего газа обеспечивает быстрый и равномерный нагрев слоя за счет протекающих непосредственно в слое экзотермических реакций и, таким образом, его эффективную регенерацию. Применение кислорода в составе регенерирующего газа дает возможность управлять тепловым балансом, в том числе, обеспечивая его энергонейтральность способа или даже его некоторую энергоизбыточность, что позволяет полностью отказаться от использования внешней энергии и сторонних энергоносителей, а также существенно снизить энергозатраты на осуществление способа. Кроме того, реализация способа при умеренных температурах (не выше 600-650°С) позволяет использовать для создания оборудования общепринятые конструкционные материалы вместо специальных термостойких сталей, что существенно снижает его стоимость.
В сравнении с основным традиционным способом получения серы из сероводорода - процессом Клауса, основным достоинством предлагаемого способа является возможность производства не только серы, но и водорода, стоимость которого в современных ценах в несколько раз превышает стоимость производимой серы.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Для разложения сероводорода используется технологическая схема с двумя параллельными реакторами, в которых находятся неподвижные слои гранулированного хемосорбента, содержащего 95% FeS.
Переработке подвергается кислый газ нефтепереработки, содержащий 86% об. H2S, 13.8% об. СО2, 0.2% углеводородов (в основном, метан). Расход кислого газа 3400 норм.м3/час, естественная температура кислого газа 40°С. Кислый газ без нагрева подается непосредственно в реактор, работающий в режиме хемосорбции. При этом достигается средняя за цикл степень превращения сероводорода в водород около 90%. Полученный газовый поток направляется на блок аминовой очистки, где выделяются продуктовый водород, сероводород и смесь СО2 с углеводородами (~98.6% об СО2). Выделенный сероводород рециркулируется на вход реактора, работающего в режиме хемосорбции, за счет чего общий объем сероводородсодержащего газа на входе в указанный реактор в установившемся режиме составляет ~3700 норм.м3/час.
В это же время во втором реакторе проводится регенерация хемосорбента, для чего в этот реактор подается воздух. Температура воздуха на входе в реактор 20°С, направление его подачи противоположено направлению подачи кислого газа. Выходящий из реактора воздух охлаждают до 140°С и конденсируют образовавшуюся серу.
При снижении температуры хемосорбента в точке слоя хемосорбента в первом реакторе, отстоящей от точки входа сероводородсодержащего газа на расстоянии 30% от длины слоя, ниже 150°С производят смену режимов в реакторах. Для этого в первый реактор прекращают подачу сероводородсодержащего газа и начинают подавать регенерирующий газ, а во втором - прекращают подачу регенерирующего воздуха и начинают подавать сероводородсодержащий газ, также соответствующим образом перенаправляя потоки газов, выходящие из реакторов. В следующем цикле смену режимов производят при снижении температуры хемосорбента в точке слоя хемосорбента во втором реакторе, отстоящей от точки входа сероводородсодержащего газа на расстоянии 30% от длины слоя, ниже 150°С. Далее подобная процедура периодической смены режимов по достижению указанной температуры повторяется в течение сколь угодно длительного времени. В описанных условиях фактическая длительность каждого такого цикла составляет около 15 мин.
В установившемся циклическом режиме выработка водорода составляет 2500 норм.м3/час, степень очистки газов от сероводорода - 100%, степень превращения сероводорода в водород ~85%, объем производства серы - 4.2 т/час, максимальная температура в слоях хемосорбента - не более 620°С.
Пример 2
То же, что и в примере 1, но смену режимов производят при снижении температуры хемосорбента в точке слоя хемосорбента, отстоящей от точки входа сероводородсодержащего газа на расстоянии 30% от длины слоя, ниже 200°С. Длительность цикла снижается до 12 мин, максимальная температура в цикле возрастает до 640°С. Степень превращения сероводорода в водород за проход через реактор увеличивается до 100%, рециркуляции водорода на вход реактора не требуется. В установившемся циклическом режиме выработка водорода составляет 2250 норм.м3/час, степень очистки газов от сероводорода - 100%, степень превращения сероводорода в водород ~76%, объем производства серы не изменяется.
Пример 3
То же, что и в примере 1, но в качестве хемосорбента используют гранулированный материал, содержащий NiS (55% мас.) и CoS (30%). Длительность цикла снижается до 13 мин, максимальная температура в цикле снижается до 605°С. Степень превращения сероводорода в водород за проход через реактор снижается до 80%, объем газов на входе в реактор, с учетом возрастающего рецикла увеличивается до 5800 м3/час. В установившемся циклическом режиме выработка водорода составляет 2370 норм.м3/час, степень очистки газов от сероводорода - 100%, степень превращения сероводорода в водород ~80%, объем производства серы - 4.2 т/час, максимальная температура в слоях хемосорбента - не более 630°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения водорода и элементарной серы из сероводорода | 2019 |
|
RU2709374C1 |
| СПОСОБ РАЗЛОЖЕНИЯ СЕРОВОДОРОДА | 2003 |
|
RU2239594C1 |
| СПОСОБ РАЗЛОЖЕНИЯ СЕРОВОДОРОДА И/ИЛИ МЕРКАПТАНОВ | 2003 |
|
RU2239593C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА И ЭЛЕМЕНТАРНОЙ СЕРЫ ИЗ СЕРОВОДОРОДА | 2002 |
|
RU2216506C1 |
| Способ переработки сероводородсодержащих газов с получением элементарной серы и установка для его осуществления | 2024 |
|
RU2827896C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЕРЫ ИЗ СЕРОВОДОРОДСОДЕРЖАЩЕГО ГАЗА | 1992 |
|
RU2040464C1 |
| СПОСОБ РАЗЛОЖЕНИЯ СЕРОВОДОРОДА И/ИЛИ МЕРКАПТАНОВ | 2004 |
|
RU2261838C1 |
| СПОСОБ НИЗКОТЕМПЕРАТУРНОГО РАЗЛОЖЕНИЯ СЕРОВОДОРОДА С ПОЛУЧЕНИЕМ ВОДОРОДА И СЕРЫ | 2015 |
|
RU2600375C1 |
| Способ низкотемпературного разложения сероводорода с получением водорода и серы | 2019 |
|
RU2725636C1 |
| Способ очистки газа, содержащего водяные пары, от сероводорода | 1988 |
|
SU1722210A3 |
Изобретение может быть использовано в производстве водорода и элементарной серы, а также при очистке от сероводорода газовых выбросов. Способ получения водорода и элементарной серы из сероводорода включает пропускание исходного сероводородсодержащего газа через неподвижный слой гранулированного твердого хемосорбента, способного адсорбировать сероводород с образованием водорода и образованием твердых серосодержащих соединений на поверхности хемосорбента. Водород выделяют из полученного газового потока и проводят периодическую регенерацию слоя путем разложения указанных серосодержащих соединений и выделения паров элементарной серы при повышенной температуре с последующей конденсацией паров серы при пониженной температуре. Способ осуществляют по меньшей мере в двух параллельных реакторах, содержащих слои хемосорбента. В каждом из реакторов попеременно чередуют режим хемосорбции с подачей исходного сероводородсодержащего газа и режим регенерации с подачей в противоположном направлении регенерирующего газа, не содержащего водород. Регенерацию осуществляют с подачей в слой хемосорбента регенерирующего газа, содержащего от 0,1 до 50% об. кислорода, с температурой от 0 до 250°С. Изобретение позволяет снизить энергозатраты на регенерацию хемосорбента при разложении H2S в непрерывном режиме. 9 з.п. ф-лы, 3 ил., 3 пр.
1. Способ получения водорода и элементарной серы из сероводорода, включающий пропускание исходного сероводородсодержащего газа через неподвижный слой гранулированного твердого хемосорбента, способного адсорбировать сероводород с образованием водорода и образованием твердых серосодержащих соединений на поверхности хемосорбента, выделение водорода из полученного газового потока и периодическую регенерацию слоя путем разложения указанных серосодержащих соединений и выделения паров элементарной серы при повышенной температуре с последующей конденсацией паров серы при пониженной температуре, указанный способ осуществляют по меньшей мере в двух параллельных реакторах, содержащих слои указанного хемосорбента, при этом в каждом из реакторов попеременно чередуют режим хемосорбции с подачей исходного сероводородсодержащего газа и режим регенерации с подачей в противоположном направлении регенерирующего газа, не содержащего водорода, отличающийся тем, что регенерацию осуществляют с подачей в слой хемосорбента регенерирующего газа, содержащего от 0,1 до 50% об. кислорода, с температурой от 0 до 250°С.
2. Способ по п.1, отличающийся тем, что в качестве регенерирующего газа используют смеси кислорода с одним или несколькими газообразными веществами.
3. Способ по п.2, отличающийся тем, что в качестве регенерирующего газа используют смеси кислорода с одним или несколькими газообразными веществами из списка: азот, водяной пар, углекислый газ, аргон, метан.
4. Способ по п.1, отличающийся тем, что в качестве регенерирующего газа используют воздух.
5. Способ по любому из пп.1-4, отличающийся тем, что переход с режима хемосорбции на режим регенерации осуществляется при снижении температуры хемосорбента ниже заданного значения в диапазоне 120-250°С в точке слоя хемосорбента, отстоящей от точки входа сероводородсодержащего газа на расстоянии от 30 до 60% высоты слоя.
6. Способ по любому из пп.1-5, отличающийся тем, что в качестве хемосорбента, способного адсорбировать сероводород с образованием водорода и образованием твердых серосодержащих соединений на поверхности хемосорбента, используют материал, содержащий соединения никеля, железа или кобальта в индивидуальном виде или в виде их смеси, в общем количестве не менее 85% вес., остальное - минеральное связующее.
7. Способ по любому из пп.1-6, отличающийся тем, что из газового потока, выходящего из реактора, работающего в режиме хемосорбции, раздельно выделяют водород и непрореагировавший сероводород, при этом выделенный сероводород рециркулируют обратно на вход реактора, работающего в режиме хемосорбции.
8. Способ по любому из пп.1-7, отличающийся тем, что диоксид серы, содержащийся в газовом потоке, выходящем из реактора, работающего в режиме регенерации, подвергают дальнейшему окислению с получением дополнительных товарных продуктов.
9. Способ по п.8, отличающийся тем, что диоксид серы, содержащийся в газовом потоке, выходящем из реактора, работающего в режиме регенерации, подвергают дальнейшему окислению с получением серной кислоты.
10. Способ по п.8, отличающийся тем, что диоксид серы, содержащийся в газовом потоке, выходящем из реактора, работающего в режиме регенерации, подвергают дальнейшему окислению и взаимодействию с аммиаком с получением сульфата аммония.
| Способ получения водорода и элементарной серы из сероводорода | 2019 |
|
RU2709374C1 |
| US 20070129240 A1, 07.06.2007 | |||
| КНУНЯНЦ И.Л | |||
| и др., Химический энциклопедический словарь, Москва, Советская энциклопедия, 1983, с | |||
| Транспортер для перевозки товарных вагонов по трамвайным путям | 1919 |
|
SU105A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА И ЭЛЕМЕНТАРНОЙ СЕРЫ ИЗ СЕРОВОДОРОДА | 2002 |
|
RU2216506C1 |
| СИСТЕМА ОЧИСТКИ И УТИЛИЗАЦИИ ДЫМОВОГО ГАЗА И СПОСОБ | 2011 |
|
RU2575714C2 |
| СПОСОБ РАЗЛОЖЕНИЯ СЕРОВОДОРОДА И/ИЛИ МЕРКАПТАНОВ | 2003 |
|
RU2239593C1 |
| СПОСОБ РАСПОЗНАВАНИЯ ЦЕЛЕЙ ОТ СЛУЧАЙНЫХ РЕВЕРБЕРАЦИОННЫХ ПОМЕХ | 2008 |
|
RU2365938C1 |
Авторы
Даты
2024-03-26—Публикация
2023-05-26—Подача