Изобретение относится к области медицины, а именно к инфекционным болезням, педиатрии, анестезиологии-реаниматологии, и может найти применение для дифференциальной диагностики мультисистемного воспалительного синдрома у детей, ассоциированного с SARS-CoV-2, синдрома Кавасаки или инфекционных заболеваний, осложненных сепсисом.
Мультисистемный воспалительный синдром у детей, ассоциированный с SARS-CoV-2 (МВС-Д), впервые был описан у детей в начале пандемии новой коронавирусной инфекцией (НКИ). В настоящее время данный синдром встречается в различных возрастных когортах, включая новорожденных, молодых, взрослых, детей и подростков.
Согласно данным Всемирной организации здравоохранения (ВОЗ, 2020), МВС-Д развивается через 2-8 недель после перенесенной НКИ, чаще в возрасте от 0 до 19 лет и характеризуется фебрильной лихорадкой (≥3 дней), вовлечением в патологический процесс двух и более органов и систем, повышением маркеров воспаления, отсутствием инфекционных агентов, способных вызывать подобную симптоматику. По данным литературы 50-80% детей с МВС-Д требуют экстренной госпитализации в отделение реанимации и интенсивной терапии в связи с развитием неотложных состояний. Летальность составляет 0,8-1,7%, отдаленные исходы к настоящему времени не изучены.
По клиническим проявлениям МВС-Д схож с другими состояниями, характеризующимися выраженным воспалительным ответом (синдромом стафилококкового или стрептококкового токсического шока, а также гемофагоцитарным синдромом, синдромом Кавасаки (СК), сепсисом и прочими). При этом лечение МВС-Д кардинально отличается от лечения перечисленных состояний, а несвоевременно поставленный диагноз и отсрочено назначенная терапия неблагоприятно отражается на исходах и прогнозе у пациентов.
В связи с продолжающейся пандемией НКИ, тяжестью течения МВС-Д возникает необходимость в поиске дополнительных критериев для верификации диагноза, что является основополагающим для определения тактики ведения пациента и определения исходов и прогноза заболевания.
Известен метод оценки тяжести состояния больных и ранней диагностики септических осложнений у детей с гнойно-септическими заболеваниями. Сущность изобретения заключается в определении содержания плазминоген/плазмина, α1-макроглобулина, α2-антитрипсина на 1, 3, 5, 10 сутки заболевания и при выписке из стационара [«Способ диагностики септического процесса и прогнозирования развития септических осложнений у детей». Патент №2248572. Однако приведенный способ имеет ряд недостатков. Рекомендуемые авторами маркеры не входят в стандартное обследование септического больного и не являются общедоступными. Уровень показателей необходимо отслеживать в динамике заболевания, что приводит к поздней диагностике и отсутствию своевременной терапии. С учетом возникшей в 2019 году НКИ данный способ не включает дифференциальную диагностику сепсиса и МВС-Д.
Известен метод диагностики МВС-Д и СК на основе 13 цитокинов, циркулирующих в сыворотке крови или плазме. В качестве групп сравнения были включены пациенты с НКИ и здоровые дети. С помощью линейного дискриминантного анализа была создана модель, которая могла бы различать МВС-Д и СК [Esteve-Sole А. et al. Similarities and differences between the immunopathogenesis of COVID-19-related pediatric multisystem inflammatory syndrome and Kawasaki disease //The Journal of clinical investigation. 2021;131(6)]. Однако, при тестировании модели были найдены различия для групп пациентов с НКИ, МВС-Д+СК и здоровых детей, но не было получено разницы в уровне цитокинов у детей с МВС-Д и СК. Кроме того, недостатком метода является дороговизна исследования, что существенно затрудняет его использование в рутинной практике.
Известен способ диагностики МВС-Д и СК на основании возраста пациента и уровня ферритина. С помощью анализа ROC-кривой было определено, что при уровне ферритина >140 мкг/дл у ребенка в возрасте старше 5 лет при соответствующей клинической картине заболевания возможно подтвердить течение МВС-Д [Pouletty М. et al. Paediatric multisystem inflammatory syndrome temporally associated with SARS-CoV-2 mimicking Kawasaki disease (Kawa-COVID-19): a multicentre cohort //Annals of the rheumatic diseases. 2020;79(8):999-1006]. Однако предложенные критерии не позволяют с высокой точностью диагностировать МВС-Д при наличии других симптомов заболевания, так как клиника синдрома достаточно разнообразна, а уровень ферритина не всегда повышен в начале заболевания. Недостатком способа также является отсутствие критериев для проведения дифференциальной диагностики с другими схожими состояниями, включая ИЗоС.
Наиболее близкой к предлагаемому способу диагностики МВС-Д и СК является шкала KMDscore (Kawasaki/MIS-C differentiation score - шкала дифференциальной диагностики СК и МВС-Д), включающая 5 критериев, за каждый из которых начисляются баллы: СРБ >11 мг/дл (18 б.), D-димер >607 нг/мл (27 б.), возраст старше 5 лет (30 б.), тромбоцитопения (25 б.), поражение желудочно-кишечного тракта (ЖКТ) (28 б.). Сумма баллов, начисляемая за каждый показатель, позволяет различать данные заболевания: при количестве балов >55 пациенту следует выставить диагноз МВС-Д [Kostik М.М., Bregel L.V., Avrusin I.S. et al. Distinguishing between multisystem inflammatory syndrome, associated with COVID-19 in children and the Kawasaki disease: development of preliminary criteria based on the data of the retrospective Multicenter Cohort Study. Frontiers in Pediatrics. 2021;9:787353]. Однако в данном методе не учитывается конкретный уровень тромбоцитов (как, например, для СРБ и D-димера) и степень проявлений поражения ЖКТ (например, частота рвоты, которая также может быть признаком интоксикации, частота нарушения стула, наличие и интенсивность болей в животе и др.), что затрудняет расчет шкалы KMDscore. Также предложенный метод не предназначен для дифференциальной диагностики МВС-Д с инфекционными заболеваниями, осложненными сепсисом (ИЗоС). Способ не обеспечивает точности диагностики.С целью устранения вышеуказанных недостатков, авторы предлагают принципиально новый способ дифференциальной диагностики мультисистемного воспалительного синдрома у детей, ассоциированного с SARS-CoV-2.
Технический результат, достигаемый в данном способе, заключается в повышении точности ранней и своевременной диагностики за счет учета клинических данных и лабораторных показателей. Данный метод применим для первичной постановки МВС-Д на этапе дифференциальной диагностики.
Этот результат достигается тем, что путем клинического и лабораторного обследования определяют: пол, возраст, поражение кожи и слизистых оболочек, поражение нервной системы, уровень тромбоцитов и прокальцитонина. Полученные значения вносят в формулу расчета линейных дискриминантных функций (ЛДФ): ЛДФ1, которая характеризует течение у ребенка мультисистемного воспалительного синдрома, ассоциированного с SARS-CoV-2 (МВС-Д); ЛДФ2, которая характеризует течение у ребенка синдрома Кавасаки (СК) и ЛДФЗ, которая характеризует течение у ребенка инфекционного заболевания, осложненного сепсисом (ИЗоС):
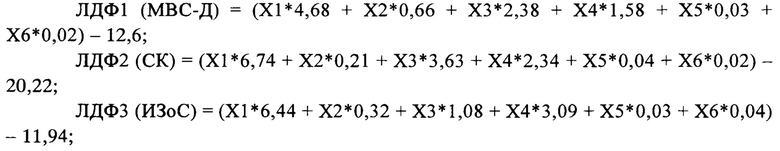
где
X1 - пол (1 - женский; 2 - мужской),
Х2 - возраст (годы),
Х3 - поражение кожи и слизистых оболочек (сумма баллов: 0 - нет; 1 балл -сыпь, 1 балл - двусторонний негнойный конъюнктивит и/или склерит; 1 балл -поражение слизистых оболочек ротовой полости и губ и/или сосочковый язык; 1 балл - изменения кожи кистей и/или стоп (плотный отек, яркая эритема кожных покровов)),
Х4 - поражение нервной системы (сумма баллов: 0 - нет; 1 балл -положительные менингеальные симптомы; 1 балл - наличие очаговой симптоматики),
Х5 - уровень тромбоцитов (*109/л),
Х6 - уровень прокальцитонина (нг/мл).
Сравнивают значения показателей ЛДФ1, ЛДФ2 и ЛДФ3: при максимальном значении ЛДФ1, 2 или 3 диагностируют соответственно МВС-Д, СК или ИЗоС.
Авторы, профессионально занимаясь диагностикой и лечением детей с СК, ИЗоС в течение многих лет, а также МВС-Д в течение последних 3 лет обратили внимание на тот неочевидный факт, что при одной и той же терапии у пациентов с данными заболеваниями отмечается разный характер течения воспалительного процесса. При этом традиционно используемые методики такие, как сбор анамнеза, клинический осмотр пациента и лабораторные данные не всегда позволяют с точностью провести дифференциальную диагностику между МВС-Д и СК, ИЗоС, а сопутствующее выявление этиологического агента не всегда исключает течение другого основного процесса. В связи с этим фактом, авторы для осуществления прогноза впервые предложили 6 клинико-лабораторных параметров, выбор которых был не очевиден и получен экспериментальным путем при анализе клинических и лабораторных показателей в группах детей с МВС-Д, СК и ИЗоС, госпитализированных в ФГБУ ДНКЦИБ ФМБА России с 2017 по 2022 г. Путем статистической обработки полученных данных авторы впервые выявили наиболее значимые для прогноза характера течения признаки, имевшие достоверные различия в анализируемых группах. Статистическая обработка результатов исследования проводилась с использованием пакета прикладных программ Statistica 7.0. При нормальном распределении выборки сравнительный анализ количественных данных в трех независимых группах проводился с помощью однофакторного дисперсионного анализа. Если распределение в выборках отличалось от нормального, сравнительный анализ количественных признаков в трех независимых группах проводили с помощью критерия Краскела-Уоллиса. Сравнительный анализ качественных признаков в трех независимых группах проводили с помощью критерия хи-квадрат Пирсона. Различия считались статистически значимыми при р<0,05. Расчет ЛДФ проводился помощью дискриминантного анализа.
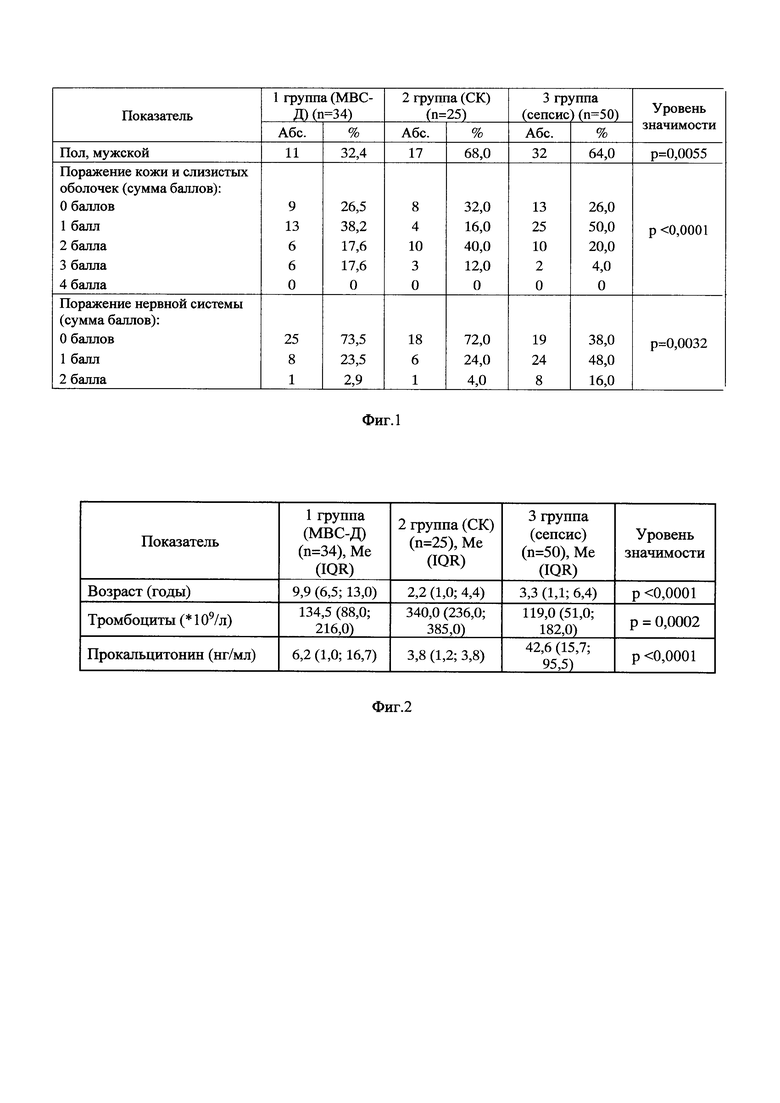
Впервые авторами при сопоставлении клинико-лабораторных показателей были выявлены достоверные различия пола, возраста, поражения кожи и слизистых оболочек, поражения нервной системы, а также уровня тромбоцитов и прокальцитонина у детей с МВС-Д, СК и ИЗоС. Качественные и количественные показатели у детей с МВС-Д, СК и ИЗоС (фиг.1 и 2 соответственно). За каждый симптом, относящийся к поражению той или иной системы, начислялся балл.
При поражении кожи и слизистых оболочек сумма баллов складывалась из наличия/отсутствия следующих признаков: 0 - нет признаков поражения кожи и слизистых оболочек; 1 балл - сыпь, 1 балл - двусторонний негнойный конъюнктивит и/или склерит; 1 балл - поражение слизистых оболочек ротовой полости и губ и/или сосочковый язык; 1 балл - изменения кожи кистей, стоп (плотный отек, яркая эритема кожных покровов).
При поражении нервной системы сумма баллов складывалась из наличия/отсутствия следующих признаков: 0 - нет признаков поражения нервной системы; 1 балл - положительные менингеальные симптомы; 1 балл - наличие очаговой симптоматики.
Путем статистической обработки данных, авторами впервые доказано, что прокальцитонин, являясь более чувствительным маркером, выступает как более значимый лабораторный критерий воспаления: у детей с МВС-Д был выше, чем у детей с СК, и значительно ниже, чем у пациентов с ИЗоС. Количественные показатели (возраст, уровень тромбоцитов и прокальцитонина) у детей с МВС-Д, СК и ИЗоС (фиг. 2).
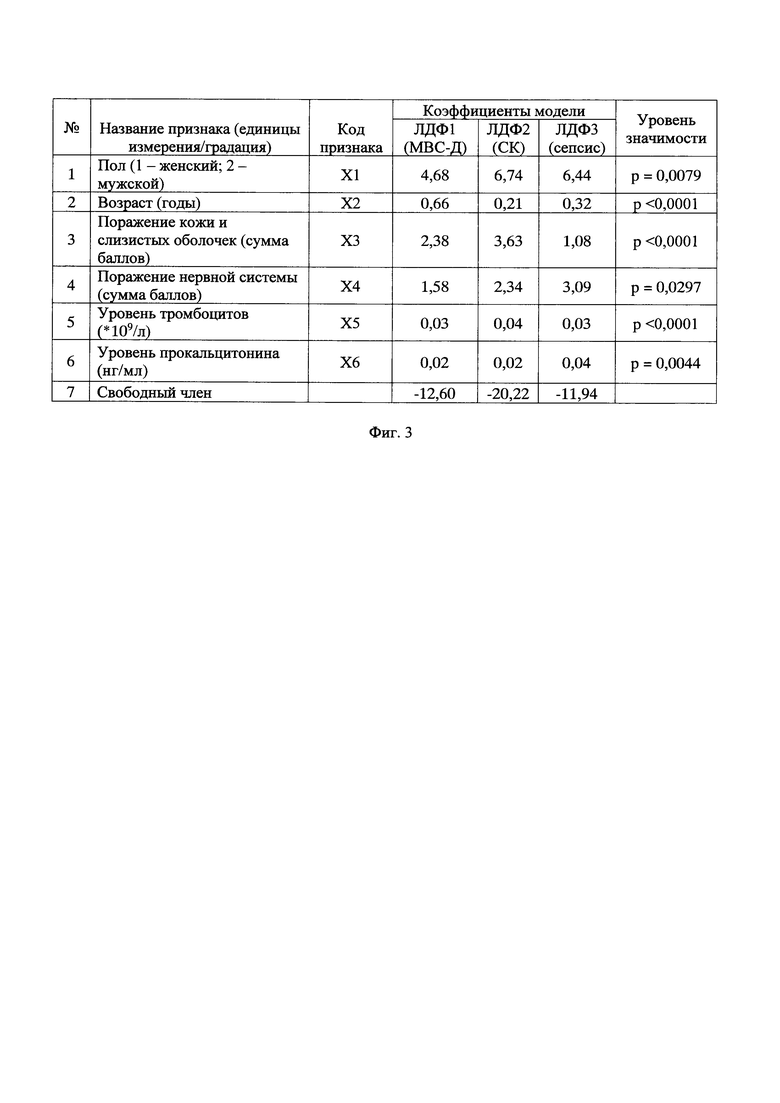
На основании полученных статистических данных, для каждого пациента с помощью математической модели был определен диагноз (МВС-Д, СК или ИЗоС) по преобладающему абсолютному значению одной из трех ЛДФ. Перечень факторов, включенных в дискриминантную модель, их коды и коэффициенты модели (фиг. 3).
Авторы впервые доказали, что только совокупность шести клинико-лабораторных параметров с последующим расчетом ЛДФ1, ЛДФ2 и ЛДФ3 позволяет диагностировать МВС-Д, СК или ИЗоС соответственно. Точность диагностики в среднем характеризуется достоверностью 85,3%, для первой группы - 82,4%, второй - 88,0%, третьей - 86,0%. Недостаточная точность для первой группы объясняется * перекрытием симптомов для этой группы с группами сравнения (2 и 3) (р<0,0001).
Новизна и неочевидность использования совокупности таких признаков как пол, возраст, кожные проявления, поражение нервной системы, уровень тромбоцитов и прокальцитонина в сыворотке крови позволяют проводить дифференциальную диагностику МВС-Д с СК и ИЗоС с высокой диагностической точностью.
В доступной нам литературе подобных способов дифференциальной диагностики МВС-Д не обнаружено, а совокупность предложенных клинических и лабораторных признаков, новизна и эффективность позволяют нам представить способ, как заявочный материал на изобретение.
Способ осуществляется следующим образом.
При госпитализации ребенка с подозрением на МВС-Д, СК или ИЗоС определяется пол и возраст пациента, проводится первичный клинический осмотр, где оцениваются симптомы поражения кожи и слизистых оболочек, а также нервной системы (количество симптомов складывается в сумму баллов). В клиническом анализе крови определяют уровень тромбоцитов, выполняют прокальцитониновый тест.
Для проведения дифференциальной диагностики у конкретного больного необходимо исследовать у него значения признаков, включенных в модель, подставить их в приведенные уравнения ЛДФ и решить их. Под X понимается конкретное значение показателя у конкретного больного. Наиболее вероятно будет тот диагноз, значение ЛДФ которого окажется наибольшим с учетом знака.
Разработанный нами способ диагностики МВС-Д, СК или ИЗоС у детей был апробирован у 109 детей в возрасте от 1 месяца до 17 лет 11 месяцев 29 дней, поступивших в ФГБУ ДНКЦИБ ФМБА России в период с 2017 по 2022 гг. Из них 34 пациента составили группу МВС-Д (1 группа), 25 детей - СК (2 группа) и 50 детей - ИЗоС (3 группа). Всем пациентам (n=109) было проведено стандартное клиническое и лабораторное обследование, включая определение прокальцитонина (нг/мл).
Высокая эффективность заявляемого способа дифференциальной диагностики МВС-Д, СК или ИЗоС у детей проиллюстрирована нижеследующими примерами.
Пример 1
Девочка 13 лет. В январе 2021 года госпитализирована в ФГБУ ДНКЦИБ ФМБА России с подозрением на генерализованную вирусно-бактериальную инфекцию неуточненной этиологии, осложненную синдромом системного воспалительного ответа (ССВО). Заболевание развилось через 4 недели после перенесенной НКИ. При обследовании выявлено повышение СОЭ (58 мм/ч), уровня СРБ (444,0 мг/л), ферритина (21,4 мкг/дл), фибриногена (7,7 г/л). Этиологический агент не обнаружен. Заподозрено течение МВС-Д.
С целью проведения дифференциального диагноза пациентке была определена концентрация тромбоцитов (94*109/л) и прокальцитонина (1,2 нг/мл). Полученные данные (женский пол (1), возраст - 13 лет, поражение кожных покровов и слизистых оболочек - 3 балла, поражение нервной системы - 0 баллов) были подставлены в ЛДФ. При расчете математико-статистической модели получено:
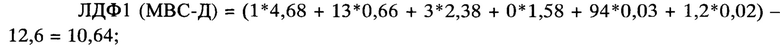
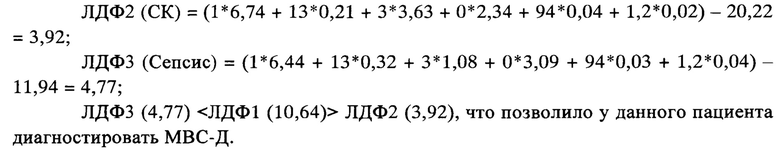
По итогам динамике течения и исхода заболевания, а также по результатам экспертного опроса ведущих специалистов ФГБУ ДНКЦИБ ФМБА России, проведенного ретроспективно, девочке установлен диагноз МВС-Д, чем подтвержден расчетный метод.
Пациентке начата терапия иммуноглобулином человека нормальным (для внутривенного введения) и глюкокортикостероидами, назначена ацетилсалициловая кислота с целью профилактики поражения коронарных сосудов.
Приведенный пример доказывает эффективность предложенного способа дифференциальной диагностики МВС-Д.
Пример 2
Мальчик 11 месяцев 14 дней. В феврале 2021 года госпитализирован в ФГБУ ДНКЦИБ ФМБА России с предварительным диагнозом: острый энтероколит, осложненный эксикозом 1 степени. Впоследствии течение заболевания осложнилось ССВО. При обследовании выявлено повышение СОЭ (55 мм/ч), уровня СРБ (106,9 мг/л), ферритина (17,0 мкг/дл), фибриногена (4,0 г/л). Этиологический агент не установлен, обнаружены IgG к SARS-CoV-2. Проводился дифференциальный диагноз синдрома Кавасаки с МВС-Д.
С целью дальнейшей диагностики была определена концентрация тромбоцитов (449*109/л) и прокальцитонина (11,5 нг/мл). Полученные данные (мужской пол (2), возраст - 0,94 года, поражение кожных покровов и слизистых оболочек - 4 балла, поражение нервной системы - 0 баллов) были подставлены в ЛДФ. При расчете математико-статистической модели получено:

По итогам динамики течения и исхода заболевания, а также по результатам экспертного опроса ведущих специалистов ФГБУ ДНКЦИБ ФМБА России, проведенного ретроспективно, мальчику установлен диагноз СК, чем подтвержден расчетный метод.
Пациенту начата терапия иммуноглобулином человека нормальным (для внутривенного введения) и назначена ацетилсалициловая кислота с целью профилактики поражения коронарных сосудов.
Приведенный пример доказывает эффективность предложенного способа дифференциальной диагностики МВС-Д и СК.
Пример 3
Девочка 5 лет. В июне 2021 года госпитализирована в ФГБУ ДНКЦИБ ФМБА России с подозрением на острый менингоэнцефалит неуточненной этиологии, осложненный сепсисом. При обследовании выявлено повышение СОЭ (66 мм/ч), уровня СРБ (505,4 мг/л), ферритина (15,9 мкг/дл), фибриногена (11,2 г/л). Обнаружены IgG к SARS-CoV-2. Заподозрено течение МВС-Д, проводился дифференциальный диагноз с сепсисом.
Пациентке была определена концентрация тромбоцитов (51*109/л, прокальцитонина (200 нг/мл). Полученные данные (женский пол (1), возраст - 5 лет, поражение кожных покровов и слизистых оболочек - 2 балла, поражение нервной системы - 2 баллов) были подставлены в ЛДФ. При расчете математико-статистической модели получено:

В дальнейшем по результатам люмбальной пункции диагностирован бактериальный гнойный менингит, методом полимеразной цепной реакции из крови и ликвора выделены нуклеиновые кислоты Haemophilus influenzae (нетипирована). Таким образом, у ребенка имела место генерализованная гемофильная инфекция, осложненная сепсисом, что подтверждено расчетным методом.
Девочке начата антибактериальная терапия.
Приведенный пример доказывает эффективность предложенного способа дифференциальной диагностики МВС-Д и сепсиса.
Таким образом, использование предлагаемого метода позволяет на основании определения простых и широкодоступных показателей своевременно диагностировать МВС-Д. Ранняя диагностика заболевания позволяет своевременно назначить терапию, направленную на подавление гипервоспалительного ответа, и положительно влияет на исход заболевания, улучшает качество жизни ребенка и предотвращает развитие отдаленных осложнений (например, поражение миокарда и коронарных сосудов).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения мультисистемного воспалительного синдрома у детей, ассоциированного с SARS-CoV-2 | 2021 |
|
RU2780939C1 |
| Способ ранней дифференциальной диагностики вирусной и бактериальной внебольничной пневмонии у детей | 2022 |
|
RU2790239C1 |
| СПОСОБ РАННЕГО ПРОГНОЗИРОВАНИЯ ХАРАКТЕРА ТЕЧЕНИЯ ОСТРОЙ РЕСПИРАТОРНОЙ ИНФЕКЦИИ У ДЕТЕЙ | 2017 |
|
RU2659384C1 |
| Способ прогнозирования развития неспецифических осложнений острых кишечных инфекций с синдромом гемоколита у детей | 2019 |
|
RU2704132C1 |
| Способ прогнозирования характера течения воспалительных заболеваний нервной системы у детей | 2018 |
|
RU2689797C1 |
| Способ прогноза риска летального исхода COVID-19 у пациентов молодого возраста | 2023 |
|
RU2803002C1 |
| Способ дифференциальной диагностики латентной и активной форм ВГЧ-6 инфекции у детей | 2023 |
|
RU2817089C1 |
| Способ комплексной терапии пациентов детского возраста с вирусной инфекцией с использованием продуктов пробиотического питания | 2021 |
|
RU2793833C1 |
| Способ прогнозирования степени тяжести гемолитико-уремического синдрома у детей с инфекционными заболеваниями | 2022 |
|
RU2797122C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЛЕТАЛЬНОГО ИСХОДА У ПАЦИЕНТОВ С COVID-19 В ТЕЧЕНИЕ ПЕРВЫХ СУТОК ГОСПИТАЛИЗАЦИИ ПО ДАННЫМ КОМПЛЕКСНОГО ОБСЛЕДОВАНИЯ | 2024 |
|
RU2838790C1 |
Изобретение относится к медицине, а именно к инфекционным болезням, педиатрии, анестезиологии-реаниматологии, и может быть использовано для дифференциальной диагностики мультисистемного воспалительного синдрома у детей, ассоциированного с SARS-CoV-2, синдрома Кавасаки или инфекционных заболеваний, осложненных сепсисом. Определяют: пол, возраст, поражение кожи и слизистых оболочек, поражение нервной системы, уровень тромбоцитов и прокальцитонина, полученные значения вносят в формулу расчета линейных дискриминантных функций. Способ позволяет осуществить своевременную диагностику МВС-Д, своевременно назначить терапию, направленную на подавление гипервоспалительного ответа, что положительно влияет на исход заболевания, улучшает качество жизни ребенка и предотвращает развитие отдаленных осложнений за счет оценки совокупности наиболее значимых показателей. 3 табл., 3 пр.
Способ дифференциальной диагностики мультисистемного воспалительного синдрома у детей, ассоциированного с SARS-CoV-2, включающий клиническо-лабораторное обследование, отличающийся тем, что определяют: пол, возраст, поражение кожи и слизистых оболочек, поражение нервной системы, уровень тромбоцитов и прокальцитонина, полученные значения вносят в формулу расчета линейных дискриминантных функций:
ЛДФ1 - мультисистемный воспалительный синдром, ассоциированный с SARS-CoV-2:
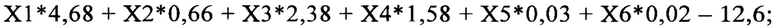
ЛДФ2 - синдром Кавасаки:
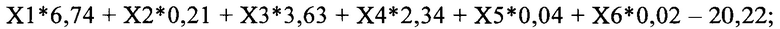
ЛДФ3 - инфекционное заболевание, осложненное сепсисом:
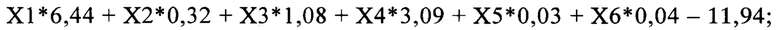
где
X1 - пол: 1 - женский; 2 - мужской;
Х2 - возраст: годы;
Х3 - поражение кожи и слизистых оболочек: сумма баллов: 0 - нет; 1 балл - сыпь; 1 балл - двусторонний негнойный конъюнктивит и/или склерит; 1 балл - поражение слизистых оболочек ротовой полости и губ и/или сосочковый язык; 1 балл - изменения кожи кистей и/или стоп: плотный отек, яркая эритема кожных покровов;
Х4 - поражение нервной системы: сумма баллов: 0 - нет; 1 балл - положительные менингеальные симптомы; 1 балл - наличие очаговой симптоматики;
Х5 - уровень тромбоцитов: *109/л;
Х6 - уровень прокальцитонина: нг/мл;
сравнивают значения показателей ЛДФ1, ЛДФ2 и ЛДФ3: при максимальном значении ЛДФ1, 2 или 3 диагностируют соответственно мультисистемный воспалительный синдром, ассоциированный с SARS-CoV-2, синдром Кавасаки или инфекционное заболевание, осложненное сепсисом.
| Судно | 1934 |
|
SU41867A1 |
| АШИНА Л.Н | |||
| и др | |||
| Мультисистемный воспалительный синдром, ассоциированный с covid-19 (Кавасаки-подобный синдром), у детей (случай из практики) | |||
| Здравоохранение Дальнего Востока | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| стр | |||
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| PEREZ-GOMEZ HR | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2024-03-29—Публикация
2023-03-24—Подача