Настоящее изобретение относится к пестицидно активным, в частности к инсектицидно активным, гетероциклическим производным, содержащим сульфоксиминовые заместители, к способам их получения, к композициям, содержащим такие соединения, а также к их применению для контроля животных-вредителей, включая членистоногих, и в частности насекомых или представителей отряда Acarina.
Пестицидно активные гетеробициклические замещенные циклопропильные производные с серосодержащими заместителями известны и описаны в литературе, например, в WO 2018/077565, WO 2018/070502, WO 2017/146226, WO 2017/089190, WO 2017/084879, WO 2016/121997, WO 2016/104746, WO 2016/096584, WO 2016/046071, WO 2016/071214, WO 2016/039441, WO 2016/026848, WO 2016/023954, WO 2014/142292 и WO 2016/020286. Пестицидно активные гетероциклические сульфоксиминовые производные были ранее описаны в литературе, например, в WO 2015/071180.
В настоящее время неожиданно было обнаружено, что некоторые новые бициклические сульфоксиминсодержащие замещенные циклопропильные производные обладают подходящими свойствами в качестве пестицидов.
Таким образом, в настоящем изобретении предусматриваются соединения формулы (I)
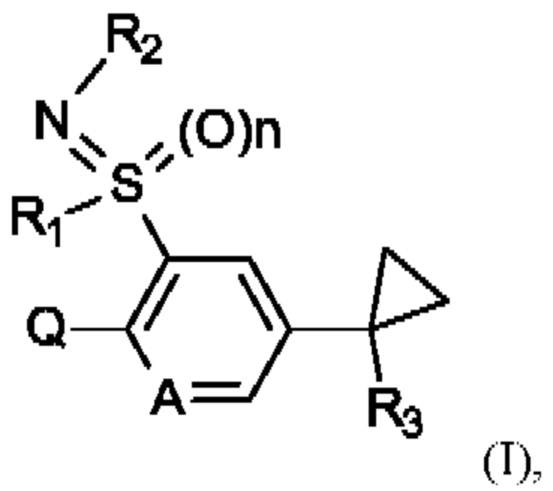
где
А представляет собой СН или N,
R1 представляет собой С1-С4алкил,
R2 представляет собой водород, циано, -C(О)R7, -C(О)OR8, С1-С6алкил или -CONR9R10,
SO2R11,
при этом
R7 представляет собой водород, C1-С6алкил или C1-С6галогеналкил, и R8 представляет собой C1-С6алкил или C1-С6галогеналкил;
R9, R10 независимо друг от друга представляют собой водород или C1-С6алкил;
R11 представляет собой C1-С6алкил;
R3 представляет собой водород, C1-С3алкил, C1-С3галогеналкил, циано, -СО2Н, -CO2NH2, С1-С4алкоксикарбонил, С1-С4алкиламинокарбонил, C1-С4диалкиламинокарбонил;
n равняется 0 или 1;
Q представляет собой радикал, выбранный из группы, состоящей из формул Q1, Q2, Q3, Q4 и Q5,
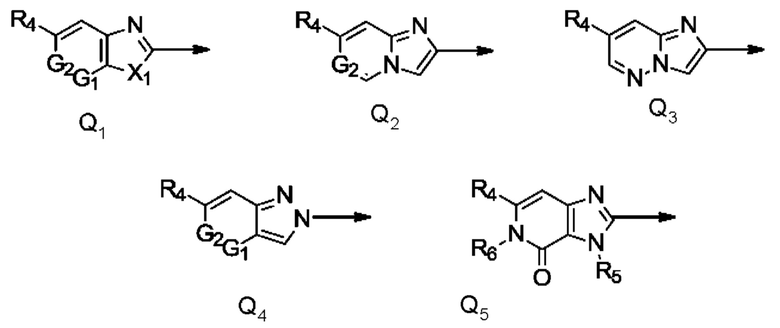
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой галоген, C1-С6галогеналкил, С1-С4галогеналкилсульфанил, C1-С4галогеналкилсульфинил, С1-С4галогеналкилсульфонил или C1-С6галогеналкокси;
X1 представляет собой О или NR5;
R5 представляет собой С1-С4алкил;
R6 представляет собой С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси или С3-С6циклоалкил;
G1 и G2 независимо друг от друга представляют собой N или СН;
или агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид соединения формулы I.
Соединения формулы I, которые содержат по меньшей мере один основный центр, могут образовывать, например, соли присоединения кислоты, например, с сильными неорганическими кислотами, такими как минеральные кислоты, например, хлорная кислота, серная кислота, азотная кислота, азотистая кислота, фосфорная кислота или галогенводородная кислота, с сильными органическими карбоновыми кислотами, такими как С1-С4алканкарбоновые кислоты, которые являются незамещенными или замещенными, например, галогеном, например, уксусная кислота, такими как насыщенные или ненасыщенные дикарбоновые кислоты, например, щавелевая кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота или фталевая кислота, такими как гидроксикарбоновые кислоты, например, аскорбиновая кислота, молочная кислота, яблочная кислота, винная кислота или лимонная кислота, или такими как бензойная кислота, или с органическими сульфоновыми кислотами, такими как С1-С4алкан- или арилсульфоновые кислоты, который являются незамещенными или замещенными, например, галогеном, например, метан- или п-толуолсульфоновая кислота. Соединения формулы I, которые содержат по меньшей мере одну кислотную группу, могут образовывать, например, соли с основаниями, например минеральные соли, такие как соли щелочных металлов или щелочноземельных металлов, например, соли натрия, калия или магния, или соли с аммиаком или органическим амином, таким как морфолин, пиперидин, пирролидин, низший моно-, ди- или триалкиламин, например, этил-, диэтил-, триэтил- или диметил пропил амин, либо низший моно-, ди- или тригидроксиалкиламин, например, моно-, ди- или триэтаноламин.
Термин "С1-Сnалкил", применяемый в данном документе, относится к насыщенному углеводородному радикалу с прямой или разветвленной цепью, присоединенному с помощью любого из атомов углерода, имеющему от 1 до n атомов углерода, например к любому из радикалов, представляющих собой метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, пентил, гексил, и их разветвленным изомерам. Например, также могут быть указаны любые из радикалов, представляющих собой 1-метилбутил, 2-метилбутил, 3-метилбутил, 2,2-диметилпропил, 1-этилпропил, н-гексил, н-пентил, 1,1-диметилпропил, 1,2-диметилпропил, 1-метилпентил, 2-метилпентил, 3 метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил или 1-этил-2-метилпропил. Как указано ниже, радикалы, представленные галогеналкилом, галогеналкилсульфанилом, галогеналкилсульфинилом, галогеналкилсульфонилом, алкокси и галогеналкокси, получены из алкильных радикалов.
Галоген, как правило, представляет собой фтор, хлор, бром или йод. Это также применимо, соответственно, к галогену в комбинации с другими значениями, такими как галогеналкил.
Термин "C1-Сnгалогеналкил", применяемый в данном документе, относится к насыщенному С1-Сnалкильному радикалу с прямой или разветвленной цепью, имеющему от 1 до n атомов углерода (как указанно выше), при этом некоторые или все атомы водорода в данных радикалах могут быть заменены на фтор, хлор, бром и/или иод, т.е., например, например, любому из хлорметила, дихлорметила, трихлорметила, фторметила, дифторметила, трифторметила, хлорфторметила, дихлорфторметила, хлордифторметила, 2-фторэтила, 2-хлорэтила, 2-бромэтила, 2-иодэтила, 2,2-дифторэтила, 2,2,2-трифторэтила, 2-хлор-2-фторэтила, 2-хлор-2,2-дифторэтила, 2,2-дихлор-2-фторэтила, 2,2,2-трихлорэтила, пентафторэтила, 2-фторпропила, 3-фторпропила, 2,2-дифторпропила, 2,3-дифторпропила, 2-хлорпропила, 3-хлорпропила, 2,3-дихлорпропила, 2-бромпропила, 3-бромпропила, 3,3,3-трифторпропила, 3,3,3-трихлорпропила, 2,2,3,3,3-пентафторпропила, гептафторпропила, 1-(фторметил)-2-фторэтила, 1-(хлорметил)-2-хлорэтила, 1-(бромметил)-2-бромэтила, 4-фторбутила, 4-хлорбутила, 4-бромбутила, нонафторбутила, 1,1-дифтор-2,2,2-трихлорэтила и 2,2,3,3-тетрафторэтила; предпочтительно трихлорметила, дифторхлорметила, дифторметила, трифторметила и дихлорфторметила.
Термин "С1-Сnалкокси", применяемый в данном документе, относится к насыщенному С1-Сnалкильному радикалу с прямой или разветвленной цепью, имеющему от 1 до n атомов углерода (как указано выше), который присоединен с помощью атома кислорода, т.е., например, любому из радикалов, представляющих собой метокси, этокси, пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, 1-метилпропокси, 2-метилпропокси и 1,1-диметилэтокси, а также изомерным формам радикалов пентилокси и гексилокси; предпочтительно метокси и этокси.
Термин "С1-Сnгалогеналкокси", применяемый в данном документе, относится к насыщенному С1-Сnгалогеналкильному радикалу с прямой или разветвленной цепью, имеющему от 1 до n атомов углерода (как указано выше), который присоединен с помощью атома кислорода, аналогично С1-Сnалкокси.
Термин "С1-Сnалкилсульфанил" применяемый в данном документе относится к насыщенному алкильному радикалу с прямой или разветвленной цепью, имеющему от 1 до n атомов углерода (как указано выше), который присоединен с помощью атома серы, т.е., например, любому из метилтио, этилтио, н-пропилтио, 1-метилэтилтио, бутилтио, 1-метилпропилтио, 2-метилпропилтио или 1,1-диметилэтилтио.
Термин "С1-Сnгалогеналкилсульфанил", применяемый в данном документе, относится к С1-Сnалкилсульфанильному радикалу, как указано выше, который частично или полностью замещен фтором, хлором, бромом и/или иодом, т.е., например, любому из фторметилтио, дифторметилтио, трифторметилтио, хлордифторметилтио, бромдифторметилтио, 2-фторэтилтио, 2-хлорэтилтио, 2-бромэтилтио, 2-иодэтилтио, 2,2-дифторэтилтио, 2,2,2-трифторэтилтио, 2,2,2-трихлорэтилтио, 2-хлор-2-фторэтилтио, 2-хлор-2,2-дифторэтилтио, 2,2-дихлор-2-фторэтилтио, пентафторэтилтио, 2-фторпропилтио, 3-фторпропилтио, 2-хлорпропилтио, 3-хлорпропилтио, 2-бромпропилтио, 3-бромпропилтио, 2,2-дифторпропилтио, 2,3-дифторпропилтио, 2,3-дихлорпропилтио, 3,3,3-трифторпропилтио, 3,3,3-трихлорпропилтио, 2,2,3,3,3-пентафторпропилтио, гептафторпропилтио, 1-(фторметил)-2-фторэтилтио, 1-(хлорметил)-2-хлорэтилтио, 1-(бромметил)-2-бромэтилтио, 4-фторбутилтио, 4-хлорбутилтио или 4-бромбутилтио.
Подобные принципы применимы к терминам "С1-Сnгалогеналкилсульфинил" и "C1-Сnгалогеналкилсульфонил", которые относятся к С1-Сnгалогеналкилсульфанилу (как указано выше), но с атомом серы, находящимся в разных степенях окисления, например, сульфоксид-S(О)С1-Сnгалогеналкилу или сульфон-S(О)2С1-Сnгалогеналкилу соответственно. Соответственно, например, предусматриваются группы, такие как трифторметилсульфинил, трифторметилсульфонил или 2,2,2-трифторэтилсульфонил.
Термин "С3-С6циклоалкил", применяемый в данном документе, относится к 3-6-членным циклоалкильным группам, таким как циклопропан, циклобутан, циклопропан, циклопентан и циклогексан.
Термин "С1-Сnалкоксикарбонил" относится к насыщенному С1-Сnалкокси-радикалу с прямой или разветвленной цепью, имеющему от 1 до n атомов углерода (как указано выше), который присоединен с помощью карбонильной группы.
Термин "С1-Сnалкиламинокарбонил" относится к насыщенному С1-Сnалкильному радикалу с прямой или разветвленной цепью, имеющему от 1 до n атомов углерода (как указано выше), который присоединен с помощью атома азота аминокарбонильной группы.
Термин "С1-Сnдиалкиламинокарбонил" относится к двум насыщенным С1-Сnалкильным радикалам с прямой или разветвленной цепью, имеющим от 1 до n атомов углерода (как указано выше), являющимся одинаковыми или различными, которые присоединены с помощью атома азота аминокарбонильной группы.
Концевые одинарные связи (свободные радикалы) представляют собой метальную группу в контексте приведенной молекулярной структуры или представляют собой точку присоединения в контексте определения переменной группы.
Соединения формулы I в соответствии с настоящим изобретением также включают гидраты, которые могут быть образованы в ходе солеобразования.
Варианты осуществления согласно настоящему изобретению изложены ниже.
В варианте осуществления 1 предусмотрены соединения формулы I или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид, определенные выше.
В варианте осуществления 2 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
А представляет собой СН или N;
R1 представляет собой этил, пропил или изопропил;
R2 представляет собой водород, циано, C1-С3алкил, C1-С3алкилкарбонил, C1-С3алкоксикарбонил, C1-С3галогеналкилкарбонил;
R3 представляет собой водород, C1-С3галогеналкил, циано, -СО2Н, -CO2NH2, C1-С4диалкиламинокарбонил; и
n равняется 1.
В варианте осуществления 3 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород, С1-С2галогеналкил, циано, -CO2NH2, C1-С2диалкиламинокарбонил; и
n равняется 1.
В варианте осуществления 4 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород, циано или CO2NH2; и
n равняется 1.
В варианте осуществления 5 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород или циано; и
n равняется 1.
В варианте осуществления 6 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
Q представляет собой радикал, выбранный из Q1, Q2, Q4 и Q5,
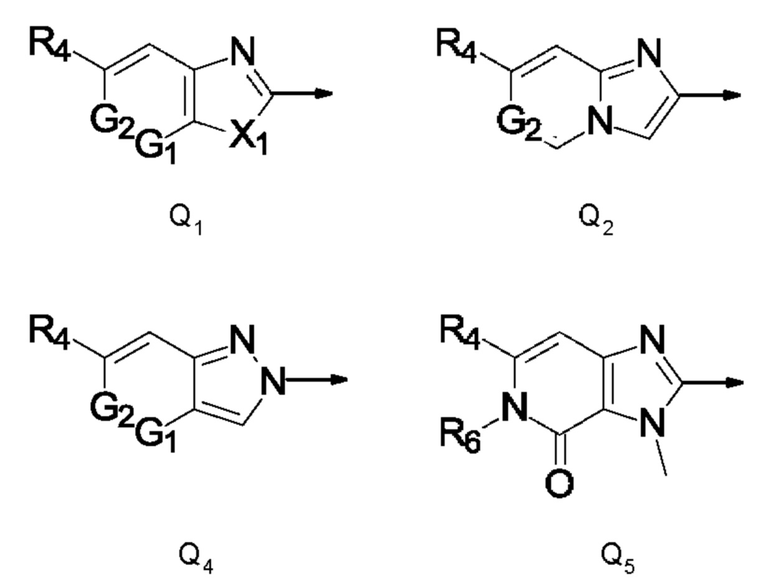
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой С1-С2галогеналкил, С1-С2галогеналкилсульфанил, C1-С2галогеналкилсульфинил или С1-С2галогеналкилсульфонил;
X1 представляет собой кислород или NCH3;
R6 представляет собой С1-С2алкил, С1-С2галогеналкил, С1-С2алкокси или циклопропил;
и
G1 и G2 независимо друг от друга представляют собой N или СН.
В варианте осуществления 7 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
представляет собой радикал, выбранный из Q1, Q2 и Q5,
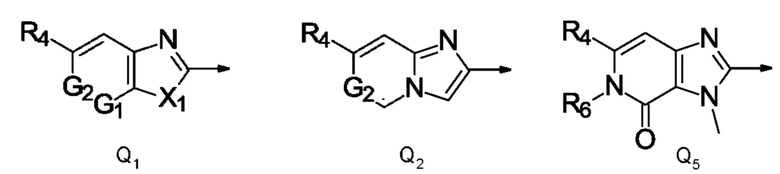
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой С1-С2фторалкил, трифторметилсульфанил, трифторметилсульфинил, трифторметилсульфонил, дифторметилсульфанил, дифторметилсульфинил или дифторметилсульфонил;
X1 представляет собой NCH3;
R6 представляет собой метил, этил, 2,2,2-трифторэтил, метокси или циклопропил; и
G1 и G2 независимо друг от друга представляют собой N или СН.
В варианте осуществления 8 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
Q представляет собой радикал, выбранный из Q1 и Q5,
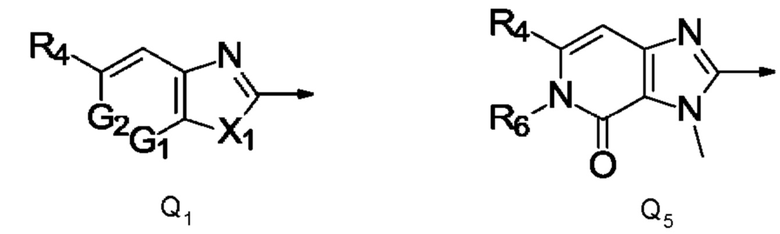
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой трифторметил, пентафторэтил, трифторметилсульфанил, трифтор метилсульфинил или трифторметилсульфонил;
X1 представляет собой NCH3;
R6 представляет собой этил, метокси или циклопропил; и
G1 представляет собой N, a G2 представляет собой СН, или G1 представляет собой СН, а
G2 представляет собой N, или G1 и G2 представляют собой N, или G1 и G2 представляют собой СН.
В варианте осуществления 9 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
Q представляет собой радикал Q1,
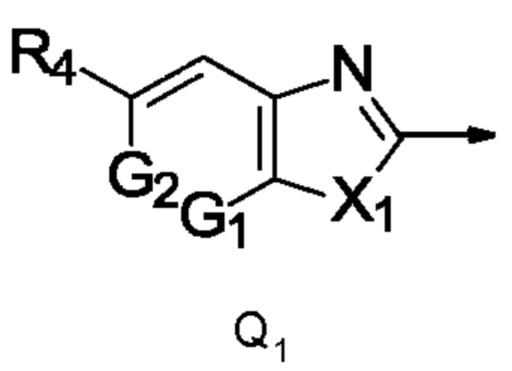
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой трифторметил;
X1 представляет собой NCH3; и
G1 представляет собой N, a G2 представляет собой СН, G1 представляет собой СН, a G2 представляет собой N, или G1 и G2 представляют собой N.
В варианте осуществления 10 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
А представляет собой СН или N;
R1 представляет собой этил, пропил или изопропил;
R2 представляет собой водород, циано, C1-С3алкил, C1-С3алкилкарбонил, C1-С3алкоксикарбонил, C1-С3галогеналкилкарбонил;
R3 представляет собой водород, C1-С3галогеналкил, циано, CO2H, CO2NH2, C1-С4диалкиламинокарбонил;
n равняется 1;
Q представляет собой радикал, выбранный из Q1, Q2, Q4 и Q5,
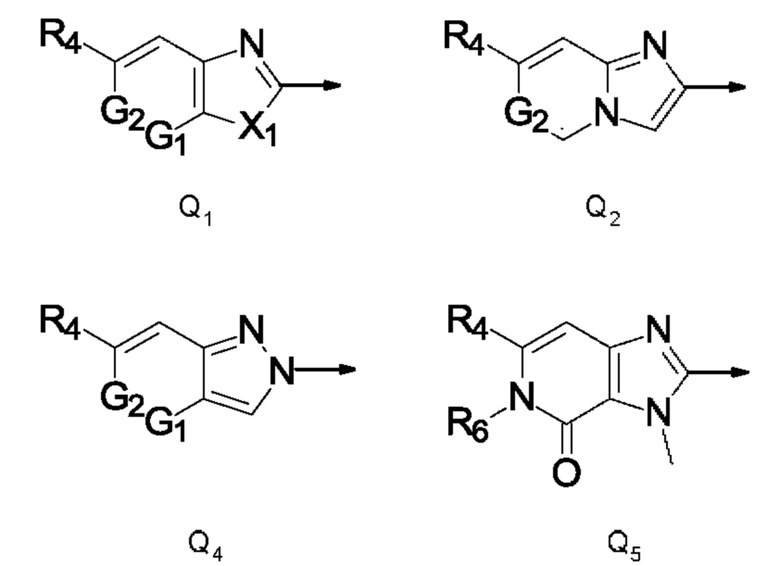
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой С1-С2галогеналкил, С1-С2галогеналкилсульфанил, C1-С2галогеналкилсульфинил или С1-С2галогеналкилсульфонил;
X1 представляет собой кислород или NCH3;
R6 представляет собой С1-С2алкил, С1-С2галогеналкил, С1-С2алкокси или циклопропил; и
G1 и G2 независимо друг от друга представляют собой N или СН.
В варианте осуществления 11 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород, С1-С2галогеналкил, циано, CO2NH2, C1-С2диалкиламинокарбонил;
n равняется 1;
Q представляет собой радикал, выбранный из Q1, Q2 и Q5,
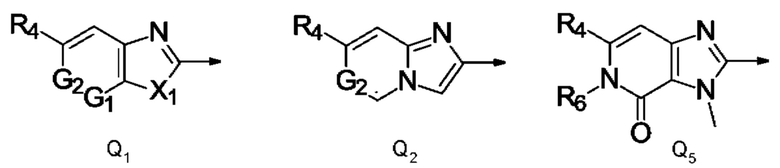
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой С1-С2фторалкил, трифторметилсульфанил, трифторметилсульфинил, трифторметилсульфонил, дифторметилсульфанил, дифторметилсульфинил или дифторметилсульфонил;
X1 представляет собой NCH3;
R6 представляет собой метил, этил, 2,2,2-трифторэтил, метокси или циклопропил; и
G1 и G2 независимо друг от друга представляют собой N или СН.
В варианте осуществления 12 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород, циано или CO2NH2;
n равняется 1;
Q представляет собой радикал, выбранный из Q1 и Q5,
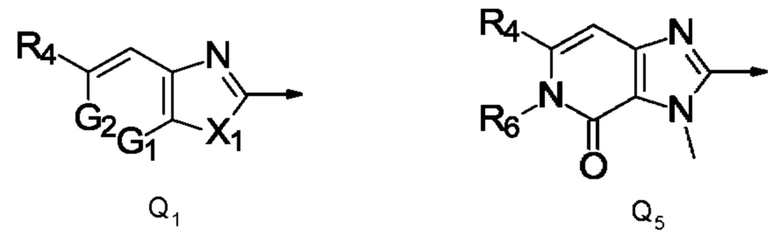
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой трифторметил, пентафторэтил, трифторметилсульфанил, трифторметилсульфинил или трифторметилсульфонил;
X1 представляет собой NCH3;
R6 представляет собой этил, метокси или циклопропил; и
G1 представляет собой N, a G2 представляет собой СН, или G1 представляет собой СН, а
G2 представляет собой N, или G1 и G2 представляют собой N, или G1 и G2 представляют собой СН.
В варианте осуществления 13 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород или циано;
n равняется 1;
Q представляет собой радикал Q1,
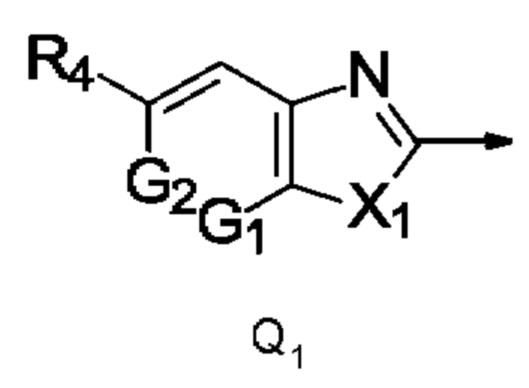
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
и где
R4 представляет собой трифторметил; X1 представляет собой NCH3; и
G1 представляет собой N, a G2 представляет собой СН, G1 представляет собой СН, a G2 представляет собой N, или G1 и G2 представляют собой N.
В варианте осуществления 14 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантами осуществления 1, 2, 3, 4 или 5, где
Q представляет собой радикал, выбранный из Q1-1, Q1-2, Q1-3, Q1-4 и Q1-5,
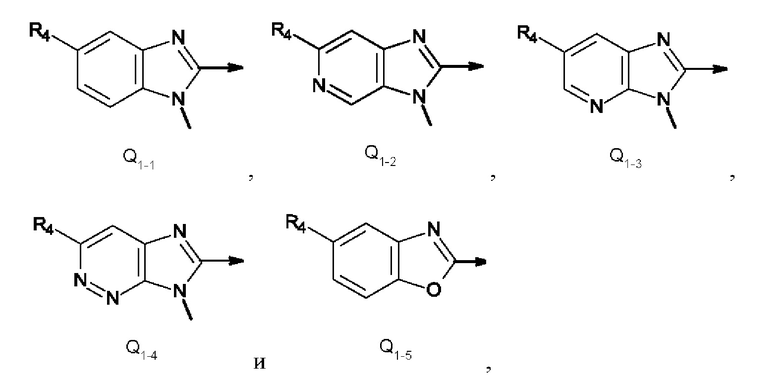
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
R4 представляет собой трифторметил, трифторметилсульфанил или трифторметилсульфонил.
В варианте осуществления 15 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантом осуществления 14,
где Q представляет собой радикал, выбранный из Q1-2, Q1-3, Q1-4 и Q1-5.
В варианте осуществления 16 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантами осуществления 1, 2, 3, 4 или 5, где
Q представляет собой радикал, выбранный из Q5,
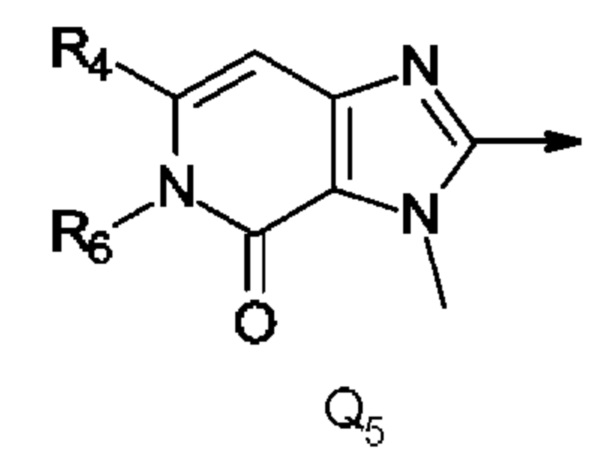
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
R4 представляет собой трифторметил, трифторметилсульфанил или трифторметилсульфонил; и
R6 представляет собой ОСН3, СН2СН3 или циклопропил.
В варианте осуществления 17 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантами осуществления 1, 2, 3, 4 или 5, где
Q представляет собой радикал Q2,
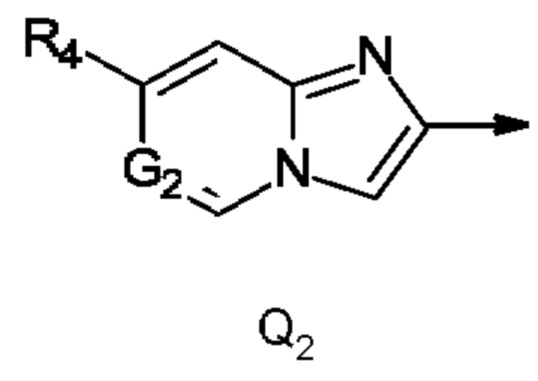
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
R4 представляет собой трифторметил, трифторметилсульфанил или трифторметилсульфонил; и
G2 представляет собой N или СН.
В варианте осуществления 18 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантами осуществления 1, 2, 3, 4 или 5, где
Q представляет собой Q3; и
R4 представляет собой трифторметил, трифторметилсульфанил или трифторметилсульфонил.
В варианте осуществления 19 предусмотрены соединения или их агрохимически приемлемая соль, стереоизомер, энантиомер, таутомер или N-оксид в соответствии с вариантами осуществления 1, 2, 3, 4 или 5, где
Q представляет собой Q4,
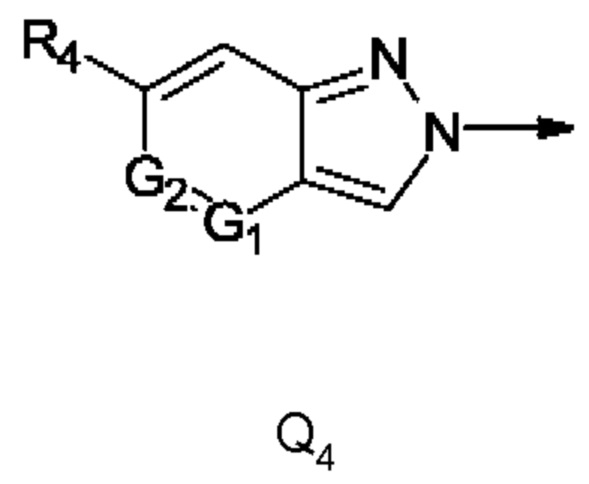
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
R4 представляет собой трифторметил, трифторметилсульфанил или трифторметилсульфонил; и
G1 представляет собой N, a G2 представляет собой СН, G1 представляет собой СН, a G2 представляет собой N, G1 и G2 представляют собой СН, или G1 и G2 представляют собой N; предпочтительно G1 представляет собой СН, a G2 представляет собой N.
В другом аспекте в настоящем изобретении предусмотрена композиция, содержащая инсектицидно, акарицидно, нематоцидно или моллюскоцидно эффективное количество соединения формулы (I) или его агрохимически приемлемой соли, стереоизомера, энантиомера, таутомера или N-оксида, как определено в любом из вышеуказанных вариантах осуществления 1-19, и необязательно вспомогательное вещество или разбавитель.
В дополнительном аспекте настоящее изобретение обеспечивает способ борьбы с насекомыми, клещами, нематодами или моллюсками и осуществления их контроля, который предусматривает применение по отношению к вредителю, к месту обитания вредителя или к растению, восприимчивому к поражению вредителем, инсектицидно, акарицидно, нематоцидно или моллюскоцидно эффективного количества соединения формулы (I) или его агрохимически приемлемой соли, стереоизомера, энантиомера, таутомера или N-оксида, как определено в любом из вышеуказанных вариантах осуществления 1-19, или композиции, как определено выше.
В еще одном дополнительном аспекте в настоящем изобретении предусмотрен способ защиты материала для размножения растения от поражения насекомыми, клещами, нематодами или моллюсками, который предусматривает обработку материала для размножения или участка, где посажен материал для размножения, с помощью композиции, определенной выше.
Процедуру получения соединений формулы (I) в соответствии с настоящим изобретением осуществляют, в целом, посредством способов, известных специалистам в данной области техники. Подгруппа соединений формулы I, где n равняется 0, т.е. представляет собой сульфилимин Ia, при этом R1, R2, R3, А и Q определены выше, может быть получена с помощью проведения реакции с участием соответствующего сульфида формулы II, где R1, R2, R3, А и Q определены выше, в условиях реакции иминирования (стадия А, схема 1). Конкретная подгруппа соединений формулы I, где n равняется 1, определенная как сульфоксимин I, где R1, R2, R3, А и Q определены выше, может быть получена с помощью окисления сульфилиминовых соединений формулы Ia, где R1, R2, R3, А, и Q определены выше (стадия В).
Схема 1
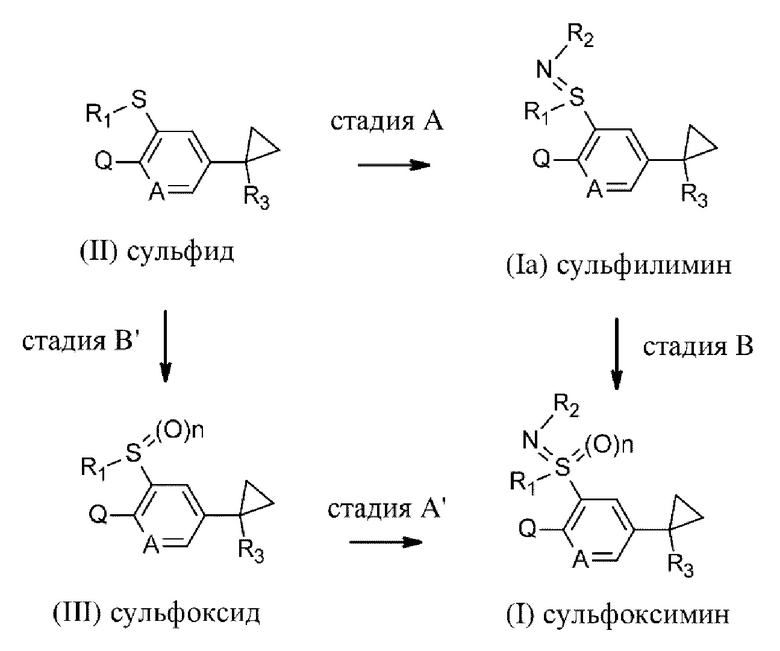
С другой стороны, порядок следования двух стадий может быть обращен, вследствие чего сульфоксиминовые соединения формулы I, где R1, R2, R3, А и Q определены выше, определены выше, могут быть получены из сульфоксидов формулы III, где R1, R2, R3, А и Q определены выше, в подходящих условиях реакции иминирования (стадия А').
Типичные способы получения и условия реакций для получения соединений формулы I, обеспечивающие получение либо сульфилиминов Ia (стадия А), либо сульфоксиминов I (стадия А'), могут быть найдены, например, в Н. Okamura, С. Bolm, Org. Lett., 2004, 6, 1305-1307; Н. Okamura, С. Bolm, Chem. Lett., 2004, 33, 482-487; D. Leca, K. Song, M. Amatore, L. Fensterbank, E. Lacote, M. Malacria, Chem. Eur. J., 2004, 10, 906-916; или M. Reggelin, C. Zur, Synthesis, 2000, 1-64. Типичные реагенты/условия для проведения иминирования могут быть определены как использование NaN3/H2SO4, О-мезитиленсульфонилгидроксиламина (MSH) или способов, предусматривающих катализ металлом [см. O.G. Mancheno, С. Bolm, Chem. Eur. J., 2007, 13, 6674-6681], как например R2-N3/FeCl2, R2-NH2/Fe(ацетилацетон)3/PhI=O, PhI=N-R2/Fe(OTf)2, PhI=N-R2/CuOTf, PhI=N-R2/Cu(OTf)2, PhI=N-R2/CuPF6, PhI(OAc)2/R2-NH2/MgO/Rh2(OAc)4 или оксазиридины (например, сложный трет-бутиловый эфир 3-(4-цианофенил)-оксазиридин-2-карбоновой кислоты).
Особый интерес представляют не предусматривающие использования металлов способы иминирования сульфидов формулы II и/или сульфоксидов формулы III для получения сульфилиминов формулы Ia (стадия А) и/или сульфоксиминов формулы I (стадия А). Такие реакции иминирования предусматривают R2-NH2 и окислитель, например, PhI(OAc)2/R2-NH2, как описано в G.Y. Cho, С. Bolm, Tempahedron Lett., 2005, 46, 8007-8008; или N-бромсукцинимид (NBS)/R2-NH2 и основание, такое как трет-бутоксид натрия или калия, как описано в С. Bolm et al., Synthesis, 2010, №17, 2922-2925. Окислители, такие как N-иодсукцинимид (NIS) или иод, могут также применяться в качестве альтернативы, как описано, например, в O.G. Mancheno, С. Bolm, Org. Lett. 2007, 9, 3809-3811. Пример применения в качестве окислителя гипохлоритных солей, как например гипохлорит натрия NaOCl или гипохлорит кальция Са(ОС1)2, был описан в WO 2008/106006.
Для преобразования сульфилимина Ia в сульфоксимин I (стадия В) классические окислительные реагенты могут предусматривать, например, KMnO4, NaMnO4, mCPBA, NaIO4/RuO2, NaIO4/RuCl3, H2O2, оксон. В частности, применение солей рутения в комбинации с периодатами щелочных металлов и в качестве альтернативы применение перманганатов щелочных металлов было описано в WO 2008/097235 и WO 2008/106006.
Подробные условия получения, применимые для синтеза таких соединений сульфилиминовых и/или сульфоксиминовых соединений формулы Ia и I соответственно, также приводятся, например, в WO 2006/061200 или WO 2007/080131.
В качестве альтернативы подгруппа сульфоксиминовых соединений формулы I, где R2 представляет собой водород, а n равняется 1, и в которой R1, R3, А и Q определены в формуле I,
Схема la
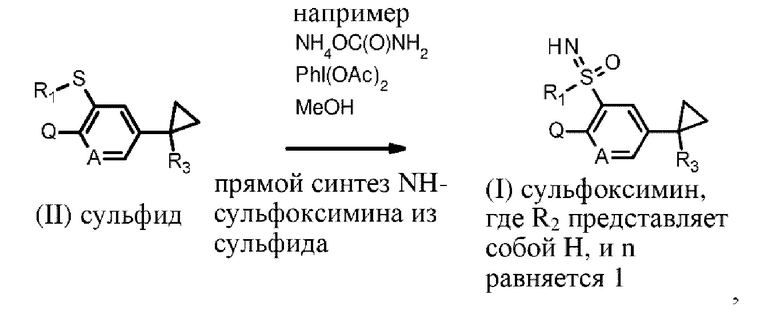
может быть получена (схема 1а) с помощью проведения реакции сульфидных соединений II, где R1, R3, А и Q определены в формуле I, с подходящим источником азота, таким как, например, аммиак, карбамат аммония или ацетат аммония (предпочтительно карбамат аммония), в присутствии реагентов на основе гипервалентного иода, как, например диацетоксииодбензол, в растворителе, как, например толуол, ацетонитрил или метанол, при температурах от 0 до 100°С, предпочтительно около комнатной температуры, аналогично описаниям, приведенным, например, в Chem. Commun. 53, 348-351; 2017 (и ссылкам, цитируемых в нем).
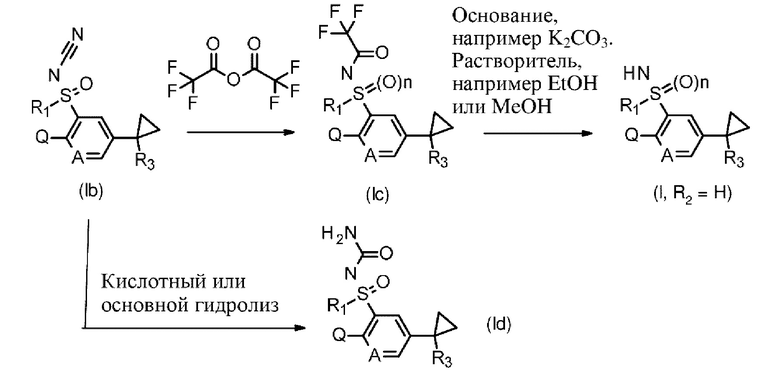
Соединение формулы Ib, где R1, R3, А и Q определены выше, и где n равняется 1, a R2 представляет собой CN, может быть трансформировано в соединение формулы Ic, где R1, R3, А и Q определены выше, определены выше, и где n равняется 1, a R2 представляет собой С(О)CF3, с помощью обработки трифторуксусным ангидридом в растворителе, таком как дихлорметан, как описано, например, в O.G. Mancheno, С. Bolm, Org. Lett. 2007, 9, 3809-3811. Соединение формулы Ic, где R1, R3, А, и Q определены выше, и где n равняется 1, a R2 представляет собой С(О)CF3, может быть трансформировано в соединение формулы I, где R1, R3, А, и Q определены выше, и где n равняется 1, a R2 представляет собой водород, с помощью обработки основанием, таким как карбонат натрия или калия, в полярном протонном растворителе, таком как метанол или этанол, как описано, например, в Н. Okamura, С. Bolm, Org. Lett. 2004, 6, 1305-1307. Соединение формулы Id, где R1, R3, А и Q определены выше, определены выше, и где n равняется 1, a R2 представляет собой C(О)NH2, может быть получено из соединения формулы Ib, где R1, R3, А и Q определены выше, и где n равняется 1, и в котором R2 представляет собой CN, с помощью обработки сильной кислотой, такой как концентрированная серная кислота, в органическом растворителе, таком как ацетонитрил, как описано, например, в WO 09/111309. Химические реакции подытожены на схеме 2.
Схема 2
Соединение формулы Ie, где R1, R3, А и Q определены выше, и где n равняется 1, a R2 представляет собой C1-С6алкил, может быть получено из соединения формулы I, где R1, R3, А и Q определены выше, и где n равняется 1, и в котором R2 представляет собой водород, с помощью обработки алкилирующим средством формулы LG-R2, где LG представляет собой уходящую группу, такую как галоген (особенно бром или иод), сульфонат OSO2R12 (особенно мезилат или тозилат), где R12 представляет собой C1-С6алкил, C1-С6галогеналкил или фенил, необязательно замещенные нитро или C1-С3алкилом, или сульфат (такой как диметилсульфат), предпочтительно в присутствии подходящего основания, как например карбонаты щелочных металлов, например, карбонат натрия или карбонат калия, или гидридов щелочных металлов, как например гидрид натрия, или гидроксидов щелочных металлов, как например гидроксид натрия и гидроксид калия, в инертном растворителе при температурах от -20 до 150°С, предпочтительно от 0 до 80°С. Примеры растворителей, подлежащих применению, включают эфиры, такие как тетрагидрофуран, диметиловый эфир этиленгликоля (1,2-диметоксиэтан), трет-бутилметиловый эфир и 1,4-диоксан, ароматические углеводороды, как например толуол и ксилол, нитрилы, как например ацетонитрил, или полярные апротонные растворители, как например N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон или диметилсульфоксид.
Соединение формулы If, где R1, R3, А и Q определены выше, и где n равняется 1, и R2 представляет собой C(О)R7, и R7 представляет собой C1-С6алкил или C1-С6галогеналкил, может быть получено из соединения формулы I, где R1, R3, А и Q определены выше, и где n равняется 1, a R2 представляет собой водород, с помощью обработки реагентом формулы LG1-C(О)R7 или ангидридом реагента формулы R7C(О)-О-C(О)R7, где R7 определен выше, a LG1 представляет собой уходящую группу, как например галоген (особенно хлор), необязательно в присутствии ацилирующего катализатора, как например 4-диметиламинопиридин (DMAP), предпочтительно в присутствии основания, как например триэтиламин, диизопропилэтиламин или пиридин, в инертном растворителе при температурах от 0 до 50°С. Примеры растворителей, подлежащих применению, включают эфиры, как например тетрагидрофуран, диметиловый эфир этиленгликоля, трет-бутилметиловый эфир и 1,4-диоксан, ароматические углеводороды, как например толуол и ксилол, галогенированные углеводороды, как например дихлорметан и хлороформ, нитрилы, как например ацетонитрил, или полярные апротонные растворители, как например N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон или диметилсульфоксид. Реакцию можно проводить в присутствии избытка основания, которое затем может также выступать в качестве растворителя или разбавителя.
Соединение формулы Ig, где R1, R3, А и Q определены выше, и где n равняется 1, и в котором R2 представляет собой C(О)OR8, a R8 представляет собой C1-С6алкил, C1-С6галогеналкил, может быть получено из соединения формулы I, где R1, R3, А и Q определены выше, и где n равняется 1, a R2 представляет собой водород, с помощью обработки реагентом формулы LG2-C(О)OR8, где R8 определен выше, и LG2 представляет собой уходящую группу, как например галоген (особенно хлор), необязательно в присутствии ацилирующего катализатора, как например 4-диметиламинопиридин (DMAP), предпочтительно в присутствии основания, как например триэтиламин, диизопропилэтиламин или пиридин, в инертном растворителе при температурах от 0 до 50°С. Примеры растворителей, подлежащих применению, включают эфиры, как например тетрагидрофуран, диметиловый эфир этиленгликоля, трет-бутилметиловый эфир и 1,4-диоксан, ароматические углеводороды, как например толуол и ксилол, галогенированные углеводороды, как например дихлорметан и хлороформ, нитрилы, как например ацетонитрил, или полярные апротонные растворители, как например N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон или диметилсульфоксид. Реакцию можно проводить в присутствии избытка основания, которое затем может также выступать в качестве растворителя или разбавителя.
Соединение формулы Ih, где R1,R3, А и Q определены выше, и где n равняется 1, и в котором R2 представляет собой CONR9R10, a R9, R10 независимо друг от друга представляют собой водород или C1-С6алкил, может быть получено из соединения формулы I, где R1, R3, А и Q определены выше, и где n равняется 1, и в котором R2 представляет собой водород, с помощью обработки реагентом формулы LG3-C(О)NR9R10, где R9 и R10 определены выше, и LG3 представляет собой уходящую группу, как например галоген (особенно хлор), необязательно в присутствии ацилирующего катализатора, как, например 4-диметиламинопиридин (DMAP), предпочтительно в присутствии основания, как например триэтиламин, диизопропилэтиламин или пиридин, в инертном растворителе при температурах от 0 до 50°С. Примеры растворителей, подлежащих применению, включают эфиры, как например тетрагидрофуран, диметиловый эфир этиленгликоля, трет-бутилметиловый эфир и 1,4-диоксан, ароматические углеводороды, как например толуол и ксилол, галогенированные углеводороды, как например дихлорметан и хлороформ, нитрилы, как например ацетонитрил, или полярные апротонные растворители, как например N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон или диметилсульфоксид. Реакцию можно проводить в присутствии избытка основания, которое затем может также выступать в качестве растворителя или разбавителя.
Соединение формулы Ii, где R1, R3, А и Q определены выше, и где n равняется 1, и в котором R2 представляет собой SO2R11, a R11 представляет собой C1-С6алкил, может быть получено из соединения формулы I, где R1, R3, А и Q определены выше, и где n равняется 1, и в котором R2 представляет собой водород, с помощью обработки реагентом формулы LG4- SO2R11, где R11 определен выше, и LG4 представляет собой уходящую группу, как например галоген (особенно хлор), необязательно в присутствии ацилирующего катализатора, как например 4-диметиламинопиридин (DMAP), предпочтительно в присутствии основания, как например триэтиламин, диизопропилэтиламин или пиридин, в инертном растворителе при температурах от 0 до 50°С. Примеры растворителей, подлежащих применению, включают эфиры, как, например тетрагидрофуран, диметиловый эфир этиленгликоля, трет-бутилметиловый эфир и 1,4-диоксан, ароматические углеводороды, как, например толуол и ксилол, галогенированные углеводороды, как например дихлорметан и хлороформ, нитрилы, как например ацетонитрил, или полярные апротонные растворители, как например N,N-диметилформамид, N,N-диметилацетамид, N-метил-2-пирролидон или диметилсульфоксид. Реакцию можно проводить в присутствии избытка основания, которое затем также выступает в качестве растворителя или разбавителя. Соединение формулы Ij, где R1, R2, R3 и Q определены выше, и где n равняется 1, и в котором R2 представляет собой C(О)R7, a R7 представляет собой водород, может быть получено из соединения формулы I, где R1, R3, А и Q определены выше, и где n равняется 1, a R2 представляет собой водород, с помощью обработки триалкилортоформиатом, как, например триметилортоформиат, необязательно в присутствии кислотного активатора, как например пара-толуолсульфоновая кислота, необязательно в присутствии инертного органического растворителя и при температурах от 0 до 180°С. Реакцию можно проводить в присутствии избытка триалкилортоформиата, который затем может также выступать в качестве растворителя или разбавителя. Такой способ проиллюстрирован, например, в WO 2006/037945. Преобразования, описанные выше, проиллюстрированы на схеме 3.
Схема 3
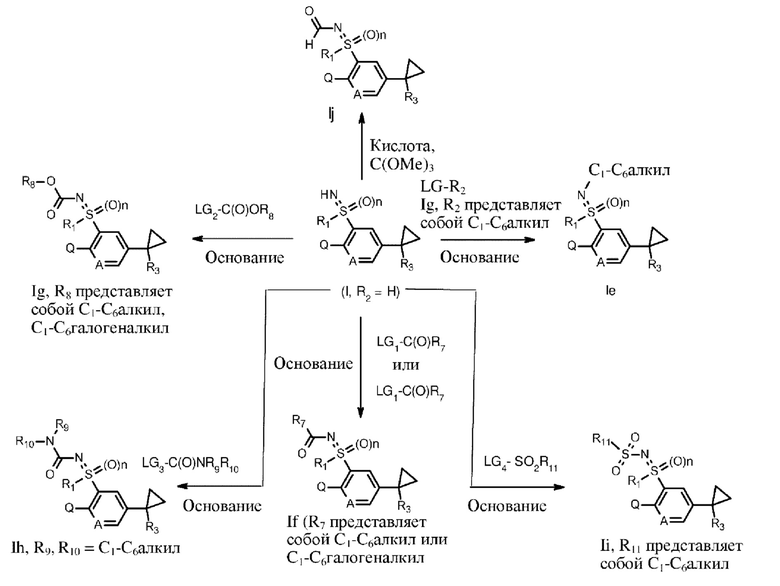
В некоторых случаях соединения формулы II, где R3 представляет собой водород, являются известными, например,
2-(5-циклопропил-3-этилсульфанил-2-пиридил)-5-(трифторметокси)-1,3-бензоксазол, CAS [2128705-99-5], WO 2017146226; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-5-(дифторметилсульфанил)-1,3-бензоксазол, CAS [2128706-06-7], WO 2017146226; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-5-(дифторметокси)-1,3-бензоксазол, CAS [2128706-01-2], WO 2017146226; 5-циклопропил-2-(5-циклопропил-3-этилсульфанил-2-пиридил)-3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-4-он, CAS [2098699-63-7], WO 2017089190; 5-циклопропил-2-(4-циклопропил-2-этилсульфанилфенил)-3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-4-он, CAS [2098699-80-8], WO 2017089190; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-5-(1,1,2,2,2-пентафторэтил)-1,3-бензоксазол, CAS [1975147-97-7], WO 2016121997; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-5-(трифторметилсульфанил)-1,3-бензоксазол, CAS [1975147-94-4], WO 2017146226; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-1-метил-5-(трифторметил)бензимидазол, CAS [1975147-91-1], WO 2016121997; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-6-(трифторметил)оксазоло[5,4-Ь]пиридин, CAS [1975147-87-5], WO 2016121997; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-3-метил-6-(1,1,2,2,2-пентафторэтил)имидазо[4,5-b]пиридин, CAS [1975147-85-3], WO 2016121997; 6-(5-циклопропил-3-этилсульфанил-2-пиридил)-7-метил-3-(2,2,2-трифторэтокси)имидазо[4,5-с]пиридазин, CAS [1957168-99-8], WO 2016104746; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-3-метил-6-(трифторметил)имидазо[4,5-Ь]пиридин, CAS [1951416-89-9], WO 2016096584; 2-(4-циклопропил-2-этилсульфанилфенил)-7-(трифторметил)имидазо[1,2-с]пиримидин, CAS [1923785-41-4], WO 2016071214; 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-7-(трифторметил)имидазо[1,2-с]пиримидин, CAS [1923784-36-4], WO 2016071214; 2-(4-циклопропил-2-этилсульфанилфенил)-5-этил-3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-4-он, CAS [1879051-89-4], WO 2016023954; 2-(4-циклопропил-2-этилсульфанилфенил)-3,5-диметил-6-(трифторметил)имидазо[4,5-с]пиридин-4-он, CAS [1879051-88-3], WO 2016023954.
Соединения формулы II, где R3 представляет собой Н, т.е. соединения формулы IIa,
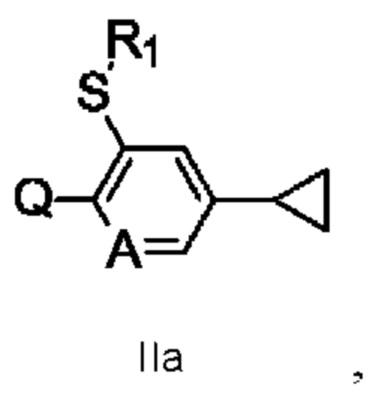
в целом, могут быть получены путем проведения реакции соединения формулы IV, где A, Q и R1 определены в формуле I выше, с соединением формулы V, как показано на схеме 4.
Схема 4
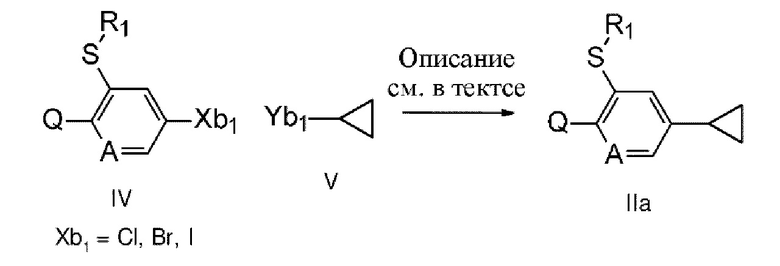
Более конкретно, соединения формулы Па можно получать (как показано на схеме 4) посредством проведения реакции соединений формулы Па с соединениями формулы V, где Хы может представлять собой галоген, предпочтительно хлор, бром или иод, и Vb1 может представлять собой функциональную группу на основе бора, как например В(ОН)2 или B(ORb1)2, где Rb1 может представлять собой C1-С6алкильную группу, или две группы ORb1 могут образовывать вместе с атомом бора пяти- или шестичленное кольцо, как например сложный пинаколовый эфир бороновой кислоты (реакция перекрестного сочетания Сузуки, см., например, Tetrahedron Letters, 43(39), 6987-6990; 2002). В формуле IIa A, R1 и Q являются такими, как описано для формулы I. Реакция может быть катализирована с помощью катализатора на основе палладия, например, тетракис(трифенилфосфин)палладия(О), дихлорида бис(трифенилфосфин)палладия(II), хлор(2-дициклогексилфосфино-2',4',6'-триизопропил-1,1'-бифенил)[2-(2'-амино-1,1'-бифенил)]палладия(II) (палладацикла XPhos), (1,1'-бис(дифенилфосфино)ферроцен)дихлорпалладийдихлорметана (комплекс 1:1) или ацетата палладия плюс фосфиновые лиганды (такие как, например, трифенилфосфин или трициклогексилфосфин) в присутствии основания, как, например карбонат натрия, трикалийфосфат или фторид цезия, в растворителе (таком как толуол, 1,2-диметоксиэтан DME, тетрагидрофуран или диоксан) или смеси растворителей, как например смесь 1,2-диметоксиэтана (или диоксана, толуола или тетрагидрофурана) и воды, предпочтительно в инертной атмосфере. Температура реакции предпочтительно может находиться в диапазоне от температуры окружающей среды до температуры кипения реакционной смеси, или в качестве альтернативы можно также осуществлять нагревание под воздействием микроволнового излучения.
В качестве альтернативы соединения формулы IV, где Xb1 может представлять собой галоген, предпочтительно хлор, бром или иод, могут вступать в реакцию с соединениями формулы V, где Yb1 представляет собой группу в виде галогенида магния, такую как -MgBr (реакция перекрестного сочетания по Кумада), необязательно в присутствии добавок, таких как галогениды цинка (Journal of Organic Chemistry, 75(19), 6677-6680; 2010). Реакция может быть катализирована с помощью катализатора на основе палладия, или может предусматривать катализатор на основе никеля, такой как дихлорид 1,3-бис(дифенилфосфино)пропанникеля (dppp)NiCl2. Также известны реакции между соединениями формулы IV и соединениями формулы V, где Yb1 представляет собой группу в виде галогенида цинка, такую как ZnBr (реакция перекрестного сочетания по Негиши), как проиллюстрировано, например, в Synthetic Communications, 28(2), 225-232; 1998. Реакция может быть катализирована с помощью катализатора на основе палладия, такого как, например, (1,1'-бис(дифенилфосфино)ферроцен)дихлорпалладий Pd(dppf)Cl2 или дихлорид бис(трифенилфосфин)палладия(II), необязательно в присутствии фосфиновых добавок (таких как, например, 2-дициклогексилфосфино-2',6'-диметоксибифенил S-PHOS), в растворителе, как например 1,2-диметоксиэтан, диоксан, толуол или тетрагидрофуран, предпочтительно в инертной атмосфере. Температура реакции предпочтительно может находиться в диапазоне от температуры окружающей среды до температуры кипения реакционной смеси.
В некоторых случаях соединения формулы II, где R3 представляет собой циано, являются известными, например, 1-[5-этилсульфанил-6-[5-метокси-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]-3-пиридил]циклопропанкарбонитрил, CAS [2225113-68-6], WO 2018/077565; 1-[3-этилсульфанил-4-[5-метокси-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрил, CAS [CAS [2225113-73-3], WO 2018/077565; 1-[4-[5-циклопропил-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]-3-этилсульфанилфенил]циклопропанкарбонитрил, С AS [2098699-74-0], WO 2017/089190; 1-[6-[5-циклопропил-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]-5-этилсульфанил-3-пиридил]циклопропанкарбонитрил, CAS [2098699-59-1], WO 2017/089190; 1-[5-этилсульфанил-6-[5-(трифторметилсульфанил)-1,3-бензоксазол-2-ил]-3-пиридил]циклопропанкарбонитрил, CAS [1975148-53-8], WO 2016/121997; 1-[3-этилсульфанил-4-[7-(трифторметил)имидазо[1,2-с]пиримидин-2-ил]фенил]циклопропанкарбонитрил, CAS [1923785-47-0], WO 2016/071214; 1-[5-этилсульфанил-6-[7-(трифторметил)имидазо[1,2-с]пиримидин-2-ил]-3-пиридил]циклопропанкарбонитрил, CAS [1923784-42-2], WO 2016/071214.
Другие соединения формулы II, где R3 представляет собой циано, a R1, А и Q определены в формуле I, т.е. соединения формулы IIb,
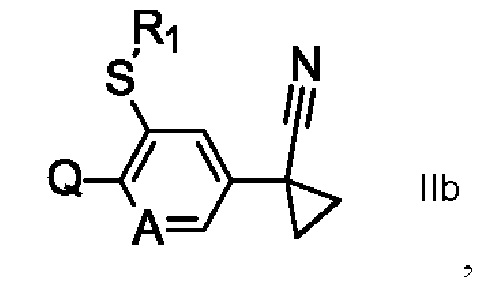
могут быть получены, как показано на схеме 5.
Схема 5
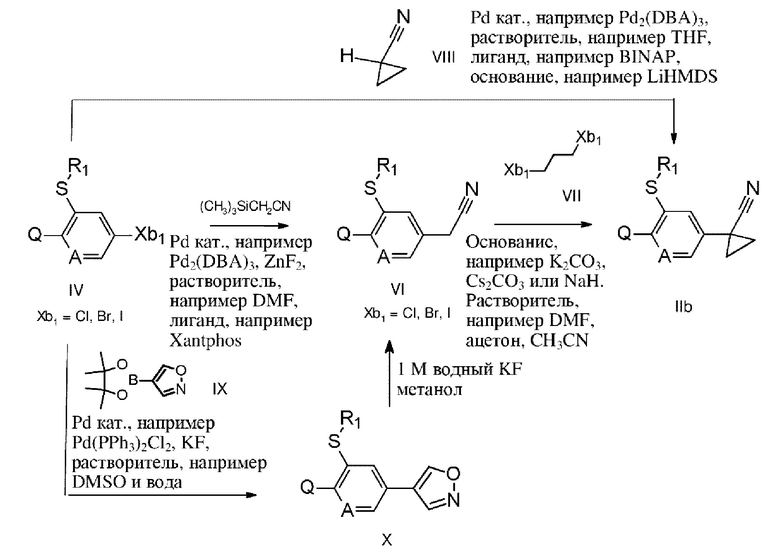
Как показано на схеме 5, обработка соединений формулы IV, где R1, Q и А описаны в формуле I, и где Xb1 предпочтительно представляет собой галоген (еще более предпочтительно хлор, бром или иод), с помощью триметилсилилацетонитрила TMSCN, в присутствии фторида цинка(II) и катализатора на основе палладия(О), такого как аддукт хлороформа и трис(дибензилиденацетон)дипалладия(О) (Pd2(dba)3), лиганда, например, Xantphos, в инертном растворителе, таком как DMF, при температурах в диапазоне 100-160°С, необязательно при микроволновом нагревании, приводит к получению соединений формулы VI. Такие химические реакции были описаны в литературе, например в Org. Lett., 16(24), 6314-6317; 2014. Соединения формулы IV могут быть обработаны соединениями формулы VII, где Xb1 описан выше, в присутствии основания, такого как гидрид натрия, K2CO3 или Cs2CO3, в инертном растворителе, таком как DMF, ацетон, или ацетонитрил, с получением соединений формулы IIb. В качестве альтернативы соединения формулы IIb могут быть получены непосредственно из соединений формулы IV с помощью обработки соединений формулы VIII Pd2(dba)3, лигандом, таким как BINAP, сильным основанием, таким как LiHMDS, в инертном растворителе, таком как THF, при температурах в диапазоне 40-70°С. Такие химические реакции были описаны в, например, J. Am. Chem. Soc, 127(45), 15824-15832; 2005.
Другие процедуры применительно к соединениям формулы IIb предусматривают проведение реакции соединений формулы IV, где A, R1 и Q описаны для формулы I, и в которых Xb1 представляет собой галоген, предпочтительно хлор, бром, иод, с 4-изоксазолбороновой кислотой или сложным пинаколовым эфиром 4-изопропенилбороновой кислоты (соединение формулы IX) в присутствии фторида калия KF и катализатора на основе палладия, такого как дихлорид бис(трифенилфосфин)палладия(II) Pd(PPh3)2Cl2, в инертном растворителе, таком как диметилсульфоксид DMSO, необязательно в смеси с водой, при температурах в диапазоне 40-150°С, необязательно при микроволновом нагревании, что приводит к получению соединений формулы IX, где Q, R1 и А описаны для формулы I выше. Проведение реакции соединений формулы IX с водным раствором фторида калия KF (в концентрации от 0,5 до 3 М, предпочтительно 1 М) в инертном растворителе, таком как диметилсульф оксид DMSO или метанол, при температурах в диапазоне 20-150°С, необязательно при микроволновом нагревании приводит к получению соединений формулы VI, где A, R1 и Q описаны для формулы I выше. Превращение соединений формулы V в соединения формулы lib осуществляется описанным выше образом. Такие химические реакции были описаны в литературе, например в J Am Chem Soc 2011,133, 6948-6951.
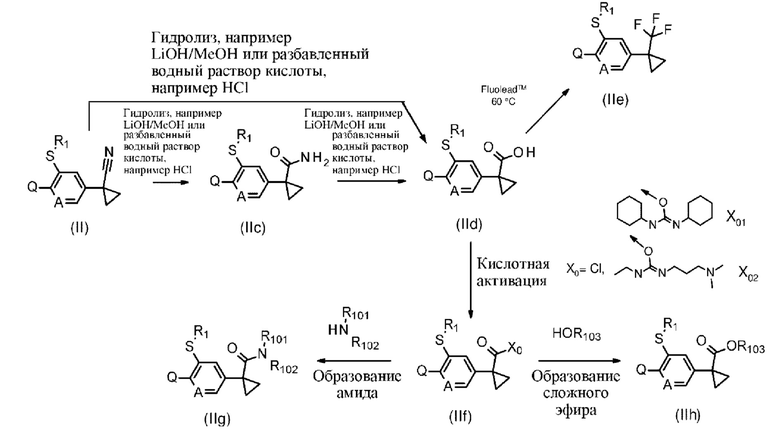
Соединения формулы lib можно дополнительно использовать для получения соединений формулы II (схема 6), где R3 дополнительно функционализирован. Действительно, соединения формулы IIb, где A, R1, X1 и R2 определены в формуле I выше, могут быть подвергнуты частичному гидролизу при кислотных или основных условиях, известных специалистам в данной области техники, с получением соединений формулы IIc или полному гидролизу с получением соединений формулы IId. Обработка соединений формулы IIc реагентами, такими как SF4 или Fluolead (трифторид 4-трет-бутил-2,6-диметилфенилсеры), необязательно в присутствии HF, приводит к получению соединений формулы Не (как описано в, например, Organic Letters, 16, 6314-6317; 2014).
Активация соединений формулы (IId), где R1, Q и А определены в формуле I, с помощью способов, известных специалистам в данной области техники и описанных в, например, Tempahedron, 2005, 61 (46), 10827-10852, приводит к образованию активированных форм соединений (IIf), где Q, R1 и А определены в формуле I, и где Хо представляет собой галоген, предпочтительно хлор. Например, соединения (IIf), где Хо представляет собой галоген, предпочтительно хлор, образуются с помощью обработки (IId), например, оксалилхлоридом (COCl)2 или тионилхлоридом SOCl2 в присутствии каталитических количеств N,N-диметилформамида DMF в инертном растворителе, таком как метиленхлорид CH2Cl2 или тетрагидрофуран THF, при температурах от 20 до 100°С, предпочтительно 25°С. В качестве альтернативы обработка соединений формулы (IId), например, 1-этил-3-(3-диметиламинопропил)карбодиимидом EDC или дициклогексилкарбодиимидом DCC будет приводить к образованию активированных форм соединений (XII), где Х0 представляет собой X01 или Х02 соответственно, осуществляемая при этом в инертном растворителе, таком как пиридин или тетрагидрофуран THF, необязательно в присутствии основания, такого как триэтиламин, при температурах в диапазоне 50-180°С; причем такие активированные промежуточные соединения формулы Iif можно вводить в реакцию с нуклеофилами, такими как амины формулы HNR101R012, где R101 и R102 представляют собой водород или C1-С6алкил, или HOR103, где R103 представляет собой C1-С6алкил, необязательно в присутствии основания, такого как триэтиламин, пиридин или DMAP, в инертном растворителе, таком как CH2Cl2, THF или ацетонитрил, с получением соединений формулы IIg и IIb, соответственно. Такие реакции хорошо известны специалистам в данной области техники. Последующее преобразование цианоциклопропилов проиллюстрировано на схеме 6.
Схема 6
Соединения формулы II, где Q представляет собой Q1, определяющие соединения формулы II-Q1,
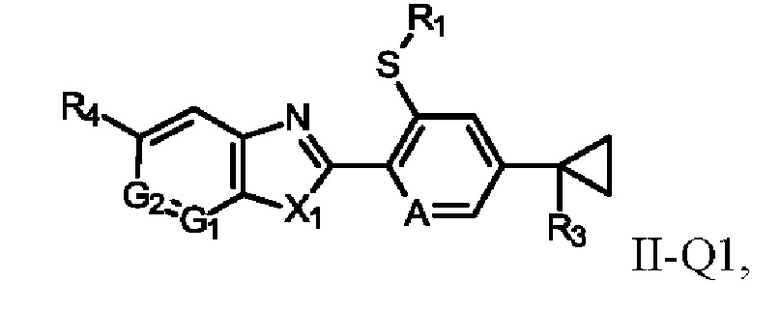
где R1, R3, R4, X1, G1 и G2 определены в формуле I, могут быть получены как показано на схеме 7.
Схема 7
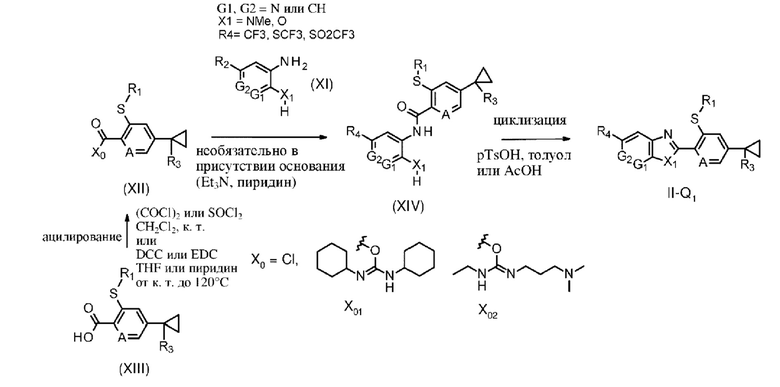
Как показано на схеме 7, соединения формулы II-Q1 могут быть получены с помощью циклизации соединений формулы (XIV), где R1, R3, R4, A, X1, G1 и G2 определены в формуле I, например, посредством нагревания в уксусной кислоте или трифторуксусной кислоте (предпочтительно если X1 представляет собой NR5, где R5 представляет собой С1-С4алкил) при температурах от 0 до 180°С, предпочтительно от 20 до 150°С, необязательно под воздействием микроволнового излучения. Циклизация соединений формулы (XIV) может также достигаться в присутствии кислотного катализатора, например метансульфоновой кислоты или пара-толуолсульфоновой кислоты p-TsOH, в инертном растворителе, таком как N-метилпирролидон, толуол или ксилол, при температурах в диапазоне 25-180°С, предпочтительно 100-170°С. Такие способы были описаны ранее, например, в WO 2016096584. В качестве альтернативы, соединения формулы (XIV) можно превращать в соединения формулы II-Q1 (предпочтительно если X1 представляет собой О) с применением трифенилфосфина, диизопропилазодикарбоксилата (или диэтилазодикарбоксилата) в инертном растворителе, таком как тетрагидрофуран THF, при температурах в диапазоне 20-50°С. Такие условия реакции Мицунобу были описаны ранее для данных преобразований (см. WO 2009/131237 и WO 2016/121997).
Соединения формулы (XIV), где R1, R3, R4, А, Х1, G1 и G2 определены в формуле I, могут быть получены посредством ацилирования с помощью
i) активации соединений формулы (XIII), где R1, R3 и А определены в формуле I, с помощью способов, известных специалистам в данной области техники и описанных в, например, Tetrahedron, 2005, 61 (46), 10827-10852, с образованием активированных форм соединений (XII), где R1, R3 и А определены в формуле I, и где Хо представляет собой галоген, предпочтительно хлор. Например, образование соединений (XII), где Хо представляет собой галоген, предпочтительно хлор, осуществляют путем обработки (XIII) с помощью, например, оксалилхлорида (COCl)2 или тионилхлорида SOCl2 в присутствии каталитических количеств N,N-диметилформамида DMF в инертных растворителях, таких как метиленхлорид CH2Cl2 или тетрагидрофуран THF, при температурах в диапазоне 20-100°С, предпочтительно 25°С. В качестве альтернативы обработка соединений формулы (XIII), например, 1-этил-3-(3-диметиламинопропил)карбодиимидом EDC или дициклогексилкарбодиимидом DCC будет приводить к образованию активированных форм соединений (XII), где Хо представляет собой X01 или Х02 соответственно, осуществляемая при этом в инертном растворителе, таком как пиридин или тетрагидрофуран THF, необязательно в присутствии основания, такого как триэтиламин, при температурах в диапазоне 50-180°С; с последующей
ii) обработкой активированных форм соединений (XII) соединениями формулы (XI), где X1, G1, G2 и R4 определены в формуле I, в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин или пиридин, в инертных растворителях, таких как дихлорметан, тетрагидрофуран, диоксан, N,N-диметилформамид, N,N-диметилацетамид, ацетонитрил, этилацетат или толуол, при температурах от 0 до 50°С с образованием соединений формулы (XIV). Соединения формулы XIII, где R3 представляет собой Н, т.е. соединение, где R1 представляет собой этил, R3 представляет собой Н, и А представляет собой N или СН, известны и описаны в WO 2017146226 или WO 2016121997 (для 5-циклопропил-3-этилсульфанилпиридин-2-карбоновой кислоты, С AS [1975148-58-3]), и WO 2016023954 (для 4-циклопропил-2-этилсульфанилбензойной кислоты, CAS [1879052-58-0]). Соединение формулы XIII, где R3 представляет собой циано, R1 представляет собой этил, и А представляет собой СН (4-(1-цианоциклопропил)-2-этилсульфанилбензойную кислоту, CAS [2225113-79-9]), и соединение формулы XIII, где R3 представляет собой циано, R1 представляет собой этил, и А представляет собой N (5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбоновую кислоту, CAS [2225113-77-7]), известны и описаны в WO 2018/077565.
Соединения формулы (XI), где X1, G1, G2 и R2 определены в формуле I, были ранее описаны, например, в WO 2012/086848, WO 2015/000715 и WO 2016/116338.
Соединения формулы II, где Q представляет собой Q2, определяющие соединения формулы II-Q2,
где R1, R3, R4, А и G2 определены в формуле I,
Схема 8
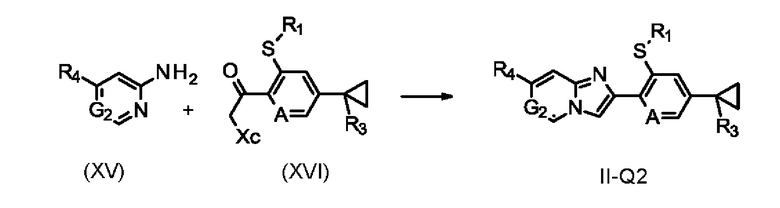
могут быть получены (схема 8) путем проведения реакции конденсации соединений формулы (XVI), где R1, R3, А определены в формуле I, и в которых Хс представляет собой уходящую группу, такую как, например, хлор, бром или иод (предпочтительно хлор или бром), с соединениями формулы (XVI), где G2 и R2 определены в формуле I, в инертном растворителе, например, этаноле или ацетонитриле, необязательно в присутствии подходящего основания, такого как карбонат натрия, калия или цезия или оксид магния, при температурах от 80 до 150°С, необязательно в условиях микроволнового нагревания. Такие способы были описаны ранее, например, в WO 2012/49280 или WO 2003/031587. Соединения формулы (XV), где G2 и R2 определены в формуле I, являются либо известными коммерчески доступными соединениями, либо могут быть получены с помощью известных способов, хорошо известных специалистам в данной области техники.
Соединения формулы (XVI), где R1, R3 и А определены в формуле I, и в которых Хс представляет собой уходящую группу, такую как, например, хлор, бром или иод (предпочтительно хлор или бром),
Схема 9
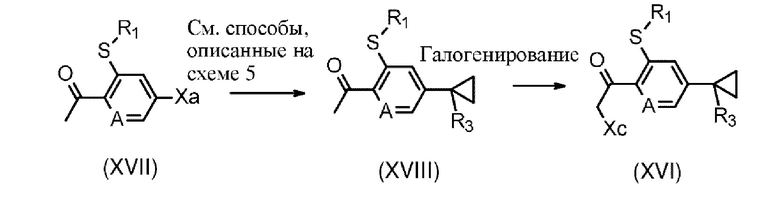
могут быть получены (схема 9) с помощью обработки соединений формулы (XVIII), где R1, R3 и А определены в формуле I, галогенирующим средством (источник "Хс+"), например N-бромсукцинимидом, N-иодсукцинимидом, N-хлорсукцинимидом, I2, CuBr2, Br2 в уксусной кислоте, PhNMe3+Br3-, обычно в растворителе, таком как метанол, ацетонитрил, тетрагидрофуран, этилацетат, хлороформ или дихлорметан или их смесях, при температурах от 0°С до 150°С, предпочтительно от комнатной температуры и до 120°С, необязательно в условиях микроволнового нагревания. Такие способы были описаны ранее, например, в WO 2016/071214.
Соединения формулы (XVIII), где R1, R3 и А определены в формуле I, могут быть получены с помощью проведения реакции с участием соединений формулы (XVII), где R1 и А определены в формуле I, и в которой Ха представляет собой уходящую группу, такую как, например, хлор, бром или иод (предпочтительно хлор или бром), при условиях уже описанных выше (см. схему 5, преобразование соединений IV в IIb).
Соединения формулы (XVII), где R1 и А определены в формуле I, и где Ха представляет собой уходящую группу, такую как, например, хлор, бром или иод, в частности те соединения, где Ха представляет собой галоген (еще более предпочтительно хлор, бром или иод; причем особенно предпочтительными являются хлор или бром), являются либо известными коммерчески доступными соединениями, либо могут быть получены с помощью известных способов, описанных в литературе, как например в WO 2016/071214.
В качестве альтернативы соединения формулы II, где Q представляет собой Q5, определяющие соединения формулы II-Q5, где R1, R3, R4, Re и А определены в формуле
Схема 9а:
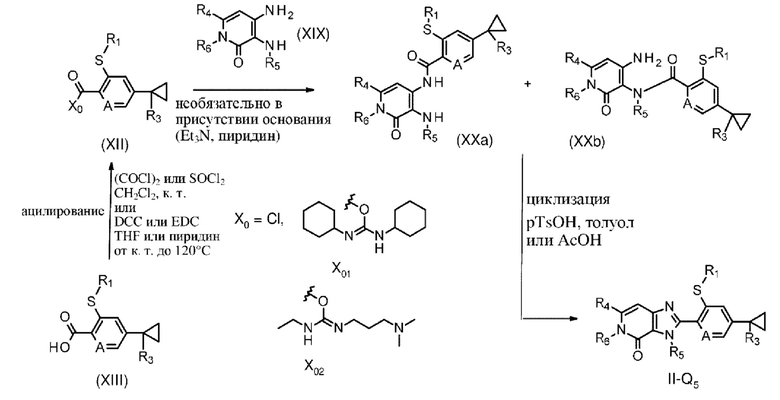
могут быть получены (схема 9а) с помощью циклизации соединений формулы (ХХа), где R1, R3, R4, R5, R6 и А определены в формуле I, или региоизомеров формулы (XXb) с идентичными определениями заместителей, или их смеси в любом соотношении, при условиях, уже описанных выше (см. схему 7, преобразование соединений (XIV) в II-Q1).
Соединения формулы (ХХа), где R1, R3, R4, R5, R6 и А определены в формуле I, или региоизомеры формулы (XXb) с идентичными определениями заместителей, или их смесь в любом соотношении могут быть получены с помощью обработки активированных форм соединений (XII), описанных выше, соединениями формулы (XIX), где R4, R5 и R6 определены в формуле I, при условиях, уже описанных выше (см. схему 7, преобразование соединений (XII) и (XIII) в соединения (XIV)).
Соединения формулы (XIX), где R4, R5 и R6 определены в формуле I, были ранее описаны, например, в WO 2016/023954, WO 2016/142326, WO 2017/133994 и WO 2018077565.
В качестве альтернативы соединения формулы II, где Q представляет собой Q3, определяющие соединения формулы II-Q3, где R1, R4, R3 и А определены в формуле I,
Схема 10
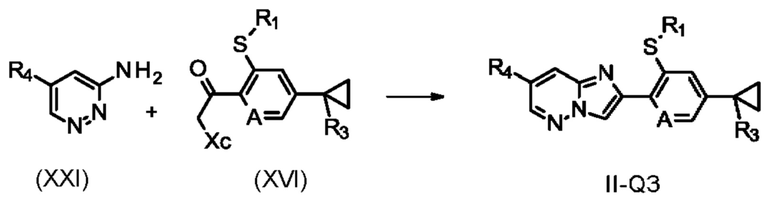
могут быть получены (схема 10) путем проведения реакции конденсации соединений формулы (XVI), описанных выше, где R1, R3 и А определены в формуле I, и в которых Хс представляет собой уходящую группу, такую как, например, хлор, бром или иод (предпочтительно хлор или бром), с соединениями формулы (XXI), где R4 определен в формуле I, в инертном растворителе, например, этаноле, толуоле или ацетонитриле, необязательно в присутствии подходящего основания, такого как карбонат натрия, калия или цезия (гидрокарбонат либо натрия, либо калия) или оксида магния, при температурах от 80 до 150°С, необязательно в условиях микроволнового нагревания. Такие процедуры были описаны ранее, например, в WO 2011/074658. Соединения формулы (XXI), где R4 определен в формуле I, являются либо известными коммерчески доступными соединениями, либо могут быть получены с помощью известных способов, хорошо известных специалистам в данной области техники (см. например WO 2011/074658 и WO 2010/083145).
Соединения формулы II, где Q представляет собой Q4, определяющие соединения формулы II-Q4,
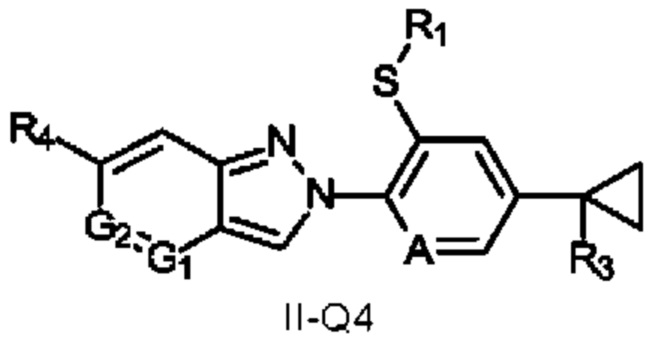
где R1, R3, R4, G1, G2 и А определены в формуле I,
Схема 11
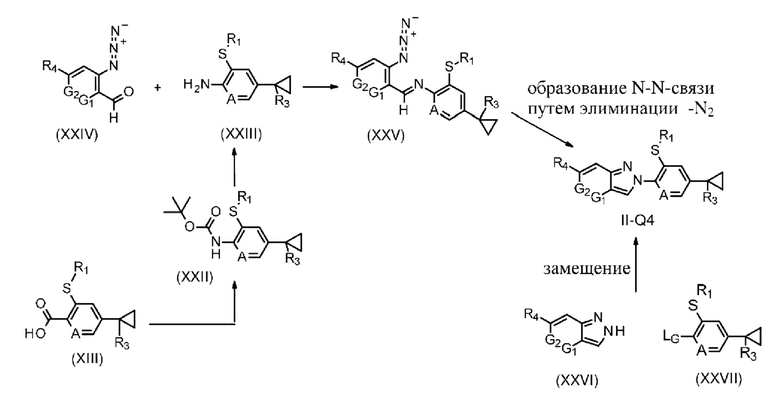
могут быть получены (схема 11) посредством реакции образования связи N-N с участием азидоиминов соединений формулы (XXV), где R1, R4, R7, R8, A, G1, G2 и R2 определены в формуле I, при пиролитических условиях, которые способствуют выделению N2. В качестве альтернативы данная реакция может проводиться в присутствии катализатора на основе металла, например катализатора на основе Cu(I), как, например CuI, CuBr, CuCl или CuCN или в более общем случае с переходными металлами, в комбинации с лигандом, как например тетраметилэтилендиамин, 2,2'-бипиридин или 1,10-фенантролин. Подходящие растворители могут включать применение толуола, хлорбензола или ксилола при температурах от комнатной температуры до 200°С, предпочтительно от 100 до 160°С, необязательно в условиях микроволнового нагревания. Такие условия восстановительной циклизации были описаны в, например, Organic Letters, 2011, Vol. 13, No. 13, 3542-3545 и US 2017/0260183.
Соединения формулы (XXV), где R1, R3, R4, G1, G2 и А определены в формуле I, могут быть получены с помощью проведения реакции между соединениями формулы (XXIII), где R1, R3 и А определены в формуле I, и соединениями формулы (XXIV), где G1, G2 и R4 определены в формуле I, обычно при нагревании при температурах от комнатной температуры до 200°С, предпочтительно от 40 до 160°С, необязательно в условиях микроволнового нагревания, в подходящих растворителях, которые могут включать, например, толуол или ксилол. Для образования соединений формулы (XXV) может быть необходимо удаление воды либо с помощью азеотропной перегонки, либо с помощью высушивающих средств, таких как, например, TiCl4 или молекулярные сита. Такое образование Шиффовых оснований формулы (XXV) известно специалистам в данной области техники и было описано в, например, WO 2017/134066. Соединения формулы XXIV приведены в литературе (см. CAS 2211908-96-0, описанное в WO 2018/052136).
Соединения формулы XXIII могут быть получены с помощью проведения реакции с участием соединения формулы XXII в присутствии кислоты, такой как HCl, H2SO4, Н3РО4, HNO3, TFA. Такая реакция снятия защитной группы N-связанного карбамата широко известна специалистам в данной области техники и описана, например, в RSC Advances, 5(5), 3200-3205; 2015
Соединения формулы XXII могут быть получены с помощью проведения реакции соединений формулы XIII и органического азида или производных аммиака, например, NH4OH, NH3, NH2BoC, в присутствии подходящего основания и в присутствии или отсутствии кислот Льюиса и растворителя, при температурах от 50°С до 200°С. Примеры органического азида включают TMSN3, азид натрия, дифенилфосфорилазид или тозилазид, и подходящим растворителем может быть t-BuOH, толуол, ксилол, THF или ацетонитрил. Пример подходящей кислоты Льюиса может включать Zn(OTf)2. Такие реакции превращения карбоновых кислот в амины широко известны специалистам в данной области техники под названием реакция Курция и описаны в Org. Lett, 2005, 7, 4107-4110; Journal of Medicinal Chemistry, 49(12), 3614-3627; 2006.
В качестве альтернативы соединения формулы II-Q4, где R1, R3, R4, G1, G2 и А определены в формуле I, могут быть получены с помощью проведения реакции соединений формулы (XXVI), где R4, G1, G2 определены в формуле I, и в которых LG представляет собой уходящую группу, такую как, например, хлор, бром или иод (предпочтительно хлор или бром), или арил-, алкил- или галогеналкилсульфонат, такой как трифторметансульфонат, с соединениями формулы (XXVII), где G1, G2 и R4 определены в формуле I, в присутствии основания, такого как, например, карбонат цезия, натрия, калия или лития или гидрид натрия, необязательно в присутствии катализатора на основе металла, такого как катализатор на основе иодида меди(1) или палладия, при наличии или отсутствии добавок, таких как L-пролин, N,N'-диметилэтилендиамин или лиганд на основе фосфора, в инертном растворителе, таком как ацетонитрил, N,N-диметилформамид, N-метил-2-пирролидон или диметилсульфоксид, при температурах от комнатной температуры до 200°С, необязательно в условиях микроволнового нагревания. Такие условия реакции ароматического нуклеофильного замещения были описаны в, например, WO 2017/134066. Соединения формулы XXVII могут быть получены с помощью реакции Зандмейера, т.е. диазотирования соединения XXIII с помощью NaNO2 или tBu-ONO в инертном растворителе, таком как t-BuOH или воде, с последующим добавлением неорганического галогенида, такого как CuBr2, CuCl или KI. Такие реакции Зандмейера широко известны в литературе (см., например, Synthesis, 2007, 2534-2538, Org. Lett, 2008, 10, 3961-3964, и ссылки, цитируемые в нем).
Реагенты можно вводить в реакцию в присутствии основания. Примерами подходящих оснований являются гидроксиды щелочных металлов или щелочноземельных металлов, гидриды щелочных металлов или щелочноземельных металлов, амиды щелочных металлов или щелочноземельных металлов, алкоксиды щелочных металлов или щелочноземельных металлов, ацетаты щелочных металлов или щелочноземельных металлов, карбонаты щелочных металлов или щелочноземельных металлов, диалкиламиды щелочных металлов или щелочноземельных металлов или алкилсилиламиды щелочных металлов или щелочноземельных металлов, алкиламины, алкилендиамины, свободные или N-алкилированные насыщенные или ненасыщенные циклоалкиламины, основные гетероциклы, гидроксиды аммония и карбоциклические амины. Примерами, которые можно упомянуть, являются гидроксид натрия, гидрид натрия, амид натрия, метоксид натрия, ацетат натрия, карбонат натрия, трет-бутоксид калия, гидроксид калия, карбонат калия, гидрид калия, диизопропиламид лития, бис(триметилсилил)амид калия, гидрид кальция, триэтиламин, диизопропилэтиламин, триэтилендиамин, циклогексиламин, N-циклогексил-N,N-диметиламин, N,N-диэтиланилин, пиридин, 4-(N,N-диметиламино)пиридин, хинуклидин, N-метилморфолин, бензилтриметиламмония гидроксид и 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU).
Реагенты можно вводить в реакцию друг с другом как есть, т.е. без добавления растворителя или разбавителя. Однако в большинстве случаев преимущественным является добавление инертного растворителя, или разбавителя, или их смеси. Если реакцию проводят в присутствии основания, то основания, которые применяют в избытке, такие как триэтиламин, пиридин, N-метилморфолин или N,N-диэтиланилин, могут также выступать в качестве растворителей или разбавителей.
Реакцию преимущественно проводят при температуре в диапазоне от примерно -80°С до примерно +140°С, предпочтительно от примерно -30°С до примерно +100°С, во многих случаях в диапазоне от температуры окружающей среды до примерно +80°С.
Соединение формулы I можно преобразовать известным per se способом в другое соединение формулы I путем замены одного или нескольких заместителей исходного соединения формулы I традиционным способом другим(-и) заместителем (заместителями) в соответствии с настоящим изобретением.
В зависимости от выбора условий реакции и исходных веществ, подходящих в каждом случае, можно, например, на одной стадии реакции заменить лишь один заместитель другим заместителем в соответствии с настоящим изобретением, или можно заменить несколько заместителей другими заместителями в соответствии с настоящим изобретением на одной и той же стадии реакции.
Соли соединений формулы I можно получать известным per se способом. Таким образом, например, соли присоединения кислоты соединений формулы I получают посредством обработки подходящей кислотой или подходящим ионообменным реагентом, а соли с основаниями получают посредством обработки подходящим основанием или подходящим ионообменным реагентом.
Соли соединений формулы I можно превращать традиционным способом в свободные соединения I, соли присоединения кислоты, например, посредством обработки подходящим основным соединением или подходящим ионообменным реагентом, а соли с основаниями, например, посредством обработки подходящей кислотой или подходящим ионообменным реагентом.
Соли соединений формулы I можно преобразовывать известным per se способом в другие соли соединений формулы I, соли присоединения кислот, например, в другие соли присоединения кислот, например, посредством обработки соли неорганической кислоты, например гидрохлорида, подходящей солью металла и кислоты, такой как соль натрия, бария или серебра, например ацетатом серебра, в подходящем растворителе, в котором неорганическая соль, которая образуется, например, хлорид серебра, является нерастворимой и, таким образом, осаждается из реакционной смеси.
В зависимости от процедуры или условий реакции соединения формулы I, которые обладают солеобразующими свойствами, можно получать в свободной форме или в форме солей.
Соединения формулы I и, в соответствующих случаях, их таутомеры, в каждом случае в свободной форме или в форме соли, могут присутствовать в форме одного из возможных изомеров или в виде их смеси, например, в форме чистых изомеров, таких как антиподы и/или диастереомеры, или в виде смесей изомеров, таких как смеси энантиомеров, например рацематы, смесей диастереомеров или смесей рацематов в зависимости от числа, абсолютной и относительной конфигурации асимметричных атомов углерода, которые находятся в молекуле, и/или в зависимости от конфигурации неароматических двойных связей, которые находятся в молекуле; настоящее изобретение относится к чистым изомерам, а также ко всем возможным смесям изомеров, и его следует понимать в каждом случае выше и ниже в данном документе в данном смысле, даже если стереохимические подробности не были упомянуты конкретно в каждом случае.
Смеси диастереомеров или смеси рацематов соединений формулы I, в свободной форме или в форме соли, которые могут быть получены в зависимости от того, какие исходные вещества и процедуры были выбраны, можно разделять известным способом на чистые диастереомеры или рацематы на основе физико-химических различий компонентов, например, с помощью фракционной кристаллизации, дистилляции и/или хроматографии.
Смеси энантиомеров, такие как рацематы, которые можно получать аналогичным способом, можно разделять на оптические антиподы с помощью известных способов, например, с помощью перекристаллизации из оптически активного растворителя, с помощью хроматографии на хиральных адсорбентах, например, с помощью высокоэффективной жидкостной хроматографии (HPLC) на ацетилцеллюлозе, с помощью подходящих микроорганизмов, путем расщепления специфичными иммобилизованными ферментами, путем образования соединений включения, например, с применением хиральных краун-эфиров, где только один энантиомер участвует в образовании комплекса, или путем превращения в диастереомерные соли, например, путем проведения реакции рацемата основного конечного продукта с оптически активной кислотой, такой как карбоновая кислота, например, камфорная, винная или яблочная кислота, или сульфоновая кислота, например камфорсульфоновая кислота, и разделения смеси диастереомеров, которая может быть получена таким образом, например, путем фракционной кристаллизации, основанной на их разной растворимости, с получением диастереомеров, из которых необходимый энантиомер может быть высвобожден под действием подходящих средств, например основных средств.
Чистые диастереомеры или энантиомеры можно получать согласно настоящему изобретению не только путем разделения подходящих смесей изомеров, но также с помощью общеизвестных способов диастереоселективного или энантиоселективного синтеза, например, посредством осуществления способа согласно настоящему изобретению с исходными веществами подходящей стереохимической конфигурации.
N-оксиды можно получать посредством проведения реакции соединения формулы I с подходящим окислителем, например аддуктом H2O2/мочевина, в присутствии ангидрида кислоты, например, ангидрида трифторуксусной кислоты. Такие типы реакций окисления известны из литературы, например, из J. Med. Chem., 32 (12), 2561-73, 1989 или WO 2000/15615.
Преимущественным является выделение или синтез в каждом случае биологически более эффективного изомера, например энантиомера или диастереомера, или смеси изомеров, например смеси энантиомеров или смеси диастереомеров, если отдельные компоненты характеризуются различной биологической активностью.
Соединения формулы I и, в соответствующих случаях, их таутомеры, в каждом случае в свободной форме или в форме соли, могут быть также получены, если необходимо, в форме гидратов и/или могут включать другие растворители, например, которые могли быть использованы для кристаллизации соединений, присутствующих в твердой форме.
Соединения формулы I в соответствии с приведенными далее таблицами от Y-1 до Y-8, от Х-1 до Х-8, от U-1 до U-2 и от V-1 до V-6, представленными ниже, могут быть получены в соответствии со способами, описанными выше. Следующие примеры предназначены для иллюстрации настоящее изобретение и показывают предпочтительные соединения формулы I.
Таблицы от Y-1 до Y-8 относятся к соединениям формулы
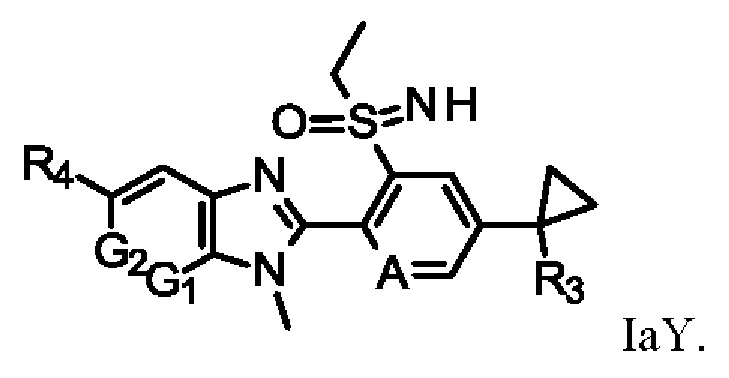
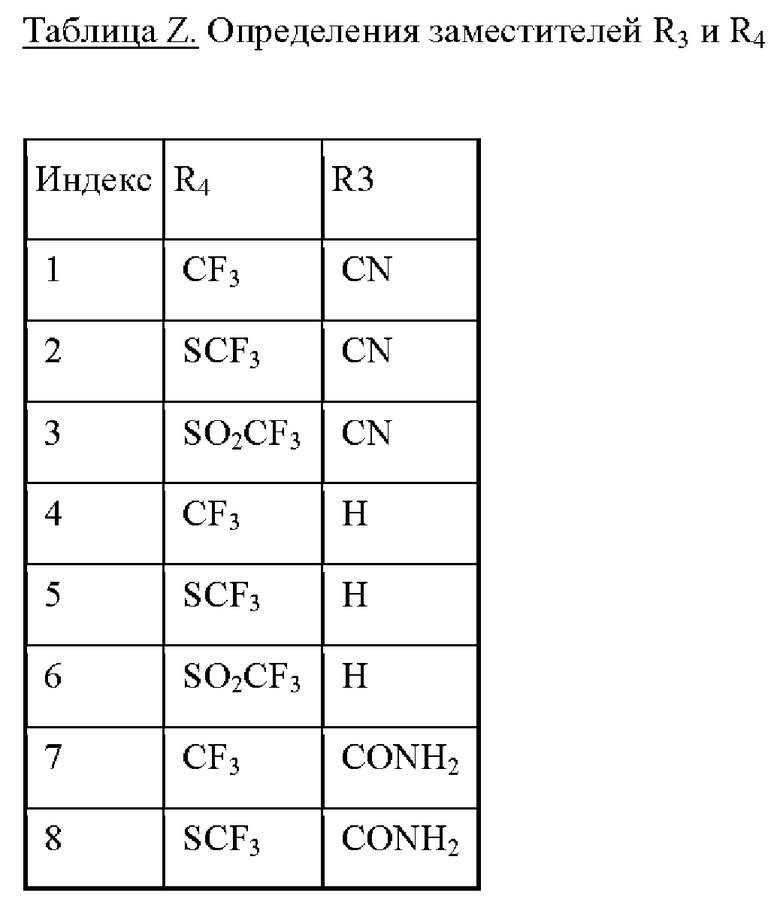
В таблице Y-45 представлены 8 соединений от Y-45.001 до Y-45.008 формулы IaY, где А представляет собой СН, G1 представляет собой СН, G2 представляет собой СН, a R3, R4 определены в таблице Z.
Например, соединение Y-1.001 характеризуется следующей структурой:
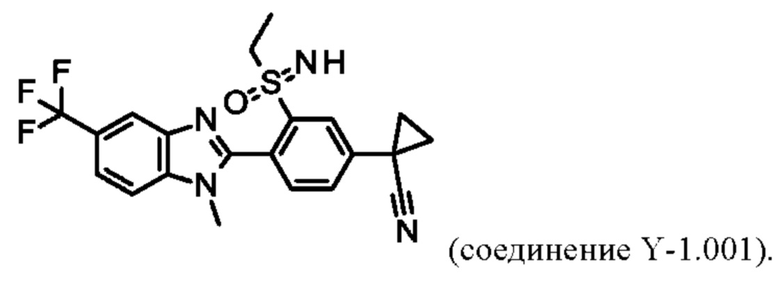
В таблице Y-2 представлены 8 соединений от Y-2.001 до Y-2.008 формулы IaY, где А представляет собой СН, G1 представляет собой СН, G2 представляет собой N, a R3, R4 определены в таблице Z.
Например, соединение Y-2.001 характеризуется следующей структурой:
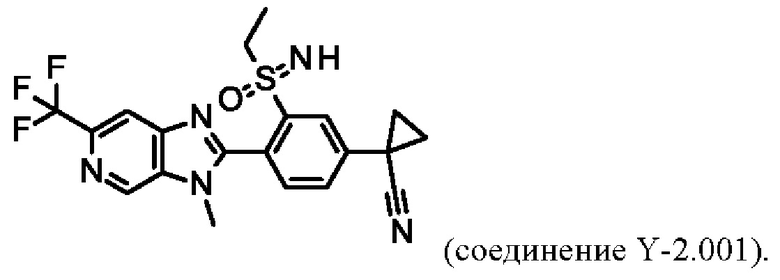
В таблице Y-3 представлены 8 соединений от Y-3.001 до Y-3.008 формулы IaY, где А представляет собой СН, G1 представляет собой N, G2 представляет собой СН, a R3, R4 определены в таблице Z.
Например, соединение Y-3.001 характеризуется следующей структурой:
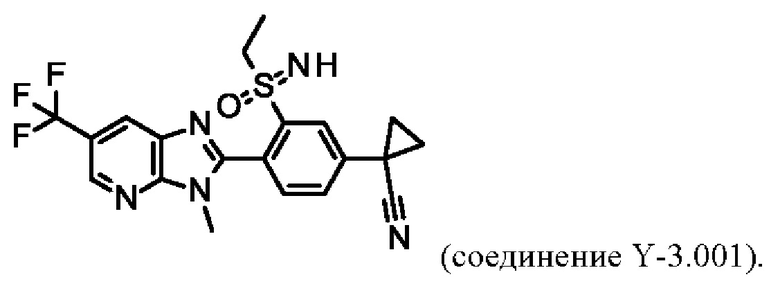
В таблица Y-46 представлены 8 соединений от Y-46.001 до Y-46.008 формулы IaY, где А представляет собой СН, G1 представляет собой N, G2 представляет собой N, a R3, R4 определены в таблице Z.
Например, соединение Y-4.001 характеризуется следующей структурой:
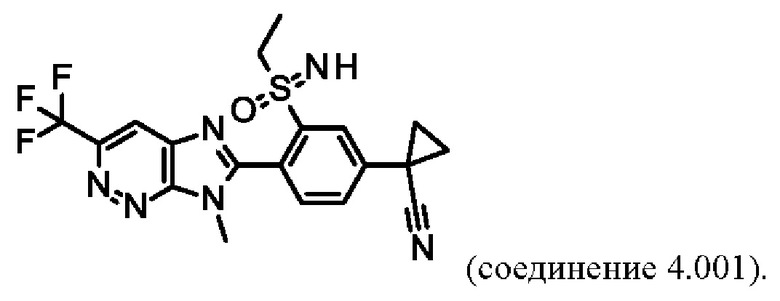
В таблице Y-5 представлены 8 соединений от Y-5.001 до Y-5.008 формулы IaY, где А представляет собой N, G1 представляет собой СН, G2 представляет собой СН, a R3, R4 определены в таблице Z.
Например, соединение Y-5.001 характеризуется следующей структурой:
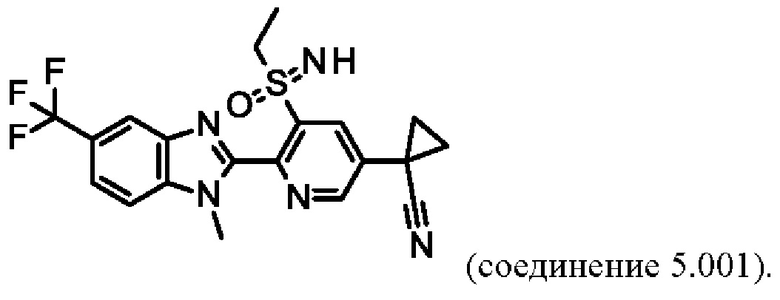
В таблице Y-6 представлены 8 соединений от Y-6.001 до Y-6.008 формулы IaY, где А представляет собой N, G1 представляет собой СН, G2 представляет собой N, a R3, R4 определены в таблице Z.
Например, соединение Y-6.001 характеризуется следующей структурой:
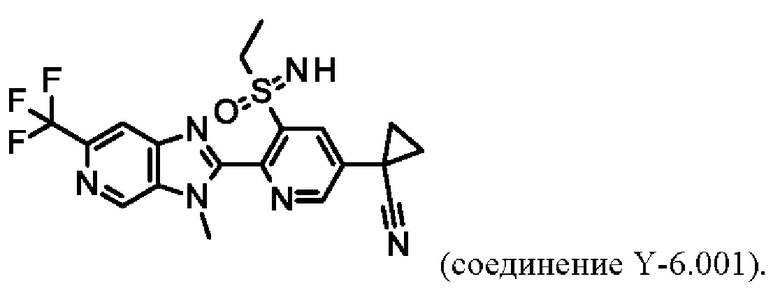
В таблице Y-7 представлены 8 соединений от Y-7.001 до Y-7.008 формулы IaY, где А представляет собой N, G1 представляет собой N, G2 представляет собой СН, a R3, R4 определены в таблице Z.
Например, соединение Y-7.001 характеризуется следующей структурой:
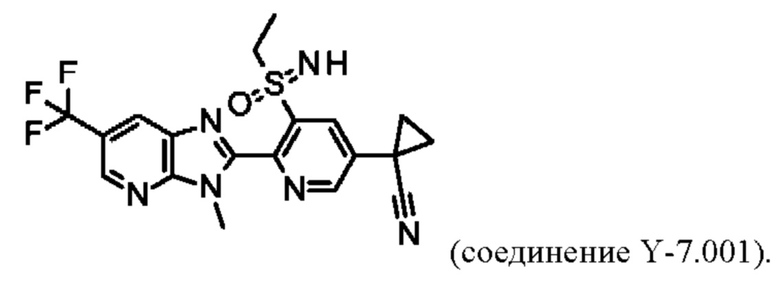
В таблице Y-8 представлены 8 соединений от Y-8.001 до Y-8.008 формулы IaY, где А представляет собой N, G1 представляет собой N, G2 представляет собой N, a R3, R4 определены в таблице Z.
Например, соединение Y-8.001 характеризуется следующей структурой:
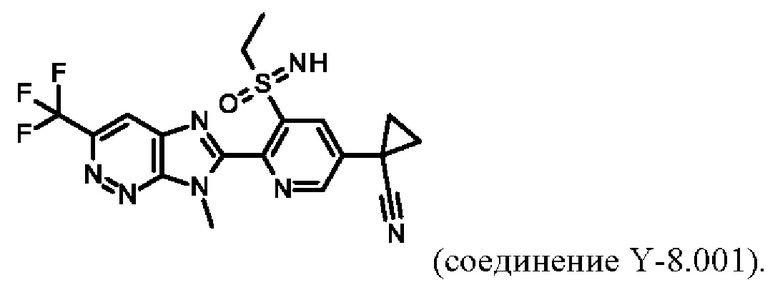
Таблицы от Х-1 до Х-8 относятся к соединениям формулы
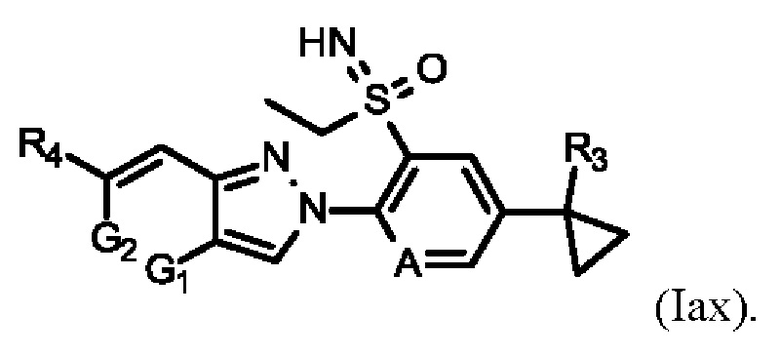
В таблице Х-1 представлены 8 соединений от Х-1.001 до Х-1.008 формулы Iax, где А представляет собой СН, G1 представляет собой СН, G2 представляет собой СН, a R3, R4 определены в таблице Z.
Например, соединение Х-1.001 характеризуется следующей структурой:
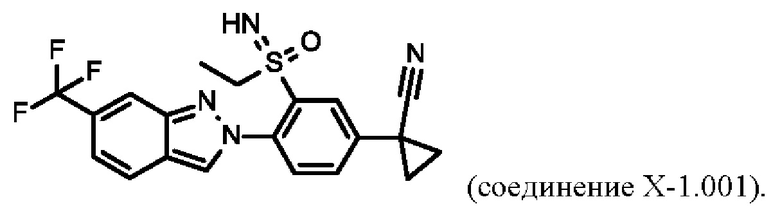
В таблице Х-2 представлены 8 соединений от Х-2.001 до Х-2.008 формулы Iax, где А представляет собой СН, G1 представляет собой СН, G2 представляет собой N, a R3, R4 определены в таблице Z.
В таблице Х-3 представлены 8 соединений от Х-3.001 до Х-3.008 формулы Iax, где А представляет собой СН, G1 представляет собой N, G2 представляет собой СН, a R3, R4 определены в таблице Z.
В таблице Х-4 представлены 8 соединений от Х-4.001 до Х-4.008 формулы Iax, где А представляет собой СН, G1 представляет собой N, G2 представляет собой N, a R3, R4 определены в таблице Z.
В таблице Х-5 представлены 8 соединений от Х-5.001 до Х-5.008 формулы Iax, где А представляет собой N, G1 представляет собой СН, G2 представляет собой СН, a R3, R4 определены в таблице Z.
В таблице Х-6 представлены 8 соединений от Х-6.001 до Х-6.008 формулы Ib, где А представляет собой N, G1 представляет собой СН, G2 представляет собой N, a R3, R4 определены в таблице Z.
В таблице Х-7 представлены 8 соединений от Х-7.001 до Х-7.008 формулы Ib, где А представляет собой N, G1 представляет собой N, G2 представляет собой СН, a R3, R4 определены в таблице Z.
В таблице Х-8 представлены 8 соединений от Х-8.001 до Х-8.008 формулы Ib, где А представляет собой N, G1 представляет собой N, G2 представляет собой N, a R3, R4 определены в таблице Z.
В таблицах от V-1 до V-6 ниже проиллюстрированы конкретные соединения формулы I по настоящему изобретению (где R2 представляет собой Н, и n равняется 1).
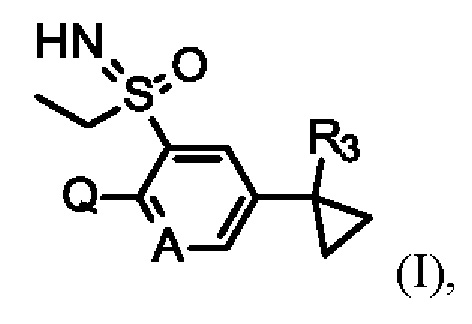
В таблице V-1 представлены 9 соединений от V-1.001 до V-1.009 формулы I, где А представляет собой СН, R3 представляет собой CN, a Q определены в таблице W.
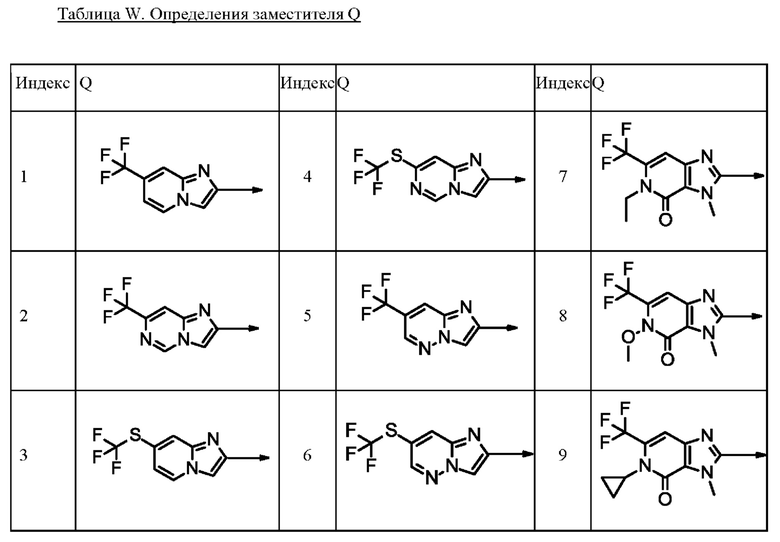
Например, соединение V-1.002 характеризуется следующей структурой:
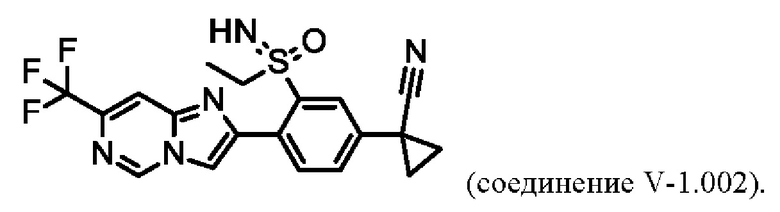
В таблице V-2 представлены 9 соединений от V-2.001 до V-2.009 формулы I, где А представляет собой N, R3 представляет собой CN, a Q определены в таблице W.
Например, соединение V-2.005 характеризуется следующей структурой:
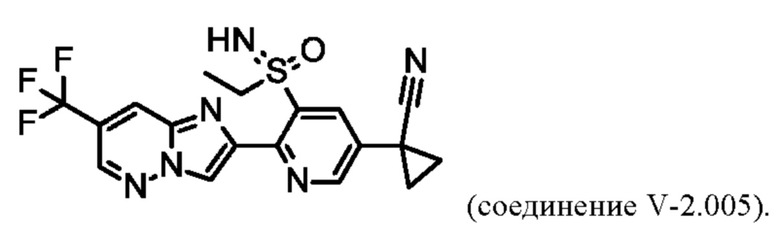
В таблице V-3 представлены 9 соединений от V-3.001 до V-3.009 формулы I, где А представляет собой СН, R3 представляет собой Н, a Q определены в таблице W.
Например, соединение V-3.008 характеризуется следующей структурой:
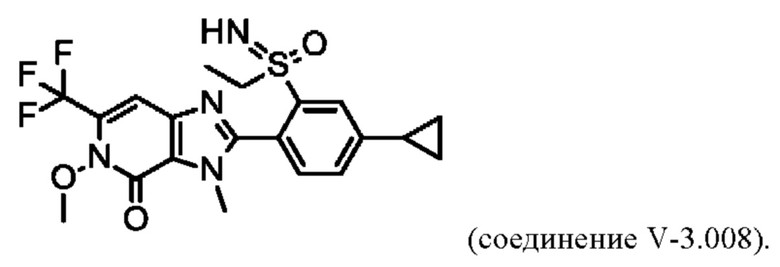
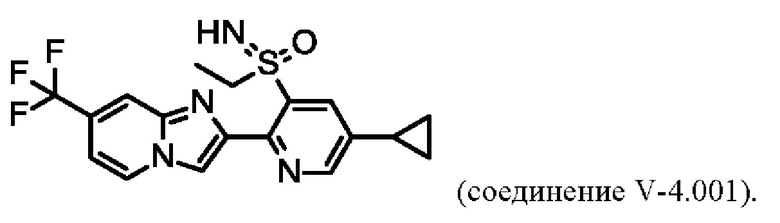
В таблице V-4 представлены 9 соединений от V-4.001 до V-4.009 формулы I, где А представляет собой N, R3 представляет собой Н, a Q определены в таблице W.
Например, соединение V-4.001 характеризуется следующей структурой:
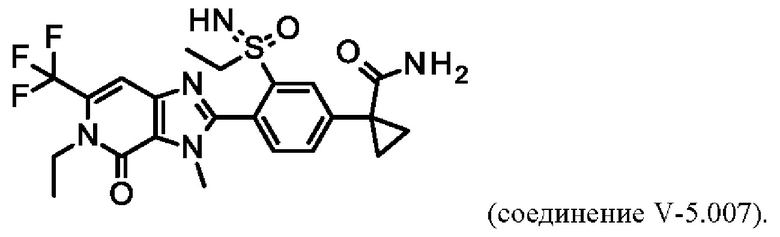
В таблице V-5 представлены 9 соединений от V-5.001 до V-5.009 формулы I, где А представляет собой СН, R3 представляет собой CONH2, a Q определены в таблице W.
Например, соединение V-5.007 характеризуется следующей структурой:
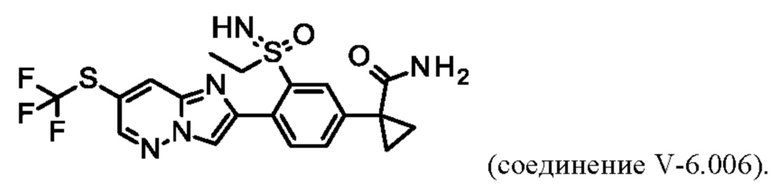
В таблице V-6 представлены 51 соединений от V-6.001 до V-6.009 формулы I, где А представляет собой N, R3 представляет собой CONH2, a Q определены в таблице W.
Например, соединение V-6.006 характеризуется следующей структурой:
Таблицы от U-1 до U-2 относятся к соединениям формулы
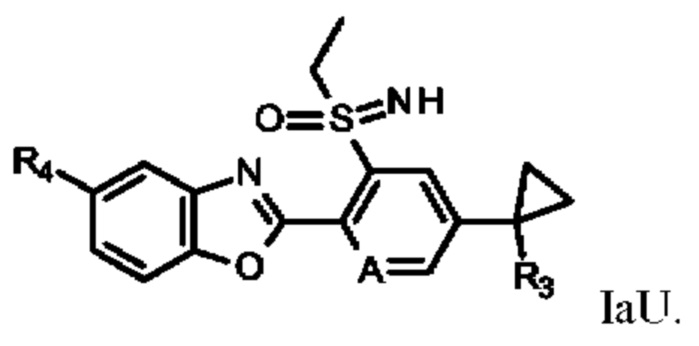
В таблице U-1 представлены 8 соединений от U-1.001 до U-1.008 формулы IaU, где А представляет собой СН, a R3, R4 определены в таблице Z.
Например, соединение U-1.001 характеризуется следующей структурой:
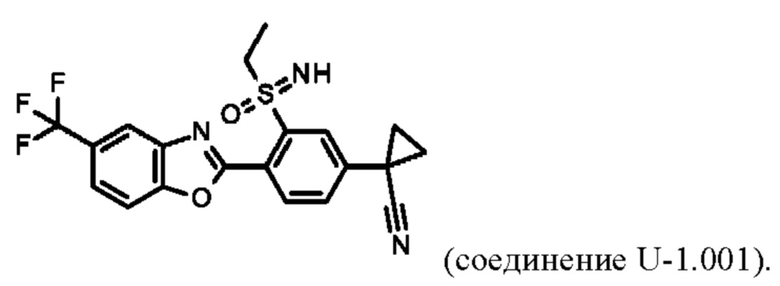
В таблице U-2 представлены 8 соединений от U-2.001 до U-2.008 формулы IaU, где А представляет собой N, a R3, R4 определены в таблице Z.
Соединения формулы I по настоящему изобретению представляют собой активные ингредиенты, имеющие важное значение в области контроля вредителей для предупреждения и/или лечения даже при низких нормах применения, которые обладают весьма подходящим биоцидным спектром и хорошо переносятся теплокровными видами, рыбами и растениями. Активные ингредиенты по настоящему изобретению действуют против обычно чувствительных, но также устойчивых, животных-вредителей, таких как насекомые, моллюски, нематоды или представители отряда Acarina, на всех или отдельных стадиях развития. Инсектицидная, моллюскицидная, нематоцидная или акарицидная активность активных ингредиентов по настоящему изобретению может проявляться непосредственно, т.е. в уничтожении вредителей, которое происходит либо немедленно, либо по прошествии некоторого времени, например, во время линьки, или косвенно, например, в сниженной степени откладывания яиц и/или вылупления, при этом хорошая активность соответствует степени уничтожения (смертности), составляющей по меньшей мере 50-60%.
Соединения формулы (I) по настоящему изобретению могут обладать любым числом преимуществ, включая, среди прочего, преимущественные уровни биологической активности для защиты растений от насекомых или превосходные свойства для применения в качестве агрохимически активных ингредиентов (например, более высокая биологическая активность, преимущественный спектр активности, повышенный профиль безопасности, улучшенные физико-химические свойства или повышенная биоразлагаемость или экологические характеристики). В частности, неожиданно было обнаружено, что определенные соединения формулы (I) показывают преимущественный профиль безопасности в отношении нецелевых организмов, например, нецелевых членистоногих, в частности опылителей, таких как медоносные пчелы, одиночные пчелы и шмели. Наиболее конкретно, Apis mellifera.
В связи с этим некоторые соединения формулы (I) по настоящему изобретению могут отличаться от известных соединений за счет более высокой эффективности при низких нормах применения, что способен проверить специалист в данной области с использованием экспериментальных процедур, аналогичных тем или адаптированными из тех, которые указаны в биологических примерах, используя при необходимости более низкие нормы применения, например, 50 ppm, 12,5 ppm, 6 ppm, 3 ppm, 1,5 ppm, 0,8 ppm или 0,2 ppm.
Дополнительно неожиданно было обнаружено, что соединения формулы (I) демонстрируют преимущественные физико-химические свойства для применения в защите растений, в частности сниженную точку плавления, сниженную липофильность и повышенную растворимость в воде. Было обнаружено, что такие свойства являются преимущественными для поглощения растениями и системного распределения по их организму (см., например, A. Buchholz, S. Trapp, Pest Manag Sci 2016; 72: 929-939) с целью контроля некоторый видов вредителей, перечисленных ниже.
Примерами вышеупомянутых животных-вредителей являются:
из отряда Acarina, например,
Acalitus spp, Aculus spp, Acaricalus spp, Aceria spp, Acarus siro, Amblyomma spp., Argas spp., Boophilus spp., Brevipalpus spp., Bryobia spp, Calipitrimerus spp., Chorioptes spp., Dermanyssus gallinae, Dermatophagoides spp, Eotetranychus spp, Eriophyes spp., Hemitarsonemus spp, Hyalomma spp., Ixodes spp., Olygonychus spp., Ornithodoros spp., Polyphagotarsone latus, Panonychus spp., Phyllocoptruta oleivora, Phytonemus spp, Polyphagotarsonemus spp, Psoroptes spp., Rhipicephalus spp., Rhizoglyphus spp., Sarcoptes spp., Steneotarsonemus spp, Tarsonemus spp. и Tetranychus spp.;
из отряда Anoplura, например,
Haematopinus spp., Linognathus spp., Pediculus spp., Pemphigus spp. и Phylloxera spp.; из отряда Coleoptera, например, Agriotes spp., Amphimallon majale, Anomala orientalis, Anthonomus spp., Aphodius spp, Astylus atromaculatus, Ataenius spp, Atomaria linearis, Chaetocnema tibialis, Cerotoma spp., Conoderus spp., Cosmopolites spp., Cotinis nitida, Curculio spp., Cyclocephala spp, Dermestes spp., Diabrotica spp., Diloboderus abderus, Epilachna spp., Eremnus spp., Heteronychus arator, Hypothenemus hampei, Lagria vilosa, Leptinotarsa decemLineata, Lissorhoptrus spp., Liogenys spp., Maecolaspis spp, Maladera castanea, Megascelis spp., Melighetes aeneus, Melolontha spp., Myochrous armatus, Orycaephilus spp., Otiorhynchus spp., Phyllophaga spp, Phlyctinus spp., Popillia spp., Psylliodes spp., Rhyssomatus aubtilis, Rhizopertha spp., Scarabeidae, Sitophilus spp., Sitotroga spp., Somaticus spp., Sphenophorus spp, Sternechus subsignatus, Tenebrio spp., Tribolium spp. и Trogoderma spp.;
из отряда Diptera, например,
Aedes spp., Anopheles spp., Antherigona soccata, Bactrocea oleae, Bibio hortulanus, Bradysia spp., Calliphora erythrocephala, Ceratitis spp., Chrysomyia spp., Culex spp., Cuterebra spp., Dacus spp., Delia spp, Drosophila melanogaster, Fannia spp., Gastrophilus spp., Geomyza tripunctata, Glossina spp., Hypoderma spp., Hyppobosca spp., Liriomyza spp., Lucilia spp., Melanagromyza spp., Musca spp., Oestrus spp., Orseolia spp., Oscinella frit, Pegomyia hyoscyami, Phorbia spp., Rhagoletis spp., Rivelia quadrifasciata, Scatella spp., Sciara spp., Stomoxys spp., Tabanus spp., Tannia spp. и Tipula spp.;
из отряда Hemiptera, например,
Acanthocoris scabrator, Acrostemum spp, Adelphocoris lineolatus, Amblypelta nitida, Bathycoelia thalassina, Blissus spp., Cimex spp., Clavigralla tomentosicollis, Creontiades spp, Distantiella theobroma, Dichelops furcatus, Dysdercus spp., Edessa spp., Euschistus spp., Eurydema pulchram, Eurygaster spp., Halyomorpha halys, Horcias nobilellus, Leptocorisa spp., Lygus spp, Margarodes spp, Murgantia histrionic, Neomegalotomus spp, Nesidiocoris tenuis, Nezara spp., Nysius simulans, Oebalus insularis, Piesma spp., Piezodorus spp, Rhodnius spp., Sahlbergella singularis, Scaptocoris castanea, Scotinophara spp., Thyanta spp, Triatoma spp., Vatiga illudens;
Acyrthosium pisum, Adalges spp, Agalliana ensigera, Agonoscenatargionii, Aleurodicus spp, Aleurocanthus spp, Aleurolobus barodensis, Aleurothrixus floccosus, Aleyrodes brassicae, Amarasca biguttula, Amritodus atkinsoni, Aonidiella spp., Aphididae, Aphis spp., Aspidiotus spp., Aulacorthum solani, Bactericera cockerelli, Bemisia spp, Brachycaudus spp, Brevicoryne brassicae, Cacopsylla spp, Cavariella aegopodii Scop., Ceroplaster spp., Chrysomphalus aonidium, Chrysomphalus dictyospermi, Cicadella spp, Cofana spectra, Cryptomyzus spp, Cicadulina spp, Coccus hesperidum, Dalbulus maidis, Dialeurodes spp, Diaphorina citri, Diuraphis noxia, Dysaphis spp, Empoasca spp., Eriosoma larigerum, Erythroneura spp., Gascardia spp., Glycaspis brimblecombei, Hyadaphis pseudobrassicae, Hyalopterus spp, Hyperomyzus pallidus, Idioscopus clypealis, Jacobiasca lybica, Laodelphax spp., Lecanium corni, Lepidosaphes spp., Lopaphis erysimi, Lyogenys maidis, Macrosiphum spp., Mahanarva spp, Metcalfa pruinosa, Metopolophium dirhodum, Myndus crudus, Myzus spp., Neotoxoptera sp, Nephotettix spp., Nilaparvata spp., Nippolachnus piri Mats, Odonaspis ruthae, Oregma lanigera Zehnter, Parabemisia myricae, Paratrioza cockerelli, Parlatoria spp., Pemphigus spp., Peregrinus maidis, Perkinsiella spp, Phorodon humuli, Phylloxera spp, Planococcus spp., Pseudaulacaspis spp., Pseudococcus spp., Pseudatomoscelis seriatus, Psylla spp., Pulvinaria aethiopica, Quadraspidiotus spp., Quesada gigas, Recilia dorsalis, Rhopalosiphum spp., Saissetia spp., Scaphoideus spp., Schizaphis spp., Sitobion spp., Sogatella furcifera, Spissistilus festinus, Tarophagus Proserpina, Toxoptera spp, Trialeurodes spp, Tridiscus sporoboli, Trionymus spp, Trioza erytreae, Unaspis citri, Zygina llammigera, Zyginidia scutellaris;
из отряда Hymenoptera, например,
Acromyrmex, Arge spp, Atta spp., Cephus spp., Diprion spp., Diprionidae, Gilpinia polytoma, Hoplocampa spp., Lasius spp., Monomorium pharaonis, Neodiprion spp., Pogonomyrmex spp, Slenopsis invicta, Solenopsis spp. и Vespa spp.;
из отряда Isoptera, например,
Coptotermes spp, Corniternes cumulans, mcisitermes spp, Macrotermes spp, Mastotermes spp, Microtermes spp, Reticulitermes spp.; Solenopsis geminate
из отряда Lepidoptera, например,
Acleris spp., Adoxophyes spp., Aegeria spp., Agrotis spp., Alabama argillaceae, Amylois spp., Anticarsia gemmatalis, Archips spp., Argyresthia spp, Argyrotaenia spp., Autographa spp., Bucculatrix thurberiella, Busseola fusca, Cadra cautella, Carposina nipponensis, Chilo spp., Choristoneura spp., Chrysoteuchia topiaria, Clysia ambiguella, Cnaphalocrocis spp., Cnephasia spp., Cochylis spp., Coleophora spp., Colias lesbia, Cosmophila flava, Crambus spp, Crocidolomia binotalis, Cryptophlebia leucotreta, Cydalima perspectalis, Cydia spp., Diaphania perspectalis, Diatraea spp., Diparopsis castanea, Earias spp., Eldana saccharina, Ephestia spp., Epinotia spp, Estigmene acrea, Etiella zinckinella, Eucosma spp., Eupoecilia ambiguella, Euproctis spp., Euxoa spp., Feltiajaculiferia, Grapholita spp., Hedya nubiferana, Heliothis spp., Hellula undalis, Herpetogramma spp, Hyphantria cunea, Keiferia lycopersicella, Lasmopalpus lignosellus, Leucoptera scitella, Lithocollethis spp., Lobesia botrana, Loxostege bifidalis, Lymantria spp., Lyonetia spp., Malacosoma spp., Mamestra brassicae, Manduca sexta, Mythimna spp, Noctua spp, Operophtera spp., Orniodes indica, Ostrinia nubilalis, Pammene spp., Pandemis spp., Panolis flammea, Papaipema nebris, Pectinophora gossypiela, Perileucoptera coffeella, Pseudaletia unipuncta, Phthorimaea operculella, Pieris rapae, Pieris spp., Plutella xylostella, Prays spp., Pseudoplusia spp, Rachiplusia nu, Richia albicosta, Scirpophaga spp., Sesamia spp., Sparganothis spp., Spodoptera spp., Sylepta derogate, Synanthedon spp., Thaumetopoea spp., Tortrix spp., Trichoplusia ni, Tuta absoluta, и Yponomeuta spp.;
из отряда Mallophaga, например,
Damalinea spp. и Trichodectes spp.;
из отряда Orthoptera, например,
Blatta spp., Blattella spp., Gryllotalpa spp., Leucophaea maderae, Locusta spp., Neocurtilla hexadactyla, Periplaneta spp., Scapteriscus spp, и Schistocerca spp.;
из отряда Psocoptera, например,
Liposcelis spp.;
из отряда Siphonaptera, например,
Ceratophyllus spp., Ctenocephalides spp. и Xenopsylla cheopis;
из отряда Thysanoptera, например,
Calliothrips phaseoli, Frankliniella spp., Heliothrips spp, Hercinothrips spp., Parthenothrips spp, Scirtothrips aurantii, Sericothrips variabilis, Taeniothrips spp., Thrips spp; из отряда Thysanura, например, Lepisma saccharina.
Активные ингредиенты в соответствии с настоящим изобретением можно применять для контроля, т.е. сдерживания или уничтожения, вредителей вышеуказанного типа, которые встречаются, в частности, на растениях, особенно на полезных растениях и декоративных растениях в сельском хозяйстве, в садоводстве и в лесоводстве, или на органах таких растений, таких как плоды, цветки, листья, стебли, клубни или корни, и в некоторых случаях даже на органах растений, которые образуются в более поздние сроки и при этом остаются защищенными от данных вредителей.
Подходящими целевыми сельскохозяйственными культурами являются, в частности, зерновые культуры, такие как пшеница, ячмень, рожь, овес, рис, маис или сорго; свекла, такая как сахарная свекла или кормовая свекла; плодовые культуры, например, семечковые, косточковые или ягодные культуры, такие как сорта яблони, груши, сливы, персика, миндаля, черешни или ягод, например, сорта клубники, малины или ежевики; бобовые культуры, такие как сорта бобов, чечевицы, гороха или сои; масличные культуры, такие как масличный рапс, горчица, мак, маслины, сорта подсолнечника, кокосовая пальма, клещевина, какао или сорта арахиса; тыквенные культуры, такие как тыквы, огурцы или дыни; волокнистые растения, такие как хлопчатник, лен, конопля или джут; цитрусовые, такие как апельсины, лимоны, грейпфрут или мандарины; овощи, такие как шпинат, салат-латук, спаржа, сорта капусты, моркови, лука, томата, картофеля или болгарского перца; представители Lauraceae, такие как авокадо, Cinnamonium или камфорное дерево; а также табак, орехи, кофе, сорта баклажана, сахарный тростник, чай, перец, сорта культурного винограда, хмеля, подорожниковые и каучуконосные растения.
Композиции и/или способы по настоящему изобретению также можно применять по отношению к любым декоративным и/или овощным культурам, в том числе цветам, кустарникам, широколиственным деревьям и вечнозеленым растениям.
Например, настоящее изобретение можно применять по отношению к любому из следующих видов декоративных растений: Ageratum spp., Alonsoa spp., Anemone spp., Anisodontea capsenisis, Anthemis spp., Antirrhinum spp., Aster spp., Begonia spp. (например, В. elatior, В. semperflorens, B. tubéreux), Bougainvillea spp., Brachycome spp., Brassica spp. (декоративные виды), Calceolaria spp., Capsicum annuum, Catharanthus roseus, Carina spp., Centaurea spp., Chrysanthemum spp., Cineraria spp. (C. maritime), Coreopsis spp., Crassula coccinea, Cuphea ignea, Dahlia spp., Delphinium spp., Dicentra spectabilis, Dorotheantus spp., Eustoma grandiflorum, Forsythia spp., Fuchsia spp., Geranium gnaphalium, Gerbera spp., Gomphrena globosa, Heliotropium spp., Helianthus spp., Hibiscus spp., Hortensia spp., Hydrangea spp., Hypoestes phyllostachya, Impatiens spp. (I. Walleriana), Iresines spp., Kalanchoe spp., Lantana camara, Lavatera trimestris, Leonotis leonurus, Lilium spp.,Mesembryanthemum spp., Mimulus spp., Monarda spp., Nemesia spp., Tagetes spp., Dianthus spp. (гвоздика), Canna spp., Oxalis spp., Bellis spp., Pelargonium spp. (P. peltatum, P. Zonale), Viola spp.(анютины глазки), Petunia spp., Phlox spp., Plecthranthus spp., Poinsettia spp., Parthenocissus spp. (P. quinquefolia, P. tricuspidata), Primula spp., Ranunculus spp., Rhododendron spp., spp. (роза), Rudbeckia spp., Saintpaulia spp., Salvia spp., Scaevola aemola, Schizanthus wisetonensis, Sedum spp., Solanum spp., Surfinia spp., Tagetes spp., Nicotinia spp., Verbena spp., Zinnia spp и другие грядковые растения.
Например, настоящее изобретение можно применять по отношению к любому из следующих видов овощей: Allium spp. (A. sativum, А., сера, A. oschaninii, А. Porrum, А. ascalonicum, A. fistulosum), Anthriscus cerefolium, Apium graveolus, Asparagus officinalis, Beta vulgarus, Brassica spp. (B. Oleracea, B. Pekinensis, B. rapa), Capsicum annuum, Cicer arietinum, Cichorium endivia, Cichorum spp. (C. intybus, C. endivia), Citrillus lanatus, Cucumis spp. (C. sativus, C. melo), Cucurbita spp. (С. pepo, С. maxima), Cyanara spp. (C. scolymus, C. cardunculus), Daucus carota, Foeniculum vulgare, Hypericum spp., Lactuca sativa, Lycopersicon spp. (L. esculentum, L. lycopersicum), Mentha spp., Ocimum basilicum, Petroselinum crispum, Phaseolus spp. (P. vulgaris, P. coccineus), Pisum sativum, Raphanus sativus, Rheum rhaponticum, Rosemarinus spp., Salvia spp., Scorzonera hispanica, Solanum melongena, Spinacea oleracea, Valerianella spp. (K locusta, V. eriocarpa) и Vicia faba.
Предпочтительные виды декоративных растений включают африканскую фиалку, Begonia, Dahlia, Gerbera, Hydrangea, Verbena, Rosa, Kalanchoe, Poinsettia, Aster, Centaurea, Coreopsis, Delphinium, Monarda, Phlox, Rudbeckia, Sedum, Petunia, Viola, Impatiens, Geranium, Chrysanthemum, Ranunculus, Fuchsia, Salvia, Hortensia, розмарин, шалфей, зверобой, мяту, сладкий перец, томат и огурец.
Активные ингредиенты в соответствии с настоящим изобретением являются особенно подходящими для контроля Aphis craccivora, Diabrotica balteata, Heliothis virescens, Myzus persicae, Plutella xylostella и Spodoptera littoralis на хлопчатнике, овощных, кукурузных, рисовых и соевых культурах. Кроме того, активные ингредиенты в соответствии с настоящим изобретением являются особенно подходящими для контроля Mamestra (предпочтительно в овощных культурах), Cydia pomonella (предпочтительно в сортах яблони), Empoasca (предпочтительно в овощных культурах, виноградниках), Leptinotarsa (предпочтительно в сортах картофеля) и Chilo supressalis (предпочтительно в рисе).
Активные ингредиенты в соответствии с настоящим изобретением являются особенно подходящими для контроля Aphis craccivora, Diabrotica balteata, Heliothis virescens, Myzus persicae, Plutella xylostella и Spodoptera littoralis на хлопчатнике, овощных, кукурузных, рисовых и соевых культурах. Кроме того, активные ингредиенты в соответствии с настоящим изобретением являются особенно подходящими для контроля Mamestra (предпочтительно в овощных культурах), Cydia pomonella (предпочтительно в сортах яблони), Empoasca (предпочтительно в овощных культурах, виноградниках), Leptinotarsa (предпочтительно в сортах картофеля) и Chilo supressalis (предпочтительно в рисе).
В дополнительном аспекте настоящее изобретение может также относиться к способу контроля повреждения растения и его частей паразитирующими на растении нематодами (эндопаразитными, полуэндопаразитными и эктопаразитными нематодами), в частности, паразитирующими на растении нематодами, такими как клубеньковые нематоды, Meloidogyne hapla, Meloidogyne incognita, Meloidogyne javanica, Meloidogyne arenaria и другие виды Meloidogyne; образующие цисты нематоды, Globodera rostochiensis и другие виды Globodera; Heterodera avenae, Heterodera glycines, Heterodera schachtii, Heterodera trifolii и другие виды Heterodera; галловые нематоды семян, виды Anguina; стеблевые и листовые нематоды, виды Aphelenchoides; жалящие нематоды, Belonolaimus longicaudatus и другие виды Belonolaimus; нематоды хвойных, Bursaphelenchus xylophilus и другие виды Bursaphelenchus; кольцевые нематоды, виды Criconema, виды Criconemella, виды Criconemoides, виды Mesocriconema; стеблевые и луковичные нематоды, Ditylenchus destructor, Ditylenchus dipsaci и другие виды Ditylenchus; шилоносые нематоды, виды Dolichodorus; спиральные нематоды, Heliocotylenchus multicinctus и другие виды Helicotylenchus; оболочковые и оболочкоподобные нематоды, виды Hemicycliophora и виды Hemicriconemoides; виды Hirshmanniella; ланцетоподобные нематоды, виды Hoploaimus; нематоды ненастоящих корневых наростов, виды Nacobbus; игольчатые нематоды, Longidorus elongatus и другие виды Longidorus; короткотелые нематоды, виды Pratylenchus; ранящие нематоды, Pratylenchus neglectus, Pratylenchus penetrans, Pratylenchus curvitatus, Pratylenchus goodeyi и другие виды Pratylenchus; роющие нематоды, Radopholus similis и другие виды Radopholus; почковидные нематоды, Rotylenchus robustus, Rotylenchus reniformis и другие виды Rotylenchus; виды Scutellonema; нематоды щетинистых корнеплодов, Trichodorus primitivus и другие виды Trichodorus, виды Paratrichodorus; карликовые нематоды, Tylenchorhynchus claytoni, Tylenchorhynchus dubius и другие виды Tylenchorhynchus; цитрусовые нематоды, виды Tylenchulus; ксифинема американская, виды Xiphinema; а также другие паразитирующие на растениях виды нематод, такие как Subanguina spp., Hypsoperine spp., Macroposthonia spp., Melinius spp., Punctodera spp. и Quinisulcius spp.
Соединения по настоящему изобретению также могут обладать активностью по отношению к моллюскам. Примеры данных моллюсков включают, например, Ampullariidae; Arion (A. ater, A. circumscriptus, A. hortensis, A. rufus); Bradybaenidae (Bradybaena fruticum); Cepaea (C. hortensis, C. Nemoralis); ochlodina; Deroceras (D. agrestis, D. empiricorum, D. laeve, D. reticulatum); Discus (D. rotundatus); Euomphalia; Galba (G. trunculata); Helicelia (H. itala, H. obvia); Helicidae Helicigona arbustorum); Helicodiscus; Helix (H. aperta); Limax (L. cinereoniger, L. flavus, L. marginatus, L. maximus, L. tenellus); Lymnaea; Milax (M. gagates, M. marginatus, M. sowerbyi); Opeas; Pomacea (P. canaticulata); Vallonia и Zanitoides.
Термин "сельскохозяйственные культуры" следует понимать как включающий также культурные растения, которые были трансформированы с помощью методик с применением рекомбинантных ДНК таким образом, что они приобрели способность к синтезу одного или нескольких токсинов избирательного действия, таких как известные, например, у токсинообразующих бактерий, в особенности бактерий рода Bacillus.
Токсины, которые могут быть экспрессированы такими трансгенными растениями, включают, например, инсектицидные белки, например инсектицидные белки из Bacillus cereus или Bacillus popilliae; или инсектицидные белки из Bacillus thuringiensis, такие как 6-эндотоксины, например, Cry1Ab, Cry1Ac, Cry1F, Cry1Fa2, Cry2Ab, Cry3A, Cry3Bb1 или Cry9C, или вегетативные инсектицидные белки (Vip), например, Vip1, Vip2, Vip3 или Vip3A; или инсектицидные белки бактерий, колонизирующих нематод, например, Photorhabdus spp. или Xenorhabdus spp., таких как Photorhabdus luminescens, Xenorhabdus nematophilus; токсины, продуцируемые животными, такие как токсины скорпионов, токсины паукообразных, токсины ос и другие специфические по отношению к насекомым нейротоксины; токсины, продуцируемые грибами, такие как токсины Streptomycetes, растительные лектины, такие как лектины гороха, лектины ячменя или лектины подснежника; агглютинины; ингибиторы протеиназы, такие как ингибиторы трипсина, ингибиторы серинпротеазы, пататин, цистатин, ингибиторы папаина; белки, инактивирующие рибосому (RIP), такие как рицин, RIP кукурузы, абрин, люффин, сапорин или бриодин; ферменты метаболизма стероидов, такие как 3-гидроксистероидоксидаза, экдистероид-UDP-гликозилтрансфераза, холестеролоксидазы, ингибиторы экдизона, HMG-COA-редуктаза, блокаторы ионных каналов, такие как блокаторы натриевых или кальциевых каналов, эстераза ювенильного гормона, рецепторы диуретических гормонов, стильбенсинтаза, дибензилсинтаза, хитиназы и глюканазы.
В контексте настоящего изобретения под δ-эндотоксинами, например, Cry1Ab, Cry1Ac, Cry1F, Cry1Fa2, Cry2Ab, Cry3A, Cry3Bb1 или Cry9C, или вегетативными инсектицидными белками (Vip), например, Vip1, Vip2, Vip3 или Vip3A, определенно следует понимать также гибридные токсины, усеченные токсины и модифицированные токсины. Гибридные токсины получают рекомбинантным способом с помощью новой комбинации различных доменов этих белков (см., например, WO 2002/15701). Известны усеченные токсины, например усеченный Cry1Ab. В случае модифицированных токсинов одна или несколько аминокислот токсина, встречающегося в природе, являются замененными. При таких аминокислотных заменах в токсин предпочтительно вводят не встречающиеся в природном токсине последовательности, распознаваемые протеазами, так, например, в случае Cry3A055 в токсин Cry3A вводят последовательность, распознаваемую катепсином G (см. WO 2003/018810).
Примеры таких токсинов или трансгенных растений, способных синтезировать такие токсины, раскрыты, например, в ЕР-А-0374753, WO 1993/07278, WO 1995/34656, ЕР-А-0427529, ЕР-А-451878 и WO 2003/052073.
Способы получения таких трансгенных растений в целом известны специалисту в данной области и описаны, например, в публикациях, упомянутых выше.
Дезоксирибонуклеиновые кислоты CryI-типа и их получение известно, например, из WO 95/34656, ЕР-А-0367474, ЕР-А-0401979 и WO 1990/13651.
Токсин, содержащийся в трансгенных растениях, придает растениям толерантность в отношении вредных насекомых. Такие насекомые могут принадлежать к любой таксономической группе насекомых, но особенно часто встречаются среди жуков (Coleoptera), двукрылых насекомых (Diptera) и мотыльков (Lepidoptera). Трансгенные растения, содержащие один или несколько генов, которые кодируют устойчивость к насекомым и экспрессируют один или несколько токсинов, являются известными, и некоторые из них коммерчески доступны. Примерами таких растений являются: YieldGard® (сорт маиса, экспрессирующий токсин Cry1Ab); YieldGard Rootworm® (сорт маиса, экспрессирующий токсин Cry3Bb1); YieldGard Plus® (сорт маиса, экспрессирующий токсин Cry1Ab и токсин Cry3Bb1); Starlink® (сорт маиса, экспрессирующий токсин Cry9C); Herculex I® (сорт маиса, экспрессирующий токсин Cry1Fa2 и фермент фосфинотрицин-N-ацетилтрансферазу (PAT) с достижением толерантности к гербициду глюфосинату аммония); NuCOTN 33В® (сорт хлопчатника, экспрессирующий токсин Cry1Ac); Bollgard I® (сорт хлопчатника, экспрессирующий токсин Cry1Ac); Bollgard II® (сорт хлопчатника, экспрессирующий токсин Cry1Ac и токсин Cry2Ab); VipCot® (сорт хлопчатника, экспрессирующий токсин Vip3A и токсин Cry1Ab); NewLeaf® (сорт картофеля, экспрессирующий токсин Cry3A); NatureGard® Agrisure® GT Advantage (GA21 с признаком толерантности к глифосату), Agrisure® СВ Advantage (Bt11 с признаком устойчивости к кукурузному мотыльку (СВ)) и Protecta®. Дополнительными примерами таких трансгенных сельскохозяйственных культур являются следующие.
1. Маис Bt11 от Syngenta Seeds SAS, Chemin de l'Hobit 27, F-31 790 Сен-Совер, Франция, регистрационный номер C/FR/96/05/10. Генетически модифицированный Zea mays, которому придали устойчивость к поражению кукурузным мотыльком (Ostrinia nubilalis и Sesamia nonagrioides) в результате трансгенной экспрессии усеченного токсина Cry1Ab. Маис Bt11 также трансгенно экспрессирует фермент PAT с достижением толерантности к гербициду глюфосинату аммония.
2. Маис Bt176 от Syngenta Seeds SAS, Chemin de l'Hobit 27, F-31 790 Сен-Совер, Франция, регистрационный номер C/FR/96/05/10. Генетически модифицированный Zea mays, которому придали устойчивость к поражению кукурузным мотыльком (Ostrinia nubilalis и Sesamia nonagrioides) в результате трансгенной экспрессии токсина Cry1Ab.
Маис Bt176 также трансгенно экспрессирует фермент PAT с достижением толерантности к гербициду глюфосинату аммония.
3. Маис MIR604 от Syngenta Seeds SAS, Chemin de l'Hobit 27, F-31 790 Сен-Совер, Франция, регистрационный номер C/FR/96/05/10. Маис, которому придали устойчивость к насекомым в результате трансгенной экспрессии модифицированного токсина Cry3A. Данный токсин представляет собой Cry3A055, модифицированный путем вставки последовательности, распознаваемой протеазой катепсином G. Получение таких трансгенных растений маиса описано в WO 2003/018810.
4. Маис MON 863 от Monsanto Europe S.A. 270-272 Авеню-Де-Тервюрен, В-1150 Брюссель, Бельгия, регистрационный номер C/DE/02/9. MON 863 экспрессирует токсин Cry3Bb1 и обладает устойчивостью к некоторым насекомым из отряда Coleoptera.
5. Хлопчатник IPC 531 от Monsanto Europe S.A. 270-272 Авеню-Де-Тервюрен, В-1150 Брюссель, Бельгия, регистрационный номер C/ES/96/02.
6. Маис 1507 от Pioneer Overseas Corporation, Авеню-Тедеско, 7 B-1160 Брюссель, Бельгия, регистрационный номер C/NL/00/10. Генетически модифицированный маис для экспрессии белка Cry1F для достижения устойчивости к некоторым насекомым из отряда Lepidoptera и белка PAT для достижения толерантности к гербициду глюфосинату аммония.
7. Маис NK603 × MON 810 от Monsanto Europe S.A. 270-272 Авеню-Де-Тервюрен, В-1150 Брюссель, Бельгия, регистрационный номер C/GB/02/M3/03. Состоит из гибридных сортов маиса, выведенных традиционным способом скрещивания генетически модифицированных сортов NK603 и MON 810. Маис NK603 × MON 810 трансгенно экспрессирует белок СР4 EPSPS, полученный из Agrobacterium sp. штамма СР4, который придает толерантность к гербициду Roundup® (содержит глифосат), а также токсин Cry1Ab, полученный из Bacillus thuringiensis подвида kurstaki, который придает толерантность к конкретным представителям отряда Lepidoptera, включая кукурузного мотылька.
Трансгенные сельскохозяйственные культуры устойчивых к насекомым растений также описаны в отчете BATS за 2003 год ( Zentrum BATS, Clarastrasse 13, 4058 Базель, Швейцария) (http://bats.ch). Термин "сельскохозяйственные культуры" следует понимать как включающий также культурные растения, которые были трансформированы путем применения технологий рекомбинантной ДНК таким образом, что они стали способными синтезировать антипатогенные вещества с селективным действием, такие как, например, так называемые "связанные с патогенезом белки" (PRP, см., например, ЕР-А-0392225). Примеры таких антипатогенных веществ и трансгенных растений, способных синтезировать такие антипатогенные вещества, известны, например, из ЕР-А-0392225, WO 1995/33818 и ЕР-А-0353191. Способы получения таких трансгенных растений в целом известны специалисту в данной области и описаны, например, в публикациях, упомянутых выше.
Zentrum BATS, Clarastrasse 13, 4058 Базель, Швейцария) (http://bats.ch). Термин "сельскохозяйственные культуры" следует понимать как включающий также культурные растения, которые были трансформированы путем применения технологий рекомбинантной ДНК таким образом, что они стали способными синтезировать антипатогенные вещества с селективным действием, такие как, например, так называемые "связанные с патогенезом белки" (PRP, см., например, ЕР-А-0392225). Примеры таких антипатогенных веществ и трансгенных растений, способных синтезировать такие антипатогенные вещества, известны, например, из ЕР-А-0392225, WO 1995/33818 и ЕР-А-0353191. Способы получения таких трансгенных растений в целом известны специалисту в данной области и описаны, например, в публикациях, упомянутых выше.
Антипатогенные вещества, которые могут быть экспрессированы такими трансгенными растениями, включают, например, блокаторы ионных каналов, такие как блокаторы натриевых и кальциевых каналов, например, вирусные токсины KP1, KP4 или KP6; стильбенсинтазы; бибензилсинтазы; хитиназы; глюканазы; так называемые "связанные с патогенезом белки" (PRP; см., например, ЕР-А-0392225); антипатогенные вещества, вырабатываемые микроорганизмами, например, пептидные антибиотики или гетероциклические антибиотики (см., например, WO 1995/33818) или белковые или полипептидные факторы, вовлеченные в защиту растения от патогенов (так называемые "гены сопротивляемости растений к заболеваниям", как описано в WO 2003/000906).
Дополнительными областями применения композиций в соответствии с настоящим изобретением являются защита хранящихся товаров и складских помещений и защита сырьевых материалов, таких как древесина, ткани, покрытия для пола или строительные материалы, а также применение в области санитарии, в частности защиты человека, домашних животных и продуктивного скота от вредителей упомянутого типа.
В настоящем изобретении также предусмотрен способ контроля вредителей (таких как комары и другие переносчики заболеваний; см. также http://www.who.int/malaria/vector_control/irs/en/). В одном варианте осуществления способ контроля вредителей включает применение композиций по настоящему изобретению по отношению к целевым вредителям, по отношению к их месторасположению или по отношению к поверхности или субстрату путем нанесения кистью, нанесения валиком, опрыскивания, нанесения методом растекания или протравливания погружением. В качестве примера способ по настоящему изобретению предполагает IRS-применение (опрыскивание пестицидами остаточного действия внутри помещений) по отношению к поверхности, такой как поверхность стены, потолка или пола. В другом варианте осуществления предполагается применение данных композиций по отношению к субстрату, такому как нетканый или тканый материал в виде (или который может применяться в изготовлении) сетки, одежды, постельных принадлежностей, занавесок и палаток.
В одном варианте осуществления способ контроля таких вредителей включает применение пестицидно эффективного количества композиций по настоящему изобретению по отношению к целевым вредителям, по отношению к их месторасположению или по отношению к поверхности или субстрату, чтобы тем самым обеспечить эффективный уровень активности пестицидов остаточного действия на поверхности или субстрате. Такое применение пестицидной композиции по настоящему изобретению можно осуществлять путем нанесения кистью, нанесения валиком, опрыскивания, нанесения методом растекания или протравливания погружением. В качестве примера способ по настоящему изобретению предполагает IRS-применение по отношению к поверхности, такой как поверхность стены, потолка или пола, для обеспечения таким образом эффективной активности пестицидов остаточного действия на поверхности. В другом варианте осуществления предполагается применение таких композиций для контроля вредителей на субстрате, таком как тканый материал в виде (или который может применяться в изготовлении) сетки, одежды, постельных принадлежностей, занавесок и палаток, благодаря остаточному действию.
Субстраты, включая подлежащие обработке нетканые материалы, тканые материалы или сетку, могут быть изготовленными из натуральных волокон, таких как хлопок, рафия, джут, лен, сизаль, мешковина или шерсть, или из синтетических волокон, таких как полиамид, сложный полиэфир, полипропилен, полиакрилонитрил или подобные. Сложные полиэфиры являются особенно подходящими. Способы обработки тканей известны, например, из WO 2008/151984, WO 2003/034823, US 5631072, WO 2005/64072, WO 2006/128870, ЕР 1724392, WO 2005/113886 или WO 2007/090739.
Другими областями применения композиций согласно настоящему изобретению являются область введения в дерево/обработки ствола всех декоративных деревьев, а также всех сортов плодовых и ореховых деревьев.
В области введения в дерево/обработки ствола соединения согласно настоящему изобретению являются особенно подходящими против насекомых-древоточцев из отряда Lepidoptera, как упоминалось выше, и из отряда Coleoptera, особенно против древоточцев, перечисленных в следующих таблицах А и В.
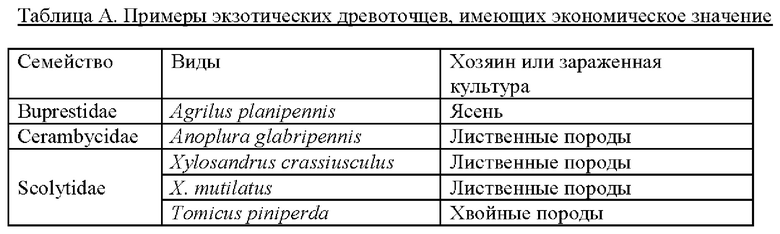
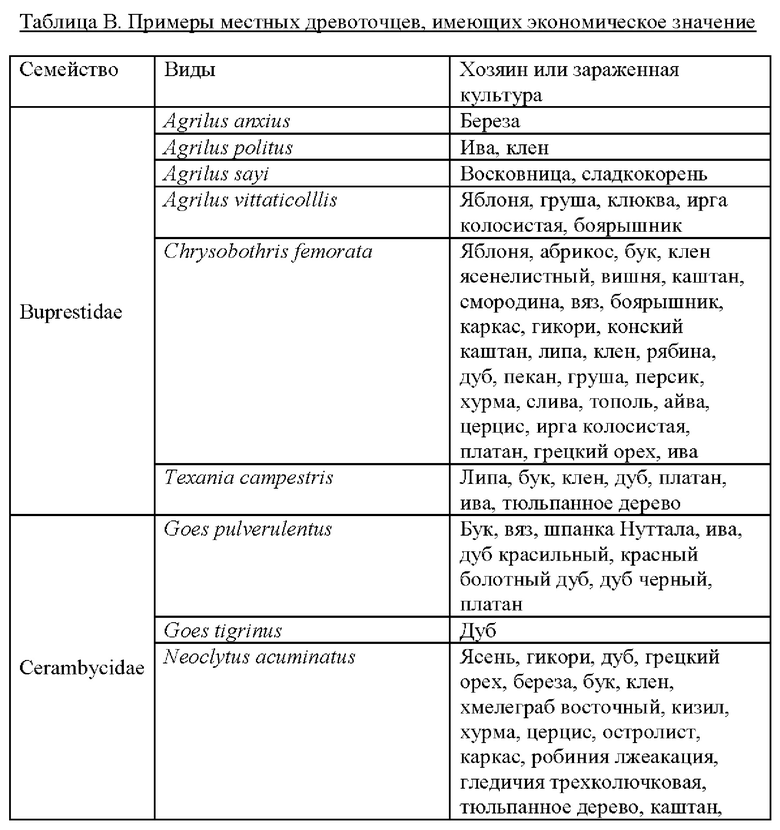
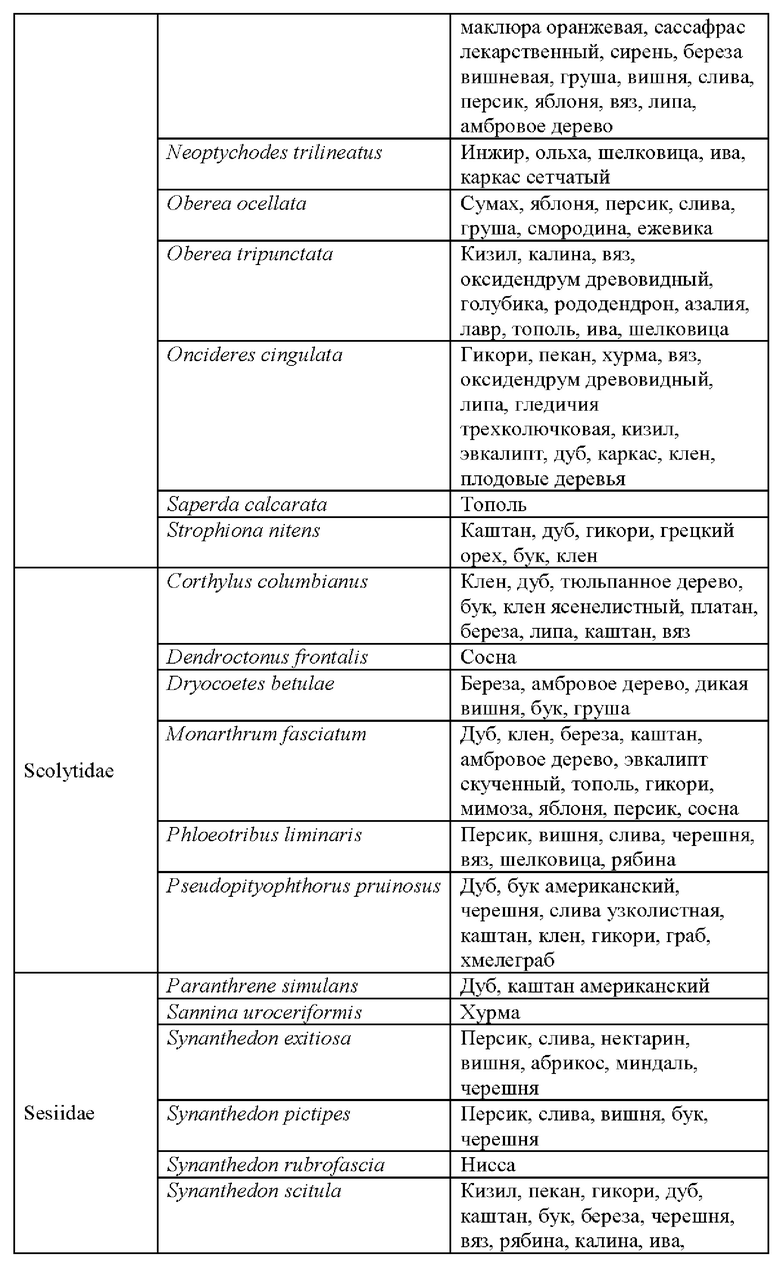

Настоящее изобретение также можно применять для контроля любых насекомых-вредителей, которые могут присутствовать в газонной траве, в том числе, например, жуки, гусеницы, огненные муравьи, червецы, двупарноногие многоножки, мокрицы, клещи, медведки, щитовки, войлочники, иксодовые клещи, пенницы, Blissus insularis и личинки хруща. Настоящее изобретение можно применять для контроля насекомых-вредителей на различных стадиях их жизненного цикла, в том числе на стадии яиц, личинок, нимф и взрослых особей.
В частности, настоящее изобретение можно применять для контроля насекомых-вредителей, которые питаются корнями газонной травы, в том числе личинки хруща (такие как Cyclocephala spp. (например, масковый хрущ, С. lurida), Rhizotrogus spp. (например, хрущ европейский, R. majalis), Cotinus spp. (например, хрущ блестящий зеленый, С. nitida), Popillia spp.(например, хрущик японский, P. japonica), Phyllophaga spp.(например, майский/июньский хрущ), Ataenius spp. (например, черный корневой жук рода Ataenius, A. spretulus), Maladera spp.(например, хрущик азиатский садовый М. castaned) и Tomarus spp.), червецы (Margarodes spp.), медведки (темно-желтая, южная и короткокрылая; Scapteriscus spp., Gryllotalpa africand) и личинки комаров долгоножек (долгоножка болотная, Tipula spp.).
Настоящее изобретение также можно применять для контроля насекомых-вредителей газонной травы, которые обитают в соломине, в том числе "походные черви" (такие как совка травяная Spodoptera frugiperda и совка луговая Pseudaletia unipuncta), гусеницы озимой совки, долгоносики (Sphenophorus spp., такие как S. venatus verstitus и S. parvulus) и луговые мотыльки (такие как Crambus spp. и тропические луговые мотыльки, Herpetogramma phaeopteralis).
Настоящее изобретение также можно применять для контроля насекомых-вредителей газонной травы, которые живут над землей и питаются листьями газонной травы, в том числе земляные клопы (такие как земляные клопы, Blissus insularis), клещ бермудской травы (Eriophyes cynodoniensis), червец хлорис гвианской (Antonina graminis), пенница двухполосая (Propsapia bicincta), цикадки, гусеницы озимой совки (семейства Noctuidae) и тли злаковые.
Настоящее изобретение также можно применять для контроля других вредителей газонной травы, таких как муравьи огненные импортные красные (Solenopsis invicta), которые создают муравейники на поверхности газона.
В области санитарии композиции согласно настоящему изобретению активны против эктопаразитов, таких как твердые клещи, мягкие клещи, зудни чесоточные, краснотелки, мухи (жалящие и лижущие), личинки паразитических мух, вши, головные вши, пухоеды и блохи.
Примерами таких паразитов являются следующие.
Из отряда Anoplurida: Haematopinus spp., Linognathus spp., Pediculus spp. и Phtirus spp., Solenopotes spp.
Из отряда Mallophagida: Trimenopon spp., Menopon spp., Trinoton spp., Bovicola spp., Werneckiella spp., Lepikentron spp., Damalina spp., Trichodectes spp. и Felicola spp.
Из отряда Diptera и подотрядов Nematocerina и Brachycerina, например, Aedes spp., Anopheles spp., Culex spp., Simulium spp., Eusimulium spp., Phlebotomus spp., Lutzomyia spp., Culicoides spp., Chrysops spp., Hybomitra spp., Atylotus spp., Tabanus spp., Haematopota spp., Philipomyia spp., Braula spp., Musca spp., Hydrotaea spp., Stomoxys spp., Haematobia spp., Morellia spp., Fannia spp., Glossina spp., Calliphora spp., Lucilia spp., Chrysomyia spp., Wohlfahrtia spp., Sarcophaga spp., Oestrus spp., Hypoderma spp., Gasterophilus spp., Hippobosca spp., Lipoptena spp. и Melophagus spp.
Из отряда Siphonapterida, например, Pulex spp., Ctenocephalides spp., Xenopsylla spp., Ceratophyllus spp.
Из отряда Heteropterida, например, Cimex spp., Triatoma spp., Rhodnius spp., Panstrongylus spp.
Из отряда Blattarida, например Blatta orientalis, Periplaneta americana, Blattela germanica и Supella spp.
Из подкласса Acaria (Acarida) и отрядов Meta- и Mesostigmata, например, Argas spp., Ornithodorus spp., Otobius spp., Ixodes spp., Amblyomma spp., Boophilus spp., Dermacentor. Из отрядов Actinedida (Prostigmata) и Acaridida (Astigmata), например, Acarapis spp., Cheyletiella spp., Ornithocheyletia spp., Myobia spp., Psorergatesspp., Demodex spp., Trombicula spp., Listrophorus spp., Acarus spp., Tyrophagus spp., Caloglyphus spp., Hypodectes spp., Pterolichus spp., Psoroptes spp., Chorioptes spp., Otodectes spp., Sarcoptes spp., Notoedres spp., Knemidocoptes spp., Cytodites spp. и Laminosioptes spp.
Композиции согласно настоящему изобретения также являются подходящими для защиты от заражения насекомыми в случае материалов, таких как древесина, ткани, пластики, адгезивы, виды клея, краски, бумага и картон, кожа, покрытия для пола и строительные материалы.
Композиции согласно настоящему изобретению можно применять, например, против следующих вредителей: жуков, таких как Hylotrupes bajulus, Chlorophorus pilosis, Anobium punctatum, Xestobium rufovillosum, Ptilinuspecticornis, Dendrobium pertinex, Ernobius mollis, Priobium carpini, Lyctus brunneus, Lyctus africanus, Lyctus planicollis, Lyctus linearis, Lyctus pubescens, Trogoxylon aequale, Minthesrugicollis, Xyleborus spec, Tryptodendron spec, Apate monachus, Bostrychus capucins, Heterobostrychus brunneus, Sinoxylon spec, и Dinoderus minutus, а также перепончатокрылых насекомых, таких как Sirex juvencus, Urocerus gigas, Urocerus gigas taignus и Urocerus augur, и термитов, таких как Kalotermes flavicollis, Cryptotermes brevis, Heterotermes indicola, Reticulitermes flavipes, Reticulitermes santonensis, Reticulitermes lucifugus, Mastotermes darwiniensis, Zootermopsis nevadensis и Coptotermes formosanus, и щетинохвосток, таких как Lepisma saccharina.
Соединения согласно настоящему изобретению можно применять в качестве пестицидных средств в немодифицированной форме, но, как правило, их различными способами составляют в композиции с применением вспомогательных веществ для составления, таких как носители, растворители и поверхностно-активные вещества. Составы могут быть представлены в различных физических формах, например, в форме распыляемых порошков, гелей, смачиваемых порошков, диспергируемых в воде гранул, диспергируемых в воде таблеток, шипучих драже, эмульгируемых концентратов, концентратов микроэмульсий, эмульсий типа "масло в воде", масляных текучих составов, водных дисперсий, масляных дисперсий, суспоэмульсий, капсульных суспензий, эмульгируемых гранул, растворимых жидкостей, водорастворимых концентратов (с водой или смешиваемым с водой органическим растворителем в качестве носителя), пропитанных полимерных пленок или в других формах, известных, например, из Manual on Development and Use of FAO and WHO Specifications for Pesticides, United Nations, First Edition, Second Revision (2010). Такие составы можно либо применять непосредственно, либо разбавлять перед применением. Разбавления можно осуществлять, например, с помощью воды, жидких удобрений, питательных микроэлементов, биологических организмов, масла или растворителей.
Составы можно получать, например, путем смешивания активного ингредиента со вспомогательными веществами для составления с получением композиций в форме тонкодисперсных твердых веществ, гранул, растворов, дисперсий или эмульсий. Активные ингредиенты также можно составлять с другими вспомогательными веществами, например, тонкодисперсными твердыми веществами, минеральными маслами, маслами растительного или животного происхождения, модифицированными маслами растительного или животного происхождения, органическими растворителями, водой, поверхностно-активными веществами или их комбинациями.
Активные ингредиенты также могут содержаться в очень мелких микрокапсулах. Микрокапсулы содержат активные ингредиенты в пористом носителе. Это обеспечивает возможность высвобождения активных ингредиентов в окружающую среду в регулируемых количествах (например, медленного высвобождения). Микрокапсулы обычно имеют диаметр от 0,1 до 500 микрон. Они содержат активные ингредиенты в количестве от приблизительно 25 до 95% по весу от веса капсулы. Активные ингредиенты могут находиться в форме монолитного твердого вещества, в форме мелких частиц в твердой или жидкой дисперсии или в форме подходящего раствора. Инкапсулирующие мембраны могут содержать, например, природные и синтетические каучуки, целлюлозу, сополимеры стирола и бутадиена, полиакрилонитрил, полиакрилат, сложные полиэфиры, полиамиды, полимочевины, полиуретан или химически модифицированные полимеры и ксантаты крахмала или другие полимеры, которые известны специалисту в данной области. В качестве альтернативы могут быть образованы очень мелкие микрокапсулы, в которых активный ингредиент содержится в форме тонкодисперсных частиц в твердой матрице основного вещества, однако микрокапсулы сами по себе не являются инкапсулированными.
Вспомогательные вещества для составления, которые являются подходящими для получения композиций в соответствии с настоящим изобретением, являются известными per se. В качестве жидких носителей можно применять воду, толуол, ксилол, петролейный эфир, растительные масла, ацетон, метилэтилкетон, циклогексанон, ангидриды кислот, ацетонитрил, ацетофенон, амилацетат, 2-бутанон, бутиленкарбонат, хлорбензол, циклогексан, циклогексанол, алкиловые сложные эфиры уксусной кислоты, диацетоновый спирт, 1,2-дихлорпропан, диэтаноламин, п-диэтилбензол, диэтиленгликоль, абиетат диэтиленгликоля, простой бутиловый эфир диэтиленгликоля, простой этиловый эфир диэтиленгликоля, простой метиловый эфир диэтиленгликоля, N,N-диметилформамид, диметилсульфоксид, 1,4-диоксан, дипропиленгликоль, метиловый эфир дипропиленгликоля, дибензоат дипропиленгликоля, дипрокситол, алкилпирролидон, этилацетат, 2-этилгексанол, этиленкарбонат, 1,1,1-трихлорэтан, 2-гептанон, альфа-пинен, d-лимонен, этиллактат, этиленгликоль, простой бутиловый эфир этиленгликоля, простой метиловый эфир этиленгликоля, гамма-бутиролактон, глицерин, ацетат глицерина, диацетат глицерина, триацетат глицерина, гексадекан, гексиленгликоль, изоамилацетат, изоборнилацетат, изооктан, изофорон, изопропилбензол, изопропилмиристат, молочную кислоту, лауриламин, мезитилоксид, метоксипропанол, метил-изоамилкетон, метил-изобутилкетон, метиллаурат, метилоктаноат, метилолеат, метиленхлорид, м-ксилол, н-гексан, н-октиламин, октадекановую кислоту, октиламинацетат, олеиновую кислоту, олеиламин, о-ксилол, фенол, полиэтиленгликоль, пропионовую кислоту, пропиллактат, пропиленкарбонат, пропиленгликоль, простой метиловый эфир пропиленгликоля, п-ксилол, толуол, триэтилфосфат, триэтиленгликоль, ксилолсульфоновую кислоту, парафин, минеральное масло, трихлорэтилен, перхлорэтилен, этилацетат, амилацетат, бутилацетат, простой метиловый эфир пропиленгликоля, простой метиловый эфир диэтиленгликоля, метанол, этанол, изопропанол и высокомолекулярные спирты, такие как амиловый спирт, тетрагидрофурфуриловый спирт, гексанол, октанол, этиленгликоль, пропиленгликоль, глицерин, N-метил-2-пирролидон и т.п.
Подходящими твердыми носителями являются, например, тальк, диоксид титана, пирофиллитовая глина, диоксид кремния, аттапульгитовая глина, кизельгур, известняк, Большое количество поверхностно-активных веществ можно успешно использовать как в твердых, так и в жидких составах, особенно в тех составах, которые можно разбавлять носителем перед применением. Поверхностно-активные вещества могут быть анионными, катионными, неионогенными или полимерными, и их можно применять в качестве эмульгаторов, смачивающих средств или суспендирующих средств или для других целей. Типичные поверхностно-активные вещества включают, например, соли алкилсульфатов, такие как лаурилсульфат диэтаноламмония; соли алкиларилсульфонатов, такие как додецилбензолсульфонат кальция; продукты присоединения алкилфенола/алкиленоксида, такие как этилоксилат нонилфенола; продукты присоединения спирта/алкиленоксида, такие как этоксилат тридецилового спирта; мыла, такие как стеарат натрия; соли алкилнафталинсульфонатов, такие как дибутилнафталинсульфонат натрия; сложные диалкиловые эфиры сульфосукцинатных солей, такие как ди(2-этилгексил)сульфосукцинат натрия; сложные эфиры сорбита, такие как сорбитолеат; четвертичные амины, такие как хлорид лаурилтриметиламмония, сложные полиэтиленгликолевые эфиры жирных кислот, такие как стеарат полиэтиленгликоля; блок-сополимеры этиленоксида и пропиленоксида и соли моно- и диалкилфосфатных сложных эфиров; а также дополнительные вещества, описанные, например, в McCutcheon's Detergents and Emulsifiers Annual, MC Publishing Corp., Ridgewood New Jersey (1981).
Дополнительные вспомогательные вещества, которые можно использовать в пестицидных составах, включают ингибиторы кристаллизации, модификаторы вязкости, суспендирующие средства, красители, антиоксиданты, вспенивающие средства, поглотители света, вспомогательные средства для смешивания, противовспениватели, комплексообразующие средства, нейтрализующие или рН-модифицирующие вещества и буферы, ингибиторы коррозии, отдушки, смачивающие средства, усилители поглощения, питательные микроэлементы, пластификаторы, вещества, способствующие скольжению, смазывающие вещества, диспергирующие вещества, загустители, антифризы, микробиоциды, а также жидкие и твердые удобрения.
Композиции в соответствии с настоящим изобретением могут включать добавку, предусматривающую масло растительного или животного происхождения, минеральное масло, сложные алкиловые эфиры таких масел или смеси таких масел и производных масел. Количество масляной добавки в композиции согласно настоящему изобретению обычно составляет от 0,01 до 10% в пересчете на смесь, подлежащую применению. Например, масляную добавку можно добавлять в резервуар опрыскивателя в требуемой концентрации после получения смеси для опрыскивания. Предпочтительные масляные добавки включают минеральные масла или масло растительного происхождения, например, рапсовое масло, оливковое масло или подсолнечное масло, эмульгированное растительное масло, сложные алкиловые эфиры масел растительного происхождения, например метиловые производные, или масло животного происхождения, такое как рыбий жир или говяжий жир. Предпочтительные масляные добавки включают сложные алкиловые эфиры С8-С22-жирных кислот, особенно метиловые производные С12-С18-жирных кислот, например, сложные метиловые эфиры лауриновой кислоты, пальмитиновой кислоты и олеиновой кислоты (метиллаурат, метилпальмитат и метилолеат соответственно). Многие производные масел известны из Compendium of Herbicide Adjuvants, 10th Edition, Southern Illinois University, 2010.
Композиции по настоящему изобретению, как правило, содержат от 0,1 до 99% по весу, в частности от 0,1 до 95% по весу соединений по настоящему изобретению и от 1 до 99,9% по весу вспомогательного вещества для составления, которое предпочтительно включает от 0 до 25% по весу поверхностно-активного вещества. Поскольку коммерческие продукты предпочтительно могут быть составлены в виде концентратов, то конечный потребитель обычно будет использовать разбавленные составы.
Нормы применения варьируются в широких пределах и зависят от свойств почвы, способа применения, культурного растения, вредителя, подлежащего контролю, преобладающих климатических условий и других факторов, определяемых способом применения, временем применения и целевой сельскохозяйственной культурой. В качестве общего руководства, соединения можно применять при норме от 1 до 2000 л/га, в частности от 10 до 1000 л/га.
Предпочтительные составы могут характеризоваться следующими композициями (вес.%).
Эмульгируемые концентраты:
активный ингредиент: 1-95%, предпочтительно 60-90%;
поверхностно-активное вещество: 1-30%, предпочтительно 5-20%;
жидкий носитель: 1-80%, предпочтительно 1-35%.
Пылевидные препараты:
активный ингредиент: 0,1-10%, предпочтительно 0,1-5%;
твердый носитель: 99,9-90%, предпочтительно 99,9-99%.
Суспензионные концентраты:
активный ингредиент: 5-75%, предпочтительно 10-50%;
вода: 94-24%, предпочтительно 88-30%;
поверхностно-активное вещество: 1-40%, предпочтительно 2-30%.
Смачиваемые порошки:
активный ингредиент: 0,5-90%, предпочтительно 1-80%;
поверхностно-активное вещество: 0,5-20%, предпочтительно 1-15%;
твердый носитель: 5-95%, предпочтительно 15-90%.
Гранулы:
активный ингредиент: 0,1-30%, предпочтительно 0,1-15%;
твердый носитель: 99,5-70%, предпочтительно 97-85%.
Следующие примеры дополнительно иллюстрируют, но не ограничивают настоящее изобретение.


Комбинацию тщательно смешивают со вспомогательными веществами и смесь тщательно измельчают в подходящей мельнице с получением смачиваемых порошков, которые можно разбавлять водой с получением суспензий с необходимой концентрацией.
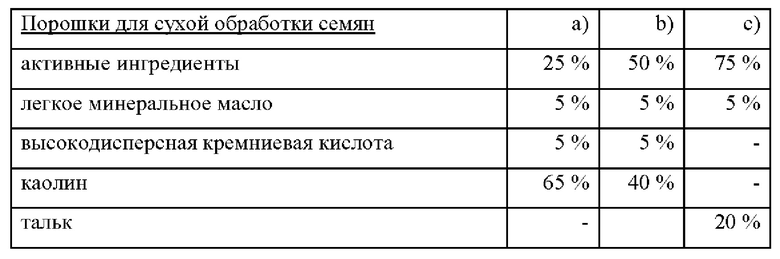
Комбинацию тщательно смешивают со вспомогательными веществами и тщательно измельчают смесь в подходящей мельнице с получением порошков, которые можно использовать непосредственно для обработки семян.

Из этого концентрата путем разбавления водой можно получить эмульсии любого необходимого разбавления, которые можно применять для защиты растений.


Готовые к применению пылевидные препараты получают путем смешивания комбинации с носителем и измельчения смеси в подходящей мельнице. Такие порошки также можно применять для сухого протравливания семян.

Комбинацию смешивают и измельчают со вспомогательными веществами, и смесь увлажняют водой. Смесь экструдируют и затем высушивают в потоке воздуха.
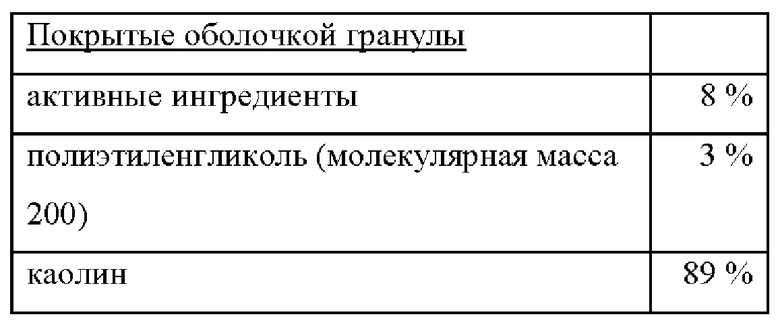
Тонкоизмельченную комбинацию в перемешивающем устройстве равномерно наносят на увлажненный полиэтиленгликолем каолин. Таким способом получают непылевидные покрытые оболочкой гранулы.
Суспензионный концентрат


Тонкоизмельченную комбинацию тщательно смешивают со вспомогательными веществами с получением суспензионного концентрата, из которого путем разбавления водой можно получать суспензии любого требуемого разбавления. С помощью таких разбавленных растворов можно обработать и защитить от заражения микроорганизмами живые растения, а также материал для размножения растений путем опрыскивания, полива или погружения. Текучий концентрат для обработки семян
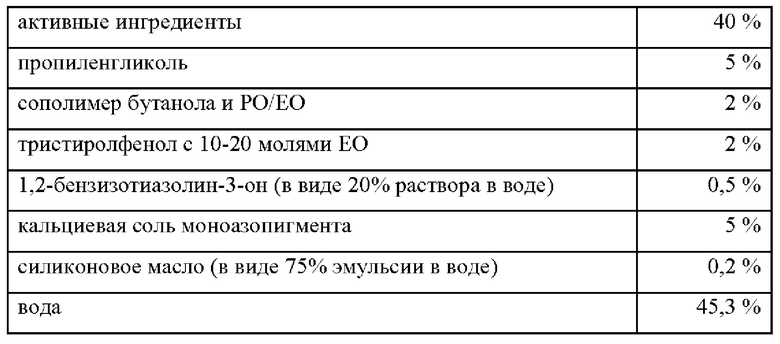
Тонкоизмельченную комбинацию тщательно смешивают со вспомогательными веществами с получением суспензионного концентрата, из которого путем разбавления водой можно получать суспензии любого требуемого разбавления. С помощью таких разбавленных растворов можно обработать и защитить от заражения микроорганизмами живые растения, а также материал для размножения растений путем опрыскивания, полива или погружения.
Капсульная суспензия медленного высвобождения
Смешивают 28 частей комбинации с 2 частями ароматического растворителя и 7 частями смеси толуолдиизоцианат/полиметилен-полифенилизоцианат (8:1). Эту смесь эмульгируют в смеси из 1,2 части поливинилового спирта, 0,05 части пеногасителя и 51,6 части воды до получения частиц требуемого размера. К этой эмульсии добавляют смесь из 2,8 части 1,6-диаминогексана в 5,3 части воды. Смесь перемешивают до завершения реакции полимеризации. Полученную капсульную суспензию стабилизируют путем добавления 0,25 части загустителя и 3 частей диспергирующего средства. Состав капсульной суспензии содержит 28% активных ингредиентов. Средний диаметр капсул составляет 8-15 микрон. Полученный состав применяют в виде водной суспензии по отношению к семенам в устройстве, подходящем для данной цели.
Типы составов включают эмульсионный концентрат (ЕС), суспензионный концентрат (SC), суспоэмульсию (SE), капсульную суспензию (CS), диспергируемую в воде гранулу (WG), эмульгируемую гранулу (EG), эмульсию типа "вода в масле" (ЕО), эмульсию типа "масло в воде" (EW), микроэмульсию (ME), масляную дисперсию (OD), смешиваемый с маслом текучий состав (OF), смешиваемую с маслом жидкость (OL), растворимый концентрат (SL), суспензию для ультрамалообъемного внесения (SU), жидкость для ультрамалообъемного внесения (UL), технический концентрат (ТК), диспергируемый концентрат (DC), смачиваемый порошок (WP), растворимую гранулу (SG) или любой другой технически возможный состав в комбинации с приемлемыми для сельскохозяйственного применения вспомогательными веществами.
Примеры получения
"Mp" означает температуру плавления в °С. Свободные радикалы представляют собой метильные группы. 1Н ЯМР-измерения регистрировали на спектрометре Brucker 400 МГц, химические сдвиги приведены в ppm согласно стандарту TMS. Спектры измеряли в указанных дейтерированных растворителях. Для определения характеристик соединений применяли любой из приведенных ниже способов LCMS. Характеристические значения LCMS, полученные для каждого соединения, представляли собой время удерживания ("Rt", регистрируемое в минутах) и измеренное содержание молекулярного иона (М+Н)+ или (М-Н)-.
Способы LCMS и GCMS
Способ 1.
Спектры регистрировали на масс-спектрометре от Waters (одноквадрупольный масс-спектрометр SQD, SQDII), оснащенном источником электрораспыления (полярность: положительные и отрицательные ионы, напряжение на капилляре: 3,00 кВ, диапазон напряжений на конусе: 30 В, напряжение на экстракторе: 2,00 В, температура источника: 150°С, температура десольватации: 350°С, расход газа в конусе: 50 л/ч., расход газа для десольватации: 650 л/ч., диапазон масс: от 100 до 900 Да), и Acquity UPLC от Waters: насос для двухкомпонентных смесей, нагреваемый участок колонки, детектор на диодной матрице и детектор ELSD. Колонка: UPLC HSS Т3, 1,8 мкм, 30×2,1 мм от Waters, температура: 60°С, диапазон значений длины волны DAD (нм): от 210 до 500; градиент растворителя: А=вода+5% МеОН+0,05% НСООН, В=ацетонитрил+0,05% НСООН; градиент: 10-100% В за 1,2 мин; расход (мл/мин.) 0,85.
Способ 2.
Спектры регистрировали на масс-спектрометре от Waters (одноквадрупольный масс-спектрометр SQD, SQDII), оснащенном источником электрораспыления (полярность: положительные и отрицательные ионы), напряжение на капилляре: 3,00 кВ, диапазон напряжений на конусе: 30 В, напряжение на экстракторе: 2,00 В, температура источника: 150°С, температура десольватации: 350°С, расход газа в конусе: 50 л/ч., расход газа для десольватации: 650 л/ч., диапазон масс: от 100 до 900 Да), и Acquity UPLC от Waters: насос для двухкомпонентных смесей, нагреваемый участок колонки, детектор на диодной матрице и детектор ELSD. Колонка: UPLC HSS Т3, 1,8 мкм, 30×2,1 мм от Waters, температура: 60°С, диапазон значений длины волны DAD (нм): от 210 до 500; градиент растворителя: А=вода+5% МеОН+0,05% НСООН, В=ацетонитрил+0,05% НСООН; градиент: 10-100% В за 2,7 мин.; расход (мл/мин.) 0,85.
Способ 3.
Спектры регистрировали на масс-спектрометре от Waters (одноквадрупольный масс-спектрометр SQD, SQDII или ZQ), оснащенном источником электрораспыления (полярность: положительные и отрицательные ионы), напряжение на капилляре: 3,00 кВ, диапазон напряжений на конусе: 30 В, напряжение на экстракторе: 2,00 В, температура источника: 150°С, температура десольватации: 350°С, расход газа в конусе: 50 л/ч, расход газа для десольватации: 650 л/ч, диапазон масс: от 100 до 900 Да), и Acquity UPLC от Waters: насос для двухкомпонентных смесей, нагреваемый участок колонки, детектор на диодной матрице и детектор ELSD. Колонка: UPLC HSS Т3, 1,8 мкм, 30×2,1 мм от Waters, температура: 60°С, диапазон значений длины волны DAD (нм): от 210 до 500; градиент растворителя: А=вода+5% МеОН+0,05% НСООН, В=ацетонитрил+0,05% НСООН; градиент: 0-10% В за 2,5 мин; расход (мл/мин) 0,85.
Способ 4.
Спектры регистрировали на масс-спектрометре от Waters (одноквадрупольный масс-спектрометр SQD, SQDII), оснащенном источником электрораспыления (полярность: положительные и отрицательные ионы), напряжение на капилляре: 3,00 кВ, диапазон напряжений на конусе: 30 В, напряжение на экстракторе: 2,00 В, температура источника: 150°С, температура десольватации: 350°С, расход газа в конусе: 50 л/ч., расход газа для десольватации: 650 л/ч, диапазон масс: от 100 до 900 Да), и Acquity UPLC от Waters: насос для двухкомпонентных смесей, нагреваемый участок колонки, детектор на диодной матрице и детектор ELSD. Колонка: UPLC HSS Т3, 1,8 мкм, 30×2,1 мм от Waters, температура: 60°С, диапазон значений длины волны DAD (нм): от 210 до 500; градиент растворителя: А=вода+5% МеОН+0,05% НСООН, В=ацетонитрил+0,05% НСООН; градиент: 40-100% В за 1,2 мин; расход (мл/мин) 0,85.
Способ 5.
Спектры регистрировали на масс-спектрометре от Waters (масс-спектрометр Acquity SDS), оснащенном источником электрораспыления (полярность: переключатель положительной и отрицательной полярности, напряжение на капилляре: 3,00 кВ, напряжение на конусе: 41,00 В, температура источника: 150°С, расход газа для десольватации: 1000 л/ч, температура десольватации: 500°С, расход газа в конусе: 50 л/ч, диапазон масс: 110-800 Да, диапазон значений длины волны PDA: 210-400 нм. Колонка: Acquity UPLC HSS Т3 C18, длина 30 мм, диаметр 2,1 мм, размер частиц 1,8 мкм. Температура термостата колонки 40°С. Градиент растворителя: А=вода с 0,1% муравьиной кислоты: ацетонитрил (95:5 об./об.). В=ацетонитрил с 0,05% муравьиной кислоты. Градиент=0 мин. 90% А, 10% В; 0,2 мин. 50% А, 50% В; 0,7-1,3 мин. 0% А, 100% В; 1,4-1,6 мин. 90% А, 10% В. Расход: 0,6 мл/мин.
Пример H1. Получение 1-[5-(этилсульфонимидоил)-6-[7-метил-3-(трифторметил)имидазо[4,5-с]пиридазин-6-ил]-3-пиридил]циклопропанкарбонитрила (таблица Р, пример Р10)
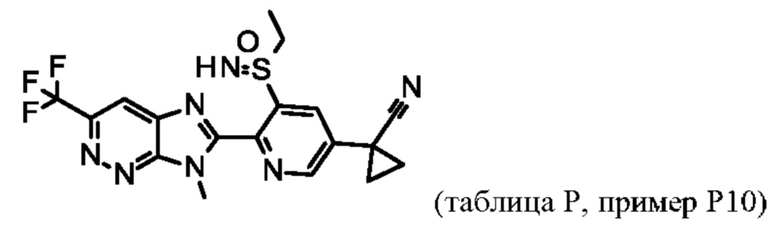
Стадия 1. Получение метил-5-(1-циано-2-этокси-2-оксоэтил)-3-этилсульфанилпиридин-2-карбоксилата
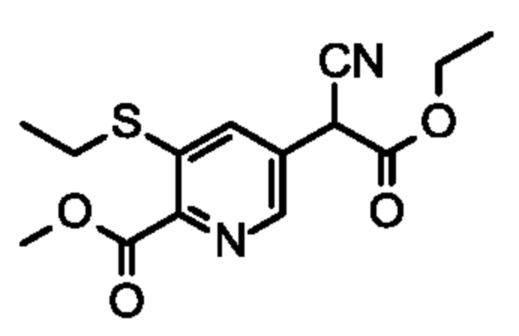
Метил-5-бром-3-этилсульфанилпиридин-2-карбоксилат, полученный, как описано в патенте WO 2017/089190 (32 г, 115,88 ммоль), растворяли в диметилсульфоксиде (350 мл). Затем последовательно при комнатной температуре добавляли этил-2-цианоацетат (18,5 мл, 173,82 ммоль), карбонат калия (40,442 г, 289,70 ммоль) и бромид тетрабутиламмония (3,81 г, 11,588 ммоль). Полученную суспензию перемешивали в течение одной ночи при 90°С и затем охлаждали до комнатной температуры. Добавляли воду и этилацетат, полученную смесь охлаждали до 0°С, и для подкисления реакционной смеси до рН 4-5 медленно добавляли хлористоводородную кислоту (2 М). Водный слой три раза экстрагировали этилацетатом. Объединенные органические слои высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Полученный неочищенный продукт нагревали при 80°С в этаноле (250 мл) в течение 1 часа. Полученный раствор охлаждали до 0°С, перемешивали 1 час и фильтровали. Осадок промывали охлажденным этанолом с получением метил-5-(1-циано-2-этокси-2-оксоэтил)-3-этилсульфанилпиридин-2-карбоксилата.
LCMS (способ 1): 309 (М+Н)+; время удерживания: 0,85 мин.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-D) δ ppm 1,33 (t, J=7,15 Гц, 3 Н) 1,45 (t, J=7,34 Гц, 3 Н) 2,98-3,05 (m, 2 Н) 4,04 (s, 3 Н) 4,28-4,35 (m, 2 Н) 4,84 (s, 1 Н) 7,83 (d, J=1,83 Гц, 1 Н) 8,49 (d, J=1,83 Гц, 1 Н).
Стадия 2. Получение метил-5-(цианометил)-3-этилсульфанилпиридин-2-карбоксилата
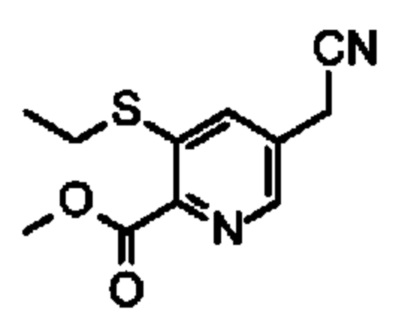
Метил-5-(1-циано-2-этокси-2-оксоэтил)-3-этилсульфанилпиридин-2-(7,3 г, 24 ммоль) растворяли в диметилсульфоксиде (70 мл). К нему последовательно при комнатной температуре добавляли NaCl (14 г, 240 ммоль) и воду (35 мл). Полученную суспензию перемешивали в течение 3 часов при 125°С. Реакционную смесь охлаждали до комнатной температуры, разбавляли с помощью 50 мл воды и 100 мл этилацетата. Водный слой три раза экстрагировали этилацетатом. Органические слои объединяли, высушивали над сульфатом натрия и концентрировали in vacuo. Неочищенный продукт очищали на силикагеле с получением метил-5-(цианометил)-3-этилсульфанилпиридин-2-карбоксилата.
LCMS (способ 1): 237 (М+Н)+; время удерживания: 0,72 мин.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-D) δ ppm 1,45 (t, J=7,52 Гц, 3 Н) 3,01 (q, J=7,34 Гц, 2 Н) 3,87 (s, 2 Н) 4,04 (s, 3 Н) 7,72 (d, J=1,83 Гц, 1 Н) 8,35-8,41 (m, 1 Н).
Стадия 3. Получение метил-5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбоксилата
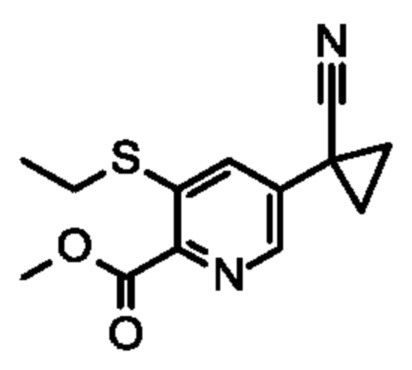
Метил-5-(цианометил)-3-этилсульфанилпиридин-2-карбоксилат (5 г, 21,16 ммоль) растворяли в ацетонитриле (170 мл) и обрабатывали карбонатом цезия (20,7 г, 63,48 ммоль) и 1,2-дибромэтаном (2,19 мл, 25,39 ммоль) при комнатной температуре. Полученную смесь перемешивали 3 ч. 30 часов при 80°С и затем при комнатной температуре в течение ночи. Реакционную смесь разбавляли водой и этилацетатом. Водный слой 3 раза экстрагировали этилацетатом. Объединенные органические слои промывали солевым раствором, высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo с получением неочищенного продукта, который очищали посредством хроматографии с получением метил-5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбоксилата.
LCMS (способ 1): 263 (М+Н)+; время удерживания: 0,85 мин.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-D) δ ppm 1,45 (t, J=7,34 Гц, 3 Н) 1,54-1,62 (m, 2 Н) 1,89-1,96 (m, 2 Н) 3,01 (q, J=7,34 Гц, 2 Н) 4,02 (s, 3 Н) 7,74 (d, J=2,20 Гц, 1 Н) 8,17 (d, J=1,83 Гц, 1 Н).
Стадия 4. Получение 5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбоновой кислоты
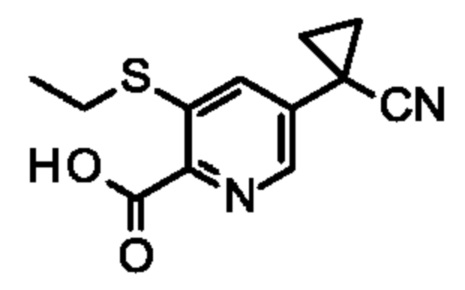
Метил-5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбоксилат (2,63 г, 10,0 ммоль) растворяли в тетрагидрофуране (50 мл) и воде (15 мл). Затем добавляли гидроксид лития (0,375 г, 15,0 ммоль), и реакционную смесь перемешивали в течение одной ночи при к.т. По прошествии этого времени добавляли дополнительную порцию гидроксида лития (0,160 г, 7,0 ммоль), и реакционную смесь перемешивали в течение дополнительных 2 часов при к.т. Реакционную смесь концентрировали in vacuo, и остаток растворяли в дихлорметане. Добавляли 1 М водную HCl, и водный слой (рН 1) 3 раза экстрагировали дихлорметаном. Объединенные органические слои высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo с получением 5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбоновой кислоты.
LCMS (способ 1): 249 (М+Н)+; время удерживания: 0,67 мин.
1Н ЯМР (400 МГц, DMSO-d Solvent) δ ppm 1,26 (t, J=7,34 Гц, 3 H) 1,70-1,78 (m, 2 H) 1,83-1,92 (m, 2 H) 3,03 (q, J=7,34 Гц, 2 H) 7,63 (d, J=2,20 Гц, 1 H) 8,37 (d, J=l,83 Гц, 1 H) 13,16-13,40 (m, 1 H).
Стадия 5. Получение 5-(1-цианоциклопропил)-3-этилсульфанил-М-[3-(метиламино)-6-(трифторметил)пиридазин-4-ил1пиридин-2-карбоксамида
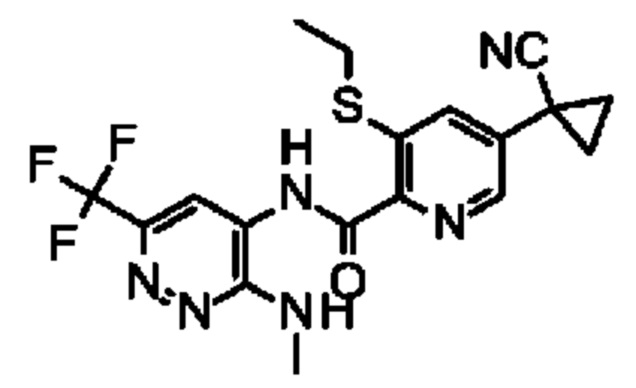
5-(1-Цианоциклопропил)-3-этилсульфанилпиридин-2-карбоновую кислоту (200 мг, 0,8055 ммоль) растворяли в дихлорметане (10 мл) и добавляли N,N-диметилформамид (10,0 мкл). В данную суспензию по каплям через шприц добавляли оксалилдихлорид (0,118 мл, 1,369 ммоль). Полученную желтоватую суспензию перемешивали при комнатной температуре. Через 1,5 ч. реакционную смесь концентрировали in vacuo с получением 5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбонилхлорида.
Свежий 5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбонилхлорид (250 мг, 0,9370 ммоль) растворяли в тетрагидрофуране (12 мл) и по каплям добавляли N,N-диэтилэтанамин (0,27 мл, 1,933 ммоль), затем при 0°С добавляли N3-метил-6-(трифторметил)пиридазин-3,4-диамин (651 мг, 3,222 ммоль) в тетрагидрофуране (12 мл). Полученную смесь перемешивали при комнатной температуре в течение 12 часов. Реакционную смесь затем выливали в воду (20 мл) и экстрагировали дихлорметаном (3 × 20 мл). Объединенные экстракты промывали солевым раствором (30 мл), высушивали с помощью сульфата натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали посредством хроматографии на силикагеле с получением N-[4-амино-6-(трифторметил)пиридазин-3-ил]-5-(1-цианоциклопропил)-3-этилсульфанил-N-метилпиридин-2-карбоксамида.
LCMS (способ 2): время удерживания: 1,04 минуты, 423 (М+Н)+.
Стадия 6. Получение 1-[5-этилсульфанил-6-[7-метил-3-(трифторметил)имидазо[4.5-с]пиридазин-6-ил]-3-пиридил]циклопропанкарбонитрила
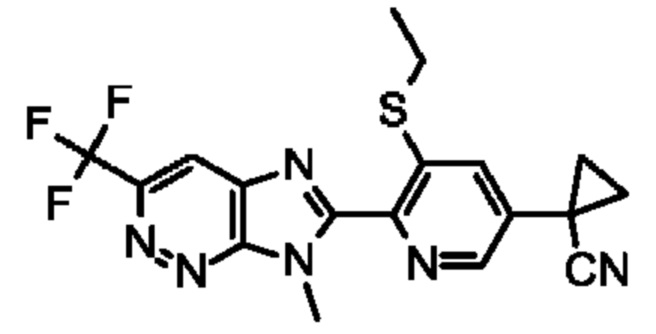
Смешивали 5-(1-цианоциклопропил)-3-этилсульфанил-N-[3-(метиламино)-6-(трифторметил)пиридазин-4-ил]пиридин-2-карбоксамид (240 мг, 0,5682 ммоль) и ледяную уксусную кислоту (3 мл) и перемешивали в течение одной ночи с обратным холодильником, а затем охлаждали до комнатной температуры. Уксусную кислоту удаляли при пониженном давлении, и полученный остаток растворяли в этилацетате, и повышали его основность с применением водного раствора бикарбоната. Водный слой экстрагировали этилацетатом (3 × 20 мл), и объединенный органический слой высушивали с помощью сульфата натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали посредством хроматографии на силикагеле с получением 1-[5-этилсульфанил-6-[7-метил-3-(трифторметил)имидазо[4,5-с]пиридазин-6-ил]-3-пиридил]циклопропанкарбонитрила.
LCMS (способ 2): время удерживания: 1,05 минуты, (М+Н)+ 405.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) d ppm 1,34-1,46 (m, 1 H) 1,38 (s, 2 H) 1,62 - 1,66 (m, 2 H) 1,89-2,02 (m, 2 H) 2,97-3,10 (m, 2 H) 4,26 (s, 3 H) 7,76-7,84 (m, 1 H) 8,22-8,27 (m, 1 H) 8,34-8,41 (m, 1 H).
Стадия 7. Получение 1-[5-(этилсульфонимидоил)-6-[7-метил-3-(трифторметил)имидазо[4,5-с]пиридазин-6-ил]-3-пиридил1циклопропанкарбонитрила (таблица Р, пример Р10)
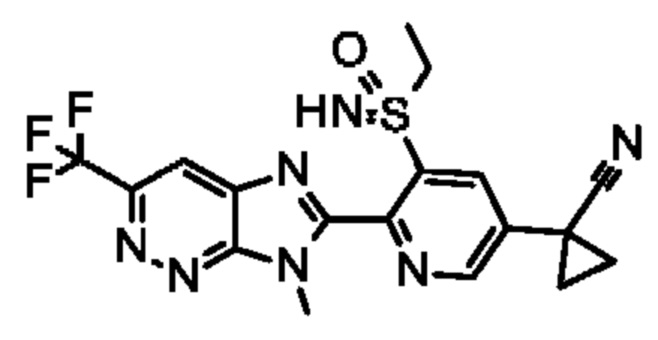 (таблица Р, пример Р10)
(таблица Р, пример Р10)
1-[5-Этилсульфанил-6-[7-метил-3-(трифторметил)имидазо[4,5-с]пиридазин-6-ил]-3-пиридил]циклопропанкарбонитрил (120 мг, 0,2967 ммоль) растворяли в метаноле (6 мл). Затем при комнатной температуре добавляли карбамат аммония (46 мг, 0,5935 ммоль) и (диацетоксииод)бензол (243 мг, 0,7418 ммоль). Полученная суспензия становилась раствором после нескольких минут, и ее перемешивали в течение 2 часов при комнатной температуре. Реакционную смесь гасили водой (20 мл) и экстрагировали дихлорметаном (3 × 20 мл). Объединенные органические слои промывали солевым раствором (30 мл), высушивали с помощью безводного сульфата натрия, фильтровали и концентрировали in vacuo. Остаток очищали посредством хроматографии на силикагеле с применением метанола и дихлорметана с получением 1-[5-(этилсульфонимидоил)-6-[7-метил-3-(трифторметил)имидазо[4,5-с]пиридазин-6-ил]-3-пиридил]циклопропанкарбонитрила.
LCMS (способ 2): время удерживания: 0,85 минуты, 436,36 (М+Н)+.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-d) d ppm 1,14-1,32 (m, 3 Н) 1,25-1,32 (m, 2 Н) 1,37-1,44 (m, 3 Н) 1,67-1,77 (m, 2 Н) 2,03-2,12 (m, 1 Н) 2,06-2,10 (m, 1 Н) 2,11 (br dd, J=3,48, 2,38 Гц, 1 H) 2,68-2,84 (m, 1 Н) 3,71-3,81 (m, 1 Н) 3,84-3,94 (m, 1 Н) 4,00-4,14 (m, 3 Н) 8,18 (s, 1 Н) 8,36 (d,J=2,20 Гц, 1 Н) 9,04 (d, J=2,20 Гц, 1 Н)
Пример Н2. Получение 1-[5-(этилсульфонимидоил)-6-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил1-3-пиридил1ииклопропанкарбонитрила (пример Рб, таблица Р)
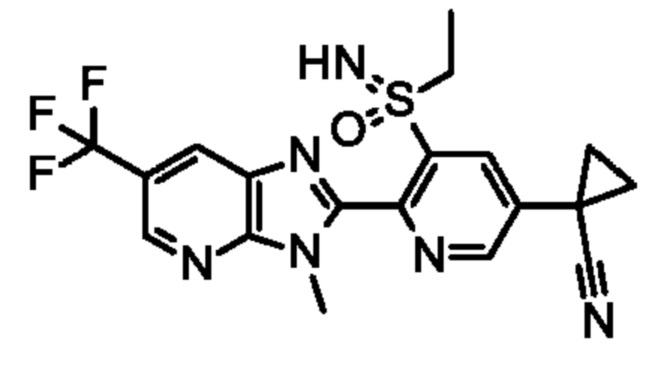 (пример Р6, таблица Р)
(пример Р6, таблица Р)
Стадия 1. Получение 5-(1-цианоциклопропил)-3-этилсульфанил-М-[2-(метиламино)-5-(трифторметил)-3-пиридил]пиридин-2-карбоксамида
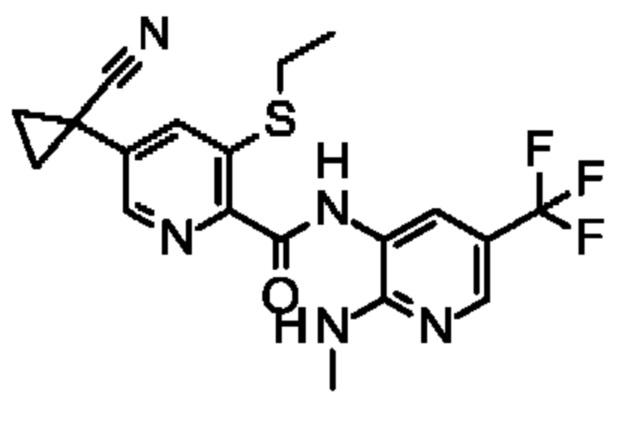
5-(1-Цианоциклопропил)-3-этилсульфанилпиридин-2-карбоновую кислоту (2,4 г, 9,7 ммоль) растворяли в дихлорметане (100 мл). Добавляли N,N-диметилформамид (10,0 мкл) с последующим добавлением по каплям оксалилдихлорида (1 мл, 12 ммоль) через шприц. Полученную желтоватую суспензию перемешивали при комнатной температуре в течение 1 часа, затем растворитель концентрировали in vacuo. Полученное твердое вещество растворяли в тетрагидрофуране (30 мл) и добавляли к раствору К2-метил-5-(трифторметил)пиридин-2,3-диамина (1,8 г, 9,7 ммоль) и N,N-диэтилэтанамина (3,3 мл, 23 ммоль) в тетрагидрофуране (75 мл) при 0°С. Полученную смесь перемешивали 30 минут при 0°С, затем 2 часа при комнатной температуре. Реакционную смесь обрабатывали насыщенным раствором NH4Cl и разбавляли этилацетатом. Водный слой 3 раза экстрагировали этилацетатом. Объединенные органические слои промывали солевым раствором, высушивали над Na2SO4, фильтровали и концентрировали in vacuo с получением 5-(1-цианоциклопропил)-3-этилсульфанил-Н-[2-(метиламино)-5-(трифторметил)-3-пиридил]пиридин-2-карбоксамида в виде неочищенного продукта, который применяли на следующей стадии без дополнительной очистки.
LCMS (способ 1): 422 (М+Н)+; время удерживания: 1,03 мин.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ ppm 1,48 (t, J=7,34 Гц, 3 H) 1,58-1,63 (m, 2 H) 1,93-1,99 (m, 2 H) 3,01 (q, J=7,34 Гц, 2 H) 3,09 (d, J=4,77 Гц, 3 H) 5,02 (br d, J=4,03 Гц, 1 H) 7,71 (d, J=2,20 Гц, 1 H) 7,94 (d, J=2,20 Гц, 1 H) 8,16 (d, J=2,20 Гц, 1 H) 8,36 (d, J=0,73 Гц, 1 H) 9,53-9,60 (m, 1 H).
Стадия 2. Получение 1-[5-этилсульфанил-6-[3-метил-6-(трифторметил)имидазо[4.5-b]пиридин-2-ил]-3-пиридил]циклопропанкарбонитрила
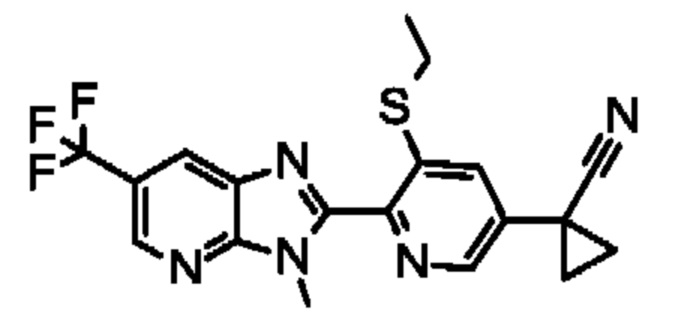
5-(1-Цианоциклопропил)-3-этилсульфанил-Н-[2-(метиламино)-5-(трифторметил)-3-пиридил]пиридин-2-карбоксамид (4,2 г, 10 ммоль) растворяли в уксусной кислоте (100 мл), и полученный раствор перемешивали 18 часов при 110°С. Уксусную кислоту удаляли in vacuo, и неочищенный продукт очищали посредством хроматографии на силикагеле с получением 1-[5-этилсульфанил-6-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]-3-пиридил]циклопропанкарбонитрила, точка плавления 142-144°С.
LCMS (способ 1): 404 (М+Н)+; время удерживания: 1,07 мин.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-d) δ ppm 1,40 (t, J=7,34 Гц, 3 Н) 1,59-1,64 (m, 2 Н) 1,90-1,97 (m, 2 Н) 3,03 (q, J=7,46 Гц, 2 Н) 4,07 (s, 3 Н) 7,77 (d, J=2,20 Гц, 1 Н) 8,35 (d, J=2,20 Гц, 1 Н) 8,42 (d, J=l,47 Гц, 1 Н) 8,73-8,78 (m, 1 Н).
Стадия 3. Получение 1-[5-(этилсульфонимидоил)-6-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]-3-пиридил]циклопропанкарбонитрила
(пример Р6, таблица Р)
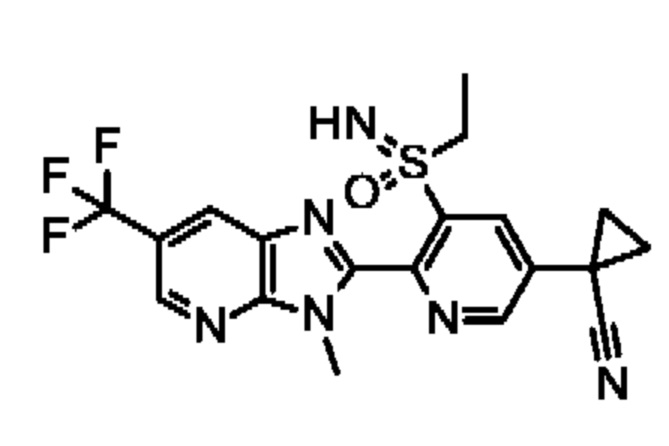 (пример Р6, таблица Р)
(пример Р6, таблица Р)
Образование сульфоксимина происходит аналогично тому, как описано в примере H1, стадия 7.
LCMS (способ 1): 435 (М+Н)+; время удерживания: 0,87 мин.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 1,44 (t, J=7,34 Гц, 3 Н) 1,75-1,80 (m, 2 Н) 2,02-2,08 (m, 2 Н) 3,94 (s, 3 Н) 3,94-4,26 (m, 2 Н) 8,33 (d, J=l,47 Гц, 1 Н) 8,39 (d, J=2,20 Гц, 1 Н) 8,79 (d, J=l,47 Гц, 1 Н) 9,06 - 9,09 (m, 1 Н).
Пример Н3. Получение 1-[5-(этилсульфонимидоил)-6-[5-метокси-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]-3-пиридил1циклопропанкарбонитрила
(пример Р8, таблица Р)
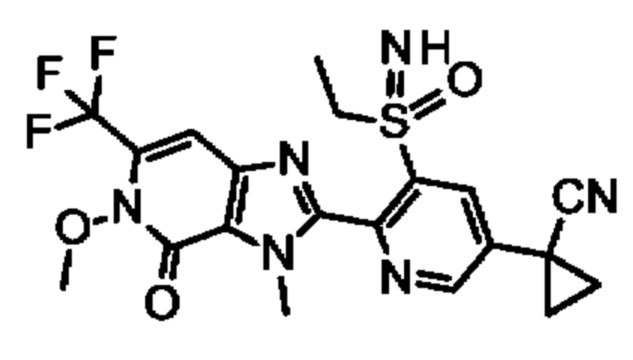 (пример Р8, таблица Р)
(пример Р8, таблица Р)
Стадия 1. Получение N-[4-бром-6-(дифторметил)-1-метокси-2-оксо-3-пиридил]-2,2,2-трифтор-N-метилацетамида
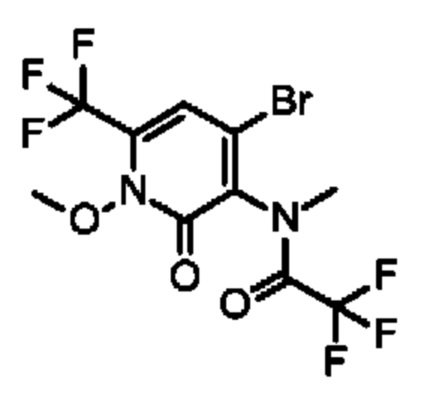
К раствору 4-бром-1-метокси-3-(метиламино)-6-(трифторметил)пиридин-2-она (5,0 г, 16,61 ммоль) в дихлорметане (100 мл) добавляли трифторуксусный ангидрид (7,09 мл, 49,82 ммоль) при комнатной температуре. Реакционную смесь перемешивали в течение 30 минут при комнатной температуре и затем концентрировали in vacuo. Добавляли воду (100 мл), затем водный насыщенный раствор карбоната калия (50 мл) и водный слой экстрагировали этилацетатом (100 мл). Органический слой промывали солевым раствором (100 мл), высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали на силикагеле с получением чистого N-[4-бром-6-(дифторметил)-1-метокси-2-оксо-3-пиридил]-2,2,2-трифтор-N-метилацетамида.
Данный материал использовали на следующей стадии без дополнительной очистки.
LCMS (способ 5): 397/399 (M+H)+, время удерживания 0,96 мин. 1Н ЯМР (400 МГц, CDCl3) 5 ppm 3,27 (s, 3Н), 4,16 (s, 3Н), 6,84 (s, 1Н).
Стадия 2. Получение N-[4-азидо-1-метокси-2-оксо-6-(трифторметил)-3-пиридил]-2.2,2-трифтор -N- метил ацетамида
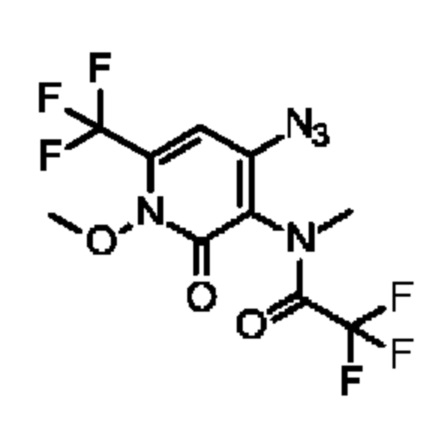
К раствору N-[4-бром-1-метокси-2-оксо-6-(трифторметил)-3-пиридил]-2,2,2-трифтор-N-метилацетамида (11,8 г, 29,7 ммоль) в N,N-диметилформамиде (110 мл) добавляли азид натрия (2,9 г, 44,6 ммоль) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение ночи. Отдельно повторяли указанную выше реакцию, затем объединенные реакционные смеси разбавляли холодной водой (500 мл) и экстрагировали этилацетатом (3 × 150 мл). Объединенные органические слои промывали водой (100 мл) и солевым раствором, высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo при температуре ниже 40°С с получением N-[4-азидо-1-метокси-2-оксо-6-(трифторметил)-3-пиридил]-2,2,2-трифтор-N-метил ацетамида. Данный материал использовали на следующей стадии без дополнительной очистки.
LCMS (способ 5): 360 (М+Н)+, время удерживания 0,90 мин.
1H ЯМР (400 МГц, CDCl3) δ ppm 3,23 (s, 3Н), 4,15 (s, 3Н), 6,40 (s, 1H).
Стадия 3. Получение 4-азидо-1-метокси-3-(метиламино)-6-(трифторметил)пиридин-2-она
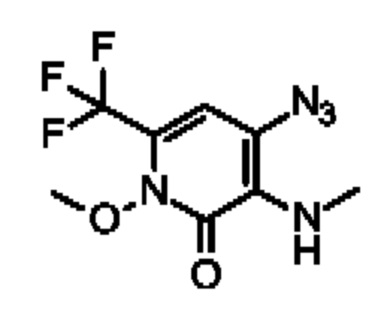
К раствору N-[4-азидо-1-метокси-2-оксо-6-(трифторметил)-3-пиридил]-2,2,2-трифтор-N-метил ацетамид а (4,6 г, 13,0 ммоль) в метаноле (100 мл) добавляли карбонат калия (4,7 г, 33,0 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи, затем разбавляли водой (150 мл). Водный слой экстрагировали этилацетатом (2 × 75 мл), объединенные органические слои промывали солевым раствором (150 мл), высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали на силикагеле (40% этилацетат в циклогексане) с получением 4-азидо-1-метокси-3-(метиламино)-6-(трифторметил)пиридин-2-она (2,2 г, 8,4 ммоль).
LCMS (способ Е): 264 (М+Н)+, время удерживания 0,94 мин.
1H ЯМР (400 МГц, CDCl3) δ ppm 3,18 (s, 3Н), 4,11 (s, 3Н), 6,46 (s, 1H).
Стадия 4. Получение 4-амино-1-метокси-3-(метиламино)-6-(трифторметил)пиридин-2-она
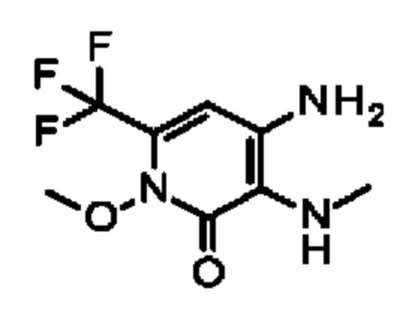
К раствору 4-азидо-1-метокси-3-(метиламино)-6-(трифторметил)пиридин-2-она (1,7 г, 6,5 ммоль) в тетрагидрофуране (50 мл) и воде (5 мл) при комнатной температуре добавляли трифенилфосфин (5,1 г, 19 ммоль), и полученную смесь перемешивали при комнатной температуре в течение 2 часов. Добавляли 2 М водный раствор хлористоводородной кислоты (9 мл, 18 ммоль, 2 моль/л), и перемешивание продолжали в течение ночи при комнатной температуре. Реакционную смесь концентрировали и гасили с применением водного насыщенного раствора карбоната калия (20 мл). Водный слой экстрагировали этилацетатом (2 х 75 мл), объединенные органические слои промывали солевым раствором (100 мл), высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Остаток очищали на силикагеле (50-60% этилацетат в циклогексане) с получением 4-амино-1-метокси-3-(метиламино)-6-(трифторметил)пиридин-2-она.
LCMS (способ 5): 238 (М+Н)+, время удерживания 0,18 мин.
1Н ЯМР (400 МГц, d6-DMSO) δ ppm 2,60 (s, 3Н), 3,98 (s, 3Н), 5,75 (s, 2Н), 6,42 (s, 1H).
Стадия 5. Получение 5-(1-цианоциклопропил)-3-этилсульфанил-N-[1-метокси-3-(метиламино)-2-оксо-6-(трифторметил)-4-пиридил1пиридин-2-карбоксамида и N-[4-амино-1-метокси-2-оксо-6-(трифторметил)-3-пиридил1-5-(1-цианоциклопропил)-3-этилсульфанил-М-метилпиридин-2-карбоксамида (изомерная смесь)
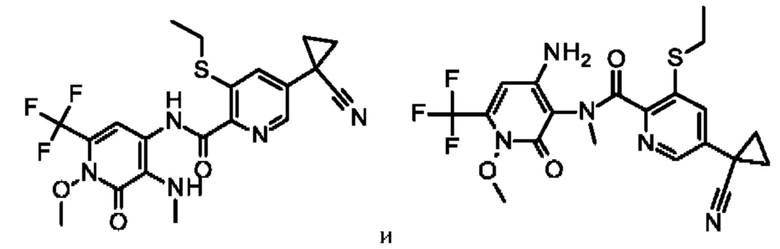
К суспензии 5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбоновой кислоты (400 мг, 1,61 ммоль) в дихлорметане (16 мл) по каплям добавляли каталитическое количество М,М-диметилформамида (2 капли) и оксалилхлорид (3,22 ммоль, 0,287 мл). Реакционную смесь перемешивали при комнатной температуре в течение 6 часов и растворитель удаляли in vacuo с получением 5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбонилхлорида.
Раствор указанного выше 5-(1-цианоциклопропил)-3-этилсульфанилпиридин-2-карбонилхлорида (428 мг, 1,60 ммоль) в сухом тетрагидрофуране (20 мл) медленно добавляли к смеси 4-амино-1-метокси-3-(метиламино)-6-(трифторметил)пиридин-2-она (456,6 мг, 1,92 ммоль) и триэтиламина (0,678 мл, 4,81 ммоль) в тетрагидрофуране (9,6 мл). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов, затем гасили водой и экстрагировали дихлорметаном (100 мл). Объединенные органические слои промывали водой и солевым раствором, высушивали с помощью безводного сульфата натрия и концентрировали in vacuo с получением требуемой изомерной смеси 5-(1 -цианоциклопропил)-3-этилсульфанил-N-[1-метокси-3-(метиламино)-2-оксо-6-(трифторметил)-4-пиридил]пиридин-2-карбоксамида и N-[4-амино-1-метокси-2-оксо-6-(трифторметил)-3-пиридил]-5-(1-цианоциклопропил)-3-этилсульфанил-N-метилпиридин-2-карбоксамида (750 мг, 1,60 ммоль). Данный материал использовали на следующей стадии без дополнительной очистки.
LCMS (способ 5): 468 (М+Н)+, время удерживания 0,86 мин.
Стадия 6. Получение 1-[5-этилсульфанил-6-[5-метокси-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил1-3-пиридил]пиклопропанкарбонитрила
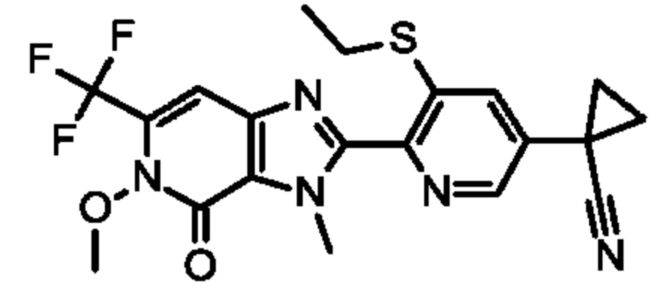
Раствор указанной выше изомерной смеси 5-(1-цианоциклопропил)-3-этилсульфанил-N-[1-метокси-3-(метиламино)-2-оксо-6-(трифторметил)-4-пиридил]пиридин-2-карбоксамида и N-[4-амино-1-метокси-2-оксо-6-(трифторметил)-3-пиридил]-5-(1-цианоциклопропил)-3-этилсульфанил-N-метилпиридин-2-карбоксамида (750 мг, 1,60 ммоль) в уксусной кислоте (4,8 мл) нагревали до 100°С в течение 48 часов. После охлаждения до комнатной температуры реакционную смесь концентрировали in vacuo. Остаток выливали в воду и экстрагировали этилацетатом (3 × 100 мл), объединенные органические слои промывали солевым раствором, высушивали над сульфатом натрия и концентрировали in vacuo. Неочищенный продукт очищали посредством хроматографии на силикагеле (40% этилацетат в циклогексане) с получением требуемого продукта, представляющего собой 1-[5-этилсульфанил-6-[5-метокси-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]-3-пиридил]циклопропанкарбонитрил (350 мг), в виде твердого вещества.
LCMS (способ Е): 450 (М+Н)+, время удерживания 1,03 мин.
1Н ЯМР (400 МГц, CDCl3) δ ppm 1,37 (t, 3Н), 1,59 (m, 2Н), 1,93 (m, 2Н), 3,01 (q, 2Н), 4,20 (s, 3Н), 4,21 (s, 3Н), 7,25 (s, 1Н), 7,76 (d, J=2,0 Гц, 1H), 8,32 (d, J=2,0 Гц, 1H).
Стадия 7. Получение 1-[5-(этилсульфонимидоил)-6-[5-метокси-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил1-3-пиридил]циклопропанкарбонитрила
(пример Р8, таблица Р)
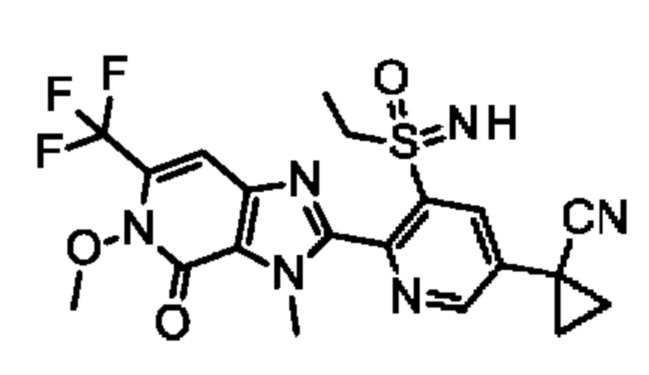 (пример Р8, таблица Р)
(пример Р8, таблица Р)
Образование сульфоксимина происходит аналогично тому, как описано в примере H1, стадия 7.
LCMS (способ 5): 481 (М+Н)+; время удерживания: 0,85 мин.
1Н ЯМР (400 МГц, DMSO-d6) δ ppm 1,14 (t, J=7,40 Гц, 3 H) 1,83-1,94 (m, 2 Н) 1,97-2,06 (m, 2 Н) 3,44-3,66 (m, 2 Н) 3,86 (s, 3 Н) 4,12 (s, 3 Н) 4,56 (s, 1 Н) 7,41 (s, 1 Н) 8,38 (d, J=2,20 Гц, 1 H) 8,90 (d, J=2,20 Гц, 1 H).
Пример Н4. Получение 1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-c]пиридин-2-ил]фенил]циклопропанкарбонитрила
(пример Р9, таблица Р)
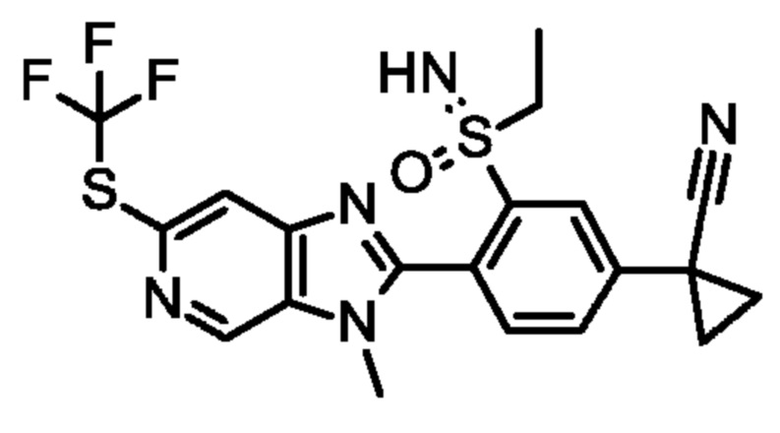 (пример Р9, таблица Р)
(пример Р9, таблица Р)
Стадия 1. Получение N-[4-амино-6-(трифторметилсульфанил)-3-пиридил1-4-бром-2-этилсульфанил-N-метилбензамида
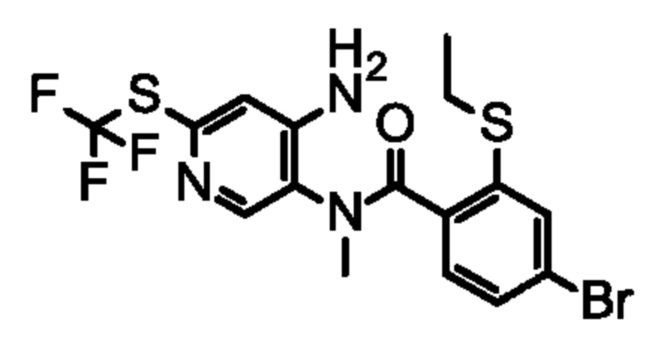
В атмосфере аргона 4-бром-2-этилсульфанилбензойную кислоту (полученную, как описано в патенте WO 2016/120182 (1,96 г, 7,51 ммоль)) суспендировали в дихлорметане (30 мл) и добавляли 2 капли DMF. По каплям добавляли оксалилдихлорид (1,24 г, 0,851 мл, 9,76 ммоль), и наблюдали выделение газа. Смесь перемешивали 4 часа при комнатной температуре и затем концентрировали in vacuo с получением 4-бром-2-этилсульфанилбензоилхлорида в виде продукта, полученного на первой стадии. В атмосфере аргона только что полученный неочищенный 4-бром-2-этилсульфанилбензоилхлорид (2,07 г, 7,39 ммоль) растворяли в тетрагидрофуране (20 мл) и добавляли N3-метил-6-(трифторметилсульфанил)пиридин-3,4-диамин, полученный, как описано в патенте WO 2016/169886 (1,50 г, 6,72 ммоль). Полученную смесь перемешивали в течение одной ночи при комнатной температуре, затем 8 часов при 70°С. После охлаждения при комнатной температуре добавляли бикарбонат натрия и воду. Водный слой 2 раза экстрагировали этилацетатом. Объединенный органический слой высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo с получением смеси, содержащей N-[4-амино-6-(трифторметилсульфанил)-3-пиридил]-4-бром-2-этилсульфанил-N-метилбензамид.
LCMS (способ 1): 450 (М+Н)+; время удерживания: 1,14 мин.
Стадия 2. Получение 2-(4-бром-2-этилсульфанилфенил)-3-метил-6-(трифторметилсульфанил)имидазо[4,5-c]пиридина
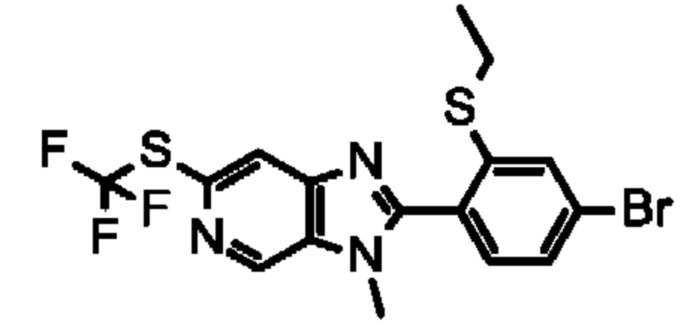
N-[4-Амино-6-(трифторметилсульфанил)-3-пиридил]-4-бром-2-этилсульфанил-N-метилбензамид (3,4 г, 5,1 ммоль) растворяли в уксусной кислоте (51 мл). Полученный раствор перемешивали в течение одной ночи при 120°С и затем охлаждали при комнатной температуре. Уксусную кислоту удаляли при пониженном давлении, и неочищенный продукт очищали посредством хроматографии на силикагеле. Полученную смесь растворяли в этилацетате, промывали бикарбонатом, высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo с получением 2-(4-бром-2-этилсульфанилфенил)-3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридина.
LCMS (способ 1): 450 (М+Н)+; время удерживания: 1,14 мин.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 1,29 (t, J=7,34 Гц, 3 Н) 2,92 (q, J=7,34 Гц, 2 Н) 3,79 (s, 3 Н) 7,32 (d, J=8,07 Гц, 1 Н) 7,50 (dd, J=8,07, 1,83 Гц, 1 Н) 7,61 (d, J=l,83 Гц, 1 Н) 8,15-8,17 (m, 1 Н) 8,90 (d, J=l,10 Гц, 1 Н).
Стадия 3. Получение 4-[3-этилсульфанил-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил]Фенил]изоксазола
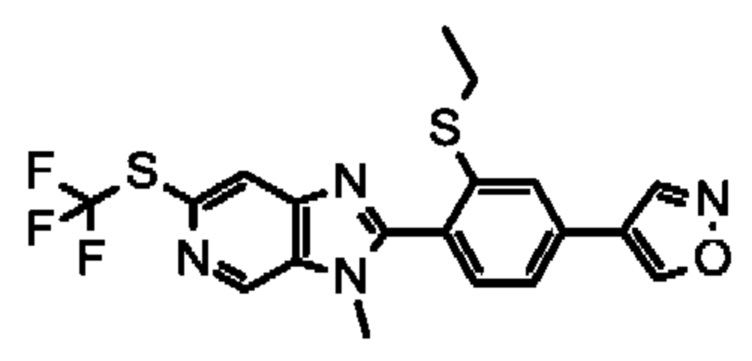
Во флакон для микроволновой обработки в атмосфере аргона добавляли DMSO (1,11 мл) и воду (0,53 мл), и раствор продували аргоном в течение 5 мин. Затем добавляли 2-(4-бром-2-этилсульфанилфенил)-3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин (0,2 г, 0,446 ммоль), пинаколовый сложный эфир 4-изоксазолбороновой кислоты (0,104 г, 0,535 ммоль) и фторид калия (0,077 г, 1,33 ммоль). Добавляли трифенилфосфан дихлорпалладия (0,0031 г, 0,0044 ммоль), полученную смесь продували аргоном в течение 5 мин., перемешивали в течение 40 мин. при 90°С в системе для микроволнового обучения, охлаждали при комнатной температуре и затем выливали в ледяную воду. Водный слой 3 раза экстрагировали дихлорметаном. Затем молочно-белый водный слой фильтровали, и полученное твердое вещество растворяли в дихлорметане и добавляли в органический слой. Объединенные органические слои высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Полученное масло промывали водой. Образованный в воде осадок фильтровали, затем снова растворяли в дихлорметане и растворитель концентрировали in vacuo с получением 4-[3-этилсульфанил-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил]фенил]изоксазола, который применяли как таковой для следующей стадии.
LCMS (способ 1): 437 (М+Н)+; время удерживания: 0,95 мин.
Стадия 4. Получение 2-[3-этилсульфанил-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил] фенил]ацетонитрила
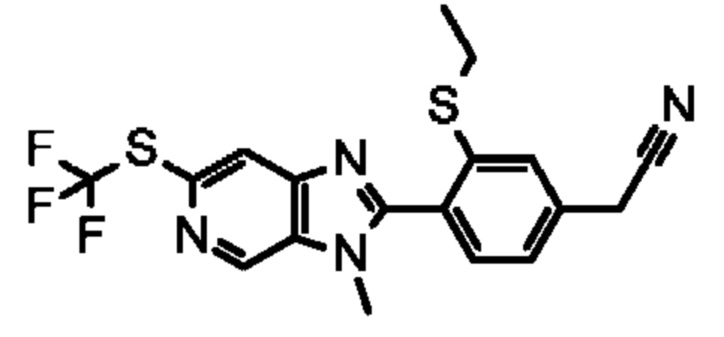
4-[3-Этилсульфанил-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил]фенил]изоксазол (236 мг, 0,3785 ммоль, 70 мас. %) растворяли в метаноле (2 мл) и воде (1,14 мл) и добавляли фторид калия (1,14 мл, 1,135 ммоль). Реакционную смесь перемешивали в течение 3 часов при 90°С. Темно-красную реакционную смесь (суспензию) фильтровали, промывали дихлорметаном и концентрировали in vacuo. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем с получением 2-[3-этилсульфанил-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил]фенил]ацетонитрила.
LCMS (способ 1): 409 (М+Н)+; время удерживания: 0,98 мин.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 1,29 (t, J=7,34 Гц, 4 Н) 2,93 (q, J=7,34 Гц, 2 Н) 3,80 (s, 3 Н) 3,89 (s, 2 Н) 7,34 (dd, J=7,89, 1,65 Гц, 1 Н) 7,47-7,48 (m, 1 Н) 7,48-7,51 (m, 1 Н) 8,16-8,18 (m, 1 Н) 8,92 (d, J=0,73 Гц, 1 Н).
Стадия 5. Получение 1-[3-этилсульфанил-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-c] пиридин-2-ил]фенил]циклопропанкарбонитрила
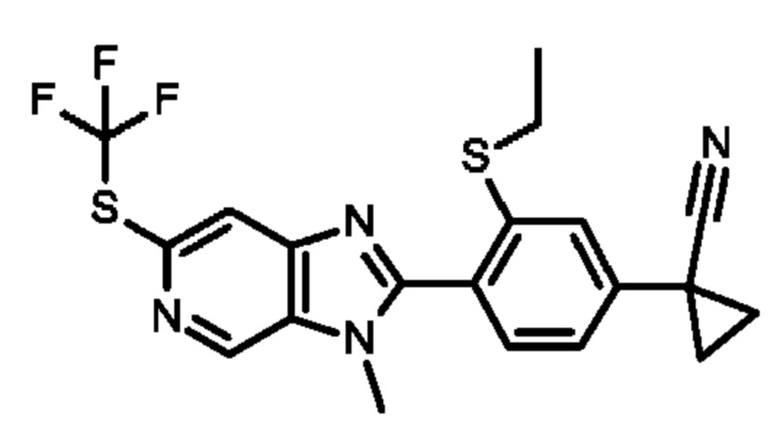
1-[3-Этилсульфанил-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрил (0,108 г, 0,2644 ммоль) растворяли в ацетонитриле (1,322 мл). Затем добавляли карбонат дицезия (0,2584 г, 0,7931 ммоль) и 1,2-дибромэтан (0,1490 г, 0,0683 мл, 0,7931 ммоль). Реакционную смесь перемешивали в системе для микроволнового облучения при 100°С в течение 2 часов. Реакционную смесь концентрировали in vacuo. Остаток растворяли в этилацетате и промывали несколько раз водой и солевым раствором. Органический слой высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали посредством хроматографии на силикагеле с получением 1-[3-этилсульфанил-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрила.
LCMS (способ 1): 435 (М+Н)+; время удерживания: 1,04 мин.
1H ЯМР (400 МГц, Хлороформ) δ ppm 1,28 (t, J=7,34 Гц, 4 Н) 1,55 (br d, J=2,20 Гц, 2 Н) 1,86 - 1,91 (т, 2 Н) 2,93 (q, J=7,58 Гц, 2 Н) 3,79 (s, 3 Н) 7,17 (dd, J=7,89, 2,02 Гц, 1 Н) 7,44 - 7,47 (т, 1 Н) 7,52 (d, J=l,83 Гц, 1 Н) 8,16 (d, J=0,73 Гц, 1 Н) 8,91 (d, J=0,73 Гц, 1 Н).
Стадия 6. Синтез 1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-c]пиридин-2-ил]фенил]циклопропанкарбонитрила
(пример Р9, таблица Р)
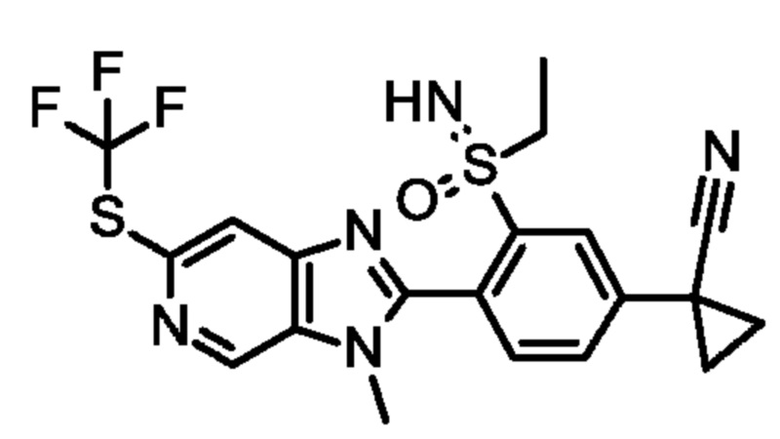 (пример Р9, таблица Р)
(пример Р9, таблица Р)
Образование сульфоксимина осуществляют, как описано в примере H1, стадия 7.
LCMS (способ 1): 466 (М+Н)+; время удерживания: 0,86 мин.
Пример Н5. Синтез 1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрила
(пример Р13, таблица Р)
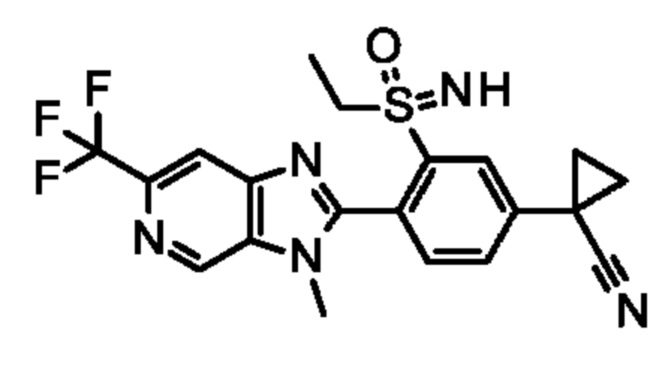 (пример Р13, таблица Р)
(пример Р13, таблица Р)
Стадия 1. Получение 1-[3-этилсульфанил-4-[3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрила
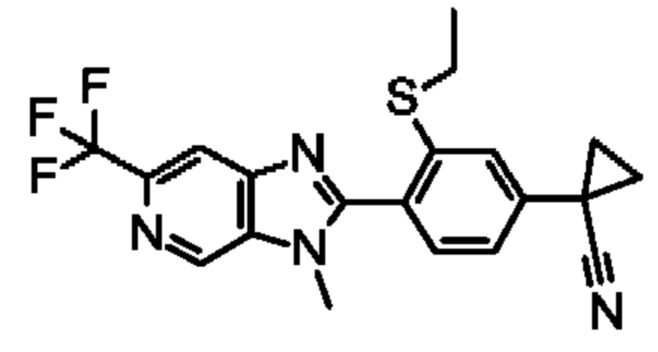
К смеси 2-(4-бром-2-этилсульфанилфенил)-3-метил-6-(трифторметил)имидазо[4,5-с]пиридина, полученного, как описано в патенте WO 2016/030229 (0,5 г, 1,201 ммоль), Pd2dba3 (0,056 г, 0,060 ммоль) и BINAP (0,077 г, 0,120 ммоль) в тетрагидрофуране (1,2 мл) добавляли циклопропанкарбонитрил (0,090 г, 1,32 ммоль) и циклопропилметилэфир (1,20 мл) в атмосфере аргона при к. т.Смесь охлаждали до -25°С, и по каплям добавляли бис(триметилсилил)амид лития (1,3 мл, 1,321 ммоль) при -25°С в атмосфере аргона. Смесь перемешивали при 80°С в течение 2 часов. После охлаждения при комнатной температуре смесь фильтровали через слой целита, который промывали этилацетатом. Фильтрат промывали водой. Водный слой отделяли и дважды экстрагировали этилацетатом. Органические слои объединяли, высушивали над безводным сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали посредством хроматографии на силикагеле с получением 1-[3-этилсульфанил-4-[3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрила.
LCMS (способ 1): 403 (М+Н)+; время удерживания: 1,00 мин.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 1,27 (t, J=7,34 Гц, 3 Н) 1,52 - 1,57 (m, 2 Н) 1,86-1,91 (m, 2 Н) 2,91 (q, J=7,46 Гц, 2 Н) 3,82 (s, 3 Н) 7,18 (dd, J=8,07, 1,83 Гц, 1 Н) 7,46 (d, J=8,07 Гц, 1 Н) 7,52 (d, J=l,83 Гц, 1 Н) 8,14 (d, J=0,73 Гц, 1 Н) 8,95 (s, 1 Н).
Стадия 2. Синтез 1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрила (пример Р13. таблица Р)
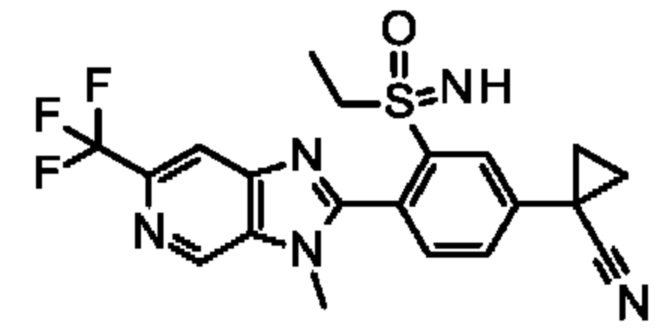 (пример Р13, таблица Р)
(пример Р13, таблица Р)
Требуемый продукт получали с применением стандартной процедуры, описанной для стадии 7, пример Н1.
LCMS (способ 1): 434 (М+Н)+; время удерживания: 0,83 мин.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 1,28 (t, J=7,34 Гц, 3 Н) 1,63 - 1,68 (m, 2 Н) 1,96 -
2.01 (m, 2 Н) 3,42-3,62 (m, 2 Н) 3,75 (s, 3 Н) 7,56 (d, J=8,07 Гц, 1 Н) 7,89 (dd, J=7,89,
2.02 Гц, 1 Н) 8,05 (d, J=l,83 Гц, 1 Н) 8,10 (d, J=0,73 Гц, 1 Н) 8,93-8,96 (m, 1 Н).
Пример Н5. Синтез 1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]фенил]циклопропанкарбонитрила (пример Р15, таблица Р)
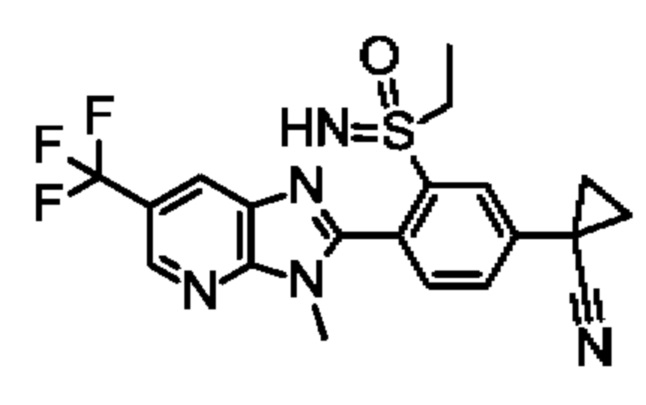 (пример Р15, таблица Р)
(пример Р15, таблица Р)
Стадия 1. Синтез метил-2-этилсульфанил-4-изоксазол-4-илбензоата
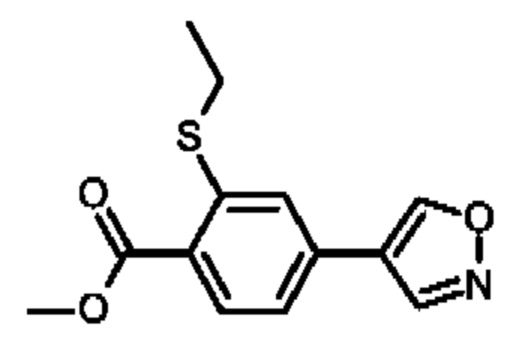
К раствору метил-4-бром-2-этилсульфанилбензоата (WO 2016/023954) (250 мг, 0,91 ммоль) в диметилсульфоксиде (8 мл) в атмосфере аргона добавляли воду (4 мл), пинаколовый сложный эфир 4-изоксазолбороновой кислоты (213 мг, 1,09 ммоль) и фторид калия (158 мг, 2,73 ммоль). Густую реакционную смесь продували аргоном в течение 5 минут, затем добавляли дихлорид бис(трифенилфосфин)палладия(II) (6,4 мг, 0,009 ммоль). Сосуд герметично закрывали, и смесь перемешивали в микроволновой печи при 90°С в течение 40 минут. Реакционную смесь выливали в ледяную воду, и полученную желтоватую суспензию фильтровали и промывали с помощью холодной воды. Данное твердое вещество растворяли в дихлорметане, раствор высушивали над сульфатом натрия и выпаривали до сухого состояния под вакуумом с получением метил-2-этилсульфанил-4-изоксазол-4-илбензоата в виде желтоватого твердого вещества. Данный материал использовали на следующей стадии без дополнительной очистки.
LCMS (способ 1): 262 (М-Н)-, время удерживания 0,88 мин.
Стадия 2. Синтез метил-4-(цианометил)-2-этилсульфанилбензоата
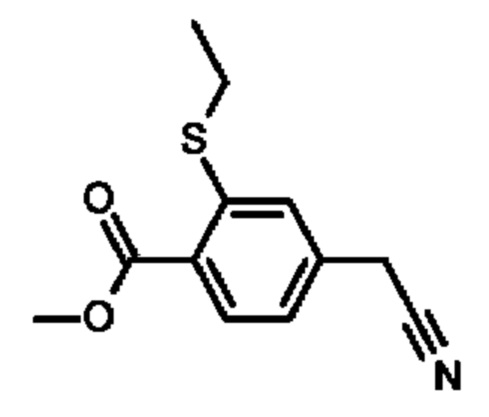
К раствору метил-2-этилсульфанил-4-изоксазол-4-илбензоата (760 мг, 2,89 ммоль) в метаноле (15 мл) добавляли 1 М раствор фторида калия в воде (8,66 мл, 8,66 ммоль). Реакционную смесь перемешивали с обратным холодильником в течение 3 часов. После охлаждения суспензию фильтровали и фильтрат концентрировали in vacuo. Остаток очищали с помощью Combiflash на силикагеле с получением метил-4-(цианометил)-2-этилсульфанилбензоата в виде смолы.
LCMS (способ 5): 236 (М+Н)+, время удерживания 0,90 мин.
1Н ЯМР (400 МГц, CDCl3) δ ppm 1,42 (t, 3Н), 2,99 (q, 2Н), 3,80 (s, 2Н), 3,93 (s, 3Н), 7,10 (dd, 1H), 7,28 (d, 1H), 7,99 (d, 1H).
Стадия 3. Синтез метил-4-(1-цианоциклопропил)-2-этилсульфанилбензоата
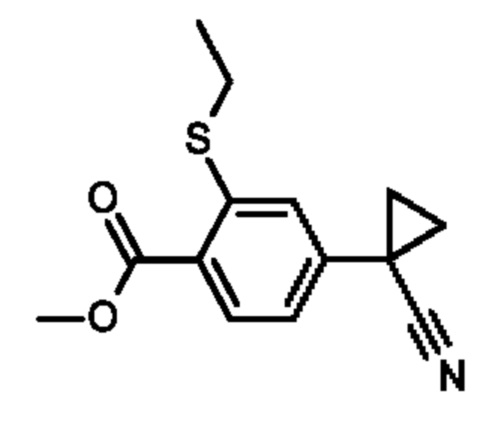
К раствору метил-4-(цианометил)-2-этилсульфанилбензоата (300 мг, 1,275 ммоль) в ацетонитриле (15 мл) добавляли карбонат цезия (1,24 г, 3,825 ммоль) и 1,2-дибромэтан (719 мг, 3,825 ммоль). Реакционную смесь перемешивали с обратным холодильником в течение 90 минут. После охлаждения суспензию фильтровали и фильтрат концентрировали in vacuo. Остаток очищали с помощью Combiflash на силикагеле с получением метил-4-(цианометил)-2-этилсульфанилбензоата в виде масла.
LCMS (способ 1): 262 (М+Н)+, время удерживания 0,98 мин.
1Н ЯМР (400 МГц, CDCl3) δ ppm 1,43 (t, 3Н), 1,48 (m, 2Н), 1,82 (m, 2Н), 3,01 (q, 2Н), 3,92 (s, 3Н), 6,88 (dd, 1Н), 7,35 (d, 1H), 7,94 (d, 1H).
Стадия 4. Синтез 4-(1-цианоциклопропил)-2-этилсульфанилбензойной кислоты
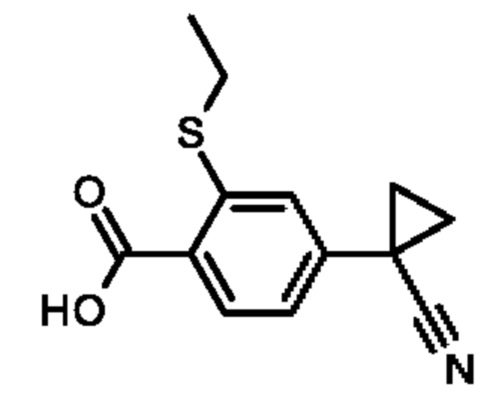
К раствору метил-4-(1-цианоциклопропил)-2-этилсульфанилбензоата (198 мг, 0,758 ммоль) в смеси тетрагидрофурана (9 мл) и воды (3 мл) при 0-5°С добавляли гидроксид лития (1,5 экв., 1,137 ммоль), и реакционную смесь перемешивали при комнатной температуре в течение ночи. Раствор концентрировали in vacuo, остаток разбавляли трет-бутилметиловым эфиром (10 мл) и подкисляли с помощью 1 М водного раствора хлористоводородной кислоты (10 мл). Органический слой отделяли, водный слой экстрагировали с помощью трет-бутилметилового эфира, объединенные органические слои промывали с помощью воды и солевого раствора, высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo с получением 4-(1-цианоциклопропил)-2-этилсульфанилбензойной кислоты в виде твердого вещества. Данный материал использовали на следующей стадии без дополнительной очистки.
LCMS (способ 5): 246 (М-Н)-, время удерживания 0,83 мин.
1Н ЯМР (400 МГц, CDCl3) δ ррт 1,44 (t, 3Н), 1,51 (т, 2Н), 1,85 (т, 2Н), 3,03 (q, 2Н), 6,90 (dd, 1H), 7,41 (d, 1H), 8,10 (d, 1H).
Стадия 5. Получение 1-[3-этилсульфанил-4-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]фенил]циклопропанкарбонитрила
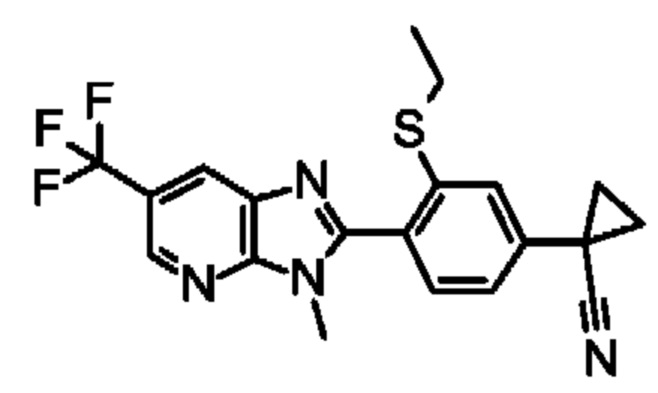
4-(1-Цианоциклопропил)-2-этилсульфанилбензойную кислоту (1,7 г, 6,9 ммоль) растворяли в нитробензоле (14 мл), и добавляли N2-метил-5-(трифторметил)пиридин-2,3-диамине (WO 2017/043342) (1,6 г, 1,2 экв.) после медленного добавления фосфорилхлорида (1,6 мл, 17 ммоль) при комнатной температуре. Полученный раствор нагревали при 120°С в течение 7 часов, контролировали с помощью TLC и LC-MS.
Реакционную массу гасили 30% раствором гидроксида натрия, и добавляли воду (100 мл). Водный слой экстрагировали этилацетатом (3× 100 мл). Объединенный органический слой высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали хроматографией с получением 1-[3-этилсульфанил-4-[3-метил-6-(трифторметил)имидазо[4,5-b] пиридин-2-ил]фенил]циклопропанкарбонитрила.
LCMS (способ 2): 403 (М+Н)+; время удерживания: 1,18 мин.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-d) d ppm 1,26 (t, J=7,34 Гц, 3 H) 1,44-1,61 (m, 2 Н) 1,80 - 1,92 (m, 2 Н) 2,91 (q, J=7,42 Гц, 2 H) 3,78 (s,3 Н) 7,16 (dd, J=8,01, 1,77 Гц, 1 H) 7,44 (d, J=7,60 Гц, 1 H) 7,50 (s, 1 Н) 8,33 (s, 1 Н) 8,72 (s, 1 Н).
Стадия 6. Получение 1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]фенил]циклопропанкарбонитрила (пример Р15, таблица Р)
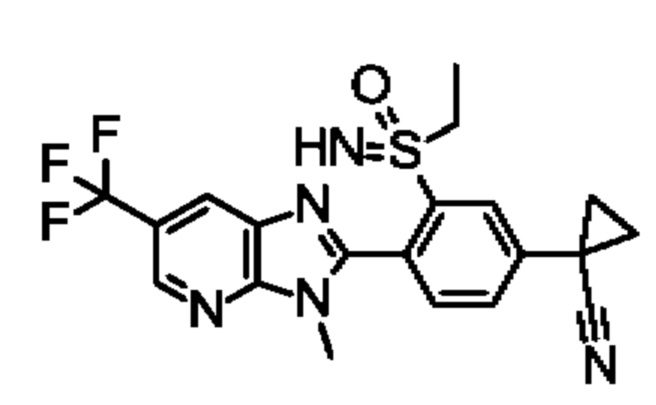 (пример Р15, таблица Р)
(пример Р15, таблица Р)
Требуемый продукт получали с применением стандартной процедуры, описанной в примере H1, стадии 7.
LCMS (способ 1): 434 (М+Н)+; время удерживания: 0,88 мин.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 1,28 (t, J=7,34 Гц, 4 Н) 1,63-1,68 (m, 2 Н) 1,96-2.01 (m, 2 Н) 3,41-3,62 (m, 2 Н) 3,75 (s, 3 Н) 7,56 (d, J=8,07 Гц, 1 Н) 7,89 (dd, J=7,89, 2.02 Гц, 1 Н) 8,05 (d, J=l,83 Гц, 1 Н) 8,10 (d, J=0,73 Гц, 1 Н) 8,94 - 8,97 (m, 1 Н).
Пример Н6. Синтез [5-циклопропил-2-[7-(трифторметил)имидазо[1.2-b]пиридазин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (пример Р16, таблица Р)
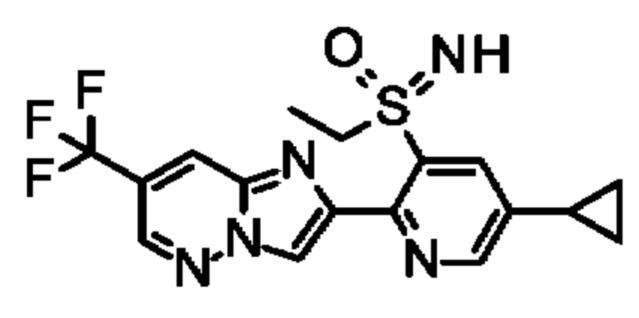 (пример Р16, таблица Р).
(пример Р16, таблица Р).
Стадия 1. Получение 2-бром-1-(5-бром-3-этилсульфанил-2-пиридил)этанона
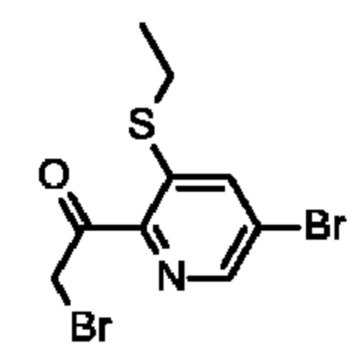
Образец 1-(5-бром-3-этилсульфанил-2-пиридил)этанона (получение описано в WO 2016/071214 (1 г, 3,8439 ммоль) суспендировали в ацетонитриле (3 мл) и хлороформе (3 мл). Добавляли дибромид меди (1,7171 г, 7,6879 ммоль), и реакционную смесь нагревали до 70°С и перемешивали в течение 22 часов, после чего LC-MS показывала завершение реакции. Реакционную смесь фильтровали через целит и с использованием дихлорметана. Фильтрат концентрировали in vacuo, и полученный остаток очищали с помощью хроматографии на силикагеле с получением 2-бром-1-(5-бром-3-этилсульфанил-2-пиридил)этанона.
LCMS (способ 1): время удерживания 1,10 min; 339/341 (М+Н)+.
1Н ЯМР (400 МГц, DMSO) δ ppm 1,28 (t, J=7,34 Гц, 3 Н) 3,06 (q, J=7,34 Гц, 2 Н) 4,93 (s, 2 Н) 8,11 (d, J=l,83 Гц, 1 Н) 8,58-8,60 (m, 1 Н).
Стадия 2. Получение 2-(5-бром-3-этилсульфанил-2-пиридил)-7-(трифторметил)имидазо[1,2-b]пиридазина
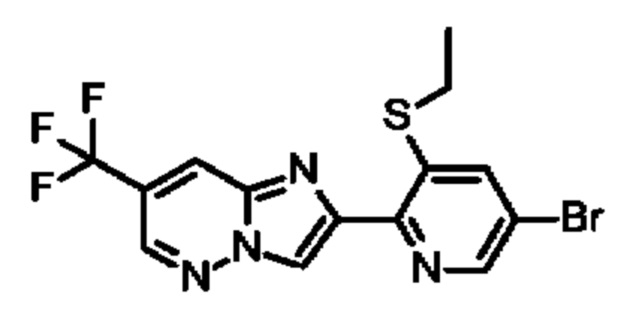
В трехгорлой колбе, оснащенной обратным холодильником, 2-бром-1-(5-бром-3-этилсульфанил-2-пиридил)этанон (0,50 г, 1,5 ммоль) и 5-(трифторметил)пиридазин-3-амин (CAS [1211591-88-6]) (0,27 г, 1,5 ммоль) суспендировали в ацетонитриле (11 мл) и добавляли оксид магния (0,12 г, 2,9 ммоль). Полученную смесь нагревали до 90°С и перемешивали в течение ночи. Реакционную смесь фильтровали, и фильтрат концентрировали in vacuo. Полученное твердое вещество растворяли в этилацетате и промывали один раз насыщ. раств. NaHCO3. Органический слой предварительно высушивали солевым раствором, высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали с помощью хроматографии на силикагеле с получением 2-(5-бром-3-этилсульфанил-2-пиридил)-7-(трифторметил)имидазо[1,2-b]пиридазина.
LCMS (способ 1): время удерживания 1,15 min; 403/405 (М+Н)+.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 1,44 (t, J=7,34 Гц, 3 Н) 3,04 (q, J=7,34 Гц, 2 Н) 7,82 (d, J=l,83 Гц, 1 Н) 8,33 - 8,39 (m, 1 Н) 8,57 (dd, J=3,85, 2,02 Гц, 2 Н) 8,81-8,86 (m, 1 Н).
Стадия 3. Получение 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-7-(трифторметил)имидазо [1,2-b]пиридазина
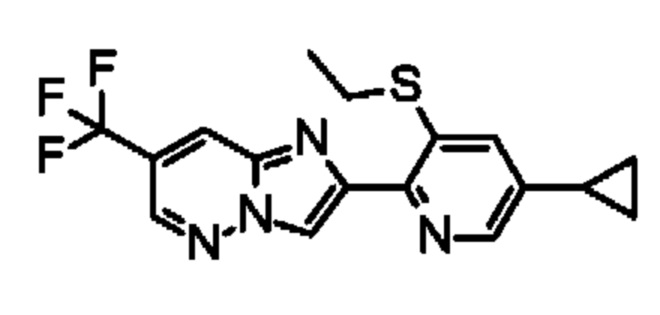
В 3-горлую колбу объемом 100 мл помещали толуол (14 мл) и воду (0,69 мл) и продували аргоном 5 мин. В атмосфере аргона добавляли 2-(5-бром-3-этилсульфанил-2-пиридил)-7-(трифторметил)имидазо[1,2-b]пиридазин (0,30 г, 0,74 ммоль), циклопропилбороновую кислоту (0,087 г, 0,97 ммоль), трикалийфосфат (0,58 г, 2,6 ммоль), трициклогексилфосфан (0,022 г, 0,074 ммоль) и ацетат палладия(II) (0,0084 г, 0,050 экв., 0,037 ммоль). Коричневую реакционную смесь нагревали до 110°С и перемешивали в течение одной ночи. Затем смесь охлаждали при комнатной температуре и добавляли воду и этилацетат. Полученную смесь фильтровали через целит, и осадок на целите промывали этилацетатом. Органический слой выделяли, высушивали над сульфатом натрия, фильтровали и концентрировали под вакуумом. Неочищенный продукт очищали с помощью хроматографии на силикагеле с получением 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-7-(трифторметил)имидазо [1,2-b]пиридазина.
LCMS (способ 1): время удерживания 1,08 min; 365 (М+Н)+.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 0,81-0,86 (m, 2 Н) 1,09-1,16 (m, 2 Н) 1,39 (t, J=7,34 Гц, 3 Н) 1,94-2,03 (m, 1 Н) 3,00 (q, J=7,34 Гц, 2 Н) 7,36-7,39 (m, 1 Н) 8,33 (d, J=l,83 Гц, 1 Н) 8,33 (s, 1 Н) 8,54 (d, J=2,20 Гц, 1 Н) 8,83-8,86 (m, 1 Н).
Стадия 4. Получение [5-циклопропил-2-[7-(трифторметил)имидазо[1,2-b]пиридазин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана ((пример Р16. таблица Р).)
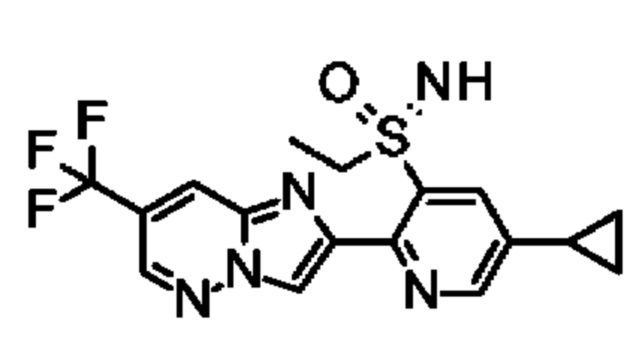 (пример Р16, таблица Р).
(пример Р16, таблица Р).
2-(5-Циклопропил-3-этилсульфанил-2-пиридил)-7-(трифторметил)имидазо[1,2-b]пиридазин (0,07 г, 0,1921 ммоль) суспендировали в метаноле (0,5763 мл) и добавляли PhI(ОАс)2 (0,1894 г, 0,5763 ммоль) и карбамат аммония (0,03826 г, 0,4802 ммоль) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре и через 45 мин. гасили ледяной водой и тиосульфатом натрия. Водный слой экстрагировали дважды с помощью этилацетата. Органические слои объединяли, промывали с помощью солевого раствора, высушивали над безводным сульфатом натрия, фильтровали и концентрировали. Неочищенный продукт очищали с помощью хроматографии на силикагеле с получением [5-циклопропил-2-[7-(трифторметил)имидазо[1,2-b]пиридазин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана.
LCMS (способ 1): время удерживания 0,87 min; 396 (М+Н)+.
1Н ЯМР (400 МГц, Хлороформ) δ ppm 0,89-0,95 (т, 2 Н) 1,18-1,25 (т, 2 Н) 1,36 (t, J=7,52 Гц, 3 Н) 2,08 (tt, J=8,44, 5,14 Гц, 1 Н) 3,21-3,37 (br s, 1 Н) 3,71-3,98 (m, 2 Н) 8,19 (d, J=2,20 Гц, 1 Н) 8,26-8,29 (m, 1 Н) 8,58 (d, J=2,20 Гц, 1 Н) 8,64 (d, J=2,20 Гц, 1 Н) 8,71-8,74 (т, 1 Н).
Пример Н7. Синтез [5-циклопропил-2-[6-(трифторметил)пиразоло[4.3-с]пиридин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (пример Р7, таблица Р)
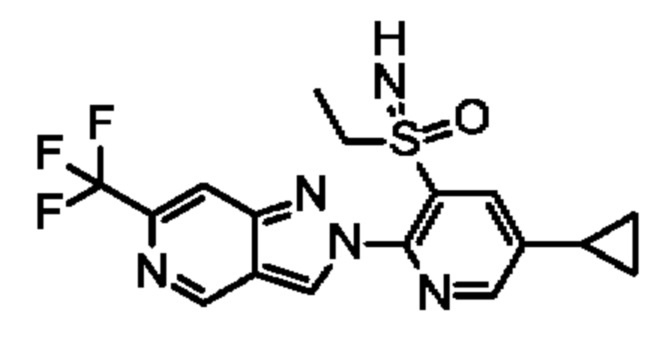 (пример Р7. таблица Р)
(пример Р7. таблица Р)
Стадия 1. Получение 2,5-дибром-3-этилсульфанилпиридина
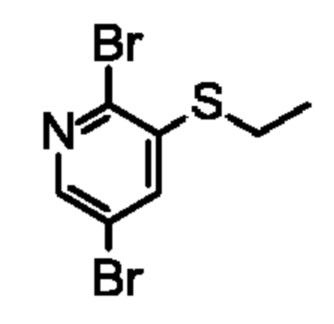
Раствор диэтилдисульфида (7,76 г, 63,5 ммоль, 2,00 экв.) и трет-бутилнитрита (4,91 г, 47,6 ммоль, 1,50 экв.) в DCE (60 мл) и DCM (40 мл) нагревали до 40°С. К данной смеси медленно добавляли раствор 2,5-дибромпиридин-3-амина (8,00 г, 31,7 ммоль, 1,00 экв.) в дихлорэтане (200 мл) медленно в течение 90 мин., и реакционную смесь перемешивали в течение дополнительного 1 ч. при 40°С. После завершения реакции реакционную массу охлаждали, разбавляли водой (100 мл) и экстрагировали с помощью дихлорметана (2 × 100 мл). Органический слой разделяли, объединенные органические слои высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали с помощью колоночной хроматографии (силикагель, 5-15% этилацетат/циклогексан) с получением 2,5-дибром-3-этилсульфанилпиридина.
LCMS (способ 4): 296 (М+Н)+, время удерживания 1,16 мин.
1H ЯМР (400 МГц, CDCl3) δ/ppm: 1,32 (t, 3 Н), 2,98 (m, 2 Н), 7,52 (s, 1 Н) 8,19 (s, 1 Н). Стадия 2. Получение (5-бром-3-этилсульфанил-2-пиридил)гидразина
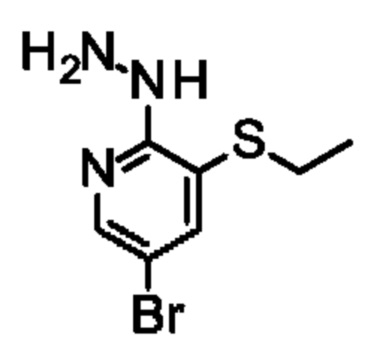
К раствору 2,5-дибром-3-этилсульфанилпиридина (1 г, 3,3669 ммоль) в 1,4-диоксане (10,34 г), добавляли моногидрат гидразина (1,0113 г, 20,201 ммоль) и полученную смесь перемешивали при 120°С в течение 10 часов. После завершения реакции смесь разбавляли водой (30 мл) и экстрагировали с помощью этилацетата. Объединенные органические слои промывали водой (20 мл), высушивали с помощью сульфата натрия, фильтровали и концентрировали in vacuo с получением (5-бром-3-этилсульфанил-2-пиридил)гидразина.
LCMS: 250 (M+H)+, время удерживания 0,6 мин.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-d) d ppm 1,26 (t, 3 Н) 2,81 (q, 2 Н) 3,10 (br 2 Н) 6,67 (br s, 1H) 7,65 (d, 1 H) 8,15 (d, 1 H).
Стадия 3. Получение 4-[2-(5-бром-3-этилсульфанил-2-пиридил)гидразино]-6-(трифторметил)пиридин-3-карбоновой кислоты
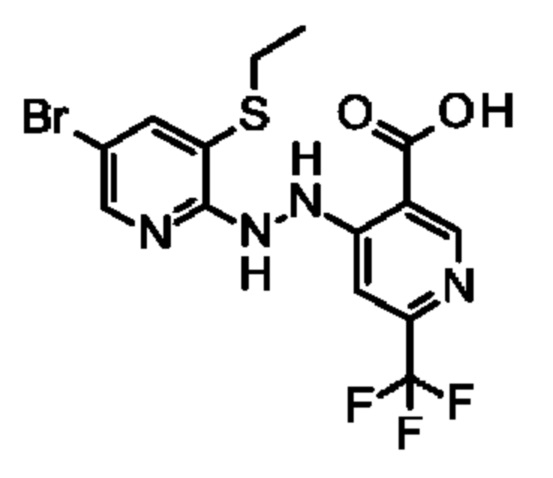
4-Хлор-6-(трифторметил)пиридин-3-карбоновую кислоту (CAS [1060810-66-3]) (20 г, 88,672 ммоль), (5-бром-3-этилсульфанил-2-пиридил)гидразин (33,005 г, 133,01 ммоль) и пентан-1-ол (120 мл) смешивали, и смесь перемешивали при 110°С в течение 15 часов. После завершения реакции смесь концентрировали in vacuo для удаления всего пентанола. Полученный остаток совместно выпаривали с толуолом. Неочищенный продукт разбавляли водой (100 мл), солевым раствором (100 мл) и экстрагировали с помощью этилацетата (3 × 200 мл). Объединенный органический слой высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Полученное твердое вещество растирали в порошок с циклогексаном с получением 4-[2-(5-бром-3-этилсульфанил-2-пиридил)гидразино]-6-(трифторметил)пиридин-3-карбоновой кислоты.
LCMS (способ 5): время удерживания 1,50 минуты, 439 (М+2)+.
1Н ЯМР (400 МГц, DMSO-d6) d ppm 1,26 (t, 3 H) 3,05 (q, 2 H) 7,16 (s, 1 H) 7,89 (d, 1 H) 8,11 (d, 1 H) 8,77 (s, 1 H) 8,88 (s, 1 H) 9,83 (s, 1 H) 13,38-14,36 (m, 1 H).
Стадия 4. Получение 2-(5-бром-3-этилсульфанил-2-пиридил)-3-хлор-6-(трифторметил)пиразоло[4,3-с]пиридина
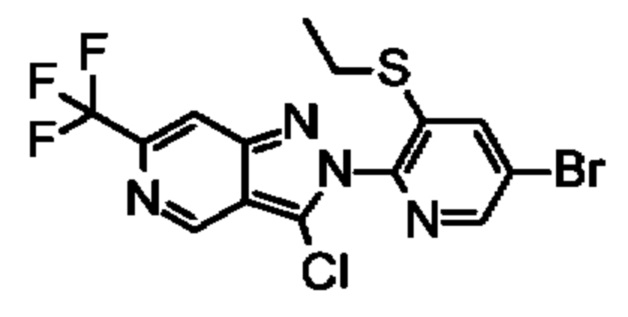
4-[2-(5-Бром-3-этилсульфанил-2-пиридил)гидразино]-6-(трифторметил)пиридин-3-карбоновую кислоту (22,87 ммоль, 10 г) растворяли в оксихлориде фосфора (100 мл), и полученную смесь нагревали при 110°С. Полученный прозрачный раствор нагревали с обратным холодильником при 110°С в течение 50 мин. После завершения реакции смесь концентрировали (оксихлорид фосфора отгоняли при пониженном давлении) и реакционную смесь разбавляли дихлорметаном (110 мл), выливали в ледяную воду (200 мл). Водный слой экстрагировали дихлорметаном (2 × 100 мл). Объединенный органический слой промывали водой (200 мл), высушивали над сульфатом натрия, фильтровали и концентрировали in vacuo. Неочищенный продукт очищали с помощью хроматографии на силикагеле с получением 2-(5-бром-3-этилсульфанил-2-пиридил)-3-хлор-6-(трифторметил)пиразоло[4,3-с]пиридина.
LCMS: 437 (М+Н)+, время удерживания 1,21 мин.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-d) d ppm 1,34 (m, 3 Н) 2,85 (m, 2 Н) 7,92 (S, 2 Н) 8,02 (m, 1 Н)8,60 (m, 1 Н) 9,32 (m, 1 Н).
Стадия 5. Получение 2-(5-бром-3-этилсульфанил-2-пиридил)-6-(трифторметил)пиразоло[4,3-с]пиридина
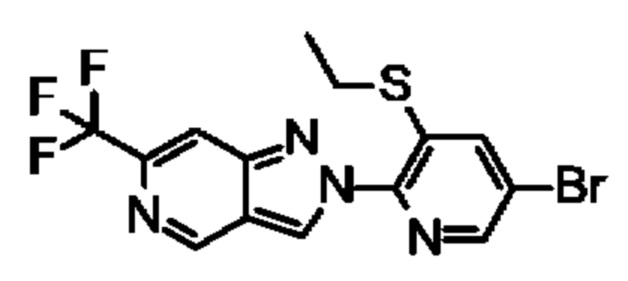
2-(5-Бром-3-этилсульфанил-2-пиридил)-3-хлор-6-(трифторметил)пиразоло[4,3-с]пиридин (0,2 ммоль, 0,1 г) растворяли в уксусной кислоте (2 мл), и цинк (0,5 ммоль, 0,03 г) медленно добавляли к смеси. Реакционную массу перемешивали при 55°С в течение 40 мин. Реакцию контролировали с помощью LCMS и TLC. После завершения реакционную смесь выливали в воду (30 мл), и полученный раствор экстрагировали этилацетатом (20 мл × 3). Объединенный органический слой промывали водным насыщенным раствором хлорида натрия (30 мл), высушивали над безводный сульфатом натрия, фильтровали и концентрировали in vacuo. Остаток подвергали колоночной хроматографии на силикагеле с получением 2-(5-бром-3-этилсульфанил-2-пиридил)-6-(трифторметил)пиразоло[4,3-с]пиридина.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-d) d ppm 1,29 (m, 4 Н) 2,95 (m, 2 Н) 7,85 (m, 1 Н) 8,35 (m, 1 Н) 8,38 (d, 1 Н) 8,95 (m, 1 Н) 9,44 (m, 1 Н).
LCMS: время удерживания 1,6 минуты, 403 (М+Н)+.
Стадия 6. Получение 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-6-(трифторметил)пиразоло[4,3-с]пиридина
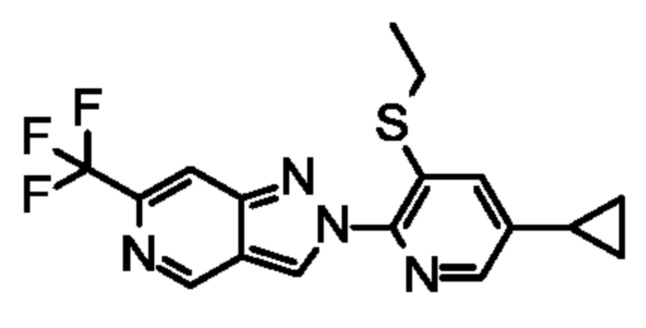
Во флакон для микроволновой обработки добавляли 2-(5-бром-3-этилсульфанил-2-пиридил)-6-(трифторметил)пиразоло[4,3-с]пиридин (0,1 г, 0,2 ммоль), циклопропилбороновую кислоту (0,03 г, 0,3 ммоль), трикалийфосфат (0,2 г, 0,9 ммоль), трициклогексилфосфан (0,007 г, 0,02 ммоль) в толуоле (2 мл) и воде (1 мл). Реакционную массу продували азотом в течение 30 мин. К этому затем добавляли ацетат палладия(II) (0,003 г, 0,01 ммоль), и реакционную смесь перемешивали при 150°С в микроволновой печи в течение 4 часов. Затем при комнатной температуре реакционную смесь разбавляли этилацетатом (20 мл) и промывали с помощью воды (20 мл). Органический слой промывали водой (20 мл), высушивали органический слой над сульфатом натрия, фильтровали и концентрировали in vacuo. Соединение выделяли посредством хроматографии на силикагеле с получением 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-6-(трифторметил)пиразоло[4,3-с]пиридина.
LCMS: 365 (М+Н)+, время удерживания 1,12 мин.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-d) d ppm 0,86 (m, 2 Н) 1,13 (br, 2 Н) 1,23 (m, 4 Н) 2,90 (q, 2 Н) 7,47 (d, 1 Н) 8,13 (m, 2 Н) 8,94 (s, 1 Н) 9,40 (m, 1 Н).
Стадия 7. Синтез [5-циклопропил-2-[6-(трифторметил)пиразоло[4.3-с]пиридин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (пример Р7, таблица Р)
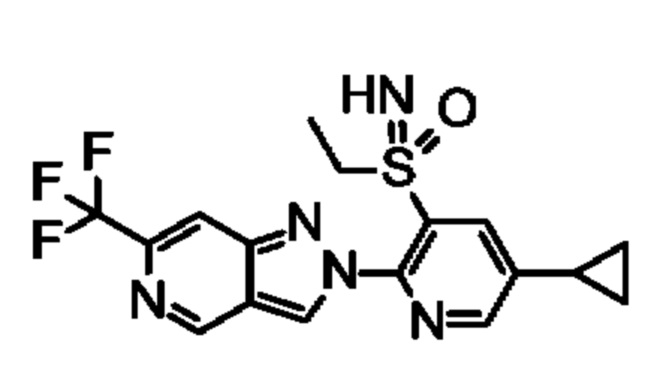 (пример Р7, таблица Р)
(пример Р7, таблица Р)
Требуемый продукт получали с применением стандартного способа, описанного в примере H1, стадии 7.
LCMS (способ 5): время удерживания 0,94 минуты, 396 (М+Н)+.
1H ЯМР (400 МГц, ХЛОРОФОРМ-d) d ppm 1,25 (m, 4 H) 1,44 (m, 3 H) 2,16 (m, 1 H) 3,87(m, 2 H) 8,06 (s, 1 H) 8,29 (d, 1 H) 8,56 (d, 1 H) 8,87 (d, 1 H) 9,40(s, 1 H).
Пример H8. Синтез [5-циклопропил-2-[5-(трифторметилсульфанил)-1,3-бензоксазол-2-ил]-3-пиридил1этилиминооксо-λ6-сульфана (пример PI8, таблица Р)
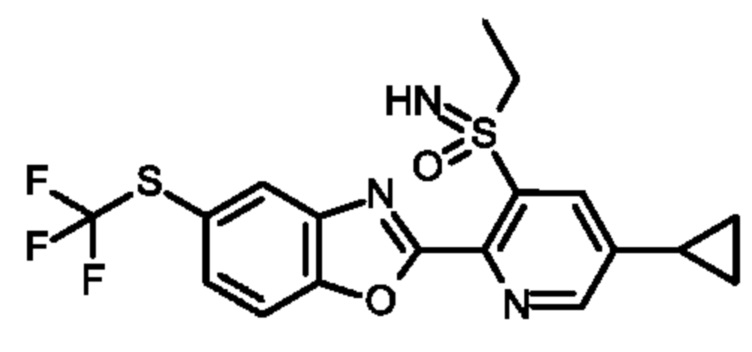 (пример Р18, таблица Р)
(пример Р18, таблица Р)
Требуемый продукт получали с применением стандартного способа, описанного в примере H1, стадии 7, исходя из 2-(5-циклопропил-3-этилсульфанил-2-пиридил)-5-(трифторметилсульфанил)-1,3-бензоксазола (известного из WO 19/009307).
LCMS (способ 5): 428 (М+Н)+, время удерживания: 1,03 мин.
Дополнительные соединения по настоящему изобретению могут быть получены аналогично способу, описанному выше. Соединения, полученные для дополнительного иллюстрирования настоящего изобретения перечислены в таблице Р.
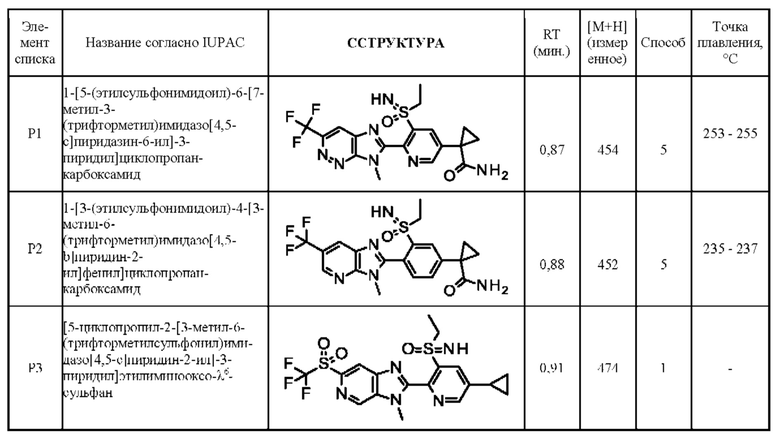
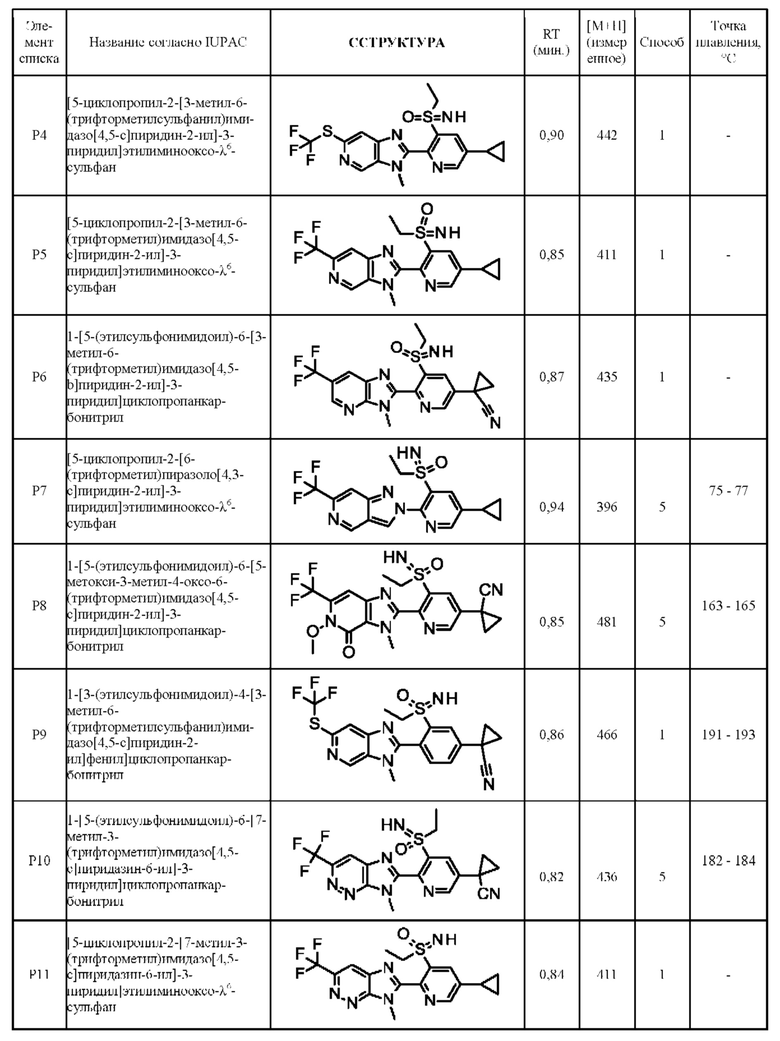
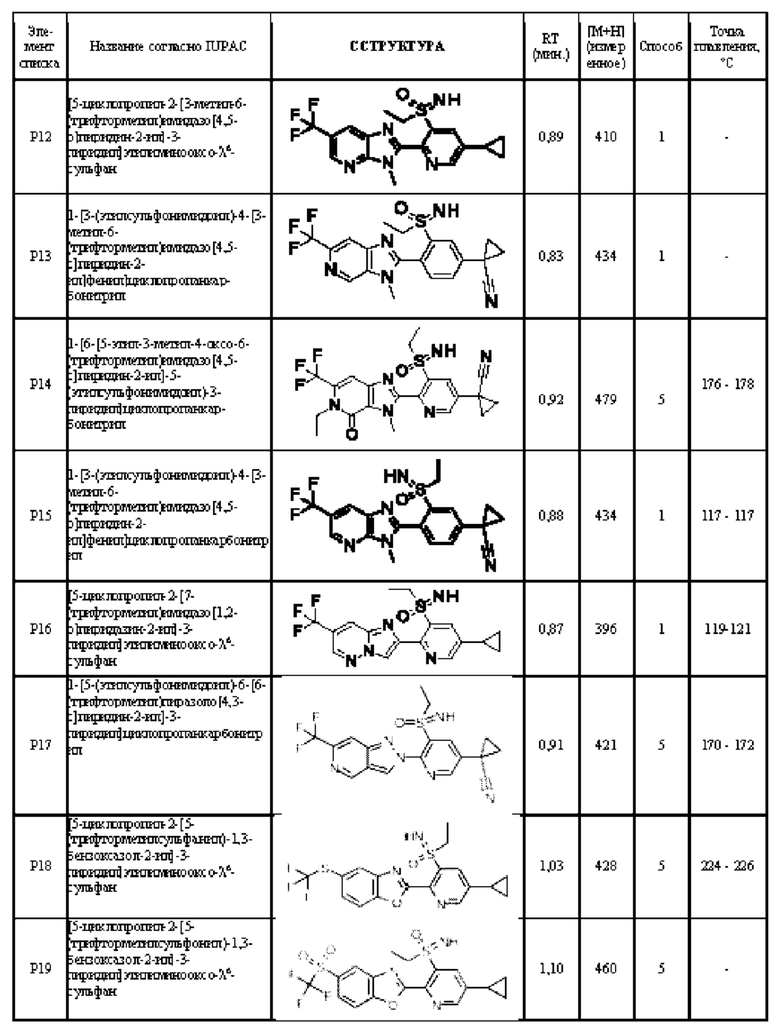
Активность композиций согласно настоящему изобретению можно 3Начительно расширить и адаптировать применительно к преобладающим условиям путем добавления других инсектицидно, акарицидно и/или фунгицидно активных ингредиентов. Смеси соединений формулы I с другими инсектицидно, акарицидно и/или фунгицидно активными ингредиентами также могут обладать дополнительными неожиданными преимуществами, которые также могут быть описаны в более широком смысле как синергетическая активность. Например, лучшая выносливость у растений, пониженная фитотоксичность, возможность контроля насекомых на разных стадиях их развития или лучшие характеристики при их получении, например, при измельчении или смешивании, при их хранении или при их использовании. Подходящими дополнениями к рассматриваемым в данном документе активным ингредиентам являются, например, представители следующих классов активных ингредиентов: фосфорорганические соединения, производные нитрофенола, тиомочевины, ювенильные гормоны, формамидины, производные бензофенона, мочевины, производные пиррола, карбаматы, пиретроиды, хлорированные углеводороды, ацилмочевины, производные пиридилметиленамина, макролиды, неоникотиноиды и препараты Bacillus thuringiensis.
Предпочтительными являются следующие смеси соединений формулы I с активными ингредиентами (сокращение "ТХ" означает "одно соединение, выбранное из группы, состоящей из соединений, описанных в таблицах Y-l - Y-8, Х-1 - Х-8, U-1 - U-2 и V-1 -V-6 и таблице Р настоящего изобретения"):
вспомогательное вещество, выбранное из группы веществ, состоящей из нефтяных масел (альтернативное название) (628)+ТХ,
акарицид, выбранный из группы веществ, состоящей из 1,1-бис(4-хлорфенил)-2-этоксиэтанола (название согласно IUPAC) (910)+ТХ, 2,4-дихлорфенилбензолсульфоната (название согласно IUPAC/Химической реферативной службе) (1059)+ТХ, 2-фтор-N-метил-N-1-нафтилацетамида (название согласно IUPAC) (1295)+ТХ, 4-хлорфенилфенилсульфона (название согласно IUPAC) (981)+ТХ, абамектина (1)+ТХ, ацеквиноцила (3)+ТХ, ацетопрола [CCN]+ТХ, акринатрина (9)+ТХ, алдикарба (16)+ТХ, альдоксикарба (863)+ТХ, альфа-циперметрина (202)+ТХ, амидитиона (870)+ТХ, амидофлумета [CCN]+ТХ, амидотиоата (872)+ТХ, амитона (875)+ТХ, амитона гидрооксалата (875)+ТХ, амитраза (24)+ТХ, арамита (881)+ТХ, оксида мышьяка (882)+ТХ, AVI 382 (код соединения)+ТХ, AZ 60541 (код соединения)+ТХ, азинфос-этила (44)+ТХ, азинфос-метила (45)+ТХ, азобензола (название согласно IUPAC) (888)+ТХ, азоциклотина (46)+ТХ, азотоата (889)+ТХ, беномила (62)+ТХ, беноксафоса (альтернативное название) [CCN]+ТХ, бензоксимата (71)+ТХ, бензил бе нзоата (название согласно IUPAC) [CCN]+ТХ, бифеназата (74)+ТХ, бифентрина (76)+ТХ, бинапакрила (907)+ТХ, брофенвалерата (альтернативное название)+ТХ, бромоциклена (918)+ТХ, бромофоса (920)+ТХ, бромофос-этила (921)+ТХ, бромопропилата (94)+ТХ, бупрофезина (99)+ТХ, бутокарбоксима (103)+ТХ, бутоксикарбоксима (104)+ТХ, бутилпиридабена (альтернативное название)+ТХ, полисульфида кальция (название согласно IUPAC) (111)+ТХ, камфехлора (941)+ТХ, карбанолата (943)+ТХ, карбарила (115)+ТХ, карбофурана (118)+ТХ, карбофенотиона (947)+ТХ, CGA 50'439 (код разработки) (125)+ТХ, хинометионата (126)+ТХ, хлорбензида (959)+ТХ, хлордимеформа (964)+ТХ, гидрохлорида хлордимеформа (964)+ТХ, хлорфенапира (130)+ТХ, хлорфенетола (968)+ТХ, хлорфенсона (970)+ТХ, хлорфенсульфида (971)+ТХ, хлорфенвинфоса (131)+ТХ, хлоробензилата (975)+ТХ, хлоромебуформа (977)+ТХ, хлорометиурона (978)+ТХ, хлорпропилата (983)+ТХ, хлорпирифоса (145)+ТХ, хлорпирифос-метила (146)+ТХ, хлортиофоса (994)+ТХ, цинерина I (696)+ТХ, цинерина II (696)+ТХ, цинеринов (696)+ТХ, клофентезина (158)+ТХ, клозантела (альтернативное название) [CCN]+ТХ, кумафоса (174)+ТХ, кротамитона (альтернативное название) [CCN]+ТХ, кротоксифоса (1010)+ТХ, куфранеба (1013)+ТХ, циантоата (1020)+ТХ, цифлуметофена (регистрационный №по CAS: 400882-07-7)+ТХ, цигалотрина (196)+ТХ, цигексатина(199)+ТХ, циперметрина (201)+ТХ, DCPM (1032)+ТХ, DDT(219)+TX, демефиона(1037)+ТХ, демефиона-О (1037)+ТХ, демефиона-S (1037)+ТХ, деметона(1038)+ТХ, деметон-метила (224)+ТХ, деметона-О (1038)+ТХ, деметон-О-метила (224)+ТХ, деметона-S (1038)+ТХ, деметон-8-метила (224)+ТХ, деметон-8-метилсульфона (1039)+ТХ, диафентиурона (226)+ТХ, димпропиридаза+ТХ, диалифоса (1042)+ТХ, диазинона (227)+ТХ, дихлофлуанида (230)+ТХ, дихлорфоса (236)+ТХ, диклифоса (альтернативное название)+ТХ, дикофола (242)+ТХ, дикротофоса (243)+ТХ, диенохлора (1071)+ТХ, димефокса (1081)+ТХ, диметоата (262)+ТХ, динактина (альтернативное название) (653)+ТХ, динекса (1089)+ТХ, динекс-диклексина (1089)+ТХ, динобутона (269)+ТХ, динокапа (270)+ТХ, динокапа-4 [CCN]+ТХ, динокапа-6 [CCN]+ТХ, диноктона (1090)+ТХ, динопентона (1092)+ТХ, диносульфона (1097)+ТХ, динотербона (1098)+ТХ, диоксатиона (1102)+ТХ, дифенилсульфона (название согласно IUPAC) (1103)+ТХ, дисульфирама (альтернативное название) [CCN]+ТХ, дисульфотона (278)+ТХ, DNOC (282)+ТХ, дофенапина (1113)+ТХ, дорамектина (альтернативное название) [CCN]+ТХ, эндосульфана (294)+ТХ, эндотиона (1121)+ТХ, EPN (297)+ТХ, эприномектина (альтернативное название) [CCN]+ТХ, этиона (309)+ТХ, этоат-метила (1134)+ТХ, этоксазола (320)+ТХ, этримфоса (1142)+ТХ, феназафлора (1147)+ТХ, феназаквина (328)+ТХ, оксида фенбутатина (330)+ТХ, фенотиокарба (337)+ТХ, фенпропатрина (342)+ТХ, фенпирада (альтернативное название)+ТХ, фенпироксимата (345)+ТХ, фензона (1157)+ТХ, фентрифанила (1161)+ТХ, фенвалерата (349)+ТХ, фипронила (354)+ТХ, флуакрипирима (360)+ТХ, флуазурона (1166)+ТХ, флубензимина (1167)+ТХ, флуциклоксурона (366)+ТХ, флуцитрината (367)+ТХ, флуенетила (1169)+ТХ, флуфеноксурона (370)+ТХ, флуметрина (372)+ТХ, флуорбензида (1174)+ТХ, флувалината (1184)+ТХ, FMC 1137 (код разработки) (1185)+ТХ, форметаната (405)+ТХ, гидрохлорида форметаната (405)+ТХ, формотиона (1192)+ТХ, формпараната (1193)+ТХ, гамма-НСН (430)+ТХ, глиодина (1205)+ТХ, галфенпрокса (424)+ТХ, гептенофоса (432)+ТХ, гексадецилциклопропанкарбоксилата (название согласно IUPAC/Химической реферативной службе) (1216)+ТХ, гекситиазокса (441)+ТХ, йодметана (название согласно IUPAC) (542)+ТХ, изокарбофоса (альтернативное название) (473)+ТХ, изопропил-(9-(метоксиаминотиофосфорил)салицилата (название согласно IUPAC) (473)+ТХ, ивермектина (альтернативное название) [CCN]+ТХ, жасмолина I (696)+ТХ, жасмолина II (696)+ТХ, йодофенфоса (1248)+ТХ, линдана (430)+ТХ, люфенурона (490)+ТХ, малатиона (492)+ТХ, малонобена (1254)+ТХ, мекарбама (502)+ТХ, мефосфолана (1261)+ТХ, месульфена (альтернативное название) [CCN]+ТХ, метакрифоса (1266)+ТХ, метамидофоса (527)+ТХ, метидатиона (529)+ТХ, метиокарба (530)+ТХ, метомила (531)+ТХ, метилбромида (537)+ТХ, метолкарба (550)+ТХ, мевинфоса (556)+ТХ, мексакарбата (1290)+ТХ, милбемектина (557)+ТХ, милбемицин-оксима (альтернативное название) [CCN]+ТХ, мипафокса (1293)+ТХ, монокротофоса (561)+ТХ, морфотиона (1300)+ТХ, моксидектина (альтернативное название) [CCN]+ТХ, наледа (567)+ТХ, NC-184 (код соединения)+ТХ, NC-512 (код соединения)+ТХ, нифлуридида (1309)+ТХ, никкомицинов (альтернативное название) [CCN]+ТХ, нитрилакарба (1313)+ТХ, комплекса нитрилакарба и хлорида цинка 1:1 (1313)+ТХ, NNI-0101 (код соединения)+ТХ, NNI-0250 (код соединения)+ТХ, ометоата (594)+ТХ, оксамила (602)+ТХ, оксидепрофоса (1324)+ТХ, оксидисульфотона (1325)+ТХ, pp'-DDT (219)+ТХ, паратиона (615)+ТХ, перметрина (626)+ТХ, нефтяных масел (альтернативное название) (628)+ТХ, фенкаптона (1330)+ТХ, фентоата (631)+ТХ, фората (636)+ТХ, фозалона (637)+ТХ, фосфолана (1338)+ТХ, фосмета (638)+ТХ, фосфамидона (639)+ТХ, фоксима (642)+ТХ, пиримифос-метила (652)+ТХ, полихлортерпенов (традиционное название) (1347)+ТХ, полинактинов (альтернативное название) (653)+ТХ, проклонола (1350)+ТХ, профенофоса (662)+ТХ, промацила (1354)+ТХ, пропаргита (671)+ТХ, пропетамфоса (673)+ТХ, пропоксура (678)+ТХ, протидатиона (1360)+ТХ, протоата (1362)+ТХ, пиретрина 1(696)+ТХ, пиретрина II (696)+ТХ, пиретринов (696)+ТХ, пиридабена (699)+ТХ, пиридафентиона (701)+ТХ, пиримидифена (706)+ТХ, пиримитата (1370)+ТХ, квиналфоса (711)+ТХ, квинтиофоса (1381)+ТХ, R-1492 (код разработки) (1382)+ТХ, RA-17 (код разработки) (1383)+ТХ, ротенона (722)+ТХ, шрадана (1389)+ТХ, себуфоса (альтернативное название)+ТХ, селамектина (альтернативное название) [CCN]+ТХ, SI-0009 (код соединения)+ТХ, софамида (1402)+ТХ, спиродиклофена (738)+ТХ, спиромезифена (739)+ТХ, SSI-121 (код разработки) (1404)+ТХ, сульфирама (альтернативное название) [CCN]+ТХ, сульфлурамида (750)+ТХ, сульфотепа (753)+ТХ, серы (754)+ТХ, SZI-121 (код разработки) (757)+ТХ, тау-флувалината (398)+ТХ, тебуфенпирада (763)+ТХ, ТЕРР (1417)+ТХ, тербама (альтернативное название)+ТХ, тетрахлорвинфоса (777)+ТХ, тетрадифона (786)+ТХ, тетранактина (альтернативное название) (653)+ТХ, тетрасула (1425)+ТХ, тиафенокса (альтернативное название)+ТХ, тиокарбоксима (1431)+ТХ, тиофанокса (800)+ТХ, тиометона (801)+ТХ, тиоквинокса (1436)+ТХ, турингиенсина (альтернативное название) [CCN]+ТХ, триамифоса (1441)+ТХ, триаратена (1443)+ТХ, триазофоса (820)+ТХ, триазурона (альтернативное название)+ТХ, трихлорфона (824)+ТХ, трифенофоса (1455)+ТХ, тринактина (альтернативное название) (653)+ТХ, вамидотиона (847)+ТХ, ванилипрола [CCN] и YI-5302 (код соединения)+ТХ, альгицид, выбранный из группы веществ, состоящей из бетоксазина [CCN]+ТХ, диоктаноата меди (название согласно IUPAC) (170)+ТХ, сульфата меди (172)+ТХ, цибутрина [CCN]+ТХ, дихлона (1052)+ТХ, дихлорофена (232)+ТХ, эндотала (295)+ТХ, фентина (347)+ТХ, гашеной извести [CCN]+ТХ, набама (566)+ТХ, квинокламина (714)+ТХ, квинонамида (1379)+ТХ, симазина (730)+ТХ, ацетата трифенилолова (название согласно IUPAC) (347) и гидроксида трифенилолова (название согласно IUPAC) (347)+ТХ,
антигельминтик, выбранный из группы веществ, состоящей из абамектина (1)+ТХ, круфомата (1011)+ТХ, дорамектина (альтернативное название) [CCN]+ТХ, эмамектина (291)+ТХ, бензоата эмамектина (291)+ТХ, эприномектина (альтернативное название) [CCN]+ТХ, ивермектина (альтернативное название) [CCN]+ТХ, милбемицин-оксима (альтернативное название) [CCN]+ТХ, моксидектина (альтернативное название) [CCN]+ТХ, пиперазина [CCN]+ТХ, селамектина (альтернативное название) [CCN]+ТХ, спиносада (737) и тиофаната (1435)+ТХ,
авицид, выбранный из группы веществ, состоящей из хлоралозы (127)+ТХ, эндрина (1122)+ТХ, фентиона (346)+ТХ, пиридин-4-амина (название согласно IUPAC) (23) и стрихнина (745)+ТХ,
бактерицид, выбранный из группы веществ, состоящей из 1-гидрокси-1H-пиридин-2-тиона (название согласно IUPAC) (1222)+ТХ, 4-(хиноксалин-2-иламино)бензолсульфонамида (название согласно IUPAC) (748)+ТХ, сульфата 8-гидроксихинолина (446)+ТХ, бронопола (97)+ТХ, диоктаноата меди (название согласно IUPAC) (170)+ТХ, гидроксида меди (название согласно IUPAC) (169)+ТХ, крезола [CCN]+ТХ, дихлорофена (232)+ТХ, дипиритиона (1105)+ТХ, додицина (1112)+ТХ, фенаминосульфа (1144)+ТХ, формальдегида (404)+ТХ, гидраргафена (альтернативное название) [CCN]+ТХ, касугамицина (483)+ТХ, гидрата гидрохлорида касугамицина (483)+ТХ, никеля бис(диметилдитиокарбамата) (название согласно IUPAC) (1308)+ТХ, нитрапирина (580)+ТХ, октилинона (590)+ТХ, оксолиновой кислоты (606)+ТХ, окситетрациклина (611)+ТХ, калия гидроксихинолинсульфата (446)+ТХ, пробеназола (658)+ТХ, стрептомицина (744)+ТХ, стрептомицина сесквисульфата (744)+ТХ, теклофталама (766)+ТХ и тиомерсала (альтернативное название) [CCN]+ТХ,
биологическое средство, выбранное из группы веществ, состоящей из Adoxophyes огапа GV (альтернативное название) (12)+ТХ, Agrobacterium radiobacter (альтернативное название) (13)+ТХ, Amblyseius spp.(альтернативное название) (19)+ТХ, Anagrapha falcifera NPV (альтернативное название) (28)+ТХ, Anagrus atomus (альтернативное название) (29)+ТХ, Aphelinus abdominalis (альтернативное название) (33)+ТХ, Aphidius colemani (альтернативное название) (34)+ТХ, Aphidoletes aphidimyza (альтернативное название) (35)+ТХ, Autographa californica NPV (альтернативное название) (38)+ТХ, Bacillus firmus (альтернативное название) (48)+ТХ, Bacillus sphaericus Neide (научное название) (49)+ТХ, Bacillus thuringiensis Berliner (научное название) (51)+ТХ, Bacillus thuringiensis подвид aizawai (научное название) (51)+ТХ, Bacillus thuringiensis подвид israelensis (научное название) (51)+ТХ, Bacillus thuringiensis подвид japonensis (научное название) (51)+ТХ, Bacillus thuringiensis подвид kurstaki (научное название) (51)+ТХ, Bacillus thuringiensis подвид tenebrionis (научное название) (51)+ТХ, Beauveria bassiana (альтернативное название) (53)+ТХ, Beauveria brongniartii (альтернативное название) (54)+ТХ, Chrysoperla cornea (альтернативное название) (151)+ТХ, Cryptolaemus montrouzieri (альтернативное название) (178)+ТХ, Cydia pomonella GV (альтернативное название) (191)+ТХ, Dacnusa sibirica (альтернативное название) (212)+ТХ, Diglyphus isaea (альтернативное название) (254)+ТХ, Encarsia formosa (научное название) (293)+ТХ, Eretmocerus eremicus (альтернативное название) (300)+ТХ, Helicoverpa zea NPV (альтернативное название) (431)+ТХ, Heterorhabditis bacteriophora и Н. megidis (альтернативное название) (433)+ТХ, Hippodamia convergens (альтернативное название) (442)+ТХ, Leptomastix dactylopii (альтернативное название) (488)+ТХ, Macrolophus caliginosus (альтернативное название) (491)+ТХ, Mamestra brassicae NPV (альтернативное название) (494)+ТХ, Metaphycus helvolus (альтернативное название) (522)+ТХ, Metarhizium anisopliae вар acridum (научное название) (523)+ТХ, Metarhizium anisopliae вар anisopliae (научное название) (523)+ТХ, Neodiprion sertifer NPV и N. lecontei NPV (альтернативное название) (575)+ТХ, Orius spp.(альтернативное название) (596)+ТХ, Paecilomyces fumosoroseus (альтернативное название) (613)+ТХ, Phytoseiulus persimilis (альтернативное название) (644)+ТХ, мультикапсидный вирус ядерного полиэдроза Spodoptera exigua (научное название) (741)+ТХ, Steinernema bibionis (альтернативное название) (742)+ТХ, Steinernema carpocapsae (альтернативное название) (742)+ТХ, Steinernema feltiae (альтернативное название) (742)+ТХ, Steinernema glaseri (альтернативное название) (742)+ТХ, Steinernema riobrave (альтернативное название) (742)+ТХ, Steinernema riobravis (альтернативное название) (742)+ТХ, Steinernema scapterisci (альтернативное название) (742)+ТХ, Steinernema spp.(альтернативное название) (742)+ТХ, Trichogramma spp.(альтернативное название) (826)+ТХ, Typhlodromus occidentalis (альтернативное название) (844) и Verticillium lecanii (альтернативное название) (848)+ТХ, стерилизатор почвы, выбранный из группы веществ, состоящей из йодметана (название согласно IUPAC) (542) и метилбромида (537)+ТХ,
хемостерилизатор, выбранный из группы веществ, состоящей из афолата [CCN]+ТХ, бисазира (альтернативное название) [CCN]+ТХ, бусульфана (альтернативное название) [CCN]+ТХ, дифлубензурона (250)+ТХ, диматифа (альтернативное название) [CCN]+ТХ, хемела [CCN]+ТХ, хемпы [CCN]+ТХ, метепы [CCN]+ТХ, метиотепы [CCN]+ТХ, метилафолата [CCN]+ТХ, морзида [CCN]+ТХ, пенфлурона (альтернативное название) [CCN]+ТХ, тепы [CCN]+ТХ, тиохемпы (альтернативное название) [CCN]+ТХ, тиотепы (альтернативное название) [CCN]+ТХ, третамина (альтернативное название) [CCN] и уредепы (альтернативное название) [CCN]+ТХ,
феромон насекомого, выбранный из группы веществ, состоящей из (Е)-дец-5-ен-1-илацетата с (Е)-дец-5-ен-1-олом (название согласно IUPAC) (222)+ТХ, (E)-тридец-4-ен-1-ил ацетата (название согласно IUPAC) (829)+ТХ, (E)-6-метилгепт-2-ен-4-ола (название согласно IUPAC) (541)+ТХ, (E,Z)-тетрадека-4,10-диен-1-илацетата (название согласно IUPAC) (779)+ТХ, (2)-додец-7-ен-1-илацетата (название согласно IUPAC) (285)+ТХ, (2)-гексадец-11-еналя (название согласно IUPAC) (436)+ТХ, (7)-гексадец-11-ен-1-илацетата (название согласно IUPAC) (437)+ТХ, (2)-гексадец-13-ен-11-ин-1-илацетата (название согласно IUPAC) (438)+ТХ, (7)-эйкоз-13-ен-10-она (название согласно IUPAC) (448)+ТХ, (2)-тетрадец-7-ен-1-аля (название согласно IUPAC) (782)+ТХ, (2)-тетрадец-9-ен- 1-ола (название согласно IUPAC) (783)+ТХ, (7)-тетрадец-9-ен-1-илацетата (название согласно IUPAC) (784)+ТХ, (7E,9Z)-додека-7,9-диен-1-илацетата (название согласно IUPAC) (283)+ТХ, (9Z,11E)-тетрадека-9,11-диен-1-илацетата (название согласно IUPAC) (780)+ТХ, (9Z, 12E)-тетрадека-9,12-диен-1-илацетата (название согласно IUPAC) (781)+ТХ, 14-метилоктадец-1-ена (название согласно IUPAC) (545)+ТХ, 4-метилнонан-5-ола с 4-метилнонан-5-оном (название согласно IUPAC) (544)+ТХ, альфа-мултистриатина (альтернативное название) [CCN]+ТХ, бревикомина (альтернативное название) [CCN]+ТХ, кодлелура (альтернативное название) [CCN]+ТХ, кодлемона (альтернативное название) (167)+ТХ, куелура (альтернативное название) (179)+ТХ, диспарлура (277)+ТХ, додец-8-ен-1-ил ацетата (название согласно IUPAC) (286)+ТХ, додец-9-ен-1-илацетата (название согласно IUPAC) (287)+ТХ, додека-8+ТХ, 10-диен-1-илацетата (название согласно IUPAC) (284)+ТХ, доминикалура (альтернативное название) [CCN]+ТХ, этил-4-метилоктаноата (название согласно IUPAC) (317)+ТХ, эвгенола (альтернативное название) [CCN]+ТХ, фронталина (альтернативное название) [CCN]+ТХ, госсиплура (альтернативное название) (420)+ТХ, грандлура (421)+ТХ, грандлура I (альтернативное название) (421)+ТХ, грандлура II (альтернативное название) (421)+ТХ, грандлура III (альтернативное название) (421)+ТХ, грандлура IV (альтернативное название) (421)+ТХ, гексалура [CCN]+ТХ, ипсдиенола (альтернативное название) [CCN]+ТХ, ипсенола (альтернативное название) [CCN]+ТХ, японилура (альтернативное название) (481)+ТХ, линеатина (альтернативное название) [CCN]+ТХ, литлура (альтернативное название) [CCN]+ТХ, луплура (альтернативное название) [CCN]+ТХ, медлура [CCN]+ТХ, мегатомоевой кислоты (альтернативное название) [CCN]+ТХ, метилэвгенола (альтернативное название) (540)+ТХ, мускалура (563)+ТХ, октадека-2,13-диен-1-илацетата (название согласно IUPAC) (588)+ТХ, октадека-3,13-диен-1-илацетата (название согласно IUPAC) (589)+ТХ, орфралура (альтернативное название) [CCN]+ТХ, орикталура (альтернативное название) (317)+ТХ, острамона (альтернативное название) [CCN]+ТХ, сиглура [CCN]+ТХ, сордидина (альтернативное название) (736)+ТХ, сулкатола (альтернативное название) [CCN]+ТХ, тетрадей-11-ен-1-илацетата (название согласно IUPAC) (785)+ТХ, тримедлура (839)+ТХ, тримедлура А (альтернативное название) (839)+ТХ, тримедлура Bi (альтернативное название) (839)+ТХ, тримедлура В2 (альтернативное название) (839)+ТХ, тримедлура С (альтернативное название) (839) и транк-кола (альтернативное название) [CCN]+ТХ, средство для отпугивания насекомых, выбранное из группы веществ, состоящей из 2-(октилтио)этанола (название согласно IUPAC) (591)+ТХ, бутопироноксила (933)+ТХ, бутокси(полипропиленгликоля) (936)+ТХ, дибутиладипата (название согласно IUPAC) (1046)+ТХ, дибутилфталата (1047)+ТХ, дибутилсукцината (название согласно IUPAC) (1048)+ТХ, диэтилтолуамида [CCN]+ТХ, диметилкарбата [CCN]+ТХ, диметилфталата [CCN]+ТХ, этилгександиола (1137)+ТХ, гексамида [CCN]+ТХ, метоквин-бутила (1276)+ТХ, метилнеодеканамида [CCN]+ТХ, оксамата [CCN] и пикаридина [CCN]+ТХ,
инсектицид, выбранный из группы веществ, состоящей из 1-дихлор-1-нитроэтана (название согласно IUPAC/Химической реферативной службе) (1058)+ТХ, 1,1-дихлор-2,2-бис(4-этилфенил)этана (название согласно IUPAC) (1056),+ТХ, 1,2-дихлорпропана (название согласно IUPAC/Химической реферативной службе) (1062)+ТХ, 1,2-дихлорпропана с 1,3-дихлорпропеном (название согласно IUPAC) (1063)+ТХ, 1-бром-2-хлорэтана (название согласно IUPAC/Химической реферативной службе) (916)+ТХ, 2,2,2-трихлор-1-(3,4-дихлорфенил)этилацетата (название согласно IUPAC) (1451)+ТХ, 2,2-дихлорвинил-2-этилсульфинилэтилметилфосфата (название согласно IUPAC) (1066)+ТХ, 2-(1,3-дитиолан-2-ил)фенилдиметилкарбамата (название согласно IUPAC/Химической реферативной службе) (1109)+ТХ, 2-(2-бутоксиэтокси)этилтиоцианата (название согласно IUPAC/Химической реферативной службе) (935)+ТХ, 2-(4,5-диметил-1,3-диоксолан-2-ил)фенилметилкарбамата (название согласно IUPAC/Химической реферативной службе) (1084)+ТХ, 2-(4-хлор-3,5-ксилилокси)этанола (название согласно IUPAC) (986)+ТХ, 2-хлорвинилдиэтилфосфата (название согласно IUPAC) (984)+ТХ, 2-имидазолидона (название согласно IUPAC) (1225)+ТХ, 2-изовалерилиндан-1,3-диона (название согласно IUPAC) (1246)+ТХ, 2-метил(проп-2-инил)аминофенилметилкарбамата (название согласно IUPAC) (1284)+ТХ, 2-тиоцианатоэтиллаурата (название согласно IUPAC) (1433)+ТХ, 3-бром-1-хлорпроп-1-ена (название согласно IUPAC) (917)+ТХ, 3-метил-1-фенилпиразол-5-илдиметилкарбамата (название согласно IUPAC) (1283)+ТХ, 4-метил(проп-2-инил)амино-3,5-ксилилметилкарбамата (название согласно IUPAC) (1285)+ТХ, 5,5-диметил-3-оксоциклогекс-1-енилдиметилкарбамата (название согласно IUPAC) (1085)+ТХ, абамектина (1)+ТХ, ацефата (2)+ТХ, ацетамиприда (4)+ТХ, ацетиона (альтернативное название) [CCN]+ТХ, ацетопрола [CCN]+ТХ, акринатрина (9)+ТХ, акрилонитрила (название согласно IUPAC) (861)+ТХ, аланикарба (15)+ТХ, алдикарба (16)+ТХ, альдоксикарба (863)+ТХ, альдрина (864)+ТХ, аллетрина (17)+ТХ, аллозамидина (альтернативное название) [CCN]+ТХ, алликсикарба (866)+ТХ, альфа-циперметрина (202)+ТХ, альфа-экдизона (альтернативное название) [CCN]+ТХ, фосфида алюминия (640)+ТХ, амидитиона (870)+ТХ, амидотиоата (872)+ТХ, аминокарба (873)+ТХ, амитона (875)+ТХ, амитона гидрооксалата (875)+ТХ, амитраза (24)+ТХ, анабазина (877)+ТХ, атидатиона (883)+ТХ, AVI 382 (код соединения)+ТХ, AZ 60541 (код соединения)+ТХ, азадирахтина (альтернативное название) (41)+ТХ, азаметифоса (42)+ТХ, азинфос-этила (44)+ТХ, азинфос-метила (45)+ТХ, азотоата (889)+ТХ, дельта-эндотоксинов Bacillus thuringiensis (альтернативное название) (52)+ТХ, гексафторсиликата бария (альтернативное название) [CCN]+ТХ, полисульфида бария (название согласно IUPAC/Химической реферативной службе) (892)+ТХ, бартрина [CCN]+ТХ, Bayer 22/190 (код разработки) (893)+ТХ, Bayer 22408 (код разработки) (894)+ТХ, бендиокарба (58)+ТХ, бенфуракарба (60)+ТХ, бенсултапа (66)+ТХ, бета-цифлутрина (194)+ТХ, бета-циперметрина (203)+ТХ, бифентрина (76)+ТХ, биоаллетрина (78)+ТХ, изомера биоаллетрин-S-циклопентенила (альтернативное название) (79)+ТХ, биоэтанометрина [CCN]+ТХ, биоперметрина (908)+ТХ, биоресметрина (80)+ТХ, простого бис(2-хлорэтилового) эфира (название согласно IUPAC) (909)+ТХ, бистрифлурона (83)+ТХ, буры (86)+ТХ, брофенвалерата (альтернативное название)+ТХ, бромфенвинфоса (914)+ТХ, бромоциклена (918)+ТХ, бром-DDT (альтернативное название) [CCN]+ТХ, бромофоса (920)+ТХ, бромофос-этила (921)+ТХ, буфенкарба (924)+ТХ, бупрофезина (99)+ТХ, бутакарба (926)+ТХ, бутатиофоса (927)+ТХ, бутокарбоксима (103)+ТХ, бутоната (932)+ТХ, бутоксикарбоксима (104)+ТХ, бутилпиридабена (альтернативное название)+ТХ, кадусафоса (109)+ТХ, арсената кальция [CCN]+ТХ, цианида кальция (444)+ТХ, полисульфида кальция (название согласно IUPAC) (111)+ТХ, камфехлора (941)+ТХ, карбанолата (943)+ТХ, карбарила (115)+ТХ, карбофурана (118)+ТХ, дисульфида углерода (название согласно IUPAC/Химической реферативной службе) (945)+ТХ, четыреххлористого углерода (название согласно IUPAC) (946)+ТХ, карбофенотиона (947)+ТХ, карбосульфана (119)+ТХ, картапа (123)+ТХ, гидрохлорида картапа (123)+ТХ, цевадина (альтернативное название) (725)+ТХ, хлорбициклена (960)+ТХ, хлордана (128)+ТХ, хлордекона (963)+ТХ, хлордимеформа (964)+ТХ, гидрохлорида хлордимеформа (964)+ТХ, хлорэтоксифоса (129)+ТХ, хлорфенапира (130)+ТХ, хлорфенвинфоса (131)+ТХ, хлорфлуазурона (132)+ТХ, хлормефоса (136)+ТХ, хлороформа [CCN]+ТХ, хлорпикрина (141)+ТХ, хлорфоксима (989)+ТХ, хлорпразофоса (990)+ТХ, хлорпирифоса (145)+ТХ, хлорпирифос-метила (146)+ТХ, хлортиофоса (994)+ТХ, хромафенозида (150)+ТХ, цинерина I (696)+ТХ, цинерина II (696)+ТХ, цинеринов (696)+ТХ, цис-ресметрина (альтернативное название)+ТХ, цисметрина (80)+ТХ, клоцитрина (альтернативное название)+ТХ, клоэтокарба (999)+ТХ, клозантела (альтернативное название) [CCN]+ТХ, клотианидина (165)+ТХ, ацетоарсенита меди [CCN]+ТХ, арсената меди [CCN]+ТХ, олеата меди [CCN]+ТХ, кумафоса (174)+ТХ, кумитоата (1006)+ТХ, кротамитона (альтернативное название) [CCN]+ТХ, кротоксифоса (1010)+ТХ, круфомата (1011)+ТХ, криолита (альтернативное название) (177)+ТХ, CS 708 (код разработки) (1012)+ТХ, цианофенфоса (1019)+ТХ, цианофоса (184)+ТХ, циантоата (1020)+ТХ, циклетрина [CCN]+ТХ, циклопротрина (188)+ТХ, цифлутрина (193)+ТХ, цигалотрина (196)+ТХ, циперметрина (201)+ТХ, цифенотрина (206)+ТХ, циромазина (209)+ТХ, цитиоата (альтернативное название) [CCN]+ТХ, d-лимонена (альтернативное название) [CCN]+ТХ, d-тетраметрина (альтернативное название) (788)+ТХ, DAEP (1031)+ТХ, дазомета (216)+ТХ, DDT(219)+TX, декарбофурана (1034)+ТХ, дельтаметрина (223)+ТХ, демефиона (1037)+ТХ, демефиона-О (1037)+ТХ, демефиона-S (1037)+ТХ, деметона (1038)+ТХ, деметон-метила (224)+ТХ, деметона-О (1038)+ТХ, деметон-О-метила (224)+ТХ, деметона-S (1038)+ТХ, деметон-S-метила (224)+ТХ, деметон-S-метилсульфона (1039)+ТХ, диафентиурона (226)+ТХ, диалифоса (1042)+ТХ, диамидафоса (1044)+ТХ, диазинона (227)+ТХ, дикаптона (1050)+ТХ, дихлофентиона (1051)+ТХ, дихлорфоса (236)+ТХ, диклифоса (альтернативное название)+ТХ, дикрезила (альтернативное название) [CCN]+ТХ, дикротофоса (243)+ТХ, дицикланила (244)+ТХ, диелдрина (1070)+ТХ, диэтил-5-метилпиразол-3-илфосфата (название согласно IUPAC) (1076)+ТХ, дифлубензурона (250)+ТХ, дилора (альтернативное название) [CCN]+ТХ, димефлутрина [CCN]+ТХ, димефокса (1081)+ТХ, диметана (1085)+ТХ, диметоата (262)+ТХ, диметрина (1083)+ТХ, диметилвинфоса (265)+ТХ, диметилана (1086)+ТХ, динекса (1089)+ТХ, динекс-диклексина (1089)+ТХ, динопропа (1093)+ТХ, диносама (1094)+ТХ, диносеба (1095)+ТХ, динотефурана (271)+ТХ, диофенолана (1099)+ТХ, диоксабензофоса (1100)+ТХ, диоксакарба (1101)+ТХ, диоксатиона (1102)+ТХ, дисульфотона (278)+ТХ, дитикрофоса (1108)+ТХ, DNOC (282)+ТХ, дорамектина (альтернативное название) [CCN]+ТХ, DSP (1115)+ТХ, экдистерона (альтернативное название) [CCN]+ТХ, EI 1642 (код разработки) (1118)+ТХ, эмамектина (291)+ТХ, бензоата эмамектина(291)+ТХ, ЕМРС (1120)+ТХ, эмпентрина (292)+ТХ, эндосульфана (294)+ТХ, эндотиона(1121)+ТХ, эндрина (1122)+ТХ, ЕРВР (1123)+ТХ, EPN (297)+ТХ, эпофенонана (1124)+ТХ, эприномектина (альтернативное название) [CCN]+ТХ, эсфенвалерата (302)+ТХ, этафоса (альтернативное название) [CCN]+ТХ, этиофенкарба (308)+ТХ, этиона (309)+ТХ, этипрола (310)+ТХ, этоат-метила (1134)+ТХ, этопрофоса (312)+ТХ, этилформиата (название согласно IUPAC) [CCN]+ТХ, этил-DDD (альтернативное название) (1056)+ТХ, этилендибромида (316)+ТХ, этилендихлорида (химическое название) (1136)+ТХ, этиленоксида [CCN]+ТХ, этофенпрокса (319)+ТХ, этримфоса (1142)+ТХ, EXD (1143)+ТХ, фамфура (323)+ТХ, фенамифоса (326)+ТХ, феназафлора (1147)+ТХ, фенхлорфоса (1148)+ТХ, фенетакарба (1149)+ТХ, фенфлутрина (1150)+ТХ, фенитротиона (335)+ТХ, фенобукарба (336)+ТХ, феноксакрима (1153)+ТХ, феноксикарба (340)+ТХ, фенпиритрина (1155)+ТХ, фенпропатрина (342)+ТХ, фенпирада (альтернативное название)+ТХ, фенсульфотиона (1158)+ТХ, фентиона (346)+ТХ, фентион-этила [CCN]+ТХ, фенвалерата (349)+ТХ, фипронила (354)+ТХ, флоникамида (358)+ТХ, флубендиамида (регистрационный №CAS: 272451-65-7)+ТХ, флукофурона (1168)+ТХ, флуциклоксурона (366)+ТХ, флуцитрината (367)+ТХ, флуенетила (1169)+ТХ, флуфенерима [CCN]+ТХ, флуфеноксурона (370)+ТХ, флуфенпрокса (1171)+ТХ, флуметрина (372)+ТХ, флувалината (1184)+ТХ, FMC 1137 (код разработки) (1185)+ТХ, фонофоса (1191)+ТХ, форметаната (405)+ТХ, гидрохлорида форметаната (405)+ТХ, формотиона (1192)+ТХ, формпараната (1193)+ТХ, фосметилана (1194)+ТХ, фоспирата (1195)+ТХ, фостиазата (408)+ТХ, фостиэтана (1196)+ТХ, фуратиокарба (412)+ТХ, фуретрина (1200)+ТХ, гамма-цигалотрина (197)+ТХ, гамма-НСН (430)+ТХ, гуазатина (422)+ТХ, ацетатов гуазатина (422)+ТХ, GY-81 (код разработки) (423)+ТХ, галфенпрокса (424)+ТХ, галофенозида (425)+ТХ, НСН (430)+ТХ, HEOD (1070)+ТХ, гептахлора (1211)+ТХ, гептенофоса (432)+ТХ, гетерофоса [CCN]+ТХ, гексафлумурона (439)+ТХ, HHDN (864)+ТХ, гидраметилнона (443)+ТХ, циановодорода (444)+ТХ, гидропрена (445)+ТХ, хиквинкарба (1223)+ТХ, имидаклоприда (458)+ТХ, имипротрина (460)+ТХ, индоксакарба (465)+ТХ, йодметана (название согласно ) (542)+ТХ, IPSP (1229)+ТХ, исазофоса (1231)+ТХ, изобензана (1232)+ТХ, изокарбофоса (альтернативное название) (473)+ТХ, изодрина (1235)+ТХ, изофенфоса (1236)+ТХ, изолана (1237)+ТХ, изопрокарба (472)+ТХ, изопропил-(3-(метоксиаминотиофосфорил)салицилата (название согласно IUPAC) (473)+ТХ, изопротиолана (474)+ТХ, изотиоата (1244)+ТХ, изоксатиона (480)+ТХ, ивермектина (альтернативное название) [CCN]+ТХ, жасмолина I (696)+ТХ, жасмолина II (696)+ТХ, йодофенфоса (1248)+ТХ, ювенильного гормона I (альтернативное название) [CCN]+ТХ, ювенильного гормона II (альтернативное название) [CCN]+ТХ, ювенильного гормона III (альтернативное название) [CCN]+ТХ, келевана (1249)+ТХ, кинопрена (484)+ТХ, лямбда-цигалотрина (198)+ТХ, арсената свинца [CCN]+ТХ, лепимектина (CCN)+ТХ, лептофоса (1250)+ТХ, линдана (430)+ТХ, лиримфоса (1251)+ТХ, люфенурона (490)+ТХ, литидатиона (1253)+ТХ, ж-куменилметилкарбамата (название согласно ) (1014)+ТХ, фосфида магния (название согласно ) (640)+ТХ, малатиона (492)+ТХ, малонобена (1254)+ТХ, мазидокса (1255)+ТХ, мекарбама (502)+ТХ, мекарфона(1258)+ТХ, меназона (1260)+ТХ, мефосфолана (1261)+ТХ, хлорида ртути (513)+ТХ, месульфенфоса (1263)+ТХ, метафлумизона (CCN)+ ТХ, метама (519)+ТХ, метам-калия (альтернативное название) (519)+ТХ, метам-натрия (519)+ТХ, метакрифоса (1266)+ТХ, метамидофоса (527)+ТХ, метансульфонилфторида (название согласно IUPAC/Химической реферативной службе) (1268)+ТХ, метидатиона (529)+ТХ, метиокарба (530)+ТХ, метокротофоса (1273)+ТХ, метомила (531)+ТХ, метопрена (532)+ТХ, метоквин-бутила (1276)+ТХ, метотрина (альтернативное название) (533)+ТХ, метоксихлора (534)+ТХ, метоксифенозида (535)+ТХ, метилбромида (537)+ТХ, метилизотиоцианата (543)+ТХ, метилхлороформа (альтернативное название) [CCN]+ТХ, метиленхлорида [CCN]+ТХ, метофлутрина [CCN]+ТХ, метолкарба (550)+ТХ, метоксадиазона (1288)+ТХ, мевинфоса (556)+ТХ, мексакарбата (1290)+ТХ, милбемектина (557)+ТХ, милбемицин-оксима (альтернативное название) [CCN]+ТХ, мипафокса (1293)+ТХ, мирекса (1294)+ТХ, монокротофоса (561)+ТХ, морфотиона (1300)+ТХ, моксидектина (альтернативное название) [CCN]+ТХ, нафталофоса (альтернативное название) [CCN]+ТХ, наледа (567)+ТХ, нафталина (название согласно /Химической реферативной службе) (1303)+ТХ, NC-170 (код разработки) (1306)+ТХ, NC-184 (код соединения)+ТХ, никотина (578)+ТХ, сульфата никотина (578)+ТХ, нифлуридида (1309)+ТХ, нитенпирама (579)+ТХ, нитиазина (1311)+ТХ, нитрилакарба (1313)+ТХ, комплекса нитрилакарба и хлорида цинка 1:1 (1313)+ТХ, NNI-0101 (код соединения)+ТХ, NNI-0250 (код соединения)+ТХ, норникотина (традиционное название) (1319)+ТХ, новалурона (585)+ТХ, новифлумурона (586)+ТХ, O-5-дихлор-4-йодфенил-O-этилэтилфосфонотиоата (название согласно IUPAC) (1057)+ТХ, O,O-диэтил-O-4-метил-2-оксо-2H-хромен-7-илфосфоротиоата (название согласно IUPAC) (1074)+ТХ, O,O-диэтил-O-6-метил-2-пропилпиримидин-4-илфосфоротиоата (название согласно IUPAC) (1075)+ТХ, O,O,O',O'-тетрапропилдитиопирофосфата (название согласно IUPAC) (1424)+ТХ, олеиновой кислоты (название согласно IUPAC) (593)+ТХ, ометоата (594)+ТХ, оксамила (602)+ТХ, оксидеметон-метила (609)+ТХ, оксидепрофоса (1324)+ТХ, оксидисульфотона (1325)+ТХ, pp'-DDT (219)+ТХ, пара-дихлорбензола [CCN]+ТХ, паратиона (615)+ТХ, паратион-метила (616)+ТХ, пенфлурона (альтернативное название) [CCN]+ТХ, пентахлорфенола (623)+ТХ, пентахлорфениллаурата (название согласно IUPAC) (623)+ТХ, перметрина (626)+ТХ, нефтяных масел (альтернативное название) (628)+ТХ, РН 60-38 (код разработки) (1328)+ТХ, фенкаптона (1330)+ТХ, фенотрина (630)+ТХ, фентоата (631)+ТХ, фората (636)+ТХ, фозалона (637)+ТХ, фосфолана (1338)+ТХ, фосмета (638)+ТХ, фоснихлора (1339)+ТХ, фосфамидона (639)+ТХ, фосфина (название согласно IUPAC) (640)+ТХ, фоксима (642)+ТХ, фоксим-метила (1340)+ТХ, пириметафоса (1344)+ТХ, пиримикарба (651)+ТХ, пиримифос-этила (1345)+ТХ, пиримифос-метила (652)+ТХ, полихлордициклопентадиеновых изомеров (название согласно IUPAC) (1346)+ТХ, полихлортерпенов (традиционное название) (1347)+ТХ, арсенита калия [CCN]+ТХ, тиоцианата калия [CCN]+ТХ, праллетрина (655)+ТХ, прекоцена I (альтернативное название) [CCN]+ТХ, прекоцена II (альтернативное название) [CCN]+ТХ, прекоцена III (альтернативное название) [CCN]+ТХ, примидофоса (1349)+ТХ, профенофоса (662)+ТХ, профлутрина [CCN]+ТХ, промацила (1354)+ТХ, промекарба (1355)+ТХ, пропафоса (1356)+ТХ, пропетамфоса (673)+ТХ, пропоксура (678)+ТХ, протидатиона (1360)+ТХ, протиофоса (686)+ТХ, протоата (1362)+ТХ, протрифенбута [CCN]+ТХ, пиметрозина (688)+ТХ, пираклофоса (689)+ТХ, пиразофоса (693)+ТХ, пиресметрина (1367)+ТХ, пиретрина I (696)+ТХ, пиретрина II (696)+ТХ, пиретринов (696)+ТХ, пиридабена (699)+ТХ, пиридалила (700)+ТХ, пиридафентиона (701)+ТХ, пиримидифена (706)+ТХ, пиримитата (1370)+ТХ, пирипроксифена (708)+ТХ, квассии (альтернативное название) [CCN]+ТХ, квиналфоса (711)+ТХ, квиналфос-метила (1376)+ТХ, квинотиона (1380)+ТХ, квинтиофоса (1381)+ТХ, R-1492 (код разработки) (1382)+ТХ, рафоксанида (альтернативное название) [CCN]+ТХ, ресметрина (719)+ТХ, ротенона (722)+ТХ, RU 15525 (код разработки) (723)+ТХ, RU 25475 (код разработки) (1386)+ТХ, риании (альтернативное название) (1387)+ТХ, рианодина (традиционное название) (1387)+ТХ, сабадиллы (альтернативное название) (725)+ТХ, шрадана (1389)+ТХ, себуфоса (альтернативное название)+ТХ, селамектина (альтернативное название) [CCN]+ТХ, SI-0009 (код соединения)+ТХ, SI-0205 (код соединения)+ТХ, SI-0404 (код соединения)+ТХ, SI-0405 (код соединения)+ТХ, силафлуофена (728)+ТХ, SN 72129 (код разработки) (1397)+ТХ, арсенита натрия [CCN]+ТХ, цианида натрия (444)+ТХ, фторида натрия (название согласно /Химической реферативной службе) (1399)+ТХ, гексафторсиликата натрия (1400)+ТХ, пентахлорфеноксида натрия (623)+ТХ, селената натрия (название согласно ) (1401)+ТХ, тиоцианата натрия [CCN]+ТХ, софамида (1402)+ТХ, спиносада (737)+ТХ, спиромезифена (739)+ТХ, спиротетрамата (CCN)+ТХ, сулкофурона (746)+ТХ, сулкофурон-натрия (746)+ТХ, сульфлурамида (750)+ТХ, сульфотепа (753)+ТХ, сульфурилфторида (756)+ТХ, сульпрофоса (1408)+ТХ, дегтярных масел (альтернативное название) (758)+ТХ, тау-флувалината (398)+ТХ, тазимкарба (1412)+ТХ, TDE (1414)+ТХ, тебуфенозида (762)+ТХ, тебуфенпирада (763)+ТХ, тебупиримфоса (764)+ТХ, тефлубензурона (768)+ТХ, тефлутрина (769)+ТХ, темефоса (770)+ТХ, ТЕРР (1417)+ТХ, тераллетрина (1418)+ТХ, тербама (альтернативное название)+ТХ, тербуфоса (773)+ТХ, тетрахлорэтана [CCN]+ТХ, тетрахлорвинфоса (777)+ТХ, тетраметрина (787)+ТХ, тета-циперметрина (204)+ТХ, тиаклоприда (791)+ТХ, тиафенокса (альтернативное название)+ТХ, тиаметоксама (792)+ТХ, тикрофоса (1428)+ТХ, тиокарбоксима (1431)+ТХ, тиоциклама (798)+ТХ, тиоциклама гидрооксалата (798)+ТХ, тиодикарба (799)+ТХ, тиофанокса (800)+ТХ, тиометона (801)+ТХ, тионазина (1434)+ТХ, тиосултапа (803)+ТХ, тиосултап-натрия (803)+ТХ, турингиенсина (альтернативное название) [CCN]+ТХ, толфенпирада (809)+ТХ, тралометрина (812)+ТХ, трансфлутрина (813)+ТХ, трансперметрина (1440)+ТХ, триамифоса (1441)+ТХ, триазамата (818)+ТХ, триазофоса (820)+ТХ, триазурона (альтернативное название)+ТХ, трихлорфона (824)+ТХ, трихлорметафоса-3(альтернативное название) [CCN]+ТХ, трихлороната (1452)+ТХ, трифенофоса (1455)+ТХ, трифлумурона (835)+ТХ, триметакарба (840)+ТХ, трипрена (1459)+ТХ, вамидотиона (847)+ТХ, ванилипрола [CCN]+ТХ, вератридина (альтернативное название) (725)+ТХ, вератрина (альтернативное название) (725)+ТХ, ХМС(853)+ТХ, ксилилкарба (854)+ТХ, YI-5302 (код соединения)+ТХ, зета-циперметрина (205)+ТХ, зетаметрина (альтернативное название)+ТХ, фосфида цинка (640)+ТХ, золапрофоса (1469) и ZXI 8901 (код разработки) (858)+ТХ, циантранилипрола [736994-63-19]+ТХ, хлорантранилипрола [500008-45-7]+ТХ, циенопирафена [560121-52-0]+ТХ, цифлуметофена [400882-07-7]+ТХ, пирифлуквиназона [337458-27-2]+ТХ, спинеторама [187166-40-1+187166-15-0]+ТХ, спиротетрамата [203313-25-1]+ТХ, сульфоксафлора [946578-00-3]+ТХ, флуфипрола [704886-18-0]+ТХ, меперфлутрина [915288-13-0]+ТХ, тетраметилфлутрина [84937-88-2]+ТХ, трифлумезопирима (раскрытого в WO 2012/092115)+ТХ, флуксаметамида (WO 2007/026965)+ТХ, эпсилон-метофлутрина [240494-71-7]+ТХ, эпсилон-момфлуоротрина [1065124-65-3]+ТХ, флуазаиндолизина [1254304-22-7]+ТХ, хлоропраллетрина [399572-87-3]+ТХ, флуксаметамида [928783-29-3]+ТХ, цигалодиамида [1262605-53-7]+ТХ, тиоксазафена [330459-31-9]+ТХ, брофланилида [1207727-04-5]+ТХ, флуфипрола [704886-18-0]+ТХ, цикланилипрола [1031756-98-5]+ТХ, тетранилипрола [1229654-66-3]+ТХ, гуадипира (описанного в WO2010/060231) +ТХ, циклоксаприда (описанного в WO 2005/077934)+ТХ, спиропидиона+ТХ, афидопиропена+ТХ, флупиримина+ТХ, момфлуоротрина+ТХ, каппа-бифентрина+ТХ, каппа-тефлутрина+ТХ, дихлормезотиаза+ТХ, тетрахлоранилипрола+ТХ, бензпиримоксана+ТХ;
моллюскоцид, выбранный из группы веществ, состоящей из оксида бис(трибутилолова) (название согласно IUPAC) (913)+ТХ, бромацетамида [CCN]+ТХ, арсената кальция [CCN]+ТХ, клоэтокарба (999)+ТХ, ацетоарсенита меди [CCN]+ТХ, сульфата меди (172)+ТХ, фентина (347)+ТХ, фосфата железа(1H) (название согласно ) (352)+ТХ, метальдегида (518)+ТХ, метиокарба (530)+ТХ, никлозамида (576)+ТХ, никлозамид-оламина (576)+ТХ, пентахлорфенола (623)+ТХ, пентахлорфеноксида натрия (623)+ТХ, тазимкарба (1412)+ТХ, тиодикарба (799)+ТХ, оксида трибутилолова (913)+ТХ, трифенморфа (1454)+ТХ, триметакарба (840)+ТХ, ацетата трифенилолова (название согласно IUPAC) (347) и гидроксида трифенилолова (название согласно IUPAC) (347)+ТХ, пирипрола [394730-71-3]+ТХ,
нематоцид, выбранный из группы веществ, состоящей из AKD-3088 (код соединения)+ТХ, 1,2-дибром-3-хлорпропана (название согласно IUPAC/Химической реферативной службе) (1045)+ТХ, 1,2-дихлорпропана (название согласно /Химической реферативной службе) (1062)+ТХ, 1,2-дихлорпропана с 1,3-дихлорпропеном (название согласно IUPAC) (1063)+ТХ, 1,3-дихлорпропена (233)+ТХ, 3,4-дихлортетрагидротиофена 1,1-диоксида (название согласно /Химической реферативной службе) (1065)+ТХ, 3-(4-хлорфенил)-5-метилроданина (название согласно OUPAC) (980)+ТХ, 5-метил-6-тиоксо-1,3,5-тиадиазинан-3-илуксусной кислоты (название согласно IUPAC) (1286)+ТХ, 6-изопентениламинопурина (альтернативное название) (210)+ТХ, абамектина (1)+ТХ, ацетопрола [CCN]+ТХ, аланикарба (15)+ТХ, алдикарба (16)+ТХ, альдоксикарба (863)+ТХ, AZ 60541 (код соединения)+ТХ, бенклотиаза [CCN]+ТХ, беномила (62)+ТХ, бутилпиридабена (альтернативное название)+ТХ, кадусафоса (109)+ТХ, карбофурана (118)+ТХ, дисульфида углерода (945)+ТХ, карбосульфана (119)+ТХ, хлорпикрина (141)+ТХ, хлорпирифоса (145)+ТХ, клоэтокарба (999)+ТХ, цитокининов (альтернативное название) (210)+ТХ, дазомета (216)+ТХ, DBCP (1045)+ТХ, DCIP(218)+TX, диамидафоса (1044)+ТХ, дихлофентиона (1051)+ТХ, диклифоса (альтернативное название)+ТХ, диметоата (262)+ТХ, дорамектина (альтернативное название) [CCN]+ТХ, эмамектина (291)+ТХ, бензоата эмамектина (291)+ТХ, эприномектина (альтернативное название) [CCN]+ТХ, это профоса (312)+ТХ, этилендибромида (316)+ТХ, фенамифоса (326)+ТХ, фенпирада (альтернативное название)+ТХ, фенсульфотиона (1158)+ТХ, фостиазата (408)+ТХ, фостиэтана (1196)+ТХ, фурфураля (альтернативное название) [CCN]+ТХ, GY-81 (код разработки) (423)+ТХ, гетерофоса [CCN]+ТХ, йодметана (название согласно IUPAC) (542)+ТХ, изамидофоса (1230)+ТХ, исазофоса (1231)+ТХ, ивермектина (альтернативное название) [CCN]+ТХ, кинетина (альтернативное название) (210)+ТХ, мекарфона (1258)+ТХ, метама (519)+ТХ, метам-калия (альтернативное название) (519)+ТХ, метам-натрия (519)+ТХ, метилбромида (537)+ТХ, метилизотиоцианата (543)+ТХ, милбемицин-оксима (альтернативное название) [CCN]+ТХ, моксидектина (альтернативное название) [CCN]+ТХ, композиции с Myrothecium verrucaria (альтернативное название) (565)+ТХ, NC-184 (код соединения)+ТХ, оксамила (602)+ТХ, фората (636)+ТХ, фосфамидона (639)+ТХ, фосфокарба [CCN]+ТХ, себуфоса (альтернативное название)+ТХ, селамектина (альтернативное название) [CCN]+ТХ, спиносада (737)+ТХ, тербама (альтернативное название)+ТХ, тербуфоса (773)+ТХ, тетрахлортиофена (название согласно IUPAC/Химической реферативной службе) (1422)+ТХ, тиафенокса (альтернативное название)+ТХ, тионазина (1434)+ТХ, триазофоса (820)+ТХ, триазурона (альтернативное название)+ТХ, ксиленолов [CCN]+ТХ, YI-5302 (код соединения) и зеатина (альтернативное название) (210)+ТХ, флуэнсульфона [318290-98-1]+ТХ, флуопирама+ТХ,
ингибитор нитрификации, выбранный из группы веществ, состоящей из этилксантата калия [CCN] и нитрапирина (580)+ТХ;
активатор роста растения, выбранный из группы веществ, состоящей из ацибензолара (6)+ТХ, ацибензолар-S-метила (6)+ТХ, пробеназола (658) и экстракта Reynoutria sachalinensis (альтернативное название) (720)+ТХ,
родентицид, выбранный из группы веществ, состоящей из 2-изовалерилиндан-1,3-диона (название согласно ) (1246)+ТХ, 4-(хиноксалин-2-иламино)бензолсульфонамида (название согласно IUPAC) (748)+ТХ, альфа-хлоргидрина [CCN]+ТХ, фосфида алюминия (640)+ТХ, ANTU (880)+ТХ, оксида мышьяка (882)+ТХ, карбоната бария (891)+ТХ, бистиосеми (912)+ТХ, бродифакума (89)+ТХ, бромадиолона (91)+ТХ, брометалина (92)+ТХ, цианида кальция (444)+ТХ, хлоралозы (127)+ТХ, хлорофацинона (140)+ТХ, холе кальциферола (альтернативное название) (850)+ТХ, кумахлора (1004)+ТХ, кумафурила (1005)+ТХ, куматетралила (175)+ТХ, кримидина (1009)+ТХ, дифенакума (246)+ТХ, дифетиалона (249)+ТХ, дифацинона (273)+ТХ, эргокальциферола (301)+ТХ, флокумафена (357)+ТХ, фторацетамида (379)+ТХ, флупропадина (1183)+ТХ, гидрохлорида флупропадина (1183)+ТХ, гамма-НСН (430)+ТХ, НСН (430)+ТХ, циановодорода (444)+ТХ, йодметана (название согласно IUPAC) (542)+ТХ, линдана (430)+ТХ, фосфида магния (название согласно IUPAC) (640)+ТХ, метилбромида (537)+ТХ, норбормида (1318)+ТХ, фосацетима (1336)+ТХ, фосфина (название согласно IUPAC) (640)+ТХ, фосфора [CCN]+ТХ, пиндона (1341)+ТХ, арсенита калия [CCN]+ТХ, пиринурона (1371)+ТХ, сциллирозида (1390)+ТХ, арсенита натрия [CCN]+ТХ, цианида натрия (444)+ТХ, фторацетата натрия (735)+ТХ, стрихнина (745)+ТХ, сульфата таллия [CCN]+ТХ, варфарина (851) и фосфида цинка (640)+ТХ, синергист, выбранный из группы веществ, состоящей из 2-(2-бутоксиэтокси)этилпиперонилата (название согласно IUPAC) (934)+ТХ, 5-(1,3-бензодиоксол-5-ил)-3-гексилциклогекс-2-енона (название согласно IUРАС) (903)+ТХ, фарнезола с неролидолом (альтернативное название) (324)+ТХ, МВ-599 (код разработки) (498)+ТХ, MGK 264 (код разработки) (296)+ТХ, пиперонилбутоксида (649)+ТХ, пипротала(1343)+ТХ, изомера пропила (1358)+ТХ, S421 (код разработки) (724)+ТХ, сезамекса (1393)+ТХ, сезасмолина (1394) и сульфоксида (1406)+ТХ,
средство для отпугивания животных, выбранное из группы веществ, состоящей из антрахинона (32)+ТХ, хлоралозы (127)+ТХ, нафтената меди [CCN]+ТХ, оксихлорида меди (171)+ТХ, диазинона (227)+ТХ, дициклопентадиена (химическое название) (1069)+ТХ, гуазатина (422)+ТХ, ацетатов гуазатина (422)+ТХ, метиокарба (530)+ТХ, пиридин-4-амина (название согласно IUPAC) (23)+ТХ, тирама (804)+ТХ, триметакарба (840)+ТХ, нафтената цинка [CCN] и зирама (856)+ТХ,
вируцид, выбранный из группы веществ, состоящей из иманина (альтернативное название) [CCN] и рибавирина (альтернативное название) [CCN]+ТХ, защитное средство для ран, выбранное из группы веществ, состоящей из оксида ртути (512)+ТХ, октилинона (590) и тиофанат-метила (802)+ТХ,
и биологически активные соединения, выбранные из группы веществ, состоящей из азаконазола (60207-31-0]+ТХ, битертанола [70585-36-3]+ТХ, бромуконазола [116255-48-2]+ТХ, ципроконазола [94361-06-5]+ТХ, дифеноконазола [119446-68-3]+ТХ, диниконазола [83657-24-3]+ТХ, эпоксиконазола [106325-08-0]+ТХ, фенбуконазола [114369-43-6]+ТХ, флуквинконазола [136426-54-5]+ТХ, флусилазола [85509-19-9]+ТХ, флутриафола [76674-21-0]+ТХ, гексаконазола [79983-71-4]+ТХ, имазалила [35554-44-0]+ТХ, имибенконазола [86598-92-7]+ТХ, ипконазола [125225-28-7]+ТХ, метконазола [125116-23-6]+ТХ, миклобутанила [88671-89-0]+ТХ, пефуразоата [101903-30-4]+ТХ, пенконазола [66246-88-6]+ТХ, протиоконазола [178928-70-6]+ТХ, пирифенокса [88283-41-4]+ТХ, прохлораза [67747-09-5]+ТХ, пропиконазола [60207-90-1]+ТХ, симеконазола [149508-90-7]+ТХ, тебуконазола [107534-96-3]+ТХ, тетраконазола [112281-77-3]+ТХ, триадимефона [43121-43-3]+ТХ, триадименола [55219-65-3]+ТХ, трифлумизола [99387-89-0]+ТХ, тритиконазола [131983-72-7]+ТХ, анцимидола [12771-68-5]+ТХ, фенаримола [60168-88-9]+ТХ, нуаримола [63284-71-9]+ТХ, бупиримата [41483-43-6]+ТХ, диметиримола [5221-53-4]+ТХ, этиримола [23947-60-6]+ТХ, додеморфа [1593-77-7]+ТХ, фенпропидина [67306-00-7]+ТХ, фенпропиморфа [67564-91-4]+ТХ, спироксамина [118134-30-8]+ТХ, тридеморфа [81412-43-3]+ТХ, ципродинила [121552-61-2]+ТХ, мепанипирима [110235-47-7]+ТХ, пириметанила [53112-28-0]+ТХ, фенпиклонила [74738-17-3]+ТХ, флудиоксонила [131341-86-1]+ТХ, беналаксила [71626-11-4]+ТХ, фуралаксила [57646-30-7]+ТХ, металаксила [57837-19-1]+ТХ, R-металаксила [70630-17-0]+ТХ, офураса [58810-48-3]+ТХ, оксадиксила [77732-09-3]+ТХ, беномила [17804-35-2]+ТХ, карбендазима [10605-21-7]+ТХ, дебакарба [62732-91-6]+ТХ, фуберидазола [3878-19-1]+ТХ, тиабендазола [148-79-8]+ТХ, хлозолината [84332-86-5]+ТХ, дихлозолина [24201-58-9]+ТХ, ипродиона [36734-19-7]+ТХ, миклозолина [54864-61-8]+ТХ, процимидона [32809-16-8]+ТХ, винклозолина [50471-44-8]+ТХ, боскалида [188425-85-6]+ТХ, карбоксина [5234-68-4]+ТХ, фенфурама [24691-80-3]+ТХ, флутоланила [66332-96-5]+ТХ, мепронила [55814-41-0]+ТХ, оксикарбоксина [5259-88-1]+ТХ, пентиопирада [183675-82-3]+ТХ, тифлузамида [130000-40-7]+ТХ, гуазатина [108173-90-6]+ТХ, додина [2439-10-3] [112-65-2] (свободное основание)+ТХ, иминоктадина [13516-27-3]+ТХ, азоксистробина [131860-33-8]+ТХ, димоксистробина [149961-52-4]+ТХ, энестробурина {Proc. ВСРС, Int. Congr., Glasgow, 2003, 1, 93}+ТХ, флуоксастробина [361377-29-9]+ТХ, крезоксим-метила [143390-89-0]+ТХ, метоминостробина [133408-50-1]+ТХ, трифлоксистробина [141517-21-7]+ТХ, оризастробина [248593-16-0]+ТХ, пикоксистробина [117428-22-5]+ТХ, пираклостробина [175013-18-0]+ТХ, фербама [14484-64-1]+ТХ, манкозеба [8018-01-7]+ТХ, манеба [12427-38-2]+ТХ, метирама [9006-42-2]+ТХ, пропинеба [12071-83-9]+ТХ, тирама [137-26-8]+ТХ, зинеба [12122-67-7]+ТХ, зирама [137-30-4]+ТХ, каптафола [2425-06-1]+ТХ, каптана [133-06-2]+ТХ, дихлофлуанида [1085-98-9]+ТХ, фторимида [41205-21-4]+ТХ, фолпета [133-07-3]+ТХ, толилфлуанида [731-27-1]+ТХ, бордосской смеси [8011-63-0]+ТХ, гидроксида меди [20427-59-2]+ТХ, оксихлорида меди [1332-40-7]+ТХ, сульфата меди [7758-98-7]+ТХ, оксида меди [1317-39-1]+ТХ, манкоппера [53988-93-5]+ТХ, оксината меди [10380-28-6]+ТХ, динокапа [131-72-6]+ТХ, нитротал-изопропила [10552-74-6]+ТХ, эдифенфоса [17109-49-8]+ТХ, ипробенфоса [26087-47-8]+ТХ, изопротиолана [50512-35-1]+ТХ, фосдифена [36519-00-3]+ТХ, пиразофоса [13457-18-6]+ТХ, толклофос-метила [57018-04-9]+ТХ, ацибензолар-8-метила [135158-54-2]+ТХ, анилазина [101-05-3]+ТХ, бентиаваликарба [413615-35-7]+ТХ, бластицидина-S [2079-00-7]+ТХ, хинометионата [2439-01-2]+ТХ, хлоронеба [2675-77-6]+ТХ, хлороталонила [1897-45-6]+ТХ, цифлуфенамида [180409-60-3]+ТХ, цимоксанила[57966-95-7]+ТХ, дихлона[117-80-6]+ТХ, диклоцимета [139920-32-4]+ТХ, дикломезина [62865-36-5]+ТХ, диклорана [99-30-9]+ТХ, диэтофенкарба [87130-20-9]+ТХ, диметоморфа [110488-70-5]+ТХ, SYP-LI90 (флуморфа) [211867-47-9]+ТХ, дитианона[3347-22-6]+ТХ, этабоксама[162650-77-3]+ТХ, этридиазола [2593-15-9]+ТХ, фамоксадона [131807-57-3]+ТХ, фенамидона [161326-34- 7]+ТХ, феноксанила [115852-48-7]+ТХ, фентина [668-34-8]+ТХ, феримзона[89269-64-7]+ТХ, флуазинама[79622-59-6]+ТХ, флуопиколида [239110-15-7]+ТХ, флусульфамида [106917-52-6]+ТХ, фенгексамида [126833-17-8]+ТХ, фосетил-алюминия [39148-24-8]+ТХ, химексазола [10004-44-1]+ТХ, ипроваликарба [140923-17-7]+ТХ, IKF-916 (циазофамида) [120116-88-3]+ТХ, касугамицина [6980-18-3]+ТХ, метасульфокарба [66952-49-6]+ТХ, метрафенона [220899-03-6]+ТХ, пенцикурона [66063-05-6]+ТХ, фталида [27355-22-2]+ТХ, полиоксинов [11113-80-7]+ТХ, пробеназола [27605-76-1]+ТХ, пропамокарба [25606-41-1]+ТХ, проквиназида [189278-12-4]+ТХ, пироквилона [57369-32-1]+ТХ, квиноксифена [124495-18-7]+ТХ, квинтозена [82-68-8]+ТХ, серы [7704-34-9]+ТХ, тиадинила [223580-51-6]+ТХ, триазоксида [72459-58-6]+ТХ, трициклазола [41814-78-2]+ТХ, трифорина [26644-46-2]+ТХ, валидамицина [37248-47-8]+ТХ, зоксамида (RH7281) [156052-68-5]+ТХ, мандипропамида [374726-62-2]+ТХ, изопиразама [881685-58-1]+ТХ, седаксана [874967-67-6]+ТХ, (9-дихлорметилен-1,2,3,4-тетрагидро-1,4-метанонафтален-5-ил)-амида 3-дифторметил-1-метил-1H-пиразол-4-карбоновой кислоты (раскрытого в WO 2007/048556)+ТХ, (3',4',5'-трифторбифенил-2-ил)-амида 3-дифторметил-1-метил-1H-пиразол-4-карбоновой кислоты (раскрытого в WO 2006/087343)+ТХ, [(3S,4R,4aR,6S,6aS,12R,12aS,12b5-3-[(циклопропилкарбонил)окси]-1,3,4,4а,5,6,6а,12,12а,12b-декагидро-6,12-дигидрокси-4,6а,12b-триметил-11-оксо-9-(3-пиридинил)-2H,11H-нафто[2,1-b]пирано[3,4-е]пиран-4-ил]метилциклопропанкарбоксилата [915972-17-7]+ТХ и 1,3,5-триметил-N-(2-метил-1-оксопропил)-N-[3-(2-метилпропил)-4-[2,2,2-трифтор-1-метокси-1-(трифторметил)этил]фенил]-1Н-пиразол-4-карбоксамида [926914-55-8]+ТХ, ланкотриона [1486617-21-3]+ТХ, флорпирауксифена [943832-81-3]+ТХ, ипфентрифлуконазола [1417782-08-1]+ТХ, мефентрифлуконазола [1417782-03-6]+ТХ, квинофумелина [861647-84-9]+ТХ, хлоропраллетрина [399572-87-3]+ТХ, цигалодиамида [1262605-53-7]+ТХ, флуазаинд о лизина [1254304-22-7]+ТХ, флуксаметамида [928783-29-3]+ТХ, эпсилон-метофлутрина [240494-71-7]+ТХ, эпсилон-момфлуоротрина [1065124-65-3]+ТХ, пидифлуметофена [1228284-64-7]+ТХ, каппа-бифентрина [439680-76-9]+ТХ, брофланилида [1207727-04-5]+ТХ, дихлоромезотиаза [1263629-39-5]+ТХ, дипиметитрона [16114-35-5]+ТХ, пиразифлумида [942515-63-1]+ТХ и каппа-тефлутрина [391634-71-2]+ТХ, фенпикоксамида [517875-34-2]+ТХ; флуфенпирролидона+ТХ, бензпиримоксана [1449021-97-9]+ТХ; изоциклосерама+ТХ, рескалура [64309-03-1]+ТХ; аминопирифена [1531626-08-0]+ТХ; и
микроорганизмы, в том числе Acinetobacter hvoffii+ТХ, Acremonium alternatum+ТХ+ТХ, Acremonium cephalosporium+ТХ+ТХ, Acremonium diospyri+ТХ, Acremonium obclavatum+ТХ, Adoxophyes orana gramdovirus (AdoxGV) (Capex®)+TX, Agrobacterium radiobacter, штамм K84 (Galltrol-A®)+TX, Alternaria alternate+TX, Alternaria cassia+TX, Alternaria destruens (Smolder®)+TX, Ampelomyces quisqualis (AQ10®)+TX, Aspergillus flams AF36 (AF36®)+TX, Aspergillus flavus NRRL 21882 (Aflaguard®)+TX, Aspergillus spp.+TX, Aureobasidiumpullulans+TX, Azospirillum+TX, (MicroAZ®+TX, T.AZO B®)+TX, Azotobacter+TX, Azotobacter chroocuccum (Azotomeal®)+TX, цисты Azotobacter (Bionatural Blooming Blossoms®)+TX, Bacillus amyloliquefaciens+TX, Bacillus cereus+TX, Bacillus chitinosporus, штамм CM-1+TX, Bacillus chitinosporus, штамм AQ746+TX, Bacillus licheniformis, штамм HB-2 (Biostart™ Rhizoboost®)+TX, Bacillus licheniformis, штамм 3086 (EcoGuard®+TX, Green Releaf®)+TX, Bacillus circulans+TX, Bacillus flrmus (BioSafe®+TX, BioNem-WP®+ТХ, VOTiVO®)+ТХ, Bacillus firmus, штамм 1-1582+ТХ, Bacillus macerans+ТХ, Bacillus marismortui+TX, Bacillus megaterium+TX, Bacillus mycoides, штамм AQ726+TX, Bacillus papillae (Milky Spore Powder®)+TX, Bacillus pumilus spp.+TX, Bacillus pumilus, штамм GB34 (Yield Shield®)+TX, Bacillus pumilus, штамм AQ717+TX, Bacillus pumilus, штамм QST 2808 (Sonata®+TX, Ballad Plus®)+TX, Bacillus spahericus (VectoLex®)+TX, Bacillus spp.+TX, Bacillus spp., штамм AQ175+TX, Bacillus spp., штамм AQ177+TX, Bacillus spp., штамм AQ178+TX, Bacillus subtilis, штамм QST 713 (CEASE®+TX, Serenade®+TX, Rhapsody®)+TX, Bacillus subtilis, штамм QST 714 (JAZZ®)+TX, Bacillus subtilis, штамм AQ153+TX, Bacillus subtilis, штамм AQ743+TX, Bacillus subtilis, штамм QST3002+TX, Bacillus subtilis, штамм QST3004+TX, Bacillus subtilis вар amyloliquefaciens, штамм FZB24 (Taegro®+TX, Rhizopro®)+TX, Cry 2Ae Bacillus thuringiensis+TX, CrylAb Bacillus thuringiensis+TX, Bacillus thuringiensis aizawai GC 91 (Agree®)+TX, Bacillus thuringiensis israelensis (BMP 123®+TX, Aquabac®+TX, VectoBac®)+TX, Bacillus thuringiensis kurstaki (Javelin®+TX, Deliver®+TX, CryMax®+TX, Bonide®+TX, Scutella WP®+TX, Turilav WP®+TX, Astuto®+TX, Dipel WP®+TX, Biobit®+TX, Foray®)+TX, Bacillus thuringiensis kurstaki BMP 123 (Baritone®)+TX, Bacillus thuringiensis kurstaki HD-1 (Bioprotec-CAF/3P®)+TX, Bacillus thuringiensis, штамм BD№32+TX, Bacillus thuringiensis, штамм AQ52+TX, Bacillus thuringiensis вар aizawai (XenTari®+TX, DiPel®)+TX, разновидности бактерий (GROWMEND®+TX, GROWSWEET®+TX, Shootup®)+TX, бактериофаг Clavipacter michiganensis (AgriPhage®)+TX, Bakflor®+TX, Beauveria bassiana (Beaugenic®+TX, Brocaril WP®)+TX, Beauveria bassiana GHA (Mycotrol ES®+TX, Mycotrol O®+TX, BotaniGuard®)+TX, Beauveria brongniartii (Engerlingspilz®+TX, Schweizer Beauveria®+TX, Melocont®)+TX, Beauveria spp.+TX, Botrytis cineria+TX, Bradyrhizobium japonicum (TerraMax®)+TX, Brevibacillus brevis+TX, Bacillus thuringiensis tenebrionis (Novodor®)+TX, BtBooster+TX, Burkholderia cepacia (Deny®+TX, Intercept®+TX, Blue Circle®)+TX, Burkholderia gladii+TX, Burkholderia gladioli+TX, Burkholderia spp.+TX, грибок полевого бодяка (CBH Canadian Bioherbicide®)+TX, Candida butyri+TX, Candida famata+TX, Candida fructus+TX, Candida glabrata+TX, Candida guilliermondii+TX, Candida melibiosica+TX, Candida oleophila, штамм О+TX, Candida parapsilosis+TX, Candida pelliculosa+TX, Candida pulcherrima+TX, Candida reukaufii+TX, Candida saitoana (Bio-Coat®+TX, Biocure®)+TX, Candida sake+TX, Candida spp.+TX, Candida tenius+TX, Cedecea dravisae+TX, Cellulomonas flavigena+TX, Chaetomium cochliodes (Nova-Cide®)+TX, Chaetomium globosum (Nova-Cide®)+TX, Chromobacterium subtsugae, штамм PRAA4-1T (Grandevo®)+TX, Cladosporium cladosporioides+TX, Cladosporium oxysporum+TX, Cladosporium chlorocephalum+TX, Cladosporium spp.+TX, Cladosporium tenuissimum+TX, Clonostachys rosea (EndoFine®TX, Colletotrichum acutatum+TX, Coniothyrium minitans (Cotans WG®)+TX, Coniothyrium spp.+TX, Cryptococcus albidus (YIELDPLUS®)+TX, Cryptococcus humicola+TX, Cryptococcus infirmo-miniatus+TX, Cryptococcus laurentii+TX, Cryptophlebia leucotreta granulovirus (Cryptex®)+TX, Cupriavidus campinensis+TX, Cydia pomonella granulovirus (CYD-X®)+TX, Cydia pomonella granulovirus (Madex®+TX, Madex Plus®+TX, Madex Max/Carpovirusine®)+TX, Cylindrobasidium laeve (Stumpout®)+TX, Cylindrocladium+TX, Debaryomyces hansenii+TX, Drechslera hawaiinensis+TX, Enterobacter cloacae+TX, Enterobacteriaceae+TX, Entomophtora virulenta (Vektor®)+TX, Epicoccum nigrum+TX, Epicoccum purpurascens+TX, Epicoccum spp.+TX, Filobasidium floriforme+TX, Fusarium acuminatum+TX, Fusarium chlamydosporum+TX, Fusarium oxysporum (Fusaclean®/Biofox C®)+TX, Fusarium proliferatum+TX, Fusarium spp.+TX, Galactomyces geotrichum+TX, Gliocladium catenulatum (Primastop®+TX, Prestop®)+TX, Gliocladium roseum+TX, Gliocladium spp.(SoilGard®)+TX, Gliocladium virens (Soilgard®)+TX, Granulovirus (Granupom®)+TX, Halobacillus halophilus+TX, Halobacillus litoralis+TX, Halobacillus trueperi+TX, Halomonas spp.+TX, Halomonas subglaciescola+TX, Halovibrio variabilis+TX, Hanseniaspora uvarum+TX, вирус ядерного полиэдроза Helicoverpa armigera (Helicovex®)+TX, вирус ядерного пситэщюъа. Helicoverpa zea (Gemstar®)+TX, изофлавон - формононетин (Myconate®)+TX, Kloeckera apiculata+TX, Kloeckera spp.+TX, Lagenidium giganteum (Laginex®)+TX, Lecanicillium longisporum (Vertiblast®)+TX, Lecanicillium muscarium (Vertikil®)+TX, вирус ядерного полиэдроза Lymantria Dispar (Disparvirus®)+TX, Marinococcus halophilus+TX, Meira geulakonigii+TX, Metarhizium anisopliae (Met52®)+TX, Metarhizium anisopliae (Destruxin WP®)+TX, Metschnikowia fruticola (Shemer®)+TX, Metschnikowia pulcherrima+TX, Microdochium dimerum (Antibot®)+TX, Micromonospora coerulea+TX, Microsphaeropsis ochracea+TX, Muscodor albus 620 (Muscudor®)+TX, Muscodor roseus, штамм A3-5+TX, Mycorrhizae spp.(AMykor®+TX, Root Maximizer®)+TX, Myrothecium verrucaria, штамм AARC-0255 (DiTera®)+TX, BROS PLUS®+TX, Ophiostoma piliferum, штамм D97 (Sylvanex®)+TX, Paecilomyces farinosus+TX, Paecilomyces fumosoroseus (PFR-97®+TX, PreFeRal®)+TX, Paecilomyces linacinus (Biostat WP®)+TX, Paecilomyces lilacinus, штамм 251 (MeloCon WGi)+TX, Paenibacillus polymyxa+TX, Pantoea agglomerans (BlightBan C9-1®)+TX, Pantoea spp.+TX, Pasteuria spp.(Econem®)+TX, Pasteuria nishizawae+TX, Penicillium aurantiogriseum+TX, Penicillium billai (Jumpstart®+TX, TagTeam®)+TX, Penicillium brevicompactum+TX, Penicillium frequentans+TX, Penicillium griseqfulvum+TX, Penicillium purpurogenum+TX, Penicillium spp.+TX, Penicillium viridicatum+TX, Phlebiopsis gigantean (Rotstop®)+TX, фосфат солюбилизирующие бактерии (Phosphomeal®)+TX, Phytophthora cryptogea+TX, Phytophthora palmivora (Devine®)+TX, Pichia anomala+TX, Pichia guilermondii+TX, Pichia membranaefaciens+TX, Pichia onychis+TX, Pichia stipites+TX, Pseudomonas aeruginosa+TX, Pseudomonas aureofasciens (Spot-Less Biofungicide®)+TX, Pseudomonas cepacia+TX, Pseudomonas chlororaphis (AtEze®)+TX, Pseudomonas corrugate+TX, Pseudomonas fluorescens, штамм A506 (BlightBan A506®)+TX, Pseudomonas putida+TX, Pseudomonas reactans+TX, Pseudomonas spp.+TX, Pseudomonas syringae (Bio-Save®)+TX, Pseudomonas viridiflava+TX, Pseudomons fluorescens (Zequanox®)+TX, P seudozyma flocculosa, штамм PF-A22 UL (Sporodex L®)+TX, Puccinia canaliculata+TX, Puccinia thlaspeos (Wood Warrior®)+TX, Pythium paroecandrum+TX, Pyihium oligandrum (Polygandron®+TX, Polyversum®)+TX, Pyihium periplocum+TX, Rhanella aquatilis+TX, Rhanella spp.+TX, Rhizobia (Dormal®+TX, Vault®)+TX, Rhizoctonia+TX, Rhodococcus globerulus, штамм AQ719+TX, Rhodosporidium diobovatum+TX, Rhodosporidium toruloides+TX, Rhodotorula spp.+TX, Rhodotorula glutinis+TX, Rhodotorula graminis+TX, Rhodotorula mucilagnosa+TX, Rhodotorula rubra+TX, Saccharomyces cerevisiae+TX, Salinococcus roseus+TX, Sclerotinia minor+TX, Sclerotinia minor (SARRITOR®)+TX, Scytalidium spp.+TX, Scytalidium uredinicola+TX, вирус ядерного полиэдроза Spodoptera exigua (Spod-X®+TX, Spexit®)+TX, Serratia marcescens+TX, Serratia plymuthica+TX, Serratia spp.+TX, Sordaria fimicola+TX, вирус ядерного полиэдроза Spodoptera littoralis (Littovir®)+TX, Sporobolomyces roseus+TX, Stenotrophomonas maltophilia+TX, Streptomyces ahygroscopicus+TX, Streptomyces albaduncus+TX, Streptomyces exfoliates+TX, Streptomyces galbus+TX, Streptomyces griseoplanus+TX, Streptomyces griseoviridis (Mycostop®)+TX, Streptomyces lydicus (Actinovate®)+TX, Streptomyces lydicus WYEC-108 (ActinoGrow®)+TX, Streptomyces violaceus+TX, Tilletiopsis minor+TX, Tilletiopsis spp.+TX, Trichoderma asperellum (T34 Biocontrol®)+TX, Trichoderma gamsii (Tenet®)+TX, Trichoderma atroviride (Plantmate®)+TX, Trichoderma hamatum TH 382+TX, Trichoderma harzianum rifai (Mycostar®)+TX, Trichoderma harzianum T-22 (Trianum-P®+TX, PlantShield HC®+TX, RootShield®+TX, Trianum-G®)+ТХ, Trichoderma harzianum T-39 (Trichodex®)+TX, Trichoderma inhamatum+TX, Trichoderma koningii+TX, Trichoderma spp.LC 52 (Sentinel®)+TX, Trichoderma lignorum+TX, Trichoderma longibrachiatum+TX, Trichoderma polysporum (Binab T®)+TX, Trichoderma taxi+TX, Trichoderma virens+TX, Trichoderma virens (ранее Gliocladium virens GL-21) (SoilGuard®)+TX, Trichoderma viride+TX, Trichoderma viride, штамм ICC 080 (Remedier®)+TX, Trichosporon pullulans+TX, Trichosporon spp.+TX, Trichothecium spp.+TX, Trichothecium roseum+TX, Typhula phacorrhiza, штамм 94670+TX, Typhula phacorrhiza, штамм 94671+TX, Ulocladium atrum+TX, Ulocladium oudemansii (Botry-Zen®)+TX, Ustilago maydis+TX, различные бактерии и дополнительные микроэлементы (Natural II®)+ТХ, различные грибы (Millennium Microbes®)+ТХ, Verticillium chlamydosporium+ТХ, Verticillium lecanii (Mycotal®+TX, Vertalec®)+TX, Vip3Aa20 (VTPtera®)+TX, Virgibaclillus marismortui+TX, Xanthomonas campestris pv. Poae (Camperico®)+TX, Xenorhabdus bovienii+TX, Xenorhabdus nematophilus; и
экстракты растений, в том числе сосновое масло (Retenol®)+ТХ, азадирахтин (Plasma Neem Oil®+ТХ, AzaGuard®+ТХ, MeemAzal®+ТХ, Molt-X®+ТХ, Botanical IGR (Neemazad®+TX, Neemix®)+TX, каноловое масло (Lilly Miller Vegol®)+TX, Chenopodium ambrosioides near ambrosioides (Requiem®)+TX, экстракт Chrysanthemum (Crisant®)+TX, экстракт масла маргозы (Trilogy®)+TX, эфирные масла Labiatae (Botania®)+TX, экстракты масла гвоздики, розмарина, перечной мяты и тимьяна (Garden insect killer®)+ТХ, глицинбетаин (Greenstim®)+ТХ, чеснок+ТХ, масло лемонграсса (GreenMatch®)+ТХ, масло маргозы+ТХ, Nepeta cataria (масло котовника кошачьего)+ТХ, Nepeta catarina+ТХ, никотин+ТХ, масло душицы (MossBuster®)+ТХ, масло Pedaliaceae (Nematon®)+ТХ, пиретрум+ТХ, Quillaja saponaria (NemaQ®)+ТХ, Reynoutria sachalinensis (Regalia®+TX, Sakalia®)+TX, ротенон (Eco Roten®)+TX, экстракт растения Rutaceae (Soleo®)+TX, соевое масло (Ortho ecosense®)+TX, масло чайного дерева (Timorex Gold®)+TX, масло тимьяна+TX, AGNIQUE® MMF+TX, BugOil®+TX, смесь экстрактов розмарина, кунжута, перечной мяты, тимьяна и корицы (EF 300®)+ТХ, смесь экстрактов гвоздики, розмарина и перечной мяты (EF 400®)+ТХ, смесь гвоздики, перечной мяты, масла чеснока и мяты (Soil Shot®)+ТХ, каолин (Screen®)+ТХ, глюкан, который запасают бурые водоросли, (Laminarin®); и
феромоны, в том числе феромон листовертки черноголовой (3М Sprayable Blackheaded Fireworm Pheromone®)+TX, феромон яблоневой плодожорки (Paramount dispenser-(CM)/ Isomate C-Plus®)+TX, феромон листовертки виноградной (3M MEC-GBM Sprayable Pheromone®)+TX, феромон листовертки (3М MEC - LR Sprayable Pheromone®)+TX, мускамон (Snip7 Fly Bait®+TX, Starbar Premium Fly Bait®)+TX, феромон листовертки восточной персиковой (3М oriental fruit moth sprayable pheromone®)+TX, феромон стеклянницы персиковой (Isomate-P®)+TX, феромон томатной острицы (3М Sprayable pheromone®)+ТХ, Entostat в виде порошка (экстракт пальмового дерева) (Exosex СМ®)+ТХ, (Е+TX,Z+TX,Z)-3+ТХ,8+ТХД1 тетрадекатриенилацетат+ТХ, (Z+TX,Z+ТХ,Е)-7+ТХ,11+ТХД3-гексадекатриеналь+ТХ, (Е+TX,Z)-7+ТХ,9-додекадиен-1-илацетат+ТХ, 2-метил-1-бутанол+ТХ, ацетат кальция+ТХ, Scenturion®+ТХ, Biolure®+ТХ, Check-Mate®+ТХ, лавандулилсенеционат; и
макроорганизмы, в том числе Aphelinus abdominalis+ТХ, Aphidius ervi (Aphelinus-System®)+TX, Acerophagus papaya+TX, Adalia bipunctata (Adalia-System®)+TX, Adalia bipunctata (Adaline®)+TX, Adalia bipunctata (Aphidalia®)+TX, Ageniaspis citricola+TX, Ageniaspis fuscicollis+TX, Amblyseius andersoni (Anderline®+TX, Andersoni-System®)+TX, Amblyseius californicus (Amblyline®+TX, Spical®)+TX, Amblyseius cucumeris (Thripex®+TX, Bugline cucumeris®)+TX, Amblyseius fallacis (Fallacis®)+TX, Amblyseius swirskii (Bugline swirskii®+TX, Swirskii-Mite®)+TX, Amblyseius womersleyi (WomerMite®)+TX, Amitus hesperidum+TX, Anagrus atomus+TX, Anagyrus fusciventris+TX, Anagyrus kamali+TX, Anagyrus loecki+TX, Anagyrus pseudococci (Citripar®)+TX, Anicetus benefices+TX, Anisopteromalus calandrae+TX, Anthocoris nemoralis (Anthocoris-System®)+TX, Aphelinus abdominalis (Apheline®+TX, Aphiline®)+TX, Aphelinus asychis+TX, Aphidius colemani (Aphipar®)+TX, Aphidius ervi (Ervipar®)+TX, Aphidius gifuensis+TX, Aphidius matricariae (Aphipar-M®)+TX, Aphidoletes aphidimyza (Aphidend®)+TX, Aphidoletes aphidimyza (Aphidoline®)+TX, Aphytis lingnanensis+TX, Aphytis melinus+TX, Aprostocetus hagenowii+TX, Atheta coriaria (Staphyline®)+TX, Bombus spp.+TX, Bombus terrestris (Natupol Beehive®)+TX, Bombus terrestris (Beeline®+TX, Tripol®)+TX, Cephalonomia stephanoderis+TX, Chilocorus nigritus+TX, Chrysoperla cornea (Chrysoline®)+TX, Chrysoperla carnea (Chrysopa®)+TX, Chrysoperla rufllabris+TX, Cirrospilus ingenuus+TX, Cirrospilus quadristriatus+TX, Citrostichus phyllocnistoides+TX, Closterocerus chamaeleon+TX, Closterocerus spp.+TX, Coccidoxenoides perminutus (Planopar®)+TX, Coccophagus cowperi+TX, Coccophagus lycimnia+TX, Cotesia flavipes+TX, Cotesia plutellae+TX, Cryptolaemus montrouzieri (Cryptobug®+TX, Cryptoline®)+TX, Cybocephalus nipponicus+TX, Dacnusa sibirica+TX, Dacnusa sibirica (Minusa®)+TX, Diglyphus isaea (Diminex®)+TX, Delphastus catalinae (Delphastus®)+TX, Delphastus pusillus+TX, Diachasmimorpha krausii+TX, Diachasmimorpha longicaudata+TX, Diaparsis jucunda+TX, Diaphorencyrtus aligarhensis+TX, Diglyphus isaea+TX, Diglyphus isaea (Miglyphus®+TX, Digline®)+TX, Dacnusa sibirica (DacDigline®+TX, Minex®)+TX, Diversinervus spp.+TX, Encarsia citrina+TX, Encarsia formosa (Encarsia max®+TX, Encarline®+TX, En-Strip®)+TX, Eretmocerus eremicus (Enermix®)+TX, Encarsia guadeloupae+TX, Encarsia haitiensis+TX, Episyrphus balteatus (Syrphidend®)+TX, Eretmoceris siphonini+TX, Eretmocerus californicus+TX, Eretmocerus eremicus (Ercal®+TX, Eretline e®)+TX, Eretmocerus eremicus (Bemimix®)+TX, Eretmocerus hayati+TX, Eretmocerus mundus (Bemipar®+TX, Eretline m®)+TX, Eretmocerus siphonini+TX, Exochomus quadripustulatus+TX, Feltiella acarisuga (Spidend®)+TX, Feltiella acarisuga (Feltiline®)+TX, Fopius arisanus+TX, Fopius ceratitivorus+TX, формононетин (Wirless Beehome®)+TX, Franklinothrips vespiformis (Vespop®)+TX, Galendromus occidentalis+TX, Goniozus legneri+TX, Habrobracon hebetor+TX, Harmonia axyridis (HarmoBeetle®)+TX, Heterorhabditis spp.(Lawn Patrol®)+TX, Heterorhabditis bacteriophora (NemaShield HB®+TX, Nemaseek®+TX, Terranem-Nam®+TX, Terranem®+TX, Larvanem®+TX, B-Green®+TX, NemAttack ®+TX, Nematop®)+TX, Heterorhabditis megidis (Nemasys H®+TX, BioNem H®+TX, Exhibitline hm®+TX, Larvanem-M®)+TX, Hippodamia convergens+TX, Hypoaspis aculeifer (Aculeifer-System®+TX, Entomite-A®)+TX, Hypoaspis miles (Hypoline m®+TX, Entomite-M®)+TX, Lbalia leucospoides+TX, Lecanoideus floccissimus+TX, Lemophagus errabundus+TX, Leptomastidea abnormis+TX, Leptomastix dactylopii (Leptopar®)+TX, Leptomastix epona+TX, Lindorus lophanthae+TX, Lipolexis oregmae+TX, Lucilia caesar (Natufly®)+TX, Lysiphlebus testaceipes+TX, Macrolophus caliginosus (Mirical-N®+TX, Macroline c®+TX, Mirical®)+TX, Mesoseiulus longipes+TX,Metaphycusflavus+TX,Metaphycus lounsburyi+TX,Micromus angulatus (Milacewing®)+TX, Microterys flavus+TX, Muscidifurax raptorellus и Spalangia cameroni (Biopar®)+TX, Neodryinus typhlocybae+TX, Neoseiulus californicus+TX, Neoseiulus cucumeris (THRYPEX®)+TX, Neoseiulus fallacis+TX, Nesideocoris tenuis (NesidioBug®+TX, Nesibug®)+TX, Ophyra aenescens (Biofly®)+TX, Orius insidiosus (Thripor-I®+TX, Oriline i®)+TX, Orius laevigatus (Thripor-L®+TX, Oriline 1®)+TX, Orius majusculus (Oriline m®)+TX, Orius strigicollis (Thripor-S®)+TX, Pauesia juniperorum+TX, Pediobius foveolatus+TX, Phasmarhabditis hermaphrodita (Nemaslug®)+TX, Phymastichus coffea+TX, Phytoseiulus macropilus+TX, Phytoseiulus persimilis (Spidex®+TX, Phytoline p®)+TX, Podisus maculiventris (Podisus®)+TX, Pseudacteon curvatus+TX, Pseudacteon obtusus+TX, Pseudacteon tricuspis+TX, Pseudaphycus maculipennis+TX, Pseudleptomastix mexicana+TX, P' syllaephagus pilosus+TX, Psyttalia concolor (комплекс видов)+TX, Quadrastichus spp.+TX, Rhyzobius lophanthae+TX, Rodolia cardinalis+TX, Rumina decollate+TX, Semielacher petiolatus+TX, Sitobion avenae (Ervibank®)+TX, Steinernema carpocapsae (Nematac C®+TX, Millenium®+TX, BioNem C®+TX, NemAttack®+TX, Nemastar®+TX, Capsanem®)+TX, Steinernema feltiae (NemaShield®+TX, Nemasys F®+TX, BioNem F®+TX, Steinernema-System®+TX, NemAttack®+TX, Nemaplus®+TX, Exhibitline sf®+TX, Scia-rid®+TX, Entonem®)+TX, Steinernema kraussei (Nemasys L®+TX, BioNem L®+TX, Exhibitline srb®)+TX, Steinernema riobrave (BioVector®+TX, BioVektor®)+TX, Steinernema scapterisci (Nematac S®)+TX, Steinernema spp.+TX, Steinernematid spp.(Guardian Nematodes®)+TX, Stethorus punctillum (Stethorus®)+TX, Tamarixia radiate+TX, Tetrastichus setifer+TX, Thripobius semiluteus+TX, Torymus sinensis+TX, Trichogramma brassicae (Tricholine b®)+TX, Trichogramma brassicae (Tricho-Strip®)+TX, Trichogramma evanescens+TX, Trichogramma minutum+TX, Trichogramma ostriniae+TX, Trichogramma platneri+TX, Trichogramma pretiosum+TX, Xanthopimpla stemmator; и
другие биологические средства, в том числе абсцизовая кислота+ТХ, bioSea®+ТХ, Chondrostereum purpureum (Chontrol Paste®)+TX, Colletotrichum gloeosporioides (Collego®)+TX, октаноат меди (Cueva®)+TX, дельтовидные ловушки (Trapline d®)+TX, Erwinia amylovora (харпин) (ProAct®+TX, Ni-HIBIT Gold CST®)+TX, феррофосфат (Ferramol®)+TX, воронковидные ловушки (Trapline у®)+TX, Gallex®+TX, Grower's Secret®+TX, гомобрассинолид+TX, фосфат железа (Lilly Miller Worry Free Ferramol Slug & Snail Bait®)+TX, ловушка MCPhail (Trapline f®)+TX, Microctonus hyperodae+TX, Mycoleptodiscus terrestris (Des-X®)+TX, BioGain®+TX, Aminomite®+TX, Zenox®+TX, феромонная ловушка (Thripline ams®)+TX, бикарбонат калия (MilStop®)+TX, калиевые соли жирных кислот (Sanova®)+ТХ, раствор силиката калия (Sil-Matrix®)+ТХ, йодид калия+тиоцианат калия (Enzicur®)+ТХ, SuffOil-X®+ТХ, яд паука+ТХ, Nosema locustae (Semaspore Organic Grasshopper Control®)+TX, клеевые ловушки (Trapline YF®+TX, Rebell Amarillo®)+TX и ловушки (Takitrapline у+b®)+TX;
или биологически активные соединение или средство, выбранные из брофлутрината+ТХ, дифловидазина+ТХ, флометоквина+ТХ, флугексафона+ТХ, вируса гранулеза Plutella xylostella+ТХ, вируса гранулеза Cydia pomonella+ТХ, имициафоса+ТХ, вируса ядерного полиэдроза Heliothis virescens+ТХ, вируса ядерного полиэдроза Heliothis punctigera+ТХ, вируса ядерного полиэдроза Helicoverpa zea+ТХ, вируса ядерного полиэдроза Spodoptera frugiperda+ТХ, вируса ядерного полиэдроза Plutella xylostella+ТХ, п-цимола+ТХ, пифлубумида+ТХ, пирафлупрола+ТХ, QRD 420+ТХ, QRD 452+ТХ, QRD 460+ТХ, терпеноидных смесей+ТХ, терпеноидов+ТХ, тетранилипрола+ТХ и α-терпинена+ТХ;
или активное вещество, указанное с помощью кода+ТХ, как например код АЕ 1887196 (BSC-BX60309)+ТХ, код NNI-0745 GR+ТХ, код IKI-3106+ТХ, код JT-L001+ТХ, код ZNQ-08056+ТХ, код IPPA152201+ТХ, код HNPC-A9908 (CAS: [660411-21-2])+ТХ, код HNPC-A2005 (CAS: [860028-12-2])+ТХ, код JS118+ТХ, код ZJ0967+ТХ, код ZJ2242+ТХ, код JS7119 (CAS: [929545-74-4])+ТХ, код SN-1172+ТХ, код HNPC-А9835+ТХ, код HNPC-A9955+ТХ, код HNPC-A3061+ТХ, код Chuanhua 89-1+ТХ, код IPP-10+ТХ, код ZJ3265+ТХ, код JS9117+ТХ, код ZJ3757+ТХ, код ZJ4042+ТХ, код ZJ4014+ТХ, код ITM-121+ТХ, код DPX-RAB55 (DKI-2301)+ТХ, код NA-89+ТХ, код MIE-1209+ТХ, код MCI-8007+ТХ, код BCS-CL73507+ТХ, код S-1871+ТХ, код DPX-RDS63+ТХ, код AKD-1193+ТХ;
или другие биологически активные соединение или средства, выбранные из квинофумелина+ТХ, мефентрифлуконазола+ТХ, фенпикоксамида+ТХ, флуиндапира+ТХ, инпирфлуксама+ТХ или индифлуметпира+ТХ, изофлуципрама+ТХ, пирапропоина+ТХ, флорилпикоксамида+ТХ, метилтетрапрола+ТХ, ипфлуфеноквина+ТХ, пиридахлометила+ТХ или хлопиридифлу+ТХ, тетрахлорантранилипрола+ТХ, тетрахлоранилипрола+ТХ, тетфлупиролимета+ТХ, трифлуфенпирролидона+ТХ, тиклопиразофлора+ТХ, флупиримина+ТХ или пирифлурамида+ТХ, бензпиримоксана+ТХ, бефлубутамида-М+ТХ, бензосуфила+ТХ или оксазосулфила+ТХ, этпирафена+ТХ, ацинонапира+ТХ или пиринонафена+ТХ, оксотриона+ТХ, бикслозона+ТХ или клофенлизона+ТХ или диклороксизона+ТХ, циклопиранила+ТХ или пиразоциклонила+ТХ или циклопиразонила+ТХ, альфа-бромадиолона+ТХ, оксатиапипролина+ТХ, флуопирама+ТХ, пенфлуфена+ТХ, флуоксопиросада+ТХ, флуоксапипролина+ТХ и флупирадифурона+ТХ.
Ссылки в квадратных скобках после активных ингредиентов, например [3878-19-1], относятся к номеру согласно реестру Химической реферативной службы. Вышеописанные ингредиенты для смешивания являются известными. Если активные ингредиенты включены в "The Pesticide Manual" [The Pesticide Manual - A World Compendium; Thirteenth Edition; Editor: C. D.S. TomLin; British Crop Protection Council], то они описаны в нем под номером записи, приведенном в данном документе выше в круглых скобках для конкретного соединения; например, соединение "абамектин" описано под номером записи (1). Если в данном документе выше добавлено "[CCN]" к конкретному соединению, то рассматриваемое соединение включено в "Compendium of Pesticide Common Names", который доступен в Интернете [A. Wood; Compendium of Pesticide Common Names, Copyright © 1995-2004]; например, соединение "ацетопрол" описано по адресу в Интернете http://www.alanwood.net/pesticides/acetoprole.html.
Большинство вышеописанных активных ингредиентов приведены в данном документе выше по так называемому "общепринятому названию", соответствующему "общепринятому названию согласно ISO" или другому "общепринятому названию", которое используют в отдельных случаях. Если обозначение не является "общепринятым названием", суть обозначения, применяемого вместо него, представлена в круглых скобках для конкретного соединения; в этом случае применяют название по IUPAC, название по IUPAC/Химической реферативной службе, "химическое название", "традиционное название", "название соединения" или "код разработки" или, если не применяют ни одно из этих обозначений или "общепринятого названия", то используют "альтернативное название". "Регистрационный №по CAS" означает регистрационный номер согласно Химической реферативной службе.
Смесь активных ингредиентов соединений формулы I, выбранных из таблиц Y-1 - Y-8, Х-1 - Х-8, U-1 - U-2 и V-1 - V-6 и таблицы Р, с вышеописанными активными ингредиентами содержит соединение, выбранное из таблиц Y-1 - Y-8, Х-1 - Х-8, U-1 -U-2 и V-1 - V-6 и таблицы Р, и вышеописанный активный ингредиент предпочтительно при соотношении компонентов в смеси от 100:1 до 1:6000, в частности от 50:1 до 1:50, более предпочтительно при соотношении от 20:1 до 1:20, еще более предпочтительно от 10:1 до 1:10, крайне предпочтительно от 5:1 до 1:5, при этом особое предпочтение отдают соотношению от 2:1 до 1:2, и при этом соотношение от 4:1 до 2:1 является также предпочтительным, прежде всего при соотношении 1:1 или 5:1, или 5:2, или 5:3, или 5:4, или 4:1, или 4:2, или 4:3, или 3:1, или 3:2, или 2:1, или 1:5, или 2:5, или 3:5, или 4:5, или 1:4, или 2:4, или 3:4, или 1:3, или 2:3, или 1:2, или 1:600, или 1:300, или 1:150, или 1:35, или 2:35, или 4:35, или 1:75, или 2:75, или 4:75, или 1:6000, или 1:3000, или 1:1500, или 1:350, или 2:350, или 4:350, или 1:750, или 2:750, или 4:750. Эти соотношения компонентов смеси указаны по весу.
Вышеописанные смеси можно применять в способе контроля вредителей, который предусматривает применение композиции, содержащей вышеописанную смесь, в отношении вредителей или их среды обитания, за исключением способа лечения организма человека или животного путем хирургического вмешательства или терапии и способов диагностики, применяемых на практике в отношении организма человека или животного.
Смеси, содержащие соединение формулы I, выбранное из таблиц Y-1 - Y-8, Х-1 - Х-8, U-1 - U-2 и V-1 - V-6 и таблицы Р, а также один или несколько активных ингредиентов, которые описаны выше, можно применять, например, в форме отдельной "готовой смеси", в объединенной смеси для опрыскивания, состоящей из отдельных составов отдельных компонентов, представляющих собой активные ингредиенты, такой как "баковая смесь", и при объединенном применении отдельных активных ингредиентов, в случае их применения последовательным образом, т.е. один за другим с приемлемым коротким периодом, таким как несколько часов или дней. Порядок применения соединений формулы I, выбранных из таблиц Y-1 - Y-8, Х-1 - Х-8, U-1 - U-2 и V-1 - V-6, а также активных ингредиентов, описанных выше, не является существенным для осуществления настоящего изобретения.
Композиции согласно настоящему изобретению также могут содержать дополнительные твердые или жидкие вспомогательные средства, такие как стабилизаторы, например неэпоксидированные или эпоксидированные растительные масла (например, эпоксидированное кокосовое масло, рапсовое масло или соевое масло), противовспениватели, например силиконовое масло, консерванты, регуляторы вязкости, связывающие и/или придающие липкость вещества, удобрения или другие активные ингредиенты для достижения определенных эффектов, например, бактерициды, фунгициды, нематоциды, активаторы роста растения, моллюскоциды или гербициды.
Композиции согласно настоящему изобретению получают способом, известным per se, при отсутствии вспомогательных средств, например, посредством измельчения, просеивания и/или прессования твердого активного ингредиента, и в присутствии по меньшей мере одного вспомогательного средства, например, посредством тщательного перемешивания и/или измельчения активного ингредиента со вспомогательным (вспомогательными) средством (средствами). Такие способы получения композиций и применение соединений I для получения таких композиций также являются объектом настоящего изобретения.
Способы применения композиций, то есть способы контроля вредителей вышеупомянутого типа, такие как распыление, разбрызгивание, опудривание, нанесение кистью, дражирование, разбрасывание или полив, которые подлежат выбору для удовлетворения намеченных целей с учетом обстоятельств, и применение композиций для контроля вредителей вышеупомянутого типа являются другими объектами настоящего изобретения. Типичные нормы концентрации активного ингредиента составляют от 0,1 до 1000 ppm, предпочтительно от 0,1 до 500 ppm. Норма применения на гектар, как правило, составляет от 1 до 2000 г активного ингредиента на гектар, в частности от 10 до 1000 г/га, предпочтительно от 10 до 600 г/га.
Предпочтительным способом нанесения в области защиты культур является нанесение на листву растений (внекорневое внесение), при этом можно выбрать частоту и норму применения в соответствии с опасностью заражения рассматриваемым вредителем. В качестве альтернативы, активный ингредиент может достигать растений посредством корневой системы (системное действие) за счет орошения места произрастания растений жидкой композицией или за счет внедрения активного ингредиента в твердой форме в место произрастания растений, например в почву, например, в виде гранул (внесение в почву). В случае сельскохозяйственной культуры риса-падди такие гранулы могут подаваться в определенном количестве в затопляемое рисовое поле.
Соединения по настоящему изобретению и композиции на их основе также являются подходящими для защиты материала для размножения растений, например семян, таких как плод, клубни или зерна, или саженцев, от вредителей упомянутого выше типа. Материал для размножения можно обрабатывать с помощью соединения перед посадкой, например семена можно обрабатывать перед посевом. В качестве альтернативы, соединение можно применять по отношению к косточкам семени (нанесение покрытия) либо с помощью замачивания косточек в жидкой композиции, либо с помощью нанесения слоя твердой композиции. Также можно применять композиции при посадке материала для размножения в отношении места применения, например в борозду для семян во время рядового сева. Данные способы обработки материала для размножения растений и обработанный таким образом материал для размножения растений являются дополнительными объектами настоящего изобретения. Типичные нормы обработки будут зависеть от растения и вредителя/грибов, подлежащих контролю, и обычно они составляют от 1 до 200 грамм на 100 кг семян, предпочтительно от 5 до 150 грамм на 100 кг семян, как, например от 10 до 100 грамм на 100 кг семян.
Термин "семя" охватывает семена и вегетативные части растения всех видов, в том числе без ограничения истинные семена, кусочки семян, корневые побеги, зерно злаковых, луковицы, плод, клубни, зерна, ризомы, черенки, нарезанные побеги и т.п., и согласно предпочтительному варианту осуществления означает истинные семена.
Настоящее изобретение также предусматривает семена, покрытые или обработанные с помощью соединения формулы I или содержащие таковое. Термин "покрытый или обработанный и/или содержащий" обычно означает, что активный ингредиент находится на большей части поверхности семени во время применения, хотя большая или меньшая часть ингредиента может проникать в семенной материал в зависимости от способа применения. Если указанный семенной продукт (повторно) садят, он может поглощать активный ингредиент. В одном варианте осуществления с помощью настоящего изобретения получают материал для размножения растений с возможностью прикрепления к нему соединения формулы (I). Кроме того, в настоящем документе представлен содержащий композицию материал для размножения растений, обработанный соединением формулы (I).
Обработка семян предусматривает все подходящие методики обработки семян, известные из уровня техники, такие как дражирование семян, покрытие семян, опудривание семян, пропитывание семян и гранулирование семян. Применение соединения формулы (I) при обработке семян может быть осуществлено с помощью любых известных способов, таких как распыление или опудривание семян перед посевом или во время посева/высаживания семян.
Биологические примеры
Пример В1. Активность в отношении Bemisia tabaci (белокрылка табачная) Листовые диски хлопчатника помещали на агар в 24-луночные микротитровальные планшеты и опрыскивали исследуемыми водными растворами, полученными из 10000 ppm исходных растворов в DMSO. После высушивания листовые диски заражали взрослыми особями белокрылки. Через 6 дней после инкубирования образцы проверяли в отношении смертности.
Следующие соединения обеспечивали по меньшей мере 80% смертность при норме применения 200 ppm:
Р3, Р4, Р6, Р8, Р10, Р13, Р14, и Р15.
Пример В2. Активность в отношении Diabrotica balteata (блошка длинноусая) Ростки кукурузы, помещенные на слой агара в 24-луночные микротитровальные планшеты, обрабатывали исследуемыми водными растворами, полученными из 10000 исходных растворов в DMSO, путем распыления. После высушивания планшеты заражали личинками L2 (6-10 на лунку). Образцы оценивали в отношении смертности и ингибирования роста по сравнению с необработанными образцами через 4 дня после заражения.
Следующие соединения обеспечивали эффект, составляющий по меньшей мере 80%, в по меньшей мере одной из двух категорий (смертность или ингибирование роста) при норме применения 200 ppm:
Р3, Р4, Р5, Р7, Р8, Р10, Р11, Р12, Р13, Р14 и Р16.
Пример В3. Активность в отношении Euschistus heros (неотропический коричневый клоп-щитник)
Листья сои на агаре в 24-луночных микротитровальных планшетах опрыскивали исследуемыми водными растворами, полученными из 10000 ppm исходных растворов в DMSO. После высушивания листья заражали нимфами N2. Образцы оценивали в отношении смертности и ингибирования роста по сравнению с необработанными образцами через 5 дней после заражения.
Следующие соединения обеспечивали эффект, составляющий по меньшей мере 80%, в по меньшей мере одной из двух категорий (смертность или ингибирование роста) при норме применения 200 ppm:
Р3, Р4, Р8, Р9, Р10, Р13, Р14, и Р15.
Пример В4. Активность в отношении Myzus yersicae (тля персиковая зеленая): Листовые диски подсолнечника помещали на агар в 24-луночный микротитровальный планшет и опрыскивали исследуемыми водными растворами, полученными из 10000 исходных растворов в DMSO. После высушивания листовые диски заражали популяцией тли разного возраста. Через 6 дней после заражения образцы оценивали в отношении смертности.
Следующие соединения обеспечивали по меньшей мере 80% смертность при норме применения 200 ppm:
Р3, Р4, Р5, Р6, Р7, Р8, Р9, Р10, Р11, Р12, Р13, Р14, Р15, Р16, и Р17.
Пример В5. Активность в отношении Myzus yersicae (тля персиковая зеленая). Корни проростков гороха, зараженных популяцией тли разного возраста, помещали непосредственно в исследуемые водные растворы, полученные из 10000 исходных растворов в DMSO. Через 6 дней после помещения проростков в исследуемые растворы образцы оценивали в отношении смертности.
Следующие соединения обеспечивали по меньшей мере 80% смертность при исследуемой норме 24 ppm:
Р3, Р4, Р5, Р6, Р7, Р8, Р9, Р10, Р11, Р12, Р13, Р14, Р15, Р16, и Р17.
Пример В6. Активность в отношении Plutella xyloStella (моль капустная) 24-луночные микротитровальные планшеты с искусственной питательной средой с помощью пипетки обрабатывали исследуемыми водными растворами, полученными из 10000 ppm исходных растворов в DMSO. После высушивания планшеты заражали личинками L2 (10-15 на лунку). Образцы оценивали в отношении смертности и ингибирования роста по сравнению с необработанными образцами через 5 дней после заражения.
Следующие соединения обеспечивали эффект, составляющий по меньшей мере 80%, в по меньшей мере одной из двух категорий (смертность или ингибирование роста) при норме применения 200 ppm:
Р3, Р4, Р5, Р6, Р7, Р8, Р11, Р12, Р14, и Р15.
Пример В7. Активность в отношении Syodoytera littoralis (египетская хлопчатниковая совка)
Листовые диски хлопчатника помещали на агар в 24-луночные микротитровальные планшеты и опрыскивали исследуемыми водными растворами, полученными из 10000 исходных растворов в DMSO. После высушивания листовые диски заражали пятью личинками L1. Образцы оценивали в отношении смертности, антифидантного эффекта и ингибирования роста по сравнению с необработанными образцами через 3 дня после заражения. Контроль Spodoptera littoralis исследуемыми образцами присутствовал, если по меньшей мере одна из категорий смертности, антифидантного эффекта и ингибирования роста являлась выше, чем для необработанного образца. Следующие соединения обеспечивали по меньшей мере 80% контроль при норме применения 200 ppm:
Р3, Р4, Р5, Р7, Р8, Р11, Р12, Р14, Р15, и Р16.
Пример В8. Активность в отношении Nilaparvata lugens (дельфацид коричневый) Растения риса обрабатывали разведенными тестируемыми растворами в оросительной камере. После высушивания растения заражали ~20 нимфами N3. Через 7 дней после обработки образцы оценивали в отношении смертности и регуляции роста.
Р6, Р10, Р11, Р12, Р13, и Р15
Пример В9. Активность в отношении Nilayarvata luzem (дельфацид коричневый) Растения риса, культивированные в питательном растворе, обрабатывали разведенными тестовыми растворами в питательной системе выращивания. Через 1 день после нанесения растения заражали ~20 нимфами N3. Через 7 дней после заражения образцы оценивали в отношении смертности и регуляции роста.
Р6, Р10, Р11, Р12, Р13, и Р15
Пример В10. Активность в отношении Tetranvchus urticae (обыкновенный паутинный клещ):
Листовые диски боба на агаре в 24-луночных микротитровальных планшетах опрыскивали исследуемыми водными растворами, полученными из 10000 ppm исходных растворов в DMSO. После высушивания листовые диски заражали популяцией клещей разного возраста. Через 8 дней после заражения на смешанной популяции (подвижные стадии) образцы оценивали в отношении смертности.
Следующее соединение обеспечивало по меньшей мере 80% смертность при норме применения 200 ppm:
Р3.
Пример В11. Активность в отношении Plutella xylostella (моль капустная) 24-луночные микротитровальные планшеты с искусственной питательной средой с помощью пипетки обрабатывали исследуемыми водными растворами, полученными из 10000 исходных растворов в DMSO. После высушивания яйца Plutella помещали с помощью пипетки через пластиковый трафарет на бумагу для блоттинга в геле и накрывали ей планшет. Образцы оценивали в отношении смертности и ингибирования роста по сравнению с необработанными образцами через 8 дней после заражения. Следующие соединения обеспечивали эффект, составляющий по меньшей мере 80%, в по меньшей мере одной из двух категорий (смертность или ингибирование роста) при норме применения 200 ppm:
Р16, Р17, Р18, и Р19.
Пример В12. Активность в отношении Heterodera schachtii. Профилирование подвижности ювенильных особей in vitro в 96-луночном планшете Тестовые растворы получали из 10000 ppm исходных растворов в DMSO с помощью робота TECAN с получением объемов 20 мкл для 500, 100, 50, 25, 12,5 и 6,25 ppm. Для каждой концентрации получали три повторности. На лунку добавляли 80 мкл раствора с нематодами, содержащего 100-150 свежесобранных ювенильных особей второй стадии Heterodera schachtii. Планшеты накрывали, хранили при комнатной температуре в темноте и инкубировали в течение 48 ч. Подвижность ювенильных особей, подвергшихся воздействию, в обработанной лунке измеряли с помощью инструмента визуализации и сравнивали со средним значением для 12 необработанных повторностей.
Следующие соединения достигали по меньшей мере 60% контроля 100 через 48 ч: Р10, Р15.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕСТИЦИДНО АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ С СЕРОСОДЕРЖАЩИМИ ЗАМЕСТИТЕЛЯМИ | 2018 |
|
RU2796535C2 |
| ПЕСТИЦИДНО АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ С СЕРОСОДЕРЖАЩИМИ ЗАМЕСТИТЕЛЯМИ | 2018 |
|
RU2804355C2 |
| ПЕСТИЦИДНО АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ С СЕРОСОДЕРЖАЩИМИ ЗАМЕСТИТЕЛЯМИ | 2015 |
|
RU2765282C2 |
| ПЕСТИЦИДНО АКТИВНЫЕ ПОЛИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ С СЕРОСОДЕРЖАЩИМИ ЗАМЕСТИТЕЛЯМИ | 2015 |
|
RU2738359C2 |
| ФУНГИЦИДНЫЕ КОМПОЗИЦИИ | 2021 |
|
RU2833878C1 |
| ФУНГИЦИДНЫЕ КОМПОЗИЦИИ | 2021 |
|
RU2834637C1 |
| ПРОИЗВОДНЫЕ ИМИНОПИРИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МИКРОБИОЦИДОВ | 2008 |
|
RU2532135C2 |
| БИСАМИДНЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНСЕКТИЦИДНЫХ СОЕДИНЕНИЙ | 2008 |
|
RU2515966C2 |
| ФУНГИЦИДНАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2566992C2 |
| ПРОИЗВОДНЫЕ 2-АРИЛИМИДАЗО[1,2-b]ПИРИДАЗИНА, 2-ФЕНИЛИМИДАЗО[1,2-a]ПИРИДИНА И 2-ФЕНИЛИМИДАЗО[1,2-a]ПИРАЗИНА | 2011 |
|
RU2598385C2 |
Изобретение относится к соединению формулы (I), где А представляет собой СН или N, R1 представляет собой С1-С4алкил, R2 представляет собой водород, R3 представляет собой водород или циано, n равняется 1; Q представляет собой радикал, выбранный из группы, состоящей из формул Q1, Q2, Q3, Q4 и Q5, где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и где R4 представляет собой галоген, С1-С6галогеналкил, С1-С4галогеналкилсульфанил, C1-С4галогеналкилсульфинил или С1-С4галогеналкилсульфонил; X1 представляет собой О или NR5; R5 представляет собой С1-С4алкил; R6 представляет собой С1-С4алкил, С1-С4галогеналкил или С1-С4алкокси; и G1 и G2 независимо друг от друга представляют собой N или СН. Кроме того, настоящее изобретение относится к агрохимическим композициям, которые содержат соединения формулы (I), к способу борьбы с насекомыми, клещами или нематодами и способу защиты материала для размножения растений. Соединения формулы (I) по настоящему изобретению представляют собой активные ингредиенты, имеющие важное значение в области контроля вредителей для предупреждения и/или лечения даже при низких нормах применения, которые обладают весьма подходящим биоцидным спектром и хорошо переносятся теплокровными видами, рыбами и растениями. 4 н. и 14 з.п. ф-лы, 5 табл., 20 пр.
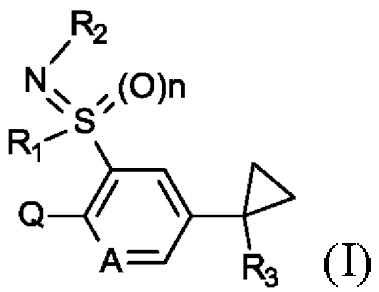
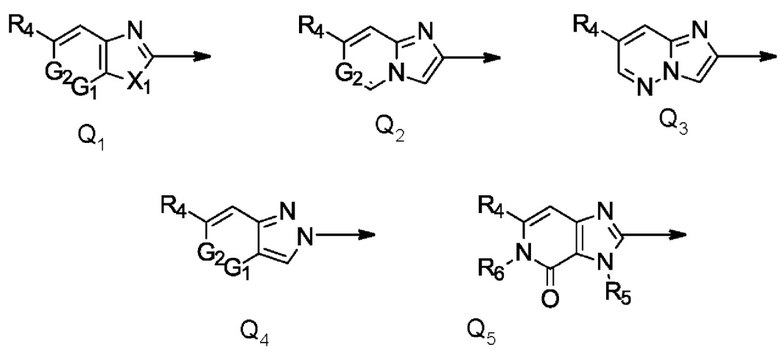
1. Соединение формулы (I)
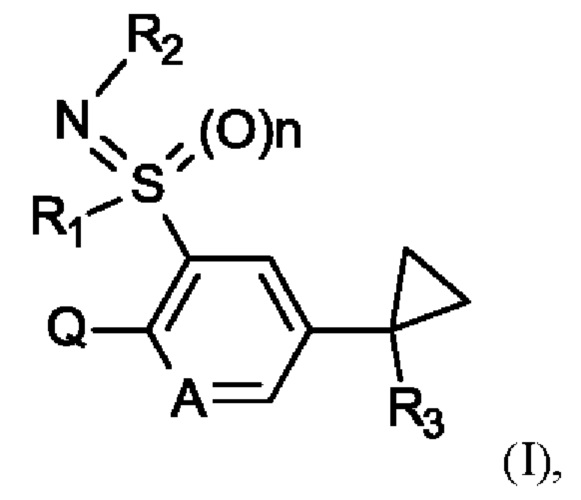
где А представляет собой СН или N,
R1 представляет собой С1-С4алкил,
R2 представляет собой водород,
R3 представляет собой водород или циано,
n равняется 1;
Q представляет собой радикал, выбранный из группы, состоящей из формул Q1, Q2, Q3, Q4 и Q5:
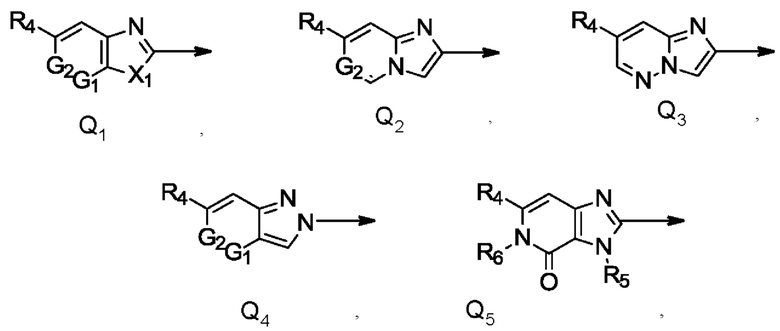
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой галоген, С1-С6галогеналкил, С1-С4галогеналкилсульфанил, C1-С4галогеналкилсульфинил или С1-С4галогеналкилсульфонил;
X1 представляет собой О или NR5;
R5 представляет собой С1-С4алкил;
R6 представляет собой С1-С4алкил, С1-С4галогеналкил или С1-С4алкокси; и
G1 и G2 независимо друг от друга представляют собой N или СН.
2. Соединение по п. 1, где
А представляет собой СН или N;
R1 представляет собой этил, пропил или изопропил;
R2 представляет собой водород;
R3 представляет собой водород или циано; и
n равняется 1.
3. Соединение по п. 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород или циано; и
n равняется 1.
4. Соединение по любому из пп. 1-3, где
Q представляет собой радикал, выбранный из Q1, Q2, Q4 и Q5:
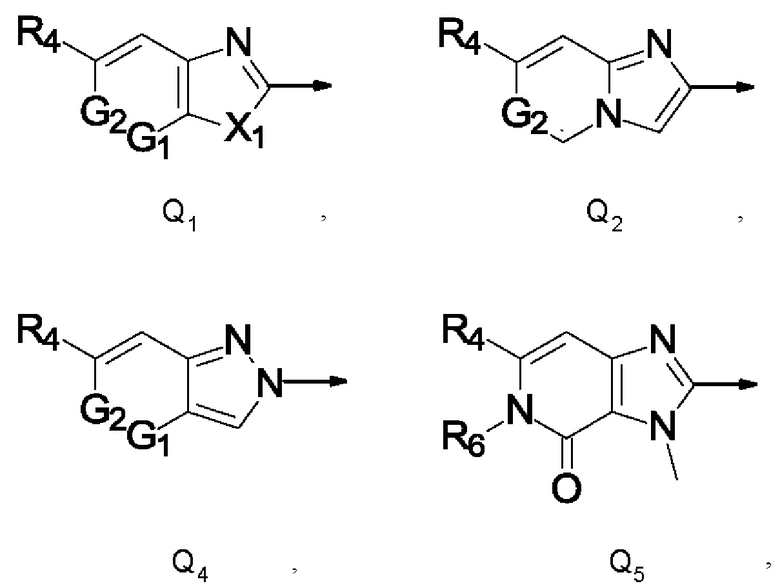
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой С1-С2галогеналкил, С1-С2галогеналкилсульфанил, C1-С2галогеналкилсульфинил или С1-С2галогеналкилсульфонил;
X1 представляет собой кислород или NCH3;
R6 представляет собой C1-С2алкил или C1-С2алкокси; и
G1 и G2 независимо друг от друга представляют собой N или СН.
5. Соединение по любому из пп. 1-3, где
Q представляет собой радикал, выбранный из Q1, Q2 и Q5:
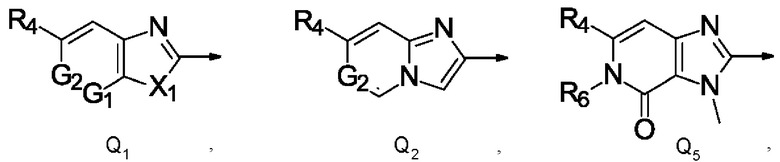
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой С1-С2фторалкил, трифторметилсульфанил, трифторметилсульфинил, трифторметилсульфонил, дифторметилсульфанил, дифторметилсульфинил или дифторметилсульфонил;
X1 представляет собой NCH3;
R6 представляет собой метил, этил, 2,2,2-трифторэтил или метокси; и
G1 и G2 независимо друг от друга представляют собой N или СН.
6. Соединение по любому из пп. 1-3, где
Q представляет собой радикал, выбранный из Q1 и Q5:
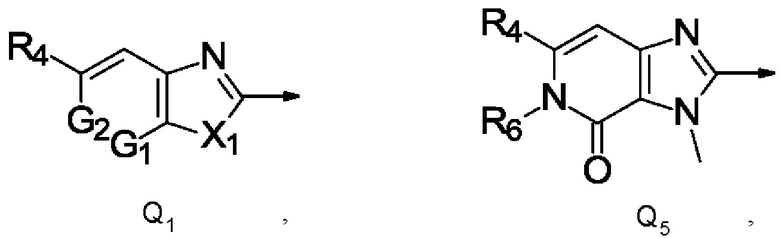
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой трифторметил, пентафторэтил, трифторметилсульфанил, трифторметилсульфинил или трифторметилсульфонил;
X1 представляет собой NCH3;
R6 представляет собой этил или метокси; и
G1 представляет собой N, a G2 представляет собой СН, или G1 представляет собой СН, а G2 представляет собой N, или G1 и G2 представляют собой N, или G1 и G2 представляют собой СН.
7. Соединение по любому из пп. 1-3, где
Q представляет собой радикал Q1
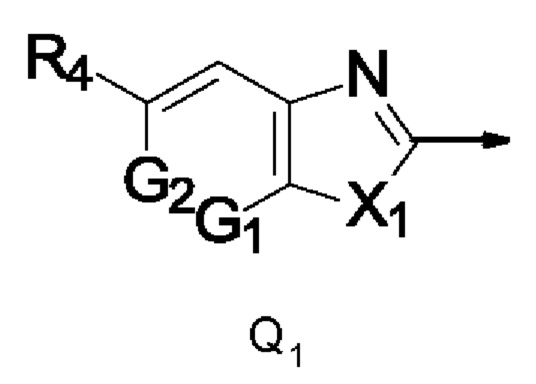 ,
,
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой трифторметил;
X1 представляет собой NCH3; и
G1 представляет собой N, a G2 представляет собой СН, G1 представляет собой СН, a G2 представляет собой N или G1 и G2 представляют собой N.
8. Соединение по п. 1, где
А представляет собой СН или N;
R1 представляет собой этил, пропил или изопропил;
R2 представляет собой водород;
R3 представляет собой водород или циано;
n равняется 1;
Q представляет собой радикал, выбранный из Q1, Q2, Q4 и Q5:
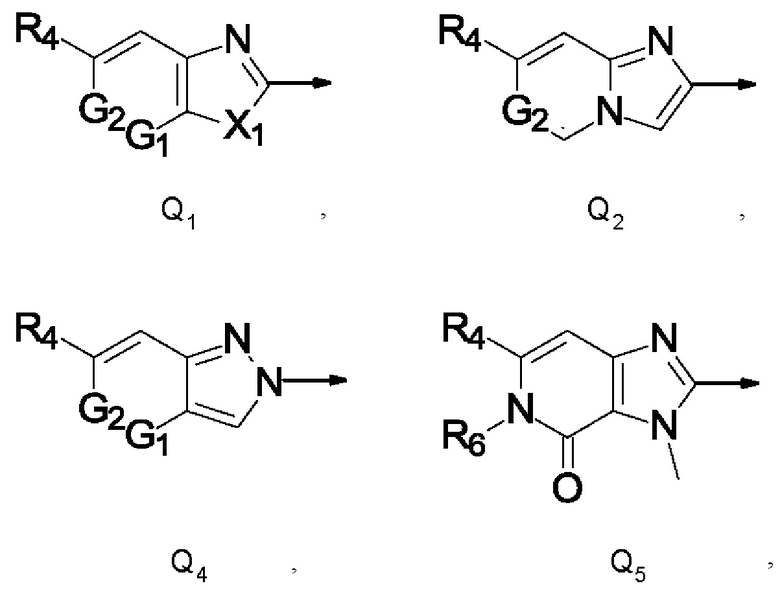
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой С1-С2галогеналкил, С1-С2галогеналкилсульфанил, C1-С2галогеналкилсульфинил или С1-С2галогеналкилсульфонил;
X1 представляет собой кислород или NCH3;
R6 представляет собой C1-С2алкил, С1-С2галогеналкил или С1-С2алкокси; и
G1 и G2 независимо друг от друга представляют собой N или СН.
9. Соединение по п. 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород или циано;
n равняется 1;
Q представляет собой радикал, выбранный из Q1, Q2 и Q5:
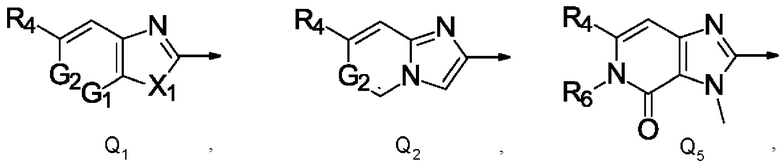
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой С1-С2фторалкил, трифторметилсульфанил, трифторметилсульфинил, трифторметилсульфонил, дифторметилсульфанил, дифторметилсульфинил или дифторметилсульфонил;
X1 представляет собой NCH3;
R6 представляет собой метил, этил, 2,2,2-трифторэтил или метокси; и
G1 и G2 независимо друг от друга представляют собой N или СН.
10. Соединение по п. 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород или циано;
n равняется 1;
Q представляет собой радикал, выбранный из Q1 и Q5:
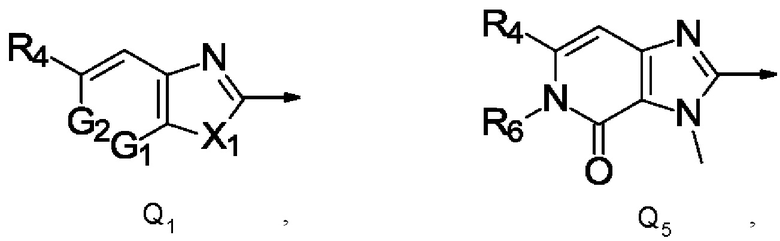
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой трифторметил, пентафторэтил, трифторметилсульфанил, трифторметилсульфинил или трифторметилсульфонил;
X1 представляет собой NCH3;
R6 представляет собой этил или метокси; и
G1 представляет собой N, a G2 представляет собой СН, или G1 представляет собой СН, а G2 представляет собой N, или G1 и G2 представляют собой N, или G1 и G2 представляют собой СН.
11. Соединение по п. 1, где
А представляет собой СН или N;
R1 представляет собой этил;
R2 представляет собой водород;
R3 представляет собой водород или циано;
n равняется 1;
Q представляет собой радикал Q1
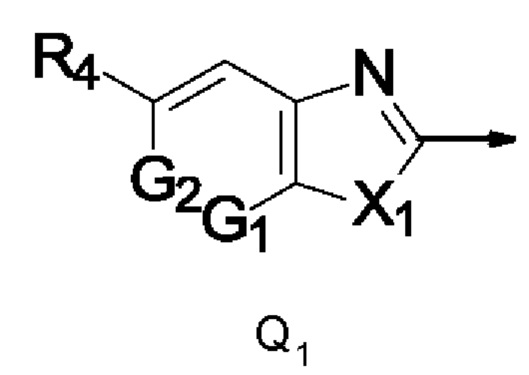 ,
,
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
где R4 представляет собой трифторметил;
X1 представляет собой NCH3; и
G1 представляет собой N, a G2 представляет собой СН, G1 представляет собой СН, a G2 представляет собой N или G1 и G2 представляют собой N.
12. Соединение по любому из пп. 1-3, где
Q представляет собой радикал, выбранный из Q1-1, Q1-2, Q1-3, Q1-4 и Q1-5; предпочтительно Q представляет собой радикал, выбранный из Q1-2, Q1-3, Q1-4 и Q1-5:
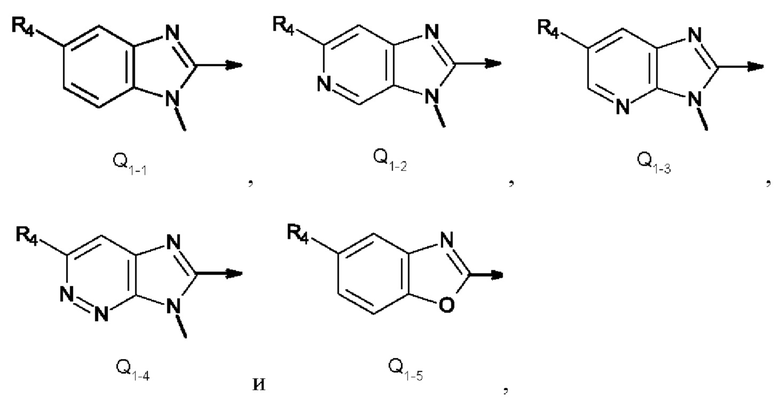
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А; и
R4 представляет собой трифторметил, трифторметилсульфанил или трифторметилсульфонил.
13. Соединение по любому из пп. 1-3, где
Q представляет собой радикал, выбранный из Q5
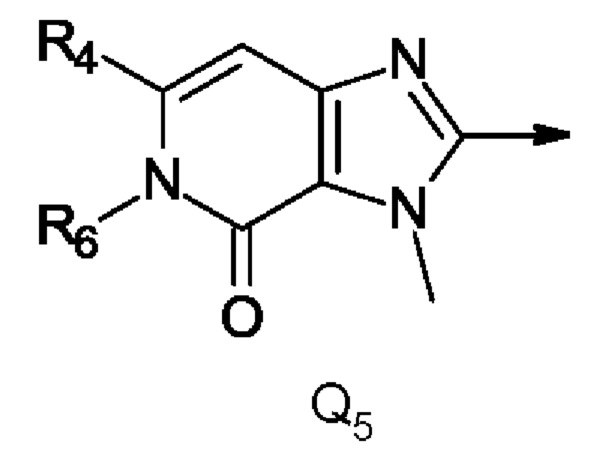 ,
,
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
R4 представляет собой трифторметил, трифторметилсульфанил или трифторметилсульфонил; и
R6 представляет собой ОСН3 или СН2СН3.
14. Соединение по любому из пп. 1-3, где
Q представляет собой радикал, выбранный из Q4
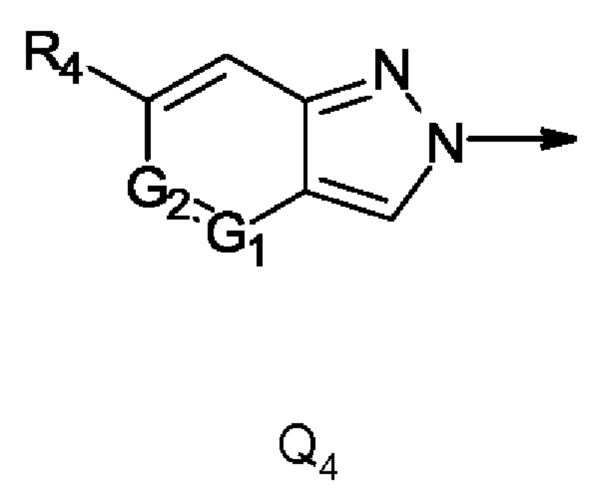 ,
,
где стрелка обозначает точку присоединения к кольцу, содержащему радикал А;
R4 представляет собой трифторметил, трифторметилсульфанил или трифторметилсульфонил; и
G1 представляет собой N, a G2 представляет собой СН, G1 представляет собой СН, a G2 представляет собой N, G1 и G2 представляют собой СН или G1 и G2 представляют собой N; предпочтительно G1 представляет собой СН, a G2 представляет собой N.
15. Соединение формулы (I) по п. 1, выбранное из группы, состоящей из 1-[5-(этилсульфонимидоил)-6-[7-метил-3-(трифторметил)имидазо[4,5-с]пиридазин-6-ил]-3-пиридил]циклопропанкарбоксамида (соединение Р1);
1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]фенил]циклопропанкарбоксамида (соединение Р2);
[5-циклопропил-2-[3-метил-6-(трифторметилсульфонил)имидазо[4,5-с]пиридин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение Р3);
[5-циклопропил-2-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение Р4);
[5-циклопропил-2-[3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение Р5);
1-[5-(этилсульфонимидоил)-6-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]-3-пиридил]циклопропанкарбонитрила (соединение Р6);
[5-циклопропил-2-[6-(трифторметил)пиразоло[4,3-с]пиридин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение Р7);
1-[5-(этилсульфонимидоил)-6-[5-метокси-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]-3-пиридил]циклопропанкарбонитрила (соединение Р8);
1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметилсульфанил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрила (соединение Р9);
1-[5-(этилсульфонимидоил)-6-[7-метил-3-(трифторметил)имидазо[4,5-с]пиридазин-6-ил]-3-пиридил]циклопропанкарбонитрила (соединение Р10);
[5-циклопропил-2-[7-метил-3-(трифторметил)имидазо[4,5-с]пиридазин-6-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение P11);
[5-циклопропил-2-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение Р12);
1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]фенил]циклопропанкарбонитрил (соединение Р13);
1-[6-[5-этил-3-метил-4-оксо-6-(трифторметил)имидазо[4,5-с]пиридин-2-ил]-5-(этилсульфонимидоил)-3-пиридил]циклопропанкарбонитрила (соединение Р14);
1-[3-(этилсульфонимидоил)-4-[3-метил-6-(трифторметил)имидазо[4,5-b]пиридин-2-ил]фенил]циклопропанкарбонитрила (соединение Р15);
[5-циклопропил-2-[7-(трифторметил)имидазо[1,2-b]пиридазин-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение Р16);
1-[5-(этилсульфонимидоил)-6-[6-(трифторметил)пиразоло[4,3-с]пиридин-2-ил]-3-пиридил]циклопропанкарбонитрила (соединение Р17);
[5-циклопропил-2-[5-(трифторметилсульфанил)-1,3-бензоксазол-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение Р18) и
[5-циклопропил-2-[5-(трифторметилсульфонил)-1,3-бензоксазол-2-ил]-3-пиридил]этилиминооксо-λ6-сульфана (соединение Р19).
16. Композиция, обладающая инсектицидной, акарицидной или нематоцидной активностью, содержащая инсектицидно, акарицидно или нематоцидно эффективное количество соединения формулы (I) по любому из пп. 1-15 и необязательно вспомогательное средство или разбавитель.
17. Способ борьбы с насекомыми, клещами или нематодами и осуществления их контроля, который предусматривает применение по отношению к вредителю, к месту обитания вредителя или к растению, восприимчивому к поражению вредителем, инсектицидно, акарицидно или нематоцидно эффективного количества соединения формулы (I) по любому из пп. 1-15 или композиции по п. 16.
18. Способ защиты материала для размножения растений от поражения насекомыми, клещами или нематодами, который предусматривает обработку материала для размножения или участка, где посажен материал для размножения, с помощью композиции по п. 16.
| EP 3252046 A1, 06.12.2017 | |||
| WO 2017084879 A1, 26.05.2017 | |||
| RU 2013134464 A, 27.01.2015 | |||
| WO 2014142292 A1, 18.09.2014 | |||
| WO 2014119679 A1, 07.08.2014 | |||
| ИНСЕКТИЦИД, АКАРИЦИД И НЕМАТОЦИД, СОДЕРЖАЩИЕ В КАЧЕСТВЕ АКТИВНОГО КОМПОНЕНТА ПРОИЗВОДНОЕ 3-ТРИАЗОЛИЛФЕНИЛСУЛЬФИДА | 2005 |
|
RU2394819C2 |
Авторы
Даты
2024-03-29—Публикация
2019-06-06—Подача