Настоящее изобретение относится к композиции для применения для устранения воспаления у субъекта, нуждающегося в этом, где указанная композиция включает следующие ингредиенты: Achillea millefolium, Aconitum napellus, Arnica montana, Atropa bella-donna, Bellis perennis, Calendula officinalis, Echinacea purpurea, Echinacea, Hamamelis virginiana, Hepar sulfuris, Hypericum perforatum, Matricaria recutita, Mercurius solubilis Hahnemanni и Symphytum officinale. Настоящее изобретение также относится к фармацевтической композиции, включающей указанную композицию и противовоспалительное лекарственное средство. Кроме того, настоящее изобретение также включает набор для применения для устранения воспаления у субъекта, нуждающегося в этом, включающий (i) указанную композицию и (ii) противовоспалительное лекарственное средство.
Поскольку острый воспалительный ответ является защитной реакцией, формирующейся для восстановления поврежденных тканей и удаления инвазивных организмов, он идеально само-ограничивается и приводит к полному расслоению лейкоцитарных инфильтратов и клиренсу клеточного дебриса, обеспечивающего возвращение к гомеостазу (Serhan, 2014).
Бесчисленное число раз каждый день острый воспалительный ответ защищает от инвазивных микроорганизмов, повреждений и внутренних кровоизлияний, например, вызванных хирургическими операциями повреждений тканей. Эти проблемы остаются незамеченными, поскольку они являются самоограничивающимися и разрешаются естественным путем без прогрессирования до хронического воспаления. Маркеры воспаления периферической крови присутствуют при развитии множества распространенных заболеваний, включая воспалительное заболевание кишечника, сердечно-сосудистое заболевание, нейродегенеративное заболевание и рак. Несмотря на то, что острое воспаление является защитным, избыточное скопление нейтрофилов усиливает повреждение и воспаление коллатеральных тканей (Serhan and Levy, 2018).
В течение многих лет устранение воспаления считалось пассивным явлением, связанным с исключением воспалительного стимула, завершением синтеза хемоаттрактантов, разбавлением хемокинов и предотвращением дополнительного накопления лейкоцитов. Однако некоторые исследования показали, что эндогенные ингибиторы миграции лейкоцитов действуют в качестве нейтрализующего механизма против промотеров хемокинов и адгезии молекул рекрутинга клеток. Более того, существуют указания на то, что разрешение воспаления является активным процессом, вызванным биосинтезом активных медиаторов, так называемых специфических про-разрешающих медиаторов (SPM). В связи с этим, гомеостаз восстанавливается после индукции SPM, которые действуют как специфичные клеточные рецепторы для регуляции миграции лейкоцитов и снижения продуцирования воспалительных медиаторов, а также ускоряют клиренс мертвых клеток и восстановление тканей (Salisbury and Spite, 2016).
Основные признаки устранения воспаления включают ограничение или прекращение скоплений кроветворных клеток, контррегуляцию хемокинов и цитокинов, выключение сигнальных путей, связанных с выживаемостью лейкоцитов, индукцию лейкоцитарного апоптоза и их последовательного удаления с использованием эффероцитоза макрофагами, перепрограммирование макрофагов из клеток, активированных по классическому пути, в клетки активированные по альтернативному пути, возвращение не-апоптозных клеток в сосудистую систему или лимфатическую систему, и в итоге индукцию процесса заживления. Неэффективность одного или более этапов разрешения воспаления может быть включенной в патогенез некоторых хронических заболеваний человека, таких как замедленное заживление раны или ткани или фиброз. Дополнительно, хроническое неразрешенное воспаление может принимать участие в развитии аутоиммунных заболеваний (Sugimoto et al, 2016).
Описаны различные лекарственные средства, представляющие собой модуляторы воспаления. Однако такие лекарственные средства обычно оказывают антагонистическое действие на противовоспалительную среду (Serhan, 2014). Наиболее известными противовоспалительными агентами являются нестероидные противовоспалительные лекарственные средства, такие как селективные и неселективные ингибиторы циклооксигеназы 2. Кроме того, сообщалось, что гомеопатические лекарственные композиции, такие как Traumeel® (фирмы Biologische Heilmittel Heel GmbH, Германия), характеризуются противовоспалительной активностью при остром воспалении (Schneider, 2011).
Таким образом, существует только ограниченное количество про-разрешающих средств, которые находятся на стадии клинических испытаний. Резольвин Е1 и его синтетический аналог RX-100045 исследовали при различных воспалительных заболеваниях (Lee, 2012). Соединение на основе LXA4 исследовали при местном лечении экземы (Wu et al, 2013). Препарат АР214, который является агонистом меланокортина, характеризуется про-разрешающими эффектами в экспериментальных системах и при почечной недостаточности (Montero-Melendez et al, 2011).
Существует необходимость в разработке композиций, способных устранять воспаление у субъекта, чтобы оказывать лечебное действие на патофизиологические состояния, при которых наблюдается замедленное разрешение воспаления.
Техническая проблема, лежащая в основе настоящего изобретения, заключается в обеспечении средств и способов для удовлетворения упомянутых выше потребностей. Техническая проблема решена, как описано в вариантах осуществления настоящего изобретения, определенных в пунктах формулы изобретения и в настоящем описании, приведенном ниже.
Настоящее изобретение относится к композиции для применения для устранения воспаления у субъекта, нуждающемся в этом, где указанная композиция включает следующие ингредиенты: Achillea millefolium, Aconitum napellus, Arnica montana, Atropa bella-donna, Bellis perennis, Calendula officinalis, Echinacea purpurea, Echinacea, Hamamelis virginiana, Hepar sulfuris, Hypericum perforatum, Matricaria recutita, Mercurius solubilis Hahnemanni и Symphytum officinale.
Термин "композиция", использованный здесь, означает смесь экстрактов, кроме прочего, из биологических источников, таких как растения, которые здесь описаны. Предпочтительно, указанная композиция может дополнительно включать другие ингредиенты и, более предпочтительно, включать фармацевтически приемлемый носитель и/или разбавитель.
Предпочтительно, такими дополнительными ингредиентами могут являться стабилизаторы, смачивающие агенты, фармацевтические носители, дополнительные фармацевтически активные агенты, агенты, регулирующие высвобождение и т.п. Предпочтительные разбавители включают воду, спирты, физиологические солевые растворы, буферные растворы, такие как фосфатно-солевые буферные растворы, сироп, масло, воду, эмульсии, различные типы смачивающих агентов и т.п.Согласно настоящему изобретению предпочтительной является композиция, которая также включает по меньшей мере один фармацевтически приемлемый носитель и/или разбавитель. Носитель(и) должен быть приемлемым в смысле совместимости с другими ингредиентами состава и не оказывать вредного воздействия на пациента, которому вводят указанный состав. Используемый фармацевтический носитель может включать твердое вещество, гель или жидкость. Типичные твердые носители включают лактозу, сульфат кальция, сахарозу, тальк, желатин, агар, пектин, аравийскую камедь, стеарат магния, стеариновую кислоту и т.п.Аналогичным образом, носитель или разбавитель может включать материал для замедленного высвобождения, хорошо известный в данной области техники, такой как глицерилмоностеарат или глицерилдистеарат в отдельности или в смеси с воском. Указанные приемлемые носители включают описанные выше и другие вещества, известные в данной области техники, см., например, справочник Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, Pennsylvania, European Pharmacopeia, Homeopathic Pharmacopeia of the USA или HAB. Фармацевтический приемлемый разбавитель выбирают таким образом, чтобы он не влиял на биологическую активность комбинации. Примеры таких разбавителей включают дистиллированную воду, физиологический солевой раствор, растворы Рингера, раствор декстрозы и раствор Ханка. Кроме того, фармацевтическая композиция или состав может включать также другие носители, адъюванты или нетоксичные нетерапевтические неиммуногенные стабилизаторы и т.п.
Композицию можно перерабатывать для применения для устранения воспаления. Соответственно, следует понимать, что в зависимости от требуемого способа введения, композицию можно перерабатывать в формы для системного или местного лечения. Предпочтительно, композиция описанная здесь, предназначена для системного или местного лечения. Предпочтительно предполагается пероральное введение, например, в форме таблеток, раствора или ампул с раствором, или введение в виде инъекции. Однако, в зависимости от природы или механизма действия, композицию можно вводить другими способами, включающими чрескожное, внутримышечное, подкожное, пероральное, внутривенное или местное введение. Предпочтительно, композицию можно перерабатывать в формы для струйного введения или для непрерывного введения, как подробно здесь описано. Предпочтительно композицию по настоящему изобретению перерабатывают в лекарственное средство, как подробно здесь описано.
Термин "воспаление" использованный здесь, означает патофизиологический ответ субъекта на вредное воздействие, например, патогенов, клеточное повреждение или раздражители. Типичные признаки воспаления включают повышенную температуру, боль, покраснение или другие кожные реакции, отек или нарушенное функционирование ткани. Воспаление может представлять собой острое воспаление или хроническое воспаление. Предпочтительно, воспалением по настоящему изобретению является хроническое воспаление. Воспаление, или особенно хроническое воспаление, может предпочтительно быть связанным с заболеванием или нарушением, выбранным из группы, состоящей из ревматоидного артрита, остеоартрита, перитонита, синдрома раздраженного кишечника, COPD, системной красной волчанки, рассеянного склероза, псориаза, сахарного диабета типа 1, скелетно-мышечных повреждений, мышечного воспаления и воспаления суставов, такого как растяжение связок голеностопного сустава.
Термин "устранение (разрешение) воспаления", использованный здесь, означает активный процесс, который приводит к восстановлению целостности ткани и функции ткани, поврежденной воспалением. Более подробно, воспаление представляет собой патофизиологический процесс в ответ на инфекцию или повреждение ткани. Обычно процесс начинается при детектировании инфекции или повреждения ткани тканерезидентными клетками врожденной иммунной системы. Секреция химических сигналов, таких как хемокины и цитокины, приводит к накоплению (рекрутингу) циркулирующих нейтрофилов в участке повреждения или инфекции. При скоплении нейтрофилов в гное или гнойном эксудате происходит переключение класса липидных медиаторов. Липоксины (LX) стимулируют нефлогистонное накопление моноцитов. LX, резолвины (Rv) и другие специализированные про-разрешающие медиаторы (SPM) продуцируются в гное для ограничения или остановки дополнительной инфильтрации ткани нейтрофилами. Медиаторы SPM, Rv, марезины (MaR) и протектины стимулируют эффероцитоз апоптотических нейтрофилов и клеточного дебриса макрофагами. Разрешающие макрофаги и апоптотические нейтрофилы также продуцируют SPM. При отеке также происходит перенос циркулирующих n-З полиненасыщенных жирных кислот (PUFA) в эксудаты для временного преобразования в SPM клетками эксудата. MaR и специфичные Rv ускоряют заживление ран и регенерацию ткани (Serhan (2017)). Затем гомеостаз ткани может быть восстановлен. Существуют различные воспалительные заболевания, при которых устранение воспаления явно ухудшается, что приводит, например, к хроническому воспалению.
Термин "устранение (разрешение) воспаления" по настоящему изобретению означает, что запущен активный процесс разрешения воспаления и что такие хронические воспалительные процессы могут быть устранены. Типичные характеристические изменения разрешения воспаления представляют собой синтез так называемых специализированных про-разрешающих медиаторов (SPM) и накопление макрофагов, особенно, разрешающего фенотипа. Таким образом, устранение воспаления, как здесь описано, предпочтительно включает уменьшение накопления нейтрофилов в участке воспаления. Кроме того, устранение воспаления предпочтительно включает индукцию синтеза по меньшей мере одного SPM и, более предпочтительно, по меньшей мере одного SPM, который выбирают из группы, включающей LxA4, LxB4, RvD2, RvD5, Mar-2 и NPD1. Содержание таких SPM предпочтительно в значительной степени увеличивается через 4 ч после введения композиции субъекту по сравнению с контрольным субъектом. Кроме того, устранение воспаления включает предпочтительно накопление макрофагов. Более предпочтительно, содержание указанных макрофагов в очаге воспаления значительно увеличивается через 24 ч после введения композиции субъекту по сравнению с контрольным субъектом.
Предпочтительно, термин "устранение (разрешение) воспаления", использованный здесь, может означать любое значительное улучшение разрешения, такое как индукция синтеза SPM и/или рекрутинг макрофагов. Однако, более предпочтительно, термин "устранение (разрешение) воспаления" означает лечение воспаления, при котором полностью восстанавливаются целостность ткани и ее функционирование. Следует понимать, что устранение воспаления может не происходить у 100% субъектов, которым вводили композицию. Термин, однако, требует, чтобы устранение произошло у статистически значимой части субъектов (например, в группе людей в ходе когортного исследования). Специалист в данной области техники может определить, является ли часть статистически значимой, с использованием различных хорошо известных статистических методов оценки, например, определения доверительных интервалов, определения величины р, т-теста Стъюдента, теста Манна-Витни и т.п.Подробное описание представлено в монографии Dowdy and Wearden, Statistics for Research, John Wiley & Sons, New York (1983). Предпочтительные доверительные интервалы составляют по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99%. Величины р предпочтительно составляют 0,05, 0,01, 0,005 или 0,0001.
Термин "субъект", использованный здесь, означает млекопитающее и предпочтительно человека. Указанный субъект должен нуждаться в устранении воспаления, т.е. он должен страдать от острого или хронического воспаления. Более предпочтительно, субъект страдает от хронического воспаления и/или кроме того страдает от связанного с ним заболевания, и предпочтительно от заболевания или нарушения, выбранного из группы, состоящей из ревматоидного артрита, остеоартрита, перитонита, синдрома раздраженного кишечника, COPD, системной красной волчанки, рассеянного склероза, псориаза, сахарного диабета типа 1, скелетно-мышечных повреждений, мышечного воспаления и воспаления суставов, такого как растяжение связок голеностопного сустава.
Растения в соответствии с настоящим изобретением, т.е. Achillea millefolium (тысячелистник), Aconitum napellus (аконит аптечный), Arnica montana (арника горная), Atropa bella-donna (беладонна обыкновенная), Bellis perennis (маргаритка многолетняя), Calendula officinalis (календула), Echinacea purpurea (эхинацея пурпурная), Echinacea (эхинацея узколистная), Hamamelis virginiana (гамамелис виргинский), Hypericum perforatum (зверобой обыкновенный), Matricaria recutita (ромашка лекарственная) и Symphytum officinale (окопник лекарственный), хорошо известны специалистам в данной области техники и ботанически охарактеризованы. Соответственно, указанные растения легко идентифицировать в качестве исходного материала для получения композиции по настоящему изобретению, культивировать и/или собирать. Например, растения можно получать при выращивании растущей рассады в теплице в стандартных условиях влажности, температуры и освещения растения, культивировании указанных растений в течение достаточного времени для продуцирования вторичных растительных метаболитов и сборе растений или их частей, необходимых для процесса экстракции, описанного здесь. Кроме того, указанные растения в качестве исходного материала для получения композиции по настоящему изобретению можно предпочтительно также получить из дикорастущих источников. В таком случае растения идентифицируют с использованием микро- и макроскопических методов исследования.
Другие компоненты композиции также являются хорошо известными химическими реагентами в гомеопатии, такими как Hepar sulfuris (сульфид кальция) и Mercurius solubilis Hahnemanni (амидонитрат ртути). Кроме того, эти компоненты, прежде всего, в качестве гомеопатических ингредиентов, хорошо известны специалистам в данной области техники.
Композиция по настоящему изобретению включает указанные компоненты в следующих гомеопатических разведениях:
Achillea millefolium D3,
Aconitum napellus D2,
Arnica montana D2,
Atropa bella-donna D2,
Bellis perennis D2,
Calendula officinalis D2,
Echinacea purpurea D2,
Echinacea D2,
Hamamelis virginiana Dl,
Hepar sulfuris D6,
Hypericum perforatum D2,
Matricaria recutita D3,
Mercurius solubilis Hahnemanni D6, и
Symphytum officinale D6.
Термин "Achillea millefolium D3", использованный здесь, означает разведение матричной настойки Achillea millefolium, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка (тинктура), используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. D-разбавления матричной настойки можно осуществить с использованием следующей схемы разбавления: 3 части матричной настойки разбавляют 7 частями этанола (70% об./об.) получая разведение D1. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин " Aconitum napellus D2", использованный здесь, означает разведение матричной настойки Aconitum napellus, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 2 части матричной настойки разбавляют 8 частями этанола (50% об./об.) получая разведение D1. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин "Arnica montana D2", использованный здесь, означает разведение матричной настойки Arnica montana, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка (соответствующая разбавлению D1), используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 1 часть разбавления D1 разбавляют 9 частями этанола (90% об./об.) получая разведение D2. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин "Atropa bella-donna D2", использованный здесь, означает разведение матричной настойки Atropa bella-donna, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 2 части матричной настойки разбавляют 8 частями этанола (50% об./об.) получая разведение D1. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин "Bellis perennis D2", использованный здесь, означает разведение матричной настойки Bellis perennis, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 2 части матричной настойки разбавляют 8 частями этанола (50% об./об.) получая разведение D1. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин "Calendula officinalis D2", использованный здесь, означает разведение матричной настойки Calendula officinalis, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 3 части матричной настойки разбавляют 7 частями этанола (70% об./об.) получая разведение D1. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин " Echinacea purpurea D2", использованный здесь, означает разведение матричной настойки Echinacea purpurea, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 3 части матричной настойки разбавляют 7 частями этанола (70% об./об.) получая разведение D1. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин " Echinacea D2", использованный здесь, означает разведение матричной настойки Echinacea, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 3 части матричной настойки разбавляют 7 частями этанола (70% об./об.) получая разведение D1. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин "Hamamelis virginiana D1", использованный здесь, означает разведение матричной настойки Hamamelis virginiana, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. Матричную настойку дополнительно обрабатывают, как описано ниже.
Термин "Hepar sulfuris D6", использованный здесь, означает разведение материала Hepar sulfuris, полученного согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутый выше материал, используемый в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 1 часть материала растирают с 9 частями моногидрата лактозы, получая таким образом порошкообразный материал D1. 1 часть порошкообразного материала растирают с 9 частями моногидрата лактозы, получая таким образом порошкообразный материал D2. Обработанный материал D2 дополнительно растирают (1:10), как указано выше, получая таким образом порошкообразные материалы D3 и D4. Порошкообразный материал D4 дополнительно обрабатывают, как описано ниже.
Термин " Hypericum perforatum D2", использованный здесь, означает разведение матричной настойки Hypericum perforatum, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 3 части матричной настойки разбавляют 7 частями этанола (70% об./об.), получая таким образом разведение D1. Данное разведение дополнительно обрабатывают как описано ниже.
Термин "Matricaria recutita D3", использованный здесь, означает разведение матричной настойки Matricaria recutita, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 3 части матричной настойки разбавляют 7 частями этанола (70% об./об.) получая разведение D1. Данное разведение дополнительно обрабатывают, как описано ниже.
Термин " Mercurius solubilis Hahnemanni D6", использованный здесь, означает разведение материала Mercurius solubilis Hahnemanni, полученного согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутый выше материал, используемый в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 1 часть материала растирают с 9 частями моногидрата лактозы, получая таким образом порошкообразный материал D1. 1 часть порошкообразного материала D1 растирают с 9 частями моногидрата лактозы, получая таким образом порошкообразный материал D2. Порошкообразный материал D2 дополнительно растирают (1:10), как указано выше, получая порошкообразные материалы D3 и D4. Порошкообразный материал D4 дополнительно обрабатывают, как описано ниже.
Термин "Symphytum officinale D6", использованный здесь, означает разведение матричной настойки Symphytum officinale, полученной согласно текущей версии гомеопатической фармакопеи, и прежде всего, Германской гомеопатической фармакопеи (НАВ), предпочтительно, вышедшей в 2017 г, или Европейской фармакопеи (Ph. Eur.), предпочтительно версии 9.5. Предпочтительно, упомянутая выше матричная настойка, используемая в композиции по настоящему изобретению, характеризуется аналитическими параметрами, установленными в соответствующей монографии. 1 часть разведения D1 последовательно разбавляют 9 частями этанола (70% об./об.), получая таким образом разведение D2. 1 часть разведения D2 дополнительно разбавляют 9 частями этанола (70% об./об.), получая таким образом D3, 1 часть разведения D3 затем разбавляют 9 частями этанола (50% об./об.), получая таким образом разведение D4. Данное разведение D4 дополнительно обрабатывают как описано ниже.
Разведение D1 Achillea millefolium, разведение D1 Matricaria recutita и разведение D4 Symphytum officinale смешивали и действие смеси усиливали дважды 1:10 с использованием воды для инъекций, получая таким образом разведение D3 Achillea millefolium, разведение D3 Matricaria recutita и разведение D6 Symphytum officinale.
Разведение D1 Aconitum napellus, разведение D1 Atropa bella-donna, разведение D1 Bellis perennis, разведение D1 Calendula officinalis, разведение D1 Echinacea, разведение D1 Echinacea purpurea, разведение D1 Hypericum perforatum смешивали и действие смеси усиливали дважды 1:10 с использованием воды для инъекций получая таким образом разведение D2 Aconitum napellus, разведение D2 Atropa bella-donna, разведение D2 Bellis perennis, разведение D2 Calendula officinalis, разведение D2 Echinacea, разведение D2 Echinacea purpurea, разведение D2 Hypericum perforatum.
Действие порошкообразного материала D4 Hepar sulfuris и порошкообразного материала D4 Mercurius solubilis Hahnemanni усиливали дважды 1:10 с использованием воды для инъекций, получая таким образом разведение D6 Hepar sulfuris и разведение D6 Mercurius solubilis Hahnemanni, соответственно.
Действие матричной настойки Hamamelis virginiana усиливали 1:10 с использованием воды для инъекций, получая таким образом разведение D1 Hamamelis virginiana.
Эти конечные полученные разведения последовательно смешивали друг с другом, с разведением D2 Arnica montana, водой для инъекций и хлоридом натрия, получая таким образом композицию для применения по настоящему изобретению.
Предпочтительно, композиция предназначенная для применения по настоящему изобретению, представляет собой коммерческий лекарственный препарат Traumeel® в виде капель, таблеток, мази, раствора для инъекций или геля (фирмы Biologische Heilmittel Heel GmbH, Германия).
В приведенной ниже таблице перечислены компоненты и количества в составе композиции по настоящему изобретению для таблеток, мази, капель, геля и раствора для инъекций (в ампулах).


Обычно композиция для применения по настоящему изобретению предназначена для введения в количестве, достаточном для устранения воспаления. Следует понимать, что доза для введения зависит от нескольких факторов, хорошо известных лечащим врачам и включающих пол, возраст, массу тела и общее состояние здоровья. Более того, доза будет зависеть от способа введения. Обычно для местного введения необходима доза, отличная от системного введения. Аналогичным образом, способ введения также будет влиять на терапевтически эффективную дозу. Например, при пероральном введении может потребоваться другая доза, отличающаяся от внутрибрюшинной инъекции. Предпочтительно, композицию по настоящему изобретению вводят в виде раствора. Более предпочтительно, доза, предлагаемая субъекту, должна соответствовать количеству, обеспечиваемому по меньшей мере 1,5 мл композиции (раствор для инъекций) на 1 кг массы тела мыши в течение 6 дней.
Если композицию по настоящему изобретению получают в виде раствора, то в день следует вводить 2,2 мл (30 мкл/кг массы тела) раствора в ампуле. Такой раствор в ампуле, предпочтительно, можно вводить от 1 до 3 раз в неделю. Однако, предпочтительно дозу можно увеличить вплоть до дозы в 5 или 10 раз превышающей указанную дозу. В острых случаях раствор в ампуле можно вводить ежедневно.
Предпочтительно, упомянутую выше дозу можно обеспечить при однократном введении (вливание) или несколько раз в течение дня. Кроме того, предполагается также, что доза предпочтительно обеспечивается с использованием устройств для непрерывного высвобождения, которые обеспечивают непрерывное введение дозы в течение дня.
Способы получения композиции надлежащим образом для обеспечения упомянутой выше суточной дозы хорошо известны в данной области техники. Стандартными составами могут являться таблетки, капсулы, растворы, такие как настойки для кожного, или жидкости для перорального применения, растворы для инъекций, гели или мази.
Композицию по настоящему изобретению можно использовать совместно с противовоспалительными лекарственными средствами или с другими лекарственными средствами, устраняющими воспаление. Противовоспалительные лекарственные средства могут представлять собой нестероидные противовоспалительные средства (NSAID). Такие NSAID могут являться селективными или неселективными ингибиторами циклооксигеназы 2 (СОХ-2), которые широко используют для противовоспалительной терапии. Типичными NSAID являются салицилаты, и предпочтительно аспирин, дифлунизал, салициловая кислота и другие салицилаты, салсалат, производные пропионовой кислоты, и предпочтительно ибупрофен, дексибупрофен, напроксен, фенопрофен, кетопрофен, декскетопрофен, флурбипрофен, оксапрозин, локсопрофен, производные уксусной кислоты, и предпочтительно индометацин, толметин, сулиндак, этодолак, кеторолак, диклофенак, ацеклофенак, набуметон, производные еноловой кислоты (оксикам), и предпочтительно пироксикам, мелоксикам, теноксикам, дроксикам, лорноксикам, фенилбутазон, производные антраниловой кислоты (фенаматы), и предпочтительно мефенамовая кислота, меклофенамовая кислота, флуфенамовая кислота, толфенамовая кислота, и селективные ингибиторы СОХ-2 (коксибы), предпочтительно целекоксиб, парекоксиб и эторикоксиб. Кроме NSAID совместно с композицией по настоящему изобретению можно использовать другие гомеопатические лекарственные средства или композиции.
Упомянутые выше противовоспалительные лекарственные средства или другие лекарственные средства для устранения воспаления можно вводить одновременно с композицией по настоящему изобретению или последовательно до или после введения указанной композиции. Одновременное введение композиции с указанными противовоспалительными лекарственными средствами или другими лекарственными средствами для разрешения воспаления можно обеспечить при введении единой композиции, состоящей из композиции по настоящему изобретению и указанных противовоспалительных лекарственных средств или других лекарственных средств для устранения воспаления, или их можно вводить в виде отдельных композиций.
Преимущество настоящего изобретения заключается в том, что при введении мыши, страдающей от вызванного зимозаном перитонита, композиции включающей указанные ингредиенты, можно обеспечить эффективное устранение воспаления. Композиция положительно влияет на кинетику скопления нейтрофилов и укорачивает индекс разрешения почти на 6 ч по сравнению с контролем. Кроме того, значительно увеличивается количество макрофагов по сравнению с контрольной группой в участке воспаления, оказывающее положительное действие на устранение воспаления через 24 ч. В итоге было установлено, что синтез различных SPM значительно увеличивался через 4 ч в лечебной группе по сравнению с контрольной группой. Соответственно, композиция по настоящему изобретению была идентифицирована как проявляющая высокую эффективность для устранения воспаления на модельном организме. Благодаря настоящему изобретению можно эффективно устранять воспаление, и особенно, хроническое воспаление при различных патологических процессах.
В основном, настоящее изобретение также относится к способу устранения воспаления у субъекта, нуждающегося в этом, включающему введение указанному субъекту терапевтически эффективного количества композиции, включающей следующие ингредиенты: Achillea millefolium, Aconitum napellus, Arnica montana, Atropa bella-donna, Bellis perennis, Calendula officinalis, Echinacea purpurea, Echinacea, Hamamelis virginiana, Hepar sulfuris, Hypericum perforatum, Matricaria recutita, Mercurius solubilis Hahnemanni и Symphytum officinale. Обычно, субъектом, нуждающимся в разрешении воспаления, является субъект, как описано здесь, и прежде всего, субъект, страдающий от хронического воспаления или связанного с ним заболевания, как описано здесь.
Ниже описаны наиболее предпочтительные варианты композиции для применения по настоящему изобретению.
В одном предпочтительном варианте композиции для применения, указанное устранение воспаления включает снижение накопления нейтрофилов в участке воспаления.
В другом предпочтительном варианте композиции для применения, указанное устранение воспаления включает индукцию синтеза по меньшей мере специализированного про-разрешающего медиатора (SPM). Более предпочтительно указанный по меньшей мере один SPM выбирают из группы, включающей LxA4, LxB4, RvD2, RvD5, Mar-2 и NPD1. Более предпочтительно указанный по меньшей мере один SPM значительно увеличивается через 4 ч после введения композиции субъекту по сравнению с контрольным субъектом.
В предпочтительном варианте композиции для применения, указанное устранение воспаления включает накопление макрофагов. Более предпочтительно количество указанных макрофагов в значительной степени увеличивается в очаге воспаления через 24 ч после введения композиции субъекту по сравнению с контрольным субъектом.
В еще более предпочтительном варианте композиции для применения, указанные ингредиенты композиции используют в следующих гомеопатических разведениях:
Achillea millefolium D3,
Aconitum napellus D2,
Arnica montana D2,
Atropa bella-donna D2,
Bellis perennis D2,
Calendula officinalis D2,
Echinacea purpurea D2,
Echinacea D2,
Hamamelis virginiana Dl,
Hepar sulfuris D6,
Hypericum perforatum D2,
Matricaria recutita D3,
Mercurius solubilis Hahnemanni D6 и
Symphytum officinale D6.
Более предпочтительно указанная композиция предназначена для введения в количестве, соответствующем количеству, которое обеспечивает по меньшей мере 1,5 мл композиции на кг массы тела мыши в течение 6 дней.
В предпочтительном варианте композиции для применения, указанное воспаление является хроническом воспалением. Более предпочтительно указанное воспаление связано с заболеванием или нарушением, которые выбирают из группы, состоящей из ревматоидного артрита, остеоартрита, перитонита, синдрома раздраженного кишечника, COPD, системной красной волчанки, рассеянного склероза, псориаза, сахарного диабета типа 1, скелетно-мышечных повреждений, мышечного воспаления и воспаления суставов, такого как растяжение связок голеностопного сустава.
В предпочтительном варианте композиции для применения, указанная композиция предназначена для введения субъекту совместно с противовоспалительным лекарственным препаратом.
В еще более предпочтительном варианте осуществления композиции для применения, указанная композиция предназначена для введения субъекту после его лечения противовоспалительным лекарственным препаратом.
Более предпочтительно указанное противовоспалительное лекарственное средство является нестероидным противовоспалительным лекарственным средством (NSAID) и, более предпочтительно, его выбирают из группы, включающей салицилаты, и предпочтительно аспирин, дифлунизал, салициловая кислота и другие салицилаты, салсалат, производные пропионовой кислоты, и предпочтительно ибупрофен, дексибупрофен, напроксен, фенопрофен, кетопрофен, декскетопрофен, флурбипрофен, оксапрозин, локсопрофен, производные уксусной кислоты, и предпочтительно индометацин, толметин, сулиндак, этодолак, кеторолак, диклофенак, ацеклофенак, набуметон, производные еноловой кислоты (оксикам), и предпочтительно пироксикам, мелоксикам, теноксикам, дроксикам, лорноксикам, фенилбутазон, производные антраниловой кислоты (фенаматы), и предпочтительно мефенамовая кислота, меклофенановая кислота, флуфенамовая кислота, толфенамовая кислота, и селективные ингибиторы СОХ-2 (коксибы), предпочтительно целекоксиб, парекоксиб и эторикоксиб.
В предпочтительном варианте композиции для применения, указанным субъектом является человек.
Настоящее изобретение относится также к фармацевтической композиции, включающей композицию, описанную здесь выше, и противовоспалительное лекарственное средство, предпочтительно, как описано здесь выше.
Настоящее изобретение относится также к набору для применения для устранения воспаления у субъекта, нуждающегося в этом, включающему (i) композицию, описанную здесь выше, и (ii) противовоспалительное лекарственное средство, предпочтительно, как описано здесь выше.
Все ссылки, процитированные в данном описании, включены в него в полном объеме в качестве ссылки, в том числе в отношении раскрытия содержания, на которое конкретно ссылаются.
Фигуры
Фиг. 1. Миграция нейтрофилов в процессе вызванного зимозаном перитонита. НЕ-100 и носитель (1,5 мл/кг) вводили внутрибрюшинно один раз в день в течение 6 дней. Через временной интервал 12-13 ч после последней инъекции перитонит индуцировали зимозаном (0,1 мг/мышь). В день 0, 4, 8 и 24 ч мышей (6-8 животных/группа/время) умерщвляли, перитонеальные эксудаты собирали и анализировали методом проточной цитометрии. НЕ-100 положительно модифицирует кинетику накопления нейтрофилов и укорачивает индекс разрешения (Ri) почти на 6 ч. Ri для исследованного соединения определяется как время для достижения снижения числа нейтрофилов до 50% по сравнению с контрольным соединением: Ri=Т50 носитель - Т50 соединения.
Фиг. 2. Миграция макрофагов в процессе вызванного зимозаном перитонита. НЕ-100 и носитель (1,5 мл/кг) вводили внутрибрюшинно один раз в день в течение 6 дней. Через временной интервал 12-13 ч после последней инъекции перитонит индуцировали цимозаном (0,1 мг/мышь). Через 0, 4, 8 и 24 ч мышей умерщвляли, перитонеальные эксудаты собирали и анализировали методом проточной цитометрии. Большее число макрофагов детектировали в группе лечения через 24 ч. Макрофаги принимают участие в клиренсе дебриса в очаге воспаления (эффероцитоз). Считается, что увеличение их числа приводит к положительному действию на разрешение. Величина *р<0,05.
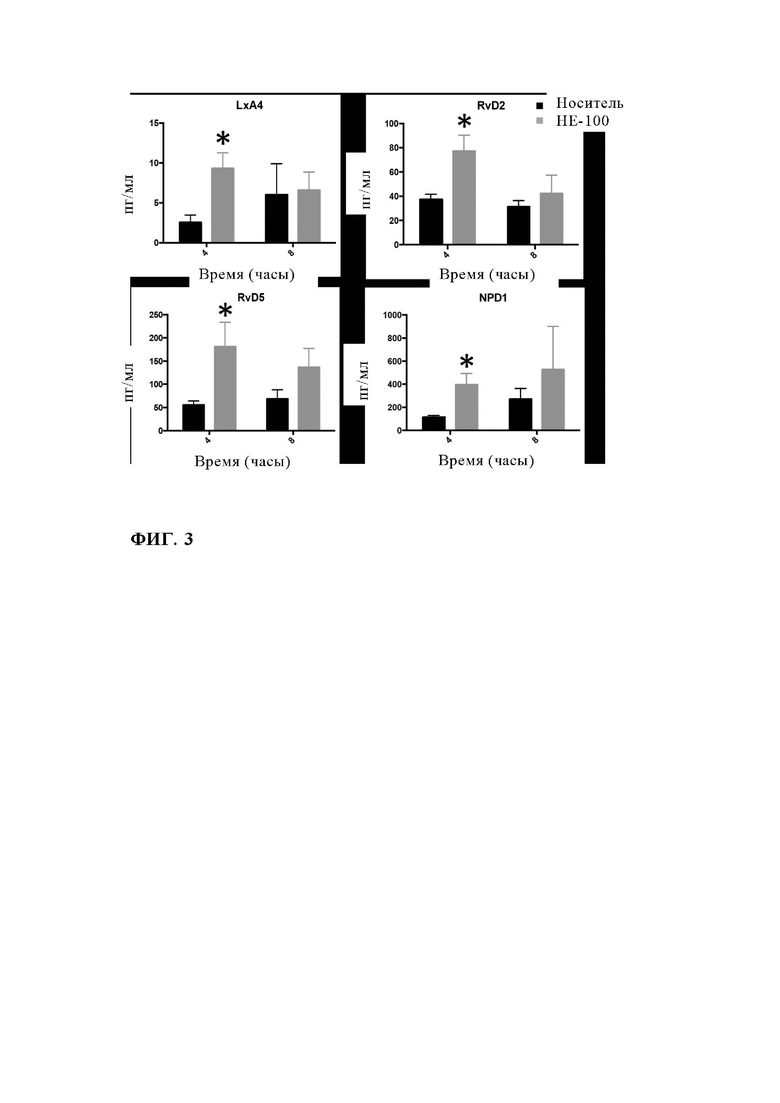
Фиг. 3. Синтез SPM через 4 ч после вызванного зимозаном перитонита. НЕ-100 и носитель (1,5 мл/кг) вводили внутрибрюшинно ежедневно в течение 6 дней. Через временной интервал 12-13 ч после последней инъекции перитонит индуцировали цимозаном (0,1 мг/мышь). Через 0, 4, 8 и 24 ч мышей умерщвляли, перитонеальные эксудаты собирали и анализировали методом ЖХ-МС/МС. Увеличенный синтез SPM детектировали в группе лечения через 4 ч. Считается, что увеличение их числа приводит к положительному действию на разрешение. Величина *р<0,05.
Примеры
Изобретение проиллюстрировано ниже следующими примерами, которые в любом случае не ограничивают объем изобретения.
Пример 1.
НЕ-100 и носитель (1,5 мл/кг) вводили внутрибрюшинно ежедневно в течение 6 дней. Мышей взвешивали раз в день для расчета дозы соединений. Через временной интервал 12-13 ч после последней инъекции перитонит индуцировали зимозаном (0,1 мг/мышь). Через 0, 4, 8 и 24 ч мышей (6-8 животных/группа/время) умерщвляли. Воспалительный эксудат получали при промывании брюшной полости PBS. Число клеток немедленно подсчитывали с использованием счетчика клеток Scepter (Merck Millipore) и наносили метку для идентификации подпопуляции и количественного определения методом цитометрии (анализатор Macs quant - Miltenyi). Эксудаты центрифугировали и суспендировали для получения суспензии с концентрацией 1×106 клеток/мл. Затем на клетки наносили метку соответствующим антителом (Miltenyi biotech): CD45-vioblue (Miltenyi), F4/80-FITC (Miltenyi), GR1-PE (Biolegend). Среди CD45 положительных клеток нейтрофилы сортировали следующим образом: GR1+, F4/80-.
Пример 2.
НЕ-100 и носитель (1,5 мл/кг) вводили внутрибрюшинно ежедневно в течение 6 дней. Мышей взвешивали раз в день для расчета дозы соединений. Через временной интервал 12-13 ч после последней инъекции перитонит индуцировали зимозаном (0,1 мг/мышь). Через 0, 4, 8 и 24 ч мышей (6-8 животных/группа/время) умерщвляли. Воспалительный эксудат получали при промывании брюшной полости PBS. Число клеток немедленно подчитывали с использованием счетчика клеток Scepter (Merck Millipore) и наносили метку для идентификации подпопуляции и количественного определения методом цитометрии (анализатор Macs quant Miltenyi). Эксудаты центрифугировали и суспендировали для получения суспензии с концентрацией 1×106 клеток/мл. Затем на клетки наносили метку соответствующим антителом (Miltenyi biotech): CD45-vioblue (Miltenyi), F4/80-FITC (Miltenyi), GR1-PE (Biolegend). Среди положительных клеток CD45 резидентные макрофаги сортировали следующим образом: GR1-, F4/80+, higt, моноциты инфильтрата сортировали как GR1-, F4/80+
Пример 3.
Протокол экстракции и анализ ЖХ/МС/МС осуществляли, как описано в статье (Le Faouder et al (2013)) с использованием модифицированного метода Ambiotis Standard Operating Procedure. Полученные образцы брюшных лаважей экстрагировали с использованием 96-луночного твердофазного экстрактора (Oasis HLB фирмы Waters). Анализ ЖХ-МС/МС осуществляли в системе U-HPLC (фирмы Agilent LC1290 Infinity), совмещенной с тройным квадрупольным масс-спектрометром фирмы Agilent 6490 (фирмы Agilent Technologies), снабженным электрораспылительной ионизацией, работающей в отрицательном режиме. Обратно-фазную U-ВЭЖХ проводили на колонке Kinetex Biphenyl (2,1 мм*50 мм*1,7 мкм) (фирмы Phenomenex) при 50°С.Для мониторинга и количественного анализа биоактивных липидов анализ проводили в режиме детектирования мультиреакционного мониторинга (MRM). Идентификацию осуществляли с использованием чистых аутентичных стандартов. Детектирование, интегрирование и количественный анализ пиков осуществляли с использованием программного обеспечения MassHunter Quantitative Analysis (фирмы Agilent Technologies). Биоактивными липидами, которые определяли количественно, являлись:
LxA4 - медиаторы, производные арахидоновой кислоты.
RvD2, RvD5 и NPD1 - медиаторы, производные докозагексановой кислоты кислоты.
Список процитированной литературы
1. Le Faouder P. et al. 'LC MS/MS method for rapid and concomitant quantification of pro-inflammatory and pro-resolving polyunsaturated fatty acid metabolites', Journal of Chromatography В, т.932, cc. 123 133 (2013). doi: 10.1016/j.jchromb.2013.06.14
2. Lee С.H. 'Resolvins as new fascinating drug candidates for inflammatory diseases', Archives of Pharmacal Research, т.35(1), cc. 3-7 (2012). doi: 10.1007/sl2272-012-0121-z
3. Montero-Melendez T. et al. 'The melanocortin agonist AP214 exerts antiinflammatory and proresolving properties', American Journal of Pathology. Elsevier Inc., т.179(1), cc. 259-269 (2011). doi: 10.1016/j.ajpath.2011.03.042
4. Sansbury В.E., Spite M. 'Resolution of acute inflammation and the role of resolvins in immunity, thrombosis, and vascular biology', Circulation Research, т.119(1), cc. 113-130 (2016). doi: 10.1161/CIRCRESAHA. 116.307308
5. Schneider C. 'Traumeel: an emerging option to nonsteroidal anti-inflammatory drugs in the management of acute musculoskeletal injuries', International Journal of General Medicine, т.4, cc. 225-234 (2011). doi: 10.2147/ijgm.sl6709
6. Serhan C.N. 'Pro-resolving lipid mediators are leads for resolution physiology', Nature, т.510(7503), cc. 92-101 (2014). doi: 10.1038/naturel3479
7. Serhan C.N. 'Treating inflammation and infection in the 21st century: New hints from decoding resolution mediators and mechanisms', FASEB Journal, т.31(4), cc. 1273-1288 (2017). doi: 10.1096/fj.201601222R
8. Serhan C.N., Levy B.D. 'Resolvins in inflammation: Emergence of the pro-resolving superfamily of mediators', Journal of Clinical Investigation, т.128(7), cc. 2657-2669 (2018). doi: 10.1172/JCI97943
9. Sugimoto M. A. et al. 'Resolution of inflammation: What controls its onset?', Frontiers in Immunology, 7(APR) (2016). doi: 10.3389/fimmu.2016.00160
10. Wu S.-H. et al. 'Efficacy and safety of 15(R/S)-methyl-lipoxin A 4 in topical treatment of infantile eczema', British Journal of Dermatology, т.168(1), cc. 172-178 (2013). doi: 10.1111/j. 1365-2133.2012.11177.x


Группа изобретений относится к области фармацевтики, а именно к композициям для устранения острого воспаления у субъекта, нуждающегося в этом, и к набору вышеуказанного назначения. Композиция для устранения острого воспаления у субъекта, нуждающегося в этом, где эта композиция состоит из следующих ингредиентов: Achillea millefolium, Aconitum napellus, Arnica montana, Atropa bella-donna, Bellis perennis, Calendula officinalis, Echinacea purpurea, Echinacea, Hamamelis virginiana, Hepar sulfuris, Hypericum perforatum, Matricaria recutita, Mercurius solubilis Hahnemanni и Symphytum officinale, а также фармацевтически приемлемого носителя и/или разбавителя, где указанные ингредиенты композиции применяют в следующих гомеопатических разведениях: Achillea millefolium D3, Aconitum napellus D2, Arnica montana D2, Atropa bella-donna D2, Bellis perennis D2, Calendula officinalis D2, Echinacea purpurea D2, Echinacea D2, Hamamelis virginiana D1, Hepar sulfuris D6, Hypericum perforatum D2, Matricaria recutita D3, Mercurius solubilis Hahnemanni D6 и Symphytum officinale D6. Фармацевтическая композиция для устранения острого воспаления у субъекта, нуждающегося в этом, включающая вышеуказанную композицию и нестероидное противовоспалительное лекарственное средство (NSAID), где указанное NSAID выбрано из группы, состоящей из салицилатов, и предпочтительно аспирина, дифлунизала, салициловой кислоты и других салицилатов, салсалатов, производных пропионовой кислоты, и предпочтительно ибупрофена, дексибупрофена, фенопрофена, кетопрофена, декскетопрофена, флурбипрофена, оксапрозина, локсопрофена, производных уксусной кислоты, и предпочтительно индометацина, толметина, сулиндака, этодолака, кеторолака, диклофенака, ацеклофенака, набуметона, производных еноловой кислоты (оксикам), и предпочтительно пироксикама, мелоксикама, теноксикама, дроксикама, лорноксикама, фенилбутазона, производных антраниловой кислоты (фенаматы), и предпочтительно мефенамовой кислоты, меклофенамовой кислоты, флуфенамовой кислоты, толфенамовой кислоты, и селективных ингибиторов СОХ-2 (коксибы), предпочтительно целекоксиба, парекоксиба и эторикоксиба. Набор для устранения острого воспаления у субъекта, нуждающегося в этом, включающий композицию, выбранную из вышеуказанных, и нестероидное противовоспалительное лекарственное средство (NSAID), где указанное NSAID выбрано из группы, состоящей из салицилатов, и предпочтительно аспирина, дифлунизала, салициловой кислоты и других салицилатов, салсалатов, производных пропионовой кислоты, и предпочтительно ибупрофена, дексибупрофена, фенопрофена, кетопрофена, декскетопрофена, флурбипрофена, оксапрозина, локсопрофена, производных уксусной кислоты, и предпочтительно индометацина, толметина, сулиндака, этодолака, кеторолака, диклофенака, ацеклофенака, набуметона, производных еноловой кислоты (оксикам), и предпочтительно пироксикама, мелоксикама, теноксикама, дроксикама, лорноксикама, фенилбутазона, производных антраниловой кислоты (фенаматы), и предпочтительно мефенамовой кислоты, меклофенамовой кислоты, флуфенамовой кислоты, толфенамовой кислоты, и селективных ингибиторов СОХ-2 (коксибы), предпочтительно целекоксиба, парекоксиба и эторикоксиба. Вышеуказанная группа изобретений проявляет высокую эффективность в отношении устранения воспаления. 3 н. и 8 з.п. ф-лы, 3 ил., 1 табл., 3 пр.
1. Композиция для устранения острого воспаления у субъекта, нуждающегося в этом, где эта композиция состоит из следующих ингредиентов: Achillea millefolium, Aconitum napellus, Arnica montana, Atropa bella-donna, Bellis perennis, Calendula officinalis, Echinacea purpurea, Echinacea, Hamamelis virginiana, Hepar sulfuris, Hypericum perforatum, Matricaria recutita, Mercurius solubilis Hahnemanni и Symphytum officinale, а также фармацевтически приемлемого носителя и/или разбавителя, где указанные ингредиенты композиции применяют в следующих гомеопатических разведениях:
Achillea millefolium D3,
Aconitum napellus D2,
Arnica montana D2,
Atropa bella-donna D2,
Bellis perennis D2,
Calendula officinalis D2,
Echinacea purpurea D2,
Echinacea D2,
Hamamelis virginiana D1,
Hepar sulfuris D6,
Hypericum perforatum D2,
Matricaria recutita D3,
Mercurius solubilis Hahnemanni D6 и
Symphytum officinale D6.
2. Композиция по п. 1, где указанное воспаление связано с заболеванием или нарушением, выбранным из группы, состоящей из ревматоидного артрита, остеоартрита, перитонита, синдрома раздраженного кишечника, COPD, системной красной волчанки, рассеянного склероза, псориаза, сахарного диабета типа 1, скелетно-мышечных повреждений, мышечного воспаления и воспаления суставов, такого как растяжение связок голеностопного сустава.
3. Композиция по любому из пп. 1,2, где указанная композиция предназначена для введения субъекту совместно с противовоспалительным лекарственным средством.
4. Композиция по любому из пп. 1,2, где указанная композиция предназначена для введения субъекту после лечения указанного субъекта противовоспалительным лекарственным средством.
5. Композиция по п. 3 или 4, где указанным противовоспалительным средством является нестероидное противовоспалительное лекарственное средство (NSAID).
6. Композиция по п. 5, где указанное NSAID выбрано из группы, состоящей из салицилатов, и предпочтительно аспирина, дифлунизала, салициловой кислоты и других салицилатов, салсалатов, производных пропионовой кислоты, и предпочтительно ибупрофена, дексибупрофена, фенопрофена, кетопрофена, декскетопрофена, флурбипрофена, оксапрозина, локсопрофена, производных уксусной кислоты, и предпочтительно индометацина, толметина, сулиндака, этодолака, кеторолака, диклофенака, ацеклофенака, набуметона, производных еноловой кислоты (оксикам), и предпочтительно пироксикама, мелоксикама, теноксикама, дроксикама, лорноксикама, фенилбутазона, производных антраниловой кислоты (фенаматы), и предпочтительно мефенамовой кислоты, меклофенамовой кислоты, флуфенамовой кислоты, толфенамовой кислоты, и селективных ингибиторов СОХ-2 (коксибы), предпочтительно целекоксиба, парекоксиба и эторикоксиба.
7. Композиция по любому из пп. 1-6, где указанным субъектом является человек.
8. Фармацевтическая композиция для устранения острого воспаления у субъекта, нуждающегося в этом, включающая композицию, описанную в любом из пп. 1-7, и нестероидное противовоспалительное лекарственное средство (NSAID), где указанное NSAID выбрано из группы, состоящей из салицилатов, и предпочтительно аспирина, дифлунизала, салициловой кислоты и других салицилатов, салсалатов, производных пропионовой кислоты, и предпочтительно ибупрофена, дексибупрофена, фенопрофена, кетопрофена, декскетопрофена, флурбипрофена, оксапрозина, локсопрофена, производных уксусной кислоты, и предпочтительно индометацина, толметина, сулиндака, этодолака, кеторолака, диклофенака, ацеклофенака, набуметона, производных еноловой кислоты (оксикам), и предпочтительно пироксикама, мелоксикама, теноксикама, дроксикама, лорноксикама, фенилбутазона, производных антраниловой кислоты (фенаматы), и предпочтительно мефенамовой кислоты, меклофенамовой кислоты, флуфенамовой кислоты, толфенамовой кислоты, и селективных ингибиторов СОХ-2 (коксибы), предпочтительно целекоксиба, парекоксиба и эторикоксиба.
9. Фармацевтическая композиция по п. 8, которая предпочтительно является такой, как описано в любом из пп. 2-7.
10. Набор для устранения острого воспаления у субъекта, нуждающегося в этом, включающий (i) композицию по любому из пп. 1-9 и (ii) нестероидное противовоспалительное лекарственное средство (NSAID), где указанное NSAID выбрано из группы, состоящей из салицилатов, и предпочтительно аспирина, дифлунизала, салициловой кислоты и других салицилатов, салсалатов, производных пропионовой кислоты, и предпочтительно ибупрофена, дексибупрофена, фенопрофена, кетопрофена, декскетопрофена, флурбипрофена, оксапрозина, локсопрофена, производных уксусной кислоты, и предпочтительно индометацина, толметина, сулиндака, этодолака, кеторолака, диклофенака, ацеклофенака, набуметона, производных еноловой кислоты (оксикам), и предпочтительно пироксикама, мелоксикама, теноксикама, дроксикама, лорноксикама, фенилбутазона, производных антраниловой кислоты (фенаматы), и предпочтительно мефенамовой кислоты, меклофенамовой кислоты, флуфенамовой кислоты, толфенамовой кислоты, и селективных ингибиторов СОХ-2 (коксибы), предпочтительно целекоксиба, парекоксиба и эторикоксиба.
11. Набор по п. 10, который предпочтительно является таким, как описано в любом из пп. 2-9.
| US 2016000917 A1, 07.01.2016 | |||
| US 2017290873 A1, 12.10.2017 | |||
| Мотрин | |||
| Таблетки | |||
| УСТРОЙСТВО ДЛЯ МЕХАНИЧЕСКОЙ РАЗГРУЗКИ ЖЕЛ.-ДОР. ПЛАТФОРМ | 1925 |
|
SU2874A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| КОЛПАКОВА М.Э | |||
| Патофизиология воспаления / М.Э | |||
| Колпакова, Е.Ю | |||
| Васина, С.А | |||
| Шестакова; под ред | |||
| проф | |||
Авторы
Даты
2024-04-03—Публикация
2019-10-29—Подача