Область техники
Изобретение относится к области противовоспалительной терапии полипозного риносинусита, а именно к применению препарата, содержащего аммония глицирризинат в качестве активного компонента, в противовоспалительной терапии полипозного риносинусита.
Уровень техники
Полипозный риносинусит является многофакторным заболеванием, которое складывается из результатов сложного взаимодействия организма хозяина и окружающей среды и множества механизмов, ведущих к хроническому воспалению. Его особенностью является длительное воспалительное состояние, которое протекает без идентифицируемого триггера. Хотя существует множество теорий его этиопатогенеза, причина заболевания остается неясной [1]. Хотя воспаление Th2-типа является центральной характеристикой активного патологического процесса, поскольку в Российской Федерации в 81,69% отмечается эозинофильный тип назальных полипов, независимо от гендерных признаков, климатических условий, региона проживания пациентов [2], неизвестно, что в первую очередь запускает локальную продукцию цитокинов и инфильтрацию лимфоцитов и эозинофилов.
При лечении пациентов с полипозным риносинуситом необходимо учитывать две параллельные проблемы: рецидив роста полипов и обострение хронического воспалительного процесса, которое сопровождается жалобами на усиление заложенности носа, появлением обильных слизисто-гнойных выделений из носа и стеканием их по задней стенке глотки, усилением малопродуктивного кашля [3]. Кроме того, у этих больных наблюдаются усталость, нарушения сна, тревога и повышение вероятности развития депрессии, поскольку наличие вышеперечисленных симптомов диктует им необходимость проводить некоторое время для посещения медицинских учреждений и в медицинских мероприятиях, например, в промывании носа. Это потерянное время для отдыха, вероятно, приводит к фрустрации и потенциальной депрессии, что ухудшает качество жизни пациентов [4]. При этом нет связи между тяжестью заболевания, показателями данных компьютерной томограммы околоносовых пазух (ОНП) и эндоскопии полости носа и уровнем нарушения качества жизни у этих пациентов [5].
Для предотвращения рецидива роста полипов применяется базовая терапия интраназальными глюкокортикостероидами, разрабатываются методы таргетного лечения моноклональными антителами на разном уровне патогенетических звеньев [6], но вместе с тем, проблема обострения полипозного риносинусита также требует активного разрешения. Проводя анализ амбулаторных карт лечения полипозного риносинусита в Москве антибиотики назначались в 28,2% случаев, из них в 73% из группы макролидов [7]. С другой стороны, в обзоре Cochrane по применению антибиотиков при хроническом риносинусите не найдено доказательств их клинической эффективности [8], а при бактериологическом исследовании отделяемого из полости носа при обострении полипозного риносинусита выявляются представители нормальной флоры, а среди условно-патогенной лидирует Staphylococcus aureus, при этом его количество, как правило, также близко к норме, соответственно, инфекционные агенты не являются ключевыми факторами возникновения этого состояния [3].
Учитывая гетерогенность заболевания и наличия нескольких клинических фенотипов полипозного риносинусита с доказанной разницей воспалительного механизма при каждом из них, поиск альтернативных противовоспалительных методов лечения для отдельных групп пациентов также весьма значим для клинической практики [7, 9, 10].
Из UA 15178 (Харьковская медицинская академия последипломного образования), 15.06.2006 известен способ лечения полипозного аллергического риносинусита у больных бронхиальной астмой и предусматривающий введение препарата “Дипроспана” с активным действующим веществом бетаметазоном через пункцию верхнечелюстной пазухи в объеме 1 мл один раз в три месяца в течение года.
Провоспалительные цитокины являются важными факторами, опосредующими воспаление, и потенциально могут инициировать и поддерживать реакции слизистой оболочки носа и ОНП на различные триггеры [11], они регулируют фагоцитарную активность и производство арахидоновой кислоты [12]. Развитие полипозного риносинусита является следствием персистирующих воспалительных и ремоделирующих процессов. Современные методы лечения облегчают симптомы, но не устраняют высокую частоту рецидивов, что подчеркивает необходимость специальных исследований, связывающих новые молекулярные мишени, воспаление и функцию слизистой оболочки носа [6,7].
Аларминами или эндокинами называют группу эндогенных факторов, которые взаимодействуют с мембранными рецепторами иммунных клеток после высвобождения во внеклеточное пространство, активируя воспалительный ответ [13]. Провоспалительный цитокин амфотерин относят к так называемой группе белков с высокой подвижностью (HMGB1, high-mobility group protein B1) в связи с их мобильностью при электрофорезе. Он представляет собой протеин из группы ядерных негистоновых белков, присутствующих в ядре всех клеток и играющих ключевую роль в поддержании ядерного гомеостаза. HMGB1 играет роль в патогенезе хронических воспалительных заболеваний верхних дыхательных путей (ВДП), таких как аллергический ринит, хронический риносинусит и полипозный риносинусит, обеспечивая выживание эозинофилов и ряда других ключевых клеток, участвующих в аллергических и неаллергических иммунных нарушениях слизистой оболочки носа и ОНП [14].
Относящийся к классу «аларминов», он участвует в рекомбинации, транскрипции, репарации и других ключевых процессах, обеспечивающих функционирование ДНК в клеточном ядре [15]. В нормальных условиях этот белок находится в ядре клетки, где он выполняет определенные структурные и метаболические задачи; при внеклеточном высвобождении он становится активатором врожденного иммунитета и мощным воспалительным фактором [16].
Основными компонентами врожденной иммунной системы являются клеточные элементы (моноциты, макрофаги, антигенпрезентирующие клетки, NK-клетки) и различные паттерн-распознающие рецепторы (PRRs, pattern recognition receptors), в том числе, Toll-like рецепторы (TLRs) [17]. Под воздействием определенных триггеров, к которым относятся инфекционные агенты, аллергены, эндогенные пептиды, высвобождаемые из поврежденных клеток, происходит релиз провоспалительных цитокинов [18]. Начальная фаза секреции HMGB1 эпителиоцитами, моноцитами или макрофагами требует сигнала в виде липополисахаридов, интерлейкина (IL)-1 или фактор некроза опухоли (TNF, tumor necrosis factor)-α. Являющийся компонентом внешней мембраны грамотрицательных бактерий липополисахарид участвует во взаимодействии и активации иммунных клеток, в которых он перемещает ядерный HMGB1 в цитоплазму и внеклеточное пространство, что вызывает в них активизацию, пролиферацию и релиз цитокинов, участвующих в последующих звеньях патогенеза полипозного риносинусита [19]. Механизм переноса HMGB1 из ядер в секреторные лизосомы, которые являются специальными цитоплазматическими органеллами, связан с ацетилированием специфических остатков лизина [20]. Далее HMGB1 находится в цитоплазме с блокированным возвращением в ядро и высвобождается во внеклеточную среду, где он связывается со своими рецепторами для конечных продуктов гликирования (RAGE, receptor for advanced glycation end products), TLR-2, TLR-4 и TLR-9 [21,22]. Далее посредством активации нуклеарного фактора kB (NF-kB, nuclear factor kappa) амфотерин вызывает высвобождение провоспалительных медиаторов, цитокинов и хемокинов. RAGE представляет собой мультилигандный трансмембранный гликопротеин I типа, член суперсемейства иммуноглобулинов рецепторов клеточной поверхности, которые обнаружены на гладкомышечных клетках, макрофагах, эндотелиальных клетках и астроцитах. RAGE связывается непосредственно с ДНК и РНК и способствует их поглощению клетками, снижая порог иммунного распознавания для TLR9, основного ДНК-распознающего трансмембранного сигнального рецептора [23]. Повышенное количество HMGB1 связывается с рецепторами RAGE, которые экспрессируются эндотелиальными клетками, что способствует рекрутированию эозинофилов в слизистую оболочку носа и ОНП, созданию условий для их выживания и высвобождения эозинофильного катионного протеина и основного белка эозинофилов с последующим повреждением эпителиального барьера [24].
Ингибирование HMGB1 может быть эффективной и инновационной терапевтической мишенью для пациентов с хроническими заболеваниями ВДП. В связи с его патогенетической значимостью большие усилия были направлены на изучение возможностей противодействия провоспалительным эффектам HMGB1. Ингибирование действия любого цитокина, в том числе HMGB1, может достигаться несколькими способами:
1) Блокирование высвобождения HMGB1 активированными иммунными клетками. Но поскольку при этом подавляется физиологическая гомеостатическая функцию белка во всех клетках, это может быть связано с серьезными побочными эффектами.
2) Блокирование препаратами-антагонистами рецепторов RAGE, TLR2, TLR9. Но, в связи с тем, что эти рецепторы HMGB1 также индуцируют антибактериальную активность и другие иммунные эффекты, этот механизм также терапевтически невыгоден.
3) Инактивация HMGB1, что является самой эффективной и безопасной стратегией.
Хотя на доклиническом уровне предлагались разные лекарственные препараты, почти ни один из них не достиг клинического применения за редким исключением [25].
Низкомолекулярный ингибитор HMGB1 глицирризин являются тритерпеновым сапонином, состоит из одной молекулы глицирретиновой кислоты в виде агликона (активный компонент молекулы), соединенного с двумя молекулами глюкуроновой кислоты, и входит в состав Glycyrrhiza glabra (солодка голая, солодка гладкая, лакриил, лакричник) [26]. По строению она имеет сходство с фенантреновой частью глюкортикостероидов. При этом, в отличие от традиционной фитотерапии, глицирризин следует рассматривать не как растительный экстракт, а как конкретное химическое соединение, выделенные из растения солодки. Глицирризин оказывает противовоспалительное действие, ингибирует хемотаксическую и митогенную функцию HMGB1, связываясь с их гидрофобными остатками, без существенного искажения их вторичной структуры и без нарушения их способности связывания ДНК, при этом препятствуя способности белка HMGB1 связываться с родственными ему рецепторами и оказывать провоспалительное и хемотаксическое действие [30]. Так как HMGB1, способствует выживанию эозинофилов [31], глицирризин избирательно индуцирует их гибель. Кроме того, глицирризин обладает противовирусным действием в отношении цитомегаловируса человека, вируса простого герпеса, вируса гриппа, увеличивает пролиферацию лимфоцитов, действует как промотор поздней передачи сигнала Т-лимфоцитами для продукции IL-2, а через активацию NF-κB усиливает индуцированную липополисахаридами продукцию ИЛ-12 макрофагами, синтез IFN-γ и IL-10 NK (Natural killer)-клетками [26]. Глицирризин оказывает антиоксидантное действие, значительно снижает продуцируемые нейтрофилами активные форм кислорода (АФК) дозозависимым образом [27,28], образование которых может быть причиной более тяжелого течения заболевания [29].
Известны данные об успешном применении назального спрея “Narivent”, содержащего в своем составе дикалия глицирризинат, при полипозном риносинусите в отношении купирования симптомов воспаления и заложенности носа. Применение топического препарата “Narivent” приводило к стойкой клинической положительной динамике в виде уменьшения выраженности заложенности носа, а также объективному снижению содержания HMGB1 в носовой жидкости, что было сопоставимо с эффектом от лечения интраназальным будесонидом [14].
На сегодня опубликованы данные Овчинникова А.Ю. и соавт. об эффективном применении препарата Реглисам у пациентов с затяжным риносинуситом после перенесенной SARS-CoV-2-инфекции. Включение препарата Реглисам в схемы лечения затяжного риносинусита способствует эффективному купированию отека и воспаления в слизистой оболочке полости носа, улучшению мукоцилиарного транспорта и дренированию ОНП, что объективно позволяет к седьмому дню терапии значимо снизить выраженность местных воспалительных симптомов (отека, гиперемии, выделений) и постназального затека, нормализовать носовое дыхание с минимальным использованием деконгестантов, улучшить качество жизни данной группы пациентов.
Однако, из уровня техники не известно применение препарата, содержащего аммония глицирризинат в качестве активного компонента, в частности, препарата Реглисам, в противовоспалительной терапии полипозного риносинусита.
Раскрытие сущности изобретения
Задачей заявленного изобретения является расширение арсенала средств для противовоспалительной терапии полипозного риносинусита, которые имели бы высокую эффективность и доступность.
Технический результат заявленного изобретения заключается в расширении арсенала средств для противовоспалительной терапии полипозного риносинусита, патогенетической мишенью которой является эффективное противодействие провоспалительным эффектам HMGB1, что клинически определяется снижением основных симптомов заболевания (заложенности, выделений из носа и т.д.), отечности слизистой носа, отсутствием дальнейшего роста и/или уменьшением размера полипов, повышением контроля над течением заболевания.
Технический результат достигается за счет применения препарата, содержащего аммония глицирризинат в качестве активного компонента, в противовоспалительной терапии полипозного риносинусита.
Глицирризиновая кислота гидролизуется в организме до глицирретиновой кислоты, химическая структура которой сходна со стероидными гормонами, она может связываться с глюкокортикоидными рецепторами и обладает слабым глюкокортикоидоподобным действием [32, 33]. В ходе многочисленных исследований, было обнаружено, что действующее вещество аммония глицирризинат эффективно инактивирует цитокин HMGB1, ингибирует трансформирующий фактор роста-β (TGF-β, transforming growth factor β)-1 [34], который принимает участие в развитии фиброза ткани носовых полипов, активирует синтез и способствует накоплению компонентов внеклеточного матрикса с одновременным уменьшением их деструкции матриксными металлопротеиназами, и количество которого повышено при полипозном риносинусите[35]. Глицирризин вызывает снижение GATA-3, вследствие чего происходит снижение количества Th2 и смещение соотношения Th1/Th2, что также важно для лечения полипозного риносинусита. Кроме того, глицирризин повышает уровень экспрессии FoxP3, являющегося ключевым маркером Т-регуляторных лимфоцитов. Транскрипционный фактор FoxP3 способен снижать экспрессию провоспалительных цитокинов TNFα, IL-2, IL-17, IFNγ, а также, IgE и IL-4 [36,37], что способствует регрессу воспалительного процесса.
Кроме того, глицирризин оказывает антиоксидантное действие, значительно снижает продуцируемые нейтрофилами активные форм кислорода (АФК) дозозависимым образом [20,21], образование которых может быть причиной более тяжелого течения заболевания [22].
Таким образом, терапевтических точек приложения действующего вещества аммония глицирризината для применения при полипозном риносинусите несколько, что делает его изучение и использование при данном заболевании актуальным.
В частных случаях препарат, содержащий аммония глицирризинат в качестве активного компонента, используется в твердой лекарственной форме, предпочтительно таблетированной.
В качестве препарата, содержащего аммония глицирризинат в исследованиях применяется препарат Реглисам в дозировке 50 мг, зарегистрированный на территории Российской Федерации.
Для данного препарата в его различных лекарственных формах показаны положительные результаты при лечении экссудативного и гнойного средних отитов [38], бронхиальной астмы, обструктивного бронхита, пневмонии [39,40,41], острой инфекции дыхательных путей, в том числе COVID-19, аллергического ринита [42].
В настоящей же заявке раскрывается применение и эффективность препарата Реглисам в комплексном лечении обострения полипозного риносинусита.
В предпочтительных вариантах препарат Реглисам применяется комплексно, совместно с интраназальным применением мометазона фуроата и орошением изотоническим солевым раствором слизистой оболочки носа. По необходимости также могут применяться местные сосудосуживающие средства не более 5 дней, при этом пероральный препарат Реглисам»в таблетках (50 мг в таблетке) принимается ежедневно по 2 т. 2-3 раза в день в течение 90 дней (3 мес.).
Чертежи
Изобретение будет более понятно из описания, не имеющего ограничительного характера и приводимого со ссылками на прилагаемые чертежи, на которых изображено:
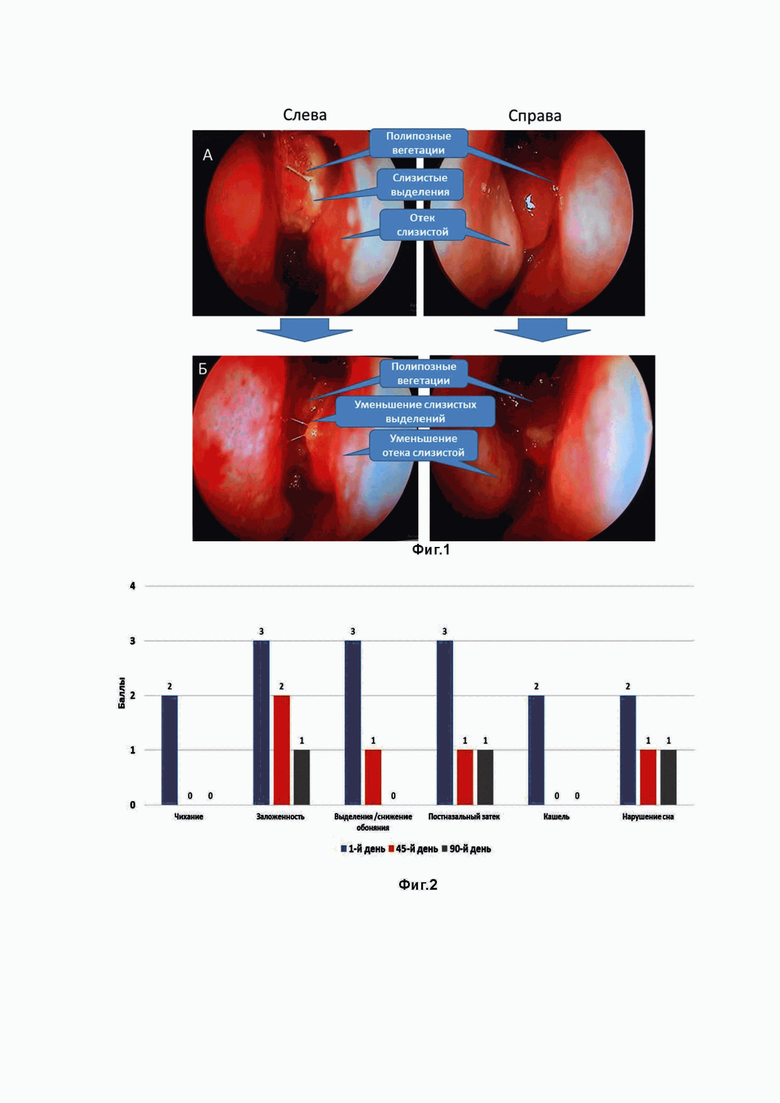
Фиг.1 - Эндоскопическая картина полости носа пациента О. (пример 1) а - при поступлении (до терапии), b - при поступлении через 90 дней терапии с включением препарата Реглисам.
Фиг.2 - Динамика выраженности по визуально-аналоговой шкалевизуально-аналоговой шкале основных симптомов полипозного риносуинусита пациента О. (пример 1).
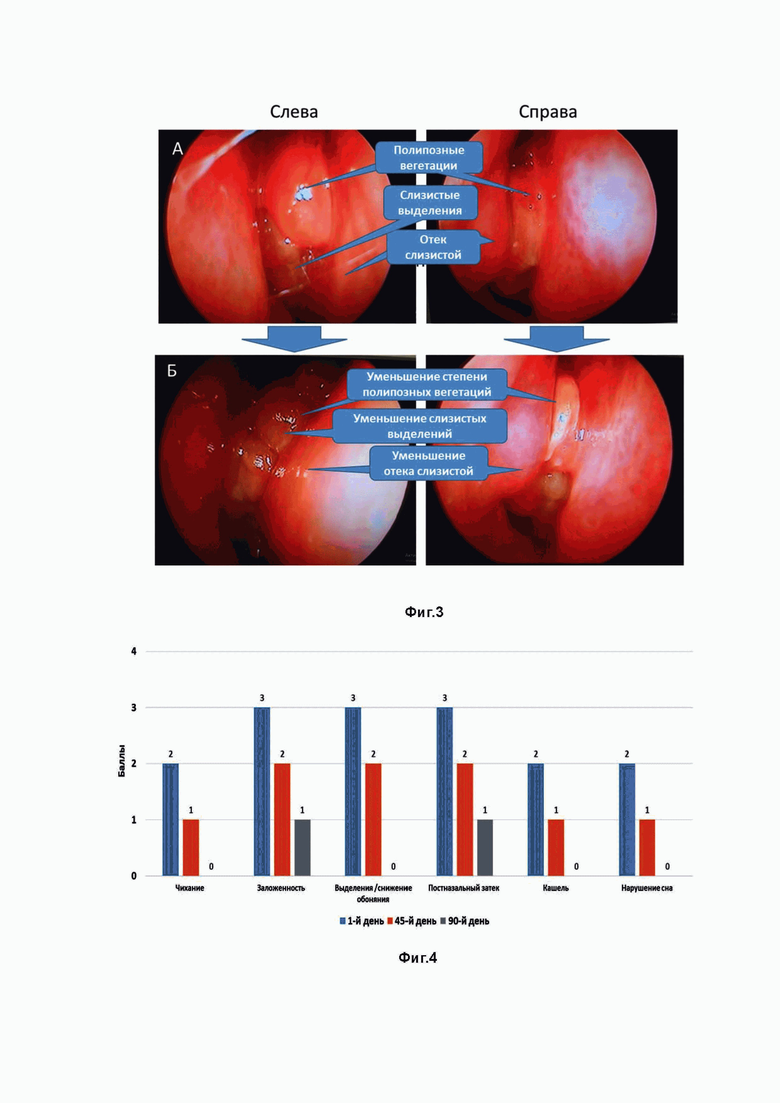
Фиг.3 - Эндоскопическая картина полости носа пациента П. (пример 2) а - при поступлении (до терапии), b - при поступлении через 90 дней терапии с включением препарата Реглисам.
Фиг.4 - Динамика выраженности по визуально-аналоговой шкалевизуально-аналоговой шкале основных симптомов полипозного риносуинусита пациента П. (пример 2).
Фиг.5 - Динамика выраженности по визуально-аналоговой шкалевизуально-аналоговой шкале основных симптомов полипозного риносуинусита.
Фиг.6 - Динамика количества пациентов, предъявляющих жалобы на различные симптомы полипозного риносуинусита, на фоне проводимой терапии.
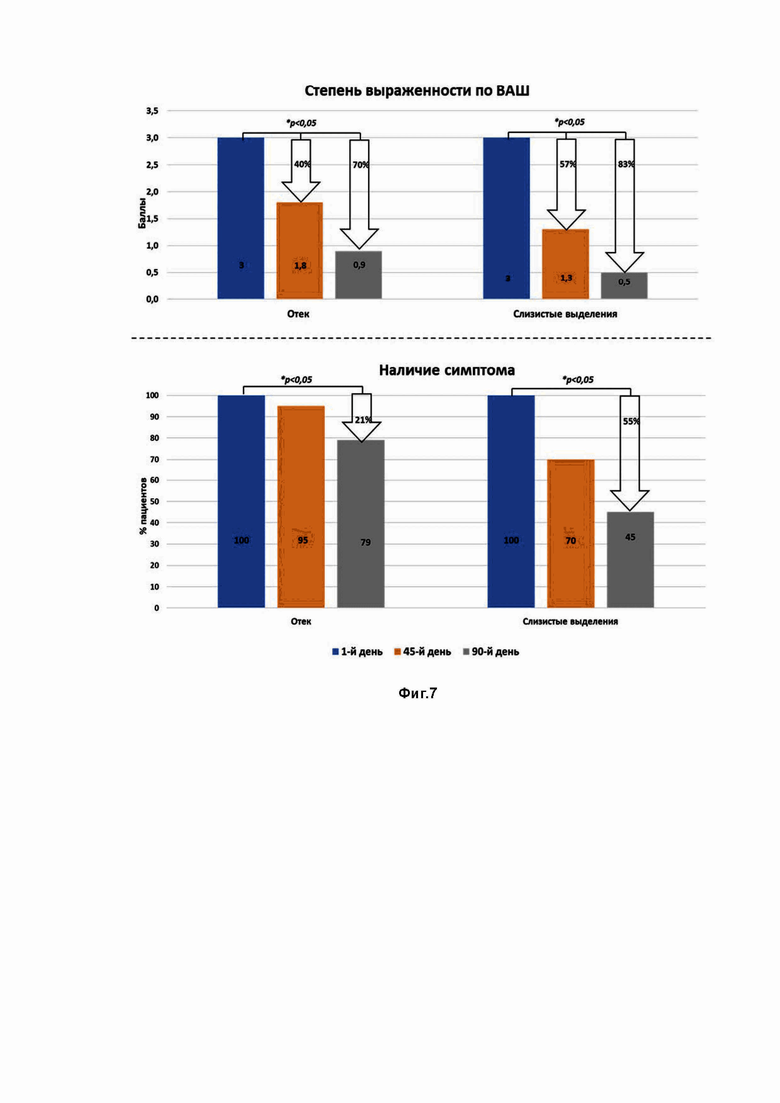
Фиг.7 - Оценка наличия и выраженности по визуально-аналоговой шкалевизуально-аналоговой шкале отека и слизистых выделений по данным эндоскопии носоглотки в динамике на фоне терапии.
Осуществление изобретения
Применение препарата, содержащего аммония глицирризинат в качестве активного компонента, в противовоспалительной терапии полипозного риносинусита было исследовано и проиллюстрировано в настоящей заявке на примере применения, зарегистрированного на территории Российской Федерации перорального препарата Реглисам в таблетках (50 мг в таблетке).
Препарат может применяться для лечения полипозного риносинусита комплексно:
- мометазона фуроат по две дозы (100 мкг в 1 дозе) два раза в день интраназально в течение 3 мес.,
- ежедневное орошение изотоническим солевым раствором слизистой оболочки полости носа
- по необходимости местные сосудосуживающие средства не более 5 дней,
- в качестве системной противовоспалительной терапии пероральный препарат Реглисам в таблетках (50 мг в таблетке) ежедневно по 2 таблетки 2-3 раза в день в течение 90 дней (3 мес.).
При применении препарата, содержащего аммония глицирризинат в качестве активного компонента, в частности препарата Реглисам в противовоспалительной терапии полипозного риносинусита обеспечивается расширение арсенала средств для противовоспалительной терапии полипозного риносинусита. Обеспечивается позитивная клиническая динамика симптомов полипозного риносинусита, уменьшение отечности слизистой носа и слизистого отделяемого, отсутствие дальнейшего роста полипов и уменьшение размера имеющихся полипов.
Примеры осуществления
Ниже представлены примеры осуществления заявленного изобретения, подтверждающие достижение технического результата при осуществлении заявленного изобретения, а именно при применении препарата, содержащего аммония глицирризинат в качестве активного компонента, на примере препарата Реглисам, в противовоспалительной терапии полипозного риносинусита.
Клинический пример №1. Больной О., 50 лет,
Анамнез заболевания. Считает себя больным с 2012 года, когда впервые начал отмечать заложенность и обильное слизистое отделяемое из носа. Консультирован оториноларингологом, диагностирован полипозный риносинусит, в этом же году выполнено хирургическое лечение в объёме FESS (functional endoscopic sinus surgery). Через год после операции возник рецидив полипозного риносинусита, постоянно использует интраназальные глюкокортикостероиды (ИнГКС).
В 2019 г. появился затяжной кашель при обследовании выявлена бронхиальная астма и аллергический ринит, по результатам кожных скарификационных проб обнаружена сенсибилизация к клещу домашней пыли, в связи с чем рекомендована аллерген-специфическая иммунотерапия (АСИТ), которая по настоящее время не проводилась.
Методология наблюдения за пациентом. На визитах оценку жалоб и объективных признаков при эндоскопическом осмотре полости носа проводили по 4-х балльной визуально-аналоговой шкале (ВАШ) («0» – отсутствие, «1» – незначительно выраженные, «2» – умеренно, «3» – выраженные проявления), при эндоскопическом исследовании полости носа объективно оценивались наличие и степень выраженности по ВАШ отечности слизистой оболочки носа и наличия слизистого отделяемого.
На первом визите:
Пациент предъявлял активные жалобы на симптомы заложенности носа, выделений из носа/снижения обоняния, постназального затека, нарушения сна, чихания и кашля. Балльная оценка исходно фиксируемых жалоб представлена в таблице 1.
Таблица 1. Исходная балльная оценка жалоб и данных эндоскопии пациента О. до включения в терапию препарата Реглисам.
Объективно при эндоскопии (Фиг.1а) носовое дыхание умеренно затруднено, слизистая оболочка отечная нормальной окраски, справа и слева определяются полипозные вегетации 2-й степени. Ткань носовых полипов отечная покрыта обильными выделениями слизистого характера. Носоглотка – без патологических изменений. Глотка – при фарингоскопии небные миндалины интактные, слизистая оболочка задней стенки глотки слегка гиперемирована за счет вязкого слизистого отделяемого, стекающего из носоглотки.
Диагноз: Полипозный риносинусит. Аллергический ринит, персистирующая форма. Сенсибилизация к бытовым аллергенам. Аллергическая бронхиальная астма.
Пациенту назначено лечение: Реглисам по 2 таблетки по 50 мг 3 раза в день (курс – 90 дней), мометазона фуроат по 2 дозы (100 мкг) 2 раза в день в каждую половину носа, орошение изотоническим солевым раствором слизистой оболочки полости носа 3-4 раза в день.
В динамике через 45 дней:
На фоне назначенной терапии к 45-му дню лечения получена стойкая положительная динамика в виде регресса выраженности по ВАШ исходно фиксируемых основных симптомов заболевания: заложенности носа, выделений из носа/снижения обоняния, постназального затека, нарушения сна. Симптомы чихания и кашля были полностью купированы. Таблица 2.
Таблица 2. Балльная оценка жалоб и данных эндоскопии пациента О. через 45 дней терапии с включением препарата Реглисам.
Объективно при эндоскопии полости носа отмечается положительная динамика в виде уменьшения отека слизистой оболочки носа и выраженности выделений слизистого характера, определяются полипозные вегетации 2-й степени. Глотка – при фарингоскопии небные миндалины интактные, слизистая оболочка задней стенки глотки нормальной окраски чистая, все воспалительные явления регрессировали.
За период наблюдения курс терапии препаратом Реглисам выдержан в полном объеме, нежелательных реакций не отмечалось, дополнительного консервативного лечения добавлено не было.
В динамике через 90 дней:
На фоне назначенной терапии к 90-му дню лечения симптомы заложенности носа, постназальные выделения и нарушение сна беспокоили лишь незначительно, оставшиеся симптомы были полностью купированы. Таблица 3.
Таблица 3. Балльная оценка жалоб и данных эндоскопии пациента О. через 90 дней терапии с включением препарата Реглисам.
Объективно при эндоскопии (Фиг.1b) полости носа отмечается положительная динамика в виде уменьшения отека слизистой оболочки носа и выраженности выделений слизистого характера, определяются полипозные вегетации 2-й степени. Глотка – при фарингоскопии небные миндалины интактные, слизистая оболочка задней стенки глотки нормальной окраски чистая.
За период наблюдения курс терапии препаратом Реглисам выдержан в полном объеме, нежелательных реакций не отмечалось, дополнительно препараты не назначались.
У пациента полипозный риносинусит, сопровождающийся респираторной аллергией (аллергический ринит и аллергическая бронхиальная астма). Пациент находился на постоянной базисной терапии интраназальными ГКС. При добавлении к патогенетической терапии препарата Реглисам в конце курса лечения отмечался полный регресс основных жалоб чихания, выделений из носа, кашля; значительное уменьшение выраженности симптомов заложенности носа, постназального затека и нарушения сна (Фиг.2). Положительная динамика подтверждалась эндоскопическим осмотром полости носа.
Клинический пример №2. Больной П., 37 лет,
Анамнез заболевания. Считает себя больным с 2018 года, когда впервые начал отмечать заложенность и обильное слизистое отделяемое из носа. Консультирован оториноларингологом, диагностирован полипозный риносинусит, в 2020 году выполнено хирургическое лечение в объеме эндоскопической полипотомии носа. Через год после операции возник рецидив полипозного риносинусита, постоянно использует ИнГКС. С 2016 г. страдает неаллергической бронхиальной астмой.
На первом визите:
Пациент предъявлял активные жалобы на симптомы чихания, заложенности носа, выделений из носа/снижения обоняния, постназального затека, кашля и нарушения сна. Балльная оценка исходно фиксируемых жалоб пациента представлена в таблице 4.
Таблица 4. Исходная балльная оценка жалоб и данных эндоскопии пациента П. до включения в терапию препарата Реглисам.
Объективно при эндоскопии (Фиг.3а) носовое дыхание умеренно затруднено, слизистая оболочка отечная нормальной окраски, справа и слева определяются полипозные вегетации 3-й степени. Ткань носовых полипов отечная покрыта обильными выделениями слизистого характера. Носоглотка – без патологических изменений. Глотка – при фарингоскопии небные миндалины интактные, слизистая оболочка задней стенки глотки слегка гиперемирована за счет вязкого слизистого отделяемое, стекающего из носоглотки. На фиг.3а слева отек слизистой оболочки указан на носовую перегородку, изменить
Диагноз: Полипозный риносинусит. Неаллергическая бронхиальная астма.
Пациенту назначено лечение: Реглисам по 2 таблетки 3 раза в день (курс – 90 дней), мометазона фуроат спрей по 2 дозы (100 мкг) 2 раза в день в каждую половину носа, орошение изотоническим солевым раствором слизистой оболочки полости носа 3-4 раза в день.
В динамике через 45 дней:
На фоне назначенной терапии к 45-му дню лечения получена стойкая положительная динамика в виде регресса выраженности по ВАШ исходно фиксируемых основных симптомов заболевания. Таблица 5.
Таблица 5. Балльная оценка жалоб и данных эндоскопии пациента П. через 45 дней терапии с включением препарата Реглисам.
Объективно при эндоскопии полости носа отмечается положительная динамика в виде уменьшения отека слизистой оболочки носа и выраженности выделений слизистого характера, определяются полипозные вегетации 2-й степени. Глотка – при фарингоскопии небные миндалины интактные, слизистая оболочка задней стенки глотки нормальной окраски чистая, все воспалительные явления регрессировали.
За период наблюдения курс терапии препаратом Реглисам выдержан в полном объеме, нежелательных реакций не отмечалось, дополнительно препараты не назначались.
В динамике через 90 дней:
На фоне назначенной терапии к 90-му дню симптомы заложенности носа, постназальные выделения беспокоили лишь незначительно, оставшиеся симптомы были полностью купированы. Таблица 6.
Таблица 6. Балльная оценка жалоб и данных эндоскопии пациента П. через 90 дней терапии с включением препарата Реглисам.
Объективно при эндоскопии (Фиг.3b) полости носа отмечается положительная динамика в виде уменьшения отека слизистой оболочки носа и выраженности выделений слизистого характера, определяются полипозные вегетации 2-й степени. Глотка – при фарингоскопии небные миндалины интактные, слизистая оболочка задней стенки глотки нормальной окраски чистая.
За период наблюдения курс терапии препаратом Реглисам выдержан в полном объеме, нежелательных реакций не отмечалось, дополнительно препараты не назначались.
Комментарий: у пациента полипозный риносинусит, сопровождающийся неаллергической БА. Этот фенотип полипозного риносинусита характеризуется более тяжелым течением в отличии от сочетания полипозного риносинусита с респираторной аллергией. В данном случае уменьшение всех ключевых клинических признаков (Фиг.4) и степени выраженности полипозных вегетаций (с 3-й до 2-й степени) свидетельствуют о хорошем клиническом ответе на проводимую противовоспалительную терапию. Следует особенно отметить объективное снижение отека ткани носовых полипов при эндоскопическом осмотре уже на втором визите (45-й день лечения).
Пример 3 (с широкой выборкой).
В клинико-диагностическом отделении ГБУЗ МО МОНИКИ им. М. Ф. Владимирского за период с июня 2022 по февраль 2023 находились под наблюдением 33 пациента старше 18 лет с диагнозом обострение полипозного риносинусита в сочетании с аллергической или неаллергической БА. Полипозный риносинусит был подтвержден при помощи эндоскопического осмотра, данных мультиспиральной компьютерной томографии (МСКТ) ОНП и гистологического исследования ткани носовых полипов, БА подтверждалась спирометрией, по показаниям проводилась проба с бронхолитиком. Аллергологическое обследование включало сбор аллергологического анамнеза, постановку прик-тестов с диагностическими водно-солевыми аллергенами («НПО Микроген») для определения типа сенсибилизации. Обострение полипозного риносинусита устанавливали на основе клинической картины и результатах эндоскопического осмотра полости носа (отек, гиперемия и наличие слизисто-гнойных выделений на слизистой оболочке полости носа). Пациенты предъявляли жалобы на чихание, заложенность носа, выделение из носа/снижение обоняния, постназальный затек, головную/лицевую боль, слезотечение, кашель, нарушение сна. Критериями невключения больных в исследование являлись: подозрение на острую респираторную инфекцию, наличие указаний на непереносимость/гиперчувствительность и противопоказаний на любые компоненты исследуемого препарата; тяжелая, неконтролируемая форма артериальной гипертензии, хроническая сердечная недостаточность; невозможность участника исследования соблюдать требования протокола и назначений врача; беременность и кормление грудью; возраст до 18 лет и старше 65 лет.
Всем пациентам было назначено комплексное консервативное лечение полипозного риносинусита: мометазона фуроат по две дозы (100 мкг в 1 дозе) два раза в день интраназально в течение 3 мес., ежедневное орошение изотоническим солевым раствором слизистой оболочки полости носа, по необходимости местные сосудосуживающие средства не более 5 дней, в качестве системной противовоспалительной терапии пероральный препарат «Реглисам» в таблетках (50 мг в таблетке) ежедневно в дозировке согласно инструкции применения в течение 90 дней (3 мес.).
Период наблюдения за пациентами составил 90 дней (3 мес.) и включал 3 визита: 1-й визит (1-й день) - начало лечения, 2-й и 3-й визиты проводились на 45-й и 90-й дни от начала терапии соответственно. На 1-м, 2-м и 3-м визитах проводили оценку жалоб (чихание, заложенность носа, выделение из носа/снижение обоняния, постназальный затек, головная/лицевая боль, слезотечение, кашель, нарушение сна) по 4-х балльной визуально-аналоговой шкале (ВАШ) («0» – отсутствие, «1» – незначительно выраженные, «2» – умеренно, «3» – выраженные проявления), при эндоскопическом исследовании полости носа объективно оценивались наличие и степень выраженности по ВАШ отечности слизистой оболочки носа и наличия слизистого отделяемого.
Результаты, полученные в ходе наблюдательной программы, обрабатывались с использованием пакета Statistica for Windows 10.0 (StatsoftInc. USA). Данные представлены в зависимости от типа распределения: в виде среднего (М) и его среднеквадратичного отклонения (±σ); в виде медианы и верхнего и нижнего квартиля Me [Q25; Q75]. Качественные параметры представлены в виде абсолютных чисел и относительного количества (%). Статистическую значимость различий при сравнении несвязанных групп по доле (частоте признака) вычисляли с помощью двустороннего точного критерия Фишера, различия результатов несвязанных выборок по количественному признаку определяли с помощью критерия Манна-Уитни, связанных выборок – по критериям Фридмана. Различия считали статистически значимыми при р<0,05.
Результаты исследования и их обсуждение
Наблюдательную программу завершили в соответствии с протоколом все 33 пациента, из которых 25 (76%) женщин и 8 (24%) мужчин, средний возраст больных составил 53,5±1,74 лет. Все пациенты имели в анамнезе бронхиальную астму БА, 27% (n=9) страдали аллергическим ринитом, трое пациентов имели профессиональные вредности (каменная промышленность, металлодобывающее предприятие, пары бензина). К моменту включения в исследование средний стаж заболевания составил 9,4±1,2 лет, 2 пациента ранее не были оперированы в связи с полипозном, остальные пациенты в анамнезе имели полипэктомию носа.
На фоне терапии получена стойкая положительная достоверная динамика в виде регресса выраженности по ВАШ исходно фиксируемых основных симптомов заболевания: чихания, заложенности носа, выделений из носа/снижения обоняния, постназального затека, головной/лицевой боли, слезотечения, кашля, нарушения сна (Таблица 7., фиг.5.).
Таблица 7. Балльная оценка по ВАШ выраженности симптомов полипозного в динамике по визитам.
(визиты 1-3)
1-й день
45-й день
90-й день
Выраженность симптомов чихания, головной\лицевой боли, слезотечения и кашля к 45-му дню терапии снизились до минимальных значений и к 90-му дню лечения были полностью купированы. Интенсивность симптомов заложенности носа, выделений из носа/снижения обоняния, нарушения сна на фоне проводимой терапии стойко уменьшалась, к 90-му дню наблюдения балльная оценка выраженности данных симптомов была более чем в 2,5 раза ниже исходной и процент ее снижения достигал 62-75% (p<0,05).
К 90-му дню лечения в сравнении с первым визитом количество больных, предъявляющих жалобы на выделения из носа/снижение обоняния и постназальный затек, уменьшилось более чем в 2 раза (снижение на 52% и 58%, соответственно, p<0,05), доля пациентов с нарушением сна снизилась на 28%, жалобы на чихание, головную/лицевую боль, слезотечение и кашель к 3-му визиту у наблюдаемой группы больных не наблюдались (Фиг. 6). В отношении частоты симптома заложенности носа аналогичного значимого снижения в динамике не отмечалась (1-й визит – 100%, 3-й визит – 96%), но несмотря на то, что к 3-му визиту данный симптом еще сохранялся у значительной доли пациентов, в отличии от 1-го визита, его выраженность в соответствии с результатами балльной оценки по ВАШ на фоне терапии уменьшилась на 62% (Таблица 7.).
При оценке наличия и степени выраженности по ВАШ местных воспалительных симптомов по данным эндоскопической картины носоглотки на фоне проводимого лечения были также получены статистически значимые различия в динамике (фиг.7). Исходно у всех пациентов при эндоскопии определялись отек и слизистые выделения, степень их выраженности была значительной и составляла 3 балла. На 90-й день лечения слизистые выделения отсутствовали более чем у половины больных (55% (n=18)), степень выраженности симптома к 45-му и 90-му дню лечения уменьшилась на 57% и 83% соответственно (p<0,05) На 90-й день лечения отек не фиксировался у 21% (n=7) пациентов, при этом степень выраженности симптома значительно уменьшилась к 45-му и 90-му лечения на 40%, и 79% соответственно (p<0,05).
За период наблюдения не отмечено нежелательных явлений, связанных с приемом исследуемого препарата, в том числе, аллергических реакций, реакций индивидуальной непереносимости.
Таким образом, данные, полученные в ходе проведенных исследований, продемонстрировали, что включение препарата содержащего аммония глицирризинат в качестве активного компонента, в частности противовоспалительного препарата Реглисам, в терапию полипозного риносинусита эффективно способствует купированию чихания, головной/лицевой боли, слезотечения и кашля, а также регрессу симптомов заложенности носа, выделений из носа/снижения обоняния, нарушения сна, что значительно повышает качество повседневной жизни пациентов. Также по данным эндоскопии в динамике на фоне терапии было зафиксировано уменьшение степени выраженности местных воспалительных симптомов (отека и слизистых выделений), что объективно подтверждало эффективность проводимого лечения и определяло восстановление носового дыхания у значительной доли больных.
Изобретение было раскрыто выше со ссылкой на конкретный вариант его осуществления. Для специалистов могут быть очевидны и иные варианты осуществления изобретение, не меняющие его сущность, как она раскрыта в настоящем описании. Соответственно, изобретение следует считать не ограниченным по объему приведенными описанием и примерами.
Список литературы
1. Biggs TC, Hayes SM, Harries PG, Allan RN, Walls AF, Pender SLF, Salib RJ. Immunological profiling of key inflammatory drivers of nasal polyp formation and growth in chronic rhinosinusitis. Rhinology. 2019;57(5):336-342 https://doi.org/10.4193/Rhin19.167.
2. Савлевич E.Л., Гаганов Л.Е., Герасимов А.Н., Курбачева О.М., Егоров В.И., Зурочка А.В. Анализ клинического течения полипозного риносинусита и патоморфологического состава ткани носовых полипов у пациентов, проживающих в различных регионах Российской Федерации. Head and neck. Голова и шея. Российский журнал=Head and neck. Russian Journal. 2021;9(3):15–24. Savlevich E.L., Gaganov L.E., Gerasimov A.N., Kurbacheva O.M., Egorov V.I., Zurochka A.V. Analysis of clinical course of chronic rhinosinusitis with nasal polyp (CRSWNP) and pathomorphological composition of nasal polyp tissue in patients living in different regions of the Russian Federation. Head and neck. Russian Journal. 2021;9(3):15–24 (In Russian). https://doi.org/10.25792/HN.2021.9.3.15–24
3. Савлевич Е.Л, Егоров В.И., Савушкина Е.Ю., Зурочка А.В., Герасимов А.Н., Митрофанова Е.С., Любимова Е.В. Изучение микробных факторов при обострении полипозного риносинусита. Журнал микробиологии, эпидемиологии и иммунобиологии. 2022;99(4):445-452. Savlevich E.L., Egorov V.I., Savushkina E.Yu, Zurochka A.V., Gerasimov A.N., Mitrofanova E.S., Lyubimova E.V. Study of microbial factors in exacerbation of chronic rhinosinusitis with nasal polyps. Journal of microbiology, epidemiology and immunobiology. 2022;99(4):445-452. (In Russ.) https://doi.org/10.36233/0372-9311-201
4. Schlosser RJ, Gage SE, Kohli P, Soler ZM. Burden of illness: A systematic review of depression in chronic rhinosinusitis. Am J Rhinol Allergy. 2016;30(4):250-6. https://doi.org/10.2500/ajra.2016.30.4343
5. Alt JA, Smith TL, Mace JC, Soler ZM. Sleep quality and disease severity in patients with chronic rhinosinusitis. Laryngoscope. 2013;123(10):2364-70. https://doi.org/10.1002/lary.24040
6. Савлевич Е.Л., Козлов В.С., Курбачева О.М. Современные тенденции диагностического поиска и терапии полипозного риносинусита. Российская ринология. 2018;26(2):41-47. Savlevich EL, Kozlov VS, Kurbacheva OM. The modern trends in the diagnostic search for and the treatment of chronic rhinosinusitis with nasal polyps. Russian Rhinology. 2018;26(2):41-47. (In Russ.). https://doi.org/10.17116/rosrino201826241
7. Савлевич Е.Л. Егоров В.И. Шачнев К.Н. Татаренко Н.Г. Анализ схем лечения полипозного риносинусита в Российской Федерации. Российская оториноларингология. 2019;18;1(98). Savlevich E.L., Egorov V.I., Shachnev K.N., Tatarenko N.G. The analysis of polypous rhinosinusitis treatment regimens in the Russian Federation. Rossiiskaya otorinolaringologiya. 2019;18(1):124–134. (in Russ.) https://doi.org/10.18692/1810-4800-2019-1-124-134
8. Head K, Chong LY, Piromchai P, Hopkins C, Philpott C, Schilder AG, Burton MJ. Systemic and topical antibiotics for chronic rhinosinusitis. Cochrane Database Syst Rev. 2016;4:CD011994. https://doi.org/10.1002/14651858.CD011994
9. Савлевич Е.Л., Черенкова В.А., Молодницкая А.Ю. Принципы базисной терапии полипозного риносинусита. Медицинский Совет. 2020;(16):73-78. https://doi.org/10.21518/2079-701X-2020-16-73-78 Savlevich E.L., Cherenkova V.A., Molodnitskaia A.Yu. Basic principles for the treatment of chronic rhinosinusitis with nasal polyps. Meditsinskiy sovet = Medical Council. 2020;(16):73-78. (In Russ.) https://doi.org/10.21518/2079-701X-2020-16-73-78
10. Савлевич Е.Л., Курбачева О.М., Зурочка А.В., Митрофанова Е.С., Смолкин Ю.С., Любимова Е.В. Роль блокаторов лейкотриеновых рецепторов в терапии аллергического ринита в сочетании с полипозным риносинуситом. Медицинский Совет. 2022;(8):111-116. Savlevich E.L., Kurbacheva O.M., Zurochka A.V., Mitrofanova E.S., Smolkin Yu.S., Lyubimova E.V. The role of leukotriene receptor blockers in the treatment of allergic rhinitis in combination with chronic rhinosinusitis with nasal polyps. Meditsinskiy sovet = Medical Council. 2022;(8):111-116. (In Russ.) https://doi.org/10.21518/2079-701X-2022-16-8-111-116
11. Савлевич Е.Л., Бродовская О.Б., Ремизова И.И., Чистякова Г.Н., Ищенко А.М., Симбирцев А.С. Клинико-иммунологическая эффективность применение новой аэрозольной формы рекомбинантного интерферона-α2b в лечении больных с острыми назофарингитами. Цитокины и воспаление. 2010;1(9): 49-56. Savlevich E.L., Brodovskaya O.B., Remizova I.I., Chistyakova G.N., Ishchenko A.M., Simbirtsev A.S. Clinical and immunological aspects of application of the new aerosol form of recombinant interferon α2b in the treatment of patients with acute nasopharyngitis. Tsitokiny i vospalenie. 2010;1(9):49-56. (In Russ.)
12. Коркмазов М.Ю., Дубинец И.Д., Ленгина М.А., Коркмазов А. М., Корнова Н.В., Рябенко Ю.И. Отдельные показатели иммунологической реактивности при хирургической альтерации лор-органов. Российский иммунологический журнал. 2022; 25(2): 201-206. Korkmazov M.Yu., Dubinets I.D., Lengina M.A., Korkmazov A.M., Kornova N.V., Ryabenko Yu.I. Distinct indexes of immunological reactivity in surgical alteration of ORL organs. Rossiyskiy immunologicheskiy zhurnal = Russian journal of immunology. 2022; 25(2): 201-206. (In Russ.). https://doi.org/10.46235/1028-7221-1121-DIO
13. Dumitriu IE, Baruah P, Manfredi AA, Bianchi ME, Rovere-Querini P. HMGB1: guiding immunity from within. Trends Immunol. 2005 ;26(7):381–387. https://doi.org/10.1016/j.it.2005.04.009
14. Cavone L, Cuppari C, Manti S, Grasso L, Arrigo T, Calamai L, Salpietro C, Chiarugi A. Increase in the Level of Proinflammatory Cytokine HMGB1 in Nasal Fluids of Patients With Rhinitis and its Sequestration by Glycyrrhizin Induces Eosinophil Cell Death. Clin Exp Otorhinolaryngol. 2015;8(2):123-8. https://doi.org/10.3342/ceo.2015.8.2.123
15. Чихиржина Е.В., Поляничко А.М., Старкова Т.Ю. Внеядерные функции негистонового белка HMGB1. Цитология. 2020;62,(10):716-725. Chikhirzhinaa E. V., Polyanichkoa A. M., Starkova T. Yu. Extranuclear Functions of Nonhistone Protein HMGB1. Cytology. 2020;62,(10):716-725. https://doi.org/10.31857/S0041377120100016
Lotze MT16. , Tracey KJ. High-mobility group box 1 protein (HMGB1):nuclear weapon in the immune arsenal. Nat Rev Immunol 2005;5(4):331–342. (In Russ.) https://doi.org/10.1038/nri1594
17. Егоров В.И., Савлевич Е.Л. Место врожденного иммунитета в развитии хронического риносинусита и перспективы тактики консервативного лечения. Альманах клинической медицины. 2016;44(7):850-856. Egorov V.I., Savlevich E.L. Тhe role of innate immunity in the development of chronic rhinosinusitis and perspectives of its conservative management. Almanac of Clinical Medicine. 2016;44(7):850-856. (in Russ) https://doi.org/10.18786/2072-0505-2016-44-7-850-856
18. Vroling AB, Fokkens WJ, van Drunen CM. How epithelial cells detect danger: aiding the immune response. Allergy. 2008;63(9):1110–1123. https://doi.org/10.1111/j.1398-9995.2008.01785.x
19. Chen D, Bellussi LM, Passali D, Chen L. LPS may enhance expression and release of HMGB1 in human nasal epithelial cells in vitro. Acta Otorhinolaryngol Ital. 2013 Dec;33(6):398-404. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3870446/
20. Gardella S, Andrei C, Ferrera D, Lotti LV, Torrisi MR, Bianchi ME, Rubartelli A. The nuclear protein HMGB1 is secreted by monocytes via a non-classical, vesicle-mediated secretory pathway. EMBO Rep. 2002;3(10):995-1001. https://doi.org/10.1093/embo-reports/kvf198.
21. Park JS, Svetkauskaite D, He Q, Kim JY, Strassheim D, Ishizaka A, Abraham E. Involvement of toll-like receptors 2 and 4 in cellular activation by high mobility group box 1 protein. J Biol Chem. 2004 Feb 27;279(9):7370-7. https://doi.org/10.1074/jbc.M306793200
22. Kokkola R, Andersson A, Mullins G, Ostberg T, Treutiger CJ, Arnold B, Nawroth P, Andersson U, Harris RA, Harris HE. RAGE is the major receptor for the proinflammatory activity of HMGB1 in rodent macrophages. Scand J Immunol. 2005 Jan;61(1):1-9. https://doi.org/10.1111/j.0300-9475.2005.01534.x
23. Sims GP, Rowe DC, Rietdijk ST, Herbst R, Coyle AJ. HMGB1 and RAGE in inflammation and cancer. Annu Rev Immunol. 2010;28:367-388. https://doi.org/10.1146/annurev.immunol.021908.132603
24. Bellussi LM, Cocca S, Passali GC, Passali D. HMGB1 in the Pathogenesis of Nasal Inflammatory Diseases and its Inhibition as New Therapeutic Approach: A Review from the Literature. Int Arch Otorhinolaryngol. 2017;21(4):390-398. https://doi.org/10.1055/s-0036-1597665
25. Yang H, Wang H, Czura CJ, Tracey KJ. HMGB1 as a cytokine and therapeutic target. J Endotoxin Res. 2002;8(6):469-72 https://doi.org/10.1179/096805102125001091
26. Bordbar N, Karimi MH, Amirghofran Z. The effect of glycyrrhizin on maturation and T cell stimulating activity of dendritic cells. Cell Immunol. 2012;280(1):44-49. https://doi.org/10.1016/j.cellimm.2012.11.013
27. Дадаев Х.А., Садырова М.А., Акилов Д.Х.Лекарственное растение солодка голая. Биология и интегративная медицина. 2021. № 1 (48). С. 250-263. Dadaev K., Sadyrova M., Akilov J. Medicinal plant Glycyrrhiza Glabra. Biology and integrative medicine. 2021. № 1 (48). С. 250-263. https://cyberleninka.ru/article/n/lekarstvennoe-rastenie-solodka-golaya
28. Shamsa F., Ohtsuki K., Hasanzadeh E., Rezazadeh Sh. The anti-nflammatory and anti-viral effects of an ethnic medicine: glycyrrhizin, J. Med. Plants. 2010;9(6):1–28. https://jmp.ir/article-1-504-en.pdf
29. Коркмазов М.Ю., Солодовник А.В., Коркмазов А.М., Ленгина М.A. Перспективы использования растительного препарата в сочетании с физическими методами при комплексной терапии хронического аденоидита. Медицинский Совет. 2021;(18):19-27. Korkmazov M.Yu., Solodovnik A.V., Korkmazov A.M., Lengina M.A. Prospects for using herbal preparation in combination with physical methods in complex therapy of chronic adenoiditis. Meditsinskiy sovet = Medical Council. 2021;(18):19-27. (In Russ.) https://doi.org/10.21518/2079-701X-2021-18-19-27
30. Mollica L, De Marchis F, Spitaleri A, Dallacosta C, Pennacchini D, Zamai M, Agresti A, Trisciuoglio L, Musco G, Bianchi ME. Glycyrrhizin binds to high-mobility group box 1 protein and inhibits its cytokine activities. Chem Biol. 2007;14(4):431-41. https://doi.org/10.1016/j.chembiol.2007.03.007
31. Lotfi R, Herzog GI, DeMarco RA, Beer-Stolz D, Lee JJ, Rubartelli A, Schrezenmeier H, Lotze MT. Eosinophils oxidize damage-associated molecular pattern molecules derived from stressed cells. J Immunol. 2009;183(8):5023-31. https://doi.org/10.4049/jimmunol.0900504
32. Wang Y, Yang M, Ma Z, Liang Q, Tan H, Xiao C, Gao Y. Effects of 18beta-glycyrrhizic acid and 18alpha-glycyrrhizic acid on mRNA and protein expression of cytochrome P450 3A in cultured rat primary hepatocyte. Zhongguo Zhong Yao Za Zhi. 2009;34(3):307-311.
33. Li J, Zhao M, Xiang X, He Q, Gui R. A novel biomimetic nanomedicine system with anti-inflammatory and anti-osteoporosis effects improves the therapy efficacy of steroid-resistant nephrotic syndrome. J Nanobiotechnology. 2021;19(1):417. https://doi.org/10.1186/s12951-021-01165-z
34. Yao Z, Fu Y. Glycyrrhizic acid restrains airway inflammation and remodeling in asthma via the TGF-β1/Smad signaling pathway. Exp Ther Med. 2021;21(5):461. https://doi.org/10.3892/etm.2021.9892
35. Савлевич Е.Л., Зурочка А.В., Курбачева О.М., Егоров В.И., Гаганов Л.В., Любимова Е.В. Трансформирующие факторы роста TGF-β1, TGF-β2 и TGF-β3 в ткани носовых полипов при разных фенотипах полипозного риносинусита. Медицинская иммунология. 2022;24(1):1417-1426. Savlevich E.L., Zurochka A.V., Kurbacheva O.M., Egorov V.I., Gaganov L.E., Lyubimova E.V. Transforming growth factors TGF-β1, TGF-β2 and TGF-β3 in the tissue of nasal polyps in different phenotypes of chronic rhinosinusitis with nasal polyps. Medical Immunology (Russia)/Meditsinskaya Immunologiya. 2022;24(1):147-156. (in Russ.) https://doi.org/10.15789/1563-0625-TGF-2365
36. Еремеева А.В., Сорокина Л.Н., Минеев В.Н., Лим В.В., Нёма М.А., Трофимов В.И. Экспрессия фактора транскрипции FoxP3 при бронхиальной астме. Медицинская иммунология. 2016;18(4):373-378. Eremeeva A.V., Sorokina L.N., Mineev V.N., Lim V.V., Nyoma M.A., Trofimov V.I. Expression of FoxP3 transcription factor in bronchial asthma. Medical Immunology (Russia). 2016;18(4):373-378. (In Russ.) https://doi.org/10.15789/1563-0625-2016-4-373-378
37. Fouladi S, Masjedi M, Ghasemi R, G Hakemi M, Eskandari N. The In Vitro Impact of Glycyrrhizic Acid on CD4+ T Lymphocytes through OX40 Receptor in the Patients with Allergic Rhinitis. Inflammation. 2018;41(5):1690-1701. https://doi.org/10.1007/s10753-018-0813-8
38. Дроздова М.В., Рязанцев С.В., Быкова А.В. Новые возможности терапии экссудативного среднего отита у детей. Вопросы практической педиатрии. 2022; 17(2): 65–71. Drozdova M.V., Bykova A.V., Ryazantsev S.V. New therapeutic options for otitis media with effusion in children. Vopr. prakt. pediatr. (Clinical Practice in Pediatrics). 2022; 17(2): 65–71. (In Russ). https://doi.org/10.20953/1817-7646-2022-2-65-71.
39. Камаев А.В., Трусова О.В., Макарова И.В., Коростовцев Д.С. Исследование клинической эффективности аммония глицирризината у детей дошкольного возраста из группы высокого риска формирования бронхиальной астмы. Вопросы практической педиатрии. 2018;13(4):104-11. Kamaev AV, Trusova OV, Makarova IV, Korostovtsev DS. Study of ammonium glycyrrhizinate clinical effectiveness in preschool age children of high risk for asthma. Voprosy prakticheskoi pediatrii. 2018;13(4):104-11 (in Russ) https://doi.org/10.20953/1817-7646-2018-4-104-111
40. Березовский А.С., Незабудкин С.Н., Незабудкина А.С., Антонова Т.И. Место аммония глицирризината (глицирама) в терапии легкой персистирующей бронхиальной астмы у детей. Аллергология и иммунология в педиатрии. 2012;3(30):2-6. Berezovskii AS, Nezabudkin SN, Nezabudkina AS, Antonova TI. Place of Ammonium glycyrrisinate (Glycyram) in the treatment of mild persistent asthma in children. Allergologiia i immunologiia v pediatrii. 2012;3(30):2-6 (in Russ)
41. Ревякина В.А., Ларькова И.А., Кувшинова Е.Д. Возможности превентивной противовоспалительной терапии в острый период ОРИ у детей с бронхиальной астмой легкого и среднетяжелого течения. Вопросы практической педиатрии. 2020;15(6):35-41. Revyakina VA, Larkova IA, Kuvshinova ED. Preventive anti-inflammatory therapy during the acute respiratory infections in children with mild and moderate bronchial asthma. Voprosy prakticheskoi pediatrii. 2020;15(6):35-41 (in Russ). https://doi.org/10.20953/1817-7646-2020-6-35-41
42. Геппе Н.А., Малахов А.Б., Бойцова Е.В., Гаймоленко И.Н., Ермакова И.Н., Зайцев А.А., Ивахненко Е.Ф., Ильенкова Н.А., Камаев А.В., Клюхи- на Ю.Б., Кондюрина Е.Г., Конова О.М., Кулагина В.В., Лев Н.С., Лютина Е.И., Мегирян М.М., Мельникова И.М., Мещеряков В.В., Мизерницкий Ю.Л., Миронова А.К., Михалев Е.В., Мозжухина Л.И., Одинаева Н.Д., Павлинова Е.Б., Побединская Н.С., Скачкова М.А., Сорока Н.Д., Тришина С.В., Царькова С.А., Шуляк И.П. Резолюция Экспертного совета по вопросу применения противовоспалительного препарата аммония глицирризинат в лечении острых инфекций дыхательных путей и аллергических заболеваний респираторного тракта. Педиатрия. Consilium Medicum. 2022;4:317–321. Geppe NA, Malakhov AB, Boitsova EV, Gaimolenko IN, Ermakova IN, Zaitsev AA, Ivakhnenko EF, Il'enkova NA, Kamaev AV, Kliukhina IuB, Kondiurina EG, Konova OM, Kulagina VV, Lev NS, Liutina EI, Megirian MM, Mel'nikova IM, Meshcheriakov VV, Mizernitskii IuL, Mironova AK, Mikhalev EV, Mozzhukhina LI, Odinaeva ND, Pavlinova EB, Pobedinskaia NS, Skachkova MA, Soroka ND, Trishina SV, Tsar'kova SA, Shuliak IP. Resolution of the Expert Council on the use of the anti-inflammatory drug ammonium glycyrrhizinate in the treatment of acute respiratory infections and allergic diseases of the respiratory tract. Pediatrics. Consilium Medicum. 2022;4:317–321. https://doi.org/10.26442/26586630.2022.4.201953

Изобретение относится к области противовоспалительной терапии полипозного риносинусита, а именно к применению перорального препарата, содержащего аммония глицирризинат в качестве активного компонента, в противовоспалительной терапии полипозного риносинусита. Изобретение обеспечивает расширение арсенала средств для противовоспалительной терапии полипозного риносинусита, патогенетической мишенью которой является эффективное противодействие провоспалительным эффектам HMGB1, что клинически определяется снижением основных симптомов заболевания (заложенности, выделений из носа и т.д.), отечности слизистой носа, отсутствием дальнейшего роста и/или уменьшением размера полипов, повышением контроля над течением заболевания. 4 з.п. ф-лы, 7 табл., 3 пр., 7 ил.
1. Применение перорального препарата, содержащего аммония глицирризинат в качестве активного компонента, в противовоспалительной терапии полипозного риносинусита.
2. Применение по п.1, в котором препарат используется в твердой лекарственной форме, предпочтительно таблетированной.
3. Применение по п.2, в котором в качестве препарата, содержащего аммония глицирризинат, применяется препарат Реглисам в дозировке 50 мг в таблетке.
4. Применение по п.3, в котором препарат Реглисам применяется комплексно, совместно с использованием мометазона фуроата интраназально и орошением изотоническим солевым раствором слизистой оболочки носа.
5. Применение по п.3 или 4, в котором препарат Реглисам применяется в течение 90 дней по 1 таблетке 2-3 раза в день.
| ОВЧИННИКОВ А.Ю | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Эффективная фармакотерапия, 2022, Т | |||
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| CHANG G.-H | |||
| et al | |||
| Nasal irrigation with | |||
Авторы
Даты
2024-04-17—Публикация
2023-07-06—Подача