Изобретение относится к области химического синтеза, в частности к способу получения трититаната натрия допированного медью, перспективного для применения в энергетике, а именно в качестве материала для отрицательного электрода натрий-ионных аккумуляторов.
Титанаты натрия представляют собой трехмерные структуры, сшитые из отрицательно заряженных слоев искаженных октаэдров [TiO6]8- между которыми размещаются катионы Na+. В пределах слоев кислородные октаэдры соединяются друг с другом общими вершинами и/или ребрами. Титанаты состава Na2TinO2n+1 (n=2-9) кристаллизуются в моноклинной сингонии, при этом натрий в каркасе способен к физико-химическим реакциям катионного обмена. Различия в структуре (особенности расположения и упаковки октаэдров TiO6, размещения катионов щелочного металла) определяют физико-химические свойства титанатов натрия, включая электрохимическую работоспособность при использовании в роли интеркаляционных матриц для натрий-ионных аккумуляторов, в частности, удельную емкость, энергию, допустимые токовые нагрузки, устойчивость к циклированию и т. д.
Трититанат натрия, Na2Ti3O7, обладает моноклинной симметрией, каркас Na2Ti3O7 составлен из зигзагообразных октаэдрических слоев [Ti3O7]2−. Катионы Na+ локализуются в межслоевом пространстве в двух кристаллографически различных позициях Na1 и Na2 и окружены 9 и 7 анионами кислорода, соответственно. В решетке Na2Ti3O7 для внедрения ионов, таких как Li+, Na+ или K+, доступно два типа пустот: тетраэдрические (только для лития) и октаэдрические. Важным свойством является сохранение двухфазного равновесия Na2Ti3O7/Na4Ti3O7 в ходе заряда/разряда, что обеспечивает слабое изменение потенциала. Интеркаляция двух ионов Na+ на формульную единицу Na2Ti3O7 (~0,3 В отн. Na/Na+) подразумевает удельную емкость, равную ~177 мА⋅ч/г, при деформации решетки 6% (меньше 9-12% характерных для графита при интеркаляции в него лития). По некоторым данным, имеется возможность обратимого поглощения 3,5 ионов натрия на формульную единицу Na2Ti3O7 с емкостью до 311 мА⋅ч/г.
Недостатком трититаната натрия является малая электронная проводимость (~10-8 См/см), так как для него характерно наличие широкой запрещенной зоны ~3,28 эВ. Помимо этого, усилия исследователей направлены на ускорение транспорта ионов Na+ в Na2Ti3O7 и совершенствование циклической стабильности. Транспортные свойства Na2Ti3O7 могут быть в значительной степени улучшены за счет создания в структуре примесных или собственных дефектов, уровень которых располагается в запрещенной зоне. Этого можно добиться за счет допирования. Более того, допирование определенными элементами может способствовать и увеличению устойчивости структуры материала к натрированию и денатрированию, например, за счет расширения решетки при введении ионов с бóльшим, в сравнении с решетчатыми, радиусом. Помимо электрохимической работоспособности, изменение химического состава Na2Ti3O7 оказывает положительное влияние на его каталитическую и фотокаталитическую активность, газосенсорные, магнитные и другие свойства.
К способам допирования полупроводниковых структур относится эпитаксия - ориентированное выращивание на подложке монокристаллических слоев с контролируемым составом. Такой способ подходит для изготовления тонких пленок. Химический состав уже готовых титанатов натрия можно изменить в процессе ионного обмена, что можно рассматривать как ex situ дропирование. Получение допированных титанатов натрия в одну стадию можно считать in situ допированием. Такой подход обычно осуществляют с помощью гидротермального, золь-гель, твердофазного или механохимического метода за счет обработки реакционной композиции из TiO2 и NaOH с определенным содержанием допирующей добавки. Для получения допированных титанатов натрия в нанокристаллической форме наиболее перспективна гидротермальная технология.
Известен способ получения допированного медью трититаната натрия за счет многостадийного процесса, объединяющего золь-гель технологию, метод ионного обмена и высокотемпературную обработку [Vithal M. et al. «Synthesis of Cu2+ and Ag+ doped Na2Ti3O7 by a facile ion-exchange method as visible-light-driven photocatalysts» // Ceramics International (2013), v. 39, pp. 8429-8439]. На первой стадии получали трититанат натрия Na2Ti3O7 из металлического титана и трет-бутоксида натрия. Для этого порошок металлического титана растворяли в смеси 30 % H2O2 и 25 % NH4OH при температуре 0-5°С в течение 4-5 ч до получения пероксокомплекса титана. К нему добавляли водный раствор трет-бутоксида натрия в стехиометрическом количестве при постоянном перемешивании. Затем вводили C6H8O7 при мольном соотношении металлов к кислоте 1:2 для получения металл-цитратного комплекса и доводили pH до 7, вводя разбавленный раствор NH4OH. Смесь перемешивали в течение нескольких часов при комнатной температуре и медленно выпаривали до получения вязкой жидкости. На этом этапе добавляли гелеобразующий реагент - этиленгликоль при молярном соотношении 1:2,4. Смесь вываривали при температуре 100°С в течение 2-3 ч при постоянном перемешивании. В начале затвердевания температуру повышали до 160-180°С. Полученную массу перетирали и прогревали при температуре 400°С для удаления органических примесей. Наконец, продукт обрабатывали в муфельной печи при 950°С в течение 12 ч. На втором этапе проводили допирование трититаната натрия медью в процессе ионного обмена до образования CuTi3O7. Для этого 1 г Na2Ti3O7 помещали в 100 мл 0,1 М раствора CuCl2 и перемешивали при комнатной температуре в течение ночи. Полученный продукт промывали водой и сушили при 200°С в течение 3 ч. В процессе ионного обмена цвет материала менялся с белого (Na2Ti3O7) на светло-голубой (CuTi3O7).
Недостатками описанного способа является сложность и затратность получения из-за многостадийности, необходимости подготовительных операций, повышенной трудоемкости, теплоемкости процесса и времени синтеза более 35 ч.
Из [Machida Masato et al. «Pillaring and photocatalytic property of partially substituted layered titanates, Na2Ti3-xMxO7 and K2Ti4-xMxO9 (M=Mn, Fe, Co, Ni, Cu)» // Journal of Molecular Catalysis A: Chemical, 2000, V.155, pp. 131-142] известен многостадийный способ получения Al2O3- и SiO2-пилларированного допированного медью трититаната натрия. Для этого Na2CO3, TiO2 и CuO прокаливали при температуре 800°С в течение 30 ч. Далее проводили ионный обмен 3 г синтезированного допированного трититаната натрия в 200 мл раствора 1 моль/л HCl при комнатной температуре в течение 1 недели с получением протонированных производных. Интеркаляцию гексиламина осуществляли смешиванием 1 г протонированной формы с 5 моль/л водным раствором при комнатной температуре в течение 1 недели. Затем продукт обрабатывали тетраэтилортосиликатом или водным раствором гидроксокомплекса [Al13O4(OH)24(H2O)12]7+ при 60°C в течение 3 дней. Раствор готовили путем медленного добавления C6H13NH2 к гидроксокомплексу до получения конечного коэффициента гидролиза OH/Al=2,3 (pH=4,0-4,5) и последующего созревания при 60°C в течение 4 ч. После такой обработки, продукт отфильтровывали от маточного раствора центрифугированием, промывали водой или этанолом и сушили на воздухе при комнатной температуре. На последней стадии образец прокаливали при температурах 300-500°С в токе кислорода.
К недостаткам можно отнести длительность, многостадийность, использование специфических реагентов, необходимость поддержания узкого диапазона рН.
Известен способ синтеза допированного медью титаната натрия в форме нанотрубок гидротермальным методом с использованием микроволнового излучения [Manfroi D.C. et al. «Microwave-assisted hydrothermal synthesis of Cu-doped titanate nanotubes: photoluminescence and photocatalysis properties» // NSTI-Nanotech, 2014, www.nsti.org, V.3]. Для его получения определенное количество TiO2 диспергировали в 50 мл 10 М раствора NaOH, затем в смесь вводили допирующий агент, обеспечивающий содержание меди в продукте, равное 5 мас.%. Далее проводили гидротермально-микроволновую обработку реакционной смеси при температуре 130°C и мощности микроволнового излучения 450 Вт в течение 2-4 часов с помощью системы MARS-5 (“CEM”, США). По окончании процесса образец охлаждали до комнатной температуры, промывали деионизированной водой до тех пор, пока значение pH не достигло 6 и сушили при комнатной температуре.
К недостаткам, прежде всего, можно отнести необходимость использования специализированного дорогостоящего оборудования. Помимо этого, в аналоге не приведена информация об условиях синтеза, в частности не раскрыто соединение меди, используемое в качестве допирующего агента, нет сведений о массе навески TiO2. Существенным недостатком также является отсутствие термообработки для дегидратации и кристаллизации конечного продукта, что привело к получению смеси титанатов, а не чистого однофазного допированного Na2Ti3O7.
Наиболее близким аналогом по условиям синтеза является способ гидротермального получения нанотрубчатого титаната натрия, допированного медью из [Umek Polona, et al., «Coordination of Intercalated Cu2+ Sites in Copper Doped Sodium Titanate Nanotubes and Nanoribbons» // J. Phys. Chem. C, 2008, V.112, pp.15311-15319]. Допирование материала по указанному способу осуществляли в режиме in situ. Для этого 2 г TiO2 в фазе анатаза смешивали с допирующим прекурсором в концентрации 3 мас.% Cu2+ и 25 мл 10 М раствора NaOH. Реакционную смесь помещали в автоклав с тефлоновым вкладышем объемом 23 мл (степень заполнения - 88%) и выдерживали при 135°C в течение 72 часов. Полученный продукт диспергировали в 100 мл деионизированной воды, отфильтровывали, промывали в 50 мл этилового спирта и сушили в течение ночи при 100 и 300°C.
Недостатками способа, прежде всего, являются длительность, а также неоднородность по составу полученного продукта, что связано с отсутствием информации какие именно титанаты были получены, так как известно, что для получения трититанатов натрия требуется высокотемпературная обработка. Помимо этого в источнике информации не раскрыто соединение меди, однако специалисту понятно, что природа прекурсора может оказывать влияние на структуру конечного продукта.
Техническим результатом заявляемого изобретения является получение однофазного допированного медью трититаната натрия, имеющего двухуровневую структуру из микрочастиц, состоящих из нанотрубок и нанолистов, что достигается совместной гидротермальной обработкой тетрахлорида титана, гидроксида натрия и нитрата меди в присутствии перекиси водорода при температуре 150-180°С в течение 18 часов с последующей промывкой, сушкой и отжигом при 500°С на протяжении 2 часов. Уменьшение времени синтеза и получение однофазного продукта в сравнении с прототипом обеспечивается главным образом использованием прекурсора хлорида титана(IV), а также введением перекиси водорода.
Достижение технического результата заявляемого изобретения подтверждается рядом методов. Фазовый состав изучали методом рентгеновской дифрактометрии (РД). Морфологию исследовали методами сканирующей (СЭМ), сканирующей просвечивающей (СПЭМ) и просвечивающей (ПЭМ) электронной микроскопии. Элементный состав исследовали с помощью энергодисперсионной спектроскопии (ЭДС) и рентгенофлуоресцентным методом (РФА). Текстурные характеристики исследовали методом низкотемпературной адсорбции-десорбции N2. Химический состав изучали методом рентгеновской фотоэлектронной спектроскопии (РФЭС). Оптоэлектронные свойства исследовали методом спектрофотометрии. Электронную проводимость определяли методом потенциостатической хроноамперометрии (ХП).
Электрохимические испытания проводили методами, общепринятыми в данной области техники. Электрод из заявленного материала готовили по стандартной намазной технологии. Электродную композицию получали смешением заявленного материала, полученного по одному из способов, проиллюстрированных в примерах 1-4), с одной или несколькими электропроводящими добавками с содержанием до 25 мас.% и одним или несколькими связующими с содержанием от 1 до 15 мас.%. В качестве электропроводящей добавки использовали сажу марки Super P или углеродные нанотрубки Tuball™ Bat NMP от “OCSiAl” (Россия). В роли связующего выступал поливинилиденфторид.
Изобретение проиллюстрировано на следующих рисунках:
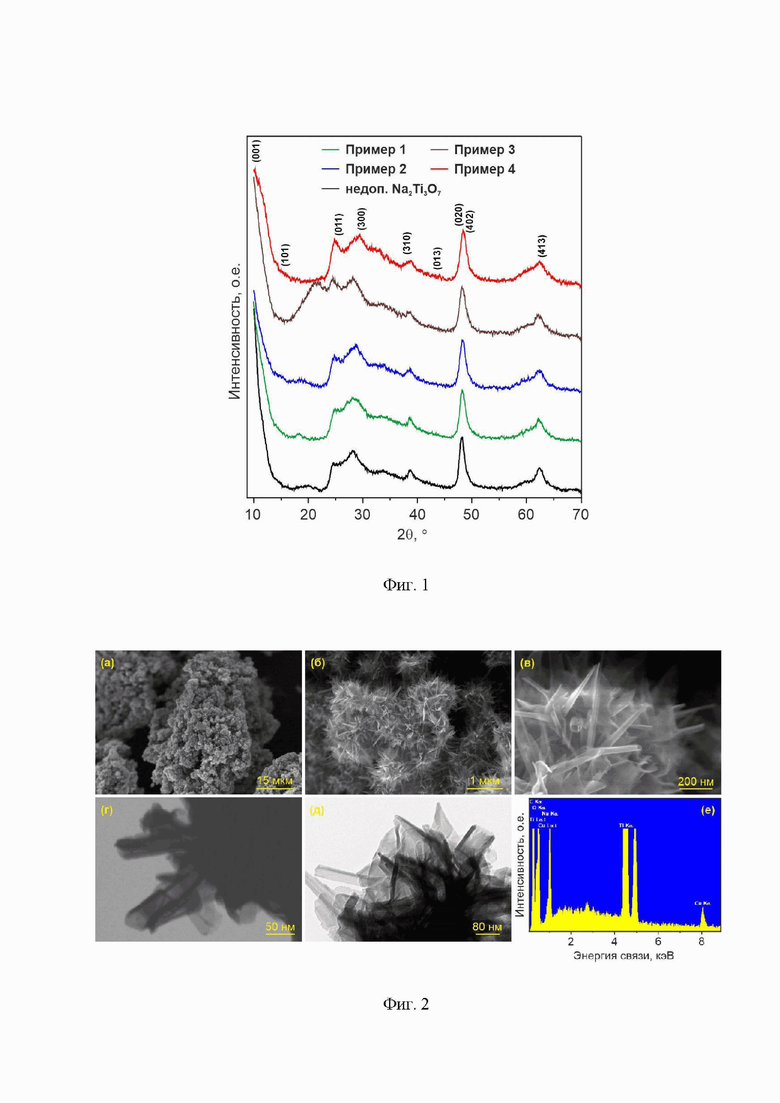
фиг. 1. Дифрактограммы допированного медью трититаната натрия, полученного по примерам 1-4 с индексами основных рефлексов элементарной ячейки Na2Ti3O7;
фиг. 2. Изображения частиц при съемке в режимах СЭМ при увеличении 1,5Кх (а), 22Кх (б), 100Кх (в), СПЭМ (г), ПЭМ (д) и данные рентгеноспектрального микроанализа (е) для допированного медью трититаната натрия, синтезированного по примеру 2;
фиг. 3. Обзорные рентгеновские фотоэлектронные спектры и соответствующие РФЭС-спектры высокого разрешения для уровня Cu 2p допированного медью трититаната натрия, полученного по примерам 2 (а, б) и 4 (в, г), на вставках приведено оцененное по РФЭС-спектрам содержание элементов;
фиг. 4. Оптические спектры поглощения (а) и соответствующие им зависимости Тауца (б) для допированного медью трититаната натрия, полученного по примерам 1-4 с фотографиями внешнего вида заявленного материала с разным содержанием меди;
фиг. 5. Результаты электрохимических испытаний допированного медью трититаната натрия, синтезированного по примерам 2 и 4 в натриевой полуячейке в интервале потенциалов 2,5-0,01 В отн. Na/Na+ при комнатной температуре: зарядно-разрядные кривые (а) и зависимость емкости от номера цикла (б) при различных плотностях тока 0,1С, 0,5С, 1С, 2С, 3С и 4С (1С = 177 мА/г), циклируемость при плотности тока 2С (в).
Рефлексы на зарегистрированных дифрактограммах на фиг. 1 проиндексированы в соответствии базой данных PDF-2 (2015 г.) и отнесены к Na2Ti3O7 в моноклинной сингонии с пространственной группой P21/m (карточка PDF № 00-031-1329). Линий, отвечающих примесным фазам меди, на дифрактограммах не обнаружено. Результаты уточнения кристаллической структуры по методу Ритвельда демонстрируют увеличение объема элементарной ячейки Na2Ti3O7 при допировании медью до 9,5 %, что объясняется вхождением меди в решетку Na2Ti3O7.
Согласно электронно-микроскопическим исследованиям (фиг. 2а-д), допированный медью трититанат натрия представлен образованиями структур с размерами в несколько единиц микрон, состоящих, в свою очередь, из нанотрубок и нанолистов. Согласно измерениям, большинство нанотрубок имеют внешний диаметр от 30 до 40 нм, толщина их стенок составляет 2-3 нм, а длина достигает несколько сотен нанометров. Нанолисты характеризуются непланарной формой и имеют один или более сгибов (вероятно, представляют собой развернутые нанотрубки). Толщина нанолистов равна нескольким нанометрам. Основываясь на данных, полученных в ходе электронно-микроскопических исследований, можно заключить, что введение допанта не оказывает влияния на морфологию. По данным рентгеноспектрального локального микроанализа (фиг. 2е) в состав заявляемого материала входят элементы Na, Ti, O и Cu. Из данных рентгеновской фотоэлектронной спектроскопии (фиг. 3) следует, что медь имеет заряд +2.
Согласно спектрофотометрическим исследованиям, допирование медью оказывает влияние на оптические свойства трититаната натрия. Так в оптических спектрах (фиг. 4а) заявляемого материала, полученного по примерам 1-4, в интервале 550-1400 нм (видимый и ближний инфракрасный диапазоны) регистрируется широкий пик поглощения, интенсивность которого увеличивается с ростом содержания меди. В ультрафиолетовом диапазоне в результате допирования наблюдается изменение положения края собственного поглощения Na2Ti3O7 со сдвигом в длинноволновую часть спектра, коррелирующее с концентрацией допанта. Это обусловлено возникновением дополнительных межзонных переносов заряда внутри запрещенной зоны трититаната натрия. Для оценки ширины запрещенной зоны использовали метод Тауца (фиг. 4б), согласно которому по мере увеличения количества меди наблюдается уменьшение ширины запрещенной зоны. Допированный медью Na2Ti3O7 имеет окраску (фиг. 4, соответствующие вставки), основной тон которой - зеленый, не характерную для Na2Ti3O7 (белый). В зависимости от содержания меди оттенок зеленого цвета изменяется от светлого до темного.
Результаты аттестации заявляемого материала в качестве электроактивного компонента отрицательного электрода для натрий-ионных аккумуляторов приведены на фиг. 5. Из данных (Фиг. 5а) следует, что при низких плотностях тока (0,1С и 0,5С) показатели электрохимической емкости не зависят от наличия меди в материале. С увеличением же токовой нагрузки картина меняется. При высоких плотностях тока 3С и 4С электрохимическая емкость заявляемого материала, полученного по примеру 4, в 2-2,5 раза выше таковой для недопированного Na2Ti3O7 (и примерно в 1,3-1,5 раза больше по сравнению с материалом, синтезированным по примеру 2). Фиг. 5а содержит кривые заряда и разряда допированного медью трититаната натрия, синтезированного по примеру 4, при различных токовых нагрузках. Как видно, форма кривых заявляемого материала аналогична таковой для Na2Ti3O7 в процессах электрохимического натрирования/денатрирования. Фиг. 5в показывает эволюцию электрохимической емкости для электрода из допированного медью трититаната натрия, полученного по примеру 4, при непрерывном циклировании в течение 300 циклов заряда-разряда при плотности тока 2С. Как следует из рисунка заявляемый материал демонстрирует хорошие показатели цикличности. После 300 цикла электрохимическая разрядная (экстракция натрия) емкость допированного медью трититаната натрия все еще равна примерно 90 мА⋅ч/г. Это соответствует сохраняемости (обратимость относительно значения на первом цикле) емкости на уровне 85%.
Заявляемый способ получения допированного медью трититаната натрия реализован в следующих примерах.
Пример 1. Синтез допированного медью трититаната натрия осуществляют следующим образом. Вначале смешивают 1 мл TiCl4 и 30 мг Cu(NO3)2⋅3H2O в 75 мл 10 M раствора NaOH, содержащего 6 мл 36 мас.% H2O2, при постоянном перемешивании. Далее смесь помещают в реактор-автоклав объемом 100 мл и выдерживают при температуре 180°С в течение 18 часов. По окончании процесса реакционную смесь отфильтровывают с помощью бумажного фильтра “синяя лента”. Полученный осадок промывают деионизированной водой 8-10 раз по 50 мл до нейтральной реакции (pH = 6-7) и сушат на воздухе при 120°С в течение 2 ч. Отжиг проводят при 500°С на протяжении 2 часов.
В полученном продукте содержание натрия, титана и меди в пересчете на оксиды по данным РФА составляет: 21,0 мас.% (Na2O), 77,8 мас.% (TiO2) и 1,2 мас.% (CuO). Удельная площадь поверхности равна 91,3 м2/г, суммарный удельный объем пор оценен как 0,12 см3/г, средний размер пор составляет 5,3 нм. Ширина запрещенной зоны равна 3,19 эВ, что меньше, чем для недопированного Na2Ti3O7 (3,55 эВ).
Пример 2. Получение допированного медью трититаната натрия выполняли по примеру 1 с теми отличиями, что в реакционную смесь добавляли 60 мг Cu(NO3)2⋅3H2O, а гидротермальную обработку проводили при температуре 150°С.
Из данных РФА содержание натрия, титана и меди в пересчете на оксиды равно: 20,4 мас.% (Na2O), 76,9 мас.% (TiO2) и 2,7 мас.% (CuO). Методом ЭДС выявлено присутствие элементов Na, Ti, O, Cu и С в следующих количествах, соответственно: 10,9, 41,0, 33,8, 1,2 и 13,1 вес%. Общий объем и средний размер пор составляют 0,13 см3/г и 4,0 нм соответственно, удельная площадь поверхности рассчитана как 80,6 м2/г. Энергия запрещенной зоны равна 2,88 эВ. Электрохимическая разрядная емкость при токовых нагрузках при 1С, 2C, 3C и 4С составила около 110, 83, 64 и 50 мА⋅ч/г, соответственно. Для недопированного Na2Ti3O7 показатели электрохимической разрядной емкости в указанном коридоре токовых нагрузок меньше: примерно 102, 73, 44 и 28 мА⋅ч/г.
Пример 3. Допированный медью трититанат натрия получали по примеру 1, но при введении в реакционную смесь 90 мг Cu(NO3)2⋅3H2O. Содержание натрия, титана и меди в пересчете на оксиды согласно данным РФА равно: 19,3 мас.% (Na2O), 76,2 мас.% (TiO2) и 4,5 мас.% (CuO). Удельная площадь поверхности составляет 80,9 м2/г, суммарный удельный объем пор - 0,11 см3/г, средний размер пор - 5,1 нм. Ширина запрещенной зоны определена как 2,65 эВ.
Пример 4. Получение трититаната натрия, допированного медью, выполняли по примеру 2, но при добавлении в реакционную смесь 120 мг Cu(NO3)2⋅3H2O. Натрий, титан и медь в пересчете на оксиды по данным РФА присутствует в следующих количествах: 18,5 мас.% (Na2O), 75,9 мас.% (TiO2) и 5,6 мас.% (CuO). Оцененное по результатам ЭДС анализа содержание элементов Na, Ti, O, Cu и С составляет 11,5, 43,1, 34,1, 2,3 и 9,0 вес%, соответственно. Удельная площадь поверхности определена как 73,3 м2/г. Общий объем и средний размер пор оценены как 0,1 см3/г и 5,3 нм соответственно. Ширина запрещенной зоны равна 2,42 эВ. Электронная проводимость, по данным метода ХП, составила 2,3⋅10-9 См/см, что выше, чем для недопированного Na2Ti3O7 (9,3⋅10-10 См/см). Электрохимическая разрядная емкость при токовых нагрузках 1С, 2C, 3C и 4С равна приблизительно 116, 97, 84 и 73 мА⋅ч/г соответственно.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГИБРИДНЫЙ НАНОКОМПОЗИТНЫЙ ФУНКЦИОНАЛЬНЫЙ МАТЕРИАЛ NaTiO - α-FeO | 2023 |
|
RU2811202C1 |
| АНОДНЫЙ МАТЕРИАЛ ДЛЯ ЛИТИЙ- И НАТРИЙ-ИОННЫХ АККУМУЛЯТОРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2730001C1 |
| АНОДНЫЙ МАТЕРИАЛ ДЛЯ ЛИТИЙ-ИОННОГО АККУМУЛЯТОРА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2703629C1 |
| Способ получения титаната натрия | 2019 |
|
RU2716186C1 |
| Способ получения оксида вольфрама, допированного кобальтом | 2020 |
|
RU2748755C1 |
| Композитный материал для фотокатализатора и способ его получения | 2020 |
|
RU2748372C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ η-МОДИФИКАЦИИ ДИОКСИДА ТИТАНА, ДОПИРОВАННОГО ВАНАДИЕМ, АКТИВНОГО В ВИДИМОЙ ОБЛАСТИ СПЕКТРА | 2013 |
|
RU2540336C1 |
| СПОСОБ МОДИФИЦИРОВАНИЯ МАРГАНЦЕМ НАНОРАЗМЕРНОГО ДИОКСИДА ТИТАНА | 2014 |
|
RU2565689C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКОВ ФАЗ СЛОИСТЫХ ТИТАНАТОВ S- И P-ЭЛЕМЕНТОВ | 2011 |
|
RU2487849C2 |
| Способ получения модифицированного фотокатализатора на основе диоксида титана | 2017 |
|
RU2640811C1 |


Изобретение относится к области химического синтеза, в частности к способу получения допированного медью трититаната натрия с иерархической микро/наноструктурой, перспективного для применения в натрий-ионных аккумуляторах в качестве материала отрицательного электрода. Способ включает гидротермальную обработку хлорида титана(IV) и трехводного нитрата меди(II), которые смешивают в водном растворе 10 М NaOH с добавкой 36 мас.% перекиси водорода при температурах 150-180°C в течение 18 ч, с последующей промывкой, сушкой на воздухе в течение 2 ч при температуре 120°C и отжигом при температуре 500°C в течение 2 ч. Способ обеспечивает получение однофазного допированного медью трититаната натрия, имеющего двухуровневую структуру из микрочастиц, состоящих из нанотрубок и нанолистов, при уменьшении времени синтеза. 5 ил., 4 пр.
Способ получения допированного медью трититаната натрия, включающий гидротермальную обработку смеси прекурсоров титана и меди в растворе щелочи с последующей промывкой, сушкой и температурной обработкой, отличающийся тем, что в качестве исходных веществ используют хлорид титана(IV) и трёхводный нитрат меди(II), которые смешивают в водном растворе 10 М NaOH с добавкой 36 мас.% H2O2, гидротермальную обработку проводят при температурах 150–180°C в течение 18 ч, а после промывки проводят сушку на воздухе в течение 2 ч при температуре 120°C и отжиг при температуре 500°C в течение 2 ч.
| UMEK POLONA et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Chem., 2008, v | |||
| Прялка для изготовления крученой нити | 1920 |
|
SU112A1 |
| ОПРА Д.П | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Пишущая машина | 1922 |
|
SU37A1 |
| HAGER SAMIR et al | |||
Авторы
Даты
2024-05-02—Публикация
2023-12-06—Подача