Изобретение относится к области литиевой электрохимической энергетики, в частности к анодным материалам литий-ионных аккумуляторов (ЛИА), применяемых для энергообеспечения крупногабаритных энергоустановок гибридного и электрического автотранспорта, систем бесперебойного электроснабжения, робототехнических средств, автономных аппаратов и т.п.
В настоящее время в качестве источников питания техники повсеместно применяются ЛИА, основу которых составляют углеродный анод (обычно графит или графитизированный углерод) и катод на основе литированного оксида металла (LiCoO2, LiMn2O4, LiNiO2). К недостаткам таких ЛИА относят существенные ограничения при функционировании в условиях форсированного заряда.
В настоящее время активно разрабатываются анодные материалы на основе соединений титана, высокие электрохимические потенциалы которых находятся в пределах окна стабильности 1,2-4,5 В типичных электролитов ЛИА (на основе 1 М раствора LiPF6 в смеси ЭК/ДМК/ДЭК, 1:1:1 объемн. ед.). Так, теоретическая удельная емкость β-фазы диоксида титана TiO2(B) достигает 335 мА⋅ч/г в расчете на заряженную форму LiTiO2(B), что имеет неоспоримые преимущества по сравнению с альтернативными материалами, например, на основе титаната лития Li4Ti5O12, TiO2 (анатаз), TiO2 (рутил). Кроме того, внедрение ионов лития в решетку TiO2 (В) осуществляется по принципу псевдоемкости - за счет протекания быстрых фарадеевских реакций с переносом заряда, скорость которых не ограничивается твердотельной диффузией Li+. К сожалению, использованию TiO2 (В) в качестве анода ЛИА препятствуют низкая электропроводность (~10-12 См/см) и деформация его кристаллической решетки при внедрении/извлечении ионов лития. К способам модифицирования TiO2(В), призванным устранить вышеуказанные недостатки, на сегодняшний день можно отнести создание гибридов или композитов (в том числе, материалов со структурой «ядро в оболочке») и допирование металлами/неметаллами.
Так, известен отрицательный электрод [пат. US 9184445, опубл. 10.11.2015] на основе композита из диоксида титана TiO2(B) и допированного рядом металлов титаната лития Li4Ti5-xMxO12. В режиме слабой токовой нагрузки 0,1С материал, включающий 60% Li4Ti5-xMxO12 и 40% TiO2(В), характеризуется достаточно высоким значением первоначальной емкости, равным 201 мА⋅ч/г. К недостаткам описанного материала относится низкая стабильность при циклировании (<95% уже после 50 циклов заряда/разряда). При этом увеличение доли титаната лития вплоть до 90% хоть и способствует повышению обратимости электрохимического процесса для композита, сопровождается, в то же время, существенным снижением его общего энергозапаса (до 177 мА⋅ч/г уже на первом цикле), что объясняется применением TiO2(В) в немодифицированном виде. Помимо этого, указано достижение более или менее хороших значений удельной емкости около 179 мА⋅ч/г (значение приведено для композитной смеси Li4Ti5-xMxO12/TiO2(В) в процентном соотношении 90:10) в условиях лишь пятидесятикратного циклирования, что не гарантирует работоспособность электрода при длительной эксплуатации.
В работе [Ventosa Е., Mei В., Xia W., Muhler М., Schuhmann W. "TiO2(В)/anatase composites synthesized by spray drying as high performance negative electrode material in Li-ion batteries" // ChemSusChem, 2013, V. 6, PP. 1312-1315] предложен способ получения допированного ниобием композита TiO2(В)/анатаз, основанный на длительном способе многократной распылительной сушки. Процесс получения Nb-TiO2(В)/анатаз осуществляют растворением оксосульфата титана TiOSO4⋅H2SO4⋅H2O в 1 М растворе H2NO3 при перемешивании в течение не менее 4 часов. Затем добавляют гидратированный оксалат ниобата аммония (NH4)NbO(C2O4)2⋅H2O и перемешивают в течение 1 часа. После этого смесь помещают в устройство, обеспечивающее нанесение раствора в виде мелких капель на подогреваемую пластину. После испарения всей жидкости, с пластины собирают порошок и отжигают при 600°С в кислородно-гелиевой атмосфере в течение 1 часа. Затем порошок промывают дистиллированной водой и сушат на воздухе при 110°С на протяжении 24 часов. В полученном композите Nb-TiO2(В)/анатаз содержание Nb составляет 1 ат. %, а доля TiO2 в модификации анатаз достигает 70%. Конечный продукт демонстрирует достаточно высокую удельную емкость, равную 180 мА⋅ч/г после пятидесяти циклов заряда/разряда при токовой нагрузке С/2. Существенным недостатком способа получения Nb-TiO2(В)/анатаз является значительная длительность процесса, требующая постоянного контроля, энергозатратность стадии отжига, небольшой выход конечного продукта с высокой долей TiO2 в модификации анатаз при существенном содержании ниобиевого допанта. Кроме того, характеристики материала указаны лишь для менее чем 50 циклов заряда/разряда, что не позволяет оценить его применимость в условиях более продолжительного циклирования.
Перспективным способом получения допированных форм TiO2(В) с высокой дисперсностью твердой фазы является гидротермальный синтез, при котором химические реакции протекают в водной среде при температурах выше 100°С и давлениях более 0,1 МПа. Метод несложен в технологическом оформлении и позволяет в широком диапазоне контролировать физико-химические характеристики получаемых оксидных соединений за счет изменения параметров режима обработки - температуры, длительности синтеза, концентрации реагентов, водородного показателя раствора, давления и пр. Следует отметить, что гидротермальный синтез проводится в замкнутой системе герметичного реактора-автоклава, результатом чего является его технологическая безопасность при условии соблюдения правил техники безопасности.
Известно получение гидротермальным синтезом и использование в качестве анода ЛИА допированного совместно ванадием и кобальтом диоксида титана Ti1-xCox-yVyO2(B) в виде нанолент [Amirsalehi М., Askari М. "Inflence of vanadium, cobalt-codoping on electrochemical performance of titanium dioxide bronze nanobelts used as lithium ion battery anodes" // Journal of Materials Science: Materials in Electronics, 2018, V. 29, PP. 13068-13076]. Процесс осуществляют автоклавированием в тефлоновом реакторе смеси, включающей TiO2/анатаз, метаванадат аммония NH4VO3 и нитрат кобальта Со(NO3)2⋅6H2O в присутствии 10 М раствора NaOH при температуре 170°С на протяжении 72 часов. Затем проводят ионный обмен в 0,1 М растворе HCl в течение 3 суток, отмывку и сушку при 80°С на протяжении 24 часов. Отжиг осуществляют при 400°С в течение 4 часов в атмосфере аргона. Конечный продукт Со/V-TiO2(В) демонстрирует высокую емкость, равную 250 мА⋅ч/г после 50 циклов при низкой скорости циклирования С/2. Существенным недостатком полученного материала является использование кобальта, стоимость которого в последние годы растет по экспоненте. Кроме того, токсичность кобальта и ванадия может привести к удорожанию процесса утилизации ЛИА. Также к недостаткам относится то, что в описанном материале полученные значения емкости достигаются при высоком суммарном содержании допантов, равном 5 мас. %. Кроме того, отсутствуют экспериментальные данные о работоспособности Ti1-xCox-yVy(B) материала при повышенных токовых нагрузках (>1С), что не позволяет судить о его пригодности в качестве анода для ЛИА высокой мощности.
Известно С-замещенное производное TiO2(В) с улучшенными электрохимическими характеристиками [з. WO 2017060407, опубл. 13.04.2017]. Заявленный анодный материал TiO2-yCy(B) получают многоступенчатым методом, объединяющим высокотемпературное окисление карбида титана и гидротермальный синтез. Для этого сначала окисляют при 500°С в течение 5 часов TiC до С-допированного TiO2. Затем в ходе гидротермальной обработки в щелочной среде при 160°С в течение 48 часов проводят трансформацию получившегося продукта в нанопроволоки С-допированного TiO2(В). Полученный продукт трехкратно, по очереди промывают 0,1 М HCl и деионизированной водой с последующим центрифугированием. После обработки этанолом материал сушат в вакууме при 40°С в течение 12 часов. Отжиг полученного продукта проводят при 300°С в течение 2 часов. На электродах из синтезированного по описанному способу С-TiO2(В) достигают устойчивое циклирование (~160 мА⋅ч/г после 1000 циклов заряда/разряда) даже при высокой токовой нагрузке 10С. К недостаткам известного способа относится существенная длительность и сложность получения TiO2-yCy(B) из-за необходимости включения в него дополнительных технологических этапов с использованием специализированного оборудования и реагентов, что необходимо на стадии предварительного окисления прекурсора и отмывки продукта синтеза в нескольких растворителях.
В качестве наиболее близкого к заявляемому выбран описанный в работе [Grosjean R., Fehse М., Pigeot-Remy S., Stievano L., Monconduit L., Cassaignon S. "Facile synthetic route towards nanostructured Fe-TiO2(В), used as negative electrode for Li-ion batteries" // J. Power Sourses, 2015, V. 278, PP. 1-8] активный материал анода ЛИА допированный железом TiO2(В), синтезированный в гидротермальных условиях. Как показали проведенные испытания, электроды из полученного материала обнаруживают достаточно высокую удельную емкость при низкой скорости циклирования. Так, удельная емкость составляет 230 мА⋅ч/г после 15 циклов заряда/разряда в режиме С/10.
Однако отсутствие данных о продолжительном циклировании этих электродов при высоких скоростях циклирования не позволяет в полной мере оценить электрохимические характеристики известного материала и вынести суждение о его практической применимости.
Способ получения указанного анодного материала включает смешение Fe(NO3)3⋅9H2O и TiO2 (атомное отношение Fe/Ti=0,1%) в присутствии 15 М раствора KOH в течение 30 минут, чередуя перемешивание смеси на магнитной мешалке и диспергирование компонентов в ультразвуковой ванне. Подготовленную смесь помещают в реактор и автоклавируют на протяжении 72 часов при 150°С. Полученный в результате гидротермального синтеза продукт многократно промывают деионизированной водой, фильтруют и помещают на 4 часа в 0,1 М раствор HCl для проведения ионного обмена. Затем материал еще раз промывают водой и сушат при 70°С в течение 15 часов. Кристаллизацию образца проводят в течение 3 часов при 400°С.
К недостаткам способа относится то, что приведенные условия всех стадий синтеза не обеспечивают получение анодного материала ЛИА с другим допантом в структуре.
Задача настоящего изобретения заключается в получении активного материала анода ЛИА, обладающего высокой устойчивостью структуры в процессе циклирования и высокими удельными электрохимическими характеристиками.
Технический результат изобретения заключается в увеличении устойчивости структуры анодного материала в процессе циклирования минимум до 90 циклов заряда/разряда и улучшении удельных электрохимических характеристик за счет формирования допированного цирконием наноструктурированного диоксида титана в кристаллографической модификации бронз, а также разработке способа его получения.
Технический результат достигают наноструктурированным допированным цирконием диоксидом титана в кристаллической модификации бронз, относящимся к твердым растворам с формулой Ti1-xZrxO2(B) (х=0,03-0,06). Его получают при гидротермальной обработке в щелочной среде наночастиц диоксида титана в модификации анатаз и соли металла, проведении ионного обмена в растворе соляной кислоты и последующем отжиге и отличается от известного способа тем, что гидротермальную обработку диоксида титана проводят в присутствии оксихлорида циркония ZrOCl2⋅8H2O в течение не менее 48 и не более 96 часов при температуре не менее 150°С и не более 170°С, а ионный обмен осуществляют в течение 72 часов с заменой раствора соляной кислоты каждые 24 часа.
Электроды на основе полученного анодного материала демонстрируют повышенные значения первоначальной зарядной и разрядной емкости в практически важном диапазоне и хорошую удельную емкость даже при высоких скоростях циклирования. Заявляемый положительный эффект достигается при соотношении Zr/Ti менее 0,1%.
Патентный поиск показал, что заявляемый анодный материал Ti1-xZrxO2(B) (х=0,03-0,06) не известен. Его синтез и электрохимические свойства не описаны.
Микроструктуру синтезированного Zr-TiO2(B) исследовали методом сканирующей электронной микроскопии. Распределение элементов изучали посредством микрозондового анализа. Кристаллическую структуру исследовали методом рентгенофазового анализа. Анализ экспериментальных дифрактограмм проводили в соответствии с базой эталонных данных PDF-2 (2006 г.). Удельную поверхность определяли из изотерм адсорбции азота.
Приготовление электродной массы из полученных анодных материалов производили посредством смешения в N-метилпирролидоне 80 мас % Ti1-xZrxO2(B), 10 мас % ацетиленовой сажи Super Р и 10 мас % поливинилиденфторида. Источник тока изготавляли в боксе в атмосфере аргона (99,999%). Диск металлического лития использовали в качестве противоэлектрода и электрода сравнения. Электролит состоял из смеси 1 М раствора LiClO4, пропиленкарбоната и диметоксиэтана в объемном соотношении 5:1.
Электрохимические испытания проводили с использованием потенциостата/гальваностата в режиме гальваностатического заряда/разряда в диапазоне от 3 до 1 В, при различных плотностях тока. Механизм электрохимического внедрения/извлечения ионов лития в/из Zr-TiO2(B) изучали методом циклической вольтамперометрии при скорости развертки потенциала 100 мкВ/с.
Результаты испытаний заявляемого анодного материала и его свойств представлены следующими иллюстрациями.
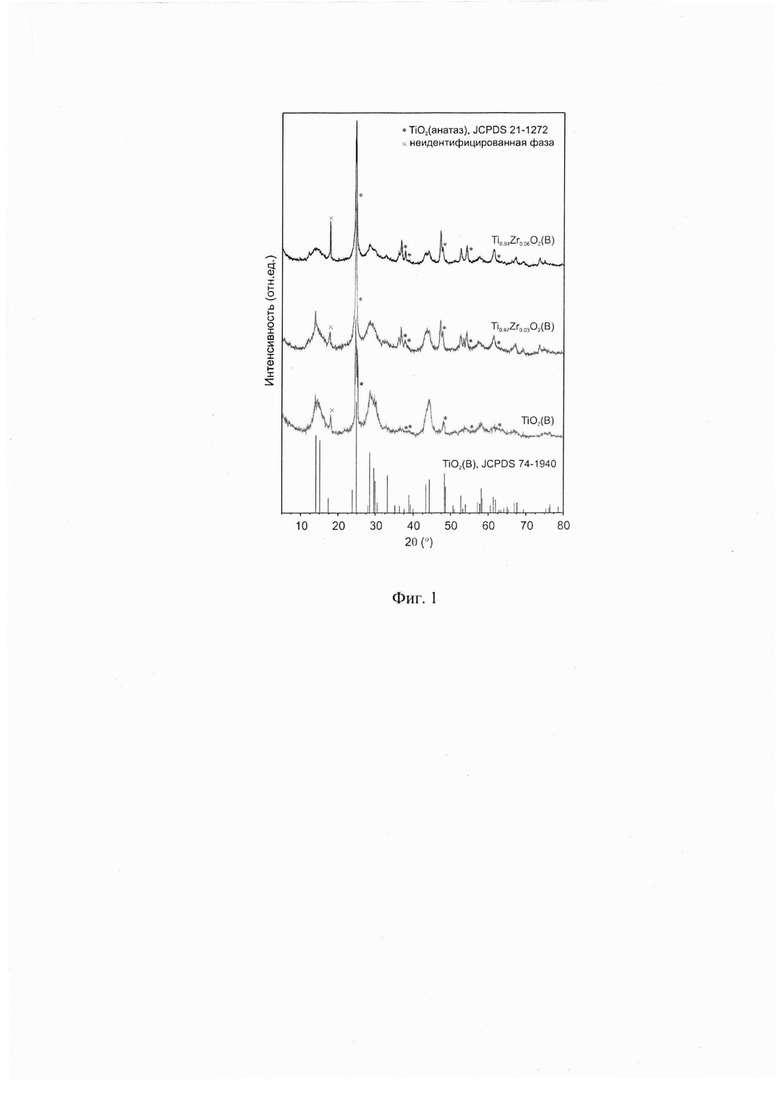
Фиг. 1. Дифрактограмма TiO2(В) и Ti1-xZrxO2(B) (х=0,03; 0,06).
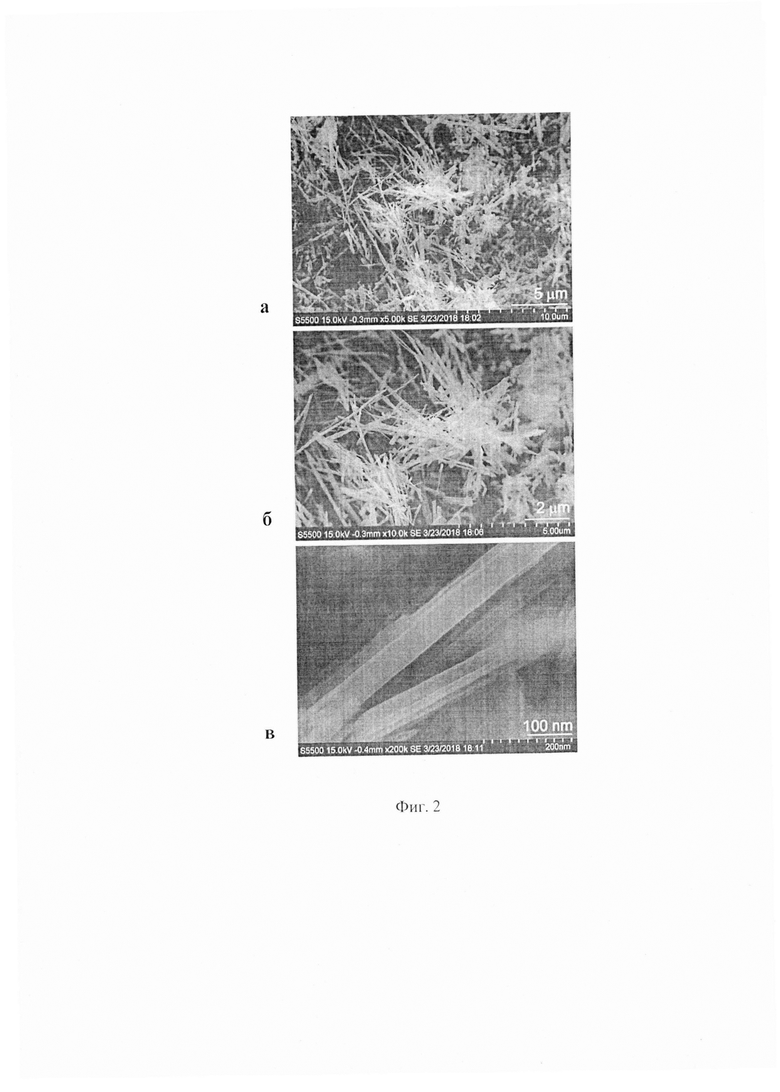
Фиг. 2. Микрофотографии структуры образца Ti0,94Zr0,06O2(B): а) увеличение в 5000 раз; б) увеличение в 10000 раз; в) увеличение в 200000 раз.
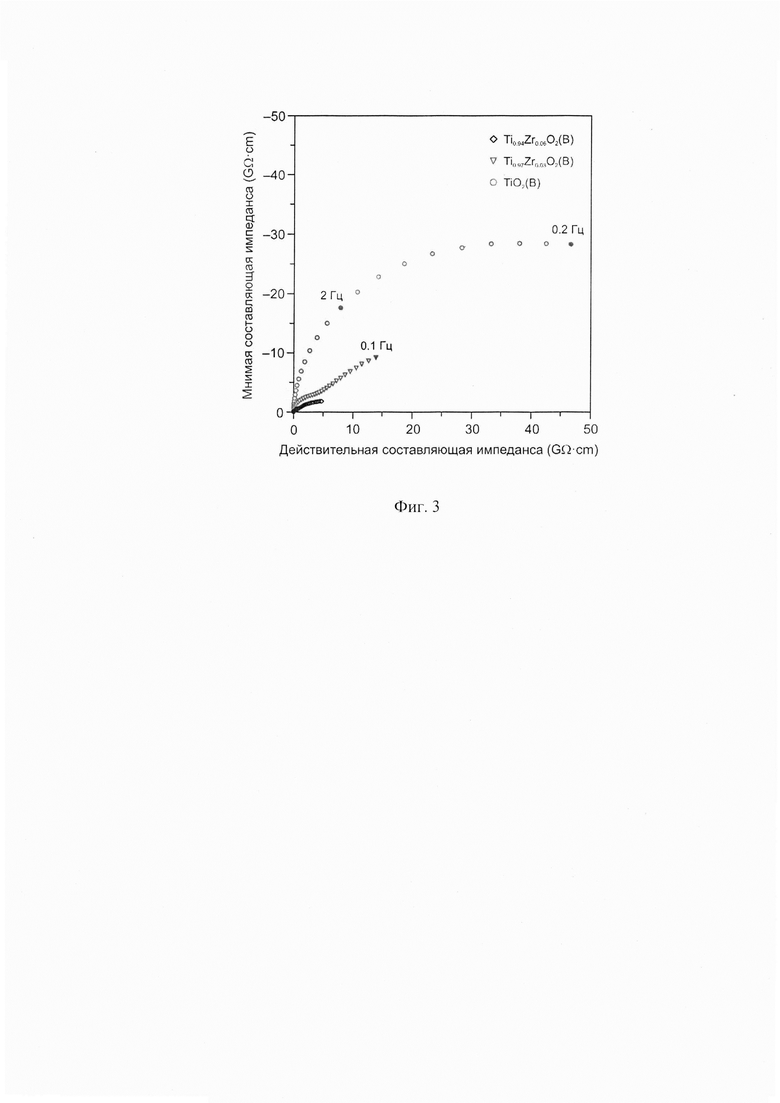
Фиг. 3. Импедансные спектры образцов TiO2(В), Ti0,97Zr0,03O2(B) и Ti0,94Zr0,06O2(B), синтезированных гидротермальным способом.
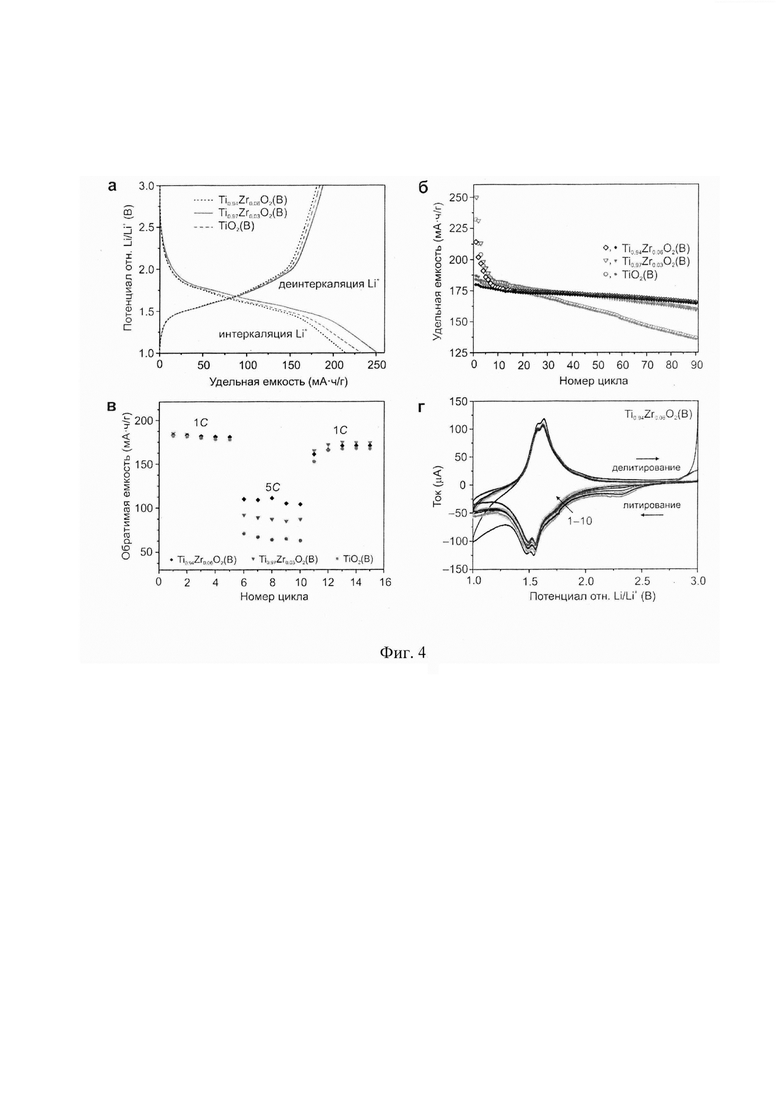
Фиг. 4. а) Кривые заряда/разряда первого цикла для TiO2(В), Ti0,97Zr0,03O2(B) и Ti0,94Zr0,06O2(B); б) Результаты 90-кратного циклирования TiO2(В), Ti0,97Zr0,03O2(B) и Ti0,94Zr0,06O2(B); в) Зависимость обратимой емкости TiO2(В), Ti0,97Zr0,03O2(B) и Ti0,94Zr0,06O2(B) от скорости циклирования; г) Циклические вольтамперограммы с первого по десятый цикл для Ti0,94Zr0,06O2(B) электрода.
Результаты рентгеновских дифрактограмм образцов на Фиг. 1. подтверждают, что допирование TiO2(В) сопровождается внедрением ионов Zr4+ в решетку путем частичного замещения Ti4+ с образованием твердого раствора Ti1-xZrxO2(B). При этом, значения a, b, c и β параметров решетки и объема элементарной ячейки Ti1-xZrxO2(B) строго коррелируют с атомным отношением Zr/Ti. На микрофотографиях сканирующей электронной микроскопии (Фиг. 2) видно, что синтезированные материалы представляют собой ленточные (nanobelts) наноструктуры TiO2(В) толщиной 10-15 нм, шириной 50-100 нм и длиной в несколько микрометров. Удельная площадь поверхности синтезированных образцов составляет 72-76 м2/г. Проведенные исследования свидетельствуют, что заявляемый анодный материал является наноструктурированным и относится к классу соединений нестехиометрического состава с общей формулой Ti1-xZrxO2(B) (х=0,03-0,06), представляющих собой твердые растворы на основе диоксида титана в модификации бронз и диоксида циркония.
Примеры конкретного осуществления способа.
Пример 1. Диоксид титана в модификации анатаз (в виде наночастиц) и оксихлорид циркония ZrOCl2⋅8H2O в стехиометрическом соотношении Zr/Ti=0,03, смешивают в присутствии 10М водного раствора NaOH. Синтез Ti0,97Zr0,03O2(B) осуществляют посредством совместной одностадийной гидротермальной обработки в автоклаве при температуре 150°С в течение 96 часов. Степень заполнения автоклава составляет ~80%. После завершения стадии гидротермальной обработки, автоклав извлекают из печи и охлаждают до комнатной температуры. Полученный продукт помещают в 0,05 М раствор HCl на 72 часа при постоянном перемешивании на магнитной мешалке с целью осуществления ионного обмена Na+ на Н+. Раз в 24 часа производят замену раствора HCl. По окончании стадии ионного обмена, осадок отделяют от раствора на центрифуге, промывают дистиллированной водой до рН=7, а затем сушат на воздухе в течение 12 часов при температуре 90°С. Отжиг образцов проводят путем выдержки в атмосфере воздуха при температуре 350°С в течение 5 часов.
Результаты исследования электрофизических свойств заявляемого анодного материала методом электрохимической импедансной спектроскопии (Фиг. 3) свидетельствуют о повышении электропроводности до 1,7⋅10-11 См/см. Методом гальваностатического заряда/разряда в диапазоне от 1,0 до 3,0 В при плотности тока 33,5 мА/г (С/10) показано, что первоначальные значения (Фиг. 4а) зарядной (интеркаляционной) и разрядной (деинтеркаляционной) емкости образца достигают 250 мА⋅ч/г и 187 мА⋅ч/г. При этом, даже после 90-кратного циклирования (Фиг. 4б) обратимая емкость для электрода на основе Ti0.97Zr0.03О2(B) составила 159 мА⋅ч/г, в то время ка значение данного параметра для недопированного TiO2(В) не превышает 135 мА⋅ч/г. Таким образом, эффективность циклирования Ti0.97Zr0.03O2(B) электрода равна ~85%. При высокой скорости циклирования 5С (плотность тока 1675 мА/г) электрод на основе Ti0,94Zr0,03O2(B), в диапазоне от 1,0 до 3,0 В, сохранял удельную емкость около 87 мА⋅ч/г (Фиг. 4в) против 63 мА⋅ч/г для недопированного TiO2(В).
Пример 2. Диоксид титана в модификации анатаз (в виде наночастиц) и оксихлорид циркония ZrOCl2⋅8H2O в стехиометрическом соотношении Zr/Ti=0,06 совместно диспергируют в 12 М водном растворе NaOH. Синтез Ti0,94Zr0,06O2(B) осуществляют посредством совместной одностадийной гидротермальной обработки в автоклаве при температуре 170°С в течение 48 часов. Степень заполнения автоклава составляет ~80%. Стадию ионного обмена Na+ на Н+ проводят как описано в примере 1. По окончании ионного обмена, осадок отделяют от раствора на центрифуге, промывают дистиллированной водой до рН=7, а затем сушат на воздухе в течение 15 часов при температуре 80°С. Отжиг образцов проводят путем выдержки в атмосфере воздуха при температуре 400°С в течение 3 часов.
Согласно данным метода электрохимической импедансной спектроскопии (Фиг. 3) допирование диоксида титана вплоть до Zr/Ti=0,06 приводит к увеличению электропроводности материала до 8,2⋅10-10 См/см. Кривые заряда/разряда первого цикла для Ti0.94Zr0.06O2(B) электрода (Фиг. 4а), зарегистрированные в диапазоне 1,0-3,0 В при токовой нагрузке 33,5 мА/г (С/10), показывают, что его зарядная (интеркаляционная) и разрядная (деинтеркаляционная) емкости равны 214 мА⋅ч/г и 180 мА⋅ч/г. По результатам 90 циклов заряда/разряда (Фиг. 4б) величина обратимой емкости для электрода на основе Ti0.94Zr0.06O2(B) достигает 165 мА⋅ч/г, что соответствует эффективности около 91,7%. При скорости циклирования 5С (плотность тока 1675 мА/г) в диапазоне от 1,0 до 3,0 В, Ti0.94Zr0.06O2(B) электрод сохраняет удельную емкость около 107 мА⋅ч/г (Фиг. 4в), что практически в два раза выше емкости недопированного TiO2(В), равной 64 мА⋅ч/г. Циклические вольтамперограммы с первого по десятый цикл (Фиг. 4г) для Ti0.94Zr0.06O2(B) электрода, полученные в диапазоне 1,0-3,0 В при скорости развертки потенциала 100 мкВ/с подтверждают высокую обратимость электрохимического процесса литирования/делитирования - симметричность пиков в катодной и анодной областях вольтамперограмм свидетельствует о практически полном извлечении внедренных ионов лития.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНОДНЫЙ МАТЕРИАЛ ДЛЯ ЛИТИЙ- И НАТРИЙ-ИОННЫХ АККУМУЛЯТОРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2730001C1 |
| Способ синтеза анодного материала для литий-ионных батарей | 2023 |
|
RU2803313C1 |
| Способ получения композиционного анодного материала TiNbO/C для литий-ионных аккумуляторов | 2022 |
|
RU2799067C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДОПИРОВАННОГО МЕДЬЮ ТРИТИТАНАТА НАТРИЯ | 2023 |
|
RU2818559C1 |
| ЛИТИЙ-ИОННЫЙ АККУМУЛЯТОР | 2015 |
|
RU2608598C2 |
| Композитный материал для фотокатализатора и способ его получения | 2020 |
|
RU2748372C1 |
| Способ получения ферромагнитного кислород-дефицитного диоксида титана в фазе бронз | 2023 |
|
RU2801392C1 |
| СЛОИСТЫЕ ТИТАНАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2010 |
|
RU2564339C2 |
| ТОНКОПЛЕНОЧНЫЙ НАНОСТРУКТУРИРОВАННЫЙ ЭЛЕКТРОДНЫЙ МАТЕРИАЛ И СПОСОБ ПОЛУЧЕНИЯ | 2009 |
|
RU2414771C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИТИЧЕСКОГО ДИОКСИДА ТИТАНА МОДИФИКАЦИИ АНАТАЗ И БРУКИТ НА ПОВЕРХНОСТИ КЕРАМИЧЕСКОГО ИЗДЕЛИЯ ИЗ РУТИЛА, ПОЛУЧЕННОГО ОКИСЛИТЕЛЬНЫМ КОНСТРУИРОВАНИЕМ | 2017 |
|
RU2678206C1 |
Изобретение может быть использовано при получении анодного материала литий-ионных аккумуляторов, применяемых для энергообеспечения крупногабаритных энергоустановок гибридного и электрического автотранспорта, систем бесперебойного электроснабжения, робототехнических средств и автономных аппаратов. В качестве такого материала предложен наноструктурированный допированный цирконием диоксид титана в кристаллической модификации бронз, относящийся к твердым растворам, с формулой Ti1-xZrxO2(B), где х=0,03-0,06. Для его получения проводят гидротермальную обработку в щелочной среде наночастиц диоксида титана в модификации анатаз в присутствии оксихлорида циркония ZrOCl2⋅8H2O в течение 48-96 ч при температуре не менее 150°С и не более 170°С. Затем осуществляют ионный обмен в течение 72 ч в 0,05 М растворе соляной кислоты с его заменой каждые 24 ч. Осадок отделяют на центрифуге, промывают дистиллированной водой до рН 7, сушат на воздухе в течение 12 ч при температуре 90°С и проводят отжиг. Изобретение позволяет увеличить устойчивость структуры анодного материала в процессе циклирования как минимум до 90 циклов заряда/разряда. 2 н.п. ф-лы, 4 ил., 2 пр.
1. Наноструктурированный допированный цирконием диоксид титана в кристаллической модификации бронз, относящийся к твердым растворам, с формулой Ti1-xZrxO2(B), где х=0,03-0,06.
2. Способ получения наноструктурированного допированного металлом диоксида титана в кристаллической модификации бронз по п. 1, заключающийся в гидротермальной обработке в щелочной среде наночастиц диоксида титана в модификации анатаз и соли металла, проведении ионного обмена в растворе соляной кислоты и последующем отжиге, отличающийся тем, что гидротермальную обработку диоксида титана проводят в присутствии оксихлорида циркония ZrOCl2⋅8H2O в течение 48-96 ч при температуре не менее 150°С и не более 170°С, ионный обмен осуществляют в течение 72 часов в 0,05 М растворе соляной кислоты с его заменой каждые 24 часа, осадок отделяют на центрифуге, промывают дистиллированной водой до рН=7, сушат на воздухе в течение 12 часов при температуре 90°С.
| ОПРА Д.П | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| В.В | |||
| Гусарова, 21-27 мая 2018 года, Санкт-Петербург, с | |||
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| ГНЕДЕНКОВ С.В | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Схема обмотки ротора для пуска в ход индукционного двигателя без помощи реостата, с применением принципа противосоединения обмоток при трогании двигателя с места | 1922 |
|
SU122A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕГИРОВАННОГО ДИОКСИДА ТИТАНА | 1992 |
|
RU2043302C1 |
| US 5445806 A1, 29.08.1995 | |||
| WO 2017154743 A1, 14.09.2017 | |||
| JP 10095667 A, 14.04.1998 | |||
| GROSJEAN R | |||
| et al., Facile synthetic route towards nanostructured Fe-TiO2(В), used as negative electrode for Li-ion batteries, Journal Power Sourses, 2015, v | |||
| ПАРОВАЯ ИЛИ ГАЗОВАЯ ТУРБИНА | 1914 |
|
SU278A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2019-10-21—Публикация
2019-01-10—Подача