Область техники
Настоящее изобретение относится к разработке систем для кожного барьера, в частности для младенцев или детей младшего возраста, при этом уровень защиты кожи оценивают посредством анализа результатов тестов на коже взрослого человека. Изобретение позволяет оценивать уровень защиты системы для кожного барьера на основании объективных данных, не прибегая при этом к проведению тестов на детях младшего возраста или младенцах.
Предпосылки создания изобретения
Очищающие средства для кожи содержат поверхностно-активные вещества, которые могут вызывать нарушение целостности кожного барьера, защищающего от проникновения внешних агрессивных агентов, что приводит к раздражению кожи. Оценивание мягкости действия очищающего средства на кожу обычно проводят путем клинической оценки и измерения изменений трансэпидермальной потери воды (ТЭПВ) по результатам проведения тестов согласно протоколам преувеличенного теста на аллергию с наложением пластыря или преувеличенного промывочного теста. Эти способы частично субъективны и часто дают различающиеся результаты.
Мягкость действия продуктов для ухода за кожей (в частности, очищающих продуктов, которые содержат потенциально раздражающие поверхностно-активные системы) обычно оценивают in vivo у взрослых с использованием тестов нормального применения, тестов преувеличенного (повторного) применения или тестов на аллергию с наложением пластыря. Даже для детских продуктов оценку сначала проводят среди взрослых, а после получения положительных результатов иногда проводят тесты нормального применения среди младенцев. Мягкость действия оценивают как отсутствие раздражения (как правило, кожной эритемы (покраснения)). Воздействие на кожный барьер обычно оценивают с помощью инструментов путем измерения трансэпидермальной потери воды (ТЭПВ). Воздействие продуктов на кожный барьер можно также изучать ex vivo, используя ячейки Франца и измеряя сопротивление кожи.
Однако предшествующие способы страдают от ряда недостатков и сложностей. Например, тесты нормального применения, как правило, требуют большого размера участка нанесения для различения разных уровней мягкости действия, что может быть привести к большим затратам средств и времени. В тестах на аллергию с наложением пластыря поверхностно-активные вещества могут проявлять себя по-разному в условиях закрытия пластырем по сравнению с условиями нормального применения. Результаты тестов с погружением руки могут зависеть от погодных условий. В тестах с промывкой сгибов тестируемый участок кожи может не быть репрезентативным для других участков тела.
Каждый из перечисленных выше пунктов дополнительно оценивают субъективно (клиническое наблюдение), что может привнести разброс в результаты оценки. Наконец, большинство этих тестов либо предназначены для выполнения на коже взрослого человека без требуемой корреляции с кожей младенца, либо такие исследования выполняют среди младенцев/детей младшего возраста, а клинические исследования на младенцах вызывают этические и технические вопросы. Как было отмечено, корректность прямого переноса данных, полученных для взрослых, на случай кожи младенцев уже ставилась под сомнение. Например, с кожей младенцев обычно не работают в ячейках Франца, и перенос таких данных на кожу младенцев вызывает сомнение. Эти способы всегда используют с учетом коэффициента безопасности (как правило, 10-кратного), который отражает неопределенность таких тестов.
Стоило бы разработать способ, с помощью которого можно было бы оценивать воздействие поверхностно-активной системы на кожный барьер младенца и/или ребенка младшего возраста путем объективного оценивания профиля концентрации некоторого маркера (такого как кофеин), который проникает в кожу взрослых пациентов. В настоящем изобретении ориентировано на оценку воздействия путем проведения тестов с биомаркером на коже взрослого человека, используя вычислительную модель для оценки воздействия на кожу младенца/ребенка младшего возраста и разрабатывая поверхностно-активную систему на основании результатов проведенных тестов и анализов.
Увлажнители представляют собой смеси химических агентов, специально выполненные с возможностью смягчения внешних слоев кожи или волос. Известны композиции для личной гигиены, имеющие увлажняющие свойства. Потребители ожидают, что такие композиции удовлетворяют ряду требований. Помимо эффектов ухода за кожей/волосами, которые определяют их целевое применение, важными считаются такие различные параметры, как дерматологическая совместимость, внешний вид, органолептические ощущения, стабильность при хранении и простота применения. Другим положительным эффектом от применения многих увлажнителей является защита кожи от воздействия внешней среды и агентов.
Описание графических материалов
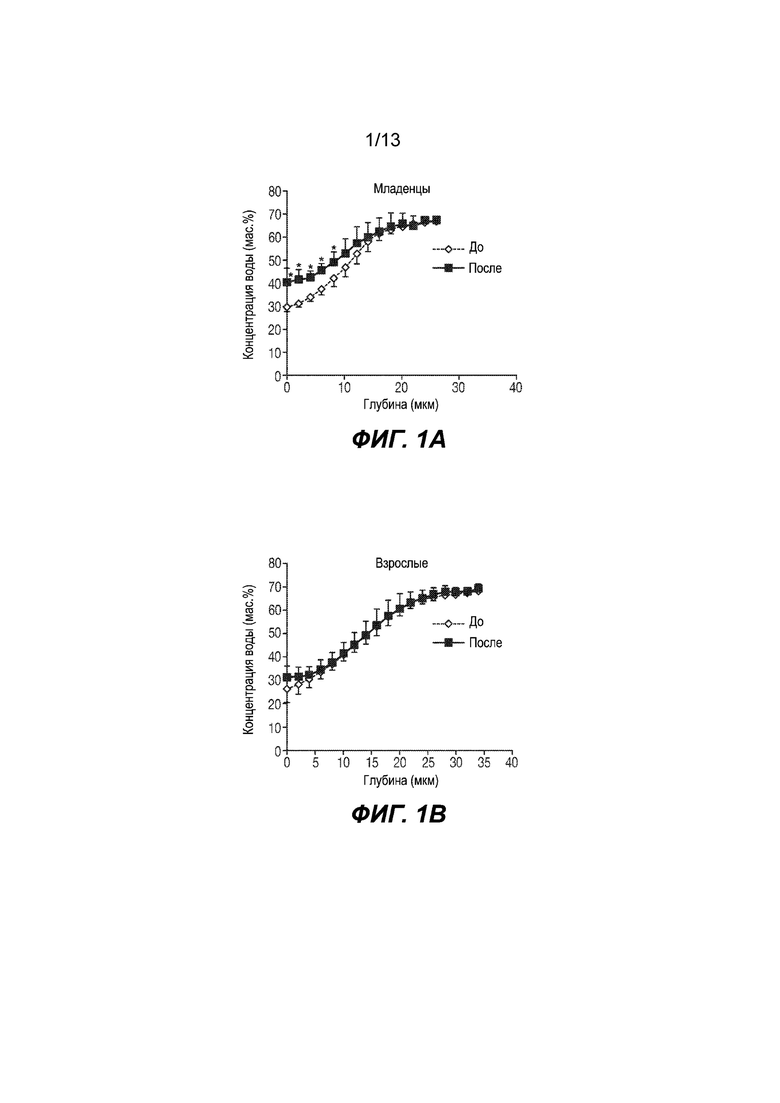
На Фиг. 1А и 1В изображено наблюдение поглощения экзогенно нанесенной воды с помощью рамановской конфокальной микроспектроскопии через 10 секунд после нанесения воды на кожу нижней передней части руки.
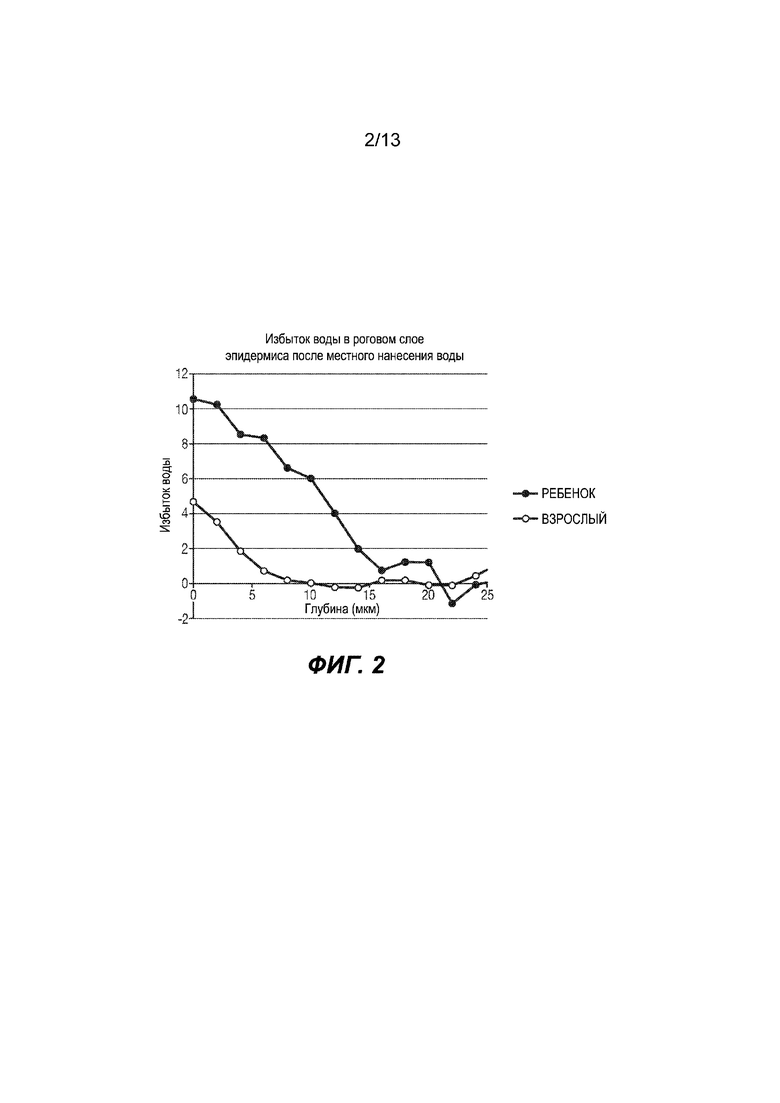
На Фиг. 2 изображено сравнение эксперимента (взрослый), модели (взрослый) и прогноза (ребенок).
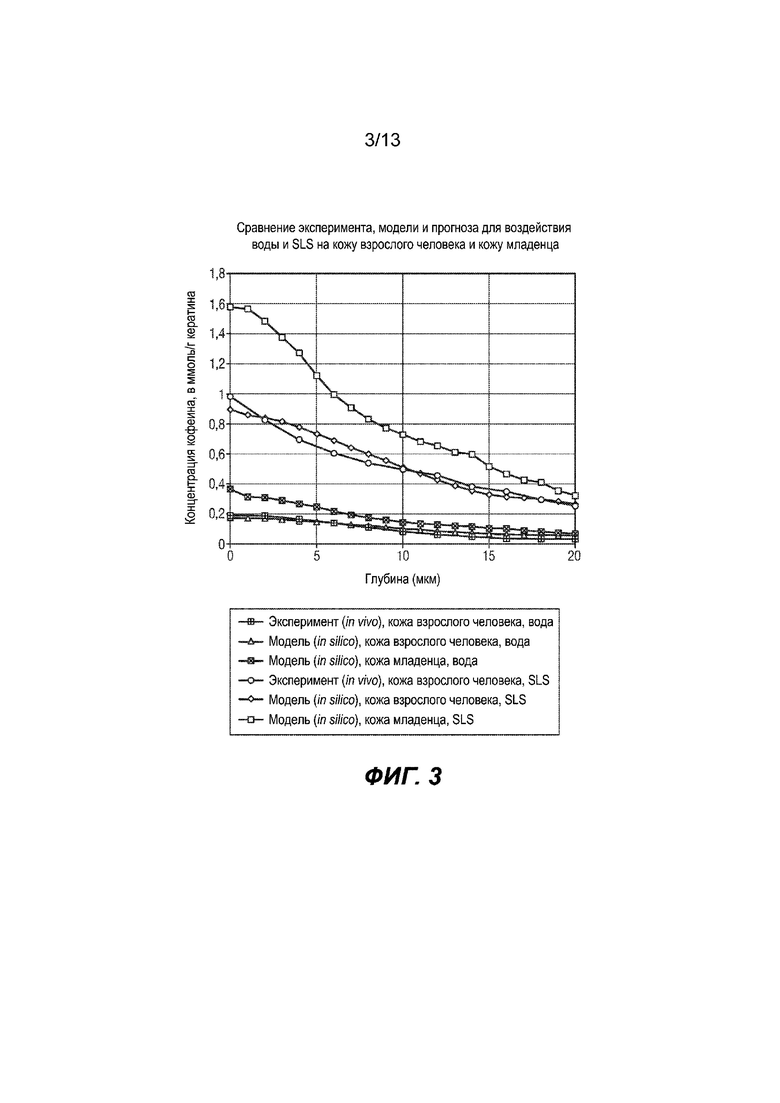
На Фиг. 3 изображено сравнение эксперимента, модели и прогноза для воздействия воды и SLS на кожу взрослого человека и кожу младенца.
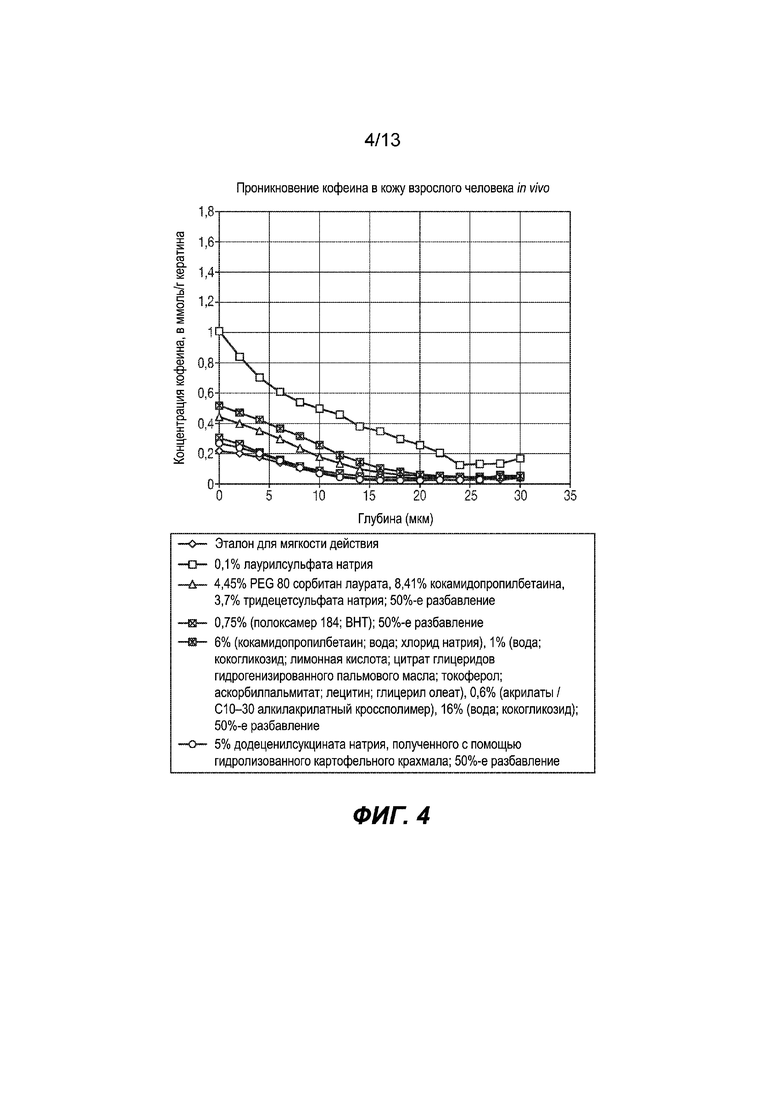
На Фиг. 4 изображено сравнение нескольких составов поверхностно-активных веществ.
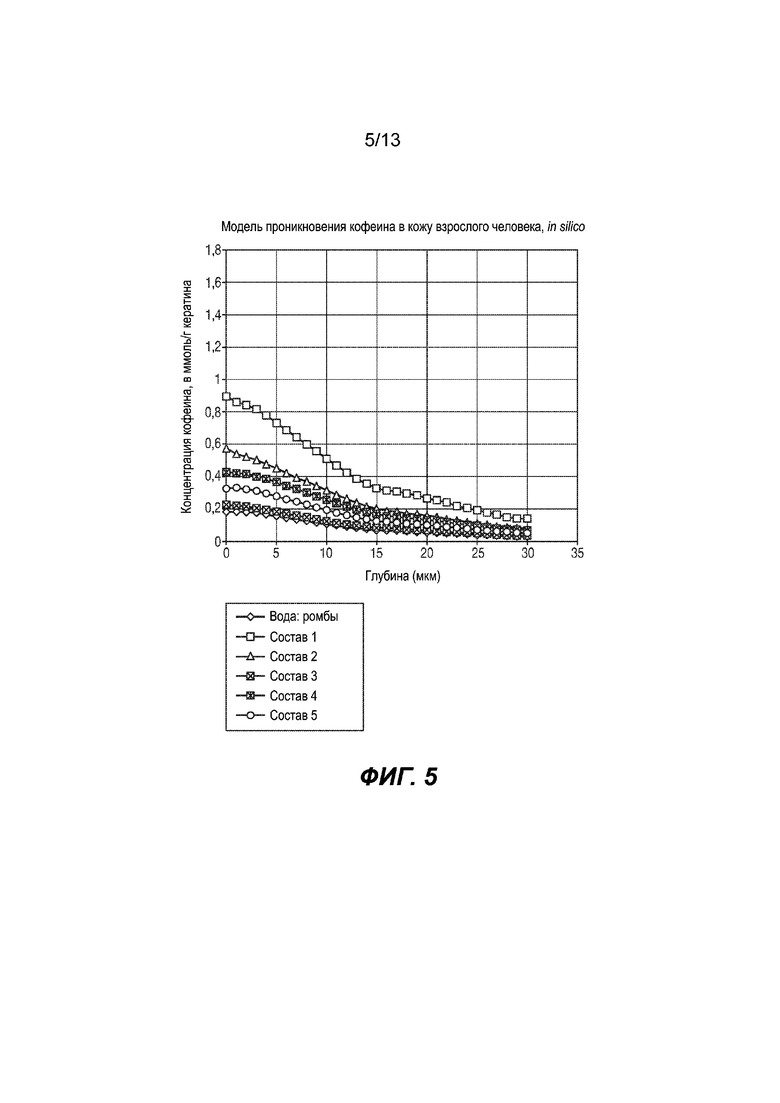
На Фиг. 5 изображено моделирование экспериментальных данных в модели эпидермиса взрослого человека in silico.
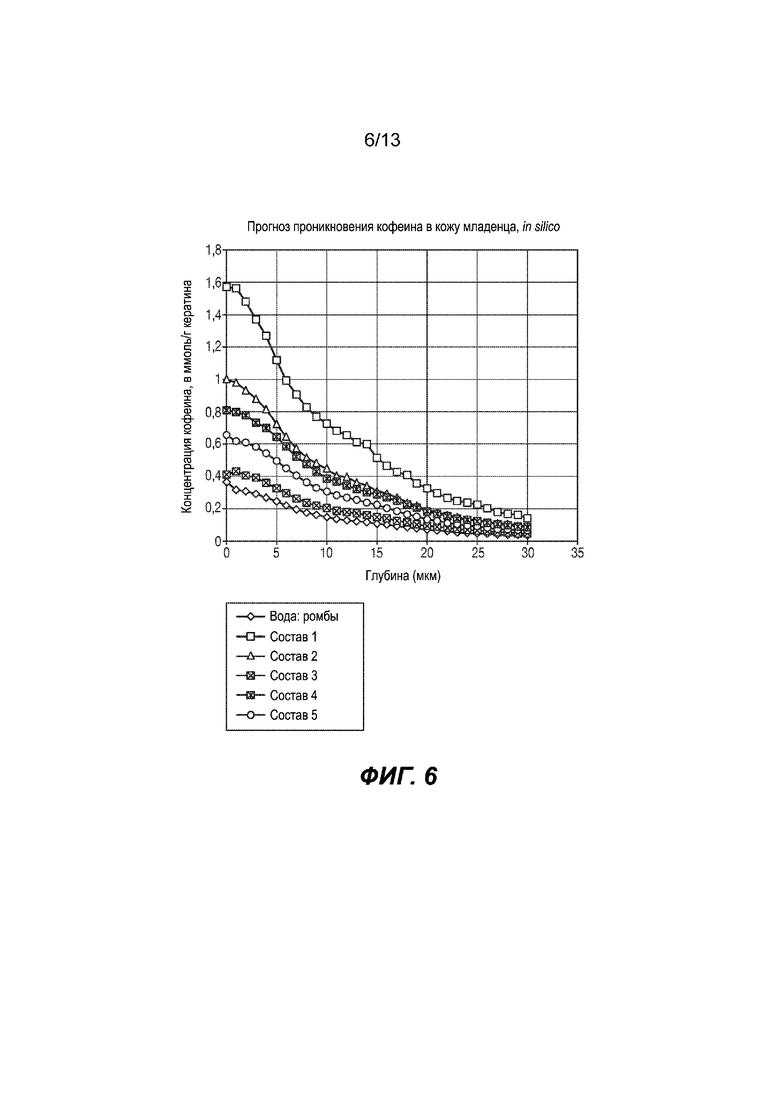
На Фиг. 6 изображены кривые прогнозируемой проницаемости кофеина после обработки поверхностно-активными веществами.
На Фиг. 7 изображено прогнозируемое поглощенное количество в роговом слое эпидермиса у ребенка, площадь под кривой в диапазоне глубин 0-10 мкм (ммоль кофеина/г кератина)
На Фиг. 8 изображены экспериментальные данные для кожи взрослого человека.
На Фиг. 9 изображено моделирование кожи взрослого человека.
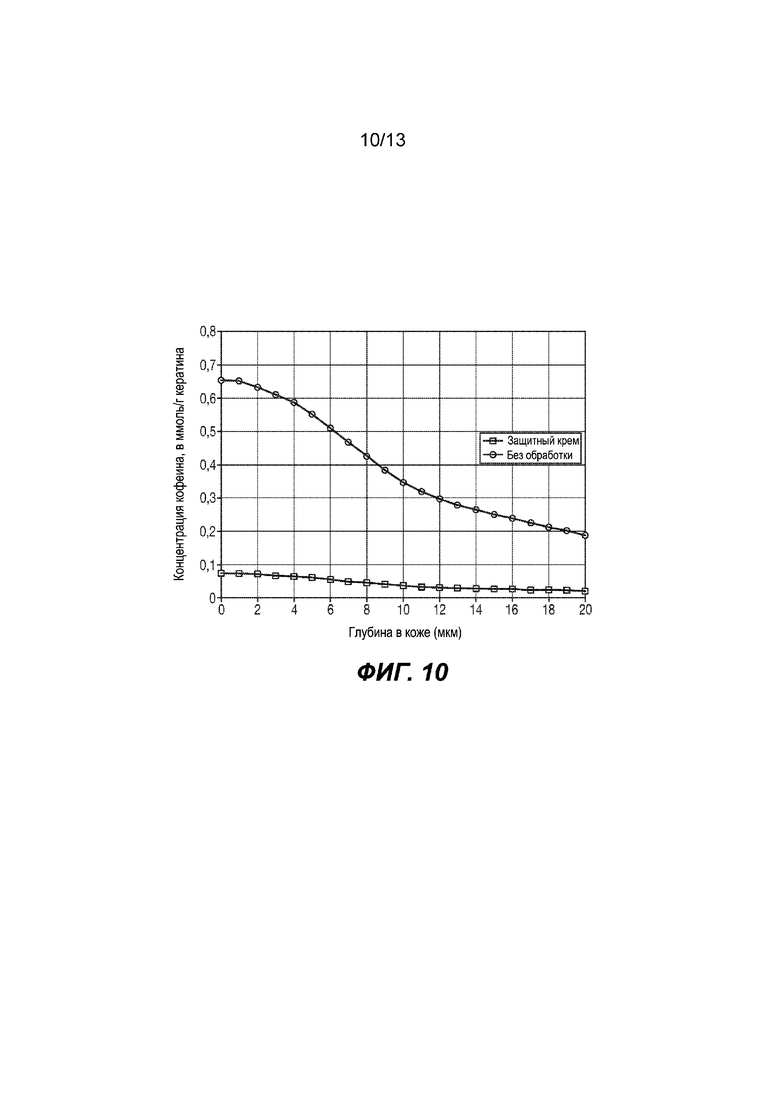
На Фиг. 10 изображены прогнозируемые результаты для кожи младенца.
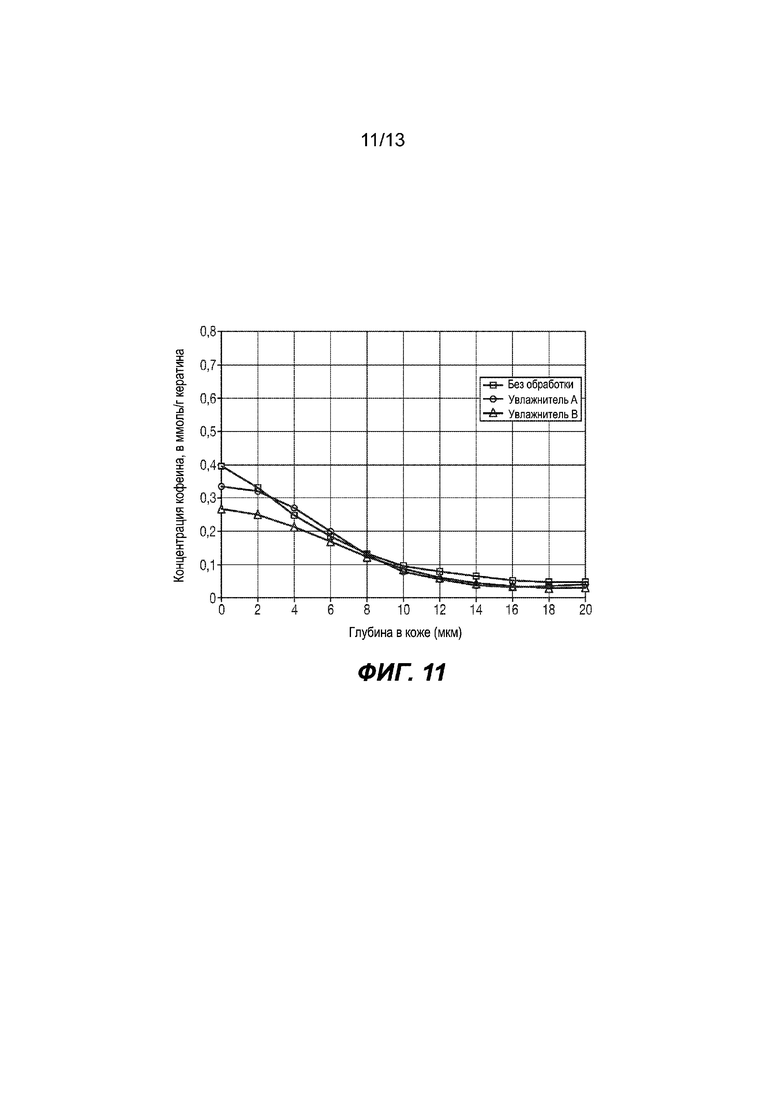
На Фиг. 11 изображены экспериментальные данные для кожи взрослого человека.
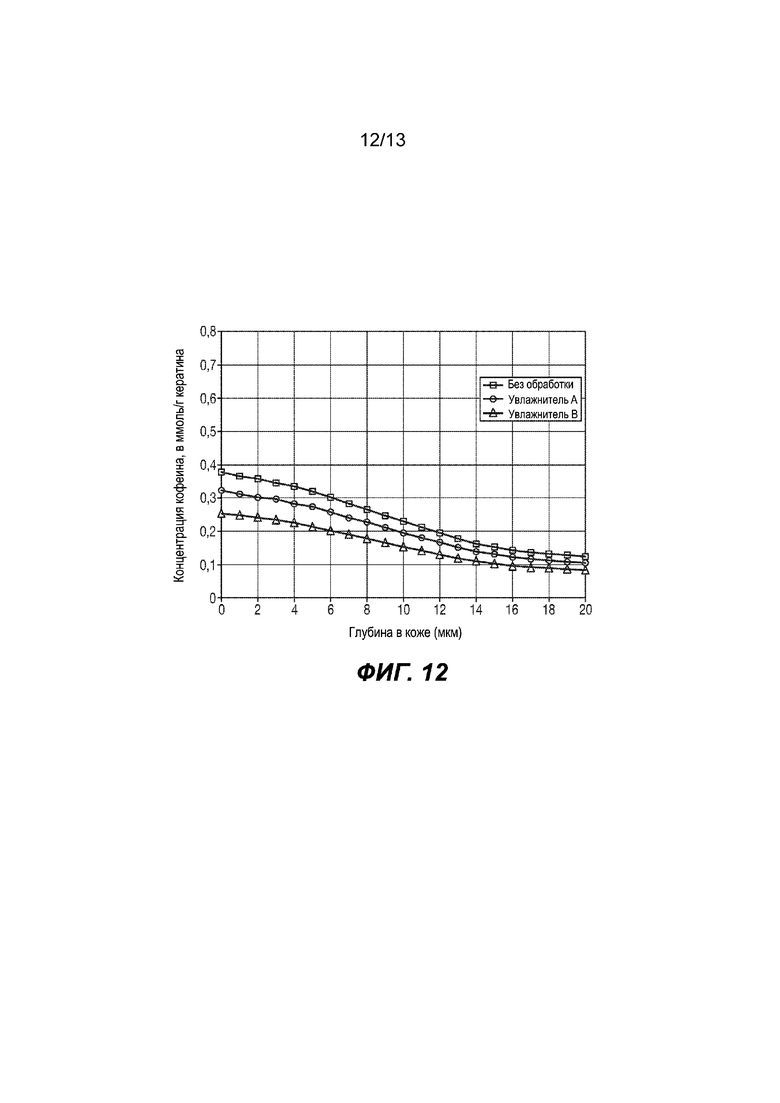
На Фиг. 12 изображено моделирование кожи взрослого человека.
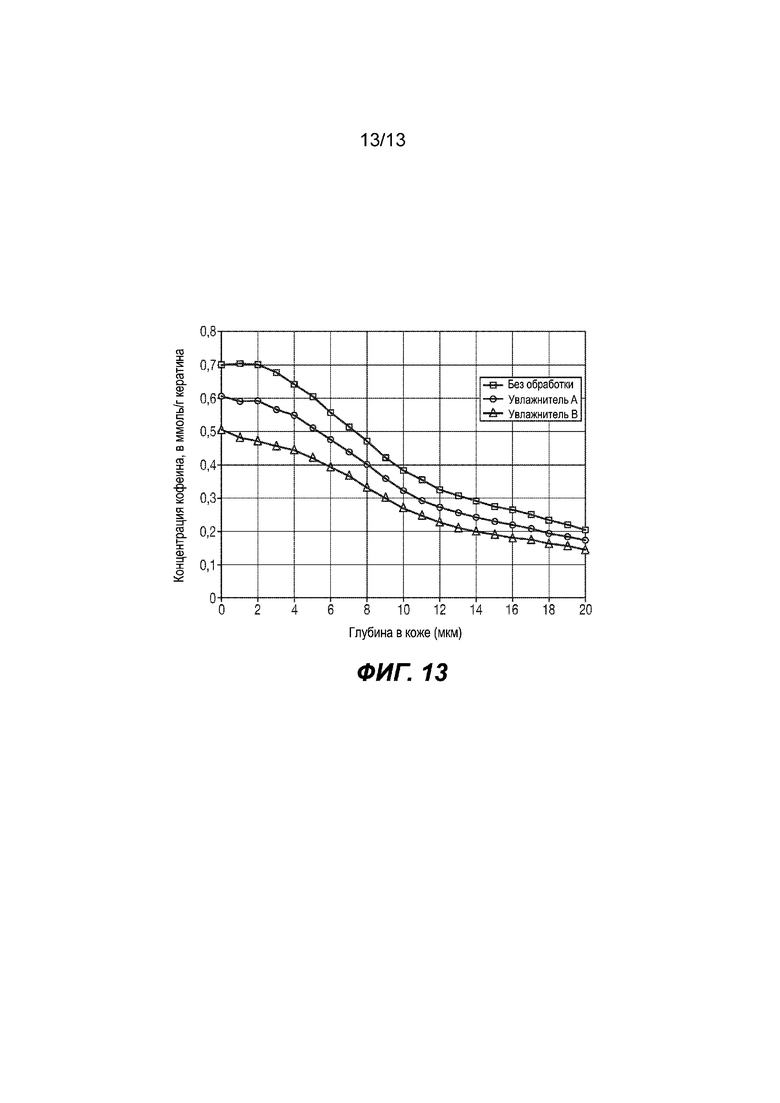
На Фиг. 13 изображены прогнозируемые результаты для кожи младенца.
Подробное описание
Настоящее изобретение относится к способу оценивания мягкости действия продукта для ухода за кожей на кожу младенца и, в частности, воздействию местного нанесения вещества и/или состава на кожный барьер младенцев и получению и/или применению поверхностно-активной системы на основании такой оценки. При использовании в настоящем документе термин «кожа младенца» относится к коже новорожденных детей человека, но также относится к и включает в себя кожу детей в возрасте до 12 месяцев. Термин «ребенок младшего возраста» или «дети младшего возраста» относится к младенцам, но также включает в себя детей в возрасте от 12 до 36 месяцев.
Цель настоящего изобретения заключается в получении возможности оценивать безопасность, мягкость действия и т. п. продукта относительно кожи младенцев и/или детей младшего возраста путем безопасной оценки продукта на коже взрослого человека. Способ включает нанесение вещества на кожу взрослого человека, сбор данных по проникновению маркера на обработанной коже взрослого человека, перенос информации в вычислительную модель кожи взрослого человека, извлечение из этой модели параметров проникновения, перенос параметров в вычислительную модель кожи младенца и визуализацию проникновения маркера в модели кожи младенца с формулировкой выводов о воздействии на кожу младенца продукта для местного нанесения. В конечном итоге способ включает получение в результате такой оценки поверхностно-активной системы и/или применение поверхностно-активной системы на основании результатов такой оценки и итогового получения системы.
В опубликованной заявке на патент США № 20150285787, поданной Laboratoires Expanscience, описан способ выявления по меньшей мере одного биологического маркера для кожи ребенка, который включает: a) измерение уровня экспрессии предполагаемого биологического маркера в по меньшей мере одной пробе (A) клеток кожи, причем указанная проба получена от донора в возрасте менее 16 лет, b) измерение уровня экспрессии указанного предполагаемого биологического маркера в по меньшей мере одной контрольной пробе (B) клеток кожи, c) вычисление соотношения уровня экспрессии на стадии a) и уровня экспрессии на стадии b) и d) определение того, является ли предполагаемый маркер биологическим маркером кожи ребенка.
В WO2015150426 и WO2017103195, выданных Laboratoires Expanscience, описаны способы оценки in vivo составов, которые содержат a) приведение активного агента или состава в контакт с восстановленной моделью кожи, причем указанная модель получена из пробы кожи ребенка; b) приведение восстановленной модели кожи после стадии a) в контакт с мочой; и c) измерение уровня экспрессии по меньшей мере одного из установленных биологических маркеров в модели кожи после стадии b).
В опубликованной заявке на патент США № 20180185255, поданной Procter & Gamble, описан способ скрининга очищающих средств по мягкости действия, включающий: a) измерение уровня одного или более церамидов на области кожи перед нанесением очищающего средства; b) нанесение очищающего средства на область кожи в течение по меньшей мере 7 дней; c) измерение уровня одного или более церамидов после нанесения продукта на область кожи в течение по меньшей мере 7 дней; причем очищающее средство является мягким, если уровень одного или более церамидов составляет по меньшей мере 10% по сравнению с не проходившим обработку контролем.
В патенте США № 10,036,741, выданном Procter & Gamble, описан способ оценки воздействия пертурбагена на гомеостаз кожи и составления содержащей пертурбаген композиции для ухода за кожей, включающий инициирование запроса процессором компьютера архитектуры данных сохраненных образцов кожи, связанных с пертурбагеном, с сигнатурой экспрессии генов для нездоровой кожи, причем запрос содержит сравнение сигнатуры экспрессии генов для нездоровой кожи для каждого сохраненного образца кожи и присвоение каждому образцу индекса связности.
В EP 1248830A1, выданном Procter & Gamble, описано применение теста с контролируемым нанесением на предплечье для оценки мягкости действия поверхностно-активного вещества.
В Saadatmand et al., Skin hydration analysis by experiment and computer simulations and its implications for diapered skin, Skin Res. Technol., 2017: 1-14 описана модель обратимой гидратации рогового слоя эпидермиса, которая моделирует потерю воды на испарение и толщину рогового слоя эпидермиса в зависимости от возможных сценариев воздействия, таких как зависящая от времени относительная влажность, температура воздуха, температура кожи и скорость ветра.
В Maxwell et al., Application of a systems biology approach for skin allergy risk assessment, Proc. 6th World Congress on Alternatives & Animal Use in Life Sciences, pp. 381-388 (2007) описана модель in silico индуцирования сенсибилизации кожи для составления характеристики и количественного описания вклада каждого пути в общий биологический процесс.
В Strube et al., The flex wash test: a method for evaluating the mildness of personal washing products, J. Soc. Cosmet. Chem., 40:297-306 (1989) описано применение промывки локтевого сгиба в течение шестидесяти секунд трижды в день для оценки потенциальной раздражающей способности продуктов для промывки.
В Keswick et al., Comparison of exaggerated and normal use techniques for accessing the mildness of personal cleansers, J. Soc. Cosmet. Chem., 43:187-193 (1992) описано сравнение теста на предплечье и теста с промывкой локтевого сгиба с применением в домашних условиях с целью определить, насколько хорошо тесты имитируют применение в быту.
В Frosch et al., Journal of the American Academy of Dermatology, Volume 1, Issue 1, 35-41 (1979) описан тест в камере для оценки раздражающего действия мыл, который предполагает воздействие в течение пяти рабочих дней недели 8-процентными растворами с записью данных об отшелушивании и покраснении.
Многие тесты in vivo неприемлемы для экспериментального применения на коже младенца. Перечисленные выше ссылки не описывают и не предлагают оценку кожи взрослого человека и применение вычислительных моделей для установления корреляции с тем, как некоторый ингредиент может воздействовать на кожу младенца. Таким образом, изобретение не требует проведения теста in vivo на коже младенца.
Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют общепринятое значение, понятное любому специалисту в области, к которой относится изобретение. Кроме того, все публикации, заявки на патенты, патенты и другие упоминаемые в настоящем документе литературные источники включены в настоящий документ в полном объеме путем ссылки. В настоящем документе все процентные значения представляют собой массовое процентное содержание, если не указано иное. Кроме того, все указанные в настоящем документе диапазоны предполагают включение любых комбинаций значений между двумя конечными значениями включительно.
В настоящем изобретении способ можно применять для различения разных составов очищающих средств в соответствии с их воздействием на устойчивость кожного барьера к внешним проникновениям. В настоящем изобретении изложен способ анализа состава, который позволяет объективно оценить воздействие местных очищающих средств на устойчивость кожного барьера к проникновению агрессивных внешних агентов, и который можно применять для оценки мягкости действия очищающего средства. Результаты этого анализа можно использовать для обеспечения или получения приемлемого состава, который будет считаться имеющим мягкое действие на кожу младенца и/или подростка.
Настоящее изобретение направлено на создание прогнозирующего способа оценивания мягкости действия вещества для местного нанесения в отношении кожи пациента, предпочтительно маленького ребенка. Оно также относится к прогнозирующему способу оценки проникновения соединения (маркера) через кожу младенцев. Настоящее изобретение также относится к прогнозирующему способу оценивания воздействия вещества для местного нанесения на проникновение соединения (маркера) через кожу младенца. Кроме того, настоящее изобретение может обеспечивать способ измерения и/или прогнозирования эффекта усиления барьера вещества (веществ) для местного нанесения.
В одном аспекте настоящее изобретение может включать в себя определенное число стадий способа. Он может включать фазу 1 (in vivo) и фазу 2 (in silico), с необязательной фазой 3 (интеллектуальный процесс), и в конечном итоге способ завершается приготовлением приемлемой поверхностно-активной системы, которая по результатам анализов проходит упомянутые выше тесты, или способ завершается нанесением поверхностно-активной системы на кожу младенца и/или ребенка младшего возраста.
Фаза I, in vivo
A. Нанесение вещества для местного нанесения на кожу взрослого человека, например, путем прямого нанесения или нанесения на пластыре или иной системе доставки.
B. Местное нанесение маркера на кожу взрослого человека и сбор данных по проникновению указанного маркера на обработанной веществом коже взрослого человека. Данная стадия включает нанесение маркера и впоследствии прослеживание его профиля концентрации в коже, например, с использованием конфокальной микроспектроскопии комбинационного рассеяния (CRM).
Фаза II, in silico
C. Перенос информации (данных по проникновению) в вычислительную модель кожи взрослого человека и извлечение из этой модели параметров проникновения.
Эту стадию также можно описать как применение вычислительной модели кожи взрослого человека для визуализации проникновения маркера путем оптимизации параметров проникновения (например, локальной поверхностной концентрации и коэффициентов проницаемости) таким образом, чтобы модельные профили проникновения соответствовали экспериментальным данным.
D. Перенос полученных параметров проникновения (после соответствующих преобразований) в вычислительную модель кожи младенца и визуализация проникновения маркера в модели кожи младенца.
Необязательная фаза III, интеллектуальный процесс
E. Формулировка выводов о мягкости действия (воздействии) продукта для местного на нанесения на кожу младенца на основании количества маркера, которое проникло через модель кожи младенца.
После завершения приведенных выше стадий способа и формулировки выводов на стадии E поверхностно-активную систему можно получать, наносить или распространять пользователям.
Вещество для местного нанесения
Изобретение включает в себя одно или более веществ для местного нанесения для оценки, причем вещество для местного нанесения рассматривается для применения в конечной поверхностно-активной системе. Вещество для местного нанесения представляет собой наносимое на кожу вещество любого типа, которое оказывает воздействие на проницаемость рогового слоя эпидермиса. Вещество для местного нанесения модифицирует проникновение маркера через кожу. Воздействие вещества для местного нанесения можно оценить путем измерения проникновения маркера. Как правило, в описанных выше тестах веществом для местного нанесения пропитывают пластырь, который затем удерживают в контакте с кожей в течение 30 минут, после чего наносят маркер. Пластырь для аппликационного тестирования может включать в себя одно или более веществ для местного нанесения.
В рамках настоящего изобретения можно оценивать различные типы веществ для местного нанесения, например вещество для местного нанесения может представлять собой агрессивное (-ые) вещество (-а), которое (-ые) может (могут) снижать защитные свойства кожи и повышать проникновение маркера. В этом случае настоящее изобретение может позволять создавать классификацию вещества (веществ) по мягкости действия и помогать выбирать при разработке новой композиции продукта по уходу за кожей более мягкий вариант, не проводя тестирования in vivo или in vitro. В других аспектах вещество для местного нанесения может включать в себя защитное вещество (-а), которое (-ые) выполнено (-ы) с возможностью помощи в защите кожи и повышения ее защитных свойств, тем самым снижая проникновение маркера через кожу. Как отмечено выше, настоящее изобретение может помогать в выборе наиболее эффективного решения без необходимости проведения тестов in vitro или in vivo на коже младенца.
Маркер
В настоящем изобретении в способе оценки используют один или более маркеров или биомаркеров. Любой тип маркера является приемлемым, если существует способ отслеживать маркер и генерировать его профиль концентрации (например, данные по проникновению). В примере с использованием конфокальной микроспектроскопии комбинационного рассеяния маркер должен иметь прослеживаемый сигнал в спектре комбинационного рассеяния. В другом примере возможно прослеживание флуоресцентного маркера с использованием конфокальной флуоресцентной микроскопии. Кинетика проникновения маркера предпочтительно должна быть такой, чтобы равновесное состояние его профиля концентрации достигалось за разумное время (например, за время до одного часа).
Маркер может быть гидрофильным, липофильным или амфотерным, что будет определять тип защитного эффекта, который будет исследовать проводящий оценку специалист. Например, одним приемлемым маркером является кофеин. В случае с кофеином при анализе изучают защитные свойства к гидрофильным веществам.
Маркер в соответствии с настоящим изобретением может включать в себя любую молекулу, которая токсикологически и дерматологически безопасна, имеет разумную кинетику проникновения и может быть прослежена с помощью методик конфокального анализа.
- Безопасность. Некоторые использовавшиеся в прошлом маркеры неприемлемы по токсикологическим причинам (применение дансил хлорида (предложенного в Paye et al. «Dansyl chloride labelling of stratum corneum: its rapid extraction from skin can predict skin irritation due to surfactants and cleansing products» Contact Dermatitis 30(2), 91-96, 1994) было прекращено в силу риска сенсибилизации и повреждения кожи при контакте с кожей).
- Кинетика проникновения. Молекула, которая проникает через кожу, например делает это достаточно быстро, но не слишком быстро. Например, можно использовать молекулу, имеющую коэффициент проницаемости близкий к кофеину: kp=1,16 × 10-4 см/ч, как сообщается в Dias M et al. «Topical delivery of caffeine from some commercial formulations» Int J Pharm 1999182(1):41-7.
- Методики конфокального анализа неинвазивны и обеспечивают получение данных о глубине проникновения маркеров. Напротив, например, соскоб липкой лентой является инвазивным и разрушает барьер; в настоящем изобретении это недопустимо.
Данные по проникновению
В настоящем изобретении проводится анализ данных по проникновению. Данные по проникновению представляют собой профиль концентрации; это означает концентрацию маркера в зависимости от глубины в коже. В настоящем изобретении можно использовать любой желаемый способ анализа, приемлемый для измерения профиля концентрации маркера в зависимости от глубины в коже, а более точно - в эпидермисе и, в частности, в роговом слое эпидермиса. Возможно использование любых желаемых способов, но предпочтительными являются неинвазивные способы. Конфокальные методики предпочтительны, поскольку они неинвазивны и обеспечивают достаточное разрешение, например разрешение от 3 до 5 мкм в перпендикулярном к поверхности кожи направлении на глубине до 200 мкм. Один такой способ включает конфокальную микроспектроскопию комбинационного рассеяния, но возможно использование и других способов, включая конфокальную флуоресцентную микроскопию.
Вычислительная модель кожи взрослого человека/кожи младенца
В настоящем изобретении для оценки компонентов тестируемой поверхностно-активной системы используют вычислительные модели. Можно применять любую модель, которая может построить профиль концентрации маркера в коже. Пользователь может выбрать любой тип вычислительной модели проникновения через кожу, которая по заданным параметрам проникновения может построить профиль концентрации маркера в коже. Одновременное использование и модели кожи взрослого человека, и модели кожи требует от моделей учета структуры кожной архитектуры и различий, существующих между двумя типами кожи.
Например, можно использовать физиологическую модель, опубликованную в Sutterlin et al., «A 3D self-organizing multicellular epidermis model of barrier formation and hydration with realistic cell morphology based on EPISIM», Scientific Reports, volume 7, article 43472, 2017; с модификациями для интегрирования диффузии веществ (например, маркера) через слои кожи. В Sutterlin et al. описана клеточная поведенческая модель (CBM), охватывающая регуляторные циклы обратной связи между эпидермальным барьером, потерей воды в окружающую среду и протеканием кальция внутри ткани. Платформа EPISIM состоит из двух готовых к использованию программных инструментов: (i) EPISIM Modellar (система графического моделирования) и (ii) EPISIM Simulator (среда моделирования на основе агентов). Каждая модель на основе EPISIM выполнена из по меньшей мере клеточной поведенческой модели и биомеханической модели (CBM и BM). BM покрывает все пространственные и биофизические свойства клетки. CBM представляют собой принимаемые клетками решения. В соответствии с изобретением можно использовать двухмерную или трехмерную версию модели (вариант двухмерной модели, но без компонента рогового слоя эпидермиса, описан в: Suetterlin et al. «Modeling multi-cellular behavior in epidermal tissue homeostasis via finite state machines in multi-agent systems», Bioinformatics, 25(16), 2057-2063, 2009.
В одном способе процесс запускает пользователь, позволяя моделированию достичь равновесного состояния, соответствующего гомеостазу эпидермиса. Впоследствии в заданный момент времени, соответствующий местному нанесению маркера, проводящий оценку специалист вводит задаваемую пользователем переменную, соответствующую концентрации маркера на поверхности кожи (Cповерхность). Величину этого параметра определяют из полученного экспериментально профиля концентрации, и она соответствует концентрации маркера на глубине 0 (поверхность кожи). В модель вводят клеточную переменную, определяющую концентрацию маркера в клетке (Cклетка). В каждый момент времени этот параметр корректируется на основании закона диффузии Фика, по мере того как маркеру позволяют диффундировать от каждой клетки к ее непосредственным соседям. Для применения закона Фика, в модель вводят параметр коэффициента проницаемости (P). Данный параметр коэффициента проницаемости по существу соответствует коэффициенту диффузии, сопротивлению диффузии из-за коэффициента распределения и сопротивление диффузии из-за длины пути, который вещество должно пройти для перехода из одной клетки в другую. Коэффициент проницаемости различается для рогового слоя эпидермиса (PРС) и живого эпидермиса (PЖЭ). Если вещество достигает нижней части эпидермиса, ему позволяют диффундировать в дермальный компартмент, который моделируют как «сток» для проникновения.
Эти модификации вводят и в модель кожи взрослого человека, и в модель кожи младенца.
Модель кожи младенца создают путем изменения параметров модели кожи взрослого человека для отражения более высокой скорости обновления (пролиферации и шелушения) детской кожи.
Параметры проникновения
Параметры проникновения характеризуют кинетику проникновения, т. е. насколько легко веществу проходить через поверхность и проникать вглубь кожи. В этой роли могут выступать, например, коэффициент распределения, коэффициент диффузии и/или коэффициент проницаемости.
Индекс мягкости действия
Профиль концентрации маркера в модели кожи взрослого человека в равновесном состоянии сравнивают с экспериментальным профилем концентрации. Если профили не согласуются, корректируют параметры проникновения (Cповерхность, PРС и PЖЭ) и моделирование повторяют. Впоследствии после согласования двух профилей параметры используют для вычисления соответствующих параметров для проникновения маркера в модели кожи младенца. В силу более высокой гидрофильности детской кожи параметр Cповерхность оказывается выше (как правило вдвое выше, чем для кожи взрослого человека*), а остальные параметры проникновения остаются теми же в обеих моделях.
*См., например, Nikolovski et al., Barrier function and water-holding and transport properties of infant stratum comeum are different from adult and continue to develop through the first year of life, Journal of Investigative Dermatology (2008), Vol. 128, где использованы такие инструменты, как измерение трансэпидермальной потери воды (ТЭПВ), емкости кожи, абсорбции-десорбции и конфокальная спектроскопия комбинационного рассеяния, чтобы показать, что влагоудерживающие и водотранспортные свойства рогового слоя эпидермиса у младенца отличаются от таких свойств у взрослого. В частности, в работе по ссылке описано наблюдение поглощения экзогенно нанесенной воды с помощью конфокальной микроспектроскопии комбинационного рассеяния через 10 секунд после нанесения воды на кожу нижней передней части руки. На Фиг. 5а (и воспроизведенной на Фиг. 1А) изображено, что на роговой слой эпидермиса у младенцев в возрасте менее 12 месяцев приходится значительная часть поглощения воды. На Фиг. 5b (и воспроизведенной на Фиг. 1В) изображено, что, в отличие от этого, существенного поглощения воды в коже взрослого человека после нанесения воды на кожу не наблюдается. Ожидается, что проникновение кофеина, который является сильно гидрофильным, будет происходить аналогично проникновению воды.
Впоследствии проникновению маркера позволяют достичь равновесного состояния в модели кожи младенца (около 1000 стадий, где каждая стадия соответствует 30 мин физиологического времени). Вычисляют профиль средней концентрации маркера в равновесном состоянии (зависимость средней концентрации от глубины). Для профиля концентрации рассчитывают площадь под кривой (AUC, интеграл) вплоть до заданной глубины (например, до 20 μм).
Затем из величин AUC, соответствующих обработкам разными продуктами, можно определять шкалу индекса мягкости действия. Так получается условная шкала, используемая для классификации мягкости действия веществ для местного нанесения.
Величина индекса мягкости действия позволяет проводящему оценку специалисту сравнивать мягкость действия тестируемого вещества для местного нанесения с мягкостью действия двух эталонных веществ: вода (мягкое) и лаурилсульфат натрия (SLS) 0,1% (агрессивное). С водой и SLS 0,1% в качестве двух базовых точек возможно построить шкалу для измерения мягкости действия других веществ для местного нанесения.
Следует отметить, что данный индикатор мягкости действия необязателен, и мягкости действия можно опустить и напрямую сравнивать относительные мягкости действия различных веществ для местного нанесения непосредственно друг с другом на основании объединения их кривых прогнозируемого проникновения (например, рассчитанных величин AUC).
Примеры
1- Сравнение эксперимента (взрослый), модели (взрослый) и прогноза (ребенок). См. Фиг. 2.
Цели
Продемонстрировать прогнозируемое воздействие на кожу младенца двух растворов для местного нанесения предельной концентрации, одного агрессивного (содержащего 0,1% SLS) и одного мягкого (вода).
Продемонстрировать, что модель для взрослого человека соответствует экспериментальным данным.
Продемонстрировать, что вещества для местного нанесения не оказывают одинаковое воздействие на кожу взрослого человека и на кожу младенца, и кожа младенца более проницаема для маркера.
Сравнение эксперимента, модели и прогноза для воздействия воды и SLS на кожу взрослого человека и кожу младенца См. Фиг. 3.
На Фиг. 3 выше изображена глубина проникновения (в мкм) кофеина (маркер), выраженная в ммоль на грамм кератина, полученные в эксперименте in vivo на коже взрослого человека (линии+и ○) и в прогнозирующей модели in silico (линии ∆, ×, ◊ и □).
На Фиг. 3 изображено воздействие на проникновение кофеина 2 растворов для местного нанесения: воды и 0,1% SLS. Рассчитанные в модели данные для взрослого представлены линиями ∆ и ◊; для воды и SLS соответственно. Прогнозируемые данные для младенца представлены линиями × и □ для воды и SLS соответственно.
Экспериментальные данные in vivo, собранные для кожи взрослого человека, впоследствии переносят в вычислительную модель кожи взрослого человека для моделирования глубины проникновения кофеина в кожу взрослого человека. Прогноз проникновения кофеина в кожу младенца, даваемый моделью настоящего изобретения, представлен линией с косыми крестиками (×) для случая, когда кожу перед нанесением кофеина обрабатывают пластырем с водой, и линией с квадратами (□) для случая, когда кожу перед нанесением кофеина обрабатывают пластырем с 0,1% SLS.
Площадь под кривой в диапазоне глубины кожи от 0 до 20 мкм указывает уровень мягкости действия вещества для местного нанесения. Чем она меньше, тем мягче действие вещества на кожу. Площадь под кривой - ключевой параметр, позволяющий сравнивать между собой различные обработки.
2- Сравнение нескольких поверхностно-активных составов. См. Фиг. 4.
Цель
Создать прогнозирующую классификацию поверхностно-активных составов на основе их мягкости действия на кожу младенца.
Стадия 2.1. Экспериментальные данные, проникновение кофеина в кожу взрослого человека, in vivo
Исследуемые составы изображены на Фиг. 4.
Экспериментальный протокол соответствует описанному в Stamatas et al., Development of a non-invasive optical method for assessment of skin barrier to external penetration, Biomedical Optics and 3D Imaging OSA (2012) для материала и способа. В работе Stamatas et al. описано применение характерного спектра комбинационного рассеяния кофеина для прослеживания проникновения кофеина через кожу взрослого человека с целью продемонстрировать воздействие (1) лаурилсульфата натрия и (2) защитного крема на защитную функцию рогового слоя эпидермиса.
Стадия 2.2. Моделирование экспериментальных данных в модели эпидермиса взрослого человека in silico. См. Фиг. 5.
Экспериментальные данные по проникновению кофеина, полученные на стадии 2.1, переносят в вычислительную модель кожи взрослого человека. Для каждого вещества для местного нанесения проводят моделирования проникновения в кожу; одного моделирования на вещество может быть достаточно. Извлекают параметры проникновения кофеина (локальная концентрация на поверхности и коэффициенты проницаемости).
Стадия 2.3. Кривые прогнозируемого проникновения кофеина после обработки поверхностно-активными веществами. См. Фиг. 6.
Параметры проникновения кофеина, полученные из модели кожи взрослого человека на стадии 2.2, переносят в вычислительную модель кожи младенца. Для каждого вещества для местного нанесения проводят моделирование проникновения в кожу младенца. Извлекают результаты прогнозируемого проникновения кофеина и строят по ним график, как показано на представленном выше графике 4.
Стадия 2.4. Прогнозируемое поглощенное количество в роговом слое эпидермиса у ребенка, площадь под кривой в диапазоне глубины 0-10 мкм (ммоль кофеина/г кератина). См. Фиг. 7.
Прогнозирующие кривые для каждого агента для местного нанесения, представленные на Фиг. 6 стадии 2.3, интегрируют с получением для каждого агента для местного нанесения прогнозируемого поглощенного количества кофеина в роговом слое эпидермиса у младенца. Эти значения отражены на Фиг. 7.
Иными словами, данная прогнозирующая схема показывает, сколько кофеина проникнет в первые 10 мкм (не мм) рогового слоя эпидермиса. Чем большее количество кофеина имеется, тем более данное агрессивно вещество для местного нанесения.
Результаты
Было неожиданно обнаружено, что по данной схеме можно сделать прогноз, что агент для местного нанесения не всегда будет иметь значение индекса мягкости действия на кожу младенца, отраженное в экспериментальных значениях, полученных для кожи взрослого человека:
Состав 3 будет иметь более мягкое действие, чем состав 5.
Состав 4 будет иметь более мягкое действие, чем состав 2.
В результате данного эксперимента композицию, включающую в себя состав из составов 3 и/или 4, можно получать и наносить на кожу младенца и/или кожу ребенка младшего возраста как более предпочтительную по сравнению с составом из составов 5 и 2 соответственно.
В следующем варианте осуществления изобретение относится к разработке защитных систем, в частности для младенцев или детей младшего возраста, при этом уровень защитного эффекта оценивают посредством анализа результатов тестов на коже взрослого человека.
Изобретение позволяет оценивать уровень защиты защитной системы на основании объективных данных, не прибегая при этом к проведению тестов на детях младшего возраста или младенцах.
Способ
Описанные выше стадии I и II остаются без изменений. Генерируют прогнозирующие данные по проникновению маркера в кожу младенца.
Стадия III отличается тем , что данные теперь относятся к применению низкой проницаемости и диффузии маркера через кожу для составления прогноза защитного эффекта, который вещество для местного нанесения, наносимое на стадии I A, оказало бы на кожу младенца или маленького ребенка.
Эту методологию можно использовать для оценки продуктов, не требующих смывания (например, кремов/увлажнителей)
Эксперименты
Пример 3
Материал и способ
Данные по коже взрослого человека получали на здоровых добровольцах, с нормальной кожей, которые согласились не применять никаких других средств по уходу за кожей на предплечьях в течение по меньшей мере 24 часов до начала исследования и в ходе исследования.
Использованные инструменты.
In vivo конфокальный микроспектрометр комбинационного рассеяния (Skin Composition Analyzer Model 3510, River Diagnostics, Роттердам, Нидерланды)
Пластырь с кофеином: 180 мг кофеина в 10 мл деминерализованной воды, 1,8%.
Пример 4. Моделирование защитного крема
Экспериментальные данные получали на 5 женщинах-добровольцах в возрасте от 20 до 35 лет.
Тестируемые вещества для местного нанесения.
Защитный крем: Desitin® Creamy (крем от опрелости под подгузник)
Перечень наименований по Международной номенклатура косметических ингредиентов (США): оксид цинка 10%, неактивные компоненты (сок листьев алоэ-вера), циклометикон, диметикон, ароматизатор, метилпарабен, микрокристаллический воск, минеральное масло, пропилпарабен, очищенная вода, борат натрия, сорбитансесквиолеат, витамин E, белый вазелин, белый воск.
Протокол
1 - Акклиматизация в течение 5 минут в помещении с контролируемыми температурой и влажностью
2 - Нанесение вещества для местного нанесения на предплечье
3 - Акклиматизация в течение 30 минут в помещении с контролируемыми температурой и влажностью
4 - Наложение пластыря с кофеином на предплечье (в то же место) на 30 минут
5 - Измерение в характерной области спектра комбинационного рассеяния
Результаты
1- Экспериментальные данные по коже взрослого человека. См. Фиг. 8.
Данные по обработанной кремом Desitin коже (квадраты) сравнивают с данными по не проходившей обработку коже (т. е. коже, на которую на стадии 2 протокола не наносили вещество для местного нанесения) (круги).
Из экспериментальных результатов извлекают данные по проникновению и переносят их в вычислительную модель кожи взрослого человека.
2- Построение модели кожи взрослого человека. См. Фиг. 9.
Следующая стадия - определение параметров проницаемости кожи на вычислительной модели кожи взрослого человека таким образом, чтобы она могла точно моделировать представленные выше экспериментальные данные.
Эти параметры рассчитывают из наклона профиля проникновения кофеина.
Полученные из модели кожи взрослого человека результаты показаны ниже.
Обработанную защитным кремом кожу (квадраты) сравнивают с не проходившей обработку кожей (круги).
Из вычислительной модели кожи взрослого человека извлекают параметры проникновения.
3- Прогнозируемые результаты для кожи младенца. См. Фиг. 10.
Последняя стадия включает перенос параметров проникновения кофеина с соответствующими преобразованиями в вычислительную модель кожи младенца для моделирования прогнозируемого проникновения кофеина в кожу младенца.
Прогнозируемые результаты для проникновения кофеина на обработанной защитным кремом коже (квадраты) и не проходившей обработку коже (круги) показаны ниже
Наконец, из показанного ниже отношения, в которое входят площадь под кривой (AUC) для необработанной кожи и AUC для обработанной защитным кремом кожи, можно рассчитывать прогнозируемый процент защиты для защитного крема:
% защиты=100 × (AUC (необработанной) - AUC (обработанной)) / AUC (необработанной)=89,18%
Примеры 5 Моделирование увлажнителя
Экспериментальные данные получали на 6 добровольцах в возрасте от 18 до 40 лет.
Тестируемые вещества для местного нанесения.
- Увлажнитель A: эмульсия, содержащая: глицерин (12%), вазелин (4%), дистеарилдимония хлорид, воду
- Увлажнитель B: структурированная эмульсия, содержащая: вазелин (40%), глицерин (12%), дистеарилдимония хлорид, воду
Протокол
1- Акклиматизация в течение 5 минут в помещении с контролируемыми температурой/влажностью
2- Нанесение вещества для местного нанесения на предплечье на 30 минут
3- Наложение пластыря с кофеином на предплечье (в то же место) на 30 минут
4- Измерение в характерной области спектра
Результаты
1- Экспериментальные данные по коже взрослого человека
Данные по обработанной увлажнителем A коже (квадраты) сравнивают с данными по обработанной увлажнителем B коже (треугольники) и не проходившей обработку коже (т. е. коже, на которую на стадии 2 протокола не наносили вещество для местного нанесения) (круги).
Из экспериментальных результатов извлекают данные по проникновению и переносят их в вычислительную модель кожи взрослого человека.
2- Построение модели кожи взрослого человека. См. Фиг. 12.
Следующая стадия - определение параметров проницаемости кожи на вычислительной модели кожи взрослого человека таким образом, чтобы она могла точно моделировать представленные выше экспериментальные данные.
Эти параметры рассчитывают из наклона профиля проникновения кофеина.
Полученные из модели кожи взрослого человека результаты показаны ниже.
Обработанную увлажнителем A кожу (квадраты) сравнивают с обработанной увлажнителем B кожей (треугольники) и не проходившей обработку кожей (круги).
Из вычислительной модели кожи взрослого человека извлекают параметры проникновения.
3- Прогнозируемые результаты для кожи младенца
Последняя стадия включает перенос параметров проникновения кофеина с соответствующими преобразованиями в вычислительную модель кожи младенца для моделирования прогнозируемого проникновения кофеина в кожу младенца.
Прогнозируемые результаты для проникновения кофеина на обработанной увлажнителем A коже (квадраты), обработанной увлажнителем B коже (треугольники) и не проходившей обработку коже (круги) изображены на Фиг. 13.
Наконец, из показанного ниже отношения, в которое входят площадь под кривой (AUC) для необработанной кожи и AUC для обработанной увлажнителем кожи, можно рассчитывать прогнозируемый процент защиты для увлажнителя.
Для увлажнителя А
% защиты: Не применимо.
Для увлажнителя А площадь под кривой оказалась больше площади под кривой для необработанного эталона. Моделирование прогнозирует отсутствие защитного действия для кожи младенца.
Для увлажнителя B
% защиты=100 × (AUC (необработанной) - AUC (обработанной)) / AUC (необработанной)=17,72%.
Модель острого воспаления кожи
Модель проникновения вещества использовали для получения надежной модели острого воспаления кожи.
Модель может быть использована для оценки реакции кожи на местные внешние раздражители. Необходимым поведением модели является то, что нанесение и проникновение раздражителя в кожу могут вызвать продуцирование воспалительных молекул. Затем, если кератиноциты больше не контактируют с раздражителем, система вернется к гомеостазу.
Воспалительные молекулы продуцируются и разлагаются кератиноцитами. Воспалительная реакция начинается, когда раздражитель пересекает барьер, образованный SC. Затем, когда кажущаяся концентрация раздражителя в клетке достигает определенного значения, называемого пороговым значением раздражения, кератиноциты начинают продуцировать воспалительные молекулы [IM] в соответствии со следующим уравнением:
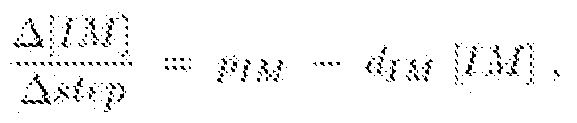
где pIM и dIM представляют собой скорость продуцирования и разложения воспалительных молекул в кератиноцитах.
Когда кажущаяся концентрация вещества ниже порога раздражения, воспалительные молекулы больше не продуцируются (pIM=0), но продолжают разлагаться. На каждом этапе клетки диффундируют свои воспалительные молекулы к соседним клеткам в соответствии со следующим уравнением:
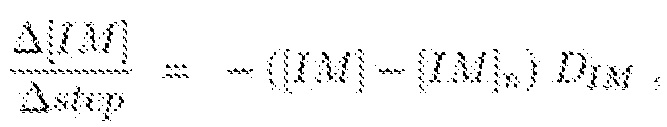
где нижний индекс n относится к соседним клеткам, а DIM представляет собой коэффициент диффузии воспалительных молекул.
Наконец, воспалительные клетки теряются в дерме в базальном уровне в соотвтетствии с
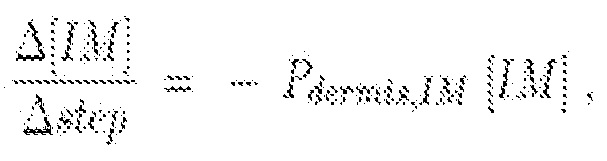
где Pdermis;IM [IM] соответствует проницаемости дермы для раздражителя.
Данные из литературы использовали для оценки различных частей модели в соответствии с приведенными ниже критериями.
раздражающее вещество наносили местно;
исследование проводили in vivo на людях;
воспаление измеряли количественно (размер эритемы или покраснение, кровоток и т.д.);
тестировали несколько концентраций раздражителя;
раздражитель не влияет на нормальную функцию кожного барьера (наблюдается лишь незначительное изменение трансэпидермальной потери воды, ТЭПВ).
Andersen et al. изучали раздражение кожи с использованием отражающей спектроскопии [14]. Они исследовали кожную реакцию восьми добровольцев в отношении четырех соединений: лаурилсульфат натрия (SLS), соляной кислоты (HCl), нонановой кислоты (NON) и имипрамина (IMI). Они измеряли уровень оксигенированного и дезоксигенизированного гемоглобина с помощью отражающей спектроскопии, кровоток с помощью лазерной доплеровской проточной цитометрии и ТЭПВ с помощью испарителя. Для каждого соединения четыре концентрации тестировали с помощью пластырей в течение 24 часов. Авторы изобретения обращали внимание на два соединения, которые повышали наименьшее значение ТЭПВ: имипрамин и нонановую кислоту. Оксигенированный гемоглобин оказался эффективным показателем воспаления и демонстрировал дозозависимые кривые. Данные для этих молекул не подтверждали нашу модель.
Авторы изобретения решили исследовать больше липофильных соединений, поскольку как нонановая кислота, так и имипрамин являются липофильными. В их распоряжении находились данные по проникновению чистых масел в SC из исследования, опубликованного в 2008 [18]. Концентрации парафина и вазелина при нескольких глубинах в SC измеряли с помощью рамановской спектроскопии. В литературе авторы изобретения обнаружили значения Kp для парафина и вазелина [19]:
Kp(парафин)=13:3 (см=h)
Kp(вазелин)=2:02 103 (см=h)
Для обоих этих соединений авторы изобретения смогли получить эффективные аппроксимации клинических данных с помощью модельных расчетов.
Воспаление, демонстрируемое моделью, является дозозависимым. Кроме того, авторы изобретения продемонстрировали, что в зависимости от значений параметров, полученных на основе физических свойств молекул (PSC (проницаемость рогового слоя) и PVE (проницаемость жизнеспособного эпидермиса), модель демонстрирует воспаление с различными интенсивностями. Наконец, авторы изобретения продемонстрировали, что модель воспаления является полностью функциональной в условиях модели кожи взрослого человека и ребенка, и даже получили представление о роли того, что структура кожи может иметь значение в динамике воспаления.
Следует понимать, что хотя различные аспекты настоящего описания были проиллюстрированы и описаны с помощью примеров, заявляемое в настоящем документе изобретение ими не ограничивается, но может быть реализовано иными различными способами в соответствии с объемом формулы изобретения, включенной в настоящую и/или любую родственную настоящей заявку на патент.
[1] Recognizing neglected tropical diseases through changes on the skin: a training guide for front-line health workers," World Health Organization, Geneva, Tech. Rep., 2018. [Online]. Доступно: http://www.who.int/neglected diseases/en.
[2] US Food and Drug Administration, Advancing Regulatory Science," Regulatory Science Strategic Plan, 2011.
[3] L. B. Edelman, J. A. Eddy, and N. D. Price, In silico models of cancer," 2010.
[4] Y. Yamamoto, P. A. Valitalo, D. R. Huntjens, J. H. Proost, A. Vermeulen, W. Krauwinkel, M. W. Beukers, D. J. Van Den Berg, R. Hartman, Y. C. Wong, M. Danhof, J. G. Van Hasselt, and E. C. De Lange, Predicting drug concentration-time profiles in multiple CNS compartments using a comprehensive physiologically-based pharmacokinetic model," CPT: Pharmacometrics and Systems Pharmacology, 2017.
[5] E. Passini, O. J. Britton, H. R. Lu, J. Rohrbacher, A. N. Hermans, D. J. Gallacher, R. J. Greig, A. Bueno-Orovio, and B. Rodriguez, Human in silico drug trials demonstrate higher accuracy than animal models in predicting clinical pro-arrhythmic cardiotoxicity," Frontiers in Physiology, 2017.
[6] T. Suterlin, S. Huber, H. Dickhaus, and N. Grabe, Modeling multi-cellular behavior in epidermal tissue homeostasis via _finite state machines in multi-agent systems," Bioinformatics, 2009.
[7] T. Sutterlin, E. Tsingos, J. Bensaci, G. N. Stamatas, and N. Grabe, A 3D self-organizing multicellular epidermis model of barrier formation and hydration with realistic cell morphology based on EPISIM," Scientific Reports, 2017.
[8] G. N. Stamatas, The Structural and Functional Development of Skin During the First Year of Life: Investigations Using Noninvasive Methods," in Textbook of Aging Skin, 2017, ch. 88, pp. 1141{1153.
[9] G. Stamatas, J. Nikolovski, M. Luedtke, N. Kollias, and B. Wiegand, Infant Skin Microstructure Assessed In Vivo Differs from Adult Skin in Organization and at the Cellular Level," Pediatr Dermatol, 2010.
[10] J. Nikolovski, G. N. Stamatas, N. Kollias, and B. C. Wiegand, Barrier function and water-holding and transport properties of infant stratum corneum are different from adult and continue to develop through the _first year of life," Journal of Investigative Dermatology, 2008.
[11] T. Sutterlin, C. Kolb, H. Dickhaus, D. Jager, and N. Grabe, Bridging the scales: Semantic integration of quantitative SBML in graphical multi-cellular models and simulations with EPISIM and COPASI," Bioinformatics, 2013.
[12] Q. Liu, Y. Zhang, S. G. Danby, M. J. Cork, and G. N. Stamatas, Infant Skin Barrier, Structure, and Enzymatic Activity Differ from Those of Adult in an East Asian Cohort," BioMed Research International, 2018. [Online]. Доступно: https://doi.org/10.1155/2018/1302465.
[13] G. N. Stamatas and E. Boireau-Adamezyk, Development of a Non-Invasive Optical Method for Assessment of Skin Barrier to External Penetration," Biomedical Optics and 3D Imaging, 2012.
[14] P. H. Andersen and H. I. Maibach, Skin irritation in man: a comparative bioengineering study using improved reflectance spectroscopy," Contact Dermatitis, vol. 33, pp. 315{322, 1995.
[15] H. Rothe, C. Obringer, J. Manwaring, C. Avci, W. Wargniez, J. Eilstein, N. Hewitt, R. Cubberley, H. Duplan, D. Lange, C. Jacques-Jamin, M. Klaric, A. Schepky, and S. Gregoire, Comparison of protocols measuring diffusion and partition coefficients in the stratum corneum," Journal of Applied Toxicology, 2017.
[16] P. D. A. Pudney, M. Melot, P. J. Caspers, A. Van Der Pol, and G. J. Puppels, An In Vivo Confocal Raman Study of the Delivery of Trans- Retinol to the Skin," Applied Spectroscopy, vol. 61, 2007.
[17] S. Geinoz, R. H. Guy, B. Testa, and P. A. Carrupt, Quantitative Structure-Permeation Relationships (QSPeRs) to Predict Skin Permeation: A Critical Evaluation," Pharmaceutical Research, 2004.
[18] G. N. Stamatas, J. de Sterke, M. Hauser, O. von Stetten, and A. van der Pol, Lipid uptake and skin occlusion following topical application of oils on adult and infant skin," Journal of Dermatological Science, 2008.
[19] T. Petry, D. Bury, R. Fautz, M. Hauser, B. Huber, A. Markowetz, S. Mishra, K. Rettinger, W. Schuh, and T. Teichert, Review of data on the dermal penetration of mineral oils and waxes used in cosmetic applications," 2017.



Группа изобретений относится к разработке систем для кожного барьера, в частности, для младенцев или детей младшего возраста. Предложен способ оценки способности защитной системы защищать кожу младенца от внешних раздражителей, включающий: a) местное нанесение указанной защитной системы на кожу взрослого человека; b) местное нанесение внешнего раздражителя на указанную обработанную защитной системой кожу взрослого человека; c) наблюдение за продуцированием воспалительных молекул в указанной обработанной защитной системой коже взрослого человека; d) применение вычислительной модели воспаления кожи взрослого человека для визуализации влияния внешнего раздражителя путем оптимизации параметров воспаления таким образом, чтобы модель профилей воспаления кожи взрослого человека соответствовала экспериментальным данным; e) перенос оптимизированных параметров воспаления в вычислительную модель кожи младенца и f) определение влияния раздражителя в вычислительной модели кожи младенца. Также предложена система, представляющая собой крем или увлажнитель, выбранная путем оценки в соответствии со способом. Группа изобретений обеспечивает выбор системы для кожного барьера, приемлемой для младенцев и детей младшего возраста. 2 н. и 3 з.п. ф-лы, 14 ил.
1. Способ оценки способности защитной системы защищать кожу младенца от внешних раздражителей, включающий:
a) местное нанесение указанной защитной системы на кожу взрослого человека;
b) местное нанесение внешнего раздражителя на указанную обработанную защитной системой кожу взрослого человека;
c) наблюдение за продуцированием воспалительных молекул в указанной обработанной защитной системой коже взрослого человека;
d) применение вычислительной модели воспаления кожи взрослого человека для визуализации влияния внешнего раздражителя путем оптимизации параметров воспаления таким образом, чтобы модель профилей воспаления кожи взрослого человека соответствовала экспериментальным данным;
e) перенос оптимизированных параметров воспаления в вычислительную модель кожи младенца; и
f) определение влияния раздражителя в вычислительной модели кожи младенца.
2. Способ по п. 1, в котором раздражитель выбирают из парафина и вазелина.
3. Способ по п. 1, в котором в качестве вычислительной модели проникновения в кожу взрослого человека используют EPISIM.
4. Способ по п. 1, в котором в качестве вычислительной модели воспаления кожи взрослого человека используют модель на основе агентов.
5. Защитная система, представляющая собой крем или увлажнитель, выбранная путем оценки в соответствии со способом по п. 1.
| Hansen, S., et al, In-silico model of skin penetration based on experimentally determined input parameters | |||
| Part I: Experimental determination of partition and diffusion coefficients | |||
| European Journal of Pharmaceutics and Biopharmaceutics, 2008, 68(2), 352-367 | |||
| Лутфуллина Г | |||
| Г | |||
| и др | |||
| Испытания ПАВ на острую токсичность, раздражающее и |
Авторы
Даты
2024-05-14—Публикация
2020-05-28—Подача