Область техники
Настоящее раскрытие имеет отношение к способу скрининга происходящих из стволовых клеток, способствующих регенерации нейрональных клеток, обладающих нейрональной регенеративной активностью, и фармацевтической композиции для предотвращения или лечения неврологического заболевания, содержащей способствующие регенерации нейрональные клетки.
Уровень техники
Мезенхимальные стволовые клетки (MSC) используются для создания целого ряда средств для клеточной терапии, поскольку они дифференцируются в различные типы клеток в ответ на специфическую стимуляцию, не обладают туморогенностью индуцированных стволовых клеток и не имеют отношения к этическим проблемам, связанным с использованием эмбриональных стволовых клеток. Мезенхимальные стволовые клетки являются стволовыми клетками взрослых и в большинстве случаев изолируются из жировой ткани, пуповинной крови, костного мозга и т.п. взрослых людей. Способы изолирования этих тканей связаны с некоторыми проблемами, так как они являются инвазивными, вызывают боль и не могут обеспечить большое количество стволовых клеток.
Раскрытие изобретения
Техническая задача
Авторы настоящего изобретения разработали способ скрининга способствующих регенерации нейрональных клеток, проявляющих нейрональный регенеративный эффект из числа разных клеток, дифференцированных из мезенхимальных стволовых клеток, на основе анализа специфических CD маркеров.
Настоящее изобретение направлено на предоставление способа скрининга происходящих из мезенхимальных стволовых клеток, способствующих регенерации нейрональных клеток, обладающих нейрональной регенеративной активностью.
Настоящее раскрытие также направлено на предоставление нейрональных способствующих регенерации клеток, отобранных при помощи данного способа скрининга.
Настоящее раскрытие также направлено на предоставление фармацевтической композиции, предназначенной для предотвращения или лечения неврологического заболевания и содержащей нейрональные способствующие регенерации клетки в качестве активного ингредиента.
Другие цели и преимущества настоящего изобретения станут более очевидными благодаря последующему подробному описанию, формуле изобретения и чертежам.
Техническое решение
В одном аспекте настоящее раскрытие предоставляет способ скрининга происходящих из мезенхимальных стволовых клеток, способствующих регенерации нейрональных клеток, обладающих нейрональной регенеративной активностью, включающий:
i) стадию подготовки клеток, дифференцированных из мезенхимальных стволовых клеток; и
ii) стадию скрининга клеток, в которых повышен один или более маркеров, выбранных из группы, состоящей из CD121a, CD106 и CD112, из числа дифференцированных клеток стадии i) по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В другом аспекте настоящее изобретение предоставляет способ скрининга происходящих из мезенхимальных стволовых клеток, способствующих регенерации нейрональных клеток, обладающих нейрональной регенеративной активностью, включающий:
i) стадию подготовки клеток, дифференцированных из мезенхимальных стволовых клеток; и
ii) стадию скрининга клеток, в которых понижен один или более маркеров, выбранных из группы, состоящей из CD26 и CD141, из числа дифференцированных клеток стадии i) по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
Авторы настоящего изобретения дифференцировали мезенхимальные стволовые клетки, происходящие из различных источников, и изучили профили экспрессии различных маркеров в разных дифференцированных клетках. В результате было неожиданно установлено, что клетки, дифференцированные в способствующие регенерации нейрональные клетки, демонстрируют общую тенденцию в профиле экспрессии специфических маркеров (например, CD маркеров, таких как CD121a, CD106 и CD112).
В настоящем изобретении термин «способствующая регенерации нейрональная клетка» или «NRPC» относится к клетке, дифференцированной из мезенхимальной стволовой клетки, обладающей эффектом регенерации нейронов (например, действием, способствующим нейрональной регенерации прямо или опосредованно с точки зрения структуры или функции путем миелонизации поврежденных периферических нервов или секреции цитокинов, необходимых для нейрональной регенерации).
Согласно отдельному примеру осуществления настоящего изобретения способ скрининга включает:
i) стадию подготовки клеток, дифференцированных из мезенхимальных стволовых клеток;
ii) стадию скрининга клеток, в которых повышен один или более маркеров, выбранных из группы, состоящей из CD121a, CD106 и CD112, из числа дифференцированных клеток стадии i) по сравнению с мезенхимальными стволовыми клетками до дифференцировки; и
iii) стадию скрининга клеток, в которых понижен один или более маркеров, выбранных из группы, состоящей из CD26 и CD141, из числа дифференцированных клеток стадии i) по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
Согласно отдельному примеру осуществления настоящего изобретения способ скрининга включает:
i) стадию подготовки клеток, дифференцированных из мезенхимальных стволовых клеток;
ii) стадию скрининга клеток, в которых понижен один или более маркеров, выбранных из группы, состоящей из CD26 и CD141, из числа дифференцированных клеток стадии i) по сравнению с мезенхимальными стволовыми клетками до дифференцировки; и
iii) стадию скрининга клеток, в которых повышен один или более маркеров, выбранных из группы, состоящей из CD121a, CD106 и CD112, из числа дифференцированных клеток стадии i) по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В настоящем изобретении термин «стволовая клетка» имеет отношение к клетке, которая может воспроизвести себя и в то же время обладает способностью дифференцироваться в два или более типов клеток. Стволовые клетки включают стволовые клетки взрослого человека, плюрипотентные стволовые клетки, индуцированные плюрипотентные стволовые клетки или эмбриональные стволовые клетки. Конкретнее, они могут быть мезенхимальными стволовыми клетками.
В настоящем изобретении термин «мезенхимальная стволовая клетка» относится к недифференцированной стволовой клетке, изолированной из ткани человека или млекопитающего. Мезенхимальная стоволовая клетка может происходить из различных тканей. В частности, она может происходить из одной или более тканей, выбранных из группы, состоящей из небной миндалины, пуповины, пуповинной крови, костного мозга, жировой ткани, мышцы, нерва, кожи, амниона, хориона, отпадающей плаценты и плаценты. Методики изолирования стволовых клеток из каждой ткани хорошо известны в данной области техники.
Согласно отдельному примеру осуществления настоящего изобретения мезенхимальная стволовая клетка происходит из небной миндалины или жировой ткани.
В примере настоящего изобретения подтверждено, что наиболее предпочтительно использовать мезенхимальные стволовые клетки, происходящие из небной миндалины или жировой ткани.
В настоящем изобретении термин «CD» или «кластер дифференцировки» относится к поверхностной молекулярной структуре, присутствующей на клеточной поверхности. Поскольку некоторые клеточные популяции совместно пользуются одними и теми же CD молекулами, их используют для различения популяции клеток (т.е. в качестве маркеров). Клетки одной и той же линии дифференцировки имеют одинаковые CD молекулы, но даже та же самая клеточная популяция имеет разные CD молекулы в зависимости от стадии дифференцировки или активации. Поэтому их удобно использовать для идентификации клеточного ростка, дифференцировки, активации и т.д. клеток.
В примере настоящего изобретения было подтверждено в результате сравнения профиля экспрессии CD молекул в происходящих из стволовой клетки, нейрональных способствующих регенерации клетках, обладающих нейрональной регенерационной активностью настоящего раскрытия, и в мезенхимальных стволовых клетках, что нейрональные способствующие регенерации клетки согласно настоящему раскрытию отличаются от мезенхимальных стволовых клеток. В настоящем изобретении CD10, CD39, CD106, CD112, CD121a, CD338 и т.д., экспрессия которых является повышенной по сравнению с мезенхимальными стволовыми клетками, или CD26 CD54, CD126, CD141 и т.д., экспрессия которых является пониженной, могут использоваться в качестве маркеров дифференцировки способствующих регенерации нейрональных клеток.
Согласно отдельному примеру осуществления настоящего изобретения дифференцированные клетки стадии i) дифференцируются из нейросфер, образованных культивируемыми мезенхимальными стволовыми клетками.
Согласно отдельному примеру осуществления настоящего изобретения нейрональная регенерационная активность включает миелинизацию периферических нервов.
В настоящем изобретении термин «миелинизация» относится к явлению, при котором миелин окружает аксоны периферических нервов для увеличения скорости, с которой доставляется стимул. Поврежденные периферические нервы приходят в норму (т.е. регенерируют) за счет миелинизации.
В примере настоящего изобретения некоторые из кандидатных клеток, отобранных методом скрининга настоящего изобретения, были миелинизированы цитоморфологически путем совместного культивирования с дорсальными корешковыми ганглиями.
В другом аспекте настоящее изобретение предоставляет нейрональные способствующие регенерации клетки, отобранные методом скрининга, описанным выше.
Согласно отдельному примеру осуществления настоящего изобретения нейрональные способствующие регенерации клетки имеют следующие характеристики:
a) экспрессия маркеров CD121a, CD106 и CD112 является повышенной по сравнению с мезенхимальными стволовыми клетками до дифференцировки; и
b) экспрессия маркеров CD26 и CD141 является пониженной по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В нейрональных способствующих регенерации клетках экспрессия маркера CD121a повышается, как правило, на 30% или больше, конкретнее на 40% или больше по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В примере настоящего изобретения было подтверждено, что экспрессия маркера CD121a повышается на 94% в происходящих из T-MSC-1-1 нейрональных способствующих регенерации клетках, на 71% в происходящих из T-MSC-1-2 нейрональных способствующих регенерации клетках, на 51% в происходящих из T-MSC-13- нейрональных способствующих регенерации клетки и на 48% в происходящих из T-MSC-14 нейрональных способствующих регенерации клетках, на 66% или более в среднем по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В нейрональных способствующих регенерации клетках экспрессия маркера CD106 повышена, как правило, на 5% или более, конкретнее на 10% или более по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В примере настоящего изобретения подтверждено, что экспрессия маркера CD106 повышается на 30% в происходящих из T-MSC-1-1 нейрональных способствующих регенерации клетках, на 11% в происходящих из T-MSC-1-2 нейрональных способствующих регенерации клетках, на 16% в происходящих из T-MSC-1-3 нейрональных способствующих регенерации клетках и на 13% в происходящих из T-MSC-1-4 нейрональных способствующих регенерации клетках, на 17% или более в среднем по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В нейрональных способствующих регенерации клетках экспрессия маркера CD112 повышена, как правило, на 10% или больше, конкретнее на 15% или больше по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В примере настоящего изобретения было подтверждено, что экспрессия маркера CD112 повышается на 49% в происходящих из T-MSC-1-1 нейрональных способствующих регенерации клетках, на 25% в происходящих из T-MSC-1-2 нейрональных способствующих регенерации клетках, на 30% в происходящих из T-MSC-1-3 нейрональных способствующих регенерации клетках и на 19% в происходящих из T-MSC-1-4 нейрональных способствующих регенерации клетках, на 30% или более в среднем по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
Согласно отдельному примеру осуществления настоящего изобретения в нейрональных способствующих регенерации клетках экспрессия маркера CD26 понижается по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В нейрональных способствующих регенерации клетках экспрессия маркера CD26 понижается, как правило, на 5% или больше, конкретнее на 8% или больше по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В примере настоящего изобретения экспрессия маркера CD26 понижается на 9% в происходящих из T-MSC-1-1 нейрональных способствующих регенерации клетках, 11% в происходящих из T-MSC-1-2 нейрональных способствующих регенерации клетках, 27% в происходящих из T-MSC-1-3 нейрональных способствующих регенерации клетках и 16% в происходящих из T-MSC-1-4 нейрональных способствующих регенерации клетках, на 16% или более в среднем по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В нейрональных способствующих регенерации клетках экспрессия маркера CD141 понижается, как правило, на 5% или больше, конкретнее на 8% или больше по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В примере настоящего изобретения экспрессия маркера CD141 понижается на 9% в происходящих из T-MSC-1-1 нейрональных способствующих регенерации клетках, на 20% в происходящих из T-MSC-1-2 нейрональных способствующих регенерации клетках, 16% в происходящих из T-MSC-1-3 нейрональных способствующих регенерации клетках и на 38% в происходящих из T-MSC-1-4 нейрональных способствующих регенерации клетках, на 20% или более в среднем по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию для предотвращения или лечения неврологического заболевания, содержащую нейрональные способствующие регенерации клетки в качестве активного ингредиента.
В другом аспекте настоящее изобретение предоставляет способ лечения неврологического заболевания, включающий стадию введения эффективного количества нейрональных способствующих регенерации клеток субъекту.
В другом аспекте настоящее изобретение обеспечивает использование нейрональных способствующих регенерации клеток в терапии.
В настоящем изобретении термин «неврологическое заболевание» имеет отношение к болезни, вызванной повреждением нервных тканей вследствие внутренних факторов, таких как наследственность, старение и т.д. или внешних факторов, таких как травма и т.п.
Согласно отдельному примеру осуществления настоящего изобретения неврологическое заболевание является одним или более заболеваниями, выбранными из группы, состоящей из нейропатии Шарко-Мари-Тута, диабетической периферической нейропатии, повреждения спинного мозга, амиотрофического латерального склероза, туннельного синдрома запястья, детского паралича, проказы, мышечной дистрофии, полимиозита и миастении гравис.
В настоящем изобретении термин «субъект» относится к индивидууму, нуждающемуся во введении композиции или нейрональных способствующих регенерации клеток настоящего изобретения, и включает млекопитающих, птиц, рептилий, земноводных, рыб и т.д., без ограничения.
В настоящем изобретении «предотвращение» имеет отношение к любого рода ингибированию или отсрочке неврологического заболевания при введении композиции согласно настоящему раскрытию. И «лечение» имеет отношение к любого рода улучшению или благоприятному изменению симптомов неврологического заболевания при введении композиции согласно настоящему изобретению.
Согласно отдельному примеру осуществления настоящего изобретения фармацевтическая композиция настоящего изобретения содержит фармацевтически приемлемый носитель или эксципиент.
Фармацевтическая композиция настоящего изобретения может быть приготовлена в виде однодозовой или многодозовой композиции с использованием фармацевтически приемлемого носителя и/или эксципиента согласно способу, который легко может быть осуществлен средним специалистом в области техники, к которой относится настоящее раскрытие.
Фармацевтическая композиция согласно настоящему изобретению может быть приготовлена в виде разных композиций согласно общепринятым методам. Например, она может быть приготовлена в виде композиции для перорального приема, такой как порошок, гранула, таблетка, капсула, суспензия, эмульсия, сироп и т.п. и также может быть приготовлена в виде композиции для наружного применения, суппозитория или стерильного раствора для инъекции.
Композиция настоящего изобретения может содержать один или более известный активный ингредиент, обладающий действием предотвращения или лечения неврологического заболевания вместе с происходящими из стволовой клетки нейрональными способствующими регенерации клетками, обладающими нейрональной регенеративной активностью.
Фармацевтическая композиция настоящего изобретения может вводиться перорально или парентерально. Конкретнее, композиция может вводиться парентерально, например, путем внутривенной инъекции, трансдермального введения, подкожной инъекции, внутримышечной инъекции, интравитреальной инъекции, субретинальной инъекции, супрахориоидальной инъекции, введения в виде глазных капель, интрацеребровентрикулярной инъекции, интратекальной инъекции, внутриамниотической инъекции, внутриартериальной инъекции, внутрисуставной инъекции, внутрисердечной инъекции, внутрикавернозной инъекции, внутричерепной инъекции, интрацистернальной инъекции, внутрикоронарной инъекции, внутричерепной инъекции, интрадуральной инъекции, эпидуральной инъекции, интрагиппокампальной инъекции, интраназальной инъекции, внутрикостной инъекции, внутрибрюшинной инъекции, внутриплевральной инъекции, инъекции в спинно-мозговой канал, интраторакальной инъекции, внутритимусной инъекции, внутриматочной инъекции, внутривагинальной инъекции, внутрижелудочковой инъекции, внутрипузырной инъекции, субконъюнктивальной инъекции, внутриопухолевой инъекции, местной инъекции и т.п.
Композиции для парентерального введения включают стерилизованный водный раствор, неводный раствор, суспензию, эмульсию, лиофилизированную композицию и суппозиторий. Для неводного раствора или суспензии можно использовать пропиленгликоль, полиэтиленгликоль, растительное масло, такое как оливковое масло, инъецируемый сложный эфир, такой как этилолеат и т.д. В качестве основы для суппозиториев могут использоваться витепсол, макрогол, Твин 61, масло какао, лауриновое масло, глицерожелатин и т.п.
Дозировка для введения фармацевтической композиции настоящего изобретения может варьировать в зависимости от различных факторов, таких как способ составления композиции, способ введения, время введения, путь введения, ответ, которого необходимо достигнуть при введении фармацевтической композиции, и его выраженность, возраст, вес тела, общее состояние здоровья, патологическое состояние или его тяжесть, пол, диета и скорость экскреции у субъекта, которому вводится фармацевтическая композиция, и другие лекарственные средства или ингредиенты, использованные совместно, и других подобных факторов, хорошо известных в области медицины, причем вводимая дозировка, эффективная для достижения желаемого лечения, может быть легко определена и назначена средним специалистом в данной области техники.
Путь и способ введения фармацевтической композиции настоящего изобретения могут быть независимыми друг от друга и не ограничиваются каким-либо специальным образом, если только фармацевтическая композиция может достигать целевого места.
Полезные эффекты
Признаки и преимущества настоящего изобретения могут быть суммированы, как изложено ниже:
(i) Настоящее изобретение предоставляет способ скрининга происходящих из мезенхимальных стволовых клеток, нейрональных способствующих регенерации клеток, обладающих нейрональной регенерационной активностью, и фармацевтическую композицию, содержащую способствующие регенерации нейрональные клетки.
(ii) Нейрональные способствующие регенерации клетки настоящего изобретения полностью отличаются от стволовых клеток в отношении профиля экспрессии CD маркера и демонстрируют отличный результат регенерации нейронов. Соответственно, они могут использоваться в различных областях для предотвращения или лечения неврологических заболеваний.
Краткое описание чертежей
На фиг. 1 показаны изображения нейрональных способствующих регенерации клеток, индуцированных из происходящих из небной миндалины мезенхимальных стволовых клеток T-MSC-1-1.
На фиг. 2 показаны тепловые карты, визуализирующие экспрессию CD маркеров в нейрональных способствующих регенерации клетках согласно настоящему изобретению путем скрининга CD маркеров.
На фиг. 3a и 3b продемонстрирован результат скрининга CD маркеров, показывающий различие в уровне экспрессии нейрональных способствующих регенерации клеток по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками. На фиг. 3a показан результат сравнения CD маркеров, уровень экспрессии которых повышен по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками, а на фиг. 3b показан результат сравнения CD маркеров, уровень экспрессии которых понижен по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками.
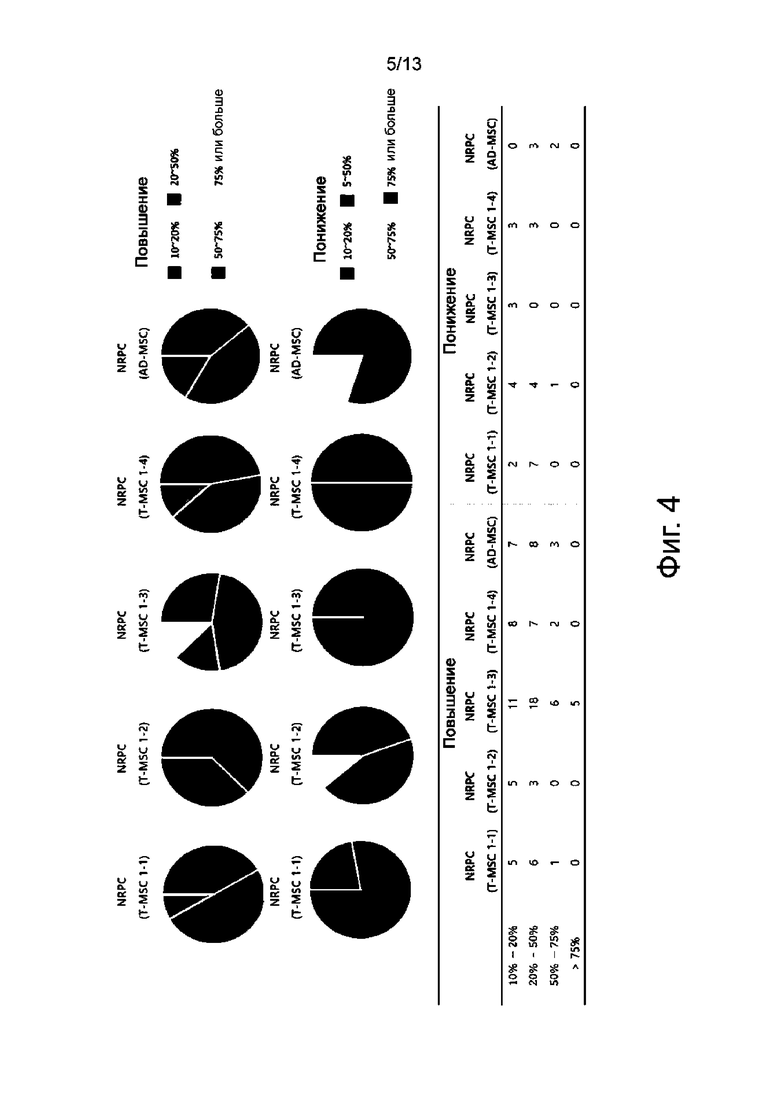
На фиг. 4 показан результат сравнения профиля экспрессии CD маркеров, экспрессия которых повышается, и CD маркеров, экспрессия которых понижается в нейрональных способствующих регенерации клетках по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками.
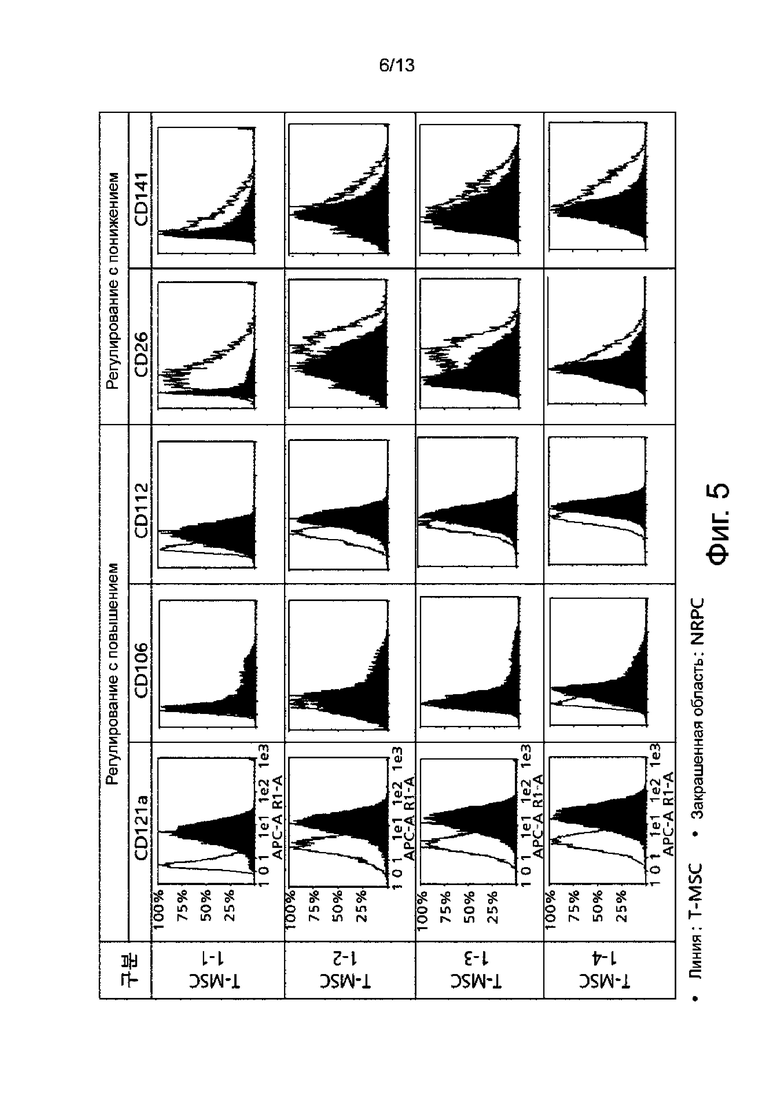
На фиг. 5 показан результат скрининга CD маркеров, экспрессия которых была повышена или понижена в нейрональных способствующих регенерации клетках.
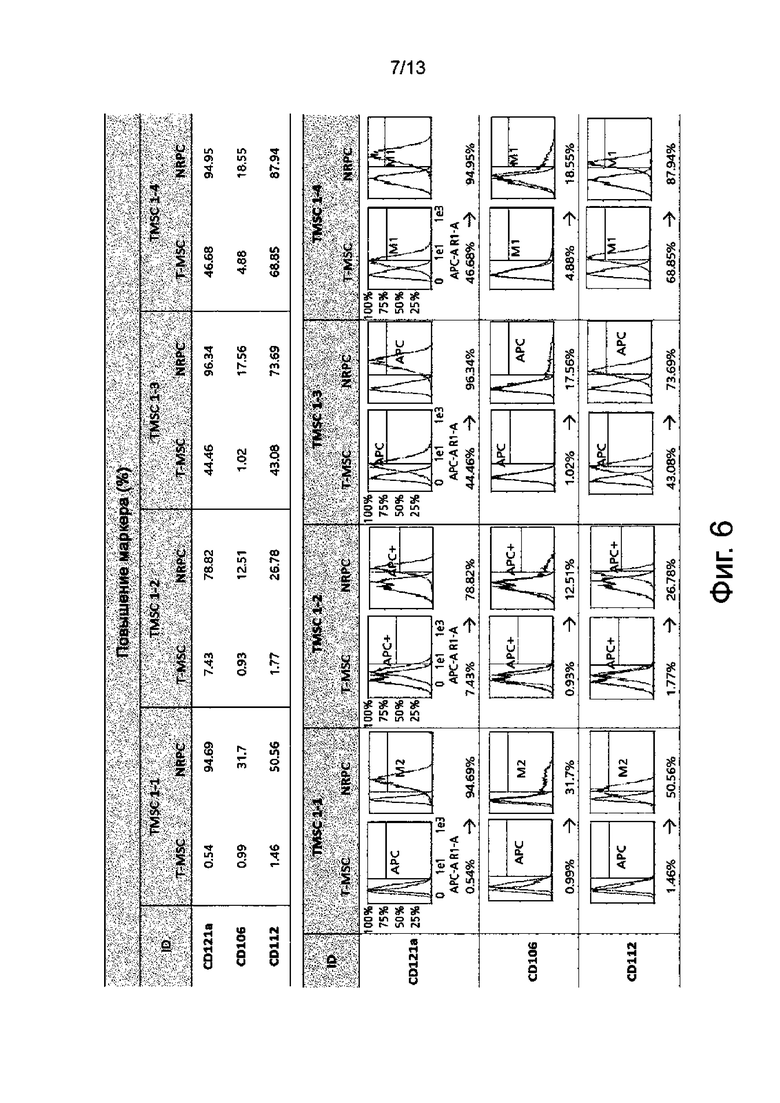
На фиг. 6 показан результат сравнения профиля экспрессии маркеров CD121a, CD106 и CD112, экспрессия которых повышается в нейрональных способствующих регенерации клетках по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками.
На фиг. 7 показан результат сравнения профиля экспрессии маркеров CD26 и CD141, экспрессия которых понижается в нейрональных способствующих регенерации клетках по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками.
На фиг. 8 показан результат сравнения профиля экспрессии CD маркеров в происходящих из небной миндалины мезенхимальных стволовых клетках (T-MSC) и нейрональных способствующих регенерации клетках (NRPC) с использованием тепловых карт.
На фиг. 9 показан результат проведения анализа роста нейритов для сравнения роста нейритов из нейрональных способствующих регенерации клеток.
На фиг. 10 показано, что миелинизация была достигнута цитоморфологически в некоторых из кандидатных клеток, совместно культивированных с дорсальными корешковыми ганглиями.
На фиг. 11 показан результат проведения проточной цитометрии по повышенным и пониженным CD маркерам, отобранным с помощью CD скрининга с использованием индивидуальных антител.
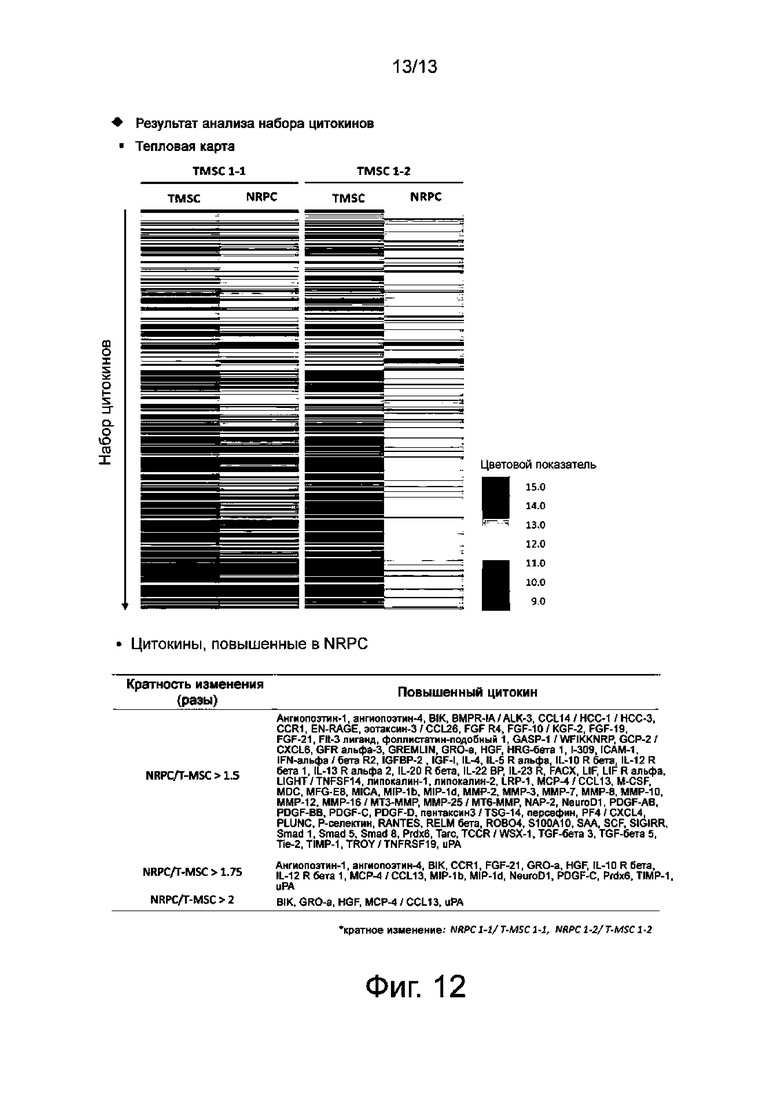
На фиг. 12 показан результат анализа цитокинов T-MSC и NRPC с использованием тепловых карт (слева) и долю цитокинов, увеличенных в NRPC по сравнению с T-MSC (справа) (кратность изменения: NRPC 1-1/ T-MSC 1-1, NRPC 1-2/ T-MSC 1-2).
Лучший вариант осуществления изобретения
Далее настоящее изобретение будет описано более подробно с помощью примеров. Примеры предоставляются только для более подробного описания настоящего изобретения, при этом средним специалистам в данной области техники будет понятно, что объем настоящего изобретения не ограничивается примерами.
Примеры
Пример 1. Приготовление мезенхимальных стволовых клеток
1-1. Изоляция и культивирование мезенхимальных стволовых клеток, происходящих из небной миндалины
Ткани небных желез, полученные от нескольких доноров, приобретенные в медицинском колледже Женского университета Ихва, помещали в пробирки с 10 мл DPBS (фосфатно-солевой буфер Дульбекко) с добавлением 20 мкг/мл гентамицина, центрифугировали при 1,500 об/мин в течение 5 минут, а затем промывали дважды. Промытые ткани небной железы нарезали с помощью стерильных ножниц.
Для того чтобы изолировать происходящие из ткани небной миндалины мезенхимальные стволовые клетки, после добавления ферментативного реакционного раствора того же самого веса, ткани небной железы инкубировали в инкубаторе-встряхивателе при 37°C и 200 об/мин в течение 60 минут. Состав ферментативного реакционного раствора описан в таблице 1.
После добавления в культуру 5% FBS (эмбриональной бычьей сыворотки) смесь центрифугировали при 1500 об/мин в течение 5 минут. После центрифугирования супернатант удаляли, а оставшийся осадок ресуспендировали в 30 мл DPBS, а затем центрифугировали при 1500 об/мин в течение 5 минут. После центрифугирования супернатант удаляли, а оставшийся осадок ресуспендировали в 10 мл DPBS для приготовления суспензии. Суспензию пропускали через 100-мкм фильтр. Происходящие из небной железы мезенхимальные стволовые клетки, оставшиеся на фильтре, промывали 20 мл DPBS, а затем центрифугировали при 1500 об/мин в течение 5 минут. После центрифугирования супернатант удаляли и проводили инкубацию на водяной бане с постоянной температурой 37°C в течение 5 мин после добавления лизирующего буфера ACK. После добавления к суспензии DPBS центрифугировали при 1500 об/мин в течение 5 минут. После центрифугирования супернатант удаляли, а оставшийся осадок ресуспендировали в DMEM с высоким содержанием глюкозы (10% FBS, 20 мкг/мл гентамицина) для получения суспензии. Затем, подсчитывали число клеток в приготовленной клеточной суспензии. Клеточную суспензию высевали в T175 флаконы и инкубировали при 37°C в 5% CO2 инкубаторе.
1-2. Изолирование и культивирование мезенхимальных стволовых клеток, происходящих из жировой ткани
Происходящие из жировой ткани мезенхимальные стволовые клетки покупали у компании Lonza (стволовые клетки, происходящие из человеческой жировой ткани, Cat#PT-5006, Lonza, Швейцария). Происходящие из жировой ткани мезенхимальные стволовые клетки культивировали, используя среду, предоставленную Lonza (Bulletkit ADSD, Cat#PT-4505).
Пример 2. Образование нейросфер
Нейросферы были сформированы при культивировании мезенхимальных стволовых клеток из примера 1. Конкретнее, мезенхимальные стволовые клетки субкультивировали до 4-7 пассажей. После удаления культуральной среды мезенхимальные стволовые клетки промыли DPBS. После обработки промытых клеток TrypLE подсчитывали собранные клетки. После центрифугирования собранных клеток и удаления супернатанта клетки ресуспендировали в среде для образования нейросфер. Состав среды для образования нейросфер описан в таблице 2.
Клетки, ресуспендированные в среде для образования нейросфер (1x106 клеток), высевали в чашки со сверхнизким «сцеплением» (60 мм). Высеянные клетки культивировали в течение 3 дней в условиях 37°C и 5% CO2. После культивирования в течение 3 дней образованные в чашке нейросферы собирали в 15-мл пробирку. После центрифугирования собранных клеток и удаления супернатанта готовили суспензию нейросфер путем добавления свежей среды для формирования нейросфер. Суспензию нейросфер переносили в чашку со сверхнизким «сцеплением» и культивировали нейросферы в течение 4 дней в условиях 37°C и 5% CO2.
Пример 3. Дифференцировка в кандидатные клетки нейрональных способствующих регенерации клеток (NRPC) с использованием нейросфер
Нейросферы, образованные в примере 2, тонко измельчали, используя иглу для шприца 23-26G. Измельченные нейросферы переносили в 15-мл пробирку с помощью пипетки, а затем центрифугировали. После удаления супернатанта, измельченные нейросферы ресуспендировали, добавив в пробирку индукционную среду для нейрональных способствующих регенерации клеток. Были приготовлены разные индукционные среды для нейрональных способствующих регенерации клеток путем комбинирования трех или более из 1) 5-20% FBS (эмбриональная бычья сыворотка, 2) 5-20 нг/мл bFGF (основной фактор роста фибробластов, Peprotech, США), 3) 100-400 мкM бутилгидроксианизол (Sigma, США), 4) 5-40 мкM форсколин (MedCheExpress, США), 5) 0.1-10% N2 добавка (GIBCO, США), 6) 1-100 нг/мл нейротрофический фактор головного мозга (BDNF, Sigma-Aldrich, США), 7) 1-100 нг/мл фактор роста нервов (NGF, Santa Cruz, США), 8) 0,01-1 нг/мл «sonic hedgehog» (SHH, R & D Systems, США), 9) 1-10 нг/мл PDGF-AA (фактор роста тромбоцитов-AA, Peprotech, США) и 10) 50-300 нг/мл херегулин-бета1, Peprotech, США) в DMEM/F12, содержащей GlutaMAX.
Ресуспендированные в разных средах нейросферы высевали во флаконы T175, покрытые ламинином (2 мкг/мл). Высеянные нейросферы культивировали в течение 8-10 дней, меняя при этом индукционную среду у нейрональных способствующих регенерации клеток с 3-дневным интервалом (фиг. 1).
Пример 4. Первый скрининг кандидатных клеток из нейрональных способствующих регенерации клеток путем подтверждения миелинизации периферических нервов
Было изучено, обладают ли нейрональные способствующие регенерации кандидатные клетки, полученные в примере 3, способностью миелинизировать периферические нервы. Конкретнее, дифференцированные нейрональные способствующие регенерации кандидатные клетки совместно культивировали с ганглиями задних корешков (DRG), и наблюдали, происходит ли миелинизация.
Клетки ганглиев задних корешков (DRG), извлеченные у крыс, покупали у Lonza (крысиные клетки ганглиев задних корешков, Cat# R-DRG-505, Lonza, Швейцария). Кандидатные клетки совместно культивировали с ганглиями задних корешков. Клетки DRG культивировали с использованием культуральной среды, предоставленной Lonza (среда для выращивания первичных нейронов (PNGM), Cat# CC-4461).
Культуральную среду заменяли каждые 3 дня. В результате совместного культивирования кандидатных клеток с ганглиями задних корешков было подтверждено цитоморфологическое достижение миелинизации в некоторых клетках (фиг. 10).
Пример 5. Второй скрининг нейрональных способствующих регенерации клеток при помощи анализа экспрессии CD маркеров
Всего была проанализирована экспрессия 242 CD маркеров в T-MSC-1-1 (происходящих из небной миндалины мезенхимальных стволовых клетках 1), T-MSC-1-2 (происходящих из небной миндалины мезенхимальных стволовых клетках 2), T-MSC-1-3 (происходящих из небной миндалины мезенхимальных стволовых клетках 3) и T-MSC-1-4 (происходящих из небной миндалины мезенхимальных стволовых клетках 4), в которых миелинизация была подтверждена цитоморфологически среди нейрональных способствующих регенерации клеток-кандидатов из примера 4, и среди нейрональных способствующих регенерации клеток, дифференцированных из них.
Для анализа CD маркеров собирали 3x107 целевых клеток. Клетки промывали DPBS и затем центрифугировали при 2000 об/мин в течение 5 минут. После удаления супернатанта и одной промывки DPBS проводили центрифугирование, а оставшийся осадок ресуспендировали в 30 мл FACS буфера. 100 мкл клеточной суспензии (1x105 клеток) высевали в каждую лунку круглодонного 96-луночного планшета. Затем, 10 мкл первичных антител CD маркеров добавили в каждую лунку 96-луночного планшета. После 30 минут прохождения реакции на льду с приглушенным светом каждую лунку два раза промыли 100 мкл FACS буфера и затем центрифугировали при 300 g в течение 5 минут. После удаления супернатанта и добавления 200 мкл FACS буфера к каждой лунке провели центрифугирование при 300 g в течение 5 минут. Вторичные антитела были приготовлены в FACS буфере в соотношении 1:200 (1.25 мкг/мл). После завершения центрифугирования супернатант удалили, а затем добавили в каждую лунку 100 мкл приготовленных вторичных антител. После проведения реакции в течение 20-30 минут на льду при приглушенном свете каждую лунку промыли 100 мкл FACS буфера, а затем провели центрифугирование при 300 g в течение 5 минут. После удаления супернатанта целевые клетки промыли, добавив 200 мкл FACS буфера в каждую лунку. Промывку повторили дважды. После промывки клетки ресуспендировали, добавив 200 мкл FACS буфера в каждую лунку, и исследовали экспрессию CD маркеров в целевых клетках с помощью проточной цитометрии или FACS (сортировка флуоресцентно-активированных клеток).
Результат сравнения экспрессии CD маркеров в индуцированных нейрональных способствующих регенерации клетках с использованием тепловых карт показан на фиг. 2. Как видно на фиг. 2, нейрональные способствующие регенерации клетки (NRPC) и мезенхимальные стволовые клетки (MSC) продемонстрировали сходные профили экспрессии CD маркеров, но показали различие в профилях экспрессии некоторых маркеров.
Профиль экспрессии CD маркеров мезенхимальных стволовых клеток (MSC) T-MSC-1-1, T-MSC-1-2, T-MSC-1-3 и T-MSC-1-4 и нейрональных способствующих регенерации клеток (NRPC) сравнили для того, чтобы выбрать CD маркеры, экспрессия которых повышалась или понижалась, в качестве маркеров дифференцировки нейрональных способствующих регенерации клеток. CD маркеры, экспрессия которых повышается или понижается, показаны на фиг. 3.
Как видно на фиг. 3a, CD маркеры, экспрессия которых повышается в нейрональных способствующих регенерации клетках происходящих из T-MSC-1-1, T-MSC-1-2, T-MSC-1-3 и T-MSC-1-4 (по меньшей мере, в трех из четырех NRPC) по сравнению с происходящими из небной железы мезенхимальными стволовыми клетками - это CD10, CD39, CD106, CD112, CD121a, CD338 и т.д. И, как видно на фиг. 3b, CD маркеры, экспрессия которых понижается (по меньшей мере в трех из четырех NRPC) - это CD26, CD54, CD126, CD141 и т.д.
Результат сравнения повышения и понижения CD маркеров в происходящих из небной железы нейрональных способствующих регенерации клетках показан на фиг. 4.
Как видно на фиг. 4, экспрессия 12 CD маркеров была повышена, и экспрессия 9 CD маркеров была понижена в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-1. И, экспрессия 8 CD маркеров была повышена, и экспрессия 9 CD маркеров была понижена в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-2. Экспрессия 40 CD маркеров была повышена, и экспрессия 3 CD маркеров была понижена в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-3. Экспрессия 17 CD маркеров была повышена, и экспрессия 6 CD маркеров была понижена в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-4.
Из приведенных выше результатов был проведен поиск маркеров CD, экспрессия которых, как правило, повышается или понижается в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-1, T-MSC-1-2, T-MSC-1-3 и T-MSC-1-4. Были отобраны следующие маркеры:
- CD маркеры, экспрессия которых, как правило, повышается: CD106, CD112 и CD121a.
- CD маркеры, экспрессия которых, как правило, понижается: CD26 и CD141.
Профиль CD маркеров, экспрессия которых повышается или понижается, также наблюдался в нейрональных способствующих регенерации клетках, дифференцированных из происходящих из жировой ткани мезенхимальных стволовых клеток из примера 1-2.
Результат CD-скрининга CD маркеров, экспрессия которых повышается или понижается в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-1, T-MSC-1-2, T-MSC-1-3 и T-MSC-1-4, показана на фиг. 5.
Как видно на фиг. 5, уровень экспрессии CD маркеров, экспрессия которых, как правило, повышается в нейрональных способствующих регенерации клетках, т.е. CD121a, CD106 и CD112, повышается на 10% или больше после дифференцировки. В то же время, уровень экспрессии маркеров, экспрессия которых, как правило, понижается, т.е. CD26 и CD141, понижается примерно на 9% или больше. Этот результат говорит о том, что маркеры CD121a, CD106, CD112, CD26 и CD141, экспрессия которых изменяется, могут использоваться в качестве маркеров дифференцировки нейрональных способствующих регенерации клеток. В частности, CD121a, CD106 и CD112 могут использоваться в качестве типичных маркеров дифференцировки.
6-1. Сравнение экспрессии маркеров ко-экспрессии CD121a, CD106 и CD112
Экспрессия маркеров CD121a, CD106 и CD112, как правило, повышается в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-1, T-MSC-1-2, T-MSC-1-3 и T-MSC-1-4 на 10% или больше по сравнению с мезенхимальными стволовыми клетками, что является наиболее выраженным признаком нейрональных способствующих регенерации клеток. Результат сравнения экспрессии маркеров CD121a, CD106 и CD112 в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-1, T-MSC-1-2, T-MSC-1-3 и T-MSC-1-4, показан на фиг. 6.
Как видно на фиг. 6, экспрессия маркеров CD121a, CD106 и CD112 была значительно повышена в нейрональных способствующих регенерации клетках (NRPC) по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками (T-MSC).
6-2. Сравнение экспрессии маркеров ко-экспрессии CD26 и CD141
Экспрессия маркеров CD26 и CD141, как правило, понижается в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-1, T-MSC-1-2, T-MSC-1-3 и T-MSC-1-4. Результат сравнения экспрессии CD маркеров в нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-1, T-MSC-1-2, T-MSC-1-3 и T-MSC-1-4, показан на фиг. 7.
Как видно на фиг. 7, экспрессия маркеров CD26 и CD141 была понижена в нейрональных способствующих регенерации клетках по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками.
6-3. Сравнение профилей экспрессии CD маркеров
Для того, чтобы сравнить профиль экспрессии CD маркеров в происходящих из небной миндалины мезенхимальных стволовых клетках и нейрональных способствующих регенерации клетках, были построены тепловые карты на основе результатов сравнения экспрессии CD маркеров ко-экспрессии из примеров 6-1 и 6-2. Результат показан на фиг. 8.
Как показано на фиг. 8, нейрональные способствующие регенерации клетки показали разную экспрессию маркеров ко-экспрессии с происходящими из небной миндалины мезенхимальными стволовыми клетками.
6-4. Средняя экспрессия CD маркеров ко-экспрессии
Для того, чтобы изучить, сохраняется ли профиль экспрессии CD маркеров в происходящих из небной миндалины мезенхимальных стволовых клетках и нейрональных способствующих регенерации клетках после замораживания клеток, была исследована экспрессия CD маркеров ко-экспрессии в живых клетках, замороженных клетках и размороженных клетках. Результат показан на фиг. 11.
Как видно на фиг. 11, экспрессия CD106, CD121a и CD112 была повышена, а экспрессия CD26 и CD141 была понижена в нейрональных способствующих регенерации клетках по сравнению с происходящими из небной миндалины мезенхимальными стволовыми клетками даже после замораживания. Нейрональные способствующие регенерации клетки продемонстрировали разную экспрессию маркеров ко-экспрессии из происходящих из небной миндалины мезенхимальных стволовых клеток независимо от замораживания.
Пример 7. Действие нейрональных способствующих регенерации клеток на рост нейритов
Нейрит (или отросток нейрона), выступающий из тела нейрона, как известно, вовлечен в транспорт веществ, необходимых для роста и регенерации аксонов, нейромедиаторов и факторов роста нервов и т.д. (L McKerracher et al., Spinal Cord Repair: Strategies to Promote Axon Regeneration, Neurobiol Dis, 2001). Был проведен анализ удлинения (роста) нейритов для сравнения роста нейритов в нейрональных способствующих регенерации клетках настоящего изобретения.
Клетки N1E-115 (клетки нейробластомы мыши, ATCC, США) культивировали и высевали на микропористый фильтр (набор для анализа роста нейритов, Millipore, США). Высеянные клетки культивировали в течение 48 часов в культуральной среде, из которой были собраны нейрональные способствующие регенерации клетки или стволовые клетки. Оптическую плотность измеряли после окрашивания нейритов, проросших через мелкопористый фильтр. В результате анализа роста нейритов было установлено, что культура нейрональных способствующих регенерации клеток регулирует или стимулирует рост нейритов (аксонов) в клетках N1E-115 (мышиная нейробластома).
Сравнили рост нейритов в N1E-115 клетках, культивированных с нейрональными способствующими регенерации клетками, происходящими от T-MSC-1-2. Результат показан на фиг. 9 (NRPC: нейрональные способствующие регенерации клетки, происходящие из T-MSC-1-2, T-MSC: T-MSC-1-2, Отрицательный контроль: группа отрицательный контроль, Положительный контроль: группа положительный контроль). Большое количество нейритов наблюдалось в нейрональных способствующих регенерации клетках по сравнению с происходящими из небной миндалины стволовыми клетками, и оптическая плотность была также повышена в нейрональных способствующих регенерации клетках по сравнению с происходящими из небной миндалины стволовыми клетками (Отрицательный контроль: пористый фильтр (мембранная вкладка, предоставленная вместе с набором для роста нейритов) был покрыт BSA, и N1E-115 клетки культивировали в DMEM (+ 20 мкг/мл гентамицина). Положительный контроль: пористый фильтр был покрыт ламинином, и N1E-115 клетки культивировали в DMEM (+ 20 мкг/мл гентамицина + 1 мкг/мл BSA). NRPC и T-MSC группы: пористый фильтр был покрыт BSA, и N1E-115 клетки культивировали в культуральной среде NRPC или T-MSC).
Пример 8. Количественное определение цитокинов нейрональных способствующих регенерации клеток
Экспрессию 507 цитокинов анализировали в T-MSC-1-1 и T-MSC-1-2, которые продемонстрировали наиболее выраженную миелинизацию в примере 4, и нейрональных способствующих регенерации клетках, дифференцированных из них.
Целевые клетки культивировали для анализа цитокинов. Клетки высевали во флаконы и культивировали в течение 3-4 дней. Когда клетки заполняли 80% или больше площади флакона, культуральную среду удаляли, а клетки дважды промывали DPBS. После промывки, культуральную среду заменяли на DMEM (забуференный фосфатом Дульбекко физиологический раствор), не содержащую FBS (эмбриональную бычью сыворотку), цитокины и т.п. для того, чтобы исключить влияние цитокинов. Культуральную среду целевых клеток собирали после культивирования в течение 30 часов.
Собранную культуральную среду центрифугировали при 3600 об/мин в течение 30 минут. Супернатант переносили в центрифужную пробирку, снабженную целлюлозной мембраной и концентрировали с помощью центрифугирования при 3600 об/мин в течение 20 минут. После центрифугирования кондиционированную среду, пропущенную через разделительную мембрану, отбрасывали и добавляли такое же количество (объем) культуры. Центрифугирование продолжалось до тех пор, пока объем концентрированной культуры был снижен до 1 мл или ниже, и концентрированную культуру характеризовали количественно методом Бредфорда. Концентрированная культура была отрегулирована до конечной концентрации 1 мг/мл путем смешивания с DMEM.
Реакция на мембране, покрытой антителами, способными детектировать 507 цитокинов (набор для анализа цитокинов, RayBiotech, США), проходила в течение 30 минут до обработки блокирующим буфером. После удаления блокирующего буфера оставшегося на мембране и замены концентрированной культуры реакция на мембране проходила в течение ночи в холодильнике. Мембрану промывали 7 раз промывочным буфером. После добавления HRP-конъюгированного раствора стрептавидина мебрану оставляли для прохождения реакции при комнатной температуре в течение 2 часов. После удаления HRP-конъюгированного раствора стрептавидина мембрану промыли 7 раз промывочным буфером. После промывки мембрану пропитывали ECL (для увеличения хемилюминесценции) реагентом, и подтверждали экспрессию цитокинов с помощью визуализирующего устройства.
Результат сравнения экспрессии цитокинов в нейрональных способствующих регенерации клетках с использованием тепловых карт показан на фиг. 12. Как видно на фиг. 12, нейрональные способствующие регенерации клетки и происходящие из небной миндалины мезенхимальные стволовые клетки показали разные профили экспрессии.
Цитокины, экспрессия которых повышается в мезенхимальных стволовых клетках и нейрональных способствующих регенерации клетках, происходящих из T-MSC-1-1 и T-MSC-1-2, показаны на фиг. 12.
- В 1,5 раза или больше: ангиопоэтин-1, ангиопоэтин-4, BIK, BMPR-IA / ALK-3, CCL14 / HCC-1 / HCC-3, CCR1, EN-RAGE, эотаксин-3 / CCL26, FGF R4, FGF-10 / KGF-2, FGF-19, FGF-21, Flt-3 лиганд, фоллистатин-подобный 1, GASP-1 / WFIKKNRP, GCP-2 / CXCL6, GFR альфа-3, GREMLIN, GRO-a, HGF, HRG-бета 1, I-309, ICAM-1, IFN-альфа / бета R2, IGFBP-2 , IGF-I, IL-4, IL-5 R альфа, IL-10 R бета, IL-12 R бета 1, IL-13 R альфа 2, IL-20 R бета, IL-22 BP, IL-23 R, FACX, LIF, LIF R альфа, LIGHT / TNFSF14, липокалин-1, липокалин-2, LRP-1, MCP-4 / CCL13, M-CSF, MDC, MFG-E8, MICA, MIP-1b, MIP-1d, MMP-2, MMP-3, MMP-7, MMP-8, MMP-10, MMP-12, MMP-16 / MT3-MMP, MMP-25 / MT6-MMP, NAP-2, NeuroD1, PDGF-AB, PDGF-BB, PDGF-C, PDGF-D, пентаксин3 / TSG-14, персефин, PF4 / CXCL4, PLUNC, P-селектин, RANTES, RELM бета, ROBO4, S100A10, SAA, SCF, SIGIRR, Smad 1, Smad 5, Smad 8, Prdx6, Tarc, TCCR / WSX-1, TGF-бета 3, TGF-бета 5, Tie-2, TIMP-1, TROY / TNFRSF19, uPA.
- В 1,75 раза или больше: ангиопоэтин-1, ангиопоэтин-4, BIK, CCR1, FGF-21, GRO-a, HGF, IL-10 R бета, IL-12 R бета 1, MCP-4 / CCL13, MIP-1b, MIP-1d, NeuroD1, PDGF-C, Prdx6, TIMP-1, uPA.
- В 2 раза или больше: BIK, GRO-a, HGF, MCP-4 / CCL13, uPA.
Итак, авторы настоящего изобретения получили нейрональные способствующие регенерации клетки из мезенхимальных стволовых клеток, происходящих из ткани небной миндалины и жировой ткани, изучили их профили экспрессии с помощью анализа CD маркеров. Кроме того, они установили нейрональное регенерационное действие нейрональных способствующих регенерации клеток. Это говорит о том, что ткани небной миндалины, которые выкидываются как медицинские отходы, могут использоваться для получения клеток, обладающих нейрональным регенерационным действием. Нейрональные способствующие регенерации клетки настоящего изобретения могут различным образом использоваться в области нейрональной регенерации.
Хотя отдельные примеры осуществления настоящего изобретения описаны, средние специалисты в данной области техники могут по-разному модифицировать и изменить настоящее изобретение посредством добавления, изменения, опущения и т.д. в пределах объема настоящего изобретения, определенного прилагаемыми пунктами формулы изобретения.









Изобретение относится к области биотехнологии, в частности к способу скрининга происходящих из мезенхимальных стволовых клеток способствующих регенерации нейрональных клеток (варианты). Кроме того, настоящее изобретение относится к нейрональной способствующей регенерации клетке, индуцированной из происходящей из небных миндалин мезенхимальной стволовой клетки, а также к фармацевтической композиции, ее содержащей, и ее применению для лечения неврологического заболевания. Указанная нейрональная клетка имеет следующие характеристики: a) экспрессия маркеров CD121a, CD106 и CD112 является повышенной по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки; и b) экспрессия маркеров CD26 и CD141 является пониженной по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки. Настоящее изобретение обеспечивает скрининг способствующих регенерации нейрональных клеток, проявляющих нейрональный регенеративный эффект из числа разных клеток, дифференцированных из мезенхимальных стволовых клеток, на основе анализа специфических CD маркеров. 5 н. и 9 з.п. ф-лы, 12 ил., 2 табл., 8 пр.
1. Способ скрининга происходящих из мезенхимальных стволовых клеток способствующих регенерации нейрональных клеток, обладающих нейрональной регенерационной активностью, включающий:
i) стадию получения клеток, дифференцированных из мезенхимальных стволовых клеток; и
ii) стадию скрининга клеток, в которых один или более маркеров, выбранных из группы, состоящей из CD121a, CD106 и CD112, является повышенным из числа дифференцированных клеток стадии i) по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
2. Способ скрининга происходящих из мезенхимальных стволовых клеток способствующих регенерации нейрональных клеток, обладающих нейрональной регенерационной активностью, включающий:
i) стадию получения клеток, дифференцированных из мезенхимальных стволовых клеток; и
ii) стадию скрининга клеток, в которых один или более маркеров, выбранных из группы, состоящей из CD26 и CD141, является пониженным из числа дифференцированных клеток стадии i) по сравнению с мезенхимальными стволовыми клетками до дифференцировки.
3. Способ скрининга нейрональных способствующих регенерации клеток по п. 1 или 2, согласно которому мезенхимальные стволовые клетки получают из небной миндалины или жировой ткани.
4. Способ скрининга нейрональных способствующих регенерации клеток по п. 1 или 2, согласно которому дифференцированные клетки стадии i) дифференцируются из нейросфер, образованных культивируемыми мезенхимальными стволовыми клетками.
5. Способ скрининга нейрональных способствующих регенерации клеток по п. 1 или 2, согласно которому нейрональная регенерационная активность включает миелинизацию периферических нервов.
6. Нейрональная способствующая регенерации клетка, индуцированная из происходящей из небных миндалин мезенхимальной стволовой клетки, при этом эта нейрональная способствующая регенерации клетка имеет следующие характеристики:
a) экспрессия маркеров CD121a, CD106 и CD112 является повышенной по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки; и
b) экспрессия маркеров CD26 и CD141 является пониженной по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки.
7. Нейрональная способствующая регенерации клетка по п. 6, при этом в нейрональной способствующей регенерации клетке экспрессия маркера CD121a является повышенной на 30% или более по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки.
8. Нейрональная способствующая регенерации клетка по п. 6, при этом в нейрональной способствующей регенерации клетке экспрессия маркера CD106 является повышенной на 5% или более по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки.
9. Нейрональная способствующая регенерации клетка по п. 6, при этом в нейрональной способствующей регенерации клетке экспрессия маркера CD112 является повышенной на 10% или более по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки.
10. Нейрональная способствующая регенерации клетка по п. 6, при этом в нейрональной способствующей регенерации клетке экспрессия маркера CD26 является пониженной на 5% или более по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки.
11. Нейрональная способствующая регенерации клетка по п. 6, при этом в нейрональной способствующей регенерации клетке экспрессия маркера CD141 является пониженной на 5% или более по сравнению с происходящей из небной миндалины мезенхимальной стволовой клетки.
12. Фармацевтическая композиция для предотвращения или лечения неврологического заболевания, содержащая нейрональную способствующую регенерации клетку по п. 6 в качестве активного ингредиента и фармацевтически приемлемый носитель, где неврологическое заболевание является одним или более заболеваниями, выбранными из группы, состоящей из нейропатии Шарко-Мари-Тута, диабетической периферической нейропатии, повреждения спинного мозга, амиотрофического латерального склероза, туннельного синдрома запястья, детского паралича, проказы, мышечной дистрофии, полимиозита и миастении гравис.
13. Фармацевтическая композиция по п. 12, причем нейрональная регенерационная активность включает миелинизацию периферических нервов.
14. Применение нейрональной способствующей регенерации клетки по п. 6 для лечения неврологического заболевания, где неврологическое заболевание является одним или более заболеваниями, выбранными из группы, состоящей из нейропатии Шарко-Мари-Тута, диабетической периферической нейропатии, повреждения спинного мозга, амиотрофического латерального склероза, туннельного синдрома запястья, детского паралича, проказы, мышечной дистрофии, полимиозита и миастении гравис.
| CELLATOZ THERAPEUTICS, INC | |||
| A new era of cell therapies for intractable diseases (веб | |||
| Актинометр | 1935 |
|
SU43747A1 |
| ПЕТРОВА Е.С., Восстановление поврежденного нерва с помощью клеточной терапии (фундаментальные аспекты), Acta Naturae (русскоязычная версия), 2015, no 3(26), стр | |||
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
| WO 2013151725 | |||
Авторы
Даты
2024-05-20—Публикация
2022-01-12—Подача