Изобретение относится к области фармацевтики и медицины, и представляет собой применение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона или его фармацевтически приемлемой соли для лечения и/или профилактики кашля, вызванного вирусными инфекциями.
Кашель является защитной реакцией организма, направленной на освобождение дыхательных путей от инородных тел или секрета, когда активность мерцательного эпителия снижена. Различают физиологический и патологический кашель. Физиологический кашель обеспечивает механизм выведения трахеобронхиального секрета. Патологический или неадекватный тяжелый кашель развивается на фоне различных заболеваний и может вызывать многочисленные осложнения [1, 2].
Кашель находится на пятом месте среди причин, заставляющих больных обращаться к врачу, и на первом месте - среди симптомов, обусловленных патологией органов дыхания [3]. Кашель - один из главных симптомов респираторных заболеваний и одна из наиболее часто встречающихся проблем со здоровьем в медицинской практике, как у детей, так и у взрослых. Обычной причиной кашля являются инфекции верхних дыхательных путей и острый бронхит, которые, как правило, имеют вирусную этиологию [4].
ОРВИ, как правило, сопровождаются изнуряющим сухим непродуктивным кашлем, который может оказывать негативное влияние на качество жизни, нарушения сна, повседневную активность пациента. Поэтому важным компонентом лечения ОРВИ является своевременное и адекватное лечение кашля.
Из уровня техники известно соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион.
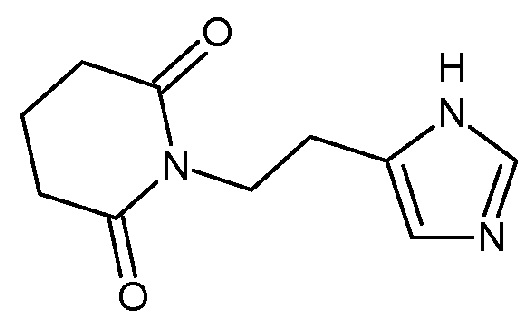
Соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион известно и описано в заявке на изобретение WO 2014/168522 (опубл. 16.10.2014). В указанной патентной заявке раскрывается способ получения данного соединения, а также исследована его противовирусная активность и применение для лечения риновирусов и других заболеваний верхних дыхательных путей.
В заявке WO 2015/072893 (опубл. 21.05.2015) описано применение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона для лечения заболеваний, ассоциированных с развитием эозинофильного воспаления, включая эозинофильную астму.
В заявке WO 2019/050429 (опубл. 14.03.2019) раскрывается применение соединения 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона для терапии заболеваний, связанных с аберрантной активностью фракталкина и моноцитарных хемоаттрактантных белков 1-4 (CCL2, CCL7, CCL8, CCL13), терапии болевого синдрома, лихорадки, пневмонии, бронхита, бронхиолита, альвеолита, ревматоидного артрита и псориаза.
Заявка WO 2020/106191 (опубл. 28.05.2020) описывает применение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона для терапии заболеваний, ассоциированных с аберрантным сигналингом интерферона гамма, таких, как синдром Шегрена, дерматомиозит, системная красная волчанка или системный склероз, а также при лечении пациентов, страдающих кашлем, и лечения расстройств у пациентов со стероидной резистентностью, таких, как астма, ревматоидный артрит.
В материалах WO 2020/106191 были показаны данные по оценке специфического фармакологического действия на моделях кашля, индуцированного ингалированием лимонной кислоты морским свинкам, эффективность препарата проявлялась в диапазоне доз 1,4-14 мг/кг животного, что эквивалентно 20-200 мг для человека.
Однако существует большое количество сложностей с экстраполяцией данных, полученных на животных. Даже если на стадии доклинического изучения у животных была установлена зависимость токсических эффектов от концентрации препарата в крови, существует ряд неизвестных на тот момент факторов, не позволяющих переносить эти данные на человека. Прежде всего, возможно существенное различие в биодоступности и метаболизме нового потенциального лекарственного средства у животных и человека. Фармакокинетическое моделирование на животных для расчета безопасных начальных доз для человека можно использовать только в тех случаях, когда требуется ввести небольшое число исходных различий. Но даже в этих случаях было показано, что наличие определенных факторов, например, различия в чувствительности рецепторов или их плотности у человека и животных, могут иметь очень большое значение при экстраполяции данных с животных на человека [5].
Таким образом, одним из ключевых вопросов остается выбор эффективной и безопасной дозы для человека.
Неожиданно, авторы настоящего изобретения обнаружили, что соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион является эффективным и безопасным при применении для лечения кашля, вызванного вирусными инфекциями, в дозе 80 мг в сутки.
Задачей настоящего изобретения является создание эффективного лекарственного средства при применении у пациентов с сухим непродуктивным кашлем на фоне вирусных инфекций, в том числе при COVID-19 и постковидном синдроме.
Техническим результатом является создание лекарственного средства, эффективного и безопасного при терапии и лечении кашля, вызванного вирусными инфекциями.
Поставленная задача решается, и технический результат достигается путем применения соединения 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона или его фармацевтически приемлемой соли для лечения и/или профилактики кашля у пациента человека, при котором активное соединение вводят в количестве 80 мг в сутки.
Еще одним вариантом настоящего изобретения является применение соединения 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона или его фармацевтически приемлемой соли для лечения и/или профилактики кашля у пациента человека, при котором соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль вводят 2 раза в сутки.
Предметом настоящего изобретения также является фармацевтическая композиция, содержащая соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый носитель для лечения и/или профилактики кашля, пригодная для перорального введения в дозе 80 мг в сутки.
Более предпочтительной является фармацевтическая композиция для лечения и/или профилактики кашля, включающая:
Авторами настоящего изобретения было неожиданно обнаружено, что данная фармацевтическая композиция является более стабильной (химическая стабильность действующего вещества при хранении, неизменность его кристаллической формы с течением времени) и технологичной (получение таблетки с хорошими механическими свойствами - прочность на раздавливание, сколы, устойчивость таблетки к нанесению пленочного покрытия) при использовании в качестве наполнителя безводной лактозы.
Таким образом, более предпочтительной является фармацевтическая композиция для лечения и/или профилактики кашля, включающая:
Более предпочтительной является фармацевтическая композиция для лечения и/или профилактики кашля, включающая:
Предметом настоящего изобретения также является применение фармацевтической композиции, содержащей 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый носитель для лечения и/или профилактики кашля у пациента человека, характеризующаяся тем, что 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль вводят в количестве 80 мг в сутки.
Более предпочтительным является применение фармацевтической композиции, содержащей 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый носитель для лечения и/или профилактики кашля, характеризующееся тем, что фармацевтическую композицию вводят 2 раза в сутки.
Предметом настоящего изобретения является применение соединения 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона или его фармацевтически приемлемой соли для получения фармацевтической композиции содержащей 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый носитель для лечения и/или профилактики кашля у пациента человека, характеризующаяся тем, что 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль вводят в количестве 80 мг в сутки.
Предметом настоящего изобретения также является способ лечения и/или профилактики кашля, включающий введение пациенту человеку, нуждающемуся в этом, соединения 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона или его фармацевтически приемлемой соли в количестве 80 мг в сутки.
Более предпочтительным является способ лечения и/или профилактики кашля, характеризующийся тем, что соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль вводят 2 раза в сутки.
Предметом настоящего изобретения также является соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемая соль для лечения и/или профилактики кашля, характеризующееся тем, что активное соединение вводят в количестве 80 мг в сутки.
Предметом настоящего изобретения также является соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемая соль для применения в качестве лекарственного средства, характеризующееся тем, что активное соединение вводят в количестве 80 мг в сутки.
Предметом настоящего изобретения является единичная дозированная форма для лечения и/или профилактики кашля у пациента человека, содержащая соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль в количестве 10-80 мг и фармацевтически пригодные вспомогательные вещества.
Более предпочтительной является единичная дозированная форма для лечения и/или профилактики кашля у пациента человека, содержащая соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль в количестве 10-40 мг.
Более предпочтительной является единичная дозированная форма для лечения и/или профилактики кашля у пациента человека, содержащая соединение 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль в количестве 40 мг.
Более предпочтительной является единичная дозированная форма для лечения и/или профилактики кашля у пациента человека, пригодная для перорального введения в дозе 80 мг в сутки.
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
Термин «лекарственное средство» означает вещество (или комбинацию веществ), вступающее в контакт с организмом человека или животного, проникающее в органы и ткани организма человека или животного, и предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней. К лекарственным средствам относятся фармацевтические субстанции и лекарственные препараты.
Термин «лекарственный препарат», «препарат» означает лекарственное средство в виде лекарственной формы, применяемой для лечения и профилактики заболевания.
Термин «лекарственная форма» означает состояние лекарственного препарата, соответствующее способам его введения и применения и обеспечивающее достижение необходимого лечебного эффекта.
Термин «фармацевтическая композиция» обозначает композицию, включающую в себя 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемые соли, сольваты, гидраты и, по крайней мере, один из компонентов выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, дезинтегранты, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от их природы, способа введения композиции и дозировки.
Термин «фармацевтически приемлемые соли» или «соли» включает соли активных соединений, которые получены с помощью относительно нетоксичных кислот. Примерами фармацевтически приемлемых нетоксичных солей могут служить соли, образованные неорганическими кислотами, такими как соляная, бромоводородная, фосфорная, серная и хлорная кислоты, или органическими кислотами, такими как уксусная, щавелевая, малеиновая, винная, янтарная, лимонная или малоновая кислоты, или полученные другими методами, используемыми в данной области. К другим фармацевтически приемлемым солям относятся адипинат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептанат, гексанат, гидройодид, 2-гидрокси-этансульфонат, лактобионат, лактат, лаурат, лаурил сульфат, малат, малеат, малонат, метансульфонат (мезилат), 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, полуфумарат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат (тозилат), ундеканат, валериат и подобные.
Термины «содержащий», «содержит» означает, что указанные комбинации, композиции и наборы включают перечисленные компоненты, но не исключают включение других компонентов.
Термины «лечение», «терапия» охватывают лечение патологических состояний у млекопитающих, предпочтительно у человека, и включают: а) снижение, б) блокирование (приостановку) течения заболевания, в) облегчение тяжести заболевания, т.е. индукцию регрессии заболевания, г) реверсирование заболевания или состояния, к которому данный термин применяется, или одного или более симптомов данного заболевания или состояния.
Термин «профилактика», «предотвращение» охватывает устранение факторов риска, а также профилактическое лечение субклинических стадий заболевания у млекопитающих, предпочтительно у человека, направленное на уменьшение вероятности возникновения клинических стадий заболевания. Пациенты для профилактической терапии отбираются на основе факторов, которые, на основании известных данных, влекут увеличение риска возникновения клинических стадий заболевания по сравнению с общим населением. К профилактической терапии относятся а) первичная профилактика и б) вторичная профилактика. Первичная профилактика определяется как профилактическое лечение у пациентов, клиническая стадия заболевания у которых еще не наступила. Вторичная профилактика - это предотвращение повторного наступления того же или близкого клинического состояния или заболевания.
В контексте настоящего изобретения термин «профилактика», «предотвращение» относится в том числе к профилактике постковидного синдрома и кашля на фоне хронических заболеваний легких, таких как бронхиальная астма, ХОБЛ. Также данный термин относится к профилактике тяжелых и затяжных течений кашля при эпизодах вирусных заболеваний у часто болеющих людей.
Представленные ниже примеры иллюстрируют, но не охватывают все возможные варианты осуществления изобретения и не ограничивают изобретение.
Пример 1. Получение таблеток 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона
1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион, наполнитель, разрыхлитель, просеивают через сито с установленным диаметром ячеек. Просеянные компоненты помещают в смеситель, где смешивают в течение времени необходимого для получения однородной смеси.
К полученной смеси добавляют лубриканты, глиданты и другие опудривающие вещества и проводят смешивание.
Полученную массу таблетируют на роторном автомате прессования. Получают таблетки белого или белого с кремоватым оттенком цвета, с цельными краями, гладкой и однородной поверхностью, без трещин и сколов.
Дополнительно таблетки покрывают пленочным покрытием.
В качестве наполнителя предпочтительно использовать безводную лактозу и комбинированные наполнители, в составе которых входит лактоза, микрокристаллическая целлюлоза, маннитол или их смеси.
Разрыхлитель выбирают из кросповидона, повидона, коповидона, карбоксиметилкрахмала натрия, натрия гликолята крахмала и их смесей.
Лубрикант выбрают из талька, солей стеариновой кислоты, солей стерилфумарата, кремния диоксида коллоидного и их смесей.
Состав таблетки:
Более предпочтительными являются следующие составы:
В качестве пленочного покрытия используют Opadry II (белый).
Пример 2. Исследование активности 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона
Было проведено двойное слепое плацебо-контролируемое многоцентровое рандомизированное клиническое исследование фазы II.
Исследование проводилось с участием пациентов с сухим непродуктивным кашлем на фоне ОРВИ.
Пациенты были случайным образом распределены на 4 группы:
1-я группа (n=35) пациентов получала препарат 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона по 1 таблетке 2 раза в день. Суточная доза: 20 мг;
2-я группа (n=35) пациентов получала препарат 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона по 2 таблетки 2 раза в день. Суточная доза: 40 мг;
3-я группа (n=35) пациентов получала препарат 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона по 4 таблетки 2 раза в день. Суточная доза: 80 мг.
4-я группа (n=36) пациентов получала плацебо:
- подгруппа 4-1 (n=12): по 1 таблетке 2 раза в день;
- подгруппа 4-2 (n=12): по 2 таблетки 2 раза в день;
- подгруппа 4-3 (n=12): по 4 таблетки 2 раза в день.
Всего в исследование принял участие 141 пациент.
Оценка эффективности исследуемых препаратов была основана на статистическом анализе первичных и вторичных конечных точек:
Снижение частоты приступов кашля на ≥ 50% к 5 дню относительно визита 1.
Для анализа конечной точки проводились попарные сравнения между группами препарата 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона (группы 1, 2, 3) и соответствующими подгруппами плацебо (группы 4-1, 4-2, 4-3), сравнения между группами препарата 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона (группы 1, 2, 3) и объединенной группой плацебо (группа 4), а также сравнения групп препарата 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона (группы 1, 2, 3) между собой. В соответствии с протоколом исследования необходимо было оценить снижение частоты приступов кашля на ≥ 50% к 5 дню относительно визита 1. В оценку вошли данные за 24 ч до 1 и 5 дня.
Статистически значимые различия в долях пациентов, достигших снижения частоты приступов кашля на ≥ 50% к 5 дню относительно визита 1, выявлены:
между группой 3 (суточная доза: 80 мг) и группой 4-3 (плацебо) (p=0,0071). Доля пациентов, достигших снижения частоты приступов кашля на ≥ 50% к 5 дню, в группе 3 составила 71,43% (25/35), а в группе 4-3 - 25,00% (3/12). Разница в долях между группами 3 и 4-3 составила 46,43%, 95% ДИ [9,59%;69,08%];
между группой 3 (суточная доза: 80 мг) и группой 4 (плацебо) (p=0,00003). Доля пациентов, достигших снижения частоты приступов кашля на ≥ 50% к 5 дню, в группе 3 составила 71,43% (25/35), а в группе 4 - 22,22% (8/36). Разница в долях между группами 3 и 4 составила 49,21%, 95% ДИ [24,23%;66,81%];
между группами 1 (суточная доза: 20 мг) и 3 (суточная доза: 80 мг) (p=0,0157), а также группами 2 (суточная доза: 40 мг) и 3 (суточная доза: 80 мг) (p=0,0040). В группе 1 доля пациентов, достигших снижения частоты приступов кашля на ≥ 50% к 5 дню относительно визита 1, составила 0,4286 (42,86%), в группе 2 - 0,3714 (37,14%), в группе 3 - 0,7143 (71,43%).
Время (дни) от визита 1 до достижения клинического излечения кашля
В соответствии с протоколом исследования проводилась оценка времени (в днях) от визита 1 до достижения клинического излечения кашля. Под клиническим излечением кашля понимается наличие ≤ 1 балла по разделам «дневной кашель» и «ночной кашель» Шкалы дневного и ночного кашля в течение не менее 3-х дней подряд. В оценку вошло время от визита 1 до первого дня из последовательных дней, на которых зарегистрировано ≤ 1 балла по разделам «дневной кашель» и «ночной кашель» Шкалы дневного и ночного кашля.
Медиана времени от визита 1 до достижения клинического излечения кашля в группах 1 и 2 составила 8 дней, в группе 3 - 5, дней в группе 4 - 12 дней.
Доля пациентов, которым был назначен ацетилцистеин по поводу перехода сухого кашля во влажный
В соответствии с протоколом исследования проводилась оценка доли пациентов, которым был назначен ацетилцистеин по поводу перехода сухого кашля во влажный.
В группе 1 доля пациентов, которым был назначен ацетилцистеин по поводу перехода сухого кашля во влажный, составила 14,29% (5/35), в группе 2 - 11,43% (4/35), в группе 3 - 8,57% (3/35), в группе 4 - 41,67% (15/36).
Таким образом, проведенное клиническое исследование по оценке эффективности и безопасности применения препарата 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-диона, у пациентов с сухим непродуктивным кашлем на фоне острой респираторной вирусной инфекции продемонстрировало превосходство в суточной дозе 80 мг, над плацебо. Было показано снижение частоты приступов кашля и более короткое время достижения клинического излечения от кашля. Кроме того, препарат является безопасным в указанной дозировке.
Список литературы
1. Селюк М.Н., Козачок Н.Н., Селюк О.В. Современные алгоритмы диагностики и лечения кашля // Пульмонология. Пракикум лiкаря. - 2013. - №3 (304). - С. 40-42.
2. Ziad C Boujaoude, Melvin R Pratter. Clinical approach to acute cough. Lung. 2010 Jan;188 Suppl 1(Suppl 1):S41-6. Epub 2009 Aug 22.
3. Акопов А.Л., Александрова Е.Б., Илькович М.М. и др. Ренгалин - новый эффективный и безопасный препарат в лечении кашля. Результаты многоцентрового сравнительного рандомизированного клинического исследования у больных с острыми респираторными инфекциями // Антибиотики и химиотерапия. - 2015. - Т. 60. - № 1- 2. - С. 19-25.
4. Шеффер А., Кер М.С., Джианетти Б.М., Булитта М. Результаты рандомизированного, контролируемого, двойного слепого, многоцентрового исследования эффективности и безопасности препарата на основе сухого экстракта листьев плюща (EA 575®) по сравнению с плацебо при лечении острого кашля у взрослых // Журнал поликлиника. - 2019. - №5 (2). - С. 71-78.
5. Гуськова Т.А. Доклиническое токсикологическое изучение лекарственных средств как гарантия безопасности проведения их клинических исследований // Токсикологический вестник. 2010. №5 (104).
Изобретение относится к области фармацевтики и медицины, а именно к лечению и профилактике кашля. Раскрывается применение фармацевтической композиции, включающей 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион 5,0-25,0 мас.% и вспомогательные вещества, мас.%: микрокристаллическую целлюлозу 35,0-50,0, карбоксиметилкрахмал натрия 0,5-1,0, тальк 0,1-0,5, магния стеарат 0,1-1,5, лактозу безводную 35,0-45,0, для лечения и профилактики кашля у пациента-человека. Технический результат изобретения заключается в эффективном и безопасном лечении кашля, в том числе вызванного вирусными инфекциями. 3 з.п. ф-лы, 2 пр.
1. Применение фармацевтической композиции, включающей, мас.%:
для лечения и профилактики кашля у пациента-человека.
2. Применение по п.1, отличающееся тем, что фармацевтическая композиция включает, мг:
3. Применение по п.1, характеризующееся тем, что 1-(2-(1Н-имидазол-4-ил)этил)пиперидин-2,6-дион или его фармацевтически приемлемую соль вводят в количестве 80 мг в сутки.
4. Применение по п.3, характеризующееся тем, что фармацевтическую композицию вводят 2 раза в сутки.
| WO 2020106191 A1, 28.05.2020 | |||
| EA 201792071 A1, 28.09.2018 | |||
| ПРИМЕНЕНИЕ ПРОИЗВОДНОГО ГЛУТАРИМИДА ДЛЯ ПРЕОДОЛЕНИЯ РЕЗИСТЕНТНОСТИ К СТЕРОИДАМ И ТЕРАПИИ ЗАБОЛЕВАНИЙ, АССОЦИИРОВАННЫХ С АБЕРРАНТНЫМ СИГНАЛИНГОМ ИНТЕРФЕРОНА ГАММА | 2018 |
|
RU2712281C1 |
| WO 2019050429 A1, 14.03.2019 | |||
| RU 2020121363 A, 27.12.2021. | |||
Авторы
Даты
2024-05-23—Публикация
2022-03-18—Подача