Изобретение относится к химической технологии, в частности к способу получения перфторированного винилового эфира, содержащего сульфофторидную группу, а именно 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена. Перфторированные мономеры, содержащие сульфофторидные группы могут быть использованы для получения фторполимеров с ионообменными свойствами (так называемых иономеров) для получения ионообменных мембран.
5-Трифторметил-3,6-диокса-8-сульфонилфторидперфтороктен (далее PSVE), может быть представлен структурной формулой:
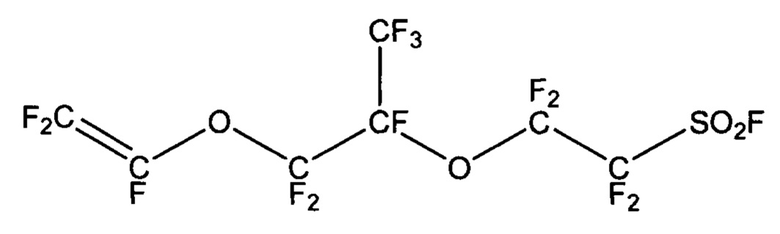
Основные способы получения PSVE можно описать следующими стадиями:
1) контактирование 2,5-ди(трифторметил)-3,6-диокса-8-сульфонил-фторидперфтороктаноилфторида с суспензией карбоната натрия или калия в растворителе (диглим), или без растворителя при температуре 20-90°С с образованием натриевой или калиевой соли 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктановой кислоты;
2) пиролиз соли 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктановой кислоты в растворителе или без него при температуре от 120 до 250°С с образованием PSVE.
Реакция получения PSVE протекает по следующей схеме:
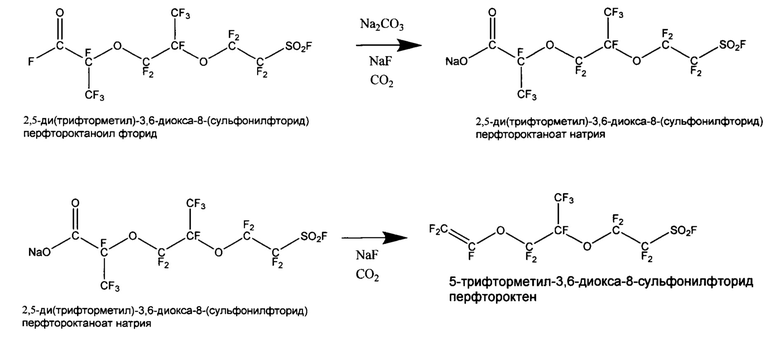
Сложность получения PSVE связана с образованием в ходе процесса примеси 2-гидро-1,1,1,2,4,4,5,7,7,8,8-ундекафтор-5-трифторметил-8-сульфонилфторид-3,6-диоксаоктана (далее H-PSVE), которая может быть представлена структурной формулой:
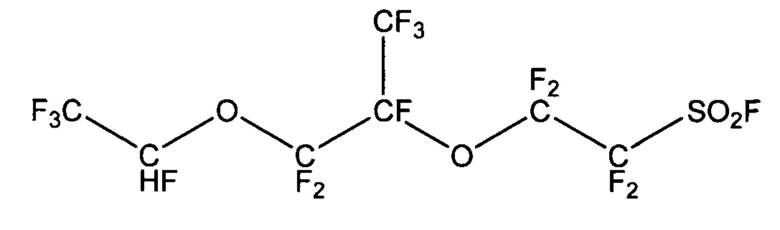
Примесь H-PSVE является трудноотделяемой, разница в температурах кипения PSVE и H-PSVE составляет менее 5°С, что не позволяет получать PSVE высокой чистоты с высоким выходом и малым количеством образующихся отходов. Наличие большого количества H-PSVE в PSVE не позволяет получать мономер с высокой молекулярной массой, в связи с чем показатель количественного содержания H-PSVE в PSVE является критически важным. H-PSVE образуется из-за наличия в исходном для PSVE 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноил фторида продуктов гидролиза, а также из-за наличия влаги в реагентах и растворителях. Известен способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена (KR 1956826, 12.03.2019) пропусканием через нагревательную камеру раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия, подающегося через форсунку. Недостатками данного способа является недостаточная степень конверсии и невысокий выход продукта (60-80%). Содержание примеси H-PSVE в продукте после синтеза авторами не приведено.
Известен также способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена (CN 102992969 А, 27.03.2013), который заключается в получении раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия в диглиме. Полученный раствор карбоксилата подается в течение 6 часов в тонкопленочный испаритель при температуре 200-250°С. Продукт пиролиза через теплообменник попадает в сборник, откуда подается в ректификационную колонну. Недостатками данного способа является отсутствие стадии разделения целевого продукта от растворителя, что приводит к дополнительным потерям при проведении стадии ректификации. Несмотря на высокий выход (85-95%) содержание примеси H-PSVE в продукте после синтеза авторами не приведено. Известен также патент (CN 102702035 А, 03.10.2012), где описан способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена продукта в 2-шнековом экструдере CTE-SC-25. В экструдер подается сухой карбонат натрия и 2,5-ди(трифторметил)-3,6-диокса-8-(сульфонилфторид)перфтороктаноилфторид при температуре 60-270°С. К преимуществам «сухого» способа пиролиза можно отнести получения более чистого продукта из-за отсутствия влаги в растворителе. К недостаткам относится низкий выход целевого продукта (73-88%).
Известен также способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена (RU 2272806 С1, 27.03.2006), который заключается в контактировании 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида с суспензией карбоната натрия в диглиме с образованием натриевой соли 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктановой кислоты, последующего пиролиза соли при повышенной температуре с получением 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена и выделения последнего из зоны реакции отгонкой с дальнейшей ректификацией на колонке эффективностью 40 теоретических тарелок. В результате получают целевой продукт чистотой 99,6% и выходом 92,8%. К недостаткам данного способа получения можно отнести сложность аппаратурного оформления производства. Известен способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена (PSVE) (CN 114773239 А, 22.07.2022), взятый за прототип, который заключается во взаимодействии 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида с карбонатом натрия в среде диглима при нагревании (50°С~60°С) с получением раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия. Полученный раствор далее обрабатывается гидридом натрия для удаления остаточной влаги и проводится процесс высокотемпературного пиролиза в среде высокотемпературного растворителя, например, диглим, ДМСО, ДМСО, перфторэфирное масло, при температуре 190°С~220°С с образованием целевого 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена с содержанием H-PSVE менее 20 м.д. и выходом 93-94%.
Недостатком известного способа является проведение процесса при температуре 190°С~220°С, что приводит к усложнению технологического оборудования, а также разделение процессов дозировки раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия и разделения слоев целевого 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена и растворителя, что увеличивает время цикла и усложняет технологию процесса. Кроме этого, использование в производстве гидрида натрия повышает его пожароопасность. Технической задачей настоящего изобретения является упрощение технологии процесса и повышение его безопасности при сохранении высокого выхода и высокой чистоты целевого продукта.
Поставленная задача достигается предложенным способом получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена включающим взаимодействие 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида с карбонатом натрия в среде диглима при нагревании, обработку полученного раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия гидридом щелочного металла и последующий пиролиз обработанного 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия в среде диглима, отличающийся тем, что исходный 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид предварительно пропускают через колонку с безводным фторидом калия, в качестве гидрида щелочного металла используют гидрид кальция, а процесс пиролиза проводят путем подачи обработанного гидридом кальция 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия в кипящий безводный диглим с одновременным отделением фторорганического слоя при температуре от -10°С до -20°С на фазоразделителе, где первую порцию продукта, содержащего повышенное содержание примеси 2-гидро-1,1,1,2,4,4,5,7,7,8,8-ундекафтор-5-трифторметил-8-сульфонилфторид-3,6-диоксаоктана, в количестве 1-3% отбирают в качестве предгона, с последующим выделением целевого продукта.
Стадию взаимодействия 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида с карбонатом натрия в среде диглима проводят, преимущественно, при температуре 30-40°С и давлении 100-800 кПа. Исходные реагенты для приготовления 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия расходуют в мольном отношении диглим : карбонат натрия : 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид, равном 2,05:1,11:1. Процесс пиролиза раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия в диглиме проводят при температуре 140-165°С.
Сущность изобретения состоит в том, что предложен способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена взаимодействием 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида, пропущенного через колонку с безводным фторидом калия для удаления примесей частичного гидролиза, с карбонатом натрия в диглиме с получением раствора соответствующего карбоксилата, обработка полученного раствора гидридом кальция для удаления остатков влаги, подачей обработанного раствора карбоксилата в кипящий безводный диглим с одновременным отделением фторорганического слоя при температуре от -10°С до -20°С на фазоразделителе, где первую порцию продукта, содержащего повышенное содержание H-PSVE, в количестве 1-3% отбирают в качестве предгона. Полученный PSVE с содержанием H-PSVE менее 0,005%, отмывают раствором карбоната натрия для удаления примесей растворителя, сушат над безводным сульфатом магния и перегоняют. Выход целевого продукта на поданный 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид составляет 94%. Способ отличается тем, что задача по снижению содержанию примеси Н-PSVE достигается за счет обработки 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида безводным фторидом калия для удаления примесей в результате частичного гидролиза 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида. Способ отличается и тем, что задача по снижению содержанию примеси Н-PSVE достигается за счет обработки раствора натриевой соли 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата достаточно безопасным в производстве и доступным гидридом кальция, что позволяет убрать остаточную влагу из раствора.
Способ отличается и тем, что пиролиз проводится с одновременным отделением из отгона фторорганического слоя, содержащего преимущественно 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид с использованием фазоразделителя при температуре от -10°С до -20°С, что позволяет получать целевой 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид с минимальным содержанием остаточно растворенного растворителя.
Способ отличается и тем, что во время пиролиза проводится отбор предгона, содержащего повышенное количество H-PSVE, что позволяет получать целевой PSVE с высоким выходом и низким содержанием примесей. Техническим результатом предлагаемого изобретения является упрощение технологии процесса и повышение его безопасности с получением целевого продукта с высоким выходом (93-94%) и низким содержанием примесей. Изобретение иллюстрируется примерами, не ограничивающими его объем.
Пример 1.
А. Получение раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия
Синтез 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия проводят в реакторе из нержавеющей стали, вместимостью 5000 см3, снабженном загрузочным люком, мешалкой, термостатируемой рубашкой, термометром, манометром, дозировочным насосом, системой дозировки газообразных реагентов, донным клапаном, патронным фильтром. В реактор загружают 537 г (4,0 моль) диглима с содержанием влаги менее 0,01% и 230 г (2,17 моль) прокаленного карбоната натрия. Реактор продувают азотом и вакуумируют до остаточного давления 1 кПа. Далее при помощи дозировочного насоса, соединенного с реактором синтеза через колонку из нержавеющей стали (10*2 см), заполненной 50 г (0,86 моль) безводным фторидом калия, в течение 2 часов дозируют 1000 г (1,95 моль) 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида так, чтобы температура реакционной массы не превышала 40°С. После окончания дозировки проводят выдержку при температуре 40°С в течение 4 часов до полной конверсии, давление в реакторе при этом возрастает до 800 кПа. Далее сбрасывают избыточное давление из реактора в течение 2 часов и через загрузочный люк загружают 2 г (0,05 моль) гидрида кальция, реакционную массу выдерживают дополнительно 4 часа при интенсивном перемешивании. Далее реакционную массу давлением азота в 200 кПа фильтруют через патронный фильтр (фильтрующий элемент PTFE 10 мкм) в промежуточную емкость из нержавеющей стали. Конверсия 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида определяется методом ЯМР и составляет более 99%.
Б. Пиролиз раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия
Синтез 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена проводят в реакторе из нержавеющей стали, вместимостью 5000 см3, снабженном мешалкой, термостатируемой рубашкой, термометром, манометром, дозировочным насосом, системой дозировки газообразных реагентов, донным клапаном, ректификационной колонной длиной 1,5 м (насадка спирально-призматическая из нержавеющей стали 2,0*2,0 мм) с фазоразделителем из толстостенного стекла с рубашкой, охлаждаемой до -10°С. В реактор загружают 1863 г (13,9 моль) диглима с содержанием влаги менее 0,01% и 2 г гидрида кальция. Нагревают диглим до 165°С для начала кипения и орошения колонны. Далее насосом дозатором под слой жидкости проводят дозировку раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия из примера 1А в течение 6 часов. После начала дозировки в фазоразделителе начинает копиться фторорганический слой. Первые 10 г фторорганического слоя, содержащего повышенное количество H-PSVE, отбирают в качестве предгона. Последующий продукт имеет содержание H-PSVE менее 0,005%) и отбирается в количестве 840 г одновременно с дозировкой раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия из примера 1А. Продукт отмывается 5% раствором карбоната натрия и далее дистиллированной водой в объемном соотношении 1:1:1. Отмытый продукт сушат над 10 г (0,08 моль) безводного сульфата магния и перегоняют, отбирая фракцию с температурой кипения 132,5-133,5°С в количестве 820 г (1,84 моль, выход 94%) в пересчете на поданный 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноил фторид.
Пример 2.
А. Получение раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия
Синтез 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия проводят в реакторе из нержавеющей стали, вместимостью 5000 см3, снабженном загрузочным люком, мешалкой, термостатируемой рубашкой, термометром, манометром, дозировочным насосом, системой дозировки газообразных реагентов, донным клапаном, патронным фильтром, сдувочной линией с барботером. В реактор загружают 537 г (4,0 моль) диглима с содержанием влаги менее 0,01% и 230 г (2,17 моль) прокаленного карбоната натрия. Реактор продувают азотом. Далее при помощи дозировочного насоса, соединенного с реактором синтеза через колонку из нержавеющей стали (10*2 см), заполненной 50 г (0,86 моль) безводным фторидом калия, в течение 4 часов дозируют 1000 г (1,95 моль) 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноил фторида так, чтобы температура реакционной массы не превышала 30°С. После окончания дозировки проводят выдержку при температуре 30°С в течение 4 часов до прекращения газовыделения (контроль по сдувочной линией с барботером). Далее через загрузочный люк загружают 2 г (0,05 моль) гидрида кальция, реакционную массу выдерживают дополнительно 4 часа при интенсивном перемешивании. Далее реакционную массу давлением азота в 200 кПа фильтруют через патронный фильтр (фильтрующий элемент PTFE 10 мкм) в промежуточную емкость из нержавеющей стали. Конверсия 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноил фторида определяется методом ЯМР и составляет более 99%.
Б. Пиролиз раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия
Синтез 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена проводят в реакторе из нержавеющей стали, вместимостью 5000 см3, снабженном мешалкой, термостатируемой рубашкой, термометром, манометром, дозировочным насосом, системой дозировки газообразных реагентов, донным клапаном, ректификационной колонной длиной 1,5 м (насадка спирально-призматическая из нержавеющей стали 2,0*2,0 мм) с фазоразделителем из толстостенного стекла с рубашкой, охлаждаемой до -20°С. В реактор загружают 1863 г (13,9 моль) диглима с содержанием влаги менее 0,01% и 2 г гидрида кальция. Нагревают диглим до 140°С. Далее насосом дозатором под слой жидкости проводят дозировку раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия из примера 2А в течение 7 часов. После начала дозировки реакционная масса начинает кипеть и в фазоразделителе начинает копиться фторорганический слой. Первые 10 г фторорганического слоя, содержащего повышенное количество H-PSVE, отбирают в качестве предгона. Последующий продукт имеет содержание H-PSVE менее 0,005%) и отбирается в количестве 831 г одновременно с дозировкой раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия из примера 2А. Продукт отмывается 5% раствором карбоната натрия и далее дистиллированной водой в объемном соотношении 1:1:1. Отмытый продукт сушат над 10 г (0,08 моль) безводного сульфата магния и перегоняют, отбирая фракцию с температурой кипения 132,5-133,5°С в количестве 811 г (1,82 моль, выход 93%) в пересчете на поданный 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторид)перфтороктаноилфторида | 2023 |
|
RU2820722C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-ТРИФТОРМЕТИЛ-3,6-ДИОКСА-8-СУЛЬФОНИЛФТОРИДПЕРФТОРОКТЕНА | 2004 |
|
RU2272806C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-ТРИФТОРМЕТИЛ-3,6-ДИОКСА-8-СУЛЬФОНИЛФТОРИДПЕРФТОРОКТЕНА | 2010 |
|
RU2456270C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,5-ДИ(ТРИФТОРМЕТИЛ)-3,6-ДИОКСА-8-СУЛЬФОНИЛФТОРИДПЕРФТОРОКТАНОИЛФТОРИДА | 2004 |
|
RU2269513C1 |
| Способ получения десфлурана | 2024 |
|
RU2833270C1 |
| Способ получения перфтор-4-(фторсульфонил)бутилвинилового эфира | 2022 |
|
RU2800857C1 |
| Способ получения полифтораллилокси-СОЕдиНЕНий | 1977 |
|
SU795452A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОР-3-ОКСА-ПЕНТЕН-СУЛЬФОНИЛФТОРИДА | 2013 |
|
RU2546109C1 |
| 1,1,1,2,3,3-ГЕКСАФТОР-2-ЙОД-3-МЕТОКСИПРОПАН В КАЧЕСТВЕ ПОЛУПРОДУКТА ДЛЯ ПОЛУЧЕНИЯ 2,3,3,3-ТЕТРАФТОР-2-ЙОДПРОПИОНИЛ ФТОРИДА И СПОСОБ ПОЛУЧЕНИЯ ПОСЛЕДНЕГО | 2017 |
|
RU2641110C1 |
| ПРОИЗВОДНЫЕ УРАЦИЛА, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ (ВАРИАНТЫ) | 2001 |
|
RU2264395C2 |
Изобретение относится к химической технологии, а именно к способу получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена. Способ заключается во взаимодействии 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида с карбонатом натрия в среде диглима при нагревании, обработке полученного раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия гидридом щелочного металла и пиролизе обработанного 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия в среде диглима. При этом исходный 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид предварительно пропускают через колонку с безводным фторидом калия, в качестве гидрида щелочного металла используют гидрид кальция, а процесс пиролиза проводят путем подачи обработанного гидридом кальция 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия в кипящий безводный диглим с одновременным отделением фторорганического слоя при температуре от -10°С до -20°С на фазоразделителе, где первую порцию продукта, содержащего повышенное содержание примеси 2-гидро-1,1,1,2,4,4,5,7,7,8,8-ундекафтор-5-трифторметил-8-сульфонилфторид-3,6-диоксаоктана, в количестве 1-3% отбирают в качестве предгона, с последующим выделением целевого продукта. Технический результат заключается в способе получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена, характеризующемся упрощенной и более безопасной технологией процесса с сохранением высокого выхода и высокой чистоты целевого продукта. 2 з.п. ф-лы, 2 пр.
1. Способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена, включающий взаимодействие 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида с карбонатом натрия в среде диглима при нагревании, обработку полученного раствора 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия гидридом щелочного металла и пиролиз обработанного 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия в среде диглима, отличающийся тем, что исходный 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид предварительно пропускают через колонку с безводным фторидом калия, в качестве гидрида щелочного металла используют гидрид кальция, а процесс пиролиза проводят путем подачи обработанного гидридом кальция 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноата натрия в кипящий безводный диглим с одновременным отделением фторорганического слоя при температуре от -10°С до -20°С на фазоразделителе, где первую порцию продукта, содержащего повышенное содержание примеси 2-гидро-1,1,1,2,4,4,5,7,7,8,8-ундекафтор-5-трифторметил-8-сульфонилфторид-3,6-диоксаоктана, в количестве 1-3% отбирают в качестве предгона, с последующим выделением целевого продукта.
2. Способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена по п. 1, отличающийся тем, что стадию взаимодействия 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторида с карбонатом натрия в среде диглима проводят, преимущественно, при температуре 30-40°С и давлении 100-800 кПа при мольном соотношении исходных реагентов диглим : карбонат натрия : 2,5-ди(трифторметил)-3,6-диокса-8-сульфонилфторидперфтороктаноилфторид, равном 2,05:1,11:1.
3. Способ получения 5-трифторметил-3,6-диокса-8-сульфонилфторидперфтороктена по п. 1, отличающийся тем, что процесс пиролиза проводят при температуре 140-165°С.
| CN 114773239 A, 22.07.2022 | |||
| СПОСОБ ПОЛУЧЕНИЯ 5-ТРИФТОРМЕТИЛ-3,6-ДИОКСА-8-СУЛЬФОНИЛФТОРИДПЕРФТОРОКТЕНА | 2004 |
|
RU2272806C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-ТРИФТОРМЕТИЛ-3,6-ДИОКСА-8-СУЛЬФОНИЛФТОРИДПЕРФТОРОКТЕНА | 2010 |
|
RU2456270C2 |
| CN 102992969 A, 24.12.2012 | |||
| СЕМЕНОВ С | |||
| Г | |||
| и др., Синтез и свойства 2-гидро-1,1,1,2,4,4,5,7,7,8,8-ундекафтор-5-трифторметил-8-сульфонилфторид-3,6-диоксаоктана, Фторные заметки, 2011, том 78, номер 5, | |||
Авторы
Даты
2024-06-07—Публикация
2023-12-08—Подача