Изобретение относится к медицине и может быть использовано в хирургической и ортопедической стоматологии, так же в экспериментальной медицине.
Удаление дентальных имплантатов вследствие воспалительного процесса тканей, окружающих имплантата, наблюдается у 10-15% пациентов.
Патологический процесс может возникнуть как сразу, так и через несколько лет после установки дентальных имплантатов. Главной причиной считается скопление патогенной микрофлоры в периимплантных тканях на фоне низкого уровня гигиены полости рта, что приводит к воспалению тканей вокруг установленных имплантатов.
Восстановление утраченной костной ткани вокруг пришеечной дентального имплантата необходимо в клинических случаях, когда в средней и апикальной частях его (имплантата) сохранилась остеоинтеграция, поддерживающая стабильность имплантата при функциональных нагрузках. Такое состояние может возникать в случаях неполного погружения имплантата во время его установки, дефиците костной ткани в пришеечной области при непосредственной (одномоментной с удалением зуба) имплантации при сильном разрушении стенок лунки, при периимлантитах, при убыли костной ткани в пришеечной области в процессе функционирования имплантата из-за неудовлетворительной гигиены полости рта, погрешностей в супраструктурах имплантатов, наличии функциональных недогрузок и перегрузок имплантата при эксплуатации.
При убыли костной ткани в пришеечной области обнажается поверхность имплантата и возникает контакт с десной. Десна соприкасается с телом имплантата, оказывается в неестественных, крайне неблагоприятных условиях, что впоследствии приводит к воспалительному процессу десны, который при отсутствии надлежащего лечения приводит к потере имплантата.
В полости рта при нарушении соединения «имплантат-кость» происходит загрязнение пришеечной части имплантата микроорганизмами, что приводит к образованию гранулематозной ткани, что, возможно, приведет к потере имплантата. Поверхность пришеечной части имплантата нелегко поддается дезинфекции, вследствие чего, в окружающих имплантат тканях постоянно поддерживается воспалительный процесс, который усиливает дальнейшую убыль костной ткани. Особенно неблагоприятные условия возникают для слизистой оболочки, которая контактирует с обнаженной шероховатой поверхностью имплантата. В данных условиях связь десны с имплантатом нарушается, система «имплантат - десна» перестает быть защитным барьером для остеоинтегрированной части имплантата и превращается в разрушающий фактор.
Существует несколько причин негативного результата, к которым относят: погрешности дезинфекции и стерилизации зоны вмешательства; недостаточная активность остеопластического материала; отсутствие гарантированных условий для локального репаративного остеогенеза, включая создание контактного остеогенеза, лежащего в основе остеоинтеграции имплантатов.
Создание модели периимплантита в эксперименте на животных необходимо для прогнозирования возможных исходов после установки дентальных имплантатов, а также предназначена для совершенствования лечения периимплантита.
В результате проведенного патентного поиска отобраны следующие аналоги.
Для создания модели периимплантита некоторые авторы применяли методы, аналогичные методу формирования пародонтита. Например, Т. Berglundh, Т. Lindhe (1996) разработали экспериментальную модель периимплантита на собаках. Суть способа состоит во введении лигатуры в десневую борозду, что приводит к формированию патологического кармана с культивированием поддесневой бактериальной флоры и в последующем - воспалению тканей десны (периимплантный мукозит) и формированию воспалительного поражения кости (периимплантит) [1].
Известна модель периимплантита, которую формировали у половозрелых приматов. Для обеспечения скопления патогенной микрофлоры вокруг имплантатов в периимплантатную борозду авторы закладывали ватные лигатуры [2].
Известен способ формирования экспериментальной модели периимплантита на белых крысах, которым после удаления первого моляра верхней челюсти проводили установку имплантата. Нестабильное положение имплантата в лунке удаленного зуба за счет недостаточного количества костной ткани и дополнительно наложения лигатуры из хлопковой нити на область шейки имплантата приводили к формированию воспаления и развитию периимплантита с эффективностью 86,4%. [3].
Недостатками представленных экспериментальных моделей периимплантита являются неопределенные сроки окончания формирования модели периимплантита, недостаток места в челюстях экспериментальных животных для установки имплантатов определенного размера, необходимость удаления зубов у экспериментальных животных с последующей установкой дентальных имплантатов. Совокупность вышеперечисленных факторов существенно влияет на качество формирования экспериментальной модели.
Наиболее близким аналогом был выбран способ создания экспериментальной модели периимплантита, при котором у взрослых овец проводили перфорацию кортикальной пластинки челюстной кости по вершине альвеолярного гребня с помощью хирургической фрезы диаметром 2 мм со скоростью вращения 1200 об/мин на глубину 5 мм без охлаждения. Устанавливали дентальный имплантат диаметром 2,5 мм, длиной 10 мм, с крутящим моментом 15 Н/см, на внутрикостную часть которой предварительно накручивали лигатуру из хлопковой нити (Патент РФ №2730970).
Недостатком данной модели является фиксация лигатуры из хлопковой ткани, так как данный материал может частично резорбироваться под действием физических и химических факторов полости рта. Кроме этого, модель периимплантита формировалась в течение 30 дней, что не является окончательным сроком формирования модели, так как из описания следует, что к данному сроку не было потеряно ни одного имплантата, но при этом плотность костной ткани вокруг имплантата была существенно снижена до 250 ЕД по шкале Хаунсфилда. В связи с этим, срок окончания формирования модели остается неуточненным. При этом также не уточняется уровень резорбции костной ткани в области шейки имплантата.
Задачей предлагаемого технического решения является разработка способа экспериментальной модели периимплантита с понятными сроками окончания формирования модели и получением полноценной модели с резорбцией костной ткани вокруг шейки имплантата с сохранением его устойчивости.
Техническим результатом, полученным от использования предлагаемого способа создания экспериментальной модели периимплантита, является возможность получить патологический очаг без механического повреждения тканей, окружающих имплантат и ускорить патологические процессы.
Для проведения исследования и создания уникальной модели периимплантита использовали экспериментальных животных (Новозеландских белых кроликов) в количестве 36 голов для получения статистически достоверных результатов. Животные были поделены на две группы - основную и контрольную по 18 голов в каждой группе.
Кроликам были установлены дентальные имплантаты по классическому хирургическому протоколу. Операции на животных проводили с соблюдением анестезиологического протокола под внутривенным наркозом с использованием Ксилазина (4-6 мг/кг) внутримышечно, затем через 20 минут вводили Золетил-100 (5-10 мг/кг). Таким образом, была обеспечена анальгезия и релаксация в течение 30-40 мин.
В обеих группах проводили препарирование кортикального слоя в промежутке между молярами и резцами фрезой со скоростью вращения 2500 об/мин и костной ткани челюсти с использованием фрезы под имплантат диаметром 3,2 мм на глубину 6 мм с охлаждением с применением физиологического раствора. Затем проводили установку дентального имплантата диаметром 3,7 мм, длиной 7 мм машинным способом с крутящим моментом 25 Н/см, контроль которого производился с помощью физиодиспенсера. В обеих группах устанавливали в имплантат винты-заглушки и ушивали раны наглухо.
Диаметр фрезы для имплантата диаметром 3,7 использовали 3,2 намеренно для создания отверстия чуть меньше по диаметру, чтобы добиться первично стабилизации имплантата, препарирование на глубину 5 мм достаточно для установки имплантата без заглубления длиной 7 мм.
Через 5 недель (35 суток) после установки имплантатов после достижения остеоинтеграции имплантатов в основной группе производился линейный разрез для создания доступа к имплантату, извлекался винт-заглушка. Затем к винту-заглушке закрепляли лигатурную проволоку диаметром 0,5 мм с использованием кламмерных щипцов закручивали вокруг винта, обрезали скрученную лигатуру с использованием кусачек, таким образом, чтобы оставался конец длиной 5 мм. После этого устанавливали винт-заглушку в имплантат. Далее рану ушивали таким образом, чтобы скрученный конец проволоки выходил за пределы шва примерно на 2-3 мм. В контрольной группе никаких дополнительных манипуляций не проводили.
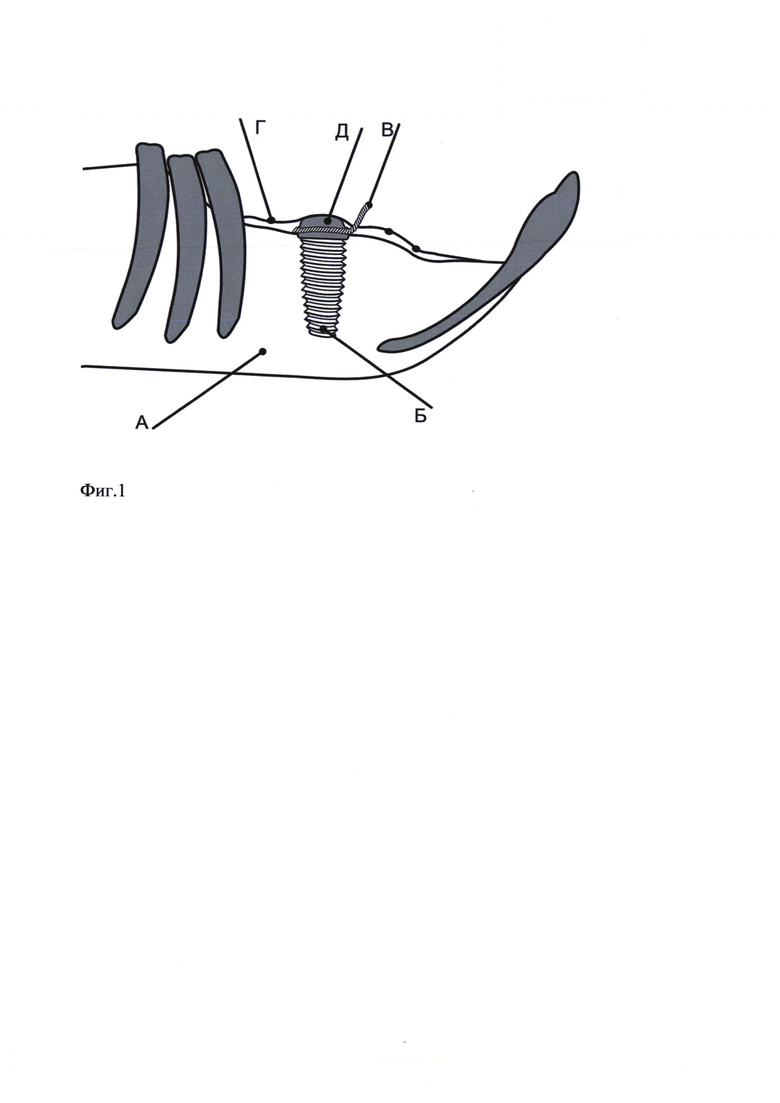
Фиксация лигатуры под винт-заглушку с выведением окончания за пределы мягких тканей обеспечивает постоянное обсеменение области вокруг имплантата, а также создает постоянное давление на костную ткань вокруг имплантата с целью создания очага резорбции костной ткани. Схематичное изображение модели представлено на Фиг. 1, где А - костная ткань челюсти; Б - имплантат; В - проволока, установленная под винт-заглушку; Г - швы на слизистой оболочке; Д - винт-заглушка.
За время эксперимента ни один кролик не умер. Срок формирования периимплантита в основной группе составил 21 день, что доказывает ускорение срока формирования периимплантита по сравнению с аналогами. Ускорение срока формирования экспериментальной модели позволяет раньше перейти к экспериментальным исследованиям по проведению лечению, а также позволяет уменьшить нагрузку на системы жизнеобеспечения экспериментального животного. В контрольной группе ни у одного животного не развился периимплантит.
Наблюдение за состоянием животных проводили по результатам рентгенологических и морфологических исследований. Все наблюдения проводили в сроки после установки имплантатов через 56 суток в обеих группах. Рентгенографию челюстей проводили в боковой проекции. После выведения животных из эксперимента проводили морфологические исследования челюстных костей.
По данным рентгенограмм у животных через 21 день после фиксации лигатурной проволоки в основной группе отмечалось повреждение кортикальной пластинки и появление очагов разряжения в области пришеечной части имплантата (Фиг. 2). В контрольной группе разряжения костной ткани в пришеечной области на рентгенограммах отмечено не было (Фиг. 3).
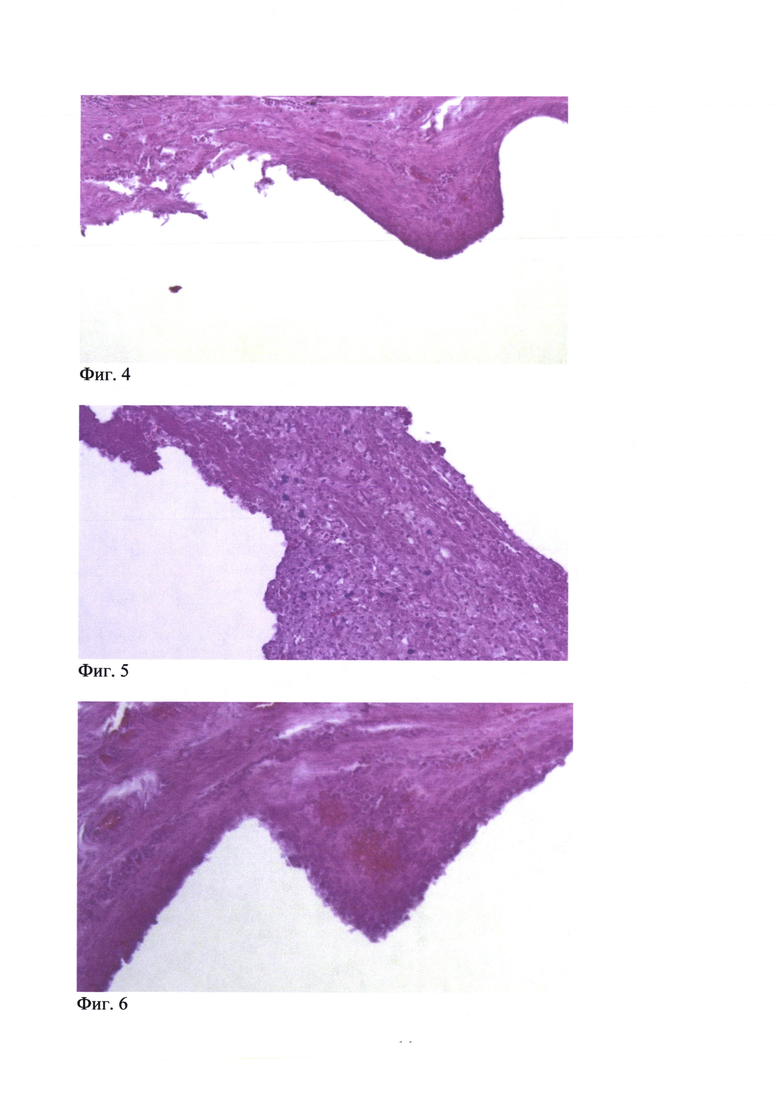
Данные морфологических исследований челюстей указывают на наличие деструктивных изменений, отмеченных нами на рентгенограммах, в области шеек имплантатов. Определяется выраженная воспалительная лимфоплазмоцитарная инфильтрация с обилием сегментоядерных лейкоцитов с формированием абсцессов и поля ксантомных клеток (Фиг. 4), а также деструктивные изменения в области шейки имплантатов с обилием детритов (Фиг. 5). В контрольной группе определяется костная ткань в области ложа с фокусами остеогенеза в виде формирования остеоида, со скоплением пролиферирующих остеобластов и фибробластов (Фиг. 6).
В результате проведенного исследования получена экспериментальная модель периимплантита, наиболее пригодная для исследований в области челюстно-лицевой хирургии, травматологии, дентальной имплантологии, пародонтологии.
Анализ полученных результатов предлагаемого способа экспериментальной модели позволяет создать патологический очаг без механического повреждения тканей, окружающих имплантат и ускорить патологические процессы.
Предлагаемый способ позволяет добиться устойчивой, воспроизводимой в 100% случаев модели периимплантита, полностью соответствующей наиболее часто встречающейся клинической картине. Данная модель позволяет испытывать эффективность всевозможных вариантов хирургических и терапевтических подходов к лечению периимплантита. Предоставленная модель, может быть, использована при оценке различных вариантов периимплантита в лабораторных условиях.
Применение предложенного способа удовлетворяет всем требованиям, позволяет в короткие сроки сформировать воспалительный процесс и очаг деструкции, увеличить количество ближайших осложнений и обострений.
Список источников литературы:
1. Abrahamsson I, Berglundh Т, Wennström J, Lindhe J. The peri-implant hard and soft tissues at different implant systems. A comparative study in the dog. // Clin Oral Implants Res. - 1996. - 7(3): 212-219.
2. Warrer K.B., Lang D., Karring N.P. Plaque-induced peri-implantitis in the presence or absence of keratinized mucosa. An experimental study in monkeys. Clin. Oral Implants Res. 1995; 6 (3): 131-138.
3. Плюхин Д.В., Асташина Н.Б., Соснин Д.Ю., Мудрова О.А. Экспериментальная модель периимплантита // Патологическая физиология и экспериментальная терапия. 2019. Т. 63. №2. С. 153-158
4. Патент РФ на изобретение №2730970 Способ создания экспериментальной модели периимплантита / Сирак С.В., Щетинин Е.В., Сирак А.Г., Рубникович С.П., Диденко М.О., Перикова М.Г., Кочкарова З.М., Гатило И.А., Андреев А.А., Сирак Е.С. заяв. №2019137611 от 21.11.2019, опубл. 26.08.2020. Бюллетень «Изобретения. Полезные модели» №24. - 2019.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОЗДАНИЯ ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ ПЕРИИМПЛАНТИТА | 2019 |
|
RU2730970C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРИИМПЛАНТИТОВ С ПРИМЕНЕНИЕМ ЛАЗЕРНОЙ БЕСПИГМЕНТНОЙ ФОТОАБЛЯЦИИ | 2023 |
|
RU2809568C1 |
| УСТРОЙСТВО ДЛЯ ВОССТАНОВЛЕНИЯ УТРАЧЕННОЙ КОСТНОЙ ТКАНИ ВОКРУГ ОБНАЖЕННОЙ ПОВЕРХНОСТИ ИМПЛАНТАТА И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 2015 |
|
RU2604049C1 |
| Способ ремоделирования костной ткани челюстей при лечении периимплантитов | 2022 |
|
RU2793163C1 |
| СПОСОБ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ (ВАРИАНТЫ) | 2012 |
|
RU2519630C2 |
| СПОСОБ ФОРМИРОВАНИЯ СТАБИЛЬНОЙ МЯГКОТКАННОЙ БУФЕРНОЙ ЗОНЫ ПРИ ОТСРОЧЕННОЙ УСТАНОВКЕ ФОРМИРОВАТЕЛЯ ДЕСНЕВОЙ МАНЖЕТЫ С ИСПОЛЬЗОВАНИЕМ ХИРУРГИЧЕСКОГО НАВИГАЦИОННОГО ШАБЛОНА | 2022 |
|
RU2788356C1 |
| СПОСОБ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ | 2018 |
|
RU2688447C1 |
| СПОСОБ НЕПОСРЕДСТВЕННОЙ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ У ПАЦИЕНТОВ С ВКЛЮЧЕННЫМИ ДЕФЕКТАМИ ЗУБНЫХ РЯДОВ | 2010 |
|
RU2447859C1 |
| Способ формирования стабильной мягкотканной буферной зоны вокруг постоянных индивидуальных абатментов при одномоментной установке дентальных имплантатов в условиях тонкого биотипа десны на нижней челюсти | 2018 |
|
RU2680481C1 |
| ОСТЕОПЛАСТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ РЕМОДЕЛИРОВАНИЯ ПЕРИИМПЛАНТНОЙ ЗОНЫ ЧЕЛЮСТНОЙ КОСТИ | 2020 |
|
RU2765850C1 |

Изобретение относится к медицине и предназначено для использования в экспериментальной медицине. Осуществляют установку дентальных имплантатов в отпрепарированное фрезой в костной ткани челюсти животного отверстие в беззубом промежутке с последующей остеоинтеграцией. При этом препарирование осуществляют в промежутке между молярами и резцами нижней челюсти кролика фрезой диаметром 3,2 мм длиной 5 мм с охлаждением с применением физиологического раствора. Затем машинным способом с крутящим моментом 25 Н/см, устанавливают дентальный имплантат диаметром 3,7 мм, длиной 7 мм, в имплантат устанавливают винт-заглушку и ушивают рану наглухо. Через 35 суток проводят повторный разрез, извлекают винт-заглушку, под нее вводят лигатурную проволоку диаметром 0,5 мм, скручивают вокруг винта и обрезают скрученную лигатуру с оставлением окончания скрученной части длиной 5 мм. Затем устанавливают винт-заглушку в имплантат, рану ушивают, выводя скрученный конец за пределы мягких тканей, после ушивания раны, на 2-3 мм. Способ позволяет получить полноценную модель с резорбцией костной ткани у шейки имплантата для осуществления исследований по эффективности купированию воспаления и регенерации костной ткани и мягких тканей при лечении данной нозологии. 6 ил.
Способ создания экспериментальной модели периимплантитов, включающий установку дентальных имплантатов в отпрепарированное фрезой в костной ткани челюсти животного отверстие в беззубом промежутке с последующей остеоинтеграцией, моделированием воспаления и резорбцией костной ткани вокруг имплантата, отличающийся тем, что препарирование осуществляют в промежутке между молярами и резцами нижней челюсти кролика фрезой диаметром 3,2 мм длиной 5 мм с охлаждением с применением физиологического раствора, затем машинным способом с крутящим моментом 25 Н/см, устанавливают дентальный имплантат диаметром 3,7 мм, длиной 7 мм, в имплантат устанавливают винт-заглушку и ушивают рану наглухо, через 35 суток проводят повторный разрез, извлекают винт-заглушку, под нее вводят лигатурную проволоку диаметром 0,5 мм, скручивают вокруг винта и обрезают скрученную лигатуру с оставлением окончания скрученной части длиной 5 мм, затем устанавливают винт-заглушку в имплантат, рану ушивают, выводя скрученный конец за пределы мягких тканей, после ушивания раны, на 2-3 мм.
| СПОСОБ СОЗДАНИЯ ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ ПЕРИИМПЛАНТИТА | 2019 |
|
RU2730970C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДЕЛИ ХРОНИЧЕСКОГО ПАРОДОНТИТА У КРЫС | 2014 |
|
RU2545923C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ПАРОДОНТИТА | 2017 |
|
RU2654598C1 |
| Экстракционный аппарат для получения канифоли и скипидара | 1929 |
|
SU23358A1 |
| JP 2011109951 A, 09.06.2011 | |||
| ПЛЮХИН Д.В | |||
| и др., Экспериментальная модель периимплантита, Патологическая физиология и экспериментальная терапия, 2019, 63(2), стр | |||
| Паровозный золотник (байпас) | 1921 |
|
SU153A1 |
| WARRER K.В., et al., Plaque-induced peri-implantitis in the presence or | |||
Авторы
Даты
2024-06-17—Публикация
2023-08-07—Подача