Способ относится к области медицины, а именно к онкологии, и может быть использован для прогнозирования прогрессирования у больных раком толстого кишечника, на основании данных микрочиповой экспрессии генов ZDHHC11, MIR4432HG, GZMB в образцах опухолевой ткани.
Прогрессирование заболевания у больного значительно ухудшает общее состояние, а также отрицательно влияет на прогноз [1]. При колоректальном раке типичной локализацией метастазов являются печень, лёгкие и головной мозг [2].
Развитие молекулярно-генетических методов в онкологии позволяет оценивать шанс прогрессирование, а значит корректировать проводимую терапию. Важное место среди этих методов отводится изучению экспрессионного профиля опухоли с использованием микрочипов, поскольку именно экспрессионный профиль является функционально активным отражением генетического «портрета» эукариотических клеток.
Например, для снижения риска прогрессирования у радикально пролеченных больных, необходимо проведение адъювантной полихимиотерапии, однако существуют клинические ситуации, когда не смотря на проводимое лечение, больной прогрессирует и погибает. Это заставляет сделать вывод о наличии еще неизвестных факторов, влияющих независимо и свойственных конкретному больному или группе пациентов.
На сегодняшний день существует несколько известных методов оценки прогрессирования больных колоректальным раком.
Прогрессирование колоректального рака в зависимости от степени, характера накопления и гормональной активности жировой ткани. Авторы на основании ретроспективных данных о пациентах, проходивших лечение от колоректального рака, делают вывод о том, что определение индекса массы тела (ИМТ), характера отложения жировой ткани и определении уровня лептина в сыворотке крови можно использовать в качестве прогностического фактора [3]. Однако, по данным ряда авторов секреция лептина подвержена значительным колебаниям, которые зависят от множества факторов, таких как возраст, пол, время забора крови, уровень инсулина, наличия вредных привычек, в частности - курения и ряда других [4]. Поэтому данные полученные авторами трудно экстраполировать на популяцию больных колоректальным раком.
Близкими по тематике к нашему изобретению также являются следующие:
1. «Способ диагностики метастазов колоректального рака в печень» (см. патент на изобретение RU №2642247, опубл. 24.01.2018), основанный на определении концентрации ионов меди в плазме крови.
2. «Способ диагностики метастазов рака толстой кишки» (см. патент на изобретение RU №2016115679, опубл. 26.10.2017), основанный на анализе метилирования CpG-сайтов 3 генов (АРС, CDH13 и MGMT).
3. «Способ диагностики метастазов рака толстой кишки» (см. патент на изобретение RU №2647470, опубл. 15.03.2018), основанный так же на анализе метилирования CpG-сайтов гена CDH13.
4. «Способ прогнозирования развития метастазов в печени у больных раком прямой кишки» (см. патент на изобретение RU №2686687, опубл. 30.04.2019) основанный на амплификации генов MAGEB1, SSX2, SCP1, GAPDH и GUSB и расчете относительной экспрессии генетических локусов.
Однако все вышеописанные способы трудоёмки и сложны (из-за использующихся для вычислений параметров). К тому же в изобретениях 2,3,4 используется метод полимеразной цепной реакции позволяющий оценить лишь небольшое количество заранее известных генов. В то же время мы в своем изобретении используем экспрессионный микрочип SurePrint G3 Human Gene Exp v3, содержащий зонды для определения 26,803 генов и 30,606 не кодирующих РНК. При этом все вышеперечисленные изобретения имеют меньшие значения чувствительности и специфичности, чем предлагаемые нашим коллективом.
Технический результат – эффективный и технологичный способ прогнозирования прогрессирования больных колоректальным раком на основе микрочиповой экспрессии генов ZDHHC11, MIR4432HG и GZMB в опухолевой ткани.
Осуществление изобретения
В исследовании приняли участие 36 пациентов. Они были разделены на 2 группы в зависимости от наличия или отсутствия прогрессирования. Верификация диагноза имелась у всех пациентов. Гистологически опухоли были представлены аденокарциномами, преимущественно умеренной дифференцировки. Стадию заболевания устанавливали согласно Международной классификации TNM 8-й редакции (2018 г.). До начала лечения больным выполняли фиброколоноскопию с биопсией опухоли. Для транспортировки и хранения биоматериала использовался раствор стабилизирующего реагента RNAlater (Thermo Fisher Scientific Inc., США). Гомогенизация ткани проводилась механическим методом, в 500 мкл лизирующего раствора с добавлением меркаптоэтанола. Далее происходило выделение рибонуклеиновой кислоты (РНК) на спинколонках набора RNeasy Plus Mini Kit (Qiagen, США) с использованием фильтрующих ДНК и РНК-мембран согласно инструкции производителя. Качество и количество РНК в элюированном растворе оценивались с помощью наноспектрофотометра IMPLEN (Германия). В работу брались образцы, строго отвечающие оптимальным параметрам чистоты (с RIN не менее 7,5). Для оценки экспрессии генов использован набор микрочипов SurePrint G3 HumanGeneExpv3 ArrayKit (Agilent, США). Сканирование микрочипов выполнено на аппарате InnoScan 1100 AL (США). Данные с микрочипового анализатора далее проходили дополнительную нормализацию. Следующим этапом делали поправку на множественное тестирование с помощью метода FDR (False Discovery Rate) и фиксировали вероятность её совершить на уровне значимости. P-value (<0.05). Для процедуры поиска дифференциально экспрессируемых генов использовали метод Moderated t-statistics, который реализован в пакете limma.
В табл. 1 представлены результаты анализа дифференциальной экспрессии генов в образцах с прогрессированием и без прошедшие по критерию P-value (<0.05). GENE_SYMBOL – Наименование гена. ProbeName - Наименование зонда на микрочипе. ENSEMBL_ID – Идентификатор базы данных Ensembl. CHROMOSOMAL_LOCATION – Геномные координаты. logFC – Логарифм меры изменения экспрессии, значения с минусом - означают низкую экспрессию гена, значения с плюсом - высокую экспрессию. P.Value – Вероятность ошибки при отклонении нулевой гипотезы.
Табл. 1
При дифференциальном анализе экспрессии генов было выявлено топ 10-генов с повышенной и топ-10 с пониженной экспрессией как представлено в табл. 1.
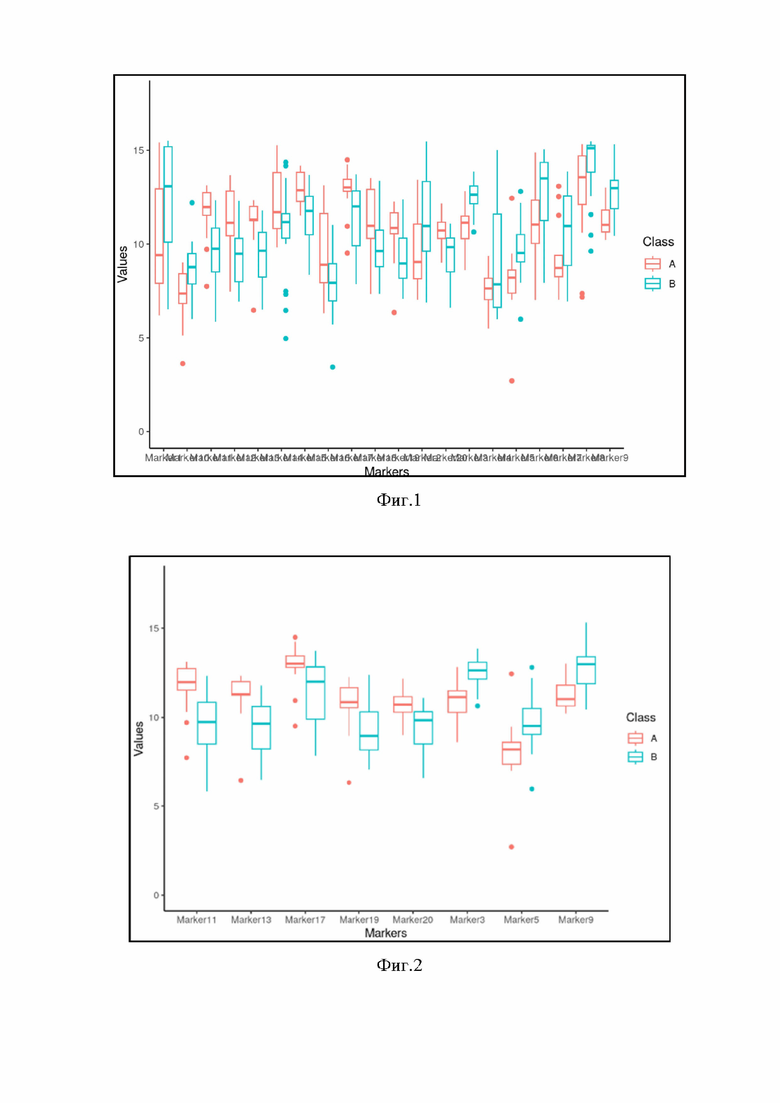
Следующим этапом построили диаграммы размаха для каждого маркера как указано на фиг. 1. Class A – экспрессия гена в тканях с прогрессированием, Class B – экспрессия гена в тканях без прогрессирования. С помощью которых определили наиболее различающиеся по уровню экспрессии гены в образцах опухолевой ткани с прогрессированием и без.
На основе диаграммы размаха, показанной на фиг. 1 были выбраны наиболее различающиеся гены в образцах с прогрессированием и без.
На следующем этапе нами была построена бинарная диагностическая модель, классифицирующая образец как с прогрессированием или без для различных комбинаций, наиболее различающихся по профилю экспрессии генов как указано на фиг. 2.
В табл. 2 продемонстрированы параметры чувствительности и специфичности для комбинаций генов ранжированные по критерию Юдена (SE – чувствительность, SE_B – чувствительность по Class B, SP_A – специфичность по Class A, SP - специфичность, #Markers – количество (комбинация) маркеров, Youden – критерий Юдена).
Табл. 2
Также для каждой комбинации были рассчитаны значения чувствительности и специфичности. Проанализировав данные представленные в табл. 2 с диагностическими показателями комбинаций, выявили, что интерес представляют первые пять из-за их показателей чувствительности и специфичности.
Следующим этапом проводили ROC-анализ для пяти комбинаций генов.
На фиг. 3 представлена ROC- кривая для изучаемых комбинаций генов оценки риска прогрессирования. (specificity – специфичность, sensitivity – чувствительность). Для количественной оценки информативности используется сравнительный анализ площадей под ROC-кривыми (Area under ROC curve - AUC) (Коэффициент площади кривой, лежащий в интервале 0.9-1, следует рассматривать как показатель наивысшей информативности диагностического метода, в интервале 0.8-0.9 - хорошая информативность, в интервале 0.7-0.8 - удовлетворительная, в интервале 0.6-0.7 - посредственная информативность, и ниже - бесполезная классификация).
Табл. 3
В табл. 3 представлены комбинации генов, ранжированные в зависимости от коэффициента площади ROC-кривой, где Marker9 (GZMB), Marker5 (CXCL11), Marker3 (SYNE4), Marker20 (MIR4432HG), Marker19 (ZDHHC11), Marker11 (COL17A1), Marker13 (ZDHHC11B), Marker17 (AGR3).
Исходя из результатов ROC – анализа указанных в табл. 3 выявили – наиболее информативную комбинацию генов для прогнозирования прогрессирования при колоректальном раке.
Полученные результаты позволили нам прийти к выводу, что экспрессия комбинации генов ZDHHC11, MIR4432HG, GZMB, где экспрессия ZDHHC11, MIR4432HG повышена, а GZMB снижена, прогнозирует риск прогрессирования у пациентов с колоректальным раком с чувствительностью 93% и специфичностью 83%.
Список литературы
1. Sponholz S., Bölükbas S., Schirren M., Oguzhan S., Kudelin N., Schirren J. Leber- und Lungenmetastasen des kolorektalen Karzinoms. Langzeitüberleben und Prognosefaktoren [Liver and lung metastases of colorectal cancer. Long-term survival and prognostic factors]. Chirurg. 2016 Feb;87(2):151-6. German. doi: 10.1007/s00104-015-0024-x. PMID: 26016711.
2. Tan K.K., Lopes Gde L Jr, Sim R. How uncommon are isolated lung metastases in colorectal cancer? A review from database of 754 patients over 4 years. J Gastrointest Surg. 2009 Apr;13(4):642-8. doi: 10.1007/s11605-008-0757-7. Epub 2008 Dec 11. PMID: 19082673.
3. Солодкий В.А., Чхиквадзе В.Д., Станоевич У.С., Дехисси Е.И. Прогрессирование колоректального рака в зависимости от степени, характера накопления и гормональной активности жировой ткани. Онкология. Журнал им. П.А. Герцена. 2015;4(6):25-30. Solodky VA, Chkhikvadze VD, Stanoevich US, Dekhissi EI. Progression of colorectal cancer in relation to the degree, pattern of accumulation, and hormonal activity of fatty tissue. P.A. Herzen Journal of Oncology. 2015;4(6):25-30. (In Russ.) https://doi.org/10.17116/onkolog20154625-30
4. Терещенко И.В. "Лептин и его роль в организме", Проблемы эндокринологии, vol. 47, no. 4, pp. 40-46, авг. 2001. [Online]. Available: 10.14341/probl11588.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА ВОЗНИКНОВЕНИЯ РЕЦИДИВА ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2015 |
|
RU2626603C2 |
| СПОСОБ ПРОГНОЗА МЕТАСТАЗИРОВАНИЯ ОПУХОЛЕЙ РАКА ЖЕЛУДКА | 2021 |
|
RU2806432C2 |
| Тест-классификатор клинического ответа на лечение сорафенибом индивидуальных пациентов с раком почки | 2018 |
|
RU2747746C2 |
| НАБОР РЕАГЕНТОВ ДЛЯ ОПРЕДЕЛЕНИЯ РИСКА ВОЗНИКНОВЕНИЯ РЕЦИДИВА ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2017 |
|
RU2671557C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВЕРОЯТНОСТИ РЕЦИДИВИРОВАНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2609199C2 |
| Способ прогнозирования исхода у больных раком желудка после комбинированного лечения, включающего неоадъювантную химиотерапию по схемам FOLFOX6 или FLOT и хирургическое лечение | 2024 |
|
RU2831907C1 |
| Тест-система "miR-M-SCREEN" для прогнозирования развития метастазов у больных колоректальным раком на основании уровня микро-РНК miR-26a и miR-143 в плазме крови | 2022 |
|
RU2786386C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ МЕТАСТАЗОВ В ПЕЧЕНИ У БОЛЬНЫХ РАКОМ ТОЛСТОЙ КИШКИ | 2018 |
|
RU2686687C1 |
| СПОСОБЫ КЛАССИФИКАЦИИ ПАЦИЕНТОВ С СОЛИДНЫМ РАКОМ | 2017 |
|
RU2745730C2 |
| Способ прогнозирования выживаемости больных светлоклеточным почечно-клеточным раком | 2018 |
|
RU2699792C1 |

Изобретение относится к медицине, а именно к онкологии, и может быть использовано для прогнозирования прогрессирования при колоректальном раке. Осуществляют взятие образца опухолевой ткани, выделение РНК из образца опухолевой ткани и определение комбинации генов. При повышенной экспрессии генов ZDHHC11, MIR4432HG и сниженной экспрессии гена GZMB прогнозируют прогрессирование заболевания. Способ обеспечивает эффективное прогнозирование прогрессирования при колоректальном раке за счет определения экспрессии генов ZDHHC11, MIR4432HG и GZMB в опухолевой ткани. 3 ил., 3 табл.
Способ прогнозирования прогрессирования при колоректальном раке, включающий взятие образца опухолевой ткани, выделение РНК из образца опухолевой ткани и определение комбинации генов, отличающийся тем, что при повышенной экспрессии генов ZDHHC11, MIR4432HG и сниженной экспрессии гена GZMB прогнозируют прогрессирование заболевания.
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ МЕТАСТАЗОВ В ПЕЧЕНИ У БОЛЬНЫХ РАКОМ ТОЛСТОЙ КИШКИ | 2018 |
|
RU2686687C1 |
| WO 2020223233 A1, 05.11.2020 | |||
| KR 20100112755 A, 20.10.2010 | |||
| MURAKAMI Y | |||
| et al | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Cancer Med | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
Авторы
Даты
2024-06-26—Публикация
2024-01-31—Подача