Изобретение относится к способу определения накопленных поглощенных доз препаратов, содержащих радиоактивные вещества, для использования в терапии или для исследований in vivo, а именно к способу определения накопленных поглощенных доз от β-изучения радиофармпрепарата в органах и тканях лабораторных животных
Известен способ определения накопленных поглощенных доз от β-излучения радиофармпрепарата (РФП) в органах и тканях лабораторных животных (В.Г. Скворцов, В.Ф. Степаненко, В.М. Петриев, М.Ю. Орлов, И.Г. Крюкова, В.А. Соколов, Н.Б. Борышева, В.К. Ширяева, С.П. Орленко, А.М. Хайлов, А.Ф. Цыб. Фармакокинетические и дозиметрические характеристики нового радиофармпрепарата 103Pd - Микросферы альбумина // Радиационная биология. Радиоэкология. 2010. Т. 50, №6. С. 703-711), в котором накопленные поглощенные дозы определяют в органах - мишенях (модельных камерах), при этом учитывается форма, размер и элементный состав тканей данного органа, производится измерение активности ANэксп(t) одновременно во всех N-модельных камерах на каждом из четырех животных в течение времени - t не менее 48 часов, учитывающий динамику физического распада радионуклида, его фармакокинетику и вклад в облучение органа - мишени от других источников излучения в организме.
Недостатком данного способа является его большая длительность и сложность, а также невозможность определить поглощенную дозу при t → ∞.
Технической задачей заявляемого решения является повышение точности и надежности измерения поглощенных доз в заданных органах и тканях для определения пригодности радиофармпрепаратов для лечения данных органов и тканей по назначению.
Технической результатом заявляемого решения является достижения точности определения моделирования поглощенных доз в органах и тканях выше или равной точности измерения активности в них для сравнения пригодности различных радиофармпрепаратов для лечения данных органов и тканей.
Указанный технический результат достигается тем, что предложен способ определения накопленных поглощенных доз от β-излучения радиофармпрепарата в органах и тканях лабораторных животных заключающийся в том, что предварительно органы и ткани, в которых необходимо определить поглощенные дозы, моделируют камерами: камера плазмы крови, камера коленного сустава, камера бедер, камера ребер, камера черепа, камера позвоночника, камера печени, камера почек, камера щитовидной железы, камера легких, камера сердца, камера селезенки, камера желудка, камера кишечника, камера мышцы бедра, после чего производят измерение активности ANэксп(t) одновременно во всех N модельных камерах на каждом из четырех животных в течение времени не менее 48 часов, отличающийся тем, что накопленные к моментам времени ti значения поглощенных доз DN(ti) в каждой из N модельных камер определяют из решения системы дифференциальных уравнений:
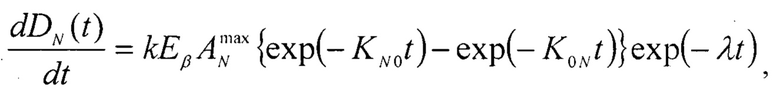
а транспортные константы - из условия минимума функционала невязки:
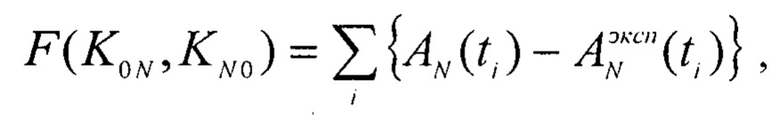
затем если экспериментальная точность измерения активности - 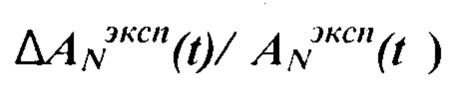 в некоторых из заданных N камер меньше точности моделирования поглощенной дозы ΔDS(t)/D(t) в них:
в некоторых из заданных N камер меньше точности моделирования поглощенной дозы ΔDS(t)/D(t) в них:
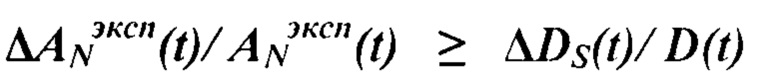
то данные - S камер, кроме камеры крови, - исключают из повторных измерений активности, после этого проводят K-повторные экспериментальные измерения активности AN-Sэксп(t) во всех N-S модельных камерах органов и тканей на второй и следующей K группе лабораторных животных, при этом проводится повторное решение системы дифференциальных уравнений для расчета уточненных транспортных констант, эксперимент и моделирование повторяется K раз до достижения точности определения значения поглощенной дозы в органах и тканях выше и равной, чем точность измерения активности в них:
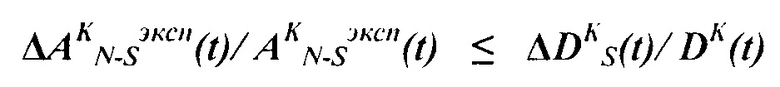
где:
AN(ti) - модельные значения активности в N-ой камере в момент времени
ANmax - максимальные удельные значения активности в N-ой камере (Бк/г);
K0N - транспортная константа накопления (ч-1);
KN0 - транспортная константа выведения (ч-1);
λ - постоянная распада радиофармпрепарата (ч-1);
k - коэффициент пропорциональности;
Eβ - средняя энергия β-излучения от радиофармпрепарата;
t - время;
N - модельная камера;
DN(ti) - поглощенная доза в N-ой камере в момент времени ti;
ANэксп(ti) - экспериментальные значения активности в N-й камере в момент времени ti;
F(K0N,KN0) - функционал невязки;
ΔANэксп(t) - величина абсолютного отклонения экспериментального значения активности в некоторой из заданных N-камер;
ANэксп(t) - экспериментальные значения активности в некоторой из заданных N-камер;
ΔAKN-Sэксп(t) - величина абсолютного отклонения экспериментального значения активности в некоторой из заданных N-S-ой камере при K-повторе;
AKN-Sэксп(t) - экспериментальное значение активности в некоторой из заданных N-S-ой камере при K-повторе;
ΔDS(t) - суммарная накопленная поглощенная доза в исключаемых S-камерах модели;
D(t) - суммарная накопленная поглощенная доза по всем камерам;
ΔDKS(t) - суммарная накопленная поглощенная доза в исключаемых S-камерах модели при K-повторе;
DK(t) - суммарная накопленная поглощенная доза по всем камерам при K-повторе.
Возможность достижения технического результата обеспечивается тем, что для определения накопленных поглощенных доз в органах и тканях был выбран остеотропный препарат на основе этилендиаминтетра(метиленфосфоновой) кислоты, меченный 177Lu (177Lu-ЭДТМФ), а исследования были проведены на интактных крысах Wistar, самках, с массой тела 160±40 г. Всего было использовано 20 животных. Им внутривенно (в хвостовую вену) вводили 0,1 мл 177Lu-ЭДТМФ с активностью 0,37 МБк (0,37 МБк/крыса). Для сравнительного анализа и оценки стабильности 177Lu-ЭДТМФ invivo также было исследовано распределение свободного лютеция в виде 177LuСl3 в организме аналогичных крыс (еще 20 животных). Им также внутривенно вводили 0,1 мл 177LuCl3 с активностью 0,37 МБк (0,37 МБк/крыса). Через 5 мин, 1, 3, 24 и 48 ч после введения животных подвергали эвтаназии (по 4 животных на каждый срок) путем декапитации и производили забор внутренних органов и тканей. Полученные образцы помещали в пластиковые пробирки, взвешивали на электронных весах «Sartorius» (Германия) и проводили радиометрию с помощью автоматического гамма-счетчика «Wizard» версии 2480 фирмы «PerkinElmer/Wallac» (Финляндия). По данным радиометрии на каждый срок наблюдения рассчитывали содержание 177Lu-ЭДТМФ или 177LuCl3 в 1 г органа или ткани в процентах от введенного количества. Результаты радиометрии обрабатывали статистически в программе MicrosoftExcel 2010 с вычислением средних арифметических значений (М) и стандартных ошибок среднего (m). На основе полученных таким образом радиометрических данных далее определяли транспортные константы и рассчитывали накопленные поглощенные дозы в камерах (органах и тканях).
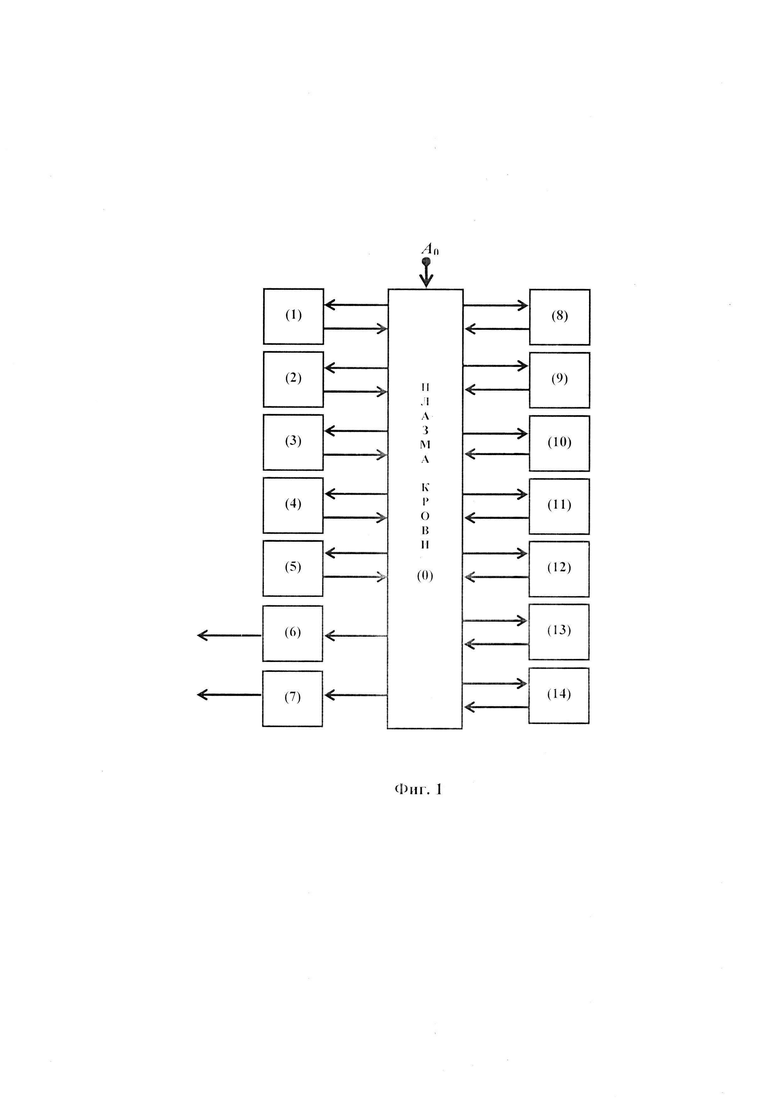
На фиг. 1 представлена блок-схема камерной модели, использованной в заявленном решении. Данная модель включает в себя камеру плазмы крови - 0, камеру коленного сустава - 1, камеру бедра - 2, камеру черепа - 3, камеру ребра - 4, камеру позвоночника - 5, камеру печени - 6, камеру почек - 7, камеру щитовидной железы - 8, камеру легких - 9, камеру сердца - 10, камеру селезенки - 11, камеру желудка - 12, камеру кишечника - 13, камеру мышцы бедра - 14.
На фиг. 2 представлен вид фармакокинетической кривой.
ПРИМЕР: радиофармпрепарат 177Lu-ЭДТМФ
Было выбрано 15 модельных камер: камера плазмы крови, камера коленного сустава, камера бедер, камера ребер, камера черепа, камера позвоночника, камера печени, камера почек, камера щитовидной железы, камера легких, камера сердца, камера селезенки, камера желудка, камера кишечника, камера мышцы бедра, после чего произвели измерение активности ANэксп(t) одновременно во всех 15 модельных камерах на каждом из четырех животных в течение: 5 минут, 1 час, 3 часа, 24 часа, 48 часов.
В таблице 1 представлены экспериментальные значения накопленной активности 177Lu-ЭДТМФ в органах и тканях после их внутривенного введения (в % от введенной активности на 1 г органа).
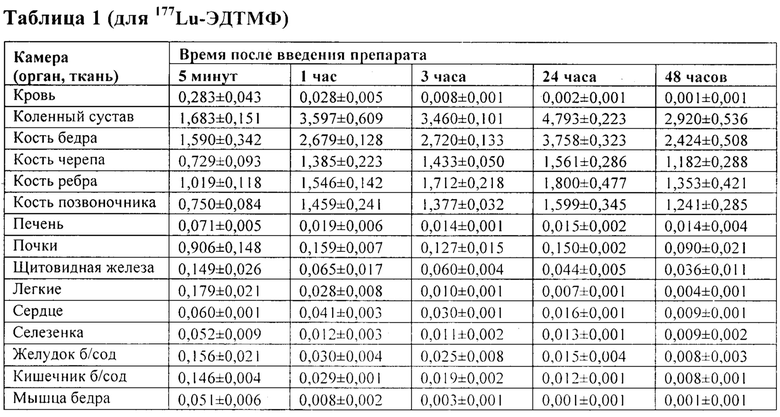
Затем данные таблицы 1 использованы для определения транспортных констант и накопленных поглощенных доз от β-излучения РФП. В таблице 2 представлены рассчитанные в органах и тканях значения транспортных констант (ч-1) и накопленных поглощенных доз (мГр/МБк) 177Lu-ЭДТМФ
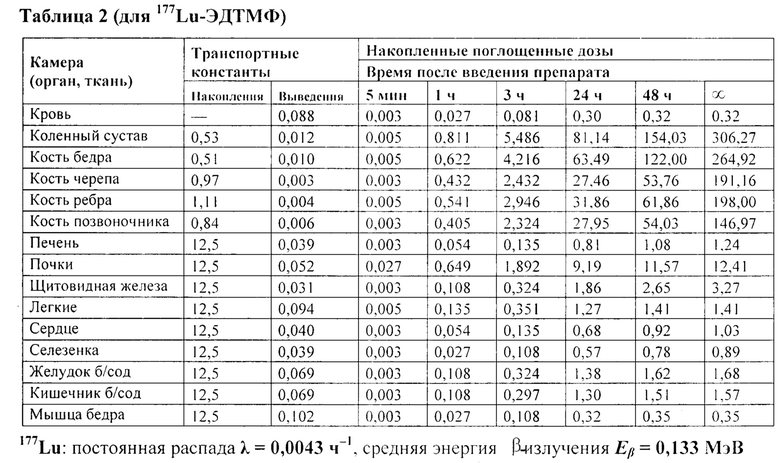
Затем точность моделирования поглощенной дозы ΔD S(t)/ D (I) в них была выбрана не менее 1% (Экспериментальна погрешность измерения активности составляла 1%). Были исключены, кроме камеры крови S=8 камер: камеры мышцы бедра, селезенки, сердца, печени, легких, кишечника, желудка и щитовидной железы, накопленная полная доза (при t → ∞) в которых в сумме не превышает 1% от суммарной поглощенной дозы по всем камерам.
Следовательно, требуется повтор моделировании в оставшихся 7 камерах. При первом повторе K=1: были заново измерены экспериментальные значения накопленной активности Lu-ЭДТМФ в 7 камерах после внутривенного введения. В таблице 3 представлены экспериментальные значения накопленной активности 177Lu-ЭДТМФ в 7 камерах после внутривенного введения (в % от введенной активности на 1 г органа).
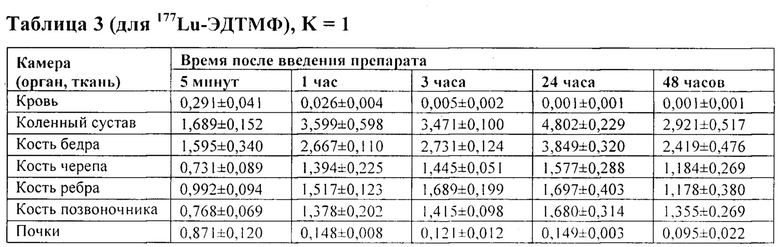
В таблице 4 представлены рассчитанные в органах и тканях значения транспортных констант (ч-1) и накопленных поглощенных доз (мГр/МБк) 177Lu-ЭДТМФ
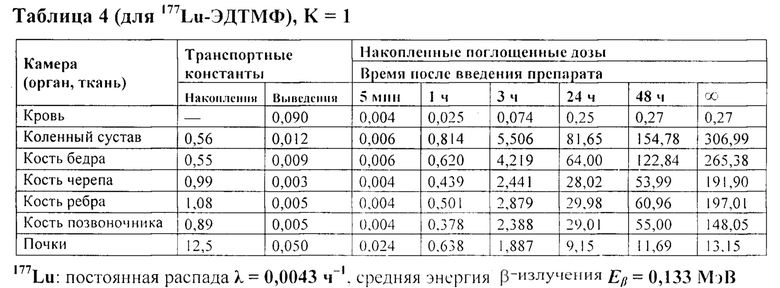
Из данных табл. 4 следует, что для данного РФП (177Lu-ЭДТМФ) повторов моделирования больше не требуется, так как накопленная поглощенная доза в каждой камере, кроме камеры крови превышает 1% от суммарной поглощенной дозы по всем камерам.
ПРИМЕР: радиофармпрепарат l77LuCl3
Было выбрано 15 модельных камер: камера плазмы крови, камера коленного сустава, камера бедер, камера ребер, камера черепа, камера позвоночника, камера печени, камера почек, камера щитовидной железы, камера легких, камера сердца, камера селезенки, камера желудка, камера кишечника, камера мышцы бедра, после чего произвели измерение активности ANэксп(t) одновременно во всех 15 модельных камерах на каждом из четырех животных в течение: 5 минут, 1 час, 3 часа, 24 часа, 48 часов.
В таблице 5 представлены экспериментальные значения накопленной активности 177LuСl3 и соответственно в органах и тканях после их внутривенного введения (в % от введенной активности на 1 г органа).

Затем данные таблицы 5 использованы для определения транспортных констант и накопленных поглощенных доз от β-излучения РФП. В таблице 6 представлены рассчитанные в органах и тканях значения транспортных констант (ч-1) и накопленных поглощенных доз (мГр/МБк) 177LuCl3.
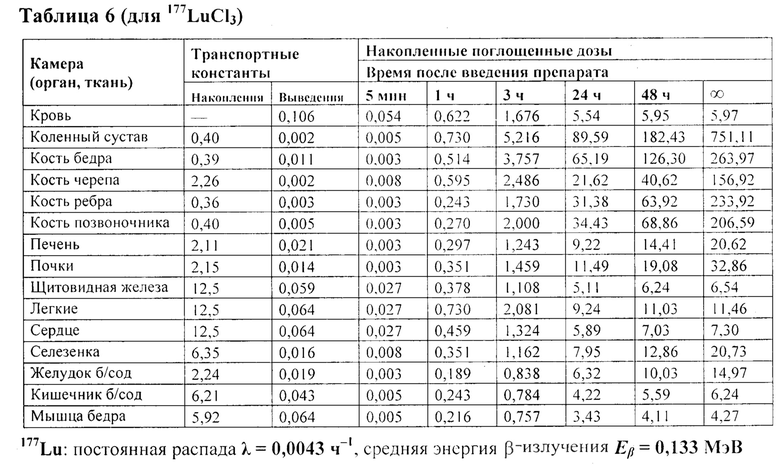
Затем точность моделирования поглощенной дозы ΔD S(t)/ D(t) в них тоже была выбрана не менее 1% и были исключены, кроме камеры крови S=3 камер: камеры мышцы бедра, кишечника и щитовидной железы, накопленная полная доза (при t → ∞) в которых в сумме не превышает 1% от суммарной поглощенной дозы по всем камерам.
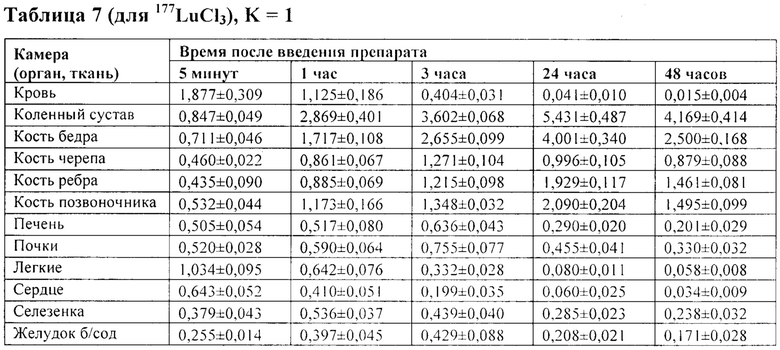
Следовательно требуется повтор моделировании в оставшихся 12 камерах. При первом повторе K=1: были заново измерены экспериментальные значения накопленной активности 177Lu-ЭДТМФ в 12 камерах после внутривенного введения. В таблице 7 представлены экспериментальные значения накопленной активности 177LuCl3 в 12 камерах после внутривенного введения (в % от введенной активности на 1 г органа).
В таблице 8 представлены рассчитанные в органах и тканях значения транспортных констант (ч) и накопленных поглощенных доз (мГр/МБк) 77LuCl3.
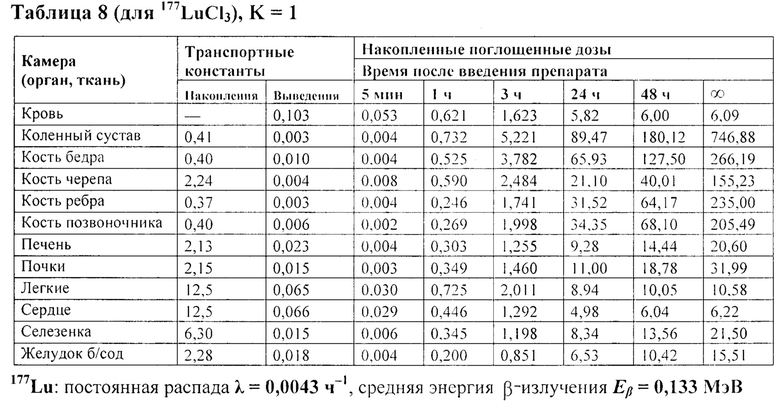
Из последней колонки таблицы 8 видно, что имеются 2 камеры (сердца и легких), накопленная полная доза в которых не превышает 1% от суммарной полной дозы по всем камерам. Следовательно, для 177LuCl3 требуется второй повтор моделирования (K=2). В таблице 9 представлены экспериментальные значения накопленной активности 177LuСl3 в 10 камерах после их внутривенного введения (в % от введенной активности на 1 г органа).
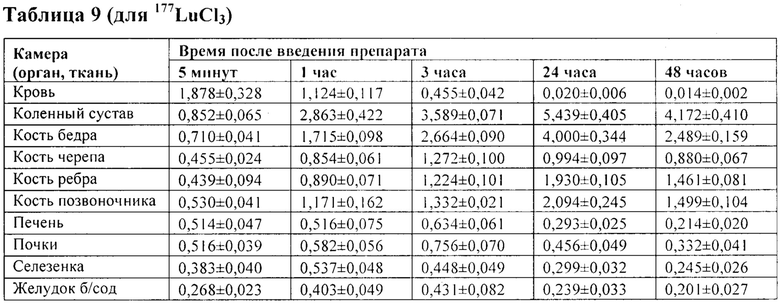
В таблице 10 представлены рассчитанные в органах и тканях значения транспортных констант (ч-1) и накопленных поглощенных доз (мГр/МБк) l77LuCl3.
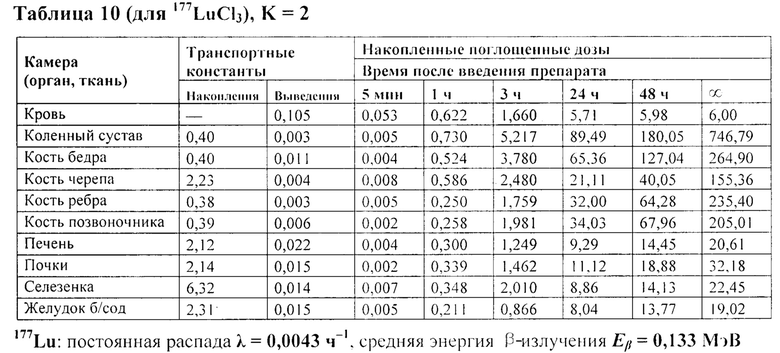
Из данных табл. 10 следует, что для данного РФП (l77LuCl3) повторов моделирования больше не требуется, так как накопленная поглощенная доза в каждой камере превышает 1% от суммарной поглощенной дозы по всем камерам.
Видно, что значения транспортных констант 177Lu-ЭДТМФ в камерах коленного сустава, костей бедра, черепа, ребер и позвоночника интактных крыс в десятки раз меньше, чем в других камерах, что указывает на его депонирование в костных тканях. В целом фармакокинетика 177Lu-ЭДТМФ соответствует фармакокинетике остеотропных РФП. Рассчитанные значения накопленных поглощенных доз в камерах коленного сустава, костей бедра, черепа, ребер и позвоночника в десятки и сотни раз больше, чем в других камерах. Критическим органом для 177Lu-ЭДТМФ являются почки, в котором значения поглощенных доз в несколько раз больше, чем в других периферических органах и тканях. В сравнении с 177LuСl3 накопленные поглощенные дозы 177Lu-ЭДТМФ в целом в костных тканях примерно одинаковые, а в других органах и тканях существенно ниже, что позволяет сделать вывод о перспективности дальнейших исследований препарата 177Lu-ЭДТМФ и возможности его клинического применения для терапии костных метастазов.
Таким образом, решается техническая задача заявляемого решения повышение точности и надежности измерения поглощенных доз в заданных органах и тканях для определения пригодности радиофармпрепаратов для лечения данных органов и тканей по назначению.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПСМА-ТАРГЕТНОЕ СОЕДИНЕНИЕ И ЕГО КОМПЛЕКС С РАДИОНУКЛИДАМИ ДЛЯ ТЕРАНОСТИКИ ОПУХОЛЕЙ, ЭКСПРЕССИРУЮЩИХ ПСМА | 2022 |
|
RU2803734C1 |
| Лиофилизат на основе лигандов к простат-специфическому мембранному антигену (ПСМА) для приготовления радиофармацевтической композиции в форме раствора для инъекций для лечения рака предстательной железы, радиофармацевтическая композиция на ее основе для лечения рака предстательной железы и способ приготовления радиофармацевтической композиции | 2023 |
|
RU2817970C1 |
| СОЕДИНЕНИЕ И ЕГО КОМПЛЕКС С РАДИОНУКЛИДОМ Lu ДЛЯ ТЕРАНОСТИКИ ОПУХОЛЕЙ, ЭКСПРЕССИРУЮЩИХ НА HER2 РЕЦЕПТОРЫ | 2023 |
|
RU2826247C1 |
| РАДИОФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2162714C1 |
| Способ диагностики опухоли | 2017 |
|
RU2657761C1 |
| Радиофармацевтическая композиция для лечения боли при воспалительных заболеваниях суставов | 2017 |
|
RU2662088C1 |
| ПОЛИПЕПТИДЫ АНТИТЕЛ И ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2687163C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАДИОФАРМАЦЕВТИЧЕСКОГО ПРЕПАРАТА С ГАЛЛИЕМ-68 ДЛЯ ВИЗУАЛИЗАЦИИ МЕТАСТАЗОВ СКЕЛЕТА МЕТОДОМ ПЭТ | 2020 |
|
RU2757258C1 |
| СПОСОБ ВЕРИФИКАЦИИ ДОЗЫ ПРИ МЕДИЦИНСКОМ ПРИМЕНЕНИИ ОТКРЫТЫХ РАДИОНУКЛИДОВ | 2005 |
|
RU2289458C2 |
| Способ радионуклидной диагностики злокачественных лимфом | 2018 |
|
RU2706602C1 |

Изобретение относится к медицине, а именно к экспериментальной радиотерапии, и может быть использовано для определения накопленных поглощенных доз от β-излучения радиофармпрепарата в органах и тканях лабораторных животных. Предварительно органы и ткани, в которых необходимо определить поглощенные дозы, моделируют камерами: камера плазмы крови, камера коленного сустава, камера бедер, камера ребер, камера черепа, камера позвоночника, камера печени, камера почек, камера щитовидной железы, камера легких, камера сердца, камера селезенки, камера желудка, камера кишечника, камера мышцы бедра. После чего производят измерение активности ANэксп(t) одновременно во всех N модельных камерах на каждом из четырех животных в течение времени - t не менее 48 часов. При этом накопленные к моментам времени ti значения поглощенных доз DN(ti) в каждой из N модельных камер определяют из решения системы дифференциальных уравнений
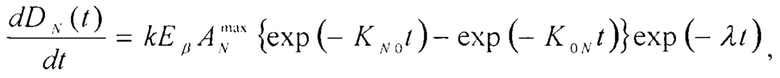
а транспортные константы - из условия минимума функционала невязки 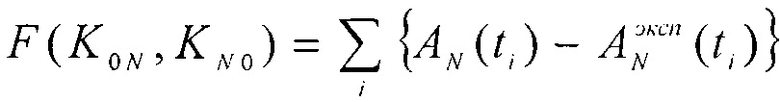 .
.
Если экспериментальная точность измерения активности - ΔANэксп(t)/ANэксп(t) в некоторых из заданных N камер меньше точности моделирования поглощенной дозы ΔDS(t)/D(t) в них, то данные S камер, кроме камеры крови, исключают из повторных измерений активности. После этого проводят K-повторные экспериментальные измерения активности AN-Sэксп(t) во всех N-S модельных камерах органов и тканей на второй и следующей K группе лабораторных животных. При этом проводится повторное решение системы дифференциальных уравнений для расчета уточненных транспортных констант. Эксперимент и моделирование повторяется K раз до достижения точности определения значения поглощенной дозы в органах и тканях выше и равной, чем точность измерения активности в них. Способ обеспечивает повышение точности и надежности измерения поглощенных доз в заданных органах и тканях для определения пригодности радиофармпрепаратов для лечения данных органов и тканей по назначению за счет повторения эксперимента и моделирования K раз до достижения точности определения значения поглощенной дозы в органах и тканях выше и равной, чем точность измерения активности в них. 2 ил., 10 табл., 2 пр.
1. Способ определения накопленных поглощенных доз от β-излучения радиофармпрепарата в органах и тканях лабораторных животных заключающийся в том, что предварительно органы и ткани, в которых необходимо определить поглощенные дозы, моделируют камерами: камера плазмы крови, камера коленного сустава, камера бедер, камера ребер, камера черепа, камера позвоночника, камера печени, камера почек, камера щитовидной железы, камера легких, камера сердца, камера селезенки, камера желудка, камера кишечника, камера мышцы бедра, после чего производят измерение активности АNэксп(t) одновременно во всех N модельных камерах на каждом из четырех животных в течение времени - t не менее 48 часов, отличающийся тем, что накопленные к моментам времени ti значения поглощенных доз DN(ti) в каждой из N модельных камер определяют из решения системы дифференциальных уравнений:
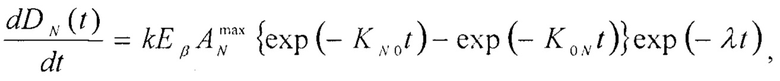
а транспортные константы - из условия минимума функционала невязки:
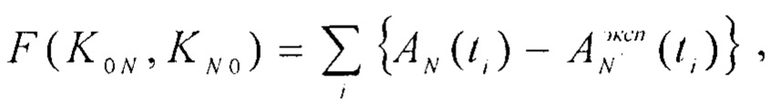
затем если экспериментальная точность измерения активности - ΔANэксп(t)/ANэксп(t) в некоторых из заданных N камер меньше точности моделирования поглощенной дозы ΔDS(t)/D(t) в них
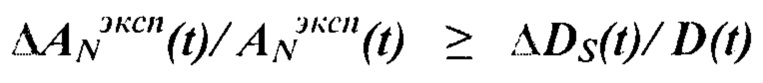 ,
,
то данные - S камер, кроме камеры крови, - исключают из повторных измерений активности, после этого проводят K-повторные экспериментальные измерения активности AN-Sэксп(t) во всех N-S модельных камерах органов и тканей на второй и следующей K группе лабораторных животных, при этом проводится повторное решение системы дифференциальных уравнений для расчета уточненных транспортных констант, эксперимент и моделирование повторяется K раз до достижения точности определения значения поглощенной дозы в органах и тканях выше и равной, чем точность измерения активности в них
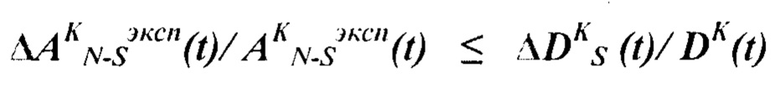
где:
АN(ti) - модельные значения активности в N-й камере в момент времени;
ANmax - максимальные удельные значения активности в N-й камере (Бк/г);
K0N - транспортная константа накопления (ч-1);
KN0 - транспортная константа выведения (ч-1);
λ - постоянная распада радиофармпрепарата (ч-1);
k - коэффициент пропорциональности;
Еβ - средняя энергия β-излучения от радиофармпрепарата;
t - время;
N - модельная камера;
DN(ti) - поглощенная доза в N-й камере в момент времени ti;
ANэксп(ti) - экспериментальные значения активности в N-й камере в момент времени ti;
F(K0N,KN0) - функционал невязки;
DK(t) - суммарная накопленная поглощенная доза по всем камерам при K-повторе;
ΔDKS(t) - суммарная накопленная поглощенная доза в исключаемых S-камерах модели при K-повторе.
| Способ моделирования токсического поражения селезенки у экспериментальных животных | 2021 |
|
RU2753130C1 |
| СПОСОБ ОЦЕНКИ РИСКА РЕЦИДИВА ДИФФЕРЕНЦИРОВАННОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ ПОСЛЕ ПРОВЕДЕНИЯ РАДИОЙОДТЕРАПИИ | 2020 |
|
RU2743275C1 |
| Способ определения поглощенной дозы от тепловых нейтронов при бор-нейтронозахватной терапии злокачественных опухолей | 2019 |
|
RU2709682C1 |
| МАТВЕЕВ А.В | |||
| и др | |||
| Модель кинетики остеотропного радиофармпрепарата и определение поглощенных доз при радионуклидной терапии костных метастазов | |||
| Вестник Омского университета | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| ДОЛЯ О.П | |||
| и др | |||
| Математическое моделирование кинетики | |||
Авторы
Даты
2024-06-28—Публикация
2022-09-30—Подача