Настоящее изобретение относится к химико-фармацевтической промышленности, а именно к разработке нового диагностического агента и способа его получения.
Флуоресцентная диагностика - неинвазивный, селективный и чувствительный диагностический метод для оценки локализации опухолевого очага [Sieroń A. et al. The role of fluorescence diagnosis in clinical practice //OncoTargets and therapy. - 2013. - P. 977-982. https://doi.org/10.2147/OTT.S42074]. Последняя используется при раке желудочно-кишечного тракта, а также раке головы и шеи, за которыми следуют легочная, нейро-, молочная и гинекологическая онкология [Schouw H.M. et al. Targeted optical fluorescence imaging: a meta-narrative review and future perspectives //European Journal of Nuclear Medicine and Molecular Imaging. - 2021. - P. 1-21. https://doi.org/10.1007/s00259-021-05504-y].
В настоящее время применяются в клинике или находятся на разных стадиях клинических испытаний флуоресцентные диагностические агенты различных классов. Особый интерес представляют природные хлорины и их производные с интенсивным поглощением в ближней ИК-области спектра. Свет с длиной волны 650-700 нм проникает в ткани на глубину до 20-25 мм, это существенно расширяет возможности используемых в настоящее время методов для диагностики опухолей. Также хлорины обладают тропностью к опухолям и не являются токсичными [Grin M.A., Suvorov N.V., Mironov A.F. Natural chlorins as a promising platform for creating targeted theranostics in oncology //Mendeleev Communications. - 2020. - V. 30. - №. 4. - P. 406-418. https://doi.org/10.1016/j.mencom.2020.07.003]. В основе большинства современных флуоресцентных агентов лежит структура хлорина е6.
Однако хлорины имеют ограниченное применение в качестве флуоресцентных агентов из-за высокой гидрофобности и умеренной селективности накопления в опухолевых клетках. Это диктует необходимость создания новых более селективных производных хлоринов с повышенной тропностью к опухолям и низкой «острой» и «системной» токсичностью для организма.
Из уровня техники известен способ флуоресцентной диагностики рака кожи 5-аминолевулиновой кислоты [патент РФ №2379026]. Недостатком данного фотосенсибилизатора (ФС) является возбуждение флуоресценции в диапазоне длин волн видимого спектра 380-460 нм, что существенно ограничивает его применение ввиду малого проникновения света в ткани.
Ближайшим аналогом заявленного изобретения является хлорин е6, который используется в качестве флуоресцентного агента [Rynda A.Y. et al. Comparative analysis of 5-ALA and chlorin E6 fluorescence-guided navigation in malignant glioma surgery //Khirurgiia. - 2022. - №. 1. - P. 5-14. https://doi.org/10.17116/hirurgia20220115]. Однако хлорин е6, не обладает высокой тропностью к опухолевым клеткам.
Таким образом, техническим результатом заявленного изобретения является повышение уровня селективности накопления диагностического агента в опухолевых клетках, а также повышение уровня флуоресцентной контрастности опухолевых клеток при проведении флуоресцентной диагностики.
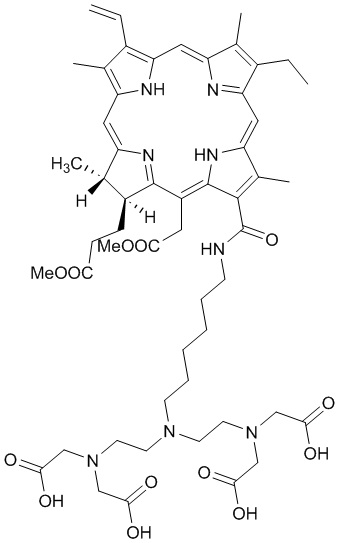
Технический результат заявленного изобретения обеспечивает диагностический агент со структурной формулой (1):
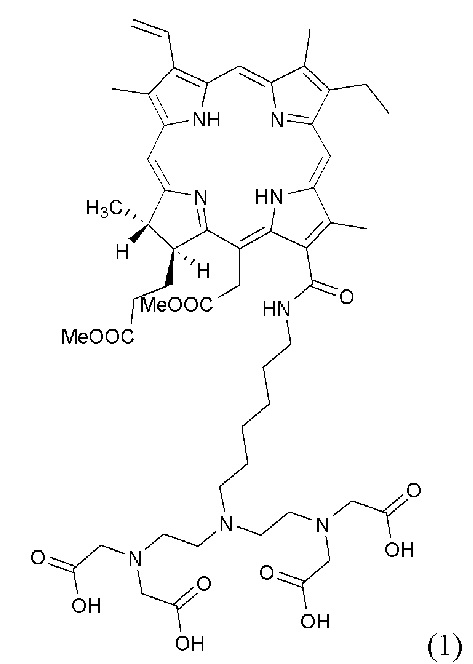
где Ме представляет CH3
Вероятно, высокая контрастность и тропность к опухолевым клеткам заявленного диагностического агента обусловлена наличием полярного фрагмента, способного образовывать цвиттер-ионные формы наподобие аминокислот [https://doi.org/10.1021/acs.bioconjchem.9b00543].
В немалой степени указанный технический результат обеспечивает способ получения указанного выше диагностического агента, включающий в себя следующие стадии:
- реакцию аминогексиламида метилфеофорбида а со структурной формулой (2)
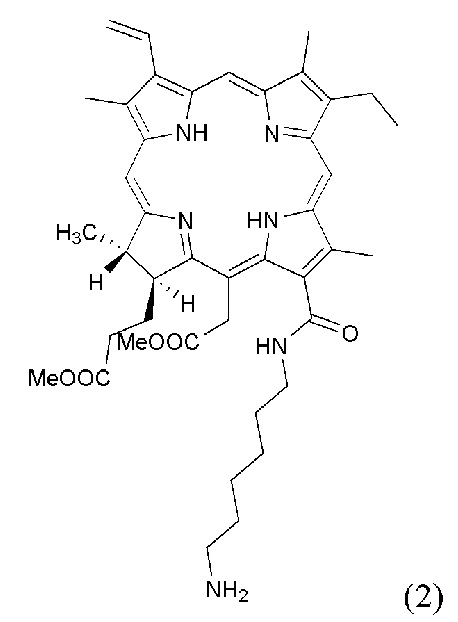
с бис(2-метил-2-пропанил)2,2'-[(2-бромэтил)имино]диацетата со структурной формулой (3)
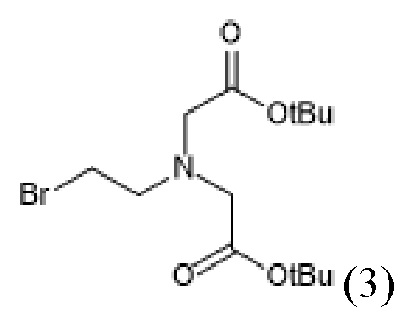
c получением соединения со структурной формулой (4)
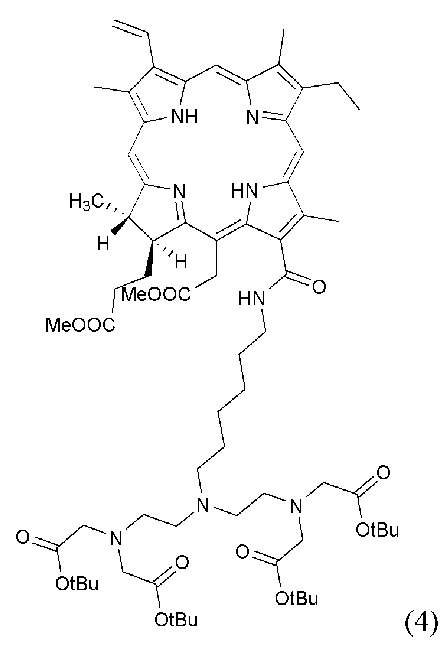
где Ме представляет CH3, OtBu представляет OCH(CH3)3.
- реакцию соединения со структурной формулой (4) и трифторуксусной кислоты в органическом растворителе с получением флуоресцентного диагностического агента по п.1.
Реакция соединения со структурной формулой 3 с аминогексиламидом метилфеофорбида а со структурной формулой 2 может осуществляться при их мольном соотношении от 2:1 до 25:1.
Реакция соединения со структурной формулой (4) и трифторуксусной кислоты может проводиться при их мольном соотношении от 1:4 до 1:1000. Как вариант, время проведения данной реакции может составлять от 30 минут до 24 часов.
Заявленный способ может дополнительно включать стадию лиофильного высушивания полученного продукта с получением его кристаллической формы.
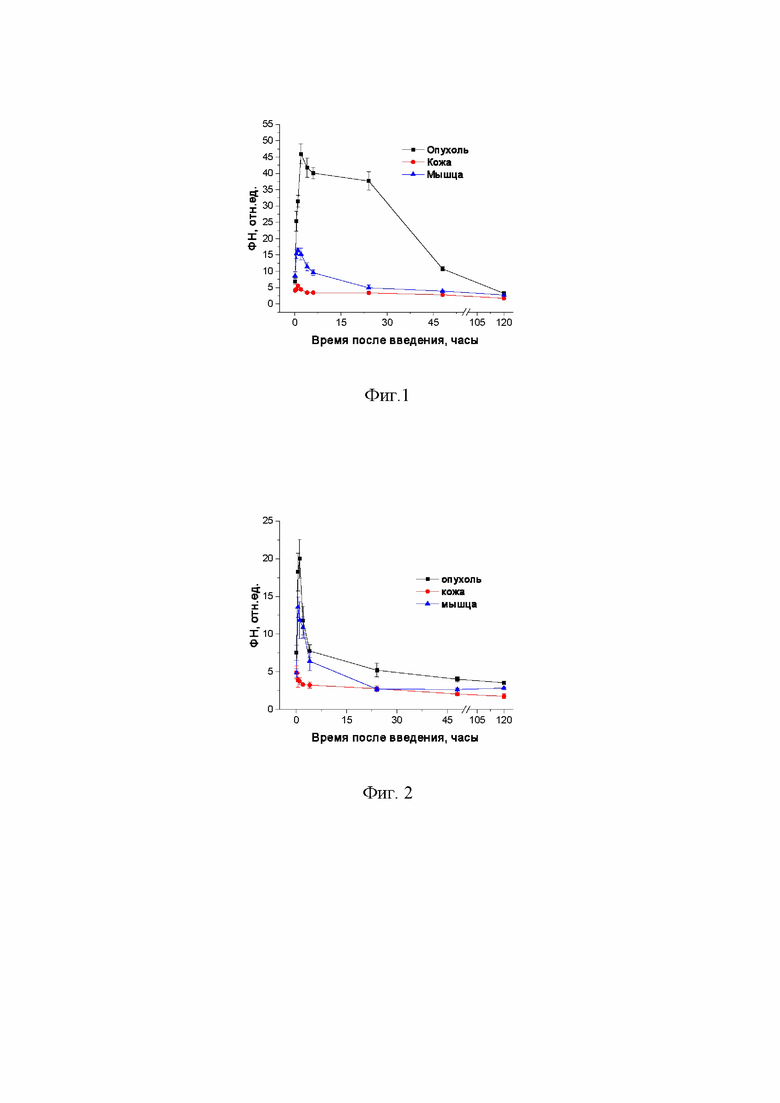
На фиг.1 приведены результаты оценки нормированной флуоресценции (ФН) заявленного диагностического агента со структурной формулой (1) в тканях мышей с опухолью LLC в интервале от 5 минут до 120 часов. Доза 7,5 мг/кг.
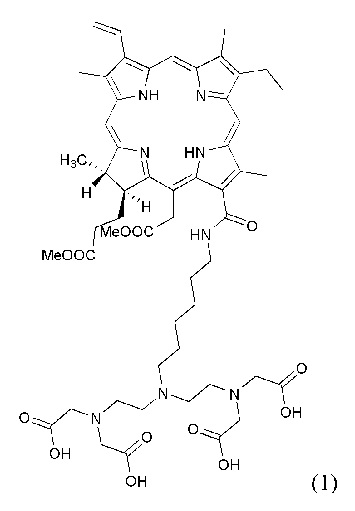
На фиг. 2 приведены результаты оценки нормированной флуоресценции (ФН) хлорина е6 в тканях мышей с опухолью LLC в интервале от 5 минут до 120 часов. Доза 7,5 мг/кг.
Предлагаемое изобретение иллюстрируется нижеследующими примерами.
Пример 1. Получение заявленного диагностического агента
К растворенным в 2 мл CH2Cl2 0,15 г (0,2 ммоль) аминогексиламида метилфеофорбида а (структурная формула (2)) добавили 0,56 г (1,6 ммоль) бис(2-метил-2-пропанил)2,2'-[(2-бромэтил)имино]диацетата (структурная формула (3)) и 55 мг (0,4 ммоль) K2CO3. Реакция проходила при постоянном перемешивании в течение 24 часов при комнатной температуре, протекание реакции отслеживали методом тонкослойной хроматографии. Продукт реакции выделяли из реакционной смеси методом экстракции (CH2Cl2/Н2О; 20/80; v/v). После продукт реакции осушали над Na2SO4 и упаривали при пониженном давлении. Очистку полученного продукта проводили с помощью колоночной хроматографии в системе растворителей (CH2Cl2/CH3OH; 25/1; v/v) и концентрировали при пониженном давлении. Выход реакции получения соединения со структурной формулой (4) составил 0,215 г (85%).
ESI MS m/z рассчитано для C70H104N8O13 [M+H]+: 1264.77; [M+2H]2+: 632.39. Найдено: 1265.77; 633.39.
1H ЯМР (300 МГц, CDCl3, δ, ppm): 9.70 (H, с, 10-H), 9.63 (H, с, 5-H), 8.80 (H, с, 20-H), 8.08 (H, дд, J = 17.9 Гц, 11.7 Гц, 31-H), 6.60 (H, м, 132-NH), 6.34 (H, д, J = 17.7 Гц, E-32-H), 6.13 (H, д, J = 11.6 Гц, Z-32-H), 5.55 (H, д, J = 18.8 Гц, 15-CH2a), 5.26 (H, д, J = 19.0 Гц,15-CH2b), 4.47 (H, кв, J = 7.6 Гц, 18-H), 4.36 (H, д, J = 8.5 Гц, 17-H), 3.80 (3H, с, 153-CO2CH3), 3.80 (2H, м, 81-CH2), 3.60 (3H, с, 174-CO2CH3), 3.57 (3H, с, 123-CH3), 3.49 (3H, с, 2-CH3), 3.44 (8Н, с, 4СН2СОО), 3.32 (3H, с, 7-CH3), 3.11 (2Н, м, N-СН2), 2.54 (2H, м, 172-CH2), 2.18 (2H, м, 171-CH2), 1.82 (3H, м, 18-CH3), 1.73 (3H, т, J = 7.7 Гц, 82-CH3), 1.63 - 1.48 (6Н, м, CH2-СН2-N, N-CH2), 1.44 (36H, c, O-tBu), 1.36 - 1.21 (4H, м, CH2-CH2), -1.81 (H, NH), -1.82 (H, NH).
Далее к 100 мг (0,079 ммоль) алкилированного продукта со структурной формулой (4) добавили 3 мл 20% раствора трифторуксусной кислоты в CH2Cl2. Реакция проходила при постоянном перемешивании в течение 3 часов при комнатной температуре. Продукт выделяли из реакционной смеси методом экстракции (CH2Cl2/Н2О/NaHCO3 (10% раствор); 20/80/5; v/v), осушали над Na2SO4 и упаривали при пониженном давлении. Очистку полученного продукта проводили с помощью колоночной хроматографии в системе растворителей (CH2Cl2/CH3OH; 20/1; v/v) и упаривали при пониженном давлении. Выход реакции получения соединения со структурной формулой (1) составил 78 мг (95%).
ESI MS m/z рассчитано для C54H72N8O13 [M+H]+: 1040.52; [M+2H]2+:520,7. Найдено: 1041.53; 521.27.
1Н ЯМР (300 МГц, ДМСО-d6, δ, ppm): 9.85 (H, c, 10-H), 9.82 (H, c, 5-H), 9.17 (H, c, 20-H), 8.33 (H, дд, J = 17.8, 11.6 Гц, 31-H), ), 7.75 (H, м, 132-NH), 6.47 (H, д, J = 17.8 Гц, E-32-H), 6.21 (H, д, J = 11.6 Гц, Z-32-H), 5.54 (2H, д, J = 18.8 Гц, 15-CH2a), 5.33 (2H, д, J = 18.9 Гц,15-CH2b), 4.62 (H, м, 18-H), 4.43 (H, д, J = 9.9 Гц, 17-H), 3.85 (5H, м, 153-CO2CH3, 81-CH2), 3.68 (3H, с, 174-CO2CH3), 3.54 (14H, м, 123-CH3, 2-CH3, 4СН2СОО), 3.34 (3H, с, 71-CH3), 3.09 (4Н, м, N-СН2, 172-CH2), 1.81 (2H, м, 171-CH2), 1.67 (6H, м, 181-CH3, 82-CH3), 1.24 (10Н, м, CH2-СН2-N, N-CH2, CH2-CH2), -1.96 (H, с, NH), -2.15 (H, с, NH).
Пример 2. Изучение биологического распределения заявленного диагностического агента
Тестируемые субстанции заявленного диагностического агента со структурной формулой (1) и хлорина е6 (контроль) вводили однократно внутривенно в дозе 7,5 мг/кг мышам линии C57Bl/6j опухоленосителям с привитым подкожно модельным опухолями (карцинома легкого Льюис LLC). Контрольным животным вводили 0,9% NaCl в дозе 5,0 мл/кг.
Через различные интервалы времени после введения субстанций (через 0,08; 0,5, 1, 2, 4, 6, 24, 48 и 120 часов) мышей с подкожно привитой опухолью LLC умерщвляли путем их помещения в СО2-камеру (ZOONLAB GmbH, Германия). Измерение экзогенной флуоресценции тканей проводили ex vivo сразу после эвтаназии мышей (спектральный диапазон 640-900 нм). На каждую точку использовали биологический материал от 3-х животных (не менее 4-х измерений в каждом образце ткани), всего 12 измерений. Математическую обработку спектров флуоресценции проводили с помощью программы «ЛЭСА-06». При возбуждении флуоресценции в красной области спектра (632 нм), интегральную интенсивность флуоресценции в диапазоне 640-900 нм (S1) нормировали на интегральную интенсивность сигнала обратного диффузного рассеяния в ткани (S2) возбуждающего лазерного излучения (632 нм) и определяли нормированную флуоресценцию (ФН = S1/S2) препарата в сыворотке крови, органах и тканях животных.
Показано, что нормированная флуоресценция заявленного диагностического агента со структурной формулой (1) достигает максимальных значений в опухоли LLC к 2 часам (45,93±3,04 отн. ед.) и сохраняется на высоком уровне до 24 часов (37,65±2,81 отн. ед.) (фиг. 2), в то время как у хлорина е6 флуоресценция достигала максимального значения через 30 минут (18,24±2,50 отн. ед.) и сохранялась на высоком уровне в течение 1 часа (20,00±2,56 отн. ед.) (фиг. 3). Флуоресцентная контрастность (соотношение флуоресценции в опухоли и здоровой ткани) заявленного диагностического агента со структурной формулой (1) составила 11, в то время хлорин е6 имеет флуоресцентную контрастность 3,5 в максимуме накопления. Полученные результаты представлены в таблице 1.
Таблица 1
Полученные данные свидетельствуют о высоком накоплении заявленного диагностического агента со структурной формулой (1) в тканях злокачественного новообразования, при этом было установлено, что последнее обладает в 3 раза большей селективностью накопления в опухолевой ткани по сравнению с хлорином е6. Кроме того, за счет долгого времени сохранения высокого уровня флуоресценции карбоксилатного производного хлорина со структурной формулой (1) в опухоли становится возможным проводить процедуру флуоресцентной диагностики в течение длительного времени, что актуально для интраоперационной флуоресцентной навигации.
Таким образом, использование заявленного флуоресцентного диагностического агента позволяет повысить уровень селективности накопления диагностического агента в опухолевых клетках, а также повысить уровень флуоресцентной контрастности опухолевых клеток при проведении флуоресцентной диагностики.
| название | год | авторы | номер документа |
|---|---|---|---|
| Фотосенсибилизатор и способ его получения | 2021 |
|
RU2772691C1 |
| Фотосенсибилизатор для лечения рака предстательной железы и способ его получения | 2018 |
|
RU2670087C1 |
| ПРЕПАРАТ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РАКА С ЕГО ИСПОЛЬЗОВАНИЕМ | 2012 |
|
RU2521327C1 |
| НОВЫЙ СПОСОБ И ПРИМЕНЕНИЕ НЕСИММЕТРИЧНО мезо-ЗАМЕЩЕННЫХ ПОРФИРИНОВ И ХЛОРИНОВ ДЛЯ ФДТ | 2009 |
|
RU2574062C9 |
| КОНЪЮГАТ ФОТОСЕНСИБИЛИЗАТОРА И ХИТОЗАНА И ЕГО ПРИМЕНЕНИЕ | 2013 |
|
RU2675830C2 |
| АМИНОАМИДЫ В РЯДУ БАКТЕРИОХЛОРОФИЛЛА A, ОБЛАДАЮЩИЕ ФОТОДИНАМИЧЕСКОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2548675C9 |
| ГЛИКОЛИПИДНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ОПУХОЛЕЙ | 2015 |
|
RU2719486C2 |
| ПРОИЗВОДНЫЕ ИЛИДА СУЛЬФОКСОНИЯ В КАЧЕСТВЕ ЗОНДОВ ДЛЯ ЦИСТЕИНОВОЙ ПРОТЕАЗЫ | 2019 |
|
RU2815018C2 |
| ПРОИЗВОДНЫЕ НАФТИЛЕНА КАК ИНГИБИТОРЫ ЦИТОХРОМА Р450 | 2004 |
|
RU2363696C2 |
| ЛЕЧЕНИЕ ИЛИ ПРОФИЛАКТИКА ПРОЛИФЕРАТИВНЫХ СОСТОЯНИЙ | 2010 |
|
RU2705548C2 |
Настоящее изобретение относится к химико-фармацевтической промышленности, а именно к разработке нового флуоресцентного диагностического агента со структурной формулой (1) и способу его получения. Техническим результатом изобретения является повышение уровня селективности накопления диагностического агента в опухолевых клетках, а также повышение уровня флуоресцентной контрастности опухолевых клеток при проведении флуоресцентной диагностики. 2 н. и 4 з.п. ф-лы, 2 ил., 1 табл., 2 пр.
1. Диагностический агент со структурной формулой (1)
 (1)
(1)
2. Способ получения диагностического агента по п.1, включающий:
- реакцию соединения со структурной формулой (2)
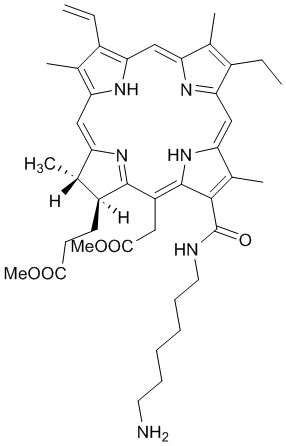 (2)
(2)
с соединением со структурной формулой (3)
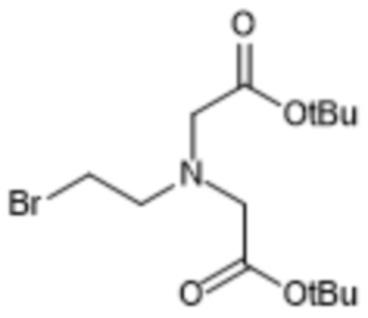 (3)
(3)
в органическом растворителе в присутствии карбоната калия с получением соединения со структурной формулой (4)
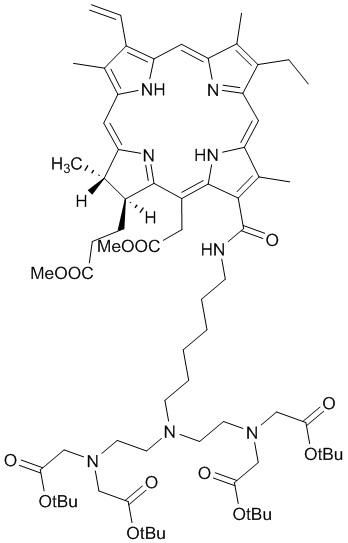 (4)
(4)
- реакцию соединения со структурной формулой (4) и трифторуксусной кислоты в органическом растворителе с получением флуоресцентного диагностического агента по п.1.
3. Способ по п. 2, где реакция соединения со структурной формулой (3) с соединением со структурной формулой (2) осуществляется при их мольном соотношении от 2:1 до 25:1.
4. Способ по п. 2, где реакция соединения со структурной формулой (4) и трифторуксусной кислоты проводится при мольном соотношении от 1:4 до 1:1000.
5. Способ по п. 2, где время реакции соединения со структурной формулой (4) и трифторуксусной кислоты составляет от 30 минут до 24 часов.
6. Способ по п. 2, отличающийся тем, что включает стадию лиофильного высушивания продукта с получением его кристаллической формы.
| РЫНДА А.Ю | |||
| и др | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Пирогова, 2022, N 1, с | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| GRIN M.A | |||
| et al | |||
| Natural chlorins as a promising platform for creating targeted theranostics in oncology, Mendeleev Communications, 2020, v | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| Электрическая лампа накаливания с двумя нитями | 1923 |
|
SU406A1 |
Авторы
Даты
2024-07-03—Публикация
2023-12-13—Подача