[Область техники]
[0001]
Настоящее изобретение относится к новому применению никотинамид мононуклеотида (NMN) и никотинамид рибозида (NR). Например, настоящее изобретение относится к композиции, содержащей NMN или NR, для применения для лечения или профилактики заболевания, расстройства или симптома, связанного с Hsd3b6 или его гомологом, или к способу с их использованием. В частности, настоящее изобретение относится к композиции, содержащей NMN или NR, для применения для улучшения функции мейбомиевой железы или к способу их использования.
[Уровень техники]
[0002]
Ввиду предполагаемой возможности, что окисленные формы промежуточных метаболитов никотинамидадениндинуклеотида (NAD+), такие как никотинамид рибозид (NR) и никотинамид мононуклеотид (NMN), т.е. продукты ферментативной реакции никотинамидфосфорибозилтрансферазы (NAMPT), могут оказывать эффект пролонгирования продолжительности жизни, разработка их в качестве добавки продолжается. Однако механизм действия активности NMN и NR до конца не изучен.
[Краткое изложение сущности изобретения]
[Решение задачи]
[0003]
Настоящее изобретение обеспечивает применение никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR) или композиции, содержащей их, для улучшения активности Hsd3b6 или его гомолога. Улучшение активности Hsd3b6 или его гомолога может обеспечить лечение или профилактику заболевания, расстройства или симптома, связанного с активностью Hsd3b6 или его гомолога.
[0004]
Настоящее изобретение, в частности, обеспечивает применение никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR) или композиции, содержащей их, для улучшения функции мейбомиевой железы. Композиция может характеризоваться тем, что ее вводят в глаз субъекта. Примеры улучшения функции мейбомиевой железы включают увеличение количества ацинарных клеток мейбомиевой железы, увеличение секреции липидов мейбомиевой железой и тому подобное. В одном варианте осуществления может быть предоставлена композиция для лечения или профилактики заболевания, сопровождающегося дисфункцией мейбомиевых желез. В другом варианте осуществления композиция по настоящему изобретению демонстрирует эффект улучшения атрофии ткани мейбомиевой железы и может повышать активность синтазы стероида, который воздействует на липид, секретируемый мейбомиевой железой. Поскольку композиция по настоящему изобретению может нормализовать состав липидов, секретируемых мейбомиевой железой, понятно, что липиды в мейбомиевой железе могут быть нормализованы. Кроме того, композиция по настоящему изобретению может способствовать выработке тестостерона, который, как известно, способствует выработке липидов мейбомиевой железой. Поскольку половые гормоны, такие как тестостерон, влияют на выработку липидов мейбомиевыми железами, понятно, что композиция по настоящему изобретению может нормализовать компонентный состав липидов в ткани мейбомиевых желез.
[0005]
Например, следующие пункты представлены в предпочтительных вариантах осуществления настоящего изобретения.
(Пункт A1)
Композиция, содержащая никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR), для применения для улучшения активности Hsd3b6 или его гомолога.
(Пункт A1-2)
Композиция, содержащая никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR), для применения для лечении или профилактики заболевания, расстройства или симптома, связанного с активностью Hsd3b6 или его гомолога.
(Пункт A1-3)
Композиция по любому из предшествующих пунктов, где заболевание, связанное с активностью Hsd3b6 или его гомолога, выбрано из группы, состоящей из дисфункции мейбомиевых желез, заболеваний, вызванных снижением уровня стероидного гормона (например, тестостерона, эстрогена и тому подобное), постменопаузального синдрома, остеопороза, заболеваний образа жизни, возрастного андрогенного дефицита у мужчин и инфаркта миокарда.
(Пункт A2)
Композиция по любому из предшествующих пунктов, где композицию вводят в глаз субъекта.
(Пункт A3)
Композиция, содержащая никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR), для применения для улучшения функции мейбомиевой железы.
(Пункт A4)
Композиция по любому из предшествующих пунктов для применения для увеличения количества ацинарных клеток мейбомиевой железы.
(Пункт A5)
Композиция по любому из предшествующих пунктов для применения для увеличения секреции липидов мейбомиевой железой.
(Пункт A6)
Композиция по любому из предшествующих пунктов для применения для лечения или профилактики заболевания, сопровождающегося дисфункцией мейбомиевой железы.
(Пункт A6-1)
Композиция для применения для лечения или профилактики дисфункции мейбомиевых желез, содержащая никотинамид мононуклеотид (NMN) и/или никотинамидрибозид (NR).
(Пункт A6-2)
Композиция по любому из предшествующих пунктов, где дисфункция мейбомиевых желез сопровождается снижением секреции мейбомиевых желез.
(Пункт A6-3)
Композиция по любому из предшествующих пунктов, где дисфункция мейбомиевых желез сопровождается воспалительным заболеванием.
(Пункт A6-4)
Композиция по любому из предшествующих пунктов, где воспалительное заболевание включает по меньшей мере одно заболевание, выбранное из группы, состоящей из мейбомита, поверхностного (точечного) кератита и блефарита.
(Пункт A6-5)
Композиция по любому из предшествующих пунктов, где дисфункция мейбомиевых желез сопровождается избыточным накоплением липидов в протоке.
(Пункт A6-6)
Композиция по любому из предшествующих пунктов, где дисфункция мейбомиевых желез сопровождается дискомфортом в глазах, ощущением инородного тела и/или ощущением давления.
(Пункт A7)
Композиция по любому из предшествующих пунктов, где заболевание, сопровождающееся дисфункцией мейбомиевых желез, представляет собой мейбомит, задний блефарит, кератит, конъюнктивит, кератоконъюнктивит, связанный с мейбомитом, глазной пемфигоид, синдром Шегрена, синдром Стивенса-Джонсона, реакция «трансплантат против хозяина» (РТПХ) и нарушение зрительной функции.
(Пункт B1)
Способ улучшения активности Hsd3b6 или его гомолога у субъекта или лечения, или профилактики заболевания, расстройства или симптома, связанного с активностью Hsd3b6 или его гомолога.
(Пункт B2)
Способ по пункту B1, включающий введение субъекту никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR).
(Пункт B3)
Способ по пункту B1 или B2, дополнительно включающий измерение активности Hsd3b6 или его гомолога у субъекта.
(Пункт B4)
Способ по любому из пунктов B1-B3, включающий введение NMN и/или NR, когда активность Hsd3b6 или его гомолога у субъекта измеряют и активность снижена.
(Пункт C1)
Способ улучшения функции мейбомиевой железы субъекта или лечения, или профилактики заболевания, расстройства или симптома, сопровождающегося дисфункцией мейбомиевой железы.
(Пункт C2)
Способ по пункту C1, включающий введение субъекту никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR).
(Пункт C3)
Способ по пункту C1 или C2, дополнительно включающий проверку функции мейбомиевой железы субъекта.
(Пункт C4)
Способ по любому из пунктов C1-C3, включающий введение NMN и/или NR, когда функцию мейбомиевых желез субъекта проверяют и функция уменьшена.
(Пункт C5)
Способ по пункту C4, где функцию мейбомиевых желез проверяют с помощью осмотра глаза с помощью щелевой лампы, мейбографии, конфокальной микроскопии, DR-1, кожно-слизистого соединения, мейбометра, химического анализа липидов, количества испарений, BUT или опросника субъективных симптомов.
(Пункт C6)
Способ по любому из пунктов C1-C5, где заболевание, расстройство или симптом, сопровождающийся дисфункцией мейбомиевой железы, выбрано из группы, состоящей из мейбомита, заднего блефарита, кератита, конъюнктивита, кератоконъюнктивита, связанного с мейбомитом, глазного пемфигоида, синдрома Шегрена, синдрома Стивенса-Джонсона, реакции «трансплантат против хозяина» (РТПХ) и нарушения зрительной функции.
(Пункт C7)
Способ по любому из пунктов C1-C6 для увеличения количества ацинарных клеток мейбомиевой железы.
(Пункт C8)
Способ по любому из пунктов C1-C6 для увеличения секреции липидов мейбомиевой железой.
(Пункт C9)
Способ по любому из пунктов C1-C6 для усиления выработки тестостерона в мейбомиевой железе.
(Пункт D1)
Применение никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR) для получения композиции, улучшающей функцию мейбомиевой железы.
(Пункт D2)
Применение по пункту D1, где композиция предназначена для увеличения количества ацинарных клеток мейбомиевой железы.
(Пункт D3)
Применение по пункту D1, где композиция предназначена для увеличения секреции липидов мейбомиевой железой.
(Пункт D4)
Применение по любому из пунктов D1-D3, где композиция предназначена для лечения или профилактики заболевания, сопровождающегося дисфункцией мейбомиевой железы.
(Пункт D5)
Применение по пункту D4, где заболевание, сопровождающееся дисфункцией мейбомиевой железы, выбрано из группы, состоящей из мейбомита, заднего блефарита, кератита, конъюнктивита, кератоконъюнктивита, связанного с мейбомитом, глазного пемфигоида, синдрома Шегрена, синдрома Стивенса-Джонсона, реакции «трансплантат против хозяина» (РТПХ) и нарушения зрительной функции.
(Пункт D6)
Применение по любому из пунктов D1-D5, где композиция предназначена для усиления выработки тестостерона в мейбомиевой железе.
(Пункт E1)
Применение никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR) для получения композиции для лечения или профилактики дисфункции мейбомиевых желез.
(Пункт E2)
Применение по пункту E1, где дисфункция мейбомиевых желез сопровождается снижением секреции мейбомиевых желез.
(Пункт E3)
Применение по пункту E1, где дисфункция мейбомиевых желез сопровождается воспалительным заболеванием.
(Пункт E4)
Применение по пункту E3, где воспалительное заболевание включает по меньшей мере одно заболевание, выбранное из группы, состоящей из мейбомита, поверхностного (точечного) кератита и блефарита.
(Пункт E5)
Применение по пункту E1, где дисфункция мейбомиевых желез сопровождается избыточным накоплением липидов в протоке.
(Пункт E6)
Применение по пункту E1, где дисфункция мейбомиевых желез сопровождается дискомфортом в глазах, ощущением инородного тела и/или ощущением давления.
(Пункт F1)
Никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR) для применения для улучшения активности Hsd3b6 или его гомолога у субъекта или лечения, или профилактики заболевания, расстройства или симптома, связанного с активностью Hsd3b6 или его гомолога.
(Пункт G1)
Никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR) для применения для улучшения функции мейбомиевой железы или лечения, или профилактики заболевания, расстройства или симптома, сопровождающегося дисфункцией мейбомиевой железы.
(Пункт G2)
Никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR) по пункту G1, где заболевание, расстройство или симптом, сопровождающийся дисфункцией мейбомиевой железы, выбрано из группы, состоящей из мейбомита, заднего блефарита, кератита, конъюнктивита, кератоконъюнктивита, связанного с мейбомитом, глазного пемфигоида, синдрома Шегрена, синдрома Стивенса-Джонсона, реакции «трансплантат против хозяина» (РТПХ) и нарушения зрительной функции.
(Пункт H1)
Композиция для применения для усиления выработки тестостерона в мейбомиевой железе, содержащая никотинамид мононуклеотид (NMN) и/или никотинамид рибозид.
(Пункт H2)
Композиция по пункту H1, где композицию вводят в глаз субъекта.
(Пункт I1)
Способ применения для повышения выработки тестостерона в мейбомиевой железе субъекта.
(Пункт I2)
Способ по пункту I1, включающий введение субъекту никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR).
(Пункт J1)
Никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR) для усиления выработки тестостерона в мейбомиевой железе.
(Пункт J2)
Никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR) по пункту J1, который вводят в глаз субъекта.
(Пункт K1)
Применение никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR) для получения лекарственного средства для усиления выработки тестостерона в мейбомиевой железе.
(Пункт K2)
Применение по пункту K1, характеризующееся введением в глаз субъекта.
[0006]
Настоящее изобретение предназначено для того, чтобы один или более признаков, описанных выше, могли быть предоставлены не только в виде явно раскрытых комбинаций, но и в виде других их комбинаций. Дополнительные варианты осуществления и преимущества настоящего изобретения очевидны специалистам в данной области техники при чтении и понимании следующего подробного описания по мере необходимости.
[Полезные эффекты изобретения]
[0007]
Настоящее изобретение обеспечивает композицию для применения для улучшения активности Hsd3b6 или его гомолога, или лечения или профилактики заболевания, расстройства или симптома, связанного с активностью Hsd3b6 или его гомолога, или способ для этого. В частности, настоящее изобретение может предоставить композицию для применения для улучшения функции мейбомиевой железы или способ для этого.
[Краткое описание чертежей]
[0008]
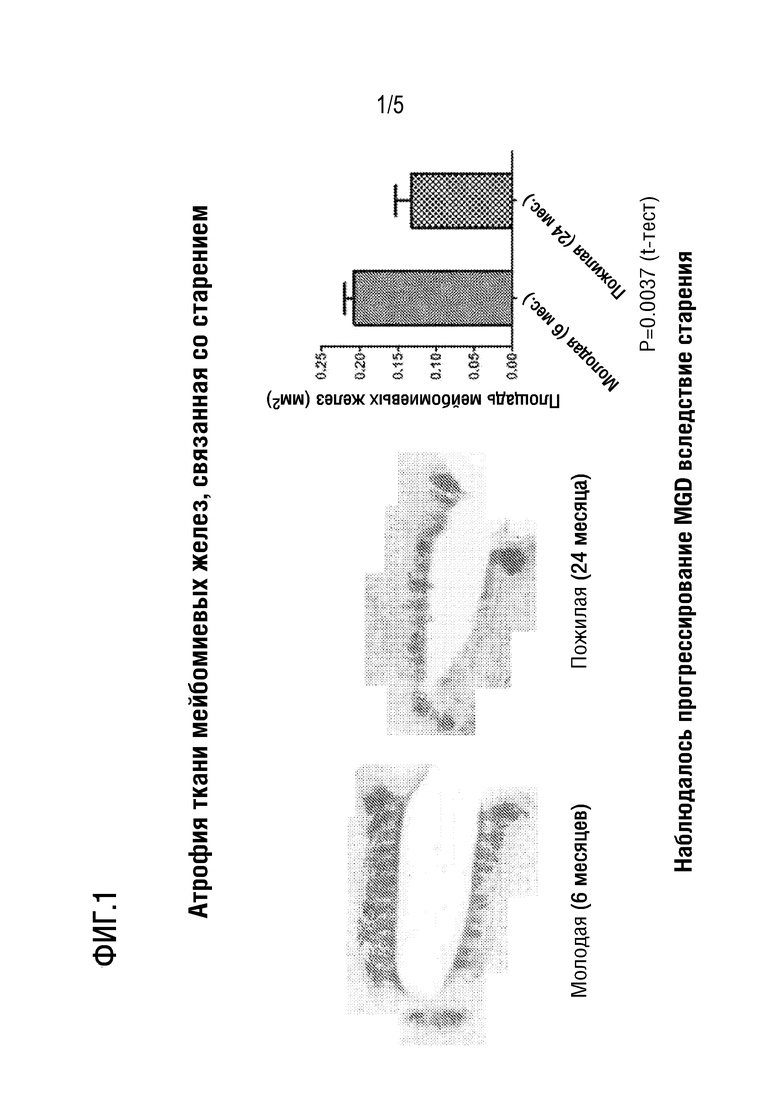
[Фигура 1] На фиг. 1 представлена диаграмма, показывающая атрофию ткани мейбомиевых желез, связанную со старением. Слева и в центре представлены изображения окрашенных век глаз 6-месячных и 24-месячных мышей соответственно. Правая сторона представляет собой гистограмму, на которой сравниваются средние окрашенные площади для 6-месячных и 24-месячных мышей.
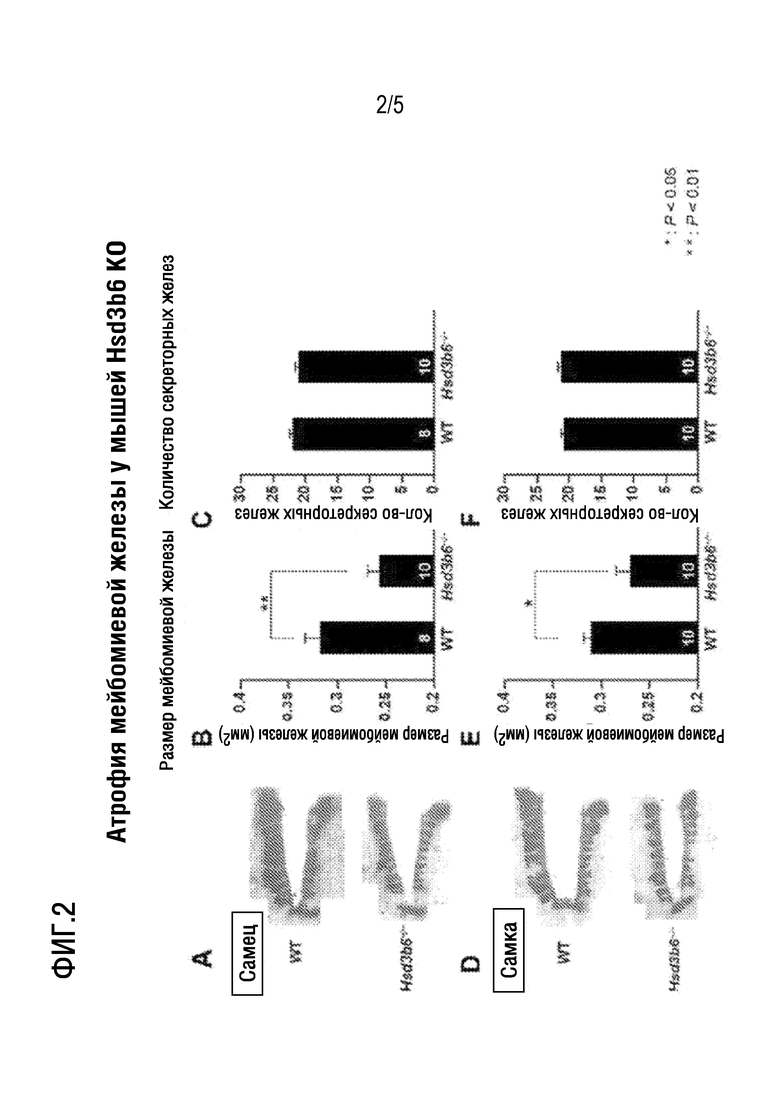
[Фигура 2] На фиг. 2 представлена диаграмма, показывающая изменение в ткани мейбомиевой железы 2-месячной нокаутной мыши по Hsd3b6 (KO) (размер мейбомиевой железы и количество секреторных протоков). В верхнем ряду показаны результаты для мышей-самцов, а в нижнем ряду показаны результаты для мышей-самок.
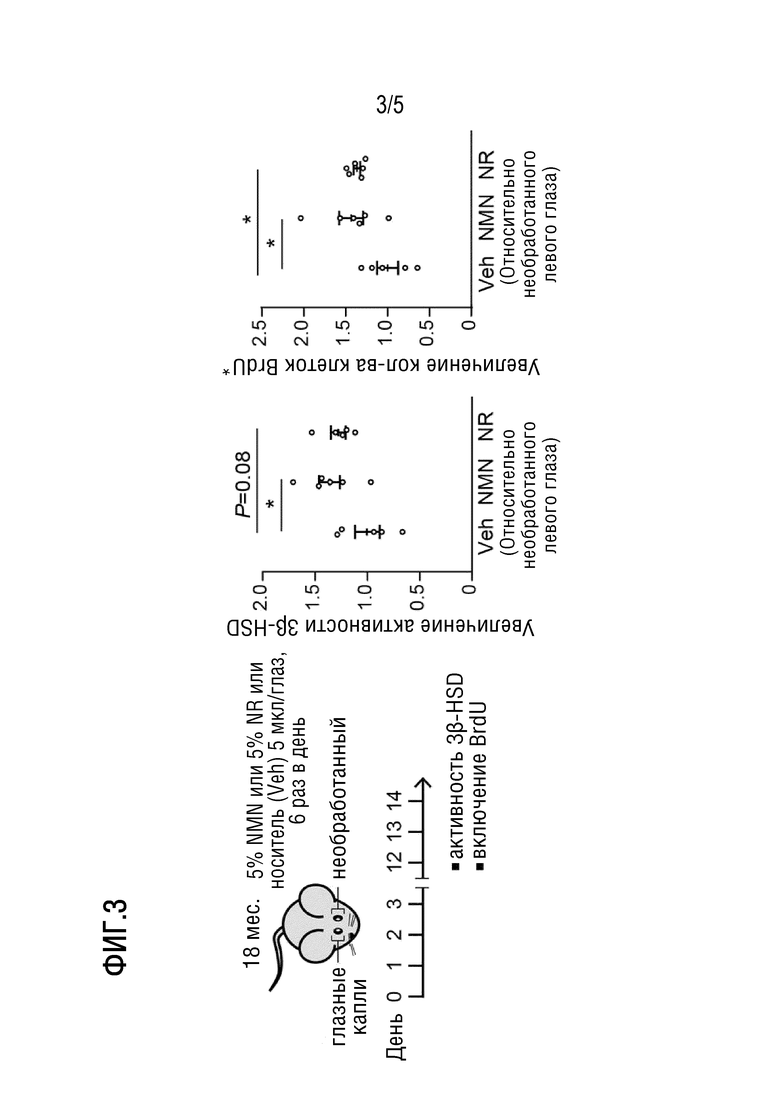
[Фигура 3] На фиг. 3 представлена диаграмма, показывающая изменение ферментативной активности Hsd3b6 и пролиферативной активности базальных клеток мейбомиевой железы в мейбомиевой железе вследствие инстилляции глазных капель NMN или NR в течение 2 недель 1,5-летним мышам дикого типа.
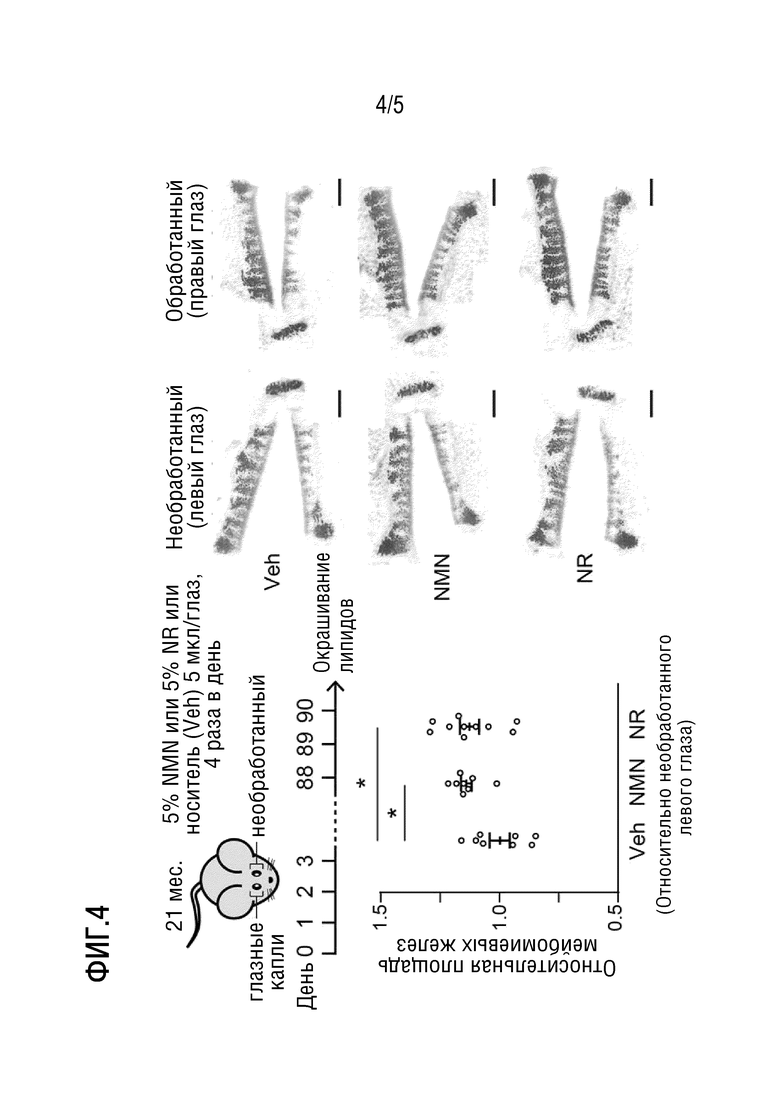
[Фигура 4] На фиг. 4 представлена диаграмма, показывающая эффект инстилляции глазных капель NMN или NR в течение 3 месяцев 1,75-летним мышам дикого типа на ткань мейбомиевых желез. На фигуре показаны репрезентативные изображения окрашивания век левого глаза (без лечения) и правого глаза (инстилляция глазных капель), а также график, показывающий окрашенную область у каждого индивида (правый глаз/левый глаз).
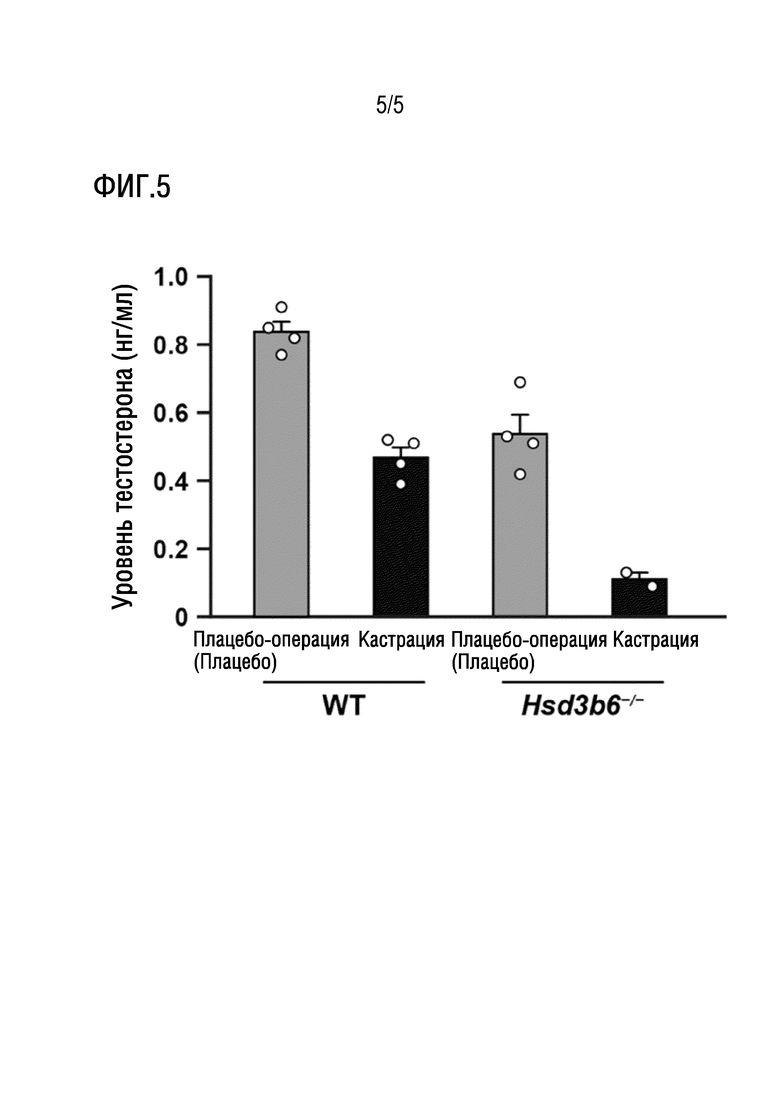
[Фигура 5] На фиг. 5 представлена диаграмма, показывающая содержание тестостерона в ткани мейбомиевых желез после кастрации и после плацебо-операции у самцов 2-месячных мышей дикого типа (WT) и нокаутных по Hsd3b6 (KO).
[Описание вариантов осуществления]
[0009]
Настоящее изобретение описано ниже. Во всем описании выражение в единственном числе следует понимать, как охватывающее его понятие во множественном числе, если специально не указано иное. Таким образом, формы единственного числа также следует понимать, как охватывающие его понятие во множественном числе, если специально не указано иное. Термины, используемые в настоящем документе, также следует понимать, как используемые в значении, которое обычно используется в данной области техники, если специально не указано иное. Таким образом, если не указано иное, все терминологии и научно-технические термины, которые используются в настоящем документе, имеют то же значение, которое обычно понимается специалистом в области, к которой относится настоящее раскрытие. В случае противоречия настоящее описание (включая определения) имеет приоритет.
[0010]
(Определения)
Используемый в настоящем документе термин «примерно» относится к диапазону ±10% от числового значения, описанного после «примерно», если не указано иное.
[0011]
Используемый в настоящем документе термин «субъект» относится к объекту назначения (трансплантации) лекарственного средства или способа лечения и профилактики по настоящему изобретению. Примеры субъектов включают млекопитающих (например, человека, мышей, крыс, хомяков, кроликов, кошек, собак, коров, лошадей, овец, обезьян и тому подобное), но предпочтительными являются приматы, и особенно предпочтительным является человек.
[0012]
В настоящем документе «или» используется, когда могут быть использованы «по меньшей мере один или несколько» из перечисленных в предложении объектов. Когда в настоящем документе явно указано "в пределах диапазона" "двух значений", диапазон также включает сами два значения.
[0013]
Используемый в настоящем документе термин «терапия (лечение)» относится к излечению заболевания или симптома, или подавлению симптома. «Предупреждение (профилактика)» относится к предупреждению проявления заболевания или симптома заблаговременно. Эта концепция также включает задержку проявления заболевания или симптома и минимизацию проявления заболевания или симптома.
[0014]
Используемый в настоящем документе термин «производное» относится к соединению, имеющему структуру ядра, которая является такой же или похожей на структуру исходного соединения, но имеет химическую или физическую модификацию, такую как другая функциональная группа или дополнительная функциональная группа. Производное имеет такую же или аналогичную биологическую активность, что и исходное соединение.
[0015]
Используемый в настоящем документе термин «фармацевтически приемлемая соль» относится к аддитивной соли с неорганической или органической кислотой соединения по настоящему изобретению, которая является относительно нетоксичной. Эти соли могут быть получены временно во время окончательного выделения и очистки соединения или путем взаимодействия очищенного соединения в форме его свободного основания отдельно с подходящей органической или неорганической солью и выделения соли, образованной таким образом.
[0016]
Примеры фармацевтически приемлемых основных солей соединения по настоящему изобретению включают соли щелочных металлов, такие как соли натрия и соли калия; соли щелочноземельных металлов, такие как соли кальция и соли магния; соли аммония; соли алифатических аминов, такие как соли триметиламина, соли триэтиламина, соли дициклогексиламина, соли этаноламина, соли диэтаноламина, соли триэтаноламина, соли прокаина, соли меглюмина, соли диэтаноламина и соли этилендиамина; соли аралкиламина, такие как соли N, N-дибензилэтилендиамина и бенетамина; соли гетероциклических ароматических аминов, такие как соли пиридина, соли пиколина, соли хинолина и соли изохинолина; соли четвертичного аммония, такие как соли тетраметиламмония, соли тетраэтиламмония, соли бензилтриметиламмония, соли бензилтриэтиламмония, соли бензилтрибутиламмония, соли метилтриоктиламмония и соли тетрабутиламмония; соли основных аминокислот, такие как соли аргинина и соли лизина; и тому подобное.
[0017]
Примеры фармацевтически приемлемых кислых солей соединения по настоящему изобретению включают соли неорганических кислот, такие как гидрохлориды, сульфаты, нитраты, фосфаты, карбонаты, гидрокарбонаты и перхлораты; соли органических кислот, такие как ацетаты, пропионаты, лактаты, малеаты, фумараты, тартраты, малаты, цитраты и аскорбаты; сульфонаты, такие как метансульфонаты, изетионаты, бензолсульфонаты и п-толуолсульфонаты; кислые аминокислоты, такие как аспартаты и глутаматы; и тому подобное.
[0018]
Используемый в настоящем документе термин «сольват» относится к сольвату соединения по настоящему изобретению или его фармацевтически приемлемой соли, включая, например, сольват органического растворителя (например, спирта (этанола или т.п.)-ата), гидрат и тому подобное. При образовании гидрата это может быть согласовано с любым количеством молекул воды. Примеры гидратов включают моногидраты, дигидраты и тому подобное.
[0019]
Используемый в настоящем документе термин «гомолог» относится к белку или гену, имеющему последовательность аминокислот или последовательность оснований, полученную от одного и того же предка. Гомолог от видообразования называется ортологом. Гомолог, вновь созданный в результате генетической дупликации в виде организма, называется паралогом.
[0020]
(Активный ингридиент)
Никотинамид мононуклеотид (NMN) представляет собой соединение со следующей структурой
[Химическая формула 1]
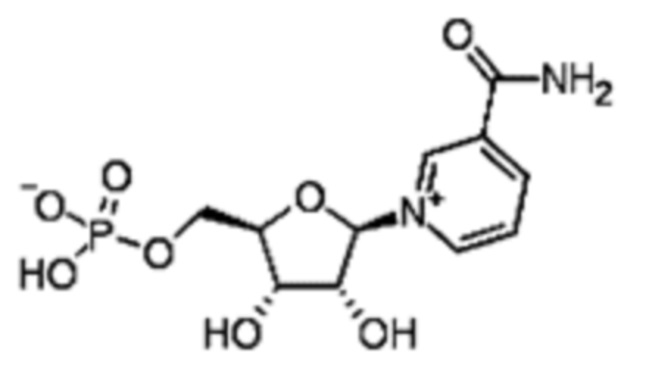 ,
,
который представляет собой нуклеотид, полученный из никотинамида и рибозы. Он известен как биохимический предшественник NAD+ (никотинамидадениндинуклеотид).
[0021]
Никотинамид рибозид (NR) представляет собой соединение со следующей структурой
[Химическая формула 2]
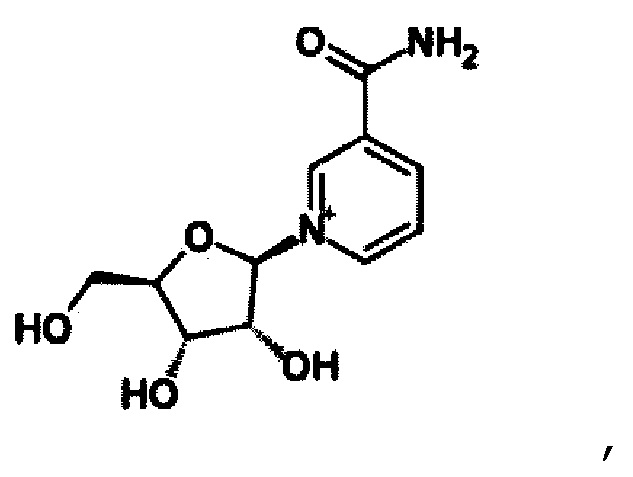
который представляет собой конъюгат рибозы и никотинамида. Это можно рассматривать как NMN с заменой нуклеотида на рибозу.
[0022]
Настоящее изобретение может обеспечить композицию, содержащую NMN и/или NR, или способ, включающий применение (например, введение) NMN и/или NR. NMN и/или NR можно использовать в виде их производных и/или их фармацевтически приемлемых солей. Приведенные в настоящем документе примеры показывают, что NMN и NR могут улучшать ферментативную активность Hsd3b6 (или ферментативную активность его гомолога, такого как HSD3B1). Приведенные в настоящем документе примеры также показывают, что NMN и NR могут восстанавливать ткань мейбомиевых желез. В одном варианте осуществления композиция может содержать NMN. В одном варианте осуществления, композиция может содержать NR.
[0023]
NMN и/или NR можно использовать в сочетании с дополнительным активным ингредиентом. Примеры дополнительного активного ингредиента включают, но не ограничиваются ими, противовоспалительное средство, противомикробное лекарственное средство, пищевую добавку, антиоксидант и т.п.
[0024]
(Заболевание)
Настоящее изобретение может обеспечить композицию для применения или способ улучшения активности Hsd3b6 или его гомолога с NMN и NR. Hsd3b6 напрямую контролируется циркадными часами, и продукт этого гена является важным элементом пути выработки альдостерона. Кроме того, может быть предоставлена композиция для применения или способ для лечения или профилактики заболевания, расстройства или симптома, связанного с активностью Hsd3b6 или его гомолога. Примеры заболевания, связанного с активностью Hsd3b6 или его гомолога, включают, но не ограничиваются ими, дисфункцию мейбомиевых желез, заболевания, вызванные снижением уровня стероидного гормона (например, тестостерона, эстрогена и тому подобное), постменопаузальный синдром, остеопороз, заболевания образа жизни, возрастной андрогенный дефицит у мужчин, инфаркт миокарда, и тому подобное.
[0025]
В частности, настоящее изобретение может обеспечить композицию для применения или способ для улучшения функции мейбомиевой железы с NMN и NR. Мейбомиевая железа представляет собой одну из сальных желез, расположенных на краю века. Мейбомиевые железы предотвращают испарение слезной пленки глаза, предотвращают попадание слез на щеку и выделяют маслянистое вещество (секрет сальных желез), которое закрывает внутреннюю часть закрытого века. Мейбомиева железа также известна как предплюсневая железа. Дисфункция мейбомиевой железы (MGD) определяется как сопровождающаяся хроническим дискомфортом в глазах при наличии диффузных нарушений в их функции. Причиной этого считается денатурация или застой мейбомиевых липидов, хроническая инфекция или гиперкератоз воспаленного эпителия протоков. Примеры по настоящему изобретению демонстрируют, что NMN и NR могут восстанавливать активность Hsd3b6 в мейбомиевой железе и могут увеличивать размер мейбомиевой железы. Примеры улучшения функции мейбомиевой железы включают увеличение количества ацинарных клеток мейбомиевой железы, увеличение секреции липидов мейбомиевой железой и лечение или профилактику заболевания, сопровождающегося дисфункцией мейбомиевой железы.
[0026]
Один вариант осуществления настоящего изобретения может обеспечить композицию для применения для или способ для лечения или профилактики заболевания, сопровождающегося дисфункцией мейбомиевой железы, с NMN и NR. Например, может быть предоставлена композиция для лечения или профилактики дисфункции мейбомиевых желез, содержащая никотинамид мононуклеотид (NMN) и/или никотинамид рибозид (NR). Дисфункция мейбомиевых желез может сопровождаться снижением секрецией мейбомиевых желез. Дисфункции мейбомиевых желез может сопровождаться воспалительным заболеванием. Воспалительное заболевание представляет собой, например, по меньшей мере одно заболевание, выбранное из группы, состоящей из мейбомита, поверхностного (точечного) кератита и блефарита. Дисфункция мейбомиевых желез может сопровождаться избыточным накоплением липидов в протоке. Дисфункция мейбомиевых желез может сопровождаться дискомфортом в глазах, ощущением инородного тела и/или ощущением давления. Например, заболевание, сопровождающееся дисфункцией мейбомиевых желез, может быть, но не ограничивается этим, заболеванием, выбранным из группы, состоящей из мейбомита, заднего блефарита, кератита, конъюнктивита, кератоконъюнктивита, связанного с мейбомитом, нарушения зрительной функции, андрогенной недостаточности, атопического дерматита, гиперплазии предстательной железы, глазного пемфигоида, дискоидной красной волчанки (эритематоз), синдрома эктодермальной дисплазии (ангидротическая эктодермальная дисплазия), трансплантации костного мозга, гипертензии, менопаузу, болезни Паркинсона, бляшечного псориаза, розацеа, синдрома Шегрена, синдрома Стивенса-Джонсона, токсического эпидермального некролиза, синдрома Тернера, реакции «трансплантат против хозяина» (РТПХ) и побочных эффектов, связанных с лекарственной терапией (ретиноиды, антиандрогены, антидепрессанты, антигистаминные препараты или постменопаузальная терапия эстрогенами). Понятно, что композиция по настоящему изобретению может улучшать саму функцию мейбомиевой железы, так что композицию можно эффективно применять при любом из заболеваний, описанных выше.
[0027]
Другой вариант осуществления настоящего изобретения может обеспечить композицию для применения для или способ для нормализации состава липидов, секретируемых мейбомиевой железой, и нормализации липидов в мейбомиевой железе. Поскольку композиция по настоящему изобретению демонстрирует эффект улучшения атрофии ткани мейбомиевой железы и повышает активность синтазы стероида, который воздействует на липид, секретируемый мейбомиевой железой, понятно, что композиция способствует нормализации липидов в мейбомиевой железе. Способ измерения липидного компонента в мейбомиевой железе особо не ограничен. Можно использовать различные способы, которые хорошо известны в данной области, при условии, что способ позволяет оценить липидный компонент в мейбомиевой железе.
[0028]
В одном варианте осуществления настоящего изобретения композиция согласно настоящему изобретению повышает ферментативную активность Hsd3b6. Таким образом, может быть повышена выработка тестостерона, который, как известно, способствует выработке липидов мейбомиевой железой. Поскольку половые гормоны, такие как тестостерон, влияют на выработку липидов в мейбомиевых железах, понятно, что композиция по настоящему изобретению способствует нормализации компонентный состав липидов в ткани мейбомиевых желез путем стимуляции выработки половых гормонов, включая тестостерон, посредством повышения ферментативной активности Hsd3b6.
[0029]
(Лекарственная форма)
Композицию по настоящему изобретению можно получить в виде подходящей лекарственной формы. Например, композиция по настоящему изобретению при использовании в качестве офтальмологической композиции может быть представлена в виде глазной инъекции, глазной мази, глазных капель или офтальмологического перфузата. Композиция может быть получена в любой лекарственной форме, такой как аэрозоль, жидкое средство, экстракт, эликсир, капсула, гранула, пилюля, мазь, порошок, таблетка, раствор, суспензия или эмульсия. Композиция может включать любую фармацевтически приемлемую добавку и/или эксципиент, которые известны в данной области. Примеры добавок включают, но не ограничиваются ими, средство для регулирования тоничности, буфер, консервант, сорастворитель и загуститель. Например, офтальмологическая композиция может быть представлена в виде жидкого средства, полученного путем растворения активного ингредиента в водном растворителе (например, в воде).
[0030]
Композицию по настоящему изобретению можно вводить любым подходящим путем, определенным специалистом в данной области. Композицию можно составить таким образом, чтобы она подходила для введения путем введения, выбранным из, но не ограничиваясь этим, глазной инъекции, местного применения (включая нанесение на глаз), глазные капли, внутривенной инъекции, внутривенного капельного введения, перорального введения, парентерального введения, трансдермального введения и тому подобное.
[0031]
Примеры изотонизирующих агентов включают сахариды, такие как глюкоза, трегалоза, лактоза, фруктоза, маннит, ксилит и сорбит, многоатомные спирты, такие как глицерин, полиэтиленгликоль и пропиленгликоль, неорганические соли, такие как хлорид натрия, хлорид калия и хлорид кальция, и тому подобное. Его количество предпочтительно составляет 0-5% масс. по отношению к общему количеству композиции.
[0032]
Примеры хелатирующих агентов включают эдентаты, такие как эдетат динатрия, натрия кальция эдетат, эдетат тринатрия, эдетат тетранатрия и эдетат кальция, этилендиаминтетраацетат, нитрилотриуксусная кислота или ее соль, гексаметафосфат натрия, лимонная кислота и тому подобное. Его количество предпочтительно составляет 0-0,2% масс. по отношению к общему количеству композиции.
[0033]
Примеры стабилизаторов включают гидросульфит натрия и тому подобное. Его количество предпочтительно составляет 0-1% масс. по отношению к общему количеству композиции.
[0034]
Примеры модификаторов рН включают кислоты, такие как хлористоводродная кислота, угольная кислота, уксусная кислота и лимонная кислота, а также гидроксиды щелочных металлов, такие как гидроксид натрия и гидроксид калия, карбонаты или бикарбонаты щелочных металлов, такие как карбонат натрия, ацетат щелочного металла, такие как ацетат натрия, цитрат щелочного металла, такой как цитрат натрия, основания, такие как трометамол и тому подобное. Его количество предпочтительно составляет 0-20% масс. по отношению к общему количеству композиции.
[0035]
Примеры консервантов включают сорбиновую кислоту, сорбат калия, сложные эфиры парагидроксибензоата, такие как метилпарагидроксибензоат, этилпарагидроксибензоат, пропилпарагидроксибензоат и бутилпарагидроксибензоат, соли четвертичного аммония, такие как хлоргексидин глюконат, хлорид бензалкония, хлорид бензетония и хлорид цетилпиридиния, алкилполиаминоэтилглицин, хлорбутанол, поликвад, полигексаметиленбигуанид, хлоргексидин и тому подобное. Его количество предпочтительно составляет 0-0,2% масс. по отношению к общему количеству композиции.
[0036]
Примеры антиоксидантов включают гидросульфит натрия, высушенный сульфит натрия, пиросульфит натрия, концентрированный смешанный токоферол и тому подобное. Его количество предпочтительно составляет 0-0,4% масс. по отношению к общему количеству композиции.
[0037]
Примеры солюбилизирующих агентов включают бензоат натрия, глицерин, D-сорбит, глюкозу, пропиленгликоль, гидроксипропилметилцеллюлозу, поливинилпирролидон, макрогол, D-маннит и тому подобное. Его количество предпочтительно составляет 0-3% масс. по отношению к общему количеству композиции.
[0038]
Примеры загустителей включают полиэтиленгликоль, метилцеллюлозу, этилцеллюлозу, кармеллозу натрия, ксантановую камедь, хондроитинсульфат натрия, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон, поливиниловый спирт и тому подобное. Его количество желательно составляет 0-70% масс. по отношению к общему количеству композиции.
[0039]
Глазные капли можно получить, например, путем растворения или суспендирования желаемого компонента, описанного выше, в водном растворителе, таком как стерильная очищенная вода, физиологический раствор или буфер (например, боратный буфер, фосфатный буфер и тому подобное), или неводном растворителе, таком как растительное масло, такое как хлопковое масло, соевое масло, кунжутное масло или арахисовое масло, регулирования осмотического давления до заданного осмотического давления и применения стерилизации, такой как механическая стерилизация.
[0040]
Офтальмологическая мазь может включать основу мази в дополнение к различным компонентам, описанным выше при получении. Примеры основы мази включают, но не ограничиваются ими, масляные основы, такие как вазелин, жидкий парафин и полиэтилен, эмульсионные основы, полученные путем эмульгирования масляной фазы и водной фазы с поверхностно-активным веществом или тому подобное, водорастворимые основы, состоящие из из гидроксипропилметилцеллюлозы, карбоксиметилцеллюлозы, полиэтиленгликоля и тому подобное.
[0041]
Композиция, терапевтическое средство или профилактическое средство по настоящему изобретению могут быть предоставлены в виде набора. В конкретном варианте осуществления настоящее изобретение обеспечивает упаковку лекарственного средства или набор, содержащий один или несколько контейнеров, заполненных одним или несколькими компонентами композиции или лекарственного средства по настоящемую изобретению. Необязательно, на такие контейнеры может быть нанесена информация, указывающая на разрешение производства, использования или продажи человеку государственным органом, регулирующим производство, использование или продажу лекарств, или биологических продуктов, в форме, установленной государственным органом.
[0042]
Используемый в настоящем документе термин «набор» относится к упаковке, содержащей предоставленные части (например, терапевтическое лекарственное средство, профилактическое лекарственное средство, каждый его компонент, руководство пользователя и тому подобное), которая обычно разделена на два или несколько сегментов. Такая форма набора предпочтительна при предоставлении композиции, которая не должна предоставляться в смешанном состоянии для стабильности или т.п. и предпочтительно используется путем смешивания непосредственно перед применением. Такой набор предпочтительно содержит инструкцию или руководство для пользователя, описывающее, как используются предоставленные части (например, терапевтическое лекарственное средство или профилактическое лекарственное средство) или как следует обрабатывать реагенты. Когда набор по настоящему документу используется в качестве набора реагентов, набор обычно содержит инструкцию или тому подобное, описывающую способ применения терапевтического средства, профилактического средства или тому подобного.
[0043]
Используемый в настоящем документе термин «инструкция» представляет собой документ с пояснением способа использования настоящего изобретения для врачей или других пользователей. Инструкция содержит описание способа обнаружения по настоящему изобретению, как использовать диагностическое препарат, или инструкцию по введению лекарственного средства и тому подобное. В инструкции может быть описание введения в глаз в качестве места введения (например, путем закапывания глазных капель, глазной мази, инъекции и тому подобное). Инструкция подготовлена в соответствии с форматом, установленным регулирующим органом страны, в которой применяется настоящее раскрытие (например, Ministry of Health, Labour and Welfare в Японии, Food and Drug Administration (FDA) в США или тому подобное), с четким описанием, подтверждающим одобрение регулирующего органа. Инструкция представляет собой так называемый вкладыш. Инструкции обычно предоставляют на бумажных носителях, но не ограничиваются ими. Инструкция также может быть предоставлена в такой форме, как электронные носители (например, веб-сайты в Интернете или высланные в электронном виде).
[0044]
В одном варианте осуществления могут быть предложены глазные капли, содержащие никотинамид мононуклеотид (NMN), где никотинамид мононуклеотид (NMN) содержится в концентрации 0,001 мкг/мл или выше, 0,01 мкг/мл или выше, 0,1 мкг/мл или выше, 1 мкг/мл или выше, 10 мкг/мл или выше, 100 мкг/мл или выше, 200 мкг/мл или выше, 500 мкг/мл или выше, 1 мг/мл или выше, 2 мг/мл или выше, 5 мг/мл или выше, 10 мг/мл или выше, или 50 мг/мл или выше.
[0045]
В одном варианте осуществления могут быть предложены глазные капли, содержащие никотинамид рибозид (NR), где никотинамид рибозид (NR) содержится в концентрации 0,001 мкг/мл или выше, 0,01 мкг/мл или выше, 0,1 мкг/мл или выше, 1 мкг/мл или выше, 10 мкг/мл или выше, 100 мкг/мл или выше, 200 мкг/мл или выше, 500 мкг/мл или выше, 1 мг/мл или выше, 2 мг/мл или выше, 5 мг/мл или выше, 10 мг/мл или выше, или 50 мг/мл или выше.
[0046]
В одном варианте осуществления может быть предложена глазная мазь, содержащая никотинамид мононуклеотид (NMN), где никотинамид мононуклеотид (NMN) содержится в концентрации 0,001 мкг/мл или выше, 0,01 мкг/мл или выше, 0,1 мкг/мл или выше, 1 мкг/мл или выше, 2 мкг/мл или выше, 5 мкг/мл или выше, 10 мкг/мл или выше, 50 мкг/мл или выше, 100 мкг/мл или выше, 200 мкг/мл или выше, или 500 мкг/мл или выше.
[0047]
В одном варианте осуществления может быть предложена глазная мазь, содержащая никотинамид рибозид (NR), где никотинамид рибозид (NR) содержится в концентрации 0,001 мкг/мл или выше, 0,01 мкг/мл или выше, 0,1 мкг/мл или выше, 1 мкг/мл или выше, 2 мкг/мл или выше, 5 мкг/мл или выше, 10 мкг/мл или выше, 50 мкг/мл или выше, 100 мкг/мл или выше, 200 мкг/мл или выше, или 500 мкг/мл или выше.
[0048]
Применение состава с концентрацией в заранее определенном количестве или выше в соответствии с лекарственной формой может быть полезным для доставки в мейбомиеву железу, которая находится на задней части века, в отличие от доставки на глазное яблоко.
[0049]
(Доза)
В одном варианте осуществления, способы применения по настоящему изобретению включают, например, глазные капли, но способы не ограничиваются этим. Их примеры включают способы введения (способы введения и лекарственные формы), такие как глазная мазь, инъекция в переднюю камеру, импрегнация средства с замедленным высвобождением, субконъюнктивальная инъекция и системное введение (пероральное введение и внутривенная инъекция).
[0050]
Концентрация NMN или NR, используемых в настоящем изобретении, обычно составляет примерно 0,001-1000 мкМ (мкмоль/л), предпочтительно примерно 0,01-300 мкМ, более предпочтительно примерно 0,03-100 мкМ и еще более предпочтительно от примерно 0,1 до примерно 30 мкМ. Например, другие диапазоны концентраций обычно составляют от 0,01 нМ до 100 мкМ, примерно от 0,1 нМ до 100 мкМ, примерно 0,001-100 мкМ, примерно от 0,01-75 мкМ, примерно 0,05-50 мкМ, примерно 1-10 мкМ, примерно 0,01-10 мкМ, примерно 0,05-10 мкМ, примерно 0,075-10 мкМ, примерно 0,1-10 мкМ, примерно 0,5-10 мкМ, примерно 0,75-10 мкМ, примерно 1,0-10 мкМ, примерно 1,25-10 мкМ, примерно 1,5-10 мкМ, примерно 1,75-10 мкМ, примерно 2,0-10 мкМ, примерно 2,5-10 мкМ, примерно 3,0-10 мкМ, примерно 4,0-10 мкМ, примерно 5,0-10 мкМ, примерно 6,0-10 мкМ, примерно 7,0-10 мкМ, примерно 8,0-10 мкМ, примерно 9,0-10 мкМ, примерно 0,01-50 мкМ, примерно 0,05-5,0 мкМ, примерно 0,075-5,0 мкМ, примерно 0,1-5,0 мкМ, примерно 0,5-5,0 мкМ, примерно 0,75-5,0 мкМ, примерно 1,0-5,0 мкМ, примерно 1,25-5,0 мкМ, примерно 1,5-5,0 мкМ, примерно 1,75-5,0 мкМ, примерно 2,0-5,0 мкМ, примерно 2,5-5,0 мкМ, примерно 3,0-5,0 мкМ, примерно 4,0-5,0 мкМ, примерно 0,01-3,0 мкМ, примерно 0,05-3,0 мкМ, примерно 0,075-3,0 мкМ, примерно 0,1-3,0 мкМ, примерно 0,5-3,0 мкМ, примерно 0,75-3,0 мкМ, примерно 1,0-3,0 мкМ, примерно 1,25-3,0 мкМ, примерно 1,5-3,0 мкМ, примерно 1,75-3,0 мкМ, примерно 2,0-3,0 мкМ, примерно 0,01-1,0 мкМ, примерно 0,05-1,0 мкМ, примерно 0,075-1,0 мкМ, примерно 0,1-1,0 мкМ, примерно 0,5-1,0 мкМ, примерно 0,75-1,0 мкМ, примерно 0,09-35 мкМ, или примерно 0,09-3,2 мкМ, более предпочтительно примерно 0,01-10 мкМ, примерно 0,1-3 мкМ, или примерно 0,1-1,0 мкМ, но диапазон концентраций не ограничивается этим.
[0051]
При использовании в виде глазных капель концентрацию состава можно определить на основе примерно 1-10000-кратного, предпочтительно примерно 100-10000-кратного, например, примерно 1000-кратного значения эффективной концентрации, описанной выше, с учетом разбавления слезной жидкостью и тому подобное, а также токсичности. Концентрация также может быть установлена на концентрацию, превышающую указанную. Концентрация составляет, например, примерно от 0,01 мкМ (мкмоль/л) до 1000 мМ (ммоль/л), от 0,03 мкМ до 1000 мМ, примерно от 0,1 мкМ до 300 мМ, примерно от 0.3 мкМ до 300 мМ, примерно от 1 мкМ до 100 мМ, примерно от 3 мкМ до 100 мМ, примерно от 10 мкМ до 100 мМ, примерно от 30 мкМ до 100 мМ, примерно от 0.1 мкМ до 30 мМ, примерно от 0.3 мкМ до 30 мМ, примерно от 1 мкМ до 30 мМ, примерно от 3 мкМ до 30 мМ, примерно от 1 мкМ до 10 мМ, примерно от 3 мкМ до 10 мМ, примерно от 10 мкМ до 1 мМ, примерно от 30 мкМ до 1 мМ, примерно от 10 мкМ до 10 мМ, примерно от 30 мкМ до 10 мМ, примерно от 100 мкМ до 10 мМ, примерно от 300 мкМ до 10 мМ, примерно от 10 мкМ до 100 мМ, примерно от 30 мкМ до 300 мМ, примерно от 100 мкМ до 300 мМ, или примерно от 300 мкМ до 300 мМ, и может составлять примерно от 1 мМ до 10 мМ или примерно от 1 мМ до 100 мМ. Диапазон концентраций может быть определен путем соответствующего сочетания этих верхних и нижних пределов.
[0052]
Величина эффекта лекарственного средства по настоящему изобретению, которое эффективно при лечении конкретного заболевания, расстройства или состояния, может варьироваться в зависимости от свойств расстройства или состояния, но может быть определено с помощью стандартной клинической методики, основанной на описаниях, приведенных в настоящем документе специалистами в данной области. Кроме того, определение оптимального диапазона доз может быть дополнительно облегчено с помощью анализа in vitro. Поскольку точная доза, используемая в соединении, может варьироваться в зависимости от пути введения или тяжести заболевания, или расстройства, дозу следует определять в соответствии с заключением врача или состоянием каждого пациента. Доза конкретно не ограничена, но может составлять, например, 0,001, 1, 5, 10, 15, 100 или 1000 мг/кг массы тела на введение или в пределах двух таких значений. Интервал дозирования конкретно не ограничен, но может составлять, например, 1, 2 или 4 дозы каждые 1, 7, 14, 21 или 28 дней или 1, 2 или 4 дозы на каждое количество дней в течение диапазона между любыми двумя из таких значений. Доза, количество доз, интервал введения доз, период введения доз и способ введения доз могут быть надлежащим образом выбраны в зависимости от возраста или массы тела пациента, симптома, способа введения, органа-мишени или тому подобное. Например, композицию по настоящему изобретению можно использовать в виде глазных капель. Кроме того, терапевтическое лекарственное средство предпочтительно содержит активный ингредиент в терапевтически эффективном количестве или в количестве, эффективном для оказания желаемого действия. Эффективную дозу можно оценить по кривой доза-эффект, полученной в тест-системе in vitro или на модели на животных.
[0053]
Введение активного ингредиента в заранее определенном более высоком количестве может быть предпочтительным для доставки в мейбомиеву железу, которая находится в задней части века, в отличие от доставки на глазное яблоко.
[0054]
(Терапевтический метод и профилактический метод)
Настоящее изобретение может обеспечить способ улучшения активности Hsd3b6 или его гомолога, или лечения или профилактики заболевания, расстройства или симптома, связанного с активностью Hsd3b6 или его гомолога. Способ может включать введение никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR) субъекту.
[0055]
Способ может необязательно включать измерение активности Hsd3b6 или его гомолога у субъекта. Один вариант осуществления может обеспечивать способ введения NMN и/или NR, когда активность Hsd3b6 или его гомолога у субъекта измеряют и активность снижена.
[0056]
Настоящее изобретение может обеспечить способ улучшения функции мейбомиевой железы или лечения, или предотвращения заболевания, расстройства или симптома, сопровождающегося дисфункцией мейбомиевых желез. Способ может включать введение никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR) субъекту.
[0057]
Настоящее изобретение может обеспечить способ усиления выработки тестостерона в мейбомиевой железе. Способ может включать введение никотинамид мононуклеотида (NMN) и/или никотинамид рибозида (NR) субъекту.
[0058]
Способ может необязательно включать исследование функции мейбомиевых желез субъекта. Один вариант осуществления может обеспечить способ введения NMN и/или NR, когда функцию мейбомиевой железы субъекта проверяют и функция снижена. Функцию мейбомиевой железы можно проверить, например, с помощью осмотра глаза с помощью щелевой лампы, мейбографии, конфокальной микроскопии, DR-1, кожно-слизистого соединения, мейбометра, химического анализа липидов, количества испарений, BUT или опросника субъективных симптомов.
[0059]
(Общая технология)
Молекулярно-биологический метод, биохимический метод и микробиологический метод, используемые в настоящем документе, хорошо известны и обычно используются в данной области, которые описаны, например, в Sambrook J. et al. (1989). Molecular Cloning: A Laboratory Manual, Cold Spring Harbor and its 3rd Ed. (2001); Ausubel, F. M. (1987). Current Protocols in Molecular Biology, Greene Pub. Associates and Wiley-Interscience; Ausubel, F. M. (1989). Short Protocols in Molecular Biology: A Compendium of Methods from Current Protocols in Molecular Biology, Greene Pub. Associates and Wiley-Interscience; Innis, M. A. (1990). PCR Protocols: A Guide to Methods and Applications, Academic Press; Ausubel, F. M. (1992). Short Protocols in Molecular Biology: A Compendium of Methods from Current Protocols in Molecular Biology, Greene Pub. Associates; Ausubel, F. M. (1995). Short Protocols in Molecular Biology: A Compendium of Methods from Current Protocols in Molecular Biology, Greene Pub. Associates; Innis, M. A. et al. (1995). PCR Strategies, Academic Press; Ausubel, F. M. (1999). Short Protocols in Molecular Biology: A Compendium of Methods from Current Protocols in Molecular Biology, Wiley, and annual updates; Sninsky, J. J. et al. (1999). PCR Applications: Protocols for Functional Genomics, Academic Press, Gait, M. J. (1985). Oligonucleotide Synthesis: A Practical Approach, IRL Press; Gait, M. J. (1990). Oligonucleotide Synthesis: A Practical Approach, IRL Press; Eckstein, F. (1991). Oligonucleotides and Analogues: A Practical Approach, IRL Press; Adams, R. L. et al. (1992). The Biochemistry of the Nucleic Acids, Chapman & Hall; Shabarova, Z. et al. (1994). Advanced Organic Chemistry of Nucleic Acids, Weinheim; Blackburn, G. M. et al. (1996). Nucleic Acids in Chemistry and Biology, Oxford University Press; Hermanson, G. T. (I996). Bioconjugate Techniques, Academic Press, Bessatsu Jikken Igaku [Experimental Medicine, Supplemental Volume], "Idenshi Donyu & Hatsugen Kaiseki Jikken Ho [Experimental Methods for Transgenesis & Expression Analysis]", Yodosha, 1997, или тому подобное. Их релевантные части (которые могут представлять собой весь документ) включены в настоящий документ посредством ссылки.
[0060]
Справочная литература, такая как научная литература, патенты и заявки на патенты, цитируемые в настоящем документе, включены в настоящий документ посредством ссылки в той же степени, как если бы каждый документ был подробно описан.
[0061]
Настоящее изобретение было описано с указанием предпочтительных вариантов осуществления для облегчения понимания. Хотя настоящее изобретение описано далее на основе примеров, приведенные выше описания и следующие примеры предоставлены исключительно с целью иллюстрации, а не ограничения настоящего изобретения. Таким образом, объем настоящего изобретения не ограничивается вариантами осуществления и примерами, которые конкретно описаны в настоящем документе, и ограничивается только объемом формулы изобретения.
[Примеры]
[0062]
Примеры настоящего изобретения описаны ниже. С биологическими образцами или тому подобное, где это применимо, обращались в соответствии со стандартами, принятыми Ministry of Health, Labour and Welfare, Ministry of Education, Culture, Sports, Science and Technology, или тому подобное, и, где применимо, на основании Хельсинской Декларации или этических принципов, подготовленных на ее основе.
[0063]
(Пример 1: Атрофия ткани мейбомиевой железы, связанная со старением/ткань мейбомиевой железы у мышей Hsd3b6 KO)
[Краткое описание]
Этот пример демонстрирует атрофию ткани мейбомиевых желез, связанную со старением, и изменение ткани мейбомиевых желез у мышей Hsd3b6 KO.
[0064]
[Материалы и методы]
(1) Протокол окрашивания целых мейбомиевых желез по Герксгеймеру
Ткань мейбомиевых желез мышей окрашивали в соответствии со следующим протоколом.
[0065]
В качестве способа получения 100 мл окрашивающего раствора, сосуд с исходным раствором, полученным путем растворения Судана IV до насыщения в 100% этаноле, заранее оставляли стоять, и 70 мл такого же количества супернатанта, 20 мл 10% NaOH, и 10 мл сверхчистой воды смешивали, перемешивали переворачиванием в течение 5 минут и центрифугировали для осаждения порошка. Супернатант фильтровали через фильтр 0,45 мкм и использовали в качестве окрашивающего раствора.
[0066]
У мышей сворачивали шейные позвонки и брали образцы кожи головы, включая мейбомиевые железы. Образец погружали в 4% параформальдегид, сохраняя образец плоским с помощью канцелярской кнопки, и иммобилизировали с помощью ротатора при 4°C в течение 24 часов. Периферию мейбомиевых желез обрезали. Мейбомиевы железы погружали в 50% этанол с помощью ротатора при комнатной температуре на 10 минут, затем погружали на 20 минут в 70% этанол и погружали в окрашивающий раствор с помощью ротатора при комнатной температуре на 24 часа в пробирке Falcon. Затем мейбомиевые железы погружали на 10 минут в 70% этанол и несколько раз повторяли промывание, чтобы подтвердить, что мейбомиевые железы хорошо окрасились. Мейбомиевые железы погружали на 24 часа в аминоспирт в глицерине, полученный путем смешивания 3,75 мл 80% аминоспирта с 8,25 мл глицерина. Мейбомиевые железы помещали на предметное стекло и инкапсулировали глицериновым желе. Глицериновое желе получали путем предварительного смешивания 10 г желатина с 60 мл сверхчистой воды и 70 мл глицерина, набухания желатина и добавления глицерина примерно через час и смешивания при нагревании.
[0067]
(2) Анализ площади мейбомиевой железы, окрашенной Суданом IV
Анализ площади после окрашивания осуществляли с использованием Photoshop и ImageJ и определением порогового значения интенсивности цвета при просмотре и сравнении с изображением пятна на основе площади участков с интенсивностью, равной или превышающей заданное пороговое значение.
[0068]
(3) Мышь
Получали мышь, фланкированную loxPу, у которой область экзона 2, включающая инициирующий кодон гена Hsd3b6 мыши, фланкирована loxP-сайтами. Мышь скрещивали с трансгенной мышью CAG-Cre для получения мыши Hsd3b6 KO, которая больше не могла экспрессировать Hsd3b6.
[0069]
Тест проводили после выращивания двухмесячной мыши в течение 10 дней в нормальных условиях (условия нормальной влажности) на условиях свободного доступа к пище/воде при цикле 12 часов свет и 12 часов темнота при влажности от 40 до 60% и комнатной температуре 25°С.
[0070]
24-месячная мышь представляла собой 78-недельного (18-месячного) самца мыши C57BL/6J, приобретенного у OrientalBioService, Inc., которого выращивали в течение 6 месяцев в нормальных условиях (условия нормальной влажности). 6-месячная мышь C57BL/6J представляла собой 6-недельную мышь, приобретенную и выращенную до 6-месячного возраста в нормальных условиях (условия нормальной влажности).
[0071]
[Результаты]
Ткань мейбомиевой железы окрашивали у 6-месячной мыши и 24-месячной мыши в соответствии с протоколом, описанным выше, и сравнивали окрашенные области. Результаты представлены на фиг. 1. Наблюдалаи атрофию ткани мейбомиевых желез и прогрессирование дисфункции мейбомиевых желез (MGD) в связи со старением (N=7).
[0072]
На фиг. 2 показан размер ткани мейбомиевой железы и количество секреторных протоков у 2-месячной мыши Hsd3b6 KO и мыши дикого типа. Как и у престарелых мышей, у мышей Hsd3b6 KO также была обнаружена атрофия мейбомиевой железы. Поскольку различий в количестве секреторных протоков в зависимости от генотипа нет, было установлено, что атрофия мейбомиевой железы не является аномалией в процессе образования протоков.
[0073]
(Пример 2: Эксперимент по инстилляции глазных капель NMN или NR 1,5-летней мыши дикого типа в течение 2 недель)
[Краткое описание]
Этот пример демонстрирует изменение ферментативной активности Hsd3b6 и пролиферативной активности базальных ацинарных клеток мейбомиевой железы в мейбомиевых железах вследствие инстилляции глазных капель NMN или NR в течение 2 недель 1,5-летним мышам дикого типа.
[0074]
[Материалы и методы]
(1) Ниже приводится краткое изложение эксперимента по инстилляции глазных капель.
[Таблица 1]
[0075]
(2) Измерение ферментативной активности Hsd3b6 мейбомиевой железы
Ферментативную активность Hsd3b6 мейбомиевой железы у мышей измеряли в соответствии со следующим протоколом.
[0076]
○Предварительная подготовка
Сбалансированный солевой раствор Хэнкса (HBSS) барботировали смесью 95% CO2/5% O2 в течение 1 часа или более и распределяли по 2 мл пробиркам по 200 мкл каждая. Крышку закрывали при заполнении 95% CO2/5% O2. HBSS нагревали на водяной бане при 37°C. Реакционный инкубатор нагревали до 37°C, и устанавливали в нем мультивортекс.
[0077]
○Запуск измерительного оборудования
Включали основное питание проточного жидкостного сцинтилляционного счетчика (Perkin Elmer, Radiomatic 625TR) и и включали основное питание ВЭЖХ (Waters, 2795 Separations Module) для выполнения настройки. Подвижную фазу А заменили водой, и подвижную фазу В заменили ацетонитрилом. После установки колонки (Kanto Chemical, LiChroCART 250-4, LiChrosphere 100RP-18, размер частиц: 5 мкм, внутренний диаметр 4 мм × 250 мм) пропускали 40% ацетонитрила (ACN) (A: 60%, B: 40%) со скоростью 0,7 мл/мин. Температуру термостата колонки в это время устанавливали на 40°C.
[0078]
○Очистка 3H-прегненолона
3H-DHEA добавляли к 1 мл 40% ACN, содержащемуся в пробирке 2 мл, и сливали смесь. Микропробирку устанавливали на держателе для ВЭЖХ и выбирали однократное введение. Пик загрязнителя, образовавшийся через 22 минуты, не собирали. Как только пик загрязняющего вещества уменьшился примерно через 23 минуты, затем проявился пик 3H-DHEA, так что сбор в стеклянную центрифужную пробирку начинали после достижения 1/3 имп./мин значения пика. Всего за 4 минуты сбора собрали примерно 2,5 мл. Жидкость внутри стеклянной центрифужной пробирки перемешивали вортексом. 25 мкл подвергали действию жидкостного сцинтилляционного счетчика и 25 мкл добавляли к 3 мл прозрачного золя. После подтверждения того, что небольшое количество N2 выходит из выпускного сопла, жидкость внутри стеклянной центрифужной пробирки высушивали азотом при 75°C с использованием инкубатора Taitec.
[0079]
○Получение субстрата
После охлаждения 3H-DHEA, высушенного азотом, до комнатной температуры, 1 мкл/4000 имп./мин (значение при измерении 25 мкл с помощью жидкостного сцинтилляционного счетчика) пропиленгликоля добавляли и 3H-DHEA растворяли встряхиванием в течение 5 минут.
[0080]
Добавляли PBS 4 мкл/4000 имп./мин. Смесь перемешивали на вортексе. 10 мкл измеряли на жидкостном сцинтилляционном счетчике, для подтверждения того, что количество превышает 400000 имп./мин. Смесь разбавляли смесью PBS:пропиленгликоль=4:1. 400000 имп./мин./10 мкл горячего раствора (1), 87 мкМ DHEA в 10% EtOH/90% D-PBS (2), 1 мМ дутастерида в 50% DMSO/50% DW (3) и 1 мМ фадрозола в 50% DMSO/50% DW (4) получали и смешивали в соотношении (1):(2):(3):(4)=5:5:1:1 в виде раствора субстрата. Перед использованием его нагревали на водяной бане с температурой 37°C.
[0081]
○Ферментативная реакция и экстракция
Вырезали мейбомиевую железу верхнего века одного из глаз и помещали на бумагу для взвешивания так, чтобы сторона, обнажающая мейбомиевую железу, находилась сверху. Образец измельчали до толщины 200 мкм с помощью измельчителя тканей. Нарезанную мейбомиевую железу переносили в HBSS. Раствор субстрата осторожно встряхивали и добавляли 24 мкл к HBSS. Смесь пипетировали.
[0082]
Смесь инкубировали в течение 30 минут при встряхивании миксером для микропробирок, установленным внутри инкубатора при 37°C. Через 30 минут смесь центрифугировали при комнатной температуре в течение 1 минуты при 700 g и давали ткани мейбомиевых желез осаждаться. Все количество HBSS переносили в пробирку, в которую добавляли 2 мл этилацетата. Смесь встряхивали в течение 10 секунд. Когда реакцию останавливали, смесь немедленно переносили на лед.
[0083]
200 мкл HBSS, подогретого до 37°C, добавляли в пробирку 2 мл с оставшейся в ней мейбомиевой железой. После осторожного встряхивания раствора субстрата, 24 мкл добавляли к HBSS и смесь пипетировали. Добавляли 2 мкл 100 мМ NAD+ в D-PBS. Смесь инкубировали в течение 30 минут при встряхивании миксером для микропробирок, установленным внутри инкубатора при 37°C. Смесь центрифугировали при комнатной температуре в течение 1 минуты при 700 g и давали ткани мейбомиевых желез осаждаться. Все количество HBSS переносили в пробирку, в которую добавляли 2 мл этилацетата. Смесь встряхивали в течение 10 секунд. Когда реакцию останавливали, смесь немедленно переносили на лед.
[0084]
○Экстракция стероидов
Смесь центрифугировали при комнатной температуре в течение 10 минут при 1500 об/мин. Собирали 1,6 мл слоя этилацетата на верхнем слое и высушивали азотом при 75°С. Когда жидкость полностью испарилась, добавляли 500 мкл 40% ACN. Смесь встряхивали в течение 3 минут. Жидкость переносили в MILLIPORE Ultra free-MC, установленный на пробирке 2 мл, и центрифугировали при комнатной температуре в течение 2 минут при 12000 g. Стеклянную центрифужную пробирку предварительно промывали 500 мкл 40% ACN и встряхивали в течение 2 минут. После прохождения через фильтр той же колонки смесь центрифугировали при комнатной температуре в течение 4 минут при 12000 g. Элюат перемешивали постукиванием и добавляли 10 мкл к 3 мл прозрачного золя. Смесь измеряли на жидкостном сцинтилляционном счетчике (измерение степень восстановления).
[0085]
○Измерение
Колонку уравновешивали в начальных условиях (до стабилизации базовой линии и давления). Наборы образцов были созданы в том же количестве, что и количество образцов, подлежащих измерению. Поскольку анализ в первой колонке не стабилизировался, в качестве образца использовали 40% ACN. Крышка пробирки 2 мл для измерения была открыта. Пробирку покрывали тонко растянутой парапленкой и готовили для ВЭЖХ. Начали непрерывный анализ.
Условия ВЭЖХ (3H-DHEA)
Скорость потока: 0,7 мл/мин
Температура колонки: 40°C
Градиент
0-30 мин: 40-50% ACN (0,3%/мин)
30-35 мин: 70% ACN
35-40 мин: 100% ACN
40-50 мин: 100-40% ACN (6%/мин)
50-60 мин: 40% ACN
[0086]
○Анализ
Хроматограф открывали с ProFSA. Сглаживание осуществляли путем установки уровня SDA (функция сглаживания) на 8. Пики отображали с помощью Find Peaks и Locate Peaks. Report Preview копировали и вставляли в Word. Данные получали для определения ферментативной активности по следующей формуле.
[Номер 1]
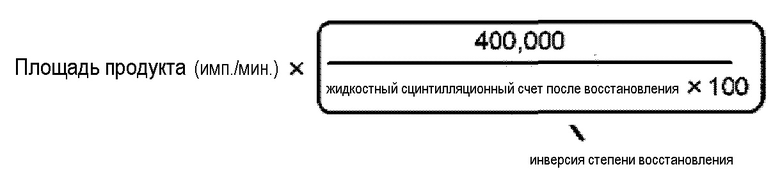
[0087]
(3) Анализ клеточной пролиферации посредством окрашивания включением BrdU
BrdU (100 мг/кг массы тела, Sigma-Aldrich) вводили внутрибрюшинно за 30 минут до забора ткани века мыши. Веко, содержащее мейбомиевые железы, иммобилизовали 4% PFA и заливали в парафин. Антигены активировали путем создания давления на сегмент толщиной 5 мкм в течение 2,5 минут в 10 мМ буфере цитрата натрия (pH 6,0). После инкубирования сегмента в течение 24 часов при 4°C с использованием анти-BrdU-антитела (разведение 1:1000; Rockland Inc.), иммунный ответ становился видимым с помощью 3,3'-диаминобензидина (DAB) с использованием вторичного антитела Envision+ System-HRP Labeled Polymer Anti-Rabbit (Dako). Для каждого сегмента ткани BrdU-положительные клетки в слое базальных клеток мейбомиевой железы подсчитывали на изображении, полученном с помощью цифрового микроскопа при 20˟ увеличении. Длину внешней окружности ацинуса мейбомиевой железы измеряли с помощью программного обеспечения ImageJ, а общее количество BrdU-положительных клеток нормализовали по длине внешней окружности. BrdU-положительные клетки подсчитывали, используя 16 сегментов на индивидуума.
[0088]
[Результаты]
На фиг. 3 показано изменение ферментативной активности Hsd3b6 в мейбомиевой железе и изменение количества BrdU-положительных клеток в базальных клетках мейбомиевой железы из-за инстилляции глазных капель NMN, NR или их растворителя (носитель, фосфатный буферный физиологический раствор). Ферментативная активность Hsd3b6 и количество BrdU-положительных клеток значительно увеличились благодаря инстилляции глазных капель NMN. Аналогичное увеличение ферментативной активности Hsd3b6 наблюдали, и количество BrdU-положительных клеток также значительно увеличилось в группе инстилляции глазных капель NR. В частности, можно понять, что ферментативная активность Hsd3b6 увеличивается местно в мейбомиевой железе, а пролиферативная активность базальных клеток мейбомиевой железы увеличивается из-за инстилляции глазных капель NMN или NR.
[0089]
(Пример 3: 3 месячный эксперимент по инстилляции глазных капель NMN или NR мышам дикого типа в возрасте 1,75 лет)
[Краткое описание]
Этот пример демонстрирует эффект инстилляции глазных капель NMN или NR в течение 3 месяцев 1,75-летней мыши дикого типа на объем ткани мейбомиевой железы.
[0090]
[Материалы и методы]
(1) Ниже приведена схема эксперимента по инстилляции глазных капель.
[Таблица 2]
глаз, 4 раза/
день)
[0091]
(2) Ткани мейбомиевых желез мыши окрашивали посредством окрашивания по Герксгеймеру всех мейбомиевых желез таким же образом, как и в примере 1.
[0092]
[Результаты]
На фиг. 4 показано изменение объема мейбомиевых желез при инстилляции глазных капель NMN, NR и их растворителя (носитель, фосфатный буферный физиологический раствор). Значительное увеличение объема мейбомиевой железы наблюдали как в группе инстилляции глазных капель NMN, так и в группе инстилляции глазных капель NR.
[0093]
(Пример 4: 3 месячный эксперимент по инстилляции глазных капель NMN или NR мышам дикого типа в возрасте 1,75 лет)
[Краткое описание]
Этот пример демонстрирует эффект 3-месячной инстилляции глазных капель NMN или NR 1,75-летней мыши дикого типа на липидные компоненты в мейбомиевых железах.
[0094]
[Материалы и методы]
(1) Эксперимент с инстилляцией глазных капель проводят так же, как в примере 3.
(2) Сбор липидов из мейбомиевых желез мыши и анализ липидов
Мейбомиевые железы извлекали из века усыпленной мыши. Каждую из двух мейбомиевых желез, взятых из одного глаза каждого животного, помещают в стеклянный флакон, содержащий 1 мл смеси растворителей хлороформ:метанол=2:1 (об./об.) для экстракции липидов, и экстрагируют липиды. Экстракт перемещают в новый флакон. Экстракт можно хранить в течение нескольких месяцев при -20°C или ниже путем выпаривания раствора в атмосфере азота. Затем экстракт растворяют в подходящем растворителе и анализируют липидный состав с помощью APCI.
[0095]
[Результаты]
Липидные компоненты в мейбомиевой железе нормализовали в группах инстилляции глазных капель NMN или NR по сравнению с контрольной группой инстилляции глазных капель с носителем (фосфатный буферный физиологический раствор).
[0096]
(Пример 5: Количественное определение тестостерона в мейбомиевой железе)
[Материалы и методы]
После гомогенизации мейбомиевой железы, вырезанной из века, смесью метанол/вода (75:25, об./об.), стероид, содержащийся в гомогенате, экстрагировали дихлорметаном с использованием картриджа Isolute SLE+ (Biotage) и выпаривали в атмосфере азота с получением остатка. Остаток растворяли в 50 мкл раствора метанола/5% уксусной кислоты, содержащего реагент Amplifex Keto (SCIEX) с концентрацией 10 мг/мл, и инкубировали в течение 1 часа при комнатной температуре. Концентрацию тестостерона затем определяли с помощью жидкостной хроматографии с тандемной масс-спектрометрией с электрораспылительной ионизацией (система QTRAP 4500 LC-MS/MS; SCIEX) (производный переход SRM: 403→164), и нормализовали по сырой массе извлеченной мейбомиевой железы.
[0097]
[Результаты]
На фиг. 5 показано количество тестостерона в ткани мейбомиевых желез мышей дикого типа и мышей с дефицитом Hsd3b6. Тестостерон, содержащийся местно в мейбомиевых железах, снизился примерно на 50% у мышей с дефицитом Hsd3b6 по сравнению с мышами дикого типа. Кроме того, тестостерон, обнаруженный местно в мейбомиевых железах, снизился до 10% или менее у нокаутной мыши по Hsd3b6 с резецированной гонадой (яичком). Отсюда можно понять, что не только циркулирующий тестостерон, поступающий из яичек, но также тот же уровень выработки тестостерона, что и в мейбомиевой железе, способствует мейбомиевым железам.
[0098]
Поскольку ферментативная активность Hsd3b6 повышается при инстилляции глазных капель NMN или NR, понятно, что повышается выработка тестостерона, который, как известно, способствует продукции липидов мейбомиевыми железами, и нормализуется компонентный состав липидов в ткани мейбомиевых желез.
[0099]
(Примечание)
Как описано выше, настоящее изобретение иллюстрируется использованием его предпочтительных вариантов осуществления. Однако следует понимать, что объем настоящего изобретения следует интерпретировать исключительно на основании формулы изобретения. Также подразумевается, что любой патент, любая патентная заявка и любые ссылки, цитируемые в настоящем документе, должны быть включены в настоящий документ в качестве ссылки таким же образом, как если бы содержания были непосредственно описаны в настоящем документе. Настоящая заявка испрашивает приоритет согласно заявке на патент Японии No. 2019-117642, поданной 25 июня 2019 г. в Патентное ведомство Японии. Полное содержание которой включено в настоящий документ посредством ссылки таким же образом, как если бы содержание было непосредственно описано в настоящем документе.
[Промышленная применимость]
[0100]
Настоящее изобретение может быть использовано в области медицины, фармацевтических продуктов, здравоохранения, биологии, биохимии и тому подобного.
Группа изобретений относится к области медицины и фармацевтики, а именно к применению никотинамида мононуклеотида (NMN) или никотинамида рибозида для (NR)получения лекарственного средства для улучшения функции мейбомиевой железы или для лечения или профилактики дисфункции мейбомиевой железы. Использование группы изобретений позволяет эффективно лечить дисфункции мейбомиевой железы. 4 н. и 18 з.п. ф-лы, 5 ил., 2 табл., 5 пр.
1. Применение никотинамида мононуклеотида (NMN) или никотинамида рибозида (NR) для улучшения функции мейбомиевой железы.
2. Применение по п. 1, где улучшение функции мейбомиевой железы включает увеличение количества ацинарных клеток мейбомиевой железы.
3. Применение по п. 1, где улучшение функции мейбомиевой железы включает увеличение секреции липидов мейбомиевой железой.
4. Применение по любому из пп. 1-3, где улучшение функции мейбомиевой железы включает лечение или профилактику заболевания, сопровождающегося дисфункцией мейбомиевой железы.
5. Применение никотинамида мононуклеотида (NMN) или никотинамида рибозида (NR) для лечения или профилактики дисфункции мейбомиевой железы.
6. Применение по п. 5, где дисфункция мейбомиевой железы сопровождается снижением секреции мейбомиевых желез.
7. Применение по п. 5, где дисфункция мейбомиевой железы сопровождается воспалительным заболеванием.
8. Применение по п. 7, где воспалительное заболевание включает по меньшей мере одно заболевание, выбранное из группы, состоящей из мейбомита, поверхностного (точечного) кератита и блефарита.
9. Применение по п. 5, где дисфункция мейбомиевой железы сопровождается избыточным накоплением липидов в протоке.
10. Применение по п. 5, где дисфункция мейбомиевой железы сопровождается дискомфортом в глазах, ощущением инородного тела и/или ощущением давления.
11. Применение по п. 4, где заболевание, сопровождающееся дисфункцией мейбомиевой железы, представляет собой мейбомит, задний блефарит, кератит, конъюнктивит, кератоконъюнктивит, связанный с мейбомитом, глазной пемфигоид, синдром Шегрена, синдром Стивенса-Джонсона, реакцию «трансплантат против хозяина» (РТПХ) и нарушение зрительной функции.
12. Применение никотинамида мононуклеотида (NMN) или никотинамида рибозида (NR) для получения лекарственного средства для улучшения функции мейбомиевой железы.
13. Применение по п.12, где улучшение функции мейбомиевой железы включает увеличение количества ацинарных клеток мейбомиевой железы.
14. Применение по п.12, где улучшение функции мейбомиевой железы включает увеличение секреции липидов мейбомиевой железой.
15. Применение по п.12, где улучшение функции мейбомиевой железы включает лечение или профилактику заболевания, сопровождающегося дисфункцией мейбомиевой железы.
16. Применение никотинамида мононуклеотида (NMN) или никотинамида рибозида (NR) для получения лекарственного средства для лечения или профилактики дисфункции мейбомиевой железы.
17. Применение по п.16, где дисфункция мейбомиевой железы сопровождается снижением секреции мейбомиевых желез.
18. Применение по п.16, где дисфункция мейбомиевой железы сопровождается воспалительным заболеванием.
19. Применение по п.18, где воспалительное заболевание включает по меньшей мере одно заболевание, выбранное из группы, состоящей из мейбомита, поверхностного (точечного) кератита и блефарита.
20. Применение по п.16, где дисфункция мейбомиевой железы сопровождается избыточным накоплением липидов в протоке.
21. Применение по п. 16, где дисфункция мейбомиевой железы сопровождается дискомфортом в глазах, ощущением инородного тела и/или ощущением давления.
22. Применение по п.15, где заболевание, сопровождающееся дисфункцией мейбомиевой железы, представляет собой мейбомит, задний блефарит, кератит, конъюнктивит, кератоконъюнктивит, связанный с мейбомитом, глазной пемфигоид, синдром Шегрена, синдром Стивенса-Джонсона, реакцию «трансплантат против хозяина» (РТПХ) и нарушение зрительной функции.
| US 20160279161 A1, 29.09.2016 | |||
| WO 2014146044 A1, 18.09.2014 | |||
| US 20160022712 A1, 28.01.2016 | |||
| JP 2018535956 A, 06.12.2018 | |||
| JP 2008542296 A, 27.11.2008 | |||
| ТЕРАПЕВТИЧЕСКИЙ ИЛИ ПРОФИЛАКТИЧЕСКИЙ АГЕНТ ОТ ДИСФУНКЦИИ МЕЙБОМИЕВЫХ ЖЕЛЕЗ ИЛИ БЛОКАДЫ МЕЙБОМИЕВЫХ ЖЕЛЕЗ | 2012 |
|
RU2586289C1 |
Авторы
Даты
2024-07-08—Публикация
2020-06-24—Подача