Область техники, к которой относится изобретение
Настоящее изобретение относится к лекарственному средству, стимулирующему пролиферацию эпителиальных клеток мейбомовой железы или эпителиальных клеток роговой оболочки глаза, которое содержит агонист PPARδ (рецептор, активируемый пролифератором пероксисом) в качестве активного ингредиента.
Уровень техники
Мейбомовая железа является железой, синтезирующей липиды, заключенной между верхним и нижним веками (веки), и она секретирует липид через отверстие, расположенное на конъюнктивной стороне от ресниц век. Липидный слой, составляющий в качестве компонента слезную жидкость, содержит липид, синтезированный мейбомовыми железами, и он предотвращает испарение слезной жидкости с поверхности глаза. Известно, что у пациентов с дисфункцией мейбомовой железы или мейбомитом развивается сухость глаз в результате гипериспарения, кератоконъюнктивные эпителиальные расстройства, эрозия эпителия роговой оболочки глаза и язва роговой оболочки глаза, которые связаны с сухостью глаз, и подобные, т.к. мейбомовая железа проявляет функциональные нарушения и секретирует липид с меньшей концентрацией.
Кроме того, роговая оболочка глаза состоит из эпителия и наружной ограничивающей мембраны (боуменовой оболочки), стромы, внутренней ограничивающей оболочки (десцеметовой оболочки) и эндотелия. Т.к. роговая оболочка глаза располагается на самой передней части глазного яблока, она является чувствительной к внешним воздействиям окружающей среды, в результате чего развиваются различные расстройства. Примеры заболеваний, связанных с повреждением или дефектом эпителиальных клеток роговой оболочки глаза, включают синдром сухого глаза, язву роговой оболочки глаза, поверхностные точечные кератиты, эрозию эпителия роговой оболочки глаза, глазные аллергические расстройства, связанные с повреждением роговой оболочки глаза, такие как весенний конъюнктивит, аллергический кератоконъюнктивит и т.д., и подобные.
В то же время, PPAR является одним из типов внутриклеточных рецепторов, экспрессируемых у большинства позвоночных, и считают, что он принадлежит к группе факторов транскрипции, тесно связанной с концентрацией внутриклеточного сахара или липидным метаболизмом и клеточной дифференцировкой. Что касается подтипов, то известны α, δ и γ-типы. PPARδ иногда обозначают, как PPARβ (непатентный документ 1).
Что касается распределения PPAR в глазной ткани, известна экспрессия PPARα и β в эпителиальных клетках роговой оболочки глаза кроликов (непатентный документ 2).
Сообщали, что 5-[4-(6-метокси-1-метил-1H-бензимидазол-2-илметокси)бензил]тиазолидин-2,4-дион, рассматриваемый в основном, как обладающий PPARγ активирующим действием, можно применять в качестве терапевтического средства для кератоконъюнктивных расстройств (патентные документы 1 и 2), и PPARα, δ и γ-агонист вводят для лечения глазных заболеваний (конъюнктивитов, синдрома сухого глаза, кератитов и т.д.) (патентный документ 3). Кроме того, известно, что PPARα распределяется в печени, почках и подобных и влияет на липидный метаболизм и транспортировку. Кроме того, также сообщают, что их агонист можно применять в качестве терапевтического средства для лечения заболеваний роговой оболочки глаза (патентный документ 4). Сообщали, что агонисты PPARδ стимулируют пролиферацию и дифференцировку эпителиальных клеток сальных желез крыс (непатентный документ 3) и способствуют заживлению ран кожи (непатентный документ 4). Помимо вышеуказанного, известен способ стимулирования пролиферации β-клеток введением нетиазолидиндионового лиганда PPAR и GLP-1 производного (патентный документ 5), ингибирование пролиферации лейкозных клеток, раковых клеток предстательной железы и подобных пиоглитазоном (PPARγ агонист) (непатентный документ 6) и подобными.
Однако многие аспекты экспрессии и функционирования PPARα, δ или γ у каждого животного вида и каждой ткани или клетки еще не прояснены, и точно не известно, является ли пригодным PPARδ агонист для лечения глазных заболеваний у людей.
Патентный документ 1: WO2005/039574,
патентный документ 2: JP-A-2001-39976,
патентный документ 3: WO2002/076177,
патентный документ 4: JP-A-2005-008570,
патентный документ 5: WO2002/69994,
патентный документ 6: WO1998/25598,
непатентный документ 1: J Med. Chem. 2000, 43:527-550,
непатентный документ 2: J Biol. Chem. 2000, 275:2837,
непатентный документ 3: Molecular Genetic and Metabolism 2001, 74:362-369,
непатентный документ 4: Am J Clin. Dermatol. 2003, 4(8):523-530.
Сущность изобретения
Проблемы, которые нужно решить с помощью настоящего изобретения
Одной целью настоящего изобретения является обеспечение лекарственного средства, способного стимулировать пролиферацию эпителиальных клеток мейбомовой железы и эпителиальных клеток роговой оболочки глаза, которое можно применять в основном лечении глазных заболеваний, таких как сухость глаз и подобных, и терапевтическим средством, в котором применяют стимулятор для глазных заболеваний, таких как дисфункция мейбомовой железы, заболевание эпителия роговой оболочки глаза, сухость глаз и подобных.
Способы решения проблем
Изобретатели настоящего изобретения провели тщательные исследования, принимая во внимание вышеупомянутые проблемы, и обнаружили, что конкретный агонист PPARγ обладает исключительной активностью при стимулировании пролиферации эпителиальных клеток мейбомовой железы и эпителиальных клеток роговой оболочка глаза, что привело к созданию настоящего изобретения.
Соответственно, настоящее изобретение включает, по меньшей мере, следующие аспекты.
(1) Лекарственное средство, стимулирующее пролиферацию эпителиальных клеток мейбомовой железы, содержащее [3-[2-[4-изопропил]-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил]-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил]-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль.
(2) Лекарственное средство, стимулирующее пролиферацию эпителиальных клеток роговой оболочки глаза, содержащее [3-[2-[4-изопропил]-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил]-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль.
(3) Лекарственное средство для лечения дисфункции мейбомовой железы, содержащее [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил]-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил]-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль.
(4) Лекарственное средство для лечения заболевания эпителия роговой оболочки глаза, содержащее [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил]-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль.
(5) Лекарственное средство для лечения сухости глаз, содержащее [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил]-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль.
(6) Лекарственное средство вышеупомянутого (5), в котором сухость глаз является сухостью глаз в результате гипериспарения.
(7) Применение [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли для получения лекарственного средства, стимулирующего пролиферацию эпителиальных клеток мейбомовой железы.
(8) Применение [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли для получения лекарственного средства, стимулирующего пролиферацию эпителиальных клеток роговой оболочки глаза.
(9) Применение [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли для получения лекарственного средства для лечения дисфункции мейбомовой железы.
(10) Применение [3-[2-[4-изопропил]-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-{4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли для получения лекарственного средства для лечения заболеваний эпителия роговой оболочки глаза.
(11) Применение [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли для получения лекарственного средства для лечения сухости глаз.
(12) Применение вышеупомянутого (11), в котором сухость глаз является сухостью глаз в результате гипериспарения.
(13) Способ стимулирования пролиферации эпителиальных клеток мейбомовой железы, включающий введение эффективного количества [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты или их фармацевтически приемлемой соли субъекту, нуждающемуся в стимулировании пролиферации эпителиальных клеток мейбомовой железы.
(14) Способ стимулирования пролиферации эпителиальных клеток роговой оболочки глаза, включающий введение эффективного количества [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли, субъекту, нуждающемуся в стимулировании пролиферации эпителиальных клеток роговой оболочки глаза.
(15) Способ лечения дисфункции мейбомовой железы, включающий введение эффективного количества [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил]-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли субъекту, нуждающемуся в лечении дисфункции мейбомовой железы.
(16) Способ лечения заболевания эпителия роговой оболочки глаза, включающий введение эффективного количества [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли субъекту, нуждающемуся в лечении заболевания эпителия роговой оболочки глаза.
(17) Способ лечения сухости глаз, включающий введение эффективного количества [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил]-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли субъекту, нуждающемуся в лечении сухости глаз.
(18) Способ вышеупомянутого (17), в котором сухость глаз является сухостью глаз в результате гипериспарения.
Осуществление настоящего изобретения
Настоящее изобретение относится к новому стимулятору пролиферации мейбомовой железы или стимулятору пролиферации роговой оболочки глаза, который стимулирует пролиферацию эпителиальных клеток мейбомовой железы или эпителиальных клеток роговой оболочки глаза.
Кроме того, терапевтическое средство настоящего изобретения можно эффективно применять для лечения или облегчения заболеваний, например, дисфункции мейбомовой железы, заболевания эпителия роговой оболочки глаза, сухости глаз и подобных.
Краткое описание чертежей
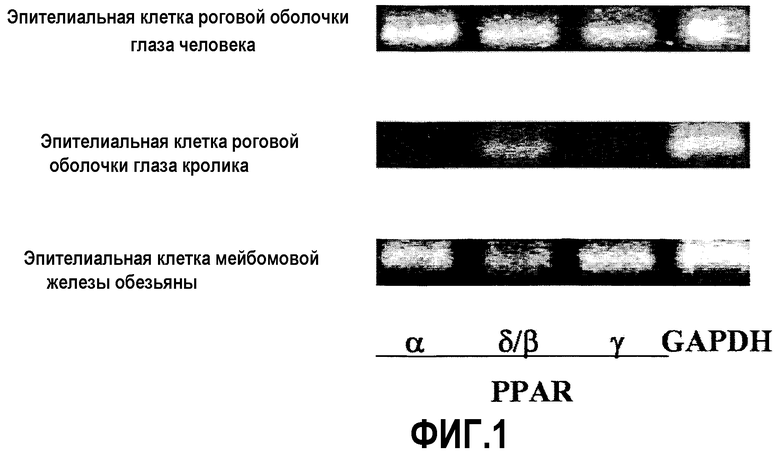
На фиг.1 показана экспрессия мРНК PPARα, δ и γ в выращенных эпителиальных клетках роговой оболочки глаза человека (верхняя панель), в выращенных эпителиальных клетках роговой оболочки глаза кролика (средняя панель) и в выращенных эпителиальных клетках мейбомовой железы обезьяны (нижняя панель).
Лучший вариант осуществления настоящего изобретения
Настоящее изобретение относится к лекарственному средству, стимулирующему пролиферацию эпителиальных клеток мейбомовой железы, содержащему [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль (в дальнейшем в настоящем изобретении иногда в совокупности будут называть "соединение настоящего изобретения") в качестве активного ингредиента. Лекарственное средство стимулирует пролиферацию эпителиальных клеток мейбомовой железы. Кроме того, настоящее изобретение относится к лекарственному средству, стимулирующему пролиферацию эпителиальных клеток роговой оболочки глаза, содержащему [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту, или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль в качестве активного ингредиента. Лекарственное средство стимулирует пролиферацию эпителиальных клеток роговой оболочки глаза. Стимулятор клеточной пролиферации в настоящем изобретении обозначает и лекарственное средство, обладающее способностью стимулировать клеточное деление для того, чтобы увеличить число клеток, и лекарственное средство, обладающее способностью подавлять некроз клеток для того, чтобы увеличить число клеток.
3-[2-[4-Изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусная кислота (CAS № 515138-06-4):
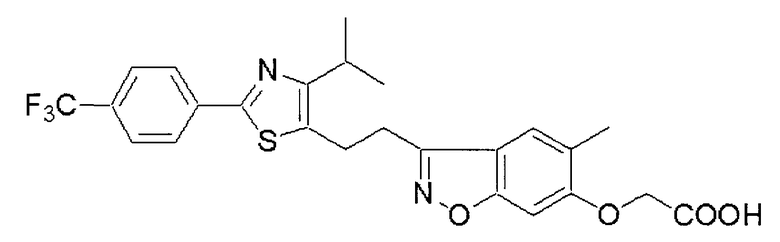
содержащийся в стимуляторе настоящего изобретения в качестве активного ингредиента, является соединением, обладающим PPARδ агонистической активностью, и его описывают в WO2003/033493 (подробно в примере 5).
[4-[3-[2-(4-Трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусная кислота (CAS № 500581-25-8):
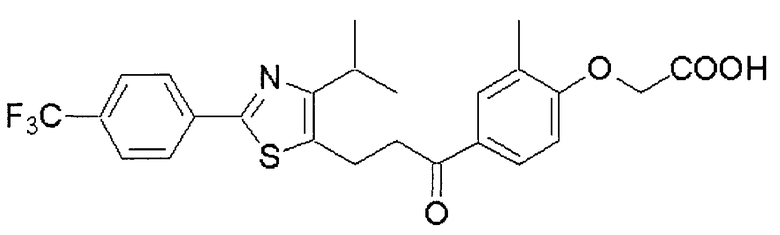
содержащийся в стимуляторе настоящего изобретения в качестве активного ингредиента, является соединением, обладающим PPARδ агонистической активностью, и его описывают в WO2003/016291 (подробно в примере 3).
[4-[3-[2-(2-Гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусная кислота (CAS № 500581-27-1):
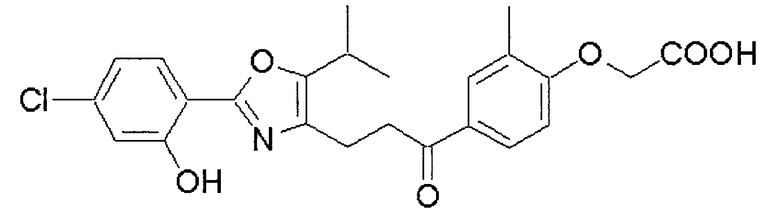
содержащийся в стимуляторе настоящего изобретения в качестве активного ингредиента, является соединением, обладающим PPARδ агонистической активностью, и его описывают в WO2003/016291 (подробно в примере 6).
Примеры фармацевтически приемлемых солей данных соединений включают металлические соли со щелочными металлами, такими как натрий, калий и т.д.; щелочноземельными металлами, такими как кальций, магний и т.д.; и подобными. Кроме того, соединение настоящего изобретения также включает свои сольваты.
PPARδ агонист настоящего изобретения является веществом, которое связывается с лиганд-связывающим доменом (LBD) PPARδ, активирует рецептор и регулирует транскрипцию PPAR гена-мишени. PPARδ агонистическую активность можно измерить дрожжевым дигибридным способом, применяя химерный рецептор LBD и GAL4 дрожжей, и репортерный ген для того, чтобы исключить влияние других ядерных рецепторов, неотъемлемо присутствующих в клетках млекопитающих. Конкретные примеры способа измерения включают PPAR-GAL4 анализы, описанные в ссылочных документах, T.M. Willson et al., Journal of Medicinal Chemistry, 2000, vol.43, № 4, pp.528-550 и J.M. Lehmann et al., The Journal of Biological Chemistry, 1995, vol.270, № 22, pp.12953-12956. Было подтверждено, что соединение настоящего изобретения обладает PPARδ агонистической активностью согласно способам, описанным в WO2003/033493, примере 12 и WO2003/01629, примере 51.
Соединение настоящего изобретения можно синтезировать согласно описаниям WO2003/033493 (подробно пример 5) и WO2003/016291 (подробно примеры 3, 6).
В стимуляторе настоящего изобретения содержание активного ингредиента обычно составляет 0,000001-1% по весу, предпочтительно 0,00001-1% по весу, самое предпочтительное 0,0001-0,1% по весу.
Стимулятор настоящего изобретения может содержать любой носитель в добавление к вышеупомянутым активным ингредиентам.
Примеры данного носителя включают растворители (например, воду, спирт и т.д.), буферы (например, фосфатный буфер, ацетатный буфер, боратный буфер, карбонатный буфер, цитратный буфер, трис-буфер, глутаминовую кислоту, γ-аминокапроновую кислоту и т.д.), консерванты (например, бензалконий хлорид, бензетоний хлорид, глюконат хлогексидина, хлорбутанол, бензиловый спирт, дегидроацетат натрия, эфиры параоксибензойной кислоты, эдетат натрия, борную кислоту и т.д.), изотонические агенты (например, хлорид натрия, хлорид калия, глицерин, маннитол, сорбитол, борная кислота, глюкоза, пропиленгликоль и т.д.) и подобные.
Стимулятор настоящего изобретения можно применять in vivo или in vitro в качестве лекарственного средства или испытуемого реагента и подобных.
Когда стимулятор настоящего изобретения применяют в качестве испытуемого реагента, его можно применять в качестве испытуемого реагента в области физиологии и биохимии и в различных вариантах осуществления.
Когда стимулятор настоящего изобретения применяют в качестве лекарственного средства, оно является пригодным в качестве терапевтического средства для лечения заболеваний, связанных с травмой или атрофией эпителиальных клеток мейбомовой железы и заболевания, вызванного гипофункцией эпителиальных клеток мейбомовой железы, т.к. лекарственное средство стимулирует пролиферацию эпителиальных клеток мейбомовой железы. Примеры заболеваний включают дисфункцию мейбомовой железы, воспаление мейбомовых желез и подобные. Кроме того, т.к. эпителиальные клетки мейбомовой железы секретируют липидный компонент в слезную жидкость, и липид предотвращает испарение слезной жидкости и стабилизирует слой слезной жидкости, терапевтическое средство настоящего изобретения является пригодным для лечения заболевания, связанного с липидными отклонениями (сниженная секреция, замена компонента) в слезной жидкости. Примеры заболеваний включают сухость глаз в результате гипериспарения.
Кроме того, стимулятор настоящего изобретения также является пригодным в качестве терапевтического средства для лечения заболевания, связанного с травмой эпителиальных клеток роговой оболочки глаза (т.е. повреждением или дефектом), т.к. он стимулирует пролиферацию эпителиальных клеток роговой оболочки глаза. Стимулятор настоящего изобретения является пригодным в качестве терапевтического средства для лечения заболеваний эпителия роговой оболочки глаза, конкретно, заболеваний, связанных с эндогенными заболеваниями, такими как синдром Шегрена, синдром Стивенса-Джонсона, синдром сухого глаза (сухость глаз) и подобных; заболеваний, связанных с экзогенными заболеваниями, такими как послеоперационные заболевания, использование лекарственных средств, травма, язва роговой оболочки глаза, воспаление мейбомовых желез, экзогенных заболеваний при ношении контактных линз и подобных; заболеваний, связанных с глазными аллергическими расстройствами, сопровождающимися поражением роговой оболочки глаза, таких как весенний конъюнктивит, аллергический кератоконъюнктивит и подобные. Стимулятор настоящего изобретения также является пригодным для лечения поверхностных точечных кератитов и эрозии эпителия роговой оболочки глаза. Кроме того, стимулятор настоящего изобретения также является пригодным в качестве стимулятора для заживления ран роговой оболочки глаза.
Кроме того, стимулятор настоящего изобретения является пригодным в качестве лекарственного средства для лечения сухости глаз, в частности является очень пригодным в качестве лекарственного средства для лечения сухости глаз в результате гипериспарения, т.к. лекарственное средство одновременно проявляет стимулирующее действие на пролиферацию эпителиальных клеток роговой оболочки глаза и действие на пролиферацию эпителиальных клеток мейбомовой железы и оказывает действие, непосредственно влияя на ткани роговой оболочки глаза и действие, улучшающее функционирование слезной жидкости при действии на клетки мейбомовых желез.
В терапевтическом средстве настоящего изобретения содержание активного ингредиента обычно составляет 0,000001-1% по весу, предпочтительно 0,00001-1% по весу, самое предпочтительное 0,0001-0,1% по весу.
Примеры субъектов для введения стимулятора или терапевтического средства настоящего изобретения включают млекопитающих (например, человека, мышь, крысу, хомяка, кролика, кошку, собаку, корову, овцу, обезьяну и т.д.).
Терапевтическое средство настоящего изобретения можно применять в виде лекарственной формы, например глазных капель, пластыря, мази, лосьона, крема, перорального лекарственного средства и подобных, и оно может содержать, в добавление к вышеупомянутым активным ингредиентам, любой носитель, например фармацевтически приемлемый носитель.
Способ введения терапевтического средства настоящего изобретения в частности не ограничен, при условии, что достигается вышеупомянутый терапевтический эффект, он предпочтительно является местным глазным введением. Примеры лекарственной формы для местного глазного введения включают глазные капли и глазную мазь.
Например, когда терапевтическое средство настоящего изобретения применяют в виде глазных капель или глазной мази, стабилизаторы (например, бисульфит натрия, тиосульфат натрия, эдетат натрия, цитрат натрия, аскорбиновую кислоту, дибутилгидрокситолуол и т.д.), агенты, увеличивающие растворимость (например, глицерин, пропиленгликоль, макрогол, полиоксиэтиленовое гидрогенизированное касторовое масло и т.д.), суспендирующие агенты (например, поливинилпирролидон, гидроксипропилметилцеллюлозу, гидроксиметилцеллюлозу, натрий карбоксиметилцеллюлозу и т.д.), эмульгаторы (например, поливинилпирролидон, соевый лецитин, лецитин яичного желтка, полиоксиэтиленовое гидрогенизированное касторовое масло, полисорбат 80 и т.д.), буферы (например, фосфатный буфер, ацетатный буфер, боратный буфер, карбонатный буфер, цитратный буфер, трис буфер, глютаминовую кислоту, γ-аминокарбоновую кислоту и т.д.), вязкие агенты (например, водорастворимое производное целлюлозы, такое как метилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза и т.д., хондроитинсульфат натрия, гиалурат натрия, карбоксивиниловый полимер, поливиниловый спирт, поливинилпирролидон, макрогол и т.д.), консерванты (например, бензалконий хлорид, бензетоний хлорид, глюконат хлогексидина, хлорбутанол, бензиловый спирт, дегидроацетат натрия, эфиры параоксибензойной кислоты, эдетат натрия, борную кислоту и т.д.), изотонические агенты (например, хлорид натрия, хлорид калия, глицерин, маннитол, сорбитол, борную кислоту, глюкозу, пропиленгликоль и т.д.), pH регуляторы (например, хлороводородную кислоту, гидроксид натрия, фосфорную кислоту, уксусную кислоту и т.д.), вещества, оказывающие охлаждающее действие (например, 1-ментол, d-камфора, d-борнеол, мятное масло и т.д.), мазевые основы (белый вазелин, очищенный ланолин, жидкий парафин, растительное масло (оливковое масло, масло камелии, кокосовое масло и т.д.) и т.д.) и подобные можно добавлять в качестве вспомогательного вещества. Когда количество вспомогательных веществ изменяется в зависимости от типа вспомогательного вещества, способа применения и подобных, их можно добавлять в таких количествах, которые дают концентрации, при которых можно достигнуть цели применения вспомогательного вещества.
Когда терапевтическое средство настоящего изобретения применяют в виде глазных капель или глазных мазей, лекарственное средство можно получить согласно способу, обычно применяемому в области фармацевтики, например, на основе способа, описанного в the Japanese Pharmacopoeia, 14th Edition, Preparation General Rules, section of eye drop и section of ophthalmic ointment.
Примеры форм глазных капель включают водные глазные капли (водные инстилляции, инстилляции водной суспензии, вискозные инстилляции и т.д.), неводные глазные капли (неводные инстилляции, инстилляции неводной суспензии и т.д.), эмульсионные глазные капли и подобные.
pH глазных капель, определенный соответствующим образом, находится в диапазоне 4-8. Когда глазные капли являются водными инстилляциями, pH в частности предпочтительно доводят до pH 6-8, исходя из растворимости активного ингредиента.
Капли для глаз обычно являются лекарственной формой, стерилизованной различными способами, такими как стерилизация фильтрацией, стерилизация облучением (например, стерилизация электронами, стерилизация ультрафиолетом, стерилизация гамма-лучами и т.д.), стерилизация в автоклаве, стерилизация горячим воздухом и подобными.
Когда лекарственную форму получают в виде глазных капель, жидкость предпочтительно добавляют в инстилляционную емкость, снабженную капельным отверстием для жидкости, имеющим маленький диаметр, что позволяет контролировать объем капли для того, чтобы облегчить инстилляцию в глаза. Материал, который нужно применять для емкости, является синтетическим полимером, стеклом, целлюлозой, целлюлозной массой и подобными, и его соответствующим образом выбирают исходя из свойства и количества применяемого активного ингредиента и основания. Что касается сжимаемости и прочности, емкость предпочтительно получают из синтетического полимера. Конкретные примеры материала синтетического полимера включают полиэтиленовый полимер (например, полиэтилен низкой плотности или полиэтилен высокой плотности), полипропиленовый полимер, этилен-пропиленовый сополимер, поли(этилентерефталатный) полимер и подобные.
Примеры емкостей для инстилляции включают емкость, в которой пробку вставляют в емкость, которые формуют независимо, формованную с цельной оболочкой емкость, в которой жидкость плотно закрывают одновременно с формованием емкости (например, WO2004/006826) и подобные. Когда применяют формованную с цельной оболочкой емкость, емкость является более важной с точки зрения стоимости или гигиены, т.к. емкость и жидкость получают непрерывно. Емкость для инстилляции может быть емкостью с одноразовой дозой, которую выбрасывают после применения (например, JP-A-9-207959). Когда применяют данную емкость, можно получать лекарственное средство без консервантов, которое является в высшей степени безопасным для роговой оболочки глаза. Кроме того, данные емкости можно упаковывать приклеиванием поглощающей ультрафиолетовое излучение пленки. Кроме того, емкости могут быть окрашены (коричневый, зеленый, голубой, желтый т.д.) для того, чтобы улучшить характеристики поглощения ультафиолетового излучения.
Настоящее изобретение относится к способу стимулирования пролиферации эпителиальных клеток мейбомовой железы, включающему введение эффективного количества соединения настоящего изобретения субъекту, нуждающемуся в стимулировании пролиферации эпителиальных клеток мейбомовой железы. Желательно применять способ для лечения дисфункции мейбомовой железы.
Кроме того, настоящее изобретение относится к способу стимулирования пролиферации эпителиальных клеток роговой оболочки глаза, включающему введение эффективного количества соединения настоящего изобретения субъекту, нуждающемуся в стимулировании пролиферации эпителиальных клеток роговой оболочки глаза. Желательно применять способ для лечения заболевания эпителия роговой оболочки глаза.
Кроме того, настоящее изобретение относится к способу лечения сухости глаз, включающему введение эффективного количества соединения настоящего изобретения пациентам, страдающим от сухости глаз.
Эффективное количество соединения настоящего изобретения можно определить автоматически, т.к. оно изменяется в зависимости от возраста, веса тела и состояния субъекта, которому вводят лекарственное средство, цели лечения и подобных. Когда стимулятор или терапевтическое средство настоящего изобретения вводят человеку, например раствор, содержащий соединение настоящего изобретения, с концентрацией 0,000001-1% по весу, предпочтительно 0,00001-1% по весу, самое предпочтительное 0,0001-0,1% по весу, обычно закапывают один - восемь раз в день по 1-2 капле в один глаз, а именно, приблизительно 50-200 мкл на инстилляцию. Количество соединения, содержащееся в растворе, имеющем концентрацию и объем в пределах данных диапазонов, можно привести в качестве примера эффективного количества.
Примеры
Настоящее изобретение подробно объясняют ниже, ссылаясь на экспериментальные примеры, которые не истолковываются в качестве ограничивающих.
(Экспериментальный пример 1)
Влияние на увеличение числа нормальных эпителиальных клеток роговой оболочки глаза человека
1. Применяемые клетки
Применяли нормальные эпителиальные клетки роговой оболочки глаза (KURABO).
2. Способ получения раствора испытуемого соединения
В качестве испытуемого соединения применяли [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту (в дальнейшем в настоящем изобретении называют соединением A). Соединение A растворяли в этаноле (Wako Pure Chemical Industries, Ltd.) до 200-кратной концентрации конечной концентрации в культуральной среде, и раствор хранили при -80°C до непосредственного применения.
В качестве культуральной среды для клеток для оценки эффекта, увеличивающего число клеток, соединения A, применяют культуральную среду (базальная среда), полученную добавлением инсулина, гидрокортизона и трансферрина, содержащихся в HCGS комплекте добавочных компонентов для роста (KURABO), к EpiLife (KURABO).
3. Способ испытания
1) Клеточная культура и добавление соединения A
Нормальные эпителиальные клетки роговой оболочки глаза человека, замороженные в жидком азоте, размораживали, и считали число клеток. Их суммарное количество переносили к EpiLife, пополненному всеми из HCGS комплекта добавочных компонентов для роста (инсулином, эпидермальным фактором роста mEGF, полученным у мышей, гидрокортизоном, трансферрином, экстрактом гипофиза мозга быка) (4 мл, полная среда), и суспендировали их. Клеточную суспензию высевали на фибронектин-покрытую 24-луночную плашку (Becton Dickinson) с числом клеток 2×104 клеток/500 мкл/лунка (1×104 клеток/см2, т.к. площадь нижней поверхности составляла 2 см2).
После завершения высевания клеток, культуральный планшет выдерживали в инкубаторе, установленном на 37°C, 5% CO2, 95% воздуха и 100% влажность, в течение 24 часов, и культуральную среду заменяли 400 мкл базальной среды (EpiLife, дополненный инсулином, гидрокортизоном и трансферрином из HCGS добавок для роста).
Через 24 часа культуральную среду заменяли следующей культуральной средой (каждая 400 мкл):
[1] одна базальная среда (группа без добавления);
[2] базальная среда + mEGF (конечная концентрация: 1 нг/мл; группа положительного контроля);
[3] базальная среда + соединение A (конечная концентрация: 0,1 нМ, 1 нМ, 0,01 мкМ, 0,1 мкМ; группа добавления соединения A).
Этанол (5 мкл) добавляли к 1 мл каждой культуральной среды [1] и [2] для того, чтобы однородно довести концентрацию этанола всей культуральной среды до 0,5%.
2) Измерение числа клеток
Через 24 часа после начала стимулирования соединением A, культуральную кондиционированную среду удаляли из каждой лунки, и базальную среду, дополненную 10% Cell Counting Kit-8 (DOJINDO), добавляли к каждой лунке по 200 мкл. После добавления культуральный планшет переносили в инкубатор, установленный на 37°C, 5% CO2, 95% воздуха и 100% влажность и выдерживали в течение 2 часов. Кондиционированную среду (100 мкл) переносили на 96-луночный культуральный планшет для культуры тканей (Corning), и поглощение каждой лунки при 450 нм измеряли считывающим устройством для планшетов (Dainippon Sumitomo Pharma Co., Ltd.), и применяли в качестве коэффициента увеличения числа клеток.
4. Статистический анализ
Величины группы положительного контроля и группы с добавлением соединения A рассчитывали исходя из средней величины поглощения группы без добавления, равной 100%, и группу без добавления сравнивали с группой добавления соединения A и группой положительного контроля согласно критерию множественного сравнения Деннета (односторонний). Критическое значение меньшее чем 5% как результат испытания считали значимым.
5. Результаты испытания
Увеличивающее число клеток действие каждой группы показано в таблице 1. Измеренные величины поглощения показывают, что количество клеток группы положительного контроля и группы добавления соединения A является значительно большим, чем количество клеток группы без добавления, где число клеток группы без добавления равно 100%, и увеличение числа клеток предполагается в данных группах (p<0,01). Из результатов испытания было выяснено, что соединение A увеличивает число нормальных эпителиальных клеток роговой оболочки глаза человека.
Изменения числа клеток при добавлении соединения A к культивируемым нормальным эпителиальным клеткам роговой оболочки глаза человека показаны в величинах, относительно средней величины группы без добавления, равной 100% (значение + стандартное отклонение, N=3-4). **В таблице показана значимая разница по сравнению с группой без добавления (p<0,01).
(Экспериментальный пример 2)
Исследование стимулирующего действия на заживление раны эпителия роговой оболочки глаза
1. Применяемое животное
Применяли мужские особи японских белых кроликов (KITAYAMA LABES Co., Ltd.). Экспериментальных животных применяли согласно международным основополагающим принципам по биомедицинским исследованиям, включающим животных.
2. Способ получения инстилляции испытуемого соединения
Соединение A применяли в качестве испытуемого соединения. Соединение A растворяли в следующей среде с концентрацией 0,0005% или суспендировали в следующей среде с концентрацией 0,005% и применяли в качестве инстилляции.
В качестве контроля для группы введения соединения A применяли вышеупомянутую группу инстилляции среды, свободной от лекарственного средства.
3. Экспериментальный способ
1) Соскоб эпителиальных клеток роговой оболочки глаза
Животным делали внутримышечную инъекцию (1 мл/кг) селактала (2% ксилазин; Bayer, Ltd.): кеталар (5% кетамин; DAIICHI SANKYO COMPANY, LIMITED)=1:1 смесь для общего наркоза, и инстилляцию гидрохлорида оксибупрокаина (инстилляции беноксила 0,4%; Santen Pharmaceutical CO., Ltd.) и затем выделяли глазные яблоки. Применяя трефин с диаметром 10 мм, ставили метку (диаметр 10 мм) на эпителии роговой оболочки глаза в центральной части роговой оболочки глаза, и цельный эпителиальный слой роговой оболочки глаза в маркированном круге соскабливали ручным инструментом для соскабливания под стереомикроскопом. После соскоба поверхность роговой оболочки глаза промывали физиологическим раствором (OTSUKA PHARMACEUTICAL FACTORY, INC.), обработку эпителиального соскоба роговой оболочки глаза завершали помещением глазного яблока обратно в глазницу.
2) Введение
Инстилляцию соединение A или инстилляционную среду закапывали по 50 мкл каждый раз в обрабатываемый глаз микропипеткой дважды в день в день соскоба эпителиальных клеток роговой оболочки глаза и четыре раза в день со следующего дня до завершения испытания.
3) Анализ
Применяя момент времени, когда осуществляли соскоб эпителиальных клеток роговой оболочки глаза у всех животных, в качестве времени начала испытания (0 часов), площадь дефекта эпителия роговой оболочки глаза определяли количественно через 40, 48, 56 и 64 часов исходя из чего оценивали заживление раны эпителия роговой оболочки глаза. Чтобы быть точными, 0,1% раствор флуоресцеина натрия (Wako Pure Chemical Industries, Ltd.) (10 мкл) закапывали в обработанный глаз в каждый момент времени, и передний глазной сегмент животных немедленно фотографировали, применяя щелевую лампу с голубым фильтром, посредством чего фиксировали дефектную область прокрашенного флуоресцеином эпителия роговой оболочки глаза. Проявленную фотографию хранили в виде цифрового изображения на компьютере, и площадь дефекта прокрашенного флуоресцеином эпителия роговой оболочки глаза измеряли, применяя программное обеспечение для анализа изображения (Image-Pro Plus).
4. Статистический анализ
Площадь дефекта прокрашенного флуоресцеином эпителия роговой оболочки глаза, измеренную в каждый момент времени, рассчитывали исходя из первоначальной величины для каждого животного, взятой за 100%, и брали в виде отношения оставшегося дефекта эпителия роговой оболочки глаза. Отношение оставшегося дефекта эпителия роговой оболочки глаза в каждый момент времени сравнивали между группой с инстилляцией среды и группой с инстилляцией соединения A, применяя критерий Стьюдента. Критическую величину, меньшую, чем 5% в качестве результата, считали значимой.
5. Результаты испытаний
Отношение оставшегося дефекта эпителия роговой оболочки глаза в группе с инстилляцией среды и группах инстилляции соединения A при концентрациях 0,0005% и 0,005% в каждый момент времени измерения показано в таблице 2. Показано, что отношение оставшегося дефекта эпителия роговой оболочки глаза значительно уменьшалось в группе инстилляции соединения A в количестве 0,005% через 40 часов после соскоба эпителиальных клеток роговой оболочки глаза. Отношение значительно уменьшалось в группах инстилляции соединения A в количестве 0,0005% и 0,005% через 48 часов. Из результатов испытаний ясно, что инстилляция соединения A стимулирует заживление дефекта эпителия роговой оболочки глаза.
Отношение (%) оставшегося дефекта эпителия роговой оболочки глаза после соскоба эпителиальных клеток роговой оболочки глаза кролика рассчитывали для каждого животного исходя из первоначальной величины, равной 100% (значение + стандартное отклонение, N=6). *В таблице показана значимая разница относительно группы инстилляции среды (p<0,05).
(Экспериментальный пример 3)
Влияние на увеличение числа эпителиальных клеток мейбомовой железы
1. Получение эпителиальных клеток мейбомовой железы обезьяны
Веко обезьяны, выделенное и хранящееся в D-PBS, переносили в ламинарный бокс, и проводили приготовление клеток в стерильных условиях следующим образом.
Выделенное веко погружали в 80% этанол в течение 30 секунд, промывали три раза D-PBS, дополненным 1% пенициллин-стрептомицина (Invitrogen), и переносили в минимальную поддерживающую среду (MEM; Invitrogen). Жировую ткань и мышечную ткань, окружающие ткань мейбомовой железы века, удаляли под стереомикроскопом. Их переносили в MEM, содержащую 0,3 ед/мл коллагеназы A (Roche Diagnostics) и 2,4 ед/мл диспазы II (Roche Diagnostics), и встряхивали при 37°C в течение 4 часов и при 4°C в течение ночи. Обработанную ферментом ткань помещали под стереомикроскоп, и соединительную ткань ресницы и века удаляли для того, чтобы выделить ткань мейбомовой железы. Трипсин-EDTA (4 мл, Invitrogen) добавляли к выделенной железистой ткани, и смесь выдерживали при 37°C в течение 10 минут. После выдерживания добавляли к ней MEM (5 мл), содержащую 10% FBS (Invitrogen) для того, чтобы остановить ферментативную реакцию, и клетки, образующие ткань, диспергировали повторяемым отсасыванием и отделением смеси 5 раз, применяя шприц для инъекций, снабженный иглой для инъекций 21G. Клеточную дисперсию пропускали через 100 мкм и 40 мкм нейлоновые фильтры (Cell Strainer; Falcon), и удаляли клеточную массу и подобные, содержащиеся в ней, которые не могут быть обработаны ферментом. Клеточную суспензию, пропущенную через фильтры, собирали в центрифужную пробирку (50 мл) и центрифугировали при комнатной температуре, 1500 об/мин в течение 5 минут. К слоям клеток, содержащим целевые клетки, полученные центрифугированием, добавляли 80 мкл D-PBS, содержащий 0,5% бычий сывороточный альбумин (BSA; Sigma-Aldrich), и клетки суспендировали в нем в течение достаточного промежутка времени. Добавляли к нему антифибробластные антитела (Militenyi Biotec, 20 мкл), и смесь выдерживали при комнатной температуре в течение 30 минут. После завершения реакции с антителами добавляли к нему 2 мл D-PBS, содержащего 0,5% BSA, и смесь центрифугировали снова при комнатной температуре, 1500 об/мин в течение 5 минут. К слоям клеток, содержащим целевые клетки, полученные центрифугированием, добавляли 1 мл D-PBS, содержащего 0,5% BSA, и клетки суспендировали в нем в течение достаточного промежутка времени. Суспензию добавляли по каплям к LD колонке (Militenyi Biotec), заранее уравновешенной с раствором для промывки колонки (D-PBS, содержащей 2 мМ EDTA (DOJINDO LABORATORIES) и 0,5% BSA). Затем, 2 мл раствора для промывки колонки добавляли по каплям к LD колонке. В течение периода сразу после добавления по каплям клеточной суспензии до завершения добавления по каплям раствора для промывки колонки, немеченые антителами целевые клетки (не фибробласты), которые не абсорбировались на колонке, извлекали в 50 мл центрифужную пробирку. Клетки, собранные в центрифужной пробирке, центрифугировали при комнатной температуре, 1500 об/мин в течение 5 минут, и кондиционированную среду удаляли. Осадок суспендировали в бессывороточной питательной среде для определенных кератиноцитов (5 мл), центрифугировали при комнатной температуре, 1500 об/мин в течение 5 минут и удаляли кондиционированную среду. Снова осадок суспендировали в DK-SFM (3 мл), центрифугировали при комнатной температуре и 1500 об/мин в течение 5 минут, и удаляли кондиционированную среду. Клетки суспендировали в DK-SFM (2 мл) и высевали на 6-луночный мультилуночный планшет для клеточных культур, который был обработан коллагеном. Высеянные клетки выращивали в культуральной среде в бессывороточной питательной среде для определенных кератиноцитов (DK-SFM; Invitrogen, прилагаемые добавочные компоненты добавляли, как указано в протоколе получения), выращивали в инкубаторе (SANYO), установленном на 37°C, 5% CO2, 95% воздуха, 100% влажность, и культуральную среду заменяли новой один раз каждые 48 часов до того, как клетки становились субконфлюентными.
2. Способ получения раствора испытуемых соединений
В качестве испытуемого соединения применяли соединение A, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту (в дальнейшем в настоящем изобретении называют соединение B) или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту (в дальнейшем в настоящем изобретении называют соединение C). Испытуемое соединение растворяли в этаноле (Nacalai Tesque) до 200-кратной концентрации конечной концентрации в культуральной среде, и раствор хранили при -80°C до непосредственного применения.
Для оценки стимулирующего клеточную пролиферацию действия испытуемого соединения культуральную среду, полученную удалением дополнительных компонент, добавленных к DK-SFM из DK-SFM, применяли в качестве базальной среды (базальная DK-SFM). В качестве положительного контроля для подтверждения стимулирующего клеточную пролиферацию действия применяли культуральную среду (полная DK-SFM), которую получали добавлением прилагаемых дополнительных компонентов к базальной среде.
3. Способ испытания
1) Коллагеновая обработка культурального планшета
За день до применения культурального планшета 50 мкл 0,01% коллагена I типа (Nitta Gelatin Inc.) добавляли в каждую лунку культурального планшета, и коллаген оставляли в качестве покрытия лунки при 4°C до непосредственного испытания. В день испытания раствор коллагена I типа удаляли, и осадок культурального планшета промывали три раза D-PBS, и применяли в испытании в качестве коллаген-обработанного культурального планшета.
2) Клеточная культура и добавление испытуемого соединения
В испытании применяли эпителиальные клетки мейбомовой железы обезьяны, которые были выращены в культуральной среде до субконфлюентности в культуральном планшете (диаметр 3,5 см) и заморожены в жидком азоте. Клетки, суспендированные в Cellbanker (Nippon Zenyaku Kogyo Co., Ltd.) и замороженные, размораживали, и переносили в 50 мл центрифужную пробирку, и добавляли 10-кратное количество полной DK-SFM. Клеточные слои собирали центрифугированием при комнатной температуре, 1500 об/мин в течение 5 минут. Подходящее количество полной DK-SFM добавляли к концентрации полученных клеток, равной 3×106 клеток/мл. Клеточную суспензию добавляли в каждую лунку до 64 мкл так, чтобы число клеток было 6×104 клетки/см2 на площадь нижней части (0,32 см2) коллаген-обработанного 96-луночного культурального планшета для тканевой культуры. После завершения высевания клеток культуральный планшет переносили в инкубатор, установленный на 37°C, 5% CO2, 95% воздуха, 100% влажность и выращивали в культуральной среде в течение 24 часов. Культуральную среду заменяли базальной DK-SFM (100 мкл) и дополнительно выращивали в культуральной среде в течение 24 часов. Затем культуральную среду в каждой лунке культурального планшета заменяли 100 мкл каждой из следующих культуральных сред, культуральный планшет помещали обратно в инкубатор и начинали стимулирование клеток.
[1] Одна базальная среда (базальная DK-SFM, группа без добавления);
[2] базальная среда + добавочные компоненты (полная DK-SFM, группа положительного контроля);
[3] базальная среда + соединение A (конечная концентрация: 0,01 мкМ, 0,1 мкМ и 1 мкМ; группа добавления соединения A);
[4] базальная среда + соединение B (конечная концентрация: 0,01 мкМ, 0,1 мкМ и 1 мкМ; группа добавления соединения B);
[5] базальная среда + соединение C (конечная концентрация: 0,01 мкМ, 0,1 мкМ и 1 мкМ; группа добавления соединения C).
Этанол (5 мкл) добавляли к 1 мл каждой культуральной среды [1] и [2] до равномерного распределения концентрации этанола во всех культуральных средах, равной 0,5%.
2) Измерение числа клеток
Через 48 часов после первого стимулирования клеток культуральную среду заменяли культуральной средой вышеупомянутых [1]-[5], приготовленных заново. Через 48 часа культуральную среду заменяли снова культуральной средой вышеупомянутых [1]-[5], приготовленных заново. Через 48 часа культуральную среду удаляли из каждой лунки, и базальную среду, пополненную 10% Cell Counting Kit-8 (DOJINDO), добавляли к каждой лунке по 100 мкл. После добавления культуральный планшет переносили в инкубатор, установленный на 37°C, 5% CO2, 95% воздуха и 100% влажность и выдерживали в течение 2 часов. После выдерживания в течение 2 часов поглощение при 450 нм измеряли считывающим устройством для планшетов (Dainippon Sumitomo Pharma Co., Ltd.), и применяли в качестве коэффициента увеличения числа клеток.
4. Статистический анализ
Величины каждой из группы положительного контроля и группы добавления испытуемого соединения рассчитывали исходя из среднего поглощения в группе без добавления, равного 100%, и группу без добавления сравнивали с группой добавления испытуемого соединения и группой положительного контроля согласно критерию множественного сравнения Деннета (односторонний). Критическую величину меньшую, чем 5% в качестве результата испытания, считали значительной.
5. Результаты испытаний
Стимулирующее действие увеличения числа клеток каждой группы показано в таблице 3. Измеренные поглощения показывают, что увеличение числа клеток в каждой группе добавления испытуемого соединения является значительно большим, чем увеличение в группе без добавления, где число клеток в группе без добавления равно 100%, и предполагали увеличение числа клеток. В группе положительного контроля для подтверждения действия, стимулирующего увеличение числа клеток, наблюдали тенденцию увеличения числа клеток, хотя и незначительную. Из результатов испытаний, ясно, что каждое испытуемое соединение увеличивает число эпителиальных клеток мейбомовой железы обезьяны.
Изменение числа клеток, когда каждое испытуемое соединение или дополнительные компоненты (положительный контроль) добавляли к выращенным в культуральной среде эпителиальным клеткам мейбомовой железы обезьяны, показаны в величинах исходя из средней величины в группе без добавления, равной 100% (значение ± стандартное отклонение, N=5 или 10). **В таблице показана значимая разница относительно группы без добавления (р<0,01).
(Экспериментальный пример 4)
Действие на увеличение числа нормальных эпителиальных клеток роговой оболочки глаза
1. Применяемые клетки
Применяли нормальные эпителиальные клетки роговой оболочки глаза (KURABO).
2. Испытуемое соединение и способ приготовления
В качестве испытуемого соединения применяли соединение B или соединение C. Каждое из соединения B и соединения C растворяли в этаноле (Wako Pure Chemical Industries, Ltd.) до 200-кратной концентрации конечной концентрации в культуральной среде, и раствор хранили при -80°C до непосредственного применения.
В качестве клеточной культуральной среды для оценки действия, увеличивающего число клеток соединением B и соединением C, применяли культуральную среду (базальная среда), полученную добавлением инсулина, гидрокортизона и трансферрина, содержащихся в наборе добавочных компонентов для роста HCGS (KURABO) к EpiLife (KURABO).
3. Способ испытания
1) Клеточная культура и добавление испытуемого соединения
Нормальные эпителиальные клетки роговой оболочки глаза, замороженные в жидком азоте, размораживали и считали число клеток. Их суммарное количество переносили к EpiLife, дополненному всеми компонентами из набора добавочных компонентов для роста HCGS (инсулин, эпидермальный фактор роста mEGF, полученный из мышей, гидрокортизон, трансферрин, экстракт гипофиза мозга быка) (4 мл, полная среда), и хорошо суспендировали в ней. Клеточную суспензию высевали на покрытый фибронектином 24-луночный планшет (Becton Dickinson) с числом клеток, равным 2×14 клеток/500 мкл/лунка (1×104 клеток/см2, т.к. площадь нижней поверхности была 2 см2). После завершения высевания клеток, культуральный планшет выдерживали в инкубаторе, установленном на 37°C, 5% CO2, 95% воздуха и 100% влажность в течение 24 часов, и культуральную среду заменяли 400 мкл базальной среды (EpiLife, дополненной инсулином, гидрокортизоном и трансферрином из дополнительных компонентов для роста HCGS). Через 24 часа после этого, культуральную среду заменяли следующей культуральной средой (каждая 400 мкл).
[1] Одна базальная среда (группа без добавления);
[2] базальная среда + mEGF (конечная концентрация: 1 нг/мл; группа положительного контроля);
[3] базальная среда + соединение B (конечная концентрация: 0,01 мкМ, 0,1 мкМ, 1 мкМ; группа добавления соединения B);
[4] базальная среда + соединение C (конечная концентрация: 0,01 мкМ, 0,1 мкМ, 1 мкМ; группа добавления соединения C).
Этанол (5 мкл) добавляли к 1 мл каждой культуральной среды [1] и [2] для того, чтобы одинаково довести концентрацию этанола всей культуральной среды до 0,5%.
2) Измерение числа клеток
Через 24 часа после начала стимулирования соединением B или соединением C культуральную кондиционированную среду удаляли из каждой лунки, и базальную среду, дополненную 10% Cell Counting Kit-8 (DOJINDO), добавляли в каждую лунку по 200 мкл. После добавления культуральный планшет переносили в инкубатор, установленный на 37°C, 5% CO2, 95% воздуха и 100% влажность и выдерживали в течение 2 часов. Кондиционированную среду (100 мкл) переносили в 96-луночный культуральный планшет для тканевой культуры (Corning), и измеряли поглощение в каждой лунке при 450 нм считывающим устройством для планшетов (Dainippon Sumitomo Pharma Co., Ltd.), и применяли в качестве коэффициента увеличения числа клеток.
4. Статистический анализ
Величины каждой из группы положительного контроля и группы добавления соединения B и соединения C рассчитывали исходя из среднего поглощения в группе без добавления, равного 100%, и группу без добавления сравнивали с группой добавления соединения B или соединения C и группой положительного контроля согласно критерию множественного сравнения Деннета (односторонний). Критическую величину меньшую, чем 5% в качестве результата испытания, считали значительной.
5. Результаты испытаний
Стимулирующее увеличение числа клеток действие каждой группы показано в таблице 4. Измеренные поглощения показывают, что число клеток в группе положительного контроля, в группе добавления соединения B и в группе добавления соединения C является значительно большим, чем число клеток в группе без добавления, где число клеток в группе без добавления равно 100%, и в данных группах предполагали увеличение числа клеток (р<0,01). Из результатов испытаний ясно, что и соединение B и соединение C увеличивает число нормальных эпителиальных клеток роговой оболочки глаза человека.
Изменение числа клеток при добавлении соединения B или соединения C к культивированным нормальным эпителиальным клеткам роговой оболочки глаза показаны в величинах относительно средней величины в группе без добавления, равной 100% (значение ± стандартное отклонение, N=4). **В таблице показана значимая разница по сравнению с группой без добавления (p<0,01).
(Экспериментальный пример 5)
Экспрессия PPAR в эпителиальных клетках роговой оболочки глаза и в эпителиальных клетках мейбомовой железы
1. Применяемые клетки
Применяемыми эпителиальными клетками мейбомовой железы обезьяны были клетки, полученные и культивированные способом, аналогичным способу экспериментального примера 3. Применяемыми эпителиальными клетками роговой оболочки глаза (KURABO) были клетки, выращенные в инкубаторе, установленном на 37°C, 5% CO2, 95% воздуха, 100% влажность в бессывороточной базальной среде для пролиферации нормальных эпителиальных клеток роговой оболочки глаза человека (EpiLife; KURABO). Применяемыми эпителиальными клетками роговой оболочки глаза кролика были клетки, полученные и выращенные следующим способом.
Роговую оболочку глаза вырезали из глазного яблока, выделенного у умерщвленного кролика, хранили в физиологическом растворе, забуференном фосфатом Дульбекко (D-PBS; Invitrogen), и переносили в ламинарный бокс. Проводили в стерильных условиях следующие операции по получению клеток.
Выделенный круглый фрагмент роговой оболочки глаза промывали три раза D-PBS, дополненным 1% пенициллин-стрептомицином (Invitrogen) и переносили в минимальную эссенциальную среду (MEM; Invitrogen). Эндотелиальные клетки роговой оболочки глаза и десцеметову оболочку круглого фрагмента роговой оболочки глаза, погруженного в MEM, отделяли ножом для глазной хирургии (Alcon), и отделенный круглый фрагмент роговой оболочки глаза (строма роговой оболочки глаза и эпителий роговой оболочки глаза) переносили к MEM, дополненной диспазой II (Roche Diagnostics) с концентрацией 2,4 ед/мл. Фрагмент выдерживали при 37°C в течение 1 часа, и круглый фрагмент роговой оболочки глаза, обработанный диспазой II, переносили к MEM. Эпителий роговой оболочки глаза круглого фрагмента роговой оболочки глаза, погруженного в MEM, отделяли ножом для глазной хирургии, и остаток круглого фрагмента роговой оболочки глаза (строма роговой оболочки глаза) удаляли из MEM. MEM, содержащую отделенные эпителиальные клетки роговой оболочки глаза, собирали в 50 мл центрифужную пробирку, центрифугировали при комнатной температуре, 1500 об/мин в течение 5 минут и кондиционированную среду удаляли, получая слои эпителиальных клеток роговой оболочки глаза. К слоям эпителиальных клеток роговой оболочки глаза добавляли 1 мл трипсин-EDTA (Invitrogen), и смесь хорошо перемешивали и выдерживали при 37°C в течение 5 минут для того, чтобы устранить межклеточную адгезию. К смеси добавляли 9 мл MEM, содержащей 10% фетальную бычью сыворотку (FBS; Invitrogen), для того, чтобы остановить ферментативную реакцию, и смесь центрифугировали снова при комнатной температуре, 1500 об/мин в течение 5 минут, получая слои эпителиальных клеток роговой оболочки глаза. К полученным слоям эпителиальных клеток роговой оболочки глаза добавляли 1 мл бессывороточной жидкой среды для роста нормальных эпителиальных клеток роговой оболочки глаза кролика (RCGM2; KURABO) для того, чтобы суспендировать в ней клетки, и клетки высевали в планшете для клеточной культуры (диаметр 10 см, 10 IWAKI), дополненной 9 мл RCGM2. Высеянные клетки выращивали в инкубаторе (SANYO), установленном на 37°C, 5% CO2, 95% воздуха, 100% влажность. Культуральную среду заменяли новой средой один раз каждые 48 часов до первого дня испытания.
2. Способ испытания
1) Экстракция суммарной РНК из клетки
Суммарную РНК экстрагировали из каждой клетки согласно общепринятому способу для TRIzol реагента (Invitrogen).
2) Получение кДНК из экстрагированной суммарной РНК
Суммарную экстрагированную РНК обрабатывали ДНКазой при 37°C в течение 30 минут для того, чтобы удалить геномную ДНК согласно общепринятому способу для освобождению от ДНК (Ambion).
кДНК получали из экстрагированной суммарной РНК согласно общепринятому способу для обратной транскриптазы Superscript II (Invitrogen). То есть кДНК, комплементарную суммарной РНК, обработанной ДНКазой, получали из 1 мкг суммарной РНК, применяя случайный праймер (Invitrogen).
3) Амплификация PPAR гена (полимеразная цепная реакция; ПЦР)
ПЦР PPAR гена проводили согласно общепринятому способу для Platinum PCR SuperMix (Invitrogen). PPAR праймер конструировали так, чтобы продукт ПЦР был, приблизительно, 200 пар оснований относительно известных последовательностей человека, шимпанзе, макаки крабоеда, коровы, мыши и подобных.
PPARα: GTAGAATCTGCGGGGACAAG (смысловая) (SEQ ID NO:1)
: GTTGTGTGACATCCCGACAG (антисмысловая) (SEQ ID NO:2)
PPARδ: TTCCTTCCAGCAGCTACACA (смысловая) (SEQ ID NO:3)
: GATCGTACGACGGAAGAAGC (антисмысловая) (SEQ ID NO:4)
PPARγ: CTCCGTGGATCTCTCCGTAA (смысловая) (SEQ ID NO:5)
: GATGCAGGCTCCACTTTGAT (антисмысловая) (SEQ ID NO:6)
ПЦР реакцию осуществляли реакцией при 94°C в течение 2 минут 15 секунд, с последующими 35 циклами 3-стадийных реакций при 94°C в течение 30 секунд, 55°C в течение 30 секунд и 72°C в течение 30 секунд. Образец после ПЦР реакции подвергали электрофорезу на 2% агарозном геле, и ДНК, разделенную в геле, прокрашивали SYBR Gold (Molecular Probes). Изображения прокрашенной ДНК, люминесцирующей под УФ трансиллюминатора, хранили в виде цифровых данных.
3. Результаты испытаний
Полоски ДНК после электрофореза показаны на фиг.1. В качестве результата данного испытания подтверждали, что все из PPARα, PPARδ и PPARγ экспрессировались в эпителиальных клетках роговой оболочки глаза человека и эпителиальных клетках мейбомовой железы обезьяны. В эпителиальных клетках роговой оболочки глаза кролика подтверждали только экспрессию PPARδ. Bonazzi et al. сообщают, что PPARα и PPARβ(=δ) из PPAR экспрессируются в эпителиальных клетках роговой оболочки глаза кролика (Bonazzi A. et al., J. Biol. Chem. (2000); 275 (4): 2837-2844). В данной статье они применяли специальный способ обнаружения PPARα, который предполагает, что уровень экспрессии PPARα в эпителиальных клетках роговой оболочки глаза кролика является крайне малым.
Промышленная применимость
Согласно настоящему изобретению обеспечивают новым лекарственным средством, стимулирующим пролиферацию эпителиальных клеток мейбомовой железы или новым средством, стимулирующим пролиферацию эпителиальных клеток роговой оболочки глаза, и лекарственное средство стимулирует пролиферацию эпителиальных клеток мейбомовой железы или эпителиальных клеток роговой оболочки глаза. Кроме того, терапевтическое средство настоящего изобретения можно эффективно применять для лечения или облегчения заболеваний, таких как дисфункция мейбомовой железы, заболевание эпителия роговая оболочка глаза, сухость глаз и подобных.
Настоящая заявка основывается на патентной заявке № 2007-134183, внесенной в реестр в Японии (дата внесения в реестр: 21 мая 2007), содержание который вводится полностью в настоящее изобретение с помощью ссылки.


Группа изобретений относится к области офтальмологии. Лекарственное средство стимулирует пролиферацию эпителиальных клеток мейбомовой железы или эпителиальных клеток роговой оболочки глаза. Лекарственное средство содержит [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси] уксусную кислоту или их фармацевтически приемлемую соль в качестве активного ингредиента. Применяют указанный активный ингредиент для получения лекарственного средства, и в качестве стимулирующего пролиферацию эпителиальных клеток мейбомовой железы или эпителиальных клеток роговой оболочки глаза. Группа изобретений обеспечивает лечение глазных заболеваний, таких как сухость глаз, дисфункция мейбомовой железы, заболевания эпителия роговой оболочки глаза. 6 н. и 12 з.п. ф-лы, 1 ил., 4 табл., 5 пр.
1. Лекарственное средство, стимулирующее пролиферацию эпителиальных клеток мейбомовой железы, содержащее [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил] пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль.
2. Лекарственное средство, стимулирующее пролиферацию эпителиальных клеток роговой оболочки глаза, содержащее [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусную кислоту, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусную кислоту или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусную кислоту, или их фармацевтически приемлемую соль.
3. Лекарственное средство по п.1, где указанное лекарственное средство используется для лечения дисфункции мейбомовой железы.
4. Лекарственное средство по п.2, где указанное лекарственное средство используется для лечения заболевания эпителия роговой оболочки глаза.
5. Лекарственное средство по любому из пп.1 или 2, где указанное лекарственное средство используется для лечения сухости глаз.
6. Лекарственное средство по п.5, в котором сухость глаз является сухостью глаз, вызванной гипериспарением.
7. Применение [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли для получения лекарственного средства, стимулирующего пролиферацию эпителиальных клеток мейбомовой железы.
8. Применение [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли для получения лекарственное средства, стимулирующего пролиферацию эпителиальных клеток роговой оболочки глаза.
9. Применение по п.7, в котором указанное лекарственного средство используется для лечения дисфункции мейбомовой железы.
10. Применение по п.8, в котором указанное лекарственного средство используется для лечения заболевания эпителия роговой оболочки глаза.
11. Применение по любому из пп.7 или 8, в котором указанное лекарственное средство используется для лечения сухости глаз.
12. Применение по п.11, в котором сухость глаз является сухостью глаз, вызванной гипериспарением.
13. Способ стимулирования пролиферации эпителиальных клеток мейбомовой железы, включающий введение эффективного количества [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли субъекту, нуждающемуся в стимулировании пролиферации эпителиальных клеток мейбомовой железы.
14. Способ стимулирования пролиферации эпителиальных клеток роговой оболочки глаза, включающий введение эффективного количества [3-[2-[4-изопропил-2-(4-трифторметил)фенил-5-тиазолил]этил]-5-метил-1,2-бензизоксазол-6-ил]оксиуксусной кислоты, [4-[3-[2-(4-трифторметил)фенил-4-изопропил-5-тиазолил]пропионил]-2-метилфенокси]уксусной кислоты или [4-[3-[2-(2-гидрокси-4-хлорфенил)-5-изопропил-4-оксазолил]пропионил]-2-метилфенокси]уксусной кислоты, или их фармацевтически приемлемой соли субъекту, нуждающемуся в стимулировании пролиферации эпителиальных клеток роговой оболочки глаза.
15. Способ по п.13, в котором указанный способ включает лечение дисфункции мейбомовой железы.
16. Способ по п.14, в котором указанный способ включает лечение заболевания эпителия роговой оболочки глаза.
17. Способ по любому из пп.13 или 14, в котором указанный способ включает лечение сухости глаз.
18. Способ по п.17, в котором сухость глаз является сухостью глаз, вызванной гипериспарением.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| WO 03016291 A1, 27.02.2003 | |||
| WO 03033493 A1, 24.04.2003 | |||
| JP 2005008570 A, 13.01.2005 | |||
| Шпиндельное устройство | 1985 |
|
SU1324774A1 |
| WO 2002013812 A1, 21.02.2002 | |||
| US 20070027184 A1, 01.02.2007. | |||
Авторы
Даты
2012-05-10—Публикация
2008-05-20—Подача