ОБЛАСТЬ ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам лечения или профилактики вызванных буллезным эпидермолизом («ЕВ») язв, индуцированных ингибиторами рецептора эпидермального фактора роста (EGFR) кожных токсических эффектов, повреждений, вызванных болезнью Хейли - Хейли («HHD»), язв Бурули и инфекций SARS-CoV-2 путем местного нанесения гипотонического кислотного окислительного раствора, содержащего хлорноватистую кислоту (HClO), на пораженную область.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Различные кожные заболевания, как природного, так и искусственного происхождения нуждаются в эффективном лечении, и сюда входят язвы, вызванные буллезным эпидермолизом, индуцированные ингибиторами EGFR кожные токсические эффекты, повреждения, вызванные болезнью Хейли - Хейли и язвы Бурули.
ЕВ представляет собой гетерогенную группу редких генетических кожных заболеваний, которые приводят к появлению на коже пузырей и ее разрывам при малейшем касании. Родившиеся с ЕВ имеют столь хрупкую кожу, что их называют «детьми-бабочками», - просто их кожа столь же хрупкая, как крыло бабочки. В местах повреждения исключительно хрупкой кожи образуются болезненные открытые раны и язвы, а в некоторых случаях также поражаются внутренние оболочки и органы. Людям с ЕВ часто приходится сталкиваться с осложнениями, обусловленными вторичной инфекцией, и с большим количеством рубцов. К большому сожалению, некоторые типы ЕВ могут быть смертельными в младенчестве, а другие серьезно ограничивают продолжительность жизни. ЕВ может наследоваться либо в доминантной, либо в рецессивной форме. ЕВ также может возникать в результате новой спонтанной мутации - ни один из родителей не имеет ЕВ, но ген спонтанно мутирует либо в сперматозоиде, либо в яйцеклетке до оплодотворения. В редких случаях тяжелая форма ЕВ может быть «приобретена» в результате аутоиммунного заболевания, при котором организм вырабатывает антитела, атакующие белки его собственных тканей.
Рецептор эпидермального фактора роста (EGFR, также известный как ErbB-1 или HER-1) представляет собой белок, который обнаруживается на поверхности некоторых клеток, и который заставляет клетки делиться при связывании с ним эпидермального фактора роста. EGFR встречается в аномально высоких количествах в раковых клетках, и активация EGFR, по-видимому, важна для роста и прогрессирования опухоли. EGFR имеет высокую экспрессию на эпидермисе, на базальном клеточном слое, на уровне сальных желез и на кератиноцитах. Ингибиторы EGFR связываются с определенными частями EGFR и замедляют или останавливают рост клеток. У пациентов с раком, получающих схемы лечения на основе ингибиторов EGFR, обычно возникают нежелательные реакции на коже, такие как папуло-пустулезная сыпь, паранихия, изменение роста волос, раздражение и сухость кожи, поскольку вышеупомянутые агенты влияют на процесс пролиферации клеток кожи.
Болезнь Хейли - Хейли представляет собой аутосомный доминантно-наследуемый дерматоз, впервые описанный братьями Хейли в 1939 г. Дефицит белка АТР2С1 в кератиноцитах приводит к утрате межклеточной адгезии (акантолиз) среди клеток супрабазального слоя эпидермиса, вероятно, из-за отхода промежуточных филаментов кератина от десмосомальных бляшек. Болезнь обычно проявляется на третьем или четвертом десятилетии жизни и характеризуется везикулярными повреждениями, эрозиями со струпьями и бугорчатыми папулами, которые возникают в основном на шее, в местах опрелостей и зонах сгибания кожи. Болезнь у взрослых полностью внедрена в организм, но имеет колеблющееся течение с переменной выраженностью. Контролировать это состояние сложно, и существующие методы лечения не обеспечивают длительного положительного терапевтического эффекта. Внешние факторы, такие как потоотделение, воздействие УФ-излучения, трение и суперинфекция бактерий, грибков и вирусов, играют важную роль в обострениях и сохранении повреждений.
Язвы Бурули представляет собой хроническое инвалидизирующее заболевание, которое главным образом поражает кожу и иногда кости. Заболевание впервые описано сэром Альбертом Куком в 1897 г. в Уганде, но лишь в 1930-х годах австралийским исследователям под руководством Питера Маккаллума впервые удалось получить культуру микроорганизма из повреждений от пациентов из региона Бернсдейл. Язвы Бурули вызывает микроорганизм Mycobacterium ulcerans, принадлежащий к тому же семейству бактерий, которые вызывают туберкулез и проказу. Несмотря на то что вызывающий язвы Бурули микроорганизм представляет собой бактерию, живущую во окружающей среде, способ ее передачи людям остается неизвестным. Организм продуцирует уникальный токсин, миколактон, который и вызывает повреждение кожи.
SARS-CoV-2 представляет собой респираторный вирус с близким генетическим сходством с коронавирусами летучих мышей. Считается, что SARS-CoV-2 распространяется главным образом через капли слюны или выделения из носа, когда инфицированные люди кашляют или чихают.Большая часть знаний о физико-химических свойствах коронавирусов получена на SARS-CoV и MERS-CoV. SARS-CoV-2 может быть инактивирован УФ или нагревом до 56°С в течение 30 мин, и он также чувствителен к большинству дезинфицирующих веществ, таких как диэтиловый эфир, 75% этанол, хлор, перуксусная кислота и хлороформ. На текущий момент не существует специфических вакцин или способов лечения SARS-CoV-2. Однако ведется множество клинических испытаний, в которых оценивают потенциальные способы лечения наиболее тяжелых форм, но пока не найден способ лечения всей популяции, который смог бы снизить и взять под контроль передачу вируса.
ОПИСАНИЕ ПОТРЕБНОСТИ
Существует неудовлетворенная медицинская потребность в безопасных и эффективных способах лечения буллезного эпидермолиза («ЕВ»), индуцированных ингибиторами EGFR кожных токсических эффектов, повреждений, вызванных болезнью Хейли - Хейли («HHD»), язв Бурули и инфекции SARS-CoV-2. Быстрое, удобное в применении и безопасное лечение для терапии базового патогенеза этих состояний и ускорения заживления ран при состояниях, вызванных ранами, значительно улучшит качество жизни пациентов, страдающих от этих состояний, и членов их семей.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Был разработан гипотонический кислотный окислительный водный раствор, охарактеризованный по рН, содержанию хлоридов и содержанию свободного хлора, обладающий неожиданной универсальностью при лечении нескольких определенных локализованных состояний и респираторных инфекций. Таким образом, в первом основном варианте осуществления в изобретении предложен способ лечения раны, вызванной буллезным эпидермолизом («ЕВ»), у нуждающегося в этом пациента, включающий местное нанесение на указанную рану терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20 140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤ 3% гипохлорита (ClO-).
Во втором основном варианте осуществления в изобретении предложен способ лечения индуцированной ингибитором EGFR кожной токсичности у нуждающегося в этом пациента, включающий местное нанесение на кожу, пораженную кожной токсичностью, терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
В третьем основном варианте осуществления в изобретении предложен способ лечения местного расстройства, вызванного болезнью Хейли - Хейли («HHD»), у нуждающегося в этом пациента, включающий местное нанесение на пораженную указанным расстройством кожу терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
В четвертом основном варианте осуществления в изобретении предложен способ лечения язв Бурули, вызванных mycobacterium ulcerans, у нуждающегося в этом пациента, включающий местное нанесение на указанные язвы терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
В пятом основном варианте осуществления в изобретении предложен способ лечения инфекции SARS Cov2 у нуждающегося в этом пациента, включающий местное нанесение в носовой проход, и/или в горло, и/или в верхние дыхательные пути указанного пациента терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
Дополнительные преимущества изобретения частично изложены в представленном ниже описании, частично будут очевидны из описания или могут быть выявлены в ходе практического применения изобретения. Преимущества изобретения будут реализованы и достигнуты с помощью элементов и комбинаций, в частности указанных в прилагаемой формуле изобретения. Следует понимать, что как приведенное выше общее описание, так и последующее подробное описание служат только для примера и разъяснения и не ограничивают объем изобретения.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Сопроводительные графические материалы, включенные в настоящее описание и составляющие его часть, иллюстрируют нескольких вариантов осуществления изобретения и вместе с данным описанием служат для пояснения принципов изобретения.
На ФИГ. 1 представлены гистологические анализы поврежденной ткани через 4 часа и 24 часа после повреждения после применения интенсивного лечения (APR TD011) и отрицательный контроль, как описано в примере 3.
На ФИГ. 2 представлена серия фотографий, отображающих результаты для 24-летнего пациента с тяжелой генерализованной рецессивной дистрофической формой буллезного эпидермолиза (RDEB), получавшего лечение способами настоящего изобретения, как описано в примере 3.
На ФИГ. 3 представлена пара фотографий нижней части ноги двухлетней хронической раны пациента с пограничным буллезным эпидермолизом (JEB), получавшего лечение в соответствии со способами настоящего изобретения, как описано в примере 3.
На ФИГ. 4 показано влияние раствора настоящего изобретения, иллюстрирующие уровни экспрессии белка Nrf2, значительно повышенные в клетках siATP2C1, обработанных раствором настоящего изобретения, по сравнению с клетками siATP2C1, обработанными несущей средой, на модели, в частности, относящейся к болезни Хейли - Хейли, как описано в примере 5.
На ФИГ. 5 показано влияние раствора настоящего изобретения на экспрессию цитокинов TGF1 и TGFB2 в дефектных по АТР2С1 кератиноцитах в модели, в частности, относящейся к болезни Хейли - Хейли, как описано в примере 5.
На ФИГ. 6 показано влияние обработки клеток siATP2C1 раствором настоящего изобретения и восстановление дефектной пролиферации обработанных siATP2C1 клеток НаСаТ, как описано в примере 5.
На ФИГ. 7 представлены значения расчетной метаболической активности бактерий Mycobacterium ulcerans, подвергнутых воздействию растворов настоящего изобретения, как описано в примере 6, в частности, применительно к язвам Бурули.
На ФИГ. 8 представлена бактерицидная активность раствора настоящего изобретения в отношении Mycobacterium ulcerans, полученная путем посева и подсчета КОЕ, как описано в примере 6, в частности, применительно к язвам Бурули.
ПОДРОБНОЕ ОПИСАНИЕ
Определения и использование терминов
В настоящей заявке приводятся ссылки на различные публикации. Описания этих публикаций полностью включены в настоящую заявку путем ссылки для более подробного описания уровня техники, к которой относится настоящее изобретение. Приведенные в настоящем документе ссылки также по отдельности и специально включены в текст настоящего документа путем ссылки на содержащиеся в них материалы, которые обсуждают в предложении, содержащем ту или иную ссылку.
В настоящем описании и пунктах формулы изобретения формы единственного числа включают обозначения множественного числа, если иное четко не следует из контекста. Например, термин «описание» относится к одному или более описаниям для применения в изложенных в настоящем документе способах и системах. Термин «углеводород» охватывает смеси двух или более таких углеводородов и т.п.Слово «или» или подобные термины, используемые в настоящем документе, означают любой элемент конкретного списка и также включают любую комбинацию элементов этого списка.
При использовании в настоящем описании и пунктах формулы слово «содержать» и варианты этого слова, такие как «содержащий» и «содержит», означают «включая, без ограничений» и не предназначены для исключения, например, других добавок, компонентов, систем или шагов. Если элемент описан как содержащий один или множество компонентов, стадий или условий, следует понимать, что элемент также может быть описан как «состоящий из» или «состоящий по существу из» компонента, стадии или условия или множества компонентов, стадий или условий.
Если диапазоны обозначаются в настоящем документе путем указания альтернативного верхнего и нижнего пределов диапазона, следует понимать, что эти конечные точки могут быть объединены любым математически осуществимым способом. Таким образом, например, диапазон от 50 или 80 до 100 или 70 можно альтернативно выразить в виде серии диапазонов от 50 до 100, от 50 до 70 и от 80 до 100. Если серия верхних и нижних границ связана с использованием фразы «и» или «или», следует понимать, что верхние границы могут быть не ограничены по нижним границам или объединены с нижними границами, и наоборот.Таким образом, например, диапазон более 40% и/или менее 80% включает в себя диапазоны более 40%, менее 80% и более 40%, но менее 80%.
Если элемент способа или объекта определяется посредством ссылки на один или более примеров, компонентов, свойств или характеристик, следует понимать, что для определения рассматриваемого объекта изобретения также может быть использован любой из или комбинация этих компонентов, свойств или характеристик. Это может происходить, например, если конкретные примеры элемента указаны в пункте формулы изобретения (как в группе Маркуша) или если элемент определяется множеством характеристик. Таким образом, например, если заявленная система содержит элемент А, определенный элементами A1, А2 и A3, в комбинации с элементом В, определенным элементами B1, В2 и В3, настоящее изобретение также следует понимать как охватывающее систему, образованную элементом А без элемента В, систему, в которой элемент А определяется элементами А1 и А2 в комбинации с элементом В, определенным элементами В2 и В3, и все другие возможные перестановки.
«Терапевтически эффективное количество» означает, что количество, которое вводят человеку для поддержания или для воздействия на метаболический процесс или для лечения или профилактики заболевания, является достаточным для обеспечения такого лечения или профилактики заболевания или поддержания или воздействия на метаболический процесс.
При использовании в настоящем документе термин «около» компенсирует вариабельность, допустимую для фармацевтической промышленности и присущую продуктам в данной отрасли, например различия в эффективности продукта из-за вариаций производства и из-за происходящей со временем деградации продукта. Этот термин допускает любую вариацию, которая, согласно надлежащей производственной практике, обеспечивает возможность расценивать оцениваемый продукт как терапевтически эквивалентный или биоэквивалентный указанной эффективности заявленного продукта для людей.
В контексте настоящего изобретения, в той мере, в которой оно относится к любому из патологических состояний, перечисленных в данном документе, термин «лечение» означает уменьшение частоты появления симптома или состояния, или устранение или облегчение по меньшей мере одного симптома, связанного с таким состоянием, или замедление или обращение вспять прогрессирования такого состояния, или контроль или влияние на метаболические процессы, лежащие в основе такого состояния. В рамках значения в настоящем изобретении эти термины также означают остановку, задержку наступления (т.е. период перед клиническим проявлением заболевания) и/или снижение риска развития или ухудшения течения заболевания. При упоминании термина «лечение» в настоящем документе или при указании конкретной цели лечения следует понимать, что такое лечение дает клинический значимый благоприятный эффект. Таким образом, например, когда лечение снижает бактериальную нагрузку или лечит вторичную инфекцию, следует понимать, что бактериальная нагрузка снижается на клинически значимую величину или вторичная инфекция лечится в клинически значимой степени.
Фраза «приемлемый», используемая в связи с композициями изобретения, относится к молекулярным образованиям и другим ингредиентам таких композиций, которые являются физиологически переносимыми и обычно не дают побочных реакций при введении субъекту (например, млекопитающему, такому как человек).
Если в настоящем документе делается ссылка на опубликованные методики испытаний и диагностические приборы, следует понимать, что методика испытаний или диагностический прибор функционирует в версии, действующей на 1 июля 2019 года, если иное не указано в настоящем документе.
Обсуждение основных вариантов осуществления
Изобретение может быть определено на основе нескольких основных вариантов осуществления, которые могут комбинироваться друг с другом и с любым подвариантом осуществления любым способом, физически и математически возможным, для создания дополнительных вариантов осуществления. В первом основном варианте осуществления в изобретении предложен способ лечения раны, вызванной буллезным эпидермолизом («ЕВ») у нуждающегося в этом пациента, включающий местное нанесение на указанную рану терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
Во втором основном варианте осуществления в изобретении предложен способ лечения индуцированной ингибитором EGFR кожной токсичности у нуждающегося в этом пациента, включающий местное нанесение на кожу, пораженную кожной токсичностью, терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
В третьем основном варианте осуществления в изобретении предложен способ лечения местного расстройства, вызванного болезнью Хейли - Хейли («HHD»), у нуждающегося в этом пациента, включающий местное нанесение на пораженную указанным расстройством кожу терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
В четвертом основном варианте осуществления в изобретении предложен способ лечения язв Бурули, вызванных mycobacterium ulcerans, у нуждающегося в этом пациента, включающий местное нанесение на указанные язвы терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
В пятом основном варианте осуществления в изобретении предложен способ лечения инфекции SARS Cov2 у нуждающегося в этом пациента, включающий местное нанесение в носовой проход, и/или в горло, и/или в верхние дыхательные пути указанного пациента терапевтически эффективного количества гипотонического кислотного окислительного водного раствора, имеющего рН от 2,5 до 6, содержание хлоридов менее 400 мг/мл и содержание свободного хлора 20-140 мг/мл, причем указанное содержание свободного хлора предполагает ≥90% хлорноватистой кислоты (HClO), ≤10% хлора (Cl2) и ≤3% гипохлорита (ClO-).
Подварианты осуществления, связанные с буллезным эпидермолизом («ЕВ»)
Последняя классификация 2008 г. названий ЕВ на четыре категории ЕВ определяется уровнем расщепления на границе дерма/эпидермис. См. Fine JD, Eady RAJ, Bauer EA, et al. The classification of inherited epidermolysis bullosa (EB): report of the Third International Consensus meeting on Diagnosis and Classification of EB. J Am Acad Dermatol 2008; 58: 931-50. Таким образом, в одном подварианте осуществления способы лечения ЕВ практически применяют на пациентах с простым буллезным эпидермолизом (EBS), при котором образование пузырей происходит в верхнем слое кожи (эпидермисе). В другом подварианте осуществления способы практически применяют на пациентах с дистрофическим буллезным эпидермолизом (DEB), при котором образование пузырей происходит под зоной базальной мембраны в верхней части дермы. В еще одном подварианте осуществления способы практически применяют на пациентах с пограничным буллезным эпидермолизом (JEB), при котором образование пузырей происходит на границе между эпидермисом и дермой (нижним слоем кожи), в слое кожи, известном как зона базальной мембраны. В еще одном подварианте осуществления способы практически применяют при синдроме Киндлер (KS) - чрезвычайно редком рецессивно-наследуемом расстройстве, при котором за образованием пузырей в младенчестве следует пойкилодермия и светочувствительность в детском возрасте. (См. Burch JM, Fassihi Н, Jones СА, Mengshol SC, Fitzpatrick JE, McGrath JA (2006) Kindler syndrome: new mutation and new diagnostic possibilities. Arch Dermatol 142(5):620-4). Образование пузырей может происходить в любом слое кожи.
Кроме того, также существует форма негенетического ЕВ с аналогичными признаками. Таким образом, в еще одном подварианте осуществления способы практически применяют на пациентах с приобретенным буллезным эпидермолизом (ЕВА), при котором образование пузырей происходит в базальной дерме. Это хронический аутоиммунный процесс, вызванный антителами, нацеленными на коллаген типа VII, основной компонент якорных фибрилл, которые соединяют базальную мембрану с дермальными структурами. См. Kasperkiewicz М, Sadik CD, Bieber K, Ibrahim SM, Manz RA, Schmidt E, Zillikens D, Ludwig RJ. Epidermolysis Bullosa Acquisita: From Pathophysiology to Novel Therapeutic Options. J Invest Dermatol. 2016 Jan;136(l):24-33.
В зависимости от фено- и генотипа, а также характера наследования, указанные выше категории дополнительно подразделяются на различные подгруппы, некоторые из которых содержат чрезвычайно редкие подформы. Laimer М, Prodinger С., Bauer JW Hereditary Epidermolysis Bullosa. J Dtsch Dermatol Ges. 2015 Nov; 13(11): 1125-33. Таким образом, в дополнительных подвариантах осуществления:
 пациент с EBS имеет мутации в кератинах 5 и 14; плектине; интегрине α6β4; плакофилине-1; или десмоплакине;
пациент с EBS имеет мутации в кератинах 5 и 14; плектине; интегрине α6β4; плакофилине-1; или десмоплакине;
 пациент с JEB имеет мутации в ламинине-332 (ламинине 5); в коллагене типа XVII; или интегрине α6β4;
пациент с JEB имеет мутации в ламинине-332 (ламинине 5); в коллагене типа XVII; или интегрине α6β4;
 пациент с DEB имеет мутации в коллагене типа VII; или
пациент с DEB имеет мутации в коллагене типа VII; или
 пациент с KS имеет мутацию в киндлине-1. См. Denyer, J., Pillay, Е. and Clapham, J. Best practice guidelines for skin and wound care in epidermolysis bullosa. International Consensus. Debra. 2007 http://www.debra-international.org/clinical-guidelines/complete-eb-guidelines/wound-care.html.
пациент с KS имеет мутацию в киндлине-1. См. Denyer, J., Pillay, Е. and Clapham, J. Best practice guidelines for skin and wound care in epidermolysis bullosa. International Consensus. Debra. 2007 http://www.debra-international.org/clinical-guidelines/complete-eb-guidelines/wound-care.html.
В другом подварианте осуществления в способах лечения буллезного эпидермолиза рана выбрана из группы, состоящей из кожных пузырей, пузырей слизистой оболочки, пузырей волосистой части кожи головы, рубцовой алопеции, атрофических рубцов, гиперкератоза, белых угрей, кариеса, дисфагии и раздраженной или болезненной кожи.
В другом подварианте осуществления в способах лечения буллезного эпидермолиза рана выбрана из пузырей и разрывов кожи и слизистой оболочки.
В другом подварианте осуществления в способах лечения буллезного эпидермолиза рана выбрана из пузырей и разрывов кожи и слизистой оболочки, и указанное лечение включает уменьшение времени, необходимого для закрытия указанной раны.
В другом подварианте осуществления в способах лечения буллезного эпидермолиза рана имеет оценку раневого ложа (WBS), и указанное нанесение уменьшает указанную WBS.
В другом подварианте осуществления в способах лечения буллезного эпидермолиза пациент страдает от повышения активности ММР2 и ММР9, и указанное нанесение уменьшает указанное повышение.
В другом подварианте осуществления в способах лечения буллезного эпидермолиза способ дополнительно включает применение у указанного пациента местной повязки, хлорида алюминия, ципрогептадиина, кератинолитика или местного смягчающего агента. После обработки растворами настоящего изобретения на пораженную буллезным эпидермолизом область можно наносить любой тип повязки, обычно используемый для лечения пролежневых язв и других типов ран, включая марлю, смоченную физраствором, повязку, модулирующую активность протеаз, коллагеназную мазь, пенную повязку, базовую повязку для контакта с раной и повязку с поливинилпирролидоном и оксидом цинка.
В другом подварианте осуществления, применимом к способам лечения индуцированных ингибиторами EGFR кожных токсических эффектов, способ дополнительно включает введение указанному пациенту перорального или местного антибиотика, или котикостероида, или увлажнителя кожи. Антибиотик можно вводить профилактически или в ответ на активную инфекцию.
В еще одном подварианте осуществления способ дополнительно включает предотвращение инфекции, вторичной по отношению к буллезному эпидермолизу путем нанесения раствора настоящего изобретения на кожу, пораженную буллезным эпидермолизом.
Подварианты осуществления, связанные с индуцированными ингибиторами EGFR токсическими эффектами
Определены различные подварианты осуществления, основанные на ингибиторе EGFR, вызвавшем токсичность. Таким образом, в нескольких подвариантах осуществления ингибитор EGFR выбран из группы, состоящей из ингибиторов тирозинкиназы (TKI) (например, эрлотиниб, гефитиниб) или моноклональных антител (например, цетуксимаб, нецитумумаб). В других подвариантах осуществления ингибитор EGFR выбран из группы, состоящей из гефитиниба, эрлотиниба, лапатиниба, цетуксимаба, нератиниба, осимертиниба, панитумумаба, вандетаниба, нецитумумаба и дакомитиниба.
В настоящее время не существует общепризнанного международного терапевтического протокола для борьбы с нежелательными кожными явлениями, вызванными ингибиторами EGFR. Однако в руководствах по общим терминологическим критериям оценки нежелательных явлений (СТСАЕ v5.0) Международной ассоциации специалистов в области симптоматической терапии рака (MASCC) и в Национальной сети многопрофильных онкологических учреждений (NCCN) дается несколько рекомендаций исключительно в отношении фармакологического лечения повреждений кожи при острых проявлениях.
Так, в одном подварианте осуществления способы лечения индуцированных ингибитором EGFR токсических эффектов практически применяют в комбинации со вторым лечением, выбранным из группы, состоящей из местного применения антисептиков, местного и/или системного применения антибиотиков (как профилактически, так и в ответ на инфекцию), местного применения ретиноидов и местного и/или системного применения стероидов. В другом подварианте осуществления пациент страдает от клинической экзематизации от легкой до умеренной степени, и настоящее изобретение практически применяют в комбинации с лечением тетрациклином, выбранным из местного применения клиндамицина 2% или эритромицина 4%, необязательно в комбинации с местным применением стероида или пероральным препаратом, выбранным из миноциклина 100 мг/сутки или доксициклина 100 мг/сутки перорально. В еще одном подварианте осуществления пациент страдает от симптомов интенсивного раздражения, и настоящее изобретение практически применяют в комбинации с антигистаминным препаратом, таким как цетиризин.
В другом подварианте осуществления, применимом к способам лечения индуцированных ингибиторами EGFR кожных токсических эффектов, токсичность выбрана из группы, состоящей из ксероза, трещин, зуда, экземы, кожных инфекций, раздражения, уртикарии, аномалий роста волос и папулопустулезной сыпи, и указанное нанесение лечит один или более из указанных токсических эффектов.
В другом подварианте осуществления в способах лечения индуцированных ингибиторами EGFR кожных токсических эффектов токсичность включает в себя рану, которая имеет оценку раневого ложа (WBS), и указанное нанесение уменьшает указанную WBS.
В другом подварианте осуществления, применимом к способам лечения индуцированных ингибиторами EGFR кожных токсических эффектов, нанесение снижает степень токсичности по шкале, выбранной из группы, состоящей из NCI-CTCAE v5.0, FACT-EGFRI-18, DIEHL-24 и MESTT.
В другом подварианте осуществления, применимом к способам лечения индуцированных ингибиторами EGRF кожных токсических эффектов, нанесение улучшает качество жизни указанного пациента, измеренное по шкале EQ-5D-5L/3L для QALYs и/или по дополнительному специфическому для данного состояния опроснику, выбранному из DLQI (дерматологический индекс качества жизни), Skindex-16 или FACT-EGFRI-18.
В другом подварианте осуществления, применимом к способам лечения индуцированных ингибиторами EGRF кожных токсических эффектов, кожная токсичность представляет собой целевое повреждение, и указанное лечение уменьшает размер указанного целевого повреждения.
В другом подварианте осуществления, применимом к способам лечения индуцированных ингибиторами EGFR кожных токсических эффектов, способ дополнительно включает введение указанному пациенту перорального или местного антибиотика, или котикостероида, или увлажнителя кожи. Антибиотик можно вводить профилактически или в ответ на активную инфекцию.
В еще одном подварианте осуществления способ дополнительно включает предотвращение инфекции, вторичной по отношению к индуцированной ингибиторами EGRF кожной токсичности путем нанесения раствора настоящего изобретения на кожу, пораженную токсичностью.
Подварианты осуществления, связанные с болезнью Хейли -Хейли
Диагноз «болезнь Хейли - Хейли» ставят на основании тщательной клинической оценки, подробного анамнеза пациента, выявления характерных признаков и различных специализированных тестов. Таким образом, в одном подварианте осуществления болезнь Хейли - Хейли диагностируется путем хирургического удаления и микроскопического исследования (биопсии) пораженной кожной ткани. В одном подварианте осуществления образец биопсии кожи демонстрирует аномальное образование кератиновой ткани (кератинизация) и отсутствие межклеточной адгезии (акантолиз). В другом подварианте осуществления пациент прошел анализ на мутации в гене АТР2С1 для подтверждения диагноза. В дополнительных подвариантах осуществления пациент с болезнью Хейли - Хейли имеет вторичные бактериальные и грибковые суперинфекции, которые необязательно могут приводить к появлению растущих или зловонных бляшек.
В других подвариантах осуществления способы настоящего изобретения практически применяют в комбинации с терапией, выбранной из холодных компрессов, повязок, кортикостероидных кремов, местных антибиотиков и системных антибиотиков. Другие дополнительные подварианты осуществления практически применяют в комбинации с терапией для закрытия потовых желез, включая ботулиновый токсин и гликопирролат.Дополнительные подварианты осуществления практически применяют в комбинации с производными витамина А (ретиноидами), такими как ацитретин и этретинат, лекарственными средствами, которые подавляют иммунную систему, такими как алефацепт или такролимус, и перорально вводимым хлоридом магния, чтобы улучшить работу ионного насоса.
В другом подварианте осуществления, применимом, в частности, к болезни Хейли - Хейли, местное расстройство выбрано из группы, состоящей из кожной сыпи, раздражения, жжения, растрескивания кожи или вторичной инфекции.
В другом подварианте осуществления, применимом, в частности, к болезни Хейли - Хейли, местное расстройство представляет собой рану, выбранную из пузырей и разрывов кожи и слизистой оболочки.
В другом подварианте осуществления, применимом, в частности, к болезни Хейли - Хейли, местное расстройство представляет собой рану, выбранную из пузырей и разрывов кожи и слизистой оболочки, и указанное лечение включает сокращение времени, необходимого для закрытия раны.
В другом подварианте осуществления, применимом, в частности, к болезни Хейли - Хейли, местное расстройство включает в себя рану, которая имеет оценку раневого ложа (WBS), и указанное нанесение уменьшает указанную WBS.
В другом подварианте осуществления, применимом, в частности, к болезни Хейли - Хейли, местное расстройство включает в себя облегчение и уменьшение кожных повреждений, и указанное нанесение уменьшает длительность обострений указанных повреждений или увеличивает время между появлениями указанных повреждений.
В другом подварианте осуществления, применимом, в частности, к болезни Хейли - Хейли, пациент страдает от состояния, выбранного из потери функциональной активности АТР2С1 в кератиноцитах, окислительного стресса в одном или более повреждениях кожи, снижения активности NRF2 или дисбаланса экспрессии TGFβ1 и TGFβ2, уменьшения пролиферации кератиноцитов, и указанный способ лечит указанное состояние. В другом подварианте осуществления, применимом, в частности, к болезни Хейли - Хейли, способ дополнительно включает применение у указанного пациента охлаждающего компресса, местной повязки, кортикостероидного крема, местного антибиотика или системного антибиотика (как профилактически, так и в ответ на активную инфекцию).
После обработки растворами настоящего изобретения на пораженную болезнью Хейли - Хейли область можно наносить любой тип повязки, обычно используемый для лечения пролежневых язв и других типов ран, включая марлю, смоченную физраствором, повязку, модулирующую активность протеаз, коллагеназную мазь, пенную повязку, базовую повязку для контакта с раной и повязку с поливинилпирролидоном и оксидом цинка.
В еще одном подварианте осуществления способ дополнительно включает предотвращение инфекции, вторичной по отношению к болезни Хейли - Хейли путем нанесения раствора настоящего изобретения на кожу, пораженную болезнью Хейли - Хейли.
Язвы Бурули
В другом подварианте осуществления, применимом, в частности, к лечению язв Бурули, язва Бурули характеризуется раной, и указанное лечение включает сокращение времени, необходимого для закрытия раны.
В другом подварианте осуществления, применимом, в частности, к лечению язв Бурули, язва Бурули характеризуется раной, которая имеет оценку раневого ложа (WBS), и указанное нанесение уменьшает указанную WBS.
В другом подварианте осуществления, применимом, в частности, к лечению язв Бурули, язва Бурули характеризуется секрецией миколактона, и указанное нанесение снижает указанную секрецию.
В другом подварианте осуществления, применимом, в частности, к лечению язв Бурули, язва Бурули характеризуется бактериальной нагрузкой Mycobacterium ulcerans, и указанное нанесение уменьшает указанную бактериальную нагрузку.
В другом подварианте осуществления, применимом, в частности, к лечению язв Бурули, способ дополнительно включает введение указанному пациенту рифампицина и одного или более антибиотиков, выбранных из стрептомицина, кларитромицина и моксифлоксацина.
После обработки растворами настоящего изобретения на пораженную язвами Бурули область можно наносить любой тип повязки, обычно используемый для лечения пролежневых язв и других типов ран, включая марлю, смоченную физраствором, повязку, модулирующую активность протеаз, коллагеназную мазь, пенную повязку, базовую повязку для контакта с раной и повязку с поливинилпирролидоном и оксидом цинка.
В еще одном подварианте осуществления способ дополнительно включает предотвращение инфекции, вторичной по отношению к язвам Бурули, путем нанесения раствора настоящего изобретения на кожу, пораженную язвами Бурули.
Подварианты осуществления, связанные с SARS Cov2
В другом подварианте осуществления, применимом, в частности, для лечения инфекции SARS Cov2, нанесение снижает вирусную нагрузку SARS Cov2 в носовом проходе и верхних дыхательных путях.
В другом подварианте осуществления, применимом, в частности, для лечения инфекции SARS Cov2, нанесение снижает распространение SARS Cov2 на нижние дыхательные пути, такие как трахея и легкие.
В другом подварианте осуществления, применимом, в частности, для лечения инфекции SARS Cov2, указанное введение защищает интраназальные обонятельные нейроны от инфицирования SARS Cov2 и от повреждения.
В другом подварианте осуществления, применимом, в частности, для лечения инфекции SARS Cov2, композицию вводят в виде назального спрея из распылительного устройства в объеме от 100 до 1500 мкл, от 250 до 1000 мкл, от 400 до 750 мкл или 500 мкл на ноздрю на одно введение, что может включать в себя более одного срабатывания устройства. В другом предпочтительном варианте осуществления эти объемы вводят по меньшей мере три раза в сутки в каждую ноздрю.
В особенно предпочтительном варианте осуществления, применимом, в частности, для лечения инфекции SARS Cov2, раствор подается из распылительного насоса, который выдает от 50 до 1000 мкл на срабатывание, от 75 до 500 мкл на срабатывание или от 85 до 300 мкл на срабатывание.
В другом предпочтительном варианте осуществления, применимом, в частности, для лечения инфекции SARS Cov2, раствор вводят по меньшей мере три или четыре раза в сутки в каждую ноздрю.
Дополнительные подварианты осуществления, применимые к множеству способов настоящего изобретения
В другом подварианте осуществления, применимом ко всем способам настоящего изобретения, пациент страдает от одной или более биохимических аномалий, выбранных из аномалий сигнализации ядерного фактора каппа-В (NF-kB), активности Nrf2, активности IL-1, активности фактора, стимулирующего колонии гранулоцитов и макрофагов (GM-CSF), активности IL-6, ММР 2, ММР 9, активности TNF-α, экспрессии KGF, экспрессии TGFβ2 и пролиферации кератиноцитов siATP2C1, и указанное нанесение лечит одну из или любую комбинацию указанных биохимических аномалий.
В другом подварианте осуществления, применимом ко всем способам настоящего изобретения, раствор хранят в исходной упаковке - бутыли из янтарного стекла с распылительной насадкой, прикрепленной к бутылке, или без нее.
В другом подварианте осуществления, применимом для лечения буллезного эпидермолиза, индуцированных ингибиторами EGFR кожных токсических эффектов, болезни Хейли - Хейли и язв Бурули, композицию наносят на пораженную поверхность для местного нанесения путем распыления в количестве приблизительно 50-500 мкл, 75-400, 75-150, 150-400 мкл, 100 мкл или 250 мкл на срабатывание из распылительного устройства насосного типа.
В другом подварианте осуществления, применимом для лечения буллезного эпидермолиза, индуцированных ингибиторами EGFR кожных токсических эффектов, болезни Хейли - Хейли и язв Бурули, композицию наносят на пораженную поверхность для местного нанесения путем распыления в количестве приблизительно 50-500 мкл, 75-400, 75-150, 150-400 мкл, 100 мкл или 250 мкл на срабатывание из распылительного устройства насосного типа и дают высохнуть на воздухе без физического вмешательства.
В случае буллезного эпидермолиза, индуцированных ингибиторами EGFR токсических эффектов, болезни Хейли - Хейли и язв Бурули общее количество раствора в расчете на нанесение будет зависеть от размера повреждения на коже и тяжести повреждения. Таким образом, но без ограничений, можно применять 2 или 3 распыления по 100 или 250 мкл для небольшой раны или 10 20 распылений по 100 или 250 мкл для большей раны. Раствор можно наносить 2, 3 или даже более раз в сутки, в зависимости от тяжести повреждения и количества необходимого орошения.
Лекарственный препарат/состав
Лекарственный препарат представляет собой гипотонический кислотный окислительный раствор, содержащий хлорноватистую кислоту (HClO), полученную в ходе процесса электролиза раствора хлорида натрия. Этот процесс дает гипотонический раствор со специфическими характеристиками с точки зрения (i) рН, (ii) окислительно-восстановительного потенциала (ОВП), (iii) содержания свободного хлора, (iv) чистоты HClO, (v) содержания хлоридов и (vi) свойств долговременной стабильности.
Концентрации соединений свободного хлора (хлор (Cl2), гипохлорита (ClO-) и хлорноватистой кислоты (HClO)) зависят от рН и общего содержания хлоридов, и ими можно манипулировать, используя следующее равновесие диссоциации газообразного хлора в воде:
Cl2+H2O=Cl-+Н++HClO при Ka1 » 3×10-4
HClO=Н++OCl- при Ka2 » 2,9×10-8
Можно вычислить процентную долю трех соединений свободного хлора в соответствии со следующими формулами:
αCl2=[Н+]2 [Cl-] / ([H+}2[Cl-]+[H+]Ka1+Ka1 Ka2)
αHClO=[H+]Ka1 / (СН+}2[Cl-]+[H+]Ka1+Ka1 Ka2)
αClO-=Ka1 Ka2 / ([H+}2[Cl-]+[H+]Ka1+Ka1 Ka2)
Для результатов, выраженных в %, приведенные выше выражения должны быть умножены на 100. Вышеуказанные концентрации ионов ([Н+] и [С1-]) выражены в виде молярности.
Содержание свободного хлора может находиться в диапазоне от 20 до 400 мг/л (ч/млн), но предпочтительно находится в диапазоне от 20 до 200 мг/л (ч/млн) или от 20 до 140 мг/л (ч/млн). Также предпочтительно, чтобы диапазон содержания свободного хлора составлял от 40 до 100 ч/млн, поскольку это гарантирует характеристики продукта с точки зрения рН, ОВП, чистоты HClO и гипотоничности (низкое содержание хлоридов). Композиции настоящего изобретения всегда будут иметь кислый рН, будут гипотоническими и будут содержать хлорноватистую кислоту в качестве основного соединения свободного хлора. Кроме того, композиции могут быть определены любой из следующих характеристик, отдельно или в комбинации:
 содержание свободного хлора от 20 до 400 мг/л, от 20 до 200 мг/л, от 20 до 140 мг/л, от 40 до 100 мг/л, от 40 до 70 мг/л или от 70 до 100 мг/л;
содержание свободного хлора от 20 до 400 мг/л, от 20 до 200 мг/л, от 20 до 140 мг/л, от 40 до 100 мг/л, от 40 до 70 мг/л или от 70 до 100 мг/л;
 содержание хлоридов менее 500 мг/л, менее 400 мг/л, менее 300 мг/л или менее 200 мг/л и предпочтительно более 20 или 50 мг/л;
содержание хлоридов менее 500 мг/л, менее 400 мг/л, менее 300 мг/л или менее 200 мг/л и предпочтительно более 20 или 50 мг/л;
 концентрация ClO- менее 5 мг/л, 2 мг/л, 0,5 мг/л или 0,1 мг/л;
концентрация ClO- менее 5 мг/л, 2 мг/л, 0,5 мг/л или 0,1 мг/л;
 рН от 2 до 6, 5, 4 или 3, или от 2,5 до 6, 5, 4 или 3;
рН от 2 до 6, 5, 4 или 3, или от 2,5 до 6, 5, 4 или 3;
 окислительно-восстановительный потенциал (ОВП) от 850 до 1350 мВ или от 1000 до 1300 мВ; и/или
окислительно-восстановительный потенциал (ОВП) от 850 до 1350 мВ или от 1000 до 1300 мВ; и/или
 содержание свободного хлора подразумевает ≥90% HClO и ≤10% Cl2 или ≥95% HClO, ≤5% ClO- и ≤5% Cl2. Таким образом, в одном подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор, имеющий содержание свободного хлора более 20 мг/л. В альтернативном варианте осуществления содержание свободного хлора может находиться в диапазоне от 20 мг/л до 400 мг/л, от 20 мг/л до 250 мг/л или от 20 до 140 мг/л.
содержание свободного хлора подразумевает ≥90% HClO и ≤10% Cl2 или ≥95% HClO, ≤5% ClO- и ≤5% Cl2. Таким образом, в одном подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор, имеющий содержание свободного хлора более 20 мг/л. В альтернативном варианте осуществления содержание свободного хлора может находиться в диапазоне от 20 мг/л до 400 мг/л, от 20 мг/л до 250 мг/л или от 20 до 140 мг/л.
В другом подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор, имеющий содержание хлоридов менее 400 мг/л.
В еще одном подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор с рН от 2,5 до 6, имеющий содержание хлоридов менее 400 мг/л и содержание свободного хлора от 20 до 140 мг/л.
В еще одном подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор с рН от 2,5 до 6, имеющий содержание хлоридов менее 400 мг/л и содержание свободного хлора от 20 до 400 мг/л, причем свободный хлор предполагает ≥90% HClO и ≤10% Cl2, а концентрация ClO- составляет менее 5%.
В еще одном подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор с рН от 2,5 до 6, имеющий содержание хлоридов менее 400 мг/л, содержание свободного хлора от 20 до 400 мг/л и окислительно-восстановительный потенциал (ОВП) от 850 до 1350 мВ, причем свободный хлор предполагает ≥90% HClO и ≤10% Cl2, а концентрация ClO- составляет менее 5%.
В другом подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор, имеющий: (а) содержание хлоридов менее 200 мг/л; (b) рН от 2,5 до 3; (с) окислительно-восстановительный потенциал (ОВП) от 1000 до 1300 мВ; и (d) содержание свободного хлора от 40 до 100 мг/л, включая ≥95% HClO, ≤5% Cl2 и ≤2% или 0,5% ClO- или 0% ClO-.
В другом подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор, имеющий: рН от 2,5 до 4,5, содержание хлоридов ≤300 мг/л и окислительно-восстановительный потенциал (ОВП) от 850 до 1350 мВ.
В другом подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор, имеющий: (а) содержание хлоридов менее 250 мг/л; (b) рН от 2,5 до 4; (с) окислительно-восстановительный потенциал (ОВП) от 850 до 1350 мВ; и (d) содержание свободного хлора от 25 до 120 мг/л, включая ≥92,5% HClO, ≤7,5% Cl2 и ≤1% или 0% ClO-.
В другом подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор, имеющий: (а) содержание хлоридов менее 200 мг/л; (b) рН от 2,5 до 3; (с) окислительно-восстановительный потенциал (ОВП) от 1000 до 1300 мВ; и (d) содержание свободного хлора от 40 до 100 мг/л, включая ≥95% HClO, ≤5% Cl2 и ≤0,1% или 0% ClO-.
Раствор настоящего изобретения предпочтительно поставляется в распылительной бутыли, оснащенной распылительным насосом, который подает в любом случае от 100 до 500 микролитров на срабатывание, предпочтительно около 250 микролитров/срабатывание. В способе лечения раствор предпочтительно наносят два или три раза в сутки.
Таким образом, в еще одном подварианте осуществления фармацевтически приемлемая композиция представляет собой гипотонический водный раствор, наносимый путем распыления в количестве 250 микролитров на срабатывание из распылительного устройства насосного типа.
Способ нанесения / схема действия
В одном варианте осуществления раствор обладает функцией механической очистки. Таким образом, в одном конкретном варианте осуществления в способах осуществляют нанесение эффективного количества раствора на пораженную кожу, так чтобы он тек по пораженной коже и удалял биологические и инертные материалы.
Неожиданно было обнаружено, что эта очистка осуществляется без промывки кожи в традиционном смысле, как в случае с промывкой пораженной кожи проточной водой, сушкой пораженной кожи салфеткой или тканью или иным удалением посторонних материалов с пораженной кожи. Вместо этого, без ограничений, накладываемых какой-либо теорией, считается, что раствор действует совместно с кожей, выталкивая биологические и инертные материалы к поверхности кожи, где они не могут более препятствовать процессу заживления под поверхностью кожи.
Таким образом, в некоторых вариантах осуществления важно удерживать раствор на коже таким образом, чтобы раствор мог увлажнять кожу в течение периода времени, достаточного для стимуляции заживления и восстановления. Таким образом, в еще одном варианте осуществления способы изобретения дополнительно включают удержание на коже влажного слоя раствора в течение периода времени, эффективного для поддержания и стимулирования физиологического заживления. В других вариантах осуществления нанесение формирует влажный слой раствора на пораженной коже, дополнительно позволяющий раствору испаряться в условиях окружающей среды без механического вмешательства.
В другом подварианте осуществления композицию наносят на пораженную поверхность для местного нанесения путем распыления в количестве приблизительно 150-400 мкл, 200-300 мкл или 250 мкл на срабатывание из распылительного устройства насосного типа.
В еще одном подварианте осуществления композицию наносят на пораженную поверхность для местного нанесения путем распыления в количестве приблизительно 150-400 мкл, 200-300 мкл или 250 мкл на срабатывание из распылительного устройства насосного типа и оставляют высыхать на воздухе без физического вмешательства.
В другом подварианте осуществления композицию наносят на пораженную поверхность для местного нанесения путем распыления в количестве приблизительно 150-400 мкл, 200-300 мкл или 250 мкл на срабатывание из распылительного устройства насосного типа и оставляют высыхать на воздухе без физического вмешательства с последующим местным нанесением вторичного лечения.
В еще одном подварианте осуществления композицию вводят в виде назального спрея из распылительного устройства в объеме от 100 до 1000 мкл на введение, которое может включать в себя более одного срабатывания устройства.
В другом варианте осуществления способы настоящего изобретения включают местное нанесение раствора с обильным покрытием пораженной кожи, оставление раствора до высыхания и повторение нанесения. В предпочтительном варианте осуществления способы настоящего изобретения повторяют один или два раза в сутки.
В еще одном варианте осуществления способы настоящего изобретения дополнительно включают местное нанесение на пораженную кожу увлажняющего крема, лосьона, геля или мази.
ПРИМЕРЫ
В приведенных ниже примерах были приложены усилия для обеспечения точности чисел (например, количества, температуры и т.п.), но следует учитывать некоторые ошибки и отклонения. Приведенные ниже примеры составлены таким образом, чтобы специалистам в данной области была представлена полностью раскрытая информация и описание того, каким образом осуществляли и оценивали способы, приведенные в формуле настоящего изобретения, и они предназначены исключительно для иллюстрации настоящего изобретения и не ограничивают объем того, что авторы рассматривают как изобретение.
ПРИМЕР 1. ОПИСАНИЕ РАСТВОРОВ HCLO НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Продукт представляет собой гипотонический кислотный окислительный раствор, содержащий хлорноватистую кислоту (HClO), полученную в ходе процесса электролиза раствора хлорида натрия. Этот процесс дает гипотонический раствор, определенный с точки зрения (i) рН, (ii) окислительно-восстановительного потенциала (ОВП), (iii) соединений свободного хлора, (iv) чистоты HClO, имеющий свойства долговременной стабильности. Способы получения продукта описаны в WO/2008/131936 и WO/2007/048772, описание которых включено в настоящий документ путем ссылки.
Характеристики гипотонического кислотного окислительного раствора, содержащего хлорноватистую кислоту (HClO), приведены ниже в таблице 1:
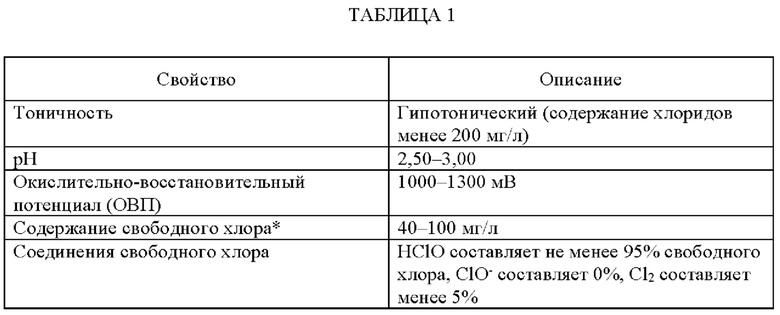
*Соединения свободного хлора представляют собой хлор (Cl2), гипохлорит (ClO-) и хлорноватистую кислоту (HClO).
В ТАБЛИЦЕ 2 приведены результаты испытаний для конкретных партий, соответствующих характеристикам, приведенным в ТАБЛИЦЕ 1.
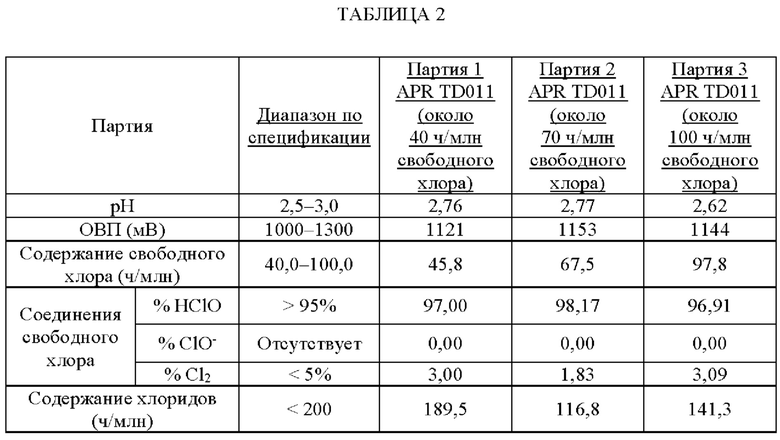
Гипотонический кислотный окислительный раствор, содержащий хлорноватистую кислоту (HClO), предложен в стеклянной бутылке из янтарного стекла, которая может быть оснащена распылительным насосом, который выдает приблизительно 100 или 250 мкл на срабатывание. ICH (Международная конференция по гармонизации). Оценка стабильности была проведена на нескольких партиях, и на основании полученных данных присвоен срок годности 24 месяца при хранении при температуре от 5°С до 25°С.
ПРИМЕР 2. ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
Подходящие инструкции по применению растворов настоящего изобретения, включая продукт из примера 1, приведены ниже.
Механизм действия
Влажный слой, остающийся на повреждении после нанесения, позволяет создавать идеальную микросреду для поддержания процесса физиологического заживления благодаря трем элементам раствора (высокочистая HClO, рН < 3,0 и ОВП > 1000 мВ).
Раствор содержит хлорноватистую кислоту (HClO), которая действует как антимикробный агент и консервант, ингибируя рост микроорганизмов в растворе, и предотвращая загрязнение путем оказания местного дополнительного антимикробного эффекта на поверхности повреждения.
HClO, характеризующаяся нейтральным зарядом, очень эффективно проникает в отрицательно заряженную бактериальную мембрану, где она оказывает антимикробное действие.
рН < 3,0 влияет на рост бактерий, создавая среду, неблагоприятную для роста бактерий. Кроме того, кислотная среда способствует оксигенации тканей из-за эффекта Бора и ингибированию проникновения в здоровые клетки аммиачных побочных продуктов катаболизма бактерий.
Высокий ОВП физически повреждает клеточную мембрану микроорганизмов, инактивируя их защитные механизмы.
Комбинация низкого рН и высокого ОВП играет роль в ингибировании матриксных металлопротеиназ (ММР). Повышенная активность ММР вызывает задержку заживления раны за счет разложения коллагенового матрикса, крайне важного для процесса заживления. Ингибирование активности ММР может способствовать перезапуску процесса физиологического заживления.
Указания по применению
Наносите раствор при возникновении проявлений. Раствор готов к применению, смешивание или разведение не требуется.
Нанесите раствор непосредственно на пораженную область:
- Откройте бутылку, отвинтив колпачок.
- Откройте пластиковый пакет-саше, содержащий распыляющий колпачок, отрезав верхнюю сторону.
- Извлеките распыляющий колпачок из пакета-саше, вытягивая его со стороны колпачка и стараясь не касаться трубки.
- Вставьте трубку в бутылку.
- Навинтите распылительный колпачок на горлышко бутылки
- Перед первым использованием продукта выполните распыление в воздух, активируя насос, пока не появится распыленный раствор.
- Наносите раствор непосредственно на поврежденную зону, распыляя его, чтобы обильно покрыть пораженную область, дайте раствору высохнуть и нанесите повторно.
- Наносите раствор один или два раза в день.
- Не отвинчивайте распылительный колпачок после его установки; не надевайте навинчиваемый колпачок на бутылку повторно, после установки распылительного колпачка.
- Закройте верхнюю крышку сразу после использования.
- Используйте устройство в течение 30 дней после первого вскрытия.
В случае нанесения препарата, когда пациент собирается использовать маскирующую или другую местную повязку, это следует делать только после высыхания продукта в течение по меньшей мере двух минут после его нанесения. Если пациенту необходимо побриться, это следует делать перед нанесением продукта.
ПРИМЕР 3. ОЦЕНКА ПРОТИВОВОСПАЛИТЕЛЬНЫХ СВОЙСТВ И РЕГЕНЕРАЦИИ ТКАНЕЙ ПРИМЕНИТЕЛЬНО КОНКРЕТНО К БУЛЛЕЗНОМУ ЭПИДЕРМОЛИЗУ
Влияние гипотонического кислотного окислительного раствора, содержащего хлорноватистую кислоту (НСЮ) (именуемого в данном описании как AR TD-011), соответствующего описанию в примере 1, оценивали на модели in vitro заживления раны FT-SKIN для определения механизма действия и оценки характеристик регенерации тканей на эпидермальном и дермальном уровнях после 4 часов и 24 часов лечения после повреждения с помощью транскрипционного исследования (qRT-PCR).
СПОСОБЫ
Тест-система
Экспериментальная модель заживления раны in vitro была разработана на основе «модели кожи на всю толщину» (FT-кожа) посредством индуцирования воспроизводимого механического повреждения, затрагивающего как эпидермальный, так и дермальный компартмент, и она имитирует различные фазы процесса заживления.
Модель кожи на всю толщину Phenion® изготовлена компанией Henkel ( , Германия, диаметр 1,3 см). В этой модели эпидермальные кератиноциты и дермальные фибробласты (полученные из биопсийного материала здоровых доноров) образуют в условиях культивирования многослойную кожу, которая напоминает кожу человека. Если коротко, фибробласты выращивают в специализированном стабильном матриксе, который не сокращается под действием тяговых усилий, создаваемых фибробластами. После формирования этого эквивалента дермы на нее накладывают кератиноциты, и в течение нескольких дней они образуют эпидермис с четко распознаваемыми слоями. Как эпидермис, так и дерма образуют физиологически функциональный модуль, и эпидермис, подобно коже человека, продуцирует различные маркеры дифференцировки (цитокератин 10, филаггрин, трансглутаминазу и инволюкрин). Эпидермально-дермальная граница характеризуется белками базальной мембраны (ламинин и коллаген IV). В дермальном компартменте был продемонстрирован синтез de novo эластина и фибронектина. Пролиферирующие клетки базального слоя идентифицированы по окрашиванию Ki-67. Модель полностью сформировалась после периода культивирования 5 недель.
, Германия, диаметр 1,3 см). В этой модели эпидермальные кератиноциты и дермальные фибробласты (полученные из биопсийного материала здоровых доноров) образуют в условиях культивирования многослойную кожу, которая напоминает кожу человека. Если коротко, фибробласты выращивают в специализированном стабильном матриксе, который не сокращается под действием тяговых усилий, создаваемых фибробластами. После формирования этого эквивалента дермы на нее накладывают кератиноциты, и в течение нескольких дней они образуют эпидермис с четко распознаваемыми слоями. Как эпидермис, так и дерма образуют физиологически функциональный модуль, и эпидермис, подобно коже человека, продуцирует различные маркеры дифференцировки (цитокератин 10, филаггрин, трансглутаминазу и инволюкрин). Эпидермально-дермальная граница характеризуется белками базальной мембраны (ламинин и коллаген IV). В дермальном компартменте был продемонстрирован синтез de novo эластина и фибронектина. Пролиферирующие клетки базального слоя идентифицированы по окрашиванию Ki-67. Модель полностью сформировалась после периода культивирования 5 недель.
Повреждение в этом эксперименте имитировали путем биопсийного прокола диаметром 2 мм. Формировали четыре симметричных повреждения, затрагивающих как дермальный, так и эпидермальный компартменты.
Испытуемые продукты наносили на каждую рану в общем объеме 50 мкл. ПНР в режиме реального времени
Извлечение РНК, ретротранскрипция кДНК и ПНР в режиме реального времени Для извлечения общей РНК из клеточных образцов использовали быструю безфенольную систему выделения РНК на основе фильтра. Для синтеза кДНК из РНК использовали набор для высокоэффективной обратной транскрипции кДНК. Для исследования экспрессии генов значимых биомаркеров использовали прибор Applied Biosystems 7500 для быстрой ПЦР в режиме реального времени с флуоресцентной химией ПЦР и выполняли анализ TaqMan.
Экспрессия генов представляет собой процесс, посредством которого наследственная информация в гене, таком как последовательность ДНК, преобразуется в функциональный продукт гена, такой как белок или РНК. Относительная количественная оценка определяет изменение экспрессии нуклеотидной последовательности в исследуемом образце относительно той же последовательности в калибровочном образце. В качестве эндогенного контрольного гена для нормализации входных количеств использовали GAPDH.
Каждую пробу исследовали в трех повторах. В 2х TaqMan Fast Universal PCR Master Mix добавляли анализ на экспрессию гена Taqman и кДНК (25 нг) в суммарном объеме 20 мкл. Стадии термообработки в ABI PRISM 7500 Fast: 95°С, 20 с; 40 циклов (95°С, 3 с + 60°С, 30 с).
Анализировали следующие гены.
Через 4 ч: NRF-2, НО-1, GPX, GSR, GST, KGF, TGFβ2, TGFβ3, Nf-kb, VEGF-C, PDGF Через 24 ч: IL-1α, TNF-α, Nf-kB, Nrf2, KGF eTGFβ2 eβ3, VEGF-C, PDGF Ранний момент времени позволяет оценить антиоксидантный механизм действия продуктов и раннюю фазу воспаления. Момент времени 24 ч позволяет оценить позднюю воспалительную фазу заживления раны с перекрывающейся реэпителизацией, пролиферативную фазу с учетом первого признака восстановления ткани, индуцирования экспрессии факторов роста, участвующих в пролиферации и стабилизации сосудов.
Для оценки восстановления после повреждения эффективность продукта сравнивают с поврежденной тканью. Оранжевые прямоугольники соответствуют значительной сверхэкспрессии генов, тогда как зеленые прямоугольники соответствуют значительному подавлению экспрессии генов относительно как отрицательного контроля (CN) (без повреждения и без лечения), так и контроля с повреждением, но без лечения (INJ). Сравнение приведено в двух столбцах в таблице 3. В частности, в таблице 3 представлены результаты ПЦР в реальном времени для APR TD011 (поврежденный образец и обработанный ADP TD011 образец). Все гены анализировали через 4 ч и через 24 ч после повреждения.
A) Калибровочный образец для всех образцов представляет собой отрицательный контроль (ткань без повреждений и лечения (CN)).
B) Калибровочный образец для всех образцов представляет собой контроль с повреждением (повреждение, но без лечения (INJ)).
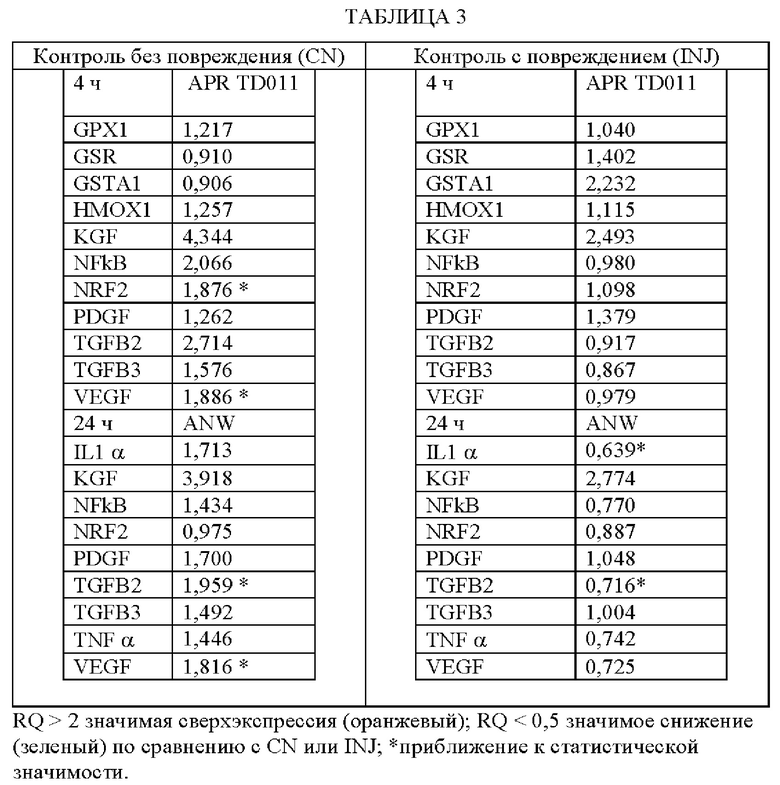
ОБСУЖДЕНИЕ РЕЗУЛЬ ТАГОВ
Противовоспалительные свойства
На основании полученных результатов можно сделать вывод о том, что на молекулярном уровне APR TD011 модулирует воспалительный ответ через 24 часа, и это основано на низкой экспрессии NF-kB и значительном снижении экспрессии IL-1 и TNF-α.
Через 4 часа APR TD011 демонстрировал повышение экспрессии GSR и GSTA1 по сравнению с контролем с повреждением, а также повышение экспрессии NRF2 относительно отрицательного контроля, и это подтверждает вывод о том, что APR TD011 модулирует воспалительный ответ ткани физиологическим способом без участия сигнализации TGFβ-2, которая, как известно, сдвигает ответ ткани в сторону келоидных рубцов.
Более низкая экспрессия NF-kB и значительное снижение экспрессии IL-1 α, TNF-α (по сравнению с поврежденной тканью) подтвердили противовоспалительную активность APR TD011, потенциально благоприятную для кожных ран у пациентов с ЕВ. Характеристики регенерации ткани
Три изоформы TGFβ, которые присутствуют у млекопитающих, демонстрируют сходную биологическую активность в большинстве анализов in vitro. Однако существуют различия в их активности in vivo и некоторых биологических активностях. Относительный баланс между TGFβ-1, TGFβ-2 и TGFβ-3 определяет результат процесса заживления раны: TGFβ-1 и TGFβ-2 участвуют в образовании кожных рубцов (фиброзный восстановительный ответ), a TGF β-3 участвует в предотвращении образования рубцов (регенеративный ответ).
TGF β-3 является наиболее распространенной изоформой TGFβ в гиперпролиферативном эпителии и, следовательно, может играть важную роль в пролиферации и дифференцировке кератиноцитов. Важно подчеркнуть, что в кислых условиях (рН < 3,8) этот белок, вероятно, не агрегирует: эта мономерная форма может сама по себе ускорять заживление раны и может быть использована для профилактики и/или лечения фиброзных расстройств.
На основании описанных ниже результатов можно сделать вывод, что на молекулярном уровне APR TD011 оказывает положительное влияние на регенерацию ткани при ЕВ через 4 часа и 24 часа, по следующим причинам:
(1) Значительное увеличение экспрессии KGF как через 4 часа, так и через 24 часа. Известно, что KGF играет важную роль в заживлении эпидермальных ран. Его продукция фибробластами повышается в присутствии интерлейкина-1. Присутствие KGF активирует пролиферацию кератиноцитов. Более сильное увеличение KGF приводит к развитию более толстого неоэпидермиса.
(2) Более низкий уровень экспрессии TGFβ-2 через 24 часа по сравнению с контролем с повреждением, что снижает риск образования келоидных рубцов (сигнализация TGFβ-2, как известно, сдвигает ответ ткани в сторону келоидных рубцов).
(3) Мономерные формы TGF-β3 способны стимулировать регенерацию эпителия в местах повреждения эпителия, увеличивая экспрессию гена KGF (по сравнению с отрицательным контролем), что указывает на реэпителиализирующее действие.
TGF-β3 преимущественно существует в двух основных формах:
 мономеры в растворе при низком рН; и
мономеры в растворе при низком рН; и
 крупные осаждающиеся агрегаты при физиологическом значении рН. Агрегация была выражена в диапазоне рН 4,3 < рН < 9,8 с максимальным значением при рН от 6,5 до 8,5. В кислых условиях, индуцированных APR TD011 (рН < 3,8), белок не агрегировался. APR TD011 с низким рН, по-видимому, сохраняет мономерную форму TGF-β3, которая может быть полезна для ускорения заживления ран и/или ингибирования рубцевания, для стимуляции регенерации эпителия и для профилактики и/или лечения фиброзных расстройств.
крупные осаждающиеся агрегаты при физиологическом значении рН. Агрегация была выражена в диапазоне рН 4,3 < рН < 9,8 с максимальным значением при рН от 6,5 до 8,5. В кислых условиях, индуцированных APR TD011 (рН < 3,8), белок не агрегировался. APR TD011 с низким рН, по-видимому, сохраняет мономерную форму TGF-β3, которая может быть полезна для ускорения заживления ран и/или ингибирования рубцевания, для стимуляции регенерации эпителия и для профилактики и/или лечения фиброзных расстройств.
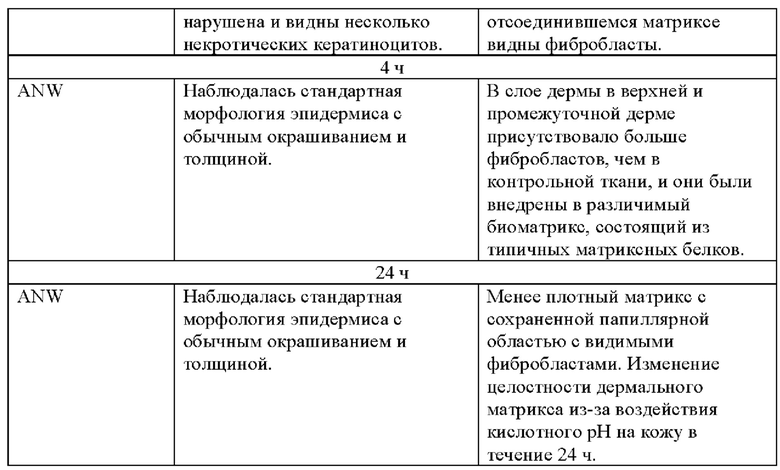
Как показано на ФИГ. 1 и обсуждается в таблице 4 ниже, гистологические анализы ткани через 4 часа и 24 часа подтвердили оптимальные характеристики регенерации ткани для APR TD011 («ANW»). После 4 часов лечения с помощью APR TD011 морфология ткани оказалась очень хорошо сохраненной по сравнению с поврежденной тканью с хорошо сохранившимся матриксом и более низким количеством мертвых клеток, что указывает на раннюю защиту/восстановление целостности ткани.

Два пациента с ЕВ и открытыми поражениями на коже из-за ЕВ получали лечение раствором, описанным в примере 1. Пациентам было предписано применять раствор в соответствии с примером 2. Через несколько недель лечения каждый из пациентов сообщил об улучшениях, на что указывало уменьшение размера хронической раны, улучшения в плане воспалительных признаков вокруг повреждения (указание на начало процесса физиологического заживления) и снижение уровня зуда, и это все является ценными аспектами с точки зрения пациента.
На ФИГ. 2 показаны результаты лечения 24-летнего пациента с тяжелой генерализованной RDEB. На ФИГ. 2(A) представлено сравнение раны на грудной клетке на неделе 0 (А-1; воспаление и шелушение, трещины, экссудат вокруг повреждения) и на неделе 6 (А-2; рана более чистая, меньшего размера, более поверхностная с минимальными признаками воспаления вокруг повреждения). На ФИГ. 2(B) представлено изображение раны на правой лопатке, демонстрирующее уменьшение размера в течение 2 недель и меньшее шелушение вокруг повреждения. На ФИГ. 2(C) показаны воспалительные признаки в левой подмышке, включая уменьшение покраснения, корок и шелушения в период между неделей 0 (С-1) и неделей 8 (С-2).
На ФИГ. 3 представлена фотография нижней части ноги с двухлетней хронической раной у пациента с JEB, получавшего лечение продуктом. На Фото 3(A) показано, что рана все еще не разрешилась после нескольких различных видов лечения. На Фото 3(B) показано сильное улучшение раны после 4 недель лечения.
ПРИМЕР 4. ОЦЕНКА ПРОДУКТА И ЕГО СПОСОБНОСТИ К ЛЕЧЕНИЮ ИНДУЦИРОВАННЫХ ИНГИБИТОРАМИ EGFR КОЖНЫХ ТОКСИЧЕСКИХ ЭФФЕКТОВ
Оценивали влияние гипотонического кислотного окислительного водного раствора, содержащего хлорноватистую кислоту (HClO) (именуемого в данном описании APR ТМ-011), соответствующего описанию в примере 1, в клиническом исследовании на пациентах на фоне лечения цетуксимабом.
СПОСОБЫ
Собирали доказательства у пациентов, получавших лечение на основе цетуксимаба. Каждый пациент выполнил 3 амбулаторных посещения в течение 3 месяцев, организованных следующим образом:
- начальный визит;
- промежуточный визит;
- заключительный визит.
Промежуточный визит запланировали с интервалом от начального и заключительного визита в 15/30 дней в зависимости от состояния здоровья пациента. Форму оценки врач заполнял во время первого визита и обновлял по двум последующим визитам. В момент первого визита пациенту было назначено ежедневное лечение в соответствии со следующей схемой:
- утро: увлажнение базовым кремом;
- полдень: опрыскивания гипотоническим кислотным раствором, содержащим хлорноватистую кислоту, лица, грудной клетки и спины;
- вечер: увлажнение базовым кремом.
Форма клинической оценки была разделена на 9 пунктов: предшествующее лечение, лечение гипотоническим кислотным раствором, содержащим хлорноватистую кислоту, домашнее лечение, вспомогательное лечение, тип раны, оценка повреждения (ширина и длина в сантиметрах), область кожи вокруг повреждения, оценка качества жизни и приостановка оценки.
Клинический внешний вид области кожи вокруг повреждения оценивали по статусу эритемы, мацерации, ксероза, жжения, раздражения и воспаления, при этом указывали степень тяжести: легкая, умеренная или тяжелая. Характеристики и изменения раневого ложа определяли с помощью модифицированной оценки раневого ложа (WBS). Были исследованы следующие параметры: активный край, черный струп, глубина грануляции/ткани, количество экссудата, величина отека, область кожи вокруг повреждения, кожная токсичность/экзема, мозоли/фиброз, розовое раневое ложе, продолжительность существования язвы до текущего лечения. Каждому параметру была присвоена балльная оценка в диапазоне от 0 до 2. Сумма всех показателей определяет общий балл, который может принимать значение от 0 (минимального или худшего показателя) до 18 (максимального или наилучшего показателя).
Качество жизни оценивали по опроснику QoL-EQ 5D. Исследовали следующие общие сферы состояния здоровья: мобильность, уход за собой, повседневная деятельность, дискомфорт/боль, тревожность и депрессия. Состояние по каждой из вышеупомянутых сфер может быть охарактеризовано одним из следующих показателей: без проблем, некоторые проблемы или значительные проблемы.
Наконец, восприятие пациентом текущего состояния измеряли с использованием числовой шкалы с диапазоном значений от 0 (соответствует плохому состоянию здоровья) до 100 (лучшее состояние здоровья). Безопасность лечения оценивали на основании наличия или отсутствия таких проявлений, как: непереносимость, инфекция раны или нежелательное явление. Методика получения ответов: возможность выбора нескольких вариантов для 7 пунктов и открытый ответ для 2 пунктов.
РЕЗУЛЬТАТЫ
Исследование проводили на 15 пациентах, 10 мужчин и 5 женщин, со средним возрастом 60 лет, у которых после первого химиотерапевтического лечения наблюдались угреподобные повреждения от цетуксимаба.
Повреждения были расположены на груди, плечах и лице. В начале лечения:
ОЦЕНКА ПОВРЕЖДЕНИЯ - измеренные повреждения имели разные размеры. Ширину и длину измеряли в сантиметрах. У 15 пациентов измеренные значения ширины находились в диапазоне от 5 см до 22 см, в то время как длина находилась в диапазоне от 10 см до 40 см. Пациент с наименьшей поврежденной зоной имел размер повреждения 5 см × 10 см, в то время как пациент с наибольшей поврежденной зоной имел размер повреждения 22 см × 40 см.
ОБЛАСТЬ КОЖИ ВОКРУГ ПОВРЕЖДЕНИЯ - у всех пациентов область кожи вокруг повреждения была преимущественно раздраженной и воспаленной. Зуд был умеренным у 60% пациентов и слабым у 40%. Умеренное воспаление присутствовало у 60% пациентов; легкое воспаление присутствовало у 40%. У 6,7% пациентов на коже присутствовало легкое жжение.
БАЛЛ WBS (модифицированной) - у 40% пациентов суммарный балл WBS составлял 14; у 33,3% пациентов суммарный балл WBS составлял 15; и у 26,7% пациентов суммарный балл WBS составлял 16.
КАЧЕСТВО ЖИЗНИ - качество жизни оценивали по опроснику QoL-EQ 5D. Значительными проблемами были дискомфорт/боль у 46,7% пациентов, тогда как 33,3% пациентов сообщили о трудностях при ведении повседневной деятельности.
Все пациенты сообщили о некоторой тревожности и депрессии. 86,7% испытывали некоторые сложности в уходе за собой, 46,7% - в повседневной деятельности и 20% испытывали состояние дискомфорта и боли.
Ни один из пациентов не испытывал проблем с мобильностью. Кроме того, не было отмечено никаких проблем с дискомфортом и болью у 33,3% пациентов, с повседневной деятельностью у 20% и с уходом за собой у 13,3%.
Оценка состояния на текущий день из суммарных 100 баллов составляла 40 баллов у 20% пациентов, и по 50 и 60 соответственно у 40% пациентов.
В конце лечения:
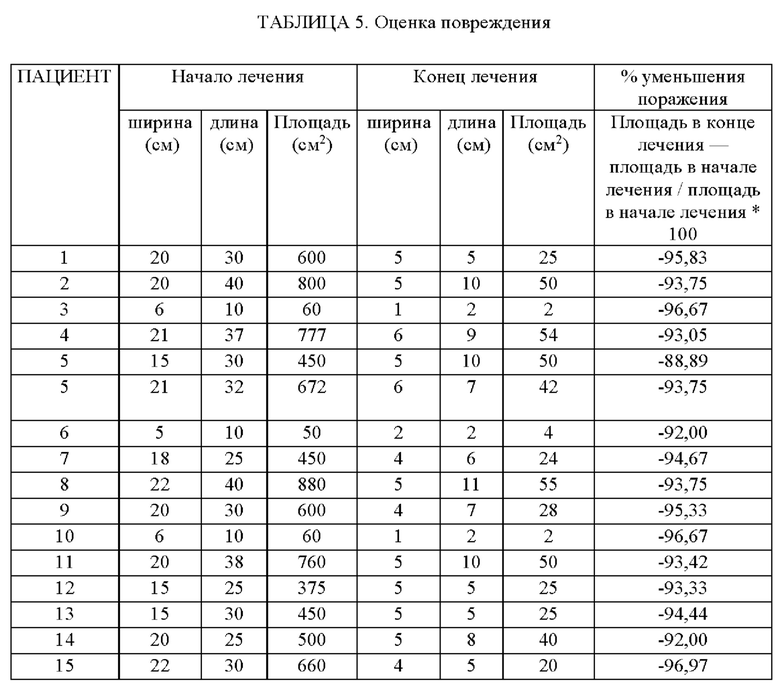
ОЦЕНКА ПОВРЕЖДЕНИЯ - у всех пациентов была обнаружено уменьшение площади повреждения: у 93,3% пациентов наблюдалось уменьшение площади на более чем 90%, и у 1 пациента наблюдалось уменьшение на 88,9% (ТАБЛИЦА 5).
ОБЛАСТЬ КОЖИ ВОКРУГ ПОВРЕЖДЕНИЯ ни один пациент не сообщил о патологических проявлениях симптомов в области кожи вокруг повреждения.
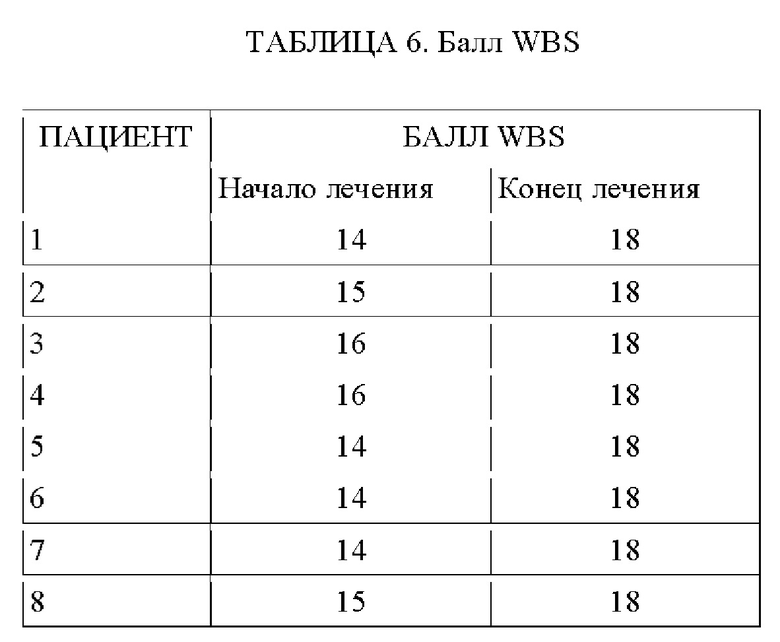
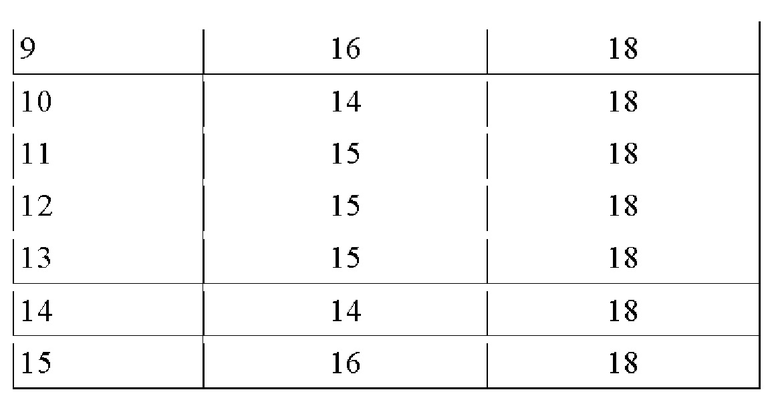
БАЛЛ WBS (модифицированной)- балл WBS у всех пациентов составил 18 (ТАБЛИЦА 6).
КАЧЕСТВО ЖИЗНИ - все пациенты отмечали, что они не страдают от каких-либо проблем, за исключением тревожности и депрессии (ТАБЛИЦА 7).
Для всех пациентов оценка состояния на текущий день в конце лечения составляла 80. Кроме того, все пациенты смогли пройти лечение гипотоническим кислотным раствором, содержащим хлорноватистую кислоту, без каких-либо проявлений непереносимости.
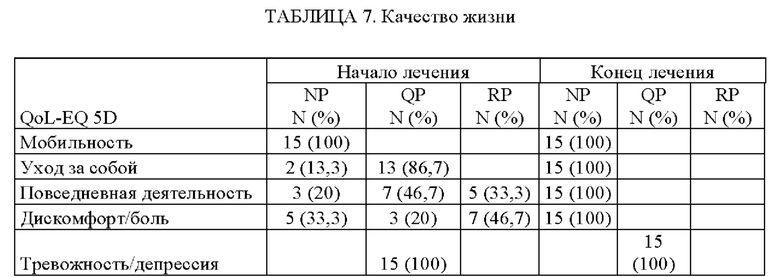
NP: БЕЗ ПРОБЛЕМ; QP: НЕКОТОРЫЕ ПРОБЛЕМЫ; RP: ЗНАЧИТЕЛЬНЫЕ ПРОБЛЕМЫ. ВЫВОДЫ
Нанесение гипотонического окислительного кислотного раствора, содержащего хлорноватистую кислоту, на вызванные цетуксимабом кожные повреждения улучшает ответ пациента на химиотерапевтическое лечение. У повреждений наблюдается прогрессирующее улучшение не только по размеру, но и по характеристикам, и по сопутствующей симптоматике: повреждение остается ограниченным и уменьшается в размере; Область кожи вокруг повреждения остается интактной, и также уменьшается частота явлений раздражения и воспаления.
Также очевидно, что, помимо тревожности и депрессии, связанных с основным состоянием заболевания, контролируемость и переносимость ситуации с кожей, не обостряющей проблемы с восприятием образа собственного тела, трансформируются в улучшение качества жизни на социальном уровне. В конце лечения параметры, обозначающие «состояние здоровья на текущий день», составляли 80/100 для всех пациентов. Полученные хорошие результаты подтверждают тот факт, что продукт должен быть использован в самом начале кожных проявлений, которые обычно возникают на первом-втором цикле противораковой терапии.
ПРИМЕР 5. ОЦЕНКА АНТИОКСИДАНТНЫХ СВОЙСТВ И РЕГЕНЕРАЦИИ ТКАНЕЙ ПРИМЕНИТЕЛЬНО КОНКРЕТНО К БОЛЕЗНИ ХЕЙЛИ ХЕЙЛИ
Влияние гипотонического кислотного окислительного водного раствора, содержащего хлорноватистую кислоту (HClO) (именуемого в данном описании APR TD-012), соответствующего описанию в примере 1, оценивали на модели in vitro для лучшего понимания молекулярных путей, модулируемых с помощью APR TD-012 при HHD: кератиноцитарную клеточную линию НаСаТ трансфицировали короткими интерферирующими РНК (киРНК), валидированными для человеческого АТР2С1, с получением нокдауна экспрессии гена, как это происходит у пациентов с HHD (именуются клетками siATP2C1).
СПОСОБЫ
Клеточная культура
Кератиноцитарную клеточную линию НаСаТ выращивали в среде DMEM с 10% эмбриональной бычьей сыворотки (FBS), 5% L-глутамина, 2% пенициллина и стрептомицина при 37°С с 5% CO2.
Культивирование клеток и трансфекция
Клетки НаСаТ (конфлюэнтность 70-80%) культивировали в модифицированной среде с низким содержанием кальция и трансфицировали с использованием реагента для трансфекции Lipofectamine RNAiMAX в соответствии с инструкциями производителя (Thermo Fisher Scientific, штат Массачусетс, США), используя 100 нмоль л-1 коротких интерферирующих РНК (киРНК), валидированных для человеческого АТР2С1 (L-006119-00; Thermo Scientific/Dharmacon, Lafayette, штат Колорадо, США), и соответствующие контрольные скремблированные киРНК. Анализ жизнеспособности клеток
Клетки НаСаТ (siCTR и siATP2C1) культивировали в покрытой коллагеном чашке и использовали для анализа [3H]тимидина на втором пассаже. Клетки трансфицировали в течение 24 ч с использованием 100 нм либо siATP2C1, либо si-CTR (Ambion) с помощью реагента RNAiMAX (Invitrogen) и обрабатывали 100 мкмоль APR-TD012. В качестве контрольных образцов использовали клетки, обработанные теми же объемами несущей среды (Н20). Жизнеспособность клеток анализировали с использованием основанного на MTS анализа CellTiter 96® AQueous One Solution Cell Proliferation Assay (G3580; Promega, Madison, штат Висконсин, США). Значения поглощения измеряли при 490 нм с использованием системы GloMax Multidetection System (Promega). Измерения проводили в трех технических повторах, и на фигурах показаны средние значения ± SEM для по меньшей мере 2 биологических повторов. Анализ методом Вестерн-блоттинга
Клетки лизировали в Tris НС1 20 ммоль рН 7,5, NaCl 150 ммоль, EDTA 1 ммоль рН 8, Triton 1%, NaF 30 ммоль, Na3V04 1 ммоль, PMFS 1 ммоль и ингибиторах протеаз (Cocktail-Roche); образцы центрифугировали при 13000 об/мин в течение 15 мин и собирали супернатант. Количественное определение проводили с помощью анализа Брэдфорда (Bio-Rad). Лизаты денатурировали при 95°С и разделяли методом ДСН-ПААГ электрофореза на 8%-м акриламидном геле. После переноса на мембрану ПВДФ белки подвергали иммуноблоттингу с использованием стандартных процедур. Следующие реагенты приобретали у компании Santa Cruz Biotechnology, Santa Cruz, штат Калифорния, США: тубулин. NRF2 (Abcam, г. Кембридж, Великобритания). Анализ РНК и полимеразная цепная реакция с обратной транскриптазой
Общую РНК выделяли из клеток в гуанидинизотиоцианате (реагент Trizol, Thermo Fisher Scientific, штат Массачусетс, США) и дополнительно обрабатывали с помощью полимеразной цепной реакции с обратной транскриптазой (RT-PCR). Каждый образец анализировали методом кПЦР-РВ в трех повторах и в по меньшей мере двух независимых экспериментах. кПЦР-РВ проводили при подходящей температуре отжига, используя указанные ниже праймеры, с помощью набора SensiFAST SyBr Hi-ROX (Biolin, Великобритания) или со специфическими праймерами/зондом TaqMan MGB с использованием анализа экспрессии гена Taqman (Thermo Fisher Scientific, штат Массачусетс, США).
Статистический анализ
Каждый эксперимент повторяли независимо по меньшей мере два раза. Все результаты выражали как средние значения со стандартным отклонением и значимыми считали данные при Р < 0,05. Для определения статистической значимости использовали однофакторный дисперсионный анализ (ANOVA) для независимых образцов.
РЕЗУЛЬТАТЫ
Обработка клеток siATP2C1 APR TD012 показала, что APR TD012 способен восстанавливать экспрессию фактора Nrf2 транскрипции, который играет ключевую роль в ответе на окислительный стресс (Kensler et al., 2007; Moi et al., 1994; Zhang, 2006); APR TD012 способен модулировать цитокины TGF-beta 1 и 2 различными способами; и APR TD012 способен восстанавливать пролиферативный потенциал кератиноцитов siATP2C1. В совокупности эти результаты указывают на то, что APR TD012 может действовать непосредственно на кератиноциты, обращая вспять некоторые аномалии, наблюдаемые в кератиноцитах siATP2C1, которые являются моделью патологии. Экспрессия белка Nrf2
Ранее было отмечено, что экспрессия NRF2 снижена в кератиноцитах siATP2C1 (Cialfi et al, 2016). Это явление может играть важную роль в развитии HHD, поскольку утрата АТР2С1 запускает механизм, который приводит к ингибированию ответа на повреждение ДНК. Повышение уровней ROS в результате уменьшения экспрессии NFR2 доводит повреждение ДНК до порогового значения, которое кератиноциты уже не могут исправить, и это может способствовать появлению повреждений. В этой модели in vitro уровни экспрессии белка Nrf2 в клетках siATP2C1, обработанных APR TD012 были значительно выше, чем в клетках siATP2C1, обработанных несущей средой (ФИГ. 4). Эти данные свидетельствуют о том, что APR TD012 способствует антиоксидантному ответу за счет активации пути Nrf2. Клетки НаСаТ кератиноцитарной клеточной линии трансфицировали либо siRNA-CTR, либо siRNA АТР2С1 и через 24 часа обрабатывали либо APR TD012, либо H2O в течение еще 24 часов. Денситометрический анализ экспрессии NRF2 в клетках НаСаТ. Показаны средние значения ± стандартная ошибка для 2 независимых экспериментов. Уровни мРНК TGFB2 и TGFB1
Повреждения при HHD характеризуются нерегулируемой экспрессией цитокинов и снижением репарационных свойств (Cialfi et al, 2016). Были проанализированы уровни экспрессии цитокинов TGFB1 и TGFB2, которые изменяются в дефектных по АТР2С1 кератиноцитах. В клетках siATP2Cl уровни мРНК TGFB2 и TGFB1 были значительно выше, чем у контрольных клеток siCTR. На ФИГ. 5 показано воздействие раствора APR TD012 на цитокины в дефектных по АТР2С1 кератиноцитах. TGFB-1 и TGFB-2 количественно определяли методом кПЦР-РВ. Данные выражены как среднее ± СО для двух независимых экспериментов, проведенных в трех повторах.
Наблюдали значительное различие в уровнях TGFB1 и TGFB2 между клетками, обработанными несущей средой, и клетками, обработанными APR TD012. В частности, экспрессия TGFB1 была более высокой в клетках siATP2C1 по сравнению с клетками siCTR. В клетках siATP2C1, обработанных APR TD012, наблюдали значительное повышение экспрессии TGBF1.
Уровни цитокина TGFB2 были значительно выше в клетках, обработанных siATP2C1, чем в контрольных клетках. Наблюдали снижение экспрессии TGFB2 в клетках siATP2C1, обработанных APR TD012. Эти данные свидетельствуют о том, что APR TD012 может влиять на профиль ряда цитокинов в HHD-кератиноцитах. Пролиферация клеток НаСаТ, обработанных siATP2C1
Ранее было продемонстрировано, что клетки siATP2C1 имеют сниженную пролиферацию по сравнению с клетками, обработанными siCTR, и это также подтверждено в данном эксперименте. Обработка клеток siATP2C1 APR TD012 позволила устранить аномалию пролиферации клеток НаСаТ, обработанных siATP2C1. На ФИГ. 6 показан анализ скорости пролиферации клеток, обработанных APR TD012. Клетки НаСаТ кератиноцитарной клеточной линии трансфицировали либо siRNA-CTR, либо siRNA-ATP2C1 и через 24 часа обрабатывали либо APR TD012, либо Н2O в течение еще 24 часов. Количество клеток анализировали с помощью анализа MTS через 48 часов после трансфекции. Показаны средние значения ± стандартная ошибка для 2 независимых экспериментов в трех повторах.
ПРИМЕР 6. ТЕСТИРОВАНИЕ НА АКТИВНОСТЬ MYCOBACTERIUM ULCERANS ПРИМЕНИТЕЛЬНО К ЯЗВАМ БУРУЛИ
Влияние гипотонического кислотного окислительного водного раствора, содержащего хлорноватистую кислоту (HClO) при двух различных концентрациях (именуется в данном описании APR TD-013), соответствующего описанию в примере 1, оценивали на модели in vitro для проверки активности против Mycobacterium ulcerans - активных бактерий, участвующих в патогенезе язв Бурули. Исследование метаболической активности
На первой стадии провели адаптацию резазуриновой пробы для анализа того, обладают ли исследуемые растворы (один с 40-70 ч/млн содержания свободного хлора именуется раствором 1, и второй с 70-100 ч/млн содержания свободного хлора именуется раствором 2) активностью против М. ulcerans, которые резистентны ко множеству противомикробных препаратов. Культивируемые бактерии (свежевыделенный африканский эталонный штамм S1013; оптическая плотность 0,3; логарифмическая фаза) подвергали воздействию исследуемых растворов. 0,1 мл бактериальной культуры смешивали с 1,9 мл исследуемого раствора и инкубировали в течение различных периодов времени. Смеси сразу же встряхивали, и пробирки оставляли стоять в течение 1 мин, 4 мин, 9 мин, 19 мин или 29 мин. После истечения указанного времени бактерии осаждали центрифугированием (13 300 х g в течение 1 мин) и удаляли супернатант. Осадок немедленно ресуспендировали в 0,2 мл среды 7Н9. Эту суспензию использовали в качестве инокулята для резазуриновой пробы.
Для анализа метаболической активности в бактериальную суспензию добавляли 20 мкл резазурина и инкубировали в течение 72 ч при 30°С. Измеряли флуоресценцию и рассчитывали метаболическую активность с использованием включенных контролей. Все описанные выше процессы выполняли в двух повторах, и результаты, представленные ниже, представляют собой среднее значение для обоих повторов. 2-минутное воздействие обоих исследуемых растворов приводило к >90% снижению метаболической активности по сравнению с необработанным контролем. В данном анализе не наблюдалось заметного различия между активностью этих двух исследуемых растворов в отношении М. ulcerans. Вычисленные метаболические активности подвергнутых воздействию бактерий показаны на ФИГ. 7.
Исследование бактерицидной активности
На следующей стадии исследовали бактерицидную активность растворов 1 и 2 путем определения количества колониеобразующих единиц (КОЕ) в анализе с посевом. Культивируемые бактерии (свежевыделенный африканский эталонный штамм S1013; оптическая плотность 0,3; логарифмическая фаза) подвергали воздействию двух исследуемых растворов, соответствующих описаниям в примере 1. 0,1 мл бактериальной культуры смешивали с 1,9 мл исследуемого раствора и инкубировали в течение 1 мин, 4 мин и 9 мин. После истечения указанного времени бактерии осаждали центрифугированием (13 300 х g в течение 1 мин) и удаляли супернатант.Осадок немедленно ресуспендировали в 0,2 мл среды 7Н9. Эту суспензию использовали в качестве инокулята для определения количества КОЕ в двух повторах. Готовили десятикратные последовательные разведения каждой суспензии (от 10-1 до 10-3) в среде 7Н9. Каждое разведение сеяли на планшеты с агаром 7Н9 (100 мкл на планшет). Все планшеты герметизировали и инкубировали при 30°С в течение до 12 недель.
Результаты, представленные на ФИГ. 8, представляют собой средние значения КОЕ для каждого разведения. После 2 минут воздействия 2 продуктов количество КОЕ снижалось на >80%. После 10 минут было уничтожено >99% бактерий в случае раствора 1 (40-70 ч/млн соединений свободного хлора) и >99,9 бактерий в случае раствора 2 (70-100 ч/млн соединений свободного хлора).
ПРИМЕР 7. ИССЛЕДОВАНИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТИ IN VIVO В ОТНОШЕНИИ COVID-19
Влияние гипотонического кислотного окислительного водного раствора, содержащего хлорноватистую кислоту (НСЮ), соответствующего описанию в примере 1, оценивали в исследовании in vitro для определения переносимости и эффективности назального введения продукта против SARS-Cov-3.
СПОСОБЫ
Вирус, среда и клетки
Маточные растворы вируса SARS-CoV-2 получали путем выращивания вируса в клетках Vero 76. В качестве среды для исследования использовали MEM с добавлением 2% FBS и 50 мкг/мл гентамицина. Анализ вирицидной активности
Гипотонический кислотный окислительный раствор, соответствующий описанию в примере 1, исследовали в полной концентрации, добавляя 90% образца к 10% раствора вируса по объему с получением конечной концентрации 90%. Исходный материал вируса SARS-CV-2 добавляли в три пробирки, и среду добавляли только в одну пробирку с каждой полученной концентрацией для использования в качестве контроля токсичности. Параллельно исследовали этанол в качестве положительного контроля и только воду в качестве вирусного контроля.
Соединение и вирус инкубировали при комнатной температуре в течение двух периодов контакта <1 минуты и 3 минуты. После периода контакта растворы нейтрализовали путем разведения 1/10 в исследуемой среде, содержащей 10%FBS. Количественное определение вируса
Нейтрализованные образцы объединяли для количественного определения среднего значения для трех повторов исследования. Образцы последовательно разбавляли с использованием восьми полулогарифмических разведений в исследуемой среде. Каждое разведение добавляли к 4 лункам 96-луночного планшета с клетками Vero 76 с конфлюентностью 80-100%. Контроли токсичности добавляли в дополнительные 4 лунки, и 2 из этих лунок были инфицированы вирусом, чтобы выступить в качестве контролен нейтрализации, и это гарантирует, что оставшийся образец в анализе титра не ингибирует рост и позволяет обнаружить выживший вирус. Все планшеты инкубировали при 37±2°С, 5%CO2.
На день 6 после инфицирования планшеты оценивали на наличие или отсутствие вирусного цитопатического эффекта (СРЕ). Для определения конечных точек титрования образцов использовали метод Рида и Менча (50%-я заражающая доза для клеточной культуры, CCID50) и рассчитывали логарифмическую величину уменьшения (LRV) для соединения по сравнению с отрицательным контролем (водой). Контроли
Вирусные контроли исследовали в воде и вычисляли уменьшение количества вирусов в исследуемых лунках по сравнению с вирусными контролями в виде логарифмической величины уменьшения (LRV). Контроли токсичности исследовали в среде, не содержащей вируса, чтобы понять, не являются ли образцы токсичными для клеток. Контроли нейтрализации исследовали для проверки того, что инактивация вируса не продолжается после указанного времени контакта и что остаточный образец на титровальных планшетах не ингибирует рост и обнаружение выжившего вируса. Для этого образцы на токсичность добавляли на титровальные планшеты для исследования и затем добавляли в каждую лунку небольшое количество вируса, которое было способно обеспечить обнаруживаемое значение СРЕ в течение периода инкубации.
РЕЗУЛЬТАТЫ
Вирусные титры и значения LRV для гипотонического кислотного окислительного раствора, содержащего хлорноватистую кислоту (HClO), применительно к SARS-CoV-2, показаны в таблице 8.
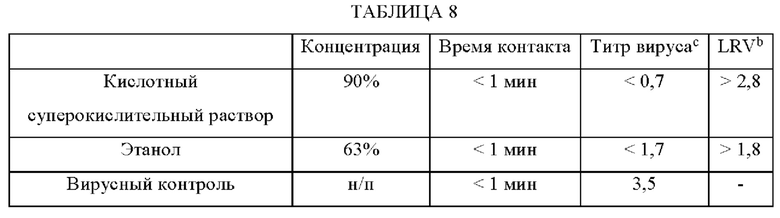
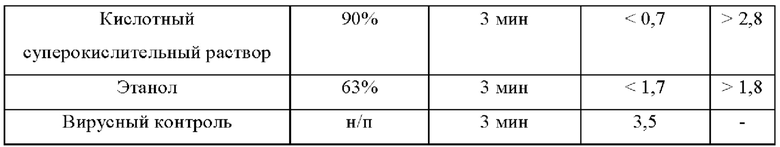
aLog10 CCID50 вируса на 0,1 мл
bLRV (логарифмическая величина уменьшения) представляет собой уменьшение количества вируса по сравнению с вирусным контролем
Вирицидная активность была продемонстрирована при исследовании раствора с концентрацией 90% в течение <1 минуты и 3 минут с уменьшением количества вируса с 3,5 log CCID50 на 0,1 мл в вирусном контроле до значения ниже предела обнаружения 0,7 log (>99,8%). Можно провести дополнительные исследования для оценки воспроизводимости и, возможно, активности при более низких концентрациях.
Контроли нейтрализации показали, что остаточный образец не ингибировал рост и обнаружение вируса в анализах конечной точки титрования в лунках, не обладавших цитотоксичностью. Положительные контроли работали так, как ожидалось, хотя этанол был токсичен для клеток в разведении 1/10, что ограничивало обнаружение вируса величиной <1,7 log CCID50 на 0,1 мл.
ПРИМЕР 7. ИССЛЕДОВАНИЕ РАЗДРАЖЕНИЯ НОСА
Цель данного исследования раздражения носа заключалась в оценке возможного потенциала раздражения гипотоническим окислительным раствором, содержащим хлорноватистую кислоту, при введении исследуемых соединений испытуемым новозеландским белым кроликам дважды в сутки в течение пяти последовательных дней.
СХЕМА ИССЛЕДОВАНИЯ
Исследуемый продукт вводили интраназально в дозе 200 мкл/ноздря и 500 мкл/ноздря с использованием шприца 1 мл, оснащенного распылительным устройством для слизистой MAD® (Mucosal Atomization Device), в каждую ноздрю два раза в день с 4-часовыми интервалами в течение 5 последовательных дней. Кроме того, животным контрольной группы вводили физиологический раствор (500 мкл/ноздря).
СПОСОБЫ
За кроликами вели наблюдение в плане общих клинических признаков, заболеваемости и смертности по два раза в сутки в дни введения, до введения дозы (перед первым введением) и после введения дозы (после последнего введения), и по одному разу в дни, когда введение не проводилось. Локальные реакции в месте применения исследовали два раза в день во все дни введения, т.е. перед первым введением и после последнего введения в каждый день введения (приблизительно через 30 минут после введения) и один раз в день в дни, когда введение не проводилось. Местную реакцию визуально наблюдали с помощью ручки-фонарика. Местные реакции оценивали в соответствии с методом Дрейза (1959). Всех животных умерщвляли через 24 часа последнего введения (день 6) и подвергали детальному макропатологическому исследованию. У животных тщательно исследовали внешние аномалии. Места введения (ноздри) всех животных вместе с окружающими тканями исследовали макроскопически. Вскрывали грудные и брюшные полости и проводили тщательное обследование органов для обнаружения аномалий. У всех животных проводили гистопатологическое исследование носа. Проводили микроскопическое исследование носа на 4 уровнях поперечных сечений (место введения). Ткани обрабатывали для типового заключения в парафин и 5-микронные срезы окрашивали гематоксилином и эозином. Срезы ткани оценивали, регистрировали балльную оценку в соответствии с методом В.3 стандарта ISO-10993-10 и рассчитывали индекс раздражения в соответствии с методом В.4 стандарта ISO-10993-10.
РЕЗУЛЬТАТЫ
Не было выявлено клинических признаков преждевременной гибели, а также влияния на массу тела. Во время макроскопического исследования в месте применения не наблюдалось местной реакции. Приблизительно через 24 часа после последнего введения всех животных умерщвляли и собирали слизистую полости носа с нижнего края нижней носовой раковины и с носовой перегородки у всех животных, регистрировали макроскопические наблюдения и выполняли подготовку к гистопатологии. Ни у одного исследованного животного при вскрытии не было обнаружено макроскопических поражений. Микроскопическая оценка слизистой оболочки носа согласно методам В.3 и В.4 стандарта ISO-10993-10 показала индекс раздражения от 0 до 0,083 в группах доз 200 мкл/ноздря и 500 мкл/ноздря соответственно (ТАБЛИЦА 9).
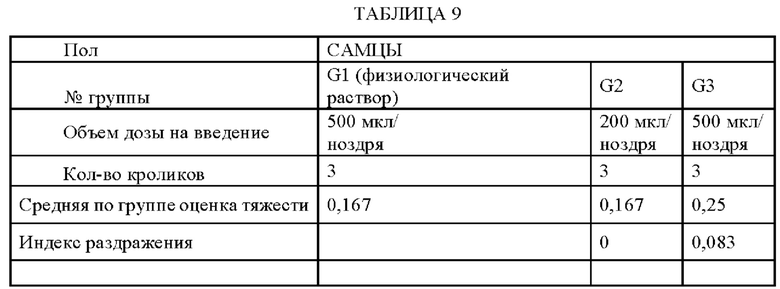
Индекс раздражения: 0 - отсутствует; 1-4 - минимальное; 5-8 - слабое; 9-11 - умеренное; 12-16 - тяжелое.
ВЫВОД
Исходя из приведенных выше результатов сделан вывод, что введение два раза в сутки гипотонического кислотного окислительного раствора, содержащего хлорноватистую кислоту, новозеландским белым кроликам в дозах 200 мкл/ноздря и 500 мкл/ноздря является «нераздражающим» для слизистой носа новозеландских белых кроликов.
В настоящей заявке приводятся ссылки на различные публикации. Описания этих публикаций полностью включены в настоящую заявку путем ссылки для более подробного описания уровня техники, к которой относится настоящее изобретение. Специалистам в данной области должно быть очевидно, что в рамках настоящего изобретения можно создавать различные модификации и вариации без отступления от объема или сущности изобретения. Из рассмотрения описания и практического применения изобретения, описанного в документе, специалистам в данной области будут очевидны другие варианты осуществления изобретения. Подразумевается, что все описания и примеры представлены только в качестве иллюстрации и находятся в пределах сущности и объема изобретения, что отражено в приведенной ниже формуле изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ВРОЖДЕННЫМ БУЛЛЕЗНЫМ ЭПИДЕРМОЛИЗОМ ПУТЕМ КОМБИНИРОВАННОГО ПРИМЕНЕНИЯ АЛЛОГЕННЫХ ФИБРОБЛАСТОВ ЧЕЛОВЕКА И ЖИВОГО ЭКВИВАЛЕНТА КОЖИ | 2020 |
|
RU2779997C2 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ ВОДЫ И УСТРОЙСТВО | 2012 |
|
RU2500625C1 |
| СРЕДСТВО ЗАЩИТЫ КОЖИ | 2020 |
|
RU2740900C1 |
| БЕТУЛИНСОДЕРЖАЩИЕ ЭКСТРАКТЫ ИЗ БЕРЕЗОВОЙ КОРЫ И СОСТАВ НА ИХ ОСНОВЕ | 2019 |
|
RU2797184C2 |
| Способ закрытия послеоперационных ран у больных врожденным буллезным эпидермолизом | 2020 |
|
RU2746662C1 |
| Способ хирургического лечения контрактур пальцев у больных с врожденным буллезным эпидермолизом | 2020 |
|
RU2732347C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЖАНОГО СОЛОДА | 2016 |
|
RU2605303C1 |
| СПОСОБЫ И ФАРМАКОЛОГИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 2004 |
|
RU2392959C1 |
| КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ, СОДЕРЖАЩАЯ ГЛИЦЕРИН И ТАНИН | 2013 |
|
RU2640020C2 |
| КОМПОЗИЦИИ ДЛЯ УДАЛЕНИЯ НЕКРОТИЧЕСКИХ ИЛИ ПОВРЕЖДЕННЫХ ТКАНЕЙ С ПОРАЖЕНИЙ ПОВЕРХНОСТИ ТЕЛА И ИЗ ПОЛОСТИ РТА | 2019 |
|
RU2820825C2 |

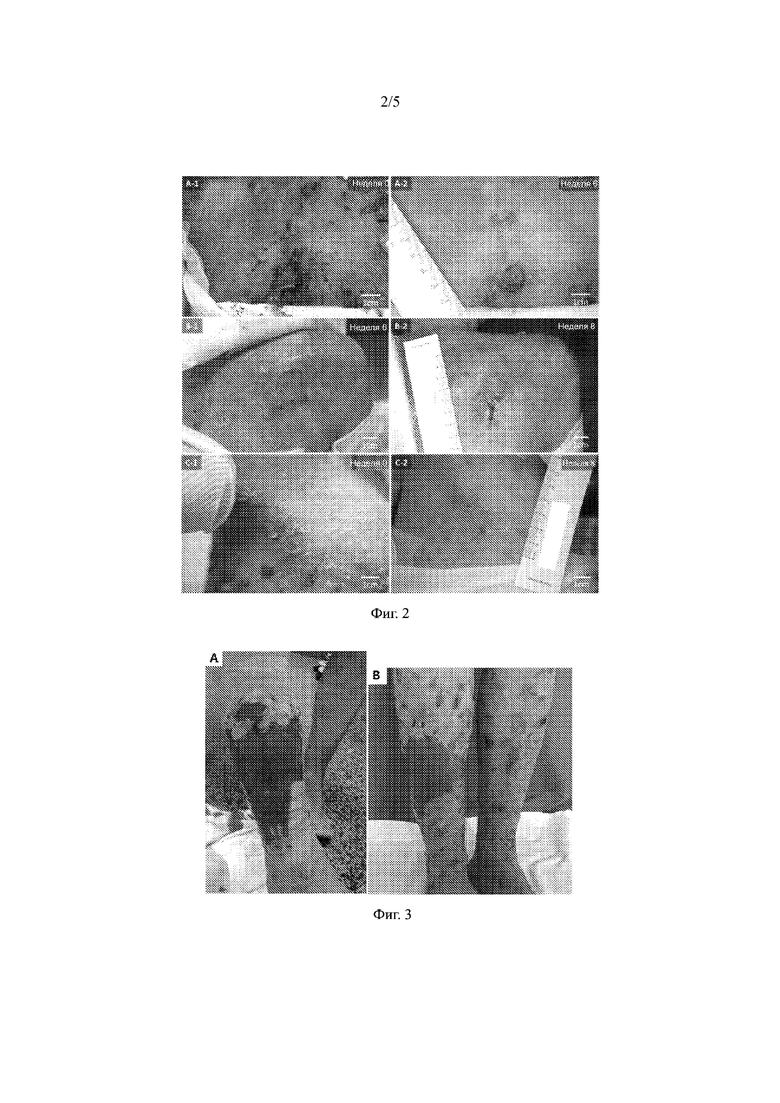
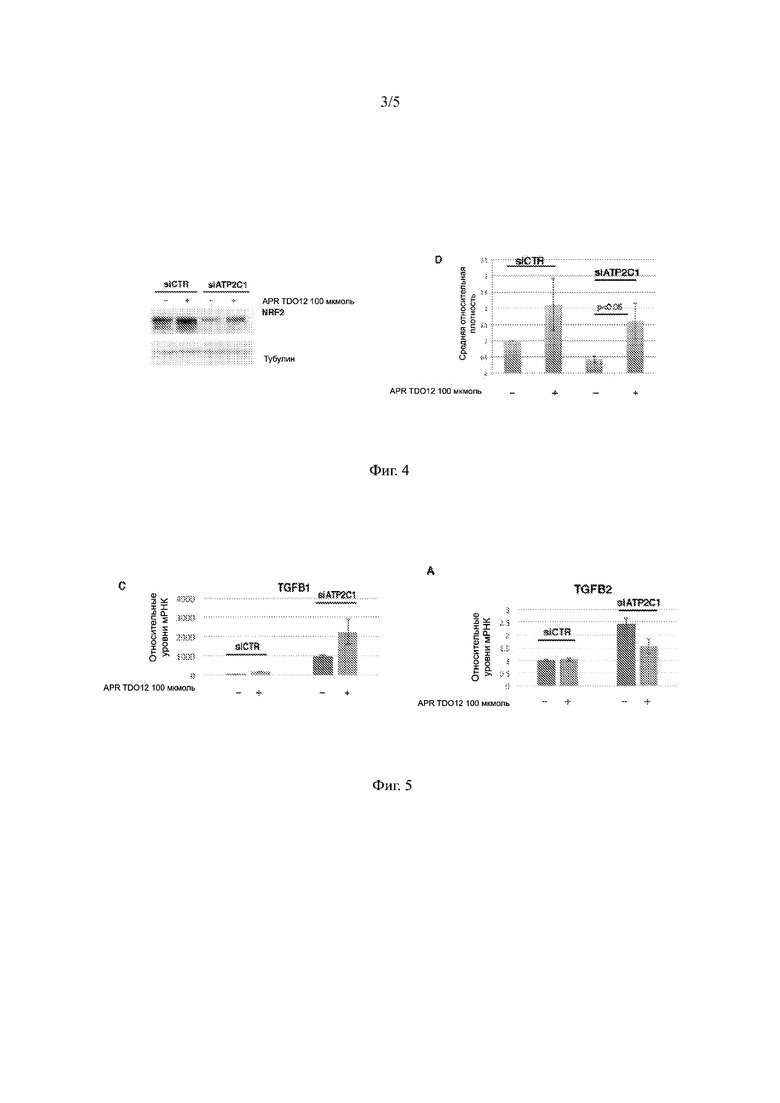
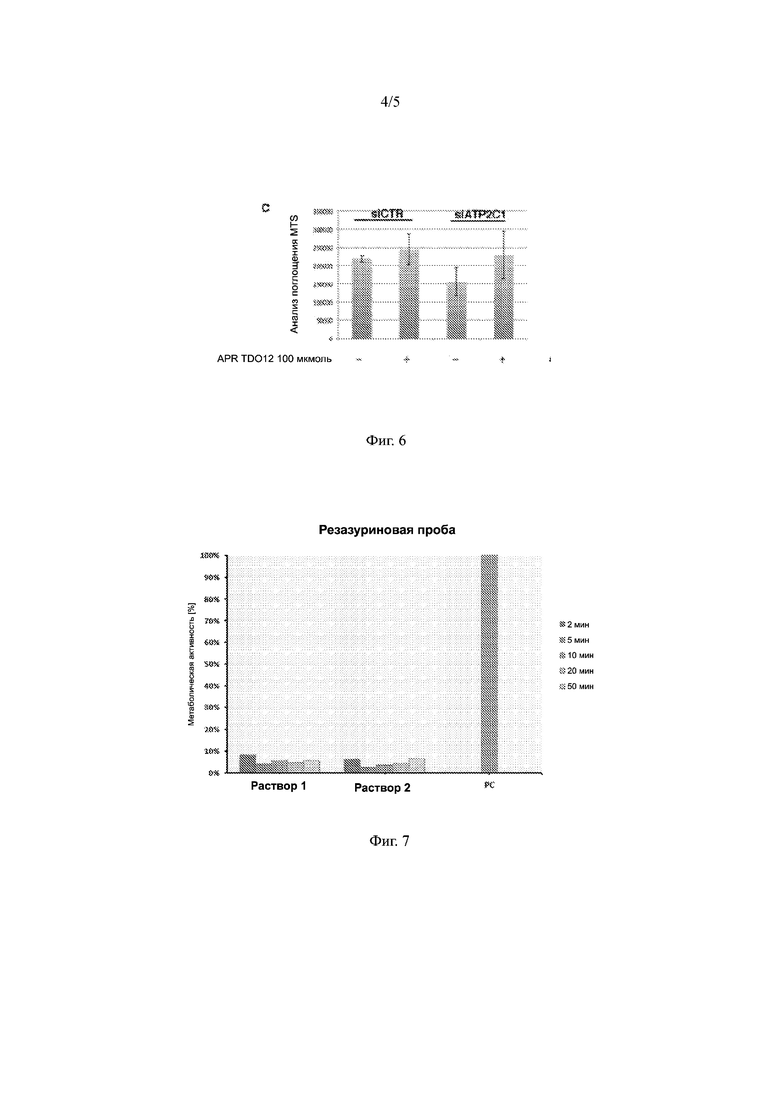
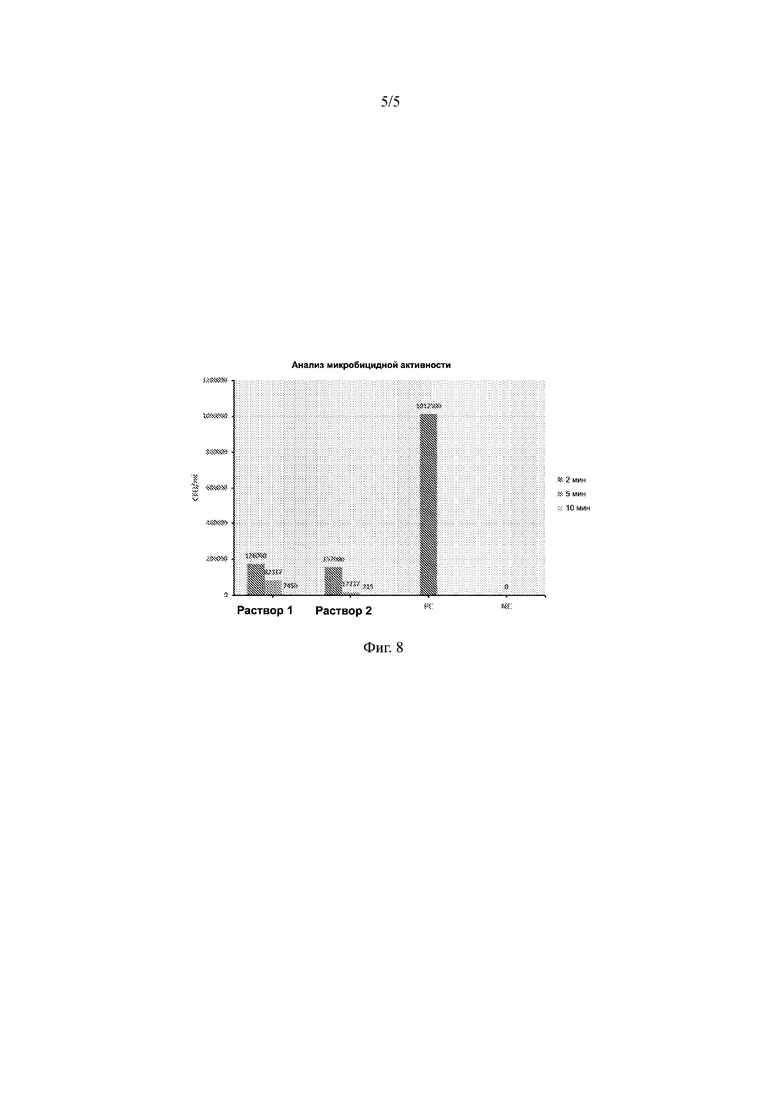
Группа изобретений относится к применениям фармацевтической композиции, содержащей гипотонический кислотный окислительный водный раствор, имеющий pH от 2,5 до 6, содержание хлоридов менее 400 мг/л и содержание свободного хлора 20–140 мг/л, причем содержание свободного хлора предполагает более или равно 90% хлорноватистой кислоты (HClO), менее или равно 10% хлора (Cl2) и менее или равно 3% гипохлорита (ClO-), для местного лечения раны, вызванной буллезным эпидермолизом («EB»), для местного лечения индуцированной ингибитором рецептора эпидермального фактора роста (EGFR) кожной токсичности, для лечения местного расстройства, вызванного болезнью Хейли — Хейли («HHD»), для местного лечения язв Бурули, вызванных mycobacterium ulcerans, для местного лечения инфекции SARS-CoV-2. Группа изобретений обеспечивает разработку гипотонического кислотного окислительного водного раствора, обладающего неожиданной универсальностью при лечении нескольких определенных локализованных состояний и респираторных инфекций, таких как буллезный эпидермолиз («ЕВ»), индуцированная ингибиторами EGFR кожная токсичность, повреждения, вызванные болезнью Хейли - Хейли («HHD»), язва Бурули и инфекция SARS-CoV-2. 5 н. и 15 з.п. ф-лы, 8 ил., 9 табл., 7 пр.
1. Применение фармацевтической композиции, содержащей гипотонический кислотный окислительный водный раствор, имеющий pH от 2,5 до 6, содержание хлоридов менее 400 мг/л и содержание свободного хлора 20–140 мг/л, причем содержание свободного хлора предполагает более или равно 90% хлорноватистой кислоты (HClO), менее или равно 10% хлора (Cl2) и менее или равно 3% гипохлорита (ClO-), для местного лечения раны, вызванной буллезным эпидермолизом («EB»).
2. Применение фармацевтической композиции, содержащей гипотонический кислотный окислительный водный раствор, имеющий pH от 2,5 до 6, содержание хлоридов менее 400 мг/л и содержание свободного хлора 20–140 мг/л, причем содержание свободного хлора предполагает более или равно 90% хлорноватистой кислоты (HClO), менее или равно 10% хлора (Cl2) и менее или равно 3% гипохлорита (ClO-), для местного лечения индуцированной ингибитором рецептора эпидермального фактора роста (EGFR) кожной токсичности.
3. Применение фармацевтической композиции, содержащей гипотонический кислотный окислительный водный раствор, имеющий pH от 2,5 до 6, содержание хлоридов менее 400 мг/л и содержание свободного хлора 20–140 мг/л, причем содержание свободного хлора предполагает более или равно 90% хлорноватистой кислоты (HClO), менее или равно 10% хлора (Cl2) и менее или равно 3% гипохлорита (ClO-), для лечения местного расстройства, вызванного болезнью Хейли — Хейли («HHD»).
4. Применение фармацевтической композиции, содержащей гипотонический кислотный окислительный водный раствор, имеющий pH от 2,5 до 6, содержание хлоридов менее 400 мг/л и содержание свободного хлора 20–140 мг/л, причем содержание свободного хлора предполагает более или равно 90% хлорноватистой кислоты (HClO), менее или равно 10% хлора (Cl2) и менее или равно 3% гипохлорита (ClO-), для местного лечения язв Бурули, вызванных mycobacterium ulcerans.
5. Применение фармацевтической композиции, содержащей гипотонический кислотный окислительный водный раствор, имеющий pH от 2,5 до 6, содержание хлоридов менее 400 мг/л и содержание свободного хлора 20–140 мг/л, причем указанное содержание свободного хлора предполагает более или равно 90% хлорноватистой кислоты (HClO), менее или равно 10% хлора (Cl2) и менее или равно 3% гипохлорита (ClO-), для местного лечения инфекции SARS-CoV-2.
6. Применение по п. 1, в котором рана выбрана из группы, состоящей из кожных пузырей, пузырей слизистой оболочки, пузырей волосистой части кожи головы, рубцовой алопеции, атрофических рубцов, гиперкератоза, белых угрей, кариеса, дисфагии и раздраженной или болезненной кожи.
7. Применение по п. 1, в котором EB ассоциировано с повышением активности MMP2 и MMP9 и композиция уменьшает активность MMP2, MMP9 или их обоих.
8. Применение по п. 1, дополнительно включающее местную повязку, хлорид алюминия, ципрогептадиин, кератинолитик или местный смягчающий агент.
9. Применение по п. 2, в котором EGFR-индуцированная кожа выбрана из группы, состоящей из ксероза, трещин, зуда, экземы, кожных инфекций, раздражения, уртикарии, аномалий роста волос и папулопустулезной сыпи.
10. Применение по п. 2, в котором композиция снижает степень токсичности по шкале, выбранной из группы, состоящей из NCI-CTCAE v5.0, FACT-EGFRI-18, DIEHL-24 и MESTT.
11. Применение по п. 2, в котором композиция улучшает качество жизни, измеренное по шкале EQ-5D-5L/3L для QALYs и/или по дополнительному специфическому для данного состояния опроснику, выбранному из DLQI (дерматологический индекс качества жизни), Skindex-16 или FACT-EGFRI-18.
12. Применение по п. 3, в котором местное расстройство, вызванное HHD, выбрано из группы, состоящей из кожной сыпи, раздражения, жжения, растрескивания кожи и вторичной инфекции.
13. Применение по п. 3, в котором местное расстройство, вызванное HHD, включает в себя облегчение и уменьшение кожных повреждений и композиция уменьшает длительность обострений повреждений или время между появлениями указанных повреждений.
14. Применение по п. 3, в котором HHD ассоциировано с состоянием, выбранным из потери функциональной активности ATP2C1 в кератиноцитах, окислительного стресса в одном или более повреждениях кожи, снижения активности NRF2 или дисбаланса экспрессии TGFβ1 и TGFβ2, уменьшения пролиферации кератиноцитов.
15. Применение по п. 4, в котором язва Бурули характеризуется раной.
16. Применение по п. 4, в котором язва Бурули характеризуется секрецией миколактона.
17. Применение по п. 5, в котором композиция снижает вирусную нагрузку SARS-CoV-2 в носовом проходе и верхних дыхательных путях.
18. Применение по п. 5, в котором композиция снижает распространение SARS-CoV-2 на нижние дыхательные пути.
19. Применение по любому из пп. 1–18, в котором композиция имеет pH от 2,5 до 4,5, содержание хлоридов менее или равно 300 мг/л и окислительно-восстановительный потенциал (ОВП) от 850 до 1350 мВ.
20. Применение по любому из пп. 1–18, в котором указанная композиция имеет:
a) содержание хлоридов менее 250 мг/л;
b) pH от 2,5 до 4;
c) окислительно-восстановительный потенциал (ОВП) от 850 до 1350 мВ; и
d) содержание свободного хлора от 25 до 120 мг/л, включая более или равно 92,5% HClO, менее или равно 7,5% Cl2 и менее 1% или 0% ClO-.
| WO 2008131936 А2, 06.11.2008 | |||
| US 2017360832 A1, 21.12.2017 | |||
| Sakarya S, Hypochlorous Acid: an ideal wound care agent with powerful microbicidal, antibiofilm, and wound healing potency | |||
| Wounds | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
Авторы
Даты
2024-07-09—Публикация
2020-07-02—Подача