Область техники, к которой относится изобретение
Настоящее изобретение относится к двухцепочечному олигонуклеотиду, способному в значительной степени специфически ингибировать экспрессию CTGF с высокой эффективностью, конструкции двухцепочечного олигонуклеотида, включающей двухцепочечный олигонуклеотид, наночастицам, включающим их, и к их применению для профилактики или лечения фиброза или респираторных заболеваний.
Предшествующий уровень техники
В 1995 году Guo и Kemphues обнаружили, что смысловая РНК так же эффективна, как и антисмысловая РНК, при ингибировании экспрессии генов с использованием антисмысловой РНК у C. elegans, поэтому были проведены исследования, чтобы определить причину этого. В 1998 г. Fire et al. впервые обнаружили явление, при котором двухцепочечная РНК (дцРНК) вводится, а соответствующая ей мРНК специфически деградирует, таким образом подавляя экспрессию гена, что называется РНК-интерференцией (RNAi). RNAi, которая представляет собой способ, используемый для ингибирования экспрессии генов, способна ясно показать эффект ингибирования экспрессии генов при низких затратах простым способом, и, таким образом, диапазон ее применения расширяется.
Поскольку технология ингибирования экспрессии генов способна регулировать экспрессию определенных генов, гены-мишени при онкологическом заболевании, генетических заболеваниях и т.п., которые вызываются сверхэкспрессией конкретных генов, могут быть устранены на уровне мРНК, на основании чего эта технология может использоваться в качестве важного инструмента для разработки терапевтических средств для лечения заболеваний и верификации мишеней. Обычно, для ингибирования экспрессии гена-мишени, раскрывается технология введения трансгена в ген-мишень, и ее примеры включают способ введения трансгена в обратном направлении (антисмысловом) относительно промотора, и способ введения трансгена в прямом направлении (смысловом) относительно промотора.
РНК-терапия, нацеленная на РНК, представляет собой способ, который устраняет функцию соответствующего гена с использованием олигонуклеотидов для РНК-мишени, и считается, что данный способ отличается от обычных методов лечения, например, с использованием антител и малых молекул, которые в основном нацелены на белки. Существует два основных подхода к направленному воздействию на РНК: RNAi, опосредованная двухцепочечной РНК и использование антисмысловых олигонуклеотидов (ASO). В настоящее время предпринимаются клинические испытания направленного воздействия на РНК при различных заболеваниях.
Антисмысловой олигонуклеотид (в дальнейшем именуемый «ASO») представляет собой короткую синтетическую ДНК, предназначенную для связывания с геном-мишенью на основе спаривания оснований по Уотсону-Крику, и используется для изучения функции генов и разработки терапевтических средств, способных лечить такие заболевания, как онкологические заболевания, на молекулярном уровне, поскольку такой олигонуклеотид способен специфически ингибировать экспрессию нуклеотидной последовательности определенного гена. Преимущество ASO заключается в том, что такой олигонуклеотид можно легко получить в различных условиях ингибирования экспрессии генов, и были проведены исследования по его применению при ингибировании экспрессии онкогенных генов и роста злокачественных опухолевых клеток. Процесс, с помощью которого ASO ингибирует экспрессию определенного гена, достигается за счет элиминации мРНК из-за активности РНКазы Н, индуцированной связыванием с комплементарной последовательностью мРНК, или путем вмешательства в формирование и продвижение рибосомного комплекса при трансляции белка. Также сообщалось, что ASO связывается с геномной ДНК, образуя структуру тройной спирали, тем самым ингибируя транскрипцию генов. Хотя ASO обладает вышеуказанным потенциалом, для его применения в клинической практике необходимо повысить устойчивость к нуклеазам и эффективно доставлять в ткани или клетки-мишени, чтобы специфически связываться с нуклеотидной последовательностью представляющего интерес гена. Более того, вторичная и третичная структуры мРНК гена важны для специфического связывания ASO, а поскольку область, в которой образуется меньше вторичной структуры мРНК, очень выгодна для доступа ASO, были предприняты усилия для эффективного достижения генноспецифического ингибирования in vitro, а также in vivo путем систематического анализа области, в которой образуется меньше вторичной структуры мРНК до синтеза ASO. Этот ASO более стабилен, чем siRNA, которая является разновидностью РНК, и имеет то преимущество, что данный олигонуклеотид легко растворим в воде и физиологическом растворе. В настоящее время Федеральное управление по лекарственным средствам (FDA) одобрило три ASO (Jessica, C., J. Postdoc Res., 4:35-50, 2016).
С момента открытия роли РНК-интерференции (далее именуемой «RNAi») было обнаружено, что она действует на специфичную последовательность мРНК в различных типах клеток млекопитающих (Barik, S., J. Mol. Med. (2005) 83: 764-773). Когда длинноцепочечная двухцепочечная РНК доставляется в клетки, доставленная двухцепочечная РНК процессируется эндонуклеазой, называемой dicer, в малые интерферирующие РНК (далее именуемые «siRNA») длиной от 21 до 23 пар оснований (п.о.), и siRNA, в свою очередь, связывается с RISC (индуцированным РНК комплексом сайленсинга), чтобы, таким образом, ингибировать экспрессию гена-мишени специфичным для последовательности образом посредством процесса, в котором направляющая (антисмысловая) цепь распознает и разрушает мРНК-мишень. Технология ингибирования экспрессии гена с использованием siRNA полезна в исследованиях для определения функции гена-мишени в клетке-мишени путем ингибирования экспрессии гена-мишени в клетке-мишени и наблюдения обусловленных этим изменений. В частности, ингибирование функции гена-мишени в инфекционном вирусе или злокачественной опухолевой клетке может оказаться полезным при разработке способа лечения заболевания, и сообщалось, что siRNA способна ингибировать экспрессию генов-мишеней на основании результатов исследований in vitro и исследований in vivo с использованием экспериментальных животных.
По данным исследовательской группы Bertrand, было обнаружено, что siRNA для одного и того же гена-мишени оказывает сильное ингибирующее действие на экспрессию мРНК in vitro и in vivo по сравнению с антисмысловым олигонуклеотидом (ASO), и этот эффект сохраняется в течение длительного времени. Более того, поскольку механизм действия siRNA заключается в регулировании экспрессии гена-мишени специфичным для последовательности способом путем комплементарного связывания с мРНК-мишенью, преимуществом этого механизма является то, что диапазон мишеней, к которым применима siRNA, значительно шире по сравнению с обычными лекарственными средствами на основе антител или низкомолекулярными лекарственными средствами (M.A. Behlke, MOLECULAR THERAPY. 2006 13(4):664-670).
Несмотря на превосходный эффект siRNA и широкий спектр ее применения, для разработки siRNA в качестве терапевтического средства siRNA должна быть эффективно доставлена в клетки-мишени за счет улучшения стабильности siRNA in vivo и повышения эффективности доставки клеток (F.Y. Xie, Drug Discov. Today, 2006 Jan.; 11(1-2):67-73). Для повышения стабильности in vivo и решения проблем, связанных со стимуляцией неспецифическим врожденным иммунитетом siRNA, проводится тщательное исследование модификации некоторых нуклеотидов или каркасов siRNA с целью придания им устойчивости к нуклеазам, использование носителя, такого как вирусный вектор, липосомы или наночастицы и т.д.
Система доставки с использованием вирусного вектора, такого как аденовирус или ретровирус, обладает высокой эффективностью трансфекции, но высокой иммуногенностью и онкогенностью. С другой стороны, невирусная система доставки, включающая наночастицы, имеет более низкую эффективность доставки в клетку, чем вирусная система доставки, но имеет преимущество, которое заключается в том, что стабильность in vivo высока, возможна адресно-специфическая доставка, олигонуклеотиды RNAi поглощаются и интернализуются в клетки или ткани, и практически отсутствует цитотоксичность или иммунная стимуляция, поэтому невирусная система доставки в настоящее время считается более эффективным способом доставки по сравнению с вирусной системой доставки (Akhtar S., J. Clin. Invest. 2007 December 3; 117(12): 3623-3632).
Среди невирусных систем доставки способ применения наноносителя включает формирование наночастиц с использованием различных полимеров, таких как липосомы, комплексы катионных полимеров и т.п., и нанесение siRNA на такие наночастицы, а именно наноносители, чтобы таким образом доставить их в клетки. В данном документе конкретные примеры наноносителя могут включать полимерные наночастицы, полимерные мицеллы, липоплексы и т.п. В частности, липоплекс, состоящий из катионных липидов, взаимодействует с анионными липидами клеточной эндосомы, вызывая дестабилизирующий эффект эндосомы, тем самым реализуя внутриклеточную доставку.
Кроме того, известно, что можно индуцировать высокую эффективность in vivo, связывая химическое вещество с концевой частью сопровождающей (смысловой) цепи siRNA для придания улучшенной фармакокинетики (J. Soutschek, Nature 11; 432(7014):173-8, 2004). В данном документе стабильность siRNA варьируется в зависимости от свойств химического вещества, связанного с концом смысловой (сопровождающей) или антисмысловой (направляющей) нити siRNA. Например, siRNA в форме, в которой полимерное соединение, такое как полиэтиленгликоль (PEG), конъюгировано, взаимодействует с анионной фосфатной группой siRNA в присутствии катионного материала с образованием комплекса, тем самым получая носитель для доставки, в котором siRNA обладает улучшенной стабильностью (S.H. Kim, J. Control Release 129(2):107-16, 2008). В частности, мицеллы, состоящие из полимерных комплексов, чрезвычайно малы по размеру по сравнению с другими системами, используемыми в качестве носителей для доставки лекарственных средств, таких как микросферы или наночастицы, но их распределение очень равномерное и происходит спонтанно, что обеспечивает легкий контроль качества состава и воспроизводимость.
Для повышения эффективности внутриклеточной доставки siRNA была разработана технология для реализации эффективной проницаемости клеточной мембраны и стабильности siRNA с использованием конъюгата siRNA, в котором биосовместимый полимерный гидрофильный материал (например, полиэтиленгликоль (PEG)) конъюгирован с siRNA через простую ковалентную связь или ковалентную связь, опосредованную линкером (корейский патент № 883471). Однако даже когда siRNA химически модифицируют или конъюгируют с полиэтиленгликолем (PEG) (PEGилирование), она все еще имеет недостатки, такие как низкая стабильность in vivo и плохая доставка к органам-мишеням. Чтобы преодолеть эти недостатки, была разработана конструкция двухцепочечной олигоРНК, в которой гидрофильные и гидрофобные материалы связаны с олигонуклеотидом, в частности двухцепочечной олигоРНК, такой как киРНК, и конструкция образует самособирающиеся наночастицы, называемые SAMiRNA™ (самособирающаяся мицеллярная ингибирующая РНК) за счет гидрофобного взаимодействия гидрофобного материала (корейский патент № 1224828). В данном документе технология SAMiRNA™ способна создавать гомогенные наночастицы, имеющие очень маленький размер по сравнению с обычными способами доставки.
В конкретном воплощении технологии SAMiRNA™ используется гидрофильный материал, такой как PEG (полиэтиленгликоль) или HEG (гексаэтиленгликоль). PEG представляет собой синтетический полимер и часто используется для повышения растворимости фармацевтических средств, особенно белков, и для контроля фармакокинетики. PEG является полидисперсным материалом, а полимер в одной партии состоит из суммы разного количества мономеров, поэтому его молекулярная масса представляет собой кривую Гаусса, а значение полидисперсности (Mw/Mn) представляет собой степень гомогенности материала. В частности, PEG с низкой молекулярной массой (от 3 до 5 кДа) демонстрирует значение полидисперсности около 1,01, тогда как PEG с высокой молекулярной массой (20 кДа) демонстрирует высокое значение полидисперсности около 1,2. Чем выше молекулярная масса, тем ниже гомогенность материала. Следовательно, когда PEG конъюгируют с фармацевтическими средствами, полидисперсность PEG отражается в конъюгате, что затрудняет проверку индивидуального материала, что нежелательно. Следовательно, материал, имеющий низкое значение полидисперсности, должен быть получен за счет усовершенствования процессов синтеза и очистки PEG. Однако, в частности, когда PEG связывается с материалом, имеющим низкую молекулярную массу, возникают проблемы, связанные с полидисперсностью материала, например, неудобство, которое заключается в том, что сложно определить, легко ли выполняется связывание (Francesco M. V. DRUG DISCOVERY TODAY(2005) 10(21):1451-1458).
Соответственно, в последние годы, в качестве усовершенствованной формы традиционной технологии самособирающихся наночастиц SAMiRNA™, блоки, в которых гидрофильный материал конструкции двухцепочечного олигонуклеотида, составляющей SAMiRNA™, собираются в основную единицу, включающую от 1 до 15 однородных мономеров, имеющих заданную молекулярную массу, и линкер по мере необходимости используется в подходящем количестве в зависимости от потребности, при этом был разработан новый тип технологии носителя для доставки с малым размером и значительно улучшенной полидисперсностью по сравнению с обычной SAMiRNA™. Уже известно, что siRNA быстро расщепляется различными ферментами, присутствующими в крови, при введении in vivo, что приводит к плохой эффективности доставки к клеткам-мишеням или тканям, а улучшенная SAMiRNA™ также показывает, что в зависимости от целевого гена наблюдаются изменения в стабильности и эффективности ингибирования экспрессии. Таким образом, авторы настоящего изобретения попытались усилить эффект ингибирования экспрессии и стабильность гена-мишени путем применения двухцепочечного олигонуклеотида в гибридной форме ДНК-РНК с использованием последовательности ДНК, которая представляет собой смысловую цепь ASO, в качестве направляющей, и последовательности РНК, которая представляет собой антисмысловую цепь в качестве сопровождающей, чтобы более стабильно и эффективно ингибировать экспрессию гена-мишени с использованием улучшенных самособирающихся наночастиц SAMiRNA™.
Хроническая обструктивная болезнь легких (далее COPD), которая является репрезентативным заболеванием легких наряду с астмой, отличается от астмы тем, что сопровождается необратимой обструкцией дыхательных путей и является респираторным заболеванием, которое не является полностью обратимым и прогрессивно ограничивает поток воздуха, сопровождающийся аномальной воспалительной реакцией легких, вызванной повторной инфекцией, вдыханием вредных частиц или газов или курением (Pauwels et al., Am J. Respir. Crit. Care Med., 163:1256-1276, 2001). COPD представляет собой заболевание, обусловленное патологическими изменениями в бронхиолах и паренхиме легких вследствие воспаления дыхательных путей и паренхимы легких, и характеризуется облитерирующим бронхиолитом и эмфиземой (разрушением паренхимы легких). Примеры COPD включают хронический обструктивный бронхит, хронический бронхиолит и эмфизему. При COPD увеличивается количество нейтрофилов и увеличивается секреция цитокинов, таких как GM-CSF, TNF-α, IL-8 и MIP-2. Более того, дыхательные пути воспаляются, мышечные стенки утолщаются, увеличивается секреция слизи, что приводит к бронхиальной обструкции. При закупорке бронхов альвеолы расширяются и повреждаются, снижается способность обмена кислорода и углекислого газа, увеличивается частота дыхательной недостаточности.
Серьезность COPD была отмечена во всем мире, поскольку COPD была 6-й по значимости причиной смерти от болезней в 1990 году, но, по прогнозам, станет 3-й по значимости причиной в 2020 году и является единственным заболеванием с растущей заболеваемостью среди 10 основных заболеваний. COPD имеет высокую распространенность, вызывает проблемы с дыханием и влечет за собой высокие прямые медицинские расходы на диагностику и лечение COPD и высокие косвенные медицинские расходы, такие как потери из-за респираторного дистресс-синдрома или разрешенного отпуска или потери из-за преждевременной смерти. По этой причине COPD становится серьезной социально-экономической проблемой во всем мире (Chronic Obstructive Pulmonary Disease (COPD) Medical Guidelines. 2005. Clinical Research Center for Chronic Obstructive Airway Diseases. p.30-31).
Не было подтверждено, что существующие методы лечения облегчают долгосрочное снижение функции легких, характерное для COPD. Поэтому фармакотерапия при COPD в основном используется с целью уменьшения симптомов или осложнений. В частности, репрезентативным симптоматическим лекарственным средством при COPD являются бронходилататоры, а в основном назначаются противовоспалительные лекарственные средства или кортикостероиды, но их эффективность незначительна, сфера применения узка, высок риск развития побочных эффектов. Что касается других лекарственных средств, то известно, что только вакцина против гриппа снижает серьезную заболеваемость и смертность у пациентов с COPD примерно на 50% (Chronic Obstructive Pulmonary Disease (COPD) Medical Guidelines. 2005. Clinical Research Center for Chronic Obstructive Airway Diseases. p.52-58).
Между тем предполагается, что многие генетические факторы увеличивают (или уменьшают) индивидуальный риск развития COPD. Генетический фактор риска, который был продемонстрирован на сегодняшний день, - это генетический дефицит α1-антитрипсина. Хотя курение значительно увеличивает риск развития COPD, развитие быстропрогрессирующей панлобулярной эмфиземы в молодом возрасте и снижение функции легких наблюдается как у некурящих, так и у курильщиков с тяжелыми генетически обусловленными недостаточностями. Никакие гены, кроме гена α1-антитрипсина, не были подтверждены как связанные с патогенезом COPD, но предпринимаются попытки идентифицировать биомаркеры заболеваний путем исследования основных клеточных, молекулярных и генетических аномалий у пациентов с COPD и использования биомаркеров для диагностики или открытия новых способов лечения (P.J. Barnes and R.A. Stockley. Eur. Respir. J. (2005) 25:1084-1106). В частности, активно проводятся исследования по диагностике COPD и выбору мишени лечения с помощью таких способов, как генный микроэррей или протеомика. В основном проводится анализ генетических факторов, приводящих к предрасположенности к COPD, и причин обострения симптомов COPD, вызванных курением (Peter J. Castaldi et al. Human Molecular Genetics, 2010, Vol. 19, No. 3 526-534).
Идиопатический легочный фиброз (далее именуемый «IPF» (Idiopathic pulmonary fibrosis)), который является разновидностью фиброза, представляет собой заболевание, при котором хронические воспалительные клетки инфильтрируют стенки альвеол (легочные альвеолы) и возникают различные изменения, которые уплотняют легкие, вызывая тяжелые структурные изменения в легочной ткани, постепенно ухудшающие функцию легких и в итоге приводящие к летальному исходу. До сих пор не существует эффективного способа лечения IPF, и когда появляются симптомы IPF и у пациентов диагностируется IPF, средняя продолжительность жизни пациентов составляет всего от 3 до 5 лет, и, таким образом, IPF является заболеванием с очень плохим прогнозом. В зарубежных странах заболеваемость им составляет около 3-5 на 100 000 человек, причем известно, что уровень заболеваемости обычно выше после 50 лет, а у мужчин в два раза чаще диагностируется заболевание, чем у женщин.
Этиология IPF до сих пор точно не идентифицирована. IPF часто встречается у курильщиков, и антидепрессанты, хроническая ингаляция легких из-за гастроэзофагеального рефлюкса, вдыхание металлической пыли, древесной пыли или растворителей и т.п., как сообщается, являются факторами риска, связанными с возникновением IPF. Однако у большинства пациентов не сообщалось об определенных причинных факторах. Для наиболее часто упоминаемых факторов, независимо от причины, когда активируются ответы Th1/Th2, коагуляционные каскады и т.д., известно, что при этом секретируются фиброзные цитокины, и активированные цитокины стимулируют фибробласты, тем самым увеличивая ECM (внеклеточный матрикс) и вызывая легочный фиброз. Таким образом, этот процесс естественным образом сопровождается воспалением легких, которое может привести к легочному фиброзу, но в настоящее время более популярно мнение, что легочный фиброз может возникать непосредственно независимо от воспаления легких. Недавняя гипотеза состоит в том, что патологический легочный фиброз возникает во время заживления ран из-за аномальной сигнальной системы эпителиально-мезенхимального взаимодействия. При повреждении эпителиальных клеток усиливается апоптоз эпителиальных клеток, ограничивается их миграция, не контролируется их дифференцировка, подавляется пролиферация, поэтому секретируются растворимые факторы (TGF, HGF, KGF, ангиотензин II, ROS и др.) и ингибируется апоптоз мезенхимальных клеток вместе с ECM, что приводит к усилению дифференцировки миофибробластов, легочному фиброзу из-за отложения ECM или повторной стимуляции эпителиальных клеток. Нельзя сказать, что воспаление легких непосредственно вызывает легочный фиброз, но это означает, что сначала возникает воспаление легких, а затем возникает легочный фиброз из-за различий между пациентами с IPF и нормальными людьми в процессе заживления для восстановления нормальной ткани. Кроме того, IPF может быть вызвана дисбалансом цитокинов Th1/Th2. Цитокиновый ответ Th1 связан с клеточно-опосредованным иммунитетом, который восстанавливает поврежденные участки ткани до нормальной ткани, тогда как цитокин Th2 индуцирует отложение ECM и фиброз посредством активации и пролиферации фибробластов. Сообщалось, что когда IFN-γ вводят модели легочного фиброза, вызванного блеомицином, он способен предотвращать легочный фиброз за счет снижения уровня мРНК TGF-β и проколлагена. Однако, поскольку его этиология точно не известна, необходимо идентифицировать первоначальные причинные факторы, вызывающие фиброз, и разработать материалы, которые способны ингибировать гены, связанные с IPF, и сигнальную систему TGF-β.
Известно, что состояние при IPF продолжает ухудшаться без лечения, и около 50% и более больных умирают в течение 3-5 лет. Кроме того, когда болезнь прогрессирует и полностью превращается в фиброз, какое бы лечение ни проводилось, улучшения не наступает. Прогнозируется, что для лечения существует высокая вероятность эффективности, если оно будет назначено на ранней стадии. Хотя комбинированная терапия стероидом с азатиоприном или циклофосфамидом является известным современным способом лечения, при этом не достигается заметного эффекта, и несколько ингибиторов фиброза были опробованы в экспериментах на животных и у небольшого числа пациентов, но ни один из них не доказал свою эффективность. В частности, у пациентов с терминальной стадией IPF не существует эффективного способа лечения, кроме трансплантации легких. Таким образом, существует острая необходимость в разработке более эффективного терапевтического агента для лечения IPF.
Фиброз — это общий термин для обозначения состояния, при котором ткань или орган становятся твердыми из-за чрезмерного фиброза соединительной ткани по какой-либо причине, и все процессы, при которых возникает фиброз, независимо от области, протекают по тому же пути, что и процесс заживления шрамов. На сегодняшний день существует несколько методов лечения симптомов фиброза, и способы лечения находятся в стадии разработки и изучения. Эффективные средства для лечения фиброза могут применяться не только при типичных фиброзах, таких как цирроз, фиброз печени, миелофиброз, фиброз миокарда, фиброз почек и фиброз легких, но и при различных заболеваниях, сопровождающихся фиброзом, поэтому существует острая необходимость в разработке эффективного терапевтического агента при фиброзе.
CTGF (фактор роста соединительной ткани; CCN2) представляет собой матрицеллюлярный белок, принадлежащий к семейству CCN, и представляет собой секреторный цитокин, который, как известно, участвует в различных биологических процессах, таких как клеточная адгезия, миграция, пролиферация, ангиогенез, заживление ран и т.п., а сверхэкспрессия CTGF считается основной причиной таких симптомов, как склеродермия, фиброзное заболевание и рубцевание (Brigstock DR. J. Cell Commun. Signal (2010) 4 (1): 1-4). В частности, в отношении фиброзного заболевания известно, что CTGF играет роль в стимулировании продуцирования ECM (внеклеточного матрикса) в условиях, которые вызывают либо устойчивый фиброз, либо фиброз вместе с фактором роста TGF-β, а в последние годы, известно, что заболевания глаз или мышечную дистрофию, вызванные аномальной экспрессией CTGF, можно лечить с помощью образца или материала, который ингибирует экспрессию CTGF или его действие (Пат. США No. 7622454, Пат. Заявка США No. 20120164151).
Как упоминалось выше, технологические разработки терапевтических агентов RNAi для CTGF и систем их доставки все еще незначительны, и рыночный спрос на терапевтические агенты на основе двухцепочечных олигонуклеотидов, способных специфически ингибировать экспрессию CTGF с высокой эффективностью, и технологии их доставки очень высоки.
Соответственно, авторы настоящего изобретения определили CTGF как ген, связанный с респираторными заболеваниями, включая COPD и фиброз, включая IPF, выбрали двухцепочечный олигонуклеотид, нацеленный на CTGF, и проверили терапевтический агент RNAi, способный ингибировать экспрессию CTGF, и его носитель для доставки, таким образом достигнув кульминации в настоящем изобретении.
Раскрытие
Целью настоящего изобретения является создание двухцепочечного олигонуклеотида, способного в значительной степени с высокой эффективностью специфически ингибировать экспрессию CTGF, предпочтительно двухцепочечного олигонуклеотида в форме гибрида РНК/РНК, ДНК/ДНК или ДНК/РНК, наиболее предпочтительно двухцепочечного олигонуклеотида, включающего последовательность в форме гибрида ДНК/РНК, конструкцию двухцепочечного олигонуклеотида, включающую двухцепочечный олигонуклеотид, и наночастицы, включающие двухцепочечный олигонуклеотид или конструкцию двухцепочечного олигонуклеотида.
Другой целью настоящего изобретения является фармацевтическая композиция для профилактики или лечения респираторных заболеваний и фиброза, содержащая двухцепочечный олигонуклеотид, конструкцию двухцепочечного олигонуклеотида и/или наночастицы в качестве активного ингредиента.
Еще одной целью настоящего изобретения является предоставление способа профилактики или лечения фиброза или респираторного заболевания, включающего введение двухцепочечного олигонуклеотида, конструкции двухцепочечного олигонуклеотида и/или наночастиц объекту, нуждающемуся в профилактике или лечение фиброза или респираторного заболевания.
Еще одной целью настоящего изобретения является обеспечение применения двухцепочечного олигонуклеотида, конструкции двухцепочечного олигонуклеотида, включающей двухцепочечный олигонуклеотид, и наночастиц, включающих двухцепочечный олигонуклеотид, или конструкции двухцепочечного олигонуклеотида для профилактики или лечения фиброза или респираторного заболевания.
Еще одной целью настоящего изобретения является обеспечение применения фармацевтической композиции для профилактики или лечения фиброза или респираторного заболевания.
Еще одной целью настоящего изобретения является обеспечение применения двухцепочечного олигонуклеотида, конструкции двухцепочечного олигонуклеотида, включающей двухцепочечный олигонуклеотид, и наночастиц, включающих двухцепочечный олигонуклеотид, или конструкции двухцепочечного олигонуклеотида для изготовления лекарственного средства для профилактики или лечения фиброза или респираторного заболевания.
Для достижения вышеуказанных целей настоящее изобретение обеспечивает двухцепочечный олигонуклеотид, включающий смысловую цепь, включающую любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-16, предпочтительно любую последовательность, выбранную из группы, состоящей из SEQ ID NO: ID NO: 1, 2, 10 и 15, более предпочтительно последовательность SEQ ID NO: 10 и антисмысловую цепь, включающую комплементарную ей последовательность.
Кроме того, настоящее изобретение обеспечивает конструкцию двухцепочечного олигонуклеотида, включающую двухцепочечный олигонуклеотид, и наночастицы, включающие двухцепочечный олигонуклеотид или конструкцию двухцепочечного олигонуклеотида.
Кроме того, настоящее изобретение обеспечивает фармацевтическую композицию для профилактики или лечения фиброза или респираторного заболевания, включающую двухцепочечный олигонуклеотид, включающий смысловую цепь, включающую любую одну последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-16, предпочтительно любую одну последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 2, 10 и 15, более предпочтительно последовательность SEQ ID NO: 10 и антисмысловую цепь, включающую комплементарную ей последовательность, конструкцию двухцепочечного олигонуклеотида, включающую двухцепочечный олигонуклеотид и/или наночастицы, включающие двухцепочечный олигонуклеотид, или конструкцию двухцепочечного олигонуклеотида.
Кроме того, настоящее изобретение обеспечивает способ профилактики или лечения фиброза или респираторного заболевания, включающий введение двухцепочечного олигонуклеотида, конструкции двухцепочечного олигонуклеотида и/или наночастиц объекту, нуждающемуся в профилактике или лечении фиброза или респираторного заболевания.
Кроме того, настоящее изобретение обеспечивает способ профилактики или лечения фиброза или респираторного заболевания, включающий введение фармацевтической композиции для профилактики или лечения фиброза или респираторного заболевания объекту, нуждающемуся в профилактике или лечении фиброза или респираторного заболевания.
Двухцепочечный олигонуклеотид, включающий смысловую цепь, включающую любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 1-16, предпочтительно любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 2, 10 и 15, более предпочтительно последовательность SEQ ID NO: 10 и антисмысловую цепь, включающую комплементарную ей последовательность, согласно аспекту настоящего изобретения, конструкция двухцепочечного олигонуклеотида, включающая двухцепочечный олигонуклеотид, и/или наночастицы, включающие двухцепочечный олигонуклеотид или конструкцию двухцепочечного олигонуклеотида, способны очень эффективно ингибировать экспрессию CTGF, поэтому двухцепочечный олигонуклеотид, конструкция двухцепочечного олигонуклеотида и наночастицы по настоящему изобретению применимы для предотвращения или лечения фиброза или респираторных заболеваний.
Последовательности SEQ ID NO: 1, 2, 10 и 15, включенные в предпочтительный двухцепочечный олигонуклеотид, предназначенный для достижения вышеуказанных целей, являются следующими.
5’-ATGTACAGTTATCTAAGTT-3’ (SEQ ID NO: 1)
5’-TGTACAGTTATCTAAGTTA-3’ (SEQ ID NO: 2)
5’-TGATTTCAGTAGCACAAGT-3’ (SEQ ID NO: 10)
5’-TCAGTAGCACAAGTTATTT-3’ (SEQ ID NO: 15)
Под двухцепочечным олигонуклеотидом согласно настоящему изобретению понимается любой материал, обладающий общим действием RNAi (РНК-интерференции), и мРНК-специфический двухцепочечный олигонуклеотид, кодирующий белок CTGF, также включает CTGF-специфическую shRNA, как будет очевидно для специалиста в данной области, к которой принадлежит изобретение. Проще говоря, олигонуклеотид может представлять собой siRNA, shRNA или miRNA.
Кроме того, пока сохраняется специфичность к CTGF, в смысловой цепи, включающей любую одну последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 2, 10 и 15, или в комплементарной ей антисмысловой цепи, CTGF-специфическая siRNA включая смысловую цепь, которая содержит последовательность, в которой по меньшей мере один нуклеотид заменен, делетирован или вставлен, и ее антисмысловая цепь и антисмысловые олигонуклеотиды также входят в объем настоящего изобретения, как будет очевидно специалистам в данной области.
В настоящем изобретении каждая из смысловой цепи и антисмысловой цепи может независимо представлять собой ДНК или РНК, и может быть использована гибридная форма, в которой смысловая цепь представляет собой ДНК, а антисмысловая цепь представляет собой РНК, или в которой смысловая цепь представляет собой РНК, а антисмысловая цепь представляет собой ДНК.
В настоящем изобретении SEQ ID NO: 1, 2, 10 и 15 описаны в форме ДНК, но при использовании РНК последовательности SEQ ID NO: 1, 2, 10 и 15 могут быть представлены в виде соответствующей формы последовательности РНК, в которой T заменена на U.
Также двухцепочечный олигонуклеотид по настоящему изобретению включает не только полное совпадение, при котором смысловая цепь последовательности представляет собой нуклеотидную последовательность, на 100% комплементарную сайту связывания гена CTGF, но также и несовпадение, при котором некоторые нуклеотидные последовательности не совпадают, при условии, что сохраняется специфичность к CTGF.
Двухцепочечный олигонуклеотид по настоящему изобретению может включать выступающую структуру, в которой один или несколько неспаренных нуклеотидов находятся на 3'-конце одной или обеих цепей.
В настоящем изобретении смысловая цепь или антисмысловая цепь предпочтительно состоит из 19-31 нуклеотида, но настоящее изобретение этим не ограничивается.
В настоящем изобретении двухцепочечный олигонуклеотид, включающий смысловую цепь, включающую любую одну последовательность, выбранную из группы, состоящей из SEQ ID NO: 1, 2, 10 и 15, и антисмысловую цепь, включающую комплементарную ей последовательность, является специфичным к CTGF (фактор роста соединительной ткани), но настоящее изобретение ими не ограничивается.
В настоящем изобретении смысловая цепь или антисмысловая цепь двухцепочечного олигонуклеотида включает любую химическую модификацию для улучшения стабильности in vivo или придания устойчивости к нуклеазам и уменьшения неспецифических иммунных ответов. Химическая модификация может включать, без ограничения указанным, по меньшей мере одну, выбранную из группы, состоящей из модификации, в которой гидроксильная группа (-ОН) в 2'-углеродном положении структуры сахара в нуклеотиде замещена любой одной, выбранной из группы, состоящей из метила (-СН3), метокси (-ОСН3), амина (-NH2), фтора (-F), О-2-метоксиэтила, О-пропила, О-2-метилтиоэтила, О-3- аминопропила, O-3-диметиламинопропила, O-N-метилацетамидо и O-диметиламидооксиэтила; модификации, в которой кислород сахарной структуры в нуклеотиде замещен серой; модификации, в которой нуклеотидная связь представляет собой любую связь, выбранную из группы, состоящей из фосфоротиоатной связи, боранофосфатной связи и метилфосфонатной связи; модификации в PNA (пептидную нуклеиновую кислоту), LNA (заблокированную нуклеиновую кислоту) или UNA (незаблокированную нуклеиновую кислоту); и модификации в форме гибрида ДНК-РНК (Ann. Rev. Med. 55, 61-65 2004; US 5660985; US 5958691; US 6531584; US 5808023; US 6326358; US 6175001; Bioorg. Med. Chem. Lett. 14:1139-1143, 2003; RNA, 9:1034-1048, 2003; Nucleic Acid Res. 31:589-595, 2003; Nucleic Acids Research, 38(17) 5761-773, 2010; Nucleic Acids Research, 39(5):1823-1832, 2011).
В настоящем изобретении по меньшей мере одна фосфатная группа, предпочтительно от 1 до 3 фосфатных групп, может быть связана с 5’-концом антисмысловой цепи двухцепочечного олигонуклеотида.
Другой аспект настоящего изобретения относится к конструкции двухцепочечного олигонуклеотида, имеющей структуру структурной формулы (1) ниже, в которой А представляет собой гидрофильный материал, В представляет собой гидрофобный материал, X и Y, каждый независимо, представляют собой простую ковалентную связь или ковалентную связь, опосредованную линкером, и R представляет собой двухцепочечный олигонуклеотид.
Структурная формула (1)
A-X-R-Y-B
В предпочтительном воплощении конструкция двухцепочечного олигонуклеотида, включающая CTGF-специфическую последовательность по настоящему изобретению, имеет структуру структурной формулы (1), приведенной ниже.
Структурная формула (1)
A-X-R-Y-B
В структурной формуле (1) A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый независимо, представляют собой простую ковалентную связь или ковалентную связь, опосредованную линкером, и R представляет собой CTGF-специфичный двухцепочечный олигонуклеотид.
Двухцепочечный олигонуклеотид по настоящему изобретению предпочтительно находится в форме гибрида ДНК-РНК, siRNA (короткой интерферирующей РНК), shRNA (короткой шпилечной РНК) или miRNA (microRNA), без ограничения указанным, а также включает одноцепочечный ингибитор miRNA, который служит антагонистом miRNA.
Далее двухцепочечный олигонуклеотид по настоящему изобретению будет описан на основе РНК, но может быть применен к другим двухцепочечным олигонуклеотидам (например, гибридам ДНК/РНК), обладающим теми же свойствами, что и двухцепочечный олигонуклеотид по настоящему изобретению, как будет очевидно специалистам в данной области техники.
Более предпочтительно конструкция двухцепочечного олигонуклеотида, включающая CTGF-специфичный двухцепочечный олигонуклеотид по настоящему изобретению, имеет структуру структурной формулы (2), приведенной ниже.
Структурная формула (2)
A-X-S-Y-B
AS
В структурной формуле (2) A, B, X и Y имеют значения, определенные в структурной формуле (1), S представляет собой смысловую цепь CTGF-специфичной нуклеотидной последовательности, а AS представляет собой антисмысловую цепь CTGF-специфичного двухцепочечного олигонуклеотида.
Более предпочтительно конструкция двухцепочечного олигонуклеотида, включающая CTGF-специфичный двухцепочечный олигонуклеотид, имеет структуру структурной формулы (3) или (4), приведенной ниже.
Структурная формула (3)

Структурная формула (4)

В структурной формуле (3) и структурной формуле (4) A, B, S, AS, X и Y имеют значения, определенные в структурной формуле (2), а 5' и 3' соответственно представляют собой 5'-конец и 3'-конец смысловой цепи CTGF-специфичного двухцепочечного олигонуклеотида.
Гидрофильный материал может быть выбран из группы, состоящей из полиэтиленгликоля (PEG), поливинилпирролидона и полиоксазолина, без ограничения указанным.
В конструкции двухцепочечного олигонуклеотида, включающей CTGF-специфичный двухцепочечный олигонуклеотид в соответствии со структурной формулой (1) - структурной формулой (4), от одной до трех фосфатных групп могут быть связаны на 5'-конце антисмысловой цепи, и shRNA можно использовать вместо РНК, как будет очевидно специалистам в данной области.
Гидрофильный материал в структурной формуле (1) - структурной формуле (4) предпочтительно представляет собой полимерный материал с молекулярной массой от 200 до 10000, более предпочтительно полимерный материал с молекулярной массой от 1000 до 2000. Например, гидрофильный полимерный материал может представлять собой неионогенное гидрофильное полимерное соединение, такое как полиэтиленгликоль, поливинилпирролидон, полиоксазолин и т.д., без обязательного ограничения указанным.
В частности, гидрофильный материал (А) в структурной формуле (1) - структурной формуле (4) может быть использован в форме блока гидрофильного материала, представленного структурной формулой (5) или структурной формулой (6) ниже. Когда эти блоки гидрофильного материала используются в соответствующем количестве (n в структурной формуле (5) или структурной формуле (6)) в зависимости от необходимости, проблемы из-за полидисперсности, которые могут возникнуть в случае использования обычных синтетических полимерных материалов, и т.д. можно сильно облегчить.
Структурная формула (5)
(A'm-J)n
Структурная формула (6)
(J-A'm)n
В структурной формуле (5) A' представляет собой мономер гидрофильного материала, J представляет собой линкер, соединяющий m мономеров гидрофильного материала друг с другом или соединяющий m мономеров гидрофильного материала и олигонуклеотид друг с другом, m представляет собой целое число от 1 до 15, n представляет собой целое число от 1 до 10, и повторяющаяся единица, представленная (A'm-J) или (J-A'm), является основной единицей блока гидрофильного материала.
Когда предлагается блок гидрофильного материала, представленный структурной формулой (5) или структурной формулой (6), конструкция двухцепочечного олигонуклеотида, включающая CTGF-специфичный двухцепочечный олигонуклеотид по настоящему изобретению, может иметь структуру структурной формулы (7) или структурной формулы (8) ниже.
Структурная формула (7)
(A'm-J)n-X-R-Y-B
Структурная формула (8)
(J-A'm)n-X-R-Y-B
В структурной формуле (7) и структурной формуле (8) X, R, Y и B имеют значения, определенные в структурной формуле (1), а A', J, m и n имеют значения, определенные в структурной формуле (5) и структурной формуле (6).
В структурной формуле (5) и структурной формуле (6) любой мономер гидрофильного материала (A’) может быть использован без ограничений, если он соответствует цели настоящего изобретения среди мономеров неионогенного гидрофильного полимера. Предпочтительно используют мономер, выбранный из соединений (1) и соединений (3), показанных в таблице 1 ниже, более предпочтительно мономер соединения (1), и G в соединении (1) предпочтительно выбирают из O, S и NH.
В частности, среди мономеров гидрофильных материалов мономер, представленный соединением (1), который может быть введен с различными функциональными группами, может проявлять превосходную биосовместимость, такую как наличие хорошей аффинности in vivo и меньший иммунный ответ, и может иметь преимущество увеличения стабильности in vivo двухцепочечного олигонуклеотида, содержащегося в конструкции в соответствии со структурной формулой (7) или структурной формулой (8), и повышения эффективности доставки, поэтому данный мономер наиболее подходит для получения конструкции в соответствии с настоящим изобретением.
Таблица 1. Структура мономера гидрофильного материала в настоящем изобретении
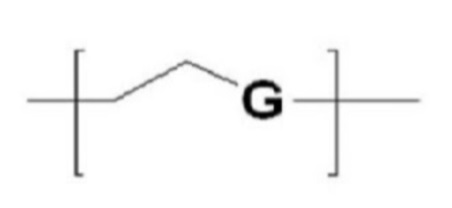
G является O, S или NH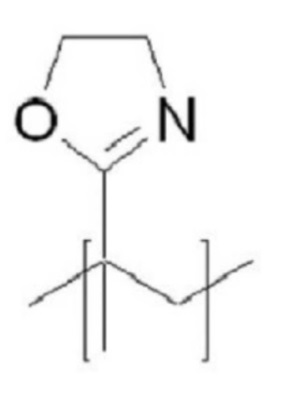

Гидрофильный материал структурной формулы (5) - структурной формулы (8) предпочтительно имеет общую молекулярную массу в диапазоне от 1000 до 2000. Так, например, в структурной формуле (7) и структурной формуле (8), когда используется гексаэтиленгликоль в соответствии с соединением (1), а именно вещество, в котором G представляет собой О, а m равно 6, молекулярная масса гексаэтилен гликолевый спейсер равна 344, и, таким образом, количество повторов (n) предпочтительно составляет от 3 до 5. В частности, повторяющееся звено гидрофильной группы, представленное (A'm-J)n или (J-A'm)n в структурной формуле (5) и структурной формуле (6), а именно блок гидрофильного материала, может быть использован в соответствующем количестве, представленном n, в зависимости от необходимости. Мономер А гидрофильного материала и линкер J, включенные в каждый блок гидрофильного материала, могут быть независимо друг от друга одинаковыми или разными между блоками гидрофильного материала. В частности, когда используются три блока гидрофильного материала (n=3), для соответствующих блоков гидрофильного материала можно использовать разные мономеры гидрофильного материала, например, можно использовать мономер гидрофильного материала в соответствии с соединением (1) для первого блока, мономер гидрофильного материала в соответствии с соединением (2) для второго блока и мономером гидрофильного материала в соответствии с соединением (3) для третьего блока или, альтернативно, любым мономером гидрофильного материала, выбранным из мономеров гидрофильного материала в соответствии с соединениями (1)-(3) можно одинаково использовать для всех блоков гидрофильного материала. Подобным образом, в качестве линкера, который опосредует связывание мономеров гидрофильного материала, для блоков гидрофильного материала можно использовать один и тот же или разные линкеры. Кроме того, m, которое представляет собой количество мономеров гидрофильного материала, может быть одинаковым или различным между блоками гидрофильного материала. В частности, можно использовать различное количество мономеров гидрофильного материала таким образом, что три мономера гидрофильного материала связаны (m=3) в первом блоке гидрофильного материала, пять мономеров гидрофильного материала связаны (m=5) во втором блоке гидрофильного материала, и четыре мономера гидрофильного материала связаны (m=4) в третьем блоке гидрофильного материала, или, альтернативно, одинаковое количество мономеров гидрофильного материала может быть использовано для всех блоков гидрофильного материала.
Кроме того, в настоящем изобретении линкер (J) предпочтительно выбирают из группы, состоящей из -PO3--, -SO3- и -CO2-, без ограничения указанным. Можно использовать любой линкер, если он соответствует цели настоящего изобретения, в зависимости от используемого мономера гидрофильного материала, как будет очевидно специалистам в данной области.
Гидрофобный материал (В) в структурной формуле (1) - структурной формуле (4) и в структурной формуле (7) и структурной формуле (8) служит для образования наночастиц, состоящих из конструкции двухцепочечного олигонуклеотида в соответствии со структурной формулой (1) - структурной формулой (4) и согласно формуле (7) и структурной формуле (8) за счет гидрофобного взаимодействия. Гидрофобный материал предпочтительно имеет молекулярную массу от 250 до 1000, и его примеры могут включать, без ограничения указанным, стероидное производное, глицеридное производное, эфир глицерина, полипропиленгликоль, ненасыщенный или насыщенный углеводород С12-С50, диацилфосфатидилхолин, жирную кислоту, фосфолипиды, липополиамины и т.п. Можно использовать любой гидрофобный материал при условии, что он соответствует цели настоящего изобретения, как будет очевидно специалистам в данной области техники.
Стероидное производное может быть выбрано из группы, состоящей из холестерина, холестанола, холевой кислоты, холестерилформиата, холестанилформиата и холестериламина, а глицеридное производное может быть выбрано из моно-, ди- и триглицеридов. В данном документе жирная кислота глицерида предпочтительно представляет собой ненасыщенную или насыщенную жирную кислоту С12-С50.
В частности, среди примеров гидрофобного материала предпочтительными являются насыщенный или ненасыщенный углеводород или холестерин, поскольку они облегчают связывание на стадии синтеза двухцепочечной олигонуклеотидной конструкции по настоящему изобретению, а углеводород С24, в частности, в форме, включающей дисульфидную связь, является наиболее предпочтительным.
Гидрофобный материал связан с дистальным концом гидрофильного материала и может быть связан с любым положением смысловой цепи или антисмысловой цепи siRNA.
CTGF-специфичный двухцепочечный олигонуклеотид и гидрофильный или гидрофобный материал в структурной формуле (1) - структурной формуле (4) и в структурной формуле (7) и структурной формуле (8) по настоящему изобретению связаны простой ковалентной связью или линкер-опосредованной ковалентной связью (X или Y). Линкер, опосредующий ковалентную связь, ковалентно связан с гидрофильным материалом или гидрофобным материалом на конце CTGF-специфичного двухцепочечного олигонуклеотида и ничем конкретно не ограничен, при условии, что он обеспечивает расщепляемую связь в определенной среде, при необходимости. Следовательно, линкер может представлять собой любое соединение, которое связывается для активации CTGF-специфичного двухцепочечного олигонуклеотида и/или гидрофильного материала (или гидрофобного материала) во время получения конструкции двухцепочечного олигонуклеотида по настоящему изобретению. Ковалентная связь может быть либо неразлагаемой связью, либо разлагаемой связью. В данном документе неразлагаемая связь включает амидную связь или фосфатную связь, а разлагаемая связь включает дисульфидную связь, разлагаемую кислотой связь, сложноэфирную связь, ангидридную связь, биоразлагаемую связь или ферментативно разлагаемую связь, но настоящее изобретение не ограничивается этим.
Кроме того, CTGF-специфичный двухцепочечный олигонуклеотид, представленный R (или S и AS) в структурной формуле (1) - структурной формуле (4) и в структурной формуле (7) и структурной формуле (8), может быть использован без ограничения указанным, при условии, что это двухцепочечный олигонуклеотид, способный специфически связываться с мРНК CTGF. Предпочтительно в настоящем изобретении он состоит из смысловой цепи, включающей любую одну последовательность, выбранную из SEQ ID NO: 1, 2, 10 и 15, и антисмысловой цепи, включающей комплементарную ей последовательность.
В конструкции двухцепочечного олигонуклеотида, включающей CTGF-специфичный двухцепочечный олигонуклеотид по настоящему изобретению, аминогруппа или полигистидиновая группа могут быть дополнительно введены в конец гидрофильного материала, противоположный концу, с которым связан олигонуклеотид.
Это облегчает внутриклеточное введение носителя и эндосомальное ускользание с помощью конструкции двухцепочечного олигонуклеотида, включающей CTGF-специфичный двухцепочечный олигонуклеотид по настоящему изобретению, и для облегчения внутриклеточного введения носителей, таких как квантовые точки, дендримеры, и липосомы, и эндосомальное ускользание, сообщалось о введении аминогруппы и использование полигистидиновой группы и их эффектах.
В частности, известно, что первичная аминогруппа, модифицированная на конце или снаружи носителя, образует конъюгат за счет электростатического взаимодействия с отрицательно заряженным геном при протонировании при pH in vivo, а также что носитель может быть защищен от деградации в лизосоме, потому что эндосомальное ускользание облегчается благодаря внутреннему третичному амину, обладающему буферным эффектом при низком pH эндосомы после внутриклеточного введения (Gene transfer and expression inhibition using polymer-based hybrid material. Polymer Sci. Technol., Vol. 23, No.3, pp254-259).
Известно, что гистидин, являющийся заменимой аминокислотой, имеет имидазольное кольцо (pKR 6,04) в остатке (-R) и, таким образом, увеличивает буферную способность в эндосомах и лизосомах, поэтому модификация гистидина может использоваться для увеличения эффективности эндосомального ускользания в невирусных носителях генов, включая липосомы (Novel histidine-conjugated galactosylated cationic liposomes for efficient hepatocyte selective gene transfer in human hepatoma HepG2 cells. J. Controlled Release 118, pp262-270).
Аминогруппа или полигистидиновая группа могут быть связаны с гидрофильным материалом или блоком гидрофильного материала по меньшей мере через один линкер.
Когда аминогруппу или полигистидиновую группу вводят в гидрофильный материал конструкции двухцепочечного олигонуклеотида в соответствии со структурной формулой (1) по настоящему изобретению, может быть получена структура, представленная структурной формулой (9) ниже.
Структурная формула (9)
P-J1-J2-A-X-R-Y-B
В структурной формуле (9) A, B, R, X и Y имеют значения, определенные в структурной формуле (1).
Кроме того, P представляет собой аминогруппу или полигистидиновую группу, а J1 и J2 представляют собой линкеры. В данном документе J1 и J2 могут быть независимо выбраны из простой ковалентной связи, PO3-, SO3, CO2, C2-12 алкила, алкенила и алкинила, без ограничения указанным, и любой линкер может быть использован в качестве J1 и J2, соответствующих цели настоящего изобретения, в зависимости от используемого гидрофильного материала, как будет очевидно специалистам в данной области техники.
При введении аминогруппы предпочтительно, чтобы J2 представлял собой простую ковалентную связь или PO3- и чтобы J1 представлял собой C6-алкил, но настоящее изобретение не ограничивается этим.
Кроме того, когда в структурную формулу (9) вводится полигистидиновая группа, предпочтительно, чтобы J2 представлял собой простую ковалентную связь или PO3-, и чтобы J1 представлял собой соединение (4), но настоящее изобретение не ограничивается этим.
Соединение (4)

Кроме того, когда гидрофильный материал конструкции двухцепочечного олигонуклеотида в соответствии со структурной формулой (9) представляет собой блок гидрофильного материала в соответствии со структурной формулой (5) или структурной формулой (6) и в него введена аминогруппа или полигистидиновая группа, может быть обеспечена структура, представленная структурной формулой (10) или структурной формулой (11) ниже.
Структурная формула (10)
P-J1-J2-(A'm-J)n-X-R-Y-B
Структурная формула (11)
P-J1-J2-(J-A'm)n-X-R-Y-B
В структурной формуле (10) и структурной формуле (11) X, R, Y, B, A', J, m и n имеют значения, определенные в структурной формуле (5) или структурной формуле (6), а P, J1 и J2 определены в структурной формуле (9).
В частности, в структурной формуле (10) и структурной формуле (11) гидрофильный материал предпочтительно находится в форме, связанной с 3'-концом смысловой цепи CTGF-специфичного двухцепочечного олигонуклеотида. В данном документе структурная формула (9) - структурная формула (11) может быть представлена структурной формулой (12) - структурной формулой (14) ниже.
Структурная формула (12)

Структурная формула (13)

Структурная формула (14)

В структурной формуле (12) - структурной формуле (14) X, R, Y, B, A, A' J, m, n, P, J1 и J2 имеют значения, определенные в структурной формуле (9) - структурной формуле (11), а 5' и 3', соответственно, представляют собой 5'-конец и 3'-конец смысловой цепи CTGF-специфичного двухцепочечного олигонуклеотида.
Аминогруппа, которая может быть введена в настоящем изобретении, может включать первичные и третичные аминогруппы, особенно предпочтительно первичную аминогруппу. Вводимая аминогруппа может быть представлена в виде соли амина, а соль первичной аминогруппы может быть представлена, например, в форме NH3+.
Кроме того, полигистидиновая группа, которая может быть введена в настоящем изобретении, может включать от 3 до 10 гистидинов, предпочтительно от 5 до 8 гистидинов, наиболее предпочтительно 6 гистидинов. Кроме того, помимо гистидина может быть включен по меньшей мере один цистеин.
В то же время, когда направляющая группа обеспечивается двухцепочечной олигонуклеотидной конструкцией, включающей CTGF-специфичный двухцепочечный олигонуклеотид по настоящему изобретению и образованные из него наночастицы, может быть обеспечена эффективная доставка в клетку-мишень и, таким образом, его доставка в клетки-мишени возможна даже при относительно низкой концентрации, тем самым проявляя сильный эффект регуляции экспрессии гена-мишени и предотвращая доставку неспецифического CTGF-специфичного двухцепочечного олигонуклеотида в другие органы и клетки.
Соответственно, настоящее изобретение относится к конструкции двухцепочечной олигоРНК, в которой лиганд (L), в частности лиганд, который специфически связывается с рецептором, который способствует интернализации клетки-мишени посредством рецептор-опосредованного эндоцитоза (RME), дополнительно связан с конструкцией в соответствии со структурной формулой (1) - структурной формулой (4) и в соответствии со структурной формулой (7) и структурной формулой (8). Например, форма, в которой лиганд связан с конструкцией двухцепочечной олигоРНК в соответствии со структурной формулой (1), имеет структуру структурной формулы (15) ниже.
Структурная формула (15)
(Li-Z)-A-X-R-Y-B
В структурной формуле (15) A, B, X и Y имеют значения, определенные в структурной формуле (1), L представляет собой лиганд, который специфически связывается с рецептором, который способствует интернализации клетки-мишени посредством рецептор-опосредованного эндоцитоза (RME), и i представляет собой целое число от 1 до 5, предпочтительно целое число от 1 до 3.
Лиганд в структурной формуле (15) предпочтительно выбирают из антител, аптамеров и пептидов, специфичных к рецептору-мишени, обладающих свойствами RME, которые способствуют интернализации клеток, специфичных для клетки-мишени; и химических веществ, включая фолат (обычно фолат и фолиевая кислота используются взаимозаменяемо, и фолат в настоящем изобретении относится к фолату в естественном или активированном состоянии в организме человека), гексозаминов, таких как N-ацетилгалактозамин (NAG), и сахаров или углеводов, таких как глюкоза и манноза, без ограничения указанным.
Кроме того, гидрофильный материал А в структурной формуле (15) может быть использован в форме блока гидрофильного материала в соответствии со структурной формулой (5) и структурной формулой (6).
Еще один аспект настоящего изобретения относится к способу получения конструкции двухцепочечного олигонуклеотида, включающей CTGF-специфичный двухцепочечный олигонуклеотид.
Способ получения конструкции двухцепочечного олигонуклеотида, включающей CTGF-специфичный двухцепочечный олигонуклеотид по настоящему изобретению, включает, например:
(1) связывание гидрофильного материала с твердой подложкой;
(2) синтез одноцепочечного олигонуклеотида на твердом носителе, с которым связан гидрофильный материал;
(3) ковалентное связывание гидрофобного материала с 5'-концом одноцепочечного олигонуклеотида;
(4) синтез одноцепочечного олигонуклеотида, имеющего последовательность, комплементарную последовательности одноцепочечного олигонуклеотида;
(5) отделение и очистку конструкции олигонуклеотид/полимер и одноцепочечного олигонуклеотида от твердой подложки после завершения синтеза; и
(6) получение конструкции двухцепочечного олигонуклеотида путем отжига конструкции олигонуклеотид/полимер и одноцепочечного олигонуклеотида, имеющего комплементарную последовательность.
Твердая подложка в настоящем изобретении предпочтительно представляет собой стекло с контролируемым размером пор (CPG), без ограничения указанным, и могут быть использованы полистирол (PS), полиметилметакрилат (PMMA), силикагель, целлюлозная бумага и т.д. CPG предпочтительно имеет диаметр от 40 до 180 мкм и размер пор от 500 до 3000 Å. После стадии (5) молекулярные массы очищенной РНК/полимерной конструкции и одноцепочечного олигонуклеотида измеряют с использованием масс-спектрометра MALDI-TOF, чтобы определить, продуцируются ли желаемая олигонуклеотидная/полимерная конструкция и одноцепочечный олигонуклеотид. В способе получения, описанном выше, стадия (4) синтеза одноцепочечного олигонуклеотида, имеющего последовательность, комплементарную последовательности одноцепочечного олигонуклеотида, синтезированного на стадии (2), может быть осуществлена до стадии (1) или во время любой из стадий (1) – (5).
Кроме того, одноцепочечный олигонуклеотид, имеющий последовательность, комплементарную последовательности одноцепочечного олигонуклеотида, синтезированного на стадии (2), можно использовать в форме, в которой фосфатная группа связана с 5'-концом.
Кроме того, предлагается способ получения конструкции двухцепочечного олигонуклеотида, в которой лиганд дополнительно связан с двухцепочечной олигонуклеотидной конструкцией, включая CTGF-специфичный двухцепочечный олигонуклеотид по настоящему изобретению.
Способ получения связанной с лигандом конструкции двухцепочечного олигонуклеотида, включающей CTGF-специфичный двухцепочечный олигонуклеотид, включает, например:
(1) связывание гидрофильного материала с твердой подложкой, с которой связана функциональная группа;
(2) синтез одноцепочечного олигонуклеотида на твердом носителе, с которым связаны функциональная группа и гидрофильный материал;
(3) ковалентное связывание гидрофобного материала с 5'-концом одноцепочечного олигонуклеотида;
(4) синтез одноцепочечного олигонуклеотида, имеющего последовательность, комплементарную последовательности одноцепочечного олигонуклеотида;
(5) отделение конструкции функциональная группа/олигонуклеотид/полимер и одноцепочечного олигонуклеотида, имеющего комплементарную последовательность, от твердой подложки после завершения синтеза;
(6) получение конструкции лиганд/олигонуклеотид/полимер в форме одной цепи путем связывания лиганда с концом гидрофильного материала с использованием функциональной группы; и
(7) получение конструкции лиганд/двухцепочечный олигонуклеотид путем отжига конструкции лиганд/олигонуклеотид/полимер и одноцепочечного олигонуклеотида, имеющего комплементарную последовательность.
После стадии (6) полученную конструкцию лиганд/олигонуклеотид/полимер и одноцепочечный олигонуклеотид, имеющий комплементарную последовательность, разделяют и очищают, а затем измеряют их молекулярные массы с использованием масс-спектрометра MALDI-TOF, чтобы определить, продуцируется ли желаемая конструкция лиганд/олигонуклеотид/полимер и комплементарный олигонуклеотид. Конструкция лиганд/двухцепочечный олигонуклеотид может быть получена путем отжига конструкции лиганд/олигонуклеотид/полимер и одноцепочечного олигонуклеотида, имеющего комплементарную последовательность. В способе получения, описанном выше, стадия (4) синтеза одноцепочечного олигонуклеотида, имеющего последовательность, комплементарную последовательности одноцепочечного олигонуклеотида, синтезированного на стадии (3), может быть независимым процессом синтеза и может выполняться до стадии (1) или во время любой из стадий (1)-(6).
Еще один аспект настоящего изобретения относится к наночастицам, включая конструкцию двухцепочечного олигонуклеотида по настоящему изобретению. Конструкция двухцепочечного олигонуклеотида по настоящему изобретению образует самособирающиеся наночастицы за счет гидрофобного взаимодействия гидрофобного материала (корейский патент № 1224828). Эти наночастицы не только обладают значительно более высокой эффективностью доставки в организм и стабильностью in vivo, но также имеют превосходную однородность размера частиц, что облегчает контроль качества (QC), тем самым упрощая процесс изготовления лекарственного средства.
В настоящем изобретении наночастицы могут быть охарактеризованы тем, что смешиваются двухцепочечные олигонуклеотидные конструкции, содержат двухцепочечные олигонуклеотиды, включающие разные последовательности. В одном воплощении наночастицы могут включать один тип CTGF-специфичного двухцепочечного олигонуклеотида, включая смысловую цепь, включающую любую одну последовательность, выбранную из SEQ ID NO: 1, 2, 10 и 15, и антисмысловую цепь, включающую комплементарную ей последовательность, и в другом воплощении наночастицы могут включать различные типы CTGF-специфических двухцепочечных олигонуклеотидов, включая смысловую цепь, включающую любую одну последовательность, выбранную из SEQ ID NO: 1, 2, 10 и 15, и антисмысловую цепь, включающую комплементарную последовательность, и может также включать CTGF-специфичный двухцепочечный олигонуклеотид, не раскрытый в настоящем изобретении.
Еще один аспект настоящего изобретения относится к фармацевтической композиции для профилактики или лечения фиброза или респираторного заболевания, содержащей двухцепочечный олигонуклеотид, конструкцию двухцепочечного олигонуклеотида или наночастицы по настоящему изобретению в качестве активного ингредиента.
Фармацевтическая композиция для профилактики или лечения фиброза или респираторного заболевания по настоящему изобретению ингибирует ремоделирование соединительной ткани, в частности ремоделирование легочной артерии и ремоделирование дыхательных путей, и, таким образом, эффективно предотвращает или лечит фиброз или респираторное заболевание.
В настоящем изобретении респираторное заболевание может представлять собой хроническую обструктивную болезнь легких (COPD), астму, острый и хронический бронхит, аллергический ринит, продуктивный кашель, бронхит, бронхиолит, ларингофарингит, тонзиллит или ларингит, а фиброз может быть выбран из числа идиопатического легочного фиброза (IPF), фиброза печени, цирроза, миелофиброза, миокардиального фиброза, почечного фиброза, келоида, легочного фиброза, сердечного фиброза и радиационно-индуцированного фиброза, но настоящее изобретение не ограничивается этим. В настоящем изобретении радиационно-индуцированный фиброз является побочным эффектом, часто вызываемым лучевой терапией, обычно используемой для лечения онкологического заболевания, опухолей и т.д., и может использоваться взаимозаменяемо с синдромом радиационного фиброза (RFS).
Композицию по настоящему изобретению можно приготовить, включив для введения по меньшей мере один фармацевтически приемлемый носитель в дополнение к активному ингредиенту, описанному выше. Фармацевтически приемлемый носитель должен быть совместим с активным ингредиентом по настоящему изобретению и может включать физиологический раствор, стерильную воду, раствор Рингера, забуференный физиологический раствор, раствор декстрозы, раствор мальтодекстрина, глицерин и этанол, которые можно использовать отдельно или в комбинации с двумя или более из них. При необходимости могут быть добавлены другие типичные добавки, такие как антиоксиданты, буферы и бактериостаты. Кроме того, могут быть дополнительно добавлены разбавители, диспергаторы, поверхностно-активные вещества, связующие вещества и смазывающие вещества для получения инъекционного состава, такого как водный раствор, суспензия, эмульсия и т.п. В частности, предпочтительно обеспечивается лиофилизированный состав. Для приготовления лиофилизированного состава можно использовать способ, широко известный в данной области, к которому относится настоящее изобретение, и можно добавить стабилизатор для лиофилизации. Предпочтительно можно приготовить состав в зависимости от каждого заболевания или компонента с использованием соответствующего способа в данной области техники или способа, раскрытого в Remington’s Pharmaceutical Science (Mack Publishing Company, Истон, Пенсильвания).
Тип композиции по настоящему изобретению может быть определен специалистами в данной области на основании симптомов типичного пациента и тяжести заболевания. Кроме того, он может быть приготовлен в различных формах, таких как порошки, таблетки, капсулы, растворы, инъекции, мази, сиропы и т.п., и может поставляться в контейнерах для однократной или многократной дозы, например, в запаянных ампулах и бутылках.
Композицию по настоящему изобретению можно вводить перорально или парентерально. Способ введения композиции по настоящему изобретению не ограничивается этим и, например, возможен пероральный, ингаляционный, внутривенный, внутримышечный, внутриартериальный, интрамедуллярный, интрадуральный, внутрисердечный, трансдермальный, подкожный, внутрибрюшинный, энтеральный, подъязычный или местный. В частности, для лечения респираторного заболевания также возможно введение в легкие путем эндобронхиальной инстилляции. Дозировка композиции по настоящему изобретению варьирует в зависимости от массы тела пациента, возраста, пола, состояния здоровья, диеты, времени введения, способа, скорости выделения, тяжести заболевания и т.д. и может быть легко определена специалистом в данной области. Кроме того, композиция по настоящему изобретению может быть приготовлена в виде подходящей лекарственной формы для клинического введения с использованием известных способов.
Еще один аспект настоящего изобретения относится к лиофилизированному составу, включающему фармацевтическую композицию по настоящему изобретению.
Еще один аспект настоящего изобретения относится к способу профилактики или лечения фиброза или респираторного заболевания, включающему введение фармацевтической композиции для профилактики или лечения фиброза или респираторного заболевания по настоящему изобретению объекту, нуждающемуся в профилактике или лечении фиброза или респираторного заболевания.
В настоящем изобретении респираторное заболевание может представлять собой хроническую обструктивную болезнь легких (COPD), астму, острый и хронический бронхит, аллергический ринит, продуктивный кашель, бронхит, бронхиолит, ларингофарингит, тонзиллит или ларингит, а фиброз может быть идиопатическим легочным фиброзом. (IPF), цирроз, миелофиброз, фиброз миокарда, почечный фиброз, келоид, легочный фиброз, сердечный фиброз, фиброз печени или радиационно-индуцированный фиброз, но настоящее изобретение не ограничивается этим.
Еще один аспект настоящего изобретения относится к применению двухцепочечного олигонуклеотида, конструкции двухцепочечного олигонуклеотида, включающей двухцепочечный олигонуклеотид, и наночастиц, включающих их, для профилактики или лечения фиброза или респираторного заболевания.
Еще один аспект настоящего изобретения относится к применению фармацевтической композиции для профилактики или лечения фиброза или респираторного заболевания.
Еще один аспект настоящего изобретения относится к применению двухцепочечного олигонуклеотида, конструкции двухцепочечного олигонуклеотида, включающей двухцепочечный олигонуклеотид, и наночастиц, включающих двухцепочечный олигонуклеотид или конструкцию двухцепочечного олигонуклеотида для профилактики или лечения фиброза или респираторного заболевания.
Еще один аспект настоящего изобретения относится к способу профилактики или лечения фиброза или респираторного заболевания, включающему введение двухцепочечного олигонуклеотида, конструкции двухцепочечного олигонуклеотида и/или наночастиц объекту, нуждающемуся в профилактике или лечение фиброза или респираторного заболевания.
Еще один аспект настоящего изобретения относится к применению двухцепочечного олигонуклеотида, конструкции двухцепочечного олигонуклеотида, включающей двухцепочечный олигонуклеотид, и наночастиц, включающих двухцепочечный олигонуклеотид или конструкцию двухцепочечного олигонуклеотида для изготовления лекарственного средства для профилактики или лечения фиброза или респираторного заболевания.
Описание чертежей
Фиг. 1 показаны результаты скрининга 1162 SAMiRNA, нацеленных на человеческий CTGF, включая результаты количественного анализа уровня экспрессии мРНК CTGF в Примере 3;
фиг. 2 представляет собой график, показывающий результаты количественного анализа уровня экспрессии мРНК CTGF в примере 4, в котором относительный уровень экспрессии мРНК (%) CTGF определяли после обработки клеточной линии рака легкого A549 с помощью SAMiRNA, имеющей в качестве смысловой цепи, каждую из последовательностей SEQ ID NO: 1, 2, 10 и 15 по настоящему изобретению в различных концентрациях (50, 100, 200, 500 и 1000 нМ);
фиг. 3 представляет собой график, показывающий результаты количественного анализа уровня экспрессии мРНК CTGF в Примере 4, в котором значение IC50 SAMiRNA определяли путем анализа относительного уровня экспрессии мРНК (%) CTGF после обработки клеточной линии рака легкого A549 с помощью SAMiRNA, имеющей в качестве смысловой цепи последовательность SEQ ID NO: 10 по настоящему изобретению в различных концентрациях;
фиг. 4 представляет собой график, показывающий результаты количественного анализа уровня экспрессии мРНК CTGF в Примере 4, в котором значение IC50 для SAMiRNA определяли путем анализа относительного уровня экспрессии мРНК (%) CTGF после обработки SAMiRNA, имеющей в качестве смысловой нити, каждую из последовательностей SEQ ID NO: 10 по настоящему изобретению и последовательности Rxi-109;
фиг. 5 представляет собой график, показывающий результаты количественного анализа уровня экспрессии мРНК CTGF в Примере 5, в котором относительный уровень экспрессии мРНК (%) CTGF анализировали с использованием двухцепочечного гибрида олиго-ДНК/РНК и гибрида РНК/РНК, включающих выбранную CTGF-специфическую SAMiRNA, и относительный уровень экспрессии мРНК (%) CTGF определяли после обработки линии клеток рака легкого A549 с помощью SAMiRNA, имеющей в качестве смысловой цепи последовательность SEQ ID NO: 10 по настоящему изобретению в различных концентрациях (200 нМ и 600 нМ);
фиг. 6 показаны результаты скрининга 94 SAMiRNA, нацеленных на CTGF крысы, и эффекты 12 последовательностей-кандидатов, выбранных из них;
фиг. 7 представляет собой график, показывающий результаты количественного анализа уровня экспрессии мРНК крысиного CTGF в примере 6, в котором относительный уровень экспрессии мРНК (%) крысиного CTGF определяли после обработки клеточной линии рака печени крысы H4-II- E с помощью SAMiRNA, имеющей в качестве смысловой цепи каждую из 12 выбранных последовательностей-кандидатов, включающих последовательности SEQ ID NO: 46, 47 и 48 по настоящему изобретению в различных концентрациях (200 нМ и 500 нМ);
фиг. 8 представляет собой графики, показывающие результаты количественного анализа уровня экспрессии мРНК крысиного CTGF в примере 6, в котором значение IC50 для SAMiRNA определяли путем анализа относительного уровня экспрессии мРНК (%) крысиного CTGF после обработки клеточной линии рака печени крысы H4-II-E с помощью SAMiRNA, имеющей в качестве смысловой цепи, каждую из последовательностей SEQ ID NO: 46, 47 и 48 по настоящему изобретению в различных концентрациях (25, 50, 100, 200, 400 и 800 нМ);
фиг. 9 представляет собой график, показывающий результаты количественного анализа уровня экспрессии мРНК CTGF крысы в примере 6, в котором относительный уровень экспрессии мРНК (%) CTGF крысы анализировали с использованием двухцепочечного гибрида олиго-ДНК/РНК и гибрида РНК/РНК, включающий выбранную SAMiRNA, специфическую к CTGF крысы, и относительный уровень экспрессии мРНК (%) CTGF крысы определяли после обработки клеточной линии рака печени H4-II-E с помощью SAMiRNA, имеющей в качестве смысловой цепи каждую из последовательности SEQ ID NO: 46, 47 и 48 по настоящему изобретению в различных концентрациях (200 нМ и 600 нМ); и
фиг. 10 представляет собой график, показывающий результаты ПЦР-анализа в реальном времени кожной ткани после внутрикожного введения 1200 мкг каждого из SAMiRNA-rCTGF(D/R)#46 и SAMiRNA-rCTGF(R/R)#46 в мышиной модели раневого келоида в Примере 7 и относительный уровень экспрессии мРНК (%) гена-мишени CTGF.
Принцип изобретения
Лучшее понимание настоящего изобретения может быть получено с помощью следующих примеров. Эти примеры приведены просто для иллюстрации настоящего изобретения и не рассматриваются как ограничивающие объем настоящего изобретения, как будет очевидно специалистам в данной области техники. Следовательно, существенный объем настоящего изобретения будет определяться прилагаемой формулой изобретения и ее эквивалентами.
В настоящем изобретении было подтверждено, что в конечном итоге была идентифицирована специфическая последовательность, способная ингибировать экспрессию CTGF, и экспрессия CTGF эффективно ингибировалась за счет комплементарного связывания с мРНК, кодирующей CTGF, что приводит к эффективному лечению фиброза и респираторных заболеваний.
Пример 1. Алгоритм скрининга SAMiRNA, нацеленных на CTGF, и выбор последовательностей-кандидатов
Высокопроизводительный скрининг лекарственных средств на основе SAMiRNA — это способ генерации всех возможных последовательностей-кандидатов путем применения алгоритма скользящего окна с одним или двумя основаниями ко всему образцу мРНК, удаления ненужных последовательностей-кандидатов путем гомологической фильтрации и определения степени ингибирования экспрессии соответствующего гена всеми окончательно отобранными SAMiRNA.
Процесс конструирования последовательностей-кандидатов SAMiRNA для CTGF был выполнен таким образом, что алгоритм скользящего окна с двумя основаниями был применен к NM_001901.2 (2358 п.о.), который представляет собой мРНК CTGF человека, чтобы, таким образом, окончательно выбрать 1162 последовательности-кандидата SAMiRNA, каждая из которых состоит из 19 нуклеотидов, и таким образом оценивали степень ингибирования CTGF.
Пример 2. Синтез конструкции двухцепочечной олигоРНК
Конструкция двухцепочечной олигоРНК (SAMiRNA), полученная в соответствии с настоящим изобретением, имеет структуру в соответствии со следующей структурной формулой.
С24-5' S 3'-(гексаэтиленгликоль-PO4-)3- гексаэтиленгликоль
AS 5'-PO4
Смысловая цепь двухцепочечной олигоконструкции monoSAMiRNA (n=4) была синтезирована таким образом, что три диметокситритил (DMT) гексаэтиленгликоль фосфорамидата, которые представляют собой мономеры гидрофильного материала, были последовательно связаны посредством описанной выше реакции с использованием 3,4,6-триацетил-1-гекса(этиленгликоль)-N-ацетилгалактозамин-CPG в качестве носителя, проводили синтез РНК или ДНК, а затем C24(C6-S-S-C18), содержащий дисульфидную связь, который является гидрофобным материалом, связывали с 5'-концом, таким образом получая смысловую цепь monoSAMiRNA (n=4), в которой NAG-гексаэтиленгликоль-(-PO3-гексаэтиленгликоль)3 был связан с 3'-концом, а C24(C6-S-S-C18) был привязан к 5'-концу.
После завершения синтеза синтезированную конструкцию одноцепочечной РНК и олиго(ДНК или РНК)/полимера отделяли от CPG с использованием 28% (об./об.) аммиака на водяной бане при 60°С с последующей реакцией снятия защиты для удаления защитных остатков. После удаления защитных остатков конструкцию одноцепочечной РНК и олиго(ДНК или РНК)/полимера обрабатывали N-метилпирролидоном, триэтиламином и триэтиламинтригидрофторидом в объемном соотношении 10:3:4 в печи при 70°С для удаления 2'-диметилсилила. Конструкцию одноцепочечной РНК и олиго(ДНК или РНК)/полимера и конструкцию лиганд-связанного олиго(ДНК или РНК)/полимера отделяли от продуктов реакции с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ), а молекулярную их массу измеряли с использованием масс-спектрометра TOF (MALDI TOF-MS, SHIMADZU, Япония) для определения того, синтезированы ли нуклеотидная последовательность и конструкция олиго/полимера. После этого для получения каждой двухцепочечной олигоконструкции смысловую цепь и антисмысловую цепь смешивали в равных количествах, добавляли к 1X буферу для отжига (30 мМ HEPES, 100 мМ ацетата калия, 2 мМ ацетата магния, рН 7,0), оставляли реагировать на водяной бане с постоянной температурой при 90°C в течение 3 минут и снова оставляли реагировать при 37°C с образованием желаемой SAMiRNA. Отжиг полученных таким образом конструкций двухцепочечной олигоРНК подтверждали с помощью электрофореза.
Пример 3. Высокопроизводительный скрининг (HTS) наночастиц SAMiRNA, индуцирующих РНК-интерференцию, нацеленную на CTGF человека
3.1 Получение наночастиц SAMiRNA
1162 SAMiRNA, нацеленных на последовательность CTGF, синтезированных в примере 2, растворяли в 1X фосфатно-солевом буфере Дульбекко (DPBS) (WELGENE, KR) и лиофилизировали в течение 5 дней в лиофилизаторе (LGJ-100F, CN). Лиофилизированный порошок наночастиц растворяли и гомогенизировали в 1,429 мл деионизированной дистиллированной воды (Bioneer, KR) и использовали в экспериментах по настоящему изобретению.
3.2 Внутриклеточный процессинг наночастиц SAMiRNA
MDA-MB231, клеточную линию рака молочной железы человеческого происхождения, использовали для обнаружения SAMiRNA, которая ингибирует экспрессию CTGF, а клеточную линию MDA-MB231 культивировали при 37°C и 5% CO2 в среде Gibco™ RPMI 1640 (Thermo, США), содержащие 10% фетальной бычьей сыворотки (Hyclone, США) и 1% пенициллина-стрептомицина (Hyclone, США). Используя ту же среду, что и выше, клеточную линию MDA-MB231 распределяли с плотностью 2×104 клеток/лунку в 96-луночный планшет (Costar, США), а на следующий день SAMiRNA, гомогенизированную с деионизированной дистиллированной водой в примере 3.1, разбавляли до 200 нМ или 600 нМ 1X DPBS и добавляли к клеткам. Обработку клеток SAMiRNA проводили всего 4 раза, один раз каждые 12 часов, а культивирование проводили при 37°С и 5% СО2.
3.3 Скрининг SAMiRNA с помощью анализа ингибирующей эффективности экспрессии мРНК CTGF
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в Примере 3-2, и синтезировали в кДНК, после чего определяли относительный уровень экспрессии мРНК гена CTGF с помощью ПЦР в реальном времени.
Для анализа уровня экспрессии мРНК гена CTGF 300 нМ прямого праймера CTGF, 300 нМ обратного праймера CTGF, 300 нМ зонда CTGF, 200 нМ прямого праймера RPL13A, 200 нМ обратного праймера RPL13A, 300 нМ обратного праймера RPL13A, 300 нМ зонда RPL13A, 400 нМ прямого праймера TBP, 400 нМ обратного праймера TBP и 300 нМ зонда TBP добавляли в каждую лунку набора AccuPower® Dual-HotStart RT-qPCR (Bioneer, Корея) и сушили (таблица 2). Эффективность приготовленного набора определяли на основе эффективности амплификации ПЦР (таблица 3) путем создания калибровочной кривой с использованием общей РНК клеток A549. RT-qPCR проводили в условиях реакции 95°C в течение 10 минут, а затем (95°C в течение 5 секунд и 58°C в течение 15 секунд) x 45 циклов, после чего осуществляли протокол, в котором значение флуоресценции определяли в каждом цикле.
96-луночный планшет, обработанный SAMiRNA (Costar, США), подвергали экстракции тотальной РНК и одностадийной RT-qPCR в соответствии с автоматизированной программой с использованием ExiStation HT™ Korea, который представляет собой автоматизированный аппарат, выполняющий все процедуры экстракции тотальной РНК для RT-qPCR, набора для экстракции ДНК/РНК HT (Bioneer, Корея) и набора AccuPower® Dual-HotStart RT-qPCR (Bioneer, Корея), который готовят отдельно, включая праймеры и зонды для количественного анализа мРНК гена CTGF.
На основании значений Ct двух генов, полученных после массива qPCR, относительный уровень экспрессии мРНК (%) гена CTGF в экспериментальной группе по сравнению с контрольной группой был рассчитан посредством относительного количественного анализа с использованием метода 2(-Delta Delta C(T)) [Livak K. J., Schmittgen T. D. 2001. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T)) Method. Methods. Dec;25(4):402-8].
Таблица 2. Последовательности праймеров и зондов гидролиза, используемые в высокопроизводительном скрининге (HTS)
Таблица 3. Эффективность 3-плексной RT-qPCR амплификации
Пример 4. Скрининг наночастиц SAMiRNA, индуцирующих RNAi, направленно воздействующую на CTGF человека
Для отбора высокоэффективной SAMiRNA клеточную линию рака легкого A549 обрабатывали последовательностями, обладающими наибольшей эффективностью снижения уровня экспрессии мРНК CTGF в конечной концентрации 200 нМ или 600 нМ по сравнению с контрольной группой, а именно 16 последовательностями с эффективностью восстановления > 60% или более (результаты вторичного скрининга в общей сложности для 49 типов SAMiRNA-hCTGF) при концентрациях 500 нМ и 1000 нМ, а информация о последовательности соответствующей SAMiRNA показана в таблице 4 ниже.
После этого, для продолжения эксперимента, чтобы подтвердить эффект снижения уровня экспрессии (нокдаун) после обработки низкой концентрацией для определения  19мер/жирный = 2'OME/ подчеркивание = 2'F / звездочка = фосфоротиоат / chol = холестерин) (WO 2009/102427), третичный скрининг линии клеток рака легкого A549 на наличие восьми наиболее сильных последовательностей проводили при 50, 100, 200, 500 и 1000 нМ. Следовательно, были выбраны четыре SAMiRNA, имеющие последовательности SEQ ID NO: 1, 2, 10 и 15 в качестве соответствующих смысловых цепей.
19мер/жирный = 2'OME/ подчеркивание = 2'F / звездочка = фосфоротиоат / chol = холестерин) (WO 2009/102427), третичный скрининг линии клеток рака легкого A549 на наличие восьми наиболее сильных последовательностей проводили при 50, 100, 200, 500 и 1000 нМ. Следовательно, были выбраны четыре SAMiRNA, имеющие последовательности SEQ ID NO: 1, 2, 10 и 15 в качестве соответствующих смысловых цепей.
Как показано на фиг. 1, четыре SAMiRNA, которые наиболее эффективно ингибируют экспрессию гена CTGF, наконец, были выбраны из 1162 SAMiRNA, нацеленных на CTGF (фиг. 2).
Таблица 4. Кандидатные последовательности SAMiRNA, специфичные к CTGF, отобранные с помощью скрининга скользящего окна с двумя основаниями и скрининга с высокой пропускной способностью (HTS)
Линию клеток рака легкого A549 обрабатывали SAMiRNA, имеющей в качестве смысловой цепи каждую из последовательностей SEQ ID NO: 1, 2, 10 и 15, выбранных в примере 3, и анализировали в клеточной линии паттерн экспрессии мРНК CTGF.
4.1 Внутриклеточный процессинг наночастиц SAMiRNA
A549 (ATCC® CCL-185™, Манассас, Вирджиния), которая представляет собой клеточную линию рака легких человека, использовали для обнаружения SAMiRNA, которая ингибирует экспрессию CTGF, а клеточную линию A549 культивировали при 37°C и 5% CO2 в среде Gibco™ F-12K (Kaighn's) (Thermo, США), содержащей 10% фетальной бычьей сыворотки (Hyclone, США) и 1% пенициллина-стрептомицина (Hyclone, США). Используя ту же среду, что и выше, клеточную линию А549 распределяли с плотностью 8×104 клеток/лунку в 12-луночный планшет (Costar, США), и на следующий день SAMiRNA, гомогенизированную деионизированной дистиллированной водой в примере 3.1, разводили до 50, 100, 200, 500 или 1000 нМ с 1X DPBS и добавляли к клеткам. Обработку клеток SAMiRNA проводили всего 4 раза, один раз каждые 12 часов, а культивирование проводили при 37°С и 5% СО2.
4.2 Скрининг SAMiRNA посредством анализа эффективности ингибирования экспрессии мРНК CTGF человека
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 4-1, и синтезировали в кДНК, а затем количественно определяли относительный уровень экспрессии мРНК гена CTGF с использованием ПЦР в реальном времени.
4-2-1 Выделение РНК из обработанных SAMiRNA клеток и синтез кДНК
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 4-1, с использованием набора для выделения РНК (набор для экстракции тотальной РНК AccuPrep Cell, Bioneer, Корея), и экстрагированную РНК синтезировали в кДНК с использованием обратной транскриптазы РНК (AccuPower® RocketScript™ Cycle RT Premix с олиго(dT)20, Bioneer, Корея) следующим образом. В частности, 1 мкг экстрагированной РНК добавляли к премиксу AccuPower RocketScript™RT с олиго(dT) 20 (Bioneer, Корея), содержащемуся в каждой из пробирок Eppendorf объемом 0,25 мл, и туда же добавляли дистиллированную воду, обработанную DEPC (диэтилпирокарбонатом), для достижения общего объема 20 мкл. В системе амплификации генов (MyGenie™ Gradient Thermal Block, Bioneer, Корея) два процесса гибридизации РНК с праймерами при 37°С в течение 30 секунд и синтеза кДНК при 48°С в течение 4 минут повторяли 12 раз, после чего реакцию амплификации останавливали путем дезактивации фермента при 95°С в течение 5 минут.
4-2-2 Относительный количественный анализ мРНК CTGF человека
Относительный уровень экспрессии мРНК CTGF по сравнению с контрольным образцом SAMiRNA анализировали следующим образом с помощью SYBR green qPCR в реальном времени с использованием кДНК, синтезированной в примере 4-2-1, в качестве матрицы. В частности, кДНК, синтезированную в примере 4-2-1, разбавляли в 5 раз дистиллированной водой и для анализа уровня экспрессии мРНК CTGF 3 мкл разведенной кДНК, 25 мкл AccuPower® GreenStar™ (Корея). В каждую лунку 96-луночного планшета добавляли 19 мкл дистиллированной воды и 3 мкл праймеров CTGF для количественной ПЦР (SEQ ID NO: 7 и 8 (таблица 5); 10 пмоль/мкл соответственно, Bioneer, Корея) для получения смешанного раствора. Между тем, чтобы нормализовать уровень экспрессии мРНК CTGF, в качестве стандартного гена использовали GAPDH (глицеральдегид-3-фосфатдегидрогеназу), которая является геном домашнего хозяйства (housekeeping, HK). 96-луночный планшет, содержащий смешанный раствор, подвергали следующей реакции с использованием термоблока Exicycler™ Real-Time Quantitative Thermal Block (Bioneer, Корея): реакция при 95°C в течение 15 минут для активации фермента и удаления вторичной структуры кДНК, 42 цикла каждый из которых включает четыре процесса денатурации при 94°C в течение 30 секунд, отжига при 58°C в течение 30 секунд, удлинения при 72°C в течение 30 секунд, сканирования SYBR green и окончательное удлинение при 72°C в течение 3 минут, после чего температуру поддерживали на уровне 55°С в течение 1 минуты и анализировали кривую плавления от 55°С до 95°С.
После завершения ПЦР значение Ct (пороговый цикл) каждого гена-мишени корректировали с помощью гена GAPDH, а затем рассчитывали разницу ΔCt в значениях Ct с использованием контрольной группы, обработанной SAMiRNA (SAMiCONT) (смысловой: 5'-CUUACGCUGAGUACUUCGA). -3' (19мер) (SEQ ID NO: 59), антисмысловой: 5'-UCGAAGUACUCAGCGUAAG-3' (19мер) (SEQ ID NO: 60)), которая представляет собой контрольную последовательность, не вызывающую ингибирования экспрессии гена. Относительный уровень экспрессии гена-мишени в клетках, обработанных CTGF-специфичной SAMiRNA, определяли количественно, используя значение ΔCt и уравнение 2 (-ΔCtx100).
Для выбора высокоэффективной SAMiRNA использовали SAMiRNA #10, имеющую в качестве смысловой цепи последовательность, обладающую наибольшей эффективностью снижения уровня экспрессии мРНК CTGF при конечной концентрации 50, 100, 200, 500 или 1000 нМ. по сравнению с контрольной группой, а именно окончательно выбрали последовательность SEQ ID NO: 10.
Как показано на фиг. 3, SAMiRNA #10, которая наиболее эффективно ингибирует экспрессию гена CTGF, наконец, выбрали из восьми SAMiRNA, нацеленных на CTGF, и значение IC50 для SAMiRNA определили путем анализа паттерна экспрессии мРНК CTGF в клеточной линии. Информация о последовательностях соответствующих SAMiRNA показана в таблице 6 ниже.
Следовательно, было подтверждено, что все CTGF-специфические SAMiRNA, имеющие последовательность SEQ ID NO: 10 в качестве смысловой цепи, снижали уровень экспрессии мРНК CTGF на 50% или более даже при низкой концентрации 50 нМ, тем самым ингибируя экспрессию CTGF с очень высокой эффективностью. Как показано на фиг. 4, было определено, что IC50 составляет 30,75 нМ для CTGF-специфичной SAMiRNA, имеющей последовательность SEQ ID NO: 10 в качестве смысловой цепи, что указывает на наиболее эффективное ингибирование экспрессии гена CTGF, а также подтвержден превосходный ингибирующий эффект по сравнению с IC50 для Rxi-109.
Таблица 5. Информация о последовательности праймеров для количественной ПЦР
(F обозначает прямой праймер, а R обозначает обратный праймер)
Таблица 6. Последовательность SAMiRNA, эффективно ингибирующая экспрессию CTGF
Пример 5. Сравнительный анализ ингибирования экспрессии CTGF человека SAMiRNA с гибридом ДНК/РНК и гибридом РНК/РНК, включая выбранную последовательность SEQ ID NO: 10 в качестве смысловой цепи
Линию клеток рака легкого A549 обрабатывали с использованием гибрида двухцепочечного гибрида олиго ДНК/РНК и гибрида РНК/РНК, включающих CTGF-специфическую SAMiRNA, имеющую последовательность SEQ ID NO: 10, выбранную в Примере 4, в качестве смысловой цепи, и относительную мРНК анализировали уровень экспрессии (%) CTGF в клеточной линии.
5.1 Внутриклеточный процессинг наночастиц SAMiRNA
A549, которая представляет собой клеточную линию рака легкого человека, использовали для обнаружения SAMiRNA, которая ингибирует экспрессию CTGF, и клеточную линию A549 культивировали при 37°C и 5% CO2 в среде Gibco™F-12K (Kaighn's) (Thermo, США), содержащей 10% фетальной бычьей сыворотки (Hyclone, США) и 1% пенициллина-стрептомицина (Hyclone, США). Используя ту же среду, что и выше, клеточную линию A549 распределяли с плотностью 8×104 клеток/лунку в 12-луночный планшет (Costar, США), а на следующий день SAMiRNA, гомогенизированную деионизированной дистиллированной водой в примере 3.1, разводили до 200 нМ или 600 нМ с 1X DPBS и добавляли к клеткам. Обработку клеток SAMiRNA проводили всего 4 раза, один раз каждые 12 часов, а культивирование проводили при 37°С и 5% СО2.
Используя ту же среду, что и выше, клеточную линию MDA-MB231 распределяли с плотностью 2×104 клеток/лунку в 96-луночный планшет (Costar, США), а на следующий день SAMiRNA, гомогенизированную с деионизированной дистиллированной водой в примере 3.1, разбавляли до 200 нМ или 600 нМ 1X DPBS и добавляли к клеткам.
5.2 Скрининг SAMiRNA посредством анализа эффективности ингибирования экспрессии мРНК CTGF человека
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 5-1, и синтезировали в кДНК, после чего относительный уровень экспрессии мРНК гена CTGF определяли количественно с использованием ПЦР в реальном времени.
5-2-1 Выделение РНК из обработанных SAMiRNA клеток и синтез кДНК
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 5-1, с использованием набора для выделения РНК (набор для экстракции общей РНК AccuPrep Cell, Bioneer, Корея), и экстрагированную РНК синтезировали в кДНК следующим образом, используя обратную транскриптазу РНК (AccuPower® RocketScript™ oligo (dT)20, Bioneer, Корея). В частности, 1 мкг экстрагированной РНК добавляли к AccuPower® RocketScript™ (Корея), содержащемуся в каждой из пробирок Eppendorf объемом 0,25 мл, и туда же добавляли дистиллированную воду, обработанную DEPC (диэтилпирокарбонатом), до достижения общего объема 20 мкл. В системе амплификации генов (MyGenie™ Gradient Thermal Block, Bioneer, Корея) два процесса гибридизации РНК с праймерами при 37°С в течение 30 секунд и синтеза кДНК при 48°С в течение 4 минут повторяли 12 раз, после чего реакцию амплификации останавливали путем дезактивации фермента при 95°С в течение 5 минут.
5-2-2 Относительный количественный анализ мРНК CTGF человека
Относительный уровень экспрессии мРНК CTGF по сравнению с контрольным образцом SAMiRNA анализировали следующим образом с помощью SYBR green количественной ПЦР в реальном времени с использованием кДНК, синтезированной в примере 5-2-1, в качестве матрицы. В частности, кДНК, синтезированную в примере 5-2-1, разбавляли в 5 раз дистиллированной водой и для анализа уровня экспрессии мРНК CTGF использовали 3 мкл разведенной кДНК, 25 мкл AccuPower® (Корея), 19 мкл дистиллированной воды и 3 мкл праймеров CTGF для кПЦР (SEQ ID NO: 44 и 45 (таблица 5); 10 пмоль/мкл соответственно, Bioneer, Корея) добавляли в каждую лунку 96-луночного планшета для получения смешанного раствора. Между тем, чтобы нормализовать уровень экспрессии мРНК CTGF, в качестве стандартного гена использовали GAPDH (глицеральдегид-3-фосфатдегидрогеназу), которая является геном домашнего хозяйства (housekeeping, HK). 96-луночный планшет, содержащий смешанный раствор, подвергали следующей реакции с использованием термоблока Exicycler™ Quantitative Thermal Block (Bioneer, Корея): реакция при 95°C в течение 15 минут для активации фермента и удаления вторичной структуры кДНК, 42 цикла, каждый из которых включает четыре процесса, денатурацию при 94°C в течение 30 секунд, отжиг при 58°C в течение 30 секунд, удлинение при 72°C в течение 30 секунд и сканирование SYBR green; и окончательное удлинение при 72°C в течение 3 минут, после чего температуру поддерживали на уровне 55°С в течение 1 минуты и анализировали кривую плавления от 55°С до 95°С.
После окончания ПЦР значение Ct (порогового цикла) каждого гена-мишени корректировали с помощью гена GAPDH, а затем рассчитывали разницу значений Δ с использованием контрольной группы, обработанной SAMiRNA (SAMiCONT), которая представляет собой контрольную последовательность, которая не вызывает ингибирования экспрессии генов. Относительный уровень экспрессии гена-мишени в клетках, обработанных CTGF-специфичной SAMiRNA, определяли количественно, используя значение Δ и уравнение 2 (-Δx100).
Для того чтобы выбрать высокоэффективную SAMiRNA среди двухцепочечных гибридов олиго ДНК/РНК и гибридов РНК/РНК, была окончательно выбрана SAMiRNA, которая представляет собой гибрид ДНК/РНК, имеющий в качестве смысловой цепи последовательность, обладающую наибольшей эффективностью снижения экспрессии мРНК уровень CTGF при конечной концентрации 200 нМ или 600 нМ по сравнению с контрольной группой, а именно последовательность ДНК SEQ ID NO: 10.
Как показано на фиг. 5, гибрид ДНК/РНК SAMiRNA #10, который наиболее эффективно ингибирует экспрессию гена CTGF, был, наконец, выбран из гибрида двухцепочечного гибрида олиго ДНК/РНК и гибрида РНК/РНК, включая выбранную CTGF-специфическую SAMiRNA.
Пример 6. Скрининг наночастиц SAMiRNA, индуцирующих RNAi, нацеленную на CTGF крысы
В терапевтических агентах siRNA трудно обнаружить оптимальную последовательность, которую можно обычно применять к различным штаммам. В данном документе приведены рекомендации FDA США для проверки фармакологической эффективности из-за ингибирования экспрессии соответствующего гена и токсичности из-за ингибирования экспрессии соответствующего гена, путем создания последовательности siRNA (суррогатной последовательности; siRNA, специфичной для гена мыши), специфичной для животной модели (подтвержденной тестом эффективности in vivo), которая анализирует терапевтический эффект (презентация Robert T. Dorsam Ph.D. Pharmacology/Toxicology Reviewer, FDA/CDER).
Последовательность на основе SAMiRNA была обнаружена с использованием программы проектирования siRNA на основе обычных алгоритмов (Turbo-si-designer, принадлежащая заявителю). Всего из полных последовательностей транскриптов крысиного гена CTGF (NM_022266.2) было создано 94 кандидата последовательностей siRNA, и была синтезирована соответствующая SAMiRNA, после чего клеточная линия H4-II-E, полученная из рака печени крысы, была обработана ими при 500 нМ в условиях культивирования клеток с 10% FBS, так что эффект ингибирования экспрессии in vitro был в первую очередь проверен с использованием праймеров, показанных в таблице 7 ниже (информация о последовательности праймеров для количественной ПЦР) (фиг. 6).
Для отбора высокоэффективных SAMiRNA был проведен вторичный скрининг последовательностей, обладающих наибольшей эффективностью снижения уровня экспрессии мРНК крысиного CTGF при конечной концентрации 500 нМ по сравнению с контрольной группой, а именно 12 последовательностей, имеющих эффективность снижения > 60% или более (всего 94 типа SAMiRNA-CTGF крысы) использовали при 200 нМ и 500 нМ на клеточной линии H4-II-E, которая представляет собой клеточную линию рака печени крысы. В результате были выбраны три SAMiRNA, имеющие последовательности SEQ ID NO: 46, 47 и 48 в качестве соответствующих смысловых цепей.
Как показано на фиг. 6, три SAMiRNA, которые наиболее эффективно ингибируют экспрессию гена CTGF крысы, были, наконец, выбраны из 94 SAMiRNA, нацеленных на CTGF крысы (фиг. 8), и информация о последовательности соответствующих SAMiRNA показана в таблице 8 ниже.
Для отбора высокоэффективной SAMiRNA использовали SAMiRNA-rat CTGF #46, имеющую в качестве смысловой цепи последовательность, обладающую наибольшей эффективностью снижения уровня экспрессии мРНК CTGF крысы при конечной концентрации 25, 50, 100, 200 , 400 или 800 нМ по сравнению с контрольной группой, а именно, выбрали последовательность SEQ ID NO: 46.
Как показано на фиг. 8, было определено, что IC50 составляет 122,9 нМ для SAMiRNA, специфической к CTGF крысы, имеющей последовательность SEQ ID NO: 46 в качестве смысловой цепи, что указывает на наиболее эффективное ингибирование экспрессии гена CTGF крысы.
Кроме того, как показано на фиг. 9, гибрид ДНК/РНК SAMiRNA #46, который наиболее эффективно ингибирует экспрессию гена CTGF крысы, был, наконец, выбран из двухцепочечного гибрида олиго ДНК/РНК и гибрида РНК/РНК, включая выбранную SAMiRNA, специфичную для CTGF крысы.
Таблица 7. (F обозначает прямой праймер, а R обозначает обратный праймер)
Таблица 8
Пример 7. Проверка эффективности SAMiRNA-rat CTGF при внутрикожном введении в животной модели раневого келоида
Была проанализирована эффективность SAMi-rCTGF на ранах, вызванных 8-миллиметровым перфоратором для биопсии (Biopsy Punch, BP-80F, Каи, Япония). Для эксперимента были приобретены 7-недельные крысы (SD Rats, Nara Biotech, Каннам, Корея), которые акклиматизировались в течение 1 недели. На коже спины крыс наносили раны с помощью перфоратора для биопсии диаметром 8 мм. 1200 мкг/участок каждого из солевого раствора (PBS) для группы отрицательного контроля, ДНК/РНК SAMiRNA-rCTGF#46(D/R) для экспериментальной группы и SAMiRNA-rCTGF#46 РНК/РНК(R/R) для другой экспериментальной группы внутрикожно вводили всего два раза за 2 дня до индукции раны и в день индукции раны. Крыс забивали на 3-й день после индукции раны.
7-1. Анализ экспрессии гена SAMiRNA в животной модели раневого келоида
Ткань кожи крысы, обработанную SAMiRNA, получали и предварительно измельчали с использованием ступки, пестика и жидкого азота. Измельченную ткань помещали в лизисный буфер набора для выделения РНК (набор для выделения общей РНК AccuPrep Cell, Bioneer, Корея) и вторично измельчали с использованием гомогенизатора. После этого тотальную РНК экстрагировали в соответствии с протоколом производителя. Экстрагированную РНК синтезировали в кДНК с использованием обратной транскриптазы РНК (премикс AccuPower® RocketScript™RT Premix с oligo (dT) 20, Bioneer, Корея) следующим образом.
Таблица 9. Параметр RT
Относительный уровень экспрессии общей мРНК в каждой группе анализировали следующим образом с помощью SYBR green количественной ПЦР в реальном времени с использованием синтезированной кДНК в качестве матрицы. В частности, синтезированную кДНК разводили в 10 раз дистиллированной водой, а для анализа уровня экспрессии мРНК CTGF использовали 10 мкл разведенной кДНК, 25 мкл AccuPower® GreenStar™ (Корея), 20 мкл дистиллированной воды и в каждую лунку 96-луночного планшета добавляли по 5 мкл праймеров CTGF для количественной ПЦР (по 3 пмоль/мкл, таблица 10) для получения смешанного раствора. Между тем, чтобы нормализовать уровни экспрессии мРНК CTGF, фибронектина и Col3α1, в качестве стандартного гена использовали RPL13A, который является геном домашнего хозяйства (HK). После прекращения количественной ПЦР значение Ct (порогового цикла) каждого целевого гена корректировали с использованием гена RPL13A, определяли значение ΔCt целевого гена, а затем рассчитывали его значение ΔΔCt по сравнению с контрольной группой. Относительные уровни экспрессии генов CTGF, фибронектина и Col3α1 определяли количественно с использованием значения ΔΔCt и уравнения 2 (-ΔΔCtx100).
Таблица 10. (F обозначает прямой праймер, а R обозначает обратный праймер)
Таблица 11. Параметр количественной ПЦР
Следовательно, было подтверждено, что экспрессия CTGF была значительно снижена в группе, обработанной 1200 мкг SAMiRNA-rCTGF(D/R), по сравнению с группой, обработанной физиологическим раствором у крыс с индуцированными ранами, и статистически значимое снижение было также подтверждено в группе, получавшей 1200 мкг SAMiRNA-rCTGF(D/R), по сравнению с группой, получавшей 1200 мкг SAMiRNA-rCTGF(R/R).
Как показано на фиг. 10, был сделан вывод, что гибрид двухцепочечного гибрида олиго ДНК/РНК наиболее эффективно ингибирует экспрессию гена CTGF по сравнению с гибридом РНК/РНК среди гибридов, включающих выбранную rCTGF-специфическую SAMiRNA.
Хотя конкретные воплощения настоящего изобретения были подробно описаны выше, специалистам в данной области техники будет очевидно, что описание представляет собой просто предпочтительные примерные воплощения и не должно рассматриваться как ограничивающее объем настоящего изобретения. Следовательно, существенный объем настоящего изобретения будет определяться прилагаемой формулой изобретения и ее эквивалентами.
Промышленная применимость
Согласно настоящему изобретению конструкция двухцепочечного олигонуклеотида, включающая CTGF-специфичный двухцепочечный олигонуклеотид, и фармацевтическая композиция, содержащая его в качестве активного ингредиента, способна ингибировать экспрессию CTGF с высокой эффективностью без побочных эффектов и очень эффективна при профилактике и лечении заболеваний и респираторных заболеваний, вызванных чрезмерным фиброзом.
Свободный текст перечня последовательностей
Электронный файл прилагается.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> BIONEER CORPORATION
<120> ДВУХЦЕПОЧЕЧНЫЙ ОЛИГОНУКЛЕОТИД, СПЕЦИФИЧНЫЙ К ГЕНУ CTGF,
И СОДЕРЖАЩАЯ ЕГО КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ФИБРОЗНЫХ ЗАБОЛЕВАНИЙ
И ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ДЫХАТЕЛЬНОЙ СИСТЕМОЙ
<130> PF-B2791
<140> PCT/KR2020/014948
<141> 2020-10-29
<150> 10-2019-0151673
<151> 2019-11-22
<160> 60
<170> версия PatentIn 3.5
<210> 1
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 1
atgtacagtt atctaagtt 19
<210> 2
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 2
tgtacagtta tctaagtta 19
<210> 3
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 3
gtacagttat ctaagttaa 19
<210> 4
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 4
atggaaattc tgctcagat 19
<210> 5
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 5
tggaaattct gctcagata 19
<210> 6
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 6
ggaaattctg ctcagatag 19
<210> 7
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 7
atttcagtag cacaagtta 19
<210> 8
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 8
tttcagtagc acaagttat 19
<210> 9
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 9
ttcagtagca caagttatt 19
<210> 10
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 10
tgatttcagt agcacaagt 19
<210> 11
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 11
gatttcagta gcacaagtt 19
<210> 12
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 12
taaaaatgat ttcagtagc 19
<210> 13
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 13
aaaaatgatt tcagtagca 19
<210> 14
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 14
aaaatgattt cagtagcac 19
<210> 15
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 15
tcagtagcac aagttattt 19
<210> 16
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Смысловая)
<400> 16
cagtagcaca agttattta 19
<210> 17
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 17
aacuuagaua acuguacau 19
<210> 18
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 18
uaacuuagau aacuguaca 19
<210> 19
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 19
uuaacuuaga uaacuguac 19
<210> 20
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 20
aucugagcag aauuuccau 19
<210> 21
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 21
uaucugagca gaauuucca 19
<210> 22
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 22
cuaucugagc agaauuucc 19
<210> 23
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 23
uaacuugugc uacugaaau 19
<210> 24
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 24
auaacuugug cuacugaaa 19
<210> 25
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 25
aauaacuugu gcuacugaa 19
<210> 26
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 26
acuugugcua cugaaauca 19
<210> 27
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 27
aacuugugcu acugaaauc 19
<210> 28
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 28
gcuacugaaa ucauuuuua 19
<210> 29
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 29
ugcuacugaa aucauuuuu 19
<210> 30
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 30
gugcuacuga aaucauuuu 19
<210> 31
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 31
aaauaacuug ugcuacuga 19
<210> 32
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> кандидатная CTGF-специфичная SAMiRNA (Антисмысловая)
<400> 32
uaaauaacuu gugcuacug 19
<210> 33
<211> 21
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 33
caccagcatg aagacatacc g 21
<210> 34
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 34
cgtcagggca cttgaactc 19
<210> 35
<211> 23
<212> DNA
<213> Искусственная последовательность
<220>
<223> Зонд
<400> 35
ccgacggccg atgctgcacc ccc 23
<210> 36
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 36
gtgtttgacg gcatcccacc 20
<210> 37
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 37
taggcttcag acgcacgacc 20
<210> 38
<211> 21
<212> DNA
<213> Искусственная последовательность
<220>
<223> Зонд
<400> 38
aagcggatgg tggttcctgc t 21
<210> 39
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 39
caccacagct cttccactc 19
<210> 40
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 40
atcccagaac tctccgaagc 20
<210> 41
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Зонд
<400> 41
acccttgccg ggcaccactc 20
<210> 42
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 42
ggtgaaggtc ggagtcaacg 20
<210> 43
<211> 25
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 43
accatgtagt tgaggtcaat gaagg 25
<210> 44
<211> 21
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 44
caccagcatg aagacatacc g 21
<210> 45
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 45
cgtcagggca cttgaactc 19
<210> 46
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> SAMi-rCTGF Смысловой
<400> 46
gacactggtt tcgagacag 19
<210> 47
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> SAMi-rCTGF Смысловой
<400> 47
cctgtcaatc tcagacact 19
<210> 48
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> SAMi-rCTGF Смысловой
<400> 48
catccggacg cctaaaatt 19
<210> 49
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 49
aacatcatcc ctgcatccac 20
<210> 50
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 50
cggatacatt gggggtagga 20
<210> 51
<211> 19
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 51
caagggtctc ttctgcgac 19
<210> 52
<211> 21
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 52
atttgcaact gctttggaag g 21
<210> 53
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 53
aggggcaggt tctagtattg 20
<210> 54
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 54
gcgtacaacc accacctttc 20
<210> 55
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 55
aggagtgggt gtgtgatgag 20
<210> 56
<211> 20
<212> DNA
<213> Искусственная последовательность
<220>
<223> Праймер
<400> 56
ttggctcgca tcatagttgg 20
<210> 57
<211> 13
<212> RNA
<213> Искусственная последовательность
<220>
<223> Rxi-109 Смысловой
<400> 57
gcaccuuucu aga 13
<210> 58
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> Rxi-109 Антисмысловой
<400> 58
ucuagaaagg ugcaaacau 19
<210> 59
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> SAMiRNA(SAMiCONT) Смысловой
<400> 59
cuuacgcuga guacuucga 19
<210> 60
<211> 19
<212> RNA
<213> Искусственная последовательность
<220>
<223> SAMiRNA(SAMiCONT) Антисмысловой
<400> 60
ucgaaguacu cagcguaag 19





Изобретение относится к области биотехнологии, а именно к CTGF-специфичному двухцепочечному олигонуклеотиду, а также к конструкции, наночастице и композиции, его содержащим. Изобретение эффективно для профилактики или лечения фиброза, а также для профилактики или лечения респираторного заболевания. 11 н. и 20 з.п. ф-лы, 10 ил., 11 табл., 7 пр.
1. CTGF-специфичный двухцепочечный олигонуклеотид, включающий смысловую цепь, содержащую последовательность SEQ ID NO: 10, и антисмысловую цепь, содержащую комплементарную ей последовательность, где смысловая цепь представляет собой ДНК, а антисмысловая цепь представляет собой РНК.
2. CTGF-специфичный двухцепочечный олигонуклеотид по п. 1, отличающийся тем, что указанный олигонуклеотид представляет собой siRNA, shRNA или miRNA.
3. CTGF-специфичный двухцепочечный олигонуклеотид по п. 1, отличающийся тем, что смысловая цепь или антисмысловая цепь двухцепочечного олигонуклеотида содержит химическую модификацию.
4. CTGF-специфичный двухцепочечный олигонуклеотид по п. 3, отличающийся тем, что химическая модификация представляет собой по меньшей мере одну, выбранную из группы, состоящей из модификации, в которой гидроксильная группа (-ОН) в 2'-углеродном положении сахарной структуры в нуклеотид замещена любой, выбранной из группы, состоящей из метила (-CH3), метокси (-OCH3), амина (-NH2), фтора (-F), O-2-метоксиэтила, O-пропила, O-2- метилтиоэтил, О-3-аминопропил, О-3-диметиламинопропил, О-N-метилацетамидо и О-диметиламидооксиэтил; модификацию, в которой кислород сахарной структуры в нуклеотиде замещен серой; модификацию, в которой нуклеотидная связь представляет собой любую связь, выбранную из группы, состоящей из фосфоротиоатной связи, боранофосфатной связи и метилфосфонатной связи; и модификацию в PNA (пептидная нуклеиновая кислота), LNA (заблокированная нуклеиновая кислота) и UNA (незаблокированная нуклеиновая кислота).
5. CTGF-специфичный двухцепочечный олигонуклеотид по п. 1, отличающийся тем, что по меньшей мере одна фосфатная группа связана с 5'-концом антисмысловой цепи двухцепочечного олигонуклеотида.
6. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида для ингибирования экспрессии CTGF, имеющая структуру структурной формулы (2), приведенную ниже:
Структурная формула (2)

в структурной формуле 2, A представляет собой гидрофильный материал, B представляет собой гидрофобный материал, X и Y, каждый независимо, представляют собой простую ковалентную связь или ковалентную связь, опосредованную линкером, и S и AS представляют собой смысловую цепь и антисмысловую цепь двухцепочечного олигонуклеотида по любому из пп. 1-5.
7. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 6, имеющая структуру структурной формулы (3) или структурной формулы (4), представленной ниже:
Структурная формула (3)

Структурная формула (4)

в структурных формулах (3) и (4) A, B, X, Y, S и AS имеют значения, определенные в п. 6, а 5' и 3' представляют собой 5' и 3' концы смысловой цепи двухцепочечного олигонуклеотида.
8. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 6, отличающаяся тем, что гидрофильный материал выбран из группы, состоящей из полиэтиленгликоля (PEG), поливинилпирролидона и полиоксазолина.
9. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 6, отличающаяся тем, что гидрофильный материал имеет структуру структурной формулы (5) или структурной формулы (6), приведенной ниже:
Структурная формула (5)
(A'm-J)n
Структурная формула (6)
(J-A'm)n
в структурной формуле (5) или структурной формуле (6) A' представляет собой мономер гидрофильного материала, J представляет собой линкер, соединяющий m мономеров гидрофильного материала друг с другом или соединяющий m мономеров гидрофильного материала и двухцепочечный олигонуклеотид друг с другом, m представляет собой целое число от 1 до 15, n представляет собой целое число от 1 до 10, мономер гидрофильного материала A' представляет собой любое соединение, выбранное из приведенных ниже соединений (1)-(3), и линкер (J) выбирают из группы, состоящей из -PO3--, -SO3- и -CO2-:
Соединение (1)

в соединении (1) G выбран из группы, состоящей из O, S и NH;
Соединение (2)
 ; и
; и
Соединение (3)
 .
.
10. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 6, отличающаяся тем, что гидрофильный материал имеет молекулярную массу от 200 до 10000.
11. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 6, отличающаяся тем, что гидрофобный материал имеет молекулярную массу от 250 до 1000.
12. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 11, отличающаяся тем, что гидрофобный материал представляет собой любой материал, выбранный из группы, состоящей из производного стероида, производного глицерида, эфира глицерина, полипропиленгликоля, ненасыщенного или насыщенного углеводорода C12-C50, диацилфосфатидилхолина, жирной кислоты, фосфолипида, липополиамина, липида, токоферола и токотриенола.
13. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 12, отличающаяся тем, что стероидное производное представляет собой любое производное, выбранное из группы, состоящей из холестерина, холестанола, холевой кислоты, холестерилформиата, холестанилформиата и холестериламина.
14. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 12, отличающаяся тем, что производное глицерида представляет собой любое производное, выбранное из группы, состоящей из моноглицеридов, диглицеридов и триглицеридов.
15. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 6, отличающаяся тем, что ковалентная связь, представленная X и Y, представляет собой неразлагаемую связь или разлагаемую связь.
16. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 15, отличающаяся тем, что неразлагаемая связь представляет собой амидную связь или фосфатную связь.
17. Конструкция CTGF-специфичного двухцепочечного олигонуклеотида по п. 15, отличающаяся тем, что разлагаемая связь представляет собой любую связь, выбранную из группы, состоящей из дисульфидной связи, связи, разлагаемой кислотой, сложноэфирной связи, ангидридной связи, биоразлагаемой связи и связи, разлагаемой ферментами.
18. Наночастица для ингибирования экспрессии CTGF, содержащая конструкцию двухцепочечного олигонуклеотида по п. 6.
19. Наночастица по п. 18, отличающаяся тем, что наночастица сконфигурирована в виде наночастицы таким образом, что смешиваются конструкции двухцепочечных олигонуклеотидов, включающие двухцепочечные олигонуклеотиды, содержащие разные последовательности.
20. Фармацевтическая композиция для профилактики или лечения фиброза, содержащая двухцепочечный олигонуклеотид по любому из пп. 1-5 или наночастицу по п. 18 и фармацевтически приемлемый носитель.
21. Фармацевтическая композиция для профилактики или лечения респираторного заболевания, содержащая двухцепочечный олигонуклеотид по любому из пп. 1-5 или наночастицу по п. 18 и фармацевтически приемлемый носитель.
22. Фармацевтическая композиция по п. 21, отличающаяся тем, что респираторное заболевание представляет собой любое заболевание, выбранное из группы, состоящей из хронической обструктивной болезни легких (COPD), астмы, острого или хронического бронхита, аллергического ринита, продуктивного кашля, бронхита, бронхиолита, ларингофарингита, тонзиллита и ларингита.
23. Фармацевтическая композиция по п. 20, отличающаяся тем, что фиброз представляет собой любой фиброз, выбранный из группы, состоящей из идиопатического легочного фиброза (IPF), фиброза печени, цирроза печени, миелофиброза, миокардиального фиброза, почечного фиброза, келоида, легочного фиброза, сердечного фиброза и радиационно-индуцированного фиброза.
24. Лиофилизированный состав для профилактики или лечения фиброза, содержащий фармацевтическую композицию по п. 20.
25. Лиофилизированный состав для профилактики или лечения респираторных заболеваний, содержащий фармацевтическую композицию по п. 21.
26. Фармацевтическая композиция для профилактики или лечения фиброза, содержащая конструкцию двухцепочечного олигонуклеотида по п. 6 и фармацевтически приемлемый носитель.
27. Фармацевтическая композиция для профилактики или лечения респираторного заболевания, содержащая конструкцию двухцепочечного олигонуклеотида по п. 6 и фармацевтически приемлемый носитель.
28. Фармацевтическая композиция по п. 27, отличающаяся тем, что респираторное заболевание представляет собой любое заболевание, выбранное из группы, состоящей из хронической обструктивной болезни легких (COPD), астмы, острого и хронического бронхита, аллергического ринита, продуктивного кашля, бронхита, бронхиолита, ларингофарингита, тонзиллита и ларингита.
29. Фармацевтическая композиция по п. 27, отличающаяся тем, что фиброз представляет собой любой фиброз, выбранный из группы, состоящей из идиопатического легочного фиброза (IPF), фиброза печени, цирроза, миелофиброза, миокардиального фиброза, почечного фиброза, келоида, легочного фиброза, сердечного фиброза и радиационно-индуцированного фиброза.
30. Лиофилизированный состав для профилактики или лечения фиброза, содержащий фармацевтическую композицию по п. 26.
31. Лиофилизированный состав для профилактики или лечения респираторного заболевания, содержащий фармацевтическую композицию по п. 27.
| KR20160033125 A, 25.03.2016 | |||
| US9446062 B2, 20.09.2016 | |||
| WO2015152693 A2, 06.04.2015 | |||
| JP2014210789 A, 13.11.2014 | |||
| ВАСИЛЬЕВА О | |||
| В | |||
| и др., Фактор роста соединительной ткани (CTGF) в дерме человека в онтогенезе, ФОНТОГЕНЕЗ, 2016, том 47, N 2, с | |||
| Фальцовая черепица | 0 |
|
SU75A1 |
Авторы
Даты
2023-11-09—Публикация
2020-10-29—Подача