Область техники, к которой относится изобретение
Настоящее изобретение относится к композиции для предупреждения или лечения заболеваний, связанных с ожирением, содержащей амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру и, в частности, к двухцепочечному олигонуклеотиду, способному ингибировать экспрессию амфирегулина очень специфическим и высокоэффективным образом, и к композиции для предупреждения или лечения заболеваний, связанных с ожирением, содержащей двухцепочечную олигонуклеотидную структуру, содержащую двухцепочечный олигонуклеотид, и наночастицы.
Сведения о предшествующем уровне техники
В 1995 г. Guo и Kemphues сообщили, что не только смысловая РНК, но и антисмысловая РНК является эффективной в отношении ингибирования экспрессии генов в C. elegans, и с тех пор были проведены исследования для выявления причины этого. В 1998 г. в работе Fire et al. впервые было описано явление, когда инъекция двухцепочечной РНК (dsRNA) ингибирует экспрессию генов путем специфической деградации соответствующей ей мРНК. Это явление было названо РНК-интерференцией (RNAi). RNAi, процесс, который используется для ингибирования экспрессии генов, может демонстрировать отчетливый эффект ингибирования экспрессии генов простым и недорогим способом, и, таким образом, диапазон применения этой технологии расширился.
Поскольку эта технология ингибирования экспрессии генов может регулировать экспрессию специфического гена, она может удалять специфический ген, связанный с раком, генетическим заболеванием или т.п. на уровне мРНК, и может применяться в качестве важного инструмента для разработки терапевтических агентов для лечения заболеваний и проверки мишеней. В качестве общепринятых методов ингибирования экспрессии целевых генов раскрыты способы введения трансгена для целевого гена. Эти способы включают способ введения трансгена в антисмысловом направлении относительно промотора и способ введения трансгена в антисмысловом направлении относительно промотора.
Такая РНК-терапия, нацеленная на РНК, представляет собой способ удаления функции интересующего гена с использованием олигонуклеотидов против РНК-мишени, и может считаться отличающимся от общепринятых способов, в которых терапевтические агенты, такие как антитела и малые молекулы, в основном нацелены на белки. Подходы к нацеливанию на РНК можно условно разделить на два типа: RNAi, опосредованная двухцепочечной РНК, и антисмысловые олигонуклеотиды (ASO). В настоящее время проводятся клинические испытания путем нацеливания на РНК при различных заболеваниях.
Антисмысловой олигонуклеотид (в дальнейшем в настоящем документе называемый «ASO») представляет собой короткую синтетическую ДНК, предназначенную для связывания с геном-мишенью в соответствии со спариванием оснований Уотсона-Крика, и может специфически ингибировать экспрессию определенной нуклеотидной последовательности гена. Таким образом, антисмысловой олигонуклеотид применяют для изучения роли генов и для разработки терапевтических агентов, способных лечить заболевания, такие как рак, на молекулярном уровне. Эти ASO имеют преимущество, состоящее в легкости получения путем установления различных мишеней для ингибирования экспрессии генов, и были проведены исследования по использованию ASO для ингибирования экспрессии онкогенов и роста раковых клеток. Процесс ингибирования экспрессии определенного гена с помощью ASO осуществляется либо путем связывания ASO с комплементарной последовательностью мРНК для индукции активности RNase H и удаления мРНК, либо путем препятствования образованию и развитию рибосомного комплекса для трансляции белка. Кроме того, сообщалось, что ASO связывается с геномной ДНК с образованием структуры тройной спирали, тем самым ингибируя транскрипцию генов. ASO обладает потенциалом, как описано выше, но для применения ASO в клинической практике требуется, чтобы стабильность ASO против нуклеаз была улучшена, и чтобы ASO эффективно доставлялся в целевые ткани или клетки, чтобы таким образом специфически связываться с нуклеотидной последовательностью целевого гена. Кроме того, вторичная и третичная структуры генетической мРНК являются важными факторами для специфического связывания ASO, и область, в которой снижается образование вторичной структуры мРНК, очень выгодна для доступа ASO. Таким образом, были предприняты усилия для эффективного достижения геноспецифического ингибирования не только in vitro, но и in vivo путем систематического анализа области, в которой снижается образование вторичной структуры мРНК, до синтеза ASO. Эти ASO являются более стабильными, чем siRNA, разновидность РНК, и имеют преимущество, состоящее в легкой растворимости в воде и физиологическом растворе. На сегодняшний день Федеральное управление по лекарственным средствам (FDA) одобрило три ASO (Jessica, C., J Postdoc Res, 4:35-50, 2016).
После выявления роли РНК-интерференции (далее в настоящем документе называемой «RNAi»), было обнаружено, что RNAi действует на последовательность-специфические мРНК в различных типах клеток млекопитающих (Barik, S., J Mol. Med. (2005) 83: 764-773). При доставке в клетку длинной цепи двухцепочечной РНК, доставленная двухцепочечная РНК превращается в малую интерферирующую РНК (далее в настоящем документе называемую «siRNA»), расщепляется до 21-23 пар оснований (bp) эндонуклеазой Dicer. siRNA связывается с РНК-индуцированным комплексом сайленсинга (RISC) и ингибирует экспрессию целевого гена последовательность-специфическим образом посредством процесса, в котором направляющая (антисмысловая) цепь узнает и расщепляет целевую мРНК. Технологию ингибирования экспрессии генов с использованием siRNA используют для ингибирования экспрессии целевого гена в клетках-мишенях и наблюдения полученного изменения, а также эффективно используют в исследованиях для идентификации функции целевого гена в клетках-мишенях. В частности, ингибирование функции целевого гена в инфекцирующих вирусах или раковых клетках можно эффективно применять для разработки способа лечения интересующего заболевания. В результате проведения исследований in vitro и исследований in vivo с использованием экспериментальных животных сообщалось, что можно ингибировать экспрессию целевого гена с помощью siRNA.
Bertrand et al. обнаружили, что siRNA обладает лучшим ингибирующим эффектом на экспрессию мРНК in vitro и in vivo по сравнению с антисмысловым олигонуклеотидом (ASO) против одного и того же целевого гена, и что этот эффект является более продолжительным. Кроме того, что касается механизма действия, siRNA регулирует экспрессию целевого гена последовательность-специфическим образом путем комплементарного связывания с мРНК-мишенью. Таким образом, siRNA имеет преимущество перед общепринятыми лекарственными средствами на основе антител или химическими лекарственными средствами (низкомолекулярными лекарственными средствами) в том, что круг субъектов, для которых можно применять siRNA, может быть значительно расширен.
siRNA обладает превосходными эффектами и может быть использована в широком диапазоне применений, но для разработки siRNA в качестве терапевтического агента необходимо улучшить стабильность siRNA in vivo и эффективность ее доставки в клетки таким образом, чтобы siRNA можно было эффективно доставлять к клеткам-мишеням. Для улучшения стабильности in vivo и решения проблем, связанных со стимуляцией siRNA неспецифического врожденного иммунитета, были проведены интенсивные исследования по модификации некоторых нуклеотидов siRNA или ее остова с целью обеспечения устойчивости к нуклеазам, или с использованием вирусных векторов, липосом или наночастиц.
Системы доставки, содержащие вирусный вектор, такой как аденовирус или ретровирус, обладают высокой эффективностью трансфекции, но и сильной иммуногенностью и онкогенностью. С другой стороны, невирусные системы доставки, содержащие наночастицы, обладают более низкой эффективностью доставки в клетки, чем вирусные системы доставки, но имеют преимущества, включая высокую безопасность in vivo, мишень-специфическую доставку, эффективное поглощение и интернализацию олигонуклеотидов RNAi в клетки или ткани, и низкую цитотоксичность и иммунностимуляцию. Таким образом, невирусные системы доставки в настоящее время считаются более перспективным способом доставки, чем вирусные системы доставки.
Из числа невирусных систем доставки, способы с использованием наноносителей, представляют собой способы, в которых наночастицы формируют с использованием различных полимеров, таких как липосомы и катионные полимерные комплексы, и в которых siRNA наносят на такие наночастицы (т.е. наноносители) и доставляют в клетки. Среди способов с использованием наноносителей, часто используемые способы включают способы с использованием полимерных наночастиц, полимерных мицелл, липоплексов и т.п. В частности, липоплексы состоят из катионных липидов и функционируют путем взаимодействия с анионными липидами клеточных эндосом для индукции дестабилизации эндосом, таким образом обеспечивая возможность внутриклеточной доставки экзосом.
Кроме того, известно, что эффективность siRNA in vivo может быть увеличена путем конъюгирования химического соединения или подобного вещества с концевым участком пассажирской (смысловой) цепи siRNA, чтобы тем самым наделить ее улучшенными фармакокинетическими характеристиками (J. Soutschek, Nature 11; 432(7014):173-8, 2004). В этом случае стабильность siRNA изменяется в зависимости от свойств химического соединения, конъюгированного с концом смысловой (пассажирской) или антисмысловой (направляющей) цепи siRNA. Например, siRNA, конъюгированная с полимерным соединением, таким как полиэтиленгликоль (PEG), взаимодействует с анионной фосфатной группой siRNA в присутствии катионного соединения с образованием комплекса, таким образом, обеспечивая носитель, обладающий улучшенной стабильностью siRNA. В частности, мицеллы, состоящие из полимерного комплекса, имеют очень малый размер и очень однородное распределение по размерам по сравнению с другими системами доставки лекарственных средств, такими как микросферы или наночастицы, и образуются спонтанно. Таким образом, эти мицеллы имеют преимущества, заключающиеся в том, что качество мицеллярного состава легко регулируется и легко обеспечивается его воспроизводимость.
Для улучшения эффективности внутриклеточной доставки siRNA была разработана технология обеспечения стабильности siRNA и увеличения проницаемости клеточных мембран для siRNA с использованием конъюгата siRNA, полученного путем конъюгирования гидрофильного соединения (например, полиэтиленгликоля (PEG)), которое представляет собой биосовместимый полимер, с siRNA посредством простой ковалентной связи или опосредованной линкером ковалентной связи (корейский патент № 883471). Однако, даже когда siRNA химически модифицирована и конъюгирована с полиэтиленгликолем (PEG) (ПЭГилирование), она все еще имеет низкую стабильность in vivo и недостаток, состоящий в том, что ее не просто доставить в целевой орган. Для устранения указанных недостатков была разработана структура, содержащая двухцепочечную олиго-РНК, которая содержит гидрофильные и гидрофобные соединения, соединенные с олигонуклеотидом, в частности, двухцепочечной олиго-РНК, такой как siRNA. Эта структура формирует самособирающиеся наночастицы, названные SAMiRNA™ (Self Assembled Micelle Inhibitory RNA), за счет гидрофобного взаимодействия гидрофобного соединения (корейский патент № 1224828). Технология SAMiRNA™ обладает преимуществами перед традиционными технологиями доставки в том, что могут быть получены однородные наночастицы, имеющие очень маленький размер.
В частности, в технологии SAMiRNA™ в качестве гидрофильного соединения используют PEG (полиэтиленгликоль) или HEG (гексаэтиленгликоль). PEG, синтетический полимер, обычно используют для повышения растворимости лекарственных средств, особенно белков, и для регулирования фармакокинетических свойств лекарственных средств. PEG представляет собой полидисперсный материал, и полимер в одной партии состоит из суммы различного числа мономеров и, таким образом, показывают молекулярную массу, распределенную по кривой Гаусса. Кроме того, однородность материала выражается в виде индекса полидисперсности (Mw/Mn). Другими словами, когда PEG имеет низкую молекулярную массу (3-5 кДа), он имеет индекс полидисперсности около 1,01, и когда PEG имеет высокую молекулярную массу (20 кДа), он имеет высокий индекс полидисперсности около 1,2, что указывает на то, что однородность PEG снижается по мере увеличения его молекулярной массы. Таким образом, когда PEG конъюгирован с фармацевтическим лекарственным средством, имеется недостаток, заключающийся в том, что показатель полидисперсности PEG отражаются на конъюгате, и поэтому затруднительно выполнить верификацию одного материала. Из-за этого недостатка способы синтеза и очистки PEG были усовершенствованы для получения материалов, имеющих низкий индекс полидисперсности. Однако, когда PEG конъюгирован с соединением, имеющим низкую молекулярную массу, возникают проблемы, связанные со свойствами полидисперсности соединения, включая трудности, связанные с подтверждением конъюгирования.
Соответственно, в последние годы технология SAMiRNA™ (то есть самособирающиеся наночастицы) была усовершенствована путем формирования гидрофильного соединения двухцепочечной структуры РНК (составляющей SAMiRNA™) в виде блоков из базовых единиц, каждый из которых содержит от 1 до 15 мономеров, имеющих одинаковую молекулярную массу, и по необходимости линкер, и по необходимости используется соответствующее число таких блоков. Таким образом, были разработаны новые типы технологий систем доставки, которые имеют малые размеры и значительно улучшенную полидисперсность по сравнению с существующими SAMiRNA™. Уже известно, что при введении siRNA, siRNA быстро расщепляется различными ферментами, присутствующими в крови, и поэтому эффективность ее доставки в целевые клетки или ткани является низкой. Таким образом, колебание стабильности и степени ингибирования экспрессии в зависимости от целевых генов также проявлялось в улучшенной SAMiRNA™. Соответственно, чтобы более стабильно и эффективно ингибировать экспрессию целевого гена с помощью SAMiRNA™, которая состоит из усовершенствованных самособирающихся наночастиц, авторы настоящего изобретения попытались усилить ингибирующий экспрессию эффект SAMiRNA™ на целевой ген и стабильность SAMiRNA™ путем применения двухцепочечного олигонуклеотида, содержащего ДНК-последовательность ASO в качестве направляющей (смысловой) цепи и РНК-последовательность в качестве пассажирской (антисмысловой) последовательности.
Между тем, ожирение является важной проблемой здравоохранения во всем мире и может привести к увеличению числа осложнений, таких как болезни сердца, диабет 2 типа и некоторые виды рака.
Одной из основных причин ожирения является избыточное накопление висцерального жира в организме [Carr DB, Diabetes. 2004 Aug;53(8):2087-94; Bouchard C, Int J Obes Relat Metab Disord 1996;20:420-7]. Висцеральный жир относится к жиру, окружающему внутренние органы, а висцеральный жир в основном вызван генетическим фактором [Rosenberg B, Panminerva Med 2005; 47:229-44], расой, физической активностью, образом жизни и воспалительными факторами [Deurenberg P, Int J Obes Relat Metab Disord 1998;22:1164-71]. Кроме того, известно, что накопление висцерального жира сильно выражено у азиатов среди представителей различных рас [WHO Expert Consultation. Lancet 2004;363:157-63; Hu FB, N Engl J Med 2001;345:790-7], и переедание или питье, меньшая физическая активность [Wannamethee SG, Am J Clin Nutr 2003; 77:1312-7; Komiya H, Tohoku J Exp Med 2006;208:123-32], и курение еще больше увеличивает количество висцерального жира [Upadhyaya S, Adipocyte, 2014; 3(1): 39-45]. При накоплении висцерального жира увеличивается секреция провоспалительных факторов, таких как интерлейкин-6, фактор некроза опухоли-альфа и моноцитарный хемоаттрактантный белок-1, из клеток висцерального жира, вызывая различные осложнения [Despres JP. Ann Med 2001;33:534-41]. Висцеральный жир вызывает метаболические нарушения и сердечно-сосудистые заболевания [Matsuzawa Y, Obes Res 1995;3 Suppl 5:645-7]. Повышенное накопление висцерального жира приводит к повышению резистентности к инсулину, а если висцеральный жир перевешивает подкожный жир, снижается функция сердца и возникают гипертония и заболевания системы кровообращения [Schaffler, Nat Clin Pract Gastroenterol Hepatol 005;2:273-80]. Висцеральный жир также вызывает расстройства пищеварения и, как известно, вызывает ожирение печени и неалкогольный стеатогепатит [Busetto L, Diabetes Obes Metab 2005; 7:301-6]. Из-за этих факторов противовоспалительные механизмы деградируют по мере снижения уровня адипонектина и способствуют формированию жировой дистрофии печени, вызывая неалкогольную жировую дистрофию печени. Висцеральный жир также вызывает множество проблем при респираторных заболеваниях [Schapira DV, Cancer 1994; 74:632-9]. Видно, что по мере того, как висцеральный жир перевешивает подкожный жир, резервный объем выдоха уменьшается, вызывая рестриктивную дисфункцию легочной вентиляции. Также известно, что висцеральный жир увеличивает заболеваемость раком молочной железы. Также известно, что висцеральный жир связан с повышенной заболеваемостью раком предстательной железы [Hsing AW, J Natl Cancer Inst 2001; 93:783-9] и колоректальным раком [Manson JE, N Engl J Med 1995; 333:677-85].
Лечение висцерального жира в основном заключается в ограничении диеты, физических упражнениях и медикаментозном лечении, но их эффект все еще недостаточен [Diamantis T, Surg Obes Relat Dis, 2014; 10(1): 177-83 ; Kelley GA, J Obes, 2013; 2013783103 ; Rhines SD, S D Med, 2013; 66(11): 471, 73 ; Sharma M, Adolesc Health Med Ther, 2010; 19-19]. Следовательно, уменьшение висцерального жира может снизить частоту сердечно-сосудистых заболеваний, нарушений обмена веществ, диабета и других заболеваний, тем самым предотвращая осложнения и улучшая качество жизни.
Соответственно, авторы настоящего изобретения провели исследования по лечению ожирения путем уменьшения висцерального жира и в результате обнаружили, что использование структуры, содержащей амфирегулин-специфический двухцепочечный олигонуклеотид, который специфически ингибирует амфирегулин, может значительно снизить висцеральный жир, включая подкожный жир, в диабетических животных моделях.
Кроме того, авторы настоящего изобретения обнаружили, что уровень экспрессии амфирегулина в эпидидимальном жире является значительно высоким в животной модели с ожирением, индуцированным диетой с высоким содержанием жиров, и, когда уровень экспрессии амфирегулина в животной модели с ожирением снижается с использованием структуры, содержащей амфирегулин-специфический двухцепочечный олигонуклеотид в соответствии с настоящим изобретением, можно значительно снизить массу тела, массу подкожного жира и массу висцерального жира, подавить увеличение размера клеток жировой ткани, уменьшить экспрессию амфирегулина в жировой ткани и ингибировать накопление жира в печени, тем самым завершая настоящее изобретение, относящееся к применению против ожирения структуры, содержащей амфирегулин-специфический двухцепочечный олигонуклеотид.
Краткое описание изобретения
Целью настоящего изобретения является обеспечение новой фармацевтической композиции для лечения или предупреждения ожирения.
Для достижения вышеуказанной цели настоящее изобретение обеспечивает фармацевтическую композицию для лечения или предупреждения ожирения, содержащую любой компонент, выбранный из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную последовательности смысловой цепи;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, содержащей структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii).
Настоящее изобретение также обеспечивает лиофилизированный состав, содержащий фармацевтическую композицию.
Настоящее изобретение также обеспечивает способ предупреждения или лечения ожирения, включающий стадию введения субъекту, нуждающемуся в предупреждении или лечении ожирения, любого компонента, выбранного из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную последовательности смысловой цепи;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, содержащей структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii).
Настоящее изобретение также обеспечивает фармацевтическую композицию для применения в способе предупреждения или лечения ожирения, при этом фармацевтическая композиция содержит любой компонент, выбранный из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную последовательности смысловой нити;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, содержащей структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляют собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii).
Настоящее изобретение обеспечивает применение любого из компонентов, выбранных из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную последовательности смысловой нити;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, содержащей структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii), в изготовлении лекарственного средства для предупреждения или лечения ожирения.
Краткое описание чертежей
На фиг. 1 показаны результаты скрининга 1257 SAMiRNA, нацеленных на человеческий амфирегулин.
На фиг. 2 показано распределение наночастиц по размерам двухцепочечных олиго ДНК/РНК гибридов, содержащих выбранный амфирегулин-специфический двухцепочечный олигонуклеотид. (а): SAMi-AREG#10; (b): SAMi-AREG#11; и (c): SAMi-AREG#12.
На фиг. 3 представлены графики, демонстрирующие результаты количественного анализа уровней экспрессии мРНК амфирегулина, описанного в примере 4. В данном случае клеточную линию рака легкого A549 обрабатывали различными концентрациями (200 и 600 нМ) SAMiRNA, имеющей каждую из последовательностей SEQ ID NO: 1-14 по настоящему изобретению в качестве смысловой цепи, и анализировали относительные уровни экспрессии мРНК амфирегулина (%) в клетках.
На фиг. 4 представлены графики, показывающие результаты количественного анализа уровней экспрессии мРНК амфирегулина, описанного в примере 5. В данном случае клеточную линию рака легкого A549 обрабатывали различными концентрациями (12,5 нМ, 25 нМ, 50 нМ, 100 нМ, 200 нМ, 600 нМ и 1200 нМ) SAMiRNA, имеющей последовательность SEQ ID NO: 10 по настоящему изобретению в качестве смысловой цепи, анализировали относительные уровни экспрессии мРНК амфирегулина (%) в клетках (фиг. 4a), и определяли значение IC50 SAMiRNA (фиг. 4b).
На фиг. 5 представлены графики, показывающие результаты количественного анализа уровней экспрессии мРНК амфирегулина, описанного в примере 5. В данном случае клеточную линию рака легкого A549 обрабатывали различными концентрациями (12,5 нМ, 25 нМ, 50 нМ, 100 нМ, 200 нМ, 600 нМ и 1200 нМ) SAMiRNA, имеющей последовательность SEQ ID NO: 11 по настоящему изобретению в качестве смысловой цепи, анализировали относительные уровни экспрессии мРНК амфирегулина (%) в клетках (фиг. 5a), и определяли значение IC50 SAMiRNA (фиг. 5b).
На фиг. 6 представлены графики, показывающие результаты количественного анализа уровней экспрессии мРНК амфирегулина, описанного в примере 5. В данном случае клеточную линию рака легкого A549 обрабатывали различными концентрациями (12,5 нМ, 25 нМ, 50 нМ, 100 нМ, 200 нМ, 600 нМ и 1200 нМ) SAMiRNA, имеющей последовательность SEQ ID NO: 12 по настоящему изобретению в качестве смысловой цепи, анализировали относительные уровни экспрессии мРНК амфирегулина (%) в клетках (фиг. 6a), и определяли значение IC50 SAMiRNA (фиг. 6b).
На фиг. 7 представлены графики, показывающие результаты теста врожденного иммунного ответа на последовательности-кандидаты амфирегулина, описанного в примере 6. В данном случае мононуклеарные клетки периферической крови (РВМС) обрабатывали 2,5 мкМ амфирегулин-специфической SAMiRNA, имеющей каждую из последовательностей SEQ ID NO: 10 (AR-1), 11 (AR-2) и 12 (AR3) по настоящему изобретению в качестве смысловой цепи, анализировали относительное увеличение уровней экспрессии мРНК цитокинов, связанных с врожденным иммунитетом, вызванного амфирегулин-специфичной SAMiRNA, и оценивали цитотоксичность in vitro с использованием мононуклеарных клеток периферической крови человека. (a): гибрид ДНК/РНК SAMiRNA и (b): гибрид РНК/РНК SAMiRNA.
На фиг. 8 показан график, показывающий результаты количественного анализа уровней экспрессии мРНК амфирегулина, описанного в примере 7. В данном случае представлен сравнительный анализ относительных уровней экспрессии мРНК (%) амфирегулина при двухцепочечном олиго-ДНК/РНК-гибриде и РНК/РНК-гибриде, каждый из которых содержит выбранные амфирегулин-специфические SAMiRNA. В частности, обрабатывали линию клеток рака легкого A549 различными концентрациями (200 нМ, 600 нМ и 1200 нМ) SAMiRNA, имеющей каждую из последовательностей SEQ ID NO: 10 (AR-1), 11 (AR-2) и 12 (AR-3) по настоящему изобретению в качестве смысловой цепи, и проводили сравнительный анализ относительных уровней экспрессии мРНК амфирегулина (%).
На фиг. 9 показаны результаты скрининга 237 SAMiRNA, нацеленных на мышиный амфирегулин, и 9 выбранных из них последовательностей-кандидатов.
На фиг. 10A представлены графики, показывающие результаты количественного анализа уровней экспрессии мРНК амфирегулина, описанного в примере 8. В данном случае клеточную линию фибробластов легкого мыши MLg обрабатывали различными концентрациями (200 и 500 нМ) SAMiRNA, имеющей каждую из последовательностей SEQ ID NO: 19, 20 и 21 по настоящему изобретению в качестве смысловой цепи, и анализировали относительные уровни экспрессии мРНК амфирегулина (%) в клетках.
На фиг. 10B представлены графики, показывающие результаты количественного анализа уровней экспрессии мРНК амфирегулина, описанного в примере 7. В данном случае линию эпителиальных клеток легкого мыши LA-4 обрабатывали различными концентрациями (200 и 500 нМ) SAMiRNA, имеющей каждую из последовательностей SEQ ID NOs : 19, 20 и 21 по настоящему изобретению в качестве смысловой цепи, и анализировали относительные уровни экспрессии мРНК амфирегулина (%) в клетках.
На фиг. 11 показан график, показывающий изменения массы тела контрольной группы и экспериментальных групп в эксперименте на мышиной животной модели в соответствии с настоящим изобретением.
На фиг. 12 представлен график, показывающий изменения в потреблении пищи контрольной группой и экспериментальными группами в эксперименте на мышиной животной модели в соответствии с настоящим изобретением.
На фиг. 13 представлен график, показывающий изменения в потреблении воды контрольной группой и экспериментальными группами в эксперименте на мышиной животной модели в соответствии с настоящим изобретением.
На фиг. 14 показаны результаты измерения доли подкожного жира в каждой из контрольной группы и экспериментальных групп в эксперименте на мышиной животной модели в соответствии с настоящим изобретением.
На фиг. 15 показаны результаты измерения доли висцерального жира в контрольной группе и экспериментальных группах в эксперименте на мышиной животной модели в соответствии с настоящим изобретением.
На фиг. 16 представлены фотографии, демонстрирующие влияние структуры в соответствии с настоящим изобретением на уменьшение висцерального жира в эксперименте на мышиной животной модели в соответствии с настоящим изобретением.
На фиг. 17 показаны результаты измерения уровня глюкозы в крови натощак в цельной крови за 8 недель до умерщвления контрольной группы и экспериментальных групп в эксперименте на мышиной животной модели в соответствии с настоящим изобретением.
На фиг. 18 показаны результаты измерения уровней глюкозы в сыворотке за 8 недель до умерщвления контрольной группы и экспериментальных групп в эксперименте на мышиной животной модели в соответствии с настоящим изобретением.
На фиг. 19 представлен график, показывающий результаты анализа уровня экспрессии амфирегулина в эпидидимальном жире после умерщвления контрольной группы и экспериментальной группы после 12 недель кормления кормом с высоким содержанием жиров в эксперименте на мышиной модели ожирения, вызванного диетой с высоким содержанием жиров, в соответствии с настоящим изобретением.
На фиг. 20 представлен график, показывающий изменения массы тела контрольной группы и экспериментальной группы в эксперименте на модели мышей с ожирением, получавших диету с высоким содержанием жиров, в соответствии с настоящим изобретением.
На фиг. 21а представлен график, показывающий среднее потребление пищи каждой из контрольной группы и экспериментальной группы в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
На фиг. 21b представлен график, показывающий среднее потребление воды каждой из контрольной группы и экспериментальной группы в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
На фиг. 22 представлен график, показывающий коэффициент пищевой эффективности (%) каждой из контрольной группы и экспериментальной группы в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
На фиг. 23а показаны результаты измерения массы подкожного жирового тела (SFP), эпидидимального жирового тела (EFP), околопочечного жирового тела (PFP), брыжеечного жирового тела (MFP), подкожного жирового тела (SFP), эпидидимального жирового тела (EFP), околопочечного жирового тела (PFP) и брыжеечного жирового тела (MFP) каждой из контрольной группы и экспериментальной группы в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
На фиг. 23а показаны соотношения (%), полученные путем деления массы подкожного жирового тела (SFP), эпидидимального жирового тела (EFP), околопочечного жирового тела (PFP), брыжеечного жирового тела (MFP), подкожного жирового тела (SFP), эпидидимального жирового тела (EFP), околопочечного жирового тела (PFP) и брыжеечного жирового тела (MFP) каждой из контрольной группы и экспериментальной группы на массу тела в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
На фиг. 24b показаны результаты измерения соотношения каждого из подкожного жира и висцерального жира к общей массе мыши в каждой из контрольной группы и экспериментальной группы в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
На фиг. 25 представлены микро-КТ-изображения, сравнивающие эффект уменьшения подкожного жира и висцерального жира между контрольной группой и экспериментальной группой в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением, и представлены графики, показывающие объем каждого из подкожного жира и висцерального жира.
На фиг. 26 представлены гистологические изображения, сравнивающие эффект уменьшения подкожного жирового тела (SFP), эпидидимального жирового тела (EFP), околопочечного жирового тела (PFP) и брыжеечного жирового тела (MFP) между контрольной группой и экспериментальной группой в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением, и представлены графики, показывающие площадь адипоцитов в каждой группе.
На фиг. 27а представлены изображения, сравнивающие эффект уменьшения накопления жира в ткани печени между контрольной группой и экспериментальной группой в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
На фиг. 27b представлен количественный график, показывающий эффект уменьшения накопления жира в ткани печени между контрольной группой и экспериментальной группой в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
На фиг. 28 представлены графики, сравнивающие эффект снижения уровней мРНК амфирегулина в подкожном жировом теле (SFP), эпидидимальном жировом теле (EFP) и околопочечном жировом теле (PFP) между контрольной группой и экспериментальной группой в эксперименте на модели мышей с ожирением, вызванным диетой с высоким содержанием жиров в соответствии с настоящим изобретением.
Подробное описание и предпочтительные варианты осуществления изобретения
Если не указано иное, все технические и научные термины, используемые в настоящем описании, имеют те же значения, которые обычно понимаются специалистами в области, к которой относится настоящее раскрытие. В общем, номенклатура, используемая в настоящем описании, хорошо известна и широко используется в данной области техники.
В настоящем изобретении было обнаружено, что при введении амфирегулин-специфической двухцепочечной олигонуклеотидной структуры животной модели диабета 2 типа она проявляет эффект значительного уменьшения подкожного жира и висцерального жира, что указывает на то, что амфирегулин-специфическая двухцепочечная олигонуклеотидная структура может быть использована в качестве композиции для предупреждения или лечения ожирения.
Кроме того, в настоящем изобретении было обнаружено, что когда амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру вводят животной модели с индуцированным ожирением, она проявляет эффекты потери веса, снижения коэффициента пищевой эффективности, уменьшения подкожного жира, уменьшения висцерального жира, уменьшения площади адипоцитов и ингибирования адипогенеза печени.
Таким образом, в одном аспекте настоящее изобретение направлено на фармацевтическую композицию для лечения или предупреждения ожирения, содержащую любой компонент, выбранный из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную последовательности смысловой цепи;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, содержащей структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii).
Последовательности SEQ ID NO: 10, 11 и 12, каждая из которых содержится в предпочтительном двухцепочечном олигонуклеотиде, обеспеченном в соответствии с настоящим изобретением, являются следующими:
5'-CACCTACTCTGGGAAGCGT-3' (SEQ ID NO: 10),
5'-ACCTACTCTGGGAAGCGTG-3' (SEQ ID NO: 11),
5'-CTGGGAAGCGTGAACCATT-3' (SEQ ID NO: 12).
Используемый в настоящем документе термин «двухцепочечный олигонуклеотид» включает все материалы, обладающие общей активностью в отношении RNAi (РНК-интерференция), и специалистам в данной области будет очевидно, что мРНК-специфический двухцепочечный олигонуклеотид который кодирует белок амфирегулин, также включает амфирегулин-специфическую shRNA и т.п. То есть олигонуклеотид может представлять собой siRNA, shRNA или miRNA.
Кроме того, специалистам в данной области будет очевидно, что амфирегулин-специфическая siRNA, которая содержит смысловую цепь и антисмысловую цепь, или антисмысловой олигонуклеотид, каждый содержащий последовательность, полученную в результате замены, делеции или вставки одного или нескольких нуклеотидов в смысловой цепи, содержащей любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, или комплементарную ей антисмысловую цепь, также входит в объем настоящего изобретения при условии, что сохраняется ее специфичность к амфирегулину.
В настоящем изобретении смысловая или антисмысловая цепь может независимо представлять собой ДНК или РНК. Кроме того, смысловая и антисмысловая цепи могут быть в форме гибрида, в котором смысловая цепь представляет собой ДНК, а антисмысловая цепь представляет собой РНК, или смысловая цепь представляет собой РНК, а антисмысловая цепь представляет собой ДНК.
В настоящем изобретении SEQ ID NO: 10, 11 и 12 представлены в форме ДНК, но когда используется форма РНК, последовательности SEQ ID NO: 10, 11 и 12 могут представлять собой соответствующие им последовательности РНК, то есть последовательности, в которых T заменен на U.
Кроме того, двухцепочечный олигонуклеотид в соответствии с настоящим изобретением включает не только случай, когда смысловая цепь последовательности является полностью комплементарной (полностью совпадает с) сайту(ом) связывания гена амфирегулина, но также и случай, когда смысловая цепь является частично комплементарной (не совпадает с) сайту(ом) связывания, до тех пор пока сохраняется специфичность к амфирегулину.
Двухцепочечный олигонуклеотид в соответствии с настоящим изобретением может содержать на 3'-конце одной или обеих цепей выступающий конец, содержащий один или несколько неспаренных нуклеотидов.
В настоящем изобретении смысловая цепь или антисмысловая цепь предпочтительно состоит из 19-31 нуклеотида, но без ограничения.
В настоящем изобретении двухцепочечный олигонуклеотид, содержащий смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую комплементарную ей последовательность, может быть специфическим в отношении амфирегулина, но настоящее изобретение этим не ограничивается.
В настоящем изобретении смысловая цепь или антисмысловая цепь двухцепочечного олигонуклеотида может содержать различные химические модификации для повышения его стабильности in vivo или придания устойчивости к нуклеазам и снижения неспецифических иммунных ответов. Химическая модификация может представлять собой одну или несколько модификаций, выбранных, но без ограничения, из группы, состоящей из следующих химических модификаций: модификация, при которой ОН-группа в положении 2'-углерода в структуре сахара у одного или нескольких нуклеотидах замещена на любую группу, выбранную из группы, состоящей из метильной группы (-CH3), метоксигруппы (-OCH3), аминогруппы (-NH2), фтора (-F), -O-2-метоксиэтильной группы, -O-пропильной группы, -O-2-метилтиоэтильной группы, -O-3-аминопропильной группы, -O-3-диметиламинопропильной группы, -O-N-метилацетамидогруппы и -O-диметиламидооксиэтильной группы; модификация, при которой кислород в структуре сахара у нуклеотидов заменен на серу; модификация нуклеотидных связей на любую связь, выбранную из группы, состоящей из фосфоротиоатной связи, боранофосфатной связи и метилфосфонатной связи; модификация в PNA (пептидную нуклеиновую кислоту), LNA (запертую нуклеиновую кислоту) или UNA (незапертую нуклеиновую кислоту); и модификация гибрида ДНК-РНК (Ann. Rev. Med. 55, 61-65 2004; US 5,660,985; US 5,958,691; US 6,531,584; US 5,808,023; US 6,326,358; US 6,175,001; Bioorg. Med. Chem. Lett. 14:1139-1143, 2003; RNA, 9:1034-1048, 2003; Nucleic Acid Res. 31:589-595, 2003; Nucleic Acids Research, 38(17) 5761-773, 2010; Nucleic Acids Research, 39(5):1823-1832, 2011).
В настоящем изобретении одна или несколько фосфатных групп, предпочтительно от одной до трех фосфатных групп, могут быть связаны с 5'-концом антисмысловой цепи двухцепочечного олигонуклеотида.
В другом аспекте настоящее изобретение направлено на двухцепочечную олигонуклеотидную структуру, имеющую структуру, представленную следующей структурной формулой (1), где А представляет собой гидрофильное соединение, В представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой двухцепочечный олигонуклеотид.
В предпочтительном варианте осуществления двухцепочечная олигонуклеотидная структура, содержащая амфирегулин-специфическую последовательность в соответствии с настоящим изобретением, предпочтительно имеет структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид.
Двухцепочечный олигонуклеотид в соответствии с настоящим изобретением предпочтительно находится в форме гибрида ДНК-РНК, siRNA (короткая интерферирующая РНК), shRNA (короткошпилечная РНК) или miRNA (микроРНК), но без ограничения, и может также включать одноцепочечный ингибитор miRNA, который может действовать как антагонист против miRNA.
Далее двухцепочечный олигонуклеотид в соответствии с настоящим изобретением будет описан с акцентом на РНК, но специалистам в данной области будет очевидно, что настоящее изобретение может также применяться к другим двухцепочечным олигонуклеотидам, обладающим теми же характеристиками, что и двухцепочечный олигонуклеотид по настоящему изобретению.
Более предпочтительно, двухцепочечная олигонуклеотидная структура, содержащая амфирегулин-специфический двухцепочечный олигонуклеотид по настоящему изобретению, имеет структуру, представленную следующей структурной формулой (2):
Структурная формула (2)
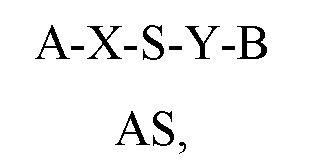
где A, B, X и Y имеют значения, указанные выше в структурной формуле (1), S представляет собой смысловую цепь амфирегулин-специфического двухцепочечного олигонуклеотида, и AS представляет собой антисмысловую цепь амфирегулин-специфического двухцепочечного олигонуклеотида.
Более предпочтительно, двухцепочечная олигонуклеотидная структура, содержащая амфирегулин-специфический двухцепочечный олигонуклеотид, имеет структуру, представленную следующей структурной формулой (3) или (4):
Структурная формула (3)

Структурная формула (4)
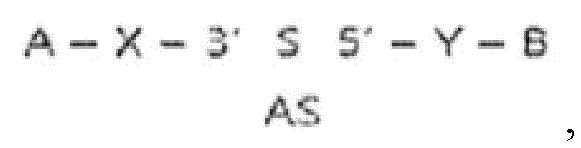
где A, B, S, AS, X и Y являются такими, как определено в структурной формуле (2) выше, а 5' и 3' представляют собой 5'-конец и 3'-конец, соответственно, смысловой цепи амфирегулин-специфического двухцепочечного олигонуклеотида.
Гидрофильное соединение может быть выбрано из группы, состоящей из полиэтиленгликоля (PEG), поливинилпирролидона и полиоксазолина, но без ограничения.
Для специалистов в области, к которой относится настоящее изобретение, очевидно, что от одной до трех фосфатных групп могут быть связаны с 5'-концом антисмысловой цепи двухцепочечной олигонуклеотидной РНК структуры, содержащей амфирегулин-специфическую siRNA, показанную в структурной формуле с (1) по (4), и что shRNA можно использовать вместо РНК.
Гидрофильное соединение в структурной формуле (1) - структурной формуле (4) выше предпочтительно представляет собой полимерное соединение с молекулярной массой от 200 до 10000, более предпочтительно полимерное соединение с молекулярной массой от 1000 до 2000. Например, в качестве гидрофильного полимерного соединения предпочтительно использовать неионогенное гидрофильное полимерное соединение, такое как полиэтиленгликоль, поливинилпирролидон или полиоксазолин, без необходимости ограничения.
В частности, гидрофильное соединение (А) со структурной формулой (1) - структурной формулой (4) может быть использовано в форме гидрофильных блоков, как показано в следующих структурных формулах (5) или (6), и подходящее количество (n в структурной формуле (5) или (6)) таких гидрофильных блоков может быть использовано по мере необходимости, тем самым преодолевая проблемы, связанные с полидисперсными свойствами, которые могут возникнуть при использовании обычных синтетических полимерных соединений:
Структурная формула (5)
(A'm-J)n
Структурная формула (6)
(J-A' m)n
где A' представляет собой гидрофильный мономер, J представляет собой линкер, который соединяет m гидрофильных мономеров вместе или соединяет m гидрофильных мономеров с двухцепочечным олигонуклеотидом, m представляет собой целое число в диапазоне от 1 до 15, n представляет собой целое число в диапазоне от 1 до 10, и повторяющееся звено, представленное (A'm-J) или (J-Am'), соответствует основному звену гидрофильного блока.
Когда используется гидрофильный блок, показанный в структурной формуле (5) или (6) выше, двухцепочечная олигонуклеотидная структура, содержащая амфирегулин-специфический олигонуклеотид в соответствии с настоящим изобретением, может иметь структуру, представленную следующей структурной формулой (7) или (8):
Структурная формула (7)
(A'm-J)n-X-R-Y-B,
Структурная формула (8)
(J-A'm) n-X-R-Y-B,
где X, R, Y и B имеют значения, определенные в структурной формуле (1) выше, а A', J, m и n имеют значения, определенные в структурных формулах (5) и (6) выше.
В качестве гидрофильного мономера (A') в структурных формулах (5) и (6) выше можно использовать без ограничений один из неионогенных гидрофильных полимеров, если он совместим с целью настоящего изобретения. Предпочтительно можно использовать мономер, выбранный из соединений с (1) по (3), представленных в таблице 1 ниже. Более предпочтительно можно использовать мономер соединения (1). В соединении (1) G предпочтительно может быть выбран из O, S и NH.
В частности, среди гидрофильных мономеров, представленный соединением (1) мономер очень подходит для получения структуры в соответствии с настоящим изобретением, поскольку мономер имеет преимущества, заключающиеся в том, что в мономер могут быть введены различные функциональные группы, и мономер индуцирует небольшой иммунный ответ благодаря хорошей аффинности in vivo и отличной биосовместимости, может повышать стабильность in vivo двухцепочечного олигонуклеотида, содержащегося в структуре, представленной структурной формулой (7) или (8), и может увеличивать эффективность доставки двухцепочечного олигонуклеотида.
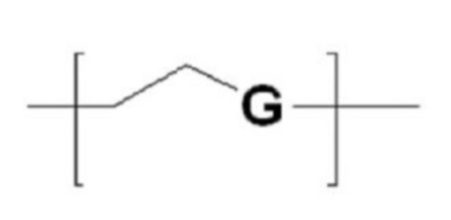 G представляет собой O, S или NH
G представляет собой O, S или NH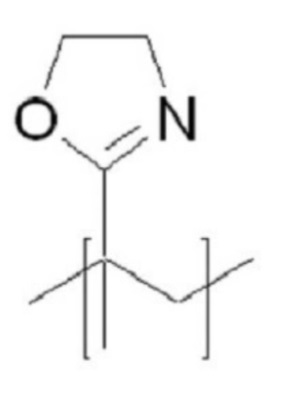
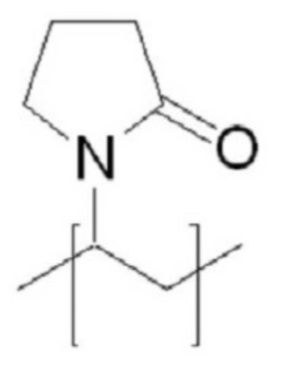
Общая молекулярная масса гидрофильного соединения в структурной формулах (5) - (8) предпочтительно находится в диапазоне от 1000 до 2000. Так, например, когда соединение (1) в структурной формуле (7) и структурной формуле (8) представляет собой гексаэтиленгликоль, то есть соединение, в котором G представляет собой О, а m равно 6, число повторов (n) предпочтительно равно 3-5, поскольку гексаэтиленгликолевый спейсер имеет молекулярную массу 344. В частности, настоящее изобретение характеризуется тем, что подходящее количество (обозначенное n) повторяющихся звеньев гидрофильной группы (гидрофильных блоков), представленных (A'm-J) или (J-A'm)n в структурной формуле (5) и структурной формуле (6), могут быть использованы по мере необходимости. Гидрофильный мономер J и линкер J, содержащиеся в каждом гидрофильном блоке, могут быть одинаковыми или разными в гидрофильных блоках. Другими словами, при использовании 3 гидрофильных блоков (n = 3) гидрофильный мономер соединения (1), гидрофильный мономер соединения (2) и гидрофильный мономер соединения (3) могут быть использованы в первом, втором и третьем блоках, соответственно, предполагая, что во всех гидрофильных блоках могут использоваться разные мономеры. Альтернативно, любой гидрофильный мономер, выбранный из гидрофильных мономеров соединений (1)-(3), также может быть использован во всех гидрофильных блоках. Точно так же в качестве линкера, который опосредует связывание гидрофильного мономера, в гидрофильных блоках можно использовать один и тот же линкер, или же в гидрофильных блоках можно использовать разные линкеры. Кроме того, m, которое представляет собой количество гидрофильных мономеров, также может быть одинаковым или различным между гидрофильными блоками. Другими словами, в первом гидрофильном блоке соединены три гидрофильных мономера (m=3), во втором гидрофильном блоке соединены пять гидрофильных мономеров (m=5), а в третьем гидрофильном блоке соединены четыре гидрофильных мономера (m=4), предполагая, что в гидрофильных блоках может быть использовано различное количество гидрофильных мономеров. Альтернативно, одинаковое количество гидрофильных мономеров может быть также использовано во всех гидрофильных блоках.
Кроме того, в настоящем изобретении линкер (J) предпочтительно выбирают из группы, состоящей из -PO3-, -SO3- и -CO2-, но без ограничения. Для специалистов в данной области очевидно, что можно использовать любой линкер, выбранный с учетом используемого гидрофильного мономера, при условии, что он совместим с целью настоящего изобретения.
Гидрофобное соединение (В) в структурных формулах (1) - (4), структурной формуле (7) и структурной формуле (8) функционирует с образованием наночастиц, состоящих из олигонуклеотидной структуры, показанной в структурных формулах (1) - (4), структурной формуле (7) и структурной формуле (8) посредством гидрофобных взаимодействий. Гидрофобное соединение предпочтительно имеет молекулярную массу от 250 до 1000 и может представлять собой любое соединение, выбранное из группы, состоящей из производного стероида, производного глицерида, простого эфира глицерина, полипропиленгликоля, ненасыщенного или насыщенного углеводорода C12-C50, диацилфосфатидилхолина, жирной кислоты, фосфолипида, липополиамина, липида, токоферола и токотриенола, но без ограничения. Для специалистов в данной области очевидно, что можно использовать любое гидрофобное соединение, если оно совместимо с целью настоящего изобретения.
Производное стероида может быть выбрано из группы, состоящей из холестерина, холестанола, холевой кислоты, холестерилформиата, холестанилформиата и холестериламина, а производное глицерида может быть выбрано из моно-, ди- и триглицеридов. и т.п. В настоящем документе жирная кислота глицерида предпочтительно представляет собой C12-C50 ненасыщенную или насыщенную жирную кислоту.
В частности, среди гидрофобных соединений предпочтительно используют насыщенный или ненасыщенный углеводород или холестерин, поскольку они могут быть легко связаны на стадии синтеза двухцепочечной олигонуклеотидной структуры в соответствии с настоящим изобретением. Наиболее предпочтительно используют углеводород C24, особенно гидрофобный углеводород, содержащий дисульфидную связь.
Гидрофобное соединение может быть связано с дистальным концом гидрофильного соединения и может быть связано с любым положением на смысловой или антисмысловой цепи двухцепочечного олигонуклеотида.
Гидрофильное соединение или гидрофобное соединение в структурных формулах (1)-(4), (7) и (8) в соответствии с настоящим изобретением связано с амфирегулин-специфическим олигонуклеотидом одинарной ковалентной связью или линкер-опосредованной ковалентной связью (X или Y). Линкер, который опосредует ковалентную связь, ковалентно соединяется с гидрофильным или гидрофобным соединением на конце амфирегулин-специфического олигонуклеотида и конкретно не ограничивается, если только он обеспечивает расщепляемую связь в конкретном окружении, если это необходимо. Таким образом, линкер, используемый в настоящем изобретении, может представлять собой любое соединение, которое присоединяется для активации амфирегулин-специфического двухцепочечного олигонуклеотида и/или гидрофильного (или гидрофобного) соединения в процессе получения двухцепочечной олигонуклеотидной структуры в соответствии с настоящим изобретением. Ковалентная связь может быть либо нерасщепляемой связью, либо расщепляемой связью. В настоящем документе примеры нерасщепляемой связи включают, но без ограничения, амидную связь и фосфатную связь, а примеры расщепляемой связи включают, но без ограничения, дисульфидную связь, расщепляемую кислотой связь, сложноэфирную связь, ангидридную связь, биоразлагаемую связь и ферментативно расщепляемую связь.
Кроме того, в качестве амфирегулин-специфического двухцепочечного олигонуклеотида, представленного R (или S и AS) в структурных формулах (1)-(4), (7) и (8), может быть использован без ограничений любой двухцепочечный олигонуклеотид, способный специфически связываться с мРНК амфирегулина. Предпочтительно, амфирегулин-специфический двухцепочечный олигонуклеотид по настоящему изобретению содержит смысловую цепь, содержащую любую последовательность, выбранную из SEQ ID NO: 10, 11 и 12, и антисмысловую нить, содержащую последовательность, комплементарную последовательности смысловой цепи.
Кроме того, в двухцепочечную олигонуклеотидную структуру, содержащую амфирегулин-специфический двухцепочечный олигонуклеотид в соответствии с настоящим изобретением, может быть дополнительно введена аминогруппа или полигистидиновая группа в концевую часть гидрофильного соединения, связанного с олигонуклеотидом в структуре.
Это облегчает внутриклеточный захват и выход из эндосом носителя, содержащего двухцепочечную олигонуклеотидную структуру, содержащую амфирегулин-специфический двухцепочечный олигонуклеотид в соответствии с настоящим изобретением, и уже сообщалось, что введение аминогруппы и полигистидиновой группы может быть использовано для облегчения внутриклеточного захвата и выхода из эндосом носителей, таких как квантовые точки, дендримеры или липосомы.
В частности, известно, что первичная аминогруппа, введенная на конце или вне носителя, протонируется при биологическом рН, при этом образуя конъюгат за счет взаимодействия с отрицательно заряженным геном, и что выход из эндосом облегчается за счет внутреннего третичного амина, оказывающего буферное действие при низком pH после внутриклеточного поглощения, посредством чего носитель может быть защищен от лизосомальной деградации (Gene Delivery and Expression Inhibition Using Polymer-Based Hybrid Material, Polymer Sci. Technol., Vol. 23, No. 3, pp 254-259).
Кроме того, известно, что незаменимая аминокислота гистидин имеет имидазольное кольцо (pKa = 6,04) на остатке (-R) и таким образом эффективно повышает буферную емкость в эндосомах и лизосомах, и, таким образом, модификация гистидином может применяться для повышения эффективности выхода из эндосом у невирусных носителей генов, включая липосомы (Novel histidine-conjugated galactosylated cationic liposomes for efficient hepatocyte selective gene transfer in human hepatoma HepG2 cells. J. Controlled Release 118, pp. 262-270).
Аминогруппа или полигистидиновая группа может соединяться с гидрофильным соединением или гидрофильным блоком через один или несколько линкеров.
При введении аминогруппы или полигистидиновой группы в гидрофильное соединение двухцепочечной олигонуклеотидной структуры, представленной структурной формулой (1) в соответствии с настоящим изобретением, структура РНК может иметь структуру, показанную в следующей структурной формуле (9):
Структурная формула (9)
P-J1-J2-A-X-R-Y-B,
где A, B, R, X и Y имеют значения, указанные выше в структурной формуле (1), P представляет собой аминогруппу или полигистидиновую группу, а J1 и J2 представляют собой линкеры, каждый из которых может быть независимо выбран из простой ковалентной связи, PO3-, SO3, CO2, C2-12 алкила, алкенила и алкинила, но без ограничения. Специалистам в данной области будет очевидно, что любые линкеры, выбранные с учетом используемого в настоящем документе гидрофильного соединения, могут быть использованы в качестве J1 и J2, если они совместимы с целью настоящего изобретения.
При введении аминогруппы предпочтительно J2 представляет собой простую ковалентную связь или PO3-, а J1 представляет собой C6 алкил, но без ограничения.
Кроме того, при введении полигистидиновой группы предпочтительно J2 в структурной формуле (9) представляет собой простую ковалентную связь или PO3-, а J1 представляет собой соединение (4), но без ограничения.
Соединение (4)
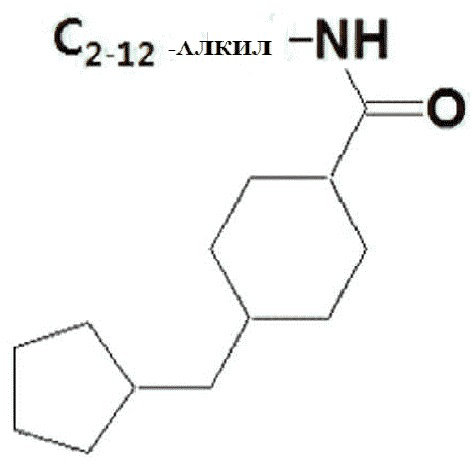
Кроме того, когда гидрофильное соединение двухцепочечной олигонуклеотидной структуры, показанной в структурной формуле (9), представляет собой гидрофильный блок, представленный структурной формулой (5) или (6), и при введении в него аминогруппы или полигистидиновой группы, двухцепочечная олигонуклеотидная структура может иметь структуру, представленную следующей структурной формулой (10) или (11):
Структурная формула (10)
P-J1-J2- (A'm-J)n -X-R-Y-B,
Структурная формула (11)
P-J1-J2- (J-A'm)n -X-R-Y-B,
где X, R, Y, B, A', J, m и n имеют значения, определенные выше в структурной формуле (5) или (6), а P, J1 и J2 имеют значения, определенные выше в структурной формуле (9).
В частности, гидрофильное соединение в структурной формуле (10) и структурной формуле (11) предпочтительно связано с 3'-концом смысловой цепи амфирегулин-специфического двухцепочечного олигонуклеотида. При этом структурные формулы (9)-(11) могут соответствовать следующим структурным формулам (12)-(14):
Структурная формула (12)
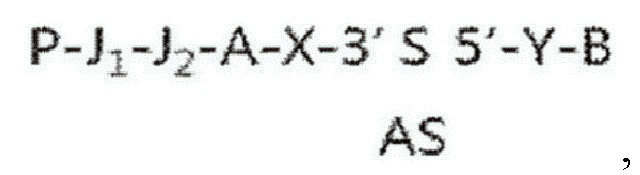
Структурная формула (13)
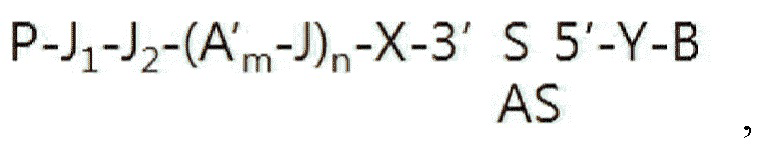
Структурная формула (14)
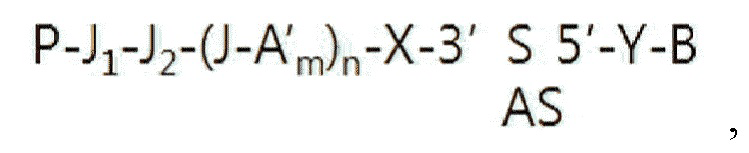
где X, R, Y, B, A, A' J, m, n, P, J1 и J2 имеют значения, определенные выше в структурных формулах (9)-(11), а 5' и 3' означают 5'-конец и 3'-конец смысловой цепи амфирегулин-специфического двухцепочечного олигонуклеотида.
Аминогруппа, которая может быть введена в настоящем изобретении, может представлять собой первичную, вторичную или третичную аминогруппу. В частности, предпочтительно используют первичную аминогруппу. Введенная аминогруппа может присутствовать в виде соли амина. Например, соль первичной аминогруппы может присутствовать в форме NH3+.
Кроме того, полигистидиновая группа, которая может быть введена в настоящем изобретении, предпочтительно содержит от 3 до 10 гистидинов, более предпочтительно от 5 до 8 гистидинов, и наиболее предпочтительно 6 гистидинов. В дополнение к гистидину может быть включен один или несколько цистеинов.
Между тем, когда нацеливающий фрагмент обеспечен в двухцепочечной олигонуклеотидной структуре, содержащей амфирегулин-специфический олигонуклеотид в соответствии с настоящим изобретением и образованные из него наночастицы, это может способствовать эффективной доставке структуры или наночастиц в клетки-мишени, таким образом, что структура или наночастицы могут быть доставлены в клетки-мишени даже в относительно низкой концентрации, где они будут проявлять сильный эффект регулирования экспрессии целевых генов. Кроме того, нацеливающий фрагмент может предотвратить неспецифическую доставку амфирегулин-специфического двухцепочечного олигонуклеотида в другие органы и клетки.
Соответственно, настоящее изобретение обеспечивает двухцепочечную олиго-РНК структуру, в которой лиганд (L), в частности, лиганд, обладающий свойством специфического связывания с рецептором, усиливающим интернализацию в клетки-мишени посредством рецептор-опосредованного эндоцитоза (RME), дополнительно связан со структурой, представленной любой из структурных формул (1)-(4), (7) и (8). Например, структура, в которой лиганд связан с двухцепочечной олиго-РНК структурой, представленной структурной формулой (1), представляет собой структуру, показанную в следующей структурной формуле (15):
Структурная формула (15)
(Li -Z)-A-X-R-Y-B,
где A, B, X и Y имеют значения, определенные выше в структурной формуле (1), L представляет собой лиганд, обладающий свойством специфического связывания с рецептором, усиливающим интернализацию в клетку-мишенью путем опосредованного рецептором эндоцитоза (RME), а «i» представляет собой целое число в диапазоне от 1 до 5, предпочтительно от 1 до 3.
Лиганд в структурной формуле (15) может быть предпочтительно выбран из: специфических к целевому рецептору антител, аптамеров и пептидов, обладающих свойством RME усиливать интернализацию в клетку-мишень; фолат (термин «фолат» обычно используется взаимозаменяемо с фолиевой кислотой, и используемый в настоящем документе термин «фолат» означает фолат, который находится в природной форме или в активированном состоянии в организме человека); и химические соединения, включая гексозамины, такие как N-ацетилгалактозамин (NAG), и сахара или углеводы, такие как глюкоза и манноза, но без ограничения.
Кроме того, гидрофильное соединение (А) в структурной формуле (15) выше можно использовать в форме гидрофильного блока, представленного структурной формулой (5) или (6).
В еще одном аспекте настоящее изобретение обеспечивает способ получения двухцепочечной олигонуклеотидной структуры, содержащей амфирегулин-специфический двухцепочечный олигонуклеотид.
Например, способ получения двухцепочечной олигонуклеотидной структуры, содержащей амфирегулин-специфический двухцепочечный олигонуклеотид в соответствии с настоящим изобретением, может включать следующие стадии:
(1) связывание гидрофильного соединения с твердой подложкой;
(2) синтез одиночной цепи олигонуклеотида на твердой подложке, связанной с гидрофильным соединением;
(3) ковалентное связывание гидрофобного соединения с 5'-концом одиночной цепи олигонуклеотида;
(4) синтез одиночной цепи олигонуклеотида, имеющей последовательность, комплементарную последовательности одиночной цепи олигонуклеотида, полученного на стадии (2);
(5) отделение и очистка структуры олигонуклеотид-полимер и одиночной цепи олигонуклеотида от твердой подложки после завершения синтеза; и
(6) отжиг полученной структуры олигонуклеотид-полимер с одиночной цепью олигонуклеотида, имеющей комплементарную последовательность, получая, таким образом, двухцепочечную олигонуклеотидную структуру.
Твердая подложка, используемая в настоящем изобретении, предпочтительно представляет собой стекло с контролируемым размером пор (CPG) и полистирол (PS), полиметилметакрилат (PMMA), силикагель, целлюлозную бумагу или т.п., но без ограничения. В случае использования CPG, оно предпочтительно имеет диаметр от 40 до 180 мм и размер пор от 500 до 3000 Å. После стадии (5) молекулярные массы полученной и очищенной структуры РНК-полимер и одиночной цепи олигонуклеотида могут быть измерены с использованием масс-спектрометра MALDI-TOF, чтобы подтвердить получение желаемой структуры олигонуклеотид-полимер и одиночной цепи олигонуклеотида. В вышеописанном способе получения стадия (4) синтеза одиночной цепи олигонуклеотида, имеющей последовательность, комплементарную последовательности одиночной цепи олигонуклеотида, синтезированной на стадии (2), может быть осуществлена до стадии (1) или во время любой стадии из стадий (1) - (5).
Кроме того, одиночная цепь олигонуклеотида, имеющая последовательность, комплементарную последовательности одиночной цепи олигонуклеотида, синтезированного на стадии (2), может быть использована в состоянии, в котором фосфатная группа связана с 5'-концом одиночной цепи олигонуклеотида.
Между тем, настоящее изобретение обеспечивает способ получения двухцепочечной олигонуклеотидной структуры, где лиганд дополнительно соединен с двухцепочечной олигонуклеотидной структурой, содержащей амфирегулин-специфический двухцепочечный олигонуклеотид.
Например, способ получения лиганд-связанной двухцепочечной олигонуклеотидной структуры, содержащей амфирегулин-специфический двухцепочечный олигонуклеотид, может включать следующие стадии:
(1) связывание гидрофильного соединения с твердой подложкой, имеющей связанную с ней функциональную группу;
(2) синтез одиночной цепи олигонуклеотида на твердой подложке, имеющей связанную с ней функциональную группу и гидрофильное соединение;
(3) ковалентное связывание гидрофобного соединения с 5'-концом одиночной цепи олигонуклеотида;
(4) синтез одиночной цепи олигонуклеотида, имеющего последовательность, комплементарную последовательности одиночной цепи олигонуклеотида, синтезированного на стадии (2);
(5) отделение структуры функциональная группа-олигонуклеотид-полимер и одиночной цепи олигонуклеотида, имеющего комплементарную последовательность, от твердой подложки после завершения синтеза;
(6) связывание лиганда с концом гидрофильного соединения с помощью функциональной группы с получением одиночной цепи структуры лиганд-олигонуклеотид-полимер; и
(7) отжиг полученной структуры лиганд-олигонуклеотид-полимер с одиночной цепью олигонуклеотида, имеющей комплементарную последовательность, с получением таким образом структуры лиганд/двухцепочечный олигонуклеотид.
После стадии (6) полученная структура лиганд-олигонуклеотид-полимер и одиночная цепь олигонуклеотида, имеющая комплементарную последовательность, могут быть разделены и очищены, а затем их молекулярные массы могут быть измерены с использованием масс-спектрометра MALDI-TOF для подтверждения получения желаемой структуры лиганд-РНК-полимер и желаемой одиночной цепи РНК, имеющей комплементарную последовательность. Путем отжига полученной структуры лиганд/РНК-олигонуклеотид с одиночной цепью олигонуклеотида, имеющей комплементарную последовательность, может быть получена структура лиганд/двухцепочечный олигонуклеотид. В вышеописанном способе получения стадия (4) синтеза одиночной цепи олигонуклеотида, имеющей последовательность, комплементарную последовательности одиночной цепи олигонуклеотида, синтезированной на стадии (3), может быть осуществлена до стадии (1) или во время любой стадии из стадий (1) - (6).
В еще одном аспекте настоящее изобретение направлено на наночастицы, содержащие двухцепочечную олигонуклеотидную структуру в соответствии с настоящим изобретением. Двухцепочечный олигонуклеотид в соответствии с настоящим изобретением образует самособирающиеся наночастицы за счет гидрофобного взаимодействия гидрофобного соединения (корейский патент № 1224828). Эти наночастицы обладают превосходной эффективностью доставки in vivo и стабильностью in vivo. Кроме того, высокая однородность наночастиц по размерам упрощает контроль качества (QC), и, таким образом, упрощается процесс изготовления этих наночастиц в качестве лекарственного средства.
В настоящем изобретении наночастица также может состоять из смеси двухцепочечных олигонуклеотидных структур, содержащей двухцепочечные структуры, содержащие различные последовательности. Например, наночастица может содержать один вид амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из SEQ ID NO: 10-12, и антисмысловую цепь, содержащую комплементарную ей последовательность; однако в другом варианте осуществления наночастица может содержать различные виды амфирегулин-специфических двухцепочечных олигонуклеотидов, каждый из которых содержит смысловую цепь, которая содержит любую последовательность, выбранную из SEQ ID NO: 10-12, и антисмысловую цепь, содержащую комплементарную ей последовательность, и может также содержать амфирегулин-специфический двухцепочечный олигонуклеотид, который не раскрыт в настоящем изобретении.
Для введения композиция по настоящему изобретению может дополнительно содержать один или несколько фармацевтически приемлемых носителей в дополнение к вышеописанному активному ингредиенту. Фармацевтически приемлемые носители должны быть совместимы с активным ингредиентом, и могут быть выбраны из физиологического раствора, стерильной воды, раствора Рингера, забуференного физиологического раствора, раствора декстрозы, раствора мальтодекстрина, глицерина, этанола и смеси двух или более из них. При необходимости композиция может содержать другие общепринятые добавки, такие как антиоксидант, буфер или бактериостатический агент. Кроме того, в композицию могут быть дополнительно добавлены разбавитель, диспергатор, поверхностно-активное вещество, связующее и смазывающее вещество для приготовления составов для инъекций, таких как водный раствор, суспензия и эмульсия. В частности, композиция предпочтительно представлена в виде лиофилизированного состава. Для приготовления лиофилизированного состава может быть использован общепринятый способ, известный в области, к которой относится настоящее изобретение, а также может быть добавлен стабилизатор для лиофилизации. Кроме того, композиция предпочтительно может быть составлена в зависимости от каждого заболевания или компонента с помощью подходящего способа, известного в данной области, или с помощью способа, раскрытого в Remington's Pharmaceutical Science, Mack Publishing Company, Easton PA.
Доза композиции по настоящему изобретению может быть определена специалистом в данной области исходя из состояния пациента и тяжести заболевания. Кроме того, композиция может быть составлена в различных дозированных формах, включая порошки, таблетки, капсулы, жидкости, растворы для инъекций, мази и рецептуры сиропов, и может поставляться в контейнерах для одной дозы или множества доз, например, в запечатанных ампулах или флаконах.
Композицию по настоящему изобретению можно вводить перорально или парентерально. Композицию по настоящему изобретению можно вводить, например, перорально, путем ингаляции, внутривенно, внутримышечно, внутриартериально, интрамедуллярно, интрадурально, интракардиально, чрескожно, подкожно, внутрибрюшинно, интраректально, сублингвально или местно без ограничения. Доза композиции в соответствии с настоящим изобретением может варьироваться в зависимости от массы тела, возраста, пола, состояния здоровья и диеты пациента, продолжительности введения, способа введения, скорости выведения, тяжести заболевания и т.п., и может быть легко определена специалистами в данной области. Кроме того, для клинического введения композиция по настоящему изобретению может быть приготовлена в виде подходящего состава с использованием известной способа.
В еще одном аспекте настоящее изобретение направлено на лиофилизированный состав, содержащий фармацевтическую композицию.
В другом аспекте настоящее изобретение направлено на способ предупреждения или лечения ожирения, включающий стадию введения субъекту, нуждающемуся в предупреждении или лечении ожирения, любого компонента, выбранного из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную последовательности смысловой цепи;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, представляющей собой структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii).
В другом дополнительном аспекте настоящее изобретение направлено на фармацевтическую композицию для применения в способе предупреждения или лечения ожирения, при этом фармацевтическая композиция содержит любой компонент, выбранный из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную смысловой цепи;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, представляющую собой структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii).
В еще одном дополнительном аспекте настоящее изобретение направлено на применение любого компонента, выбранного из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, содержащего смысловую цепь, которая содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную последовательности смысловой цепи;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, представляющей собой структуру, представленную следующей структурной формулой (1):
Структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii), в изготовлении лекарственного средства для предупреждения или лечения ожирения.
В настоящем изобретении ожирение может представлять собой ожирение по типу висцерального, вызванное диабетом, но настоящее изобретение этим не ограничивается.
В настоящем изобретении амфирегулин-специфическая двухцепочечная олигонуклеотидная структура в соответствии с настоящим изобретением может проявлять один или несколько из следующих эффектов, но настоящее изобретение этим не ограничивается:
(i) потеря массы тела,
(ii) снижение коэффициента пищевой эффективности,
(iii) уменьшение подкожного жира,
(iv) уменьшение висцерального жира,
(v) уменьшение площади адипоцитов и
(vi) ингибирование адипогенеза печени.
В настоящем изобретении эффект может проявляться путем ингибирования экспрессии амфирегулина в жировой ткани, но механизм, посредством которого этот эффект проявляется, не ограничивается.
Далее настоящее изобретение будет описано более подробно со ссылкой на примеры. Эти примеры предназначены только для иллюстрации настоящего изобретения, и специалистам в данной области техники будет очевидно, что объем настоящего изобретения не следует истолковывать как ограниченный этими примерами.
В настоящем изобретении были идентифицированы три специфические последовательности, способные ингибировать экспрессию амфирегулина, и было подтверждено, что эти последовательности могут комплементарно связываться с мРНК, кодирующей амфирегулин, и эффективно ингибировать экспрессию амфирегулина, тем самым эффективно осуществляя лечение связанных с ожирением заболеваний.
Пример 1. Алгоритм для скрининга SAMiRNA, нацеленных на амфирегулин, и отбор последовательностей-кандидатов
Высокопроизводительный скрининг лекарственных средств на основе SAMiRNA представляет собой способ, в котором все возможные последовательности-кандидаты генерируют путем применения алгоритма со скользящим окном из 1 или 2 оснований к тотальной мРНК, ненужные последовательности-кандидаты удаляют путем выполнения фильтрования по гомологии, и определяют степени, до которых ингибируется экспрессия интересующего гена всеми окончательно отобранными SAMiRNA.
Сначала выполняют процесс составления последовательностей-кандидатов SAMiRNA против амфирегулина. В частности, 1257 последовательностей-кандидатов SAMiRNA, каждая из которых состоит из 19 нуклеотидов, отбирали путем применения алгоритма со скользящим окном из 1 основания к мРНК амфирегулина человека NM_001657.3 (1290 п.н.), и проводили эксперимент по определению степени ингибирования амфирегулина.
Пример 2. Синтез двухцепочечной олиго-РНК структуры
Двухцепочечная олиго-РНК структура (SAMiRNA), полученная в настоящем изобретении, представлена следующей структурной формулой:
C24-5' S 3'-(гексаэтиленгликоль-PO3-)3-гексаэтиленгликоль AS 5'-PO4
Для синтеза смысловой цепи двухцепочечной олиго структуры мoнoSAMiRNA (n=4) в качестве подложки использовали 3,4,6-триацетил-1-гекса(этиленгликоль)-N-ацетилгалактозамин-CPG, и три деметокситритил (DMT) гексаэтиленгликоль-фосфорамидата в качестве гидрофильных мономеров непрерывно связывали с подложкой посредством реакции. Далее проводили синтез РНК или ДНК, а затем гидрофобный С24 (С6-S-S-С18), содержащий дисульфидную связь, связывали с 5'-концевым участком, тем самым синтезируя смысловую цепь моноSAMiРНК (n=4), в которой NAG- гексаэтиленгликоль-(-PO3-гексаэтиленгликоль)3 связан с 3'-концом, а C24 (C6-S-S-C18) связан с 5'-концом.
После завершения синтеза синтезированную одиночную цепь РНК и структуру олиго(ДНК или РНК)-полимер отделяли от CPG путем обработки 28% (об./об.) аммиаком на водяной бане при 60°С, а затем защитные остатки удаляли путем реакции снятия защиты. После удаления защитных остатков одиночную цепь РНК и конструкцию олиго(ДНК или РНК)-полимер обрабатывали N-метилпирролидоном, триметиламином и триэтиламинтригидрофторидом в объемном соотношении 10:3:4 в сушильном шкафу при 70°С для удаления 2'-TBDMS (трет-бутилдиметилсилила). Одиночную цепь РНК, структуру олиго(ДНК или РНК)-полимер и лиганд-связанную структуру олиго(ДНК или РНК)-полимер отделяли от продуктов реакции способом высокоэффективной жидкостной хроматографии (HPLC), и их молекулярные массы измеряли на масс-спектрофотометре MALDI-TOF (MALDI TOF-MS, SHIMADZU, Япония) для подтверждения их соответствия нуклеотидной последовательности и полимерной структуре, подлежащей синтезу. После этого для получения каждой двухцепочечной олиго структуры смешивали смысловую цепь и антисмысловую цепь, помещали в 1X буфер для отжига (30 мМ ГЭПЭС, 100 мМ ацетата калия, 2 мМ ацетата магния, рН от 7,0 до 7,5), оставляли для протекания реакции в течение 3 минут на водяной бане при 90°С, а затем оставляли для протекания реакции при 37°С, получая таким образом требуемую SAMiRNA. Отжиг полученных двухцепочечных олиго-РНК структур подтверждали с помощью электрофореза.
Пример 3. Высокопроизводительный скрининг (HTS) наночастиц SAMiRNA, которые нацелены на человеческий амфирегулин и индуцируют RNAi
3-1. Получение наночастиц SAMiRNA
1257 SAMiRNA, нацеленных на последовательности амфирегулина, синтезированных в примере 2, растворяли в 1X фосфатно-солевом буфере Дульбекко (DPBS) (WELGENE, KR) и лиофилизировали в лиофилизаторе (LGJ-100F, CN) в течение 5 дней. Лиофилизированные порошки наночастиц растворяли и гомогенизировали в 1,429 мл деионизированной дистиллированной воды (Bioneer, KR) и использовали в эксперименте по настоящему изобретению.
3-2. Обработка клеток наночастицами SAMiRNA
Для идентификации SAMiRNA, которая ингибирует экспрессию амфирегулина, использовали линию рака легкого человека A549. Линию клеток A549 культивировали в среде Gibco™ Ham's F-12K (Kaighn's) (Thermo, US), содержащей 10% фетальной бычьей сыворотки (Hyclone, США) и 1% пенициллин-стрептомицина (Hyclone, US), при 37°С и 5% СО2. Используя ту же среду, что и выше, клеточную линию А549 высевали в 96-луночный планшет (Costar, US) при плотности 2×104 клеток/лунку. На следующий день SAMiRNA, гомогенизированную деионизированной дистиллированной водой в приведенном выше примере 3.1, разбавляли 1X DPBS, и клетки обрабатывали разведением при концентрации SAMiRNA 500 нМ или 1000 нМ. Обработку с помощью SAMiRNA выполняли в общей сложности четыре раза (один раз каждые 12 часов), и клетки культивировали при 37°С и 5% CO2.
3-3. Скрининг SAMiRNA с помощью анализа ингибирования экспрессии мРНК амфирегулина человека
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 3-2, и использовали для синтеза кДНК, а затем относительный уровень экспрессии мРНК гена амфирегулина количественно определяли с помощью ПЦР в реальном времени. Для анализа уровня экспрессии мРНК гена амфирегулина, 300 нМ прямого праймера AREG, 300 нМ обратного праймера AREG, 300 нМ зонда AREG, 300 нМ прямого праймера RPL13A, 300 нМ обратного праймера RPL13A, 300 нМ зонда RPL13A, 400 нМ прямого праймера TBP, 400 нМ обратного праймера TBP и 300 нМ зонда TBP добавляли в каждую лунку набора AccuPower® Dual-HotStart кПЦР-РВ (Bioneer, Корея) и сушили (в таблице 2 ниже показаны последовательности используемых праймеров и гидролизуемых зондов в эксперименте по высокопроизводительному скринингу (HTS)). Чтобы оценить эффективность приготовленного набора, строили калибровочную кривую с использованием тотальной РНК клеток A549 и определили эффективность ПЦР амплификации (таблица 3). кПЦР-РВ выполняли с использованием следующих условий: при 95°С в течение 5 мин, а затем 45 циклов, каждый состоящий из 95°С в течение 5 сек и 58°С в течение 15 сек. Использовали протокол, в котором значение флуоресценции определяли в каждом цикле.
96-Луночный планшет (Costar, US), обработанный SAMiRNA, подвергали экстракции тотальной РНК, и выполняли одностадийную кПЦР-РВ в соответствии с автоматизированной программой с использованием автоматизированной системы ExiStation HT™ Корея и отдельно приготовленного набора AccuPower® Dual-HotStart кПЦР-РВ kit (Bioneer, Корея), содержащего праймеры и зонды для анализа амфирегулина.
На основании значений Ct двух генов, полученных после массивной кПЦР, относительный уровень экспрессии мРНК амфирегулина в тестовой группе по сравнению с таковым в контрольной группе анализировали способом с 2(-Delta Delta C(T)) [Livak KJ, Schmittgen TD. 2001. Analysis of relative gene expression data using real-time quantitative ПЦР and the 2(-Delta Delta C(T)) Method. Methods. Dec; 25(4):4 02-8].
Для отбора высокоэффективной SAMiRNA отбирали 14 SAMiRNA, которые имели каждую из последовательностей SEQ ID NO: 1-14 в качестве смысловой цепи. При этом отобранные SAMiRNA показали самую высокую эффективность, при которой уровень экспрессии мРНК амфирегулина при конечной концентрации 500 нМ или 1000 нМ снижался по сравнению с контролем.
Как показано на фиг. 1, 14 SAMiRNA, которые наиболее эффективно ингибируют экспрессию гена амфирегулина, были окончательно отобраны из 1257 SAMiRNA, нацеленных на амфирегулин. Информация о последовательностях, отобранных SAMiRNA, показана в таблице 4 ниже.
Пример 4. Скрининг наночастиц SAMiRNA, которые нацелены на амфирегулин человека и индуцируют RNAi
Линию клеток рака легкого A549 обрабатывали SAMiRNA (выбранной в примере 3), имеющей каждую из последовательностей SEQ ID NO: 1-14 в качестве смысловой цепи, и анализировали картину экспрессии мРНК амфирегулина в клеточной линии.
4-1. Обработка клеток наночастицами SAMiRNA
Для идентификации SAMiRNA, которая ингибирует экспрессию амфирегулина, использовали линию рака легкого человека A549. Линию клеток A549 культивировали в среде Gibco™ Ham's F-12K (Kaighn's) (Thermo, US), содержащей 10% фетальной бычьей сыворотки (Hyclone, US) и 1% пенициллин-стрептомицина (Hyclone, US), при 37°С и 5% СО2. Используя такую же среду, как выше, клеточную линию А549 высевали в 12-луночный планшет (Costar, US) при плотности 8×104 клеток/лунку. На следующий день SAMiRNA, гомогенизированную деионизированной дистиллированной водой в примере 3.1 выше, разбавляли 1X DPBS, и клетки обрабатывали разведением до концентрации SAMiRNA 200 нМ или 600 нМ. Обработку SAMiRNA выполняли в общей сложности четыре раза (один раз каждые 12 часов), и клетки культивировали при 37°С и 5% CO2.
4-2. Скрининг SAMiRNA путем анализа ингибирования экспрессии мРНК амфирегулина человека
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 4-1, и использовали для синтеза кДНК, а затем анализировали относительный уровень экспрессии мРНК гена амфирегулина с помощью ПЦР в реальном времени.
4-2-1. Выделение РНК из клеток, обработанных SAMiRNA, и синтез кДНК
Используя набор для экстракции РНК (AccuPrep Cell total RNA extraction kit, BIONEER, Корея), тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 4-1 выше. Экстрагированную РНК использовали для синтеза кДНК следующим образом с использованием обратной транскриптазы РНК (набор реактивов AccuPower® RocketScript™Cycle RT Premix с праймером олиго (dT)20, Bioneer, Корея). В частности, 1 мкг экстрагированной РНК добавляли к набору реактивов AccuPower® RocketScript™Cycle RT Premix с праймером oligo (dT)20 (Bioneer, Корея) в каждую пробирку Эппендорфа объемом 0,25 мл, и дистиллированную воду, обработанную DEPC (диэтилпирокарбонатом), добавляли до общего объема 20 мкл. В системе генной амплификации (MyGenie™96 Gradient Thermal Block, BIONEER, Корея) процесс гибридизации РНК с праймерами при 37°С в течение 30 секунд и процесс синтеза кДНК при 48°С в течение 4 минут повторяли 12 раз. Затем реакцию амплификации останавливали путем деактивации фермента при 95°С в течение 5 минут.
4-2-2. Количественный анализ относительного уровня экспрессии мРНК амфирегулина человека
Используя кДНК, синтезированную в примере 4-2-1, в качестве матрицы, проводили кПЦР в реальном времени с использованием SYBR Green, и анализировали относительный уровень экспрессии мРНК амфирегулина по сравнению с контрольным образцом SAMiRNA следующим образом. кДНК, синтезированную в примере 4-2-1 выше, разбавляли в 5 раз дистиллированной водой, и для анализа уровня экспрессии мРНК амфирегулина 3 мкл разбавленной кДНК, 25 мкл AccuPower® 2X GreenStar™ кПЦР MasterMix (BIONEER, Корея), 19 мкл дистиллированной воды и 3 мкл праймеров для кПЦР амфирегулина (SEQ ID NO: 17 и 18 (таблица 5); 10 пмоль/мкл каждого праймера, BIONEER, Корея) добавляли в каждую лунку 96-луночного планшета для приготовления смеси. Между тем, GAPDH (глицеральдегид 3-фосфатдегидрогеназа), ген «домашнего хозяйства» (далее именуемый геном HK), использовали в качестве стандартного гена для нормализации уровня экспрессии мРНК амфирегулина. 96-луночный планшет, содержащий смесь, подвергали следующей реакции с использованием Exicycler™ Real-Time Quantitative Thermal Block (BIONEER, Корея). В частности, смесь оставляли для протекания реакции при 95°С в течение 15 минут для активации фермента и удаления вторичной структуры кДНК, а затем смесь подвергали 42 циклам, каждый из которых состоял из денатурации при 94°С в течение 30 секунд, отжига при 58°С в течение 30 секунд, удлинения при 72°С в течение 30 секунд, сканирования по SYBR Green и окончательного удлинения при 72°С в течение 3 минут. Далее смесь поддерживали при температуре 55°С в течение 1 минуты и анализировали кривую плавления от 55°С до 95°С.
После завершения ПЦР значение Ct (пороговый цикл) целевого гена корректировали на ген GAPDH, а затем рассчитывали значение ΔCt с использованием контроля, обработанного контрольной последовательностью SAMiRNA (SAMiCONT), которая не индуцирует ингибирование экспрессии генов. Относительный уровень экспрессии целевого гена в клетках, обработанных амфирегулин-специфической SAMiRNA, количественно определяли с использованием значения ΔCt и уравнения 2(-ΔCt)×100.
Для отбора высокоэффективных SAMiRNA отбирали три SAMiRNA, которые имели каждую из последовательностей SEQ ID NO: 10, 11 и 12 в качестве смысловой цепи. При этом отобранные SAMiРНК показали самую высокую эффективность, когда уровень экспрессии мРНК амфирегулина при конечной концентрации 200 нМ или 600 нМ снижался по сравнению с контролем.
Как показано на фиг. 3, три SAMiRNA, которые наиболее эффективно ингибируют экспрессию гена амфирегулина, были в конечном итоге отобраны из 14 SAMiRNA, нацеленных на амфирегулин. Информация о последовательностях отобранных SAMiRNA показана в таблице 6 ниже.
(F обозначает прямой праймер, и R обозначает обратный праймер)
Пример 5. Ингибирование экспрессии амфирегулина человека в клеточной линии рака легкого (A549) с помощью отобранных SAMiRNA
Линию клеток рака легкого A549 обрабатывали SAMiRNA (отобранной в примере 4), имеющей каждую из последовательностей SEQ ID NO: 10, 11 и 12 в качестве смысловой цепи, и картину экспрессии мРНК амфирегулина в клеточной линии анализировали для определения значения IC50 SAMiRNA.
5-1. Получение и анализ размера частиц наночастиц SAMiRNA
Каждую из трех SAMiRNA, нацеленных на последовательность амфирегулина, синтезированных в примере 2, растворяли в 1X фосфатно-солевом буфере Дульбекко (DPBS) (WELGENE, KR) и лиофилизировали в лиофилизаторе (LGJ-100F, CN) в течение 5 дней. Лиофилизированные порошки наночастиц растворяли и гомогенизировали в 2 мл деионизированной дистиллированной воды (Bioneer, KR) и использовали в эксперименте для настоящего изобретения. Для анализа размера частиц полученных наночастиц SAMiRNA размер и индекс полидисперсности SAMiRNA измеряли с использованием Zetasizer Nano ZS (Malvern, UK). Результаты измерения размера и индекса полидисперсности наночастиц SAMiRNA показаны в таблице 7 ниже и в графическом виде представлены на фиг. 2.
5-2. Обработка клеток наночастицами SAMiRNA
Для оценки эффекта отобранных SAMiRNA, ингибирующих экспрессию амфирегулина, использовали клеточную линию рака легкого человека A549. Линию клеток A549 культивировали в среде Gibco™ Ham's F-12K (Kaighn's) (Thermo, US), содержащей 10% фетальной бычьей сыворотки (Hyclone, US) и 1% пенициллин-стрептомицина (Hyclone, US), при 37°С и 5% СО2. Используя такую же среду, что и выше, клеточную линию А549 высевали в 12-луночный планшет (Costar, US) при плотности (Costar, США) 8×104 клеток/лунку. На следующий день SAMiRNA, гомогенизированные деионизированной дистиллированной водой, как описано в примере 5.1 выше, разбавляли 1X DPBS, и клетки обрабатывали разведением до концентрации SAMiRNA 12,5 нМ, 25 нМ, 50 нМ, 100 нМ, 200 нМ, 600 нМ. нМ или 1200 нМ. Обработку клеток SAMiRNA выполняли в общей сложности четыре раза (один раз каждые 12 часов), и клетки культивировали при 37°С и 5% СО2.
5-3. Определение IC50 SAMiRNA путем анализа ингибирования экспрессии мРНК амфирегулина человека
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 5-2, и использовали для синтеза кДНК, а затем определяли относительный уровень экспрессии мРНК гена амфирегулина с помощью ПЦР в реальном времени.
5-3-1. Выделение РНК из SAMiRNA-обработанных клеток и синтез кДНК
Используя набор для экстракции РНК (AccuPrep Cell total RNA extraction kit, BIONEER, Корея), тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 5-2 выше. Экстрагированную РНК использовали для синтеза кДНК следующим образом с использованием обратной транскриптазы РНК (набор реактивов AccuPower® RocketScript™Cycle RT Premix с праймером oligo (dT)20, Bioneer, Корея). В частности, 1 мкг экстрагированной РНК добавляли к набору реактивов AccuPower® RocketScript™Cycle RT Premix с праймером oligo (dT)20 (Bioneer, Корея) в каждую пробирку Эппендорфа объемом 0,25 мл и добавляли к ней дистиллированную воду, обработанную DEPC (диэтилпирокарбонатом), до общего объема 20 мкл. В системе генной амплификации (MyGenie™96 Gradient Thermal Block, BIONEER, Корея) процесс гибридизации РНК с праймерами при 37°С в течение 30 секунд и процесс синтеза кДНК при 48°С в течение 4 минут повторяли 12 раз. Затем реакцию амплификации останавливали путем деактивации фермента при 95°С в течение 5 минут.
5-3-2. Количественный анализ относительного уровня экспрессии мРНК амфирегулина человека
Используя кДНК, синтезированную в примере 5-3-1, в качестве матрицы, выполняли кПЦР в реальном времени с использованием SYBR Green, и анализировали относительный уровень экспрессии мРНК амфирегулина по сравнению с контрольным образцом SAMiRNA следующим образом. кДНК, синтезированную в примере 5-3-1 выше, разбавляли в 5 раз дистиллированной водой, и для анализа уровня экспрессии мРНК амфирегулина 3 мкл разбавленной кДНК, 25 мкл AccuPower® 2X GreenStar™ кПЦР MasterMix (BIONEER, Корея), 19 мкл дистиллированной воды и 3 мкл праймеров для кПЦР амфирегулина (SEQ ID NO: 17 и 18 (таблица 5); 10 пмоль/мкл для каждого праймера, BIONEER, Корея) добавляли в каждую лунку 96-луночного планшета с получением смеси. Между тем, GAPDH (глицеральдегид 3-фосфатдегидрогеназа), ген «домашнего хозяйства» (далее называемый геном HK), использовали в качестве стандартного гена для нормализации уровня экспрессии мРНК амфирегулина. 96-луночный планшет, содержащий смесь, подвергали следующей реакции с использованием Exicycler™ Real-Time Quantitative Thermal Block (BIONEER, Корея). В частности, смесь оставляли для протекания реакции при 95°С в течение 15 минут для активации фермента и удаления вторичной структуры кДНК, а затем смесь подвергали 42 циклам, каждый из которых состоял из денатурации при 94°С в течение 30 секунд, отжига при 58°С в течение 30 секунд, удлинения при 72°С в течение 30 секунд, сканирования с применением SYBR Green и окончательного удлинения при 72°С в течение 3 минут. Далее смесь поддерживали при температуре 55°С в течение 1 минуты и анализировали кривую плавления от 55°С до 95°С.
После завершения ПЦР значение Ct (пороговый цикл) целевого гена корректировали на ген GAPDH, а затем рассчитывали значение ΔCt с использованием контроля, обработанного контрольной последовательностью SAMiRNA (SAMiCONT), которая не индуцирует ингибирование экспрессии генов. Относительный уровень экспрессии целевого гена в клетках, обработанных амфирегулин-специфической SAMiRNA, количественно определяли с использованием значения ΔCt и уравнения 2(-ΔCt) x 100.
В результате было подтверждено, что все амфирегулин-специфические SAMiRNA, имеющие каждую из последовательностей SEQ ID NO: 10, 11 и 12 в качестве смысловой цепи, показали снижение уровня экспрессии мРНК амфирегулина на 50% или более даже при низкой концентрации 100 нМ, что свидетельствует о том, что амфирегулин-специфические SAMiRNA проявляют эффект ингибирования экспрессии амфирегулина с высокой эффективностью. Было подтверждено, что значения IC50 составили 28,75 нМ, как показано на фиг. 4, для амфирегулин-специфической SAMiRNA, имеющей последовательность SEQ ID NO: 10 в качестве смысловой цепи, 26,04 нМ, как показано на фиг. 5, для амфирегулин-специфической SAMiRNA, имеющей последовательность SEQ ID NO: 11 в качестве смысловой цепи, и 12,07 нМ, как показано на фиг. 6, для амфирегулин-специфической SAMiRNA, имеющей последовательность SEQ ID NO: 12 в качестве смысловой цепи. В частности, было подтверждено, что амфирегулин-специфическая SAMiRNA, имеющая последовательность SEQ ID NO: 12 в качестве смысловой цепи, показала снижение уровня экспрессии мРНК амфирегулина на 50% или более даже при низкой концентрации 25 нМ, как показано на фиг. 6, на основании чего можно предположить, что она проявляла эффект наиболее эффективного ингибирования экспрессии гена амфирегулина среди трех выбранных последовательностей.
Пример 6. Оценка цитотоксичности in vitro с использованием мононуклеарных клеток периферической крови человека (РВМС)
Чтобы изучить, повышаются ли уровни экспрессии мРНК цитокинов, связанных с врожденным иммунитетом, под действием SAMi-hAREG, криоконсервированные РВМС человека ePBMC® (монокулярные периферические клетки человека, Cellular Technology Limited, США) высевали с плотностью 5 x 105 клеток на лунку в 12-луночном планшете (Costar® США) со средой RPMI1640 (Hyclone™), содержащей 10% FBS (фетальная бычья сыворотка; Hyclone™). Клетки культивировали в инкубаторе с 5% CO2 при 37°С в течение 1 часа для стабилизации, а затем высеянные РВМС обрабатывали 2,5 мкМ каждой из SAMiCON (DNA/RNA), SAMi-hAREG#10 (DNA/RNA), SAMi-hAREG#11 (DNA/RNA), SAMi-hAREG#12 (DNA/RNA), SAMiCON (RNA/RNA), SAMi-hAREG#10 (RNA/RNA), SAMi-hAREG#11 (RNA/RNA) и SAMi-hAREG#12 (RNA/RNA), и культивировали в инкубаторе с 5% CO2 при 37°С в течение 6 часов. В качестве положительного контроля использовали 20 мкг/мл конканавалина А (Sigma Aldrich, США).
После этого все клетки собирали и из них экстрагировали тотальную РНК с использованием набора RNeasy Mini Kit (Qiagen, Германия) и набора RNase-Free DNase Set (Qiagen, Германия) в соответствии с протоколами производителя.
200 нг экстрагированной РНК смешивали с деионизированным стерильным DW (Bioneer, Корея) и обратной транскриптазой РНК (набор реактивов AccuPower® RocketScript™Cycle RT Premix с праймером oligo (dT)20, Bioneer, Корея), и смесь оставляли для протекания реакции с использованием системы амплификации генов (MyGenie™96 Gradient Thermal Block, BIONEER, Корея) в условиях 12 циклов, каждый из которых состоял из 37°С в течение 30 секунд, 48°С в течение 4 минут и 55°С в течение 30 секунд и затем 95°С в течение 5 мин, таким образом, синтезируя всего 20 мкл кДНК.
Синтезированную кДНК смешивали с праймерами кПЦР для каждого из генов RPL13A, IL1B, IL6, IFNG, TNF и IL12B, а затем амплифицировали с использованием Exicycler™96 Real-Time Quantitative Thermal Block (Bioneer, Корея) в следующих условиях: 95°С в течение 5 мин и затем 45 циклов, каждый из которых состоит из 95°С в течение 5 сек и 58°С в течение 15 сек.
На основании значений Ct двух генов, полученных после массивной кПЦР, относительный уровень экспрессии мРНК (%) в тестовой группе по сравнению с таковым в контрольной группе анализировали способом с 2(-Delta Delta C(T)) Method [Livak KJ, Schmittgen TD. 2001. Analysis of relative gene expression data using real-time quantitative ПЦР and the 2(-Delta Delta C(T)) Method. Methods. Dec; 25(4):4 02-8].
В результате, как показано на фиг. 7, было подтверждено, что экспрессия цитокинов, связанных с врожденным иммунитетом, в мононуклеарных клетках периферической крови человека (РВМС человека), вызванная каждой из амфирегулин-специфических SAMiRNA #10, SAMiRNA #11 и SAMiRNA #12, не наблюдалась.
Пример 7. Сравнительный анализ ингибирования экспрессии амфирегулина человека SAMiRNA, содержащими гибрид ДНК/РНК и гибрид РНК/РНК, содержащими каждую из выбранных последовательностей SEQ ID NO: 10, 11 и 12 в качестве смысловой цепи
Линию клеток рака легкого A549 обрабатывали каждой из двухцепочечных содержащих гибрид ДНК/РНК и гибрид РНК/РНК, амфирегулин-специфических SAMiRNA (отобранных в примере 4), имеющих каждую из последовательностей SEQ ID NO: 10, 11 и 12 в качестве смысловой цепи, и проводили сравнительный анализ относительных уровней экспрессии мРНК (%) амфирегулина в клеточной линии.
7-1. Обработка клеток наночастицами SAMiRNA
Для идентификации SAMiRNA, которая ингибирует экспрессию амфирегулина, использовали линию рака легкого человека A549. Линию клеток A549 культивировали в среде Gibco™ Ham's F-12K (Kaighn's) (Thermo, US), содержащей 10% фетальной бычьей сыворотки (Hyclone, US) и 1% пенициллин-стрептомицина (Hyclone, US), при 37°С и 5% СО2. Используя такую же среду, что и выше, клеточную линию A549 высевали в 12-луночный планшет (Costar, US) при плотности 8×104 клеток/лунку. На следующий день SAMiRNA, гомогенизированную деионизированной дистиллированной водой в примере 3.1 выше, разбавляли 1X DPBS, и клетки обрабатывали разведением до концентрации SAMiRNA 200 нМ, 600 нМ или 1200 нМ. Обработку клеток SAMiRNA выполняли в общей сложности четыре раза (один раз каждые 12 часов), и клетки культивировали при 37°С и 5% СО2.
7-2. Скрининг SAMiRNA путем анализа ингибирования экспрессии мРНК амфирегулина человека
Тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 7-1, и использовали для синтеза кДНК, а затем определяли относительный уровень экспрессии мРНК гена амфирегулина с помощью ПЦР в реальном времени.
7-2-1. Выделение РНК из клеток, обработанных SAMiRNA, и синтез кДНК
Используя набор для экстракции РНК (AccuPrep Cell total RNA extraction kit, BIONEER, Корея) тотальную РНК экстрагировали из клеточной линии, обработанной SAMiRNA в примере 7-1 выше. Экстрагированную РНК использовали для синтеза кДНК следующим образом с использованием обратной транскриптазы РНК (набор реактивов AccuPower® RocketScript™Cycle RT Premix с праймером oligo (dT)20, Bioneer, Корея). В частности, 1 мкг экстрагированной РНК добавляли к набору реактивов AccuPower® RocketScript™Cycle RT Premix с праймером oligo (dT)20 (Bioneer, Корея) в каждую пробирку Эппендорфа объемом 0,25 мкл, и добавляли к ней дистиллированную воду, обработанную DEPC (диэтилпирокарбонатом), до общего объема 20 мкл. В системе амплификации генов (MyGenie™96 Gradient Thermal Block, BIONEER, Корея) процесс гибридизации РНК с праймерами при 37°С в течение 30 секунд и процесс синтеза кДНК при 48°С в течение 4 минут повторяли 12 раз. Затем реакцию амплификации останавливали путем деактивации фермента при 95°С в течение 5 минут.
7-2-2. Количественный анализ относительного уровня экспрессии мРНК амфирегулина человека
Используя кДНК, синтезированную в примере 7-2-1, в качестве матрицы, проводили количественную кПЦР в реальном времени с использованием SYBR Green и анализировали относительный уровень экспрессии мРНК амфирегулина по сравнению с контрольным образцом SAMiRNA следующим образом. кДНК, синтезированную в примере 7-2-1 выше, разбавляли в 5 раз дистиллированной водой и для анализа уровня экспрессии мРНК амфирегулина в каждую лунку 96-луночного планшета для приготовления смеси добавляли 3 мкл разбавленной кДНК, 25 мкл AccuPower® 2X GreenStar™ кПЦР MasterMix (BIONEER, Корея), 19 мкл дистиллированной воды и 3 мкл праймеров для кПЦР амфирегулина (SEQ ID NO: 17 и 18 (таблица 5); 10 пмоль/мл каждого праймера, BIONEER, Корея). Между тем, GAPDH (глицеральдегид 3-фосфатдегидрогеназа), ген «домашнего хозяйства» (далее именуемый геном HK), использовали в качестве стандартного гена для нормализации уровня экспрессии мРНК амфирегулина. 96-луночный планшет, содержащий смесь, подвергали следующей реакции с использованием Exicycler™ Real-Time Quantitative Thermal Block (BIONEER, Корея). В частности, смесь оставляли для протекания реакции при 95°С в течение 15 минут для активации фермента и удаления вторичной структуры кДНК, а затем смесь подвергали 42 циклам, каждый из которых состоял из денатурации при 94°С в течение 30 секунд, отжига при 58°С в течение 30 секунд, удлинения при 72°С в течение 30 секунд, сканирования с использованием SYBR Green и окончательного удлинения при 72°С в течение 3 минут. Далее смесь поддерживали при температуре 55°С в течение 1 минуты и анализировали кривую плавления от 55°С до 95°С.
После завершения ПЦР значение Ct (пороговый цикл) гена-мишени корректировали по гену GAPDH, а затем рассчитывали значение ΔCt с использованием контроля, обработанного контрольной последовательностью SAMiRNA (SAMiCONT), которая не индуцирует ингибирование экспрессии генов. Относительный уровень экспрессии целевого гена количественно определяли с использованием значения ΔCt и уравнения 2(-ΔCt)×100.
Для отбора высокоэффективной SAMiRNA из двухцепочечного гибрида ДНК/РНК и гибридов РНК/РНК, в конечном итоге была отобрана SAMiRNA, содержащая гибрид ДНК/РНК, имеющая последовательность SEQ ID NO: 12 в качестве смысловой цепи. При этом отобранная последовательность SAMiRNA, содержащей гибрид ДНК/РНК (ингибирование экспрессии гена на 90% и более), показала самую высокую эффективность, при которой уровень экспрессии мРНК амфирегулина при конечной концентрации 200 нМ, 600 нМ или 1200 нМ снижался по сравнению с контролем.
Как показано на фиг. 8, SAMiRNA 12, содержащая гибрид ДНК/РНК, которая наиболее эффективно ингибирует экспрессию гена амфирегулина, была в конечном итого отобрана из гибридов ДНК-РНК и РНК-РНК, содержащих три отобранные амфирегулин-специфические SAMiRNA, соответственно.
Пример 8. Высокопроизводительный скрининг (HTS) наночастиц SAMiRNA, нацеленных на мышиный амфирегулин и индуцирующих RNAi
В случае терапевтических агентов siRNA трудно идентифицировать оптимальную последовательность, применимую к различным штаммам. В этом случае применяются рекомендации Управления по контролю за качеством пищевых продуктов и медикаментов (FDA US), в соответствии с которыми последовательность ДНК (суррогатная последовательность; специфическая для мышиного гена siRNA), специфическая для животной модели для анализа терапевтических эффектов (тест на эффективность in vivo), разрабатывается таким образом, чтобы подтвердить фармакологическую активность в результате ингибирования экспрессии интересующего гена и токсичность в результате ингибирования экспрессии интересующего гена (презентация Robert T. Dorsam Ph.D. Pharmacology/Toxicology Reviewer, FDA/CDER).
Ранее разработанный скрининг модифицировали с помощью программы siRNA на основе существующего алгоритма (Turbo-si-designer, принадлежащей компании заявителя), и выполняли высокопроизводительный скрининг последовательностей siRNA на основе SAMiRNA. Выполняли сканирование со скользящим окном из 1 основания (такой же способ, как описанный выше целевой скрининг амфирегулина человека) 19-mer siRNA против всего целевого гена, и генерировали в общей сложности 1190 кандидатных последовательностей siRNA против возможной полной последовательности транскрипта мышиного гена амфирегулина (NM_009704.4). Была проведена фильтрация бластных последовательностей по гомологии для удаления ненужных последовательностей-кандидатов, которые влияют на экспрессию других генов, и было синтезировано 237 в итоге отобранных SAMiRNA. Мышиную линию клеток NIH3T3 обрабатывали каждой отобранной SAMiRNA при концентрации 1 мкМ в среде для культивирования клеток, содержащей 10% FBS, и эффекты SAMiRNA по ингибированию экспрессии in vitro, сначала подвергали скринингу с использованием праймеров, показанных в таблице 8 (информации о последовательностях праймеров для кПЦР) (фиг. 9).
После этого мышиную клеточную линию фибробластов легкого MLg обрабатывали каждой из двух последовательностей (SEQ ID NO: 19 и 20), отобранных на клеточной линии NIH3T3, и мышиным SAMiRNA-амфирегулином с последовательностью SEQ ID NO: 21, обнаруженной в ходе предыдущих промежуточных исследований, в лечебных концентрациях 200 нМ и 500 нМ в среде для культивирования клеток, содержащей 10% FBS, и выполняли дополнительный скрининг. В результате было подтверждено, что SEQ ID NO: 20 проявляет наилучший эффект ингибирования экспрессии (фиг. 10а).
Кроме того, мышиную линию эпителиальных клеток легкого LA-4 (ATCC® CCL-196™, Manassas, VA, США) обрабатывали каждой из двух выбранных последовательностей (SEQ ID NO: 19 и 20), и мышиным SAMiRNA-амфирегулином с последовательностью SEQ ID NO: 21, обнаруженной в ходе предыдущих промежуточных исследований, в лечебных концентрациях 200 нМ, 500 нМ и 1000 нМ в среде для культивирования клеток, содержащей 10% FBS, и дополнительно оценивали эффекты ингибирования экспрессии. В результате было снова подтверждено, что SEQ ID NO: 20 проявляет наилучший эффект ингибирования экспрессии (фиг. 10b).
Как показано на фиг. 10, две SAMiRNA, которые наиболее эффективно ингибируют экспрессию гена амфирегулина, в конечном итоге были отобраны из 237 SAMiRNA, нацеленных на мышиный амфирегулин, и ниже в таблице 9 показана информация о последовательностях отобранных SAMiRNA.
(F обозначает прямой праймер, и R обозначает обратный праймер)
9-1. Способ тестирования на животных
Были приобретены 5-недельные мыши BKS.Cg-m+/+ Leprdb/(KRIBB; Корейский институт бионауки и биотехнологии) и проведены эксперименты с использованием этих мышей. Приобретенных диабетических мышей с ожирением (мыши db/db), акклиматизировали в течение 3 недель, а затем в течение 8 недель кормили кормом для грызунов (2918C, Harlan, США), и эксперименты проводили с использованием мышей в следующих условиях. Для сравнения, 5-недельных нормальных мышей без ожирения (мыши C57BL/6) приобретали у Nara Biotech Co., Ltd. (Корея) и эксперименты проводили с использованием этих мышей. Этих мышей также акклиматизировали в течение 3 недель и кормили кормом для грызунов. Каждая из групп мышей, используемых в экспериментах, состояла из 6 животных.
100 мкл PBS (C-9011, Bioneer, Корея) вводили нормальной контрольной группе, а диабетических мышей с ожирением разделяли на три группы, которым вводили 100 мкл PBS, 100 мкл SAMiRNA-Cont (5 мг/кг) и 100 мкл SAMiRNA-AREG (5 мг/кг), соответственно, путем подкожной инъекции три раза в неделю. Во время эксперимента мышей содержали в постоянной окружающей среде при температуре 21 ± 2°C, влажности 55 ± 5%, 15-17/час, освещенности 150-300 люкс и цикле 12 часов свет/12 часов темнота (включение: 06:00, выключение: 18:00). После 8 недель введения лекарственного средства мышей не кормили в течение 16 часов и умерщвляли.
9-2. Измерение массы тела, потребления пищи и воды
Массу тела, потребление пищи и воды измеряли в заданные моменты времени два раза в неделю.
9-2-1. Изменения массы тела
Массу тела (г) каждой мыши измеряли в заданный момент времени два раза в неделю. Масса тела в нормальной контрольной группе имела тенденцию к постепенному увеличению с течением времени и составила 32,5±1,64 г на момент умерщвления мышей. Три диабетические группы с ожирением показали среднюю массу тела 28,9±2,35 г (введение PBS), 27,4±3,93 г (введение SAMiRNA-Cont) и 29,7±4,12 г (введение SAMiRNA-AREG), соответственно (фиг. 11).
В результате наблюдения массы тела на 8-й неделе не было статистически значимого различия в массе тела между группами, но все группы диабетических мышей с ожирением показали небольшую потерю массы тела по сравнению с нормальными контрольными мышами, и не было статистически значимого различия в массе тела между группами диабетических мышей с ожирением и группой с ожирением и диабетом.
9-2-2. Изменения в потреблении пищи и воды
В результате измерения потребления пищи мышами было подтверждено, что среднесуточное потребление пищи составило около 4 г в нормальной контрольной группе и около 8 г во всех диабетических группах с ожирением, что указывает на то, что потребление пищи увеличилось более чем в два раза у диабетических мышей с ожирением (фиг. 12). Кроме того, потребление воды составило около 5 мл/день у нормальных контрольных мышей, но 20-35 мл/день у диабетических мышей с ожирением, что является значительно более высоким (фиг. 13).
9-3. Изменения массы жира
Для измерения массы жира из умерщвленных мышей извлекали подкожный и висцеральный жир, измеряли их массу и оценивали отношение массы жира к массе мыши.
Отношение для подкожного жира составило 1,56 ± 0,36 у нормальных контрольных мышей, 4,32 ± 0,73 у диабетических мышей с ожирением, получавших PBS, 3,63 ± 1,80 у диабетических мышей с ожирением, получавших SAMiRNA-Cont, и 3,15 ± 0,58 у диабетических мышей с ожирением, получавших SAMiRNA-AREG. Таким образом, можно подтвердить, что у диабетических мышей с ожирением масса подкожного жира была значительно снижена за счет снижения уровня экспрессии амфирегулина в соответствии с настоящим изобретением (фиг. 14).
Отношение для висцерального жира составило 1,28±0,31 у нормальных контрольных мышей, 1,97±0,25 у диабетических мышей с ожирением, получавших PBS, 1,59±0,38 у диабетических мышей с ожирением, получавших SAMiRNA-Cont, и 0,76±0,12 у диабетических мышей с ожирением, получавших SAMiRNA-AREG. Таким образом, можно подтвердить, что у диабетических мышей с ожирением масса висцерального жира была значительно снижена за счет снижения уровня экспрессии амфирегулина в соответствии с настоящим изобретением (фиг. 15 и 16).
9-4. Измерение уровня глюкозы в крови натощак и измерение уровня глюкозы в сыворотке
Уровни глюкозы в крови натощак (мг/дл) измеряли с помощью простого глюкометра (Accu-ChekTM Active, Roche, Германия) за неделю до умерщвления мышей, и уровни глюкозы в сыворотке измеряли KP&T Co., Ltd.
Уровни глюкозы в крови составили 153,2±12,07 у нормальных контрольных мышей, 551,8±53,73 в среднем у диабетических мышей с ожирением, получавших PBS, в среднем 577,3±40,25 у диабетических мышей с ожирением, получавших SAMiRNA-Cont, и 555,7± 49,15 в среднем в диабетической группе с ожирением, получавшей SAMiRNA-AREG (фиг. 17).
Уровни глюкозы в сыворотке крови (мг/дл) составили 149,6±20,4 у нормальных контрольных мышей, 689,1±185,4 в среднем у диабетических мышей с ожирением, получавших PBS, 755,5±89,4 в диабетической группе с ожирением, получавшей SAMiRNA-Cont, и 874,3 ± 119,4 в среднем в диабетической группе с ожирением, получавшей SAMiRNA-AREG (фиг. 18).
Таким образом, было подтверждено, что снижение уровня экспрессии амфирегулина у диабетических мышей с ожирением в соответствии с настоящим изобретением не имело значительного эффекта на контроль уровней глюкозы в крови натощак или уровней глюкозы в сыворотке в животных моделях диабета.
Пример 10. Оценка эффекта против ожирения с использованием модели ожирения, вызванного диетой с высоким содержанием жиров
Для оценки эффекта ингибитора экспрессии амфирегулина против ожирения, ингибитор экспрессии амфирегулина SAMiRNA-AREG (SAMi-mAREG#20) вводили модели ожирения, индуцированного диетой с высоким содержанием жиров, и наблюдали его эффект в отношении уменьшения жира. После введения диеты с высоким содержанием жиров лекарственное средство вводили 3 раза в неделю в течение 5 недель, а затем анализировали различные показатели.
10-1. Анализ уровня экспрессии амфирегулина после введения диеты с высоким содержанием жиров
Приобретали 5-недельных мышей C57BL/6 (Nara Biotech Co., Ltd.), и эксперименты проводили с использованием этих мышей. Приобретенных мышей акклиматизировали в течение 1 недели, а затем кормили кормом с содержанием жира 60% ккал (D12492, Research Diets, Inc.) в течение 6 недель. Затем экстрагировали эпидидимальный жир и измеряли в нем уровни мРНК.
Экстракцию тотальной РНК из жировой ткани проводили с использованием комбинации реагента для лизиса QIAzol (QIAZEN., GER) и набора RNeasy Mini Kit (QIAZEN., GER). 100 мг жировой ткани добавляли к 1 мл реагента для лизиса QIAzol, гомогенизировали и затем инкубировали в течение 5 минут при комнатной температуре. После центрифугирования при 12000g при 4°С в течение 10 минут собирали нижний образец, исключая верхний монослой жира. К образцу добавляли 200 мкл хлороформа (Sigma-Aldrich, США), хорошо перемешивали, и выдерживали при комнатной температуре в течение 3 минут с последующим центрифугированием при 12 000 g при 4°С в течение 30 минут. Из трех разделенных фаз собирали самый верхний слой, добавляли к нему 70% EtOH и хорошо перемешивали в соотношении лизат:70% EtOH = 1:1, а затем загружали в спин-колонку RNeasy из набора RNeasy Mini Kit. Последующий процесс проводили в соответствии с протоколом производителя. Экстрагированную РНК количественно определяли с помощью спектрофотометра и оценивали ее чистоту.
(SEQ ID NO: 53)
(F обозначает прямой праймер, и R обозначает обратный праймер)
В результате было подтверждено, что уровень экспрессии амфирегулина увеличился в 12 раз по сравнению с нормальной контрольной группой после введения диеты с высоким содержанием жиров (фиг. 19).
10-2. Способ тестирования на животных
Приобретали мышей C57BL/6 в возрасте 5 недель (Nara Biotech Co., Ltd.), и эксперименты проводили с использованием этих мышей. Приобретенных мышей акклиматизировали в течение 1 недели, а затем в течение 1 недели кормили кормом с содержанием жира 60% ккал (D12492, Research Diets, Inc.), а затем проводили эксперименты с использованием этих мышей в следующих условиях. Для сравнения, нормальных мышей без ожирения кормили кормом для грызунов (2918C, Harlan, США) в тех же условиях, и эксперименты проводили с использованием мышей в следующих условиях. Для проведения экспериментов мышей разделяли на нормальную контрольную группу (НД+PBS) и группу, которой вводили тестируемое вещество (диета с высоким содержанием жиров+SAMi-AREG), при этом каждая группа состояла из 6 животных, и группу отрицательного контроля (диета с высоким содержанием жиров+PBS), состоящую из 5 животных.
100 мкл PBS (LB 001-02, WELGENE, Корея) вводили нормальной контрольной группе (НД+PBS) и группе отрицательного контроля (диета с высоким содержанием жиров+PBS), и 100 мкл SAMiRNA-AREG (5 мг/кг) вводили группе, получавшей тестируемое вещество (диета с высоким содержанием жиров+SAMi-AREG), путем подкожной инъекции три раза в неделю.
В течение периода эксперимента мышей содержали в постоянной окружающей среде при температуре 21 ± 2°C, влажности 55 ± 5%, 15-17/час, освещенности 150-300 люкс и цикле 12 часов свет/12 часов темнота (включение: 06:00, выключение: 18:00). После 8 недель введения лекарственного средства мышей не кормили в течение 16 часов и умерщвляли.
10-3. Измерение массы тела, потребления пищи и воды
Массу тела, потребление пищи и воды измеряли в заданные моменты времени два раза в неделю.
10-3-1. Изменения массы тела
Массу тела (г) каждой мыши измеряли в заданный момент времени два раза в неделю. Масса тела в группе отрицательного контроля имела тенденцию к увеличению из-за диеты с высоким содержанием жиров с течением времени после введения PBS и составила 37,3 ± 1,20 г на момент умерщвления мышей. Масса тела (г) составила в среднем 26,57 ± 0,36 в нормальной контрольной группе, получавшей PBS, и в среднем 33,21 ± 1,16 в группе, получавшей SAMiRNA-AREG. В результате наблюдения массы тела на 4-й и 5-й неделе, наблюдалось статистически значимое различие в массе тела между группой, получавшей тестируемое вещество, и группой отрицательного контроля.
По сравнению с массой тела нормальных контрольных мышей, масса тела мышей в группе отрицательного контроля, получавшей диету с высоким содержанием жиров, значительно увеличилась, при этом масса тела мышей в группе, получавшей тестируемое вещество, снизилась, что было статистически значимым (фиг. 20).
10-3-2. Изменения в потреблении пищи и воды
В результате измерения потребления пищи мышами было подтверждено, что среднесуточное потребление пищи составило 3,69±0,15 г в нормальной контрольной группе, 2,76±0,06 г в группе отрицательного контроля и 2,55±0,08 г в группе, получавшей тестируемое вещество, что указывает на то, что потребление пищи в группе, получавшей диету с высоким содержанием жиров, было меньше, чем в группе отрицательного контроля, и не было существенного различия в потреблении пищи между группой отрицательного контроля и группой, получавшей тестируемое вещество (фиг. 21а).
В результате измерения потребления воды мышами (мл) было подтверждено, что среднесуточное потребление воды составило 3,27±0,10 в нормальной контрольной группе, 4,00±0,12 в группе отрицательного контроля и 4,22±0,24 в группе, получавшей тестируемое вещество, что указывает на то, что потребление воды в группе, получавшей диету с высоким содержанием жиров, было больше, чем в группе отрицательного контроля, и не было существенного различия в потреблении воды между группой отрицательного контроля и группой, получавшей тестируемое вещество (фиг. 21b).
10-4. Коэффициент пищевой эффективности (%)
В результате измерения коэффициента пищевой эффективности путем деления прироста массы (г/день) каждой мыши на потребление пищи (г/день) было подтверждено, что коэффициент пищевой эффективности составил 0,02 ± 0,001 в нормальной контрольной группе, 0,12 ± 0,007 в группе отрицательного контроля и 0,08 ± 0,011 в группе, получавшей тестируемое вещество, что указывает на то, что, хотя коэффициент пищевой эффективности как в группе отрицательного контроля, так и в группе, получавшей тестируемое вещество, увеличился по сравнению с нормальной контрольной группой, коэффициент пищевой эффективности в группе, получавшей тестируемое вещество, был значительно ниже, чем в группе отрицательного контроля (фиг. 22).
10-5. Изменения массы жира
Для измерения массы жира у умерщвленных мышей извлекали подкожное жировое тело, эпидидимальное жировое тело, околопочечное жировое тело и брыжеечное жировое тело, измеряли их массу и определяли отношение массы жира к массе мыши.
Масса подкожного жирового тела мыши (г) составила 0,38 ± 0,02 в нормальной контрольной группе, 1,74 ± 0,12 в группе отрицательного контроля и 1,05 ± 0,14 в группе, получавшей тестируемое вещество, и масса эпидидимального жирового тела (г) составила 0,52±0,03 в нормальной контрольной группе, 2,32±0,09 в группе отрицательного контроля и 1,79±0,16 в группе, получавшей тестируемое вещество. Кроме того, масса паранефрального жирового тела (г) составила 0,20±0,02 в нормальной контрольной группе, 0,86±0,04 в группе отрицательного контроля и 0,67±0,08 в группе, получавшей тестируемое вещество, и масса мезентериального жирового тела (г) составила 0,25±0,01 в нормальной контрольной группе, 0,66±0,09 в группе отрицательного контроля и 0,45±0,04 в группе, получавшей тестируемое вещество (фиг. 23а).
Отношение (%) подкожного жирового тела мыши составило 1,39±0,08 в нормальной контрольной группе, 4,65±0,23 в группе отрицательного контроля и 3,11±0,35 в группе, получавшей тестируемое вещество, и отношение (%) массы эпидидимального жирового тела составило 1,91±0,10 в нормальной контрольной группе, 6,23±0,09 в группе отрицательного контроля и 5,36±0,29 в группе, получавшей тестируемое вещество. Кроме того, отношение (%) массы околопочечного жирового тела составило 0,73±0,06 в нормальной контрольной группе, 2,33±0,13 в группе отрицательного контроля и 2,01±0,17 в группе, получавшей тестируемое вещество, и отношение (%) массы брыжеечного жирового тела составило 0,91±0,02 в нормальной контрольной группе, 1,76±0,19 в группе отрицательного контроля и 1,35±0,07 в группе, получавшей тестируемое вещество (фиг. 23b).
Мышиный жир разделяли на подкожный жир и висцеральный жир (эпидидимальный жир, околопочечный жир и брыжеечный жир), и измеряли массу (г) и массовую долю (%).
Для мышиного подкожного жира масса составила 0,38±0,02 в нормальной контрольной группе, 1,74±0,12 в группе отрицательного контроля и 1,05±0,14 в группе, получавшей тестируемое вещество, и массовая доля составила 1,39±0,08 в нормальной контрольной группе, 4,65±0,23 в группе отрицательного контроля и 3,11±0,35 в группе, получавшей тестируемое вещество.
Для висцерального жира масса составила 0,97±0,06 в нормальной контрольной группе, 3,85±0,18 в группе отрицательного контроля и 2,92±0,27 в группе, получавшей тестируемое вещество, и массовая доля составила 3,56±0,17 в нормальной контрольной группе, 10,34±0,16 в нормальной контрольной группе и 8,73±0,50 в группе, получавшей тестируемое вещество.
В результате было подтверждено, что масса и массовая доля подкожного жира, и масса и массовая доля висцерального жира значительно увеличились в группе отрицательного контроля по сравнению с нормальной контрольной группой, и это увеличение массы и массовой доли в группе отрицательного контроля значительно уменьшилось в группе, получавшей тестируемое вещество (фиг. 24a и 24b).
10-6. Анализ микро-КТ
Для микро-КТ-анализа мышиного жира (Корейский институт фундаментальных наук, Центр в Кванджу) из каждой группы отбирали двух животных со средней массой тела. Отобранных мышей фотографировали и на график наносили объемы подкожного жира и висцерального жира.
Объем (мм3) подкожного жира составил 1661±289,5 в нормальной контрольной группе, 6356±217 в группе отрицательного контроля и 4040±284,5 в группе, получавшей тестируемое вещество, и объем (мм3) висцерального жир составил 1069±90 в нормальной контрольной группе, 3782±7 в группе отрицательного контроля и 2623±166 в группе, получавшей тестируемое вещество.
В результате смогли подтвердить, что объемы подкожного жира и висцерального жира увеличились в группе отрицательного контроля по сравнению с нормальной контрольной группой и уменьшились в группе, получавшей тестируемое вещество, по сравнению с группой отрицательного контроля (фиг. 25).
10-7. Гистопатологическое исследование жировой ткани
Подкожное жировое тело, эпидидимальное жировое тело, околопочечное жировое тело и мезентериальное жировое тело извлекали из мышей, фиксировали в 10% нейтральном забуференном формалине (Sigma, HT50-1-640) в течение 24 часов или более, обезвоживали этанолом, а затем очищали ксилолом три раза. Затем образцы тканей пропитывали и заливали жидким парафином, готовя таким образом парафиновые блоки. Затем срезы ткани толщиной 5 мкм депарафинизировали и регидратировали, а ядра окрашивали раствором гематоксилина Харриса в течение 5 мин с последующим контрастным окрашиванием раствором эозина. После окрашивания заливочную среду накапывали на срезы ткани, которые затем покрывали покровным стеклом и давали затвердеть. Срезы ткани, отвержденные с помощью раствора для консервации, фотографировали при 200-кратном увеличении с использованием инвертированного микроскопа (Nikon Eclipse TS2) и рассчитывали площадь адипоцитов.
Для подкожного жирового тела площадь адипоцитов (мм2) составила 913,8 ± 129,9 в нормальной контрольной группе, 3575,0 ± 346,7 в группе отрицательного контроля и 1337,0 ± 211,1 в группе, получавшей тестируемое вещество, а для эпидидимального жирового тела адипоциты (мм2) составили 950,6±73,2 в нормальной контрольной группе, 1598,0±99,6 в группе отрицательного контроля и 1347,0±100,1 в группе, получавшей тестируемое вещество. Для околопочечного жирового тела площадь адипоцитов (мм2) составила 1734,0±158,8 в нормальной контрольной группе, 5365,0±190,4 в группе отрицательного контроля и 2516,0±288,3 в группе, получавшей тестируемое вещество, и для брыжеечного жирового тела площадь адипоцитов (мм2) составила 1552,0±680,3 в нормальной контрольной группе, 3495,0±425,3 в группе отрицательного контроля и 1436,0±163,3 в группе, получавшей тестируемое вещество.
В результате смогли подтвердить, что площадь адипоцитов увеличилась в группе отрицательного контроля по сравнению с нормальной контрольной группой, и уменьшилась в группе, получавшей тестируемое вещество, по сравнению с группой отрицательного контроля (фиг. 26).
10-8. Гистопатологическое исследование ткани печени
У мышей извлекали печень, фиксировали в 10% нейтральном забуференном формалине (Sigma, HT50-1-640) в течение более 24 часов и подвергали окрашиванию H&E и анализу на Oil red O с последующим исследованием.
10-8-1. Окрашивание H&E
Окрашивание H&E (гематоксилином и эозином) проводили для изучения общей морфологии ткани печени, полученной после фиксации в нейтральном забуференном формалине, и степени накопления липидов в ткани печени. Образцы тканей готовили инфильтрацией парафином. После обезвоживания этанолом образцы тканей трижды очищали ксилолом. Блоки ткани разрезали на срезы толщиной 5 мкм с помощью микротома, срезы высушивали в сушильном шкафу для предметных стекол в течение 1 часа, депарафинизировали ксилолом, обрабатывали этанолом и затем гидратировали. Ядра сначала окрашивали красящим раствором гематоксилина Харриса в течение 5 минут, а затем контрастно окрашивали эозином. После окрашивания заливочную среду накапывали на срезы ткани, которые затем покрывали покровным стеклом и давали затвердетьц. Срезы ткани, отвержденные раствором консерванта, исследовали под микроскопом.
10-8-2. Окрашивание Oil Red O
Ткани печени, полученные после фиксации в нейтральном забуференном формалине, инфильтрировали в 30% растворе сахарозы. После промывания раствором PBS ткани обезвоживали и фиксировали в соединении с оптимальной температурой резания (O.C.T) (SAKURA, США), агенте для заливки замороженных тканей, для получения блоков замороженных тканей. Фиксированные ткани разрезали на срезы толщиной 14 мкм с использованием Cryostat CM3050 S (Leica) с получением образцов тканей. Ингибирующее действие AREG в отношении накопления липидов оценивали с использованием окрашивания Oil Red O, специального способа окрашивания, который может определять степень накопления липидов путем специфической и чувствительной реакции с липидным компонентом и проявления красного цвета. После фиксации в 10% нейтральном забуференном формалине (Sigma, HT50-1-640) фиксатор удаляли, образцы промывали 100% пропиленгликолем и окрашивали раствором Oil red O, который специфически реагирует с внутриклеточными липидными каплями. После окрашивания заливочную среду накапывали на срезы ткани, которые затем закрывали покровным стеклом и давали затвердеть. Срезы ткани, отвержденные раствором консерванта, исследовали под микроскопом.
10-8-3. Изменения жира в печени
В результате выполнения количественного анализа после анализа Oil Red O было подтверждено, что адипогенез увеличился в 6,6 раз в группе отрицательного контроля по сравнению с нормальной контрольной группой, и увеличился в 2,8 раза в группе, получавшей тестируемое вещество, по сравнению с нормальной контрольной группой. Таким образом, можно видеть, что адипогенез был ингибирован в группе, получавшей тестируемое вещество (фиг. 27).
10-9. Анализ экспрессии генов
У мышей измеряли уровни экспрессии амфирегулина в подкожном жировом теле, эпидидимальном жировом теле и периферическом жировом теле. Экстракцию тотальной РНК из жировой ткани проводили с использованием комбинации реагента TRI Reagent (MRC Inc., США) и универсального набора для экстракции РНК (BIONEER, Корея). 100 мг жировой ткани добавляли к 1 мл TRI Reagent, гомогенизировали и затем инкубировали в течение 5 минут при комнатной температуре. После центрифугирования при 12000g и 4°C в течение 10 минут отбирали нижний образец, исключая верхний монослой жира. К образцу добавляли 200 мкл хлороформа (Sigma-Aldrich, США), хорошо перемешивали и выдерживали при комнатной температуре в течение 3 минут с последующим центрифугированием при 12 000 g при 4°C в течение 30 минут. Из трех разделенных фаз собирали самый верхний слой, добавляли к нему изопропанол и хорошо перемешивали в соотношении лизат:изопропанол = 400:300, а затем загружали в связывающую колонку AccuPrep®-III универсального набора для выделения РНК. Последующие процессы проводили согласно протоколу производителя. Экстрагированную РНК количественно определяли с помощью спектрофотометра, оценивали ее чистоту и определяли степень ее деградации с помощью РНК-гель-электрофореза.
(F обозначает прямой праймер, а R обозначает обратный праймер)
10-9-1. Уровни мРНК амфирегулина в жировой ткани
Уровень мРНК амфирегулина в подкожной жировой клетчатке мышей увеличился в 1,8 раза в группе отрицательного контроля по сравнению с нормальной контрольной группой, но снизился в 1,6 раза в группе, получавшей тестируемое вещество, по сравнению с группой отрицательного контроля.
Уровень мРНК амфирегулина в эпидидимальном жировом теле увеличился в 3,2 раза в группе отрицательного контроля по сравнению с нормальной контрольной группой, но снизился в 1,3 раза в группе, получавшей тестируемое вещество, по сравнению с группой отрицательного контроля.
Уровень мРНК амфирегулина в околопочечном жировом теле увеличился в 3,7 раз в группе отрицательного контроля по сравнению с нормальной контрольной группой, но снизился в 1,5 раза в группе, получавшей тестируемое вещество, по сравнению с группой отрицательного контроля (фиг. 28).
Хотя настоящее изобретение было подробно описано со ссылкой на конкретные признаки, специалистам в данной области техники будет очевидно, что это описание относится только к его предпочтительному варианту осуществления и не ограничивает объем настоящего изобретения. Таким образом, основной объем настоящего изобретения будет определяться прилагаемой формулой изобретения и ее эквивалентами.
Промышленная применимость
Фармацевтическая композиция по настоящему изобретению обладает превосходным эффектом уменьшения висцерального жира, а также подкожного жира и, таким образом, может быть эффективно использована для лечения и профилактики сердечно-сосудистых заболеваний, нарушений обмена веществ, диабета и различных других заболеваний. при которых осложнения, вызванные висцеральным жиром, становятся проблемой.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> BIONEER CORPORATION
SIRNAGEN THERAPEUTICS CORPORATION
<120> COMPOSITION FOR PREVENTING OR TREATING OBESITY-RELATED DISEASE
CONTAINING AMPHIREGULIN-SPECIFIC DOUBLE-STRANDED
OLIGONUCLEOTIDE
STRUCTURE
<130> PF-B2851
<140> PCT/IB2021/054077
<141> 2021-05-13
<150> 10-2020-0057879
<151> 2020-05-14
<160> 60
<170> PatentIn version 3.5
<210> 1
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 1
cctataaagc ggcaggtgc
19
<210> 2
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 2
gagcggcgca cactcccgg
19
<210> 3
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 3
gtcccagaga ccgagttgc
19
<210> 4
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 4
gagacgccgc cgctgcgaa
19
<210> 5
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 5
ccggcgccgg tggtgctgt
19
<210> 6
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 6
ggtggtgctg tcgctcttg
19
<210> 7
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 7
cgctcttgat actcggctc
19
<210> 8
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 8
tcttgatact cggctcagg
19
<210> 9
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 9
ggacctcaat gacacctac
19
<210> 10
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 10
cacctactct gggaagcgt
19
<210> 11
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 11
acctactctg ggaagcgtg
19
<210> 12
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 12
ctgggaagcg tgaaccatt
19
<210> 13
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 13
gaagcgtgaa ccattttct
19
<210> 14
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA sense
<400> 14
ttctggggac cacagtgct
19
<210> 15
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> hGAPDH-F primer
<400> 15
ggtgaaggtc ggagtcaacg
20
<210> 16
<211> 25
<212> DNA
<213> Artificial Sequence
<220>
<223> hGAPDH-R primer
<400> 16
accatgtagt tgaggtcaat gaagg
25
<210> 17
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> hAREG F primer
<400> 17
acacctactc tgggaagcgt
20
<210> 18
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> hAREG R primer
<400> 18
gccaggtatt tgtggttcgt
20
<210> 19
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> mAmphiregulin siRNA sense strand
<400> 19
aacgggactg tgcatgcca
19
<210> 20
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> mAmphiregulin siRNA sense strand
<400> 20
acgggactgt gcatgccat
19
<210> 21
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> mAmphiregulin siRNA sense strand(control)
<400> 21
cagttgtcac tttttatga
19
<210> 22
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> mGAPDH-F primer
<400> 22
aggtcggtgt gaacggattt g
21
<210> 23
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> mGAPDH-R primer
<400> 23
tgtagaccat gtagttgagg tca
23
<210> 24
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> mAREG-F primer
<400> 24
gaggcttcga caagaaaacg
20
<210> 25
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> mAREG-R primer
<400> 25
accaatgtca tttccggtgt
20
<210> 26
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> AREG Forward primer
<400> 26
cagtgctgat ggatttgagg t
21
<210> 27
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> AREG Reverse primer
<400> 27
atagccaggt atttgtggtt cg
22
<210> 28
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> AREG probe
<400> 28
tgaaccgtcc tcgggagccg act
23
<210> 29
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> RPL13A Forward primer
<400> 29
gtgtttgacg gcatcccacc
20
<210> 30
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> RPL13A Reverse primer
<400> 30
taggcttcag acgcacgacc
20
<210> 31
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> RPL13A probe
<400> 31
aagcggatgg tggttcctgc t
21
<210> 32
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> TBP Forward primer
<400> 32
caccacagct cttccactc
19
<210> 33
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> TBP Reverse primer
<400> 33
atcccagaac tctccgaagc
20
<210> 34
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> TBP probe
<400> 34
acccttgccg ggcaccactc
20
<210> 35
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 35
gcaccugccg cuuuauagg
19
<210> 36
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 36
ccgggagugu gcgccgcuc
19
<210> 37
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 37
gcaacucggu cucugggac
19
<210> 38
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 38
uucgcagcgg cggcgucuc
19
<210> 39
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 39
acagcaccac cggcgccgg
19
<210> 40
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 40
caagagcgac agcaccacc
19
<210> 41
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 41
gagccgagua ucaagagcg
19
<210> 42
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 42
ccugagccga guaucaaga
19
<210> 43
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 43
guagguguca uugaggucc
19
<210> 44
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 44
acgcuuccca gaguaggug
19
<210> 45
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 45
cacgcuuccc agaguaggu
19
<210> 46
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 46
aaugguucac gcuucccag
19
<210> 47
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 47
agaaaauggu ucacgcuuc
19
<210> 48
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> Amphiregulin siRNA antisense
<400> 48
agcacugugg uccccagaa
19
<210> 49
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> SAMiRNA-Control(human) Sense
<400> 49
cttacgctga gtacttcga
19
<210> 50
<211> 19
<212> RNA
<213> Artificial Sequence
<220>
<223> SAMiRNA-Control(human) Antisense
<400> 50
ucgaaguacu cagcguaag
19
<210> 51
<211> 25
<212> DNA
<213> Artificial Sequence
<220>
<223> Areg Forward primer
<400> 51
agtagtagct gtcactatct ttgtc
25
<210> 52
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Areg Reverse primer
<400> 52
cccgttttct tgtcgaagc
19
<210> 53
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Areg probe
<400> 53
cctcgcagct attggcatcg gca
23
<210> 54
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Tfrc Forward primer
<400> 54
aaacttgccc aagtattctc ag
22
<210> 55
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Tfrc Reverse primer
<400> 55
atgaaaggta tccctccaac c
21
<210> 56
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Tfrc probe
<400> 56
tgccagctgg actgcaggcg act
23
<210> 57
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Areg Forward primer
<400> 57
gaggcttcga caagaaaacg
20
<210> 58
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Areg Reverse primer
<400> 58
accaatgtca tttccggtgt
20
<210> 59
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Gapdh Forward primer
<400> 59
agggtggagc caaaagggtc
20
<210> 60
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Gapdh Reverse primer
<400> 60
ggctaagcag ttggtggtgc
20
<---
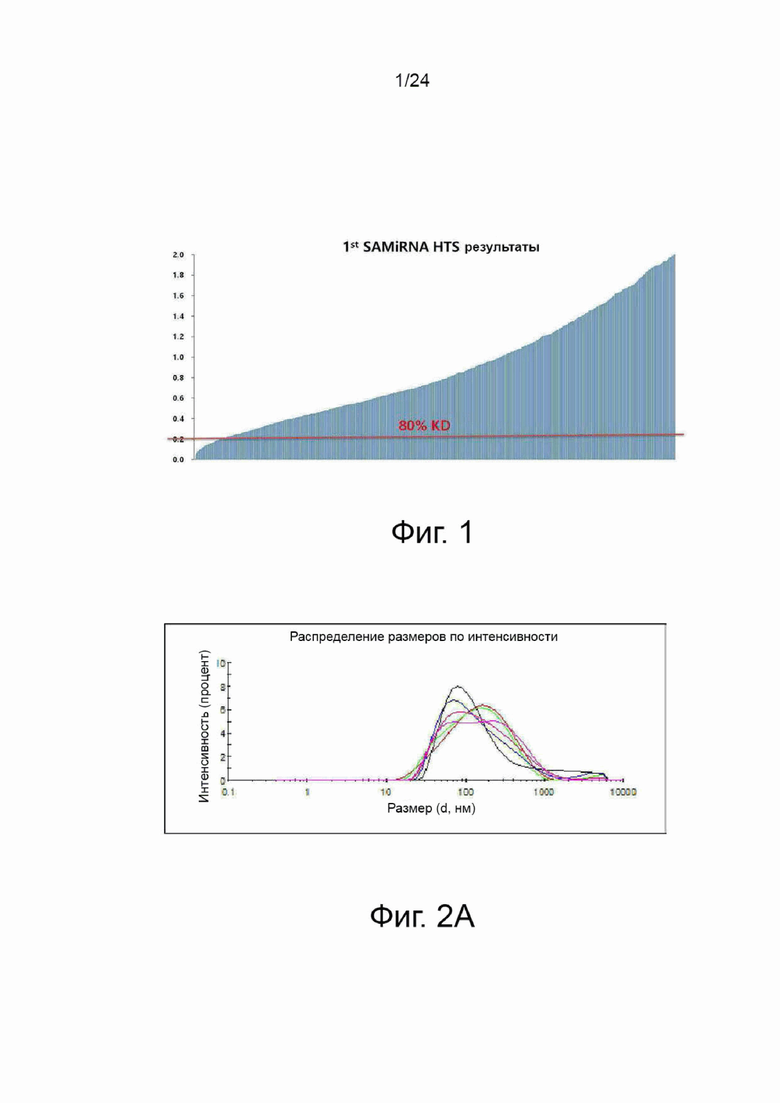
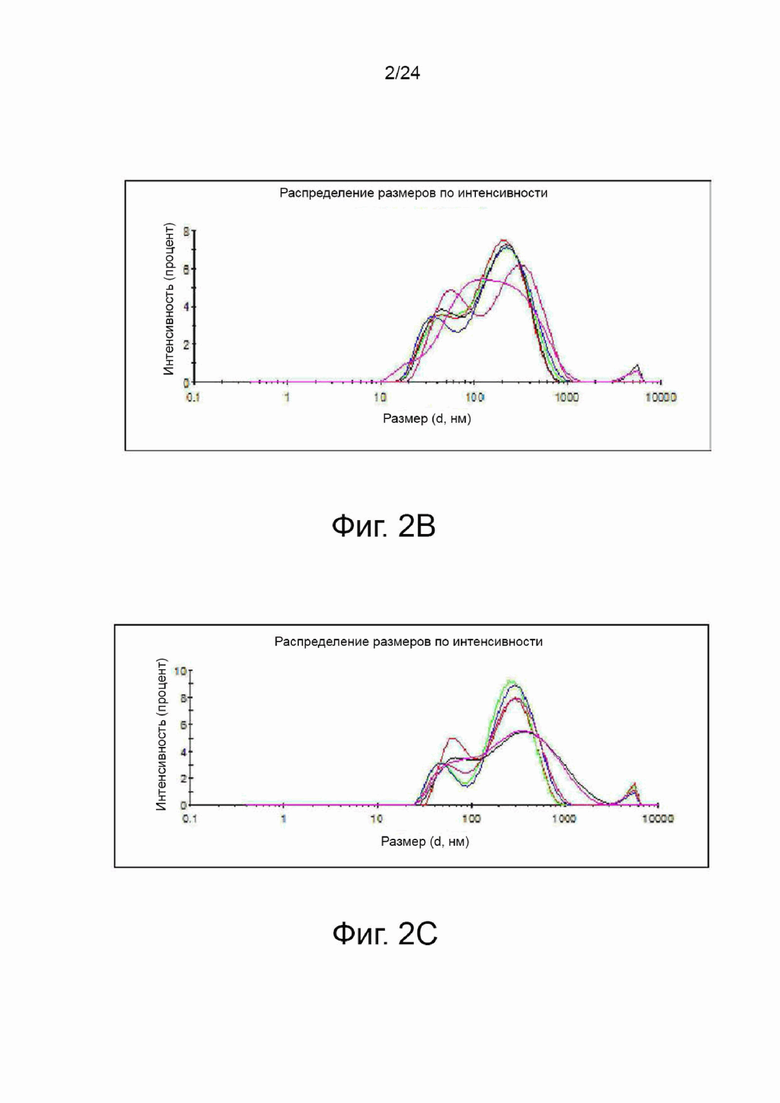
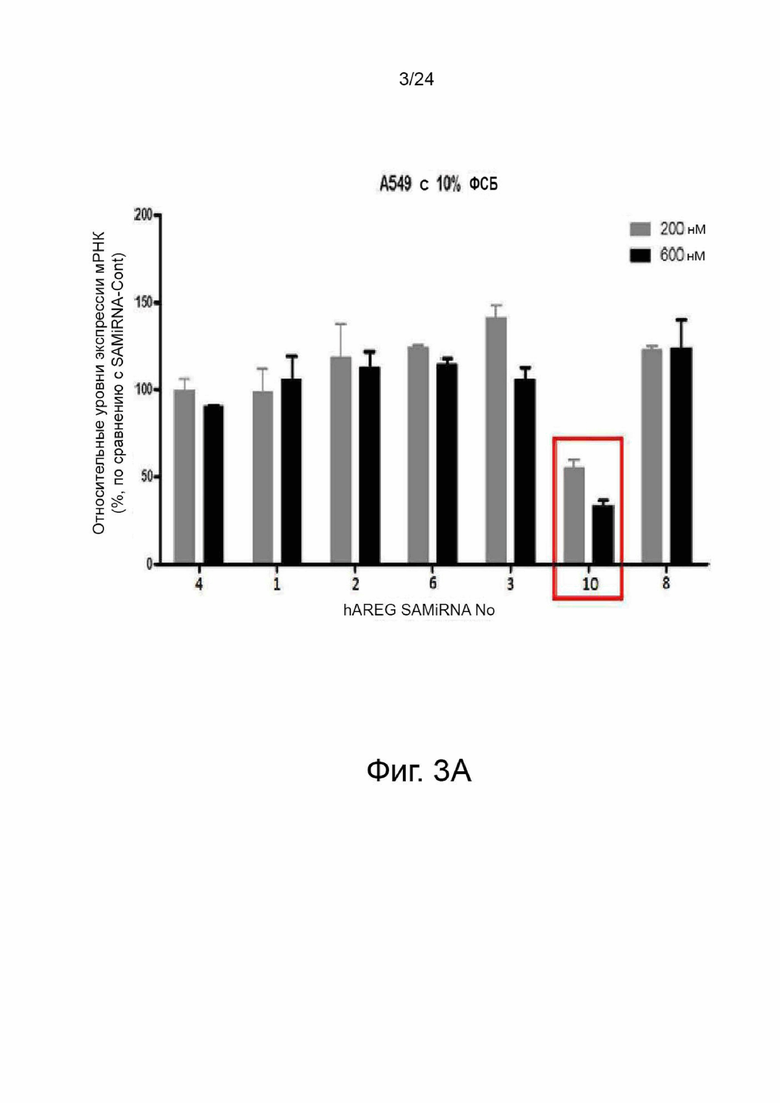
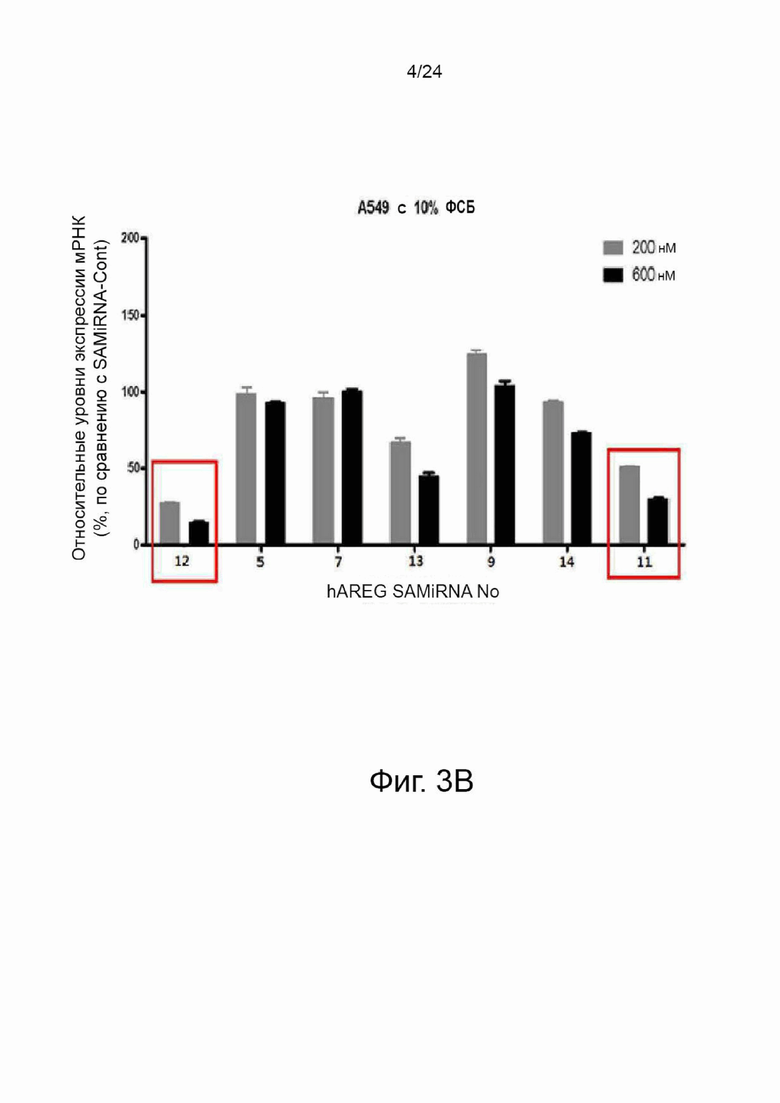
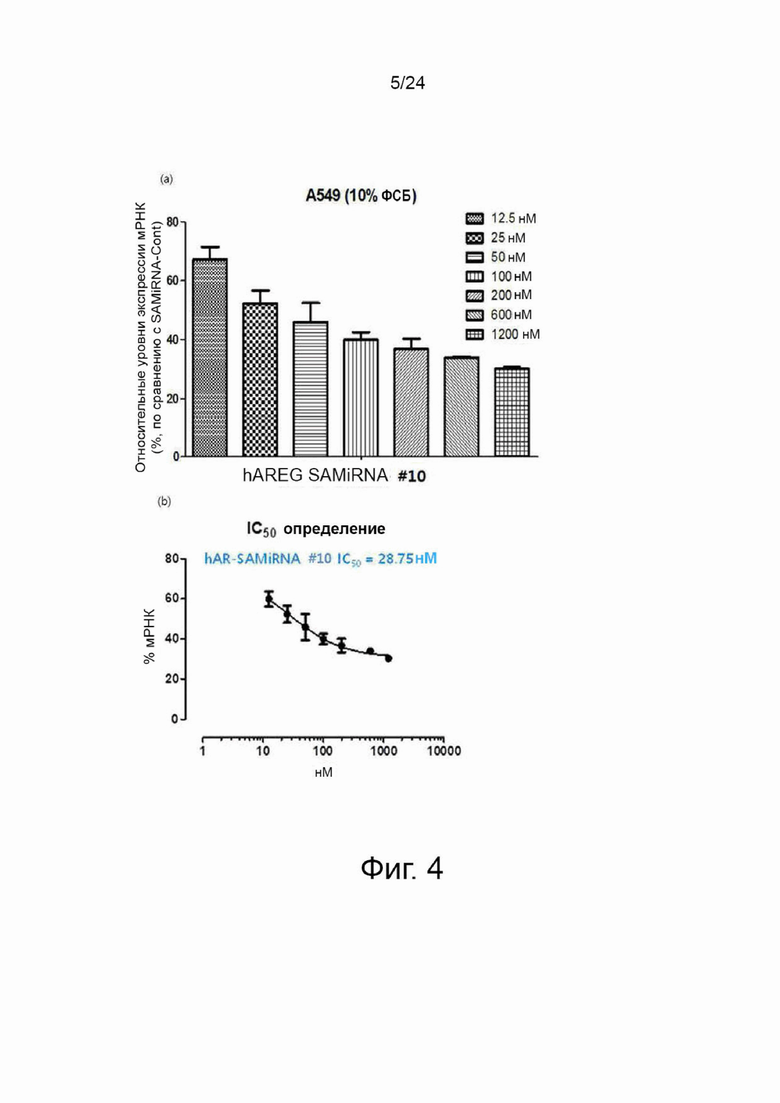
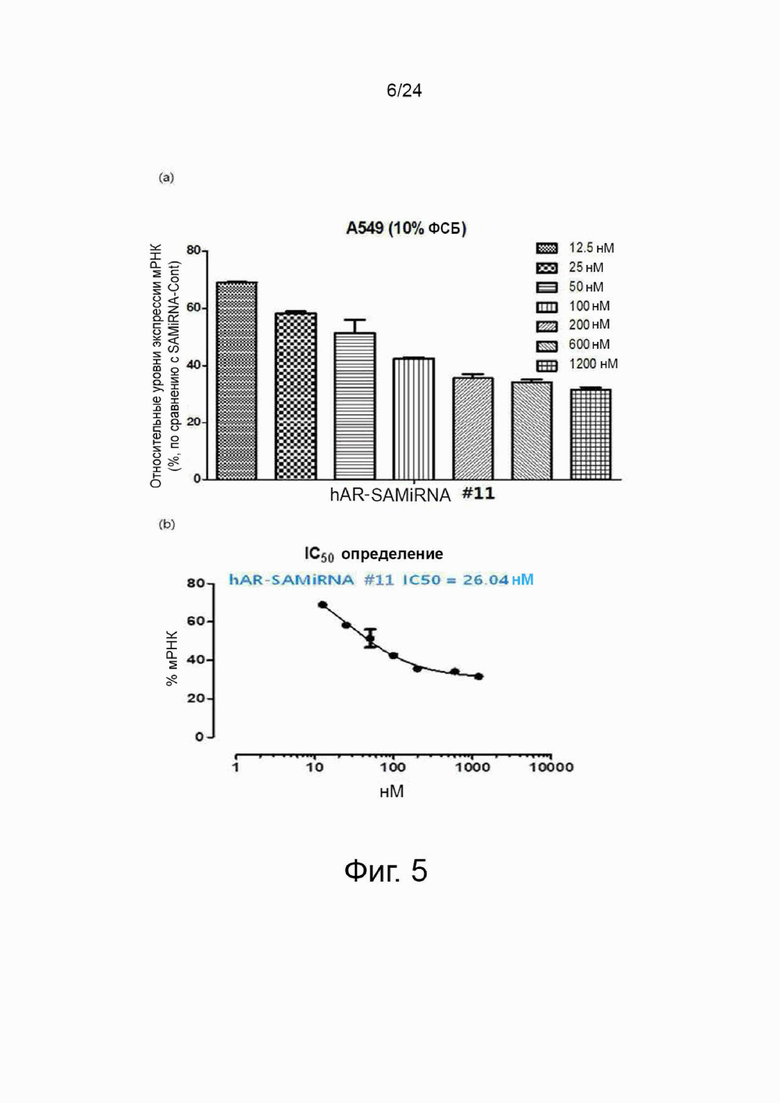
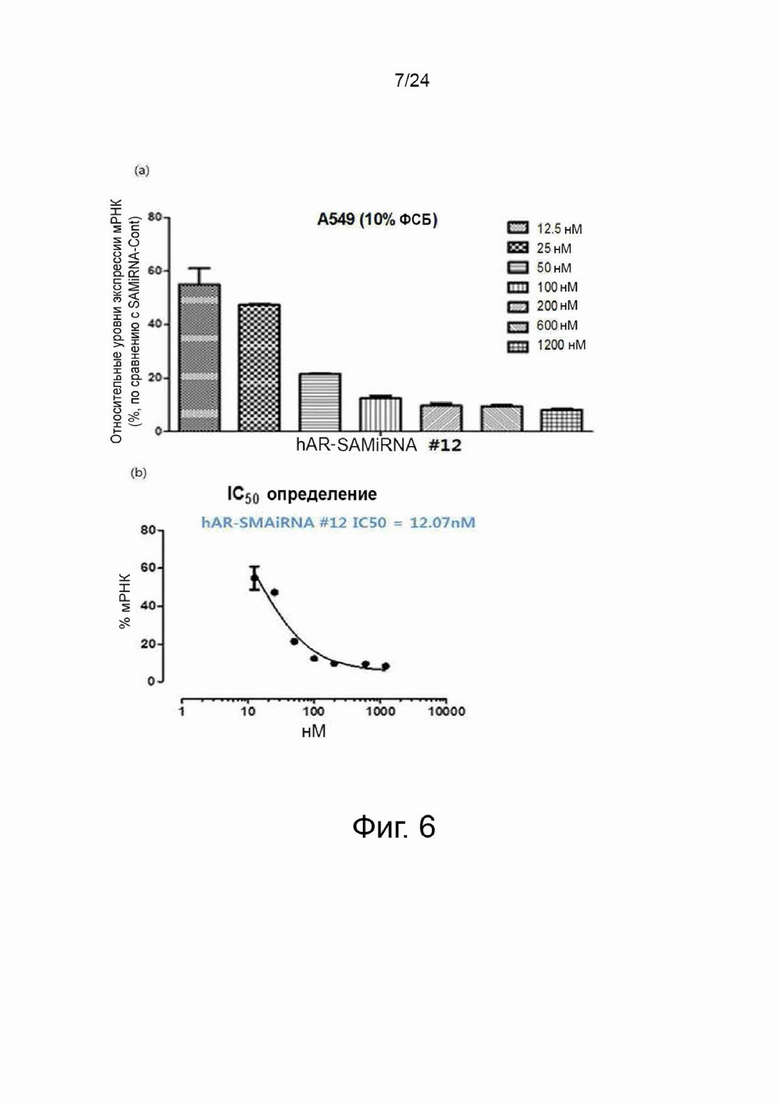
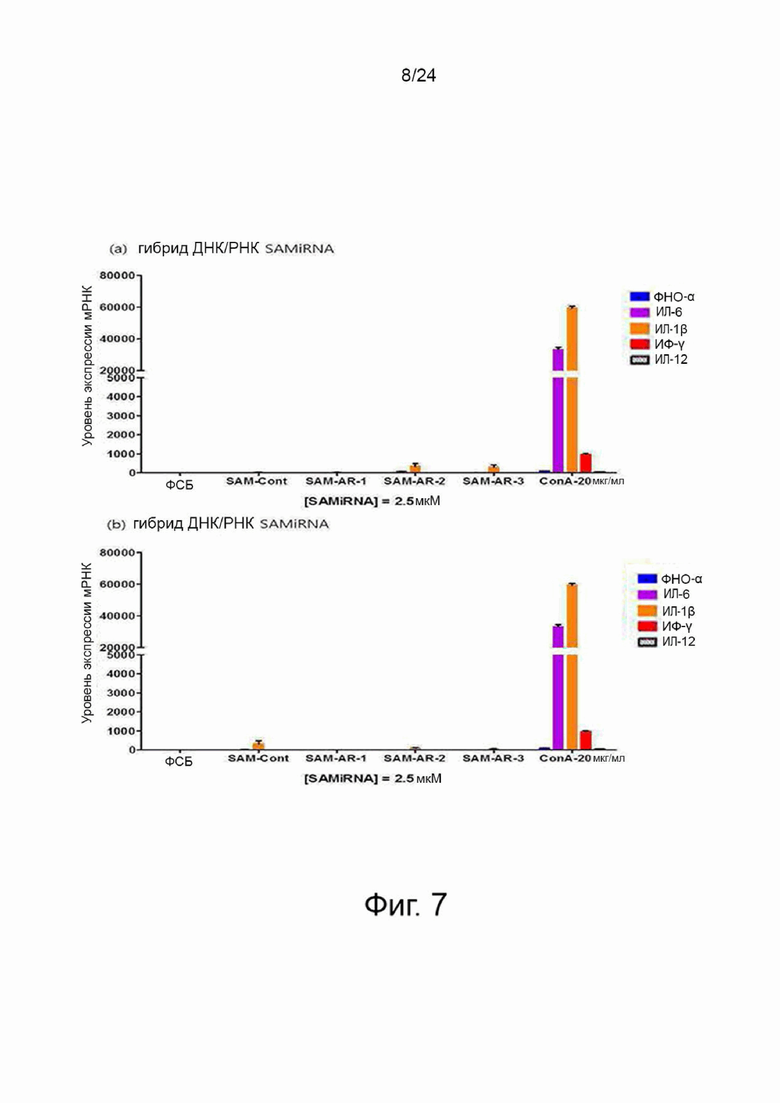
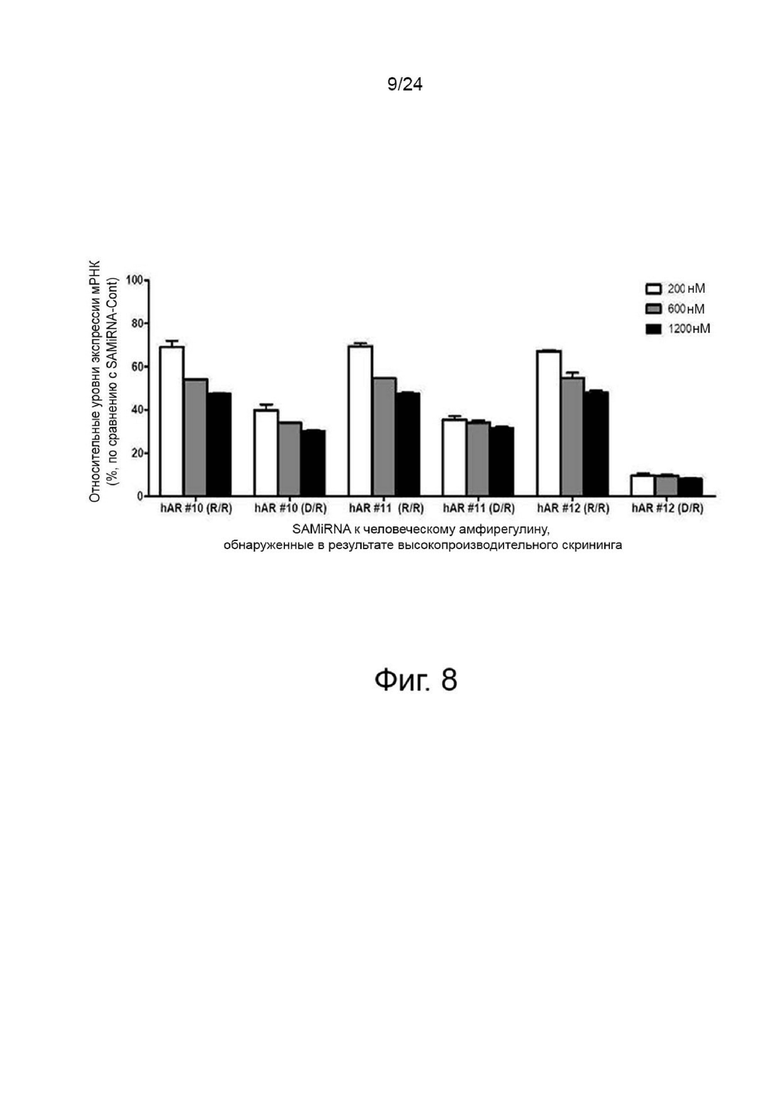
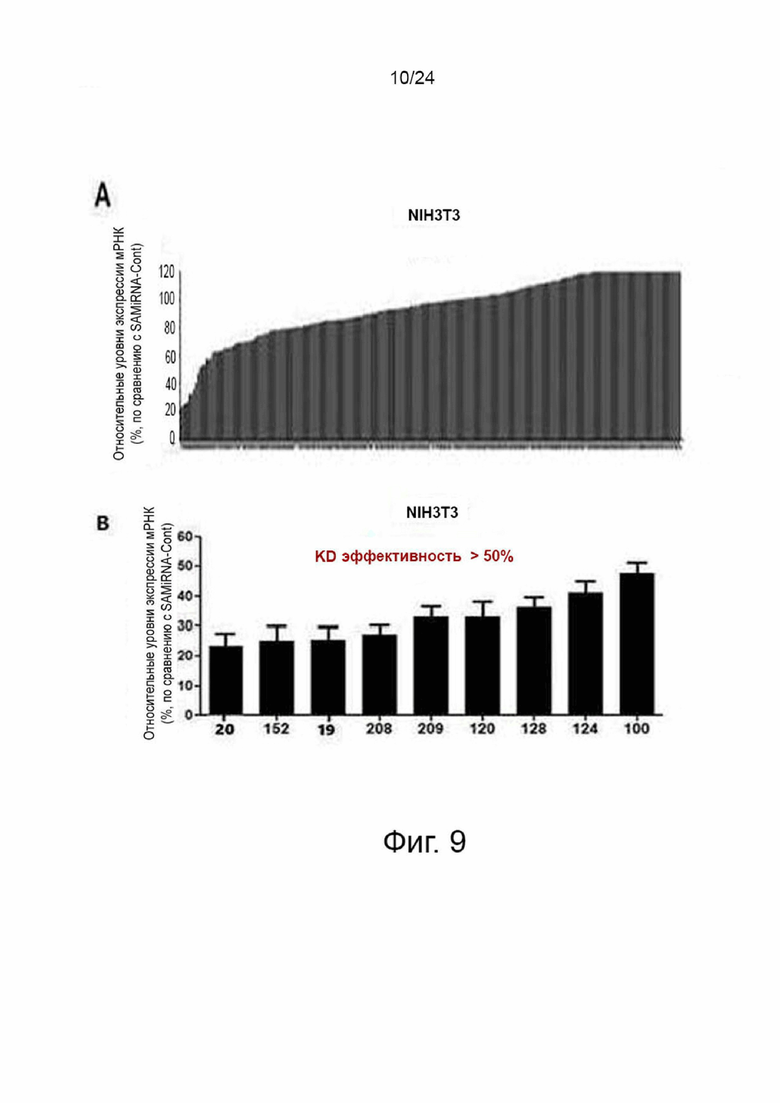
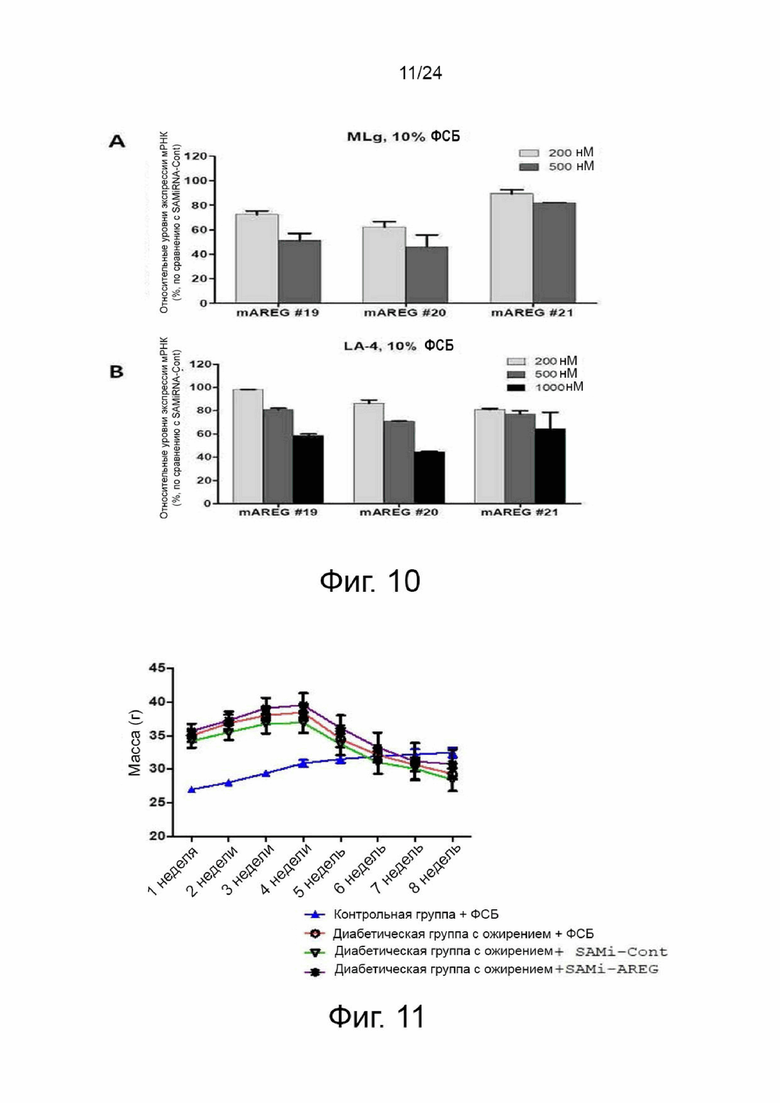
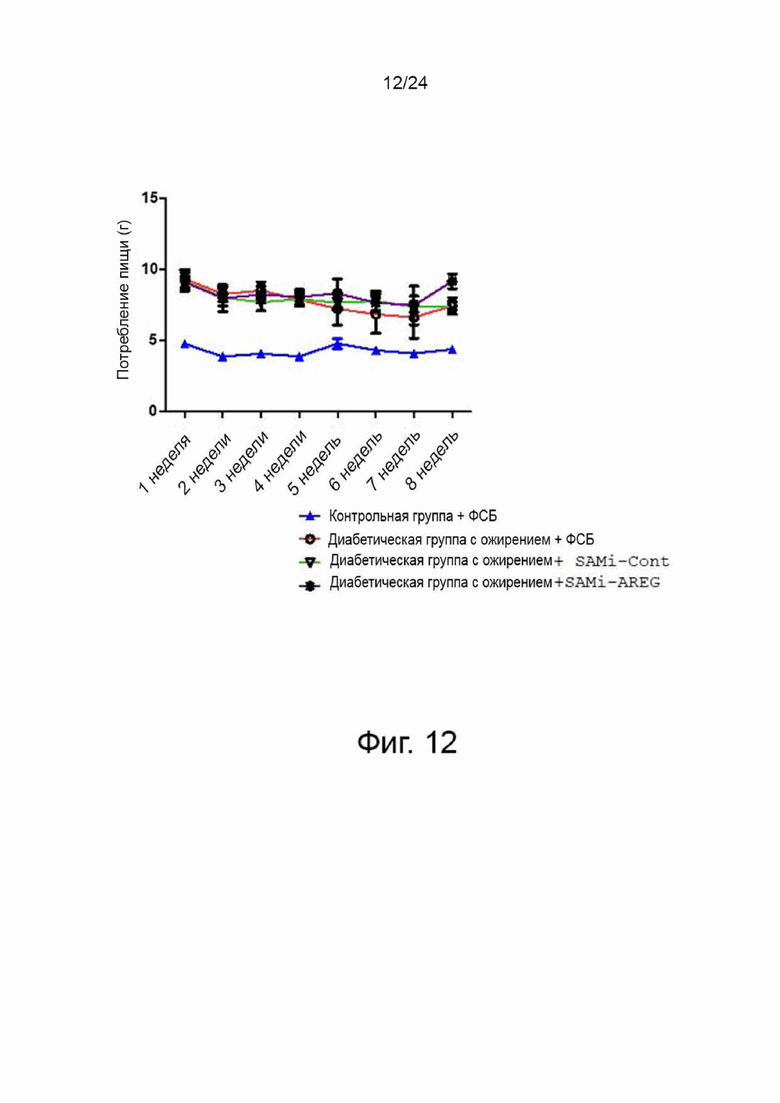
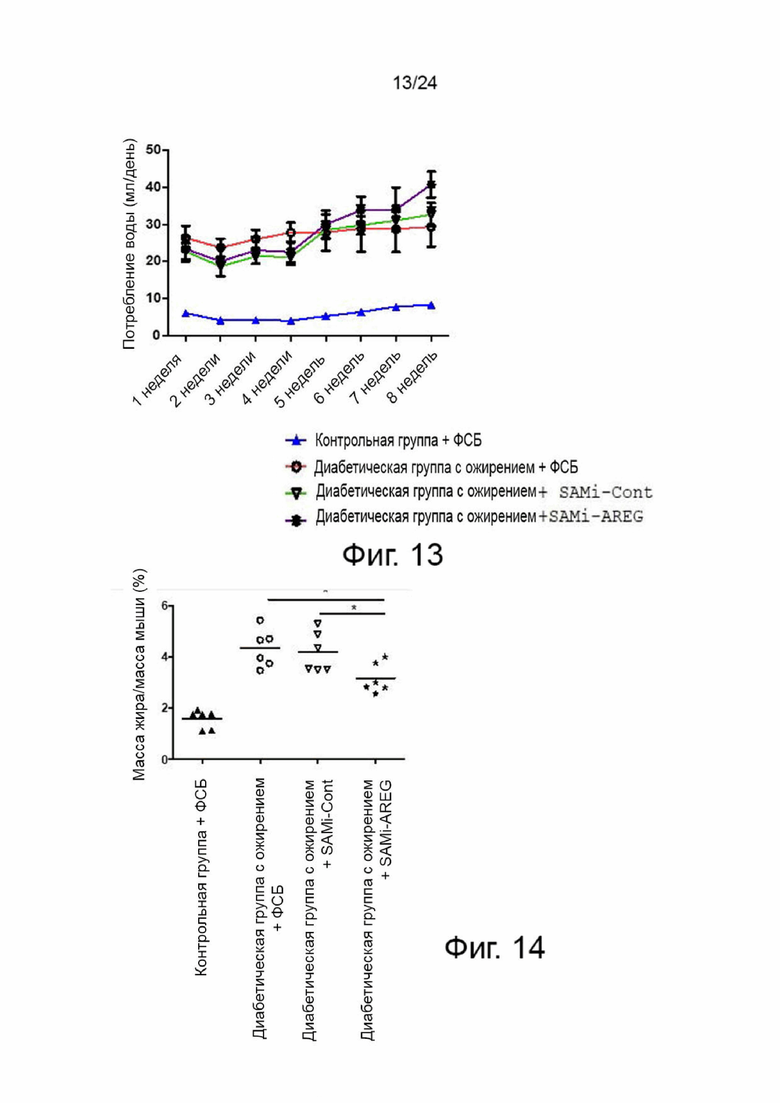
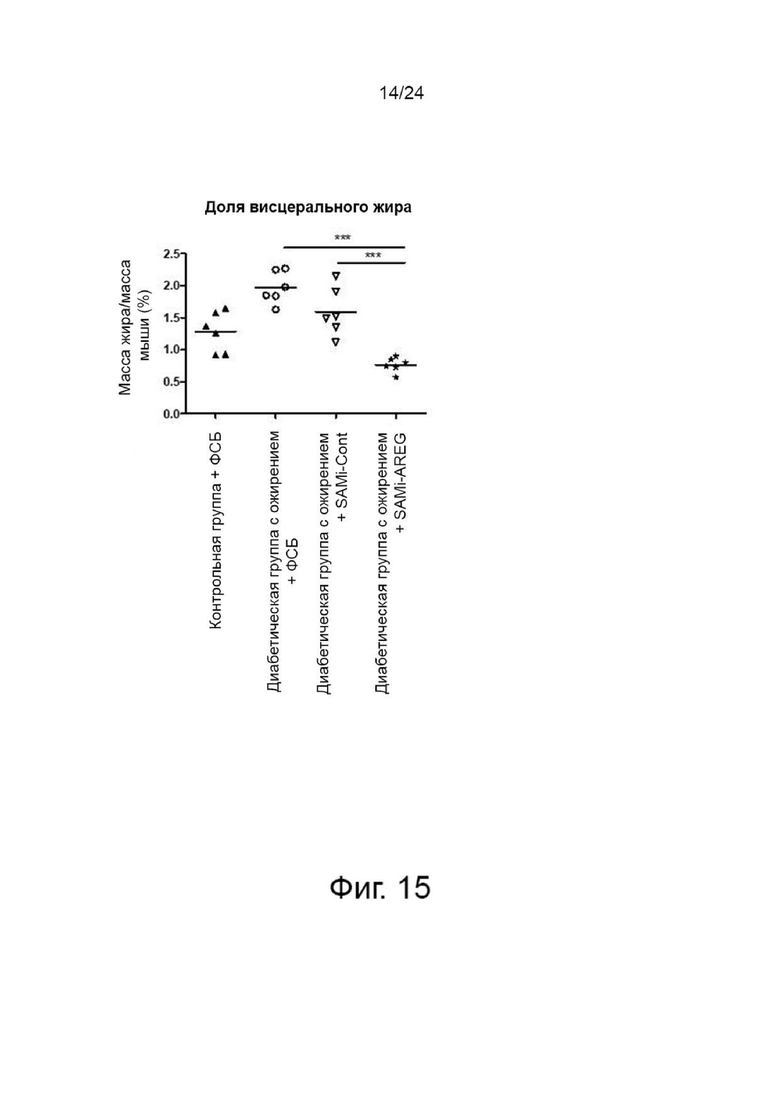
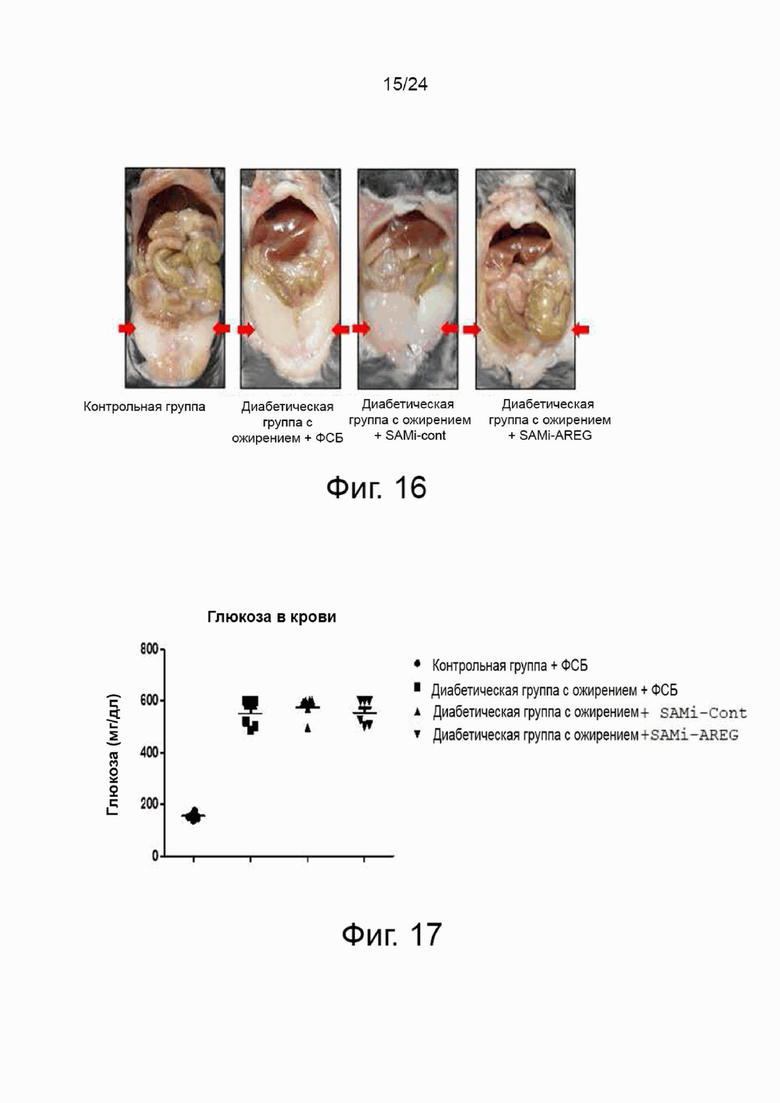
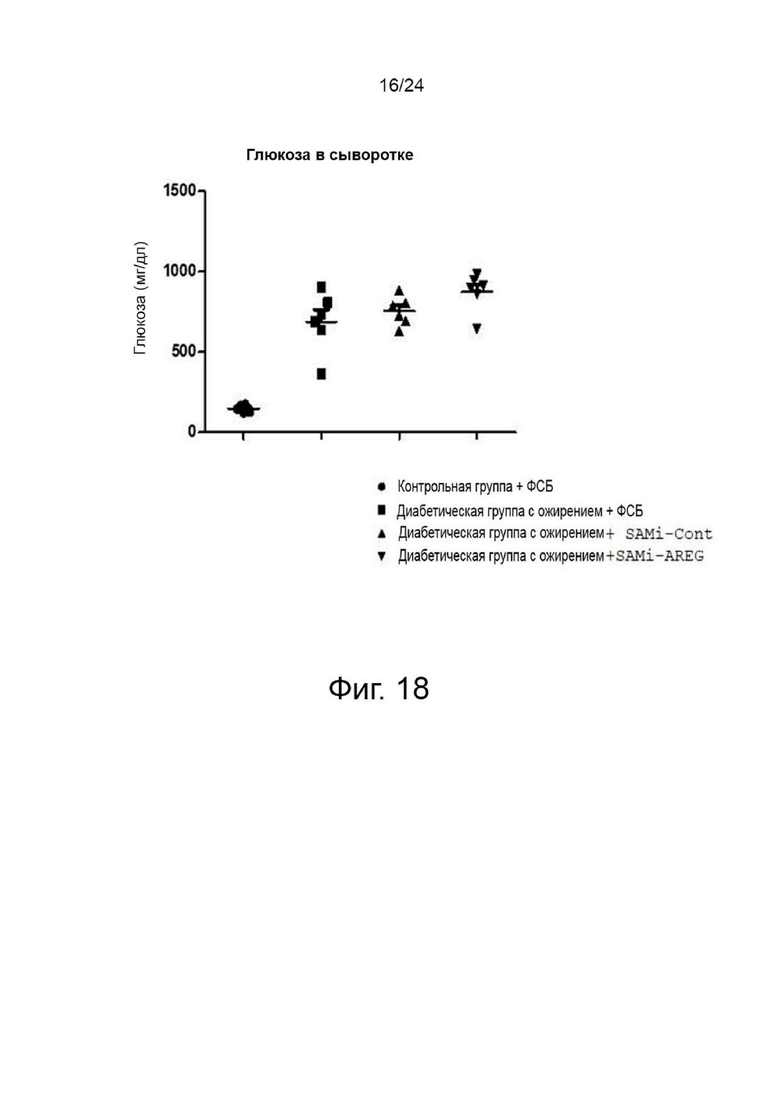
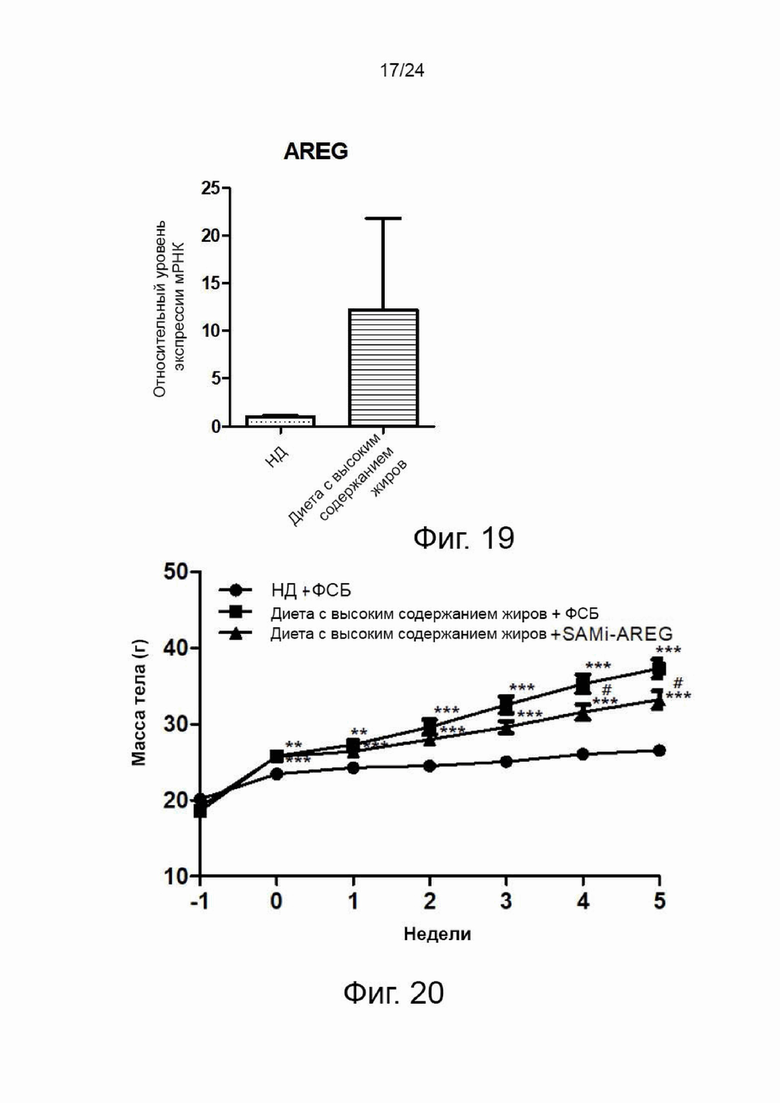
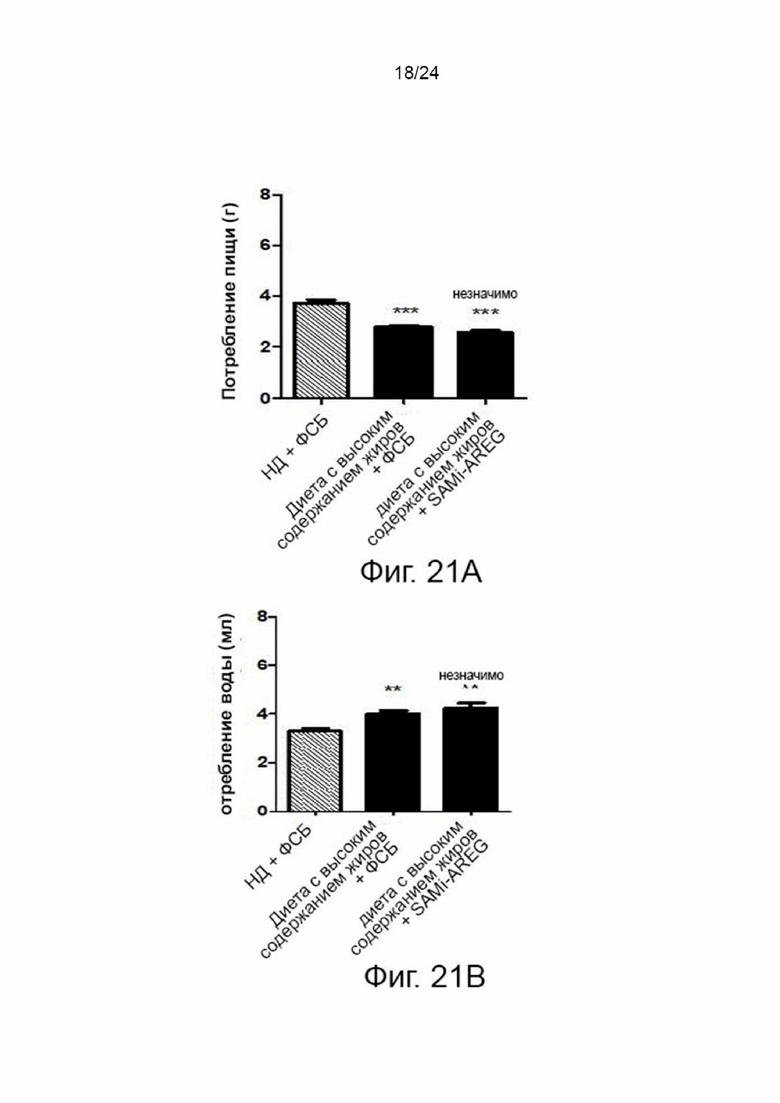
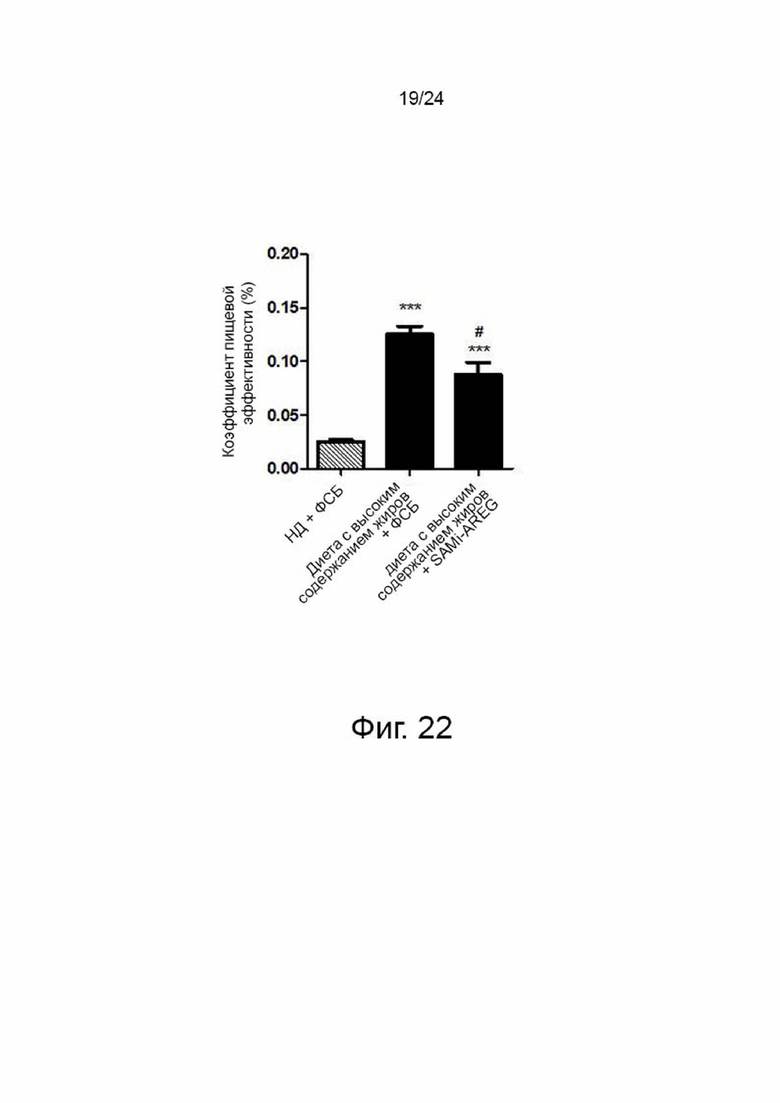

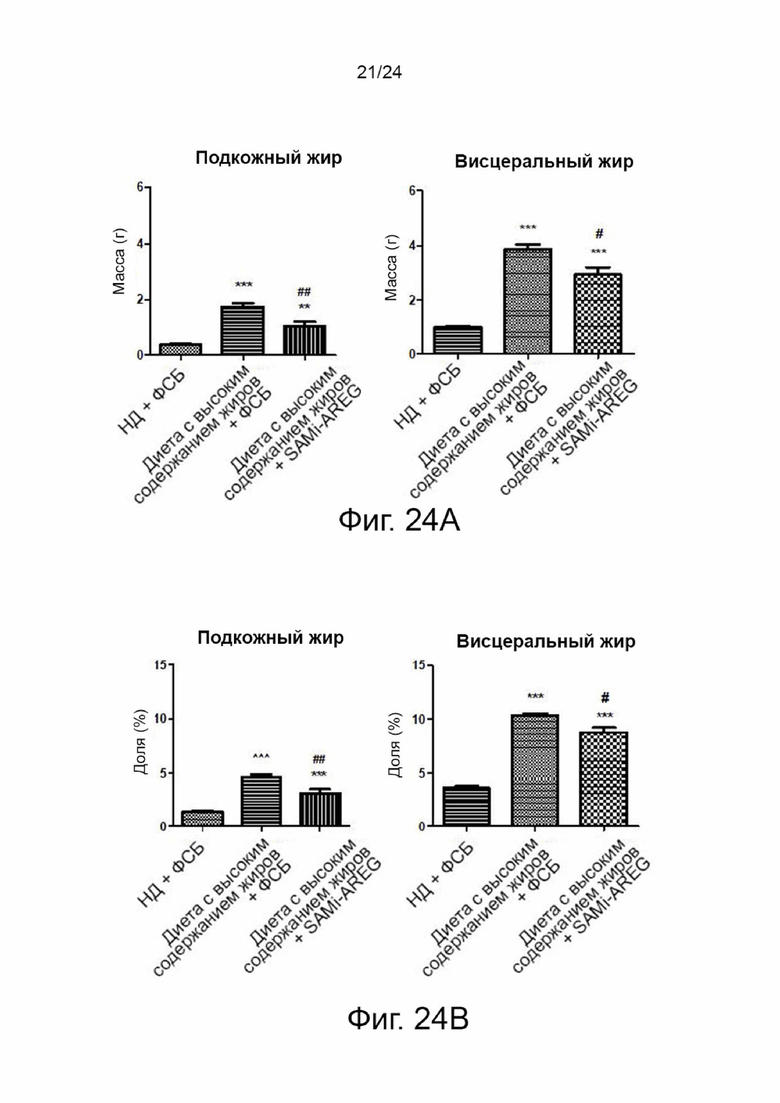
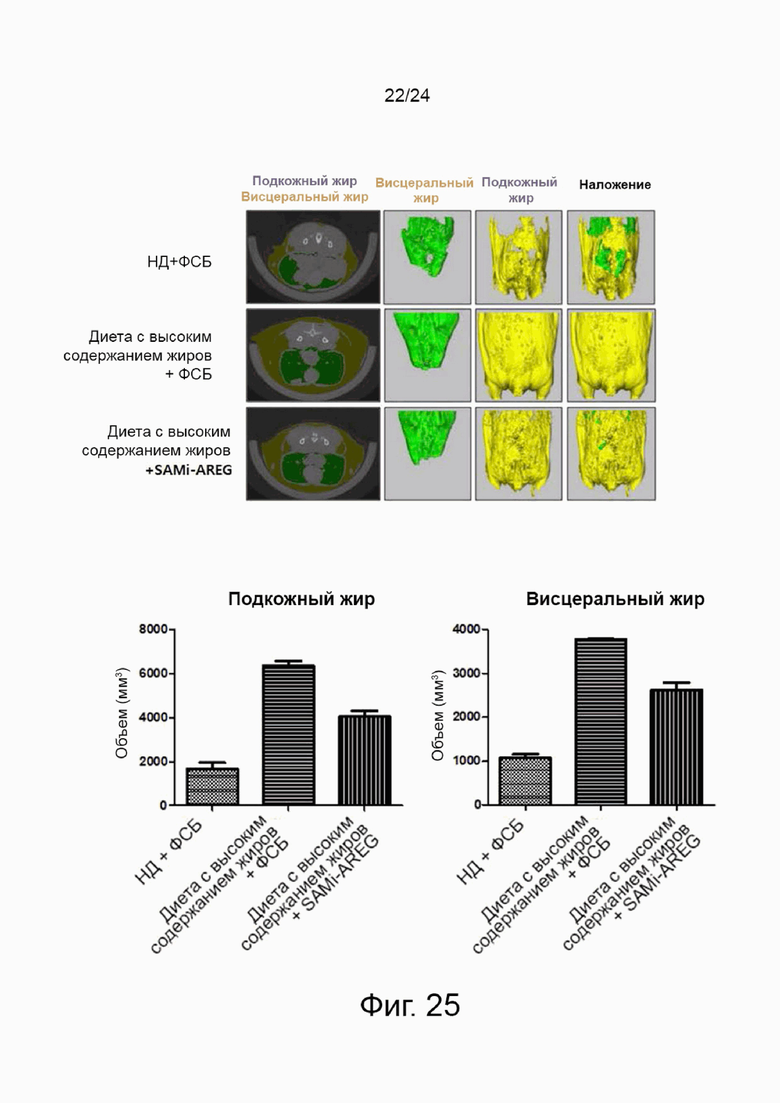
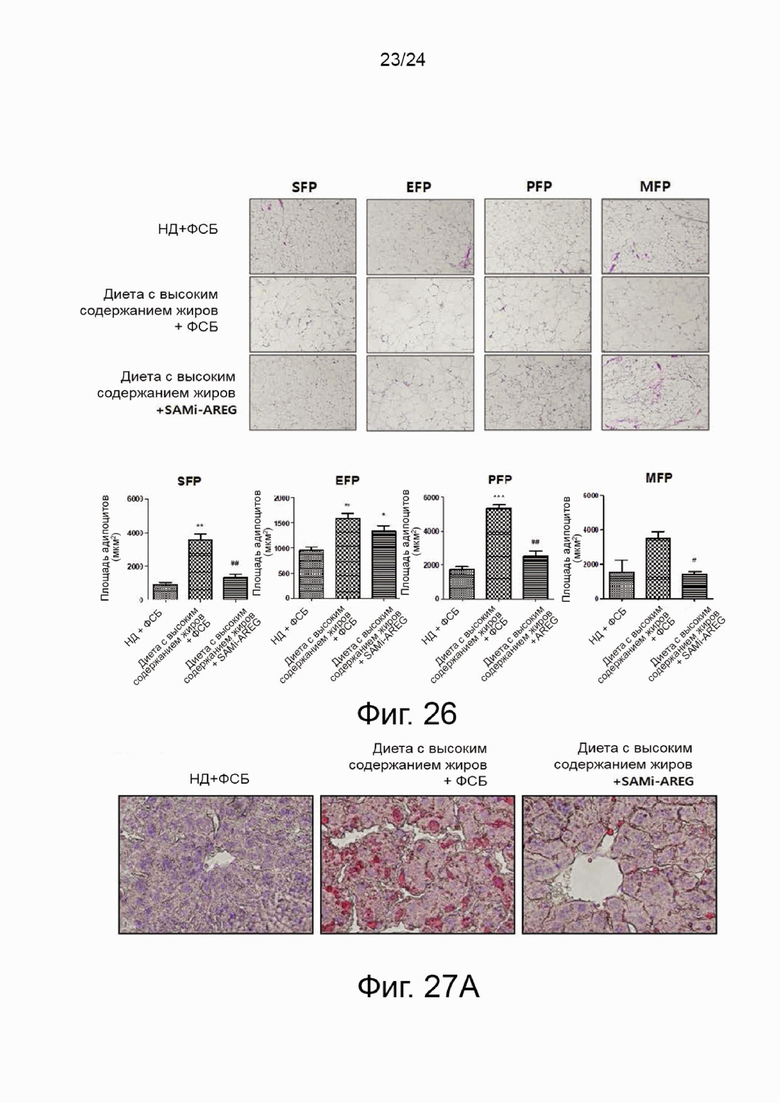
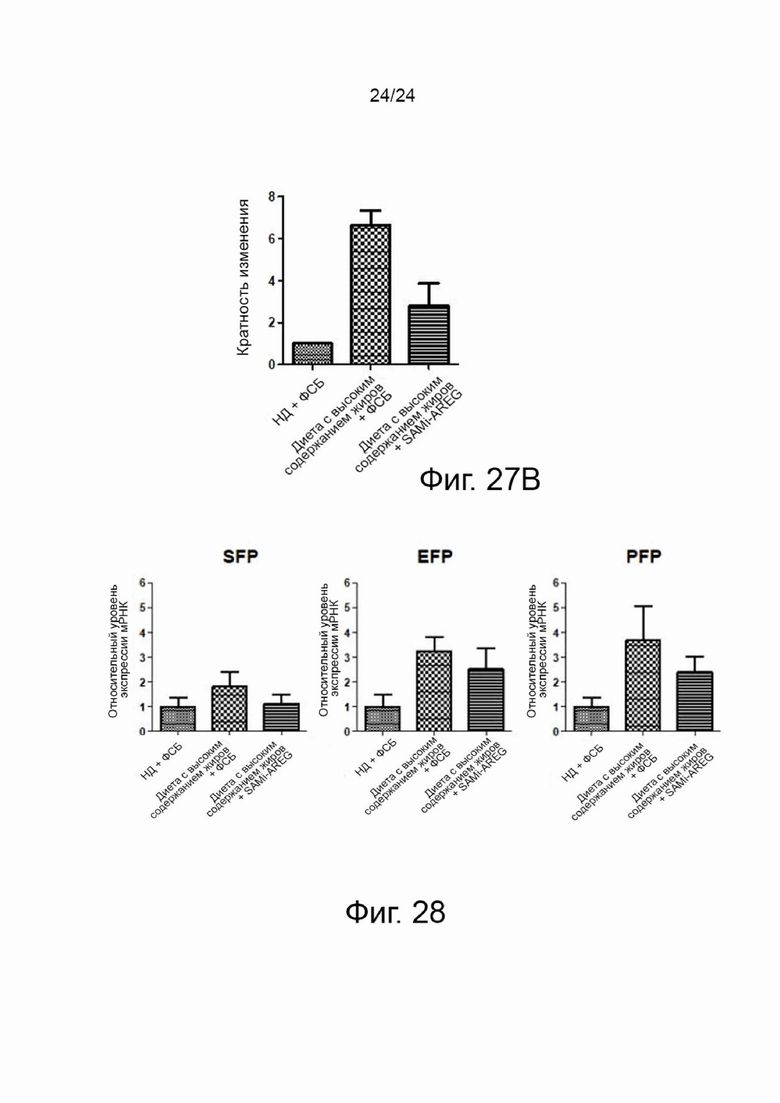
Изобретение относится к композиции для лечения или предупреждения ожирения. Предложено применение фармацевтической композиции, содержащей амфирегулин-специфический двухцепочечный олигонуклеотид, двухцепочечную олиго-РНК, которая содержит гидрофильные и гидрофобные соединения, соединенные с амфирегулин-специфическим двухцепочечным олигонуклеотидом, или наночастицы, содержащие двухцепочечную олиго-РНК. Амфирегулин-специфический двухцепочечный олигонуклеотид содержит последовательность, выбранную из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, комплементарную последовательности смысловой цепи. Изобретение обеспечивает потерю веса, снижение коэффициента пищевой эффективности, уменьшение подкожного жира, уменьшение висцерального жира, уменьшение площади адипоцитов и ингибирование адипогенеза печени. 23 з.п. ф-лы, 28 ил., 10 табл., 10 пр.
1. Применение фармацевтической композиции для лечения или предупреждения ожирения, где фармацевтическая композиция содержит любой компонент, выбранный из группы, состоящей из:
(i) амфирегулин-специфического двухцепочечного олигонуклеотида, который содержит любую последовательность, выбранную из группы, состоящей из SEQ ID NO: 10, 11 и 12, и антисмысловую цепь, содержащую последовательность, комплементарную последовательности смысловой цепи;
(ii) амфирегулин-специфической двухцепочечной олигонуклеотидной структуры, содержащей структуру, представленную следующей структурной формулой (1):
структурная формула (1)
A-X-R-Y-B,
где A представляет собой гидрофильное соединение, B представляет собой гидрофобное соединение, каждый из X и Y независимо представляет собой простую ковалентную связь или опосредованную линкером ковалентную связь, а R представляет собой амфирегулин-специфический двухцепочечный олигонуклеотид (i); и
(iii) наночастиц, содержащих амфирегулин-специфическую двухцепочечную олигонуклеотидную структуру (ii).
2. Применение по п. 1, в котором смысловая цепь или антисмысловая цепь состоит из 19-31 нуклеотида.
3. Применение по п. 1, где олигонуклеотид представляет собой siRNA, shRNA или miRNA.
4. Применение по п. 1, где смысловая цепь или антисмысловая цепь независимо представляет собой ДНК или РНК.
5. Применение по п. 1, где смысловая цепь или антисмысловая цепь двухцепочечного олигонуклеотида содержит химическую модификацию.
6. Применение по п. 5, где химическая модификация представляет собой любую одну или несколько модификаций, выбранных из группы, состоящей из:
модификации, при которой ОН-группа в 2' положении углерода сахарной структуры в одном или нескольких нуклеотидах замещена любой группой, выбранной из группы, состоящей из метильной группы (-СН3), метоксигруппы (-ОСН3), аминогруппы (-NH2), фтора (-F), -O-2-метоксиэтильной группы, -O-пропильной группы, -O-2-метилтиоэтильной группы, -O-3-аминопропильной группы, -O-3-диметиламинопропильной группы, -O-N-метилацетамидогруппы и -O-диметиламидооксиэтильной группы;
модификации, при которой кислород в сахарной структуре в нуклеотидах замещен серой; модификации связи между нуклеотидами в любую связь, выбранную из группы, состоящей из фосфоротиоатной связи, боранофосфатной связи и метилфосфонатной связи;
модификации в PNA (пептидная нуклеиновая кислота), LNA (запертая нуклеиновая кислота) или UNA (незапертая нуклеиновая кислота); и
модификации в гибрид ДНК-РНК.
7. Применение по п. 1, в котором по меньшей мере одна фосфатная группа связана с 5'-концом антисмысловой цепи двухцепочечного олигонуклеотида.
8. Применение по п. 1, в котором амфирегулин-специфическая двухцепочечная олигонуклеотидная структура содержит структуру, представленную следующей структурной формулой (2):
структурная формула (2)
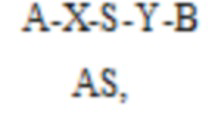
где S и AS, соответственно, представляют собой смысловую цепь и антисмысловую цепь двухцепочечного олигонуклеотида по п. 1, а A, B, X и Y являются такими, как определено в п. 1.
9. Применение по п. 8, в котором амфирегулин-специфическая двухцепочечная олигонуклеотидная структура содержит структуру, представленную следующей структурной формулой (3) или (4):
структурная формула (3)

структурная формула (4)
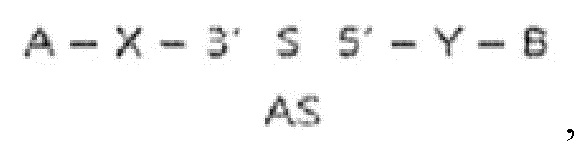
где A, B, X, Y, S и AS являются такими же, как определено в п. 8, и 5' и 3', соответственно, представляют собой 5'-конец и 3'-конец смысловой цепи двухцепочечного олигонуклеотида.
10. Применение по п. 1, в котором гидрофильное соединение выбрано из группы, состоящей из полиэтиленгликоля (PEG), поливинилпирролидона и полиоксазолина.
11. Применение по п. 1, в котором гидрофильное соединение имеет структуру, представленную следующей структурной формулой (5) или (6):
структурная формула (5)
(A'm-J)n,
структурная формула (6)
(J-A'm)n,
где A' представляет собой гидрофильный мономер, J представляет собой линкер, который соединяет m гидрофильных мономеров вместе или соединяет m гидрофильных мономеров с двухцепочечным олигонуклеотидом, m представляет собой целое число в диапазоне от 1 до 15, n представляет собой целое число в диапазоне от 1 до 10,
гидрофильный мономер (A') представляет собой любое соединение, выбранное из следующих соединений с (1) по (3), а линкер (J) выбран из группы, состоящей из -PO3–-, -SO3- и - CO2-:
соединение (1)
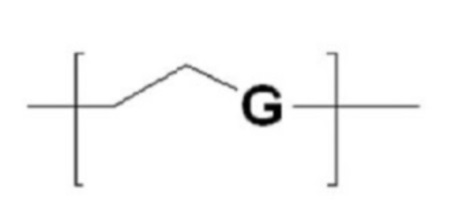 ,
,
где G выбран из группы, состоящей из O, S и NH;
соединение (2)
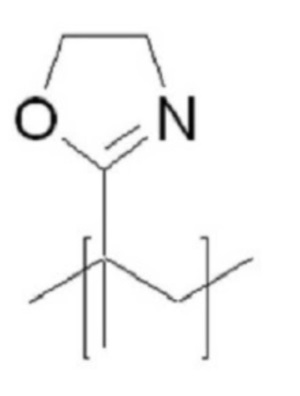 ,
,
соединение (3)
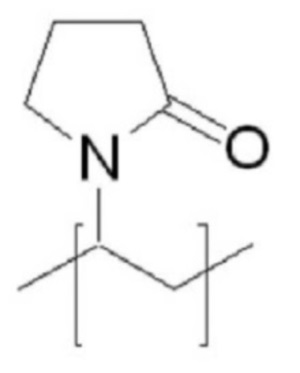 .
.
12. Применение по п. 11, в котором амфирегулин-специфическая двухцепочечная олигонуклеотидная структура имеет структуру, представленную следующей структурной формулой (7) или структурной формулой (8):
структурная формула (7)
(A'm-J)n -X-R-Y-B,
структурная формула (8)
(J-A'm)n-X-R-Y-B.
13. Применение по п. 1, в котором гидрофильное соединение имеет молекулярную массу от 200 до 10000.
14. Применение по п. 1, в котором гидрофобное соединение имеет молекулярную массу от 250 до 1000.
15. Применение по п. 14, в котором гидрофобное соединение представляет собой любое соединение, выбранное из группы, состоящей из производного стероида, производного глицерида, эфира глицерина, полипропиленгликоля, ненасыщенного или насыщенного углеводорода C12-C50, диацилфосфатидилхолина, жирной кислоты, фосфолипида, липополиамина, липида, токоферола и токотриенола.
16. Применение по п. 15, в котором производное стероида представляет собой любое производное, выбранное из группы, состоящей из холестерина, холестанола, холевой кислоты, холестерилформиата, холестанилформиата и холестаниламина.
17. Применение по п. 15, в котором производное глицерида представляет собой любое производное, выбранное из группы, состоящей из моноглицерида, диглицерида и триглицерида.
18. Применение по п. 1, в котором ковалентная связь, представленная каждым из X и Y, является нерасщепляемой связью или расщепляемой связью.
19. Применение по п. 18, в котором нерасщепляемая связь представляет собой амидную связь или фосфатную связь.
20. Применение по п. 18, в котором расщепляемая связь представляет собой любую связь, выбранную из группы, состоящей из дисульфидной связи, расщепляемой кислотой связи, сложноэфирной связи, ангидридной связи, биоразлагаемой связи и ферментативно расщепляемой связи.
21. Применение по п. 1, в котором наночастица состоит из смеси двухцепочечных олигонуклеотидных структур, содержащих двухцепочечные олигонуклеотиды, содержащие различные последовательности.
22. Применение по п. 1, в котором ожирение представляет собой ожирение по типу висцерального, вызванное диабетом.
23. Применение по п. 1, в котором фармацевтическая композиция демонстрирует один или несколько из следующих эффектов:
(i) потеря массы тела,
(ii) снижение коэффициента пищевой эффективности,
(iii) уменьшение подкожного жира,
(iv) уменьшение висцерального жира,
(v) уменьшение площади адипоцитов, и
(vi) ингибирование адипогенеза печени.
24. Применение по п. 1, где фармацевтическая композиция демонстрирует эффект предупреждения или лечения ожирения путем ингибирования экспрессии амфирегулина в жировой ткани.
| CA 3101320 A1, 28.11.2019 | |||
| US 2017130231 A1, 11.05.2017 | |||
| RU 2007105994 A, 27.08.2008. |
Авторы
Даты
2023-12-27—Публикация
2021-05-13—Подача