Способ синтеза наночастиц магнетита стержневой формы относится к нанотехнологиям, а именно к разработке методов синтеза магнитных наноструктур, которые могут быть использованы для решения следующих биомедицинских задач:
- в качестве контрастного вещества для магнитно-резонансной томографии (МРТ);
- как носитель лекарственных препаратов для адресной магнитной доставки;
- в качестве агента для магнитной гипертермии новообразований;
- как магнитный маркер для исследования биораспределения разрабатываемых лекарственных форм препаратов in vivo с помощью специальных магниточувствительных сенсоров.
Наноструктурированные материалы имеют большое количество как потенциальных, так и реализуемых в настоящее время применений: в катализе и химической промышленности [A. Meffre, B. Mehdaoui, V. Connord, et al. Complex nano-objects displaying both magnetic and catalytic properties: A proof of concept for magnetically induced heterogeneous catalysis // Nano Lett. - 2015, - Vol. 15, - P. 3241-3248; M. E. Khan, M. M. Khan and M. H. Cho. Recent progress of metal-graphene nanostructures in photocatalysis // Nanoscale. - 2018, - Vol.10, - №20. - P. 9427 9440], в качестве источников и преобразователей энергии [J. Wang, Y. Li and L. Deng, et al. High-Performance Photothermal Conversion of Narrow-Bandgap Ti2O3 Nanoparticles // Adv. Mater. - 2016, - P. 1-6; S. Ghosh and R. N. Basu. Multifunctional nanostructured electrocatalysts for energy conversion and storage: current status and perspectives // Nanoscale. - 2018, - Vol. 10, - № 24, - P. 11241-11280], в биомедицине [D. Karponis, M. Azzawi and A. Seifalian. An arsenal of magnetic nanoparticles; perspectives in the treatment of cancer // Nanomedicine. - 2016, - Vol. 11, - № 16, - P. 2215-2232; Q. A. Pankhurst, N. K. T. Thanh, S. K. Jones and J. Dobson. Progress in applications of magnetic nanoparticles in biomedicine // J. Phys. D: Appl. Phys. - 2009, - Vol. 42, - P. 224; N. T. K. Thanh. Clinical Applications of Magnetic Nanoparticle // CRC press. - 2017], в решении экологических проблем [J. Zhu, S. Wei and M. Chen, et al. Magnetic nanocomposites for environmental remediation // Adv. Powder Technol. - 2013, - Vol. 24, - № 2, - P. 459-467; F. Li, D. MacFarlane and J. Zhang. Recent Advances in Nanoengineering of Electrocatalysts for CO2 Reduction // Nanoscale. - 2018, -P. 6235-6260], в микроэлектронике [S. P. Gubin. Magnetic Nanoparticles. New York. - 2009; G. Reiss, A. Hütten. Applications beyond data storage // Nature Materials. - 2005, - Vol. 4, - № 10, - P. 725-726; V. Skumryev, S. Stoyanov, Y. Zhang, et al. Beating the superparamagnetic limit with exchange bias // Nature. - 2003, - Vol. 423, - P. 850-853] и спинтронике [P. Anil Kumar, S. Ray, S. Chakraverty, et al. Engineered spin-valve type magnetoresistance in Fe3O4-CoFe2O4 core-shell nanoparticles // Applied Physics Letters. - 2013, - Vol. 103, - № 10, - P. 106; L. Bogani, W. Wernsdorfer. Molecular spintronics using single-molecule magnets // Nature Materials. - 2008, - Vol. 7, - № 3, - P. 179]. Всё большее внимание уделяется наноструктурам с нестандартной формой: кубы, октаэдры, чешуйки, стержни, проволоки и другие, которые проявляют анизотропные свойства.
В частности, наноструктуры вытянутой формы (стержни, проволоки) обладают специфическими и даже лучшими свойствами по сравнению с другими формами. Например, наностержни из золота и серебра имеют более высокое сечение оптического поглощения по сравнению с наносферами из тех же материалов [P. K. Jain, K. S. Lee, I. El-Sayed and M. El-Sayed. Calculated Absorption and Scattering Properties of Gold Nanoparticles of Different Size, Shape, and Composition: Applications in Biological Imaging and Biomedicine // J. Phys. Chem. B. - 2006, - Vol. 110, - P. 7238-7248]. Кроме того, такие металлические наночастицы проявляют поверхностный плазмонный резонанс в красной и ближней инфракрасной области спектра [B. J. Wiley, Y. Chen, J. McLellan, et al. Synthesis and Optical Properties of Silver Nanobars and Nanorice // Nano Lett. - 2007, - Vol. 7, - P. 1032-1036; Biosensors and Bioelectronics. - 2015, - P. 17-12], что позволяет их использовать для решения некоторых биомедицинских задач [M.-F. Tsai, S.-H. G. Chang, F.-Y. Cheng, et al. Au Nanorod Design as Light-Absorber in the First and Second Biological Near-Infrared Windows for in Vivo Photothermal Therapy // ACS Nano. - 2013, - Vol. 7, - № 6, - P. 5330-5342].
Специфическими свойствами обладают также наноструктуры из полимерных материалов. Полимерные удлинённые мицеллы из ПЭГ-поликапролактона дольше циркулируют в кровеносной системе и эффективнее накапливаются в опухолевой ткани по сравнению со своими сферическими аналогами [Y. A. N. Geng, P. Dalhaimer, S. Cai, et al. Shape effects of filaments versus spherical particles in flow and drug delivery // Nat. Nanotechnol. - 2007, - Vol. 2, - № 4, - P. 249-255]. Выявлены особенности биораспределения in vivo наностержней из полистирола по сравнению с наносферами [P. Kolhar, A. C. Anselmo, et al. Using shape effects to target antibody-coated nanoparticles to lung and brain endothelium // Proc. Natl. Acad. Sci., - 2013, - Vol. 110, - № 26, - P. 10753-10758]. Данные частицы обладали сниженной адгезией к эндотелию сосудов и преимущественно накапливались в мозге и лёгких, что потенциально позволяет осуществить доставку лекарств в эти органы.
В настоящее время также активно продолжаются разработки и исследования новых частиц из оксидов железа [R. G. D. Andrade, S. R. S. Veloso, E. M. S. Castanheira. Shape Anisotropic Iron Oxide-Based Magnetic Nanoparticles: Synthesis and Biomedical Applications // International Journal of Molecular Sciences. - 2020. - Vol. 21, - № 7, - P. 455; M. Mahdavi, M. Ahmad, M. Haron, et al. Synthesis, Surface Modification and Characterisation of Biocompatible Magnetic Iron Oxide Nanoparticles for Biomedical Applications // Molecules, - 2013. - Vol., - № 18, - P. 7533-7548; J. Mohapatra, A. Mitra, H. Tyagi, et al. Iron oxide nanorods as high-performance magnetic resonance imaging contrast agents // Nanoscale. - 2015, - Vol. 7, - № 20, - P. 9174-9184] или структур на их основе [C. Oka, K. Ushimaru, N. Horiishi, et al. Core-shell composite particles composed of biodegradable polymer particles and magnetic iron oxide nanoparticles for targeted drug delivery // Journal of Magnetism and Magnetic Materials, - 2015, - Vol. 381, - P. 278-284; R. Martínez-González, J. Estelrich, M. Busquets. Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI // International Journal of Molecular Sciences. - 2016. - Vol. 17, - № 8, - P. 1209; D. Zhi, T. Yang, J. Yang, et al. Targeting Strategies for Super Paramagnetic Iron Oxide Nanoparticles in Cancer Therapy // Acta Biomaterialia. - 2019]. Так упорядоченно ориентированные наностержни магнетита демонстрируют высокую спиновую поляризацию при комнатной температуре и тем самым имеют хорошую перспективу в разработке сенсоров спинтроники нового поколения [A. Mitra, J. Mohapatra, H. Sharma, S. S. Meena. Controlled synthesis and enhanced tunnelling magnetoresistance in oriented Fe3O4 nanorod assemblies // Journal of Physics D: Applied Physics. - 2018, - Vol. 51, - № 8]. Авторы работы [J. Mohapatra, A. Mitra, H. Tyagi, D. Bahadur and M. Aslam. Iron oxide nanorods as high-performance magnetic resonance imaging contrast agents // Nanoscale. - 2015, - Vol. 7, - № 20, - P. 9174-9184] показали, что наностержни оксида железа дают более эффективный контраст в МРТ по сравнению с частицами сферической формы. J. Mohapatra, et. al. объясняют полученный результат сильным локальным магнитным полем, которое создают вокруг себя наностержни. Более высокий SAR (specific absorption rate) по сравнению со сферами продемонстрировали наностержни Fe3O4 при проведении магнитной гипертермии [R. Das, J. Alonso and P. Z. Nemati, et al. Tunable High Aspect Ratio Iron Oxide Nanorods for Enhanced Hyperthermia // J. Phys. Chem. C. - 2016, - Vol. 120, - № 18, - P. 10086-10093].
Магнитные наночастицы оксида железа сферической формы наиболее распространены и хорошо изучены, так как методы их синтеза являются более простыми и преимущественно одностадийными. Структуры более сложной формы (например, стержни) получают в несколько этапов при более сложных условиях и, как правило, с применением более дорогих органических прекурсоров. В связи с этим известно немного литературных источников с описанием методов синтеза стержней оксида железа. Для синтеза стержневых частиц Fe3O4 в основном используют два подхода.
Первый подход представляет собой одностадийный метод термального разложения железосодержащего прекурсора Fe(CO)5 в высококипящем органическом растворителе в присутствии восстановителя гексадециламина [R. Das, J. Alonso, Z. Nemati Porshokouh, et al. Tunable High Aspect Ratio Iron Oxide Nanorods for Enhanced Hyperthermia // The Journal of Physical Chemistry C. - 2016, - Vol. 120, - № 18, - P. 10086-10093; H. Sun, B. Chen, X. Jiao, Z. Jiang, Z. Qin and D. Chen. Solvothermal synthesis of tunable electroactive magnetite nanorods by controlling the side reaction // J. Phys. Chem. C. - 2012, - Vol. 116, - № 9, - P. 5476-5481]. Размеры формирующихся стержней можно контролировать путём варьирования времени синтеза и количества олеиновой кислоты, которая выступает в качестве стабилизатора роста. Получаемые стержни оксида железа являются гидрофобными за счет покрытия из олеиновой кислоты, поэтому для дальнейшего применения в биологических исследованиях частицы необходимо переводить в водную фазу, что требует дополнительной модификации их поверхности. Кроме того, одностадийный метод синтеза стержневых частиц необходимо проводить при высокой температуре реакционной среды с помощью неполярных, высококипящих, органических растворителей, что дополнительно требует создания инертной атмосферы из аргона или азота для предотвращения процессов окисления. Некоторые реактивы для этого метода синтеза являются токсичными (например, пентакарбонил железа, гексадециламин) и относительно дорогими. Ещё одна проблема синтеза частиц стержневой формы заключается в кубической кристаллической решётке оксида железа. Достаточно трудно контролировать рост определённых кристаллографических плоскостей в процессе формирования стержней магнетита. Для решения этой проблемы, как правило, используют ионогенные поверхностно-активные соединения (ПАВ).
Второй подход к получению стержневых частиц магнетита состоит из 2 этапов: сначала формируют стержни акагенита β-FeOOH путём гидролиза соли Fe3+, а затем проводят процедуру восстановления до образования фазы Fe3O4 [G. Kasparis, A. S. Erdocio, et al. Synthesis of size-tuneable β-FeOOH nanoellipsoids and a study of their morphological and compositional changes by reduction // CrystEngComm. - 2019. - Vol. 21, - № 8, - P. 1293-1301]. Следует отметить, что для формирования стержней акагенита β-FeOOH не нужны какие-либо ПАВ [C. Blanco-Andujar, D. Ortega, Q. A. Pankhurst and N. T. K. Thanh. Elucidating the morphological and structural evolution of iron oxide nanoparticles formed by sodium carbonate in aqueous medium // J. Mater. Chem. - 2012, - Vol. 22, - № 25, - P. 124; Mozo S. Lentijo, E. Zuddas, A. Casu and A. Falqui. Synthesizing Iron Oxide Nanostructures: The Polyethylenenemine (PEI) Role // Crystals. - 2017, - Vol. 7, - № 1, - P. 22]. Так в работах [Mozo S. Lentijo, E. Zuddas, A. Casu and A. Falqui. Synthesizing Iron Oxide Nanostructures: The Polyethylenenemine (PEI) Role // Crystals. - 2017, - Vol. 7, - № 1, - P. 22; A. Casu, D. Loche, S. Lentijo-Mozo. Surface Compositional Change of Iron Oxide Porous Nanorods: A Route for Tuning their Magnetic Properties // Molecules. - 2020. - Vol. 25, - № 5] сообщается, что после восстановления олеиламином изменяются морфологические характеристики наностержней, и предпринимаются усилия по сохранению морфологии частиц в процессе восстановления. Высокотемпературный отжиг позволяет перевести частицы из одной фазы в другую, однако такая обработка приводит к спеканию/агрегации наночастиц и потере необходимых свойств [C. Lui, X. Wu, T. Klemmer, N. Shukla and D. Weller. Reduction of sintering during annealing of ePt nanoparticles coated with iron oxide // Chem. Mater. - 2005, - Vol. 17, - № 6, - P. 620-625]. Фазовое превращение стержней β-FeOOH в оксид железа с сохранением размеров достигается при использовании в качестве восстановителя диэтиленгликоля и термальной обработки в течение 2 часов при 220 °C [W. Xu, M. Wang, Z. Li, et al. Chemical Transformation of Colloidal Nanostructures with Morphological Preservation by Surface-Protection with Capping Ligands // Nano Letters. - 2017, - № 17, - Vol. 4, - P. 2713-2718]. При этом частицы приобретают высокопористую структуру и небольшую намагниченность (не более 50 emu/g). Авторы работы [I. Milosevic, Н. Jouni, С. David, F. Warmont, D. Bonnin and L. Motte // Journal of Physical Chemistry C. - 2011, - Vol. 115, - P. 18999-19004] использовали в качестве восстановителя гидразин и микроволновую обработку для получения наностержней магнетита. Полученные наночастицы дополнительно покрывали дофамином, однако они обладали невысокой стабильностью в водных средах и быстро агрегировали.
Наиболее близким к предлагаемому способу является метод синтеза наностержней магнетита из акагенита при использовании в качестве восстановителя гидразин или гидразина гидрохлорид [Способ получения стержневых наночастиц магнетита, RU2 686931C1, 06.05.2019]. Данный синтез происходит в два этапа. На первом этапе путём гидролиза соли железа (III) при 80 °C в течение 2 часов получают стержни β-FeOOH, размер которых регулируется добавлением в реакционную среду полиэтиленимина (25 кДа). На втором этапе частицы акагенита в присутствии гидразина или гидразина гидрохлорида подвергают микроволновой обработке (200 Вт) при 100°С в течение 30 с. Полученные наностержни магнетита без покрытия промывают деионизованной водой и диспергируют в ней же. Частицы сохраняли свою стабильность в воде на протяжении 2 недель. Авторы патента предлагают полученные наностержни магнетита для биомедицинских применений, однако, они не представляют результаты исследования стабильности частиц в биологических средах (или средах, имитирующих биологические), а также нет данных по их токсичности. К недостаткам данного метода можно отнести малую намагниченность насыщения (13,2 emu/g) получаемых стержней Fe3O4, использование высокотоксичного гидразина и специального микроволнового реактора. Магнитные частицы с небольшой намагниченностью, как правило, обладают меньшим магнитокалорическим эффектом, хуже контрастируют в МРТ, и такие частицы становятся не пригодными для магнитной адресной доставки лекарств.
Целью предлагаемого способа является разработка экологичного метода синтеза биосовместимых наностержней Fe3O4 с высокой магнитной восприимчивостью.
Техническим результатом является получение нетоксичных стержневых частиц магнетита, обладающих высокими монодисперсностью (30±8/700±90 нм, 18±4/120±35 нм, 8±3/35±10 нм) и намагниченностью (80 emu/g).
Технический результат достигается тем, что формируют наностержни β-FeOOH путём гидролиза 20 мл 0,55 M водного раствора FeCl3 в автоклаве при 120 °C в течение 3 часов; далее наностержни β-FeOOH осаждают на центрифуге при 8000 g в течение 10 мин, осадки промывают деионизованной водой и этанолом, после чего в вакуумном шкафу высушивают при 70 °C в течение одних суток; очищенные высушенные наностержни β-FeOOH с применением ультразвуковой ванны (100 Вт, 15 мин) диспергируют в 20 мл глицерина, в котором предварительно растворяют 0,2 г полиэтиленгликоля (PEG, 4000 Да); вязкую суспензию частиц β-FeOOH в глицерине помещают в автоклав и подвергают гидротермальной обработке в течение 2 часов при температуре 200 °C; после процедуры восстановления суспензия меняет цвет с оранжевого на чёрный, что свидетельствует об образовании частиц с фазой магнетита Fe3O4; полученные наностержни магнетита собирают из раствора постоянным магнитом и промывают деионизованной водой и этанолом; к очищенным частицам приливают 20 мл раствора полиакрилата натрия (PAA, 5100 Да) с концентрацией 12 мг/мл, суспензию инкубируют в течение суток при постоянном перемешивании на магнитной мешалке; наностержни магнетита осаждают магнитом, промывают деионизованной водой от неадсорбированного полимера и диспергируют в 0,9% растворе NaCl, при этом водный раствор FeCl3 может содержать 100 мг или 500 мг поливинипирролидона (PVP, 40 кДа).
Данные характеристики наностержней удалось получить благодаря применению глицерина в качестве восстанавливающего агента и полиэтиленгликоля, выполняющего роль стабилизатора роста и формы частиц, а также за счёт создания мягких условий (гидротермальная обработка в течение заданного времени) для реакции. Дополнительное покрытие из нетоксичного полимера полиакрилата натрия повысило стабильность и биосовместимость наностержней Fe3O4. Полулетальная доза (LD50) для белых мышей линии Balb/c полученных магнитных наночастиц составила 720 мг/кг при их внутривенном введении, что позволяет отнести частицы к малотоксичным соединениям по классификации Березовской [I.V. Berezovskaya. Classification of chemicals according to the parameters of acute toxicity with parenteral routes of administration // Pharm. Chem. J. - 2003, - Vol. 37, - P. 139-141] и согласно ГОСТу 12.1.007-76. Кроме того, использованные в разработанном методе реактивы (FeCl3, поливинилпирролидон, глицерин, полиэтиленгликоль, полиакрилат натрия) являются нетоксичными (в отличие от Fe(CO)5, гидразина, полиэтиленимина, диэтиленгликоля, олеиламина часто применяемых в других методах синтеза), что позволило сделать синтез более экологически безопасным.
Используемые в синтезе реактивы являются нетоксичными, недорогими и коммерчески доступными. Из оборудования для синтеза необходимы вакуумный шкаф, автоклав, ультразвуковая ванна, магнитная мешалка и центрифуга.
Наностержни акагенита со средней длиной 700 нм (образец 1) синтезировали в отсутствии поливинилпирролидона в растворе FeCl3. Для получения наностержней акагенита с длиной 120 нм (образец 2) предварительно в водный раствор FeCl3 добавляли 100 мг поливинипирролидона (PVP, 40 кДа), а для синтеза частиц с длиной 35 нм (образец 3) - 500 мг PVP.
Электрокинетический потенциал (ζ-потенциал) полученных наностержней магнетита, покрытых полиакрилатом, составил в диапазоне от -61 до -79 мВ при pH = 7. Основные характеристики наностержней магнетита, полученных по разработанной методике, приведены в таблице 1.
Таблица 1. Характеристики наностержней Fe3O4, полученных при разных количествах поливинилпирролидона (PVP)
Краткое описание чертежей.
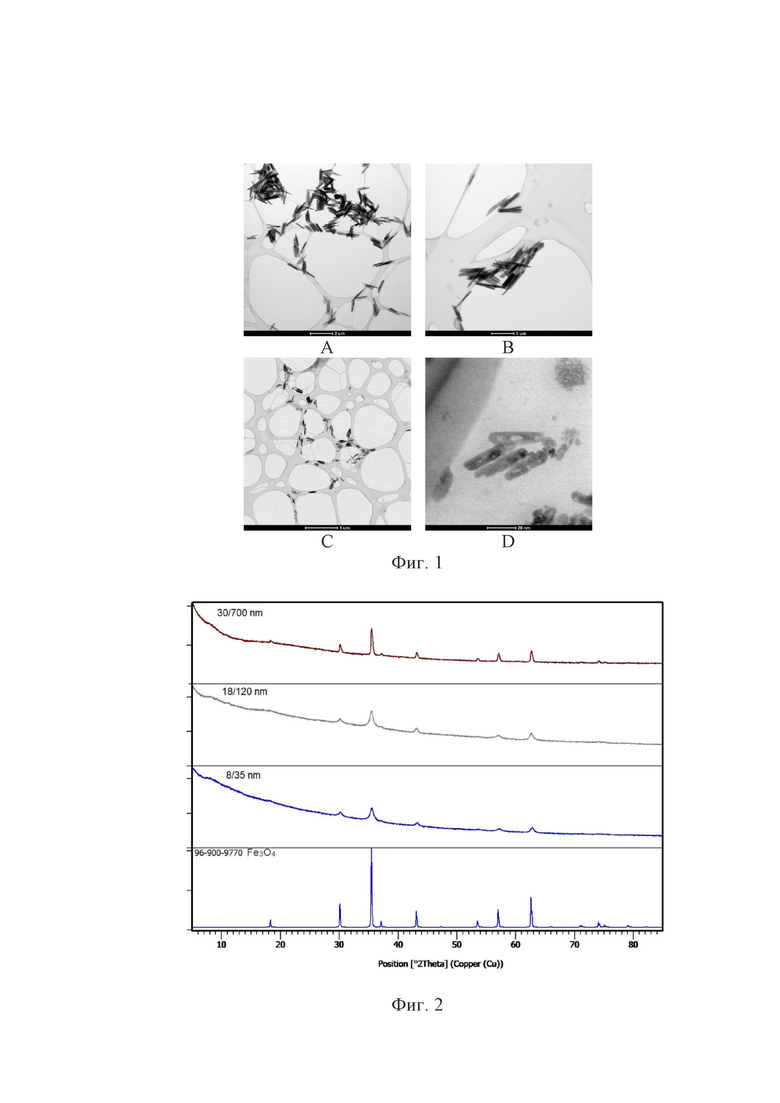
На фиг. 1 представлены изображения, полученные методом просвечивающей электронной микроскопии (ПЭМ), наностержней магнетита, которые синтезировали при разных количествах поливинилпирролидона:
А - ПЭМ-изображения наностержней β-FeOOH (без PVP),
B - D - ПЭМ-изображения наностержней Fe3O4, полученных из β-FeOOH при разных количествах PVP.
На фиг. 2 приведены рентгеновские дифрактограммы наностержней магнетита.
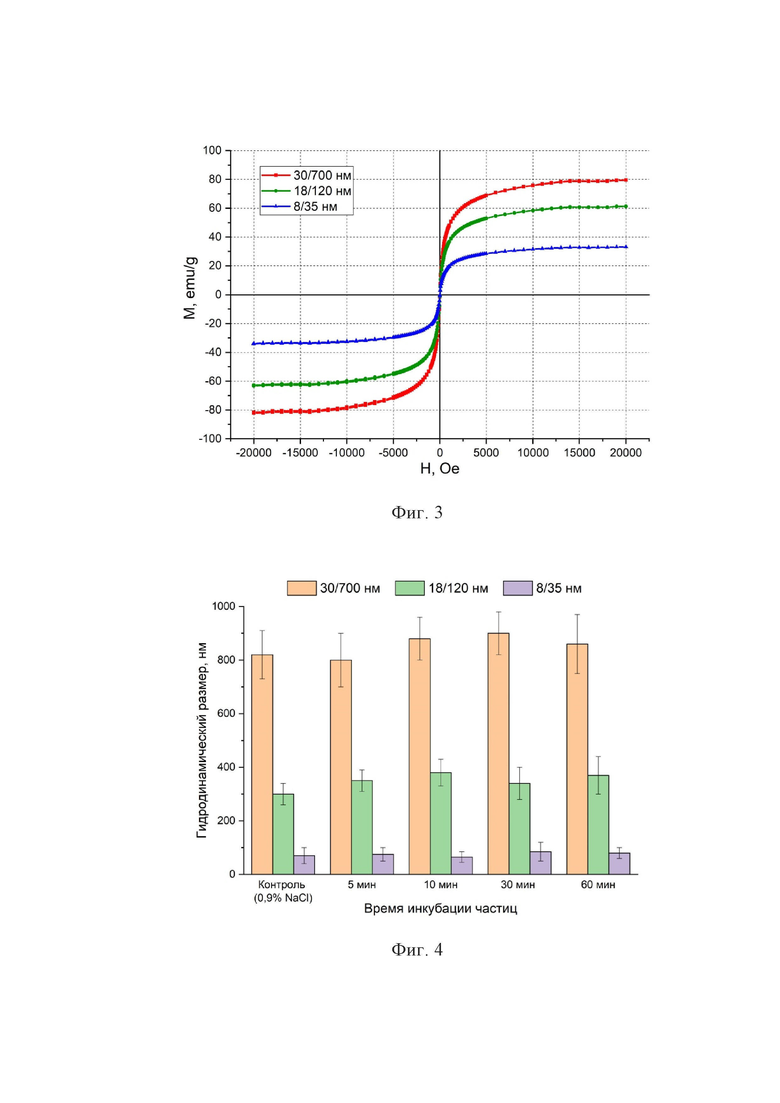
На фиг. 3 представлены кривые намагничивания полученных наностержней магнетита.
На фиг. 4 приведены результаты исследования стабильности полученных наностержней магнетита в среде, имитирующей плазму крови.
Результаты проведённого исследования морфологических характеристик методом просвечивающей электронной микроскопии показали, что увеличение количества поливинилпирролидона в растворе FeCl3 приводит к уменьшению образующихся стержневых частиц акагенита β-FeOOH (фиг. 1). После процедуры восстановления глицерином в присутствии полиэтиленгликоля частицы приобретают несколько пористую структуру без изменения формы и размеров, при этом наибольшая пористость отмечается для наностержней меньшего размера. Следует отметить, что пористость может обеспечить большую загрузку целевого вещества в частицы.
Из рентгеновских дифрактограмм (фиг. 2) можно увидеть, что полученные разного размера наностержни характеризуются основной фазой магнетита с кубической структурой обращённой шпинели (пространственная группа Fd3m). Таким образом, подтверждается, что глицерин, как и некоторые другие полиолы, обладает высоким восстановительным потенциалом и способствует образованию фазы Fe3O4. Полиэтиленимин, обычно используемый для контроля роста стержней β-FeOOH, за счёт множества аминогрупп достаточно сильно координируется ионами Fe3+ на поверхности акагенита и мешает процессу восстановления [G. Kasparis, A. S. Erdocio, et al. Synthesis of size-tuneable β-FeOOH nanoellipsoids and a study of their morphological and compositional changes by reduction // CrystEngComm. - 2019. - Vol. 21, - № 8, - P. 1293-1301]. Поливинилпирролидон, применяемый в разработанном методе для регуляции роста стержней, не повлиял на эффективность восстановления Fe3+ до Fe2+ в частицах акагенита и на образование фазы Fe3O4.
Несмотря на однофазность всех полученных наностержней, исследование магнитных свойств показало, что частицы большего размера обладают более высокой намагниченностью насыщения, магнитной восприимчивостью (фиг. 3).
В таблице 2 представлены магнитные характеристики наностержней магнетита.
Таблица 2. Магнитные характеристики полученных наностержней магнетита (частицы фиксированы в агарозном геле)
Результаты исследования стабильности полученных частиц методом динамического рассеяния света продемонстрировали высокую стабильность полученных частиц в среде, имитирующей плазму крови (раствор альбумина с концентрацией 55 г/л в фосфатно-солевом буфере с pH = 7,4) (фиг. 4). В течение одного часа инкубации в среде, имитирующей плазму крови, все образцы сохраняли свои гидродинамические размеры.
Основной заявляемой областью применения наночастиц, синтезированных по разработанному методу, является биомедицина, в связи с этим было проведено исследование острой токсичности наностержней магнетита со средним размером 30±8/700±90 нм на белых лабораторных мышах линии Balb/c. Эксперимент на животных проводился в соответствии с правилами работы с животными, сформулированными Директивой 2010/63/EU Европейского Парламента и Совета Европейского Союза о защите животных, используемых в научных целях, и были одобрены Европейским Союзом. Локальный комитет по этике при Медицинском институте Национального исследовательского Мордовского государственного университета, дата утверждения: 15 июня 2023 г., код одобрения: 115. Для данного эксперимента было сформировано 10 групп мышей в возрасте 45-50 дней (по 6 мышей в каждой группе). Наностержни магнетита, покрытые полиакрилатом, разводили в 0,9 % растворе NaCl и вводили в хвостовую вену однократно в возрастающих дозах 50, 100, 200, 400, 500, 750, 1000, 1250, 1500, 1750 мг/кг. Выживаемость и поведение животных регистрировали ежедневно. Мертвые животные были препарированы и визуально исследованы. За выжившими животными наблюдали в течение 30 дней, а затем подвергли эвтаназии. Результаты исследования острой токсичности представлены в таблице 3 и позволяют отнести полученные наностержни магнетита к малотоксичным соединениям.
Таблица 3. Параметры острой токсичности наностержней магнетита, покрытых полиакрилатом натрия
При макроскопической оценке органов брюшной полости было замечено, что печень мышей, получавших внутривенно частицы в дозе 1000 мг/кг и больше, имела более тёмный оттенок по сравнению с интактной печенью мышей из группы сравнения. Наблюдаемый эффект может свидетельствовать о преимущественном накоплении частиц в этом органе. На разрезе органов брюшной полости видимых макроскопических изменений не отмечалось. Органы грудной полости (сердце, легкие) тоже были без видимой патологии.
Данный способ может быть применен в области биомедицины и фармакологии в качестве диагностического и терапевтического средства.
Таким образом, использование поливинилпирролидона как стабилизатора роста частиц и глицерина в качестве восстановителя позволило повысить экологичность метода синтеза стержней Fe3O4, увеличить образование фазы магнетита и тем самым оптимизировать магнитные свойства частиц.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СТЕРЖНЕВЫХ НАНОЧАСТИЦ МАГНЕТИТА | 2017 |
|
RU2686931C1 |
| ТРАНСДЕРМАЛЬНЫЙ ПЛАСТЫРЬ | 2019 |
|
RU2705896C1 |
| Мягкая лекарственная форма для лечения онкологических заболеваний | 2020 |
|
RU2743342C1 |
| Способ получения микросфер оксида железа FeO | 2021 |
|
RU2762433C1 |
| Нанокомпозитный магнитный материал на основе поли-3-амино-7-метиламино-2-метилфеназина и наночастиц FeO, закрепленных на одностенных углеродных нанотрубках, и способ его получения | 2016 |
|
RU2635254C2 |
| Способ получения стеклообразных магнитных композиционных материалов (СМКМ) с двумя магнитными подсистемами (FeO/MnO) | 2023 |
|
RU2810343C1 |
| НАНОМАТЕРИАЛ ДЛЯ НАПРАВЛЕННОЙ ДОСТАВКИ ПРОТИВООПУХОЛЕВЫХ ПРЕПАРАТОВ И ПРОТИВООПУХОЛЕВЫЙ ПРЕПАРАТ НА ЕГО ОСНОВЕ | 2016 |
|
RU2610170C1 |
| Магнитный аффинный сорбент для выделения рекомбинантных белков | 2022 |
|
RU2794889C1 |
| СПОСОБ СТИМУЛИРОВАНИЯ ПРОРАСТАНИЯ РАСТЕНИЙ НАНОЧАСТИЦАМИ ОКСИДА ЦЕРИЯ С ВЫСОКОЙ АНТИРАДИКАЛЬНОЙ И БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2701950C1 |
| Способы комбинированной терапии злокачественных новообразований с использованием наночастиц оксида железа | 2023 |
|
RU2816227C1 |
Изобретение относится к получению наноструктур, которые могут быть использованы в медицине. В процессе синтеза наночастиц магнетита стержневой формы сначала формируют наностержни β-FeOOH путём гидролиза водного раствора FeCl3 в автоклаве при 120 °C в течение 3 ч. Наностержни β-FeOOH осаждают на центрифуге, осадки промывают деионизованной водой и этанолом, после чего высушивают в вакуумном шкафу. Очищенные высушенные наностержни β-FeOOH диспергируют с применением ультразвуковой ванны в 20 мл глицерина в течение 15 мин, в котором предварительно растворяют 0,2 г полиэтиленгликоля (PEG) с молекулярной массой 4000 Да. Полученную вязкую суспензию помещают в автоклав и подвергают гидротермальной обработке в течение 2 ч при температуре 200 °C. Полученные наностержни магнетита Fe3O4 собирают из раствора постоянным магнитом и промывают деионизованной водой и этанолом. К очищенным частицам приливают 20 мл раствора полиакрилата натрия (PAA) с молекулярной массой 5100 Да с концентрацией 12 мг/мл, суспензию инкубируют в течение суток при постоянном перемешивании на магнитной мешалке. Наностержни магнетита осаждают магнитом, промывают деионизованной водой от неадсорбированного полимера и диспергируют в 0,9% растворе NaCl. Изобретение позволяет повысить экологичность синтеза биосовместимых наностержней Fe3O4, обладающих высокой монодисперсностью и намагниченностью. 2 з.п. ф-лы, 4 ил., 3 табл.
1. Способ синтеза наночастиц магнетита стержневой формы, состоящий из этапов, отличающийся тем, что формируют наностержни β-FeOOH путём гидролиза 20 мл 0,55 M водного раствора FeCl3 в автоклаве при 120 °C в течение 3 ч; далее наностержни β-FeOOH осаждают на центрифуге при 8000 g в течение 10 мин, осадки промывают деионизованной водой и этанолом, после чего в вакуумном шкафу высушивают при 70 °C в течение одних суток; очищенные высушенные наностержни β-FeOOH с применением ультразвуковой ванны с мощностью 100 Вт в течение 15 мин диспергируют в 20 мл глицерина, в котором предварительно растворяют 0,2 г полиэтиленгликоля (PEG) с молекулярной массой 4000 Да; вязкую суспензию частиц β-FeOOH в глицерине помещают в автоклав и подвергают гидротермальной обработке в течение 2 ч при температуре 200 °C; после процедуры восстановления суспензия меняет цвет с оранжевого на чёрный, что свидетельствует об образовании частиц с фазой магнетита Fe3O4; полученные наностержни магнетита собирают из раствора постоянным магнитом и промывают деионизованной водой и этанолом; к очищенным частицам приливают 20 мл раствора полиакрилата натрия (PAA) с молекулярной массой 5100 Да с концентрацией 12 мг/мл, суспензию инкубируют в течение суток при постоянном перемешивании на магнитной мешалке; наностержни магнетита осаждают магнитом, промывают деионизованной водой от неадсорбированного полимера и диспергируют в 0,9% растворе NaCl.
2. Способ по п. 1, отличающийся тем, что водный раствор FeCl3 содержит 100 мг поливинипирролидона (PVP) с молекулярной массой 40 кДа.
3. Способ по п. 1, отличающийся тем, что водный раствор FeCl3 содержит 500 мг поливинипирролидона (PVP) с молекулярной массой 40 кДа.
| СПОСОБ ПОЛУЧЕНИЯ СТЕРЖНЕВЫХ НАНОЧАСТИЦ МАГНЕТИТА | 2017 |
|
RU2686931C1 |
| НАНОКОМПОЗИТНЫЙ ДИСПЕРСНЫЙ МАГНИТНЫЙ МАТЕРИАЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2426188C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ МАГНИТНЫЕ ЧАСТИЦЫ ОКСИДА ЖЕЛЕЗА, И ПРИМЕНЕНИЕ УКАЗАННЫХ КОМПОЗИЦИЙ ПРИ СПОСОБАХ ПОЛУЧЕНИЯ ИЗОБРАЖЕНИЙ | 2006 |
|
RU2417104C2 |
| CN 114843101 A, 02.08.2022 | |||
| CN 110436529 A, 12.11.2019 | |||
| XU W | |||
| et al | |||
| Chemical Transformation of Colloidal Nanostructures with Morphological Preservation by Surface-Protection with Capping Ligands, Nano Letters, 2017, N 17, pp | |||
| Воздушная турбина | 1924 |
|
SU2713A1 |
Авторы
Даты
2024-08-07—Публикация
2023-12-11—Подача