Изобретение относится к медицине, а именно к экспериментальной онкологии, и может быть использовано для лечения злокачественной меланомы.
Злокачественная меланома кожи является наиболее агрессивной формой рака кожи и причиной более чем 80% случаев смертности у пациентов с этим видом онкологической патологии. С одной стороны, наружная локализация опухоли, возможность радикального лечения ранних стадий, высокая иммуногенность позволяют рассчитывать на успех в лечении. С другой – высокая частота рецидивов, непредсказуемость клинического течения заболевания и отсутствие эффективной системной терапии делают пессимистичными прогнозы при возникновении прогрессирования болезни. Несмотря на достижения последних десятилетий, результат применения существующих химиотерапевтических препаратов для лечения злокачественной меланомы остается неудовлетворительным, поэтому лечение меланомы кожи остается крайне сложной проблемой.
По данным многочисленных исследований, метастатическая меланома является одним из наиболее мутантных, гетерогенных и летальных видов рака. Наиболее заметные мутации в меланоме затрагивают серин/треониновую киназу BRAF (50%), малую ГТФазу NRAS (25%) или опухолевый супрессор и негативный регулятор RAS, нейротромин 1 (NF1) (14%), что приводит к повышению её пролиферации и выживаемости (Ostrowski S.M., Fisher D.E. Biology of Melanoma. Hematol Oncol Clin North Am. 2021. 35(1):29-56).
До недавнего времени варианты лечения пациентов с меланомой были ограничены химиотерапевтическими препаратами, которые представлены несколькими химическими группами: алкилирующие агенты, такие как дакарбазин и темозоломид, антимикротубулярные агенты, такие как винка-алкалоиды (винбластин, виндезин) или таксаны (паклитаксел), и платиновые аналоги, такие как цисплатин и карбоплатин, которые используются в монотерапии или в комбинации в основном у пациентов с поздними стадиями меланомы (Teimouri F., Nikfar S., Abdollahi M. Efficacy and side effects of dacarbazine in comparison with temozolomide in the treatment of malignant melanoma: a meta-analysis consisting of 1314 patients. Melanoma Res. 2013. 23(5):381-9).
Однако такое лечение отличается общей низкой эффективностью, ограниченной частотой ответа у пациентов и тяжелыми побочными эффектами.
В последние несколько лет наблюдался значительный прогресс в лечении больных меланомой благодаря внедрению таргетной и иммунотерапии.
Известно, что для терапии поздних стадий меланомы успешно используются высокие дозы цитокинов, таких как IFN-α и IL-2 (Danciu C., Soica C, Antal D. Natural Compounds in the Chemoprevention of Malignant Melanoma. Anticancer Agents Med Chem. 2018. 18(5):631-644).
Однако в исследованиях и в клинической практике была отмечена их высокая токсичность.
Недавно было показано, что ингибитор цитотоксического Т-лимфоцит-ассоциированного антигена 4 (CTLA-4) (ипилимумаб) и ингибиторы белка программируемой гибели клеток 1 (PD-1) (пембролизумаб и ниволумаб) повышают общую частоту ответа, медиану выживаемости без прогрессирования и общую выживаемость больных меланомой (Luke J.J., Flaherty K.T., Ribas A., Long G.V. Targeted agents and immunotherapies: optimizing outcomes in melanoma. Nat. Rev. Clin. Oncol. 2017. 14(8): 463–482).
Однако, несмотря на убедительные результаты примерно у 30% пациентов с поздней стадией заболевания, большинство пациентов либо не реагируют на иммунотерапию, либо имеют тяжелые побочные эффекты, такие как желудочно-кишечная, легочная и печеночная токсичность, что требует прекращения лечения.
Выявление мутаций в серин/треонинкиназе BRAF, которые приводят к конститутивной активации пути МАРК у более 50% пациентов с меланомой, способствовало созданию таргетной терапии с использованием низкомолекулярных ингибиторов, действующих на мутировавший BRAF, в частности, к таким препаратам относятся вемурафениб и дабрафениб.
Однако, во многих исследованиях наблюдался очень вариабельный ответ на терапию ингибиторами BRAF: у одних пациентов полностью отсутствовал ответ на такое лечение, у других наблюдалось полное исчезновение меланомы. В ряде исследований было показано, что одной из причин вариабельного ответа на лечение такими препаратами является развитие лекарственной устойчивости, способствующей селекции наиболее резистентных клеток меланомы, обусловливающих рецидивирование и дальнейшее прогрессирование заболевания (Xue Z., Vis D., Bruna A. et al. MAP3K1 and MAP2K4 mutations are associated with sensitivity to MEK inhibitors in multiple cancer models.Cell Res. 2018. 28 (7): 719-729; Menzies A, Long G Systemic treatment for BRAF-mutant melanoma: where do we go next? Lancet Oncol. 2014.15(9):e371-81).
На сегодняшний день кроме вышеописанных препаратов существует и ряд экспериментальных соединений, используемых для терапии меланомы.
Известно лекарственное средство, содержащее рекомбинантные лектины омелы, для лечения злокачественной меланомы (RU 2639445 С2), содержащее рекомбинантный лектин омелы, для лечения злокачественной меланомы, рекомбинантный лектин омелы выбран из группы аминокислотных последовательностей SEQ ID № 1-12 или содержит их части или фрагменты или является их комбинацией.
Однако в доступной литературе имеются весьма противоречивые данные об омелотерапии, что делает результаты этих исследований сомнительными, требующими повторных исследований и являются недостатком.
Известен ряд исследований применения и других групп природных соединений для терапии меланомы, таких как полисахариды, выделенные из грибов и растений; флавоноиды (кемферол, кверцетин, апигенин, лютеолин, бутеин, нарингенин, изоликвиритигенин, генистеин и дайзеин); антоцианины; танины; лигнаны. Показано, что такие соединения обладают многочисленными видами активности, включая противоопухолевую, антиоксидантную, противовоспалительную, противомикробную и иммуносупрессивную активность (Danciu C., Soica C, Antal D. et al. Natural Compounds in the Chemoprevention of Malignant Melanoma. Anticancer Agents Med Chem. 2018. 18(5):631-644).
Однако недостатком упомянутых выше природных соединений является их низкая противоопухолевая эффективность. Кроме того, они используются преимущественно для профилактики заболевания.
Несмотря на значительный прогресс, достигнутый в клиническом лечении распространенной меланомы, неудачи в лечении, тяжелые побочные эффекты и врожденная, а также приобретенная резистентность ко многим видам современной терапии требуют продолжения исследований для поиска более эффективных и потенциально персонализированных вариантов лечения.
К настоящему моменту опубликовано достаточно большое количество работ, посвященных изучению влияния оксида азота (NO) на процессы ангиогенеза в злокачественных новообразованиях. В частности было показано, что экспрессия белка индуцибельной синтазы оксида азота (iNOS и nNOS) в опухолевых клетках меланомы связана с неблагоприятным прогнозом течения заболевания. Как показали многочисленные исследования на мышиных моделях меланомы in vivo и наблюдения на тканях человека, NO может способствовать образованию и пролиферации меланомы посредством взаимодействия через ингибирующие иммунные клетки, ингибирование апоптоза, стимуляции проопухолевых цитокинов, активации макрофагов, связанных с опухолью, изменения ангиогенных процессов и стимуляции образования самой меланомы. Такие эффекты NO на молекулярном уровне реализуются посредством сигнального каскада NO-sGC-cGMP-PKGs или реакций нитрозирования/денитрозирования многих важных сигнальных белков в опухолевых клетках. (Grimm E. A., Sikora A. G., Ekmekcioglu S. Molecular Pathways: Inflammation-associated nitric-oxide production as a cancer-supporting redox mechanism and a potential therapeutic target. Clin Cancer Res. 2013. 19(20):5557-63).
Известно также, что одной из причин низкой эффективности лечения меланомы является высокогликолитические фенотипы, приобретаемые клетками в условиях гипоксии. Такой пул клеток меланомы характеризуется высоким поглощением глюкозы, частично опосредованным через повышенный уровень киназы пируватдегидрогеназы (PDK). Существует четыре изоформы (PDK1-4), которые фосфорилируют пируватдегидрогеназу (PDH), тем самым инактивируя ее. Активная PDH катализирует превращение пирувата в ацетил-КоА, который, в свою очередь, вступает в цикл лимонной кислоты, активируя окислительное фосфорилирование (OXPHOS). Фосфорилированная неактивная PDH способствует клеточному перепрограммированию и приобретению клетками гликолитического фенотипа, что подтверждается рядом исследований, в которых отмечается активация PDK1 и PDK2 при меланоме человека в сравнении с доброкачественными невусами (Tiersma J. F., Evers B., Bakker B. M. Pyruvate Dehydrogenase Kinase Inhibition by Dichloroacetate in Melanoma Cells Unveils Metabolic Vulnerabilities. 2022. 23 (7): 3745).
Известно средство для таргетной терапии злокачественных новообразований (RU 2699558 С2), заключающееся в применении оригинального бифункционального соединения 1-изобутаноил-2-изопропилизотиомочевины дихлорацетата (соединение Т1084) со структурной формулой (Фиг. 1) в качестве средства таргетной терапии солидных злокачественных новообразований, оказывающего комплексное антинеобластное действие: NOS-ингибирующий фрагмент (1-изобутаноил-2-изопропилизотиомочевины), входящий в состав молекулы бифункционального соединения, оказывает антиангиогенное действие, а PDK-ингибирующий фрагмент (дихлорацетат) оказывает гипоксия-ориентированное токсическое действие на резистентный пул гипоксических клеток опухоли.
Соединение Т1084 и примеры его использования, являются прототипом предлагаемого способа лечения. В ранее проведенных исследованиях было показано, что соединение Т1084 оказывает выраженный противоопухолевый эффект на экспериментальных моделях солидной карциномы Эрлиха и рака шейки матки у мышей без развития признаков адаптации опухолей к воздействию Т1084 (Filimonova M., Shitova A., Soldatova O. et al. Combination of NOS- and PDK-Inhibitory Activity: Possible Way to Enhance Antitumor Effects. Int J Mol Sci. 2022. 23(2):730).
Однако данное соединение при лечении меланомы не применялось и исследования не проводились.
Учитывая вышеописанные молекулярные особенности меланомы, можно предположить, что одним из возможных способов её эффективного лечения является применение бифункционального соединения Т1084.
Техническим результатом предлагаемого изобретения является выраженное и стабильное подавление роста меланомы без индукции токсических эффектов при хроническом воздействии соединения Т1084.
Технический результат достигается тем, что ежедневно в течение не менее 5 дней парентерально вводят фармакологическое средство - бифункциональный NOS/PDK-ингибитор на основе 1-изобутаноил-2-изопропилизотиомочевины дихлорацетата - Т1084, при этом доза для мыши составляет 70,7 мг/кг, доза для человека, экстраполированная путем межвидовой коррекции, с учетом площади поверхности тела, составляет 5,89 мг/кг.
Изобретение поясняется подробным описанием, примерами in vitro и in vivo, формулами и таблицами, на которых изображено:
Фиг. 1 - структурная формула 1-изобутаноил-2-изопропилизотиомочевины дихлорацетата (соединение Т1084).
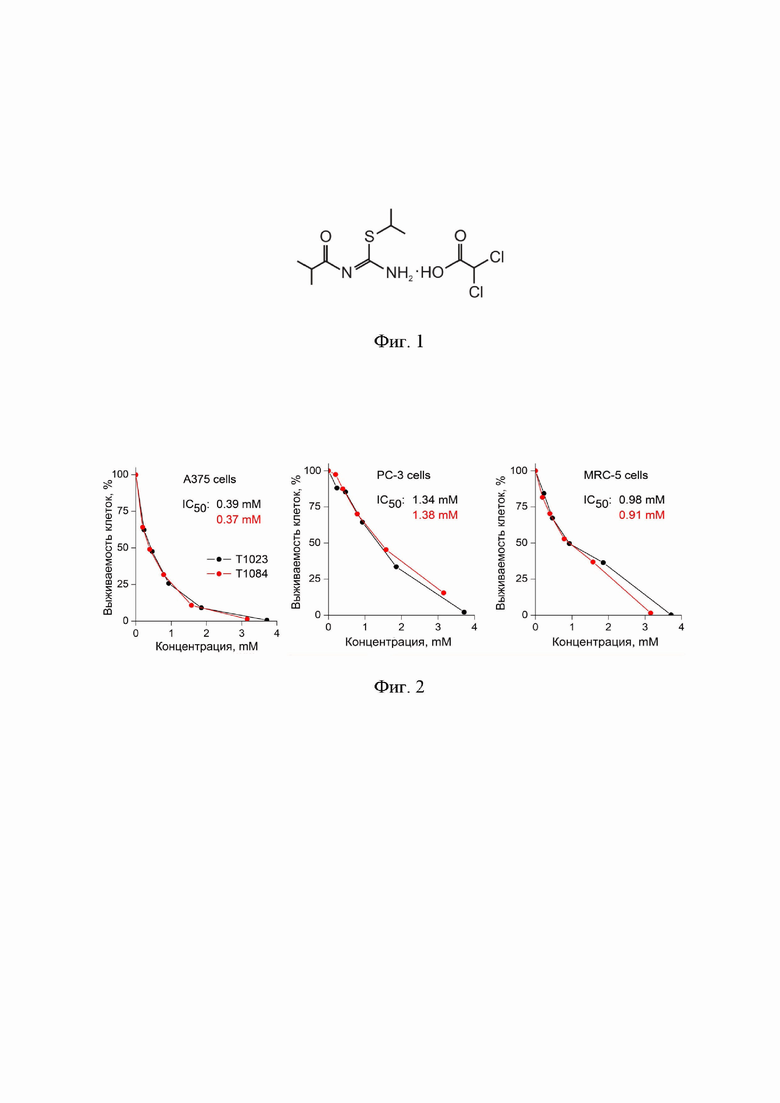
Фиг. 2 - цитотоксическая активность in vitro бифункционального соединения Т1084 и вещества-предшественника ингибитора NOS (шифр Т1023) в отношении клеток меланомы человека (A375), карциномы предстательной железы (PC-3) и нормальных фибробластов человека (MRC-5) по данным MTT-теста.
Клинические примеры
Пример 1
Результаты исследования цитотоксической активности in vitro бифункционального соединения Т1084 в сравнении с соединением-предшественником ингибитором NOS Т1023.
Цитотоксичность бифункционального соединения Т1084 и соединения-предшественника ингибитора NOS Т1023 исследовалась методом МТТ теста на культурах опухолевых клеток человека: меланомы (А375) и карциномы предстательной железы (PC-3), а также на клетках нормальных фибробластов человека (MRC-5). Клетки культивировались на среде RPMI-1640 (Sigma, США) с добавлением 10% эмбриональной телячьей сыворотки, L-глутамина, пенициллина-стрептомицина (Sigma, США) в общепринятых условиях: атмосфера 5% СО2, при температуре 37°С.
Для проведения МТТ-теста в лунки 96-луночных микротитрационных планшетов вносили 5000 клеток в 100 мкл культуральной среды. Затем клетки культивировали в СО2 инкубаторе в стандартных условиях в течение 24 часов для адгезии клеток к субстрату.
Исходные растворы (100 мг/мл) соединений, разведенных в диметилсульфоксиде (ДМСО), растворяли в среде до требуемых рабочих концентраций. Полученные растворы добавляли в лунки, содержащие культуры клеток в объёме 100 мкл. После внесения исследуемых веществ клетки культивировали в СО2 инкубаторе в стандартных условиях в течение 72 часов.
10 мг МТТ растворяли в 2 мл деионизированной воды и вносили по 20 мкл полученного раствора в каждую лунку планшета и инкубировали в СО2 инкубаторе в стандартных условиях в течение 4 часов. По истечении времени инкубации культуральную среду с исследуемыми соединениями удаляли аспирацией и в каждую лунку планшета вносили по 100 мкл ДМСО, инкубировали 5-10 минут. Количество жизнеспособных клеток в каждой лунке было пропорционально интенсивности поглощения света, которое изменяли на микропланшетном фотометре Multiskan FC при 570 нм.
В исследованиях in vitro было показано, что бифункциональное соединение Т1084 и соединение-предшественник ингибитор NOS Т1023 проявляли сходную активность в отношении различных линий нормальных и опухолевых клеток человека. Кривые выживаемости опухолевых и нормальных клеток под воздействием исследуемых соединений представлены на фиг.2.
При этом наиболее выраженное цитотоксическое действие бифункциональное соединение Т1084 проявляло по отношению к клеточной линии меланомы человека (А375) – IC50 = 0,37 мМ. Это подтверждает исходное предположение, что соединение Т1084 может быть эффективным в лечении меланомы.
Пример 2
Исследование влияния бифункционального соединения Т1084 на рост меланомы В-16 у мышей.
Сравнительное исследование противоопухолевой активности соединения T1084 и соединений предшественников (Т1023, ДХА) проведено на опухолевой модели меланомы В16 у мышей. Клетки меланомы В16 культивировали в пластиковых флаконах с поверхностью роста клеток 75 см2 (SPL Lifesciences, Корея) на среде DМЕМ с L-глутамином (ПанЭко, Россия) с добавлением 10 % эмбриональной телячьей сыворотки (ПанЭко, Россия) при температуре 37°С в атмосфере 5 % CO2. Для трансплантации опухоли животным использовали клетки меланомы В16, прошедшие от 3 до 8 пассажей культивирования. Клетки снимали с флаконов раствором 0,02% Версена (ПанЭко, Россия), отмывали в среде DМЕМ, и инокулировали мышам-самкам линии С57BL/6j подкожно в латеральную поверхность правого бедра, в количестве 1×106 клеток/мышь, в объеме 0,2 мл среды DМЕМ. После трансплантации неоплазии животных распределяли в 4 группы – контрольную и три опытных группы, по 20-21 мыши в каждой.
Воздействия на животных начинали на 8 сутки после перевивки, когда опухолевые узлы меланомы у всех особей достигали надежно измеряемого размера – 60-80 мм3. С этого дня и по 20 сутки роста опухоли мышам опытных групп ежедневно внутрибрюшинно (в/б) вводили T1023 -60.0 мг/кг, ДХА – 33.6 мг/кг и T1084 – 70.7 мг/кг в эквимолярных дозах 220 µM/kg в 0.2 мл раствора, а животным контрольной группы ежедневно в/б вводили 0.2 мл 0.9% раствора натрия хлорида. Длительность наблюдения в экспериментах составляла 21-25 суток от трансплантации опухоли.
Влияние исследуемых веществ на неоплазию оценивали по динамике роста меланомы. Для этого с 8-х суток после трансплантации у всех животных периодически измеряли калипером линейные размеры опухолевого узла и оценивали их объем в приближении  , где
, где 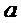 ,
,  и
и 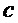 – диаметры узла в ортогональных плоскостях. Противоопухолевые эффекты оценивали путем межгруппового статистического сравнения объема неоплазии на различных сроках роста и по индексу торможения роста опухоли (ТРО), который рассчитывали по формуле
– диаметры узла в ортогональных плоскостях. Противоопухолевые эффекты оценивали путем межгруппового статистического сравнения объема неоплазии на различных сроках роста и по индексу торможения роста опухоли (ТРО), который рассчитывали по формуле 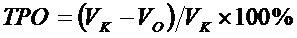 , где
, где 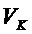 и
и  - средний объем опухолевого узла в контрольной и опытной группах.
- средний объем опухолевого узла в контрольной и опытной группах.
Результаты сравнительного исследования показали (табл. 1), что ежедневное в/б введение ДХА в эквимолярной дозе 220 μM/kg (33.6 мг/кг) оказывало слабое влияние на рост опухолевых узлов меланомы В16 – торможение роста опухоли сохранялось на уровне 20% в течение всего периода наблюдения. Соединение предшественник ингибитор NOS Т1023, вводимый в эквимолярной дозе 220 μM/kg (60 мг/кг), оказывал умеренное противоопухолевое действие, которое развивалось к 3-5-м суткам от начала применения. Анализ данных торможения роста опухолевых узлов показал, что умеренное влияние соединения предшественника Т1023 умеренно отразилось и на торможении роста опухоли – на 30-35%.
В тоже время бифункциональное соединение T1084 при ежедневном курсовом в/б введении также в дозе 220 μM/kg (70.7 мг/кг) оказывало более существенное влияние на рост меланомы В16. Противоопухолевый эффект T1084 также развивался к 3-5-м суткам от начала его применения, но был более выраженным (ТРО = 50-56%). И при дальнейшем применении T1084 не наблюдалось снижения чувствительности меланомы к действию этого соединения, и торможение роста неоплазии сохранялось на стабильном уровне (ТРО = 49-54%).
Таблица 1. Влияние Т1023, ДХА и Т1084 в эквимолярных дозах на рост меланомы В16 у самок мышей C57Bl/6j
ежедневно
ежедневно
Примечания: Показатели объема нормированы на исходный объем опухолей перед началом воздействий на 8-е сутки роста. 1, 2 и 3 – статистически достоверное различие (p < 0,05) с контрольной группой (1), с группой, получавшей ДХА (2), и с группой, получавшей Т1023 (3) по U-критерию Манна-Уитни и процедуре множественного сравнения Бонферрони-Холма. В группах n = 18-20.
Значимость такого отличия в динамике противоопухолевого действия T1084 в сравнении с действием T1023 и ДХА подтверждалась на поздних этапах высоко достоверными статистическими различиями в объеме опухолей (Табл. 2) и в индексах торможения роста у леченых животных (Табл. 1). На терминальном этапе опухолевые узлы меланомы В16 у мышей, леченых Т1084, имели значимо (в 1.8 раза) меньшую массу (Табл. 2), чем опухоли контрольных животных.
Таблица 2. Морфологические показатели узлов в экспериментальных группах на 21 сутки
Примечания: 2 и 3 – статистически достоверное различие (p < 0,05) с контрольной группой (1), с группой, получавшей ДХА (2), и с группой, получавшей Т1023 (3).
Анализ динамики веса (Табл. 3) опытных животных не выявил статистически значимых различий. Относительные массы тела животных в группах, получавших лечение, соответствовали показателям контрольных опухоленосителей. При этом развития летальных эффектов применения соединения Т1084 не наблюдалось, что свидетельствует о безопасности используемых доз и, в целом, о безопасности применения такого лечения.
Таблица 3. Динамика относительной массы тела мышей экспериментальных групп
Доказательство достижения технического результата
Данные исследований in vitro (пример 1) свидетельствовали, что меланома является одной из наиболее чувствительных опухолей человека к действию соединения Т1084.
Результаты исследований in vivo (пример 2) на перевиваемой меланоме мышей B16 показали, что соединение Т1084 значительно превосходит в противоопухолевой эффективности соединения-предшественники (Т1023, ДХА). При хроническом воздействии Т1084 в безопасных дозах 60-80 мг/кг (1/9-1/7 LD16) развивалось выраженное торможение роста меланомы (на 50-60%), и которое не ослабевало в течение всего курса воздействий. В то время как при действии Т1023 и ДХА в эквимолярных дозах торможение роста меланомы было существенно слабее (20-35%), и значительно ослабевало по ходу воздействий. При этом противоопухолевое действие Т1084 не сопровождалось какими-либо негативными токсическими эффектами.
Совокупность этих результатов свидетельствует о достижении заявленного технического результата – обеспечение выраженного и стабильного подавления роста меланомы без индукции токсических эффектов при хроническом воздействии Т1084.
Экстраполяция такого способа для лечения меланомы человека должна сопровождаться межвидовой коррекцией дозы Т1084 с учетом площади поверхности тела. В случае лечения меланомы человека соединение Т1084 должно применяться курсом не менее 5 дней в дозе 5,89 мг/кг.
Предложенный способ лечения меланомы позволит достичь выраженного и стабильного подавления роста меланомы без индукции токсических эффектов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ ТАРГЕТНОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2018 |
|
RU2699558C2 |
| КОМПЛЕКСНОЕ ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 2020 |
|
RU2751776C2 |
| Способ фармакологической защиты от ионизирующих излучений | 2017 |
|
RU2663465C1 |
| УСОВЕРШЕНСТВОВАННЫЙ СПОСОБ ПОЛУЧЕНИЯ РАДИОЗАЩИТНОГО СРЕДСТВА 1-ИЗОБУТАНОИЛ-2-ИЗОПРОПИЛИЗОТИОМОЧЕВИНЫ ГИДРОБРОМИДА | 2023 |
|
RU2806650C1 |
| РАДИОЗАЩИТНОЕ ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО | 2020 |
|
RU2733883C2 |
| Способ подавления роста меланомы В16 у лабораторных животных | 2022 |
|
RU2784443C2 |
| Способ повышения эффективности действия ионизирующих излучений на меланому | 2021 |
|
RU2774032C1 |
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ДЕЙСТВИЯ ПРОТОННОЙ ТЕРАПИИ НА СТВОЛОВЫЕ КЛЕТКИ МЕЛАНОМЫ | 2022 |
|
RU2798733C2 |
| Средство для терапии опухолей | 2019 |
|
RU2726801C1 |
| Применение полиакрилата золота в качестве ингибитора роста клеток меланомы человека | 2018 |
|
RU2708626C1 |
Изобретение относится к медицине, а именно к экспериментальной онкологии, и может быть использовано для лечения меланомы in vivo. Способ включает введение фармакологического средства - бифункционального NOS/PDK-ингибитора на основе 1-изобутаноил-2-изопропилизотиомочевины дихлорацетата Т1084 ежедневно в течение не менее 5 дней парентерально. При этом доза для мыши составляет 70,7 мг/кг, доза для человека, экстраполированная путем межвидовой коррекции, с учетом площади поверхности тела, составляет 5,89 мг/кг. Использование изобретения позволяет выраженно и стабильно подавлять рост меланомы без индукции токсических эффектов. 2 ил., 3 табл., 2 пр.
Способ лечения меланомы in vivo, характеризующийся тем, что ежедневно в течение не менее 5 дней парентерально вводят фармакологическое средство - бифункциональный NOS/PDK-ингибитор на основе 1-изобутаноил-2-изопропилизотиомочевины дихлорацетата - Т1084, при этом доза для мыши составляет 70,7 мг/кг, доза для человека, экстраполированная путем межвидовой коррекции, с учетом площади поверхности тела, составляет 5,89 мг/кг.
| СРЕДСТВО ДЛЯ ТАРГЕТНОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2018 |
|
RU2699558C2 |
| КОМПЛЕКСНОЕ ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 2020 |
|
RU2751776C2 |
| RU 94020614 A1, 27.08.1996 | |||
| ФИЛИМОНОВА М.В | |||
| и др | |||
| ПОДВИЖНАЯ ЖЕЛЕЗНОДОРОЖНАЯ КРЕСТОВИНА | 1923 |
|
SU1023A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - С | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| - EDN TJLLLD | |||
| FILIMONOVA M | |||
| et al | |||
| Combination of NOS- and PDK-Inhibitory Activity: | |||
Авторы
Даты
2024-08-07—Публикация
2023-10-26—Подача