ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[1] Настоящая заявка испрашивает приоритет по предварительной заявке на патент США № 62/848412, поданной 15 мая 2019 г., и № 62/891781, поданной 26 августа 2019 г., каждая из которых включена в данный документ посредством ссылки во всей своей полноте во всех отношениях.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[2] Терапия с применением матричной РНК (mRNA) становится все более важным подходом к лечению различных заболеваний. Терапия с применением mRNA включает введение лекарственного средства, содержащего транскрибируемую in vitro (IVT) и высокочистую матричную РНК (mRNA), пациенту, нуждающемуся в терапии, и продуцирование белка, кодируемого mRNA, в пределах организма пациента. Таким образом, существует потребность в эффективном крупномасштабном получении высокочистого продукта на основе mRNA, подходящего для терапевтического применения.
[3] Традиционно mRNA, полученную посредством транскрипции in vitro, очищают с применением коммерчески доступных хроматографических систем, например, HPLC, и/или посредством экстракции в органическую смесь (фенол:хлороформ:изоамиловый спирт) и последующего осаждения этанолом. Однако применение колоночных систем является дорогостоящим и проблематичным, и применение едких или легковоспламеняющихся растворителей при экстракции mRNA может создавать трудности с точки зрения безопасности и затрат, особенно при крупномасштабных вариантах применения.
[4] В настоящее время отсутствует безопасный и экономичный способ получения высокочистой mRNA, приемлемой для терапевтического применения.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[5] Настоящее изобретение предусматривает, среди прочего, высокоэффективный и экономичный способ очистки матричной РНК (mRNA). Настоящее изобретение частично основано на неожиданном обнаружении способа очистки mRNA с применением малых количеств летучих органических соединений или без применения летучих органических соединений, в результате которого получают mRNA, характеризующуюся высокой целостностью и высокой степенью чистоты. Таким образом, в одном аспекте настоящее изобретение предусматривает эффективный, надежный и более безопасный способ очистки mRNA, который можно применять в связанных со способом крупномасштабного получения вариантах терапевтического применения без использования каких-либо едких или легковоспламеняющихся растворителей.
[6] В некоторых аспектах настоящее изобретение предусматривает способ очистки матричной РНК (mRNA), включающий a) осаждение mRNA в суспензии, содержащей высокомолярный раствор соли и амфифильный полимер, с получением осажденной mRNA; b) захватывание осажденной mRNA; c) промывание осажденной mRNA, захваченной на стадии b), раствором для промывания с очисткой осажденной mRNA; и d) солюбилизирование осажденной mRNA, полученной на стадии c), с помощью солюбилизирующего раствора с получением композиции на основе очищенной mRNA.
[7] В некоторых вариантах осуществления композиция на основе очищенной mRNA по сути не содержит загрязняющих примесей, содержащих короткие молекулы абортивной РНК, длинные молекулы абортивной РНК, двухцепочечную РНК (dsRNA), остаточную плазмидную ДНК, остаточные ферменты транскрипции in vitro, остаточный растворитель и/или остаточную соль. В некоторых вариантах осуществления композиция на основе очищенной mRNA по сути не содержит загрязняющих примесей, содержащих короткие молекулы абортивной РНК. Например, композиция на основе очищенной mRNA содержит менее чем приблизительно 1% коротких молекул абортивной РНК. В некоторых вариантах осуществления композиция на основе очищенной mRNA по сути не содержит загрязняющих примесей, содержащих длинные молекулы абортивной РНК. Например, композиция на основе очищенной mRNA содержит не более чем приблизительно 55% длинных абортивных/расщепленных молекул, как определено посредством капиллярного гель-электрофореза (CGE). В некоторых вариантах осуществления композиция на основе очищенной mRNA по сути не содержит загрязняющих примесей, содержащих двухцепочечную РНК (dsRNA). Например, композиция на основе очищенной mRNA содержит менее чем 1% двухцепочечной РНК. В некоторых вариантах осуществления композиция на основе очищенной mRNA по сути не содержит загрязняющих примесей, содержащих остаточную плазмидную ДНК. Например, композиция на основе очищенной mRNA содержит 10 пг/мг или меньше остаточной плазмидной ДНК. В некоторых вариантах осуществления композиция на основе очищенной mRNA по сути не содержит загрязняющих примесей, содержащих остаточные ферменты транскрипции in vitro. Например, на каждые 15 мкг композиции на основе очищенной mRNA приходится менее 0,3 нг полимеразы. На каждые 15 мкг композиции на основе очищенной mRNA приходится менее 0,3 нг ферментов, применяемых при кэпировании. На каждые 15 мкг композиции на основе очищенной mRNA приходится менее 0,3 нг ферментов, применяемых при добавлении хвоста. В некоторых вариантах осуществления композиция на основе очищенной mRNA по сути не содержит загрязняющих примесей, содержащих остаточный растворитель. В некоторых вариантах осуществления композиция на основе очищенной mRNA по сути не содержит загрязняющих примесей, содержащих остаточную соль.
[8] В некоторых вариантах осуществления очищенная mRNA содержит остаточную плазмидную ДНК в количестве 10 пг/мг очищенной mRNA или меньше.
[9] В некоторых вариантах осуществления амфифильный полимер в суспензии выбран из плюроников, поливинилпирролидона, поливинилового спирта, полиэтиленгликоля (PEG), простых полиэфиров, таких как полипропиленгликоль (PPG) или полипропиленоксид, или их комбинаций. В некоторых вариантах осуществления амфифильный полимер в суспензии представляет собой плюроники. В некоторых вариантах осуществления амфифильный полимер в суспензии представляет собой поливинилпирролидон. В некоторых вариантах осуществления амфифильный полимер в суспензии представляет собой поливиниловый спирт. В некоторых вариантах осуществления амфифильный полимер в суспензии представляет собой полиэтиленгликоль (PEG). В некоторых вариантах осуществления амфифильный полимер в суспензии представляет собой простой полиэфир. В некоторых вариантах осуществления амфифильный полимер в суспензии представляет собой полипропиленгликоль (PPG). В некоторых вариантах осуществления амфифильный полимер в суспензии представляет собой полипропиленоксид.
[10] В некоторых вариантах осуществления суспензия не содержит органический растворитель. В некоторых вариантах осуществления амфифильный полимер в суспензии представляет собой PEG. В некоторых вариантах осуществления суспензия не содержит органический растворитель, и mRNA осаждают с применением полиэтиленгликоля (PEG). В некоторых вариантах осуществления суспензия содержит PEG для осаждения mRNA. В некоторых вариантах осуществления суспензия содержит PEG в концентрации, составляющей от приблизительно 10% до приблизительно 100% вес/объем.
[11] В некоторых вариантах осуществления суспензия содержит PEG в концентрации, составляющей приблизительно 50% вес/объем.
[12] В некоторых вариантах осуществления суспензия содержит PEG в конечной концентрации, составляющей менее чем 25% вес/объем. В некоторых вариантах осуществления суспензия содержит PEG в конечной концентрации, составляющей от приблизительно 5% до приблизительно 20% вес/объем. В конкретных вариантах осуществления суспензия содержит PEG в конечной концентрации, составляющей от приблизительно 10% до 15% вес/объем, например, 12% вес/объем. В некоторых вариантах осуществления молекулярная масса PEG составляет от приблизительно 2000 г/моль до приблизительно 10000 г/моль. В некоторых вариантах осуществления молекулярная масса PEG составляет от приблизительно 4000 г/моль до приблизительно 8000 г/моль. В некоторых вариантах осуществления молекулярная масса PEG составляет приблизительно 6000 г/моль (например, PEG-6000). Как показано в примерах, конечная концентрация PEG, имеющего молекулярную массу приблизительно 6000 г/моль (например, PEG-6000), в суспензии, составляющая приблизительно 12% вес/объем, обеспечивала эффективную очистку и обеспечивала получение образцов высокочистой mRNA.
[13] В некоторых вариантах осуществления суспензия не содержит органический растворитель и содержит триэтиленгликоль (TEG). В некоторых вариантах осуществления суспензия содержит TEG для осаждения mRNA. В некоторых вариантах осуществления суспензия содержит TEG в концентрации, составляющей от приблизительно 10% до приблизительно 100% вес/объем.
[14] В некоторых вариантах осуществления суспензия содержит TEG в концентрации, составляющей приблизительно 50% вес/объем.
[15] В некоторых вариантах осуществления суспензия не содержит органический растворитель и содержит монометиловый эфир триэтиленгликоля (MTEG). В некоторых вариантах осуществления суспензия содержит MTEG для осаждения mRNA. В некоторых вариантах осуществления суспензия содержит MTEG в концентрации, составляющей от приблизительно 10% до приблизительно 100% вес/объем.
[16] В некоторых вариантах осуществления суспензия содержит MTEG в концентрации, составляющей приблизительно 50% вес/объем.
[17] В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей от приблизительно 15% до приблизительно 45% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей от приблизительно 20% до приблизительно 40% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 20% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 25% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 30% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 35% вес/объем.
[18] В некоторых вариантах осуществления высокомолярный раствор соли содержит гуанидинтиоцианат (GSCN). В некоторых вариантах осуществления GSCN содержится в конечной концентрации, составляющей приблизительно 2-4 M. В некоторых вариантах осуществления GSCN содержится в конечной концентрации, составляющей 2,5-3 M. В конкретных вариантах осуществления GSCN содержится в конечной концентрации, составляющей приблизительно 2,7 M.
[19] В некоторых вариантах осуществления амфифильный полимер в растворе для промывания выбран из плюроников, поливинилпирролидона, поливинилового спирта, полиэтиленгликоля (PEG), простых полиэфиров, таких как полипропиленгликоль (PPG) или полипропиленоксид, или их комбинаций. В некоторых вариантах осуществления амфифильный полимер в растворе для промывания представляет собой плюроники. В некоторых вариантах осуществления амфифильный полимер в растворе для промывания представляет собой поливинилпирролидон. В некоторых вариантах осуществления амфифильный полимер в растворе для промывания представляет собой поливиниловый спирт. В некоторых вариантах осуществления амфифильный полимер в растворе для промывания представляет собой полиэтиленгликоль (PEG). В некоторых вариантах осуществления амфифильный полимер в растворе для промывания представляет собой простой полиэфир. В некоторых вариантах осуществления амфифильный полимер в растворе для промывания представляет собой полипропиленгликоль (PPG). В некоторых вариантах осуществления амфифильный полимер в растворе для промывания представляет собой полипропиленоксид.
[20] В некоторых вариантах осуществления раствор для промывания не содержит органический растворитель. В некоторых вариантах осуществления раствор для промывания не содержит органический растворитель и содержит полиэтиленгликоль (PEG). В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 90 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 80 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 70 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 60 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 50 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 40 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 30 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 20 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый в растворе для промывания, имеет вязкость, составляющую 10 сантистоксов или меньше. PEG, подходящий для применения в растворе для промывания, имеет вязкость, составляющую приблизительно 90 сантистоксов при 25°C, например, PEG-400. Соответственно, в конкретном варианте осуществления PEG, применяемый в растворе для промывания, представляет собой PEG-400.
[21] В некоторых вариантах осуществления раствор для промывания не содержит органический растворитель и содержит триэтиленгликоль (TEG). В некоторых вариантах осуществления раствор содержит TEG.
[22] В некоторых вариантах осуществления раствор для промывания не содержит органический растворитель и содержит монометиловый эфир триэтиленгликоля (MTEG). В некоторых вариантах осуществления раствор для промывания содержит MTEG. В некоторых вариантах осуществления MTEG содержится в растворе для промывания в концентрации, составляющей от приблизительно 90% до приблизительно 100% вес/объем. В конкретных вариантах осуществления MTEG содержится в растворе для промывания в концентрации, составляющей приблизительно 95% вес/объем.
[23] Как показано в примерах, MTEG является подходящим для применения в растворе для промывания, при этом он эффективно промывает осажденную mRNA, одновременно сохраняя ее в осажденной форме. MTEG имеет вязкость, составляющую приблизительно 7 сантистоксов при комнатной температуре. Следовательно, MTEG обеспечивает возможность высокоэффективной очистки и извлечения mRNA независимо от применяемого способа очистки (например, поточной фильтрации, глубинной фильтрации или центрифугирования).
[24] В некоторых вариантах осуществления амфифильный полимер в растворе для промывания представляет собой PEG. В конкретном варианте осуществления молекулярная масса PEG в растворе для промывания составляет от приблизительно 200 г/моль до приблизительно 600 г/моль. В конкретных вариантах осуществления PEG в растворе для промывания имеет молекулярную массу, составляющую приблизительно 400 г/моль (например, PEG-400).
[25] В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей от приблизительно 10% до приблизительно 100% вес/объем.
[26] В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей от приблизительно 50% до приблизительно 90% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей от приблизительно 90% до приблизительно 100% вес/объем.
[27] В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 90% вес/объем. В конкретных вариантах осуществления PEG в растворе для промывания имеет молекулярную массу, составляющую приблизительно 400 г/моль (например, PEG-400). В некоторых вариантах осуществления PEG в растворе для промывания имеет молекулярную массу, составляющую приблизительно 400 г/моль (например, PEG-400), и содержится в концентрации, составляющей от приблизительно 90% до приблизительно 100% вес/объем. В конкретных вариантах осуществления PEG в растворе для промывания имеет молекулярную массу, составляющую приблизительно 400 г/моль (например, PEG-400), и содержится в растворе для промывания в концентрации, составляющей приблизительно 90% вес/объем.
[28] В некоторых вариантах осуществления молекулярная масса PEG в суспензии составляет от приблизительно 200 г/моль до приблизительно 40000 г/моль. В некоторых вариантах осуществления молекулярная масса PEG в растворе для промывания составляет от приблизительно 200 г/моль до приблизительно 40000 г/моль. В некоторых вариантах осуществления молекулярная масса PEG как в суспензии, так и в растворе для промывания составляет от приблизительно 200 г/моль до приблизительно 40000 г/моль. В конкретных вариантах осуществления молекулярная масса PEG в суспензии составляет от приблизительно 2000 г/моль до приблизительно 10000 г/моль, и молекулярная масса PEG в растворе для промывания составляет от приблизительно 200 г/моль до приблизительно 600 г/моль. В конкретном варианте осуществления PEG в суспензии представляет собой PEG-6000, и PEG в растворе для промывания представляет собой PEG-400.
[29] В некоторых вариантах осуществления PEG в суспензии является линейным. В некоторых вариантах осуществления PEG в суспензии является разветвленным. В некоторых вариантах осуществления PEG в суспензии является Y-образным. В некоторых вариантах осуществления PEG в суспензии имеет многолучевую конфигурацию.
[30] В некоторых вариантах осуществления PEG в растворе для промывания является линейным. В некоторых вариантах осуществления PEG в растворе для промывания является разветвленным. В некоторых вариантах осуществления PEG в растворе для промывания является Y-образным. В некоторых вариантах осуществления PEG в растворе для промывания имеет многолучевую конфигурацию.
[31] В некоторых вариантах осуществления PEG как в суспензии, так и в растворе для промывания является линейным. В некоторых вариантах осуществления PEG как в суспензии, так и в растворе для промывания является разветвленным. В некоторых вариантах осуществления PEG как в суспензии, так и в растворе для промывания является Y-образным. В некоторых вариантах осуществления PEG как в суспензии, так и в растворе для промывания имеет многолучевую конфигурацию.
[32] В некоторых вариантах осуществления суспензия содержит PEG, выбранный из триэтиленгликоля, тетраэтиленгликоля, PEG 200, PEG 300, PEG 400, PEG 600, PEG 1000, PEG 1500, PEG 2000, PEG 3000, PEG 3350, PEG 4000, PEG 6000, PEG 8000, PEG 10000, PEG 20000, PEG 35000 и PEG 40000. В некоторых вариантах осуществления суспензия содержит триэтиленгликоль. В некоторых вариантах осуществления суспензия содержит тетраэтиленгликоль. В некоторых вариантах осуществления суспензия содержит PEG 200. В некоторых вариантах осуществления суспензия содержит PEG 300. В некоторых вариантах осуществления суспензия содержит PEG 400. В некоторых вариантах осуществления суспензия содержит PEG 600. В некоторых вариантах осуществления суспензия содержит PEG 1000. В некоторых вариантах осуществления суспензия содержит PEG 1500. В некоторых вариантах осуществления суспензия содержит PEG 2000. В некоторых вариантах осуществления суспензия содержит PEG 3000. В некоторых вариантах осуществления суспензия содержит PEG 3350. В некоторых вариантах осуществления суспензия содержит PEG 4000. В некоторых вариантах осуществления суспензия содержит PEG 6000. В некоторых вариантах осуществления суспензия содержит PEG 8000. В некоторых вариантах осуществления суспензия содержит PEG 10000. В некоторых вариантах осуществления суспензия содержит PEG 20000. В некоторых вариантах осуществления суспензия содержит PEG 35000. В некоторых вариантах осуществления суспензия содержит PEG 40000.
[33] В некоторых вариантах осуществления суспензия содержит PEG 6000.
[34] В некоторых вариантах осуществления суспензия не содержит PEG 6000.
[35] В некоторых вариантах осуществления суспензия представляет собой PEG 400.
[36] В некоторых вариантах осуществления суспензия представляет собой PEG 150.
[37] В некоторых вариантах осуществления суспензия содержит смесь одного или более полимеров PEG.
[38] В некоторых вариантах осуществления смесь полимеров PEG в суспензии содержит полимеры, имеющие различные молекулярные массы.
[39] В некоторых вариантах осуществления смесь полимеров PEG в суспензии содержит полимеры, имеющие различные геометрические конфигурации.
[40] В некоторых вариантах осуществления суспензия является водной.
[41] В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем приблизительно 50% от общего объема суспензии. Например, в некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем приблизительно 50%, 45%, 40%, 35%, 30%, 25%, 20%, 15%, 10%, 5%, 2%, 1%, 0,5%, 0,01% от общего объема суспензии. Соответственно, в некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем приблизительно 50% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 45% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 40% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 35% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 30% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 25% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 20% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 15% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 10% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 5% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 2% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 1% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 0,5% от общего объема суспензии. В некоторых вариантах осуществления суспензия содержит летучие органические соединения, составляющие менее чем 0,1% от общего объема суспензии. Многие летучие органические соединения известны из уровня техники и предусматривают, например, этанол, изопропиловый спирт и бензиловый спирт.
[42] В некоторых вариантах осуществления суспензия не содержит летучие органические соединения.
[43] В некоторых вариантах осуществления суспензия не содержит спирт.
[44] В некоторых вариантах осуществления суспензия не содержит этанол. В некоторых вариантах осуществления суспензия не содержит изопропиловый спирт. В некоторых вариантах осуществления суспензия не содержит бензиловый спирт.
[45] В некоторых вариантах осуществления суспензия содержит неводный компонент. В некоторых вариантах осуществления неводный компонент суспензии представляет собой этанол. В некоторых вариантах осуществления неводный компонент суспензии представляет собой изопропиловый спирт. В некоторых вариантах осуществления неводный компонент суспензии представляет собой бензиловый спирт.
[46] В некоторых вариантах осуществления раствор для промывания содержит PEG, выбранный из триэтиленгликоля, тетраэтиленгликоля, PEG 200, PEG 300, PEG 400, PEG 600, PEG 1000, PEG 1500, PEG 2000, PEG 3000, PEG 3350, PEG 4000, PEG 6000, PEG 8000, PEG 10000, PEG 20000, PEG 35000 и PEG 40000. В некоторых вариантах осуществления раствор для промывания содержит триэтиленгликоль. В некоторых вариантах осуществления раствор для промывания содержит тетраэтиленгликоль. В некоторых вариантах осуществления раствор для промывания содержит PEG 200. В некоторых вариантах осуществления раствор для промывания содержит PEG 300. В некоторых вариантах осуществления раствор для промывания содержит PEG 400. В некоторых вариантах осуществления раствор для промывания содержит PEG 600. В некоторых вариантах осуществления раствор для промывания содержит PEG 1000. В некоторых вариантах осуществления раствор для промывания содержит PEG 1500. В некоторых вариантах осуществления раствор для промывания содержит PEG 2000. В некоторых вариантах осуществления раствор для промывания содержит PEG 3000. В некоторых вариантах осуществления раствор для промывания содержит PEG 3350. В некоторых вариантах осуществления раствор для промывания содержит PEG 4000. В некоторых вариантах осуществления раствор для промывания содержит PEG 6000. В некоторых вариантах осуществления раствор для промывания содержит PEG 8000. В некоторых вариантах осуществления раствор для промывания содержит PEG 10000. В некоторых вариантах осуществления раствор для промывания содержит PEG 20000. В некоторых вариантах осуществления раствор для промывания содержит PEG 35000. В некоторых вариантах осуществления раствор для промывания содержит PEG 40000.
[47] В некоторых вариантах осуществления раствор для промывания содержит PEG 6000.
[48] В некоторых вариантах осуществления раствор для промывания не содержит PEG 6000.
[49] В некоторых вариантах осуществления раствор для промывания представляет собой PEG 400.
[50] В некоторых вариантах осуществления раствор для промывания содержит смесь одного или более полимеров PEG.
[51] В некоторых вариантах осуществления смесь полимеров PEG в растворе для промывания содержит полимеры, имеющие различные молекулярные массы.
[52] В некоторых вариантах осуществления смесь полимеров PEG в растворе для промывания содержит полимеры, имеющие различные геометрические конфигурации.
[53] В некоторых вариантах осуществления раствор для промывания является водным.
[54] В некоторых вариантах осуществления раствор для промывания не содержит летучие органические соединения.
[55] В некоторых вариантах осуществления раствор для промывания не содержит спирт.
[56] В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем приблизительно 50% от общего объема раствора для промывания. Например, в некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем приблизительно 50%, 45%, 40%, 35%, 30%, 25%, 20%, 15%, 10%, 5%, 2%, 1%, 0,5%, 0,01% от общего объема раствора для промывания. Соответственно, в некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем приблизительно 50% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 45% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 40% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 35% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 30% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 25% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 20% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 15% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 10% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 5% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 2% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 1% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 0,5% от общего объема раствора для промывания. В некоторых вариантах осуществления раствор для промывания содержит летучие органические соединения, составляющие менее чем 0,1% от общего объема раствора для промывания. Многие летучие органические соединения известны из уровня техники и предусматривают, например, этанол, изопропиловый спирт и бензиловый спирт.
[57] В некоторых вариантах осуществления раствор для промывания не содержит этанол. В некоторых вариантах осуществления раствор для промывания не содержит изопропиловый спирт. В некоторых вариантах осуществления раствор для промывания не содержит бензиловый спирт.
[58] В некоторых вариантах осуществления раствор для промывания содержит неводный компонент. В некоторых вариантах осуществления неводный компонент раствора для промывания представляет собой этанол. В некоторых вариантах осуществления неводный компонент раствора для промывания представляет собой изопропиловый спирт. В некоторых вариантах осуществления неводный компонент раствора для промывания представляет собой бензиловый спирт.
[59] В некоторых вариантах осуществления как суспензия, так и буфер для промывания являются водными. В некоторых вариантах осуществления как суспензия, так и буфер для промывания содержат PEG. В некоторых вариантах осуществления как суспензия, так и буфер для промывания являются водными и содержат один и тот же PEG. В некоторых вариантах осуществления как суспензия, так и буфер для промывания являются водными, и суспензия содержит первый PEG, и буфер для промывания содержит второй PEG, который отличается от первого PEG. В некоторых вариантах осуществления молекулярная масса PEG в суспензии составляет от приблизительно 2000 г/моль до приблизительно 10000 г/моль, и молекулярная масса PEG в буфере для промывания составляет приблизительно 200-600 г/моль. В некоторых вариантах осуществления молекулярная масса PEG в суспензии составляет от приблизительно 4000 г/моль до приблизительно 8000 г/моль, и молекулярная масса PEG в буфере для промывания составляет приблизительно 300-500 г/моль. В некоторых вариантах осуществления молекулярная масса PEG в суспензии составляет приблизительно 6000 г/моль (например, PEG-6000), и молекулярная масса PEG в буфере для промывания составляет приблизительно 400 г/моль (например, PEG-400).
[60] В некоторых вариантах осуществления захватывание осажденной mRNA осуществляется с помощью фильтра. В некоторых вариантах осуществления фильтр выбран из фильтра для микрофильтрации или фильтра для ультрафильтрации. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор от 0,05 мкм до 1,0 мкм. Например, в некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,05 мкм, 0,10 мкм, 0,20 мкм, 0,3 мкм, 0,4 мкм, 0,5 мкм, 0,6 мкм, 0,7 мкм, 0,8 мкм, 0,9 мкм или 1,0 мкм. Соответственно, в некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,05 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,10 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,20 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,30 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,40 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,50 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,60 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,70 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,80 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 0,90 мкм. В некоторых вариантах осуществления фильтр для микрофильтрации имеет размер пор, составляющий 1,0 мкм.
[61] В некоторых вариантах осуществления фильтр будет иметь номинальный предел молекулярной массы (NMWL), составляющий от 100 кДа до 1000 кДа. В некоторых вариантах осуществления фильтр будет иметь NMWL, составляющий от 200 кДа до 700 кДа. В некоторых вариантах осуществления фильтр будет иметь NMWL, составляющий от 200 кДа до 500 кДа. В некоторых вариантах осуществления фильтр имеет NMWL, составляющий 300 кДа. В некоторых вариантах осуществления фильтр имеет NMWL, составляющий 500 кДа.
[62] В некоторых вариантах осуществления фильтр для микрофильтрации имеет номинальный предел молекулярной массы (NMWL), составляющий более чем 1000 килодальтон (кДа). В некоторых вариантах осуществления фильтр для ультрафильтрации имеет размер пор, составляющий менее чем 0,05 мкм. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий от приблизительно 1 кДа до 1000 кДа. Например, в некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 1 кДа, 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 50 кДа, 100 кДа, 150 кДа, 200 кДа, 250 кДа, 300 кДа, 350 кДа, 400 кДа, 450 кДа, 500 кДа, 550 кДа, 600 кДа, 650 кДа, 700 кДа, 750 кДа, 800 кДа, 850 кДа, 900 кДа, 950 кДа или 1000 кДа. Соответственно, в некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 1 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 5 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 10 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 15 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 20 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 25 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 50 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 100 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 150 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 200 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 250 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 300 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 350 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 400 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 450 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 500 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 550 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 600 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 650 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 700 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 750 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 800 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 850 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 900 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 950 кДа. В некоторых вариантах осуществления фильтр для ультрафильтрации имеет NMWL, составляющий 1000 кДа.
[63] В некоторых вариантах осуществления для очистки осажденной mRNA на стадии c) применяют фильтрацию в тангенциальном потоке (TFF) или диафильтрацию. Соответственно, в некоторых вариантах осуществления для очистки осажденной mRNA на стадии c) применяют TFF. В некоторых вариантах осуществления для очистки осажденной mRNA на стадии c) применяют диафильтрацию.
[64] В некоторых вариантах осуществления применяют вспомогательное фильтрующее средство.
[65] В некоторых вариантах осуществления вспомогательное фильтрующее средство представляет собой средство на основе целлюлозы. В конкретных вариантах осуществления вспомогательное фильтрующее средство на основе целлюлозы добавляют к суспензии при массовом соотношении осажденной mRNA и вспомогательного фильтрующего средства, составляющем 1:10. В некоторых вариантах осуществления вспомогательное фильтрующее средство на основе целлюлозы содержит очищенные волокна целлюлозы, имеющие длину от приблизительно 5 мкм до приблизительно 500 мкм. В некоторых вариантах осуществления волокна целлюлозы имеют длину от приблизительно 10 мкм до приблизительно 100 мкм. В некоторых вариантах осуществления волокна целлюлозы имеют длину, составляющую приблизительно 20 мкм, 30 мкм, 40 мкм или 50 мкм. В конкретных вариантах осуществления вспомогательное фильтрующее средство на основе целлюлозы содержит очищенные волокна целлюлозы, имеющие длину приблизительно 20 мкм (например, Solka-Floc® или Sigmacell Cellulose 20).
[66] В некоторых вариантах осуществления вспомогательное фильтрующее средство содержит диатомовую землю и/или вулканический пепел. В некоторых вариантах осуществления вспомогательное фильтрующее средство содержит диатомовую землю. В некоторых вариантах осуществления вспомогательное фильтрующее средство содержит вулканический пепел. В некоторых вариантах осуществления вспомогательное фильтрующее средство содержит диатомовую землю и вулканический пепел.
[67] В некоторых вариантах осуществления солюбилизирующий раствор выбран из воды, трис-EDTA (ТЕ), цитрата натрия или их комбинаций. В некоторых вариантах осуществления солюбилизирующий раствор представляет собой воду. В некоторых вариантах осуществления солюбилизирующий раствор представляет собой TE. В некоторых вариантах осуществления солюбилизирующий раствор представляет собой цитрат натрия.
[68] В некоторых вариантах осуществления выход очищенной mRNA составляет от приблизительно 50% до приблизительно 100%.
[69] В некоторых вариантах осуществления выход очищенной mRNA составляет от приблизительно 70% до приблизительно 99%.
[70] В некоторых вариантах осуществления выход очищенной mRNA составляет от приблизительно 90 до приблизительно 99%. В конкретных вариантах осуществления выход очищенной mRNA составляет более чем приблизительно 93%, например, более чем приблизительно 94%, в частности, более чем приблизительно 95%.
[71] В некоторых вариантах осуществления чистота очищенной mRNA составляет от приблизительно 60% до приблизительно 100%.
[72] В некоторых вариантах осуществления чистота очищенной mRNA составляет от приблизительно 80% до 99%.
[73] В некоторых вариантах осуществления чистота очищенной mRNA составляет от приблизительно 90% до приблизительно 99%.
[74] В некоторых вариантах осуществления способ не включает стадию хроматографирования.
[75] В некоторых вариантах осуществления осажденную mRNA центрифугируют с получением осадка mRNA.
[76] В некоторых вариантах осуществления осадок mRNA ресуспендируют в буферном растворе.
[77] В некоторых вариантах осуществления буферный раствор выбран из воды, ТЕ, цитрата натрия или их комбинаций. В некоторых вариантах осуществления буферный раствор представляет собой воду. В некоторых вариантах осуществления буферный раствор представляет собой TE. В некоторых вариантах осуществления буферный раствор представляет собой цитрат натрия.
[78] В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере 100 мг, 1 г, 10 г, 100 г, 1 кг, 10 кг, 100 кг, одну метрическую тонну или десять метрических тонн mRNA или любое промежуточное количество. Соответственно, в некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере 100 мг mRNA. В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере 1 г mRNA. В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере 10 г mRNA. В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере 100 г mRNA. В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере 1 кг mRNA. В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере 10 кг mRNA. В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере 100 кг mRNA. В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере одну метрическую тонну mRNA. В некоторых вариантах осуществления осажденная mRNA содержит по меньшей мере десять метрических тонн mRNA.
[79] В некоторых вариантах осуществления осажденная mRNA содержит более чем 1 кг mRNA.
[80] В некоторых вариантах осуществления способ не предусматривает применение этанола.
[81] В некоторых аспектах настоящее изобретение предусматривает способ очистки матричной РНК (mRNA), включающий а) осаждение mRNA в растворе гуанидинтиоцианата (GSCN), содержащем PEG; b) центрифугирование раствора с получением осадка mRNA; c) ресуспендирование осадка mRNA в буфере; d) захватывание mRNA с помощью фильтра; e) промывание mRNA из стадии d) раствором PEG; и f) солюбилизирование промытой mRNA с получением композиции на основе mRNA, по сути не содержащей загрязняющих примесей.
[82] В определенном аспекте настоящее изобретение предусматривает способ изготовления mRNA, включающий стадии (a) осуществления транскрипции in vitro (IVT) посредством смешивания (i) ДНК-матрицы, содержащей промотор, и (ii) РНК-полимеразы с получением неочищенного препарата, содержащего полноразмерную mRNA; (b) обеспечения высокомолярной соли и амфифильного полимера в суспензии с осаждением полноразмерной mRNA и получением осажденной полноразмерной mRNA в суспензии; (c) захватывания осажденной полноразмерной mRNA посредством нанесения суспензии на фильтр; и (d) промывания осажденной полноразмерной mRNA из стадии (c) водным растворителем с получением очищенной полноразмерной mRNA в водном растворе, и (e) солюбилизирования осажденной mRNA из стадии (d) с получением композиции на основе очищенной mRNA, где очищенная полноразмерная mRNA в водном растворе, полученная на стадии (d), по сути не содержит (i) ДНК-матрицу, содержащую промотор, и (ii) РНК-полимеразу.
[83] В некоторых вариантах осуществления на стадии (a) РНК-полимераза представляет собой полимеразу SP6.
[84] В некоторых вариантах осуществления очищенная полноразмерная mRNA в водном растворе, полученная на стадии (e), также по сути не содержит (v) двухцепочечную РНК (dsRNA).
[85] В некоторых вариантах осуществления суспензия содержит PEG с молекулярной массой, составляющей около 6000 г/моль (например, PEG-6000), в конечной концентрации, составляющей от приблизительно 5% до 20% вес/объем, и GSCN в конечной концентрации, составляющей приблизительно 2-4 M. В конкретных вариантах осуществления суспензия содержит PEG с молекулярной массой, составляющей около 6000 г/моль (например, PEG-6000), в конечной концентрации, составляющей приблизительно 10%, 11%, 12%, 13%, 14% или 15% вес/объем, и GSCN в конечной концентрации, составляющей приблизительно 2,5-3 M. Как показано в примерах ниже, индуцированное полимером осаждение при конечной концентрации PEG в суспензии, составляющей менее чем 20%, приводило к получению образцов mRNA высокой степени чистоты после очистки. Более того, конечная концентрация PEG в суспензии, составляющая приблизительно 12% (например, соотношение, составляющее 1, для 50% PEG-6000), и конечная концентрация GSCN, составляющая 2,7 M, обеспечивали высокоэффективную очистку mRNA.
[86] В некоторых вариантах осуществления можно применять MTEG вместо PEG с получением суспензии осажденной mRNA. В конкретных вариантах осуществления с данной целью применяют MTEG в конечной концентрации, составляющей от приблизительно 15% до приблизительно 45% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей от приблизительно 20% до приблизительно 40% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 20% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 25% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 30% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 35% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей менее чем 35% вес/объем. Остальные условия, применяемые при осаждении, индуцируемом MTEG, представляют собой те же условия, которые применяются при осаждении, индуцируемом PEG. Как показано в примерах, суспензия, содержащая mRNA, GSCN и MTEG, где MTEG содержится в конечной концентрации, составляющей менее чем 35% вес/объем, обеспечивала эффективное извлечение mRNA без нежелательного осаждения ферментов, применяемых в способе. Особенно предпочтительной для эффективного извлечения mRNA без нежелательного осаждения ферментов, применяемых в способе, является суспензия, содержащая mRNA, GSCN и MTEG, где MTEG содержится в конечной концентрации, составляющей приблизительно 25%, в дополнение к вспомогательному фильтрующему средству (например, вспомогательному фильтрующему средству на основе целлюлозы), при массовом соотношении с осажденной mRNA, составляющем приблизительно 10:1.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[87] Следующие фигуры приведены исключительно с целью иллюстрации, а не для ограничения.
[88] На фигуре 1 показан выход mRNA, очищенной при различных условиях осаждения, из 5 мг реакционных смесей для IVT.
[89] На фигуре 2 показан окрашенный серебром гель для mRNA, очищенной при различных условиях осаждения. Окрашенный серебром гель применяли для демонстрации наличия загрязняющих ферментов, применяемых в способе. Полоса геля, отмеченная стрелкой на левой стороне геля, обозначает продвижение РНК-полимеразы SP6.
[90] На фигуре 3 показан выход mRNA, очищенной посредством индуцированного полимером осаждения, при различных соотношениях PEG-6000.
[91] На фигуре 4 показан окрашенный серебром гель для mRNA, очищенной посредством индуцированного полимером осаждения, при различных соотношениях PEG-6000.
[92] На фигуре 5 показан выход при очистке mRNA без применения этанола посредством индуцированного полимером осаждения и промывания полимером при применении различных полимерных буферов для промывания и различных концентраций.
[93] На фигуре 6 показан окрашенный серебром гель, соответствующий очистке mRNA без применения этанола посредством индуцированного полимером осаждения и промывания полимером, при применении буферов для промывания на основе 90% и 100% PEG-400 (дорожки 3 и 4 соответственно).
[94] На фигуре 7 показана процентная доля извлечения при очистке mRNA без применения этанола посредством индуцированного полимером осаждения и промывания полимером, для различных конструкций mRNA (OTC и CFTR) в масштабе 5 мг, 1 г и 10 г.
[95] На фигуре 8 показаны профили капиллярного электрофореза (CE), демонстрирующие целостность mRNA, очищенной посредством индуцированного полимером осаждения и промывания полимером, для различных конструкций mRNA (OTC и CFTR) в масштабе 5 мг, 1 г и 10 г.
[96] На фигуре 9 показан окрашенный серебром гель, соответствующий очистке mRNA без применения этанола посредством индуцированного полимером осаждения и промывания полимером, для различных конструкций mRNA (OTC и CFTR) в масштабе 5 мг, 1 г и 10 г.
[97] На фигуре 10 представлена серия дот-блотов, которые показывают наличие или отсутствие dsRNA после очистки mRNA орнитинкарбамоилтрансферазы (ОТС) в масштабе 10 граммов, 5 мг или 1 г. Условия очистки указаны над гелем и включают дорожки для положительного контроля (2 нг контроля dsRNA, 25 нг контроля dsRNA, положительный контроль), очистки на основе этанола 10 г mRNA OTC и очистки без применения этанола 10 г, 5 г или 1 г mRNA OTC.
[98] На фигуре 11 показано извлечение mRNA, очищенной посредством индуцированного полимером осаждения и промывания с помощью MTEG в различных концентрациях вес/объем.
[99] На фигуре 12 показан окрашенный серебром гель для mRNA, очищенной посредством индуцированного MTEG осаждения с применением различных соотношений mRNA:соль:MTEG в суспензии и промывания с помощью MTEG в концентрации, составляющей 95% вес/объем.
[100] На фигуре 13 показан анализ пятна, полученного при CE, для образца mRNA OTC массой 7,5 г после глубинной фильтрации с применением MTEG в качестве полимера для стадий осаждения и промывания.
[101] На фигуре 14 показан окрашенный серебром гель для образца mRNA OTC массой 7,5 г после глубинной фильтрации с применением MTEG в качестве полимера для стадий осаждения и промывания.
[102] На фигуре 15 показан анализ пятна, полученного при CE, для образца mRNA CFTR массой 15 г после глубинной фильтрации с применением MTEG в качестве полимера для стадий осаждения и промывания.
[103] На фигуре 16 показан окрашенный серебром гель для образца mRNA CFTR массой 15 г после глубинной фильтрации с применением MTEG в качестве полимера для стадий осаждения и промывания.
[104] На фигуре 17 показан анализ пятна, полученного при CE, для образца mRNA CFTR массой 15 г после фильтрации с помощью центрифуги с применением MTEG в качестве полимера для стадий осаждения и промывания.
[105] На фигуре 18 показан окрашенный серебром гель для образца mRNA CFTR массой 15 г после фильтрации с помощью центрифуги с применением MTEG в качестве полимера для стадий осаждения и промывки.
ОПРЕДЕЛЕНИЯ
[106] Для облегчения понимания настоящего изобретения сначала ниже приводятся определения некоторых терминов. Дополнительные определения следующих терминов и других терминов приводятся по всему описанию.
[107] Термины «или более», «по меньшей мере», «более чем» и т. п., например, «по меньшей мере один», как следует понимать, включают без ограничения по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149 или 150, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 2000, 3000, 4000, 5000 или более чем указанное значение. Также включены любое большее число или промежуточная дробь.
[108] И наоборот, термин «не более чем» включает каждое значение, меньшее чем указанное значение. Например, выражение «не более чем 100 нуклеотидов» включает 100, 99, 98, 97, 96, 95, 94, 93, 92, 91, 90, 89, 88, 87, 86, 85, 84, 83, 82, 81, 80, 79, 78, 77, 76, 75, 74, 73, 72, 71, 70, 69, 68, 67, 66, 65, 64, 63, 62, 61, 60, 59, 58, 57, 56, 55, 54, 53, 52, 51, 50, 49, 48, 47, 46, 45, 44, 43, 42, 41, 40, 39, 38, 37, 36, 35, 34, 33, 32, 31, 30, 29, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1 и 0 нуклеотидов. Также включены любое меньшее число или промежуточная дробь.
[109] Следует понимать, что термины «множество», «по меньшей мере два», «два или более», «по меньшей мере второй» и т. п. включают без ограничения по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149 или 150, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 2000, 3000, 4000, 5000 или более. Также включены любое большее число или промежуточная дробь.
[110] Примерно или приблизительно: Используемый в данном документе термин «примерно» или «приблизительно», применяемый в отношении одного или более представляющих интерес значений, относится к значению, которое является подобным указанному эталонному значению. В определенных вариантах осуществления термин «примерно» или «приблизительно» относится к значению, находящемуся в пределах 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0,5%, 0,1%, 0,05%, 0,01% или 0,001% от указанного значения. Если из контекста явно не следует иное, все числовые значения, представленные в данном документе, модифицированы термином «примерно» или «приблизительно».
[111] Партия: Используемый в данном документе термин «партия» относится к величине или количеству mRNA, очищенному за один раз, например, очищенному в соответствии с одним производственным заказом в течение одного и того же цикла производства. Партия может относиться к количеству mRNA, очищенному в ходе одной реакции.
[112] Биологически активный: Используемое в данном документе выражение «биологически активный» относится к характеристике любого средства, которое обладает активностью в биологической системе и, в частности, в организме. Например, средство, которое при введении в организм оказывает биологическое воздействие на данный организм, считается биологически активным.
[113] Включающий: Используемый в данном документе термин «включающий» или такие варианты, как «включает» или «содержащий», как следует понимать, подразумевают включение указанного элемента, целого числа или стадии, или группы элементов, целых чисел или стадий, но не исключение любого другого элемента, целого числа или стадии, или группы элементов, целых чисел или стадий.
[114] dsRNA: Используемый в данном документе термин «dsRNA» относится к продуцированию комплементарных последовательностей РНК в ходе реакции транскрипции in vitro (IVT). Комплементарные последовательности РНК могут продуцироваться по разным причинам, в том числе, например, короткие абортивные транскрипты, которые могут гибридизироваться с комплементарными последовательностями в образующейся цепи РНК, короткие абортивные транскрипты, действующие в качестве праймеров для РНК-зависимой ДНК-независимой транскрипции РНК, и возможный разворот матрицы РНК-полимеразы.
[115] Экспрессия: Используемый в данном документе термин «экспрессия» последовательности нуклеиновой кислоты относится к трансляции mRNA в полипептид (например, тяжелую цепь или легкую цепь антитела), сборке нескольких полипептидов (например, тяжелой цепи или легкой цепи антитела) в интактный белок (например, антитело) и/или посттрансляционной модификации полипептида или полностью собранного белка (например, антитела). В настоящей заявке термины «экспрессия» и «продуцирование», а также их грамматический эквивалент применяют взаимозаменяемо.
[116] Функциональный: Используемый в данном документе термин «функциональная» биологическая молекула представляет собой биологическую молекулу в форме, в которой она проявляет свойство и/или активность, которыми она характеризуется.
[117] Улучшать, увеличивать или уменьшать. Используемые в данном документе термины «улучшать», «увеличивать» или «уменьшать» или грамматические эквиваленты указывают на значения, относящиеся к исходному измерению, например, к измерению у одного того же индивидуума до начала лечения, описанного в данном документе, или измерению у контрольного субъекта (или нескольких контрольных субъектов) в отсутствие лечения, описанного в данном документе. Термин «контрольный субъект» представляет собой субъекта, страдающего той же формой заболевания, что и субъект, подвергающийся лечению, который имеет приблизительно тот же возраст, что и субъект, подвергающийся лечению.
[118] Примеси: Используемый в данном документе термин «примеси» относится к веществам внутри ограниченного количества жидкости, газа или твердого вещества, которые отличаются от химического состава целевого материала или соединения. Примеси также называют «загрязняющими примесями».
[119] In vitro: Используемый в данном документе термин «in vitro» относится к событиям, которые происходят в искусственной среде, например, в пробирке или реакционном сосуде, в культуре клеток и т. д., а не в пределах многоклеточного организма.
[120] In vivo: Используемый в данном документе термин «in vivo» относится к событиям, которые происходят в пределах многоклеточного организма, например, у человека и животного, отличного от человека. В контексте систем на основе клеток термин может быть использован в отношении событий, которые происходят в живой клетке (в противоположность, например, системам in vitro).
[121] Выделенный: Используемый в данном документе термин «выделенный» относится к веществу и/или объекту, который (1) был отделен по меньшей мере от некоторых компонентов, с которыми он был связан при изначальном получении (в природе и/или в экспериментальных условиях), и/или (2) был получен, приготовлен и/или изготовлен человеком. Выделенные вещества и/или объекты могут быть отделены от приблизительно 10%, приблизительно 20%, приблизительно 30%, приблизительно 40%, приблизительно 50%, приблизительно 60%, приблизительно 70%, приблизительно 80%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или более чем приблизительно 99% других компонентов, с которыми они изначально были связаны. В некоторых вариантах осуществления выделенные средства являются на приблизительно 80%, приблизительно 85%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или более чем приблизительно 99% чистыми. Как используется в данном документе, вещество является «чистым», если оно по сути не содержит других компонентов. Как используется в данном документе, расчет процентной доли чистоты выделенных веществ и/или объектов не должен включать вспомогательные вещества (например, буфер, растворитель, воду и т.д.).
[122] Матричная РНК (mRNA): Используемый в данном документе термин «матричная РНК (mRNA)» относится к полинуклеотиду, который кодирует по меньшей мере один полипептид. mRNA, как используется в данном документе, охватывает как модифицированную, так и немодифицированную РНК. mRNA может содержать одну или более кодирующих и некодирующих областей.
[123] Целостность mRNA: Используемый в данном документе термин «целостность mRNA» обычно относится к качеству mRNA. В некоторых вариантах осуществления целостность mRNA относится к процентной доле mRNA, которая не разрушается после процесса очистки. Целостность mRNA можно определить с применением способов, хорошо известных из уровня техники, например, посредством электрофореза РНК в агарозном геле (например, Ausubel et al., John Weley & Sons, Inc., 1997, Current Protocols in Molecular Biology).
[124] Нуклеиновая кислота: Используемый в данном документе термин «нуклеиновая кислота» в его самом широком смысле относится к любому соединению и/или веществу, которое включено или может быть включено в полинуклеотидную цепь. В некоторых вариантах осуществления нуклеиновая кислота представляет собой соединение и/или вещество, которое включено или может быть включено в полинуклеотидную цепь посредством фосфодиэфирной связи. В некоторых вариантах осуществления «нуклеиновая кислота» относится к отдельным остаткам нуклеиновой кислоты (например, нуклеотидам и/или нуклеозидам). В некоторых вариантах осуществления «нуклеиновая кислота» относится к полинуклеотидной цепи, содержащей отдельные остатки нуклеиновой кислоты. В некоторых вариантах осуществления термин «нуклеиновая кислота» охватывает РНК, а также одно- и/или двухцепочечную ДНК и/или cDNA. Более того, термины «нуклеиновая кислота», «ДНК», «РНК» и/или подобные термины включают аналоги нуклеиновых кислот, т. е. аналоги, имеющие остов, отличный от фосфодиэфирного. Например, так называемые «пептидные нуклеиновые кислоты», которые известны из уровня техники и содержат пептидные связи вместо фосфодиэфирных связей в остове, считаются находящимися рамках настоящего изобретения. Термин «нуклеотидная последовательность, кодирующая аминокислотную последовательность» включает все нуклеотидные последовательности, которые являются вырожденными версиями друг друга и/или кодируют одну и ту же аминокислотную последовательность. Нуклеотидные последовательности, которые кодируют белки и/или РНК, могут включать интроны. Нуклеиновые кислоты могут быть получены посредством очистки из природных источников, могут быть получены с применением рекомбинантных систем экспрессии и необязательно могут быть очищены, химически синтезированы и т. д. При необходимости, например, в случае химически синтезированных молекул, нуклеиновые кислоты могут включать аналоги нуклеозидов, такие как аналоги, содержащие химически модифицированные основания или сахара, модификации остова и т. д. Последовательность нуклеиновой кислоты представлена в направлении от 5’ к 3’, если не указано иное. В некоторых вариантах осуществления нуклеиновая кислота представляет собой или содержит природные нуклеозиды (например, аденозин, тимидин, гуанозин, цитидин, уридин, дезоксиаденозин, дезокситимидин, дезоксигуанозин и дезоксицитидин); аналоги нуклеозидов (например, 2-аминоаденозин, 2-тиотимидин, инозин, пирролопиримидин, 3-метиладенозин, 5-метилцитидин, C-5-пропинилцитидин, C-5-пропинилуридин, 2-аминоаденозин, C5-бромуридин, C5-фторуридин, C5-йодуридин, C5-пропинилуридин, C5-пропинилцитидин, C5-метилцитидин, 2-аминоаденозин, 7-деазааденозин, 7-деазагуанозин, 8-оксоаденозин, 8-оксогуанозин, O(6)-метилгуанин и 2-тиоцитидин), химически модифицированные основания; биологически модифицированные основания (например, метилированные основания); интеркалированные основания; модифицированные сахара (например, 2’-фторрибозу, рибозу, 2’-дезоксирибозу, арабинозу и гексозу) и/или модифицированные фосфатные группы (например, фосфоротиоаты и 5’-N-фосфорамидитные связи). В некоторых вариантах осуществления настоящее изобретение, в частности, направлено на «немодифицированные нуклеиновые кислоты», что означает нуклеиновые кислоты (например, полинуклеотиды и остатки, в том числе нуклеотиды и/или нуклеозиды), которые не были химически модифицированы с целью облегчения или достижения доставки.
[125] Осаждение: Используемый в данном документе термин «осаждение» (или любой его грамматический эквивалент) относится к образованию твердого вещества в растворе. При использовании в связи с mRNA термин «осаждение» относится к образованию нерастворимой или твердой формы mRNA в жидкости.
[126] Преждевременно прерванные последовательности РНК: Используемые в данном документе термины «преждевременно прерванные последовательности РНК», «короткие молекулы абортивной РНК», «шортмеры» и «длинные молекулы абортивной РНК» относятся к неполным продуктам реакции синтеза mRNA (например, реакции синтеза in vitro). По ряду причин РНК-полимеразы не всегда завершают транскрипцию ДНК-матрицы; например, синтез РНК прекращается преждевременно. Возможные причины преждевременного прекращения синтеза РНК включают качество ДНК-матрицы, последовательности терминаторов полимеразы для конкретной полимеразы, присутствующей в матрице, расщепленные буферы, температуру, истощение рибонуклеотидов и вторичные структуры mRNA. Преждевременно прерванные последовательности РНК могут иметь любую длину, которая является меньшей, чем предполагаемая длина требуемого продукта транскрипции. Например, преждевременно прерванные последовательности РНК могут представлять собой менее чем 1000 оснований, менее чем 500 оснований, менее чем 100 оснований, менее чем 50 оснований, менее чем 40 оснований, менее чем 30 оснований, менее чем 20 оснований, менее чем 15 оснований, менее чем 10 оснований или меньше.
[127] Соль: Используемый в данном документе термин «соль» относится к ионному соединению, которое является или может являться результатом реакции нейтрализации между кислотой и основанием.
[128] По сути: Используемый в данном документе термин «по сути» относится к качественному состоянию проявления полной или почти полной меры или степени представляющих интерес характеристики или свойства. Специалисту в области биологии будет понятно, что биологические и химические явления редко, если вообще когда-либо, доходят до завершения и/или подходят к завершению, или достигают абсолютного результата, или избегают его. Таким образом, термин «по сути» используют в данном документе для обозначения потенциального отсутствия завершенности, присущей многим биологическим и химическим явлениям.
[129] По сути не содержит: Используемый в данном документе термин «по сути не содержит» относится к состоянию, при котором содержится относительно небольшое количество вещества, подлежащего удалению (например, преждевременно прерванных последовательностей РНК), или таковое отсутствует. Например, выражение «по сути не содержит преждевременно прерванных последовательностей РНК» означает, что уровень содержания преждевременно прерванных последовательностей РНК составляет менее чем приблизительно 5%, 4%, 3%, 2%, 1,0%, 0,9%, 0,8%, 0,7%, 0,6%, 0,5%, 0,4%, 0,3%, 0,2%, 0,1% или меньше (вес/вес) от примеси. В качестве альтернативы «по сути не содержит преждевременно прерванных последовательностей РНК» означает, что уровень содержания преждевременно прерванных последовательностей РНК составляет менее чем приблизительно 100 нг, 90 нг, 80 нг, 70 нг, 60 нг, 50 нг, 40 нг, 30 нг, 20 нг, 10 нг, 1 нг, 500 пг, 100 пг, 50 пг, 10 пг или меньше.
[130] Если не приведено иное определение, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимает специалист в области, к которой принадлежит данная заявка, и которое обычно используют в области, к которой принадлежит данная заявка; такой уровень техники включен посредством ссылки во всей своей полноте. В случае конфликта настоящее описание, в том числе определения, будет обладать преимущественной силой.
ПОРОБНОЕ ОПИСАНИЕ
[131] Настоящее изобретение предусматривает, среди прочего, улучшенные способы очистки mRNA без применения спиртов в способе очистки.
[132] В следующих разделах подробно описаны различные аспекты настоящего изобретения. Применение разделов не предназначено для ограничения настоящего изобретения. Каждый раздел может применяться в отношении любого аспекта настоящего изобретения. В настоящей заявке применение термина «или» означает «и/или», если не указано иное.
Способы очистки
[133] Применение едких или легковоспламеняющихся растворителей при очистке mRNA может создавать трудности с точки зрения безопасности и затрат, особенно при крупномасштабных путях получения. Настоящее изобретение относится к способам очистки mRNA без применения едких или легковоспламеняющихся растворителей. Способы, предусмотренные в данном документе, обеспечивают возможность эффективного захватывания, промывания и выделения с высоким выходом mRNA, изготавливаемой в масштабах, способных удовлетворить большинство клинических и коммерческих потребностей. Соответственно, настоящее изобретение предусматривает дальнейшие перспективы для терапевтических средств, замещающих mRNA, что позволяет им становиться эффективной и успешной альтернативой более традиционным терапевтическим средствам, замещающим ферменты, и биологическим терапевтическим средствам, которые доступны в настоящее время.
[134] Для того, чтобы стать эффективной и успешной альтернативой, способ очистки mRNA должен являться безопасным, экономичным, надежным и масштабируемым для обеспечения возможностей крупномасштабного получения в плане удовлетворения всех клинических и коммерческих потребностей. Соответствующий способ очистки mRNA является безопасным, экономичным и легко масштабируемым, при этом он обеспечивает получение эквивалентного или более хорошего продукта по сравнению с доступными в настоящее время стандартными для данной отрасли способами очистки mRNA. В частности, способы, предусмотренные в данном документе, устраняют применение едких или легковоспламеняющихся растворителей и приводят к высоким выходам mRNA после очистки, сохранению целостности mRNA после очистки и удалению загрязняющих примесей, связанных со способом (например, преждевременно прерванных последовательностей РНК (коротких молекул абортивной РНК или «шортмеров»), длинных молекул абортивной РНК, двухцепочечной РНК (dsRNA), плазмидной ДНК, остаточного растворителя, остаточной соли и остаточных ферментов транскрипции in vitro ).
[135] Способы, предусмотренные в данном документе, являются применимыми в широком диапазоне масштабов. Например, и как рассматривается далее в данном документе, предусмотренные способы обеспечивают возможность очистки в различных масштабах, например, от 100 мг или ниже до более чем 1 кг. Кроме того, данные, представленные в данном документе, показывают, что настоящее изобретение представляет собой конкурентоспособную (и менее затратную) альтернативу доступным в настоящее время способам очистки mRNA, которые основаны на применении воспламеняющихся растворителей, таких как спирты. Способ очистки mRNA, предусмотренный в данном документе, является подходящим для различных путей применения, в том числе, например, для экспериментального, клинического или коммерческого применения. Более того, настоящее изобретение обладает существенным дополнительным преимуществом, представляющим собой масштабируемость, которое недоступно при применении стандартных для данной отрасли способов и наборов. Наконец, раскрытые в данном документе способы являются чрезвычайно экономичными по сравнению с доступными в настоящее время способами, такими как способы фильтрации, которые предусматривают спиртовые растворители и/или хроматографию. См., например, WO 2011/068810; WO 2012/075040; WO 2014/152659; WO 2014/152673; WO 2014/152966; WO 2015/164773; WO 2016/004318; US 62/420413 и PCT/US16/57044.
[136] Соответственно, способы, описанные в данном документе, обладают преимуществом в отношении очистки mRNA, в том числе крупномасштабных количеств mRNA (например, партии любого размера или любого объема загрузки, описанных в данном документе). Описанные способы очистки могут обеспечить получение mRNA, обладающей высоким уровнем целостности и чистотой, приемлемой для путей терапевтического применения, при минимальной потере полноразмерной mRNA за счет очистки.
[137] Описанный в данном документе способ очистки mRNA включает осаждение mRNA, захватывание осажденной mRNA и промывание захваченной осажденной mRNA с получением композиции на основе очищенной mRNA, по сути не содержащей загрязняющих примесей. Каждая из данных стадий подробно описана в следующих разделах.
Осаждение mRNA
[138] Способ очистки mRNA включает стадии осаждения mRNA в суспензии, содержащей высокомолярный раствор соли и амфифильный полимер, захватывания mRNA и промывания mRNA, тем самым получают mRNA, по сути не содержащую загрязняющих примесей.
[139] Способы, описанные в данном документе, являются подходящими для очистки mRNA в предусмотренной суспензии, содержащей mRNA (например, реакционной смеси для синтеза in vitro). Суспензия может содержать различные загрязняющие примеси, например, плазмидную ДНК и ферменты.
[140] В одном варианте осуществления соль (например, хаотропную соль, такую как гуанидинтиоцианат (GSCN)) добавляют к суспензии, содержащей mRNA, для денатурирования и солюбилизации загрязняющих белков. Соответственно, в одном варианте осуществления GSCN находится в высокомолярном растворе в суспензии. Затем следует добавление амфифильного полимера с селективным осаждением mRNA. После осаждения mRNA полученную осажденную mRNA захватывают с применением фильтра или мембраны и промывают с получением осадка, свободного от загрязняющих примесей, например, коротких молекул абортивной РНК, длинных молекул абортивной РНК, dsRNA, плазмидной ДНК, остаточных ферментов транскрипции in vitro , остаточной соли и остаточного растворителя. Последующее растворение осажденной mRNA водой приводит к получению композиции на основе очищенной mRNA.
[141] В некоторых вариантах осуществления одно средство, которое способствует осаждению mRNA, включает гуанидинтиоцианат (например, раствор, содержащий приблизительно 1-5 М гуанидинтиоцианата). Например, раствор содержит приблизительно 1 M, 1,5 M, 2,0 M, 2,5 M, 3,0 M, 3,5 M, 4,0 M, 4,5 M или приблизительно 5 M GSCN. Примеры подходящих буферов на основе GSCN включают, например, водный раствор, содержащий 4 М гуанидинтиоцианата, 25 мМ цитрата натрия, pH 6,5, 0,5% натриевой соли N-лауроилсаркозина. Дополнительный пример буфера на основе GSCN представляет собой водный раствор, содержащий 5 M GSCN в буфере на основе 10 мМ дитиотреитола (DTT). В некоторых вариантах осуществления GSCN содержится в конечной концентрации, составляющей 2-4 M. В некоторых вариантах осуществления GSCN (например, буфер на основе 5 M GSCN и 10 мМ DTT) содержится в конечной концентрации, составляющей 2,5-3 M. В конкретных вариантах осуществления GSCN содержится в конечной концентрации, составляющей приблизительно 2,7 M.
[142] Множество амфифильных полимеров известны из уровня техники. В некоторых вариантах осуществления амфифильный полимер, применяемый в описанных в данном документе способах, включает плюроники, поливинилпирролидон, поливиниловый спирт, полиэтиленгликоль (PEG) или их комбинации. В некоторых вариантах осуществления амфифильный полимер выбран из одного или более из следующего: PEG, триэтиленгликоля, тетраэтиленгликоля, PEG 200, PEG 300, PEG 400, PEG 600, PEG 1000, PEG 1500, PEG 2000, PEG 3000, PEG 3350, PEG 4000, PEG 6000, PEG 8000, PEG 10000, PEG 20000, PEG 35000 и PEG 40000 или их комбинации. В некоторых вариантах осуществления амфифильный полимер содержит смесь двух или более видов применяемых полимеров PEG с различной молекулярной массой. Например, в некоторых вариантах осуществления амфифильный полимер состоит из двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати или двенадцати видов полимеров PEG с различной молекулярной массой. Соответственно, в некоторых вариантах осуществления раствор PEG содержит смесь одного или более полимеров PEG. В некоторых вариантах осуществления смесь полимеров PEG содержит полимеры, имеющие различные молекулярные массы.
[143] В некоторых вариантах осуществления осаждение mRNA в суспензии предусматривает применение одного или более амфифильных полимеров. В некоторых вариантах осуществления осаждение mRNA в суспензии предусматривает применение полимера PEG. Различные виды полимеров PEG известны из уровня техники, некоторые из них имеют различные геометрические конфигурации. Полимеры PEG, подходящие для описанных в данном документе способов, включают, например, полимеры PEG, имеющие линейную, разветвленную, Y-образную или многолучевую конфигурацию. В некоторых вариантах осуществления PEG содержится в суспензии, содержащей один или более PEG, имеющих различные геометрические конфигурации. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением PEG-6000 для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением PEG-400 для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением триэтиленгликоля (TEG) для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением монометилового эфира триэтиленгликоля (MTEG) для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением трет-бутил-TEG-O-пропионата для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением диметакрилата TEG для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением диметилового эфира TEG для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением дивинилового эфира TEG для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением монобутилового эфира TEG для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением метакрилата метилового эфира TEG для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением монодецилового эфира TEG для осаждения mRNA. В некоторых вариантах осуществления осаждение mRNA может быть достигнуто с применением дибензоата TEG для осаждения mRNA. Любой из данных реагентов на основе PEG или TEG можно применять в комбинации с гуанидинтиоцианатом для осаждения mRNA. Структура каждого из данных реагентов показана ниже в таблице A.
[144] Таблица A: Реагенты, представляющие собой неорганические растворители, для очистки mRNA (осаждения и/или промывания mRNA)
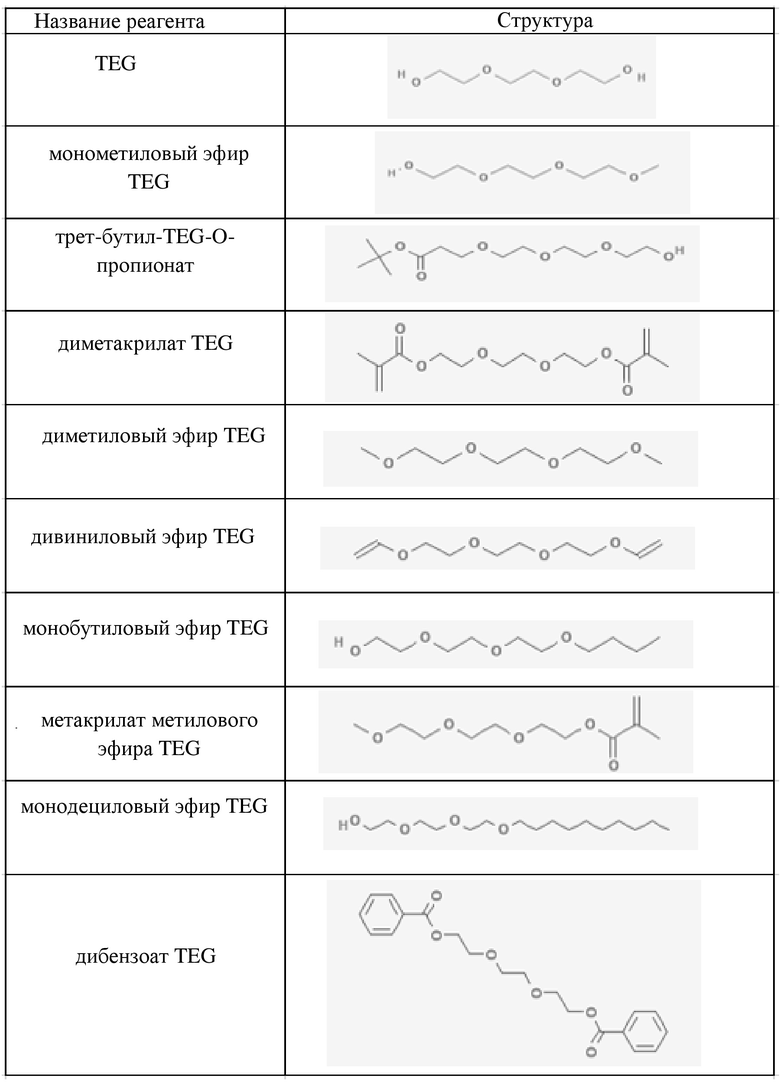
[145] В некоторых вариантах осуществления осаждение mRNA в суспензии предусматривает применение полимера PEG, где полимер PEG содержит липид, модифицированный с PEG. В некоторых вариантах осуществления липид, модифицированный PEG, представляет собой 1,2-димиристоил-sn-глицерин, метоксиполиэтиленгликоль (DMG-PEG-2K). В некоторых вариантах осуществления липид, модифицированный PEG, представляет собой конъюгат DOPA-PEG. В некоторых вариантах осуществления липид, модифицированный PEG, представляет собой конъюгат полоксамер-PEG. В некоторых вариантах осуществления липид, модифицированный PEG, содержит DOTAP. В некоторых вариантах осуществления липид, модифицированный PEG, содержит холестерин.
[146] В некоторых вариантах осуществления mRNA осаждают в суспензии, содержащей амфифильный полимер. В некоторых вариантах осуществления mRNA осаждают в суспензии, содержащей любой из вышеупомянутых реагентов на основе PEG. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей от приблизительно 10% до приблизительно 100% вес/объем. Например, в некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 100% вес/объем, включая любые промежуточные значения. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 5% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 6% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 7% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 8% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 9% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 10% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 12% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 15% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 18% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 20% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 25% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 30% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 35% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 40% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 45% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 50% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 55% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 60% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 65% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 70% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 75% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 80% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 85% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 90% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 95% вес/объем. В некоторых вариантах осуществления PEG содержится в суспензии в концентрации, составляющей приблизительно 100% вес/объем.
[147] В некоторых вариантах осуществления осаждение mRNA в суспензии предусматривает отношение объема PEG к общему объему суспензии mRNA, составляющее от приблизительно 0,1 до приблизительно 5,0. Например, в некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,25, 1,5, 1,75, 2,0, 2,25, 2,5, 2,75, 3,0, 3,25, 3,5, 3,75, 4,0, 4,25, 4,5, 4,75, 5,0. Соответственно, в некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,1. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,2. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,3. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,4. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,5. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,6. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,7. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,8. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 0,9. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 1,0. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 1,25. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 1,5. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 1,75. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 2,0. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 2,25. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 2,5. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 2,75. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 3,0. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 3,25. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 3,5. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 3,75. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 4,0. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 4,25. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 4,50. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 4,75. В некоторых вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 5,0. В конкретных вариантах осуществления PEG содержится в суспензии mRNA при объемном соотношении, составляющем приблизительно 1,0, приблизительно 1,5 или приблизительно 2,0.
[148] В некоторых вариантах осуществления объем реакционной смеси для осаждения mRNA содержит GSCN и PEG. В конкретных вариантах осуществления объем реакционной смеси для осаждения mRNA содержит GSCN и PEG, имеющий молекулярную массу от приблизительно 4000 г/моль до приблизительно 8000 г/моль, например, приблизительно 6000 г/моль (например, PEG-6000). Конечная концентрация GSCN обычно составляет от 2 М до 4 M. Конечная концентрация PEG обычно составляет от приблизительно 10% до приблизительно 20% (вес/объем).
[149] В некоторых вариантах осуществления способ очистки mRNA не предусматривает применение спирта.
[150] В некоторых вариантах осуществления добавляют неводный растворитель (например, спирт) с осаждением mRNA . В некоторых вариантах осуществления растворитель может представлять собой изопропиловый спирт, ацетон, метилэтилкетон, метилизобутилкетон, этанол, метанол, денатониум и их комбинации. В вариантах осуществления растворитель представляет собой спиртовой растворитель (например, метанол, этанол или изопропанол). В вариантах осуществления растворитель представляет собой кетоновый растворитель (например, ацетон, метилэтилкетон или метилизобутилкетон). В некоторых вариантах осуществления неводный растворитель смешивают с амфифильным раствором.
[151] В некоторых вариантах осуществления добавляют водный раствор с осаждением mRNA. В некоторых вариантах осуществления водный раствор содержит полимер. В некоторых вариантах осуществления водный раствор содержит полимер PEG.
[152] В некоторых вариантах осуществления способ дополнительно включает стадию добавления одного или более средств, которые денатурируют белки (например, РНК-полимеразы и ДНКазы I, которые добавляют после транскрипции с удалением ДНК-матриц) и/или сохраняют белки растворимыми в водной среде. В некоторых вариантах осуществления одно или более средств, которые денатурируют белки и/или сохраняют белки растворимыми в водной среде, представляют собой соль, например, хаотропную соль.
[153] В некоторых вариантах осуществления стадия осаждения предусматривает применение хаотропной соли (например, гуанидинтиоцианата), и/или амфифильного полимера (например, полиэтиленгликоля или водного раствора полиэтиленгликоля), и/или спиртового растворителя (например, абсолютного этанола или водного раствора спирта, такого как водный раствор этанола). Следовательно, в некоторых вариантах осуществления стадия осаждения предусматривает применение хаотропной соли и амфифильного полимера, такого как GSCN и PEG соответственно.
[154] В некоторых вариантах осуществления средства, которые способствуют осаждению mRNA, включают денатурирующее средство или представляют собой результат воздействия денатурирующих условий. Используемый в данном документе термин «денатурирующие условия» относится к любым химическим или физическим условиям, которые могут вызывать денатурацию. Примеры денатурирующих условий включают без ограничения применение химических реагентов, высоких температур, экстремальных значений pH и т. д. В некоторых вариантах осуществления денатурирующие условия достигаются посредством добавления одного или более денатурирующих средств к неочищенному препарату, содержащему mRNA, подлежащему очистке. В некоторых вариантах осуществления денатурирующее средство, подходящее для настоящего изобретения, представляет собой средство, денатурирующее белок и/или ДНК. В некоторых вариантах осуществления денатурирующее средство может представлять собой 1) фермент (такой как сериновая протеиназа или ДНКаза), 2) кислоту, 3) растворитель, 4) сшивающее средство, 5) хаотропное средство, 6) восстанавливающее средство и/или 7) высокую ионную силу за счет высоких концентраций соли. В некоторых вариантах осуществления конкретное средство может относиться к более чем одной из данных категорий.
[155] В некоторых вариантах осуществления один или более ферментов можно применять в качестве денатурирующих средств для расщепления белков и ДНК-матриц, применяемых в синтезе mRNA. В некоторых вариантах осуществления подходящие ферменты включают без ограничения сериновые протеазы, например, химотрипсин и химотрипсиноподобные сериновые протеазы, трипсин и трипсиноподобные сериновые протеазы, эластазу и эластазоподобные сериновые протеазы, субтилизин и субтилизиноподобные сериновые протеазы и их комбинации, дезоксирибонуклеазы (ДНКазу), например, дезоксирибонуклеазу I, II и/или IV, рестрикционные ферменты, например, EcoRI, EcoRII, BamHI, HindIII, SpeI, SphI, StuI, XbaI и их комбинации.
[156] В некоторых вариантах осуществления в качестве денатурирующего средства можно применять кислоту. В некоторых вариантах осуществления подходящая кислота может представлять собой уксусную кислоту, муравьиную кислоту, щавелевую кислоту, лимонную кислоту, бензойную кислоту, хлоруксусную кислоту, дихлоруксусную кислоту, трихлоруксусную кислоту, аскорбиновую кислоту, сульфосалициловую кислоту и их комбинации.
[157] В некоторых вариантах осуществления в качестве денатурирующего средства можно применять растворитель. В некоторых вариантах осуществления растворитель не содержит едкие или легковоспламеняющиеся средства. В некоторых вариантах осуществления растворитель не содержит этанол. В некоторых вариантах осуществления растворитель не содержит изопропиловый спирт, ацетон, метилэтилкетон, метилизобутилкетон, этанол, метанол, денатониум и их комбинации. В некоторых вариантах осуществления растворитель не содержит спиртовой растворитель (например, метанол, этанол или изопропанол). В некоторых вариантах осуществления растворитель не содержит кетоновый растворитель (например, ацетон, метилэтилкетон или метилизобутилкетон).
[158] В некоторых вариантах осуществления в качестве денатурирующего средства можно применять растворитель. В некоторых вариантах осуществления растворитель представляет собой этанол. В некоторых вариантах осуществления растворитель представляет собой изопропиловый спирт, ацетон, метилэтилкетон, метилизобутилкетон, этанол, метанол, денатониум и их комбинации. В некоторых вариантах осуществления растворитель представляет собой спиртовой растворитель (например, метанол, этанол или изопропанол). В некоторых вариантах осуществления растворитель представляет собой кетоновый растворитель (например, ацетон, метилэтилкетон или метилизобутилкетон).
[159] В некоторых вариантах осуществления в качестве денатурирующего средства можно применять хаотропное средство. Хаотропные средства представляют собой вещества, которые нарушают структуру макромолекул, таких как белки и нуклеиновые кислоты, препятствуя нековалентным силам, таким как водородные связи и силы Ван-дер-Ваальса. В некоторых вариантах осуществления хаотропное средство может представлять собой мочевину, тиомочевину, гуанидинхлорид, гуанидинтиоцианат, гуанидинизотиоцианат, ацетат лития, хлорид магния, додецилсульфат натрия, перхлорат лития и их комбинацию.
[160] В некоторых вариантах осуществления в качестве денатурирующего средства можно применять восстанавливающее средство. Восстанавливающие средства представляют собой соединения, которые отдают электрон другой молекуле, при этом сами становятся окисленными. В некоторых вариантах осуществления восстанавливающее средство может представлять собой литийалюминийгидрид, амальгаму натрия, диборан, боргидрид натрия, сульфиты, диизобутилалюминийгидрид, фосфиты, монооксид углерода, 2-меркаптоэтанол, дитиотреитол или трис(2-карбоксиэтил)-фосфин и их комбинации.
[161] В некоторых вариантах осуществления одно или более из pH, нагревания и/или тяжелых металлов (таких как свинец, ртуть или кадмий) также можно применять в качестве денатурирующих средств для обеспечения условий денатурации. Известно, что предельные значения pH обуславливают денатурацию белка. Хотя остов белковой цепи является нейтральным, аминокислотные остатки, из которых состоит белок, часто содержат кислотные и основные группы. Данные группы обычно заряжены и могут образовывать солевые мостики с группой, имеющей противоположный заряд. Соответственно, при предельных значениях pH заряды данных кислотных и основных групп могут изменяться, что разрушает солевые мостики.
[162] В некоторых вариантах осуществления менее резкие изменения pH также могут влиять на активность и растворимость белка. Подобно отдельным аминокислотам белки имеют изоэлектрическую точку, в которой количество отрицательных зарядов равно количеству положительных зарядов. Зачастую данная точка представляет собой точку минимальной водорастворимости. При изоэлектрическом pH на молекуле отсутствует суммарный заряд. Отдельные молекулы обладают тенденцией сближаться, сворачиваться и выделяться в осадок из раствора. При pH выше или ниже изоэлектрического pH молекулы имеют суммарный отрицательный или положительный заряд соответственно. Таким образом, когда белковые молекулы сближаются друг с другом, они имеют одинаковый общий заряд и отталкиваются друг от друга.
[163] В некоторых вариантах осуществления в качестве денатурирующего средства можно применять нагревание. Нагревание может придавать молекулам белка кинетическую энергию, заставляя их атомы вибрировать быстрее. В некоторых вариантах осуществления это нарушает относительно слабые силы, такие как водородные связи и гидрофобные взаимодействия. Нагревание также применяют при стерилизации для денатурирования и, следовательно, разрушения ферментов в бактериях.
[164] В некоторых вариантах осуществления соли ионов металлов, таких как ртуть(II), свинец(II) и серебро, можно применять в качестве денатурирующих средств по причине их способности образовывать прочные связи с дисульфидными группами и с карбоксилат-ионами кислотных аминокислот. Таким образом, они разрушают как дисульфидные мостики, так и солевые связи, и обуславливают осаждение белка из раствора в виде нерастворимой соли металл-белок.
[165] В некоторых вариантах осуществления в качестве денатурирующего средства можно применять высокие концентрации соли (высокую степень минерализации). Известно, что высокие концентрации солей обуславливают осаждение как белков, так и нуклеиновых кислот из водного раствора. В некоторых вариантах осуществления высокая концентрация соли может составлять от 1 М до 10 М включительно. В некоторых вариантах осуществления высокая концентрация соли может составлять от 2 М до 9 М включительно. В некоторых вариантах осуществления высокая концентрация соли может составлять от 2 М до 8 М включительно. В некоторых вариантах осуществления высокая концентрация соли может составлять от 2 М до 5 М включительно. В некоторых вариантах осуществления высокая концентрация соли может превышать концентрацию, составляющую 1 M. В некоторых вариантах осуществления высокая концентрация соли может превышать концентрацию, составляющую 2 M. В некоторых вариантах осуществления высокая концентрация соли может превышать концентрацию, составляющую 3 M. В некоторых вариантах осуществления высокая концентрация соли может превышать концентрацию, составляющую 4 M. В некоторых вариантах осуществления высокая концентрация соли может превышать концентрацию, составляющую 5 M. В некоторых вариантах осуществления высокая концентрация соли может превышать концентрацию, составляющую 6 M. В некоторых вариантах осуществления высокая концентрация соли может превышать концентрацию, составляющую 7 M. В некоторых вариантах осуществления высокая концентрация соли может превышать концентрацию, составляющую 8 M. В некоторых вариантах осуществления в качестве денатурирующего средства применяют одну соль. В некоторых вариантах осуществления в качестве денатурирующего средства применяют более чем одну соль.
[166] В некоторых вариантах осуществления соль, применяемая в качестве денатурирующего средства, может представлять собой соль кальция, соль железа, соль магния, соль калия, соль натрия или их комбинацию. Примеры специфических солей, подходящих для применения в качестве денатурирующих средств, в некоторых вариантах осуществления включают без ограничения хлорид калия (KCl), хлорид натрия (NaCl), хлорид лития (LiCl), хлорид кальция (CaCl2), бромид калия (KBr), бромид натрия (NaBr), бромид лития (LiBr). В некоторых вариантах осуществления денатурирующее средство, воздействию которого подвергают неочищенный препарат, представляет собой хлорид калия (KCl). В некоторых вариантах осуществления KCl добавляют таким образом, чтобы полученная в результате концентрация KCl составляла приблизительно 1 M или более. В некоторых вариантах осуществления KCl добавляют таким образом, чтобы полученная в результате концентрация KCl составляла приблизительно 2 M или более, 3 M или более, 4 M или более или 5 M или более.
[167] В некоторых вариантах осуществления способ не включает стадию хроматографирования. В некоторых вариантах осуществления осажденную mRNA центрифугируют с получением осадка mRNA. Осадок mRNA затем ресуспендируют в буферном растворе, таком как вода, ТЕ, цитрат натрия или их комбинации. Соответственно, в некоторых вариантах осуществления осадок mRNA ресуспендируют в воде. В некоторых вариантах осуществления осадок mRNA ресуспендируют в TE. В некоторых вариантах осуществления осадок mRNA ресуспендируют в цитрате натрия.
[168] В некоторых вариантах осуществления mRNA осаждают в суспензии, содержащей GSCN в конечной концентрации, составляющей приблизительно 2-4 M; PEG, имеющий молекулярную массу, составляющей от приблизительно 4000 г/моль до приблизительно 8000 г/моль, например, приблизительно 6000 г/моль (например, PEG-6000), в конечной концентрации, составляющей от приблизительно 5% до приблизительно 20% (вес/объем); и вспомогательное фильтрующее средство (например, фильтрующее средство на основе целлюлозы) при массовом соотношении с осажденной mRNA, составляющем приблизительно 2:1; приблизительно 5:1; приблизительно 10:1 или приблизительно 15:1. В некоторых вариантах осуществления mRNA осаждают в суспензии, содержащей GSCN в конечной концентрации, составляющей приблизительно 2,5-3 M; PEG, имеющий молекулярную массу, составляющую приблизительно 6000 г/моль (например, PEG-6000), в конечной концентрации, составляющей от приблизительно 10% до приблизительно 15% (вес/объем); и вспомогательное фильтрующее средство (например, фильтрующее средство на основе целлюлозы) при массовом соотношении с осажденной mRNA, составляющем приблизительно 10:1. В конкретных вариантах осуществления mRNA осаждают в суспензии, содержащей GSCN в конечной концентрации, составляющей приблизительно 2,7 M; PEG, имеющий молекулярную массу, составляющую приблизительно 6000 г/моль (например, PEG-6000), в конечной концентрации, составляющей приблизительно 12% (вес/объем); и вспомогательное фильтрующее средство (например, фильтрующее средство на основе целлюлозы, например, Solka-Floc) при массовом соотношении с осажденной mRNA, составляющем приблизительно 10:1. Как показано в примерах, суспензии, содержащие mRNA, соли и PEG в данных концентрациях, обеспечивают высокоэффективную очистку mRNA без осаждения ферментов, применяемых в способе.
[169] В некоторых вариантах осуществления можно применять MTEG вместо PEG с получением суспензии осажденной mRNA. В конкретных вариантах осуществления с данной целью применяют MTEG в конечной концентрации, составляющей от приблизительно 15% до приблизительно 45% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей от приблизительно 20% до приблизительно 40% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 20% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 25% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 30% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей приблизительно 35% вес/объем. В некоторых вариантах осуществления суспензия содержит MTEG в конечной концентрации, составляющей менее чем 35% вес/объем. Остальные условия, применяемые при осаждении, индуцируемом MTEG, представляют собой те же условия, которые применяются при осаждении, индуцируемом PEG. Как показано в примерах, суспензия, содержащая mRNA, GSCN и MTEG, где MTEG содержится в конечной концентрации, составляющей менее чем 35% вес/объем, обеспечивала эффективное извлечение mRNA без нежелательного осаждения ферментов, применяемых в способе. Особенно предпочтительной для эффективного извлечения mRNA без нежелательного осаждения ферментов, применяемых в способе, является суспензия, содержащая mRNA, GSCN и MTEG, где MTEG содержится в конечной концентрации, составляющей приблизительно 25%, в дополнение к вспомогательному фильтрующему средству (например, вспомогательному фильтрующему средству на основе целлюлозы), при массовом соотношении с осажденной mRNA, составляющем приблизительно 10:1.
[170] Например, можно обеспечить GSCN в виде 4-8 M раствора (например, в буфере, содержащем 10 мМ DTT), который затем объединяют с mRNA и MTEG с получением суспензии осажденной mRNA. В некоторых вариантах осуществления суспензия содержит осажденную mRNA, хаотропную соль, например, GSCN, и MTEG при объемном соотношении, составляющем 1:2-3:1-2. В некоторых вариантах осуществления суспензия содержит осажденную mRNA, хаотропную соль, например, GSCN, и MTEG при объемном соотношении, составляющем 1:2-2,5:1-2. В некоторых вариантах осуществления суспензия содержит осажденную mRNA, хаотропную соль, например, GSCN, и MTEG при объемном соотношении, составляющем 1:2,3:1-2. В конкретных вариантах осуществления суспензия содержит осажденную mRNA, GSCN и MTEG при соотношении, составляющем 1:2,3:2. В конкретных вариантах осуществления суспензия содержит осажденную mRNA, GSCN и MTEG при объемном соотношении, составляющем 1:2,3:1,7. В конкретных вариантах осуществления суспензия содержит осажденную mRNA, GSCN и MTEG при соотношении, составляющем 1:2,3:1. Как показано в примерах, суспензия, содержащая mRNA, GSCN и MTEG при объемных соотношениях, составляющих 1:2,3:1, 1:2,3:1,7 и 1:2,3:2, особенно предпочтительна в способе очистки, индуцированной полимером, в комбинации с раствором для промывания на основе MTEG в конечной концентрации, составляющей приблизительно 95%; данная комбинация стадий обеспечивает эффективное извлечение mRNA без нежелательного осаждения в ходе осуществления способа.
Захватывание mRNA
[171] Другая стадия способа очистки mRNA, описанного в данном документе, включает захватывание mRNA. Различные способы захватывания mRNA известны из уровня техники. В некоторых вариантах осуществления неочищенный препарат, содержащий осажденную mRNA, подвергают способу очистки, включающему мембранную фильтрацию, таким образом, что осажденная mRNA захватывается или удерживается с помощью мембраны или фильтра. Таким образом, в некоторых вариантах осуществления неочищенный препарат подвергают мембранной фильтрации после осаждения без предварительной обработки с удалением нерастворимых веществ.
[172] Для захватывания или удержания осажденной mRNA можно применять различные типы мембранной фильтрации. Как правило, мембранная фильтрация включает отделение твердых частиц от текучих сред с применением одной или более промежуточных проницаемых мембран. Мембранную фильтрацию также можно применять для фильтрации частиц из газообразного образца. В целом, существуют две основных формы мембранной фильтрации: пассивная фильтрация, которая осуществляется исключительно за счет диффузии раствора, и активная фильтрация, при которой применяется положительное или отрицательное давление (т. е. вакуум) для обеспечения прохождения жидкости или газа через мембрану. Как правило, мембранная фильтрация включает стадии загрузки, промывания и элюирования.
[173] Захватывание mRNA с помощью фильтра включает загрузку раствора, содержащего осажденную mRNA, на мембрану или фильтр. Данную стадию обычно называют стадией загрузки. Стадия загрузки включает загрузку исходной смеси (например, неочищенного препарата, содержащего осажденную mRNA) на мембрану или фильтр и обеспечение ее прохождения насквозь за счет положительного или отрицательного давления, в результате чего ретентат остается захваченным или удержанным на мембране. Используемый в данном документе термин «ретентат» относится к любому непроникающему растворенному веществу и/или нерастворимому веществу, которое удерживается мембраной. В соответствии с настоящим изобретением осажденная mRNA захватывается мембраной в виде ретентата. Используемый в данном документе термин «мембрана» или «фильтр» относится к любому пористому слою или листу материала. В настоящей заявке термин «мембрана» используется взаимозаменяемо с термином «фильтр».
[174] В некоторых вариантах осуществления подходящая мембрана имеет размер пор, требуемый для захватывания или удержания осажденной mRNA, при этом позволяющий примесям (включая растворимые примеси и/или нерастворимые примеси, имеющие размер, меньший чем размер поры) проходить насквозь в виде пермеата. В некоторых вариантах осуществления подходящая мембрана имеет средний размер пор, равный или превышающий приблизительно 0,10 мкм, 0,20 мкм, 0,22 мкм, 0,24 мкм, 0,26 мкм, 0,28 мкм, 0,30 мкм, 0,40 мкм, 0,5 мкм или 1,0 мкм. В конкретном варианте осуществления подходящая мембрана имеет средний размер пор, составляющий приблизительно 0,22 мкм. В некоторых вариантах осуществления подходящая мембрана имеет средний размер пор, составляющий приблизительно 1,0 мкм, 1,5 мкм, 2,0 мкм, 2,5 мкм, 3,0 мкм, 3,5 мкм, 4,0 мкм, 4,5 мкм, 5,0 мкм, 5,5 мкм, 6,0 мкм, 6,5 мкм, 7,0 мкм, 7,5 мкм, 8,0 мкм, 8,5 мкм, 9,0 мкм, 9,5 мкм и 10 мкм. В некоторых вариантах осуществления, например, для применения при фильтрации в нормальном потоке (NFF) или глубинной фильтрации, подходящая мембрана имеет средний размер пор, составляющий от приблизительно 5 мкм до приблизительно 8 мкм. В некоторых вариантах осуществления подходящая мембрана для применения при NFF или глубинной фильтрации имеет средний размер пор, составляющий 7 мкм. В некоторых вариантах осуществления, например, для применения при фильтрации с помощью центрифуги, подходящая мембрана имеет средний размер пор, составляющий от приблизительно 0,5 мкм до приблизительно 2,0 мкм. В некоторых вариантах осуществления подходящая мембрана для применения при фильтрации с помощью центрифуги представляет собой приблизительно 1 мкм. В некоторых вариантах осуществления требуемый размер пор для удержания осажденной mRNA может определяться номинальными пределами молекулярной массы (NMWL) осажденной mRNA, также называемыми отсечкой по молекулярной массе (MWCO). Как правило, применяют мембрану с размером пор, составляющим менее чем NMWL или MWCO осажденной mRNA. В некоторых вариантах осуществления применяют мембрану с размером пор, в два-шесть (например, в 2, 3, 4, 5 или 6) раз меньшим чем NMWL или MWCO осажденной mRNA. В некоторых вариантах осуществления подходящая мембрана по настоящему изобретению может иметь размер пор, равный или превышающий приблизительно 100 килодальтон (кДа), 300 кДа, 500 кДа, 1000 кДа, 1500 кДа, 2000 кДа, 2500 кДа, 3000 кДа, 3500 кДа, 4000 кДа, 4500 кДа, 5000 кДа, 5500 кДа, 6000 кДа, 6500 кДа, 7000 кДа, 7500 кДа, 8000 кДа, 8500 кДа, 9000 кДа, 9500 кДа или 10000 кДа. В некоторых вариантах осуществления мембрана имеет размер пор, больший чем NMWL и MWCO mRNA, но меньший чем NMWL и MWCO осажденной mRNA. Соответственно, в определенных вариантах осуществления настоящее изобретение предусматривает способ очистки mRNA, включающий осаждение mRNA в суспензии, содержащей высокомолярный раствор соли и полимер PEG для получения осажденной mRNA в суспензии, захватывание осажденной mRNA с помощь фильтра, имеющего размер пор, больший чем NMWL и MWCO mRNA, но меньший чем NMWL и MWCO осажденной mRNA; и промывание захваченной и осажденной mRNA с получением композиции на основе очищенной mRNA, которая по сути не содержит загрязняющих примесей.
[175] Подходящая мембрана для настоящего изобретения может быть получена из любого материала. Иллюстративные материалы для мембраны включают без ограничения полиэфирсульфон (mPES) (немодифицированный), мембрану из полых волокон полиэфирсульфона (mPES), поливинилиденфторид (PVDF), ацетат целлюлозы, нитроцеллюлозу, MCE (смешанные эфиры целлюлозы), полиэтилен со сверхвысокой MW (UPE), полифтортетраэтилен (PTFE), нейлон, полисульфон, полиэфирсульфон, полиакрилонитрил, полипропилен, поливинилхлорид и их комбинации. В конкретных вариантах осуществления мембрана представляет собой полипропиленовый фильтр со средним размером пор, составляющим приблизительно 1,0 мкм.
[176] Подходящая мембрана для настоящего изобретения может иметь различную площадь поверхности. В некоторых вариантах осуществления подходящая мембрана имеет достаточно большую площадь поверхности для обеспечения крупномасштабного получения mRNA. Например, подходящая мембрана может иметь площадь поверхности, равную или превышающую приблизительно 2000 см2, 2500 см2, 3000 см2, 3500 см2, 4000 см2, 4500 см2, 5000 см2, 7500 см2, 10000 см2, 5 м2, 10 м2, 12 м2, 15 м2, 20 м2, 24 м2, 25 м2, 30 м2 или 50 м2.
[177] Мембранную фильтрацию можно осуществлять в различном формате для захватывания осажденной mRNA. В некоторых вариантах осуществления мембранную фильтрацию осуществляют как часть фильтрации в тангенциальном потоке (TFF). В некоторых вариантах осуществления мембранная фильтрация включает фильтрацию в нормальном потоке (NFF) или глубинную фильтрацию. В некоторых вариантах осуществления мембранная фильтрация включает фильтрацию с помощью центрифуги.
Вспомогательные фильтрующие средства (в том числе диспергирующие средства)
[178] В некоторых вариантах осуществления в описанных в данном документе способах применяют вспомогательное фильтрующее средство. Вспомогательное фильтрующее средство можно применять при очистке осажденной mRNA с применением фильтрующей центрифуги. Вспомогательное фильтрующее средство может способствовать удержанию осажденной mRNA с помощью фильтра фильтрующей центрифуги и обеспечивать возможность удаления удерживаемой mRNA с поверхности фильтра фильтрующей центрифуги.
[179] В некоторых вариантах осуществления вспомогательное фильтрующее средство представляет собой диспергирующее средство. В некоторых вариантах осуществления вспомогательное фильтрующее средство включает одно или более из золы, глины, диатомовой земли, перлита, стеклянных гранул, пластмассовых гранул, полимеров, полипропиленовых гранул, полистироловых гранул, солей (например, солей целлюлозы), песка, вулканического пепла, диатомовой земли и/или сахаров. В некоторых вариантах осуществления диспергирующее средство представляет собой гранулу. В некоторых вариантах осуществления композиция на основе осажденной mRNA не содержит диспергирующее средство.
[180] В некоторых вариантах осуществления стадию добавления одного или более средств, которые способствуют осаждению mRNA, осуществляют в отсутствие каких-либо диспергирующих средств.
[181] В некоторых вариантах осуществления стадию добавления одного или более средств, которые способствуют осаждению mRNA, осуществляют в присутствии по меньшей мере одного диспергирующего средства.
[182] В некоторых вариантах осуществления диспергирующее средство добавляют к суспензии, полученной после добавления одного или более средств, которые способствуют осаждению mRNA.
[183] Таким образом, в некоторых вариантах осуществления способ очистки может дополнительно включать одну или более стадий отделения диспергирующего средства от очищенного осадка mRNA, например, промывание и высушивание осадка на фильтре. Способ может дополнительно включать стадию солюбилизирования и элюирования очищенной mRNA из осадка на фильтре с применением водной среды, например, воды, в ходе фильтрования диспергирующего средства. В вариантах осуществления стадию осаждения и стадию высушивания можно осуществлять одновременно.
[184] В вариантах осуществления вспомогательное фильтрующее средство представляет собой целлюлозу. В вариантах осуществления вспомогательное фильтрующее средство на основе целлюлозы представляет собой порошковое целлюлозное волокно (например, Solka-Floc® или Sigmacell Cellulose 20). В вариантах осуществления вспомогательное фильтрующее средство на основе целлюлозы представляет собой порошковое целлюлозное волокно, такое как Solka-Floc® 200 NF или целлюлоза Sigmacell Cellulose Type 20 (20 мкм). В некоторых вариантах осуществления вспомогательное фильтрующее средство представляет собой вулканический пепел. В некоторых вариантах осуществления вспомогательное фильтрующее средство представляет собой диатомовую землю.
[185] В некоторых вариантах осуществления осажденная mRNA и вспомогательное фильтрующее средство (например, порошковое целлюлозное волокно, такое как Solka Floc) содержатся при массовом соотношении, составляющем 1:2; 1:5; 1:10 или 1:15. В конкретных вариантах осуществления осажденная mRNA и вспомогательное фильтрующее средство (например, порошковое целлюлозное волокно, такое как Solka Floc) содержатся при массовом соотношении, составляющем 1:10.
Промывание захваченной mRNA
[186] Способ очистки mRNA также включает промывание захваченной нерастворимой mRNA перед элюированием с удалением примесей, сохраняющихся на мембране.
[187] В некоторых вариантах осуществления на стадии промывания применяют амфифильный полимер. В некоторых вариантах осуществления амфифильный полимер представляет собой полиэтиленгликоль (PEG). Соответственно, в некоторых вариантах осуществления раствор PEG («раствор PEG для промывания») применяют для промывания захваченной mRNA. Раствор PEG для промывания включает триэтиленгликоль, тетраэтиленгликоль, PEG 200, PEG 300, PEG 400, PEG 600, PEG 1000, PEG 1500, PEG 2000, PEG 3000, PEG 3350, PEG 4000, PEG 6000, PEG 8000, PEG 10000, PEG 20000, PEG 35000 и PEG 40000 или их комбинацию. В некоторых вариантах осуществления раствор PEG для промывания содержит триэтиленгликоль. В некоторых вариантах осуществления раствор PEG для промывания содержит тетраэтиленгликоль. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 200. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 300. В некоторых вариантах осуществления раствор для промывания PEG содержит PEG 400. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 600. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 1000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 1500. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 2000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 3000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 3350. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 4000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 6000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 8000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 10000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 20000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 35000. В некоторых вариантах осуществления раствор PEG для промывания содержит PEG 40000. В некоторых вариантах осуществления промывание осажденной mRNA включает одно или более промываний, предусматривающих PEG, который имеет вязкость, составляющую 90 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый для промывания осажденной mRNA, имеет вязкость, составляющую 80 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый для промывания осажденной mRNA, имеет вязкость, составляющую 70 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый для промывания осажденной mRNA, имеет вязкость, составляющую 60 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый для промывания осажденной mRNA, имеет вязкость, составляющую 50 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый для промывания осажденной mRNA, имеет вязкость, составляющую 40 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый для промывания осажденной mRNA, имеет вязкость, составляющую 30 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый для промывания осажденной mRNA, имеет вязкость, составляющую 20 сантистоксов или меньше. В некоторых вариантах осуществления PEG, применяемый для промывания осажденной mRNA, имеет вязкость, составляющую 10 сантистоксов или меньше. В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением триэтиленгликоля (TEG). В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением монометилового эфира триэтиленгликоля (MTEG). В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением трет-бутил-TEG-O-пропионата. В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением диметакрилата TEG. В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением диметилового эфира TEG. В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением дивинилового эфира TEG. В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением монобутилового эфира TEG. В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением метакрилата метилового эфира TEG. В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением монодецилового эфира TEG. В некоторых вариантах осуществления промывание осажденной mRNA может быть достигнуто с применением дибензоата TEG. Структуры каждого из данных реагентов показаны выше в таблице A.
[188] Вязкость жидкого раствора можно измерить с применением способов, хорошо известных из уровня техники, например, с применением вискозиметра при комнатной температуре (например, от приблизительно 18°C до 25°C).
[189] В некоторых вариантах осуществления PEG в растворе PEG для промывания предусматривает липид, модифицированный PEG. В некоторых вариантах осуществления PEG в растворе PEG для промывания представляет собой липид, модифицированный PEG, 1,2-димиристоил-sn-глицерин, метоксиполиэтиленгликоль (DMG-PEG-2K). В некоторых вариантах осуществления липид, модифицированный PEG, представляет собой конъюгат DOPA-PEG. В некоторых вариантах осуществления липид, модифицированный PEG, представляет собой конъюгат полоксамер-PEG. В некоторых вариантах осуществления липид, модифицированный PEG, содержит DOTAP. В некоторых вариантах осуществления липид, модифицированный PEG, содержит холестерин.
[190] В некоторых вариантах осуществления раствор PEG для промывания содержит смесь полимеров PEG двух или более видов с различной молекулярной массой. Например, в некоторых вариантах осуществления раствор PEG для промывания состоит из полимеров PEG двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати или двенадцати видов с различной молекулярной массой. Соответственно, в некоторых вариантах осуществления раствор PEG для промывания содержит смесь одного или более полимеров PEG. В некоторых вариантах осуществления смесь полимеров PEG содержит полимеры, имеющие различные молекулярные массы.
[191] PEG, применяемый в растворе PEG для промывания, может иметь различные геометрические конфигурации. Например, подходящие полимеры PEG включают полимеры PEG, имеющие линейную, разветвленную, Y-образную или многолучевую конфигурацию. В некоторых вариантах осуществления PEG содержится в суспензии, содержащей один или более PEG, имеющих различные геометрические конфигурации.
[192] В некоторых вариантах осуществления PEG в растворе для промывания содержится в концентрации, составляющей от приблизительно 10% до приблизительно 100% вес/объем. Например, в некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 100% вес/объем, включая любые промежуточные значения. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 10% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 15% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 20% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 25% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 30% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 35% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 40% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 45% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 50% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 55% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 60% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 65% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 70% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 75% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 80% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 85% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 90% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 95% вес/объем. В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей приблизительно 100% вес/объем.
[193] В некоторых вариантах осуществления буфер для промывания содержит PEG-400 в концентрации, составляющей приблизительно от 80% до 100%. Соответственно, в некоторых вариантах осуществления буфер для промывания содержит PEG-400 в концентрации, составляющей приблизительно 80%. В некоторых вариантах осуществления буфер для промывания содержит PEG-400 в концентрации, составляющей приблизительно 85%. В некоторых вариантах осуществления буфер для промывания содержит PEG-400 в концентрации, составляющей приблизительно 90%. В некоторых вариантах осуществления буфер для промывания содержит PEG-400 в концентрации, составляющей приблизительно 95%. В некоторых вариантах осуществления буфер для промывания содержит PEG-400 в концентрации, составляющей приблизительно 100%.
[194] В некоторых вариантах осуществления осажденную mRNA промывают в растворе, содержащем амфифильный полимер. В некоторых вариантах осуществления амфифильный полимер представляет собой PEG. Осажденную mRNA можно промывать 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более чем 10 раз. Соответственно, в некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, один раз. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, два раза. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, три раза. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, четыре раза. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, пять раз. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, шесть раз. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, семь раз. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, восемь раз. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, девять раз. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, десять раз. В некоторых вариантах осуществления осажденную mRNA промывают раствором, содержащим полимер PEG, более десяти раз.
[195] В некоторых вариантах осуществления раствор для промывания, применяемый для промывания захваченной mRNA, является водным. Соответственно, в некоторых вариантах осуществления раствор для промывания не содержит спирт, такой как этанол, изопропиловый спирт или бензиловый спирт.
[196] В некоторых вариантах осуществления раствор для промывания PEG содержит неводный компонент, такой как, например, этанол, изопропиловый спирт или бензиловый спирт.
[197] В некоторых вариантах осуществления стадия промывания включает несколько циклов полоскания с применением раствора, содержащего амфифильный полимер (например, полиэтиленгликоль). В некоторых вариантах осуществления стадия промывания включает несколько полосканий с применением раствора, содержащего один или более отдельных амфифильных полимеров. В некоторых вариантах осуществления стадию промывания можно осуществлять с помощью нескольких циклов полоскания с применением раствора, содержащего от приблизительно 10% до приблизительно 100% амфифильного полимера. В определенных вариантах осуществления несколько циклов полоскания предусматривают 2 цикла, 3 цикла, 4 цикла, 5 циклов, 6 циклов, 7 циклов, 8 циклов, 9 циклов, 10 циклов или более 10 циклов.
[198] В некоторых вариантах осуществления PEG содержится в растворе для промывания в концентрации, составляющей от приблизительно 90% до приблизительно 100% вес/объем. В конкретных вариантах осуществления PEG (например, PEG-400) содержится в растворе для промывания в концентрации, составляющей приблизительно 90% вес/объем. Как показано в примерах, конечная концентрация PEG, имеющего молекулярную массу приблизительно 400 г/моль (например, PEG-400), составляющая от приблизительно 90% до приблизительно 100% вес/объем, особенно предпочтительна для стадии промывания, поскольку применение данного раствора для промывания приводило к получению образцов mRNA с высоким выходом и высокой степенью чистоты.
[199] В некоторых вариантах осуществления MTEG содержится в растворе для промывания в концентрации, составляющей от приблизительно 75% до приблизительно 95% вес/объем. В некоторых вариантах осуществления MTEG содержится в растворе для промывания в концентрации, составляющей приблизительно 75%, приблизительно 80%, приблизительно 85%, приблизительно 90% или приблизительно 95% вес/объем. В некоторых вариантах осуществления MTEG содержится в растворе для промывания в концентрации, составляющей от приблизительно 90% до приблизительно 100% вес/объем. В конкретных вариантах осуществления MTEG содержится в растворе для промывания в концентрации, составляющей приблизительно 95% вес/объем. Как показано в примерах, конечная концентрация MTEG, составляющая приблизительно 90% или приблизительно 95% вес/объем, особенно предпочтительна для стадии промывания, поскольку при данных конечных концентрациях достигалось высокоэффективное извлечение mRNA без осаждения ферментов, применяемых в способе.
Элюирование или сбор
[200] Как правило, захваченную или удержанную mRNA можно элюировать или собирать посредством повторного солюбилизирования осажденной mRNA с получением раствора. Например, захваченную mRNA можно элюировать с применением воды, не содержащей РНКазу. В определенных вариантах осуществления элюирование захваченной mRNA включает рециркуляцию воды, не содержащей РНКазу. Например, воду, не содержащую РНКазу, можно подвергать циркуляции в течение приблизительно 5-30 минут (например, приблизительно 5-25 минут, приблизительно 5-20 минут или приблизительно 5-15 минут). В конкретных вариантах осуществления воду, не содержащую РНКазу, подвергают рециркуляции в течение приблизительно 5-10 минут (например, в течение приблизительно 5, 6, 7, 8, 9 или 10 минут). Для повторного солюбилизирования mRNA можно применять другие буферы, такие как TE и/или цитрат натрия. Термин «элюирование» можно использовать в контексте способов очистки, которые включают, например, глубинную фильтрацию, тогда как термин «сбор» можно использовать в контексте способов очистки, которые включают центрифугирование.
[201] В некоторых вариантах осуществления повторно солюбилизированную mRNA можно подвергать диализу с получением требуемого состава в требуемой концентрации. Для диализа можно применять различные составы. В некоторых вариантах осуществления раствор очищенной mRNA подвергают диализу с применением 1 мМ цитрата натрия. В некоторых вариантах осуществления раствор очищенной mRNA подвергают диализу с применением ацетата натрия, карбоната аммония, бикарбоната аммония, ацетата пиридиния, формиата пиридиния, ацетата аммония, мочевины, хлорида калия и т. д. В зависимости от размера mRNA, представляющей интерес, можно применять мембраны для диализа с соответствующей отсечкой по молекулярной массе (MWCO). Например, подходящие мембраны для диализа могут иметь MWCO, составляющую приблизительно 50 кДа, 60 кДа, 70 кДа, 80 кДа, 90 кДа, 100 кДа, 150 кДа, 200 кДа, 250 кДа, 300 кДа, 350 кДа, 400 кДа, 450 кДа или 500 кДа.
Масштаб и извлекаемые количества
[202] Конкретное преимущество, обеспечиваемое настоящим изобретением, представляет собой возможность очищать mRNA, в частности, mRNA, синтезированную in vitro, в крупном или коммерческом масштабе. Например, в некоторых вариантах осуществления mRNA, синтезированную in vitro, очищают в масштабе, равном или превышающем приблизительно 100 миллиграммов, 1 грамм, 10 граммов, 50 граммов, 100 граммов, 200 граммов, 300 граммов, 400 граммов, 500 граммов, 600 граммов, 700 граммов, 800 граммов, 900 граммов, 1 кг, 5 кг, 10 кг, 50 кг, 100 кг, одну метрическую тонну, десять метрических тонн или более на партию. В вариантах осуществления mRNA, синтезированную in vitro, очищают в масштабе, равном или превышающем приблизительно 1 кг.
[203] В одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 10 граммов на партию. В одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 20 граммов на партию. В одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 25 граммов на партию. В одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 50 граммов на партию. В другом конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 100 граммов на партию. В еще одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 1 кг на партию. В еще одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 10 кг на партию. В еще одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 100 кг на партию. В еще одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 1000 кг на партию. В еще одном конкретном варианте осуществления mRNA, синтезированную in vitro, очищают в масштабе, составляющем 10000 кг на партию.
[204] В некоторых вариантах осуществления mRNA очищают в масштабе, равном или превышающем 1 граммов, 5 граммов, 10 граммов, 15 граммов, 20 граммов, 25 граммов, 30 граммов, 35 граммов, 40 граммов, 45 граммов, 50 граммов, 75 граммов, 100 граммов, 150 граммов, 200 граммов, 250 граммов, 300 граммов, 350 граммов, 400 граммов, 450 граммов, 500 граммов, 550 граммов, 600 граммов, 650 граммов, 700 граммов, 750 граммов, 800 граммов, 850 граммов, 900 граммов, 950 граммов, 1 кг, 2,5 кг, 5 кг, 7,5 кг, 10 кг, 25 кг, 50 кг, 75 кг, 100 кг или более на партию.
[205] В некоторых вариантах осуществления раствор, содержащий mRNA, включает по меньшей мере один грамм, десять граммов, сто граммов, один килограмм, десять килограммов, сто килограммов, одну метрическую тонну, десять метрических тонн или более mRNA, или любое промежуточное количество. В некоторых вариантах осуществления способ, описанный в данном документе, применяют для очистки mRNA в количестве, которое составляет по меньшей мере приблизительно 250 мг mRNA. В одном варианте осуществления способ, описанный в данном документе, применяют для очистки mRNA в количестве, которое составляет по меньшей мере приблизительно 250 мг mRNA, приблизительно 500 мг mRNA, приблизительно 750 мг mRNA, приблизительно 1000 мг mRNA, приблизительно 1500 мг mRNA, приблизительно 2000 мг mRNA или приблизительно 2500 мг mRNA. В вариантах осуществления способ, описанный в данном документе, применяют для очистки mRNA в количестве, которое составляет по меньшей мере от приблизительно 250 мг mRNA до приблизительно 500 г mRNA. В вариантах осуществления способ, описанный в данном документе, применяют для очистки mRNA в количестве, которое составляет по меньшей мере от приблизительно 500 мг mRNA до приблизительно 250 г mRNA, от приблизительно 500 мг mRNA до приблизительно 100 г mRNA, от приблизительно 500 мг mRNA до приблизительно 50 г mRNA, от приблизительно 500 мг mRNA до приблизительно 25 г mRNA, от приблизительно 500 мг mRNA до приблизительно 10 г mRNA или от приблизительно 500 мг mRNA до приблизительно 5 г mRNA. В вариантах осуществления способ, описанный в данном документе, применяют для очистки mRNA в количестве, которое составляет по меньшей мере от приблизительно 100 мг mRNA до приблизительно 10 г mRNA, от приблизительно 100 мг mRNA до приблизительно 5 г mRNA или от приблизительно 100 мг mRNA до приблизительно 1 г mRNA.
[206] В некоторых вариантах осуществления способ, описанный в данном документе, обеспечивает извлекаемое количество очищенной mRNA (или «выход»), которое составляет по меньшей мере приблизительно 40%, 45%, 50%, приблизительно 55%, приблизительно 60%, приблизительно 65%, приблизительно 70%, приблизительно 75%, приблизительно 80%, приблизительно 85%, приблизительно 90%, приблизительно 95% приблизительно 97%, приблизительно 98%, приблизительно 99% или приблизительно 100%. Соответственно, в некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 40%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 45%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 50%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 55%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 60%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 65%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 70%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 75%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 75%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 80%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 85%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 90%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 91%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 92%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 93%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 94%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 95%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 96%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 97%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 98%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 99%. В некоторых вариантах осуществления извлекаемое количество очищенной mRNA составляет приблизительно 100%.
[207] В конкретных вариантах осуществления извлекаемое количество очищенной mRNA составляет более чем приблизительно 80% или более чем приблизительно 90%, например, от приблизительно 90% до 100%.
Определение характеристик очищенной mRNA
[208] Способы очистки mRNA, предусмотренные в данном документе, приводят к получению композиции на основе очищенной mRNA, которая по сути не содержит загрязняющих примесей, содержащих короткие молекулы абортивной РНК, длинные молекулы абортивной РНК, двухцепочечную РНК (dsRNA), остаточную плазмидную ДНК, остаточные ферменты транскрипции in vitro, остаточный растворитель и/или остаточную соль.
[209] Способы, описанные в данном документе, приводят к получению очищенной mRNA, которая характеризуется чистотой, составляющей от приблизительно 60% до приблизительно 100%. Соответственно, в некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 60%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 65%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 70%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 75%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 80%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 85%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 90%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 91%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 92%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 93%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 94%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 95%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 96%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 97%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 98%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 99%. В некоторых вариантах осуществления очищенная mRNA характеризуется чистотой, составляющей приблизительно 100%.
[210] В некоторых вариантах осуществления mRNA, полученная посредством способа, описанного в данном документе, характеризуется менее чем 10%, менее чем 9%, менее чем 8%, менее чем 7%, менее чем 6%, менее чем 5%, менее чем 4%, менее чем 3%, менее чем 2%, менее чем 1%, менее чем 0,5% и/или менее чем 0,1% примесей, отличных от полноразмерной mRNA. Примеси включают загрязняющие примеси IVT, например, белки, ферменты, ДНК-матрицы, свободные нуклеотиды, остаточный растворитель, остаточную соль, двухцепочечную РНК (dsRNA), преждевременно прерванные последовательности РНК («шортмеры» или «короткие молекулы абортивной РНК») и/или длинные молекулы абортивной РНК. В некоторых вариантах осуществления очищенная mRNA по сути не содержит ферменты, применяемые в способе.
[211] В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 1 пг/мг, менее чем приблизительно 2 пг/мг, менее чем приблизительно 3 пг/мг, менее чем приблизительно 4 пг/мг, менее чем приблизительно 5 пг/мг, менее чем приблизительно 6 пг/мг, менее чем приблизительно 7 пг/мг, менее чем приблизительно 8 пг/мг, менее чем приблизительно 9 пг/мг, менее чем приблизительно 10 пг/мг, менее чем приблизительно 11 пг/мг или менее чем приблизительно 12 пг/мг. Соответственно, уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 1 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 2 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 3 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 4 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 5 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 6 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 7 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 8 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 9 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 10 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 11 пг/мг. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК в mRNA, очищенной с применением способов очистки, описанных в данном документе, составляет менее чем приблизительно 12 пг/мг.
[212] В некоторых вариантах осуществления настоящее изобретение обеспечивает удаление или устранение в высокой степени преждевременно прерванных последовательностей РНК (также известных как «шортмеры»). В некоторых вариантах осуществления способ по настоящему изобретению обеспечивает удаление более чем приблизительно 90%, 95%, 96%, 97%, 98%, 99% или по сути всех преждевременно прерванных последовательностей РНК. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, по сути не содержит преждевременно прерванных последовательностей РНК. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, содержит менее чем приблизительно 5% (например, менее чем приблизительно 4%, 3%, 2% или 1%) преждевременно прерванных последовательностей РНК. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, содержит менее чем приблизительно 1% (например, менее чем приблизительно 0,9%, 0,8%, 0,7%, 0,6%, 0,5%, 0,4%, 0,3%, 0,2% или 0,1%) преждевременно прерванных последовательностей РНК. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, содержит не поддающиеся выявлению преждевременно прерванные последовательности РНК, что установлено, например, с помощью высокоэффективной жидкостной хроматографии (HPLC) (например, плечи пиков или отдельные пики), бромида этидия, окрашивания Кумасси, капиллярного электрофореза или гель-электрофореза с денатурацией глиоксалем (например, наличие отдельной полосы снизу). Используемые в данном документе термины «шортмеры», «короткие молекулы абортивной РНК», «преждевременно прерванные последовательности РНК» или «длинные молекулы абортивной РНК» относятся к любым транскриптам, длина которых меньше полноразмерной длины. В некоторых вариантах осуществления длина «шортмеров», «коротких молекул абортивной РНК» или «преждевременно прерванных последовательностей РНК» составляет менее чем 100 нуклеотидов, менее чем 90 нуклеотидов, менее чем 80 нуклеотидов, менее чем 70 нуклеотидов, менее чем 60 нуклеотидов, менее чем 50 нуклеотидов, менее чем 40 нуклеотидов, менее чем 30 нуклеотидов, менее чем 20 нуклеотидов или менее чем 10 нуклеотидов. В некоторых вариантах осуществления шортмеры выявляют или подвергают количественному определению после добавления 5’-кэпа и/или 3’-поли-A-хвоста. В некоторых вариантах осуществления преждевременно прерванные транскрипты РНК содержат менее чем 15 оснований (например, менее чем 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4 или 3 оснований). В некоторых вариантах осуществления преждевременно прерванные транскрипты РНК содержат приблизительно 8-15, 8-14, 8-13, 8-12, 8-11 или 8-10 оснований.
[213] В некоторых вариантах осуществления способ по настоящему изобретению обеспечивает удаление или устранение в высокой степени ферментных реагентов, применяемых в синтезе in vitro, в том числе без ограничения РНК-полимеразы T7, ДНКазы I, пирофосфатазы и/или ингибитора РНКазы. В некоторых вариантах осуществления настоящее изобретение является особенно эффективным в отношении удаления РНК-полимеразы T7. В некоторых вариантах осуществления способ по настоящему изобретению обеспечивает удаление более чем приблизительно 90%, 95%, 96%, 97%, 98%, 99% или по сути всех ферментных реагентов, в том числе таковых, применяемых в синтезе in vitro. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, по сути не содержит ферментных реагентов, в том числе таковых, применяемых в синтезе in vitro. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, содержит менее чем приблизительно 5% (например, менее чем приблизительно 4%, 3%, 2% или 1%) ферментных реагентов, в том числе таковых, применяемых в синтезе in vitro. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, содержит менее чем приблизительно 1% (например, менее чем приблизительно 0,9%, 0,8%, 0,7%, 0,6%, 0,5%, 0,4%, 0,3%, 0,2% или 0,1%) ферментных реагентов, в том числе таковых, применяемых в синтезе in vitro. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, содержит не поддающиеся выявлению ферментные реагенты, в том числе таковые, применяемые в синтезе in vitro, что установлено, например, с помощью окрашивания серебром, гель-электрофореза, высокоэффективной жидкостной хроматографии (HPLC), сверхвысокоэффективной жидкостной хроматографии (UPLC) и/или капиллярного электрофореза, бромида этидия и/или окрашивания Кумасси.
[214] В различных вариантах осуществления mRNA, очищенная с применением способа, описанного в данном документе, сохраняет высокую степень целостности. Используемый в данном документе термин «целостность mRNA» обычно относится к качеству mRNA после очистки. Целостность mRNA можно определить с применением способов, хорошо известных из уровня техники, например, посредством электрофореза РНК в агарозном геле. В некоторых вариантах осуществления целостность mRNA можно определить по распределению полос при электрофорезе РНК в агарозном геле. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, демонстрирует слабое образование полос или отсутствие полос по сравнению с эталонной полосой при электрофорезе РНК в агарозном геле. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, характеризуется целостностью, составляющей более чем приблизительно 95% (например, более чем приблизительно 96%, 97%, 98%, 99% или более). В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, характеризуется целостностью, составляющей более чем 98%. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, характеризуется целостностью, составляющей более чем 99%. В некоторых вариантах осуществления mRNA, очищенная способом по настоящему изобретению, характеризуется целостностью, составляющей приблизительно 100%. В некоторых вариантах осуществления способ, описанный в данном документе, обеспечивает получение композиции, обладающей повышенной активностью, например, по меньшей мере двукратной, трехкратной, четырехкратной, пятикратной или более, транслируемых полипептидов по сравнению с композицией, содержащей более низкую процентную долю полноразмерных молекул mRNA.
[215] В некоторых вариантах осуществления очищенную mRNA оценивают по одной или более из следующих характеристик: внешний вид, идентичность, количество, концентрация, наличие примесей, микробиологическая оценка, уровень pH и активность. В некоторых вариантах осуществления приемлемый внешний вид предусматривает прозрачный бесцветный раствор, практически не содержащий видимых частиц. В некоторых вариантах осуществления идентичность mRNA оценивают посредством способов секвенирования. В некоторых вариантах осуществления концентрацию оценивают подходящим способом, таким как UV-спектрофотометрия. В некоторых вариантах осуществления подходящая концентрация составляет от приблизительно 90% до 110% номинальной (0,9-1,1 мг/мл).
[216] В некоторых вариантах осуществления оценка чистоты mRNA включает оценку целостности mRNA, оценку уровня остаточной плазмидной ДНК и оценку уровня остаточного растворителя. В некоторых вариантах осуществления приемлемые уровни целостности mRNA оценивают посредством электрофореза в агарозном геле. Гели анализируют с определением соответствия паттерна полос и кажущейся длины нуклеотидов аналитическому эталонному стандарту. Дополнительные способы оценки целостности РНК включают, например, оценку очищенной mRNA с применением капиллярного гель-электрофореза (CGE). В некоторых вариантах осуществления приемлемая чистота очищенной mRNA, определенная посредством CGE, является такой, что композиция на основе очищенной mRNA содержит не более чем приблизительно 55% длинных абортивных/расщепленных молекул. В некоторых вариантах осуществления уровень остаточной плазмидной ДНК оценивают способами, известными из уровня техники, например, посредством применения qPCR. В некоторых вариантах осуществления приемлемый уровень остаточной плазмидной ДНК составляет менее чем 10 пг/мг (например, менее чем 10 пг/мг, менее чем 9 пг/мг, менее чем 8 пг/мг, менее чем 7 пг/мг, менее чем 6 пг/мг, менее чем 5 пг/мг, менее чем 4 пг/мг, менее чем 3 пг/мг, менее чем 2 пг/мг или менее чем 1 пг/мг). В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 10000 ppm, 9000 ppm, 8000 ppm, 7000 ppm, 6000 ppm, 5000 ppm, 4000 ppm, 3000 ppm, 2000 ppm, 1000 ppm. Соответственно, в некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 10000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 9000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 8000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 7000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 6000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 5000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 4000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 3000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 2000 ppm. В некоторых вариантах осуществления приемлемые уровни остаточного растворителя составляют не более чем 1000 ppm.
[217] В некоторых вариантах осуществления в отношении очищенной mRNA осуществляют микробиологическое тестирование, которое включает, например, оценку наличия бактериальных эндотоксинов. В некоторых вариантах осуществления уровень бактериальных эндотоксинов составляет <0,5 ЕЭ/мл, <0,4 ЕЭ/мл, <0,3 ЕЭ/мл, <0,2 ЕЭ/мл или <0,1 ЕЭ/мл. Следовательно, в некоторых вариантах осуществления уровень бактериальных эндотоксинов в очищенной mRNA составляет <0,5 ЕЭ/мл. В некоторых вариантах осуществления уровень бактериальных эндотоксинов в очищенной mRNA составляет <0,4 ЕЭ/мл. В некоторых вариантах осуществления уровень бактериальных эндотоксинов в очищенной mRNA составляет <0,3 ЕЭ/мл. В некоторых вариантах осуществления уровень бактериальных эндотоксинов в очищенной mRNA составляет <0,2 ЕЭ/мл. В некоторых вариантах осуществления уровень бактериальных эндотоксинов в очищенной mRNA составляет <0,2 ЕЭ/мл. В некоторых вариантах осуществления уровень бактериальных эндотоксинов в очищенной mRNA составляет <0,1 ЕЭ/мл. В некоторых вариантах осуществления очищенная mRNA содержит не более чем 1 КОЕ/10 мл, 1 КОЕ/25 мл, 1 КОЕ/50 мл, 1 КОЕ/75 мл или не более чем 1 КОЕ/100 мл. Следовательно, в некоторых вариантах осуществления очищенная mRNA содержит не более чем 1 КОЕ/10 мл. В некоторых вариантах осуществления очищенная mRNA содержит не более чем 1 КОЕ/25 мл. В некоторых вариантах осуществления очищенная mRNA содержит не более чем 1 КОЕ/50 мл. В некоторых вариантах осуществления очищенная mRNA содержит не более чем 1 КОЕ/75 мл. В некоторых вариантах осуществления очищенная mRNA содержит 1 КОЕ/100 мл.
[218] В некоторых вариантах осуществления оценивают pH очищенной mRNA. В некоторых вариантах осуществления приемлемый pH очищенной mRNA составляет от 5 до 8. Соответственно, в некоторых вариантах осуществления очищенная mRNA характеризуется pH, составляющим приблизительно 5. В некоторых вариантах осуществления очищенная mRNA характеризуется pH, составляющим приблизительно 6. В некоторых вариантах осуществления очищенная mRNA характеризуется pH, составляющим приблизительно 7. В некоторых вариантах осуществления очищенная mRNA характеризуется pH, составляющим приблизительно 7. В некоторых вариантах осуществления очищенная mRNA характеризуется pH, составляющим приблизительно 8.
[219] В некоторых вариантах осуществления оценивают точность трансляции очищенной mRNA. Точность трансляции можно оценивать различными способами, включая, например, трансфекцию и вестерн-блоттинг. Приемлемые характеристики очищенной mRNA включают паттерн образования полос при вестерн-блоттинге, который мигрирует в соответствии с молекулярной массой, подобной таковой для эталонного стандарта.
[220] В некоторых вариантах осуществления очищенную mRNA оценивают в отношении проводимости. В некоторых вариантах осуществления приемлемые характеристики очищенной mRNA включают проводимость, составляющую от приблизительно 50% до 150% эталонного стандарта.
[221] Очищенную mRNA также оценивают в отношении процентной доли кэпов и длины поли(А)-хвоста. В некоторых вариантах осуществления приемлемое процентное содержание кэпов включает кэп 1 с процентной долей площади, составляющей NLT90. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 100-1500 нуклеотидов (например, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950 и 1000, 1100, 1200, 1300, 1400 или 1500 нуклеотидов). Следовательно, в некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 100 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 200 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 250 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 300 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 350 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 400 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 450 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 500 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 550 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 600 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 650 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 700 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 750 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 800 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 850 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 900 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 950 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 1000 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 1100 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 1200 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 1300 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 1400 нуклеотидов. В некоторых вариантах осуществления приемлемая длина поли(А)-хвоста составляет приблизительно 1500 нуклеотидов.
[222] В некоторых вариантах осуществления очищенную mRNA также оценивают в отношении любого остаточного PEG. В некоторых вариантах осуществления очищенная mRNA содержит менее чем от 10 нг PEG/мг очищенной mRNA до 1000 нг PEG/мг mRNA. Соответственно, в некоторых вариантах осуществления очищенная mRNA содержит менее чем приблизительно 10 нг PEG/мг очищенной mRNA. В некоторых вариантах осуществления очищенная mRNA содержит менее чем приблизительно 100 нг PEG/мг очищенной mRNA. В некоторых вариантах осуществления очищенная mRNA содержит менее чем приблизительно 250 нг PEG/мг очищенной mRNA. В некоторых вариантах осуществления очищенная mRNA содержит менее чем приблизительно 500 нг PEG/мг очищенной mRNA. В некоторых вариантах осуществления очищенная mRNA содержит менее чем приблизительно 750 нг PEG/мг очищенной mRNA. В некоторых вариантах осуществления очищенная mRNA содержит менее чем приблизительно 1000 нг PEG/мг очищенной mRNA.
[223] Различные способы выявления и количественной оценки чистоты mRNA известны из уровня техники. Например, такие способы включают блоттинг, капиллярный электрофорез, хроматографию, флуоресценцию, гель-электрофорез, HPLC, окрашивание серебром, спектроскопию, ультрафиолетовое излучение (UV), или UPLC, или их комбинацию. В некоторых вариантах осуществления mRNA сначала денатурируют с помощью красителя с глиоксалем перед гель-электрофорезом («гель-электрофорез с денатурацией глиоксалем»). В некоторых вариантах осуществления определяют характеристики синтезированной mRNA перед кэпированием или присоединением хвоста. В некоторых вариантах осуществления определяют характеристики синтезированной mRNA после кэпирования или присоединения хвоста.
Подходящие нуклеиновые кислоты для описанных способов
[224] Любой вид нуклеиновой кислоты можно очищать с применением описанных в данном документе способов. В некоторых вариантах осуществления нуклеиновые кислоты представляют собой mRNA, транскрибируемые in vitro (IVT). Вкратце, IVT, как правило, осуществляют с применением линейной или кольцевой ДНК-матрицы, содержащей промотор, пула рибонуклеотидтрифосфатов, буферной системы, которая может включать DTT и ионы магния, и соответствующей РНК-полимеразы (например, РНК-полимеразы T3, T7 или SP6), ДНКазы I, пирофосфатазы и/или ингибитора РНКазы. В некоторых вариантах осуществления реакция IVT включает двухстадийный способ, при этом первая стадия включает транскрипцию mRNA in vitro с последующей стадией очистки, и вторая стадия включает кэпирование и присоединение хвоста к транскрибированной in vitro mRNAс последующей второй стадией очистки. В некоторых вариантах осуществления реакция IVT представляет собой одностадийный способ, который приводит к транскрипции in vitro кэпированной mRNA с присоединенным хвостом. Например, в некоторых вариантах осуществления транскрипция in vitro приводит к получению кэпированной mRNA с присоединенным хвостом, которую затем очищают. Это осуществляют, например, посредством применения плазмид, которые содержат область поли-T и/или CleanCap®. Конкретные условия будут варьировать в зависимости от конкретного применения. Содержание данных реагентов в конечном продукте является нежелательным в соответствии с несколькими вариантами осуществления и, таким образом, может упоминаться как содержание примесей, и препарат, содержащий одну или более из данных примесей, может упоминаться как неочищенный препарат. Соответственно, в одном аспекте настоящее изобретение предусматривает способ изготовления mRNA, включающий стадии (a) осуществления транскрипции in vitro (IVT) посредством смешивания (i) ДНК-матрицы, содержащей промотор, и (ii) РНК-полимеразы с получением неочищенного препарата, содержащего полноразмерную mRNA; (b) обеспечения высокомолярной соли и амфифильного полимера в суспензии с осаждением полноразмерной mRNA и получением осажденной полноразмерной mRNA в суспензии; (c) захватывания осажденной полноразмерной mRNA посредством нанесения суспензии на фильтр; и (d) промывания осажденной полноразмерной mRNA из стадии (c) водным растворителем с получением очищенной полноразмерной mRNA в водном растворе, и (e) солюбилизирования осажденной mRNA из стадии (d) с получением композиции на основе очищенной mRNA, где очищенная полноразмерная mRNA в водном растворе, полученная на стадии (d), по сути не содержит (i) ДНК-матрицу, содержащую промотор, и (ii) РНК-полимеразу.
[225] В некоторых вариантах осуществления на стадии (a) ДНК-матрица представляет собой линейную ДНК-матрицу. В некоторых вариантах осуществления на стадии (a) полимераза представляет собой полимеразу SP6. В некоторых вариантах осуществления на стадии (a) смешивание дополнительно включает смешивание пула рибонуклеотидтрифосфатов. В некоторых вариантах осуществления на стадии (a) смешивание дополнительно предусматривает применение ингибитора РНКазы, например, ингибитора РНКазы I, РНКазы A, РНКазы B и РНКазы C.
[226] В некоторых вариантах осуществления на стадии (b) высокомолярная соль представляет собой GSCN. В некоторых вариантах осуществления на стадии (b) высокомолярная соль предусматривает GSCN. В некоторых вариантах осуществления на стадии (b) амфифильный полимер предусматривает полимер PEG. В некоторых вариантах осуществления на стадии (b) амфифильный полимер предусматривает MTEG. В конкретных вариантах осуществления на стадии (b) высокомолярная соль предусматривает GSCN, а амфифильный полимер предусматривает PEG, имеющий молекулярную массу, составляющую приблизительно 6000 г/моль (например, PEG-6000), или MTEG.
[227] В некоторых вариантах осуществления на стадии (c) фильтр имеет MWCO, которая составляет менее чем осажденная полноразмерная mRNA, но более чем полноразмерная mRNA. В некоторых вариантах осуществления на стадии (c) фильтр представляет собой глубинный фильтр. В некоторых вариантах осуществления на стадии (c) фильтр применяют совместно с центрифугированием.
[228] В некоторых вариантах осуществления на стадии (d) водный растворитель содержит амфифильный полимер. В некоторых вариантах осуществления на стадии (d) амфифильный полимер в водном растворителе представляет собой тот же амфифильный полимер, который применяют на стадии (b). В некоторых вариантах осуществления на стадии (d) амфифильный полимер в водном растворителе отличается от амфифильного полимера, применяемого на стадии (b). В некоторых вариантах осуществления на стадии (d) амфифильный полимер предусматривает полимер PEG. В некоторых вариантах осуществления на стадии (d) полимер PEG в водном растворителе представляет собой тот же полимер PEG, который применяют на стадии (b). В некоторых вариантах осуществления на стадии (d) полимер PEG в водном растворителе отличается от полимера PEG, применяемого на стадии (b).
[229] В некоторых вариантах осуществления очищенная полноразмерная mRNA в водном растворе, полученная на стадии (e), также по сути не содержит (iv) преждевременно прерванные последовательности РНК. В некоторых вариантах осуществления преждевременно прерванные последовательности РНК предусматривают шортмеры. В некоторых вариантах осуществления очищенная полноразмерная mRNA в водном растворе, полученная на стадии (e), также по сути не содержит (v) двухцепочечную РНК (dsRNA). В некоторых вариантах осуществления очищенная полноразмерная mRNA в водном растворе, полученная на стадии (e), также по сути не содержит (iv) преждевременно прерванные последовательности РНК и (v) двухцепочечную РНК (dsRNA).
[230] В некоторых вариантах осуществления на стадии (a) РНК-полимераза представляет собой полимеразу SP6, и очищенная полноразмерная mRNA в водном растворе, полученная на стадии (e), также по сути не содержит (v) двухцепочечную РНК (dsRNA).
[231] В некоторых вариантах осуществления в данном способе изготовления для получения высокочистой mRNA не применяют хроматографию. В некоторых вариантах осуществления в данном способе изготовления для получения высокочистой mRNA не применяют растворители на основе спирта. В некоторых вариантах осуществления в данном способе изготовления для получения высокочистой mRNA не применяют хроматографию и растворители на основе спирта.
[232] В соответствии с различными вариантами осуществления настоящее изобретение применяют для очистки синтезированной in vitro mRNA различной длины. В некоторых вариантах осуществления настоящее изобретение применяют для очистки синтезированной in vitro mRNA, длина которой составляет более чем приблизительно 1 т. о., 1,5 т. о., 2 т. о., 2,5 т. о., 3 т. о., 3,5 т. о., 4 т. о., 4,5 т. о., 5 т. о., 6 т. о., 7 т. о., 8 т. о., 9 т. о., 10 т. о., 11 т. о., 12 т. о., 13 т. о., 14 т. о. или 15 т. о. В некоторых вариантах осуществления настоящее изобретение применяют для очистки mRNA, содержащей одну или более модификаций, которые, как правило, повышают стабильность. В некоторых вариантах осуществления одна или более модификаций выбраны из модифицированного нуклеотида, модифицированных сахарофосфатных остовов, 5’- и/или 3’-нетранслируемой области. В некоторых вариантах осуществления настоящее изобретение применяют для очистки синтезированной in vitro немодифицированной mRNA.
[233] Как правило, mRNA модифицируют для повышения стабильности. Модификации mRNA могут включать, например, модификации нуклеотидов РНК. Таким образом, модифицированная mRNA по настоящему изобретению может содержать, например, модификации остова, модификации сахара или модификации оснований. В некоторых вариантах осуществления mRNA, кодирующие антитела (например, mRNA, кодирующие тяжелую цепь и легкую цепь) можно синтезировать из встречающихся в природе нуклеотидов и/или аналогов нуклеотидов (модифицированных нуклеотидов), в том числе без ограничения пуринов (аденина (A), гуанина (G)) или пиримидинов (тимина (T), цитозина (C), урацила (U)), и в качестве модифицированных нуклеотидов аналогов или производных пуринов и пиримидинов, таких как, например, 1-метиладенин, 2-метиладенин, 2-метилтио-N-6-изопентениладенин, N-6-метиладенин, N-6-изопентениладенин, 2-тиоцитозин, 3-метилцитозин, 4-ацетилцитозин, 5-метилцитозин, 2,6-диаминопурин, 1-метилгуанин, 2-метилгуанин, 2,2-диметилгуанин, 7-метилгуанин, инозин, 1-метилинозин, псевдоурацил (5-урацил), дигидроурацил, 2-тиоурацил, 4-тиоурацил, 5-карбоксиметиламинометил-2-тиоурацил, 5-(карбоксигидроксиметил)-урацил, 5-фторурацил, 5-бромурацил, 5-карбоксиметиламинометилурацил, 5-метил-2-тиоурацил, 5-метилурацил, сложный метиловый эфир N-урацил-5-оксиуксусной кислоты, 5-метиламинометилурацил, 5-метоксиаминометил-2-тиоурацил, 5'-метоксикарбонилметилурацил, 5-метоксиурацил, сложный метиловый эфир урацил-5-оксиуксусной кислоты, урацил-5-оксиуксусная кислота (v), 1-метилпсевдоурацил, квеуозин, бета-D-маннозилквеуозин, вибутоксозин, а также фосфороамидаты, фосфоротиоаты, пептидные нуклеотиды, метилфосфонаты, 7-деазагуанозин, 5-метилцитозин и инозин. Получение таких аналогов известно специалисту в данной области, например, из патента США № 4373071, патента США № 4401796, патента США № 4415732, патента США № 4458066, патента США № 4500707, патента США № 4668777, патента США № 4973679, патента США № 5047524, патента США № 5132418, патента США № 5153319, патентов США №№ 5262530 и 5700642, описание которых включено в данный документ посредством ссылки во всей своей полноте.
[234] Как правило, синтез mRNA предусматривает добавление «кэпа» на N-конец (5’) и «хвоста» на C-конец (3’). Наличие кэпа важно для обеспечения устойчивости к нуклеазам, обнаруживаемым в большинстве эукариотических клеток. Наличие «хвоста» служит для защиты mRNA от расщепления экзонуклеазой.
[235] Таким образом, в некоторых вариантах осуществления mRNA, которые очищают с применением способов, описываемых в данном документе, содержат структуру 5’-кэп. 5’-кэп, как правило, добавляют следующим образом: сначала терминальная РНК-фосфатаза удаляет одну из концевых фосфатных групп из 5’-нуклеотида, оставляя два концевых фосфата, затем гуанозинтрифосфат (GTP) добавляется к концевым фосфатам посредством гуанилилтрансферазы, образуя 5’5’5-трифосфатную связь, и затем атом азота в положении 7 гуанина метилируют метилтрансферазой. Примеры кэп-структур включают без ограничения m7G(5')ppp (5'(A, G(5')ppp(5')A и G(5')ppp(5')G.
[236] Хотя mRNA, полученная в результате осуществления реакций транскрипции in vitro, может требоваться в некоторых вариантах осуществления, другие источники mRNA рассматриваются как входящие в объем настоящего изобретения, в том числе mRNA дикого типа, получаемая из бактерий, грибов, растений и/или животных.
[237] В некоторых вариантах осуществления mRNA, подлежащие очистке в способах, описанных в данном документе, содержат 5’- и/или 3’-нетранслируемую область. В некоторых вариантах осуществления 5’-нетранслируемая область содержит один или более элементов, которые влияют на стабильность или трансляцию mRNA, например, железозависимый элемент. В некоторых вариантах осуществления длина 5’-нетранслируемой области может составлять от приблизительно 50 до 500 нуклеотидов.
[238] В некоторых вариантах осуществления 3’-нетранслируемая область содержит один или более сигналов полиаденилирования, сайт связывания белков, которые влияют на стабильность положения mRNA в клетке, или один или более сайтов связывания miRNA. В некоторых вариантах осуществления длина 3’-нетранслируемой области может составлять от 50 до 500 или более нуклеотидов.
[239] Настоящее изобретение можно применять для очистки mRNA, которые кодируют любой белок. Неограничивающие примеры mRNA, которые очищают с применением описанных в данном документе способов, представлены в разделе ниже.
ПРИМЕРЫ
Пример 1. Синтез mRNA
Условия реакции IVT
[240] В следующих примерах, если не указано иное, mRNA синтезировали посредством транскрипции in vitro (IVT) с применением полимеразы T7 или полимеразы SP6. Вкратце, для реакции IVT с применением полимеразы SP6 на каждый грамм транскрибированной mRNA получали реакционную смесь, содержащую 20 мг линеаризованной двухцепочечной ДНК-плазмиды с промотором, специфическим в отношении РНК-полимеразы, РНК-полимеразу SP6, ингибитор РНКазы, пирофосфатазу, 5 мМ NTP, 10 мМ DTT и реакционный буфер (10x 250 мМ трис-HCl, pH 7,5, 20 мМ спирмидина, 50 мМ NaCl), с применением воды, не содержащей РНКазу, затем инкубировали при 37°C в течение 60 мин. Затем реакцию гасили посредством добавления ДНКазы I и буфера для ДНКазы I (10x 100 мМ трис-HCl, 5 мМ MgCl2 и 25 мМ CaCl2, pH 7,6) для облегчения расщепления двухцепочечной ДНК-матрицы при подготовке к очистке. Конечный реакционный объем составлял 204 мл.
5’-кэп
[241] Если не указано иное, mRNA, транскрибированную посредством IVT, кэпировали на ее 5’-конце либо посредством включения кэп-структур в качестве части реакции IVT, либо на последующей ферментативной стадии. В случае кэпирования в качестве части реакции IVT аналог кэпа может быть включен в виде первого «основания» в образующуюся цепь РНК. Аналог кэпа может представлять собой кэп 0, кэп 1, кэп 2, m6Am или не встречающиеся в природе кэпы. В качестве альтернативы некэпированную и очищенную транскрибированную in vitro (IVT) mRNA можно модифицировать ферментативным способом после IVT, с присоединением кэпа, например, посредством добавления структуры 5’- N7-метилгуанилатного кэпа 0 с применением гуанилаттрансферазы и добавления метильной группы в положение 2’-O предпоследнего нуклеотида с получением структуры кэпа 1, с применением 2’-O-метилтрансферазы, как описано в Fechter, P.; Brownlee, G.G. «Recognition of mRNA cap structures by viral and cellular proteins» J. Gen. Virology 2005, 86, 1239-1249.
3’-хвост
[242] Если не указано иное, к mRNA, транскрибированной посредством IVT, присоединяли хвост на ее 3’-конце либо посредством включения матрицы хвоста в линеаризованную плазмиду, которая присоединяет хвост к mRNA в качестве части реакции IVT, либо на последующей ферментативной стадии. В случае присоединения хвоста в качестве части реакции IVT включение поли-Т или аналогичного хвостового элемента в pDNA-матрицу выполняют таким образом, что поли(А)-хвост или схожий соответствующий хвост образуется на mRNA в качестве части способа IVT. В качестве альтернативы поли(А)-хвост можно добавлять к 3’-концу mRNA, полученной в результате IVT, ферментативным способом после реакции IVT, например, с применением поли-A-полимеразы.
Пример 2. Очистка mRNA посредством индуцированного полимером осаждения mRNA без применения VOC
[243] Данный пример показывает, что во время стадии осаждения mRNA при очистке mRNA можно применять полимер вместо летучего органического соединения (VOC), такого как этанол. Такой способ индуцированного полимером осаждения обеспечивает конечный выход и уровень чистоты, подходящие для терапевтического применения.
[244] Три партии mRNA CFTR по 5 мг синтезировали посредством IVT-синтеза, описанного в примере 1, при этом осаждение каждой партии осуществляли при трех различных условиях, описанных ниже.
Условие 1: Этанол и GSCN (экспериментальный контроль)
[245] 1 объем mRNA смешивали с 2,3 объема буфера, содержащего 5 М GSCN и 10 мМ DTT, с получением конечной концентрации GSCN, составляющей 2 М. Затем 1,7 объема 100% этанола добавляли к суспензии с получением конечной концентрации этанола, составляющей 34%.
Условие 2: PEG-6000 и GSCN (индуцированное полимером осаждение без применения этанола)
[246] 1 объем mRNA смешивали с 2,3 объема буфера, содержащего 5 М GSCN и 10 мМ DTT, с получением конечной концентрации GSCN, составляющей 2 М. Затем 1,7 объема 50% PEG-6000 добавляли к суспензии с получением конечной концентрации PEG-6000, составляющей 17%.
Условие 3: PEG-6000 и NaCl (индуцированное полимером осаждение без применения этанола)
[247] Стадию осаждения осуществляли в условиях, описанных в Schmitz et al., Notes & Tips, Anal Biochem. (2006) 311-313. 1 объем mRNA смешивали с NaCl с получением конечной концентрации NaCl, составляющей 500 мМ. Затем 50% PEG-6000 добавляли к суспензии с получением конечной концентрации PEG-6000, составляющей 19%.
[248] Образцы mRNA, осажденной при каждом из условий, захватывали с помощью колонки Qiagen RNeasy maxi, дважды промывали с помощью 10 мл 80% этанола и растворяли в 5 мл воды, не содержащей РНКазу. Концентрацию растворенных образцов mRNA подвергали количественному определению с помощью спектрофотометра NanoDrop2000 с применением поглощения при 260 нм. Выход при каждом условии осаждения показан на фигуре 1. Кроме того, наличие остаточных ферментов, применяемых в способе, выявляли посредством окрашивания серебром, описанного ниже, и результаты показаны на фигуре 2.
[249] Данные показывают, что при трех условиях осаждения получали сходные показатели выхода mRNA после очистки. Применение условий осаждения 1 и 2 приводило к получению образцов mRNA высокой степени чистоты, не содержащих ферментов, применяемых в способе, видимых при окрашивании серебром, как показано на фигуре 2. Однако индуцированное полимером осаждение с применением PEG-6000 и NaCl (условие 3) приводило к получению образца, демонстрирующего распределение полос, соответствующее наличию применяемых в способе ферментов, что потребовало бы дополнительных стадий очистки, чтобы стать приемлемым для терапевтического применения. Приведенные здесь данные подтверждают, что осаждение mRNA с применением условия 2 можно применять при очистке mRNA для достижения выхода и уровня чистоты, достаточных для терапевтического применения.
Определение чистоты mRNA и выявление наличия остаточных ферментов, применяемых в способе (окрашивание серебром)
[250] Чистоту mRNA с точки зрения наличия остаточных ферментов IVT и необязательно ферментов, применяемых при кэпировании и/или присоединении хвоста, оценивали посредством окрашивания серебром. В частности, каждый из следующих остаточных ферментов, применяемых в способе, можно выявить с применением данного подхода: РНК-полимераза, ингибитор РНК, пирофосфатаза, гуанилилтрансфераза (GuaT), 2’-O-M и поли(A)-полимераза, а также фермент РНКаза I, который применяют в качестве части подготовки геля для окрашивания серебром. В частности, гели, окрашенные серебром, анализировали в соответствии с набором Invitrogen со следующей подготовкой образцов перед окрашиванием. 15,5 мкл РНК в концентрации 1 мг/мл обрабатывали с помощью 4 мкл РНКазы I (100 Ед/мл, Invitrogen) в течение 30 минут при 37°C. Образцы подготавливали в загрузочном буфере LDS от Invitrogen с помощью восстанавливающего реагента и в конечном итоге загружали на 10% гели Bis-Tris. Электрофорез осуществляли при 200 В в течение 35 мин. Гели окрашивали с применением набора для окрашивания Silver Quest и проявляли в течение 8 мин. Считалось, что образцы, содержащие очищенную mRNA, по сути не содержали конкретного применяемого в способе фермента, если полоса для конкретного применяемого в способе фермента не была видимой.
Пример 3. Тестирование диапазонов соотношений полимеров при индуцированном полимером осаждении mRNA
[251] Данный пример показывает, что в соответствии с различными вариантами осуществления различные соотношения полимеров можно применять при индуцированном полимером осаждении mRNA для очистки mRNA, подходящей для терапевтического применения.
[252] Семь партий mRNA CFTR по 5 мг синтезировали посредством IVT-синтеза, описанного выше, при этом осаждение каждой партии осуществляли при различных условиях, представленных в таблице 1 ниже.
Таблица 1. Условия осаждения для очистки mRNA
[253] Образцы mRNA, осажденной при каждом из условий, захватывали с помощью колонки Qiagen RNeasy maxi, дважды промывали с помощью 10 мл 80% этанола и растворяли в 5 мл воды, не содержащей РНКазу. Концентрацию растворенных образцов mRNA подвергали количественному определению с помощью спектрофотометра NanoDrop2000 с применением поглощения при 260 нм. Выход при каждом условии осаждения показан на фигуре 3. Кроме того, наличие остаточных ферментов, применяемых в способе, выявляли посредством окрашивания серебром, описанного в примере 2, и результаты показаны на фигуре 4.
[254] Данные показывают, что при всех шести условиях очистки mRNA, при которых применяли индуцированное полимером осаждение mRNA, получали высокий выход mRNA после очистки, который являлся сходным с таковым для традиционного способа осаждения с применением этанола (фигура 3). Кроме того, очистка образцов mRNA посредством индуцированного полимером осаждения при конечных концентрациях PEG, составлявших менее чем 20% концентрация PEG (или при доле 50% PEG-6000, составлявшей менее чем 2,0), приводила к получению высокочистых образцов mRNA, не содержащих ферментов, применяемых в способе, видимых при окрашивании серебром, показанном на фигуре 4 (дорожки 5-8). Однако образцы, содержащие mRNA, очищенную посредством индуцированного полимером осаждения, при конечной концентрации PEG-6000, составляющей более чем 20%, демонстрировали наличие остаточных ферментов, применяемых в способе (дорожка 9). Интересно, что индуцированное полимером осаждение с применением 24% PEG-6000 приводило к более высокому уровню остаточных ферментов, применяемых в способе, в очищенном образце, чем в образце при индуцированном полимером осаждении с применением 22% PEG-6000. Без ограничения какой-либо конкретной теорией предполагается, что более высокая процентная доля PEG-6000 облегчает осаждение как нуклеиновой кислоты, так и ферментов, применяемых в способе.
[255] В совокупности приведенные в данном документе данные дополнительно подтверждают, что очистка mRNA посредством индуцированного полимером осаждения представляет собой эффективный способ очистки mRNA для достижения выхода и уровня чистоты, достаточных для терапевтического применения. Индуцированное полимером осаждение при конечной концентрации PEG-6000, составляющей 7-24%, приводит к эффективному осаждению и извлечению mRNA. В остальных примерах при индуцированном полимером осаждении PEG-6000 применяли в конечной концентрации, составляющей 12%.
Пример 4. Очистка mRNA без применения этанола и влияние применения различных полимеров на стадии промывания.
[256] Данный пример показывает, что полимер можно применять как на стадии осаждения mRNA, так и на стадии промывания без применения каких-либо VOC, таких как этанол, для очистки mRNA с получением выхода и уровня чистоты, подходящих для терапевтического применения.
[257] Двенадцать партий mRNA CFTR по 5 мг синтезировали посредством IVT-синтеза и добавляли 5’-кэпы и 3’-поли(A)-хвосты, как описано в примере 1. Каждую из полученных с помощью IVT двенадцати партий mRNA по 5 мг осаждали посредством индуцированного полимером осаждения. К каждой партии массой 5 мг добавляли буфер, содержащий 5 М GSCN и 10 мМ DTT, с получением конечной концентрации GSCN, составляющей 2,7 M. Затем 50% PEG-6000 добавляли к суспензии с получением конечной концентрации PEG-6000, составляющей 12%. Образцы осажденной mRNA захватывали с помощью колонок Qiagen RNeasy maxi и дважды промывали с помощью 10 мл одного из следующих полимерных буферов для промывания, перечисленных в таблице 2 ниже, вместо 80% этанола. VOC или спирт вообще не применяли при очистке mRNA, синтезированной посредством IVT. В частности, VOC или спирт вообще не применяли на стадии осаждения или на стадии промывания.
Таблица 2. Полимерные буферы для промывания
[258] Двенадцать образцов растворяли в 5 мл воды, не содержащей РНКазу, и концентрацию подвергали количественному определению с помощью спектрофотометра NanoDrop2000 с применением поглощения при 260 нм. Выход при каждом условии осаждения показан на фигуре 5. Кроме того, наличие остаточных ферментов, применяемых в способе, выявляли посредством окрашивания серебром, как описано в примере 2, и результаты показаны на фигуре 6.
[259] Как показано на фигуре 5, наблюдали выраженную корреляцию между процентной долей полимера в буфере для промывания и количеством извлеченной mRNA. Без ограничения какой-либо конкретной теорией предполагается, что добавление воды к данным буферам для промывания приводит к солюбилизации mRNA в ходе данных стадий промывания.
[260] В целом, данные показывают, что, неожиданно, mRNA можно очищать полностью без применения этанола посредством индуцированного полимером осаждения с последующим промыванием полимером с достижением неожиданного выхода и уровня чистоты, подходящих для терапевтического применения. Применение буфера для промывания, содержащего PEG-400 в конечной концентрации, составляющей 90-100%, приводило к высокому выходу, как показано на фигуре 5, и получению высокочистых образцов mRNA, не содержащих ферментов, применяемых в способе, видимых при окрашивании серебром, показанном на фигуре 6 (дорожки 3-4). Из протестированных буферов PEG-400 имеет самую низкую вязкость, что делает его подходящим для применения в разных системах при разных масштабах. В совокупности указанные данные демонстрировали, что очистку mRNA без применения этанола посредством индуцированного полимером осаждения и промывания с помощью полимера, описанных в данном документе, можно применять для эффективной очистки высококачественной mRNA с получением извлекаемого количества, профилей целостности, чистоты и функциональности, которые эквивалентны или превосходят таковые для стандартных для данной отрасли способов очистки mRNA, в которых применяют VOC, такие как спирты, в том числе этанол. Кроме того, настоящее изобретение обладает существенным дополнительным преимуществом в виде масштабируемости и безопасности, которые недоступны при применении существующих стандартных для данной отрасли способов, при которых применяют VOC, такие как спирты, в том числе этанол.
Пример 5. Очистка mRNA OTC и CFTR без применения этанола и анализ
[261] Данный пример показывает, что способ очистки mRNA без применения этанола, описанный выше, можно применять для очистки mRNA независимо от размера ее конструкции или нуклеотидного состава. Кроме того, очистка mRNA в соответствии с описанными в данном документе способами приводит к получению высокого выхода, чистоты и целостности.
[262] Партии mRNA OTC (~1400 нуклеотидов) по 5 мг и mRNA CFTR (~4600 нуклеотидов) по 5 мг синтезировали посредством IVT-синтеза, описанного в примере 1. Полученные в результате IVT образцы mRNA осаждали посредством индуцированного полимером осаждения. К каждой партии массой 5 мг добавляли буфер, содержащий 5 М GSCN и 10 мМ DTT, с получением конечной концентрации GSCN, составляющей 2,7 M. Затем 50% PEG-6000 добавляли к суспензии с получением конечной концентрации PEG-6000, составляющей 12%. Образцы осажденной mRNA захватывали с помощью колонок Qiagen RNeasy maxi и дважды промывали с помощью 10 мл 90% буфера для промывания на основе PEG-400. Промытые образцы растворяли в 5 мл воды, не содержащей РНКазу, буфер заменяли на ультрачистую воду с применением спин-колонок Amicon 100 кДа и концентрировали до 2 мг/мл.
[263] Затем очищенные и концентрированные mRNA, полученные посредством IVT, кэпировали и присоединяли хвост посредством ферментативной стадии, описанной в примере 1. mRNA, содержащие 5’-кэп и 3’-хвост, очищали посредством индуцированного полимером осаждения и промывания с помощью полимера без применения этанола. В частности, на стадии осаждения к каждой партии добавляли буфер, содержащий 5 M GSCN и 10 мМ DTT, с получением конечной концентрации GSCN, составляющей 2,7 M. Затем 50% PEG-6000 добавляли к суспензии с получением конечной концентрации PEG-6000, составляющей 12%. Образцы осажденной mRNA захватывали с помощью колонок Qiagen RNeasy maxi и дважды промывали с помощью 10 мл 90% буфера для промывания на основе PEG-400. Промытые образцы растворяли в 5 мл воды, не содержащей РНКазу, буфер заменяли на ультрачистую воду с применением спин-колонок Amicon 100 кДа и концентрировали до 1 мг/мл.
[264] Определяли выход для каждого конечного продукта, представляющего собой mRNA, как показано на фигуре 7. Данные демонстрировали, что выход mRNA для mRNA OTC и CFTR в масштабе 5 мг составлял 80% и 78% соответственно. Данные показатели находились в пределах или превышали показатели выхода для стандартных в данной отрасли способов очистки mRNA.
[265] Чистоту и целостность конечного продукта, представляющего собой mRNA, анализировали как описано ниже. Целостность и длину поли(A)-хвоста оценивали посредством капиллярного электрофореза, как показано на фигуре 8. Результаты указывали на то, что конечные продукты после очистки как mRNA OTC, так и mRNA CFTR в масштабе 5 мг характеризуются четко выраженным пиком, сходным с пиком для контроля (существующий в настоящее время способ с применением этанола в масштабе 10 граммов OTC). Кроме того, показатели длины хвоста для обеих конструкций находились в пределах целевого диапазона, составляющего 500 нуклеотидов (OTC=468 нуклеотидов и CFTR=649 нуклеотидов). Наличие остаточных ферментов, применяемых в способе, которое оценивали посредством окрашивания серебром, не выявляли при очистке любой конструкции mRNA в масштабе 5 мг. Уровень чистоты дополнительно подтверждали посредством дот-блоттинга dsRNA с применением J2, описываемого ниже. Результаты, как показано на фигуре 10, демонстрировали, что в конечном продукте ни одной из конструкций не выявляли dsRNA. Наконец, ELISA применяли для подтверждения того, что PEG был полностью удален в ходе стадии диализа, как показано в таблице 3.
Таблица 3. Количественное определение PEG в конечном образце mRNA с применением ELISA
BQL= ниже предела выявления.
[266] В совокупности данные показали, что очистку mRNA без применения этанола посредством индуцированного полимером осаждения и промывания полимером, описанную в данном документе, можно применять для очистки mRNA различной длины и различных конструкций. mRNA, очищенные способами, описанными в данном документе, соответствуют или превосходят предыдущие крупномасштабные партии mRNA в отношении определяющих характеристик извлечения, описанных выше. Таким образом, высокий выход, целостность и уровень чистоты, которые обеспечивает описанный в данном документе способ, являются подходящими для терапевтического применения.
Анализ целостности очищенной mRNA
Анализ целостности РНК (анализатор фрагментов и капиллярный электрофорез)
[267] Целостность РНК и длину хвоста оценивали с помощью анализатора фрагментов CE и коммерчески доступного набора для выявления РНК. Анализ профилей пиков в отношении целостности и сдвига размера для длины хвоста осуществляли с применением набора исходных данных, а также набора нормализованных данных.
Анализ кэпированных молекул mRNA (HPLC/MS)
[268] Кэпированные молекулы, содержащиеся в конечном очищенном продукте, представляющем собой mRNA, подвергали количественному определению с применением хроматографического способа, описанного в патенте США № 9970047. Данный способ позволяет точно определить количество некэпированной mRNA в виде процентной доли от общей mRNA. Данный способ также позволяет определять количество конкретных кэп-структур, например, количество кэп G, кэп 0 и кэп 1, которое можно представить в виде процентной доли от общей mRNA.
Выявление dsRNA (дот-блоттинг с применением J2)
[269] Наличие dsRNA в отдельных образцах mRNA измеряли с применением дот-блоттинга с J2 к dsRNA, ранее описанного в Kariko et al, Nucleic Acids Research, 2011. 39, № 21. Вкратце, на мембране Nytran с высоким зарядом получали отпечатки либо 200 нг РНК, либо 25 нг контрольной dsRNA. Отпечатки высушивали, блокировали с помощью 5% обезжиренного сухого молока, затем наносили 1 мкг антитела J2 в качестве зонда на каждый отпечаток. Отпечатки промывали, наносили конъюгированные с HRP антитела осла к мышиному IgG в качестве зонда перед повторным промыванием. Отпечатки подвергали выявлению с помощью выявляющего реагента для вестерн-блоттинга ECL plus и фиксировали изображения на пленке. Считали, что образцы, содержащие очищенную mRNA, по сути не содержат dsRNA, если соответствующий отпечаток не показывал заметно более темную окраску по сравнению с контролем, в котором отсутствовала какая-либо dsDNA.
Количественный анализ/выявление PEG с помощью ELISA (Abcam Kit)
[270] Наличие молекул PEG с разной молекулярной массой в образцах mRNA определяли с применением набора PEG-ELISA от Abcam. Вкратце, применяли анализ конкурентного ингибирования ELISA, с помощью которого можно выявлять PEG в образцах вплоть до 10 нг/мл и точно определять количество PEG с большой молекулярной массой на данном уровне. Образцы mRNA без разведения, в разведениях 1/10 и 1/100 очищали с применением стандартных способов осаждения на основе этанола, а также нижеупомянутого способа без применения этанола. Предел выявления составлял 10 нг/мг РНК, 100 нг/мг РНК и 1 мкг/мг РНК при неразбавленной концентрации, при разведении 1/10 и при разведении 1/100 соответственно.
Пример 6. Очистка mRNA без применения этанола в масштабе 1 грамм и 10 граммов
[271] Данный пример показывает, что способ очистки mRNA без применения этанола, описанный выше, можно применять для очистки mRNA в требуемом масштабе и с качеством, необходимым для терапевтического применения. Очистка mRNA в масштабе 1 грамм и 10 граммов в соответствии с описанными в данном документе способами, приводила к получению высокого выхода, чистоты и целостности, что демонстрирует масштабируемость способа.
[272] mRNA OTC синтезировали в масштабе 1 грамм и 10 граммов, и mRNA CFTR синтезировали в масштабе 10 граммов посредством IVT-синтеза, как описано в примере 1. Полученные в результате IVT образцы mRNA осаждали посредством индуцированного полимером осаждения. К каждому образцу mRNA добавляли буфер, содержащий 5 М GSCN и 10 мМ DTT, с получением конечной концентрации GSCN, составляющей 2,7 M. Затем 50% PEG-6000 добавляли к суспензии с получением конечной концентрации PEG-6000, составляющей 12%. К осажденной mRNA добавляли вспомогательное фильтрующее средство на основе целлюлозы Solka-Floc в соотношении вспомогательного фильтрующего средства и РНК, составляющем 10:1 (вес/вес), и хорошо перемешивали. Образцы осажденной mRNA в масштабе 1 грамм со вспомогательным фильтрующим средством захватывали с помощью колбы для вакуумного фильтрования с полиэфирсульфоном (PES) 0,22 мкм. Образцы осажденной mRNA в масштабе 10 граммов со вспомогательным фильтрующим средством захватывали с помощью фильтрующей центрифуги H300P с полипропиленовым фильтровальным мешком 1 мкм. Затем образцы mRNA массой 1 грамм и 10 граммов дважды промывали с помощью 1 л или 10 л буфера для промывания на основе 90% PEG-400. Промытую и осажденную mRNA удаляли с фильтра либо вручную, либо посредством фильтрования с помощью фильтрующей центрифуги H300P с полипропиленовым фильтровальным мешком 1 мкм. Затем промытую и осажденную mRNA солюбилизировали в 1 л или 10 л воды, не содержащей РНКазу, буфер заменяли на ультрачистую воду с применением колонки Spectrum TFF 100 кДа (mPES) и концентрировали до 2 мг/мл.
[273] Затем очищенные и концентрированные mRNA, полученные посредством IVT, кэпировали и присоединяли хвост посредством ферментативной реакции, описанной в примере 1. mRNA, содержащие 5’-кэп и 3’-хвост, очищали посредством индуцированного полимером осаждения и промывания полимером без применения этанола. К каждому образцу добавляли буфер, содержащий 5 М GSCN и 10 мМ DTT, с получением конечной концентрации GSCN, составляющей 2,7 M. Затем 50% PEG-6000 добавляли к суспензии с получением конечной концентрации PEG-6000, составляющей 12%. К осажденной mRNA добавляли вспомогательное фильтрующее средство на основе целлюлозы Solka-Floc в соотношении вспомогательного фильтрующего средства и РНК, составляющем 10:1 (вес/вес), и хорошо перемешивали. Осажденную mRNA дважды промывали с помощью 1 л или 10 л буфера для промывания на основе 90% PEG-400. Образцы промытой mRNA удаляли с фильтра либо вручную, либо посредством фильтрования с помощью фильтрующей центрифуги H300P с полипропиленовым фильтровальным мешком 1 мкм. Образцы mRNA растворяли в 1 л или 10 л воды, не содержащей РНКазу, буфер заменяли на ультрачистую воду с применением колонки Spectrum TFF 100 кДа (mPES) и концентрировали до 1 мг/мл.
[274] Определяли выход для каждого конечного продукта, представляющего собой mRNA, как показано на фигуре 7. Данные демонстрировали, что все значения выхода mRNA для mRNA OTC в масштабе 1 грамм и 10 граммов и mRNA CFTR в масштабе 10 граммов составляли более 80% и достигали 93%. Данные значения находились в пределах или превышали значения выхода для стандартного в данной отрасли способа очистки mRNA.
[275] Чистоту и целостность конечного продукта, представляющего собой mRNA, анализировали, как описано выше. Целостность и длину поли(A)-хвоста оценивали посредством капиллярного электрофореза, как показано на фигуре 8. Результаты указывали на то, что конечные продукты после очистки mRNA OTC и mRNA CFTR в масштабе 1 грамм и 10 граммов характеризуются четко выраженным пиком, сходным с пиком для контроля (существующий в настоящее время способ с применением этанола в масштабе 10 граммов OTC). Для очищенной mRNA в масштабе 10 граммов определяли количество кэпированных молекул с применением анализа HPLC-MS, описанного в примере 2. Дополнительно, показатели длины хвоста для обеих конструкций находились в пределах целевых диапазонов (OTC в масштабе 1 грамм=306 нуклеотидов; OCT в масштабе 10 граммов=158 нуклеотидов; CFTR в масштабе 10 граммов=712 нуклеотидов). Наличие остаточных ферментов, применяемых в способе, которое оценивали посредством окрашивания серебром, не выявляли при очистке обеих конструкций mRNA как в масштабе 1 грамм, так и в масштабе 10 граммов, как показано на фигуре 9. Уровень чистоты дополнительно подтверждали посредством дот-блоттинга dsRNA с применением J2, описываемого в примере 5. Результаты, как показано на фигуре 10, демонстрировали, что в конечном продукте как в масштабе 1 грамм, так и в масштабе 10 граммов не выявляли dsRNA. Наконец, ELISA применяли для подтверждения того, что PEG был полностью удален в ходе стадии диализа.
[276] В совокупности данные демонстрируют масштабируемость очистки mRNA без применения этанола посредством индуцированного полимером осаждения и промывания полимером, необходимую для очистки mRNA в требуемом масштабе и с качеством, требуемым для клинического терапевтического применения. mRNA, очищенные в масштабе 1 грамм и 10 граммов способами, описанными в данном документе, соответствуют или превосходят предыдущие крупномасштабные партии mRNA в отношении определяющих характеристик извлечения, описанных выше, что демонстрирует предпочтительность способа для применения в изготовлении mRNA и терапевтических средств на основе mRNA.
[277] Настоящее изобретение можно применять для очистки mRNA, которые кодируют любой белок. Описаны неограничивающие примеры очистки mRNA с применением указанных способов.
Пример 7. Очистка mRNA без применения этанола и влияние MTEG на стадии промывания
[278] Данный пример показывает, что амфифильный полимер MTEG можно применять на стадиях промывания без применения каких-либо VOC, таких как этанол, для очистки mRNA с получением выхода и уровня чистоты, подходящих для терапевтического применения.
[279] В таблице 4 представлены характеристики MTEG по сравнению с полимерами, тестируемыми в предыдущих примерах. Несмотря на то, что MTEG имеет молекулярную массу, сходную с молекулярной массой TEG, MTEG имеет гораздо более низкую вязкость по причине наличия метильной группы. Это означает, что MTEG имеет вязкость, намного более близкую к вязкости воды, что означает, что его легче перекачивать. Более того, Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA) классифицирует его как «безопасный», тогда как TEG, PEG-400 и PEG-6000 (50%) классифицируются как «в целом признанные безопасными» (GRAS).
Таблица 4. Характеристики полимера
[280] Пять партий mRNA CFTR по 5 мг синтезировали посредством IVT-синтеза и добавляли 5’-кэпы и 3’-поли(A)-хвосты, как описано в примере 1. Каждую из полученных посредством IVT пяти партий mRNA по 5 мг осаждали посредством индуцированного полимером осаждения. Объемное соотношение mRNA, GSCN (буфер на основе 5 M GSCN и 10 мМ DTT) и MTEG (100% вес/объем) в реакции осаждения составляло 1:2,3:1. Образцы осажденной mRNA захватывали с помощью колонок Qiagen RNeasy maxi и дважды промывали с помощью 2,5 мл одного из следующих буферов для промывания на основе MTEG, перечисленных в таблице 5 ниже, вместо 80% этанола. VOC или спирт вообще не применяли при очистке mRNA, синтезированной посредством IVT. В частности, VOC или спирт вообще не применяли на стадии осаждения или стадии промывания.
Таблица 5. Полимерные буферы для промывания
[281] Пять образцов растворяли в 5 мл воды, не содержащей РНКазу, и концентрацию подвергали количественному определению с помощью спектрофотометра NanoDrop2000 с применением поглощения при 260 нм. Концентрация извлеченной РНК показана на фигуре 11.
[282] Как показано на фигуре 11, наблюдали выраженную корреляцию между процентной долей MTEG в буфере для промывания и количеством извлеченной mRNA. Как указано выше, без ограничения какой-либо конкретной теорией предполагается, что добавление воды к данным буферам для промывания приводит к солюбилизации mRNA в ходе данных стадий промывания. Как показано на фигуре 11, применение промывочного буфера, содержащего MTEG в конечной концентрации 90-95%, приводило к получению очень высокого выхода, близкому к лишь теоретически достижимому уровню, составляющему 100% извлечения. Чистота и извлечение являлись сопоставимыми с таковыми для условий промывания с применением 80% этанола. MTEG в концентрации, составляющей 95%, выбирали для применения в качестве буфера для промывания в остальных примерах.
[283] Указанные данные дополнительно демонстрируют, что mRNA можно очищать с применением способа, совсем не предусматривающего применение этанола.
Пример 8. Очистка mRNA без применения этанола и влияние MTEG на стадии промывания.
[284] Данный пример показывает, что амфифильный полимер MTEG можно применять как на стадии осаждения mRNA, так и на стадии промывания без применения каких-либо VOC, таких как этанол, для очистки mRNA с получением выхода и уровня чистоты, подходящих для терапевтического применения.
[285] Пять партий mRNA CFTR по 5 мг синтезировали посредством IVT-синтеза и добавляли 5’-кэпы и 3’-поли(A)-хвосты, как описано в примере 1. Четыре из полученных посредством IVT пяти партий mRNA по 5 мг осаждали посредством индуцированного полимером осаждения. В случае каждой партии массой 5 мг объединяли mRNA, буфер на основе 5 M GSCN и 10 мМ DTT и MTEG в объемах, указанных в таблице 6 ниже, с образованием суспензии осажденной mRNA. Образцы осажденной mRNA захватывали с помощью колонок Qiagen RNeasy maxi и дважды промывали с помощью 2,5 мл 95% MTEG. VOC или спирт вообще не применяли при очистке mRNA, синтезированной посредством IVT. В частности, VOC или спирт вообще не применяли на стадии осаждения или стадии промывания. В качестве экспериментального контроля одну партию mRNA осаждали с применением этанола при объемном соотношении mRNA, GSCN и этанола (100% вес/объем), составляющем 1:2,3:1,7, как описано в примере 2, и дважды промывали с применением 2 мл 80% этанола.
Таблица 6. Полимерные буферы для промывания
[286] Пять образцов растворяли в 5 мл воды, не содержащей РНКазу, и концентрацию подвергали количественному определению с помощью спектрофотометра NanoDrop2000 с применением поглощения при 260 нм. Чистота образцов mRNA, полученных на стадиях осаждения и промывания, наблюдаемая с применением окрашивания серебром, показана на фигуре 12 (дорожки 6-10). Осаждение и промывание с применением MTEG позволяли достичь высокоэффективного извлечения mRNA и очистки mRNA. Добавление 1-2 объемов MTEG к 1 объему mRNA и 2,3 объема GSCN показало сопоставимые уровни чистоты и выхода. Добавление 2,5 объемов MTEG к 1 объему mRNA и 2,3 объема GSCN приводило к появлению слабой дополнительной полосы на геле, как показано на фигуре 12. Это может указывать на то, что более высокие концентрации MTEG приводят к осаждению белка, участвующего в реакции IVT.
[287] В совокупности указанные данные подтверждают, что очистка mRNA с применением MTEG как во время осаждения, так и в буфере для промывания представляет собой эффективный способ очистки mRNA для достижения выхода и уровня чистоты, достаточных для терапевтического применения.
[288] В совокупности указанные данные демонстрируют, что очистку mRNA с применением MTEG можно применять для эффективной очистки высококачественной mRNA с получением извлекаемого количества, профилей целостности и чистоты, которые эквивалентны или превосходят таковые для стандартных для данной отрасли способов очистки mRNA, в которых применяют VOC, такие как спирты, в том числе этанол. MTEG может заменять как этанол, так и высокомолекулярные полимеры, такие как PEG-6000, во время осаждения. Кроме того, MTEG может также заменять этанол или низкомолекулярные полимеры, такие как PEG-400, на стадии промывания, что делает его наиболее универсальным полимером для применения в очистке без применения этанола. Более того, как указано выше, очистка на основе MTEG, как и другие способы на основе полимеров, не предусматривающие применение этанола, описанные в данном документе, обладает существенным дополнительным преимуществом в виде масштабируемости и безопасности, которые недоступны при применении существующих стандартных для данной отрасли способов, при которых применяют VOC, такие как спирты, в том числе этанол.
Пример 9. Осаждение, индуцированное полимером MTEG, и буфер для промывания на основе MTEG, применимый для очистки, включающей глубинную фильтрацию и центрифугирование.
[289] Данный пример демонстрирует, что MTEG по причине его более низкой вязкости и связанных с этим превосходных эксплуатационных свойств является удивительно универсальным, и его можно применять в различных способах очистки mRNA без применения этанола в различных масштабах с получением извлечения, превышающего 90%.
[290] Образцы подготавливали в соответствии с приведенными выше примерами и очищали с применением глубинной фильтрации (DF) или центрифугирования.
Очистка посредством глубинной фильтрации
[291] Для меньшей партии синтезировали 7,5 г mRNA OTC посредством IVT-синтеза и добавляли 5’-кэпы и 3’-поли(A)-хвосты, как описано в примере 1, при этом масштабировали условия реакции. mRNA осаждали с применением того же индуцированного полимером MTEG осаждения, показанного в примере 7. Соответственно, объемное соотношение mRNA, GSCN (буфера на основе 5 M GSCN и 10 мМ DTT) и MTEG (100% вес/объем) в реакции осаждения составляло 1:2,3:1. Суспензию перемешивали при 60 Гц в сосуде Ли объемом 60 л с установленной на дне лопастной мешалкой перед загрузкой с расходом, составляющим 60 л/мин/м2, на глубинный фильтр площадью 0,11 м2, имеющий допустимую нагрузку 68 г/м2. Осажденную удержанную mRNA промывали с помощью 90% MTEG с расходом, составляющим 60 л/мин/м2.
[292] Для более крупной партии синтезировали 15 г mRNA CFTR посредством IVT-синтеза и добавляли 5’-кэпы и 3’-поли(A)-хвосты, как описано в примере 1, при этом масштабировали условия реакции. mRNA осаждали с применением того же индуцированного полимером MTEG осаждения, показанного в примере 7. Соответственно, объемное соотношение mRNA, GSCN (буфера на основе 5 M GSCN и 10 мМ DTT) и MTEG (100% вес/объем) в реакции осаждения составляло 1:2,3:1. Суспензию перемешивали при 60 Гц в сосуде Ли объемом 60 л с установленной на дне лопастной мешалкой перед загрузкой с расходом, составляющим 60 л/мин./м2, на глубинный фильтр площадью 0,11 м2, имеющий допустимую нагрузку 68 г/м2. Осажденную удержанную mRNA промывали с помощью 95% MTEG с расходом, составляющим 60 л/мин/м2. Расход снижали до 30 л/мин/м2 при повышении давления во время промывания. Способ фильтрации повторяли с помощью того же глубинного фильтра 0,11 м2.
Очистка посредством центрифугирования
[293] Синтезировали 15 г mRNA CFTR посредством IVT-синтеза и добавляли 5’-кэпы и 3’-поли(A)-хвосты, как описано в примере 1, при этом масштабировали условия реакции. mRNA осаждали с применением того же индуцированного полимером MTEG осаждения, показанного в примере 7. Соответственно, объемное соотношение mRNA, GSCN (буфера на основе 5 M GSCN и 10 мМ DTT) и MTEG (100% вес/объем) в реакции осаждения составляло 1:2,3:1. Суспензию перемешивали при 60 Гц в сосуде Ли объемом 60 л с установленной на дне лопастной мешалкой и добавляли вспомогательное фильтрующее средство на основе целлюлозы при массовом соотношении mRNA:вспомогательное фильтрующее средство, составляющем 1:10. Суспензию загружали в фильтрующую центрифугу и промывали с помощью 95% MTEG.
[294] Для обеих стратегий очистки конечный выход mRNA подвергали количественному определению с помощью спектрофотометра NanoDrop2000 с применением поглощения при 280 нм. Процентная доля извлечения РНК представлена в таблице 7 ниже. Кроме того, целостность mRNA оценивали с применением анализа пятна, полученного при CE, и чистоту mRNA оценивали с применением анализа окрашивания серебром для выявления наличия остаточных ферментов, применяемых в способе.
Результаты
[295] При размере партии 7,5 г или более применение MTEG в качестве осаждающего полимера и компонента буфера для промывания обеспечивало очень высокую процентную долю извлечения mRNA. Как показано в таблице 7, при применении одного и того же протокола осаждения MTEG можно применять как в способах очистки на основе центрифугирования, так и в способах очистки на основе фильтрующих мембран или фильтрующих картриджей, таких как глубинная фильтрация (DF), как для осаждения, так и в качестве буфера для промывания. Применение центрифугирования обеспечивало выход, близкий к 100% извлечению mRNA (см. таблицу 7 ниже).
Таблица 7. Эффективное извлечение mRNA с применением MTEG в различных способах очистки
[296] Более того, применение MTEG как на стадии осаждения, так и на стадии промывания поддерживало целостность и чистоту mRNA. Конечная целостность OTC (CE) составляла приблизительно 92%, как показано на фигуре 13. Более того, при окрашивании серебром остаточных ферментов, применяемых в способе, не было выявлено (см. фигуру 14). В случае 15 г образца CFTR после глубинной фильтрации целостность составляла приблизительно 73% (см. фигуру 15), и чистота являлась очень высокой с учетом отсутствия ферментов, применяемых в способе, при окрашивании серебром (фигура 16). Наконец, в случае образца CFTR массой 15 г после центрифугирования не только выход составлял 100%, но и целостность составляла приблизительно 82% (фигура 17), и окрашивание серебром не показало наличия остаточных ферментов, применяемых в способе (фигура 18). Соответственно, MTEG представляет собой весьма подходящий полимер для очистки mRNA с применением индуцированного полимером осаждения без применения этанола.
ЭКВИВАЛЕНТЫ И ОБЪЕМ
[297] Специалистам в данной области будут известны или они смогут установить, используя не более чем рутинный эксперимент, многочисленные эквиваленты конкретных вариантов осуществления настоящего изобретения, описанного в данном документе. Объем настоящего изобретения не предназначен для ограничения приведенным выше описанием, а определяется формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОЧИСТКА иРНК ФИЛЬТРАЦИЕЙ В ТАНГЕНЦИАЛЬНОМ ПОТОКЕ | 2020 |
|
RU2810003C2 |
| РЕКТАЛЬНАЯ ДОСТАВКА МАТРИЧНОЙ РНК | 2020 |
|
RU2840023C1 |
| УЛУЧШЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ЛИПИДНЫХ НАНОЧАСТИЦ, ЗАГРУЖЕННЫХ мРНК | 2020 |
|
RU2832672C2 |
| МАСШТАБНЫЙ ПРОИЗВОДСТВЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНЫХ ЛЕНТИВИРУСНЫХ ВЕКТОРОВ В СИСТЕМЕ КУЛЬТИВИРОВАНИЯ КЛЕТОК В БЕССЫВОРОТОЧНОЙ СУСПЕНЗИИ | 2014 |
|
RU2709678C2 |
| СРЕДСТВА УЛУЧШЕНИЯ САЙЛЕНСИНГА ГЕНОВ ИЛИ ЕГО ХАРАКТЕРИСТИК | 2017 |
|
RU2775479C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ IgG ПОСРЕДСТВОМ ТЕПЛОВОЙ ОБРАБОТКИ | 2013 |
|
RU2636049C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ОДНОЦЕПОЧЕЧНОЙ РНК | 2017 |
|
RU2760790C2 |
| Способ получения иммуноглобулинов | 2016 |
|
RU2708394C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СВЕРХГИДРОФИЛЬНО-АМФИФИЛЬНЫЕ СОПОЛИМЕРЫ, И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2010 |
|
RU2589836C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЭГИЛИРОВАННЫХ ОЛИГОНУКЛЕОТИДОВ | 2012 |
|
RU2564855C2 |
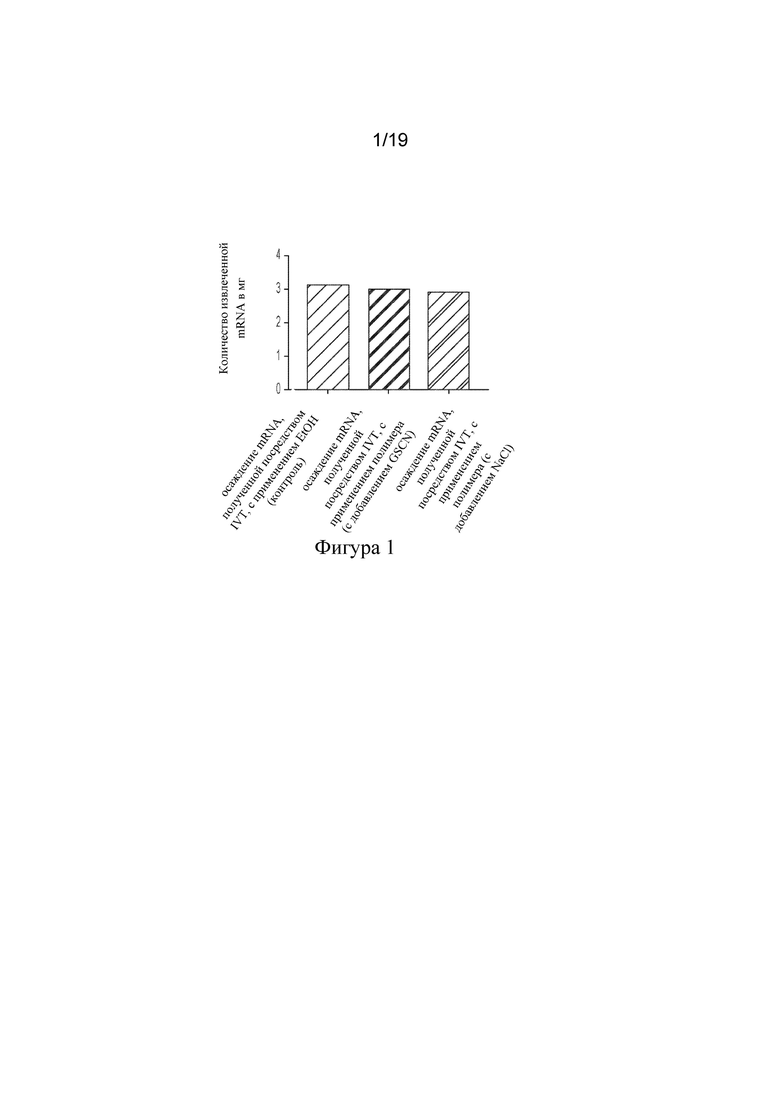



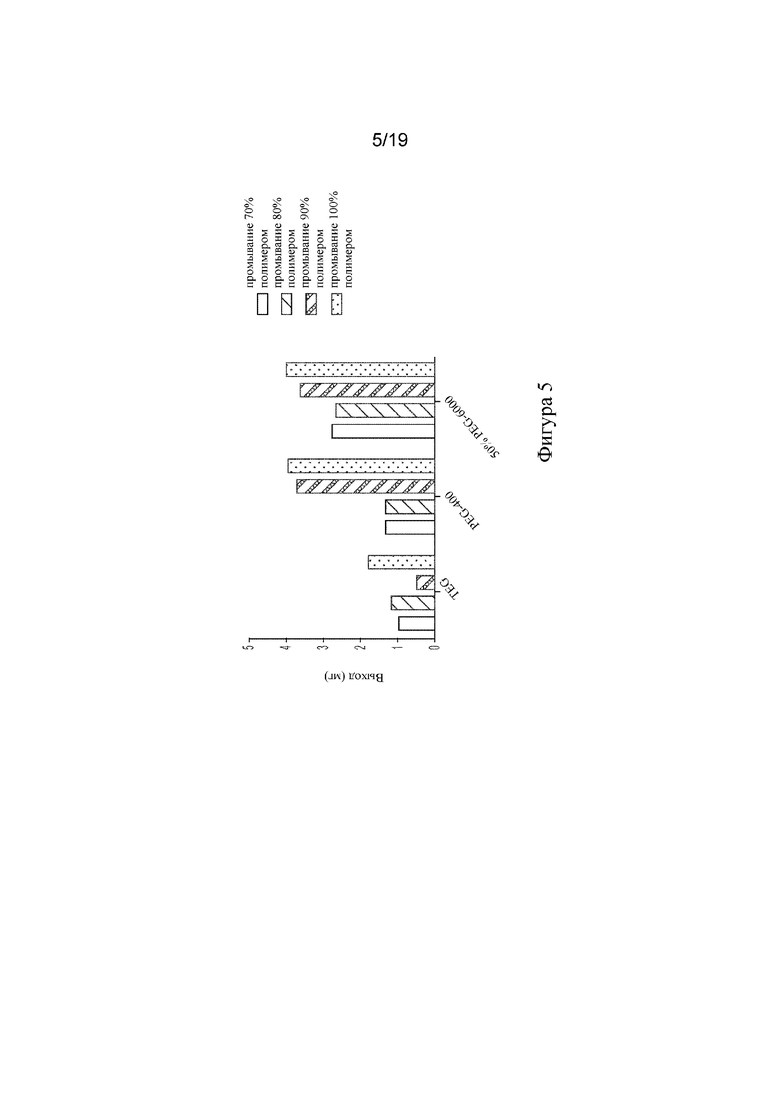


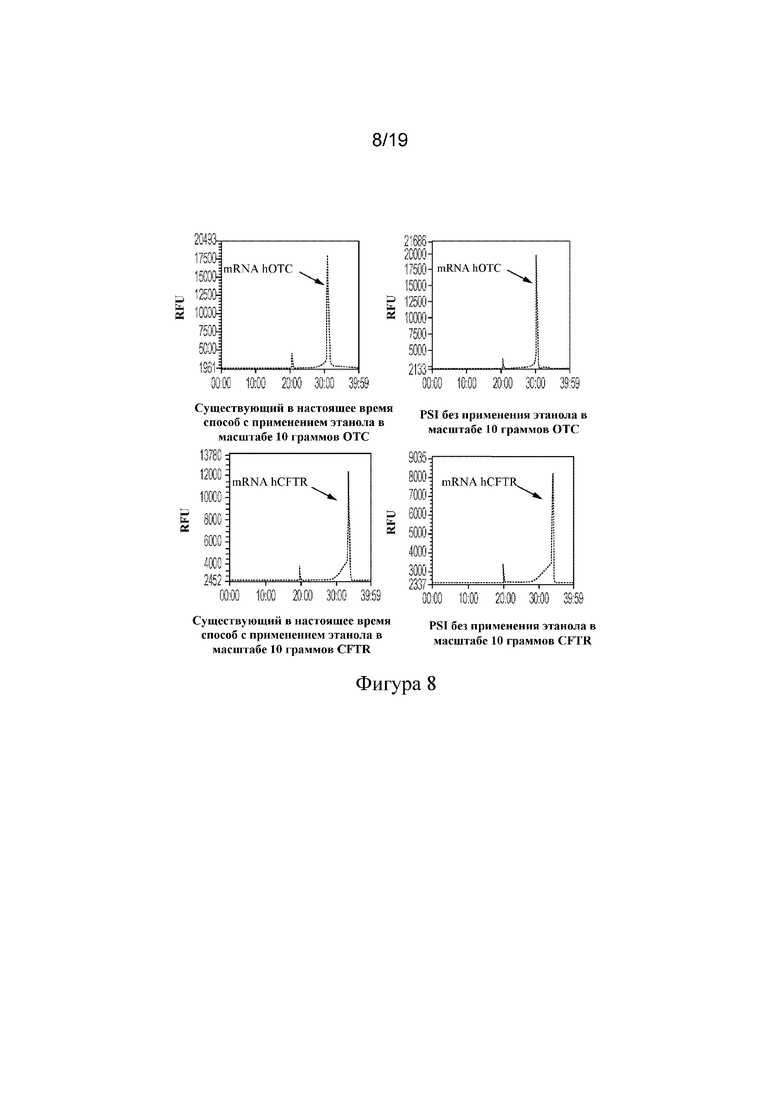




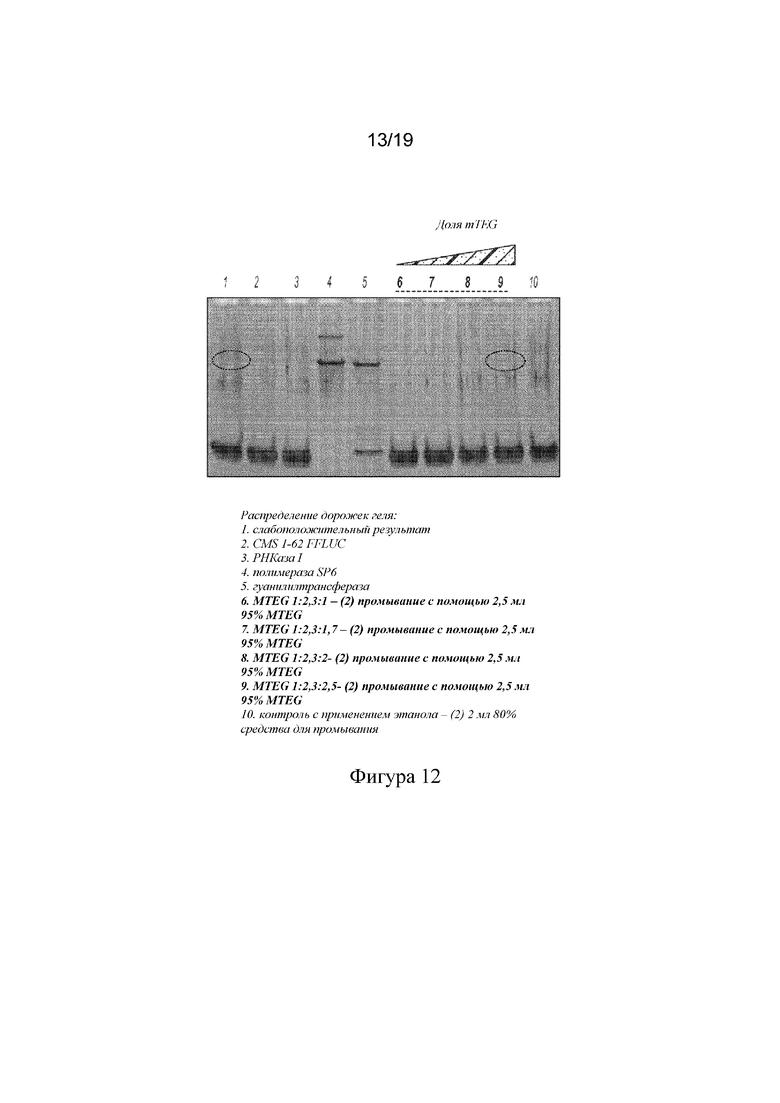


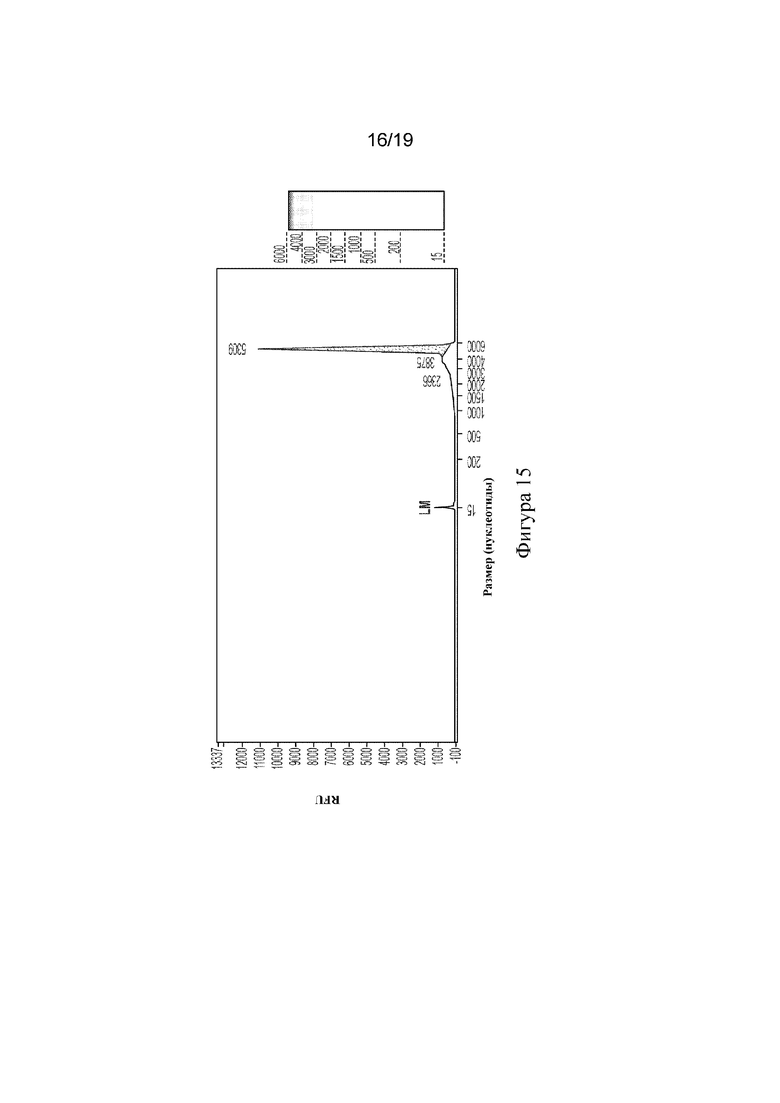

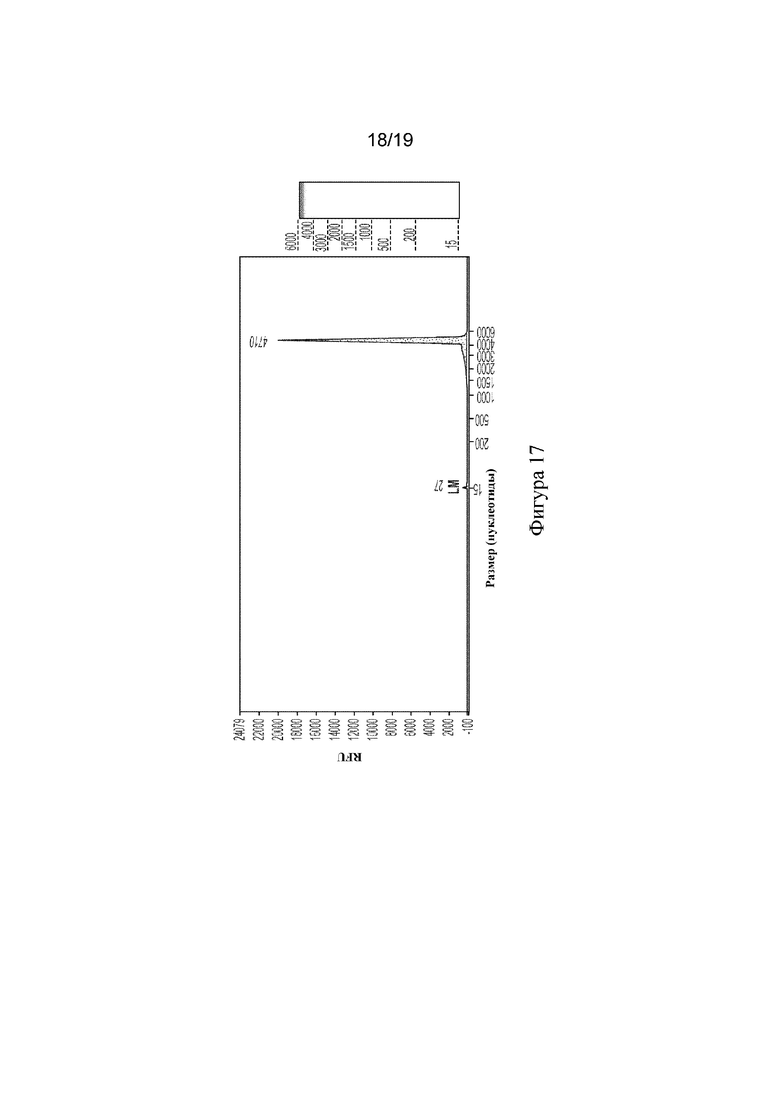
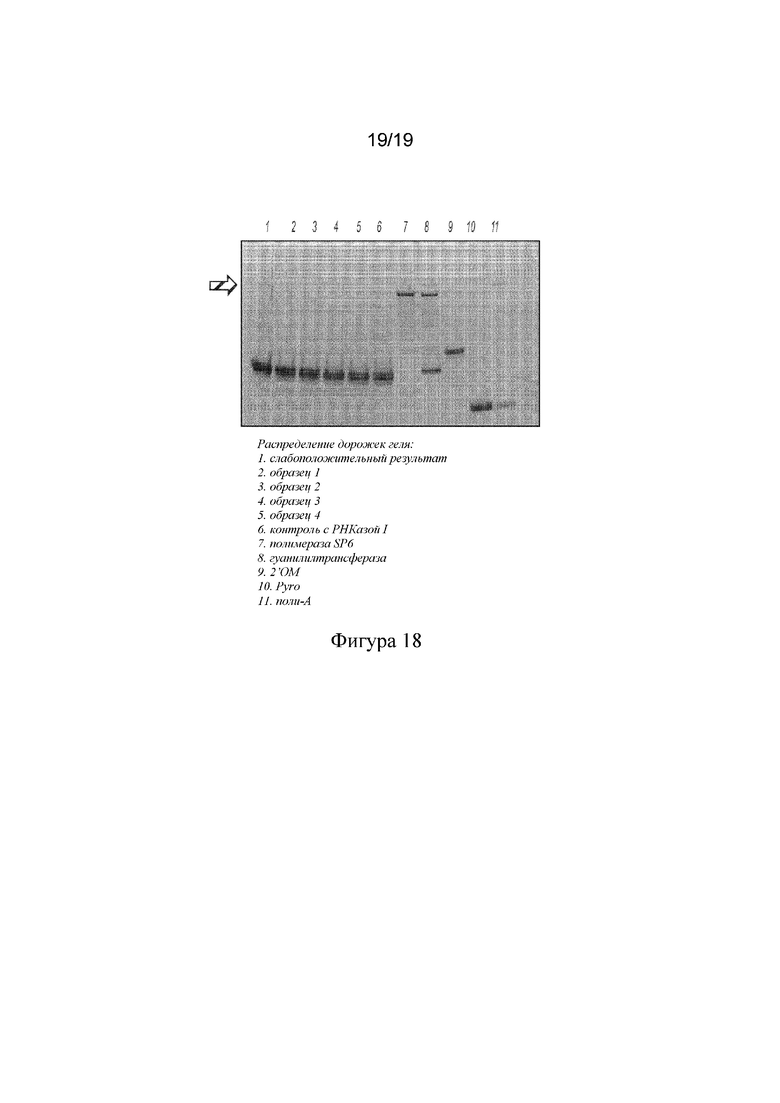
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая способ очистки матричной РНК (mRNA) (варианты). В одном из вариантов способ включает осаждение mRNA в суспензии, содержащей высокомолярный раствор соли и амфифильный полимер, с получением осажденной mRNA; захватывание осажденной mRNA; промывание осажденной mRNA раствором для промывания с очисткой осажденной mRNA и солюбилизирование осажденной mRNA с получением очищенной mRNA. Изобретение расширяет арсенал способов очистки матричной РНК (mRNA). 2 н. и 29 з.п. ф-лы, 18 ил., 8 табл., 9 пр.
1. Способ очистки матричной РНК (mRNA), включающий
a) осаждение mRNA в суспензии, содержащей высокомолярный раствор соли и амфифильный полимер, с получением осажденной mRNA;
b) захватывание осажденной mRNA;
c) промывание осажденной mRNA, захваченной на стадии b), раствором для промывания с очисткой осажденной mRNA и
d) солюбилизирование осажденной mRNA из стадии c) с получением очищенной mRNA.
2. Способ по п. 1, где очищенная mRNA по сути не содержит загрязняющих примесей, содержащих короткие молекулы абортивной РНК, длинные молекулы абортивной РНК, двухцепочечную РНК (dsRNA), остаточную плазмидную ДНК, остаточные ферменты транскрипции in vitro, остаточный растворитель и/или остаточную соль.
3. Способ по п. 1, где амфифильный полимер выбран из монометилового эфира триэтиленгликоля (MTEG), полиэтиленгликоля (PEG) или их комбинаций.
4. Способ по любому из пп. 1-3, где высокомолярный раствор соли содержит гуанидинтиоцианат (GSCN).
5. Способ по любому из пп. 1-3, где раствор для промывания, содержащий амфифильный полимер, применяют для промывания mRNA на стадии c).
6. Способ по п. 5, где амфифильный полимер выбран из монометилового эфира триэтиленгликоля (MTEG), полиэтиленгликоля (PEG) или их комбинаций.
7. Способ по п. 5, где концентрация амфифильного полимера в растворе для промывания составляет от приблизительно 50% до приблизительно 90% вес/объем.
8. Способ по любому из пп. 1-7, где раствор для промывания является водным.
9. Способ по п. 5, где раствор для промывания содержит неводный компонент, где указанный неводный компонент раствора для промывания представляет собой этанол.
10. Способ по любому из пп. 1-9, где захватывание осажденной mRNA осуществляется с помощью фильтра, где фильтр выбран из фильтра для микрофильтрации или фильтра для ультрафильтрации.
11. Способ по п. 10, где применяют вспомогательное фильтрующее средство.
12. Способ по любому из пп. 1-11, где выход и/или чистота очищенной mRNA составляет от приблизительно 90% до приблизительно 99%.
13. Способ очистки матричной РНК (mRNA), включающий
a) осаждение mRNA в суспензии, содержащей высокомолярный раствор соли и амфифильный полимер;
b) захватывание mRNA с помощью фильтра и
c) промывание mRNA из стадии b) раствором MTEG с получением очищенной mRNA, по сути не содержащей загрязняющих примесей.
14. Способ по п. 13, где выход очищенной mRNA составляет от 70% до 99%.
15. Способ по любому из пп. 13-14, где осажденная mRNA содержит по меньшей мере 100 мг, 1 г, 10 г, 100 г, 1 кг, 10 кг, 100 кг, одну метрическую тонну или десять метрических тонн mRNA или любое промежуточное количество.
16. Способ по любому из пп. 13-15, где амфифильный полимер выбран из монометилового эфира триэтиленгликоля (MTEG), полиэтиленгликоля (PEG) или их комбинаций.
17. Способ по любому из пп. 13-16, где высокомолярный раствор соли содержит гуанидинтиоцианат (GSCN).
18. Способ по любому из пп. 13-17, где способ не предусматривает применение этанола.
19. Способ по любому из пп. 13-18, где очищенная mRNA по сути не содержит загрязняющих примесей, содержащих короткие молекулы абортивной РНК, длинные молекулы абортивной РНК, двухцепочечную РНК (dsRNA), остаточную плазмидную ДНК, остаточные ферменты транскрипции in vitro, остаточный растворитель и/или остаточную соль.
20. Способ по п. 1, включающий, на стадии a), осаждение mRNA в растворе гуанидинтиоцианата (GSCN), содержащем MTEG, центрифугирование раствора с получением осадка mRNA, и ресуспендирование осадка mRNA в буфере; и, на стадии b), захватывание mRNA на фильтре посредством нанесения суспензии на фильтр; и где раствор для промывания со стадии c) представляет собой раствор MTEG; и где очищенная mRNA стадии d) по сути не содержит загрязняющих примесей.
21. Способ по п. 20, где очищенная mRNA по сути не содержит загрязняющих примесей, содержащих короткие молекулы абортивной РНК, длинные молекулы абортивной РНК, двухцепочечную РНК (dsRNA), остаточную плазмидную ДНК, остаточные ферменты транскрипции in vitro, остаточный растворитель и/или остаточную соль.
22. Способ по п. 1, где осажденная mRNA со стадии (a) представляет собой полноразмерную mRNA, полученную посредством осуществления транскрипции in vitro (IVT) посредством смешивания (i) ДНК-матрицы, содержащей промотор, и (ii) РНК-полимеразы с получением неочищенного препарата, содержащего указанную полноразмерную mRNA,
где осажденную полноразмерную mRNA захватывают на стадии (b) посредством нанесения суспензии на фильтр;
где захваченную осажденную полноразмерную mRNA со стадии (b) промывают водным растворителем; и
где очищенная mRNA со стадии (d) по сути не содержит (i) ДНК-матрицу, содержащую промотор, и (ii) РНК-полимеразу.
23. Способ по п. 22, где очищенная полноразмерная mRNA в водном растворе, полученная на стадии (d), также по сути не содержит двухцепочечную РНК (dsRNA).
24. Способ по любому из пп. 1, 13 и 22, где амфифильный полимер содержит MTEG.
25. Способ по п. 24, где суспензия содержит осажденную mRNA, высокомолярный раствор соли и MTEG, при этом конечная концентрация MTEG составляет от приблизительно 15% до приблизительно 45% вес/объем.
26. Способ по п. 1 или 22, где суспензия содержит осажденную mRNA, высокомолярный раствор соли и PEG или MTEG.
27. Способ по п. 3 или 22, где конечная концентрация высокомолярной соли составляет приблизительно 2-4 M, и где указанный амфифильный полимер представляет собой PEG в конечной концентрации PEG составляет от приблизительно 5% до приблизительно 20% вес/объем.
28. Способ по п. 22, где высокомолярный раствор соли содержит GCSN.
29. Способ по п. 28, где амфифильный полимер представляет собой PEG, и где PEG имеет молекулярную массу, составляющую 6000 г/моль.
30. Способ по п. 22, где суспензия дополнительно содержит вспомогательное фильтрующее средство при массовом соотношении с осажденной mRNA, составляющем 2:1; 5:1; 10:1 или 15:1.
31. Способ по п. 20, где на стадии a) конечная концентрация GSCN составляет приблизительно 2-4 M, и конечная концентрация MTEG составляет от приблизительно 20% до приблизительно 40% вес/объем.
| Schmitz A., Riesner D | |||
| ЭПИСКОП | 1927 |
|
SU6000A1 |
| Способ приготовления массы для карандашей | 1921 |
|
SU311A1 |
| WO 2001059098 A2, 16.08.2001 | |||
| WO 2014152966 A1, 25.09.2014 | |||
| WO 2015164773 A1, 29.10.2015 | |||
| WO 2018157133 A1, 30.08.2018 | |||
| СПОСОБ ВЫДЕЛЕНИЯ КОРОТКИХ РНК ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 2014 |
|
RU2558292C1 |
Авторы
Даты
2024-08-27—Публикация
2020-05-15—Подача