Предлагаемое изобретение относится к фармацевтической химии и фармакологии, касается новых 5-аминозамещенных 3-бром-4-нитро-1H-пиразолов, которые могут быть использованы для создания новых лекарственных препаратов, применяемых в терапии депрессивных расстройств.
Депрессивные расстройства являются второй по встречаемости психопатологией и вносят самый значительный вклад в глобальное бремя болезней (37,3% по количеству лет жизни, скорректированных по нетрудоспособности (DALYs) среди всех психических расстройств [GBD 2019 Mental Disorders Collaborators. Global, regional, and national burden of 12 mental disorders in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. The Lancet Psychiatry. 2022, 2(9), 137-150], при этом бремя и распространенность депрессивных расстройств не снижались на протяжении последних 30 лет [Herrman Н. Time for united action on depression: a Lancet-World Psychiatric Association Commission. Lancet (London, England). 2022, 10328(399), 957-1022], a пандемия COVID-19 спровоцировала 25%-ный рост распространенности тревожности и депрессивных расстройств во всем мире [WHO. COVID-19 pandemic triggers 25% increase in prevalence of anxiety and depression worldwide, 2022. - URL: https://www.who.int/news/item/02-03-2022-covid-19-pandemic-triggers-25-increase-in-prevalence-of-anxietv-and-depression-worldwide (дата обращения: 27.01.2024].
Ожидается, что к 2030 году стоимость затрат на лечение депрессивных расстройств превысит 92 миллионов долларов, которые окупятся в 2,5 раза за счет повышения производительности труда, а с учетом прибыли от улучшения здоровья - в 5,3 раза [Chisholm D. Scaling-up treatment of depression and anxiety: a global return on investment analysis.
The Lancet Psychiatry. 2016, 5(3), 415-424]. Приведенные выше факты убедительно обосновывают необходимость снижения бремени депрессивных расстройств как с медицинской, так и социальной и экономической точек зрения.
Для решения данной проблемы важным является создания новых лекарственных препаратов для лечения депрессивных расстройств.
Прототипом изобретения является производные 5-аминозамещенных тиетансодержащих 3-бром-4-нитропиразолов формулы:
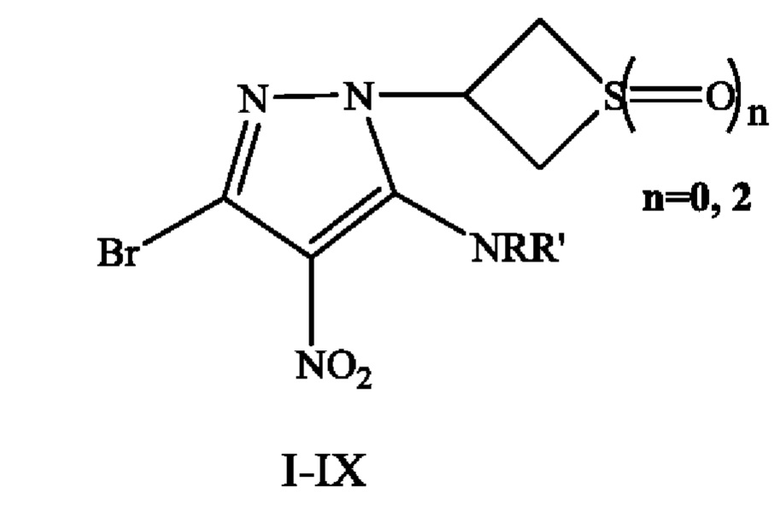
проявляющие антидепрессивную активность [Патент RU 2801039 С1, 2023 г. ].
Задачей изобретения является расширение арсенала биологически активных веществ, используемых для коррекции депрессивных расстройств, а также создание более безопасных и эффективных антидепрессантов.
Технический результат - получение новых 5-аминозамещенных 3-бром-4-нитро-1H-пиразолов, обладающих антидепрессивной активностью.
Сущность изобретения: 5-аминозамещенные 3-бром-4-нитро-1H-пиразолы (I-V) общей формулы:
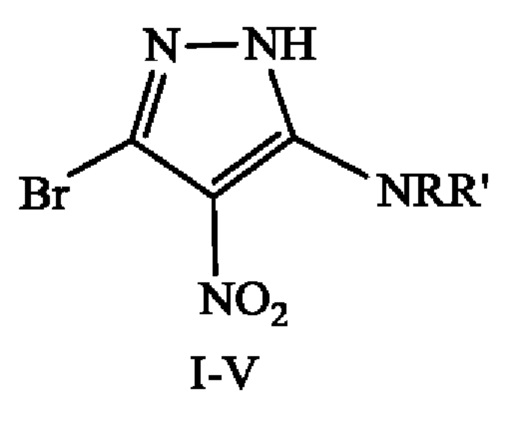
где NRR' представляет собой бензиламино (соединение I), анилино (соединение II), пирролидино-1 (соединение III), пиперидино-1 (соединение IV), 4-метилпиперазино-1 (соединение V), проявляющие антидепрессивную активность.
Указанные соединения и их свойства в литературе не описаны.
Заявляемые соединения синтезировали следующим образом.
Взаимодействие 3,5-дибром-4-нитропиразола с 2-хлорметилтиираном приводит к образованию 3,5-дибром-4-нитро-1-(тиетан-3-ил)-1H-пиразола [Реакции тииранов с NH-гетероциклами. / Ф.А. Халиуллин, Е.Э. Клен, Н.Н. Макарова и др. // ХГС.- 2020. - № 56(9). - С. 1213-1217].
Синтез 3,5-дибром-4-нитро-1-(1,1-диоксотиетан-3-ил)-1H-пиразола осуществлен с использованием 10-кратного мольного избытка 36% раствора пероксида водорода в ледяной уксусной кислоте при кипячении в течение 45 мин [Реакции тииранов с NH-гетероциклами. 2*. С-бром/нитро-1-(тиетан-3-ил)пиразолы - удобные синтоны для получения замещенных 1-(тиетан-3-ил)пиразолов. / Е.Э. Клен, Н.Н. Макарова, Ф.А. Халиуллин и др. // Журн. орг.химии. - 2022. - № 58(9). - С. 926-935].
Реакцией 3,5-дибром-1-(1,1-диоксотиетан-3-ил)-4-нитро-1H-пиразола с 3-х/5-кратным мольным избытком аминов получают 5-аминозамещенные 3-бром-1-(1,1-диоксотиетан-3-ил)-4-нитро-1H-пиразолы [Синтез и антидепрессивная активность 5-аминозамещенных 3-бром-1-(1,1-диоксотиетан-3-ил)-4-нитро-1H-пиразолов / Е.Э. Клен, И.Л. Никитина, Ф.А. Халиуллин [и др.] // Химико-фармацевтический журнал. - 2023. - № 57(8).-С. 33-40].
Поставленная задача достигается тем, что 5-аминозамещенные 3-бром-4-нитро-1-(1,1-диоксотиетан-3-ил)-1H-пиразолы кипятят с этилатом натрия в течение 2,5 часов и получают 5-аминозамещенные 3-бром-4-нитро-1H-пиразолы (I-V).
Общая схема синтеза соединений:
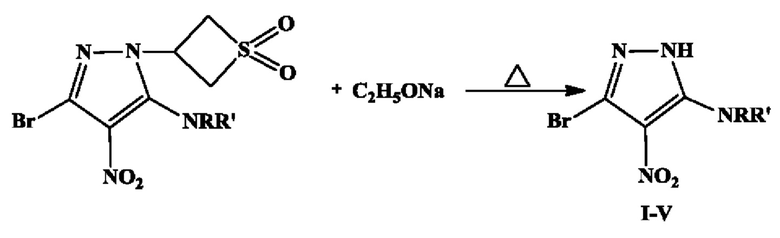
где NRR' представляет собой бензиламино (соединение I), анилино (соединение II), пирролидино-1 (соединение III), пиперидино-1 (соединение IV), 4-метилпиперазино-1 (соединение V).
Изобретение иллюстрируется следующими примерами.
Пример 1. N-Бензил-3-бром-4-нитро-1H-пиразол-5-амин (I). К 10 мл абсолютного этанола прибавляют 0,05 г (2,2 ммоль) металлического натрия и нагревают до прекращения выделения пузырьков газа. Затем прибавляют 0,80 г (2,0 ммоль) N-бензил-3-бром-1-(1,1-диоксотиетан-3-ил)-4-нитро-1H-пиразол-5-амина и кипятят 2,5 ч. Реакционную смесь упаривают при пониженном давлении, остаток обрабатывают 20 мл бензола, растворяют в 10 мл воды, фильтруют. Фильтрат нейтрализуют разбавленным раствором уксусной кислоты до рН 3-4. Выпавший осадок отфильтровывают, промывают водой, сушат. Получают 0,50 г (84%) соединения I. Очищают перекристаллизацией из этанола. Т.пл. 218,0-219,1°С.
ИК-спектр, v, см-1 (KBr): 1290, 1482, 1639 (C-N, C=N, С=С), 1320, 1515 (NO2), 3265 (NH), 3376 (NH). Спектр ЯМР 1H (DMSO-d6, 500 МГц),δ, м.д.: 4,50-4,51 (м, 2Н, СН2), 7,24-7,26 (м, 1Н, CHar 7,32-7,33 (м, 4H, CHar), 8,30 (уш.с, 1Н, NH). Спектр ЯМР 13С (DMSO-d6, 125 МГц), δ, м.д.: 46,1 (NHCH2), 115,4 (Cpyr), 122,8 (С3), 127,4 (CHar), 127,7 (CHar), 128,9 (CHar), 138,3 (Car), 148,3 (Cpyr).
Элементный анализ.
Найдено, %: С 40,43; Н 3,05; N 18,86 - C10H9O2BrH4.
Вычислено, %: С 40,40; Н 3,02; N 18,83.
Заявляемое соединение I представляет собой светло-желтый кристаллический порошок, растворимый в ацетоне, в диметилсульфоксиде, не растворимый в хлороформе, в бензоле и гексане.
Пример 2. 3-Бром-4-нитро-N-фенил-1H-пиразол-5-амин (II). Получают аналогично примеру 1 из 0,77 г (2 ммоль) 3-бром-1-(1,1-диоксотиетан-3-ил)-4-нитро-N-фенил-1H-пиразол-5-амина. Получают 0,32 г (61%) соединения П. Очищают перекристаллизацией из этанола. Т. разл. 230,8°С.
ИК-спектр, v, см-1 (KBr): 1283, 1472, 1588 (C-N, C=N, С=С), 1342, 1604 (NO2), 3292 (NH), 3304 (NH). Спектр ЯМР 1H (DMSO-d6, 500 МГц), δ, м.д.: 7,16-7,40 (м, 5Н, CHar), 9,29 (уш.с, 1Н, NH). Спектр ЯМР 13С (DMSO-d6, 125 МГц), δ, м.д.: 121,7 (Cpyr), 124,6 (Car), 124,7 (Cpyr), 129,3 (CHar), 137,9 (Car), 145,3 (Cpyr).
Элементный анализ.
Найдено, %: С 38,19; Н 2,49; N 19,79 - C9H7BrN4O2.
Вычислено, %: С 38,04; Н 2,34; N 19,64.
Заявляемое соединение II представляет собой желтый кристаллический порошок, растворимый в ацетоне, в диметилсульфоксиде, не растворимый в хлороформе, в бензоле и гексане.
Пример 3. 3-Бром-4-нитро-5-(пирролидин-1-ил)-1H-пиразол (III). Получают аналогично примеру 1 из 0,73 г (2 ммоль) 3-бром-1-(1,1-диоксотиетан-3-ил)-4-нитро-5-(пирролидин-1-ил)-1Н-пиразола. Получают 0,50 г (90%) соединения III. Очищают перекристаллизацией из смеси этанола и воды, объемное соотношение 1:2. Т.пл. 190,0-191,5°С.
ИК-спектр, v, см-1 (КВт): 1304, 1428, 1455 (C-N, C=N, С=С), 1343, 1625 (NO2), 3247 (NH). Спектр ЯМР 1H (CDC13, 500 МГц), δ, м.д.: 2,04-2,07 (м, 4Н, (СН2)2), 3,46-3,48 (м, 4H, N(CH2)2), 8,30 (уш.с, 1H, NH). Спектр ЯМР 13С (CDC13, 125 МГц), δ, м.д.: 25,6 (2СН2), 50,5 (N(CH2)2), 125,1 (Cpyr), 146,0 (Cpyr).
Элементный анализ.
Найдено, %: С 32,20; Н 3,47; N 21,46 - C7H9O2BrN4.
Вычислено, %: С 32,07; Н 3,34; N 21,33.
Заявляемое соединение III представляет собой желтый кристаллический порошок, растворимый в ацетоне, в диметилсульфоксиде, не растворимый в хлороформе, в бензоле и гексане.
Пример 4. 4-[3-Бром-4-нитро-1H-пиразол-5-ил]пиперидин (IV). Получают аналогично примеру 1 из 0,76 г (2 ммоль) 4-[3-бром-1-(1,1-диоксотиетан-3-ил)-4-нитро-1H-пиразол-5-ил]пиперидина. Получают 0,49 г (96%) соединения IV. Очищают перекристаллизацией из смеси этанола и воды, объемное соотношение 1:2. Т.пл. 186,7-187,2°С
ИК-спектр, v, см-1 (KBr): 1259, 1365, 1473 (C-N, C=N, С=С), 1328, 1603 (NO2), 3238 (NH). Спектр ЯМР 1H (DMSO-d6, 500 МГц), δ, м.д.: 1,16-1,56 (м, 6Н, (СН2)3), 3,19-3,31 (м, 4Н, N(CH2)2). Спектр ЯМР 13С (DMSO-d6, 125 МГц), δ, м.д.: 23,6 (СН2), 25,3 (2СН2) 50,5 (N(CH2)2).
Элементный анализ.
Найдено, %: С 32,20; Н 3,47; N 21,46 - C8H11O2BrN4.
Вычислено, %: С 32,07; Н 3,34; N 21,33.
Заявляемое соединение IV представляет собой желтый кристаллический порошок, растворимый в ацетоне, в диметилсульфоксиде, не растворимый в хлороформе, в бензоле и гексане.
Пример 5. 1-[3-Бром-4-нитро-1H-пиразол-5-ил]-4-метилпиперазин (V). Получают аналогично примеру 1 из 0,79 г (2 ммоль) 1-[3-бром-1-(1,1-диоксотиетан-3 -ил)-4-нитро-1H-пиразол-5-ил]-4-метилпиперазина.
Получают 0,49 г (88%) соединения V. Очищают перекристаллизацией из воды. Т.разл. 169,9°С
ИК-спектр, v, см-1 (KBr): 1279, 1492, 1557 (C-N, C=N, С=С), 1324, 1575 (NO2), 3439 (NH). Спектр ЯМР 1Н (DMSO-d6, 500 МГц), δ, м.д.: 1,87 (уш.с, 3Н, СН3), 2,40-2,41 (м, 4Н, N(CH2)2), 3,09-3,11 (м, 4Н, N(CH2)2). Спектр ЯМР 13С (DMSO-d6, 125 МГц), δ, м.д.: 46,2 (СН3), 49,7 (N(CH2)2), 54,8 (N(CH2)2), 123,0 (Cpyr), 155,3 (Cpyr).
Элементный анализ.
Найдено, %: С 33,12; Н 4,17; N 24,14 -C8H12O2BrN5.
Вычислено, %: С 32,99; Н 4,04; N 24,01.
Заявляемое соединение V представляет собой желтый кристаллический порошок, растворимый в воде, в диметилсульфоксиде, не растворимый в ацетоне, в хлороформе, в бензоле и гексане.
Пример 6. Исследование антидепрессивной активности соединений в тестах принудительного плавания и подвешивания за хвост.
Эксперимент провели на белых неинбредных мышах-самцах массой 18-20 г в соответствии с рекомендациями Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей (ETS No. 123, 1986), Правилами надлежащей лабораторной практики Евразийского экономического союза в сфере обращения лекарственных средств (Решение Совета ЕЭК от 03 ноября 2016 года № 81 «Об утверждении Правил надлежащей лабораторной практики Евразийского экономического союза в сфере обращения лекарственных средств»).
Животные содержались в стандартных условиях вивария с естественным световым режимом на полнорационной сбалансированной диете (ГОСТ Р 50258-92) при свободном доступе к воде и пище. Выполнено 2 серии экспериментов. В каждой из серий мыши (n=42 и n=21) случайным образом были распределены на группы: 1 - контроль; 2 -амитриптилин (препарат сравнения) и 3-6 - исследуемые соединения (таблица 1).
Соединения I - V ex tempore суспендировали с 1-2 каплями Твин-80 (Полисорбат Lauropan Т/80, Италия) и разводили изотоническим раствором натрия хлорида (для введения из расчета 0,2 мл / 20 г веса тела); вводили за 30 мин до тестирования однократно внутрибрюшинно (в/б) в дозе, эквимолярной 10 мг/кг амитриптилина (10,06 мг/кг; 10,20 мг/кг; 9,41 мг/кг; 9,92 мг/кг; 10,46 мг/кг, соответственно). Препарат сравнения - амитриптилин (3-(10,11-дигидро-5H-дибенз[а,d]циклогептен-5-илиден)-N,N-диметил-1-пропанамин Амитриптилин, раствор для внутривенного и внутримышечного введения, 10 мг/мл, ФГУП «Московский эндокринный завод», Россия) вводили однократно в/б в дозе 10 мг/кг за 30 мин до тестов. Мыши контрольных групп получали однократно в/б эквиобъемные количества изотонического раствора натрия хлорида с 1-2 каплями Твин-80.
Антидепрессивную активность оценивали в двух тестах: принудительного плавания (ТПП) и подвешивания за хвост (ТПХ), являющихся общепринятыми скрининговыми тестами с высокой предиктивной валидностью.
Статистическую обработку данных выполняли с помощью программы Statistica 12.0 («StatSoft», USA): определяли нормальность распределения (критерии Колмогорова-Смирнова с поправкой Лиллиефорса, Шапиро-Уилка); распределение во всех случаях отличалось от нормального); для описания вариационных рядов рассчитывали медиану (Me), квартили (25 и 75%), среднеквадратичное отклонение и минимальное / максимальное значение. Для сравнения применяли однофакторный дисперсионный анализ Краскела-Уоллиса (Н-критерий), для попарного межгруппового сравнения использовали U-критерия Манна-Уитни. Критический уровень значимости при проверке статистических гипотез принимался равным 0,05 (Гланц С. Медико-биологическая статистика. Электронная книга. Москва: Практика, 1999. 459 с).
Тест принудительного плавания
ТПП воспроизводили по методу Щетинина Е.В. и соавт. (Щетинин Е.В. Биоритмологический подход к оценке принудительного плавания как экспериментальной модели «депрессивного» состояния. Журнал высшей нервной деятельности им. И.П. Павлова. 1989, 5(39), 958-964; Porsolt R.D. Animal model of depression. Biomedicine. 1979, 3(30), 139-140), в котором регистрировали длительность иммобилизации животных (ДИМ ТПП, в секундах), количество коротких периодов иммобилизации, периодов активного плавания, периодов пассивного плавания, выскакиваний и рассчитывали биоритмологический индекс депрессивности (ИД), который представляет собой отношение числа коротких периодов иммобилизации (<6 с) к количеству периодов активного плавания. ИД считают наиболее надежным маркером депрессивного состояния и реализации антидепрессивного эффекта по сравнению с общей ДИМ. Поведение животных на протяжении 6 мин записывали на видеокамеру (Panasonic V760) и оценивали (в течение последних 4 мин) с помощью программы «BrainTest» (Габидуллин Р.А., Иванова О.А., Никитина И.Л. Свидетельство о государственной регистрации программы для ЭВМ № 2008610170. 2008).
Проведенный скрининг показал, что при однократном в/б введении в ТПП соединения I, II, III и IV проявляли антидепрессивные свойства, статистически значимо понижая ИД на 16% (р=0,0349), 38% (р=0,0022), 24% (р=0,0139) и 35% (р=0,0069). Эффект соединения I значимо уступал (р=0,00432), а эффекты соединений II - IV сопоставимы с эффектом амитриптилина, который снижал ДИМ на 23% (р=0,0011) по сравнению с контролем. При этом все соединения I-V, как и амитриптилин, статистически значимо не изменяли ДИМ ТПП (Таблица 1).
Тест подвешивания за хвост
Исследуемые соединения и препарат сравнения вводили в эквимолярной дозе однократно внутрибрюшинно (см. ТПП). Тестирование проводили через 30 мин после введения по методу Steru L. и соавт.(Stem L. The tail suspension test: A new method for screening antidepressants in mice. Psychopharmacology. 1985, 3(85), 367-370). Поведение мышей записывали на видеокамеру в течение 6 мин. и оценивали с помощью программы «BrainTest» (Габидуллин Р.А., Иванова О.А., Никитина И.Л. Свидетельство о государственной регистрации программы для ЭВМ № 2008610170. 2008), регистрируя суммарную длительность иммобилизации ТПХ в секундах (ДИМ ТПХ).
Среди изученных соединений при однократном в/б введении статистически значимо снижали ДИМ ТПХ только соединения V и II (на 55% (р=0,0081) и 52% (р=0,01) соответственно). Соединения I и III незначительно снижали этот показатель на 65% и 33% соответственно (р>0,05), а соединение IV не оказывало влияния на ДИМ ТПХ. Эффект соединений V и II по выраженности был сравним с эффектом амитриптилина (р=0,6200 и р=0,13203), который понижал ДИМ ТПХ на 53% (1 серия, р=0,0349) и не оказывал значимого влияния во 2 серии (снижал на 18,2%, р=0,3659 по сравнению с контролем) (таблица 1).
Пример 7. Изучение активности соединений в тесте открытое поле (ОП).
Для исключения ложноположительных / ложноотрицательных результатов в скрининговых тестах и дополнительной фармакодинамической характеристики исследуемых соединений их эффект оценивали в тесте ОП после однократного внутрибрюшинного введения в дозах, использованных ранее в ТПХ и ТПП (см. примеры 6 и 7), по методу, описанному Вальдман А., Пошивалов В. (1984) (Вальдман А., Пошивалов В. Фармакологическая регуляция внутривидового поведения. Медицина. 1984. 208). Через 30 мин после введения мышей помещали в восьмигранную арену ОП и в течение 4 мин записывали их поведение с помощью видеокамеры, затем анализировали видеозапись с помощью программы «BrainTest» (Габидуллин Р.А., Иванова О.А., Никитина И.Л. Свидетельство о государственной регистрации программы для ЭВМ № 2008610170. 2008). Регистрировали горизонтальную двигательную активность (паттерн перемещение), а также другие отдельные поведенческие паттерны (норка, обнюхивание, стойка с упором, стойка и движение на месте), необходимые для расчета показателей ориентировочно-исследовательской активности (ОИА; сумма паттернов норка+обнюхивание+перемещение) и эмоциональной тревожности (ЭТ; сумма паттернов стойка с упором+стойка+движение на месте) (таблица 1).
Все соединения, сравнимо с амитриптилином, продемонстрировали отсутствие значимого влияния на количество перемещений по сравнению с контролем, однако в группах, получавших соединения V и I, отмечена слабая тенденция к увеличению горизонтальной двигательной активности на 57% (р>0,05). Под влиянием изученных соединений I-V показатели ОИА и ЭТ также статистически значимо не изменялись, в то же время, в серии I наблюдалась общая тенденция к увеличению ЭТ на 54-92% (p>0,05) во всех опытных группах (Таблица). 

Таким образом, полученные результаты позволяют заключить, что при однократном внутрибрюшинном введении неинбредным мышам - самцам в эквимолярных дозах все изученные соединения I - V проявляли антидепрессивную активность разной степени выраженности. Наибольшую активность проявило соединение II, которое значимо снизило ИД, ДИМ ТПХ мышей-самцов в скрининговых тестах.
| название | год | авторы | номер документа |
|---|---|---|---|
| 5-АМИНОЗАМЕЩЕННЫЕ ТИЕТАНСОДЕРЖАЩИЕ 3-БРОМ-4-НИТРОПИРАЗОЛЫ С АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ | 2022 |
|
RU2801039C1 |
| 5-АМИНОЗАМЕЩЕННЫЕ 3-БРОМ-4-НИТРО-1-(ТИЕТАН-3-ИЛ)-1Н-ПИРАЗОЛЫ, ПРОЯВЛЯЮЩИЕ АНТИДЕПРЕССИВНУЮ АКТИВНОСТЬ | 2023 |
|
RU2817972C1 |
| N-МОНО- И N,N-ДИТИЕТАНСОДЕРЖАЩИЕ 5-БРОМ-2,4-ДИГИДРО-1,2,4-ТРИАЗОЛ-3-ОНЫ, ПРОЯВЛЯЮЩИЕ АНТИДЕПРЕССИВНУЮ АКТИВНОСТЬ | 2024 |
|
RU2826999C1 |
| 1-(1,1-ДИОКСОТИЕТАН-3-ИЛ)-4-(2-ОКСО-2-ФЕНИЛЭТИЛ)-1,2,4-ТРИАЗОЛ-4-ИЙ БРОМИД, ПРОЯВЛЯЮЩИЙ АНТИДЕПРЕССИВНУЮ АКТИВНОСТЬ | 2022 |
|
RU2785340C1 |
| ПРОИЗВОДНЫЕ 5-БРОМ-2-(ТИЕТАН-3-ИЛ)-2,4-ДИГИДРО-3H-1,2,4-ТРИАЗОЛ-3-ОНА, ПРОЯВЛЯЮЩИЕ АНТИДЕПРЕССИВНУЮ АКТИВНОСТЬ | 2011 |
|
RU2459818C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АМИНОЗАМЕЩЕННЫХ 1-(1-АДАМАНТИЛ)-3,4-ДИНИТРО-1Н-ПИРАЗОЛОВ | 2013 |
|
RU2533557C1 |
| ПРОИЗВОДНЫЕ 2-БРОМ-1-(ТИЕТАНИЛ-3)ИМИДАЗОЛ-4,5-ДИКАРБОНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ АНТИДЕПРЕССИВНУЮ АКТИВНОСТЬ | 2014 |
|
RU2537948C1 |
| ПРОИЗВОДНЫЕ 3-МЕТИЛ-7-(ТИЕТАНИЛ-3)КСАНТИНА, ОБЛАДАЮЩИЕ ГЕМОРЕОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2316551C1 |
| 2-ЗАМЕЩЕННЫЕ-1,2,4,5-ТЕТРАГИДРО-3H-ПИРРОЛО[1,2-a][1,4]ДИАЗЕПИН-3-ОНЫ | 2011 |
|
RU2472795C1 |
| ТРИПЕПТИД, ОБЛАДАЮЩИЙ НЕЙРОПСИХОТРОПНОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2823022C1 |
Изобретение относится к фармацевтической химии и фармакологии, конкретно к производному 5-аминозамещенного 3-бром-4-нитро-1Н-пиразола указанной ниже общей формулы, в которой NRR' представляет собой бензиламино (соединение I), анилино (соединение II), пирролидино-1 (соединение III), пиперидино-1 (соединение IV) и 4-метилпиперазино-1 (соединение V). Соединения по изобретению обладают антидепрессивной активностью, сравнимой с амитриптилином. 6 з.п. ф-лы, 1 табл., 7 пр.
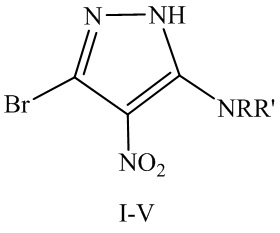
1. Производное 5-аминозамещенного 3-бром-4-нитро-1Н-пиразола (соединения I-V) общей формулы
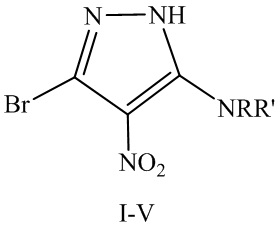 ,
,
где NRR' представляет собой бензиламино (соединение I), анилино (соединение II), пирролидино-1 (соединение III), пиперидино-1 (соединение IV), 4-метилпиперазино-1 (соединение V).
2. Производное по п. 1, представляющее собой N-бензил-3-бром-4-нитро-1H-пиразол-5-амин.
3. Производное по п. 1, представляющее собой 3-бром-4-нитро-N-фенил-1H-пиразол-5-амин.
4. Производное по п. 1, представляющее собой 3-бром-4-нитро-5-(пирролидин-1-ил)-1H-пиразол.
5. Производное по п. 1, представляющее собой 4-[3-бром-4-нитро-1H-пиразол-5-ил]пиперидин.
6. Производное по п. 1, представляющее собой 1-[3-бром-4-нитро-1H-пиразол-5-ил]-4-метилпиперазин.
7. Производное по любому из пп. 1-6, проявляющее антидепрессивную активность.
| 5-АМИНОЗАМЕЩЕННЫЕ ТИЕТАНСОДЕРЖАЩИЕ 3-БРОМ-4-НИТРОПИРАЗОЛЫ С АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ | 2022 |
|
RU2801039C1 |
| E.E | |||
| KLEN et al., Synthesis and antidepressant activity of 5-amine-substituted 3-bromo-1-(1,1-dioxothietan-3-yl)-4-nitro-1H-pyrazoles, PHARMACEUTICAL CHEMISTRY JOURNAL, 2023, vol | |||
| Способ получения на волокне оливково-зеленой окраски путем образования никелевого лака азокрасителя | 1920 |
|
SU57A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Аппарат для раструски табака | 1924 |
|
SU1202A1 |
| FR 2886142 A1, 01.12.2006 | |||
| ПРОИЗВОДНЫЕ 5-БРОМ-2-(ТИЕТАН-3-ИЛ)-2,4-ДИГИДРО-3H-1,2,4-ТРИАЗОЛ-3-ОНА, ПРОЯВЛЯЮЩИЕ АНТИДЕПРЕССИВНУЮ АКТИВНОСТЬ | 2011 |
|
RU2459818C1 |
Авторы
Даты
2024-09-20—Публикация
2024-03-01—Подача