Область техники
Техническое решение относится к фармацевтике, в частности относится к вариантам коррекции комплекса метаболических и гормональных показателей при сахарном диабете 2 типа с помощью интраназально вводимого инсулина.
Уровень техники
Известна фармацевтическая композиция на основе инсулина для интраназального введения (RU2619855C1 от 27.09.2016 класс МПК A61K 38/28, A61K 31/205, A61K 9/08, A61K 9/12, A61K 9/06, A61P 25/28), предназначенная для терапии болезни Альцгеймера, как нового способа предотвращения и лечения этого нейродегенеративного заболевания, развивающегося в пожилом возрасте. Эта композиция содержит от 0.05 до 100 МЕ инсулина и от 0.05 до 10% дихолина сукцината, как добавки, улучшающей всасывание инсулина. Указанная композиция производится в форме интраназального спрея.
Недостатком этой фармацевтической композиции является то, что ее использование ограничено болезнью Альцгеймера, которая не является широко распространенным и социально значимым заболеванием, развивается в пожилом возрасте (обычно у пациентов в возрасте старше 80 лет). Использование такой композиции для лечения и профилактики сахарного диабета 2 типа авторами не рассматривалось и не предусмотрено, отсутствуют данные о ее влиянии на метаболические и гормональные показатели у животных, а также на функциональную активность эндокринной системы.
Известен способ интраназального введения инсулина в мозг (US5624898A; US6180603B1; US6313093B1; US6342478B1 от 16.08.1999, класс МПК A61K38/18; A61K38/28; A61K38/30; A61K9/00), который состоит в нанесении фармацевтической композиции, содержащей определенное, вызывающее необходимый физиологический эффект количество инсулина, непосредственно в носовую полость экспериментального животного (млекопитающего). В результате этого инсулин всасывается через слизистую оболочку носа и далее транспортируется в мозг по аксональному пути в количествах, которые необходимы для стимуляции пролиферативной активности клеток мозга, для повышения их выживаемости, нормализации их функциональной активности, тем самым, обеспечивая нейропротекторный эффект интраназально вводимого инсулина на нейроны и глиальные клетки головного мозга.
Недостатком технического решения является то, что оно ограничено воздействием интраназально вводимого инсулина на восстановление когнитивных функций, нарушенных при нейродегенеративных заболеваниях, в том числе ассоциированных с сахарным диабетом (диабетическая энцефалопатия, диабет-ассоциированный когнитивный дефицит), в то время как возможное воздействие интраназально вводимого инсулина на метаболические и гормональные показатели, такие как глюкозный гомеостаз, липидный статус, уровни инсулина, лептина, глюкагоноподобного пептида-1, грелина, гормонов гипоталамо-гипофизарно-гонадной и гипоталамо-гипофизарно-тиреоидной осей, нарушенных в условиях сахарного диабета 2 типа в работе не рассматривается.
Известен фармацевтический препарат для интраназальной доставки инсулина мужчинам (WO9422461A1 от 13.10.1994, класс МПК A61K38/28; A61K47/40; A61K9/00), содержащий природный гормон инсулин или его синтетический аналог и метилированный β-циклодекстрин с различной степенью замещения метильными радикалами (0.5–3.0). Этот фармацевтический препарат представляет собой твердый порошок или полутвердую субстанцию. Для его создания сначала получают раствор гормона инсулина (или его фармакологического аналога) и метилированного β-циклодекстрина, затем полученный раствор замораживают и подвергают процедуре лиофилизации, что позволяет получить целевую субстанцию (твердый порошок или полутвердый продукт).
Недостатком указанной фармацевтической композиции для интраназальной доставки инсулина является то, что в патенте не представлен спектр ее возможного клинического применения у мужчин, а также отсутствуют какие-либо сведения о возможности использования и потенциальной фармакологической эффективности этой композиции для восстановления глюкозного гомеостаза, метаболических и гормональных показателей, массы тела, эндокринных показателей, нарушенных у пациентов с сахарным диабетом 2 типа.
Известно устройство для назальной доставки различных лекарственных препаратов (WO2020142206A1, US2019066921W от 17.12.2019, класс МПК A61M11/02; A61M15/00; A61M15/08), которое представляет собой генератор струи, включающей интраназально вводимое целевое лекарственное соединение и инертное вещество-носитель. Лекарственное соединение находится в виде порошка, суспензии, диспергированной субстанции или жидкости. Вводимый интраназально лекарственный препарат откладывается в верхней части полости носа – в обонятельной области. Далее, будучи депонирован в обонятельной области, он начинает поступать к структурам мозга, минуя гематоэнцефалический барьер. Вещество-носитель, являющееся производным гидрофторалканов, из баллончика под давлением поступает в диффузор и затем в канал, который содержит интраназально вводимый лекарственный препарат, в результате чего этот препарат переходит в форму аэрозоля, проходит через сопло устройства, и это обеспечивает доставку струи, содержащий лекарственный препарат, в верхнюю часть носовой полости пользователя.
Недостатком способа доставки является наличие лишь общих сведений для интраназального введения различных лекарственных препаратов, отсутствие конкретных сведений о применении этого устройства для интраназального способа доставки инсулина при сахарном диабете 2 типа в клинике и лабораторным животным в условиях эксперимента, а также отсутствие данных о влиянии инсулина, как одного из возможных лекарственных препаратов, при его доставке с помощью разработанного авторами устройства для назальной доставки лекарств на метаболические и гормональные показатели, чувствительность к инсулину и эндокринные показатели при сахарном диабете 2 типа.
Известен ряд статей по влиянию интраназально вводимого инсулина на когнитивные функции, ослабленные при сахарном диабете 2 типа, в том числе статьи, посвященные улучшению когнитивных функций у пациентов с этим заболеванием:
1) Benedic C, Hallschmid M, Hatke A, Schultes B, Fehm HL, Born J, et al. Intranasal insulin improves memory in humans. Psychoneuroendocrinology (2004) 29:1326–34. 10.1016/j.psyneuen.2004.04.003
2) Benedict C, Hallschmid M, Schmitz K, Schultes B, Ratter F, Fehm HL, et al.. Intranasal insulin improves memory in humans: superiority of insulin aspart. Neuropsychopharmacology (2007) 32:239–43. 10.1038/sj.npp.1301193
3) Novak V., Milberg W., Hao Y., Munshi M., Novak P., Galica A., Manor B., Roberson P., Craft S., Abduljalil A. Enhancement of vasoreactivity and cognition by intranasal insulin in type 2 diabetes. Diabetes Care. 2014;37:751–759. doi: 10.2337/dc13-1672.
4) Brunner YF, Kofoet A, Benedict C, Freiherr J. Central insulin administration improves odor-cued reactivation of spatial memory in young men. J Clin Endocrinol Metab. (2015) 100:212–9. 10.1210/jc.2014-3018.
5) Zhang H., Hao Y., Manor B., Novak P., Milberg W., Zhang J., Fang J., Novak V. Intranasal insulin enhanced resting-state functional connectivity of hippocampal regions in type 2 diabetes. Diabetes. 2015;64:1025–1034. doi: 10.2337/db14-1000.
6) Galindo-Mendez B, Trevino JA, McGlinchey R, Fortier C, Lioutas V, Novak P, Mantzoros CS, Ngo L, Novak V. Memory advancement by intranasal insulin in type 2 diabetes (MemAID) randomized controlled clinical trial: Design, methods and rationale. Contemp Clin Trials. 2020 Feb;89:105934. doi: 10.1016/j.cct.2020.105934. PMID: 31923471; PMCID: PMC7242142.
7) Gaddam M., Singh A., Jain N., Avanthika C., Jhaveri S., De la Hoz I., Sanka S., Goli S.R. A Comprehensive Review of Intranasal Insulin and Its Effect on the Cognitive Function of Diabetics. Cureus. 2021;13:e17219. doi: 10.7759/cureus.17219.
8) Novak V., Mantzoros C.S., Novak P., McGlinchey R., Dai W., Lioutas V., Buss S., Fortier C.B., Khan F., Aponte Becerra L., et al. MemAID: Memory advancement with intranasal insulin vs. placebo in type 2 diabetes and control participants: A randomized clinical trial. J. Neurol. 2022;269:4817–4835. doi: 10.1007/s00415-022-11119-6.
Недостатком этих статей является то, что в них не приводятся и не анализируются данные о влиянии интраназально вводимого инсулина на метаболические и гормональные показатели, в том числе определяющих функции эндокринной системы, у пациентов с сахарным диабетом 2 типа.
Известен еще один ряд клинических и экспериментальных статей по влиянию интраназально вводимого инсулина на массу тела, пищевое поведение, некоторые метаболические и гормональные показатели при сахарном диабете 2 типа:
1) Ott V, Benedict C, Schultes B, Born J, Hallschmid M. Intranasal administration of insulin to the brain impacts cognitive function and peripheral metabolism. Diabetes Obes Metab. 2012 Mar;14(3):214-21. doi: 10.1111/j.1463-1326.2011.01490.x. Epub 2011 Nov 16. PMID: 21883804.
2) Honda K, Kamisoyama H, Saneyasu T, Sugahara K, Hasegawa S. Central administration of insulin suppresses food intake in chicks. Neurosci Lett 2007; 423: 153– 157.
3) Brown LM, Clegg DJ, Benoit SC, Woods SC. Intraventricular insulin and leptin reduce food intake and body weight in C57BL/6J mice. Physiol Behav 2006; 89: 687– 691.
4) Hallschmid M, Benedict C, Schultes B, Fehm HL, Born J, Kern W. Intranasal insulin reduces body fat in men but not in women. Diabetes 2004; 53: 3024– 3029.
5) Clegg DJ, Riedy CA, Smith KA, Benoit SC, Woods SC. Differential sensitivity to central leptin and insulin in male and female rats. Diabetes 2003; 52: 682– 687.
6) Benedict C, Kern W, Schultes B, Born J, Hallschmid M. Differential sensitivity of men and women to anorexigenic and memory-improving effects of intranasal insulin. J Clin Endocrinol Metab 2008; 93: 1339– 1344.
7) Benedict C, Brede S, Schioth HB et al. Intranasal insulin enhances postprandial thermogenesis and lowers postprandial serum insulin levels in healthy men. Diabetes 2011; 60: 114– 118.
8) Stockhorst U, de Fries D, Steingrueber HJ, Scherbaum WA. Insulin and the CNS: effects on food intake, memory, and endocrine parameters and the role of intranasal insulin administration in humans. Physiol Behav. 2004 Oct 30;83(1):47-54. doi: 10.1016/j.physbeh.2004.07.022. PMID: 15501490.
9) Sanguinetti E, Guzzardi MA, Panetta D, Tripodi M, De Sena V, Quaglierini M, Burchielli S, Salvadori PA, Iozzo P. Combined Effect of Fatty Diet and Cognitive Decline on Brain Metabolism, Food Intake, Body Weight, and Counteraction by Intranasal Insulin Therapy in 3×Tg Mice. Front Cell Neurosci. 2019 May 3;13:188. doi: 10.3389/fncel.2019.00188. PMID: 31130848; PMCID: PMC6509878.
10) Hallschmid M, Higgs S, Thienel M, Ott V, Lehnert H. Postprandial administration of intranasal insulin intensifies satiety and reduces intake of palatable snacks in women. Diabetes (2012) 61:782–9. 10.2337/db11-1390.
Общим недостатком этих статей является то, что в них изучаются изолированные эффекты интраназально вводимого инсулина на пищевое поведение, отдельные метаболические и гормональные показатели при сахарном диабете 2 типа, в том числе с ожирением, но отсутствует системность в оценке его влияния на паттерн взаимосвязанных и взаимозависимых метаболических и гормональных показателей, что необходимо для оценки комплексного воздействия интраназально вводимого инсулина на метаболический, гормональный и эндокринный статус пациентов с сахарным диабетом 2 типа (в условиях клиники) и лабораторных животных с экспериментальными моделями сахарного диабета 2 типа.
Известна статья, посвященная воздействию однократного интраназального введения инсулина на метаболические показатели и когнитивные функции у здоровых мужчин (Ritze Y, Kern W, Ebner EM, Jahn S, Benedict C, Hallschmid M. Metabolic and Cognitive Outcomes of Subchronic Once-Daily Intranasal Insulin Administration in Healthy Men. Front Endocrinol (Lausanne). 2018 Nov 13;9:663. doi: 10.3389/fendo.2018.00663. PMID: 30524368; PMCID: PMC6262365).
Недостатком этой статьи является то, что в ней не рассматривается влияние интраназально вводимого инсулина на метаболические и гормональные показатели при метаболических расстройствах, в том числе при сахарном диабете 2 типа, а анализируется воздействие препарата только на здоровых мужчин. Кроме того, исследуется только однократное введение интраназального инсулина, а не его курсовое применение.
Известны экспериментальные статьи авторов данного патента о влиянии длительной обработки интраназально вводимым инсулином крыс с моделями сахарного диабета 2 типа на некоторые показатели метаболического и гормонального статуса и на экспрессию гипоталамических генов, как потенциальных мишеней инсулина мозга.
1) Сухов И.Б., Деркач К.В., Чистякова О.В., Бондарева В.М., Шпаков А.О. Функциональное состояние гипоталамических сигнальных систем у крыс с сахарным диабетом 2-го типа, леченных интраназальным инсулином // Журн. эволюц. биохимии и физиологии. 2016. T. 52. № 3. С. 184–194. PMID: 30695498.
2) Деркач К.В., Бахтюков А.А., Басова Н.Е., Бондарева В.М., Шпаков А.О. Интраназально вводимый инсулин, но не С-пептид проинсулина, нормализует гормональные показатели и экспрессию гипоталамических генов у самцов крыс с диабетом 2 типа и ожирением // Интегративная физиология. 2022. Т. 2. № 4. С. 399–411. https://www.doi.org/10.33910/2687-1270-2021-2-4-399-411.
Недостатком этих статей является использование одной, сравнительно низкой дозы интраназально вводимого инсулина (0.5 МЕ/крысу/сутки), а также отсутствие набора данных, способных в полной мере характеризовать функциональное состояние эндокринной системы (тиреоидной и гонадной осей), а также адипокиновый и инкретиновый статус у животных с сахарным диабетом 2 типа, леченых интраназально вводимым инсулином.
Имеются статьи авторов данного патента по влиянию обработки интраназально вводимым инсулином совместно с С-пептидом проинсулина, ганглиозидами или метформином на метаболические и гормональные показатели у крыс с сахарным диабетом 2 типа.
1) Деркач К.В., Бондарева В.М., Шпаков А.О. Совместное интраназальное введение инсулина и С-пептида проинсулина крысам с сахарным диабетом 1-го и 2-го типов восстанавливает у них метаболические показатели // Успехи геронтологии. 2017. Т. 30. № 6. C. 851–858. PMID: 29608829.
2) Деркач К.В., Бондарева В.М., Басова Н.Е., Кузнецова Л.А., Шпаков А.О. Совместное применение метформина и интраназального инсулина нормализует чувствительность к глюкозе и гормональный статус у крыс с диабетом 2 типа // Интегративная физиология. 2021. Т. 2. № 4. С. 399–411. doi: 10.33910/2687-1270-2021-2-4-399-411.
3) Захарова И.О., Баюнова Л.В., Деркач К.В., Илясов И.О., Шпаков А.О., Аврова Н.Ф. Влияние интраназально вводимых инсулина и ганглиозидов на метаболические показатели и активность инсулиновой системы в печени крыс с сахарным диабетом 2-го типа // Журн. эволюц. биохимии и физиологии. 2022. Т. 58. № 2. C. 141–154. https://doi.org/10.31857/S0044452922020085.
4) Захарова И.О., Баюнова Л.В., Деркач К.В., Илясов И.О., Морина И.Ю., Шпаков А.О., Аврова Н.Ф. Влияние интраназально вводимых инсулина и ганглиозидов на гипоталамический сигналинг и экспрессию генов глюконеогенеза в печени крыс с сахарным диабетом 2-го типа // Журн. эволюц. биохимии и физиологии. 2022. Т. 58. № 6. C. 520–539. https://doi.org/10.31857/S0044452922060122.
Недостатком этих статей является применение в них комплексной терапии, включающей использование интраназально вводимого инсулина совместно с другими фармакологическими препаратами или субстанциями (С-пептидом проинсулина, ганглиозидами, метформином). Кроме того, в этих статьях применялась одна, сравнительно низкая доза интраназально вводимого инсулина (0.5 МЕ/крысу/сутки), а также не оценивались адипокиновый и инкретиновый статус, а также не оценивались (за исключением статьи № 2) метаболические и гормональные показатели, позволяющие оценить функциональное состояние эндокринной системы и энергетического обмена.
Имеются статьи авторов патента, в которых изучено влияние обработки крыс с сахарным диабетом 2 типа и ожирением с помощью интраназально вводимого инсулина на аденилатциклазную сигнальную систему и NO-синтазную систему в тканях-мишенях.
1) Shpakov A.O., Chistyakova O.V., Derkach K.V., Moiseyuk I.V., Bondareva V.M. Intranasal insulin affects adenylyl cyclase system in rat tissues in neonatal diabetes. Cent. Eur. J. Biol. 2012;7:33–47. doi: 10.2478/s11535-011-0089-6.
2) Шпаков А.О., Деркач К.В., Чистякова О.В., Мойсеюк И.В., Сухов И.Б., Бондарева В.М. Влияние интраназального инсулина и серотонина на функциональную активность аденилатциклазной системы в миокарде, яичниках и матке крыс с пролонгированной неонатальной моделью сахарного диабета // Журн. эволюц. биохимии и физиологии. 2013. T. 49. № 2. С.118–127.
3) Шпаков А.О., Мойсеюк И.В., Чистякова О.В., Деркач К.В., Сухов И.Б., Бондарева В.М. Лечение интраназальным инсулином и серотонином восстанавливает чувствительность аденилатциклазы к гормонам в мозге крыс с длительным неонатальным диабетом // Бюллетень ФЦСКЭ им. В.А. Алмазова. 2013. № 1. С. 21–27.
4) Кузнецова Л.А., Плеснева С.А., Шарова Т.С., Перцева М.Н., Шпаков А.О. Ослабление ингибирующего влияния гормонов на аденилатциклазную систему в миокарде и мозге крыс с ожирением и сахарным диабетом 2-го типа и действие на него интраназального инсулина // Журн. эволюц. биохимии и физиологии. 2014. T. 50. № 5. С. 349–357. PMID: 25786317.
5) Кузнецова Л.А., Деркач К.В., Шарова Т.С., Бондарева В.М., Шпаков А.О. Активность NO-синтаз в мозге, миокарде и скелетных мышцах крыс с ожирением и влияние на нее длительного лечения интраназальным инсулином // Трансляционная медицина. 2015. № 1(30). С. 39–45.
6) Кузнецова Л.А., Шарова Т.С., Перцева М.Н., Шпаков А.О. Бета-адренергическая регуляция аденилатциклазной системы в миокарде и мозге крыс с ожирением и сахарным диабетом 2-го типа и влияние на нее длительной обработки с помощью интраназально вводимого инсулина // Журн. эволюц. биохимии и физиологии. 2015. T. 51. № 3. С. 170–180. PMID: 26281219.
7) Деркач К.В., Игнатьева П.А., Шпаков А.О. Гормональная регуляция аденилатциклазы в миокарде самцов крыс с метаболическим синдромом и влияние на нее лечения метформином и интраназально вводимым инсулином // Трансляционная медицина. 2016. Т. 3. № 1 (37). С. 72–80.
Недостатком этих статей является ограничение исследования оценкой влияния интраназально вводимого инсулина на молекулярные блоки гормональных систем (аденилатциклазной, NO-синтазной) в тканях крыс с сахарным диабетом 2 типа и ожирением без исследования гормональных показателей эндокринной системы, адипокинового и инкретинового статуса, детального исследования глюкозного гомеостаза и инсулиновой чувствительности.
В статье авторов патента (Деркач К.В., Бахтюков А.А., Басова Н.Е., Бондарева В.М., Шпаков А.О. Интраназально вводимый инсулин, но не С-пептид проинсулина, нормализует гормональные показатели и экспрессию гипоталамических генов у самцов крыс с диабетом 2 типа и ожирением // Интегративная физиология. 2022. Т. 2. № 4. С. 399–411. https://www.doi.org/10.33910/2687-1270-2021-2-4-399-411) изучено влияние 9-дневного лечения крыс с диета-индуцированным сахарным диабетом 2 типа с ожирением и гиперинсулинемией с помощью интраназально вводимого инсулина (0.5 МЕ/крысу/сутки) и его комбинации с С-пептидом проинсулина (36 мкг/крысу/сутки) на метаболические показатели, базовые и стимулированные глюкозой концентрации инсулина, адипокинов, глюкагоноподобного пептида-1, грелина, на гормональный статус тиреоидной и гонадной систем, на уровни инсулина и лептина в гипоталамусе и экспрессию гипоталамических генов, кодирующих рецепторы и пищевые факторы. Монотерапия интраназально вводимым инсулином нормализовала сниженный при диабете уровень инсулина в гипоталамусе, улучшала глюкозный гомеостаз, тиреоидный статус, ответы инсулина, лептина и инкретинов на глюкозу, восстанавливала экспрессию гипоталамических генов проопиомеланокортина и M4-меланокортинового рецептора, опосредующих снижение аппетита, и снижала экспрессию гена орексигенного нейропептида Y. Совместное применение интраназально вводимого инсулина и С-пептида не усиливало эффекты инсулина при использованной модели сахарного диабета 2 типа. Указанная статья взята за прототип для технического решения 2.
Недостатком данной статьи является то, что при лечении использовалась только одна, достаточно низкая, доза интраназально вводимого инсулина (0.5 МЕ/крысу/сутки), а также только одна, достаточно короткая, продолжительность лечения (9 дней), что не характерно для использования интраназально вводимого инсулина в условиях клиники. К тому же использовалась модель индукции сахарного диабета 2 типа, продолжительность которой составила три месяца, что недостаточно для развития тяжелых метаболических и гормональных нарушений, характерных для тяжелых форм сахарного диабета 2 типа у человека. Лечение экспериментальных животных проводили инсулином быка, в то время как в условиях клиники применяют инсулин человека или свиньи, включая рекомбинантные формы инсулина, причем известно, что метаболические эффекты, вызываемые инсулинами различных млекопитающих, могут существенно различаться и у человека, и у экспериментальных животных.
Задача заявляемого технического решения состоит в разработке способа восстановления 9 (девяти) метаболических и 15 (пятнадцати) гормональных показателей, нарушенных при сахарном диабете 2 типа, с помощью курсового лечения интраназально вводимым инсулином.
Раскрытие сущности технического решения
1) Способ коррекции комплекса метаболических и гормональных показателей при сахарном диабете 2 типа с помощью курсового применения интраназально вводимого инсулина в течение 6 недель, включающий в себя восстановление 9 (девяти) метаболических показателей, в том числе в сравнении с нелеченым сахарным диабетом 2 типа снижение массы жировой ткани не менее чем на 10%, снижение уровней глюкозы в крови, как базового, так и повышенного через 120 мин после глюкозной нагрузки не менее чем на 20%, снижение содержания гликированного гемоглобина не менее чем на 15%, снижение значения AUC0-120 для глюкозной кривой, характеризующего толерантность к глюкозе, не менее чем на 30%, снижение уровней общего холестерина и триглицеридов в крови не менее чем на 10%, повышение холестерина липопротеидов высокой плотности не менее чем на 15%, снижение индекса атерогенности не менее чем на 35%, а также восстановление 15 (пятнадцати) гормональных показателей, в том числе в сравнении и с нелеченым сахарным диабетом 2 типа снижение базовых концентраций инсулина и лептина в крови не менее чем на 20% и 15%, соответственно, снижение стимулированной глюкозой концентрации инсулина и лептина в крови не менее чем на 30% и 20%, соответственно, снижение индекса инсулиновой резистентности не менее чем на 40%, повышение стимулированной глюкозой концентрации глюкагоноподобного пептида-1 не менее чем на 35%, снижение соотношений концентраций лептин/адипонектин и лептин/грелин в крови не менее чем на 15% и 35%, соответственно, повышение концентраций свободного тироксина, свободного и общего трийодтиронина и общего тестостерона в крови не менее чем на 20%, 25%, 10% и 15%, соответственно, повышение соотношений концентраций общий трийодтиронин/тиреотропный гормон, тестостерон/лютеинизирующий гормон и тестостерон/эстрадиол в крови на 25%, 10% и 35%, соответственно, при использовании интраназально вводимого инсулина в диапазоне доз от 3.0 до 15.0 МЕ/кг/сутки.
2) Способ по п. 1 отличающийся тем, что интраназально вводимый инсулин может быть введен в виде спрея, ингаляций или капель.
Краткий перечень чертежей
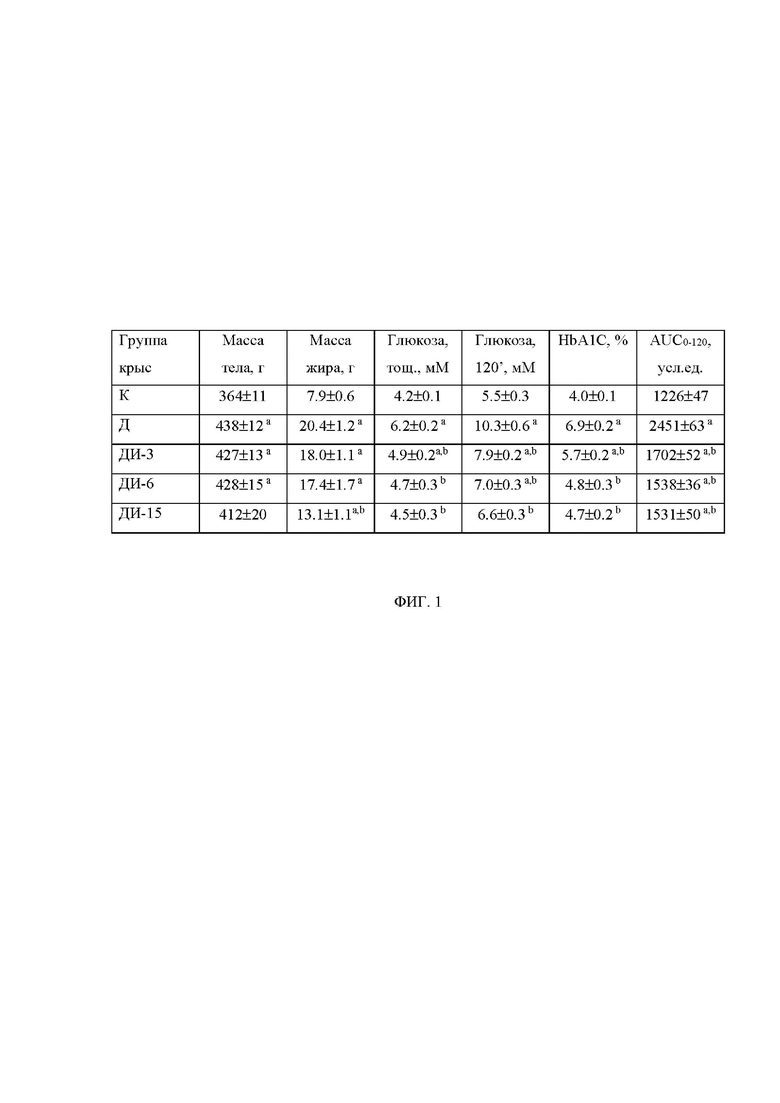
Фиг. 1. Влияние шестинедельного лечения крыс с СД2 с помощью ИВИ на массу тела и жировой ткани, на уровни глюкозы (базовый, через 120 мин после глюкозной нагрузки) и содержание гликированного гемоглобина (HbA1C) в крови и на значение AUC0-120 для кривых «концентрация глюкозы (мМ) – время (мин)» в интраперитонеальном глюкозотолерантном тесте (ИГТТ).
К – контроль, Д – СД2 без лечения; ДИ-3, ДИ-6, ДИ-15 – СД2 с лечением ИВИ в дозах 3.0, 6.0 и 15.0 МЕ/кг/сутки, соответственно. a - различия между группой К и диабетическими группами статистически значимы при p<0.05; b - различия между группой Д и диабетическими группами с лечением ИВИ статистически значимы при p<0.05. Значения AUC0-120 – интегрированная площадь под кривой «концентрация глюкозы (мМ) – время (мин)» в ИГТТ, включающая временной промежуток 120 мин от момента в/б инъекции глюкозы (2 г/кг) с пятью измерениями уровня глюкозы в крови (до и через 15, 30, 60 и 120 мин после глюкозной нагрузки).
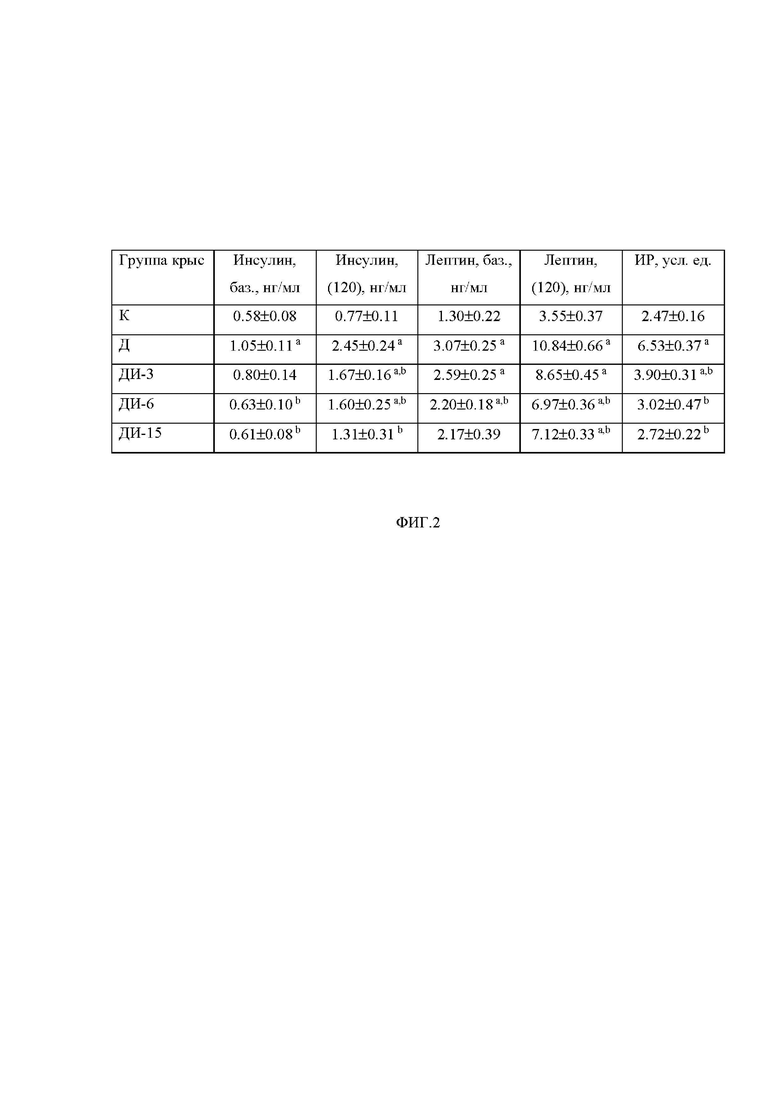
Фиг. 2. Влияние шестинедельного лечения крыс с СД2 с помощью ИВИ на базовые и стимулированные глюкозой в ИГТТ (через 120 мин после глюкозной нагрузки) концентрации инсулина и лептина в крови и на рассчитанный индекс инсулиновой резистентности (ИР).
К – контроль, Д – СД2 без лечения; ДИ-3, ДИ-6, ДИ-15 – СД2 с лечением ИВИ в дозах 3.0, 6.0 и 15.0 МЕ/кг/сутки, соответственно. a - различия между группой К и диабетическими группами статистически значимы при p<0.05; b - различия между группой Д и диабетическими группами с лечением ИВИ статистически значимы при p<0.05. Уровни лептина и инсулина оценивали до глюкозной нагрузки (базовый, натощак) и через 120 мин после нее. Индекс ИР рассчитывали, как произведение базовых (натощак) концентраций глюкозы и инсулина в крови, выражая в усл. ед.
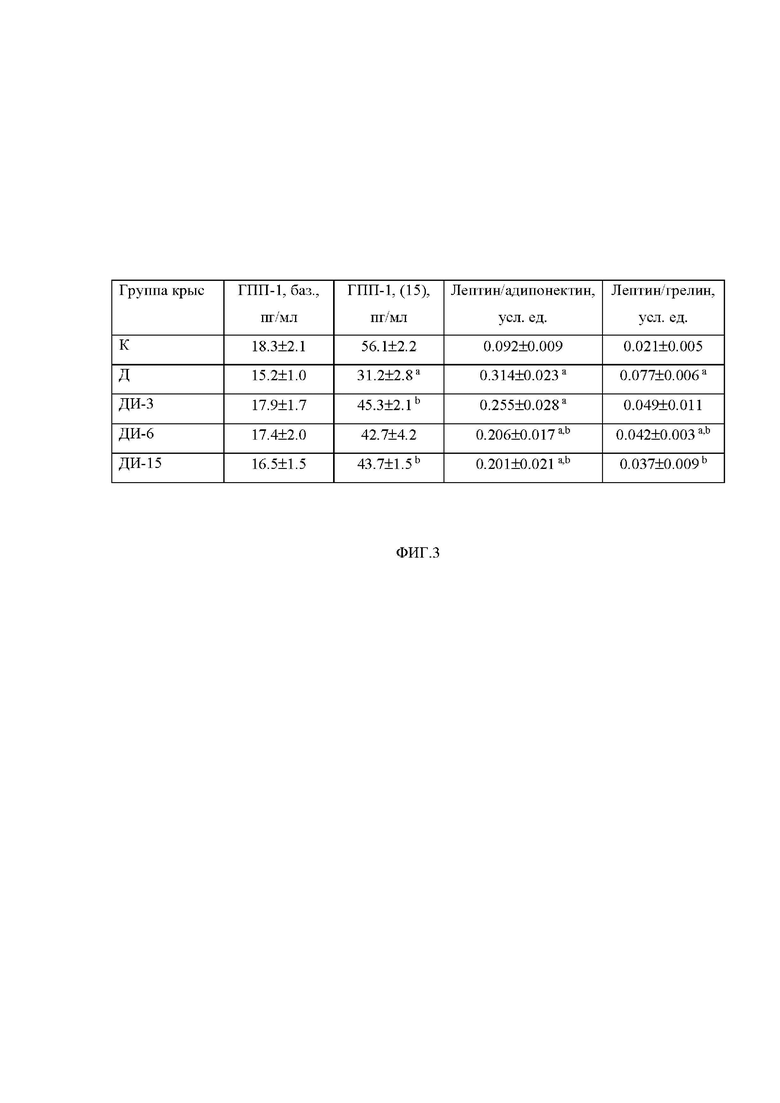
Фиг. 3. Влияние шестинедельного лечения крыс с СД2 с помощью ИВИ на базовые и стимулированные глюкозой в ИГТТ (через 15 мин после глюкозной нагрузки) концентрации глюкагоноподобного пептида-1 (ГПП-1) в крови, а также на соотношение базовых концентраций лептин/адипонектин и лептин/грелин в крови.
К – контроль, Д – СД2 без лечения; ДИ-3, ДИ-6, ДИ-15 – СД2 с лечением ИВИ в дозах 3.0, 6.0 и 15.0 МЕ/кг/сутки, соответственно. a - различия между группой К и диабетическими группами статистически значимы при p<0.05; b - различия между группой Д и диабетическими группами с лечением ИВИ статистически значимы при p<0.05. Уровни ГПП-1 оценивали до глюкозной нагрузки (базовый, натощак) и через 15 мин после глюкозной нагрузки. Для расчетов соотношений Лептин/адипонектин и Лептин/грелин брали базовые концентрации лептина, адипонектина и грелина в нг/мл.
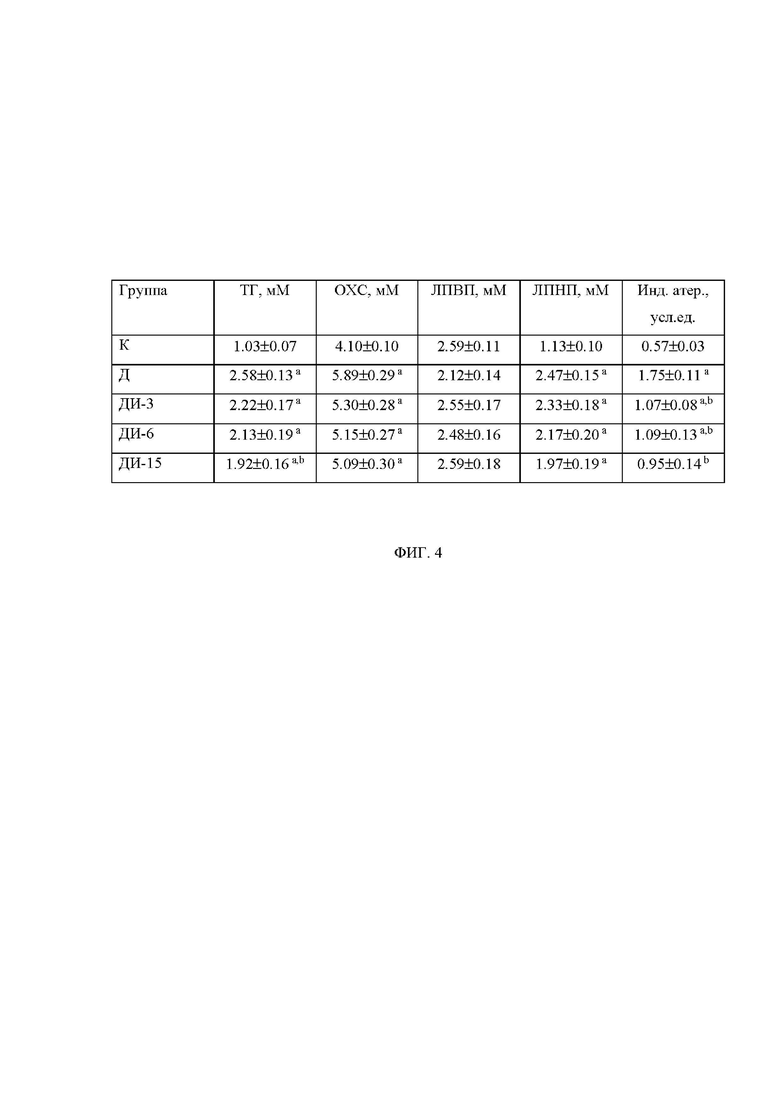
Фиг. 4. Влияние шестинедельного лечения крыс с СД2 с помощью ИВИ на показатели липидного обмена и индекс атерогенности.
К – контроль, Д – СД2 без лечения; ДИ-3, ДИ-6, ДИ-15 – СД2 с лечением ИВИ в дозах 3.0, 6.0 и 15.0 МЕ/кг/сутки, соответственно. a - различия между группой К и диабетическими группами статистически значимы при p<0.05; b - различия между группой Д и диабетическими группами с лечением ИВИ статистически значимы при p<0.05. ТГ – общие триглицериды, ОХС, ЛПВП, ЛПНП – общий холестерин, холестерин-липопротеиды высокой плотности и холестерин-липопротеиды низкой плотности, соответственно. Инд. атер. – индекс атерогенности, рассчитываемый как соотношение (ОХС-ЛПВП)/ЛПВП, в усл. ед.
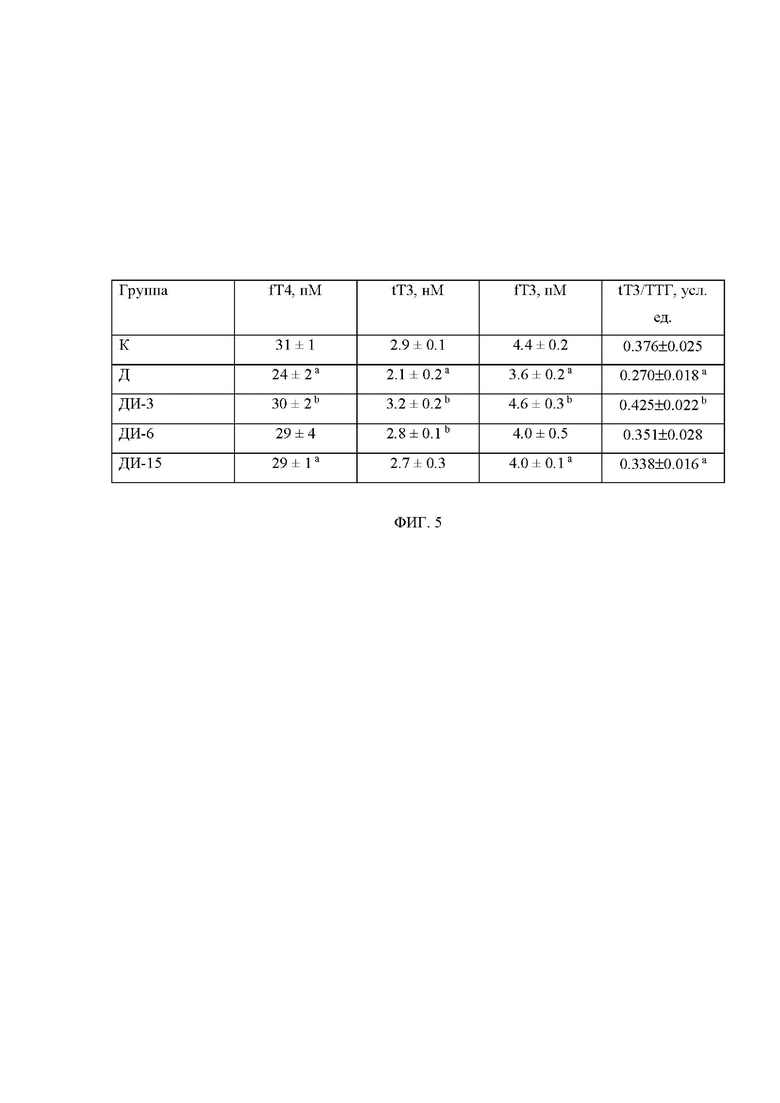
Фиг. 5. Влияние шестинедельного лечения крыс с СД2 с помощью ИВИ на гормональные показатели щитовидной железы и соотношение концентраций в крови общего трийодтиронина и тиреотропного гормона (tT3/ТТГ).
fT4 – свободный тироксин, fT3 – свободный трийодтиронин, tT4 – общий трийодтиронин. К – контроль, Д – СД2 без лечения; ДИ-3, ДИ-6, ДИ-15 – СД2 с лечением ИВИ в дозах 3.0, 6.0 и 15.0 МЕ/кг/сутки, соответственно. a - различия между группой К и диабетическими группами статистически значимы при p<0.05; b - различия между группой Д и диабетическими группами с лечением ИВИ статистически значимы при p<0.05. Для расчета соотношения tT3/ТТГ использовали концентрацию tT3 в нМ и концентрацию ТТГ в мкЕД/л.
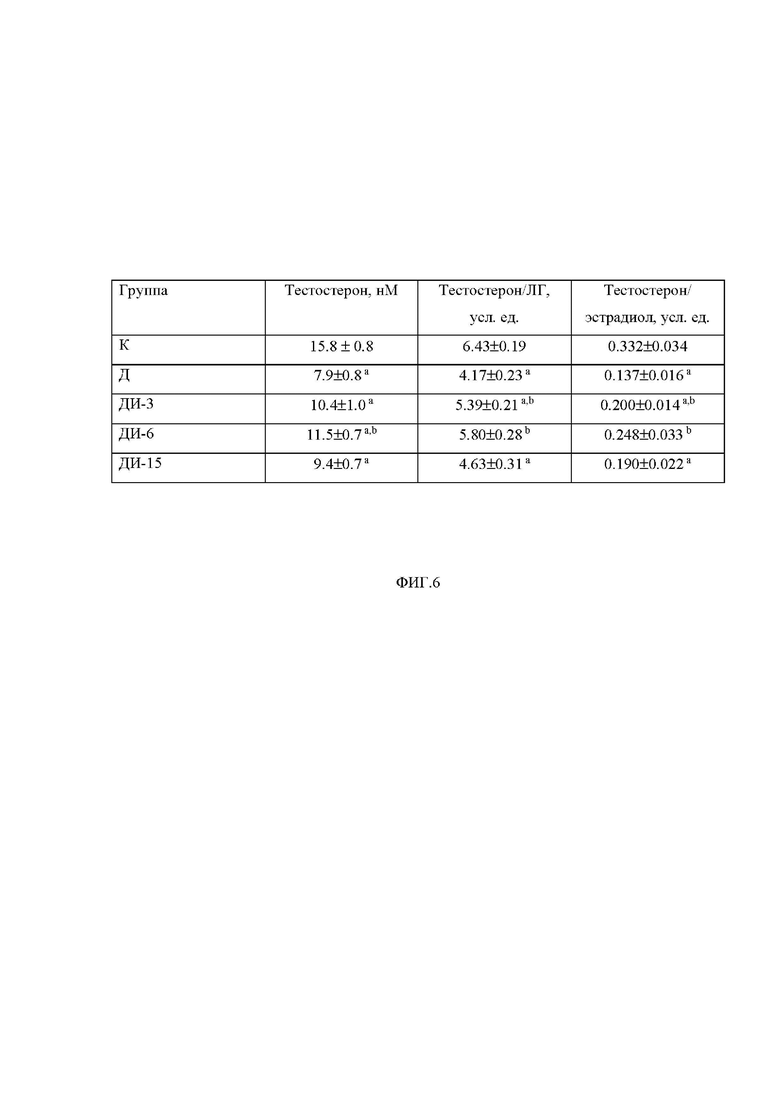
Фиг. 6. Влияние шестинедельного лечения крыс с СД2 с помощью ИВИ на гормональные показатели гонадной оси, такие как концентрация общего тестостерона в крови и соотношение концентрации тестостерона с таковыми лютеинизирующего гормона (ЛГ) и эстрадиола
К – контроль, Д – СД2 без лечения; ДИ-3, ДИ-6, ДИ-15 – СД2 с лечением ИВИ в дозах 3.0, 6.0 и 15.0 МЕ/кг/сутки, соответственно. a - различия между группой К и диабетическими группами статистически значимы при p<0.05; b - различия между группой Д и диабетическими группами с лечением ИВИ статистически значимы при p<0.05. При расчете соотношений Тестостерон/ЛГ и Тестостерон/эстрадиол концентрация тестостерона была выражена в нМ, концентрация ЛГ – в нг/мл, концентрация эстрадиола – в пМ.
Осуществление технического решения
В техническом решении под используемыми терминами понимаются следующие понятия:
Адипонектин – полипептидный гормон (адипокин), синтезируемый белой жировой тканью, регулирует энергетический гомеостаз, оказывает противовоспалительный и антиатерогенный эффекты, снижается при ожирении и отрицательно коррелирует с индексом инсулиновой резистентности.
Гипергликемия – повышение уровня глюкозы в сыворотке крови по сравнению с нормой (для человека и крысы – 3.3–5.5 мМ), является основной характеристикой сахарного диабета.
Гиперинсулинемия – повышение уровня инсулина в крови по сравнению с нормальным уровнем гормона, избыточный уровень инсулина в крови по сравнению с уровнем глюкозы, гиперинсулинемия тесно связана с инсулиновой резистентностью и непереносимостью глюкозы, является одним из характерных признаков сахарного диабета 2 типа и метаболического синдрома.
Гиперлептинемия – повышение уровня лептина в крови по сравнению с нормальным уровнем этого адипокина, тесно связана с лептиновой резистентностью, является одним из характерных признаков сахарного диабета 2 типа и метаболического синдрома с ожирением.
Глюкагоноподобный пептид-1 (ГПП-1) – полипептидный гормон из семейства инкретинов, вырабатываемый в кишечнике в ответ на прием пищи, контролирует секрецию инсулина панкреатическими бета-клетками.
Гипоталамо-гипофизарно-гонадная ось (ГГГ ось) – эндокринный комплекс, включающий в себя гипоталамус, гипофиз и семенники (у мужчин) и яичники (у женщин), регулирует репродуктивную и иммунную системы, контролирует развитие организма и размножение, в качестве эффекторного гормона включает тестостерон (у мужчин) и эстрогены (у женщин).
Гипоталамо-гипофизарно-тиреоидная ось (ГГТ ось) – эндокринный комплекс, включающий в себя гипоталамус, гипофиз и щитовидную железу, регулирует метаболизм и ответ на стрессовые воздействия, в качестве эффекторного гормона включает трийодтиронин, который образуется из тироксина.
Глюкоза натощак и постпрандиальная – уровни глюкозы в крови после ограничения приема пищи (натощак) и после приема пищи (обычно через 2 ч, постпрандиальная).
Грелин – полипептидный гормон (инкретин), синтезируемый в желудочно-кишечном тракте, являющийся регулятором метаболических и эндокринных процессов, контролирует аппетит, концентрация которого повышена при голодании и быстро снижается при потреблении пищи.
Дислипидемия (гиперлипидемия) – аномально повышенный уровень липидов или липопротеинов низкой плотности в крови.
Инсулин – полипептидный гормон, секретируемый бета-клетками поджелудочной железы, основное его действие – регуляция углеводного обмена, в том числе путем повышения утилизации глюкозы клетками, применяется для лечения пациентов с сахарным диабетом 1 типа (с абсолютной инсулиновой недостаточностью) и с сахарным диабетом 2 типа (с относительной инсулиновой недостаточностью и(или) инсулиновой резистентностью).
Инсулиновая резистентность (ИР) – снижение чувствительности к инсулину, являющееся характерным признаком сахарного диабета 2 типа и метаболического синдрома, оценивается с помощью индекса ИР – произведение концентраций инсулина и глюкозы в крови с соответствующим пересчетным коэффициентом.
Интраназально вводимый инсулин (ИВИ) (intranasally administered insulin) – инсулин, доставляемый в организм с помощью интраназального способа введения путем закапывания в нос, ингаляций или спрея, принятые синонимы – интраназальный инсулин (intranasall insulin), назальный инсулин (nasal insulin).
Интраперитонеальный глюкозотолерантный тест (ИГТТ) – лабораторный тест для диагностики нарушения толерантности к глюкозе (предиабет, метаболический синдром) и сахарного диабета 2 типа, включает нагрузку глюкозой (внутрибрюшинное введение раствора глюкозы) с последующим мониторингом уровня глюкозы (обычно в течение 120 мин).
Лептин – полипептидный гормон, вырабатываемый белой жировой тканью, регулирующий пищевое поведение и энергетический обмен, концентрация которого снижена при голодании и быстро повышается при приеме пищи.
Липидный обмен – процесс деградации липидов в клетке, включающий расщепление и накопление жиров для получения энергии, а также синтез структурных и функциональных липидов для построения мембранных структур клетки, нарушается при диабете и метаболическом синдроме.
Нарушенная толерантность к глюкозе – состояние, характеризующееся нормальным уровнем глюкозы натощак, ее отсутствием в моче, но повышенным уровнем глюкозы при глюкозной нагрузке или потреблении высокоуглеводной пищи (оценивается в глюкозотолерантном тесте).
Нейродегенеративные заболевания – группа медленно прогрессирующих наследственных или приобретенных заболеваний нервной системы, общим признаком которых является процесс нейродегенерации (гибель нервных клеток), что ведет к неврологическим симптомам, включая когнитивный дефицит и нарушение движения и ориентации в пространстве, одними из наиболее распространенных нейродегенеративных заболеваний являются болезнь Альцгеймера и болезнь Паркинсона, часто развиваются у пациентов с сахарным диабетом 2 типа (в форме диабетической энцефалопатии) и метаболическим синдромом.
Сахарный диабет (СД) – эндокринное заболевание, для которого характерны нарушения обмена веществ и обусловленное этим повышение содержания уровня глюкозы в крови, развивается в результате нарушений выработки инсулина бета-клетками поджелудочной железы, нарушением функционирования инсулиновой системы в тканях-мишенях или обоими этими факторами совместно.
Сахарный диабет 2 типа (СД2) (инсулинрезистентный или инсулиннезависимый диабет) – хроническое эндокринное заболевание, при котором организм не может эффективно использовать инсулин, вырабатываемый в достаточных количествах бета-клетками поджелудочной железы, основным симптомом СД2 является гипергликемия, часто ассоциирован с ожирением, дислипидемией и артериальной гипертензией.
Тестостерон – основной мужской половой стероидный гормон (класс – андрогены), синтезируется из холестерина в клетках Лейдига семенников под воздействием лютеинизирующего гормона, вырабатываемого аденогипофизом.
Тиреоидные гормоны – йодированные производные аминокислоты тирозина – тироксин (тетрайодтиронин) и трийодтиронин, обладающие сходными физиологическими свойствами и вырабатываемые тироцитами щитовидной железы из тиреоглобулина под воздействием тиреотропного гормона, вырабатываемого аденогипофизом.
Углеводный обмен – комплекс метаболических процессов, включающий расщепление в пищеварительном тракте поступающих с пищей, поли- и дисахаридов до моносахаридов, дальнейшее всасывание моносахаридов в кровь, синтез и распад гликогена в тканях, гликолиз (распад глюкозы), осуществляемый через образование глюкозо-6-фосфата, фруктозо-1,6-дифосфата и пирувата как в отсутствие, так и в присутствии кислорода, анаэробный путь прямого окисления глюкозы (пентозофосфатный путь), взаимопревращение гексоз, образование углеводов из соединений, не являющихся углеводами (глюконеогенез).
Центральная нервная система (ЦНС) – основная часть нервной системы у человека и позвоночных животных, состоящая из нейронов, их отростков и вспомогательной глии, основной функцией которой является реализация простых и сложных рефлексов, когнитивная деятельность, регуляция взаимосвязи и взаимодействий организма, как единого целого, с внешней средой.
AUC0-120 – интегрированная площадь под кривой «концентрация глюкозы (мМ) – время (мин)», является интегративным показателем изменений уровня глюкозы в течение 120 мин в тесте с глюкозной нагрузкой, представляется в условных единицах.
Известно при сахарном диабете 2 типа (СД2), наряду с комплексом метаболических и гормональных нарушений, характеризующих этиологию и патогенез этого заболевания, нарушается функционирование инсулиновой сигнальной системы мозга. Это приводит к ряду значимых негативных последствий, которые вносят значительный вклад в патогенез СД2 и его осложнений, а также утяжеляют течение этого заболевания и ухудшают его прогноз. Среди таких последствий – нарушение нейромедиаторной и гормональной сигнализации в различных отделах мозга, что влечет нарушение центральной регуляции энергетического обмена и функционирования эндокринной, сердечно-сосудистой, пищеварительной и выделительной систем, нарушение регуляции инсулином мозга инсулиновой чувствительности и глюкозного гомеостаза на периферии, что усугубляет характерные для СД2 инсулиновую резистентность (ИР) и гипергликемию, основные патогенетические факторы при СД2, а также приводит к развитию нейродегенеративных заболеваний, включая болезнь Альцгеймера, как результат ослабления нейропротекторного и нейротрофического действия инсулина на нейроны и глиальные клетки головного мозга. Причинами ослабления инсулиновой системы мозга являются нарушение транспорта инсулина из периферического кровотока вследствие ИР клеток, осуществляющих транспорт гормона через гематоэнцефалический барьер, усиление деградации инсулина в мозге вследствие повышения активности инсулиндеградирующего фермента и других протеолитических систем, ослабление инсулинового сигналинга в нейронах. Снижение инсулинового сигналинга обусловлено повышением активности тирозиновых фосфатаз, негативных регуляторов инсулиновой сигнальной системы, а также ослаблением активности основных компонентов этой системы – рецепторов инсулина, инсулин-рецепторных субстратов (ИРС), Akt-киназ и ряда других. Факторами, приводящими к этим нарушениям, являются вызываемое повышенными уровнями глюкозы избыточное гликирование функционально важных белков (глюкотоксичность), усиление окислительного стресса, процессов воспаления и неконтролируемой деградации белков в структурах мозга, липотоксичность, эндотелиальные дисфункции в сосудах головного мозга, повышение концентрации факторов, вызывающих гибель нервных клеток и нарушающих экспрессию в клетках мозга важных белков для его жизнедеятельности белков.
Таким образом, одним из перспективных подходов для лечения СД2 является восстановление инсулиновой системы в мозге, для чего могут быть применены различные подходы. Наиболее перспективным из них является применение интраназально вводимого инсулина, который при введении в носовую полость через нервные пути способен непосредственно поступать к структурам мозга, минуя гематоэнцефалический барьер. Преимуществами интраназально вводимого инсулина (ИВИ) является отсутствие рисков развития опасных для жизни гипогликемических эпизодов, поскольку даже в сравнительно высоких дозах ИВИ не снижает уровень инсулина ниже контрольных значений. Наряду с этим, применение ИВИ, в отличие от инъекционных форм гормона (подкожное и внутривенное введение), не усугубляет периферическую ИР, а также не ухудшает транспорт инсулина из кровотока в мозг через гематоэнцефалический барьер.
В настоящее время процедура использования ИВИ достаточно хорошо разработана, включая применение специальных добавок, обеспечивающих повышение всасываемости ИВИ в обонятельной области носовой полости и транспорта гормона по нервным путям к структурам мозга. Разработаны специальные устройства, повышающие эффективность интраназальной доставки инсулина, в том числе таргетность его абсорбции в обонятельной области носовой полости, что позволяет доставить гормон по аксональным путям непосредственно к структурам мозга. Все это, однако, направлено исключительно на улучшение когнитивных функций и предотвращение нейродегенерации при болезни Альцгеймера и при мягком когнитивном дефиците. В настоящее время ИВИ проходит вторую фазу клинических испытаний для лечения болезни Альцгеймера. Имеются отдельные сообщения о возможности его успешного клинического применения для предотвращения когнитивного дефицита при СД2, включая диабетическую энцефалопатию, в то время как данные о положительном влиянии ИВИ на метаболические и гормональные показатели при СД2 ограничены единичными экспериментальными работами, а в условиях клиники такие исследования не проводились. Имеются лишь данные о сахароснижающем эффекте ИВИ, но они ограничиваются пациентами с сахарным диабетом 1 типа (инсулин-дефицитная форма СД), а также здоровыми добровольцами (без признаков диабетической патологии и МС). В то же время гипогликемический эффект ИВИ при СД2 в клинике не изучался, и был очень ограниченно изучен авторами настоящего патента на экспериментальных моделях СД2.
Эффективность фармакологического подхода при СД2 может быть обеспечена комплексным восстановлением метаболических и гормональных показателей, нарушенных при этом заболевании и характеризующих его тяжесть, патогенез и прогноз. Эти показатели включают повышенные в сравнении с контролем уровни тощаковой и постпрандиальной глюкозы и содержание гликированного гемоглобина в крови, повышенные значения AUC0-120 для уровня глюкозы в глюкозотолерантном тесте, изменения липидного обмена, оцениваемые по значениям уровней общих триглицеридов (ТГ), общего холестерина (ОХС), холестерина липопротеидов низкой плотности (ЛПНП) и холестерина липопротеидов высокой плотности (ЛПВП) в крови и рассчитанному на их основе индексу атерогенности, измененные в сравнении с контролем базовые и стимулированные глюкозой концентрации инсулина, лептина и глюкагоноподобного пептида-1 и соотношения концентраций Лептин/грелин и Лептин/адипонектин в крови, повышенный индекс инсулиновой резистентности (ИР), измененные в сравнении с контролем концентрации общего тестостерона, свободного тироксина (fT4), общего (tT3) и свободного (fT3) трийодтиронина и соотношения концентраций Общий трийодтиронин/тиреотропный гормон, Тестостерон/лютеинизирующий гормон и Тестостерон/эстрадиол. Все это в полной мере относится к применению курсового лечения СД2 с помощью ИВИ, который через центральные и периферические механизмы обеспечивает нормализацию перечисленных выше метаболических и гормональных показателей. Это обосновывается результатами, представленными в настоящем патенте.
Для пояснения технического решения используется модель СД2 на половозрелых крысах линии Wistar, индуцированная высокожировой диетой (продолжительность 4 месяцев) и низкой дозой стрептозотоцина (15 мг/кг, внутрибрюшинно). Высокожировая диета при индукции модели СД2 включает потребление животными ежедневно по 5-7 г смеси, обогащенной насыщенными жирами. Стрептозотоцин, растворенный в 0.1 М натрий-цитратном буфере (pH 4.5), вводится однократно, внутрибрюшинно, в дозе 15 мг/кг через 3 месяца после начала потребления крысами высокожировой диеты, после чего диета продолжается еще один месяц.
При изучении влияния ИВИ на метаболические и гормональные показатели у самцов крыс с СД2, индуцированным высокожировой диетой (продолжительность 4 месяца) и низкой дозой стрептозотоцина (приблизительно 15 мг/кг, однократная внутрибрюшинная инъекция), исследовали продолжительность лечения 6 недель при использовании суточных доз ИВИ от 3.0 до 15.0 МЕ/кг. ИВИ вводили в объеме от 20 до 40 мкл (в зависимости от дозы инсулина), вводя препарат поочередно в каждую ноздрю. Использовали инсулин, который применяется в условиях клиники для лечения диабетической патологии при инъекционном способе введения инсулина (подкожно, внутривенно), а также в ходе клинических испытаний (первая и вторая фазы) при оценке эффективности интраназального способа введения инсулина для лечения болезни Альцгеймера.
При использовании ИВИ в течение 6 недель при использовании суточных доз гормона от 3.0 до 15.0 МЕ/кг у диабетических самцов крыс отмечали в различной степени выраженное восстановление ключевых метаболических и гормональных показателей, характеризующих энергетический обмен, гормональный, инкретиновый и адипокиновый статус, гормональные показатели эндокринной системы, которые были нарушены при СД2. Выраженность восстанавливающих эффектов ИВИ определялась дозой гормона.
Лечение ИВИ диабетических крыс в суточных дозах 3.0, 6.0 и 15.0 МЕ/кг в течение 6 недель приводило к значимому по сравнению с необработанными диабетическими крысами снижению следующих показателей, которые были повышены у крыс с СД2 без лечения ИВИ: массы жировой ткани, уровней глюкозы (мМ) и содержания гликированного гемоглобина HbA1C (%) в крови, расчетного показателя AUC0-120 (усл. ед.), представляющего собой интегрированную площадь под кривой «концентрация глюкозы (мМ) – время (мин)» в интраперитонеальном глюкозотолерантном тесте (ИГТТ), базовой и стимулированной глюкозой в ИГТТ (через 120 мин после глюкозной нагрузки) концентрации инсулина в крови (нг/мл) и рассчитанного на ее основе индекса ИР (усл. ед.), базовой и стимулированной глюкозой в ИГТТ (через 120 мин после глюкозной нагрузки) концентрации лептина в крови (нг/мл), соотношений базовых концентраций Лептин/адипонектин и Лептин/грелин в крови (усл. ед.), уровней общих триглицеридов и общего холестерина (мМ), расчетного показателя индекса атерогенности (усл. ед.). В ряде случаев перечисленные выше показатели значимо не отличались от их значений в контрольной группе животных, то есть были неотличимы от таковых у здоровых животных. Восстановление этих показателей до их значений в контроле при лечении крыс с СД2 с помощью ИВИ (суточные дозы от 3.0 до 15.0 МЕ/кг; продолжительность лечения 6 недель), демонстрирует терапевтическую эффективность ИВИ при СД2.
Лечение ИВИ диабетических крыс в указанных дозах приводило к значимому по сравнению с необработанными диабетическими крысами повышению следующих показателей, сниженных у крыс с СД2 без лечения ИВИ: стимулированной глюкозой концентрации глюкагоноподобного пептида-1 (ГПП-1) в крови (через 15 мин после глюкозной нагрузки в ИГТТ), уровня холестерина липопротеидов высокой плотности в крови (мМ), концентраций тиреоидных гормонов – fT4 (пМ), tT3 (нМ) и fT3 (пМ) и концентрации общего тестостерона (нМ) в крови, соотношений концентраций Общий трийодтиронин (tT3)/тиреотропный гормон (ТТГ), Тестостерон/лютеинизирующий гормон (ЛГ) и Тестостерон/эстрадиол, сниженных у диабетических крыс. В ряде случаев перечисленные выше показатели значимо не отличались от их значений в контрольной группе животных, то есть были неотличимы от таковых у здоровых животных. Восстановление этих показателей до их значений в контроле при лечении крыс с СД2 с помощью ИВИ (суточные дозы от 3.0 до 15.0 МЕ/кг; продолжительность лечения 6 недель), демонстрирует терапевтическую эффективность ИВИ при СД2.
Вывод. При лечении крыс с СД2 с помощью ИВИ в суточных дозах от 3.0 до 15.0 МЕ/кг в течение 6 недель, которые продемонстрировали наибольшую эффективность, отмечается частичное или полное восстановление ключевых метаболических и гормональных показателей, а именно массы жировой ткани, уровней глюкозы (мМ) в крови, содержания гликированного гемоглобина HbA1C (%) в крови, расчетного показателя AUC0-120 (усл. ед.), представляющего собой интегрированную площадь под кривой «концентрация глюкозы (мМ) – время (мин)» в ИГТТ, базовой и стимулированной глюкозой в ИГТТ (через 120 мин после глюкозной нагрузки) концентрации инсулина в крови (нг/мл) и рассчитанного на его основе индекса ИР (усл. ед.), базовой и стимулированной глюкозой в ИГТТ (через 120 мин после глюкозной нагрузки) концентрации лептина в крови (нг/мл), стимулированной глюкозой концентрации глюкагоноподобного пептида-1 (ГПП-1) в крови (через 15 мин после глюкозной нагрузки в ИГТТ), соотношений концентраций Лептин/адипонектин и Лептин/грелин в крови (усл. ед.), уровней общих триглицеридов и общего холестерина, холестерина липопротеидов высокой плотности в крови (мМ), расчетного показателя индекса атерогенности (усл. ед.), концентрации глюкагоноподобного пептида-1 (ГПП-1) в крови, стимулированной глюкозой в ИГТТ (через 15 мин после глюкозной нагрузки), концентраций fT4 (пМ), tT3 (нМ), fT3 (пМ) и общего тестостерона (нМ) в крови, соотношений концентраций fT3/ТТГ, Тестостерон/ЛГ и Тестостерон/эстрадиол в крови. Это указывает на эффективность лечения СД2 с помощью ИВИ при указанных выше диапазоне доз и продолжительности лечения.
Реализация технического решения поясняется на примере:
В качестве примера технического решения приводим данные по влиянию ИВИ в трех различных суточных дозах 3.0, 6.0 и 15.0 МЕ/кг при продолжительности лечения 6 недель у крыс с СД2, индуцированным четырехмесячной высокожировой диетой и низкой дозой стрептозотоцина (15 мг/кг, внутрибрюшинно). Для исследования были сформированы 5 групп животных, включая контроль, диабетическую группу (Д), диабетические группы с лечением ИВИ в различных суточных дозах – 3.0 (ДИ-3), 6.0 (ДИ-6) и 15 МЕ/кг (ДИ-15), во всех группах число животных составило 6. За три дня до окончания эксперимента животным делали интраперитонеальный глюкозотолерантный тест (ИГТТ), измеряя у них уровни гормонов (инсулина, лептина, ГПП-1, грелина, адипонектина) до и через определенное время после глюкозной нагрузки, а также оценивали значение AUC0-120, как интегрированную площадь под кривой «концентрация глюкозы (мМ) – время (мин)». В конце эксперимента у животных забирали кровь для оценки липидных показателей и концентрации исследуемых гормонов.
Лечение ИВИ в течение 6 недель существенно не влияло на повышенную у диабетических крыс массу тела, но в высокой дозе (15.0 МЕ/кг/сутки) значимо снижало (на 36%) массу жировой ткани по сравнению с группой Д (фиг. 1). При этом во всех дозах ИВИ снижал массу жировой ткани не менее чем на 10%. ИВИ значимо снижал (не менее чем на 20%) как базовый уровень глюкозы, так и повышенный через 120 мин после глюкозной нагрузки в ИГТТ уровень глюкозы, причем в группе ДИ-15 эти значения не отличались от контрольной группы. Отмечали значимое снижение повышенного при СД2 содержания гликированного гемоглобина (HbA1C) в крови (не менее чем на 15%) и рассчитанного по результатам ИГТТ значения AUC0-120 для кривых «концентрация глюкозы (мМ) – время (мин)» (не менее чем на 30%) (фиг. 1). ИВИ также снижал базовые и стимулированные глюкозой концентрации инсулина и лептина в крови (не менее чем на 15-30%), повышенные у необработанных диабетических крыс, и статистически значимо снижал индекс ИР по сравнению с группой Д, причем в группах ДИ-6 и ДИ-15 индекс ИР не отличался от такового в контроле (снижение во всех группах не менее чем на 40%) (фиг. 2). Эти данные указывают на то, что ИВИ нормализует глюкозный гомеостаз у крыс с СД2, причем сахароснижающий эффект ИВИ является дозо-зависимым и в наибольшей степени реализуется в самой высокой из использованных доз ИВИ – 15.0 МЕ/кг/сутки, а также нормализует концентрации инсулина и лептина в крови и повышает чувствительность к инсулину, на что указывает снижение индекса ИР в группах ДИ-6 и ДИ-15 до его значений в контрольной группе (фиг. 1, 2).
Исследование концентрации ГПП-1 в крови и изменения продукции этого инкретина в ответ на глюкозную нагрузку показало, что при СД2 стимулированная глюкозой концентрация ГПП-1 в крови была в значительной степени снижена и обработка ИВИ ее повышала (не менее чем на 35%), причем наименьшая из использованных доз – 3.0 МЕ/кг/сутки, также была эффективной (фиг. 3). ИВИ снижал повышенные при СД2 соотношения концентраций Лептин/адипонектин и Лептин/грелин (не менее чем на 15-35%) причем в дозах 6.0 и 15.0 МЕ/кг/сутки различия с группой Д были значимыми (фиг. 3). Это обусловлено как снижением базовой концентрации лептина в крови, так и повышением базовых концентраций адипонектина и грелина в крови, которые в группе Д были в небольшой степени снижены.
При лечении диабетических крыс с помощью ИВИ частично восстанавливались показатели липидного обмена. Значимые изменения при лечении ИВИ были достигнуты в отношении индекса атерогенности (снижение не менее чем на 35%), который был рассчитан на основе показателей ЛПВП и ЛПНП, причем в основном вследствие повышения ЛПВП (повышение не менее чем на 15%), в то время как повышенные при СД2 уровни общих триглицеридов и общего холестерина менялись в меньшей степени (снижение во всех группах с лечением ИВИ не менее чем на 10%) (фиг. 4). Эти данные свидетельствуют о том, что ИВИ частично нормализует некоторые показатели липидного обмена, повышенные при СД2, такие как индекс атерогенности (при всех изученных дозах ИВИ) и триглицеридов, в наибольшей степени при использовании ИВИ в дозе 15.0 МЕ/кг/сутки (фиг. 4).
ИВИ восстанавливал концентрации tT3 и тестостерона в крови, являющихся основными эффекторными гормонами тиреоидной и гонадной осей, также восстанавливая концентрации fT3 и fT4 в крови (повышение не менее чем на 10-25%). В случае восстановления концентраций тиреоидных гормонов в крови наиболее эффективной была самая низкая из использованных доз ИВИ – 3.0 МЕ/кг/сутки, в случае тестостерона – средняя доза 6.0 МЕ/кг/сутки, в то время как более высокая доза ИВИ 15.0 МЕ/кг/сутки в обоих случаях была менее эффективной (фиг. 5, 6). При использовании ИВИ в дозе 3.0 МЕ/кг/сутки отмечали значимое повышение соотношения концентраций tT3/ТТГ, в дозах 3.0 и 6.0 МЕ/кг/сутки – соотношений концентраций Тестостерон/ЛГ и Тестостерон/эстрадиол, в то время как в группе ДИ-15 эти соотношения слабее отличались от таковых в группе Д (во всех случаях повышение было не менее чем на 10-35%) (фиг. 5, 6). Эти данные свидетельствуют о способности ИВИ нормализовать андрогенный и тиреоидный статус (повышение концентраций общего тестостерона и tT3 в крови) и повышать чувствительность семенников к ЛГ (снижение соотношения Тестостерон/ЛГ) и щитовидной железы к ТТГ (снижение соотношения tT3/ТТГ) у самцов крыс с СД2.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ПРИМЕНЕНИЯ ИНТРАНАЗАЛЬНО ВВОДИМОГО ИНСУЛИНА И ПЕРОРАЛЬНО ВВОДИМОГО МЕТФОРМИНА ДЛЯ ВОССТАНОВЛЕНИЯ МЕТАБОЛИЧЕСКИХ И ГОРМОНАЛЬНЫХ ПОКАЗАТЕЛЕЙ ПРИ САХАРНОМ ДИАБЕТЕ 2 ТИПА И МЕТАБОЛИЧЕСКОМ СИНДРОМЕ | 2023 |
|
RU2824275C1 |
| Фармацевтическая антидиабетическая композиция на основе (+)-цис-3-(1Н-бензимидазол-2-ил)-1,2,2-триметилциклопентанкарбоновой кислоты | 2016 |
|
RU2624872C1 |
| Способ определения и расчета необходимой потребной дозы инсулина при сахарном диабете второго типа и сформировавшейся инсулиновой зависимости | 2018 |
|
RU2684393C1 |
| Твердофазная композиция природных биоактивных ингредиентов для коррекции метаболических нарушений при сахарном диабете второго типа | 2017 |
|
RU2661622C1 |
| Твердофазная композиция для коррекции метаболических нарушений при сахарном диабете второго типа | 2020 |
|
RU2747985C1 |
| Способ диагностики инсулинорезистентности у больных сахарным диабетом 1 типа | 2024 |
|
RU2825046C1 |
| СПОСОБ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА, ВКЛЮЧАЯ СОСТОЯНИЯ, АССОЦИИРОВАННЫЕ С САХАРНЫМ ДИАБЕТОМ, И ОСЛОЖНЕНИЯ САХАРНОГО ДИАБЕТА | 2003 |
|
RU2334518C2 |
| ПРОТИВОСУДОРОЖНЫЕ ПРОИЗВОДНЫЕ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПРОФИЛАКТИКИ РАЗВИТИЯ САХАРНОГО ДИАБЕТА И СИНДРОМА Х | 2001 |
|
RU2268720C2 |
| СРЕДСТВО ДЛЯ КОРРЕКЦИИ ИНСУЛИНОВОЙ РЕЗИСТЕНТНОСТИ | 1999 |
|
RU2158590C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА И ДИАБЕТИЧЕСКОЙ НЕФРОПАТИИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2519744C2 |
Изобретение относится к медицине, а именно к эндокринологии, и может быть использовано для коррекции комплекса метаболических и гормональных показателей при сахарном диабете 2 типа с помощью интраназально вводимого инсулина. Осуществляют курсовое применение интраназально вводимого инсулина в течение 6 недель в диапазоне доз от 3 до 15 МЕ/кг/сут. При этом комплекс метаболических и гормональных показателей включает девять метаболических показателей – масса жировой ткани, базовый уровень глюкозы, уровень глюкозы через 120 минут после глюкозной нагрузки, гликированный гемоглобин, значение AUC0-120 для глюкозной кривой, общий холестерин, триглицериды, липопротеиды высокой плотности, индекс атерогенности, а также пятнадцать гормональных показателей – базовые концентрации инсулина и лептина, стимулированные глюкозой концентрации инсулина и лептина, индекс инсулиновой резистентности, стимулированная глюкозой концентрация глюкагонподобного пептида-1, соотношение концентрации лептин/адипонектин и лептин/грелин, свободный тироксин, свободный и общий трийодтиронин, общий тестостерон, соотношения концентраций трийодтиронин/тиреотропный гормон, тестостерон/лютеинизирующий гормон и тестостерон/эстрадиол. Способ обеспечивает комплексное восстановление метаболических и гормональных показателей, нарушенных при сахарном диабете 2 типа и влияющих на тяжесть, патогенез и прогноз заболевания, при отсутствии рисков развития опасных для жизни гипогликемических эпизодов за счет применения интраназально вводимого инсулина, поступающего непосредственно к структурам мозга, минуя гематоэнцефалический барьер. 6 ил.
Способ коррекции комплекса метаболических и гормональных показателей при сахарном диабете 2 типа, включающий курсовое применения интраназально вводимого инсулина в течение 6 недель в диапазоне доз от 3 до 15 МЕ/кг/сут, при этом комплекс метаболических и гормональных показателей включает:
девять метаболических показателей – масса жировой ткани, базовый уровень глюкозы, уровень глюкозы через 120 минут после глюкозной нагрузки, гликированный гемоглобин, значение AUC0-120 для глюкозной кривой, общий холестерин, триглицериды, липопротеиды высокой плотности, индекс атерогенности;
пятнадцать гормональных показателей – базовые концентрации инсулина и лептина, стимулированные глюкозой концентрации инсулина и лептина, индекс инсулиновой резистентности, стимулированная глюкозой концентрация глюкагонподобного пептида-1, соотношение концентрации лептин/адипонектин и лептин/грелин, свободный тироксин, свободный и общий трийодтиронин, общий тестостерон, соотношения концентраций трийодтиронин/тиреотропный гормон, тестостерон/лютеинизирующий гормон и тестостерон/эстрадиол.
| ДЕРКАЧ К.В | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Успехи геронтологии | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Приспособление для подачи коробок в машинах для наполнения коробок | 1925 |
|
SU851A1 |
| СПОСОБ КОРРЕКЦИИ ПАТОЛОГИЧЕСКОГО АУТОИММУННОГО ПРОЦЕССА ПРИ САХАРНОМ ДИАБЕТЕ | 2002 |
|
RU2228198C1 |
| ЛЕЧЕНИЕ САХАРНОГО ДИАБЕТА С ИСПОЛЬЗОВАНИЕМ ИНЪЕКЦИЙ ИНСУЛИНА С ЧАСТОТОЙ МЕНЕЕ ОДНОГО РАЗА В ДЕНЬ | 2009 |
|
RU2540922C2 |
| XIAO C et al | |||
| Effects of intranasal insulin on endogenous glucose | |||
Авторы
Даты
2024-09-24—Публикация
2023-07-26—Подача