Изобретение относится к области медицины, а именно к офтальмологии и может быть использовано для реабилитации пациентов с синдромом пигментной дисперсии и пигментной глаукомой.
Синдром пигментной дисперсии (СПД) - заболевание молодого возраста, которое развивается в глазу с миопией и приводит к развитию глаукомы до 30% случаев [1], больше распространено среди жителей Европы и протекает в несколько раз агрессивнее, чем у чернокожих или азиатов [2]. Диагноз пигментная глаукома (ПГ) обычно ставится в возрасте от 40-50 лет, чаще у мужчин, лечение заболевания основано на медикаментозной терапии, лазерной иридотомии, селективной лазерной трабекулопластике и фильтрационных процедурах [3].
Известен способ профилактики пигментной глаукомы при синдроме пигментной дисперсии, включающий удаление прозрачного хрусталика методом факоэмульсификации с имплантацией заднекамерной интраокулярной линзы (ИОЛ) (патент RU 2731885 С2 от 09.09.2020). Способ обеспечивает устранение возможности патологического иридозонулярного контакта, что, по мнению авторов, обеспечивает эффективность в предотвращении возможности развития ПГ при СПД при удалении прозрачного хрусталика методом факоэмульсификации и имплантации заднекамерной ИОЛ полностью. Недостатком данного способа является высокая инвазивность метода, необходимость реабилитации пациента после вмешательства, риски интра и послеоперационных осложнений.
Известен способ профилактики развития ПГ при СПД - проведение профилактической лазерной иридэктомии [Okafor K, Vinod K, Gedde SJ. Update on pigment dispersion syndrome and pigmentary glaucoma. CurrOpinOphthalmol. 2017 Mar; 28(2):154-160. doi: 10.1097ЛСи.0000000000000352; Щуко А.Г., Юрьева Т.Н., Мищенко О.П., Ветрова Е.Л., Хантакова О.Ф. Эффективность лазерной иридэктомии как метода профилактики пигментной глаукомы. РМЖ. Клиническая офтальмология. 2007;4:150], который уменьшает пигментацию трабекулы [Zhou R, Tang Q, Pu L, Qing G. Changesoftrabeculairneshworkpigmentationinpatientsw ome: A 15-yearstudy. Medicine (Baltimore). 2021 Aug 6; 100(31): e26567. doi: 10.1097/MD.0000000000026567]. Он осуществляется посредством лазерной иридэктомии при помощи YAG-лазера с длиной волны 1064 нм в зоне от 10 до 2 часов или в проекции 6 часов с нанесением импульсов мощностью до 2.0-6.0 мДж с количеством импульсов 3-10. Недостатком данного способа авторы указывают то, что долгосрочная эффективность этого способа клинически не подтверждена [Michelessi M, Lindsley K. Peripheraliridotomyforpigmentaryglaucoma. CochraneDatabaseSystRev. 2016 Feb 12;2(2): CD005655. doi: 10.1002/14651858] и посредством его можно только получить снижение ВГД без учета достижения давления цели, которое и определяет прогноз заболевания [BuffaultJ, Leray B, Bouillot A, Baudouin C, Labbé A. Intérêtdel’ iridotomiepériphériqueaulaserdansleglaucomepigmentaireetlesyndromededispersio npigmentaire: unerevuedelalittérature [Role of laser peripheral iridotomy in pigmentary glaucoma and pigment dispersionsyndrome: Areviewoftheliterature [Frenchversion]].JFrOphtalmol. 2017 Dec; 40(10):889-897. French. doi: 10.1016/j.jfo.2017.04.006].
Задачей предлагаемого способа является разработка алгоритма реабилитации пациентов с СПД и ПГ включающего анализ совокупности биомеханических параметров глаза, при необходимости проведение периферической иридэктоми и контроль нормализации биомеханических параметров глаза после выполненного вмешательства.
Технология Pentacam (Oculus) и CorVis ST - самая современная методика оценки контроля биомеханических свойств фиброзной оболочки глаза в клинической практике с использованием технологии визуализации роговицы [4], а также контроля ВГД с учетом исследуемых параметров. Результат исследования зависит от возраста, генетических предрасположенностей, уровня ВГД, переднезадней оси глаза и других факторов [5,6].
С целью разработки алгоритма прогнозирования возможности реабилитации пациентов с СПД и ПГ нами были проанализированы данные 60 пациентов (35 глаз с СПД и 26 глаз с ПГ), группу контроля (ГК) составили 30 глаз близоруких пациентов без глаукомы, без ПЭС (таблица 1).
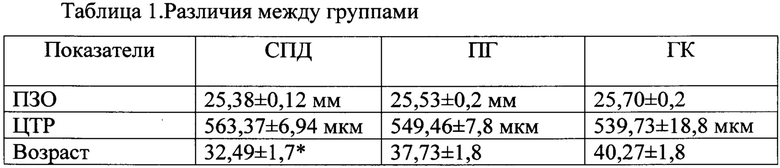
* - показатель достоверности различия между группами.
Группы достоверно различались по возрасту, так средний возраст пациентов в группе СПД был ниже в сравнении с ПГ (р=0,039) и отличался от группы контроля, однако с позиции биомеханики глаза изменения показателей глаза не наступают в данных возрастных группах и имеют значение в возрасте старше 40 лет [7].
В группе ПГ уровень ВГД на момент исследования был медикаментозно компенсирован и составил 20,4±2,6 мм рт.ст. и не различались с СПД, где офтальмотонус был на уровне 19,21±1,2 мм рт.ст.
Техническим результатом предлагаемого способа является разработка алгоритма реабилитации пациентов с СПД и ПГ на основе анализа совокупности биомеханических параметров глаза, позволяющего оценить необходимость проведения периферической иридэктомии и контроля нормализации биомеханических параметров глаза после произведенного вмешательства.
Преимущество нашего способа в сравнении с ближайшим аналогом (RU 2731885 С2 от 09.09.2020) состоит в малой инвазивности методики, отсутствии необходимости реабилитации пациента после проведения ему факоэмульсификации катаракты и в одновременном учете биомеханических характеристик глаза, что позволяет оценить достижения толерантного давления, надежность прогнозирования и точность результата. Ближайший аналог нашему изобретению (RU 2731885 С2 от 09.09.2020) позволяет устранить возможность патологического иридозонулярного контакта, предотвращает возможность развития пигментной глаукомы при синдроме пигментной дисперсии. Однако учитываются лишь анатомические параметры и не учитываются индивидуальные биомеханические особенности глаза, которые являются предикторами и, наравне с не достижением давления цели, факторами риска развития и прогрессирования пигментной глаукомы. В нашем способе после проведения периферической иридэктомии осуществляется одновременный учет биомеханических факторов риска, что повышает надежность прогнозирования и точность результата.
Технический результат достигается за счет количественного определения биомеханических параметров фиброзной оболочки глаза (bIOР, DA Ratio, Integr. Radius (R), SP-A1, BGF) до и после проведения периферической иридэктомии.
Способ осуществляют следующим образом.
У пациента с СПД и ПГ производят измерение роговично-компенсированного ВГД (bIOР), биомеханических параметров фиброзной оболочки глаза таких как DA Ratio, Integr. Radius (R), SP-A1, Stress Strain Index (SSI), BGF на приборе OCULUS CorVis ST. Если bIOР более 18,0 мм рт.ст., Integr. Radius (R) менее 7,7 мм, SP-A1 более 118mmHg/mm и BGF менее 20 проводят периферическую иридэктомию и производят повторное изменение всех параметров. При bIOР менее 16,5 мм рт.ст., Integr. Radius (R) более 8,0 мм, SP-A1 менее 118mmHg/mm и BGF более 20 рассматривают достижение толерантного ВГД, нормализацию биомеханических параметров глаза, что способствует реабилитации пациентов. Пример 1
Пациент С. 30 лет с СПД производили измерение биомеханических параметров фиброзной оболочки глаза таких как bIOР, DA Ratio, Integr. Radius (R), SP-A1, Stress Strain Index (SSI), BGFHanpn6ope OCULUS CorVis ST.
Биомеханические показатели составили: bIOР 18,2 мм рт.ст. для правого глаза, 23,5 мм рт.ст. для левого; Integr. Radius (R) 6,9 мм для правого глаза и 5,9 мм для левого глаза; SP-А1 122,3mmHg/mm для правого глаза, 146,lmmHg/mn для левого глаза; BGF0,05 для правого глаза, 0,01 для левого глаза. Проведено комплексное офтальмологическое обследование пациента.
Объективно:
Правый глаз: Vis OD с корр. (sph -5,5cyl-2.0ax20) 1,0; ПЗО 25,94 мм, ЦТР 568 мкм.
При биомикроскопии в переднем отрезке глаза: передняя камера глубокая, пигментные гранулы на передней поверхности радужной оболочки. При гониоскопии в УПК выраженная экзогенная пигментация, линия Сампаолези.
При офтальмоскопии: ДЗН бледно-розовый, с четкими границами, среднего размера, экскавация центральная, без преобладания вертикального компонента, отношением экскавации к ДЗН 0,6, ход сосудистого пучка центральный, нейроретинальный поясок розовый, сохранен в всех отделах, перипапиллярно с височной стороны атрофия в β-зоне.
Результаты периметрии: ограничение поля зрения сверху до 45 градусов.
Результаты ОКТ-исследования: AverageRNFLThickness 96 μm, AverageC/DRatio 0,59, VerticalC/DRatio 0,56, CupVolume0,189, пограничные знчения нейроретинального пояска в верхнем и нижнем отделе, СНВС (RNFLQuadrants) в верхнем отделе 124 мкм, в нижнем отделе 117 мкм, комплекс ГКС AverageGCL+IPLThickness 81 мкм, MinimumGCL+IPLThickness 82 мкм.
Левый глаз: Vis OD с корр. (sph -4,75cyl-3,0 axl75) 1.0, ПЗО 25,64 мм, ЦТР 558 мкм.
При биомикроскопии: в переднем отрезке глаза: передняя камера глубокая, пигментные гранулы на передней поверхности радужной оболочки, дисперсия пигмента на передней капсуле хрусталика. При гониоскопии в УПК выраженная экзогенная пигментация, линия Сампаолези.
При офтальмоскопии: ДЗН бледно-розовый, с четкими границами, среднего размера, экскавация центральная, без преобладания вертикального компонента, отношением экскавации к ДЗН 0,5, ход сосудистого пучка центральный, нейроретинальный поясок розовый, сохранен в всех отделах, перипапиллярно с височной стороны атрофия в β-зоне.
Результаты периметрии: центральная относительная скотома.
Результаты ОКТ-исследования: AverageRNFLThickness 93 μm, AverageC/DRatio0,54, VerticalC/DRatio0,51, CupVolume0,185,
нейроретинальный поясок не изменен, СНВС (RNFLQuadrants) в верхнем отделе 131 мкм, в нижнем отделе ПО мкм, показатели комплекса ГКС AverageGCL+IPLThickness до 82 мкм, с минимальными значениям -MinimumGCL+IPLThickness81 мкм.
Таким образом, результаты дополнительного обследования подтвердили диагноз СПД, абнормальные показания биомеханики глаза, рекомендовано проведение периферической иридэктомии.
После ее проведения биомеханические показатели составили: bIOP 16,7 мм рт. ст. для правого глаза, 21,1 мм рт.ст. для левого; Integr. Radius (R) 7,5 мм для правого глаза и 6,4 мм для левого глаза; SP-A - 112,8mmHg/mm для правого глаза, 122,8mmHg/mm для левого глаза; BGF- 0,15 для правого глаза, 0,12 для левого глаза.
Пример 2
Пациентка 40 лет с СПД производили измерение биомеханических параметров фиброзной оболочки глаза таких как bIOP, DA Ratio, Integr. Radius (R), SP-A1, Stress Strain Index (SSI), BGFHanpn6ope OCULUS CorVis ST.
Биомеханические показатели составили: bIOP 17.0 мм рт.ст. для правого глаза, 15,5 мм рт. ст. для левого; Integr. Radius (R) 7,2 мм для правого глаза и 7,4 мм для левого глаза; SР-А - 113,6mmHg/mm для правого глаза, 117,7 mmHg/mm для левого глаза; BGF-0,04 для правого глаза, 0,03 для левого глаза; Проведено комплексное офтальмологическое обследование пациента.
Объективно:
Правый глаз: Vis OD с корр. (sph -5,75 cyl -0,5ах25) 1,0; ПЗО 25,45 мм, ЦТР 587 мкм.
При биомикроскопии в переднем отрезке глаза: передняя камера глубокая, пигментные гранулы на передней поверхности радужной оболочки, пролапс радужки в прикорневой зоне, трансиллюминация, иридоденез, на передней капсуле хрусталика россыпь пигмента. При гониоскопии в УПК грубая экзогенная пигментация, линия Сампаолези.
При офтальмоскопии: ДЗН бледно-розовый, с четкими границами, малого размера, умеренно проминирует, экскавация центральная, не глубокая, без преобладания вертикального компонента, отношением экскавации к ДЗН 0,2, ход сосудистого пучка центральный, нейроретинальный поясок розовый, сохранен во всех отделах, перипапиллярно с височной стороны атрофия в β-зоне.
Результаты периметрии: без изменения светочувствительности.
Результаты ОКТ-исследования: AverageRNFLThickness 102 μm, AverageC/DRatio 0,11, VerticalC/DRatio 0,10,CupVolume 0,004, знчения нейроретинального пояска в норме, СНВС (RNFLQuadrants) в верхнем отделе 114 мкм, в нижнем отделе 116 мкм, комплекс ГКС AverageGCL + IPLThickness79 мкм, MinimumGCL + IPLThickness 79 мкм.
Левый глаз: Vis OD с корр (sph -4,00cyl-l,25axl0) 1,0; ПЗО 24,90 мм; ЦТР 593 мкм.
При биомикроскопии в переднем отрезке глаза: на эндотелии роговицы с 6 до 8 часов россыпь пигмента, передняя камера глубокая, пигментные гранулы на передней поверхности радужной оболочки, пролапс радужки в прикорневой зоне, трансиллюминация, иридоденез, на передней капсуле хрусталика россыпь пигмента. При гониоскопии в УПК грубая экзогенная пигментация, линия Сампаолези.
При офтальмоскопии: ДЗН бледно-розовый, с четкими границами, малого размера, экскавация центральная, без преобладания вертикального компонента, более глубокая, чем в правом глазу, отношением экскавации к ДЗН 0,4, ход сосудистого пучка центральный, нейроретинальный поясок розовый, сохранен в всех отделах, симптом "штыка" нижне-темпорально, перипапиллярно с височной стороны атрофия в β-зоне.
Результаты периметрии: без изменения светочувствительности.
Результаты ОКТ-исследования: AverageRNFLThickness 98 μm, AverageC/DRatio 0,34, VerticalC/DRatio 0,35, CupVolume 0,035, нейроретинальный поясок не изменен, СНВС (RNFLQuadrants) в верхнем отделе 127 мкм, в нижнем отделе 116 мкм, показатели комплекса ГКС AverageGCL+IPLThickness до 82 мкм, с минимальными значениям -MinimumGCL+IPLThickness 81 мкм.
Таким образом, результаты дополнительного обследования подтвердили диагноз СПД, абнормальные биомеханические показатели, рекомендовано проведение периферической иридэктомии.
После ее проведения биомеханические показатели составили: bIOP 15,3 мм рт.ст. для правого глаза, 14,4 мм рт.ст. для левого; Integr. Radius (R) 7,3 мм для правого глаза и 7,8 мм для левого глаза, SP-A - 118,0mmHg/mm для правого глаза, 118,2mmHg/mm для левого глаза, BGF- 0,17 для правого глаза, 0,14 для левого глаза.
Сравнительный анализ биомеханически корректированного ВГД до проведения периферической иридэктомии у пациентов с СПД демонстрирует более высокие значения, что явилось показанием к ее проведению и достоверное снижение уровня после (p=0,022). При сравнении биомеханических параметров оказалось, в показателях жесткости роговицы до и после проведения ПИ мы не получили достоверных отличий по параметру DAratio, при этом значения Integr. Radius после проведения лазерного вмешательства носят более высокие значения, что говорит о снижении упругости ткани роговицы. Параметр SP-A1, указывающий общую жесткость глаза до проведения периферической иридэктомии был выше, что характерно для глазного яблока повышенной ригидности, это указывает на необходимость ПИ. При этом после ее проведения мы получили более низкие значения, достоверно не отличающиеся от группы контроля, что говорит о снижении ригидности фиброзной капсулы глаза и достижении нормальных значений (Таблица 2).
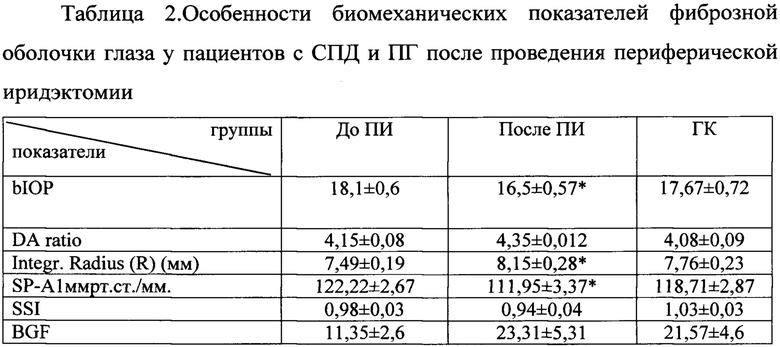
* - показатель достоверности различия между группами
В индексе напряжения-деформации, мы не получили достоверных различий между сравниваемыми группами, что вполне закономерно (Таблица 2). Зарубежные авторы установили, что SS1 коррелирует с возрастом, не зависит от ЦТР, уровня ВГД [7], от осевой длины глаза, кривизны роговицы, не связан с полом и объемом передней камеры [8].
По нашим клиническим наблюдениям, чем более низкая ригидность фиброзной оболочки глаза, чем большие значения BGF мы получаем и, при достижении толерантных значений ВГД и стабилизации биомеханических показателей, BGF у таких пациентов возрастает. Сниженный BGF при СПД до проведения ПИ можно объяснить более высокой ригидностью глазного яблока и рассматривать как показание к ее проведению. В результате мы получили динамику в показателях биомеханического глаукомного фактора (BGF), который достоверно возрос после проведения ПИ и достиг значений здорового близорукого глаза, что указывает на достижение толерантных значений показателей биомеханики фиброзной оболочки глаза (таблица 2).
Список использованной литературы
1. Niyadurupola N, Broadway DC. Pigment dispersion syndrome and pigmentaryglaucomaa major review. ClinExpOphthalmol. 2008 Dec;36(9):868-882. doi: 10.111 l/j.l442-9071.2009.01920.x.
2. Pang R, Labisi SA, Wang N. Pigmentdispersionsyndromeandpigmentaryglaucoma:
overviewandracialdisparities. Graefes Arch ClinExpOphthalmol. 2023 Mar; 261(3):601-614. doi: 10.1007/s00417-022-05817-0.
3. Scuderi G, Contestabile MT, Scuderi L, Librando A, Fenicia V, Rahimi S. Pigm entdispersionsyndromeandpigmentary glaucoma: are vi ewandupdate. IntOphthalmol. 2019 Jul; 39(7): 1651-1662. doi: 10.1007/sl0792-018-0938-7.
4. Roberts C.J., Mahmoud A.M., Bons J.P., Hossain A., Elsheikh A.,
Vinciguerra R., Vinciguerra P., Ambrosio R. Jr. Introduction of Two Novel Stiffness Parameters and Interpretation of Air Puff-Induced Biomechanical Deformation Parameters With a Dynamic Scheimpflug Analyzer. J Refract Surg. 2017 Apr l;33(4):266-273. doi: 10.3928/1081597X-20161221-03.
5. Pradhan Z.S., Deshmukh S., Dixit S., Sreenivasaiah S., Shroff S., Devi S., Webers C.A.B., Rao H.L. A comparison of the corneal biomechanics in pseudoexfoliation glaucoma, primary open-angle glaucoma and healthy controls using CorvisST.PLoS One. 2020 Oct 26; 15(10):e0241296. doi: 10.137 l/journal.pone. 0241296.
6. Wu N., Chen Y., Yang Y., Sun X. The changes of corneal biomechanical properties with long-term treatment of prostaglandin analogue measured by Corvis ST.BMCOphthalmol. 2020 Oct 20; 20(1):422. doi: 10.1186/sl2886-020-01693-6.
7. Eliasy A., Chen K.J., Vinciguerra R. et al. Determination of Corneal Biomechanical Behavior in-vivo for Healthy Eyes Using CorVis ST Tonometry: Stress-Strain Index. Front BioengBiotechnol. 2019;7:105. Published 2019 May 16. doi:10.3389/fbioe.2019.00105.
8. Liu G., Rong H., Pei R. et al. Age distribution and associated factors of cornea biomechanical parameter stress-strain index in Chinese healthy population. BMC Ophthalmol20,436 (2020). https://doi.org/10.1186/sl2886-020-01704-6.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ГЛАУКОМЫ НИЗКОГО ДАВЛЕНИЯ | 2023 |
|
RU2823133C1 |
| СПОСОБ ДИАГНОСТИКИ ГЛАУКОМЫ В ГЛАЗАХ ПОСЛЕ ПЕРЕНЕСЕННОЙ РАДИАЛЬНОЙ КЕРАТОТОМИИ | 2024 |
|
RU2834418C1 |
| Способ профилактики пигментной глаукомы при синдроме пигментной дисперсии | 2019 |
|
RU2731885C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТАДИЙ РАЗВИТИЯ СИНДРОМА ПИГМЕНТНОЙ ДИСПЕРСИИ ГЛАЗА | 2001 |
|
RU2215500C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПЕРВИЧНОЙ ОТКРЫТОУГОЛЬНОЙ ГЛАУКОМЫ | 2020 |
|
RU2752031C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГЛАУКОМЫ | 2006 |
|
RU2315585C1 |
| Способ диагностики начальных проявлений первичной открытоугольной глаукомы | 2022 |
|
RU2778966C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НОРМОТЕНЗИВНОЙ ГЛАУКОМЫ | 2015 |
|
RU2573336C1 |
| Способ измерения внутриглазного давления у пациентов, перенесших радиальную кератотомию | 2016 |
|
RU2610556C1 |
| Способ ранней диагностики оптической нейропатии на фоне системной или комбинированной химиотерапии у детей с ретинобластомой | 2020 |
|
RU2750153C1 |
Изобретение относится к медицине, а именно к офтальмологии. Проводят исследование биомеханических параметров фиброзной оболочки глаза: bIОР, DA Ratio, Integr. Radius (R), SP-A1, StressStrainlndex (SSI), BGF, и если bIОР более 18,0 мм рт.ст., Integr. Radius (R) менее 7,7 мм, SP-A1 более 118mmHg/mm и BGF менее 20, проводят периферическую иридэктомию. После чего осуществляют контроль нормализации биомеханических параметров фиброзной оболочки глаза, при этом значения bIОР менее 16,5 мм рт.ст., Integr. Radius (R) более 8,0 мм, SP-A1 менее 118mmHg/mm и BGF более 20 рассматривают как достижение толерантного ВГД, нормализацию биомеханических параметров глаза. Способ позволяет на основании биомеханических показателей фиброзной капсулы глаза определить показания к проведению периферической иридэктомии и обеспечить контроль их нормализации, а также достичь толерантного офтальмотонуса после лазерного вмешательства, чем и повышает возможность прогноза прогрессирования заболевания. 2 табл., 2 пр.
Способ реабилитации пациентов с синдромом пигментной дисперсии и пигментной глаукомой, отличающийся тем, что проводят исследование биомеханических параметров фиброзной оболочки глаза: bIОР, DA Ratio, Integr. Radius (R), SP-A1, StressStrainlndex (SSI), BGF, и если bIОР более 18,0 мм рт.ст., Integr. Radius (R) менее 7,7 мм, SP-A1 более 118mmHg/mm и BGF менее 20, проводят периферическую иридэктомию, после чего осуществляют контроль нормализации биомеханических параметров фиброзной оболочки глаза, при этом значения bIОР менее 16,5 мм рт.ст., Integr. Radius (R) более 8,0 мм, SP-A1 менее 118mmHg/mm и BGF более 20 рассматривают как достижение толерантного ВГД, нормализацию биомеханических параметров глаза.
| Способ профилактики пигментной глаукомы при синдроме пигментной дисперсии | 2019 |
|
RU2731885C2 |
| Способ определения стадии первичной открытоугольной глаукомы | 2016 |
|
RU2616212C1 |
| US 10426817 B2, 01.10.2019 | |||
| Scuderi G | |||
| et al | |||
| Pigment dispersion syndrome and pigmentary glaucoma: a review and update | |||
| Int Ophthalmol | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Niyadurupola N., Broadway D.C | |||
| Pigment dispersion syndrome and pigmentary glaucoma--a major review | |||
| Clin Exp Ophthalmol | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
Авторы
Даты
2024-10-21—Публикация
2024-03-25—Подача