ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее раскрытие относится к варианту Corynebacterium glutamicum с улучшенной способностью к продуцированию L-лизина и к способу продуцирования L-лизина с его применением.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
L-лизин представляет собой незаменимую аминокислоту, которая не синтезируется в человеческом или животном организме и должна поставляться извне, и он обычно продуцируется посредством ферментации с использованием микроорганизмов, таких как бактерии или дрожжи. При продукции L-лизина можно использовать полученные в природе штаммы дикого типа или варианты, модифицированные для наличия у них повышенной способности к продуцированию L-лизина. Недавно для того, чтобы улучшить эффективность продукции L-лизина разработали разные рекомбинантные штаммы или варианты с превосходной способностью к продуцированию L-лизина и способы продуцирования L-лизина с их использованием посредством применения технологии генной инженерии к таким микроорганизмам, как Escherichia coli и Corynebacterium, и т.д., которые широко используются при продукции L-аминокислот и других полезных веществ.
Согласно корейским патентам №10-0838038 и 10-2139806 нуклеотидные последовательности генов, кодирующих белки, включающие ферменты, связанные с продукцией L-лизина, или их аминокислотные последовательности, модифицируют для увеличения экспрессии генов или для удаления не являющихся необходимыми генов и, посредством этого, улучшают способность к продуцированию L-лизина. Кроме того, в публикации корейского патента №10-2020-0026881 раскрыт способ замены существующего промотора гена промотором с сильной активностью для того, чтобы увеличить экспрессию гена, кодирующего фермент, участвующий в продукции L-лизина.
Как было описано, разрабатывают целый ряд способов для увеличения способности к продуцированию L-лизина. Тем не менее, поскольку существуют десятки типов белков, таких как ферменты, транскрипционные факторы, транспортные белки и т.д., которые прямо или опосредованно участвуют в продукции L-лизина, необходимо проводить много исследований по тому, увеличивается ли или нет способность к продуцированию L-лизина согласно изменениям активностей данных белков.
Документы предшествующего уровня техники
Патентные документы
Корейский патент №10-0838038
Корейский патент №10-2139806
Публикация корейского патента №10-2020-0026881
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Техническая проблема
Целью настоящего раскрытия является предложение варианта Corynebacterium glutamicum с улучшенной способностью к продуцированию L-лизина.
Кроме того, другой целью настоящего раскрытия является предложение способа продуцирования L-лизина с использованием данного варианта.
Техническое решение
Авторы настоящего изобретения исследовали разработку нового варианта с улучшенной способностью к продуцированию L-лизина с использованием штамма Corynebacterium glutamicum и, в результате, они обнаружили то, что продукция L-лизина увеличивается посредством замены нуклеотидной последовательности в конкретном положении в промоторе гена tkt, кодирующего транскетолазу, который участвует в биосинтетическом пути L-лизина, посредством этого осуществляя настоящее раскрытие.
Согласно одному аспекту настоящего раскрытия предложен вариант Corynebacterium glutamicum с улучшенной способностью к продуцированию L-лизина посредством усиления активности транскетолазы.
Термин «транскетолаза» в том виде, как он здесь используется, относится к ферменту, который катализирует реакцию продуцирования седогептулозофосфата посредством переноса группы кетола (HOCH2CO-) от ксилулозофосфата на рибозофосфат в пентозофосфатном пути. Ген, кодирующий транскетолазу, состоит из оперона вместе с генами, каждый из которых кодирует трансальдолазу, глюкозо-6-фосфатдегидрогеназу и 6-фосфоглюконолактоназу, и экспрессия генов данного оперона регулируется одним промотором.
Согласно конкретному воплощению настоящего раскрытия транскетолаза может происходить из штамма рода Corynebacterium. В частности, штамм рода Corynebacterium может представлять собой Corynebacterium glutamicum, Corynebacterium crudilactis, Corynebacterium deserti, Corynebacterium callunae, Corynebacterium suranareeae, Corynebacterium lubricantis, Corynebacterium doosanense, Corynebacterium efficiens, Corynebacterium uterequi, Corynebacterium stationis, Corynebacterium pacaense, Corynebacterium singulare, Corynebacterium humireducens, Corynebacterium marinum, Corynebacterium halotolerans, Corynebacterium spheniscorum, Corynebacterium freiburgense, Corynebacterium striatum, Corynebacterium canis, Corynebacterium ammoniagenes, Corynebacterium renale, Corynebacterium pollutisoli, Corynebacterium imitans, Corynebacterium caspium, Corynebacterium testudinoris, Corynebacaterium pseudopelargi или Corynebacterium flavescens, но не ограничивается ими.
Термин «усиление активности» в том виде, как он здесь используется, означает то, что уровни экспрессии генов, кодирующих белки, такие как целевые ферменты, транскрипционные факторы, транспортные белки и т.д., увеличиваются посредством введения вновь или усиления данных генов по сравнению с генами штамма дикого типа или штамма перед модификацией. Такое усиление активности также включает случай, где активность самого белка увеличивается посредством замены, вставки или делеции нуклеотида кодирующего гена или их комбинации по сравнению с активностью белка, которым исходно обладал микроорганизм, и случай, где общая ферментативная активность в клетках выше, чем активность штамма дикого типа или штамма перед модификацией из-за повышенной экспрессии или повышенной трансляции кодирующих их генов и их комбинации.
Согласно конкретному воплощению настоящего раскрытия усиление активности транскетолазы может быть индуцировано сайт-специфичной мутацией в промоторе гена, кодирующего транскетолазу.
Согласно конкретному воплощению настоящего раскрытия промотор гена, кодирующего транскетолазу, может быть представлен нуклеотидной последовательностью SEQ ID NO: 1.
Термин «промотор» в том виде, как он здесь используется, относится к специфической области ДНК, которая регулирует транскрипцию гена посредством включения сайта связывания РНК-полимеразы, которая инициирует транскрипцию мРНК интересующего гена и обычно находится выше сайта начала транскрипции. Промотор у прокариот определяется как область около сайта начала транскрипции, где связывается РНК-полимераза, и он обычно состоит из двух коротких нуклеотидных последовательностей в областях пар оснований -10 и -35 выше сайта начала транскрипции. В настоящем раскрытии мутация промотора заключается в том, что промотор улучшен для того, чтобы иметь более высокую активность по сравнению с промотором дикого типа и может увеличивать экспрессию генов, расположенных ниже, посредством индуцирования мутаций в промоторной области, расположенной выше сайта начала транскрипции.
Согласно конкретному воплощению настоящего раскрытия усиление активности транскетолазы может быть обусловлено заменой одного или более чем одного основания в областях от -300 до -10 выше от сайта начала транскрипции в последовательности промотора гена, кодирующего транскетолазу.
Более конкретно, мутация промотора по настоящему раскрытию может представлять собой последовательную или непоследовательную замену одного или более чем одного основания в областях от -300 до -10, предпочтительно последовательную или непоследовательную замену одного, двух, трех, четырех, пяти, шести, семи, восьми, девяти или десяти оснований в областях от -250 до -50, областях от -230 до -200, областях от -190 до -160 или областях от -90 до -60.
Согласно одному типичному воплощению настоящего раскрытия ccaattaacc, которая представляет собой нуклеотидную последовательность в областях от -83 до -74 промоторной последовательности гена tkt, кодирующего транскетолазу, штамма Corynebacterium glutamicum, заменяется на tgtgctgtca с получением варианта Corynebacterium glutamicum, имеющего новую последовательность промотора гена tkt. Такой вариант Corynebacterium glutamicum может включать мутировавшую последовательность промотора гена tkt, которая представлена нуклеотидной последовательностью SEQ ID NO: 2.
Согласно одному типичному воплощению настоящего раскрытия ccaattaacc, которая представляет собой нуклеотидную последовательность в областях от -83 до -74 промоторной последовательности гена tkt, кодирующего транскетолазу штамма Corynebacterium glutamicum, заменяется на tgtggtatca с получением варианта Corynebacterium glutamicum, имеющего новую промоторную последовательность гена tkt. Такой вариант Corynebacterium glutamicum может включать мутировавшую промоторную последовательность гена tkt, которая представлена нуклеотидной последовательностью SEQ ID NO: 3.
Термин «улучшенная способность к продукции» в том виде, как он здесь используется, означает повышенную продуктивность в отношении L-лизина по сравнению с продуктивностью родительского штамма. Родительский штамм относится к штамму дикого типа или варианту штамма, который подвергся мутации, и он включает субъекта, который непосредственно мутирован или преобразован рекомбинантным вектором и т.д. В настоящем раскрытии родительский штамм может представлять собой штамм Corynebacterium glutamicum или штамм, мутировавший из дикого типа.
Согласно конкретному воплощению настоящего раскрытия родительский штамм представляет собой вариант, в котором индуцируются мутации в последовательностях генов (например, генов lysC, zwf и hom), участвующих в продукции лизина, и он может представлять собой штамм Corynebacterium glutamicum (далее именуемый «штамм DS1 Corynebacterium glutamicum»), депонированный в Корейский центр культивирования микроорганизмов 2 апреля 2021 г. с номером доступа KCCM12969P.
Вариант Corynebacterium glutamicum по настоящему раскрытию, имеющий улучшенную способность к продуцированию L-лизина, может включать мутировавшую последовательность промотора гена, кодирующего транскетолазу.
Согласно конкретному воплощению настоящего раскрытия данный вариант может включать любую из нуклеотидных последовательностей, представленных SEQ ID NO: 2-4, в качестве последовательности промотора гена транскетолазы.
Согласно одному конкретному воплощению настоящего раскрытия данный вариант может включать мутацию промотора гена tkt, кодирующего транскетолазу, демонстрируя, посредством этого, повышенную способность к продуцированию L-лизина по сравнению с родительским штаммом, и, в частности, может демонстрировать 5%-ное или большее, в частности, от 5%-ного до 40%-ного и, более конкретно, от 10%-ного до 30%-ного увеличения продукции L-лизина по сравнению с родительским штаммом, продуцируя посредством этого от 65 г до 90 г L-лизина, предпочтительно от 70 г до 80 г L-лизина на 1 л культуры данного штамма. Кроме того, данный вариант может демонстрировать примерно 4%-ное или большее увеличение продукции L-лизина по сравнению с существующим вариантом промотора гена tkt с другим сайтом мутации, посредством этого продуцируя L-лизин с высоким выходом.
Получение варианта Corynebacterium glutamicum по конкретному воплощению настоящего раскрытия может быть достигнуто посредством рекомбинантного вектора, включающего вариант, в котором часть последовательности промотора гена, кодирующего транскетолазу, у родительского штамма заменена.
Термин «часть» в том виде, как он здесь используется, означает не всю нуклеотидную последовательность или последовательность полинуклеотида, и может содержать от 1 до 300, предпочтительно от 1 до 100 и более предпочтительно от 1 до 50 нуклеотидов, но не ограничиваясь ими.
Термин «вариант» в том виде, как он здесь используется, относится к варианту промотора, в котором заменено одно или более чем одно основание в областях от -300 до -10 в последовательности промотора гена транскетолазы, участвующего в биосинтезе L-лизина.
Согласно конкретному воплощению настоящего раскрытия варианты, в каждом из которых нуклеотидная последовательность в областях от -83 до -74 в промоторной последовательности гена транскетолазы заменена на tgtgctgtca или tgtggtatca, могут иметь нуклеотидную последовательность SEQ ID NO: 2 или SEQ ID NO: 3 соответственно.
Термин «вектор» в том виде, как он используется в данном документе, представляет собой экспрессионный вектор, способный экспрессировать целевой белок в подходящей клетке-хозяине, и он относится к генетической конструкции, включающей существенные регуляторные элементы, которые связаны функциональным образом таким образом, что экспрессируется вставка гена. Здесь термин «связанный функциональным образом» означает то, что ген, требующий экспрессии, и его регуляторная последовательность функционально связаны друг с другом с индукцией экспрессии гена, и «регуляторные элементы» включают промотор для осуществления транскрипции, любую последовательность оператора для осуществления контроля транскрипции, последовательность, кодирующую подходящий сайт связывания рибосомы с мРНК, и последовательность, контролирующую терминацию транскрипции и трансляции. Такой вектор может включать плазмидный вектор, космидный вектор, бактериофаговый вектор, вирусный вектор и т.д., но не ограничивается ими.
«Рекомбинантный вектор» в том виде, как здесь используется данный термин, трансформируют в подходящую клетку-хозяина, и затем он реплицируется независимо от генома данной клетки-хозяина или может быть интегрирован в сам геном. В данном отношении «подходящая клетка-хозяин», где данный вектор является реплицируемым, может включать репликатор, который представляет собой конкретную нуклеотидную последовательность, в которой инициируется репликация.
Для трансформации выбирают подходящую технологию введения вектора, в зависимости от клетки-хозяина для экспрессии целевого гена в данной клетке-хозяине. Например, введение вектора может осуществляться электропорацией, тепловым шоком, осаждением с фосфатом кальция (CaPO4), осаждением с хлоридом кальция (CaCl2), микроинъекцией, способом с полиэтиленгликолем (PEG), способом с DEAE-декстраном, способом с катионными липосомами, способом с ацетатом лития-DMSO (диметилсульфоксид) или их комбинациями. При условии, что трансформированный ген может экспрессироваться в клетке-хозяине, он может быть включен без ограничения, независимо от того, вставлен ли или не вставлен данный ген в хромосому клетки-хозяина или локализуется вне хромосомы.
Клетки-хозяева включают клетки, трансфицированные, трансформированные или инфицированные рекомбинантным вектором или полинуклеотидом по настоящему раскрытию in vivo или in vitro. Клетки-хозяева, включающие рекомбинантный вектор по настояшему раскрытию, представляют собой рекомбинантные клетки-хозяева, рекомбинантные клетки или рекомбинантные микроорганизмы.
Кроме того, рекомбинантный вектор по настоящему раскрытию может включать селективный маркер, который предназначен для отбора трансформанта (клетки-хозяина), трансформированного данным вектором. В среде, обработанной селективным маркером, только клетки, экспрессирующие данный селективный маркер, могут выживать, и, таким образом, могут быть отобраны трансформированные клетки. Селективный маркер может быть представлен канамицином, стрептомицином, хлорамфениколом и т.д., но не ограничивается ими.
Гены, вставленные в рекомбинантный вектор для трансформации по настоящему раскрытию, могут быть введены в клетки-хозяева, такие как микроорганизмы рода Corynebacterium, из-за кроссинговера посредством гомологичной рекомбинации.
Согласно конкретному воплощению настоящего раскрытия клетка-хозяин может представлять собой штамм рода Corynebacterium, например, штамм Corynebacterium glutamicum.
Кроме того, согласно другому аспекту настоящего раскрытия предложен способ продуцирования L-лизина, включающий стадии а) культивирования варианта Corynebacterium glutamicum в среде; и б) выделения L-лизина из данного варианта или среды, в которой культивируется данный вариант.
Культивирование может осуществляться согласно подходящей среде и культуральным условиям, известным в данной области, и любой специалист в данной области может легко корректировать и применять данную среду и условия культивирования. В частности, данная среда может представлять собой жидкую среду, но не ограничивается ей. Способ культивирования может включать, например, периодическое культивирование, непрерывное культивирование, культивирование с подпиткой или их комбинации, но не ограничивается ими.
Согласно конкретному воплощению настоящего раскрытия данная среда должна удовлетворять требованиям конкретного штамма правильным образом, и она может быть подходящим образом модифицирована специалистом в данной области. Относительно культуральной среды для штамма рода Corynebacterium может быть сделана ссылка на известный документ (Manual of Methods for General Bacteriology. American Society for Bacteriology. Washington D.C., USA, 1981), но не ограничиваясь им.
Согласно конкретному воплощению настоящего раскрытия данная среда может включать разные источники углерода, источники азота и компоненты-микроэлементы. Источники углерода, которые можно использовать, включают сахариды и углеводы, такие как такие как глюкоза, сахароза, лактоза, фруктоза, мальтоза, крахмал, целлюлоза и т.д., жиры и масла, такие как соевое масло, подсолнечное масло, касторовое масло, кокосовое масло и т.д., жирные кислоты, такие как пальмитиновая кислота, стеариновая кислота и линолевая кислота, спирты, такие как глицерин и этанол, и органические кислоты, такие как уксусная кислота. Данные вещества можно использовать индивидуально или в смеси, но не ограничиваясь ими. Источники азота, которые можно использовать, включают пептон, дрожжевой экстракт, мясной экстракт, солодовый экстракт, жидкий кукурузный экстракт, соевый шрот, мочевину или неорганические соединения, например, сульфат аммония, хлорид аммония, фосфат аммония, карбонат аммония и нитрат аммония. Данные источники азота также можно использовать индивидуально или в смеси, но не ограничиваясь ими. Источники фосфора, которые можно использовать, могут включать калия дигидрофосфат или дикалия гидрофосфат, или соответствующие натрийсодержащие соли, но не ограничиваются ими. Кроме того, культуральная среда может включать соли металлов, такие как сульфат магния или сульфат железа, которые требуются для роста, но не ограничиваются ими. Кроме того, культуральная среда может включать незаменимые ростовые вещества, такие как аминокислоты и витамины. Более того, в данной культуральной среде можно использовать подходящие предшественники. Среду или индивидуальные компоненты можно добавлять в культуральную среду во время культивирования подходящим способом периодически или непрерывно, но не ограничиваясь ими.
Согласно конкретному воплощению настоящего раскрытия рН культуральной среды можно корректировать добавлением в культуральную среду микроорганизма подходящим способом во время культивирования таких соединений, как гидроксид аммония, гидроксид калия, аммиак, фосфорная кислота и серная кислота. Кроме того, во время культивирования пенообразование можно подавлять с использованием пеногасителя, такого как сложный полигликолевый эфир жирной кислоты. Кроме того, для поддержания культуральной среды в аэробном состоянии в данную культуральную среду можно инъецировать кислород или кислородсодержащий газ (например, воздух). Температура данной культуральной среды обычно может составлять от 20°С до 45°С, например, от 25°С до 40°С. Культивирование можно продолжать, пока не продуцируется желательное количество полезного вещества. Например, время культивирования может составлять от 10 часов до 160 часов.
Согласно конкретному воплощению настоящего раскрытия на стадии выделения L-лизина из культивируемого варианта и среды, в которой культивируется данный вариант, продуцированный L-лизин может быть отобран или выделен из культуральной среды с использованием подходящего способа, известного в данной области, в зависимости от способа культивирования. Например, можно использовать центрифугирование, фильтрование, экстракцию, распыление, сушку, упаривание, осаждение, кристаллизацию, электрофорез, фракционное растворение (например, осаждение сульфатом аммония), хроматографию (например, ионообменная, аффинная, гидрофобная и гель-фильтрация) и т.д., но способ не ограничивается ими.
Согласно конкретному воплощению настоящего раскрытия на стадии выделения лизина культуральную среду центрифугируют на низкой скорости для удаления биомассы, и полученный супернатант можно разделять посредством ионообменной хроматографии.
Согласно конкретному воплощению настоящего раскрытия стадия выделения L-лизина может включать способ очистки L-лизина.
Полезные эффекты
Вариант Corynebacterium glutamicum по настоящему раскрытию может улучшать продукционный выход L-лизина посредством увеличения или усиления экспрессии гена, кодирующего транскетолазу, по сравнению с родительским штаммом.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
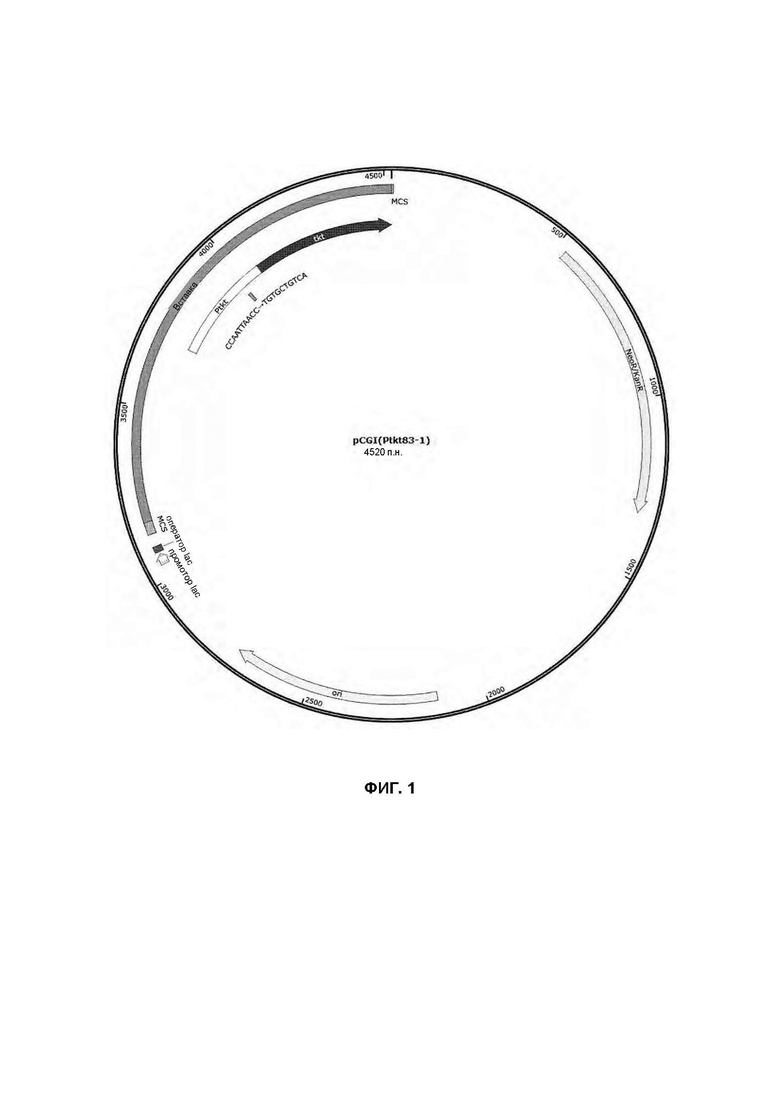
На ФИГ. 1 показана конструкция вектора pCGI(Ptkt83-1), включающего изменение, при котором согласно одному типичному воплощению настоящего раскрытия нуклеотидная промоторная последовательность транскетолазы в положениях от -83 до -74 заменена на tgtgctgtca; и
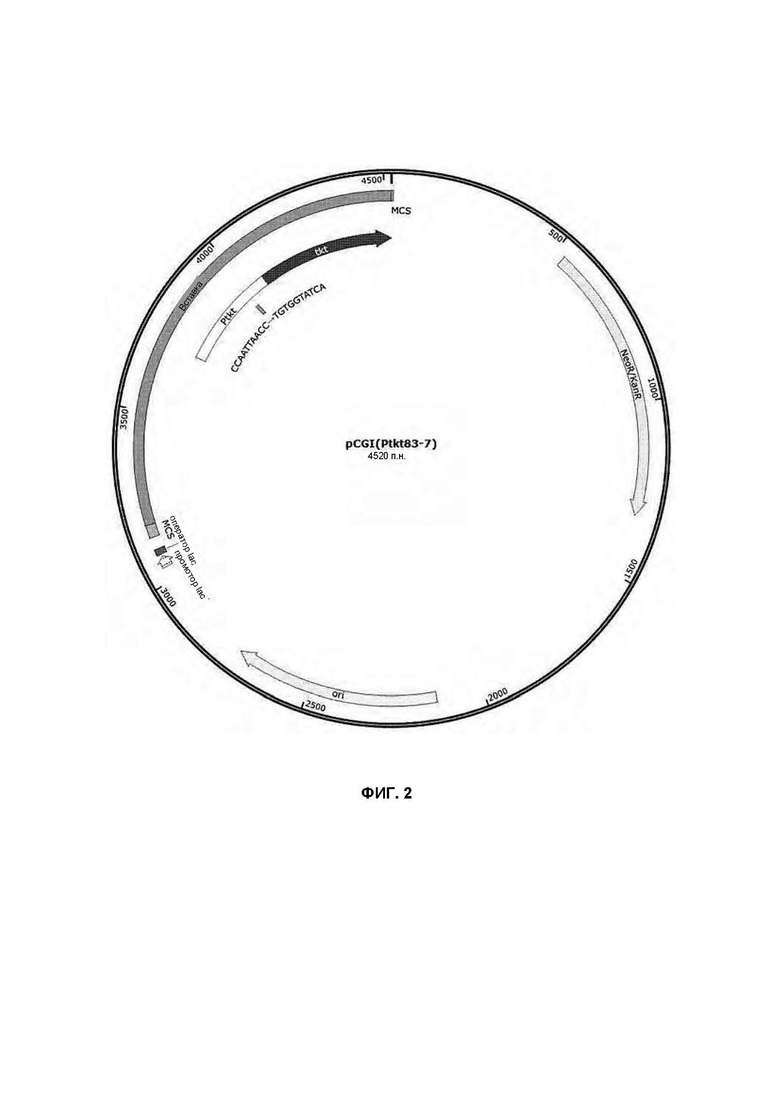
На ФИГ. 2 показана конструкция вектора pCGI(Ptkt83-7), включающего изменение, при котором согласно одному типичному воплощению настоящего раскрытия нуклеотидная промоторная последовательность транскетолазы в положениях от -83 до -74 заменена на tgtggtatca.
Способ осуществления данного изобретения
Далее настоящее раскрытие будет описано более подробно. Однако данное описание просто приводится для того, чтобы помочь пониманию настоящего раскрытия, и объем настоящего раскрытия не ограничивается данным типичным описанием.
Пример 1. Получение варианта Corynebacterium glutamicum
Для получения варианта Corynebacterium glutamicum с повышенной транскетолазной активностью для индукции случайной мутации использовали штамм DS1 Corynebacterium glutamicum.
1-1. Мутагенез
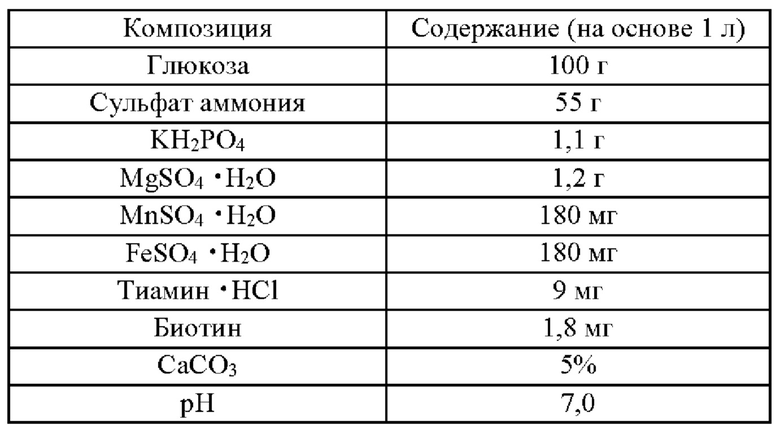
Штамм DS1 Corynebacterium glutamicum инокулировали в колбу, содержащую 50 мл жидкой среды СМ (5 г глюкозы, 2,5 г NaCl, 5,0 г дрожжевого экстракта, 1,0 г мочевины, 10,0 г полипептона и 5,0 г говяжьего экстракта, рН 6,8), и добавляли N-метил-N'-нитро-N-нитрозогуанидин (NTG), который представляет собой мутаген, в конечной концентрации 300 мкг/мл, с последующим культивированием при 30°С со встряхиванием при 200 об./мин в течение 20 часов. После завершения культивирования культуру центрифугировали при 12000 об./мин в течение 10 минут для удаления супернатанта, и получаемое в результате один раз промывали физиологическим раствором и три раза или более промывали фосфатным буфером. Это суспендировали в 5 мл фосфатного буфера, распределяли на твердой среде для посевной культуры (в жидкую среду СМ дополнительно добавляли 15 г/л агара и 8% лизина) и культивировали при 30°С в течение 30 часов для выделения 100 колоний.
1-2. Отбор вариантов с улучшенной способностью к продуцированию L-. III ti l на и получение библиотек мутаций
Каждые 5% 100 выделенных колоний инокулировали в колбу, содержащую 10 мл жидкой среды для продукции лизина, показанной ниже в Таблице 1, и культивировали со встряхиванием при 200 об./мин при 30°С в течение 30 часов. Степень роста бактерий подтверждали измерением поглощения каждой культуры при ОП (оптическая плотность) 610 нм, и продукцию L-лизина измеряли с использованием ВЭЖХ (высокоэффективная жидкостная хроматография) (Shimazu, Япония). Посредством этого сравнивали продукцию L-лизина, и отбирали колонии, продуцирующие 67,0 г/л или более L-лизина, и анализировали нуклеотидные последовательности их главных генов, связанных с лизином, и промоторные области, для идентификации штаммов с мутациями в промоторе гена tkt. 
Пример 2. Улучшение промотора tkt
2-1. Улучшение промотора: введение мутаций
Синтезировали 30 последовательностей-кандидатов с вплоть до 15 модификациями нуклеотидной последовательности, охватывающими положения на промоторе tkt, которые были выбраны в Примере 1, посредством способа [Sambrook, J. et al. (2001) "Molecular Cloning: A Laboratory Manual", Cold Spring Harbor Laboratory Press, volume 2. 13.36~13.39], последовательность промотора tkt Corynebacterium glutamicum ATCC13032 (см. SEQ ID NO: 1) и синтезированную область промотора tkt клонировали в вектор с репортером хлорамфениколацетилтрансферазой (CAT) и вектор pSK1-CAT соответственно. Во время клонирования ДНК ориентацию и присутствие или отсутствие мутаций подтверждали посредством секвенирования ДНК. Полученные таким образом библиотеки мутантов называли от pSK1-tkt1 до pSK1-tkt30. Наконец их трансформировали в Corynebacterium glutamicum ATCC 13032, соответственно, и их активности промотора сравнивали и проверяли.
2-2. Трансформация конструкции pSK1-CAT в Corynebacterium glutamicum АТСС13032
Получали компетентные клетки для трансформации каждого из полученных клонов pSK-tkt, которые идентифицировали посредством анализа последовательности, в Corynebacterium glutamicum АТСС13032. 10 мл культивируемой Corynebacterium glutamicum АТСС13032 инокулировали в 100 мл среды BHIS и культивировали при 30°С в течение ночи, затем вновь инокулировали в 100 мл жидкой среды СМ при ОП 600 нм 0,3 и культивировали при 18°С и 120 об./мин в течение примерно 28 часов пока ОП 600 не становилась равной 0,8. Данную культуральную среду центрифугировали при 4°С и 6000 об./мин в течение 10 мин для выделения клеток, которые затем суспендировали в 20 мл 10%-ного раствора глицерина, и процесс центрифугирования повторяли три раза. Выделенные клетки вновь суспендировали в 10%-ном растворе глицерина, каждые 100 мкл распределяли в Е-пробирки и хранили в морозильной камере глубокой заморозки при -70°С до применения. 1 мкг ДНК добавляли к 100 мкл компетентных клеток Corynebacterium glutamicum ATCC 13032, добавляли в охлажденную кювету для электропорации, и проводили электропорацию с использованием MicroPulser от Bio-Rad. Сразу после подачи импульсов клетки выделяли посредством добавления 1 мл жидкой среды СМ, предварительно нагретой при 46°С, проводили реакцию в течение 2 минут на льду и затем инкубировали при 180 об./мин в инкубаторе при 30°С. Затем ее 100 мкл распределяли на чашке с агаром BHIS, в который добавляли канамицин (50 мкг/мл), и культивировали в инкубаторе при 30°С.
2-3. Анализ CAT
Анализ хлорамфениколацетилтрансферазы (анализ CAT) вариантов промоторной области tkt проводили с использованием способа Shaw (Shaw et al, 1991. Biochemistry. 30(44): 10806). Вкратце, трансформированный штамм Corynebacterium glutamicum культивировали в среде СМ, дополненной канамицином (50 мкг/мл), и затем выделяли клетки с получением лизата белка. Добавляли 5 мкг каждого белка, 0,1 М буфера Tris-HCl (рН 7,8), 0,4 мг/мл 5,5'-дитиобис-2-нитробензойной кислоты (DTNB; Sigma D8130), 0,1 мМ ацетил-КоА (Sigma А2056) и 0,1 мМ хлорамфеникола, давали реагировать при RT (комнатная температура) в течение 15 минут и измеряли поглощение при ОП 412 нм. Посредством этого отбирали Ptkt83-1 и Ptkt83-7, имеющие улучшенную активность CAT по сравнению с последовательностью промотора tkt дикого типа.
В Ptkt83-1 и Ptkt83-7 нуклеотидную последовательность в областях от -83 до -74 промоторной последовательности гена tkt, кодирующего транскетолазу, заменяли на tgtgctgtca и tgtggtatca соответственно. Затем проводили эксперимент с использованием штамма DS1 Corynebacterium glutamicum для проверки увеличения продуктивности в отношении L-лизина вследствие мутации промотора гена tkt.
Пример 3. Получение варианта промотора Corynebacterium glutamicum DS1
Для получения варианта Corynebacterium glutamicum с усиленной транскетолазной активностью использовали штамм DS1 Corynebacterium glutamicum и DH5a Е. coli (HIT Competent cells™, кат. № RH618).
Штамм DS1 Corynebacterium glutamicum культивировали при температуре 30°C в среде СМ-бульон (рН 6,8), имеющей следующий состав: 5 г глюкозы, 2,5 г NaCl, 5,0 г дрожжевого экстракта, 1,0 г мочевины, 10,0 г полипептона и 5,0 г говяжьего экстракта в 1 л дистиллированной воды.
DH5a Е. coli культивировали при температуре 37°С в среде LB, имеющей следующий состав: 10,0 г триптона, 10,0 г NaCl и 5,0 г дрожжевого экстракта в 1 л дистиллированной воды.
Использовали канамицин и стрептомицин - продукты Sigma - а анализ секвенирования ДНК проводили в Macrogen Co., Ltd.
3-1. Получение рекомбинантного вектора
Для увеличения продуктивности в отношении лизина посредством усиления активности транскетолазы, участвующей в пентозофосфатном пути у данного штамма, вводили усиление транскетолазы. Способ, используемый в данном Примере, индуцировал специфичную мутацию в промоторе гена tkt для того, чтобы увеличить экспрессию гена tkt, кодирующего транскетолазу. Нуклеотидную последовательность в положениях от -83 до -74 промотора гена tkt заменяли с ccaattaacc на tgtgctgtca, получали праймеры, содержащие мутировавшие последовательности, и 696 п.н. левого плеча и 697 п.н. правого плеча с центром около мутировавшей области промотора гена tkt генома варианта DS1 Corynebacterium glutamicum, отобранного в Примере 1, амплифицировали посредством ПЦР (полимеразная цепная реакция), связывали с использованием ПЦР с перекрывающимися праймерами и затем клонировали в рекомбинантный вектор pCGI (см. [Kim et at, Journal of Microbiological Methods 84 (2011) 128-130]). Данную плазмиду называли pCGI(Ptkt83-1) (см. ФИГ. 1). Для конструирования данной плазмиды использовали праймеры, показанные в Таблице 2 ниже, для амплификации каждого фрагмента гена.

Подробности являются следующими: ПЦР проводили с использованием геномной ДНК штамма DS1 Corynebacterium glutamicum и соответствующих праймеров при следующих условиях. От 25 до 30 циклов проводили с использованием термоциклера (ТР600, TAKARA BIO Inc., Япония) в присутствии 1 единицы смеси ДНК-полимеразы pfu-X (Solgent, Корея) с использованием 1 пМ олигонуклеотида и 10 нг хромосомной ДНК штамма DS1 Corynebacterium glutamicum в качестве матрицы в реакционном растворе, в который добавляли 100 мкл каждого дезоксинуклеотидтрифосфата (дАТФ, дЦТФ, дГТФ, дТТФ). ПЦР проводили при следующих условиях: (1) стадия денатурации: при 94°С в течение 30 секунд, (2) стадия отжига: при 58°С в течение 30 секунд, и (3) стадия элонгации: при 72°С в течение 1 минуты 2 минут (время полимеризации 2 минуты на 1 т.п.н.).
Каждый фрагмент гена, полученный таким образом, клонировали в вектор pCGI с использованием рестрикционных ферментов BamHI и EcoRT и набора для лигирования ДНК Ver2.1 (Takara, Япония). Данный вектор трансформировали в Е. coli DH5a, производили посев на чашки с LB-агаром, содержащим 50 мкг/мл канамицина, и культивировали при 37°С в течение 24 часов. Образующиеся в результате колонии выделяли, и подтверждали, правильно ли присутствовала данная вставка в векторе, который выделяли и использовали при рекомбинации штамма Corynebacterium glutamicum.
3-2. Получение варианта
Штамм DS1-Ptkt83-1, который представляет собой вариант штамма, получали с использованием вектора pCGI(Ptkt83-1). Данный вектор получали в конечной концентрации 1 мкг/мл или больше, и первичную рекомбинацию индуцировали в штамме DS1 Corynebacterium glutamicum с использованием электропорации (см. документ [Tauch et al., FEMS Microbiology letters 123 (1994) 343-347]). В это время подвергнутый электропорации штамм затем распределяли на чашке с СМ-агаром, содержащей 20 мкг/мкл канамицина, с выделением колоний, и затем подтверждали посредством ПЦР и анализа секвенирования оснований, правильно ли данный вектор был вставлен во введенное положение в геноме. Для индукции вторичной рекомбинации выделенный штамм инокулировали в жидкую среду с СМ-агаром, содержащую стрептомицин, культивировали в течение ночи или дольше и затем распределяли на среде с агаром, содержащей такую же концентрацию стрептомицина, для выделения колоний. После проверки устойчивости к канамицину в конечных выделенных колониях посредством анализа секвенирования оснований подтвердили, были ли введены мутации в ген tkt в штаммах без устойчивости к антибиотику (см. документ [Schafer et al., Gene 145 (1994) 69-73]). Наконец, получали вариант Corynebacterium glutamicum (DS1-Ptkt83-10), в который вводили мутировавший ген tkt.
Пример 4. Получение варианта Corynebacterium glutamicum
Вариант Corynebacterium glutamicum получали таким же способом, как и в Примере 3, за исключением того, что производили замену нуклеотидной промоторной последовательности в положениях от -83 до -74 гена tkt с ccaattaacc на tgtggtatca.
Здесь для конструирования плазмиды использовали праймеры, показанные в Таблице 3 ниже, для амплификации каждого фрагмента гена, и штамм DS1-Ptkt83-7, который представляет собой вариант штамма, получали с использованием полученного вектора плазмиды pCGI(Ptkt83-7). Наконец, получали вариант Corynebacterium glutamicum (DS1-Ptkt83-7), в который вводили мутировавший ген tkt.

Сравнительный пример 1. Вариант Corynebacterium glutamicum
Использовали вариант (Ptkt217), раскрытый в корейском патенте №10-1504900, в котором последовательность в положениях от -217 до -206 промотора гена tkt штамма Corynebacterium glutamicum была заменена от ATTGATCACACC на CCCTGACTACAAA.
Экспериментальньш пример 1. Сравнение продуктивности в отношении L-лизина между вариантами
Продуктивность в отношении L-лизина сравнивали между родительским штаммом DS1 Corynebacterium glutamicum, штаммами DS1-Ptkt83-1 и DS1-Ptkt83-7, которые представляют собой варианты, продуцирующие лизин, полученные в Примерах 3-4, и штамм Ptkt217 Сравнительного примера 1, который представляет собой существующий вариант, продуцирующий лизин, таким же способом, как и в Примере 1-2. Результаты показаны в Таблице 4 ниже.
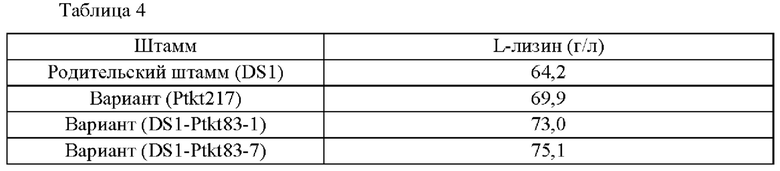
Как показано в Таблице 4, подтвердили то, что варианты Corynebacterium glutamicum - штаммы DS1-Ptkt83-1 и DS1-Ptkt83-7 - демонстрировали примерно 14%-ное и 17%-ное увеличения продуктивности в отношении L-лизина, соответственно, по сравнению с родительским штаммом DS1 Corynebacterium glutamicum из-за замены специфических частей (области от -83 до -74) в промоторной последовательности гена tkt оптимальной нуклеотидной последовательностью для усиления биосинтетического пути лизина.
Также подтвердили то, что варианты Corynebacterium glutamicum - штаммы DS1-Ptkt83-1 и DS1-Ptkt83-7 - демонстрировали примерно 4%-ное и 7%-ное увеличения продуктивности в отношении L-лизина, соответственно, по сравнению с существующим вариантом Ptkt217, имеющим другой сайт мутации (области от -217 до -206) и последовательность (CCCTGACTACAAA).
Данные результаты показывают то, что усиленная экспрессия гена tkt из-за мутации в областях от -83 до -74 промотора может стимулировать способность к биосинтезу лизина, посредством этого улучшая способность к продуцированию L-лизина данного штамма.
Выше настоящее раскрытие было описано со ссылкой на его предпочтительные типичные воплощения. Специалистам в области, к которой относится настоящее раскрытие, будет понятно то, что настоящее раскрытие можно осуществлять в модифицированных формах без отступления от важных характеристик настоящего раскрытия. Соответственно, раскрытые здесь типичные воплощения следует рассматривать в иллюстративном аспекте, а не в ограничивающем аспекте. Объем настоящего раскрытия показан не в приведенном выше объяснении, а в приложенной формуле изобретения, и все различия в пределах эквивалентного ей объема следует интерпретировать как включенные в настоящее раскрытие.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> CJ CheilJedang Corporation
<120> ВАРИАНТ CORYNEBACTERIUM GLUTAMICUM С УЛУЧШЕННОЙ СПОСОБНОСТЬЮ К
ПРОДУКЦИИ L-ЛИЗИНА И СПОСОБ ПРОДУЦИРОВАНИЯ L-ЛИЗИНА С ЕГО
ПРИМЕНЕНИЕМ
<130> OPA23235
<150> KR 10-2021-0056580
<151> 2021-04-30
<150> KR 10-2021-0067391
<151> 2021-05-26
<160> 9
<170> KoPatentIn 3.0
<210> 1
<211> 352
<212> DNA
<213> Artificial Sequence
<220>
<223> Последовательность промотора гена tkt
<400> 1
gattcgttcc gttcgtgacg ctttgtgagg ttttttgacg ttgcaccgta ttgcttgccg 60
aacatttttc ttttcctttc ggtttttcga gaattttcac ctacaaaagc ccacgtcaca 120
gctcccagac ttaagattga tcacaccttt gacacatttg aaccacagtt ggttataaaa 180
tgggttcaac atcactatgg ttagaggtgt tgacgggtca gattaagcaa agactacttt 240
cggggtagat cacctttgcc aaatttgaac caattaacct aagtcgtaga tctgatcatc 300
ggatctaacg aaaacgaacc aaaactttgg tcccggttta acccaggaag ga 352
<210> 2
<211> 352
<212> DNA
<213> Artificial Sequence
<220>
<223> Мутантная последовательность промотора гена tkt
<400> 2
gattcgttcc gttcgtgacg ctttgtgagg ttttttgacg ttgcaccgta ttgcttgccg 60
aacatttttc ttttcctttc ggtttttcga gaattttcac ctacaaaagc ccacgtcaca 120
gctcccagac ttaagattga tcacaccttt gacacatttg aaccacagtt ggttataaaa 180
tgggttcaac atcactatgg ttagaggtgt tgacgggtca gattaagcaa agactacttt 240
cggggtagat cacctttgcc aaatttgaat gtgctgtcat aagtcgtaga tctgatcatc 300
ggatctaacg aaaacgaacc aaaactttgg tcccggttta acccaggaag ga 352
<210> 3
<211> 352
<212> DNA
<213> Artificial Sequence
<220>
<223> Мутантная последовательность промотора гена tkt
<400> 3
gattcgttcc gttcgtgacg ctttgtgagg ttttttgacg ttgcaccgta ttgcttgccg 60
aacatttttc ttttcctttc ggtttttcga gaattttcac ctacaaaagc ccacgtcaca 120
gctcccagac ttaagattga tcacaccttt gacacatttg aaccacagtt ggttataaaa 180
tgggttcaac atcactatgg ttagaggtgt tgacgggtca gattaagcaa agactacttt 240
cggggtagat cacctttgcc aaatttgaat gtggtatcat aagtcgtaga tctgatcatc 300
ggatctaacg aaaacgaacc aaaactttgg tcccggttta acccaggaag ga 352
<210> 4
<211> 26
<212> DNA
<213> Artificial Sequence
<220>
<223> Ptkt-1F
<400> 4
ggaattcccc tgggcttcgt tagcgc 26
<210> 5
<211> 42
<212> DNA
<213> Artificial Sequence
<220>
<223> Ptkt83-1-F2
<400> 5
cctttgccaa atttgaatgt gctgtcataa gtcgtagatc tg 42
<210> 6
<211> 42
<212> DNA
<213> Artificial Sequence
<220>
<223> Ptkt83-1-R1
<400> 6
cagatctacg acttatgaca gcacattcaa atttggcaaa gg 42
<210> 7
<211> 27
<212> DNA
<213> Artificial Sequence
<220>
<223> Ptkt-R2
<400> 7
gggatccctc acgacgagca gccatgg 27
<210> 8
<211> 42
<212> DNA
<213> Artificial Sequence
<220>
<223> Ptkt83-7-F2
<400> 8
cctttgccaa atttgaatgt ggtatcataa gtcgtagatc tg 42
<210> 9
<211> 42
<212> DNA
<213> Artificial Sequence
<220>
<223> Ptkt83-7-R1
<400> 9
cagatctacg acttatgata ccacattcaa atttggcaaa gg 42
<---
Изобретение относится к биотехнологии, в частности к промотору, микроорганизму Corynebacterium glutamicum, продуцирующему L-лизин и содержащему указанный промотор, и способу продуцирования L-лизина с использованием указанного микроорганизма. Изобретение обеспечивает продуцирование L-лизина с улучшенным выходом. 3 н. и 1 з.п. ф-лы, 2 ил., 4 табл., 4 пр.
1. Промотор, в котором нуклеотидная последовательность в областях от -83 до -74 промоторной последовательности гена, кодирующего транскетолазу, c SEQ ID NO: 1 заменена с ccaattaacc на tgtggtatca.
2. Микроорганизм Corynebacterium glutamicum, продуцирующий L-лизин, в котором нуклеотидная последовательность в областях от -83 до -74 промоторной последовательности гена, кодирующего транскетолазу, с SEQ ID NO: 1 заменена с ccaattaacc на tgtggtatca.
3. Микроорганизм Corynebacterium glutamicum по п. 2, содержащий нуклеотидную последовательность, представленную SEQ ID NO: 3.
4. Способ продуцирования L-лизина, включающий следующие стадии:
а) культивирование микроорганизма по п. 2 в среде; и
б) выделение L-лизина из данного микроорганизма или среды, в которой культивируется данный микроорганизм.
| KR 101504900 B1, 23.03.2015 | |||
| US 20200239897 A1, 30.07.2020 | |||
| US 20100015674 A1, 21.01.2010 | |||
| Способ получения L-лизина с использованием микроорганизмов, обладающих способностью продуцировать L-лизин | 2012 |
|
RU2615454C1 |
| TARUTINA M.G | |||
| ET AL | |||
| Assessment of effectiveness of Corynebacterium glutamicum promoters and their application for the enhancement of gene activity in lysine-producing bacteria | |||
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
Авторы
Даты
2024-11-05—Публикация
2021-05-28—Подача