Настоящее изобретение относится к электродному узлу и к электролизеру, в котором используется один или более таких узлов, в частности для использования в электролизе гидроксидов щелочных металлов.
Электрохимические процессы осуществляют в ячейках двух основных типов, в которых используется анод (положительный электрод), катод (отрицательный электрод) и подходящий электролит. На положительном электроде происходит реакция окисления, в которой высвобождаются электроны. Они проходят к отрицательному электроду, на котором происходит реакция восстановления. Реакции между электродами и электролитом зависят от химического состава ячейки. Иногда материалы электродов расходуются и превращаются из одной формы в другую. В других вариантах, например, которые используются при электролизе гидроксидов щелочных металлов, электроды действуют в качестве проводников электрического заряда, проходящего от выпрямителя в электролит, причем химический состав электродов не изменяется. Процесс совершается посредством миграции ионов в электролите от одного электрода к другому.
В гальваническом элементе (также указывается как химический источник тока) реакции происходят самопроизвольно для выработки электрической энергии. Это происходит, поскольку полезное преобразование реагирующих компонентов в конечные продукты сопровождается изменением отрицательной свободной энергии Гиббса. Величина вырабатываемой электрической энергии зависит от интенсивности реакции (тока) и разницы потенциалов (напряжения) между двумя электродами в элементе. Примеры таких устройств включают топливные элементы и электрические батареи.
В электролитической ячейке происходит положительное изменение свободной энергии Гиббса, и реакция не будет происходить самопроизвольно. Поэтому она должна приводиться в действие и поддерживаться источником питания постоянного тока. Примеры таких устройств включают щелочной электролизер и мембранный хлорщелочной электролизер.
По определению напряжение (V) и ток (I), вырабатываемые гальваническим элементом, указываются с положительным знаком, и вырабатываемая мощность равна V×I. В электролитических устройствах направление тока изменяется на обратное, и напряжение становится отрицательным.
В одной из других классификаций электрохимических устройств проводится различие между гальваническим и электролитическим процессами. Важным примером является перезаряжаемый элемент (аккумулятор). В этом устройстве в режиме выработки электрической энергии (указывается как разряд) разница потенциалов на ячейке положительная, и ток протекает в прямом направлении. В режиме потребления энергии (указывается как зарядка) знак разницы потенциалов меняется на обратный, и ток протекает в обратном направлении. Поэтому электроды в устройстве должны работать в режимах протекания тока в прямом и обратном направлениях без их повреждений, чтобы обеспечить возможность работы устройства на протяжении многих циклов зарядки-разрядки. Этот процесс осуществляется посредством обратимой химической реакции внутри модуля.
Электролизер принципиально сконструирован для работы с током, протекающим в прямом направлении. При разомкнутой цепи (ток не протекает) электроды будут достигать положения равновесного потенциала (типичного для обратимых реакций) вместе с равновесным напряжением на ячейке. Когда электролизер приведен в действие, ток протекает в прямом направлении, и формируются требуемые продукты, можно наблюдать, что напряжение резко возрастает (по определению с отрицательной полярностью). При этом потенциал анода повышается, в то время как потенциал катода уменьшается, и этот эффект называют поляризацией. Величина поляризации часто указывается как электрическое перенапряжение или избыточное напряжение. Электрод, который может выдерживать ток при большой величине перенапряжения, вызывает существенное увеличение потребляемой энергии на единицу получаемого продукта.
При устойчивой работе электролизера реагирующие компоненты непрерывно расходуются для формирования продуктов, так что подаваемые химические вещества и потребляемая электрическая энергия преобразуются в аккумулируемую химическую потенциальную энергию. Обычно получаемые химические продукты (аккумулирующие химическую потенциальную энергию) выводят из электролизера. Однако, когда электропитание электролизера выключают, любые продукты, которые остаются поблизости от электродов могут самопроизвольно реагировать, и тогда ячейка работает как гальваническое устройство, выдавая аккумулированную энергию. Когда это происходит, потенциал анода упадет ниже равновесного электродного потенциала, и одновременно потенциал катода поднимется выше этого потенциала, а ток будет проходить через ячейку в обратном направлении при условии, что между анодом и катодом имеется электрическое соединение. Если происходит значительная поляризация электродов при прохождении тока в обратном направлении, то это может повредить электроды, причем этот эффект накапливается, если случаи обратных токов будут часто повторяться.
Представление технических данных электролизеров в промышленности обычно изменяется в соответствии с этим правилом, и информация о напряжении на ячейке, представленная в настоящем описании как "отрицательная полярность", эквивалентна этому альтернативному правилу.
Настоящее изобретение в высокой степени полезно для применения в биполярных электролизерах, содержащих большое количество камер электролиза, расположенных последовательно, в которых при выключении возбуждаются большие обратные токи, могущие приводить к быстрому повреждению неподходящих покрытий катодов. Однако изобретение также полезно для применения в монополярном электролизе, в котором в процессе шунтирования электролизера для вывода его из эксплуатации перед техническим обслуживанием могут возбуждаться значительные обратные токи.
Было проведено много научно-исследовательских работ по снижению перенапряжения в таких системах. Эти работы включали использование электрокаталитических покрытий, нанесенных на электроды. Примеры электролизеров (в частности биполярных электролизеров) описаны, например, в документах GB 1581348 или US 6761808. Биполярные электролизеры для осуществления электролиза водных растворов хлоридов щелочных металлов и гидроксидов щелочных металлов для получения хлора и водорода могут содержать электродный модуль с анодом, выполненным подходящим образом в форме пластины или сетки из металла, формирующего пленку, обычно из титана, и с катодом, выполненным подходящим образом в форме перфорированной металлической пластины или сетки, обычно из никеля или мягкой стали. Один или оба электрода могут иметь электрокаталитическое покрытие. Анод и катод разделены сепаратором, обычно выполненным в форме мембраны, для формирования модуля.
В промышленном модульном электролизере группа (несколько) таких модулей расположена последовательно, причем анод биполярного модуля расположен рядом с катодом соседнего биполярного модуля и электрически соединен с ним. Другим типом биполярного электролизера является так называемый "фильтр-прессный электролизер, описанный, например, в документе GB 1595183. В этих электролизерах сформированы биполярные блоки электродов, содержащие анодное устройство и катодное устройство, которые электрически соединены друг с другом. Затем биполярные блоки электродов соединены с соседними биполярными блоками электродов посредством сепаратора и уплотнительных средств между фланцами соседних блоков, и блоки сжаты вместе для формирования фильтр-прессного электролизера. Биполярные электролизеры могут также использоваться для получения кислорода и водорода. В этом случае камеры анода и камеры катода могут содержать растворы гидроксида щелочного металла.
Примеры покрытий, наносимых на аноды для получения хлора в таких системах, описаны в заявках US 2011/024289, US 2014/224666 и US 2014/224667.
Однако настоящее изобретение относится к покрытиям, наносимым на катод, и в частности для использования в процессе электролиза гидроксида щелочного металла. Пример покрытия, наносимого на катод, можно найти в документе ЕР 0129374 В1, в котором описывается нанесение смеси металла группы платины и оксида металла группы платины на металлическую подложку, и в результате отмечается улучшение в части перенапряжения. Другой пример покрытия, наносимого на катод, приведен в заявке WO 01/28714. Как указывается в этом документе, металлические частицы покрывают либо электрокаталитическим металлом, либо дисперсионной фазой электрокаталитического металла в смеси с зернистым материалом для формирования каталитического порошка. Зернистый материал может быть выбран из различных материалов, содержащих оксиды металлов. Указывается, что каталитический порошок при его нанесении на катод в качестве покрытия, обеспечивает увеличение удельной площади поверхности и снижение перенапряжения.
Другой вариант описан в CN 107858701 А. В этом документе обеспечивается пористая подложка из титана, сформированная из частиц титана диаметром 20-50 микрон (20-50 мкм). От поверхности подложки наращивают вертикально ориентированные нанотрубки из оксида титана, и затем на них осаждают наночастицы благородного металла.
Сравнительно немного исследовательских работ было выполнено в области разработки покрытий электродов, способных выдерживать обратные токи. Примеры покрытия, нанесенного для получения газообразного водорода, приведены в документе ЕР 2539490 В1, в котором предложено несколько подходов для улучшения способности катода выдерживать обратные токи. Эти подходы включают использование солей нитратов металлов вместо хлоридов (в частности, нитрозилнитрата рутения) и введение устойчивых редкоземельных металлов, таких как празеодим, которые, как выяснилось, снижают негативное воздействие циклических изменений потенциала катода таким образом, который, как считали авторы, эквивалентен изменению направления тока в электролизере. В патенте US 5494560 указывается, что устойчивый катод с низким водородным перенапряжением может быть получен путем нанесения на подложку активного слоя электрода, содержащего никель и по меньшей мере один металл из платины, родия, иридия и палладия на активированном угле в качестве носителя. Однако все еще существует потребность в получении катодов, которые способны выдерживать обратные токи и одновременно имеют улучшенные характеристики в части перенапряжения.
Авторы обнаружили, что улучшенный катод может быть получен путем нанесения на него особого покрытия. Это покрытие не только обеспечивает низкое перенапряжение катода, но также обеспечивает катод стабильным перенапряжением в течение продолжительного времени работы. Катод может обеспечивать высокую способность выдерживать обратные токи. В частности, было найдено, что катоды по настоящему изобретению сохраняют стабильность в течение многократных циклов выключений и шунтирования ячейки. Стабильность катодов улучшает их характеристики и продляет срок службы.
Соответственно, в первом аспекте настоящего изобретения предлагается электродный узел для получения водорода, включающий:
i) анодное устройство, которое содержит анод, расположенный внутри электролитической камеры;
ii) катодное устройство, которое содержит катод, расположенный внутри электролитической камеры, содержащей раствор гидроксида щелочного металла,
отличающийся тем, что катод содержит:
а) электропроводную металлическую подложку; и
б) электрокаталитический слой на подложке, содержащий:
а. по меньшей мере один металл, выбранный из металлов группы платины, рения, никеля, кобальта и молибдена, и
б. по меньшей мере 50 об. % электропроводного материала носителя, который сформирован из частиц, средний размер которых не превышает 5 микрон (5 мкм), причем частицы сформированы не из металла (неметаллические частицы).
Катод содержит электропроводную металлическую подложку. Эта подложка может быть любой металлической подложкой, обычно применяемой в технике. Электропроводная металлическая подложка может представлять собой жесткую конструкцию, а именно, сформированную из перфорированной металлической пластины или из перфорированных металлических пластин, опционально решетчатых (щелевых). В других вариантах электропроводная металлическая подложка может быть в форме металлической ткани или сетки, такой как просечно-вытяжная сетка или тканая сетка. Типичные материалы для подложки включают нержавеющую сталь, мягкую сталь, никель или медь. Предпочтительным материалом является никель.
В настоящем изобретении на подложку наносят электрокаталитический слой.
Электрокаталитический слой содержит по меньшей мере один металл, выбранный из металлов группы платины, рения, никеля, кобальта и молибдена. Предпочтительно электрокаталитический слой содержит по меньшей мере один металл группы платины. Предпочтительными являются платина, палладий и рутений, причем может использоваться один из них или их смесь. В частности, предпочтительный электрокаталитический слой содержит рутений, используемый без добавок или в смеси с платиной и/или с палладием.
Следует отметить что "по меньшей мере один металл" в электрокаталитическом слое, по меньшей мере после осаждения, как это описано ниже, может быть в "металлической" форме (то есть, как элементарный металл) или может быть в форме соединения металла, такого как оксид. Например, рутений обычно формирует оксид при нагревании после осаждения в воздушной среде.
Количество указанного по меньшей мере одного металла, наносимого на электрод, зависит от металлов в покрытии и от их пропорций и выбирается для обеспечения оптимального баланса между продолжительным эксплуатационным ресурсом и способностью выдерживать обратные токи, уменьшенным напряжением на ячейке и стоимостью. Типичный электрокаталитический слой содержит указанный по меньшей мере один металл, выбранный из металлов группы платины, рения, никеля, кобальта и молибдена, в количестве 0,5-50 г/м2, выраженном в весе металла на единицу площади поверхности электропроводной подложки (определяемой геометрией площади поверхности, до нанесения покрытия). Предпочтительные величины варьируются в пределах указанного диапазона.
Например, для покрытий, содержащих металл группы платины, электрокаталитический слой предпочтительно содержит указанный по меньшей мере один металл, выбранный из группы платины, в количестве 0,5-20 г/м2, выраженном в весе металла группы платины на единицу площади поверхности электропроводной металлической подложки (до нанесения покрытия).
Более конкретно, для покрытий, содержащих платину, ее предпочтительное содержание находится в диапазоне 0,5-5 г/м2. Количество платины в указанном диапазоне обеспечивает приемлемый срок службы и допустимую стоимость. Слои, содержащие рутений, в которых содержатся меньшие количества других металлов (в молярном отношении), предпочтительно содержат рутений в количестве 2-15 г/м2. Рутений может использоваться без других металлов или в комбинации с ними, в частности с другими металлами группы платины. Например, если рутений и платина используются в молярном отношении 9:1 (Ru:Pt), то вес платины в покрытии составит 2,15 г/м2, когда вес рутения в покрытии составляет 10 г/м2. Слои, содержащие палладий, предпочтительно содержат его в количестве 0,5-5 г/м2. Палладий может использоваться без других металлов или в комбинации с ними, в частности с другими металлами группы платины. Например, если палладий и рутений используются в молярном отношении 9:1 (Ru:Pd), то вес палладия в покрытии составит 1,2 г/м2, когда вес рутения в покрытии составляет 10 г/м2.
Электрокаталитический слой содержит также по меньшей мере 50 об. % электропроводного материала носителя, сформированного из частиц, средний размер которых менее 5 микрон (5 мкм), причем частицы сформированы не из металла.
Материал носителя может быть оксидом металла или другим соединением металла или может быть неметаллическим материалом, таким как углеродный материал. Некоторые предпочтительные материалы указаны ниже. Вообще говоря, материал носителя должен быть стабильным химически и электрохимически в условиях работы электролизера и в условиях возникновения обратных токов. В частности, в процессе работы электролизера в материале носителя не должны происходить какие-либо химические или электрохимические изменения, которые существенно влияют на характеристики покрытия, включающего материал носителя, то есть, приводящие к ухудшению характеристик напряжения за короткий промежуток времени относительно нормального срока службы электрода (который обычно составляет несколько лет). Химическая и электрохимическая стабильность может быть определена путем анализа характеристик напряжения в подходящем испытании. Один из примеров подходящего испытания описан в Примерах документа ЕР 2539490 В1. В настоящем изобретении химическая и электрохимическая стабильность может быть определена предпочтительно с помощью испытания, описанного ниже в Примере 4. Испытание, описанное ниже подробно в Примере 4, проводится для большей части времени "нормальной" работы электролизера, то есть, в условиях прямого тока. Однако один раз в сутки анод и катод шунтируют для обеспечения обратного тока, прежде чем электролизер вернется к нормальному режиму работы. Этот цикл повторяют с мониторингом стабилизированного напряжения на ячейке в нормальном режиме работы. В этом случае обеспечивается возможность многократных выключений в течение сравнительно небольшого временного интервала для воспроизведения эффектов, которые обычно накапливаются в установке в течение нескольких лет эксплуатации. В настоящем изобретении материалы носителя считаются стабильными химически и электрохимически, если в этом испытании напряжение после 30 циклов повышается (отрицательно) менее чем на 100 мВ от начального напряжения. Предпочтительно напряжение повышается (отрицательно) после 30 циклов менее чем на 50 мВ от начального напряжения.
Одна из особенностей настоящего изобретения заключается в том, что электропроводный материал носителя формируют из частиц, средний размер которых не превышает 5 микрон (5 мкм). Предпочтительно электропроводный материал носителя формируют из частиц со средним размером менее 1 микрона (1 мкм) и даже более предпочтительно менее 0,5 микрона (500 нанометров), например, от 10 до 250 нанометров. В предпочтительных вариантах средний размер частиц находится в диапазоне от 20 до 100 нанометров.
Как это понимается в настоящей заявке, если осаждаемые частицы имеют сферическую или почти сферическую форму, то размер для каждой отдельной частицы это диаметр, усредненный по всем направлениям, то есть, диаметр сферы, имеющей эквивалентный объем. Однако нет необходимости в определении размера каждой частицы по отдельности, и средний размер используемых частиц может быть определен с помощью традиционных средств, таких как динамическое рассеяние света, электрофоретическое рассеяние света, лазерная дифракция, кондуктометрический анализ и осаждение.
В тех случаях, когда осаждаемые частицы имеют удлиненную форму, например, нанотрубки, размером частицы считается ее наибольший размер (в продольном направлении), и средний размер частиц может быть определен, соответственно, по этому размеру.
Например, в патенте US 5494560 размеры частиц углерода находятся в диапазоне от 10 до 100 микрон (10-100 мкм). Пример 1 в US 5494560 показывает, что в этом случае водородное перенапряжение составляет 70-80 мВ. Однако в настоящем изобретении обычно получают перенапряжения порядка 60 мВ и менее. Это показано в нижеприведенных Примерах.
В частности, не желая вдаваться в теорию, считается, что в процессе нанесения на подложку осаждаемых частиц формируется пористый слой с каналами между частицами, которые обеспечивают требуемую пористость и удельную площадь поверхности в электрокаталитическом слое. Пористость представляет собой трехмерную сеть каналов между осажденными частицами.
Более конкретно, предпочтительно средний диаметр (D50) каналов между частицами находится в диапазоне от 5 до 500 нм. В наиболее предпочтительном варианте по меньшей мере 50 % суммарного объема пор обеспечивается порами с диаметром в диапазоне от 5 до 500 нм. В этом варианте распределение объемов пор должно измеряться с помощью ртутной интрузионной порометрии в соответствии с ASTM D4284-12(2017) Е1 ("Методика стандартных испытаний для определения распределения объемов пор катализаторов и носителей катализаторов с помощью ртутной интрузионной порометрии").
Электропроводный материал носителя, особенно в тех случаях, когда этот материал представляет собой электропроводный углеродный материал, как это будет описано ниже, обычно имеет удельную площадь поверхности по меньшей мере 50 м2/г, такую как по меньшей мере 200 м2/г. Удельная площадь поверхности может достигать 2000 м2/г, предпочтительно 1500 м2/г, и наиболее предпочтительно от 200 до 1000 м2/г (удельная площадь поверхности должна измеряться в соответствии с ASTM D3663-03(2015): "Стандартная методика определения удельной площади поверхности для катализаторов и носителей катализ аторов").
Электрокаталитический слой обычно имеет толщину от 0,5 до 100 микрон (0,5-100 мкм), предпочтительно от 0,5 до 20 микрон (0,5-20 мкм). Предпочтительно на подложку наносят однородный слой, то есть, толщина слоя в любой точке находится в пределах 50 % от средней толщины. Покрытие наносят на переднюю, заднюю и внутренние поверхности электрода. Предпочтительно покрытие наносят путем напыления, опционально наносят несколько слоев, как это будет описано ниже.
В настоящем изобретении особенно важно, что частицы материала носителя являются электропроводными, однако это не металлические частицы. В частности, было обнаружено, что в условиях обратного тока электропроводность обеспечивает возможность рассеяния накопленного заряда. Однако, было обнаружено, что хотя металлические частицы являются электропроводными, но частицы некоторых широко используемых металлов, таких как никель или рутений, как правило, электрохимически неустойчивы. Такие металлы теряются из покрытия в результате их растворения при рассеянии накопленного заряда. При перезапуске процесса после выключения эффективность покрытия снижалась, когда такие металлические частицы использовались в качестве материала носителя. Например, было обнаружено, что использование в качестве носителей переходных металлов в форме частиц, таких как скелетный никелевый катализатор гидрирования, обеспечивает ограниченную стабильность напряжения, поскольку они со временем деактивируются, по мере того как гидрид внедряется в поверхность электродов. Кроме того, они предрасположены к пиролизу при контакте с воздухом в процессе технического обслуживания.
Не желая вдаваться в теорию, можно указать, что механизм повреждений, которые могут приводить к дальнейшей деактивации катодов, используемых при производстве хлора и щелочи, может возникать в процессе аварийных выключений ячеек как результат миграции ионов гипохлорита в раствор электролита прикатодной области, которая происходит под действием обратного тока. Затем восстановление гипохлорита на катоде приводит к окислению металла, как это описывается уравнением:
OCl- + Н2О + 2е → Cl- +2OH- (катодная реакция)
Μ → М2++2е (анодная реакция)
Материал электропроводного носителя предпочтительно имеет удельное электрическое сопротивление менее 10-3 Ом, например, от 10-3 до 10-4 Ом.
В одном из вариантов электропроводный материал носителя может быть электропроводным оксидом металла. Примеры таких материалов включают двухкомпонентные оксиды металлов, такие как оксиды титана (TiOx), оксиды вольфрама (WOx), оксиды молибдена (МоОх), оксиды церия (СеОх), оксиды лантана (La2O3) и оксид марганца (MnOx), оксид индия (In2O3), оксид гафния (HfO2), оксид тантала (Ta2O5) и многокомпонентные оксиды металлов, такие как группа перовскита (АВО3) и соединения из семейства оксидов пирохлора(A2B2O6). Другие примеры включают карбиды металлов, такие как карбид вольфрама.
Можно отметить, что некоторые материалы, которые могут быть использованы в качестве электропроводного материала носителя, могут быть оксидами металла, который может использоваться в качестве указанного компонента "по меньшей мере одного металла" электрокаталитического слоя. В этом случае четко различимы два компонента, которые должны присутствовать. В частности, электропроводный материал носителя должен присутствовать в количестве по меньшей мере 50 об. % электрокаталитического слоя и должен быть сформирован из частиц, имеющих заданный максимальный размер. Указанный "по меньшей мере один металл" должен быть нанесен на электропроводный материал носителя. Таким образом, два компонента представляют собой четко различимые компоненты даже в том случае, когда они сформированы из материалов, которые являются химически родственными.
Предпочтительно электропроводный материал носителя содержит электропроводный углеродный материал. Типичные углеродные материалы включают углеродную сажу, графит, ацетиленовую сажу, графен, одностенные углеродные нанотрубки и многостенные углеродные нанотрубки. Конкретные примеры подходящих углеродных материалов включают материалы, продаваемые фирмой Cabot Corporation (США) под торговым наименованием Vulcan XC-72R или Black Pearls 2000, или материалы Ketjenblack EC600JD или EC300JD, предлагаемые фирмой Lion Specialty Chemicals Co. Ltd (Япония). Углеродный материал может использоваться в качестве электропроводного материала носителя без каких-либо добавок или с другими углеродными материалами, или же один или несколько углеродных материалов могут быть смешаны с одним или с несколькими оксидами металлов, такими как оксид празеодима, оксид неодима, или с одним или с несколькими электропроводными оксидами металлов, выбранными из вышеприведенного перечня электропроводных оксидов металлов.
Если в качестве электропроводного материала носителя используется углеродная сажа, то необходимо отметить, что процесс горения, используемый для получения углеродной сажи, производит так называемые "первичные частицы" углерода, средний размер которых зависит от подаваемого сырья и режима горения, но обычно он не превышает 500 нм. Благодаря их малым размерам и высокой удельной площади поверхности эти первичные частицы будут слипаться под действием сил Ван-дер-Ваальса с формированием агломератов, размеры которых находятся в диапазоне от 0,1 до 50 микрон (0,1-50 мкм). Размеры агломератов предпочтительно могут быть от 0,1 до 20 микрон (0,1-20 мкм). Однако, в настоящей заявке указание электропроводного материала носителя, формируемого из частиц, имеющих средний размер менее определенной величины (например, менее 5 микрон (5 мкм)), в этих случаях относится к размеру первичных частиц, а не к размеру агломератов, которые могут формироваться.
В настоящем изобретении электрокаталитический слой содержит по меньшей мере 50 об. % электропроводного материала носителя, то есть по меньшей мере 50 об. % или большая часть объема слоя состоит из материала носителя. Предпочтительно электрокаталитический слой содержит по меньшей мере 55 об. %, предпочтительно по меньшей мере 60 об. %, более предпочтительно по меньшей мере 80 об. % и наиболее предпочтительно по меньшей мере 90 об. % электропроводного материала носителя (то есть, предпочтительно по меньшей мере 55 об. %, предпочтительно по меньшей мере 60 об. %, более предпочтительно по меньшей мере 80 об. % и наиболее предпочтительно по меньшей мере 90 об. % электропроводного электрокаталитического слоя составляет электропроводный материал носителя).
В дополнение к электропроводному материалу носителя электрокаталитический слой также содержит по меньшей мере один металл, выбранный из металлов группы платины, рения, никеля, кобальта и молибдена (эти металлы далее указываются как "электрокаталитические металлы"). Обычно эти металлы присутствуют в количестве от 0,1 об. % до остальной части слоя и предпочтительно в количестве от 0,2 об. % до остальной части слоя. Таким образом, электрокаталитический слой содержит электрокаталитические металлы в количестве менее 50 об. %, предпочтительно менее 45 об. %, предпочтительно менее 40 об. %, более предпочтительно менее 20 об. % и наиболее предпочтительно менее 10 об. % (то есть, менее 50 об. %, предпочтительно менее 45 об. %, предпочтительно менее 40 об. %, более предпочтительно менее 20 об. % и наиболее предпочтительно менее 10 об. % электрокаталитического слоя составляют электрокаталитические металлы).
Наиболее предпочтительно электрокаталитический слой содержит от 0,2 до 10 об. % указанного по меньшей мере одного металла, выбранного из металлов группы платины, рения, никеля, кобальта и молибдена, и от 90 до 99,8 об. % электропроводного материала носителя.
Количества указанного по меньшей мере одного электрокаталитического металла и электропроводного материала носителя, выраженные в молях, зависят от относительных плотностей соответствующих материалов. Если в качестве электропроводного материала носителя используется электропроводный углеродный материал, то электрокаталитический слой обычно содержит от 40 до 80 мол. % указанного по меньшей мере одного электрокаталитического металла и от 60 до 20 мол. % электропроводного материала носителя.
В документе WO 01/28714 либо покрытие содержит исключительно электрокаталитический металл, либо электрокаталитический металл представляет собой дисперсионную фазу, в которой находятся частицы оксида металла. В настоящем изобретении частицы носителя выбирают таким образом, чтобы они были электропроводными и составляли основную часть покрытия, причем они являются носителями указанного по меньшей одного электрокаталитического металла. Достоинство такого решения заключается в том, что площадь активной поверхности на один грамм указанного по меньшей мере одного электрокаталитического металла существенно выше, что приводит к меньшему перенапряжению катода, повышенной нечувствительности к примесям и обеспечивает возможность уменьшения количества указанного по меньшей мере одного электрокаталитического металла, необходимого для обеспечения эквивалентной каталитической активности, и, соответственно, снижения стоимости.
В настоящем изобретении указанный по меньшей мере один электрокаталитический металл может быть нанесен на электропроводный материал носителя в электрокаталитическом слое с использованием любого подходящего способа.
Предпочтительно материал, в котором по меньшей мере один электрокаталитический металл нанесен на электропроводный материал носителя, обеспечивается до нанесения покрытия. Например, такие материалы могут быть приобретены предварительно сформированными или изготовленными до нанесения покрытия. Однако также можно обеспечивать физическую смесь электрокаталитического металла (или металлов) и электропроводного материала носителя и наносить смесь на подложку, так что указанный по меньшей мере один электрокаталитический металл будет размещен на носителе только в процессе нанесения покрытия.
Электрокаталитический металл может присутствовать на поверхности электропроводного носителя в форме сплошного слоя, или же он может быть рассеян на электропроводном носителе в форме частиц.
В общем случае (включая обеспечение электрокаталитического металла на электропроводном материале носителя перед осаждением/нанесением покрытия или его обеспечение отдельно в процессе осаждения/нанесения покрытия), когда электрокаталитический металл присутствует в форме частиц, средний размер осаждаемых частиц электрокаталитического металла обычно существенно меньше среднего размера частиц электропроводного материала носителя, используемого в электрокаталитическом слое. Обычно средний размер осаждаемых частиц электрокаталитического металла меньше 20 % среднего размера частиц электрокаталитического материала носителя, используемого в электрокаталитическом слое.
В настоящем изобретении электропроводный материал носителя формируют из частиц, средний размер которых не превышает 5 микрон (5 мкм). Таким образом, как максимум средний размер осаждаемых частиц электрокаталитического металла должен быть менее 1 микрона (1 мкм). Обычно средний размер частиц будет существенно меньшей указанной величины. Предпочтительно осаждаемые частицы электрокаталитического металла имеют средний размер менее 0,2 микрона (200 нанометров) и даже более предпочтительно менее 0,1 микрона (100 нанометров), например, в диапазоне от 2 до 50 нанометров. В предпочтительных вариантах средний размер частиц находится в диапазоне от 2 до 20 нанометров.
В более общем смысле электрокаталитический слой, содержащий указанный по меньшей мере один металл, нанесенный на электропроводный материал носителя, формируют на электропроводной металлической подложке предпочтительно путем осаждения на подложке
i. частиц электропроводного материала носителя, средний размер частиц которого меньше 5 микрон (5 мкм), и
ii. частиц по меньшей мере одного металла, выбранного из металлов группы платины, рения, никеля, кобальта и молибдена, причем средний размер частиц меньше 20 % среднего размера частиц электропроводного материала носителя.
Следует отметить, что частицы указанного по меньшей мере одного металла могут уже находиться, и предпочтительно находятся, на частицах электропроводного материала носителя перед осаждением на подложку, как это уже указывалось.
В более общем смысле нанесение электрокаталитического слоя на электропроводную металлическую подложку может осуществляться с помощью любой подходящей технологии, включая технологии, описанные в технике для других, например для анодных, применений. (В том числе источники, в которых описываются уже упомянутые в настоящем описании анодные и катодные покрытия). Обычно формируют "краску" и используют ее для нанесения покрытия. Соответствующий способ формирования такой краски зависит от формы используемых материалов и от выбранного способа ее нанесения на электрод, однако такие технологии широко применяются и хорошо известны специалистам в данной области техники. Например, краска может быть сформирована путем растворения одного или нескольких соединений-прекурсоров металлов в подходящем растворе, к которому добавляют нерастворимый материал носителя и который после этого превращается в дисперсию. Если металл уже нанесен на носитель, то дисперсия материала может быть сформирована без отдельной операции растворения соединений металлов. Могут быть введены другие добавки, такие как реологические модификаторы, для стабилизации дисперсии или улучшения ее вязкости для нанесения, как это известно специалистам в данной области техники. Кроме того, может быть добавлено связующее вещество в тех случаях, когда металл уже нанесен на углеродный материал, для улучшения адгезии внутри слоя и к электродной подложке.
Покрытие может быть нанесено на подложку с использованием любого подходящего способа нанесения покрытий. Примеры таких способов включают покрытие погружением и нанесение покрытия кистью Предпочтительным способом, особенно в промышленном производстве, является нанесение покрытия распылением. Электрокаталитический слой предпочтительно наносят на подложку в несколько проходов (многослойное покрытие). При использовании многослойного покрытия обеспечиваются более однородные, более плотные слои, не имеющие трещин, и наиболее эффективное покрытие всей площади подложки (поскольку в случае нескольких слоев уменьшается вероятность пропуска каких-либо участков). Обычно может быть нанесено от 2 до 20 слоев.
Однако обычно каждый нанесенный слой высушивают перед нанесением следующего слоя покрытия. Температура сушки зависит от технологии нанесения покрытия и в частности от используемых растворителей или растворов, однако обычно сушку выполняют при температуре 100-200°С в течение 1-10 минут. В зависимости от технологии нанесения покрытия может быть также полезно нагревать покрытие до более высоких температур между нанесением слоев. В некоторых вариантах может использоваться нагрев до температур 300-500°С в течение 10-30 минут, хотя это зависит также технологии нанесения покрытия, и могут также использоваться температуры и временные интервалы за пределами указанных диапазонов. Некоторые конкретные величины указаны в Примерах, приведенных в настоящем описании. Вообще говоря, возможные способы нанесения покрытий на электроды известны в технике, и используемые температуры и режимы могут быть определены специалистом в данной области техники в зависимости от технологии нанесения покрытия.
Электропроводная металлическая подложка может быть обработана, физически или химически, для улучшения адгезии электрокаталитического слоя. Например, подложка может быть подвергнута дробеструйной (пескоструйной) обработке, химическому травлению или им подобной обработке перед нанесением покрытия, чтобы поверхность стала более шероховатой.
В некоторых вариантах осуществления настоящего изобретения между электропроводной металлической подложкой и электрокаталитическим слоем может быть обеспечен слой химического соединения. Например, на электропроводную металлическую подложку может быть нанесен слой связующего вещества перед нанесением электрокаталитического слоя. Под "слоем связующего вещества" в настоящей заявке понимается слой химического соединения, которое улучшает сцепление электрокаталитического слоя с электропроводной металлической подложкой.
В других вариантах связующие вещества не добавляют перед нанесением электрокаталитического слоя, а вместо этого их наносят вместе с электрокаталитическим слоем. В этом случае связующее вещество, такое как политетрафторэтилен (ПТФЭ) или ионсодержащий полимер, добавляют в дисперсию покрытия, содержащую:
а. по меньшей мере один металл, выбранный из металлов группы платины, рения, никеля, кобальта и молибдена, и
б. по меньшей мере 50 об. % электропроводного материала носителя, и эту смесь наносят в качестве покрытия.
Обычно электрокаталитические слои, содержащие связующие вещества, обрабатывают при температуре, достаточной для спекания связующего вещества, в результате чего улучшается адгезия электрокаталитического слоя.
В некоторых вариантах осуществления настоящего изобретения на подложку могут быть последовательно осаждены два или более электрокаталитических слоев, причем каждый слой содержит:
а. по меньшей мере один металл, выбранный из металлов группы платины, рения, никеля, кобальта и молибдена, и
б. по меньшей мере 50 об. % электропроводного материала носителя,
как указывалось в описании, но осаждаемые слои отличаются по составу, например, отличается один или несколько используемых металлов или материал носителя.
Первый слой может использоваться для улучшения адгезии последующего слоя или последующих слоев. Будет очевидно, что такие слои могут также рассматриваться как "связующие слои", как это указывалось выше. Однако для целей настоящего описания в тексте они будут указываться как "грунтовочные слои", когда они также содержат металл и материалы носителя, как это указывалось выше.
Если используется грунтовочный слой, то обычно каждый слой может быть сформирован нанесением нескольких покрытий, имеющих требуемый состав, например, независимым нанесением 2-10 покрытий каждого состава. Если используется грунтовочный слой, то предпочтительно наносят два электрокаталитических слоя, грунтовочный слой и наносимый на него второй или "верхний" слой.
За исключением электрокаталитического слоя на катоде электродный узел для получения водорода в соответствии с настоящим изобретением может иметь традиционную конструкцию. Пример предпочтительной конструкции описан в вышеупомянутом документе US 6761808 В1.
В процессе работы камеры анода и катода будут содержать электролизуемый раствор. (Термин "камера" относится к части анодного или катодного устройства, которая содержит анод или катод и электролизуемый раствор). В процессе работы узел по настоящему изобретению может использоваться для любого процесса, в котором в камере катода электродного узла находится гидроксид щелочного металла.
В одном из вариантов электродный узел может использоваться для получения водорода и галогена. В этом случае камера анода содержит раствор галида щелочного металла, который электролизуют для получения галогена. Предпочтительно в качестве галида щелочного металла используется хлорид, предпочтительно хлорид натрия. Предпочтительным гидроксидом щелочного металла является гидроксид натрия. Хорошо известны электрохимические ячейки для получения галогенов и водорода, такие как ячейки, описанные в уже упомянутом документе US 6761808 В1.
В другом варианте электродный узел может использоваться для получения водорода и кислорода. В этом случае камера анода также содержит раствор гидроксида щелочного металла, который электролизуют для получения кислорода. Предпочтительно в качестве гидроксида щелочного металла в обеих камерах используется гидроксид калия или натрия. Хорошо известны также электрохимические ячейки для получения кислорода и водорода, в которых используется электролиз щелочной воды. Можно указать такие информационные источники, как "Успехи в технологиях производства водорода - Глава 1, Производство водорода путем электролиза воды", авторы Youssef Naimi и Amal Antar - Часть 4. (Опубликовано IntechOpen в Интернете).
Электродный узел по настоящему изобретению включает анодное устройство, содержащее анод, расположенный в камере электролиза, и катодное устройство, содержащее катод, расположенный в камере электролиза.
На практике электродный узел будет использоваться в модульном или в фильтр-прессном электролизере, содержащем группу соединенных между собой электродных узлов.
Более конкретно, термин "электродный узел", как он используется в настоящей заявке, охватывает как монополярные узлы, так и биполярные узлы, причем последние являются биполярными электродными блоками или биполярными электродными модулями, в зависимости от схемы соединения анодного и катодного устройств.
В частности, "биполярный электродный блок" представляет собой электродный узел, содержащий анодное устройство и катодное устройство, которые электрически соединены друг с другом. Биполярные электродные блоки могут быть соединены с соседними биполярными электродными блоками с помощью сепаратора и уплотнительных средств между фланцами на соседних блоках для формирования фильтр-прессного электролизера.
"Электродный модуль" представляет собой электродный узел, содержащий анодное устройство и катодное устройство, которые разделены сепаратором, установленным между соответствующими фланцами. Электродный модуль снабжен уплотнительными средствами для обеспечения непроницаемости для жидкостей и газов между сепаратором и соответствующими фланцами. Электродные модули могут быть электрически соединены с соседними электродными модулями для формирования модульного электролизера.
Таким образом, во втором аспекте обеспечивается модульный или фильтр-прессный электролизер, содержащий множество вышеописанных электродных узлов. Обычно модульный или фильтр-прессный электролизер содержит от 5 до 300 электродных узлов.
Дополнительную информацию по биполярным электродным узлам, электродным модулям, модульным или фильтр-прессным электролизерам можно найти в различных технических публикациях, таких как WO 2016169813 A1.
В третьем аспекте обеспечивается способ электролиза, который включает осуществление электролиза в электродном узле или в вышеописанном модульном или фильтр-прессном электролизере для производства водорода.
Дополнительную информацию по работе таких систем можно также найти в различных технических публикациях, таких как WO 2016169813 A1. Обычно электролизеры, производящие водород, например щелочноводные электролизеры, могут работать при давлениях в диапазоне от 50 до 15000 кПа абс. (от 0,5 до 150 бар), предпочтительно от 50 до 500 кПа абс. (от 0,5 до 50 бар). Если электролизер является модульным или фильтр-прессным хлорщелочным электролизером, то он обычно работает при давлениях от 50 до 600 кПа абс. (от 0,5 до 6 бар), предпочтительно от 50 до 180 кПа абс. (от 500 до 1800 мбар).
Жидкость, подлежащая электролизу, подается в подводящие трубы конструкции каждого электрода. Например, подводящие трубы обеспечивают возможность подачи гидроксида щелочного металла в катодное устройство и нужного раствора в анодное устройство. Продукты процесса хлорщелочного электролиза, например хлор и обедненный соляной раствор из анодного устройства, а также водород и гидроксид щелочного металла из катодного устройства, выводятся из соответствующих коллекторов.
Процесс в хлорщелочном электролизере может осуществляться с высокой плотностью тока, например >6кА/м2.
Как уже отмечалось, было обнаружено, что покрытие в соответствии с настоящим изобретением обеспечивает низкое перенапряжение катода, катод со стабильным перенапряжением в течение продолжительного времени эксплуатации и высокую степень способности выдерживать обратные токи.
Таким образом, в четвертом аспекте настоящего изобретения предлагается применение электрокаталитического слоя на электроде, который содержит:
а) электропроводную металлическую подложку; и
б) электрокаталитический слой на подложке, содержащий:
а. по меньшей мере один металл, выбранный из металлов группы платины, рения, никеля, кобальта и молибдена, и
б. по меньшей мере 50 об. % электропроводного материала носителя, причем электропроводный материал носителя сформирован из частиц со средним размером менее 5 микрон (5 мкм), которые не являются металлическими частицами,
для обеспечения по меньшей мере одного из нижеперечисленного:
i) уменьшенное перенапряжение электрода,
ii) перенапряжение электрода, которое является стабильным в течение продолжительного времени эксплуатации, и
iii) повышенная способность электрода выдерживать обратные токи.
В этом четвертом аспекте применение электрокаталитического слоя предпочтительно обеспечивает по меньшей мере два, предпочтительно все три из нижеперечисленного:
i) уменьшенное перенапряжение электрода,
ii) перенапряжение электрода, которой является стабильным в течение продолжительного времени эксплуатации, и
iii) улучшенная способность электрода выдерживать обратные токи.
В частности, предпочтительно, чтобы использование электрокаталитического слоя обеспечивало уменьшенное перенапряжение электрода, перенапряжение электрода, которое является стабильным в течение продолжительного времени эксплуатации, и, более предпочтительно, также улучшенную способность электрода выдерживать обратные токи.
Предпочтительно электрод представляет собой катод в процессе производства водорода, выводимого с этого катода. Более предпочтительно процесс представляет собой производство водорода из гидроксида щелочного металла на катоде и либо (1) галогена из галида щелочного металла, либо (2) кислорода из гидроксида щелочного металла на аноде.
Наконец, в пятом аспекте настоящее изобретение предлагается способ, включающий:
i) изготовление электрода, содержащего:
а) электропроводную металлическую подложку; и
б) электрокаталитический слой на подложке, содержащий:
а. по меньшей мере один металл, выбранный из металлов группы платины, рения, никеля, кобальта и молибдена, и
б. по меньшей мере 50 об. % электропроводного материала носителя, который сформирован из частиц, средний размер которых менее 5 микрон (5 мкм), причем частицы сформированы не из металла.
и
ii) обеспечение электрода для использования в качестве катода в процессе электролиза гидроксида щелочного металла для получения водорода.
Электрод может быть изготовлен с использованием любого известного способа, включая вышеописанные способы.
Термин "обеспечение", как он используется в настоящей заявке, может относиться к продаже электрода для его использования в качестве катода. Обеспечение может включать экспорт электрода из страны его производства.
Процесс электролиза гидроксида щелочного металла для производства водорода предпочтительно представляет собой производство водорода, получаемого на катоде, и либо (1) галогена из галида щелочного металла, либо (2) кислорода из гидроксида щелочного металла на аноде. Такие процессы уже были описаны.
Настоящее изобретение будет проиллюстрировано со ссылками на нижеприведенные Примеры.
Примеры
Для ясности, нижеприведенные примеры включают ряд композиций покрытий, которые наносят на различные конструкции электродов, изготовленные из никеля, причем их выбор определяется с помощью испытательной ячейки, в которую эти электроды устанавливают для оценки. Как правило, каждую соответствующую композицию покрытия наносят на каждый соответствующий тип никелевого электрода до эквивалентного уровня покрытия. Специалистам в области нанесения покрытий на электроды также очевидно, что покрытия, нанесенные вручную, например покрытия, наносимые с помощью кисти, и покрытия, наносимые распылением, дают эквивалентный результат, и нижеприведенные Примеры демонстрируют это.
Также следует учитывать, что электрохимические испытания осуществляли для различных конструкций ячеек электролизеров, в которых используются различные никелевые электроды с нанесенным покрытием, как это обычно делают для определения различных аспектов работы покрытий электродов. Данные испытаний сравнивали с контрпримерами покрытий, нанесенных на идентичные никелевые электроды, которые испытывали в таких же конфигурациях ячеек и в таких же рабочих условиях. Ниже описаны различные конструкции электродов, использованных в испытаниях:
а. Испытания в отношении потенциала отдельного электрода (SEP, от англ. Single Electrode Potential) проводили с образцами покрытия, наносимого на сплошные круговые диски площадью 1,65 см2 и толщиной 1 мм (указывается как электрод "Типа А") в стандартном испытании для быстрого определения электрокинетической активности покрытий (несколько испытаний в сутки, дополнительные подробности приведены ниже).
б. В полномасштабных испытаниях электролизера FM21™ использовался катод, который представлял собой щелевую никелевую пластину высотой 22 см и шириной 95 см, и площадь поверхности мембраны и электрода составляла примерно 0,21 м2. Размеры вертикальных никелевых решеток составляли 220 мм (высота) × 2 мм (ширина) × 2 мм (глубина), и расстояния между решетками было равно 2 мм (указывается как электрод "Типа В"). Анод представлял собой щелевую титановую пластину, размеры которой были идентичны размерам катода. Более подробное описание конструкции электродов и электролизера приведено в патенте US 4824542.
в. Полномасштабные испытания электролизера BICHLOR™ осуществляли на площади 2,895 м2 (площадь мембраны) с просечно-вытяжной сеткой толщиной 1 мм с покрытием (указывается как электрод "Типа С"). Эти испытания использовали для оценки работы покрытия в условиях работы реального оборудования (продолжительность испытания от нескольких месяцев до нескольких лет, дополнительные подробности приведены ниже).
г. Опытно-промышленные испытания в уменьшенном масштабе осуществляли на площади 100 см2 (площадь мембраны) с использованием просечно-вытяжной сеткой толщиной 0,15 мм с покрытием (указывается как электрод "Типа D"). Это стандартные испытания, используемые для определения влияния выключений с шунтированием, проводимых для определения способности покрытия катода выдерживать обратные токи (продолжительность испытаний - 20-30 суток, дополнительные подробности приведены ниже).
1. Испытания в части потенциала отдельного электрода
1.1 Постановка эксперимента
В этих Примерах сравнивали электрохимические характеристики покрытий. В испытаниях использовали конструкцию электрохимической ячейки, которая обычно использовалась для получения характеристик покрытий специалистами в данной области техники.
Использовался испытательный электрод Типа А с интегрированной стойкой шириной 2 мм, отходящей от края, для обеспечения возможности соединения с титановым держателем электрода ячейки с помощью титанового винта.
Электроды изготавливали из просечно-вытяжных металлических листов, которые подвергали пескоструйной обработке плавленым глиноземом для придания шероховатости поверхности, чтобы улучшить адгезию покрытия, с последующей ультразвуковой очисткой в деминерализованной воде. После нанесения покрытия на лист из него вырезали электроды для использования в электрохимической ячейке.
Работу ячейки осуществляли с 32 % NaOH при температуре 85°С, и платиновый сетчатый противоэлектрод и контрольный обратимый водородный электрод, который обеспечивал стабильный эталонный потенциал 0,000 В во время испытаний, использовали для обеспечения трехэлектродной конфигурации, обычно используемой для проведения таких испытаний. Интенсивность реакции, в которой выделялся водород, определяли измерением потенциала испытываемого электрода относительно контрольного электрода при плотности тока 3 кА/м2 в течение времени стабильности измеряемой характеристики (до 5 часов). Данные измерений корректировали для учета электролитического сопротивления путем одновременного измерения импеданса ячейки.
1.2 Композиции
Сравнительный пример 1А
Этот электрод (Тип А) представлял собой никелевый электрод без покрытия, подвергнутый пескоструйной обработке.
Сравнительный пример 2А
Краску получали путем разбавления исходного раствора дигидрогексахлорплатиновой кислоты (150 г/л в 20 % HCl) безводной уксусной кислотой для обеспечения конечной концентрации порядка 22 г/л. Эту краску распыляли в несколько слоев на электрод, предварительно подвергнутый пескоструйной обработке, с промежуточной сушкой в течение 2 минут при температуре 180°С и с термической обработкой в воздушной среде между нанесениями слоев в течение 12 минут при температуре 480°С для преобразования краски в смесь металлической платины и оксида платины. Процесс нанесения покрытия повторяли до тех пор, пока содержание платины в покрытии, измеряемое откалиброванным рентгенолюминесцентным спектрометром, не достигало 3-4 г/м2. 3-4 г/м2 - это типичное содержание платины в покрытии, используемом в промышленных применениях, для обеспечения продолжительного срока службы. Вообще говоря, в непродолжительных испытаниях, как в описываемых Примерах, исходное перенапряжение не очень сильно зависело от точного содержания платины при условии однородности покрытия поверхности электрода.
Сравнительный пример 3А
Краску, содержащую платину, получали так же, как и в сравнительном Примере 2А. Затем эту краску модифицировали путем добавления кристаллов хлорида рутения (III), полностью растворяющихся в результате интенсивного перемешивания, в количестве, достаточном для обеспечения молярного состава 4,66:1 Pt:Ru (90 вес. % Pt, 10 вес. % Ru).
Эту краску распыляли несколькими слоями на электрод (Тип А), предварительно подвергнутый пескоструйной обработке, с промежуточной сушкой в течение 2 минут при температуре 180°С и с термической обработкой в воздушной среде между нанесениями слоев в течение 12 минут при температуре 480°С для преобразования краски в смесь металлической платины, оксида платины и оксида рутения. Процесс нанесения покрытия повторяли до тех пор, пока содержание платины в покрытии, измеряемое откалиброванным рентгенолюминесцентным спектрометром, не достигало 3-4 г/м2.
Сравнительный пример 4А
Краску получали путем полного растворения кристаллов хлорида рутения (III) в безводной уксусной кислоте с использованием ультразвуковых волн до концентрации рутения 50 г/л.
Эту краску распыляли несколькими слоями на электрод (Тип А), предварительно подвергнутый пескоструйной обработке, с промежуточной сушкой в течение 2 минут при температуре 180°С и с термической обработкой в воздушной среде между нанесениями слоев в течение 12 минут при температуре 450°С для преобразования краски в оксид рутения. Процесс нанесения покрытия повторяли до тех пор, пока содержание рутения в покрытии, измеряемое откалиброванным рентгенолюминесцентным спектрометром, не достигало 10-12 г/м2.
10-12 г/м2 - это типичное содержание рутения в покрытии электродов, используемом в промышленных применениях, для обеспечения продолжительного срока службы. Вообще говоря, в непродолжительных испытаниях, как в описываемых Примерах, исходное перенапряжение не очень сильно зависело от точного содержания рутения при условии однородности покрытия поверхности электрода. Содержание Ru обычно выше содержания Pt, дающего сравнимый результат в промышленных применениях, поскольку покрытия с Ru изнашиваются быстрее, чем покрытия с Pt.
Пример 5А
В этом Примере использовался электрод с электрокаталитическим слоем, содержащим углерод и рутений. В этом случае осуществляли совместное осаждение углеродного материала и рутения.
Для получения краски сначала растворяли кристаллы хлорида рутения (III) в безводной уксусной кислоте до концентрации рутения 33 г/л с использованием ультразвуковых волн в течение по меньшей мере 10 минут. Затем добавляли порошок углеродной сажи (Cabot Vulcan XC-72R) в концентрации углерода 7,84 г/л и подвергали полученный материал действию ультразвуковых волн в течение по меньшей мере 30 минут для получения густой суспензии.
Полученная композиция содержала 2:1 C:Ru в молярном соотношении (80,8 вес. % Ru, 19,20 вес. % С). Эту краску распыляли несколькими слоями на электрод (Тип А), предварительно подвергнутый пескоструйной обработке, с промежуточной сушкой в течение 2 минут при температуре 180°С и с термической обработкой в воздушной среде между нанесениями слоев в течение 12 минут при температуре 350°С для преобразования краски в покрытие с аморфным оксидом рутения на углеродном носителе. Процесс нанесения покрытия повторяли до тех пор, пока содержание рутения в покрытии, измеряемое откалиброванным рентгенолюминесцентным спектрометром, не достигало 10-12 г/м2.
Пример 6А
В этом Примере использовался электрод с электрокаталитическим слоем, содержащим углерод, платину и рутений. Покрытие наносили в форме двух слоев.
Первый слой содержал С и Ru, и его наносили на электрод (Тип А), предварительно подвергнутый пескоструйной обработке, три раза с использованием краски и процессов нанесения покрытия и сушки как в Примере 5А за исключением того, что термическую обработку между нанесениями покрытия осуществляли при температуре 450°С.
После этого расчетное содержание Ru в покрытии составляло 3 г/м2.
Первый слой служил в качестве грунтовочного покрытия для улучшения адгезии к электроду второго слоя.
Второй слой наносили сверху первого слоя, используя другую краску. В частности, 1 г коммерческого платинового катализатора на углеродном носителе (Alfa Aesar HiSpec 4000, содержащий 40 вес. % платины, нанесенной предварительно на углеродную сажу Vulcan XC-72R) был загружен в подходящую емкость. Затем в нее добавляли 20 см3 деминерализованной воды с комнатной температурой, и получали суспензию при перемешивании с малыми сдвиговыми усилиями в течение 10 минут с помощью лабораторной магнитной мешалки с пластиной и перемешивающим стержнем. В полученную суспензию добавляли эмульсию политетрафторэтилена (Asahi Glass AD309E с 59,8 % ПТФЭ) в качестве связующего вещества в количестве, обеспечивающем эквивалентное содержание сухого PTFE в количестве 0,12 г, эквивалентное 20 вес. % углерода.
Затем суспензию перемешивали с высокой скоростью лабораторной мешалкой в течение 20 минут перед тем, как рН понижали примерно до 2 путем добавления 1 моля H2SO4 для обеспечения флокуляции. Затем полученную взвесь перемешивали в течение 10 минут с последующей гравитационной фильтрацией и промывкой 200 мл деминерализованной воды для снижения повышенной кислотности.
Полученный отфильтрованный осадок высушивали в течение 2 часов в печи в воздушной среде при температуре 80°С для удаления большей части содержащейся влаги. Полученный твердый материал помещали в подходящую емкость и дробили с помощью лопатки до консистенции панировочных сухарей. Затем добавляли 10 мл 2 % метилцеллюлозного геля, который действовал в качестве реологического модификатора в полученной краске. Гель получали отдельно путем растворения метилцеллюлозного порошка (Alfa Aesar, вязкость 400 сП) в деминерализованной воде с последующей гомогенизацией с помощью мешалки с высокими сдвигающими усилиями (Silverson L5, с эмульгирующим экраном) до растворения порошка и формирования геля.
Затем смесь отфильтрованного осадка и геля перемешивали в течение 10 минут, используя смеситель с высокими сдвиговыми усилиями (Silverson L5, с универсальной измельчительной головкой), пока не наблюдалось резкое снижение вязкости, и краска превращалась в свободнотекучую среду, подобную ньютоновской жидкости, подходящую для нанесения покрытия. Полученную таким образом краску наносили кистью на электроды, предварительно покрытые первым слоем. Покрытие наносили три раза с промежуточной сушкой в течение 5 минут при температуре 100°С, в результате чего содержание платины, измеряемое откалиброванным рентгенолюминесцентным спектрометром, достигало 3-4 г/м2.
После нанесения покрытия в третий раз электрод помещали между листами фильтровальной бумаги и сжимали холодными плитами гидравлического пресса под давлением 400 фунтов на кв. дюйм в течение 10 секунд для уплотнения слоев.
Затем электрод с полученным двойным слоем подвергали термической обработке в воздушной среде в течение 15 минут при температуре 350°С. При этом ПТФЭ плавился и растекался, в результате чего формировалось прочное покрытие электрода. (Меньшие температуры термической обработки приводили к менее оптимальному сцеплению слоя углерод-платина, а более высокие температуры не использовались, чтобы избежать разложения ПТФЭ).
Пример 7А
В этом Примере использовался электрод с электрокаталитическим слоем, содержащим углерод и платину. Платина была нанесена на углеродный носитель перед использованием ("предварительное нанесение").
Краска была изготовлена путем добавления порошка катализатора, содержащего 60 вес. % платины на углеродном носителе с высокой удельной площадью поверхности (Alfa Aesar HiSpec™ 9100), в подходящую емкость. Затем добавили 12 г монометилэфира дипропиленгликоля (Dowanol™ DPM) и 6 г дисперсии иономера перфторированной сульфокислоты (10 вес. % Nafion™ DE1021 в воде) для получения весового соотношения 150 % твердых частиц полимера относительно углерода.
Иономер предназначен для обеспечения связующего агента, который химически и электрохимические совместим внутри рабочей среды электролизера. Было обнаружено, что содержание 150 % обеспечивает оптимальные механические свойства, а при содержании меньше 100 % ухудшается адгезия, в то время как при содержании более 200 % получается хрупкое покрытие, склонное к растрескиванию с отслаиванием.
Смесь катализатора с иономером обрабатывали в течение 5 минут в смесителе с большими сдвиговыми усилиями (Silverson L5, с универсальной измельчительной головкой) для получения вязкоэластичной краски для нанесения покрытия распылением или с помощью кисти, причем покрытие не оседало при отстаивании.
Это покрытие наносили несколькими слоями на электрод, предварительно подвергнутый пескоструйной обработке (Тип А), с помощью краскопульта (с использованием азота в качестве газа-пропеллента) с промежуточной сушкой и спеканием иономера в воздушной среде в течение 2 минут при температуре 180°С между нанесениями слоев покрытия. Процесс нанесения покрытия повторяли до тех пор, пока содержание платины в покрытии, измеряемое откалиброванным рентгенолюминесцентным спектрометром, не достигало 3-4 г/м2.
После получения нужной степени покрытия электрод подвергали дополнительной термической обработке в течение 30 минут при температуре 180°С для удаления каких-либо остатков растворителя.
Пример 8А
В этом Примере использовался электрод с электрокаталитическим слоем, содержащим углерод, рутений и платину. Платина и рутений были нанесены на углеродный носитель перед использованием ("предварительное нанесение"). Покрытие электрода было осуществлено аналогичным образом как в Примере 7А за исключением того, что в качестве порошка катализатора использовался коммерческий продукт, в котором 50 % Pt и 25 % Ru были распылены на углеродном носителе с высокой удельной площадью поверхности (Alfa Aesar HiSpec™ 12100).
1.3 Результаты
В Таблице 1 приведены средние электрохимические характеристики покрытий, нанесенных на электрод Типа А, для каждого Примера, причем данные усреднялись несколько раз по разным электродам/партиям. Приведенные величины равны перенапряжениям покрытий для реакций с выделением водорода.
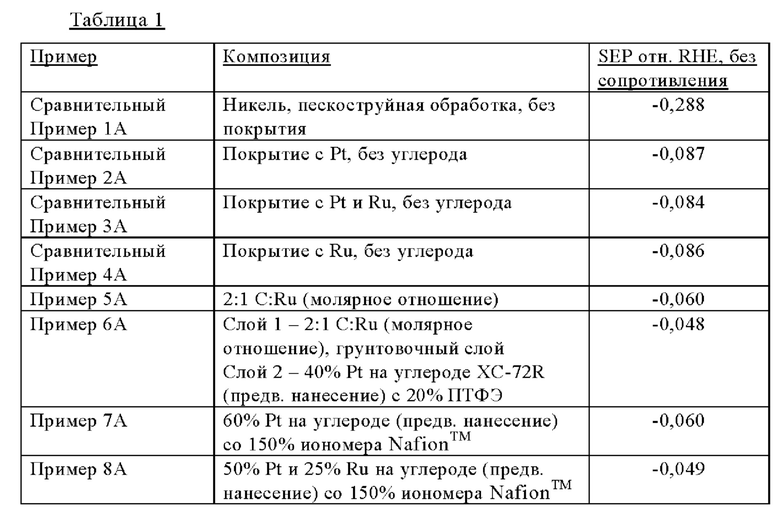
Сравнительный пример 1А обеспечивает контрольную характеристику никелевого электрода без покрытия, которая составила -0,288 В относительно RHE (от англ. Reversible Hydrogen Electrode, обратимый водородный электрод), как это измерялось в испытании потенциала отдельного электрода (SEP).
Сравнительные Примеры 2А, 3А и 4А обеспечивают характеристики для стандартных покрытий без углеродных носителей промышленных катодов для хлорщелочных электролизеров, примерно -0,087 В, -0,084 В и -0,086 В для покрытий, содержащих только платину, платину и рутений (молярное соотношение 4.66:1 Pt:Ru) и только рутений, соответственно.
Можно видеть, что все три покрытия обеспечивают улучшение перенапряжения (то есть, потенциал становится менее отрицательным) по сравнению с электродом без покрытия (СЕ1), и все остальные характеристики сопоставимы.
Пример 5А обеспечивает характеристику покрытия с рутением на углеродном носителе (молярное соотношение 2:1 C:Ru), которая была равна -0,060 В относительно RHE. Таким образом, обеспечивается улучшение перенапряжения для реакции выделения водорода (на 24-27 мВ) относительно Сравнительных примеров 2А, 3А и 4А. Это будет трансформироваться в аналогичное снижение напряжения на сборке ячеек промышленного хлорщелочного электролизера. Пример 5А демонстрирует выгоду при использовании покрытия с рутением на углеродном носителе, в результате чего улучшается характеристика электрода.
Пример 6А обеспечивает характеристику электрода с двухслойным покрытием, в котором первый слой содержит рутений на углеродном носителе, а верхний слой содержит платину, предварительно нанесенную на углеродный носитель, и ПТФЭ в качестве связующего вещества. Характеристика этой конструкции электрода составила -0,048 В относительно RHE. Таким образом, обеспечивается улучшение перенапряжения на 36-39 мВ относительно Сравнительных примеров 2А, 3А и 4А.
Пример 7А обеспечивает характеристику электрода, содержащего слой платины, предварительно нанесенной на углеродный носитель, и иономер Nafion™ в качестве связующего вещества. Характеристика этого электрода составила -0,060 В относительно RHE. Таким образом, обеспечивается улучшение перенапряжения на 24-28 мВ относительно Сравнительных примеров 2А, 3А и 4А.
Пример 7А обеспечивает характеристику электрода с однослойным покрытием, содержащим слой с платиной, предварительной нанесенной на углеродный носитель, с рутением и с иономером Nafion™ в качестве связующего вещества. Характеристика этого электрода составила -0,049 В относительно RHE. Таким образом, обеспечивается улучшение перенапряжения на 38 мВ относительно Сравнительных примеров 2А, 3А и 4А.
Поэтому Примеры 5А-8А демонстрируют, что по сравнению с эквивалентными покрытиями без углерода углеродсодержащие электроды обеспечивают существенное улучшение характеристики.
2. Полномасштабный промышленный монополярный хлорщелочной электролизер
2.1 Постановка эксперимента
Электрохимическую характеристику измеряли на продолжительных интервалах времени на ячейке, содержащей один электродный узел Типа В полномасштабного опытного промышленного электролизера (FM21, площадь мембраны - 0,21 м2).
В каждом эксперименте катод с покрытием сравнивали с анодом со стандартным покрытием (Chlorcoat™) и мембраной (Aciplex™ А4202, Asahi Kasei). В конструкции электролизера для каждого испытания использовались одинаковые конфигурации уплотнений, сжатия и внутренняя конфигурация.
Работу ячейки осуществляли при температуре 85°С (+/-2°С) с концентрациями подаваемых NaCl и NaOH, стандартными для промышленных установок, и с плотностью тока 3 кА/м2. В соответствии с обычной практикой осуществления работы промышленных электролизеров, в которые подаются жидкие электролиты, выходное напряжение ячеек нормализовали для учета незначительных колебаний температуры и концентраций, которые имели место в процессе испытаний. Такая стратегия очевидна для специалистов, хорошо знакомых с работой таких электролизеров.
2.2 Композиции
Сравнительный пример 3В
Вышеописанный Сравнительный пример 3А был воспроизведен с той же композицией краски на электродах Типа В.
Пример 5 В
Вышеописанный Пример 5А был воспроизведен с той же композицией краски на электродах Типа В.
Пример 9В
Этот Пример воспроизводился на вышеописанных электродах Типа В.
В этом Примере использовался электрод с электрокаталитическим слоем, содержащим углерод, рутений и палладий. В этом случае осуществлялось совместное осаждение рутения и палладия.
Для получения краски сначала растворяли кристаллы хлорида рутения (III) в безводной уксусной кислоте до концентрации рутения 33 г/л с использованием ультразвуковых волн в течение по меньшей мере 10 минут. Затем добавляли растворимые кристаллы ацетата палладия с концентрацией палладия 3,86 г/л, и растворение осуществляли также с использованием ультразвуковых волн. К раствору соли добавляли порошок углеродной сажи (Cabot Vulcan XC-72R) в концентрации углерода 8,71 г/л и подвергали полученный материал действию ультразвуковых волн в течение по меньшей мере 30 минут для получения суспензии.
Состав получаемой композиции был 2:0,9:0,1 C:Ru:Pd в молярном соотношении (72,41 вес. % Ru, 8,47 вес. % Pd и 19,12 вес. % С).
Эту композицию распыляли несколькими слоями на электрод, предварительно подвергнутый пескоструйной обработке, с промежуточной сушкой в течение 2 минут при температуре 180°С и с термической обработкой в воздушной среде между нанесениями слоев в течение 12 минут при температуре 450°С. Процесс нанесения покрытия повторяли до тех пор, пока содержание рутения в покрытии, измеряемое откалиброванным рентгенолюминесцентным спектрометром, не достигало 10-12 г/м2.
Пример 10 В
Этот Пример воспроизводился на вышеописанных электродах Типа В.
В этом Примере использовался электрод с электрокаталитическим слоем, содержащим углерод, рутений и платину. В этом случае осуществляли совместное осаждение рутения и платины.
Для получения краски сначала растворяли кристаллы хлорида рутения (III) в безводной уксусной кислоте до концентрации рутения 33 г/л с использованием ультразвуковых волн в течение по меньшей мере 10 минут. Затем добавляли раствор дигидрогексахлороплатиновой кислоты (150 г/л в 20 % HCl) с концентрацией платины 7,08 г/л. К раствору соли добавляли порошок углеродной сажи (Cabot Vulcan XC-72R) в концентрации углерода 8,71 г/л и подвергали полученный материал действию ультразвуковых волн в течение по меньшей мере 30 минут для получения суспензии. Состав получаемой композиции был 2:0,9:0,1 C:Ru:Pt в молярном соотношении (67,63 вес. % Ru, 14,50 вес. % Pt и 17,86 вес. % С).
Эту композицию распыляли несколькими слоями на электрод, предварительно подвергнутый пескоструйной обработке, с промежуточной сушкой в течение 2 минут при температуре 180°С и с термической обработкой в воздушной среде между нанесениями слоев в течение 12 минут при температуре 450°С. Процесс нанесения покрытия повторяли до тех пор, пока содержание рутения в покрытии, измеряемое откалиброванным рентгенолюминесцентным спектрометром, не достигало 10-12 г/м2.
2.3 Результаты
В Таблице 2 приведены нормализованные величины напряжения на ячейке для Примера, относящегося к электроду Типа В.
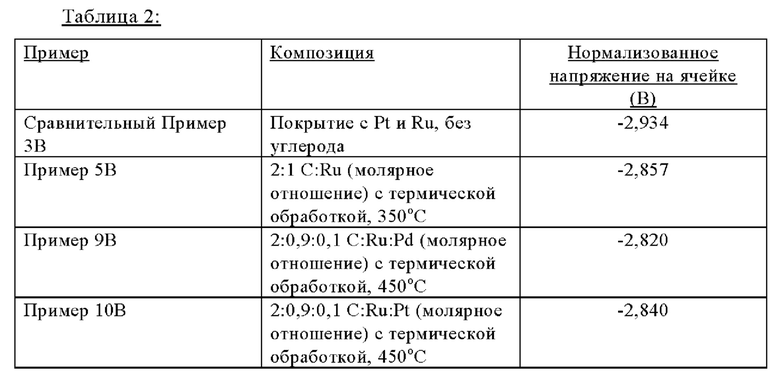
Сравнительный пример ЗВ обеспечивает характеристику для типичного промышленного покрытия, содержащего платину и рутений, без углеродного носителя.
Пример 5 В обеспечивает характеристику покрытия, содержащего рутений на углеродном носителе (молярное отношение 2:1 C:Ru). Нормализованная величина напряжения на ячейке улучшилась на 0,077 В по сравнению со Сравнительным Примером 3В. Это немного больше, чем в эквивалентных Примерах в испытаниях потенциала отдельного электрода с электродом Типа А, но согласуется с ними, и демонстрирует выгоду использования в покрытии рутения на углеродном носителе для улучшения характеристики электрода на промышленных установках.
Пример 9 В обеспечивает характеристику покрытия, содержащего углерод, рутений и палладий. Нормализованная величина напряжения на ячейке улучшилась на 0,114 В по сравнению со Сравнительным Примером 3В и на 0,037 В по сравнению с Примером 5 В на этой же ячейке.
Пример 10 В обеспечивает характеристику покрытия, содержащего углерод, рутений и платину. Нормализованная величина напряжения на ячейке улучшилась на 0,094 В по сравнению со Сравнительным Примером 3В на этом же электролизере и на 0,017 В по сравнению с Примером 5 В на этом же электролизере.
Эти Примеры показывают, что смеси металлов с углеродом могут обеспечивать дополнительные улучшения характеристик.
3. Полномасштабный промышленный биполярный хлорщелочной электролизер
3.1 Постановка эксперимента
Электрохимическую характеристику измеряли на продолжительных интервалах времени в полномасштабном промышленном хлорщелочном электролизере (поставщик - INOVYN Technologies Ltd) с электродами Типа С.
В каждом случае использовались электроды из просечно-вытяжных никелевых сеток, размеры которых составляли примерно 1,2 м × 1,2 м, с вышеописанными покрытиями.
Электроды с покрытиями сваривали в полноразмерные катодные камеры BICHLOR™, причем 2 электрода сваривали бок о бок с использованием стандартных производственных технологий. Примерная расчетная площадь электродов каждой готовой камеры составила 2,9 м2.
Хлорщелочные модули для использования в электролизере BICHLOR™ получали соединением с помощью болтов вышеописанных катодных камер с анодными камерами BICHLOR™ с мембранным сепаратором, расположенным между анодом и катодом, причем мембраны уплотняли в модуле с помощью двух прокладок из каучука на основе сополимера этилена, пропилена и диенового мономера с защитой из ПТФЭ (поставщик INOVYN Technologies Ltd), расположенных по периферии мембраны (одна прокладка с каждой стороны мембраны) и зажатых между мембраной и фланцем камеры с помощью болтов, затянутых с определенным усилием, которые вводят через два фланца, мембраны и прокладки. Каждая анодная камера содержала 2 просечно-вытяжные металлические электродные сетки со стандартным анодным покрытием Chlorcoat™ фирмы INOVYN, которые сваривали бок о бок для формирования анодных камер, используя стандартные производственные технологии для этих камер. Конструкции анода, катода и узлов модулей подробно описаны в патенте US 6761808 В1.
Электролизер содержал 14 модулей вышеописанного типа, сконфигурированных, как это описано ниже. В процессе работы в электролизер подают NaOH в концентрации примерно 30 % и соляной раствор с концентрацией 300 г/л. Концентрации выходящего соляного раствора и выходящего NaOH были примерно 220 г/л и примерно 32 %, соответственно. Работу электролизера осуществляли с температурой щелока на выходе, равной 87°С, при давлении 235 мбар изб. газообразного хлора и 250 мбар изб. водорода, и с плотностями тока от 5,5 до 6 кА/м2.
3.2 Композиции
Пример 3С
Было изготовлено двадцать катодов с использованием той же краски и той же технологии, которые использовались в Примерах 3А и 3В.
Электроды сваривали парами для получения катодных камер, как это уже описывалось, и затем присоединяли к анодам, тоже как это уже было описано, для формирования десяти модулей. В пяти модулях использовался мембранный сепаратор Aciplex F6801, поставляемый фирмой Asahi Kasei Corporation, Япония ("модуль типа 3С1", как указано ниже в Таблице 3), а в других пяти готовых модулях использовался сепаратор Flemion F8080, поставляемый фирмой Asahi Glass Co. Ltd, Япония ("модуль типа 3С2", как указано ниже в Таблице 3)
Пример 10С
Было изготовлено восемь катодов с использованием той же краски и той же технологии, которые использовались в Примере 10 В. Электроды сваривали парами для получения катодных камер, как это уже описывалось, и затем присоединяли к анодам, тоже как это уже было описано, для формирования четырех модулей. В двух модулях использовался мембранный сепаратор Aciplex F6801, поставляемый фирмой Asahi Kasei Corporation, Япония ("модуль типа 10С1", как указано ниже в Таблице 3), а в других двух модулях использовался сепаратор Flemion F8080, поставляемый фирмой Asahi Glass Co. Ltd, Япония ("модуль типа 10С2", как указано ниже в Таблице 3)
Все 14 модулей были встроены в хлорщелочной электролизер BICHLOR™ и работали одновременно.
3.3 Результаты
В Таблице 3 приведены средние величины напряжения для каждого типа модулей при запуске.
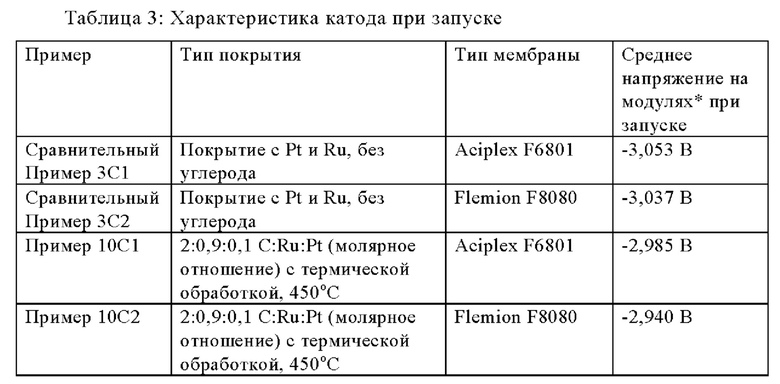
*- Величина напряжения, нормализованная для 6 кА/м, 90°С, концентрации 32 % NaOH и давления хлора 235 мбар.
Данные, приведенные в Таблице 3, показывают, что средняя величина напряжения при запуске модулей с покрытиями, содержащих совместно осажденные углерод, рутений и платину, и с одинаковыми типами мембран улучшилась на 65-90 мВ по сравнению со средней величиной напряжения при запуске модулей, покрытия которых содержат рутений и платину, без углерода, при плотности тока 6,0 кА/м2.
После 2 месяцев непрерывной работы с плотностями тока 5,5-6,0 кА/м2 величины напряжений во всех четырех Примерах были идентичны величинам напряжений при запуске, то есть, катоды продемонстрировали свою стабильность и успешно поддерживали уменьшенное напряжение.
4. Стабильность при запуске и при выключениях
4.1 Постановка эксперимента
Опытно-промышленные испытания в уменьшенном масштабе выполнялись с мембранами площадью 100 см2 для просечно-вытяжной сетки катода с покрытием толщиной 0,15 мм (электрод Типа D) в стандартном отдельном креплении ячейки, и с использованием стандартной методики определения влияния многократных последовательных выключений на рабочие характеристики покрытия катода.
В обычном режиме работы промышленных электролизеров выключения происходят нечасто, и поэтому описанные здесь испытания обеспечивают возможность многократных выключений в течение сравнительно непродолжительного времени для моделирования результатов, которые обычно накапливаются в установках в течение нескольких лет работы.
Обычно промышленные биполярные хлорщелочные электролизеры выключают при поддержании небольшой величины "прямого" тока (эта величина зависит от площади мембраны и количества модулей в электролизере) для предотвращения возникновения обратных токов между соседними элементами и для защиты от повреждений покрытий электродов, особенно покрытий катодов. Поэтому дополнительным аспектом данного испытания является выключение элемента без указанной защиты и обеспечение возможности протекания обратного тока путем шунтирования снаружи анода и катода, что происходит самопроизвольно в биполярных элементах, когда аноды и катоды соединены электрически. В указанных условиях испытания покрытие, которое не обладает способностью выдерживать обратные токи, ухудшится, и это проявится с очевидностью в росте (отрицательном) напряжения на ячейке.
Испытываемая ячейка содержит титановую раму анода с квадратным вырезом, в котором с помощью сварки закреплена просечно-вытяжная титановая сетка, на которую нанесено стандартное покрытие CHLORCOATTM анода, способное выдерживать обратные токи, и поэтому он не будет влиять на результаты испытаний. Используется идентичная никелевая рама катода с вырезом, в котором сетка катода с покрытием зафиксирована с помощью механических пружин, обеспечивающих удерживание сетки в нужном положении относительно мембраны и поддержание электрического соединения. Конструкция ячейки представляет собой сандвич-структуру, состоящую из рам анода и катода (с сетками) и двух прокладок между ними и стандартной промышленной хлорщелочной мембраны (Flemion F8080, фирма Asahi Glass). В этой конфигурации ток снимается с краев двух рам.
С обеих сторон рам анодов и катодов установлены дополнительные пластины для обеспечения подачи реагентов и сбора продуктов и для обеспечения нагрева с помощью электрических резистивных нагревателей. На концах ячейки установлены две пластины, которые используются для сжатия узла с определенным усилием с помощью стяжных стержней.
В анодную камеру ячейки подают регулируемый поток соляного раствора с концентрацией 250 г/кг для поддержания концентрации на выходе, равной 185 г/кг. В катодную камеру подают регулируемый поток деминерализованной воды для поддержания концентрации на выходе, равной 315 г/кг. Испытания проводили пре температуре 85°С.
В испытаниях для оценки стабильности покрытий сначала осуществляли работу образцов катодов в течение нескольких суток, покат не получали стабильное напряжение на ячейке при плотности прямого тока, равной 4 кА/м2. Затем источник питания постоянного тока выключали, и анод и катод шунтировали снаружи с использованием выключателя на 1 час. В этих условиях напряжение на ячейке быстро поднималось до 0 В, и наблюдался протекающий самопроизвольно обратный ток (от катода к аноду). Затем снова включали прямой ток, и ячейку выдерживали в течение 24 часов при плотности тока 4 кА/м2, пока напряжение на ячейке снова не стабилизируется. Затем ток выключали, и ячейку шунтировали еще раз, и вышеописанный процесс повторяли 10-30 раз, осуществляя мониторинг изменения стабилизированного напряжения на ячейке при токе 4 кА/м2. Изменение напряжения на ячейке порядка 300 мВ относительно начала испытаний (становится более отрицательным) является показателем серьезного повреждения покрытия катода, причем в конце концов электрод работает так, как будто это никелевый катод без покрытия.
Таким образом, покрытия демонстрируют нестабильность во время выключений в тех случаях, когда при обратных токах отмечается значительное изменение напряжения.
4.2 Композиции
Сравнительный пример 4D
Был изготовлен электрод с использованием такой же краски и такой же технологии, как в Примере 4А для электродов Типа D, для получения Сравнительного Примера 4D.
Пример 5D
Был изготовлен электрод с использованием такой же краски и такой же технологии, как в Примерах 5А и 5 В для электродов Типа D, для получения Примера 5D.
4.3 Результаты
На фиг. 1 приведены напряжения на ячейке в зависимости от количества циклов выключений для Сравнительного Примера 4D и Примера 5D. Таблица 4 обеспечивает обобщение данных, представленных на фиг. 1.
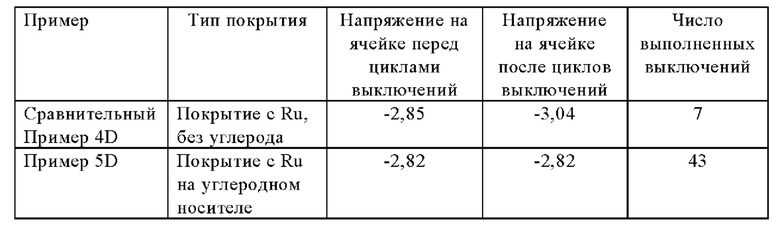
В Сравнительном Примере 4D напряжение на ячейке при запуске было -2,85 В, а в Примере 5D видно улучшение на 30 мВ с напряжением на ячейке, равным -2,82 В. Эти результаты показывают, что покрытие с рутением на углеродном носителе также имеет более высокую активность по сравнению с покрытием, содержащим только рутений, при равном весе покрытия на электроде Типа D.
В Сравнительном Примере 4D видно резкое изменение напряжения на ячейке всего лишь в течение 7 циклов выключений, до 3,04 В (равно изменению напряжения на ячейке на 190 мВ).
С другой стороны, в Примере 5D нет существенного изменения напряжения на ячейке на протяжении 43 циклов выключений. Этот Пример показывает, что покрытие с углеродом и рутением обладает существенно лучшей способностью выдерживать выключения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ МЕМБРАННО-ЭЛЕКТРОДНОГО БЛОКА С ПОРИСТЫМ КАТОДОМ | 1987 |
|
RU2015207C1 |
| РОДИЕВЫЙ ЭЛЕКТРОКАТАЛИЗАТОР И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2000 |
|
RU2230136C2 |
| БИПОЛЯРНАЯ ПЛАСТИНА ДЛЯ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 1999 |
|
RU2237317C2 |
| ЭЛЕКТРОД | 2008 |
|
RU2487197C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ И МОДИФИКАЦИИ ЭЛЕКТРОХИМИЧЕСКИХ КАТАЛИЗАТОРОВ НА УГЛЕРОДНОМ НОСИТЕЛЕ | 2015 |
|
RU2595900C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ МЕМБРАННО-ЭЛЕКТРОДНОГО БЛОКА С БИФУНКЦИОНАЛЬНЫМИ ЭЛЕКТРОКАТАЛИТИЧЕСКИМИ СЛОЯМИ | 2009 |
|
RU2392698C1 |
| УЛУЧШЕННЫЙ РОДИЕВЫЙ ЭЛЕКТРОКАТАЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2311496C2 |
| ЭЛЕКТРОД ДЛЯ ПРИМЕНЕНИЯ ПРИ ПОЛУЧЕНИИ ВОДОРОДА (ВАРИАНТЫ) И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ (ВАРИАНТЫ) | 2003 |
|
RU2268324C2 |
| КАТАЛИТИЧЕСКИЙ ЭЛЕКТРОД ДЛЯ СПИРТОВЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2012 |
|
RU2507640C1 |
| ЭЛЕКТРОКАТАЛИЗАТОР ВОССТАНОВЛЕНИЯ КИСЛОРОДА, СОДЕРЖАЩИЙ ЕГО ТОПЛИВНЫЙ ЭЛЕМЕНТ И СПОСОБ ПОЛУЧЕНИЯ ЭЛЕКТРОЭНЕРГИИ | 2006 |
|
RU2422947C2 |
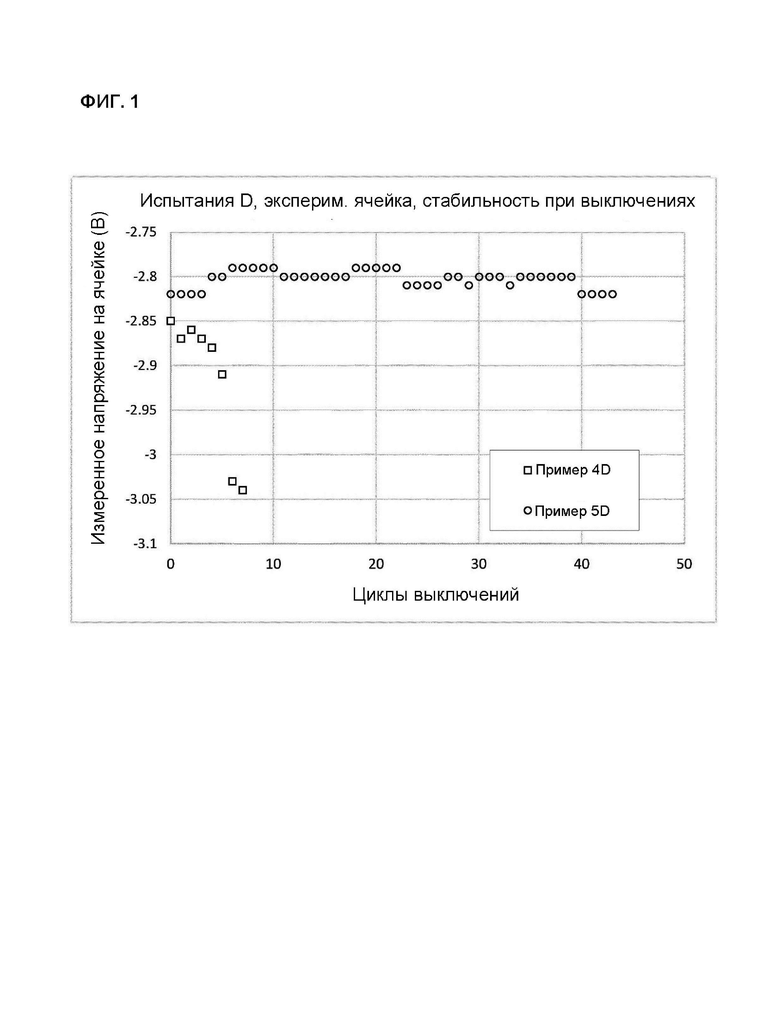
Изобретение относится к электродному узлу для получения водорода, содержащему: анодное устройство, которое содержит анод, расположенный внутри электролитической камеры; катодное устройство, содержащее катод, расположенный внутри электролитической камеры, содержащей раствор гидроксида щелочного металла. Узел характеризуется тем, что катод содержит: электропроводную металлическую подложку, выполненную из нержавеющей стали, мягкой стали, никеля или меди; и электрокаталитический слой на подложке, содержащий по меньшей мере один металл на электропроводном материале носителя. Причем указанный по меньшей мере один металл представлен в металлической форме или в форме соединения металла, такого как оксид, и выбран из металлов группы платины, рения, никеля, кобальта и молибдена, и электрокаталитический слой содержит по меньшей мере 50 об. % электропроводного материала носителя, который сформирован из частиц, средний размер которых менее 5 мкм (5 микрон) и которые не являются металлическими частицами. Также изобретение относится к способу электролиза, применению каталитического слоя на электроде, способу обеспечения катода, модульному или фильтр-прессному электролизеру. Используемый электрод обеспечивает низкое, но стабильное перенапряжение катода, который также сохраняет стабильность в течение длительного времени. 5 н. и 14 з.п. ф-лы, 1 ил., 4 табл., 5 пр.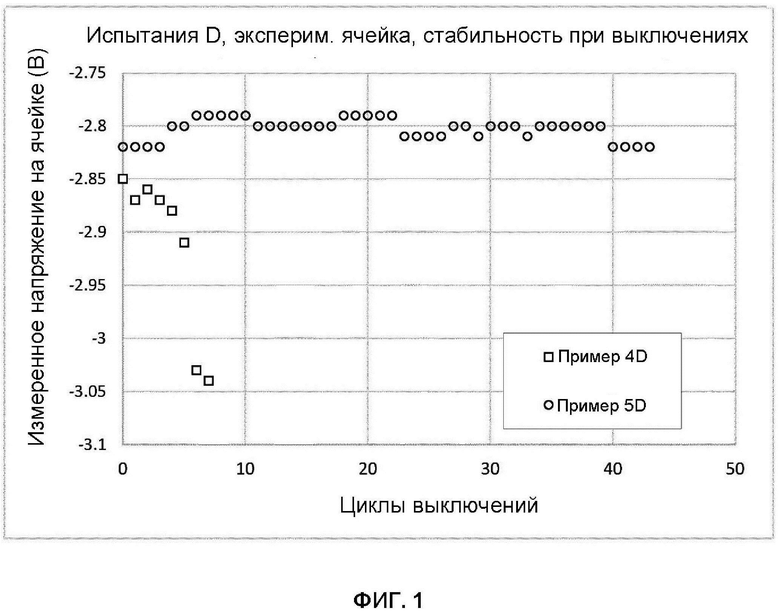
1. Электродный узел для получения водорода, содержащий:
анодное устройство, которое содержит анод, расположенный внутри электролитической камеры;
катодное устройство, содержащее катод, расположенный внутри электролитической камеры, содержащей раствор гидроксида щелочного металла,
отличающийся тем, что катод содержит:
электропроводную металлическую подложку, выполненную из нержавеющей стали, мягкой стали, никеля или меди; и
электрокаталитический слой на подложке, содержащий по меньшей мере один металл на электропроводном материале носителя,
причем указанный по меньшей мере один металл представлен в металлической форме или в форме соединения металла, такого как оксид, и выбран из металлов группы платины, рения, никеля, кобальта и молибдена, и
электрокаталитический слой содержит по меньшей мере 50 об. % электропроводного материала носителя, который сформирован из частиц, средний размер которых менее 5 мкм (5 микрон) и которые не являются металлическими частицами.
2. Узел по п. 1, в котором указанный по меньшей мере один металл включает по меньшей мере один металл группы платины.
3. Узел по п. 2, в котором указанный по меньшей мере один металл включает рутений.
4. Узел по п. 3, в котором указанный по меньшей мере один металл включает рутений и платину.
5. Узел по любому из предыдущих пунктов, в котором электропроводный материал носителя содержит электропроводный углеродный материал.
6. Узел по любому из предыдущих пунктов, в котором электрокаталитический слой содержит от 0,2 до 10 об. % указанного по меньшей мере одного металла и от 90 до 99,8 об. % электропроводного материала носителя.
7. Узел по любому из предыдущих пунктов, в котором электропроводный материал носителя имеет удельную площадь поверхности по меньшей мере 50 м2/г, предпочтительно от 200 до 1000 м2/г.
8. Узел по любому из предыдущих пунктов, в котором электропроводный материал носителя сформирован из частиц со средним размером менее 1 мкм (1 микрон), в частности от 10 до 250 нанометров, в частности от 20 до 100 нанометров.
9. Узел по любому из предыдущих пунктов, в котором катод дополнительно содержит связующее вещество, которое предпочтительно покрыто электрокаталитическим слоем.
10. Узел по любому из предыдущих пунктов, в котором катод содержит два или более электрокаталитических слоев, как это определено в предыдущих пунктах формулы изобретения, но осажденные слои имеют разный состав.
11. Узел по любому из предыдущих пунктов, который предназначен для получения водорода и галогена и в котором анодная камера содержит раствор галида щелочного металла.
12. Узел по любому из пп. 1-10, который предназначен для получения водорода и кислорода и в котором анодная камера содержит раствор гидроксида щелочного металла.
13. Модульный или фильтр-прессный электролизер, содержащий группу электродных узлов по любому из пп. 1-12 и предпочтительно содержащий от 5 до 300 электродных узлов.
14. Способ электролиза, включающий осуществление электролиза в электродном узле по любому из пп. 1-12 или в модульном или в фильтр-прессном электролизере по п. 13, для получения водорода.
15. Применение каталитического слоя на электроде, содержащем электропроводную металлическую подложку, выполненную из нержавеющей стали, мягкой стали, никеля или меди и электрокаталитический слой на подложке, включающий по меньшей мере один металл на электропроводном материале носителя, причем указанный по меньшей мере один металл представлен в металлической форме или в форме соединения металла, такого как оксид, и выбран из металлов группы платины, рения, никеля, кобальта и молибдена, и электрокаталитический слой содержит по меньшей мере 50 об.% электропроводного материала носителя, сформированного из частиц, средний размер которых менее 5 мкм (5 микрон) и которые не являются металлическими частицами,
для обеспечения по меньшей мере одного из:
i) уменьшенного перенапряжения электрода;
ii) перенапряжения электрода, которое является стабильным в течение продолжительного времени работы; и
iii) повышенной способности электрода выдерживать обратные токи.
16. Применение по п. 15, в котором электрод представляет собой катод в процессе получения водорода с катода.
17. Применение по п. 16, в котором процесс получения водорода с катода представляет собой процесс получения водорода из гидроксида щелочного металла на катоде и либо (1) галогена из галида щелочного металла, либо (2) кислорода из гидроксида щелочного металла на аноде.
18. Способ обеспечения катода для процесса электролиза гидроксида щелочного металла для получения водорода, включающий:
i) изготовление электрода, содержащего электропроводную металлическую подложку, выполненную из нержавеющей стали, мягкой стали, никеля или меди, и электрокаталитический слой на подложке, содержащий по меньшей мере один металл, нанесенный на электропроводный материал носителя, причем указанный по меньшей мере один металл представлен в металлической форме или в форме соединения металла, такого как оксид, и его выбирают из металлов группы платины, рения, никеля, кобальта и молибдена, и электрокаталитический слой содержит по меньшей мере 50 об. % электропроводного материала носителя, сформированного из частиц, средний размер которых менее 5 мкм (5 микрон) и которые не являются металлическими частицами, и
ii) обеспечение электрода для применения в качестве катода в процессе электролиза гидроксида щелочного металла для получения водорода.
19. Способ по п. 18, в котором процесс электролиза гидроксида щелочного металла для производства водорода представляет собой процесс получения водорода с катода и либо (1) галогена из галида щелочного металла, либо (2) кислорода из гидроксида щелочного металла на аноде.
| CN 107858701 A, 30.03.2018 | |||
| F | |||
| Mohammadil et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕКТРОДА | 1980 |
|
RU2045583C1 |
| АНОД ТОПЛИВНОГО ЭЛЕМЕНТА НА ОСНОВЕ МОЛИБДЕНОВЫХ БРОНЗ И ПЛАТИНЫ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2564095C1 |
Авторы
Даты
2024-11-14—Публикация
2021-01-11—Подача