Изобретение относится к медицине, в частности к экспериментальной кардиологии. Служит для моделирования хронической тромбоэмболической легочной гипертензии (ХТЭЛГ) у лабораторных грызунов с целью изучения патогенеза, разработки новых методов диагностики и лечения.
ХТЭЛГ возникает у пациентов, перенесших тромбоэмболию легочной артерии (ТЭЛА), и быстро приводит к правожелудочковой недостаточности. Для этого заболевания характерно наличие организованных тромбов в легочной артерии, которые создают препятствие кровотоку, и микрососудистое поражение ветвей легочной артерии. Оба этих фактора приводят к повышению давления в легочной артерии и легочного сосудистого сопротивления. При ТЭЛА тромбоэмбол имеет преимущественно коагуляционный генез (красный тромб), поэтому наибольшую роль в его структуре играют нити фибрина. Продукты деградации фибрина при этом обладают биологически активными свойствами, такими как иммуномодуляция и влияние на коагуляционный каскад, что вносит существенную роль в патогенез хронической тромбоэмболической легочной гипертензии (ХТЭЛГ). Отсутствие фибрина в структуре искусственных эмболов значительно снижает точность воспроизведения ХТЭЛГ. С другой стороны, из-за выраженной фибринолитической активности плазмы крови грызунов нативный фибрин быстро лизируется и не может быть использован для воспроизведения резидуальных тромбов – неотъемлемого компонента патогенеза ХТЭЛГ.
Известен патент №2675353 «Способ моделирования хронической тромбоэмболической легочной гипертензии», в котором аутологичные тромбы инкапсулируют в альгинатные микросферы диаметром 130-400 мкм и вводят животному внутривенно не менее 4 раз с интервалом не менее 2 дней.
Недостатком данного способа является сложный многоэтапный протокол воспроизведения, что резко снижает ее практическую реализацию. Кроме того, многократный забор аутологичнной крови приводит к дополнительной травматизации животного, что не укладывается в патогенез заболевания.
Известен способ моделирования ХТЭЛГ, согласно которому суспензию полистироловых микросфер Duke Scientific №7525A (США) диаметром 25±1 мкм однократно вводят лабораторной крысе в правую яремную вену в количестве 1,3 млн микросфер на 100 г веса (Liu W, Zhang Y, Lu L, et al. Expression and Correlation of Hypoxia-Inducible Factor-1α (HIF-1α) with Pulmonary Artery Remodeling and Right Ventricular Hypertrophy in Experimental Pulmonary Embolism. Med Sci Monit. 2017; 23:2083-2088).
Недостатком данного способа является тот факт, что из-за абсолютной нерастворимости полистироловых микросфер, а также отсутствия естественных биологически активных молекул (продуктов деградации фибрина), использованная модель не полностью отражает естественный патогенез ХТЭЛГ.
Известен способ моделирования ХТЭЛГ путем однократного введения полимерных эмболизирующих частиц Thermo Fisher №184942 (США) диаметром 85 мкм. Полимерные микросферы вводились в хвостовую вену лабораторной крысе однократно в объеме 90 мкл на 100 г веса животного. Спустя 1 день после введения полимерных эмболизирующих частиц животному подкожно вводился ингибитор неоангиогенеза – SU5416 (Tocris 3037 или MedChem Express HY-10374) в дозе 20 мг/кг, предварительно растворенный в диметилсульфоксиде (ДМСО) (Zagorski J, Neto-Neves E, Alves NJ, et al. Modulation of soluble guanylate cyclase ameliorates pulmonary hypertension in a rat model of chronic thromboembolic pulmonary hypertension by stimulating angiogenesis. Physiol Rep. 2022; 10(1):e15156).
Недостатком данного способа является узкая область применения этой модели в связи с тем, что нарушение неоангиогенеза, как патогенетический фактор, имеет значение только в небольшом числе случаев формирования ХТЭЛГ. Кроме того, применение нерастворимых эмболизирующих частиц снижает точность воспроизведения моделируемой патологии.
Известен способ моделирования ХТЭЛГ, когда лабораторным крысам в левую наружную яремную вену вводились аутологичные тромбы, суспензированные в 1,5 мл физиологического раствора, содержащего транексамовую кислоту в дозе 200 мг/кг. Введение эмболизирующих частиц повторяли через 4 и 7 дней после первой инъекции. Пенициллин (10 000 ЕД/кг/сут) вводили в течение 3 дней после инъекции аутологичных тромбов. Дополнительно животным вводили транексамовую кислоту в дозе 200 мг/кг/сут внутрибрюшинно (Deng C, Zhong Z, Wu D, et al. Role of FoxO1 and apoptosis in pulmonary vascular remolding in a rat model of chronic thromboembolic pulmonary hypertension. Sci Rep. 2017; 7(1):2270).
Недостатком данного способа является недостаточная эффективность из-за высокой степени фибринолитической активности плазмы крови грызунов, которая сохраняется даже на фоне применения ингибиторов фибринолиза.
Известен способ моделирования ХТЭЛГ, который является наиболее близким аналогом заявляемого изобретения. Этот способ заключается в том, что в хвостовую вену крысам вводились микросферы диаметром 45 мкм (Distrilab 7545A) с фибрин-/коллагеновым покрытием, суспензированные в физиологическом растворе, в дозе 1000 микросфер/г массы тела животного на 10 и 11 неделе и 750 микросфер/г массы тела животного на 12 неделе (Arias-Loza PA, Jung P, Abeßer M, et al. Development and Characterization of an Inducible Rat Model of Chronic Thromboembolic Pulmonary Hypertension. Hypertension. 2016; 67(5):1000-1005).
Недостатком данного способа является не полное воспроизведение патогенеза ХТЭЛГ из-за абсолютной нерастворимости микросфер. В статье не проверялась стабильность фибринового покрытия, так как фибринолитическая активность плазмы крови у грызунов очень высокая, то, вероятнее всего, покрытие разрушается в первые дни после введения.
Имеющиеся в доступных источниках информации способы моделирования ХТЭЛГ отличаются большой трудоемкостью и низкой воспроизводимостью. Данная ситуация усложняет процесс поиска новых способов лечения и диагностики этой патологии.
Технической задачей заявляемого изобретения является разработка модели для воспроизведения естественный патогенеза ХТЭЛГ хронической тромбоэмболической легочной гипертензии.
Заявленный технический результат достигается путем моделирования хронической тромбоэмболической легочной гипертензии, включающем в себя внутривенное введение лабораторным грызунам эмболизирующих частиц, полученных путем микроинкапсулирования фибрина в альгинатные микрокапсулы диаметром 100-700 мкм с соотношением фибрина к альгинату натрия от 1:100 до 1:4. Изготовленные эмболизирующие частицы вводят в количестве от 5 х 102 до 15 х 104 не менее 4 раз с интервалом не менее 2 дней. У лабораторных животных наблюдается ремоделирование сосудистого русла легких, что структурно и патогенетически соответствует изменениям при ХТЭЛГ.
Введенный в венозное русло микроинкапсулированный фибрин эмболизирует ветви легочной артерии. Первые признаки биодеградации эмболизирующих частиц наблюдаются через 2 недели после введения. Полная биодеградация большинства частиц микроинкапсулированного фибрина отмечается к 6 недели. Доля нерастворенных эмболизирующих частиц составляет до 10% от первоначального введенного объема через 6 недель наблюдения. В результате, повышается давление в легочной артерии и легочное сосудистое сопротивление, сосудистое русло легких подвергается ремоделированию, что соответствует изменениям, происходящим при ХТЭЛГ.
Диаметр эмболизирующих частиц находится в диапазоне от 100 до 700 мкм и зависит от целевого размера эмболизируемого сосуда: от дистальных до долевых ветвей легочной артерии крыс.
Благодаря соотношению объема фибрина и альгината натрия от 1:100 до 1:4, соответственно, эмболизирующие частицы имеют оптимальную прочность, позволяющую частицам биодеградировать в прогнонизрованные, а фибрин находится в достаточном количестве внутри микрокапсулы для оказания паракринного эффекта.
Однократная доза для внутривенного введения составляет от 5 х 102 до 15 х 104 эмболизирующих частиц. Этого количества достаточно для редукции необходимого объема сосудистого русла малого круга кровообращения и создания достаточной концентрации биологически активных веществ – продуктов биодеградации фибрина.
Необходимость введения микроинкапсулированного фибрина не менее 4 раз с интервалом не менее 2 дней обусловлена медленной биодеградацией эмболизирующих частиц, а также патогенезом дистальных форм ХТЭЛГ. В результате, достигается ремоделирование сосудистого русла, стойкое повышение давления в легочной артерии и формирование ХТЭЛГ.
Заявленное изобретение поясняется чертежами:
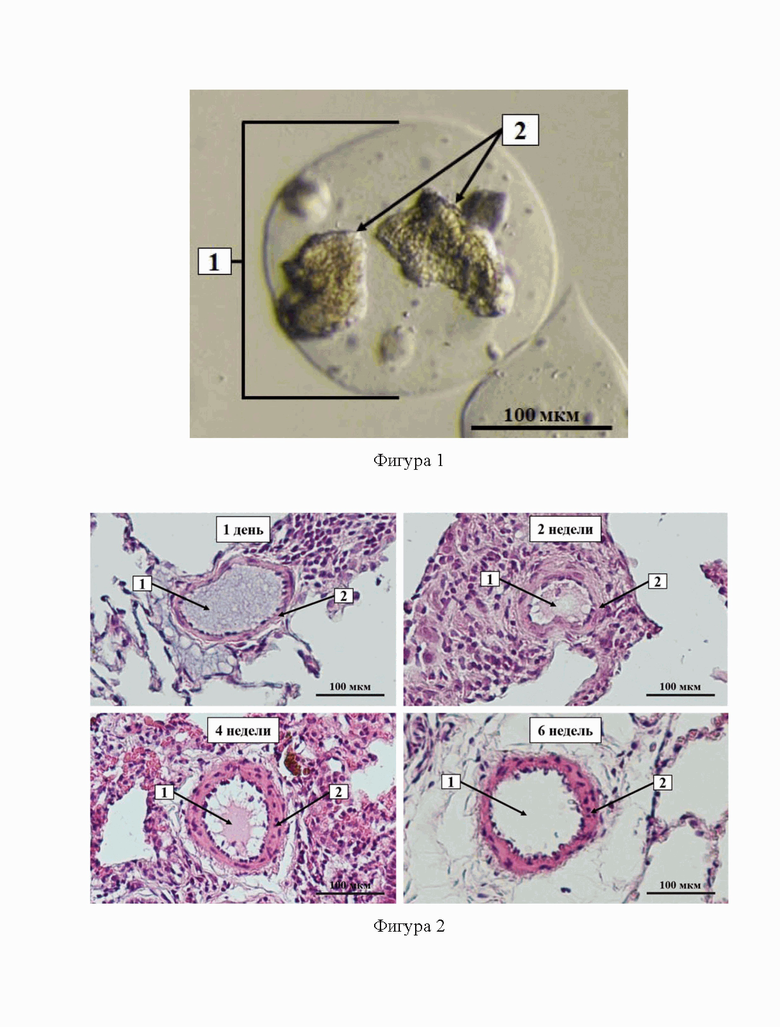
Фиг. 1 – микрофотография микроинкапсулированного фибрина, полученного по протоколу примера 1.
1. – Микрокапсула;
2. – Частицы фибрина.
Фиг. 2 – динамика биодеградации эмболизирующих частиц в примере 1.
1. – Эмболизирующая частица;
2. – Сосудистая стенка.
Фиг. 3 – морфофункциональные изменения через 6 недель после заключительного введения микроинкапсулированного фибрина в примере 1.
А – Индекс гипертрофии сосудистой стенки ветвей легочной артерии;
Б – Процент фиброзных волокон сосудистой стенки ветвей легочной артерии;
В – Систолическое давление в правом желудочке (СДПЖ). Здоров. жив. – группа здоровых животных, МС фибрин – микроинкапсулированный фибрин.
Фиг. 4 – морфофункциональные изменения через 6 недель после заключительного введения микроинкапсулированного фибрина в примере 2.
А – Индекс гипертрофии сосудистой стенки ветвей легочной артерии;
Б – Процент фиброзных волокон сосудистой стенки ветвей легочной артерии;
В – Систолическое давление в правом желудочке (СДПЖ). Здоров. жив. – группа здоровых животных, МС фибрин – микроинкапсулированный фибрин.
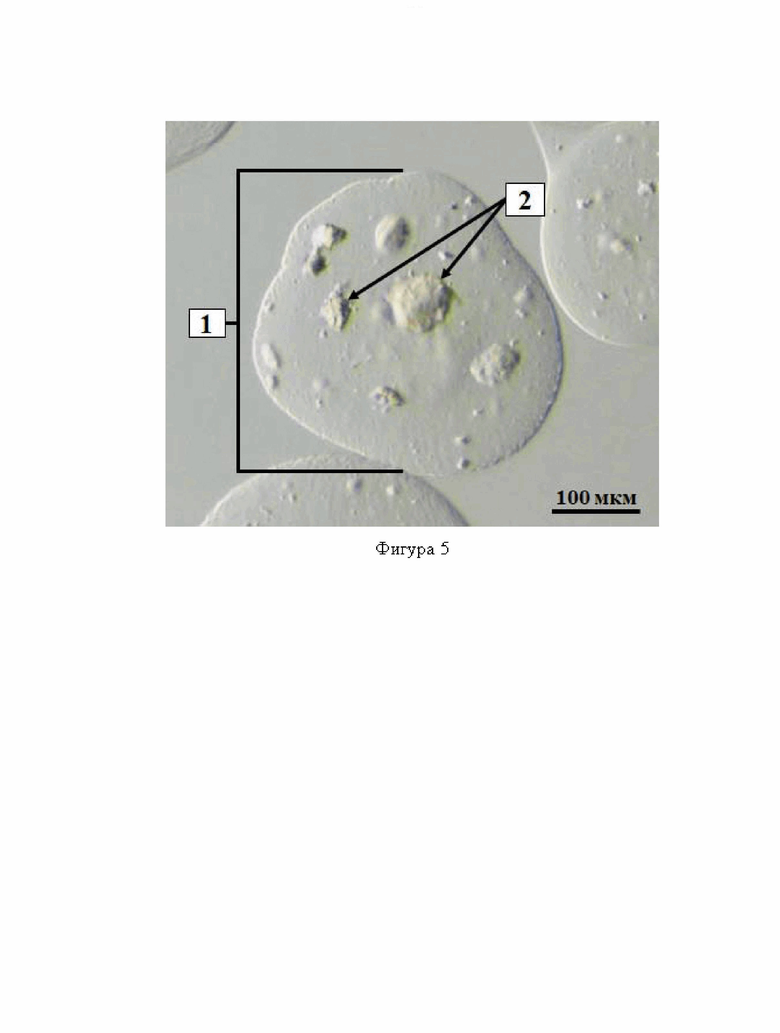
Фиг. 5 – микрофотография микроинкапсулированного фибрина, полученного по протоколу примера 3.
1. – Микрокапсула;
2. – Частицы фибрина.
Способ осуществляют, например, следующим образом.
Эмболизирующие частицы получаются при использовании фибрина человеческого или крысиного. В стерильных условиях выполняется измельчение фибрина, затем с помощью сита с ячейками заданного диаметра отбираются частицы размером меньше или равным 71 мкм.
Готовится суспензия измельченных фибриновых частиц в растворе 0,5-3% альгината натрия в соотношении по объему от 1:100 до 1:4, соответственно, для дальнейшего микроинкапсулирования. Для получения гомогенной суспензии используется лабораторный ультразвуковой диспергатор погружного типа со штативом (ООО «СпецмашСоник», Россия). Полученную суспензию подают на вход установки Encapsulator В-390 (BUCHI, Швейцария) с параметрами работы: диаметр форсунки 80-200 мкм, напряжение электродов 1300-2800 В, частота вибрации 2400-3600 Гц, давление 400-600 мбар. Благодаря заданным параметрам размеры получившихся микрокапсул составляют 100-700 мкм. Раствор 1-3% хлорида бария используется как стабилизатор поверхностного слоя микрокапсул. Перед введением эмболизирующих частиц раствор хлорида бария полностью удаляется, а микроинкапсулированный фибрин отмывается физиологическим раствором в объеме 1-1,5 мл. Эмболизирующие частицы в количестве от 5 х 102 до 15 х 104 вводятся в венозное русло крысы, предпочтительно в хвостовую вену. Данная манипуляция повторяется не менее 4 раз с интервалом не менее 2 дней.
Способ иллюстрируется следующими примерами.
Пример №1. Для изготовления эмболизирующих частиц фибрин из плазмы крови человека (Sigma, США) смешивали с 1,8% раствором альгината натрия в соотношении 1:7, соответственно. Производство микрокапсул c включенным фибрином выполнялось с помощью установки Encapsulator В-390 (BUCHI, Швейцария) с параметрами работы: диаметр используемой форсунки 120 мкм, частота вибрации 3200 Гц, напряжение электродов 2100 В, давление 500 мбар. Для стабилизации образующихся микросфер использовался 2% раствор хлорида бария. Размер полученных частиц составил 205 ± 38 мкм. На фиг. 1 представлена микрофотография микрокапсулы (1) с заключенными в нее частицами фибрина (2).
Для оценки стабильности микроинксулированного фибрина изготовленные эмболизирующие частицы вводились 12 крысам-самцам стока Wistar однократно в хвостовую вену. Гистологическое исследование легких выполнялось на разных сроках после введения эмболизирующих частиц: 1 день, 2 недели, 4 недели, 6 недель. На панели микрофотографий (фиг. 2) представлена динамика биодеградации частиц микроинкапсулированного фибрина в сосудистом русле малого круга кровообращения. 1 день после эмболизации – края четкие, структура микрокапсулы однородная; 2 неделя – неровный край, неоднородность структуры микрокапсулы; 4 неделя – почти полная биодеградация микрокапсулы, в просвете сосуда остаточные альгинатные структуры; 6 неделя – полная биодеградация микрокапсулы.
Модель ХТЭЛГ воспроизводилась на 14 крысах-самцах стока Wistar. Микроинкапсулированный фибрин в количестве 9047 ± 430 частиц (суммарный объем 0,5 мл), суспензированный в 1,5 мл физиологического раствора, вводили в хвостовую вену крысы 8 раз с интервалом в 4 дня. В качестве группы сравнения использовали 14 крыс, которым вводился неинкапсулированный фибрин диаметром 75 ± 60 мкм в объеме, эквивалентном опытной группе, и суспензированный в 1,5 мл физиологического раствора по идентичному протоколу введения. В качестве контроля взяты здоровые животные (n=7).
Через 6 недель после заключительного введения эмболизирующих частиц у наркотизированного животного выполнялась катетеризация правых камер сердца с регистрацией систолического давления в правом желудочке (СДПЖ) и гистологическое исследование легких с расчётом индекса гипертрофии сосудистой стенки (отношение площади стенки сосуда к его общей площади в процентах), а также процента фиброза сосудистой стенки.
В результате проведенных экспериментов через 6 недель после заключительного введения микроинкапсулированного фибрина по данным гистологического исследования отмечалось значимое утолщение и фиброз стенок ветвей легочной артерии (фиг. 3 А, Б), по данным катетеризации сердца – увеличение СДПЖ по сравнению с группами контроля и сравнения (фиг 3 В). Указанные изменения являются характерными признаками моделируемой патологии. Значимых различий между группой сравнения и здоровыми животными по данным гистологического исследования и катетеризации правых камер сердца выявлено не было.
Пример №2. Характеристики использованных животных и протокол приготовления микроинкапсулированного фибрина совпадал с Примером №1. Микроинкапсулированный фибрин в количестве 9140 ± 474 частиц, суспензированный в 1,5 мл физиологического раствора, вводили в хвостовую вену крысы 5 раз с интервалом в 5 дней. В качестве группы сравнения использовали животных, которым вводили неинкапсулированный фибрин диаметром 75±60 мкм, суспензированный в 1,5 физиологического раствора, по идентичному протоколу введения. Через 6 недель после заключительного введения эмболизирующих частиц производилось измерение СДПЖ, гистологическое исследование легких с расчётом индекса гипертрофии сосудистой стенки и процента фиброза сосудистой стенки.
По данным гистологического исследования легких в группе введения микроинкапсулированного фибрина отмечалось значимое повышение индекса гипертрофии и процента фиброза сосудистой стенки ветвей легочной артерии, однако значимого повышения СДПЖ выявлено не было. Таким образом, этот протокол может быть использован для моделирования состояния, характеризующегося наличием резидуальной обструкции сосудистого русла, симптомов снижения переносимости физической нагрузки без стабильного повышения давления в легочной артерии, наблюдающемуся при хронической тромбоэмболической болезни (Humbert M, Kovacs G, Hoeper MM, et al. 2022 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. Eur Heart J. 2022; 43(38):3618-3731).
Пример №3. Для изготовления эмболизирующих частиц фибрин из плазмы крови человека (Sigma, США) смешивали с 2,6% раствором альгината натрия в соотношении 1:25, соответственно. Производство микрокапсул фибрина выполнялось с помощью установки Encapsulator В-390 с параметрами работы: диаметр используемой форсунки 200 мкм, частота вибрации 2700 Гц, напряжение электродов 2600 В, давление 500 мбар. Для стабилизации образующихся микросфер использовали 2,5% раствор хлорид бария. Размер полученных частиц составил 386 ± 47 мкм
Протокол введения микроинкапсулированного фибрина совпадал с примером 1, что приводило через 6 недель к формированию ХТЭЛГ с показателями ремоделирования сосудистой стенки и давления в правом желудочке значимо не отличающимися от Примера №1.
Заявленный способ моделирования ХТЭЛГ на лабораторных животных обеспечивает наиболее полное и естественное воспроизведение патологических процессов, структурных и функциональных изменений, характерных для хронической тромбоэмболической легочной гипертензии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ ТРОМБОЭМБОЛИЧЕСКОЙ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ | 2018 |
|
RU2675353C1 |
| Средство для лечения легочных гипертензий | 2023 |
|
RU2813890C1 |
| Способ моделирования хронической тромбоэмболической легочной гипертензии у крупных животных | 2023 |
|
RU2811651C1 |
| Способ контролируемой легочной тромбэндартерэктомии при лечении хронической тромбоэмболической легочной гипертензии | 2022 |
|
RU2794557C1 |
| Способ ретроградной реканализации окклюзированных сегментарных ветвей легочной артерии у пациентов с хронической тромбоэмболической легочной гипертензией | 2024 |
|
RU2838550C1 |
| Способ оценки тяжести состояния пациентов с идиопатической и хронической тромбоэмболической легочной гипертензией по показателям эластических свойств легочной артерии | 2019 |
|
RU2723360C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОСТРОЙ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ И ХРОНИЧЕСКОЙ ПОСТЭМБОЛИЧЕСКОЙ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ | 2014 |
|
RU2545927C1 |
| Способ моделирования тромбоза легочной артерии в условиях венозного тромбоза | 2021 |
|
RU2770355C1 |
| Способ оценки эффективности баллонной ангиопластики ветвей легочной артерии при хронической тромбоэмболической легочной гипертензии | 2022 |
|
RU2804340C1 |
| СПОСОБ КОРРЕКЦИИ ГИПОПЛАЗИИ ЛЕГКИХ ПРИ ВРОЖДЕННОЙ ДИАФРАГМАЛЬНОЙ ГРЫЖЕ ПЛОДОВ КРЫС С ПРИМЕНЕНИЕМ СЕЛЕКТИВНОГО ИНГИБИТОРА СПЕЦИФИЧЕСКОЙ ФДЭ-5 ЦГМФ | 2022 |
|
RU2801604C1 |

Изобретение относится к экспериментальной медицине, а именно к кардиологии. Лабораторным животным внутривенно вводят эмболизирующие частицы фибрина, микроинкапсулированные в альгинатных микрокапсулах диаметром 100-700 мкм с соотношением по объему фибрина и альгината натрия от 1:100 до 1:4. Эмболизирующие частицы вводят не менее 4 раз с интервалом не менее 2 дней в количестве 500-150000 частиц каждый раз. Способ обеспечивает наиболее полное и естественное воспроизведение патологических процессов, структурных и функциональных изменений, характерных для хронической тромбоэмболической легочной гипертензии (ХТЭЛГ), что в свою очередь дает возможность проводить поиск новых способов лечения и диагностики ХТЭЛГ. 5 ил., 3 пр.
Способ моделирования хронической тромбоэмболической легочной гипертензии, включающий внутривенное введение животному эмболизирующих частиц, отличающийся тем, что в качестве эмболизирующих частиц используют частицы фибрина, микроинкапсулированные в альгинатные микрокапсулы диаметром 100-700 мкм с соотношением по объему фибрина и альгината натрия от 1:100 до 1:4; эмболизирующие частицы вводят не менее 4 раз с интервалом не менее 2 дней в количестве 500–150000 частиц каждый раз.
| КАРПОВ А.А | |||
| и др | |||
| Модель хронической тромбоэмболической легочной гипертензии у крыс, вызванная повторным внутривенным введением биодеградируемых микросфер из альгината натрия | |||
| Регионарное кровообращение и микроциркуляция | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Пюпитр для работы на пишущих машинах | 1922 |
|
SU86A1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ ТРОМБОЭМБОЛИЧЕСКОЙ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ | 2018 |
|
RU2675353C1 |
| Способ моделирования хронической тромбоэмболической легочной гипертензии у крупных животных | 2023 |
|
RU2811651C1 |
| CN 102760372 A, 31.10.2012 | |||
| МУЛЛОВА И.С | |||
| и др | |||
Авторы
Даты
2024-11-21—Публикация
2024-03-19—Подача